ΜΕΛΕΤΗ ΑΝΟΣΟΛΟΓΙΚΩΝ ΜΗΧΑΝΙΣΜΩΝ ΠΟΥ ΕΝΕΧΟΝΤΑΙ ΣΤΗ ΧΡΟΝΙΟΤΗΤΑ ΤΗΣ ΛΟΙΜΩΞΕΩΣ ME Brucella
|
|
|
- Αλέξιο Γεωργιάδης
- 10 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ ΔΙΕΥΘΥΝΤΗΣ: ΕΥΑΓΓΕΛΟΣ Δ. ΑΝΑΣΤΑΣΙΟΥ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΚΛΙΝΙΚΕΣ-ΚΛΙΝΙΚΟΕΡΓΑΣΤΗΡΙΑΚΕΣ ΙΑΤΡΙΚΕΣ ΕΙΔΙΚΟΤΗΤΕΣ ΜΕΛΕΤΗ ΑΝΟΣΟΛΟΓΙΚΩΝ ΜΗΧΑΝΙΣΜΩΝ ΠΟΥ ΕΝΕΧΟΝΤΑΙ ΣΤΗ ΧΡΟΝΙΟΤΗΤΑ ΤΗΣ ΛΟΙΜΩΞΕΩΣ ME Brucella ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΟΔΥΣΣΕΑΣ Γ. ΔΗΜΗΤΡΑΚΟΠΟΥΛΟΣ ΙΑΤΡΟΣ Πάτρα 2013
2
3 ΤΡΙΜΕΛΗΣ ΣΥΜΒΟΥΛΕΥΤΙΚΗ ΕΠΙΤΡΟΠΗ Παληογιάννη Φωτεινή, Καθηγήτρια Μικροβιολογίας Επιβλέπουσα Καθηγήτρια Αναστασίου Ευάγγελος, Καθηγητής Μικροβιολογίας Μέλος Συµβουλευτικής Επιτροπής Μαραγκός Μάρκος, Αν. Καθηγητής Παθολογίας Λοιµωδών Νοσηµάτων Μέλος Συµβουλευτικής Επιτροπής ΕΠΤΑΜΕΛΗΣ ΕΞΕΤΑΣΤΙΚΗ ΕΠΙΤΡΟΠΗ Παληογιάννη Φωτεινή, Καθηγήτρια Μικροβιολογίας Επιβλέπουσα Καθηγήτρια Αναστασίου Ευάγγελος, Καθηγητής Μικροβιολογίας Μέλος Συµβουλευτικής Επιτροπής Μαραγκός Μάρκος, Αν. Καθηγητής Παθολογίας Λοιµωδών Νοσηµάτων Μέλος Συµβουλευτικής Επιτροπής Σπηλιοπούλου Ίρις, Καθηγήτρια Μικροβιολογίας Μέλος εξεταστικής επιτροπής Σταράκης Ιωάννης, Αν. Καθηγητής Παθολογίας Μέλος εξεταστικής επιτροπής Κυπραίος Κυριάκος, Αν. Καθηγητής Γενικής Φαρµακολογίας Φαρµακογονιδιωµατικής Μέλος εξεταστικής επιτροπής Παναγιωτακόπουλος Γεώργιος, Επ. Καθηγητής Γενικής Φαρµακολογίας Κλινικής Φαρµακολογίας Μέλος εξεταστικής επιτροπής
4
5 There be some sports are painful, and their labour Delight in them sets off. Some kinds of baseness Are nobly undergone, and most poor matters Point to rich ends. The Tempest, William Shakespeare Σα βγεις στον πηγαιμό για την Ιθάκη, να εύχεσαι να ναι μακρυς ο δρόμος, γεμάτος περιπέτειες, γεμάτος γνώσεις. Ιθάκη, Κ. Π. Καβάφης Ils se croyaient libres et personne ne sera jamais libre tant qu'il y aura des fléaux. La Peste, Albert Camus
6
7 Σ όσους ήταν δίπλα μου τις νύχτες που μ έκαιγε ο πυρετός
8
9 I. ΠΕΡΙΕΧΟΜΕΝΑ
10
11 ΠΕΡΙΕΧΟΜΕΝΑ 11 Περιεχόμενα I. ΠΕΡΙΕΧΟΜΕΝΑ... 9 II. ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ III. ΠΡΟΛΟΓΟΣ IV. ΓΕΝΙΚΟ ΜΕΡΟΣ ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΓΕΝΙΚΑ ΥΠΟΔΟΧΕΙΣ ΤΗΣ ΦΥΣΙΚΗΣ ΑΝΟΣΙΑΣ TOLL LIKE RECEPTORS MAP ΚΙΝΑΣΕΣ ΜΕΤΑΓΡΑΦΙΚΟΙ ΠΑΡΑΓΟΝΤΕΣ NFκΒ AP CREB ΚΥΤΤΑΡΟΚΙΝΕΣ Ιντερλευκίνη 1 (IL-1) Ιντερλευκίνη 6 (IL-6) Παράγοντας νέκρωσης όγκων α (TNF-α) Ιντερλευκίνη 10 (IL-10) ΒΡΟΥΚΕΛΛΑ ΙΣΤΟΡΙΑ ΕΠΙΔΗΜΙΟΛΟΓΙΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΕΠΙΦΑΝΕΙΑΚΑ ΑΝΤΙΓΟΝΑ ΛΟΙΜΩΞΕΙΣ ΑΠΟ ΒΡΟΥΚΕΛΛΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΔΙΑΓΝΩΣΗ Καλλιέργεια Ορολογικός έλεγχος ΘΕΡΑΠΕΙΑ... 59
12 12 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 2.8 ΠΡΟΛΗΨΗ ΠΑΘΟΓΟΝΟΣ ΔΡΑΣΗ Μηχανισμοί ενδοκυττάριας επιβίωσης Αναγνώριση από τη φυσική ανοσία ΣΚΟΠΟΣ V. ΕΙΔΙΚΟ ΜΕΡΟΣ ΥΛΙΚΑ ΣΥΣΚΕΥΕΣ ΜΕΘΟΔΟΙ ΚΥΤΤΑΡΑ, ΑΝΤΙΔΡΑΣΤΗΡΙΑ Στελέχη βακτηρίων Ανθρώπινα κύτταρα, κυτταρικές σειρές Διαλύματα Απομόνωση ανθρώπινων μονοπυρήνων κυττάρων από περιφερικό αίμα Απομόνωση μονοκυττάρων με προσκόλληση σε φιάλες κυτταροκαλλιέργειας Καλλιέργεια κυτταρικής σειράς HEK Μέτρηση κυττάρων-προσδιορισμός βιωσιμότητας Κατάψυξη κυτταρικών σειρών Απόψυξη κυτταρικών σειρών Αντιδραστήρια Ανασταλτικά αντισώματα και αναστολείς MAP κινασών Αντιδραστήρια για τη διέγερση ευκαρυωτικών κυττάρων ΑΝΑΛΥΤΙΚΕΣ ΜΕΘΟΔΟΙ Δοκιμασία προστασίας από τη γενταμικίνη Προσδιορισμός κυτταροκινών σε υπερκείμενα ανθρωπίνων καλλιεργειών με ενζυμική μέθοδο ανοσοπροσρόφησης (Enzyme Linked ImmunoSorbent Assay- ELISA) Ανίχνευση και διαχωρισμός αποπτωτικών και νεκρών κυττάρων με χρώση αννεξίνης V- ιωδιούχου προπιδίου Απομόνωση πρωτεϊνικών εκχυλισμάτων Ποσοτικός προσδιορισμός πρωτεϊνών Μεθοδολογία Smith για προσδιορισμό πρωτεϊνών σε κυτταροπλασματικά εκχυλίσματα... 92
13 ΠΕΡΙΕΧΟΜΕΝΑ Μεθοδολογία Bradford για προσδιορισμό πρωτεϊνών σε κυτταροπλασματικά εκχυλίσματα Ηλεκτροφόρηση Γενικές αρχές ηλεκτροφόρησης Ηλεκτροφόρηση πρωτεϊνών Ηλεκτροφόρηση σε πήκτωμα πολυακρυλαμίδης με αποδιατακτικούς παράγοντες Μεταφορά πρωτεϊνών σε μεμβράνη νιτροκυτταρίνης (Western Blotting) Χρώση πρωτεϊνών ακινητοποιημένων σε πήκτωμα ακρυλαμίδης με Coomassie Brilliant Blue R Χρώση πρωτεϊνών ακινητοποιημένων σε μεμβράνη νιτροκυτταρίνης με Ponceau-S Κάλυψη μεμβράνης νιτροκυτταρίνης (blocking) Επώαση μεμβράνης νιτροκυτταρίνης με πρώτο και δεύτερο αντίσωμα Ανίχνευση πρωτεϊνών ακινητοποιημένων σε μεμβράνη νιτροκυτταρίνης με χημειοφωταύγεια Απομάκρυνση αντισωμάτων από τη μεμβράνη νιτροκυτταρίνης (Stripping off) Hλεκτροφόρηση νουκλεϊνικών οξέων σε πήκτωμα αγαρόζης Πολλαπλασιασμός πλασμιδίων Μετασχηματισμός στελέχους E. coli με ανασυνδυασμένο πλασμίδιο (transformation) Καλλιέργεια-πολλαπλασιασμός των μετασχηματισμένων βακτηρίων Απομόνωση πλασμιδίων με στήλες ιοντοανταλλακτικής ρητίνης Έλεγχος προϊόντων καθαρισμού πλασμιδίων Πλασμίδια Διαμόλυνση ευκαρυωτικών κυττάρων Γενικές αρχές διαμόλυνσης ευκαρυωτικών κυττάρων Διαμόλυνση ευκαρυωτικών κυττάρων με κατιονικά λιποσώματα (Lipofection) Έλεγχος ενσωμάτωσης πλασμιδίων Έλεγχος δραστικότητας μεταγραφικών παραγόντων : Μέθοδος λουσιφεράσης ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΙΝΗΤΙΚΗ ΤΗΣ ΠΑΡΑΓΩΓΗΣ ΠΡΟΦΛΕΓΜΟΝΩΔΩΝ (TNF-Α, IL-1Β, IL-6) ΚΑΙ ΑΝΤΙΦΛΕΓΜΟΝΩΔΩΝ (IL-10) ΚΥΤΤΑΡΟΚΙΝΩΝ ΣΕ ΥΠΕΡΚΕΙΜΕΝΑ ΚΑΛΛΙΕΡΓΕΙΩΝ ΑΝΘΡΩΠΙΝΩΝ ΜΟΝΟΚΥΤΤΑΡΩΝ ΜΕΤΑ ΑΠΟ ΜΟΛΥΝΣΗ ΜΕ ΖΩΝΤΑΝΑ ΒΑΚΤΗΡΙΑ B. MELITENSIS
14 14 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 4.2 ΚΙΝΗΤΙΚΗ ΤΗΣ ΦΩΣΦΟΡΥΛΙΩΣΗΣ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΣΕ ΟΛΙΚΑ ΠΡΩΤΕΪΝΙΚΑ ΕΚΧΥΛΙΣΜΑΤΑ ΑΝΘΡΩΠΙΝΩΝ ΜΟΝΟΚΥΤΤΑΡΩΝ ΜΕΤΑ ΑΠΟ ΜΟΛΥΝΣΗ ΜΕ ΖΩΝΤΑΝΑ ΒΑΚΤΗΡΙΑ B. MELITENSIS ΣΥΜΜΕΤΟΧΗ ΤΩΝ ΥΠΟΔΟΧΕΩΝ ΦΥΣΙΚΗΣ ΑΝΟΣΙΑΣ TOLL LIKE (TLRS) ΣΤΗΝ ΠΑΡΑΓΩΓΗ ΠΡΟΦΛΕΓΜΟΝΩΔΩΝ (TNF-Α, IL-1Β, IL-6) ΚΑΙ ΑΝΤΙΦΛΕΓΜΟΝΩΔΩΝ (IL-10) ΚΥΤΤΑΡΟΚΙΝΩΝ ΑΠΟ ΦΥΣΙΟΛΟΓΙΚΑ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ ΜΕΤΑ ΑΠΟ ΜΟΛΥΝΣΗ ΜΕ ΖΩΝΤΑΝΑ ΠΑΘΟΓΟΝΑ ΒΑΚΤΗΡΙΑ B. MELITENSIS ΣΥΜΜΕΤΟΧΗ ΤΩΝ ΥΠΟΔΟΧΕΩΝ ΦΥΣΙΚΗΣ ΑΝΟΣΙΑΣ TOLL LIKE (TLRS) ΣΤΗΝ ΦΩΣΦΟΡΥΛΙΩΣΗ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΣΕ ΦΥΣΙΟΛΟΓΙΚΑ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ ΜΕΤΑ ΑΠΟ ΜΟΛΥΝΣΗ ΜΕ ΖΩΝΤΑΝΑ ΠΑΘΟΓΟΝΑ ΒΑΚΤΗΡΙΑ B. MELITENSIS ΣΥΜΜΕΤΟΧΗ ΤΩΝ ΥΠΟΔΟΧΕΩΝ ΦΥΣΙΚΗΣ ΑΝΟΣΙΑΣ TOLL LIKE (TLRS) ΣΤΗΝ ΕΝΕΡΓΟΠΟΙΗΣΗ ΤΟΥ ΜΕΤΑΓΡΑΦΙΚΟΥ ΠΑΡΑΓΟΝΤΑ NFΚB ΣΤΗΝ ΚΥΤΤΑΡΙΚΗ ΣΕΙΡΑ HEK 293 ΜΕΤΑ ΑΠΟ ΜΟΛΥΝΣΗ ΜΕ ΖΩΝΤΑΝΑ ΠΑΘΟΓΟΝΑ ΒΑΚΤΗΡΙΑ B. MELITENSIS ΣΥΜΜΕΤΟΧΗ ΤΩΝ ΥΠΟΔΟΧΕΩΝ ΦΥΣΙΚΗΣ ΑΝΟΣΙΑΣ TOLL LIKE (TLRS) ΣΤΗ ΦΩΣΦΟΡΥΛΙΩΣΗ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΣΤΗΝ ΚΥΤΤΑΡΙΚΗ ΣΕΙΡΑ HEK 293 ΜΕΤΑ ΑΠΟ ΜΟΛΥΝΣΗ ΜΕ ΖΩΝΤΑΝΑ ΠΑΘΟΓΟΝΑ ΒΑΚΤΗΡΙΑ B. MELITENSIS ΣΥΜΜΕΤΟΧΗ ΤΩΝ ΜΕΛΩΝ ΤΗΣ ΟΙΚΟΓΕΝΕΙΑΣ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΣΤΗΝ ΠΑΡΑΓΩΓΗ ΠΡΟΦΛΕΓΜΟΝΩΔΩΝ (TNF-Α, IL-1Β, IL-6) ΚΑΙ ΑΝΤΙΦΛΕΓΜΟΝΩΔΩΝ (IL-10) ΚΥΤΤΑΡΟΚΙΝΩΝ ΑΠΟ ΦΥΣΙΟΛΟΓΙΚΑ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ ΜΕΤΑ ΑΠΟ ΜΟΛΥΝΣΗ ΜΕ ΖΩΝΤΑΝΑ ΠΑΘΟΓΟΝΑ ΒΑΚΤΗΡΙΑ B. MELITENSIS Η ΕΝΔΟΚΥΤΤΑΡΙΑ ΕΠΙΒΙΩΣΗ ΖΩΝΤΑΝΩΝ ΒΑΚΤΗΡΙΩΝ B. MELITENSIS ΣΕ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ ΠΑΡΟΥΣΙΑ ΑΝΑΣΤΟΛΕΩΝ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΈΛΕΓΧΟΣ ΤΗΣ ΣΥΜΜΕΤΟΧΗΣ ΤΗΣ ΑΠΟΠΤΩΣΗΣ Η ΤΟΥ ΚΥΤΤΑΡΙΚΟΥ ΘΑΝΑΤΟΥ ΤΩΝ ΜΟΝΟΚΥΤΤΑΡΩΝ ΑΠΟ ΤΟΥΣ ΧΗΜΙΚΟΥΣ ΑΝΑΣΤΟΛΕΙΣ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΣΤΗΝ ΕΝΔΟΚΥΤΤΑΡΙΑ ΕΠΙΒΙΩΣΗ ΖΩΝΤΑΝΩΝ ΒΑΚΤΗΡΙΩΝ B. MELITENSIS ΈΛΕΓΧΟΣ ΤΗΣ ΕΠΙΔΡΑΣΗΣ ΤΗΣ IL-10 ΣΤΗΝ ΕΝΔΟΚΥΤΤΑΡΙΑ ΕΠΙΒΙΩΣΗ ΖΩΝΤΑΝΩΝ ΒΑΚΤΗΡΙΩΝ B. MELITENSIS ΣΕ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ ΠΑΡΟΥΣΙΑ ΑΝΑΣΤΟΛΕΩΝ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΣΥΖΗΤΗΣΗ Η B. MELITENSIS ΠΡΟΚΑΛΕΙ ΕΝΤΟΝΗ ΠΡΟΦΛΕΓΜΟΝΩΔΗ ΑΠΑΝΤΗΣΗ ΑΠΟ ΤΑ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ Η B. MELITENSIS ΕΠΑΓΕΙ ΚΑΘΥΣΤΕΡΗΜΕΝΗ ΕΝΕΡΓΟΠΟΙΗΣΗ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΑΠΟ ΤΑ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ ΤΑ ΖΩΝΤΑΝΑ ΒΑΚΤΗΡΙΑ B. MELITENSIS ΕΝΕΡΓΟΠΟΙΟΥΝ ΤΑ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ ΚΑΙ ΤΗΝ ΚΥΤΤΑΡΙΚΗ ΣΕΙΡΑ HEK 293 ΔΙΑΜΕΣΟΥ TLR
15 ΠΕΡΙΕΧΟΜΕΝΑ ΜΕΛΗ ΤΗΣ ΟΙΚΟΓΕΝΕΙΑΣ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΕΛΕΓΧΟΥΝ ΤΗΝ ΠΑΡΑΓΩΓΗ ΠΡΟΦΛΕΓΜΟΝΩΔΩΝ ΚΑΙ ΑΝΤΙΦΛΕΓΜΟΝΩΔΩΝ ΚΥΤΤΑΡΟΚΙΝΩΝ ΑΠΟ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ ΠΟΥ ΜΟΛΥΝΘΗΚΑΝ ΜΕ B. MELITENSIS ΜΕΛΗ ΤΗΣ ΟΙΚΟΓΕΝΕΙΑΣ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΕΥΝΟΟΥΝ ΤΗΝ ΕΝΔΟΚΥΤΤΑΡΙΑ ΕΠΙΒΙΩΣΗ ΤΗΣ B. MELITENSIS ΣΕ ΑΝΘΡΩΠΙΝΑ ΜΟΝΟΚΥΤΤΑΡΑ Η ΘΕΤΙΚΗ ΕΠΙΔΡΑΣΗ ΤΩΝ MAP ΚΙΝΑΣΩΝ ΣΤΗΝ ΕΝΔΟΚΥΤΤΑΡΙΑ ΕΠΙΒΙΩΣΗ ΤΗΣ B. MELITENSIS ΔΕ ΔΙΑΜΕΣΟΛΑΒΕΙΤΑΙ ΑΠΟ ΤΗΝ IL ΣΥΜΠΕΡΑΣΜΑΤΑ VI. ΠΕΡΙΛΗΨΗ/ABSTRACT ΠΕΡΙΛΗΨΗ ABSTRACT VII. ΒΙΒΛΙΟΓΡΑΦΙΑ Εικόνες Εικόνα 1: Η σηματοδοτική οδός των υποδοχέων της φυσικής ανοσίας TLRs Εικόνα 2: Η σηματοδοτική οδός των MAP κινασών Εικόνα 3: Η σηματοδοτική οδός του μεταγραφικού παράγοντα NFκΒ Εικόνα 4: Αποικίες Brucella σε αιματούχο άγαρ και κύτταρα του βακτηρίου με Gram χρώση55 Εικόνα 5: Μηχανισμός ενδοκυττάριας επιβίωσης της Brucella Εικόνα 6: Μεθοδολογία προσδιορισμού πρωτεϊνών κατά Smith Εικόνα 7: Αντίδραση πολυμερισμού της ακρυλαμίδης Εικόνα 8: Αντίδραση χημειοφωταύγειας της λουμινόλης Εικόνα 9: Μέθοδος διαμόλυνσης ευκαρυωτικών κυττάρων με λιποσώματα Εικόνα 10: Μηχανισμός ενεργοποίησης της φυσικής ανοσίας στη λοίμωξη από βρουκέλλα158 Πίνακες Πίνακας 1: Δοκιμασίες για το διαχωρισμό των Βρουκελλών που απομονώνονται στο κλινικό εργαστήριο Πίνακας 2: Πλασμίδια που χρησιμοποιήθηκαν στην παρούσα μελέτη Πίνακας 3: Συμμετοχή της IL-10 στην ενδοκυττάρια επιβίωση της B. melitensis σε ανθρώπινα μονοκύτταρα, παρουσία αναστολέων των MAP κινασών, μετά από 48 ώρες επώασης
16 16 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σχήματα Σχήμα 1: Κινητική της παραγωγής του TNF-α από ανθρώπινα μονοκύτταρα μετά από μόλυνση με ζωντανά βακτήρια B. melitensis Σχήμα 2: Κινητική της παραγωγής της IL-1β από ανθρώπινα μονοκύτταρα μετά από μόλυνση με ζωντανά βακτήρια B. melitensis Σχήμα 3: Κινητική της παραγωγής της IL-6 από ανθρώπινα μονοκύτταρα μετά από μόλυνση με ζωντανά βακτήρια B. melitensis Σχήμα 4: Κινητική της παραγωγής της IL-10 από ανθρώπινα μονοκύτταρα μετά από μόλυνση με ζωντανά βακτήρια B. melitensis Σχήμα 5: Ενεργοποίηση των MAP κινασών σε ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis, μετά την πάροδο 30 λεπτών Σχήμα 6: Κινητική της φωσφορυλίωσης των MAP κινασών σε ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis Σχήμα 7: Παραγωγή TNF-α από ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis παρουσία αντισωμάτων έναντι των TLR2 και TLR4 μετά από 16 ώρες επώασης Σχήμα 8: Παραγωγή IL-1β από ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis παρουσία αντισωμάτων έναντι των TLR2 και TLR4 μετά από 16 ώρες επώασης Σχήμα 9: Παραγωγή IL-6 από ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis παρουσία αντισωμάτων έναντι των TLR2 και TLR4 μετά από 16 ώρες επώασης Σχήμα 10: Παραγωγή IL-10 από ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis παρουσία αντισωμάτων έναντι των TLR2 και TLR4 μετά από 16 ώρες επώασης Σχήμα 11: Ενεργοποίηση των MAP κινασών σε ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis παρουσία αντισωμάτων έναντι των TLR2 και TLR4 μετά από 4 ώρες επώασης Σχήμα 12: Δραστικότητα του μεταγραφικού παράγοντα NFκB στην κυτταρική σειρά HEK 293 που υπερεκφράζει το σύμπλοκο υποδοχέα TLR2/CD14 μετά από μόλυνση με ζωντανά βακτήρια B. melitensis, μετά από 16 ώρες επώασης Σχήμα 13: Δραστικότητα του μεταγραφικού παράγοντα NFκB στην κυτταρική σειρά HEK 293 που υπερεκφράζει το σύμπλοκο υποδοχέα TLR4/MD2/CD14 μετά από μόλυνση με ζωντανά βακτήρια B. melitensis, μετά από 16 ώρες επώασης
17 ΠΕΡΙΕΧΟΜΕΝΑ 17 Σχήμα 14: Δραστικότητα του μεταγραφικού παράγοντα AP-1 στις κυτταρικές σειρές HEK 293 που υπερεκφράζουν το σύμπλοκο υποδοχέα TLR2/CD14 ή TLR4/MD2/CD14 μετά από μόλυνση με ζωντανά βακτήρια B. melitensis, μετά από 16 ώρες επώασης Σχήμα 15: Δραστικότητα του μεταγραφικού παράγοντα CREB στις κυτταρικές σειρές HEK 293 που υπερεκφράζουν το σύμπλοκο υποδοχέα TLR2/CD14 ή TLR4/MD2/CD14 μετά από μόλυνση με ζωντανά βακτήρια B. melitensis, μετά από 16 ώρες επώασης Σχήμα 16: Κινητική της ενεργοποίησης των MAP κινασών στην κυτταρική σειρά HEK 293 που υπερεκφράζει το σύμπλοκο υποδοχέα TLR2/CD14 μετά από μόλυνση με ζωντανά βακτήρια B. melitensis Σχήμα 17: Κινητική της ενεργοποίησης των MAP κινασών στην κυτταρική σειρά HEK 293 που υπερεκφράζει το σύμπλοκο υποδοχέα TLR4/MD2/CD14 μετά από μόλυνση με ζωντανά βακτήρια B. melitensis Σχήμα 18: Παραγωγή TNF-α από ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών, μετά από 16 ώρες επώασης Σχήμα 19: Παραγωγή IL-1β από ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών, μετά από 16 ώρες επώασης Σχήμα 20: Παραγωγή IL-6 από ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών, μετά από 16 ώρες επώασης Σχήμα 21: Παραγωγή IL-10 από ανθρώπινα μονοκύτταρα που μολύνθηκαν με ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών, μετά από 16 ώρες επώασης Σχήμα 22: Ενδοκυττάρια επιβίωση της B. melitensis σε ανθρώπινα μονοκύτταρα, παρουσία αναστολέων των MAP κινασών Σχήμα 23: Απόπτωση και νέκρωση των μονοκυττάρων μετά από 48 ώρες μόλυνσης με ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών Σχήμα 24: Κυτταροτοξικότητα των μονοκυττάρων μετά από 48 ώρες μόλυνσης με ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών
18
19 II. ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ
20
21 ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ 21 Οι συντοµογραφίες που χρησιµοποιήθηκαν όπως αποδίδονται στην διεθνή βιβλιογραφία, ενώ σε παρένθεση αναγράφεται η ελληνική απόδοσή τους, όπου είναι δυνατόν. ACTH: AdrenoCorticoTropic Hormone (κορτικοτροπίνη) AP: Alkaline Phosphatase (αλκαλική φωσφατάση) AP-1: Activator Protein-1 APS: Ammonium PerSulfate (υπερθειικό αµµώνιο) ATF: Activating Transcription Factor BCA: BiCinchoninic Acid (αµφικιγχονινικό οξύ) BCV: Brucella Containing Vacuole (κυστίδιο που περιέχει την βρουκέλλα) BSA: Bovine Serum Albumin (Αλβουµίνη ορού βοός) CAMK: calcium/calmodulin-dependent protein kinase CD: Cluster of Differentiation (Σύµπλεγµα ιαφοροποίησης) CRE: camp-responsive Element CREB: camp Response Element Binding protein CREM: camp-responsive Element Modulator CRP: C Reactive Protein (C αντιδρώσα πρωτεΐνη) DEPC: Diethylpyrocarbonate ( ιεθυλπυροκαρβονικό) DMSO: DiMethyl SulfOxide (διµεθυλσουλφοξίδη) DNA: DeoxyriboNucleic Acid ( εσοξυριβονουκλεϊνικό οξύ) EDTA: EthyleneDiamineTetraAcetic acid (αιθυλεν-διαµιν-τετρα-οξικό οξύ) EEA: Early Endosomal Antigen (αντιγόνο πρώιµου ενδοσώµατος) (E) GFP: (Enhanced) Green Fluorescence Protein (ενισχυµένη πράσινη φθορίζουσα πρωτεΐνη) ELISA: Enzyme-Linked ImmunoSorbent Assay (Ενζυµική Μέθοδος Ανοσοπροσρόφησης) ERK: Extracellular signal-regulated Kinase (Κινάση ελεγχόµενη από εξωτερικό µήνυµα) EtBr: Ethidium Bromide (βρωµιούχο αιθίδιο) FCS: Fetal Calf Serum (ορός εµβρύου µόσχου) GTP: Guanosine-5'-TriPhosphate (τριφωσφορική γουανοσίνη) HEPES: 4-(2-HydroxyEthyl)-1-PiperazineEthaneSulfonic acid (υδροξυ-αιθυλπιπεραζιν-αιθαν-σουλφονικό οξύ)
22 22 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ HKBa: Heat Killed Brucella abortus (νεκρωµένα µε θέρµανση βακτήρια B. abortus) HRP: HorseRadish Peroxidase (υπεροξειδάση αγριοραπανίδας) Hsp: Heat sock protein (πρωτεΐνες θερµικής καταπληξίας) HSV: Herpes Simplex Virus (Ιός του απλού έρπητα) IFN: InterFeroN (Ιντερφερόνη) Ig: Immunoglobulin (Ανοσοσφαιρίνη) IKK: ΙκΒ Kinase (κινάση του IκB) IL: InterLeukin (Ιντερλευκίνη) IRAK: IL-1-Receptor Associated Kinase (κινάση που συνδέεται µε τον υποδοχέα της IL-1) IRF: Interferon Regulatory Factor (παράγοντας που ρυθµίζει την παραγωγή ιντερφερονών) IκB: Inhibitor κβ (Αναστολέας του NFκΒ) JNK: c-jun NH 2 -terminal Kinase LAMP: Lysosome-Associated Membrane glycoprotein (γλυκοπρωτεΐνη που συνδέεται µε την µεµβράνη του λυσοσώµατος) LB: Lysogeny Broth LBP: LPS Binding Protein (πρωτεΐνη που προσδένει LPS) LPS: LipoPolySaccharide (Λιποπολυσακχαρίτης) LRR: Leucine Rich Repeats (αλληλουχίες αµινοξέων πλούσιες σε λευκίνη) MAF: MusculoAponeurotic Fibrosarcoma MAPK: Mitogen-Activated Protein Kinases (Κινάσες που ενεργοποιούνται από µιτογόνο) MBL: Mannan Binding Lectin (λεκτίνη που προσδένει µαννάνη) MEF: Myocyte Enhancer Factor (παράγοντας επαύξησης µυοκυττάρων) MHC: Major Histocompatibility Complex (Μείζον Σύµπλεγµα Ιστοσυµβατότητας) MOI: Multiplicity Of Infection (αναλογία βακτηρίων ανά µονοκύτταρο) MyD88: Myeloid Differentiation primary response gene µε µοριακό βάρος 88kDa NADPH: Nicotinamide Adenine Dinucleotide Phosphate NFAT: Nuclear Factor of Activated T-cells (πυρηνικός παράγοντας ενεργοποιηµένων Τ λεµφοκυττάρων)
23 ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ 23 NFκB: Nuclear Factor κ-light-chain-enhancer of activated B cells (πυρηνικός παράγοντας που επαυξάνει την παραγωγή ελαφρών αλυσίδων τάξης κάπα στα ενεργοποιηµένα Β λεµφοκύτταρα) NK: Natural Killer cells (Φυσικά Φονικά κύτταρα) NLR: NOD Like Receptors NOD: Nucleotide Oligomerization Domain Omp: Outer membrane protein (πρωτεΐνη της εξώτερης µεµβράνης) PAMP: Pathogen Associated Molecular Pattern PBMC: Peripheral Blood Mononuclear Cell (µονοπύρηνα κύτταρα περιφερικού αίµατος) PBS: Phosphate Buffer Saline (Ρυθµιστικό ιάλυµα Φωσφορικών) PG: ProstaGlandin (προσταγλανδίνη) PI: Propidium Iodide (ιωδιούχο προπίδιο) PKA(B, C): Protein Kinase A (B, C) PLB: Passive Lysis Buffer (διάλυµα παθητικής λύσης) PMA: Phorbol 12-Myristate 13-Acetate (φορβολικός εστέρας) PMSF: Phenyl-Methyl-Sulphonyl-Fluoride (φαινυλ-µεθυλ-σουλφονυλ-φθορίδιο) PRR: Pattern Recognition Receptors PS: PhosphatidylSerine (φωσφατιδυλοσερίνη) RHD: Rel -Homology Domain RIPA: RadioImmunoPrecipitation Assay (µέθοδος ραδιοανοσοκαθίζησης) RLU: Relative Light Units (σχετικές µονάδες φωτός) RNA: RiboNucleic Acid (ριβοζυλ-νουκλεϊνικό οξύ) SAPK: Stress-Activated Protein Kinase (πρωτεϊνική κινάση που ενεργοποιείται από το στρες) SDS: Sodium-Dodecyl-Sulphate SDS-PAGE: SDS PolyAcrylamide Gel Electrophoresis SOC: Super Optimal broth with Catabolite repression STAT: Signal Transducer and Activator of Transcription TAD: TransActivation Domain TBE: Tris/Borate/EDTA TBK: TANK Binding Kinase (κινάση που προσδένει την TANK) TBS (T): Tris Base- Sodium chloride (Tween 20) TCR: T Cell Receptor (υποδοχέας Τ λεµφοκυττάρων)
24 24 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ TE: Tris/EDTA TEMED: N,N,N,N -TEtraMethyl-Ethane-1,2-Diamine (τετραµεθυλ-αιθανδιαµίνη) TIR: Toll / Interleukin 1 Receptor domain TIRAP/MAL: TIR-domain-containing Adaptor Protein / MyD88 Adaptor protein Like (προσαρµοστική πρωτεΐνη που περιέχει τοµέα TIR / προσαρµοστική πρωτεΐνη που προσοµοιάζει στην MyD88) TLR: Toll-Like Receptor TMB: Tetra-Methyl-Benzidine (τετρα-µεθυλ-βενζιδίνη) TNF: Tumor Necrosis Factor (παράγοντας νέκρωσης όγκων) TNFAIP/A20: TNF-α Induced Protein (πρωτεΐνη που επάγεται από τον TNF-α) TNIP/ABIN: TNFAIP3 Interacting Protein / Α20 Binding Inhibitor of NFκB (πρωτεΐνη που αλληλεπιδρά µε την TNFAIP3) TPA: 12-O-TetradecanoylPhorbol-13-Acetate TRAF: TNF Receptor Associated Factor (παράγοντας που συνδέεται µε τον υποδοχέα του TNF) TRAM/TICAM-2: TRIF-Related Adaptor Molecule (προσαρµοστικό µόριο που σχετίζεται µε την TRIF) TRE: TPA-Responsive Element TRIF/TICAM-1: TIR domain-containing adaptor inducing IFN-β (προσαρµοστικό µόριο που περιέχει τοµέα TIR και επάγει την παραγωγή IFN-β) TSA (B): Trypticase Soy Agar (Broth) U.V.: Ultra Violet radiation (Υπεριώδης Ακτινοβολία) ΕΝΥ: ΕγκεφαλοΝωτιαίο Υγρό ΠΟΥ: Παγκόσµιος Οργανισµός Υγείας
25 III. ΠΡΟΛΟΓΟΣ
26
27 ΠΡΟΛΟΓΟΣ 27 Κύριο χαρακτηριστικό των λοιµώξεων από βρουκέλλα είναι ότι συχνά οδηγεί σε µακροχρόνια νοσηρότητα. Όµως, το ερευνητικό ενδιαφέρον για τη νόσο είναι περιορισµένο στη διεθνή επιστηµονική κοινότητα. Στον ελληνικό χώρο, η βρουκέλλωση αποτελεί συνήθη λοίµωξη ανθρώπων και ζώων, αλλά δεν έχει αποτελέσει αντικείµενο µελέτης στο επίπεδο της βασικής έρευνας. Η παρούσα εργασία αποτελεί την πρώτη ερευνητική προσπάθεια του εργαστηρίου που αφορά στη διευκρίνηση των µηχανισµών της ανοσολογικής απόκρισης στη βρουκέλλωση. Η πραγµατοποίησή της έγινε εξ ολοκλήρου στο Εργαστήριο Μικροβιολογίας της Ιατρικής Σχολής του Πανεπιστηµίου Πατρών µε τη χρηµατοδότηση του προγράµµατος Πυθαγόρας II. Για να ολοκληρωθεί χρειάστηκε τη βοήθεια πολλών ανθρώπων, τους οποίους θέλω να ευχαριστήσω. Η Καθηγήτρια Φωτεινή Παληογιάννη µε την ανάθεση του θέµατος της παρούσας διατριβής µε µύησε στον κόσµο της έρευνας και µε έκανε κοινωνό του επιστηµονικού τρόπου σκέψεως. Κατά τη διάρκεια σχεδιασµού και εκπόνησης των πειραµάτων βρισκόταν πάντοτε στο πλευρό µου για να µε καθοδηγεί και να µε ενθαρρύνει. Επίσης, η συµβολή της στην αρτιότητα της συγγραφής της διατριβής ήταν ουσιαστική. Ο Καθηγητής Ευάγγελος Αναστασίου παρακολουθούσε την εξέλιξη της διατριβής µε έντονο επιστηµονικό και προσωπικό ενδιαφέρον και προσέφερε χρήσιµες συµβουλές κατά τη διάρκεια συγγραφής της. Ο Αν. Καθηγητής Μάρκος Μαραγκός µου εµφύσησε το ενδιαφέρον για τη µελέτη των λοιµώξεων και συνέβαλε, µε τις παρατηρήσεις του, στη διαµόρφωση της τελικής µορφής της διατριβής. Τα µέλη ΕΠ της Ιατρικής Σχολής Ίρις Σπηλιοπούλου, Ιωάννης Σταράκης, Κυριάκος Κυπραίος και Γεώργιος Παναγιωτακόπουλος αποδέχθηκαν ευχαρίστως τη συµµετοχή τους ως µελών της εξεταστικής επιτροπής και άσκησαν γόνιµη κριτική. Η Κασσιανή Λιόπετα αποτελεί πολύτιµο µέλος του εργαστηρίου και κατά τη διάρκεια της αγαστής συνεργασίας µας ήταν πάντοτε διαθέσιµη ώστε να λύσει όποια προβλήµατα ή απορίες παρουσιάστηκαν. Τα µέλη του Εργαστηρίου Γεώργιος Λαγουµιτζής, Παναγιώτα Ξαπλαντέρη, Σταυρούλα Μπούµπαλη, Θεοδώρα Κακαγιάννη, Παναγιώτης Παπανδρέου, Μαρία Αδαµίδου και Ελένη Αποστολοπούλου, στο βαθµό που τους αναλογεί, άφησαν παρακαταθήκη στο εργαστήριο, που διευκόλυνε το έργο µου. Οι Αναστασία Σπηλιοπούλου, Μαρία Κρεββατά, Αντιγόνη Φωκά, Νικόλαος Γιορµέζης, Ελεάννα ρούγκα, Χριστίνα Μπαρτζάβαλη και Μαρία Παξιµαδά στόλισαν
28 28 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ µε το ήθος τους το Εργαστήριο Μικροβιολογίας και δηµιούργησαν ένα ευχάριστο περιβάλλον εργασίας σε όλη τη διάρκεια που συνυπήρξαµε. Τα µέλη ΕΠ Κυριάκος Κυπραίος, Ζωή Λυγερού, Ιωάννης Ζαρκάδης, Ιωάννης Χαµπαίος και Αλέξανδρος Σπυριδωνίδης έχουν εξοπλίσει και στελεχώσει ερευνητικά εργαστήρια τα οποία κοσµούν την Ιατρική Σχολή και ανοίγουν νέες προοπτικές στους µελλοντικούς στόχους της παρούσας έρευνας. Η συνεργασία µε τους Ελένη Καραβία, Μάγδα Σπέλλα, Αναστάσιο Παπαναστασίου, ιονύσιο Χαρτουµπέκη και ήµητρα Κοκκίνου αποδεικνύει ότι η παρούσα διατριβή είναι απλώς η αφετηρία στη διευκρίνηση των µηχανισµών της ανοσολογικής απόκρισης στη βρουκέλλωση. Το προσωπικό του τµήµατος Αιµοδοσίας του Γενικού Νοσοκοµείου Πατρών Άγιος Ανδρέας και του τµήµατος Μικροβιολογίας του Πανεπιστηµιακού Νοσοκοµείου Πατρών Παναγία η Βοήθεια προσέφεραν αγόγγυστα τη βοήθειά τους, όποτε τους ζητήθηκε. Οι φίλοι µου στάθηκαν πάντα στο πλευρό µου και µου έδιναν τη δύναµη να αντιµετωπίζω τις δυσκολίες. Τέλος, η οικογένειά µου, µε την καθολική συµπαράσταση και την ανοχή της, µε εφοδίασε και µε στήριξε ώστε να µου επιτρέπει να ατενίζω το µέλλον µε αισιοδοξία. Μάλιστα, χωρίς την προτροπή και τις παραινέσεις του πατέρα µου τίποτα δε θα ήταν εφικτό.
29 IV. ΓΕΝΙΚΟ ΜΕΡΟΣ
30
31 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Γενικά 1 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Με τον όρο ανοσία χαρακτηρίζεται η αντίσταση του οργανισµού στη νόσο, ιδιαίτερα στα λοιµώδη νοσήµατα. Το σύνολο των κυττάρων, ιστών και µορίων που διαµεσολαβούν στην αντίσταση έναντι των λοιµώξεων ονοµάζεται ανοσοποιητικό σύστηµα και η συντονισµένη αντίδραση αυτών των κυττάρων και µορίων έναντι των λοιµωδών παραγόντων καλείται ανοσολογική απάντηση. Η φυσιολογική λειτουργία του ανοσοποιητικού συστήµατος αποβλέπει στην παρεµπόδιση της λοιµώξεως και στην εκρίζωση της εγκατεστηµένης λοιµώξεως. Οι µηχανισµοί ανοσίας περιλαµβάνουν τη φυσική ανοσία, η οποία αποτελεί το αρχικό στάδιο της προστασίας έναντι της λοιµώξεως και την επίκτητη ανοσία, η οποία αναπτύσσεται βραδύτερα και αποτελεί το επόµενο και αποτελεσµατικότερο στάδιο αντιµετώπισης της λοιµώξεως. Ο όρος φυσική ανοσία αναφέρεται στο µηχανισµό, ο οποίος προϋπάρχει σε κατάσταση ετοιµότητας στα υγιή άτοµα, παρεµποδίζει την είσοδο των µικροβίων και ταχέως εξοντώνει τους µικροοργανισµούς, οι οποίοι επιτυγχάνουν να εισέλθουν στους ιστούς του ξενιστή. Η επίκτητη ανοσία είναι ο αµυντικός µηχανισµός που η λειτουργία του διεγείρεται από τους µικροοργανισµούς αφού διεισδύσουν στους ιστούς. Το πρώτο στάδιο της φυσικής ανοσίας, που παρεµποδίζει την είσοδο των µικροβίων στον οργανισµό, περιλαµβάνει το φυσικό φραγµό του δέρµατος, τα επιθηλιακά κύτταρα των βλεννογόνων και φυσικές αντιµικροβιακές ουσίες (όπως για παράδειγµα είναι η λυσοζύµη). Στην περίπτωση που ο µικροοργανισµός διαπεράσει στους ιστούς ή στην κυκλοφορία ακολουθεί το δεύτερο στάδιο της φυσικής ανοσίας που περιλαµβάνει τα φαγοκύτταρα (ουδετερόφιλα, µονοκύτταρα, µακροφάγα, δενδριτικά κύτταρα), τα εξειδικευµένα λεµφοκύτταρα, Natural Killer (NK), και τις πρωτεΐνες του ορού του αίµατος που αποτελούν το σύστηµα του συµπληρώµατος. Ο µηχανισµός της φυσικής ανοσίας δεν χαρακτηρίζεται από ειδικότητα, δηλαδή η αντίδρασή του είναι η ίδια ανεξάρτητα από τον παθογόνο παράγοντα. Επίσης, δεν καταλείπει µνήµη, δηλαδή επανάληψη της επαφής µε τον ίδιο παθογόνο παράγοντα δεν προκαλεί αυξηµένη αντίδραση ( ηµητρακόπουλος, 1994; Abbas & Lichtman, 2010). Η φυσική ανοσία αντιµετωπίζει επιτυχώς πολλούς µικροοργανισµούς που είναι παθογόνοι για τον άνθρωπο. Παρ όλα αυτά, άλλοι µικροοργανισµοί έχουν αναπτύξει παθογενετικούς µηχανισµούς µε τους οποίους αντιµετωπίζουν τη φυσική ανοσία. Η
32 32 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ άµυνα του ξενιστή εναντίον αυτών των λοιµωδών παραγόντων βασίζεται στην επίκτητη ανοσία. Ο µηχανισµός της επίκτητης ανοσίας επιτελείται από τα λεµφοκύτταρα, τα οποία χωρίζονται σε δύο βασικούς πληθυσµούς, τα Β και τα Τ λεµφοκύτταρα. Τα Β λεµφοκύτταρα µετά από διέγερση διαφοροποιούνται σε πλασµατοκύτταρα που παράγουν διαλυτές πρωτεΐνες, τα αντισώµατα, ενώ τα Τ λεµφοκύτταρα πολλαπλασιάζονται και διαφοροποιούνται σε δραστικά Τ λεµφοκύτταρα. Τα αντισώµατα εκκρίνονται στην κυκλοφορία και στα υγρά των βλεννογόνων και εξουδετερώνουν τα µικρόβια και τις µικροβιακές τοξίνες. Αυτό το σκέλος της επίκτητης ανοσίας καλείται χυµική ανοσία. Τα ενδοκυττάρια παθογόνα αντιµετωπίζονται από τα Τ λεµφοκύτταρα και το σκέλος αυτό καλείται κυτταρική ανοσία. Συγκεκριµένα, τα Τ λεµφοκύτταρα παράγουν διαλυτές ουσίες, τις κυτταροκίνες, οι οποίες ενεργοποιούν τα φαγοκύτταρα ώστε να καταστρέψουν τους παθογόνους µικροοργανισµούς οι οποίοι έχουν φαγοκυτταρωθεί, ενώ µία κατηγορία Τ λεµφοκυττάρων, τα κυτταροτοξικά, καταστρέφουν τα κύτταρα του ξενιστή µαζί µε το µικρόβιο που φέρουν στο κυτταρόπλασµά τους. Σε αντίθεση µε την φυσική ανοσία, η επίκτητη ανοσία χαρακτηρίζεται από ειδικότητα και µνήµη (Paul, 2008; Abbas & Lichtman, 2010). Τα κύτταρα του ανοσοποιητικού συστήµατος είναι οργανωµένα στα λεµφικά όργανα, τα οποία διαχωρίζονται σε κεντρικά και περιφερικά. Τα κεντρικά όργανα χρησιµεύουν για την ωρίµανση των κυττάρων του ανοσοποιητικού συστήµατος και περιλαµβάνουν το θύµο αδένα και το µυελό των οστών. Τα περιφερικά όργανα περιλαµβάνουν τους λεµφαδένες, το σπλήνα, τους λεµφικούς ιστούς των βλεννογόνων, όπως τις αµυγδαλές, το φαρυγγικό λεµφοειδή δακτύλιο (δακτύλιος του Waldeyer), τη σκωληκοειδή απόφυση, τις παϋέριες πλάκες του λεπτού εντέρου και το λεµφικό ιστό των βρογχιολίων. Στα συγκεκριµένα όργανα λαµβάνουν χώρα η αναγνώριση του µικροβιακού παράγοντα από τα κύτταρα της φυσικής ανοσίας και η διέγερση των κυττάρων της επίκτητης ανοσίας (Paul, 2008; Abbas & Lichtman, 2010). Κεντρικό ρόλο στη φυσική ανοσία διαδραµατίζουν τα φαγοκύτταρα, τα οποία αναγνωρίζουν και φαγοκυτταρώνουν τους µικροβιακούς παράγοντες. Η λειτουργία της φαγοκυττάρωσης αποτελεί, από φυλογενετική άποψη, τον παλαιότερο και βασικότερο αµυντικό µηχανισµό του οργανισµού εναντίον των µικροβίων και επιτελείται από τα εξειδικευµένα φαγοκύτταρα, δηλαδή τα ουδετερόφιλα πολυµορφοπύρηνα και το σύστηµα των µονοπυρήνων φαγοκυττάρων που περιλαµβάνει τα µονοκύτταρα του αίµατος και τα µακροφάγα των ιστών. Τα ουδετερόφιλα παράγονται στο µυελό των οστών και συνεχώς φέρονται στην
33 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ 33 κυκλοφορία σε τεράστιους αριθµούς. Στο µυελό των οστών υπάρχει πάντοτε παρακαταθήκη ωρίµων ουδετεροφίλων, τα οποία κινητοποιούνται και φθάνουν στην κυκλοφορία µέσα σε λίγες ώρες σε περίπτωση φλεγµονής ή µετά από εκτεταµένη νέκρωση των ιστών. Η διάρκεια ζωής των ουδετεροφίλων στην κυκλοφορία είναι µικρή (6 10 ώρες). Από το αίµα µεταναστεύουν στους ιστούς, ιδιαίτερα σε περιοχές όπου υπάρχει φλεγµονή, ή απλώς εξαφανίζονται πιθανώς αυτοκαταστρεφόµενα από τα ένζυµά τους. Μετά τη µετανάστευση στους ιστούς δεν επανέρχονται στην κυκλοφορία, µερικές φορές όµως εγκαταλείπουν την εστία της φλεγµονής µε τα απαγωγά λεµφαγγεία τις πρώτες ώρες µετά την έναρξη της φλεγµονής. Τα ουδετερόφιλα είναι τελικά κύτταρα, δε διαιρούνται και εµφανίζουν ελαττωµένη πρωτεϊνοσύνθεση. Η φαγοκυτταρική τους λειτουργία επιτελείται κυρίως στους ιστούς, αν και µερικές φορές φαγοκυτταρώνουν και όταν βρίσκονται στο αίµα, αφού πρώτα προσκολληθούν στο ενδοθήλιο των µικρών αγγείων, ιδιαίτερα των πνευµόνων. Η ωρίµανση των ουδετεροφίλων συνοδεύεται από την απόκτηση της ικανότητας να κινούνται και από πλαστικότητα, ιδιότητα που τους επιτρέπει να περνάνε µέσα από τα στενά κολπώµατα του µυελού και να φθάνουν στην κυκλοφορία. Τα µονοκύτταρα του αίµατος παράγονται στο µυελό των οστών και µετά τη µετανάστευσή τους στους ιστούς διαφοροποιούνται στα µακροφάγα κύτταρα των ιστών. Το σύστηµα των µονοπυρήνων φαγοκυττάρων περιλαµβάνει τη µονοβλάστη, τα προµονοκύτταρα, τα µονοκύτταρα του αίµατος, τα µακροφάγα των ιστών, τα κύτταρα Kupffer στο ήπαρ, τα µακροφάγα των κυψελίδων, του σπληνός, των λεµφαδένων, του συνδετικού ιστού, των οστών και του νευρικού ιστού. Τα µονοκύτταρα κυκλοφορούν για περισσότερο διάστηµα στο αίµα από τα ουδετερόφιλα και στη συνέχεια έρχονται στους ιστούς και συνιστούν τα µακροφάγα των ιστών. Ορισµένα από τα µακροφάγα των ιστών καθηλώνονται και αποτελούν συστατικά της δοµής των οργάνων στα οποία έχουν µεταναστεύσει. Η εντόπιση των µονοκυττάρων σε έναν ιστό έχει ως αποτέλεσµα τη διαφοροποίησή τους και την απόκτηση ιδιοτήτων που είναι χαρακτηριστικές για τα µακροφάγα του συγκεκριµένου ιστού. Έτσι, τα µακροφάγα των κυψελίδων εµφανίζουν οξειδωτική φωσφορυλίωση, ενώ τα µακροφάγα της περιτοναϊκής κοιλότητας χρησιµοποιούν τη γλυκόλυση για τις ενεργειακές τους ανάγκες. Τα µακροφάγα ζουν για µεγάλο χρονικό διάστηµα (µήνες), εµφανίζουν έντονη
34 34 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ πρωτεϊνοσύνθεση και µετά από διέγερση διαιρούνται ταχέως. Αν και ο αριθµός των µακροφάγων δεν είναι τόσο µεγάλος όσο ο αριθµός των ουδετεροφίλων, η διασπορά τους σε όλους τους ιστούς του σώµατος παίζει σηµαντικό ρόλο στην άµεση άµυνα του οργανισµού εναντίον της εισόδου των µικροβίων ( ηµητρακόπουλος, 1994; Abbas & Lichtman, 2010). Επιπροσθέτως, τα µακροφάγα των ιστών γεφυρώνουν τη φυσική µε την επίκτητη ανοσία. Μετά την αποδόµηση του µικροβιακού παράγοντα εντός του φαγοκυττάρου, µικροβιακά πεπτίδια συνδέονται µε µόρια του µείζονος συµπλέγµατος ιστοσυµβατότητος (Major Histocompatibility Complex, MHC) I και II και το σύµπλοκο προβάλει στην επιφάνεια της µεµβράνης του µακροφάγου. Ταυτόχρονα, τα διεγερµένα µακροφάγα εκφράζουν στην επιφάνειά τους συνδιεγερτικά µόρια (κυρίως τα µόρια B7.1 και B7.2) και εκκρίνουν στο περιβάλλον τους κυτταροκίνες. Τα Τ λεµφοκύτταρα φέρουν υποδοχέα (T Cell Receptor, TCR), ο οποίος συνδέεται µε το σύµπλοκο µικροβιακού πεπτιδίου µορίου MHC, ενώ άλλες πρωτεΐνες της επιφάνειας των Τ λεµφοκυττάρων (κυρίως το µόριο CD28) αντιδρούν µε τα συνδιεγερτικά µόρια του αντιγονοπαρουσιαστικού κυττάρου (µακροφάγου ή δενδριτικού κυττάρου). Η σύναψη των δύο κυττάρων οδηγεί στη διέγερση και την ωρίµανση του Τ λεµφοκυττάρου. Οι κυτταροκίνες που παράγονται από τα αντιγονοπαρουσιαστικά κύτταρα διεγείρουν, επίσης, τα Τ λεµφοκύτταρα και καθορίζουν την εξέλιξη της ωρίµανσής τους (Paul, 2008; Abbas & Lichtman, 2010). 1.2 Υποδοχείς της φυσικής ανοσίας Τα κύτταρα της φυσικής ανοσίας φέρουν υποδοχείς (Pattern Recognition Receptors, PRRs), οι οποίοι αναγνωρίζουν µοριακές δοµές που υποδηλώνουν την παρουσία κινδύνου για το µεγαλοοργανισµό, όπως για παράδειγµα είναι οι µικροβιακοί παράγοντες. Η ιδιότητα της αναγνώρισης των συγκεκριµένων µοριακών δοµών (προτύπων), επιτρέπει στο σύστηµα της φυσικής ανοσίας να χρησιµοποιεί περιορισµένο αριθµό υποδοχέων καθορισµένης ειδικότητας για την αναγνώριση πολύ µεγάλου αριθµού µοριακών δοµών του µικροβιακού κυττάρου. Οι πρότυπες δοµές των µικροβίων που αναγνωρίζονται από τους υποδοχείς της φυσικής ανοσίας PRRs καλούνται µοριακές δοµές που σχετίζονται µε τα παθογόνα (Pathogen Associated Molecular Patterns, PAMPs), είναι σταθερές σε διάφορες οµάδες µικροβίων και είναι απαραίτητες για τη φυσιολογική λειτουργία των µικροβίων. Αυτό έχει ως συνέπεια τα κύτταρα της φυσικής ανοσίας να αναγνωρίζουν λίγες βασικές δοµές από τις οποίες κάθε µικρόβιο θα έχει τουλάχιστον µία. Η ζωτική σηµασία αυτών των δοµών για το µικρόβιο καθιστά αδύνατη
35 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ 35 τη µεταβολή τους µέσω µεταλλάξεων ώστε ο µικροοργανισµός να αποφύγει την αναγνώριση από το σύστηµα της φυσικής ανοσίας (Beutler, 2004; Iwasaki & Medzhitov, 2010). Οι υποδοχείς της φυσικής ανοσίας PRRs διακρίνονται σε κατηγορίες µε βάση τη λειτουργία τους και την εντόπισή τους στο κύτταρο. Υπάρχουν διαλυτοί PRRs, όπως οι πρωτεΐνες οξείας φάσεως C αντιδρώσα πρωτεΐνη (CRP) και η λεκτίνη που προσδένει µαννάνη (Mannan Binding Lectin, MBL), οι οποίες δρουν ως οψωνίνες και αδρανοποιούν τον παθογόνο παράγοντα διαµέσου της ενεργοποίησης του συµπληρώµατος και των φαγοκυττάρων. Άλλη κατηγορία είναι οι διαµεµβρανικοί PRRs στους οποίους περιλαµβάνονται οι υποδοχείς scavenger, οι C-type λεκτίνες και η οικογένεια των Toll Like υποδοχέων (TLRs). Οι δύο πρώτοι από τους παραπάνω δρουν ως υποδοχείς του φαγοκυττάρου για να ενισχύσουν την πρόσληψη του µικροβίου, ενώ οι C-type λεκτίνες έχουν, επιπλέον, την ικανότητα να µεταδίδουν σήµατα ενδοκυτταρίως. Οι TLRs είναι υποδοχείς µετάδοσης σηµάτων που ενεργοποιούν την έκφραση γονιδίων µε αποτέλεσµα να οδηγούν στην ωρίµανση των δενδριτικών κυττάρων και στην παραγωγή προφλεγµονωδών κυτταροκινών και ιντερφερονών τύπου I (IFNα, IFNβ). Τέλος, µία τρίτη κατηγορία είναι οι ενδοκυττάριοι PRRs, που είναι εξειδικευµένοι υποδοχείς για την αναγνώριση βακτηρίων και ιών. Συγκεκριµένα, η οικογένεια των NOD like υποδοχέων (NOD Like Receptors, NLRs) επάγει την παραγωγή προφλεγµονωδών κυτταροκινών αφού αναγνωρίσει στοιχεία του κυτταρικού τοιχώµατος των βακτηρίων (όπως η πεπτιδογλυκάνη) στο κυτταρόπλασµα και συνεργάζεται µε τους TLRs. Η ελικάση RIG-I αναγνωρίζει νουκλεϊνικά οξέα ιών και προάγει την παραγωγή ιντερφερονών τύπου I (Janeway & Medzhitov, 2002; Hargreaves & Medzhitov, 2005; Kawai & Akira, 2011). Η παρουσία ποικίλων PRRs και η διαφορετική κυτταρική εντόπισή τους επιτρέπει στο κύτταρο να ανιχνεύσει µεγάλο αριθµό µικροβιακών παραγόντων ασκώντας εποπτεία σε διάφορα κυτταρικά διαµερίσµατα και παράλληλα καθορίζει τον καταλληλότερο τρόπο προστασίας του. Επιπλέον, διαφορετικοί PRRs µπορούν να συνεργαστούν όταν διεγείρονται ταυτοχρόνως ή διαδοχικά κατά τη διάρκεια µίας λοιµώξεως µε αποτέλεσµα ανοσολογική απάντηση που διαφέρει από εκείνη που προκύπτει από τη µεµονωµένη ενεργοποίηση των ίδιων PRRs. Τέλος, η ετερογένεια των ανοσολογικών αποκρίσεων εξαρτάται από τη διαφορά στην έκφραση όσον αφορά στο είδος ή στην ποσότητα των PRRs σε διαφορετικούς κυτταρικούς πληθυσµούς (Palm & Medzhitov, 2009; Schenten & Medzhitov, 2011).
36 36 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 1.3 Toll like receptors Οι υποδοχείς TLRs είναι διαµεµβρανικές πρωτεΐνες που στο αµινοτελικό τους άκρο φέρουν αλληλουχίες αµινοξέων πλούσιες σε λευκίνη (Leucine Rich Repeats, LRR), οι οποίες είναι υπεύθυνες για την αναγνώριση των PAMPs. Το κυτταροπλασµατικό τους άκρο φέρει την περιοχή TIR, η οποία είναι κοινή για την οικογένεια των TLRs και των υποδοχέων της IL-1 (Toll / Interleukin 1 Receptor domain, TIR) και είναι υπεύθυνη για την ενδοκυττάρια σηµατοδότηση του υποδοχέα (Εικόνα 1). Κάθε µέλος της οικογένειας των TLRs αναγνωρίζει διαφορετικές δοµές (Imler & Hoffmann, 2001; Beutler et al., 2006; Kang & Lee, 2011). Ο υποδοχέας TLR2 αναγνωρίζει ποικιλία µικροβιακών συστατικών, στα οποία περιλαµβάνονται λιποπρωτεΐνες / λιποπεπτίδια από διάφορα παθογόνα µικρόβια, πεπτιδογλυκάνη και λιποτειχοϊκό οξύ από τα Gram θετικά βακτήρια, λιποαραβινοµαννάνη των µυκοβακτηριδίων, γλυκοζυλο φωσφατιδυλο ινοσιτόλη του παρασίτου Trypanosoma cruzi, έναν παράγοντα διαλυτό στις φαινόλες του Staphylococcus epidermidis, ζυµοζάνη των µυκήτων και γλυκολιπίδια του Treponema maltofilum. Επίσης, αναγνωρίζει τον LPS από µη εντεροβακτηριοειδή, όπως η Leptospira interrogans και η Porphyromonas gingivalis. Οι συγκεκριµένοι LPS διαφέρουν δοµικά από τον τυπικό LPS των Gram αρνητικών βακτηρίων, ο οποίος αναγνωρίζεται από τον TLR4, ως προς τον αριθµό των ακυλικών αλυσίδων του λιπιδίου A και πιθανώς η διαφορά αυτή ευθύνεται για το διαφορετικό τρόπο αναγνώρισης (Kawai & Akira, 2005; Kumar et al., 2011). Έχουν προταθεί δύο θεωρίες που προσπαθούν να εξηγήσουν το λόγο για τον οποίο ο TLR2 αναγνωρίζει µεγάλο αριθµό µικροβιακών συστατικών. Η πρώτη εξήγηση είναι ότι ο TLR2 σχηµατίζει ετεροδιµερή µε τους υποδοχείς TLR1 και TLR6. Συγκεκριµένα, είναι γνωστό ότι οι TLR1 ή TLR6 σχηµατίζουν ένα λειτουργικό σύµπλοκο µε τον TLR2 και αναγνωρίζουν τριακυλο- ή διακυλο- λιποπεπτίδια, αντιστοίχως. Η δεύτερη εξήγηση είναι ότι ο TLR2 συνεργάζεται λειτουργικά µε άλλους τύπους υποδοχέων της φυσικής ανοσίας, όπως η λεκτίνη Dectin-1 που αναγνωρίζει το συστατικό του κυτταρικού τοιχώµατος των µυκήτων, β-γλυκάνη (Trinchieri & Sher, 2007; Kawai & Akira, 2010; Tannahill & O Neill, 2011).
37 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ 37 Εικόνα 1: Η σηµατοδοτική οδός των υποδοχέων της φυσικής ανοσίας TLRs Ο υποδοχέας TLR4 είναι το πρώτο µέλος της οικογένειας των TLRs που ανακαλύφθηκε κατά τη µελέτη της σηψαιµίας από Gram αρνητικά βακτήρια και αναγνωρίζει τον LPS. Η ενεργοποίηση του TLR4 από τον LPS προϋποθέτει τη σύνδεση του LPS µε την πρωτεΐνη του ορού LBP (LPS Binding Protein), τη µεταφορά του στο επιφανειακό µόριο CD14 και την παρουσία της πρωτεΐνης MD2, ώστε να σχηµατιστεί ένα σύµπλοκο. Επίσης, ο TLR4 αναγνωρίζει ενδογενή µόρια, όπως οι πρωτεΐνες θερµικής καταπληξίας (Hsp60, Hsp70), οι ινοδονεκτίνες, οι ολιγοσακχαρίτες του υαλουρονικού οξέος, η θειική ηπαράνη και το ινωδογόνο, αλλά µε την προϋπόθεση ότι βρίσκονται σε υψηλές συγκεντρώσεις. Τέλος, ο TLR4 αναγνωρίζει το φυτικό παράγωγο, που χρησιµοποιείται ως αντικαρκινικό φάρµακο (Paclitaxel), ταξόλη.
38 38 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Ο TLR5 αναγνωρίζει την πρωτεΐνη flagellin, η οποία συνιστά τη βλεφαρίδα των βακτηρίων. Σε αντίθεση µε άλλους PAMPs, οι οποίοι είναι χαρακτηριστικοί της δοµής των παθογόνων, η flagellin ως πρωτεΐνη δεν έχει τα χαρακτηριστικά του ξένου για το µεγαλοοργανισµό. Όµως, καθώς είναι εξαιρετικά συντηρηµένη στα αµινοτελικό και καρβοξυτελικό άκρα της, αναγνωρίζεται από τον TLR5 σ αυτές τις περιοχές. Ο TLR5 εκφράζεται στα επιθήλια του εντερικού σωλήνα και του πνεύµονα, γεγονός που αναδεικνύει τη σηµασία του στην αναγνώριση παθογόνων παραγόντων στους βλεννογόνους αυτών των περιοχών. Ο TLR9 αναγνωρίζει µη µεθυλιωµένο DNA στις περιοχές κυτοσίνης φωσφορικής οµάδας γουανοσίνης (CpG). Το συγκεκριµένο DNA είναι παρόν σε βακτήρια και σε DNA ιούς λόγω της έλλειψης των καταλλήλων ενζύµων, ενώ τα ευκαρυωτικά κύτταρα φέρουν µεθυλιωµένο DNA. Ο TLR3 αναγνωρίζει ιικό dsrna. Οι TLR7 και 8 αναγνωρίζουν τα συνθετικά ανάλογα imidazoquinoline και loxoribine, τα οποία εµφανίζουν δοµική οµοιότητα µε την γουανοσίνη. Πιθανολογείται ότι η φυσιολογική τους λειτουργία είναι η αναγνώριση µονόκλωνου RNA (ssrna) των ιών. Επειδή µόρια ssrna του ξενιστού αφθονούν στα κύτταρα, ο διαχωρισµός του ιικού ssrna από αυτό του ξενιστή πραγµατοποιείται µε την εντόπιση των υποδοχέων αυτών στο ενδόσωµα, από το οποίο απουσιάζει το ssrna του κυττάρου (Kawai & Akira, 2005; Kumar et al., 2011). Οι υποδοχείς TLR εντοπίζονται σε διαφορετικά κυτταρικά διαµερίσµατα. Οι TLR1, 2, 4, 5 και 6 εκφράζονται στην επιφάνεια της κυτταροπλασµατικής µεµβράνης του κυττάρου και αναγνωρίζουν συστατικά της επιφάνειας των βακτηρίων. Οι TLR3, 7, 8 και 9 εκφράζονται σε ενδοκυττάρια διαµερίσµατα, όπως τα ενδοσώµατα. Μάλιστα, η αναγνώριση από τους TLR3, 7 και 9 προϋποθέτει την ωρίµανση του ενδοσώµατος. Τα dsrna, ssrna και CpG DNA προκύπτουν µετά την αποδόµηση των παθογόνων και καταλήγουν στα φαγοσώµατα-λυσοσώµατα ή στα ενδοσώµατα-λυσοσώµατα όπου λαµβάνει χώρα η αναγνώριση από τους αντίστοιχους TLRs. Σηµειώνεται ότι ο TLR2, αν και εκφράζεται στην επιφάνεια του κυττάρου, µετακινείται επίσης στο φαγόσωµα των µακροφάγων, αφού προηγουµένως αναγνωρίσει τη ζυµοζάνη των µυκήτων. Συνεπώς, τα διαµερίσµατα του φαγοσώµατος-λυσοσώµατος ή του ενδοσώµατος-λυσοσώµατος πιθανώς να αποτελούν τις κύριες περιοχές για την αναγνώριση των µικροβιακών συστατικών από τους TLRs. Επιπλέον, οι TLRs εµπλέκονται σε αυτήν καθ αυτήν τη διαδικασία της φαγοκυττάρωσης. Συγκεκριµένα, έχει αποδειχθεί ότι οι υποδοχείς TLR2 και TLR4, καθώς και το σηµατοδοτικό µόριο MyD88, είναι απαραίτητα για την
39 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ 39 ωρίµανση του φαγοσώµατος (Kumar et al., 2011). Μετά την διέγερση των TLRs από τα µικροβιακά συστατικά, ακολουθεί η ενδοκυττάρια σηµατοδότηση από το τµήµα των υποδοχέων που φέρει την περιοχή TIR. Την ενδοκυττάρια σηµατοδότηση διαµεσολαβούν πρωτεΐνες του κυτταροπλάσµατος που φέρουν επίσης την περιοχή TIR. Οι περιοχές TIR των TLRs και των κυτταροπλασµατικών πρωτεϊνών αλληλεπιδρούν και οδηγούν στη σταθερή προσκόλλησή τους. Οι συγκεκριµένες πρωτεΐνες είναι οι MyD88 (Myeloid Differentiation primary response gene µε µοριακό βάρος 88kDa), TIRAP (TIR domain containing Adaptor Protein), TRIF (TIR domain containing adaptor inducing IFNβ) και TRAM (TRIF Related Adaptor Molecule). Η σηµατοδότηση διαµέσου του MyD88 είναι κοινή για όλους τους TLRs εκτός από τον TLR3 και οδηγεί στην παραγωγή προφλεγµονωδών κυτταροκινών. Στην περίπτωση των TLR2 και TLR4 είναι απαραίτητη η πρωτεΐνη TIRAP για να γεφυρωθεί η σύνδεσή τους µε το µόριο MyD88. Η πρωτεΐνη TRIF είναι υπεύθυνη για µία σηµατοδοτική οδό που είναι ανεξάρτητη από την οδό της πρωτεΐνης MyD88 και οδηγεί στην παραγωγή ιντερφερονών τύπου I. Η οδός αυτή αφορά στους υποδοχείς TLR3 και TLR4 αλλά στην περίπτωση του TLR4 απαιτείται η µεσολάβηση του µορίου TRAM. Η σύνδεση του MyD88 µε το ενδοκυττάριο τµήµα των TLRs οδηγεί σε αλληλεπίδραση µε την πρωτεΐνη IRAK4 (IL-1 Receptor Associated Kinase 4) και διευκολύνει τη φωσφορυλίωση της πρωτεΐνης IRAK1 που έχει προσδεθεί στην IRAK4. Η φωσφορυλιωµένη IRAK1 σχηµατίζει σύµπλοκο µε την TRAF6 (TNF Receptor Associated Factor 6) και προάγει την ενεργοποίηση δύο διαφορετικών σηµατοδοτικών οδών. Η πρώτη καταλήγει στην ενεργοποίηση του µεταγραφικού παράγοντα AP-1 (Activator Protein-1) διαµέσου της φωσφορυλίωσης της οικογένειας των MAP (Mitogen-Activated Protein) κινασών. Η άλλη οδός προάγει την αποδόµηση της πρωτεΐνης IκB (Inhibitor κβ) µε τελικό αποτέλεσµα τη µετατόπιση του µεταγραφικού παράγοντα NFκB (Nuclear Factor κ-light-chain-enhancer of activated B cells) στον πυρήνα. Η από κοινού δράση των δύο µεταγραφικών παραγόντων προκαλεί την έκφραση των γονιδίων που κωδικοποιούν την παραγωγή προφλεγµονωδών κυτταροκινών (IL-1β, IL-6, TNF-α, IL-12/p40), και χηµειοτακτικών παραγόντων για τα φαγοκύτταρα (IL-8, MIP-1) (Beutler et al., 2006; Kawai & Akira, 2010; Schenten & Medzhitov, 2011). Η σύνδεση της πρωτεΐνης TRIF στους ενεργοποιηµένους TLR3 και TLR4 προκαλεί τη δηµιουργία συµπλόκου µε το µόριο TRAF3, το οποίο µε τη σειρά του ενεργοποιεί την κινάση TBK1 (TANK Binding Kinase 1). Η συγκεκριµένη κινάση έχει
40 40 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ ως υπόστρωµα το µεταγραφικό παράγοντα IRF3 (Interferon Regulatory Factor 3) και τον ενεργοποιεί µετά από φωσφορυλίωσή του. Ο φωσφορυλιωµένος IRF3 µετατοπίζεται στον πυρήνα του κυττάρου και προάγει την έκφραση των γονιδίων για την παραγωγή ιντερφερονών τύπου I (IFNβ και σε δεύτερο χρόνο IFNα), χηµειοτακτικών παραγόντων για τα Τ λεµφοκύτταρα (IP-10, MIG) και συνδιεγερτικών µορίων (B7.1, B7.2, CD40) (Honda & Taniguchi, 2006). 1.4 MAP κινάσες Η αναγνώριση των παθογόνων αρχίζει στο επίπεδο του υποδοχέα στην επιφάνεια του κυττάρου αλλά οι ενδοκυττάριοι σηµατοδοτικοί παράγοντες µετά τον υποδοχέα και η αλληλεπίδραση µεταξύ τους καθορίζουν τα τελικά χαρακτηριστικά της ανοσολογικής απάντησης. Κεντρική σηµατοδοτική οδό των ενεργοποιηµένων κυττάρων του ανοσοποιητικού συστήµατος αποτελεί η οδός των MAP κινασών. Οι πρωτεϊνικές κινάσες είναι ένζυµα που συνδέουν οµοιοπολικά ένα µόριο φωσφόρου στα αµινοξέα σερίνη, θρεονίνη ή τυροσίνη µίας πρωτεΐνης. Η φωσφορυλίωση αυτή µπορεί να έχει ως αποτέλεσµα τη ρύθµιση της ενζυµικής δραστικότητας της πρωτεΐνης, την αλληλεπίδρασή της µε άλλα πρωτεϊνικά µόρια ή τον καθορισµό της εντόπισής της και του προσανατολισµού της µέσα στο κύτταρο. Η ενεργοποίηση των TLRs χρησιµοποιεί την οικογένεια των κινασών σερίνης, θρεονίνης MAP για τη µετάδοση του ενδοκυττάριου σήµατος (Huang et al., 2009). Οι τέσσερις καλύτερα χαρακτηρισµένες υποοικογένειες των MAP κινασών είναι οι ERK ½ (Extracellular signal-regulated Kinase), JNK 1,2,3 (c-jun NH 2 -terminal Kinase), p38 α/β/γ/δ και ERK5. Οι υποοικογένειες των JNK και p38 ενεργοποιούνται από το κυτταρικό stress και συναποτελούν την οµάδα των SAPK (Stress Activated Protein Kinase). Η ενεργοποίηση των MAP κινασών προϋποθέτει την ταυτόχρονη φωσφορυλίωσή τους στα αµινοξέα τους θρεονίνη και τυροσίνη της αλληλουχίας Thr- Xaa-Tyr, όπου Thr είναι το αµινοξύ θρεονίνη, Tyr το αµινοξύ τυροσίνη και Xaa το αµινοξύ γλουταµικό οξύ, γλυκίνη ή προλίνη στις ERK, p38 και JNK, αντιστοίχως. Η φωσφορυλίωση των MAP κινασών επιτυγχάνεται κατά τη διάρκεια ενός σηµατοδοτικού καταρράκτη από µία κινάση των MAP κινασών (MAPK Kinase ή MAP2K), η οποία έχει φωσφορυλιωθεί από µία κινάση της MAPKK (MAPKK Kinase ή MAP3K, Εικόνα 2). Μέχρι σήµερα έχουν περιγραφεί περισσότερες από είκοσι MAP3K στα κύτταρα των θηλαστικών και η κάθε µία ανταποκρίνεται σε διαφορετικά σήµατα. Μετά τη φωσφορυλίωσή τους οι MAP κινάσες ρυθµίζουν βασικές κυτταρικές λειτουργίες στο
41 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ 41 κυτταρόπλασµα διαµέσου φωσφορυλίωσης µεµβρανικών και κυτταροπλασµατικών πρωτεϊνών και στοιχείων του κυτταροσκελετού. Επίσης, οι ενεργοποιηµένες MAP κινάσες µετατοπίζονται στον πυρήνα για να φωσφορυλιώσουν µεταγραφικούς παράγοντες µε σκοπό τη ρύθµιση της έκφρασης διαφόρων γονιδίων (Liu et al., 2007). Εικόνα 2: Η σηµατοδοτική οδός των MAP κινασών Η σηµατοδοτική οδός των ERK ½ πυροδοτείται από επιφανειακούς υποδοχείς όπως οι συνδεδεµένοι µε κινάσες της τυροσίνης και οι υποδοχείς που συνδέονται µε G πρωτεΐνες. Η µετάδοση του σήµατος γίνεται από τον καταρράκτη που περιλαµβάνει τις µικρές πρωτεΐνες Ras και Raf που προσδένουν µόρια GTP, ακολουθεί η φωσφορυλίωση των MAP2K MEK1 και MEK2 που στη συνέχεια φωσφορυλιώνουν τις ERK ½. Η ενεργοποίηση των ERK ½ οδηγεί στη συγκέντρωσή τους στον πυρήνα. Οι ERK ½ φωσφορυλιώνουν µεγάλο αριθµό υποστρωµάτων σε όλα τα διαµερίσµατα του κυττάρου, µεταξύ των οποίων περιλαµβάνονται µεµβρανικές πρωτεΐνες, οι µεταγραφικοί παράγοντες c-myc, c-fos, NFAT, MEF2, Elk1 και STAT3, πρωτεΐνες του κυτταροσκελετού και άλλες κινάσες. Το σηµατοδοτικό µονοπάτι των ERK ½ παίζει
42 42 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ κεντρικό ρόλο στις λειτουργίες της ωρίµανσης, του πολλαπλασιασµού και της επιβίωσης του κυττάρου (Roux & Blenis, 2004). Η σηµατοδοτική οδός της p38 ενεργοποιείται από ποικίλους φυσικούς και χηµικούς στρεσογόνους παράγοντες, όπως οι ελεύθερες ρίζες οξυγόνου, η υπεριώδης ακτινοβολία και η ισχαιµία και από κυτταροκίνες όπως η IL-1 και ο TNF-α. Η µετάδοση του σήµατος επιτυγχάνεται από τις κινάσες MEK3 και MEK6, οι οποίες έχουν µεγάλη ειδικότητα για την p38 και δε φωσφορυλιώνουν τις ERK ½ και JNK. Επιπλέον, η p38 φωσφορυλιώνεται από την κινάση της JNK, MEK4. Η ενεργοποιηµένη p38 έχει ως κυτταρικά υποστρώµατα την κυτταροπλασµατική φωσφολιπάση Α2, πρωτεΐνες των µικροσωληνίσκων, τους µεταγραφικούς παράγοντες ATF1 και 2, MEF2, Elk1, NFκB, p53 και άλλες κινάσες. Η δράση της p38 είναι σηµαντική στη φυσιολογική ανοσολογική και φλεγµονώδη απόκριση. Συµµετέχει στις λειτουργίες των µακροφάγων και των ουδετεροφίλων πολυµορφοπυρήνων που περιλαµβάνουν την παραγωγή ελευθέρων ριζών οξυγόνου, τη χηµειοταξία, την αποκοκκίωση των ουδετεροφίλων, την προσκολλητικότητα και την απόπτωση. Επίσης, ρυθµίζει την έκφραση της παραγωγής κυτταροκινών, µεταγραφικών παραγόντων και µεµβρανικών υποδοχέων, µέσω σταθεροποίησης των mrna τους (Roux & Blenis, 2004; Huang et al., 2009). Η σηµατοδοτική οδός της JNK ενεργοποιείται από κυτταροκίνες, υπεριώδη ακτινοβολία, έλλειψη αυξητικών παραγόντων, παράγοντες επιβλαβείς για το DNA και σε µικρότερο βαθµό από υποδοχείς συνδεδεµένους µε G πρωτεΐνες, ορό και αυξητικούς παράγοντες. Οι κινάσες MEK4 και MEK7 είναι υπεύθυνες για τη φωσφορυλίωση και την ενεργοποίηση της JNK. Η MEK4 ενεργοποιείται κυρίως σε συνθήκες περιβαλλοντικού stress, ενώ η MEK7 κυρίως από κυτταροκίνες. Η φωσφορυλιωµένη JNK µεταναστεύει στον πυρήνα και έχει ως υπόστρωµα άλλες κινάσες και τους µεταγραφικούς παράγοντες c-jun, ATF2, NFAT και STAT3. Η δράση της JNK είναι ουσιώδης για τον πολλαπλασιασµό και τη ρύθµιση της απόπτωσης του κυττάρου (Huang et al., 2009). 1.5 Μεταγραφικοί παράγοντες Μεταγραφικοί παράγοντες ονοµάζονται οι πρωτεΐνες οι οποίες συνδέονται µε συγκεκριµένη αλληλουχία του DNA και ελέγχουν τη µεταγραφή γονιδίων από DNA σε mrna. Οι µεταγραφικοί παράγοντες δρουν µόνοι τους ή σε σύµπλεγµα µε άλλες πρωτεΐνες και µπορούν να ενεργοποιούν ή να αναστέλλουν την πρόσδεση της RNA πολυµεράσης, η οποία είναι υπεύθυνη για τη µεταγραφή, σε διάφορα γονίδια. Οι θέσεις
43 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ 43 σύνδεσης των µεταγραφικών παραγόντων στο DNA καλούνται υποκινητές (promoters), ενισχυτές (enhancers) ή αποσιωπητές (silencers). Η πρόσδεση στους υποκινητές προάγει τη µεταγραφή του παρακείµενου γονιδίου, η πρόσδεση στους ενισχυτές δρα επικουρικά και ενισχύει τη δραστικότητα γειτονικών µεταγραφικών παραγόντων, ενώ η πρόσδεση στους αποσιωπητές την καταστέλλει (Latchman, 2008) NFκΒ Ο µεταγραφικός παράγοντας NFκB αποτελεί µία οικογένεια από πρωτεΐνες που παίζουν σηµαντικό ρόλο στην ανοσία, τη φλεγµονή και τον κυτταρικό πολλαπλασιασµό, διαφοροποίηση και επιβίωση. Η ενεργοποίηση του NFκB ακολουθεί την αποδόµηση στο πρωτεόσωµα των πρωτεϊνών ΙκΒ, οι οποίες τον διατηρούν σε αδρανή µορφή στο κυτταρόπλασµα. Η αποδόµηση των ΙκΒ πρωτεϊνών γίνεται µετά από φωσφορυλίωσή τους από το σύµπλοκο των κινασών των ΙκΒ (ΙκΒ kinase, IKK). Η δραστικότητα του NFκB ρυθµίζεται µε ποικιλία µετα-µεταγραφικών τροποποιήσεών του (Oeckinghaus & Ghosh, 2009). Ο µεταγραφικός παράγοντας NFκΒ εκφράζεται σχεδόν στο σύνολο των κυττάρων και ιστών. Ειδικές θέσεις δέσµευσής του υπάρχουν στους υποκινητές µεγάλου αριθµού γονιδίων. Η ενεργοποίησή του προκαλείται από βακτήρια και ιούς, φλεγµονώδεις κυτταροκίνες, από υποδοχείς των Β και Τ λεµφοκυττάρων που έχουν προσδεθεί µε αντιγόνα και από στρεσογόνους παράγοντες του κυττάρου, όπως η υπεριώδης και η γ ακτινοβολία, η ισχαιµία και οι ελεύθερες ρίζες οξυγόνου. Μετά την ενεργοποίησή του ο NFκΒ µετατοπίζεται στον πυρήνα του κυττάρου και ελέγχει την έκφραση γονιδίων που κωδικοποιούν µόρια του µείζονος συµπλέγµατος ιστοσυµβατότητος MHC, τον υποδοχέα των Τ λεµφοκυττάρων TCR, ανοσοσφαιρίνες, ιντερλευκίνες, χηµειοκίνες, µόρια προσκόλλησης, πρωτεΐνες του συµπληρώµατος, πρωτεΐνες οξείας φάσης και ρυθµιστικές πρωτεΐνες της απόπτωσης, του πολλαπλασιασµού και της επιβίωσης του κυττάρου. Επιπλέον, έχει σηµαντικό ρόλο στις λειτουργίες της εµβρυικής ανάπτυξης και τη φυσιολογική λειτουργία των οστών, του δέρµατος και του κεντρικού νευρικού συστήµατος. Τέλος, ο NFκΒ προάγει την παραγωγή πρωτεϊνών που ρυθµίζουν τη δράση του µε αποτέλεσµα τη δηµιουργία µηχανισµού ανατροφοδότησης (Oeckinghaus & Ghosh, 2009; Dev et al., 2011). Η οικογένεια του µεταγραφικού παράγοντα NFκΒ αποτελείται από πέντε πρωτεΐνες, την p65(rela), τη RelB, τη c-rel, την p105/p50 (NFκB1) και την p100/p52 (NFκB2), οι οποίες σχηµατίζουν µεταξύ τους δραστικά οµο- ή ετερο- διµερή σύµπλοκα.
44 44 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Στο αµινοτελικό τους άκρο φέρουν την περιοχή Rel Homology Domain (RHD), η οποία είναι υπεύθυνη για το διµερισµό τους, για τη σύνδεση µε το DNA, για τη σύνδεση µε τις πρωτεΐνες ΙκΒ και για τη µετατόπισή τους στον πυρήνα. Οι p65, RelB και c-rel φέρουν στο καρβοξυτελικό άκρο µία περιοχή (TransActivation Domain, TAD) που τους επιτρέπει να αλληλεπιδρούν µεταξύ τους, µε άλλους µεταγραφικούς παράγοντες ή µε ρυθµιστικά µόρια όταν είναι προσδεδεµένοι στο DNA. Από την πρωτεολυτική διάσπαση του καρβοξυτελικού άκρου των p105 και p100 προκύπτουν τα µεταγραφικώς δραστικά µόρια p50 και p52, αντιστοίχως. Τα p50 και p52 σχηµατίζουν διµερή µεταξύ τους ή µε τα µόρια p65, RelB και c-rel και συχνότερα απαντάται στο κύτταρο το ετεροδιµερές p50/p65 (Li & Verma, 2002; Ghosh & Hayden, 2008). Εικόνα 3: Η σηµατοδοτική οδός του µεταγραφικού παράγοντα NFκΒ Σε κατάσταση ηρεµίας στα κύτταρα, τα διµερή των πρωτεϊνών NFκΒ είναι συνδεδεµένα µε µία από τις πρωτεΐνες της οικογένειας των αναστολέων του κβ (ΙκΒ), οι οποίες καθορίζουν την εντόπισή του στο κυτταρόπλασµα (Εικόνα 3). Η οικογένεια των πρωτεϊνών ΙκΒ χαρακτηρίζεται από την παρουσία πέντε έως επτά περιοχών αλληλουχιών αγκυρίνης, οι οποίες διαµεσολαβούν την αλληλεπίδραση τους µε την περιοχή RHD των πρωτεϊνών NFκΒ. Τα συχνότερα µέλη της οικογένειας των ΙκΒ είναι οι ΙκΒα, ΙκΒβ και ΙκΒε, ενώ και οι πρόδροµες µορφές των NFκΒ πρωτεϊνών p105 και p100 περιέχουν περιοχές αγκυρίνης και συνεπώς έχουν όµοια δράση µε εκείνη των ΙκΒ πρωτεϊνών (Li & Verma, 2002; Ghosh & Hayden, 2008; Dev et al., 2011). Η πρωτεΐνη ΙκΒα παράγεται ταχέως µετά τη µετατόπιση του NFκΒ στον πυρήνα και την ενεργοποίηση της µεταγραφής της, αποτελώντας σηµαντικό µηχανισµό αρνητικής ρύθµισης. Η ΙκΒβ προσδένεται στο σύµπλοκο του NFκΒ µε το DNA, ρυθµίζοντας τη λειτουργία του στον πυρήνα. Η ΙκΒε παρουσιάζει οµοιότητες µε την ΙκΒβ, αλλά η έκφραση και η λειτουργία της φαίνεται να περιορίζονται σε κύτταρα του αιµοποιητικού συστήµατος. Η πρωτεΐνη p105 διασπάται µε σταθερό ρυθµό προς p50 σε κύτταρα που βρίσκονται σε κατάσταση ηρεµίας, αλλά µπορεί να διασπαστεί πλήρως παρουσία εξωτερικού ερεθίσµατος. Η p100 πρωτεολύεται µερικώς, µόνο σε κύτταρα που έχουν ενεργοποιηθεί, ώστε να σχηµατιστεί η δραστική p52 (Oeckinghaus & Ghosh,
45 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ; Dev et al., 2011). Παρουσία εξωτερικού ερεθίσµατος, οι πρωτεΐνες ΙκΒ φωσφορυλιώνονται από ένα σύµπλοκο πρωτεϊνών µε ιδιότητα κινάσης. Το σύµπλοκο αποτελείται από δύο καταλυτικές υποµονάδες, τις πρωτεΐνες ΙΚΚα και ΙΚΚβ και από µία ρυθµιστική υποµονάδα, την ΙΚΚγ. Η ενεργοποίηση από προφλεγµονώδεις κυτταροκίνες, παθογόνους µικροοργανισµούς και υποδοχείς που έχουν συνδέσει αντιγόνα, οδηγεί σε φωσφορυλίωση των πρωτεϊνών ΙκΒ διαµέσου της υποµονάδας ΙΚΚβ µε συµµετοχή της ρυθµιστικής ΙΚΚγ. Αντίθετα, η ενεργοποίηση του κυττάρου από τη λεµφοτοξίνη β ή τον υποδοχέα του µορίου CD40 οδηγεί σε ενεργοποίηση των ΙκΒ διαµέσου µόνο της υποµονάδας ΙΚΚα (Oeckinghaus & Ghosh, 2009; Dev et al., 2011). Με δεδοµένη τη µεγάλη σηµασία του NFκΒ σε πολλές βιολογικές λειτουργίες, η ισορροπηµένη ρύθµισή του είναι ουσιώδης ώστε να αποφευχθούν ανεπανόρθωτες για τον οργανισµό δυσλειτουργίες. Η συγκεκριµένη ρύθµιση περιλαµβάνει ποικιλία µετα- µεταγραφικών τροποποιήσεων, όπως η φωσφορυλίωση, η προσθήκη ουµπικουιτίνης και η ακετυλίωση σε όλα τα στάδια της ενεργοποίησής του (Ghosh & Hayden, 2008; Dev et al., 2011). Ο NFκΒ επάγει την παραγωγή της πρωτεΐνης Α20 ή TNFAIP3 (TNF-α Induced Protein 3), η οποία παρεµβαίνει στη διαδικασία προσθήκης ουµπικουιτίνης των ΙΚΚ πρωτεϊνών µε αποτέλεσµα την απενεργοποίηση του NFκΒ µε µηχανισµό αρνητικής ανατροφοδότησης (Liew et al., 2005; Sun, 2008; Coornaert et al., 2009). Η πρωτεΐνη Α20 ρυθµίζεται και υποβοηθείται από την οµάδα των πρωτεϊνών ΑΒΙΝ (Α20 Binding Inhibitor of NFκB 1, 2 και 3) ή TNIP (TNFAIP3 Interacting Protein 1, 2 και 3), η οποία περιλαµβάνει τρία µέλη (Verstrepen et al., 2009) AP-1 Ο µεταγραφικός παράγοντας AP-1 συµµετέχει σε πλήθος κυτταρικών λειτουργιών µεταξύ των οποίων είναι ο πολλαπλασιασµός, ο θάνατος, η επιβίωση και η διαφοροποίηση των κυττάρων και εµπλέκεται σε ποικιλία φυσιολογικών και παθολογικών διεργασιών, όπως η ανάπτυξη των νευρικών κυττάρων, ανοσολογικές και φλεγµονώδεις αποκρίσεις και η ογκογένεση (Shaulian & Karin, 2002; Meng & Xia, 2011). Ο µεταγραφικός παράγοντας AP-1 αποτελείται από το σχηµατισµό διµερών των οικογενειών πρωτεϊνών Jun (c-jun, JunB and JunD), Fos (c-fos, FosB, Fra1 και Fra2), ATF (ATF2, ATF3/LRF1, B-ATF, JDP1 και JDP2) και musculoaponeurotic fibrosarcoma (MAF; c-maf, MafB, MafA, MafG/F/K και Nrl; Hai et al., 1988; Angel &
46 46 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Karin, 1991). Οι πρωτεΐνες αυτές είναι δοµικά και λειτουργικά παρόµοιες και σχηµατίζουν οµοδιµερή και ετεροδιµερή. Ο διµερισµός των πρωτεϊνών επιτρέπει τη σύνδεση του συµπλόκου στο DNA, σε συγκεκριµένες αλληλουχίες νουκλεοτιδίων, όπου δρουν ως ρυθµιστές της µεταγραφής, είτε ενεργοποιώντας ή καταστέλλοντας τη µεταγραφή του στοχευόµενου γονιδίου (Ellenberger et al., 1992; Schumacher et al., 2000). Κάθε µέλος της οικογένειας του AP-1 έχει µοναδικές ιδιότητες διµερισµού. Οι πρωτεΐνες Jun σχηµατίζουν οµοδιµερή και ετεροδιµερή µε µέλη των οικογενειών Fos και ATF. Οι πρωτεΐνες ATF, αλλά όχι οι Fos, σχηµατίζουν επίσης οµοδιµερή. Οι πρωτεΐνες c-maf και Nrl µπορούν να σχηµατίσουν ετεροδιµερή και µε τη c-jun και µε τη c-fos, όµως άλλες πρωτεΐνες της οικογένειας Maf σχηµατίζουν διµερή µόνο µε τη Fos (Landschulz et al., 1988). Όλα τα διµερή συνδέονται στο DNA µε την αλληλουχία 5 - TGA(C/G)TCA-3, αλλά κάθε διµερές έχει διαφορετική συγγένεια πρόσδεσης και ειδικότητα. Το διµερές Jun/ATF προσδένεται καλύτερα στην αλληλουχία campresponsive element (CRE, 5 -TGACGTCA-3 ), ενώ το διµερές Jun/Fos έχει µεγαλύτερη συγγένεια µε την αλληλουχία 12-O-tetradecanoylphorbol-13-acetate (TPA)-responsive element (TRE, 5 -TGAG/CTCA-3 ). Επιπλέον, µεγαλύτερη πολυπλοκότητα προσθέτει το γεγονός ότι υπάρχει ποικιλία στην έκφραση και στη δραστικότητα των µελών του AP-1. Κάθε πρωτεΐνη εµφανίζει µοναδική κατανοµή ανάλογα µε τον τύπο του κυττάρου ή του ιστού, αλλά µπορεί να µεταβληθεί από περιβαλλοντικά ερεθίσµατα. Μεγάλος αριθµός αυξητικών παραγόντων, κυτταροκινών, χηµειοκινών, ορµονών και περιβαλλοντικών παραγόντων στρες ρυθµίζουν τον AP-1 στο επίπεδο της γονιδιακής έκφρασης, της ανανέωσης του mrna και της πρωτεϊνικής σταθερότητάς του µε τελικό αποτέλεσµα την σχετική αφθονία του στα κύτταρα. Μάλιστα, πολλά από αυτά τα ερεθίσµατα οδηγούν σε µεταµεταγραφικές τροποποιήσεις των πρωτεϊνών του AP-1 αλλάζοντας τις ιδιότητές τους προς σχηµατισµό διµερών, σύνδεση στο DNA και ενεργοποίηση της µεταγραφής γονιδίων (Meng & Xia, 2011). Η ενεργοποίηση του AP-1 από τους TLR γίνεται διαµέσω των MAP κινασών µε αύξηση της µεταγραφής των γονιδίων των πρωτεϊνών c-jun και c-fos, κυρίως και µε την ενεργοποίησή τους µέσω φωσφορυλίωσης από τις ίδιες κινάσες (Jeong & Lee, 2011).
47 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ CREB Ο µεταγραφικός παράγοντας CREB συµµετέχει στον πολλαπλασιασµό, τη διαφοροποίηση και την επιβίωση των κυττάρων. Όσον αφορά στο ανοσοποιητικό σύστηµα, ο CREB ενεργοποιεί την επιβίωση των µακροφάγων, συµµετέχει στη ρύθµιση, τον πολλαπλασιασµό και την επιβίωση των Τ και Β λεµφοκυττάρων και αναστέλλει την ενεργοποίηση του NFκB (Shaywitz & Greenberg, 1999). Η οικογένεια του µεταγραφικού παράγοντα CREB περιλαµβάνει τις πρωτεΐνες CREB, camp responsive element modulator (CREM) και ATF1. Οι συγκεκριµένες πρωτεΐνες προσδένονται στο DNA στις αλληλουχίες CRE που µπορούν να αποτελούνται από οκτώ (5 -TGACGTCA-3 ) ή πέντε βάσεις (5 -CGTCA-3 ). Οι αλληλουχίες αυτές απαντώνται στα γονίδια των κυτταροκινών IL-2, IL-6, IL-10 και TNF-α (Wen et al., 2010). Η ενεργοποίηση του CREB γίνεται µε φωσφορυλίωσή του από ποικιλία κινασών όπως οι πρωτεϊνικές κινάσες A, B και C (protein kinase, PKA, PKB/AKT, PKC), η κινάση της καλµοδουλίνης (calcium/calmodulin-dependent protein kinase, CAMK) και οι MAP κινάσες διαµέσου των MSK1, 2. Αφού φωσφορυλιωθεί ο CREB αλληλεπιδρά µε την πρωτεΐνη p300 και επάγει την µεταγραφή των γονιδίων που φέρουν αλληλουχίες CRE (Mayr & Montminy, 2001). Η πρωτεΐνη p300 αποτελεί συµπαράγοντα µεταγραφής και άλλων µεταγραφικών παραγόντων, µεταξύ των οποίων περιλαµβάνεται και ο NFκB. Η βέλτιστη δράση του NFκB στην επαγωγή της µεταγραφής ορισµένων γονιδίων απαιτεί τη συµµετοχή της p300. Συνεπώς, ο NFκB και ο CREB ανταγωνίζονται για τη σύνδεση µε την p300 και αλληλοαναστέλλονται (Parry & Mackman, 1997). Κατά την ενεργοποίηση των TLR ο CREB φωσφορυλιώνεται από τις MSK1, 2 και επάγει την παραγωγή της IL-10 από τα µακροφάγα. Επίσης, παίζει σηµαντικό ρόλο στον περιορισµό της φλεγµονώδους απάντησης λόγω της ανταγωνιστικής δράσης την οποία ασκεί στον NFκB (Newton & Dixit, 2012). 1.6 Κυτταροκίνες Κατά τη διάρκεια της ανοσολογικής απόκρισης παράγονται από τα κύτταρα διάφορες διαλυτές πρωτεΐνες, οι οποίες χαρακτηρίζονται ως κυτταροκίνες. Οι συγκεκριµένες πρωτεΐνες ασκούν τη δράση τους τοπικά σε άλλα κύτταρα (παρακρινής δράση), σε κύτταρα-στόχους µακριά από το σηµείο παραγωγής τους (ενδοκρινής δράση)
48 48 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ ή στα ίδια κύτταρα τα οποία τις παράγουν (αυτοκρινής δράση). Στη φυσική ανοσία, η κύρια πηγή κυτταροκινών είναι τα µακροφάγα, τα οποία ενεργοποιούνται µετά από την αναγνώριση µικροβιακών παραγόντων. Κυτταροκίνες, επίσης, παράγονται κατά τις αντιδράσεις της κυτταρικής ανοσίας, στις οποίες κύριος κυτταρικός πληθυσµός παραγωγής κυτταροκινών είναι τα Τ λεµφοκύτταρα. Όλες οι κυτταροκίνες παράγονται σε µικρές ποσότητες και συνδέονται µε υποδοχείς υψηλής συγγένειας στην επιφάνεια των κυττάρων-στόχων. Οι κυτταροκίνες διακρίνονται στις ιντερλευκίνες, τις χηµειοκίνες και τις ιντερφερόνες ( ηµητρακόπουλος, 1994; Abbas & Lichtman, 2010) Ιντερλευκίνη 1 (IL-1) ιακρίνονται δύο µόρια IL-1, η IL-1α και η IL-1β. Η IL-1β συντίθεται ως άωρη πρωτεΐνη µε 269 αµινοξέα, από την οποία προκύπτει µετά από πρωτεόλυση η δραστική µορφή µε 153 αµινοξέα. Η IL-1α συντίθεται ως άωρη πρωτεΐνη µε 271 αµινοξέα, από τη διάσπασή της προκύπτει µόριο 154 αµινοξέων και σε αντίθεση µε την IL-1β και οι δύο µορφές είναι βιολογικά ενεργείς. Τα δύο µόρια εµφανίζουν οµολογία 27%, κυρίως στο καρβοξυτελικό άκρο, το οποίο είναι το βιολογικά δραστικό. Η IL-1α και η IL-1β είναι προϊόντα δύο διαφορετικών γονιδίων τα οποία εντοπίζονται στο χρωµόσωµα 2. Το µοριακό βάρος της IL-1 είναι 17kDa και στο µόριο δεν παρατηρούνται ενδοαλυσιδικοί δισουλφιδικοί δεσµοί και περιοχές γλυκοζυλιώσεως. In vivo, η κύρια πηγή της IL-1 είναι τα µακροφάγα µετά από διέγερση µε εξωγενείς και ενδογενείς παράγοντες. Εξωγενείς παράγοντες είναι ο LPS, οι βακτηριακές εξωτοξίνες, το κυτταρικό τοίχωµα των µυκήτων και οι αιµοσυγκολητίνες των ιών. Ενδογενείς παράγοντες είναι το κλάσµα C5a του συµπληρώµατος, ο TNF-α, τα Τ λεµφοκύτταρα µετά από επαφή µε τα µακροφάγα, αλλά και η ίδια η IL-1. Άλλα κύτταρα που παράγουν IL-1 είναι τα κύτταρα Langerhans, τα κύτταρα της κερατίνης στιβάδας του δέρµατος, τα ενδοθηλιακά και επιθηλιακά κύτταρα, τα ουδετερόφιλα πολυµορφοπύρηνα, τα µεγάλα κοκκιώδη λεµφοκύτταρα, οι ινοβλάστες, οι οστεοβλάστες, οι λείες µυϊκές ίνες και ορισµένα Β και Τ λεµφοκύτταρα ( ηµητρακόπουλος, 1994; Abbas & Lichtman, 2010). Η δράση της IL-1 στα διάφορα κύτταρα-στόχους επιτυγχάνεται αφού πρώτα συνδεθεί µε τον υποδοχέα της. Συγκεκριµένα, υπάρχουν δύο υποδοχείς στην επιφάνεια των κυττάρων, ο 80kDa IL1RI και ο 68kDa IL1RII, ενώ ρόλο στη µετάδοση σήµατος παίζει και η επικουρική πρωτεΐνη IL1RAcP. Η µετάδοση του σήµατος επιτυγχάνεται από
49 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ 49 το ετεροδιµερές IL1RI και IL1RAcP, ενώ ο IL1RII δε µεταδίδει σήµα και θεωρείται ότι δρα ανταγωνιστικά στον IL1RI, µε τον οποίο προσδένουν την IL-1µε την ίδια συγγένεια (Dinarello, 2009; Netea et al., 2010; Sims & Smith, 2010). Η IL-1 ασκεί δράση σε πολλά κύτταρα. Η δράση της IL-1 στο κεντρικό νευρικό σύστηµα συνοδεύεται από πυρετό, υπνηλία, ανορεξία και έκκριση ACTH. Στο ήπαρ διεγείρει τη σύνθεση του κλάσµατος C3 του συµπληρώµατος και των πρωτεϊνών της οξείας φάσης, όπως ινωδογόνου, CRP, απτοσφαιρίνης, α1-αντιθρυψίνης και σερουλοπλασµίνης. Η δράση της IL-1 στο ενδοθήλιο εκδηλώνεται µε την έκκριση προσταγλανδινών και την προσκόλληση των λευκών αιµοσφαιρίων στα κύτταρα του ενδοθηλίου. Προκαλεί ελευθέρωση ενζύµων (κολλαγενάση) από τους οστεοκλάστες και τα χονδροκύτταρα, που οδηγεί στην οστική απορρόφηση και την καταστροφή του χόνδρου. Επίσης, προκαλεί πρωτεόλυση των µυών, πολλαπλασιασµό των επιθηλιακών και ενδοθηλιακών κυττάρων, των κυττάρων του αρθρικού υµένα και των ινοβλαστών. Η παραγόµενη από τα µακροφάγα IL-1 συµβάλλει στη διέγερση και τον πολλαπλασιασµό των Τ λεµφοκυττάρων, τα οποία έχουν στην επιφάνειά τους υποδοχέα για την IL-1. Η έκθεση των Τ λεµφοκυττάρων στην IL-1 έχει ως αποτέλεσµα την παραγωγή της IL-2, της IL-3 και την εµφάνιση λειτουργικού υποδοχέα της IL-2 στη µεµβράνη του Τ λεµφοκυττάρου. Όσον αφορά στα Β λεµφοκύτταρα, φαίνεται ότι η IL-1 επαυξάνει τη διέγερση την οποία έχουν υποστεί από το οµόλογο αντιγόνο ( ηµητρακόπουλος, 1994; Dinarello, 2009; Abbas & Lichtman, 2010; Netea et al., 2010) Ιντερλευκίνη 6 (IL-6) Το µόριο της IL-6 αποτελείται από 183 αµινοξέα, έχει µοριακό βάρος 22-29kDa και είναι προϊόν γονιδίου που εντοπίζεται στο χρωµόσωµα 7. Η IL-6 εµφανίζει διαφόρου βαθµού γλυκοζυλίωση ανάλογα µε το είδος του κυττάρου από το οποίο παράγεται. Κύτταρα που παράγουν IL-6 είναι οι ινοβλάστες και τα µακροφάγα, ενώ έχει αποδειχθεί ότι παράγεται και από τα διεγερµένα Τ λεµφοκύτταρα. Η IL-6 που παράγεται από τα Τ λεµφοκύτταρα µετέχει µαζί µε άλλες κυτταροκίνες στη διαφοροποίηση των διεγερµένων Β λεµφοκυττάρων προς πλασµατοκύτταρα. Τα κύτταρα του µυελώµατος παράγουν IL-6, η οποία δρα στα ίδια κύτταρα ως παράγοντας αναπτύξεως. Επίσης, η IL-6 εµφανίζει µικρή αντι-ιική δράση, ιδιότητα για την οποία της έχει δοθεί και η ονοµασία IFNβ2 ( ηµητρακόπουλος, 1994; Paul, 2008; Abbas & Lichtman, 2010). Σε συνδυασµό µε την IL-1 και τον TNF-α προάγει την οξεία φλεγµονώδη
50 50 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ απάντηση (πυρετός, παραγωγή πρωτεϊνών οξείας φάσης από το ήπαρ), ενώ είναι υπεύθυνη για τη µετάβαση από την οξεία φάση της φλεγµονής στην επίκτητη ανοσία ή στη χρονιότητα της φλεγµονής. Η IL-6 ασκεί τη δράση της διαµέσου του υποδοχέα της, ο οποίος είναι ένα ετεροδιµερές που αποτελείται από τις πρωτεΐνες IL6Rα και gp130. Η πρωτεΐνη IL6Rα είναι υπεύθυνη για τη σύνδεση της IL-6 και εκφράζεται στα ηπατοκύτταρα, τα µονοκύτταρα και τα λεµφοκύτταρα σε κατάσταση ηρεµίας. Η πρωτεΐνη gp130 εκφράζεται σε όλα τα κύτταρα και τους ιστούς και επιτελεί τη λειτουργία της ενδοκυττάριας σηµατοδότησης (Naugler & Karin, 2008; Fonseca et al., 2009; Neurath & Finotto, 2011) Παράγοντας νέκρωσης όγκων α (TNF-α) Το γονίδιο που κωδικοποιεί τον TNF-α εντοπίζεται στο χρωµόσωµα 6, στην περιοχή του µείζονος συµπλέγµατος ιστοσυµβατότητος. Ο TNF-α συντίθεται ως µία διαµεµβρανική πρωτεΐνη µοριακού βάρους 26kDa, που αποτελείται από 233 αµινοξέα εκ των οποίων 177 αµινοξέα αποτελούν το εξωκυττάριο τµήµα, 21 το διαµεµβρανικό και 35 το κυτταροπλασµατικό και σχηµατίζει οµοτριµερές. Το βιολογικά δραστικό µόριο προκύπτει µετά από τη διάσπαση του εξωκυτταρίου τµήµατος και συντίθεται από τα τρία όµοια µόρια του οµοτριµερούς που το καθένα αποτελείται από 157 αµινοξέα. In vivo, η κύρια πηγή του TNF-α είναι τα µακροφάγα κύτταρα όλων των περιοχών του σώµατος µετά από διέγερση µε διάφορους παράγοντες, σηµαντικότερος των οποίων είναι ο LPS των Gram αρνητικών βακτηρίων. Τα γλυκοκορτικοειδή καταστέλλουν τη σύνθεση του TNF-α όταν χορηγηθούν πριν από τη διέγερση των µακροφάγων µε LPS. Τα µακροφάγα παράγουν επίσης TNF-α, αλλά σε µικρότερα ποσά, µετά από διέγερση µε ιούς, παράσιτα και ορισµένα Gram θετικά βακτήρια. Εκτός από τα µακροφάγα, άλλα κύτταρα που παράγουν TNF-α σε πολύ µικρότερα ποσά είναι τα Τ λεµφοκύτταρα, τα ΝΚ κύτταρα και τα mast κύτταρα ( ηµητρακόπουλος, 1994; Paul, 2008). Ο TNF-α ασκεί τη δράση του στα κύτταρα στόχους µετά τη σύνδεσή του µε δύο ειδικούς υποδοχείς. Ο πρώτος (TNFRI) έχει µοριακό βάρος 55-60kDa και εκφράζεται στα κύτταρα όλων των ιστών, ενώ ο δεύτερος (TNFRII) έχει µοριακό βάρος 78-80kDa και η έκφρασή του περιορίζεται σε κύτταρα του αιµοποιητικού συστήµατος. Οι δύο υποδοχείς έχουν την ίδια συγγένεια για τον TNF-α και διεγείρουν την ενεργοποίηση του NFκΒ, αλλά µόνο ο TNFRI προάγει την απόπτωση (Bodmer et al., 2002; Gaur &
51 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ 51 Aggarwal, 2003). Ο TNF-α έχει αρκετές όµοιες βιολογικές ιδιότητες µε την IL-1. Προκαλεί πυρετό µε απευθείας δράση στον υποθάλαµο ή εµµέσως µε τη διέγερση της παραγωγής IL-1. Όπως και η IL-1, ο TNF-α ασκεί δράση στους οστεοκλάστες µε αποτέλεσµα την οστική απορρόφηση, προκαλεί διάσπαση της πρωτεογλυκάνης του χόνδρου και διεγείρει τη παραγωγή προσταγλανδίνης PGE2 και κολλαγενάσης από τα κύτταρα του αρθρικού υµένα και τους ινοβλάστες. Επίσης, ανιχνεύεται στο αρθρικό υγρό σε φλεγµονώδεις νόσους των αρθρώσεων. Επιπλέον, ο TNF-α διεγείρει τα κύτταρα του ήπατος προς παραγωγή των ουσιών οξείας φάσης, ενώ προκαλεί τις ίδιες µεταβολές στο ενδοθήλιο των αγγείων όπως η IL-1. Ο σχηµατισµός θρόµβου στο ενδοθήλιο των αγγείων πιθανώς συνδέεται µε τη διάχυτη ενδαγγειακή πήξη και την αιµορραγική νέκρωση των όγκων. Στα λιποκύτταρα καταστέλλει τη σύνθεση της λιπάσης της λιποπρωτεΐνης, ενώ στα ουδετερόφιλα διεγείρει την παραγωγή H 2 O 2 και την αποκοκκίωση των λυσοσωµάτων, αυξάνει την φαγοκυτταρική τους ικανότητα για ορισµένους µικροοργανισµούς και προκαλεί την προσκόλλησή τους στα κύτταρα του ενδοθηλίου. Τέλος, ο TNF-α ονοµάζεται και καχεκτίνη επειδή η χορήγηση µικρών ποσοτήτων του σε πειραµατόζωα για διάστηµα ορισµένων µηνών οδηγεί σε ανορεξία και απώλεια βάρους (καχεξία), όπως ακριβώς παρατηρείται σε κακοήθεις νεοπλασίες και σε διάφορα λοιµώδη νοσήµατα ( ηµητρακόπουλος, 1994; Paul, 2008) Ιντερλευκίνη 10 (IL-10) Η IL-10 κωδικοποιείται από γονίδιο που εντοπίζεται στο χρωµόσωµα 1 και αποτελείται από 178 αµινοξέα µε υδρόφοβο άκρο, το οποίο αποµακρύνεται και προκύπτει η ώριµη πρωτεΐνη από 160 αµινοξέα, η οποία απαντάται ως οµοδιµερές. Κύρια πηγή παραγωγής της είναι όλοι οι πληθυσµοί Τ λεµφοκυττάρων, άωρων, ωρίµων και µνήµης. Επίσης, παράγεται από ενεργοποιηµένα µονοκύτταρα και µακροφάγα καθώς και από Β λεµφοκύτταρα. Ασκεί τη δράση της αφού συνδεθεί µε τον υποδοχέα IL10R, µε µοριακό βάρος 110kDa, ο οποίος αποτελείται από δύο υποµονάδες, τις IL10Rα και IL10Rβ. Η υποµονάδα IL10Rα εκφράζεται κυρίως σε κύτταρα του αιµοποιητικού, ενώ η IL10Rβ σε κύτταρα όλων των ιστών. Η IL-10 προσδένεται κυρίως στην IL10Rα αλλά και οι δύο υποµονάδες είναι απαραίτητες για την ενδοκυττάρια σηµατοδότηση. Η IL-10 ασκεί τη δράση της σε πολλά κύτταρα-στόχους. Στο σύστηµα των
52 52 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ µονοπυρήνων φαγοκυττάρων η δράση της περιλαµβάνει τη µείωση της παραγωγής προφλεγµονωδών κυτταροκινών και χηµειοκινών, την αναστολή της έκφρασης προσκολλητικών και συνδιεγερτικών µορίων, ενώ παράλληλα αναστέλλει τον πολλαπλασιασµό τους και την παραγωγή ελευθέρων ριζών οξυγόνου. Ανάλογες δράσεις ασκεί και στα κοκκιοκύτταρα. Όσον αφορά στα Β λεµφοκύτταρα, η δράση της IL-10 περιλαµβάνει την επαγωγή της σύνθεσης IgA, τη µεταβολή του ισοτύπου προς IgG1 και IgG3 και παράλληλα προάγει τον πολλαπλασιασµό και την επιβίωσή τους στα περιφερικά λεµφικά όργανα. Τέλος, έχει δράση αυξητικού παράγοντα στα θυµοκύτταρα και τα mast κύτταρα (Paul, 2008; Saraiva & O Garra, 2010).
53 ΒΡΟΥΚΕΛΛΑ Ιστορία 2 ΒΡΟΥΚΕΛΛΑ Η πρώτη αποµόνωση του µικροοργανισµού έγινε το 1887 από τον Sir David Bruce. Ο Bruce αποµόνωσε το βακτήριο από το σπλήνα βρετανών στρατιωτών που πέθαναν στη νήσο Μάλτα (Μελίτη) από νόσο γνωστή ως Malta fever (Μελιταίος πυρετός). Το πρώτο είδος του γένους βρέθηκε το 1904 όταν το µικρόβιο καλλιεργήθηκε από το γάλα αιγών και έλαβε την ονοµασία B. melitensis. Η νόσος του ανθρώπου συσχετίστηκε µε το γάλα αιγών καθώς ελαττώθηκε απότοµα η συχνότητά της όταν σταµάτησε η κατανάλωσή του. Το δεύτερο είδος αποµονώθηκε το 1897 στην ανία από τον Bernhard Bang από αγελάδες που παρουσίαζαν αυτόµατες εκτρώσεις και έλαβε την ονοµασία B. abortus. Το τρίτο είδος αποµονώθηκε το 1914 στις ΗΠΑ από το έµβρυο χοίρου που είχε γεννηθεί µε πρόωρο τοκετό και έλαβε την ονοµασία B. suis. Το γένος Brucella περιλαµβάνει έξι είδη, τα ανωτέρω τρία (Β. melitensis, B. abortus, B. suis), ενώ τα τελευταία χρόνια έχουν περιγραφεί επιπλέον τα είδη Β. neotomae, Β. ovis και Β. canis. Πρόσφατα ολοκληρώθηκε η χαρτογράφηση του γονιδιώµατος των B. melitensis, B. abortus και B. suis χωρίς προς το παρόν να προκύπτουν πρωτεΐνες που ενέχονται στην παθογόνο δράση. Το γονιδίωµά τους αποτελείται από δύο κυκλικά χρωµατοσώµατα χωρίς την παρουσία πλασµιδίων σε αντίθεση µε το ένα χρωµόσωµα των περισσοτέρων βακτηρίων (Sánchez et al., 2001; DelVecchio et al., 2002). 2.2 Επιδημιολογία Οι βρουκέλλες προκαλούν στα θηλαστικά ζώα λοιµώξεις, οι οποίες ονοµάζονται βρουκελλώσεις. Στα ζώα, σε αντίθεση µε τον άνθρωπο, η βρουκέλλωση εµφανίζεται µε επιδηµική µορφή και συνοδεύεται από αυτόµατες εκτρώσεις. Η Β. melitensis είναι παθογόνος κυρίως για τις αίγες και τα πρόβατα, η Β. abortus για τις αγελάδες, η Β. suis για τους χοίρους, η Β. neotomae για τους επίµυες του δάσους, η Β. ovis για τα πρόβατα και η Β. canis για τους σκύλους. Από τα έξι είδη βρουκελλών, τα τρία, δηλαδή η Β. melitensis, η Β. abortus και η Β. suis είναι παθογόνα για τον άνθρωπο, ενώ από τα άλλα τρία είδη, που η περιγραφή τους έγινε τα τελευταία χρόνια, µόνο η Β. canis προκαλεί σπανίως λοίµωξη στον άνθρωπο. Στα ζώα οι βρουκέλλες βρίσκονται σε πολύ µεγάλους αριθµούς στον πλακούντα και τους γαλακτοφόρους αδένες. Ο µεγάλος αριθµός των βρουκελλών στον
54 54 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ πλακούντα των ζώων εξηγείται από την παρουσία µίας αλκοόλης, της ερυθριτόλης, η οποία έχει βρεθεί ότι ευνοεί την ανάπτυξη των βρουκελλών. Η αλκοόλη αυτή δεν ανιχνεύεται στον πλακούντα των γυναικών και συνεπώς λοίµωξη µε βρουκέλλα δεν οδηγεί στην αποβολή του κυήµατος στις γυναίκες. Οι βρουκελλώσεις είναι ζωονόσοι που µεταδίδονται στον άνθρωπο µε το άβραστο γάλα και τα γαλακτοκοµικά προϊόντα, µετά από λύση της συνέχειας του δέρµατος σε άτοµα που έρχονται σε επαφή µε τα ζώα (κτηνοτρόφοι, σφαγείς, κτηνίατροι κλπ.) ή σπανιότερα µετά από εισπνοή κονιορτού που είναι µολυσµένος µε τα µικρόβια. Η µόλυνση µπορεί επίσης να γίνει από τον επιπεφυκότα. Μετά την είσοδό τους στον οργανισµό, αφού διαπεράσουν τον βλεννογόνο, τα βακτήρια ελεύθερα ή εντός των µακροφάγων µεταφέρονται στους περιοχικούς λεµφαδένες. Τα βακτήρια επιζούν και πολλαπλασιάζονται εντός των µακροφάγων, µέσω των οποίων διασπείρονται στους λεµφαδένες, το σπλήνα, το ήπαρ, το µυελό των οστών, τους µαστικούς αδένες και τους όρχεις, γεγονός που εξηγεί τις κλινικές εκδηλώσεις. Οι βρουκέλλες καταστρέφονται στο γάλα µε την παστερίωση. Στο τυρί καταστρέφονται σε λίγες ήµερες από τη συγκέντρωση του γαλακτικού οξέος, ενώ στο βούτυρο παραµένουν ζωντανές για διάστηµα µεγαλύτερο από µία εβδοµάδα. Γαλακτοκοµικά προϊόντα τα οποία έχουν παρασκευασθεί µε γάλα που δεν έχει παστεριωθεί πρέπει να µένουν σε θερµοκρασία ψυγείου για 90 τουλάχιστον ηµέρες πριν καταναλωθούν. Στους πλακούντες ζώων που έχουν µολυνθεί, οι βρουκέλλες είναι δυνατό να επιζήσουν µέχρι και τρεις µήνες ( ηµητρακόπουλος, 1993; Mandell et al., 2010). 2.3 Χαρακτηριστικές ιδιότητες Οι βρουκέλλες είναι µικρά, Gram αρνητικά κοκκοβακτηρίδια, τα οποία διατάσσονται µεµονωµένα, σε ζεύγη ή σπανιότερα σε µικρές αλυσίδες. Είναι αερόβιοι µικροοργανισµοί, αλλά η ανάπτυξή τους ευνοείται από την παρουσία CO 2. Η Β. abortus δεν αναπτύσσεται σε αερόβιες συνθήκες, αλλά χρειάζεται οπωσδήποτε την παρουσία 10% CO 2 για να αναπτυχθεί. Παράγουν καταλάση και οξειδάση, υδρολύουν την ουρία αλλά δε διασπούν τα σάκχαρα. ε φέρουν έλυτρο, βλεφαρίδες ως όργανο κινήσεως, και δε σχηµατίζουν σπόρους. Η ανάπτυξη του µικροβίου είναι βραδεία και η καλλιέργεια αίµατος από πάσχοντες επωάζεται επί τέσσερις εβδοµάδες για να χαρακτηριστεί ως αρνητική. Η
55 ΒΡΟΥΚΕΛΛΑ 55 καλλιέργεια των βρουκελλών γίνεται σε εµπλουτισµένα θρεπτικά υλικά τα οποία περιέχουν λευκωµατούχες ουσίες ζωικής ή φυτικής προελεύσεως που έχουν κατεργασθεί µε πεπτικά ένζυµα (Trypticase Soy άγαρ ή ζωµός). εν προκαλούν αιµόλυση στο αιµατούχο άγαρ. Στα στερεά θρεπτικά υλικά οι αποικίες εµφανίζονται µετά από δύο τουλάχιστον ηµέρες επωάσεως στους 37 C και το µέγεθος των αποικιών φθάνει τα 2-3 mm µετά από τέσσερις ήµερες επωάσεως (Εικόνα 4). Εικόνα 4: Αποικίες Brucella σε αιµατούχο άγαρ και κύτταρα του βακτηρίου µε Gram χρώση Τα τρία είδη βρουκελλών τα οποία κυρίως προκαλούν λοίµωξη στον άνθρωπο χωρίζονται µεταξύ τους µε βάση τα ακόλουθα κριτήρια (Πίνακας 1): Παρουσία CO 2 ως προϋπόθεση για την ανάπτυξή τους, ανάπτυξη σε θρεπτικό υλικό στο οποίο έχει ενσωµατωθεί η χρωστική βασική φουξίνη σε αναλογία 1 : , ανάπτυξη σε θρεπτικό υλικό στο οποίο έχει προστεθεί η χρωστική θειονίνη σε αναλογία 1 : , παραγωγή υδροθείου, παραγωγή ουρεάσης και χρονικό διάστηµα στο οποίο γίνεται η υδρόλυση της ουρίας ( ηµητρακόπουλος, 1993). Πίνακας 1: οκιµασίες για το διαχωρισµό των Βρουκελλών που αποµονώνονται στο κλινικό εργαστήριο.
56 56 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 2.4 Επιφανειακά αντιγόνα Οι βρουκέλλες φέρουν στην επιφάνεια τους δύο αντιγόνα, το Α και το Μ. Τα αντιγόνα αυτά είναι κοινά και στα τρία είδη βρουκελλών. ιαφορές παρατηρούνται στο ποσό του κάθε αντιγόνου στα τρία είδη των βρουκελλών. Έτσι η Β. abortus και η Β. suis φέρουν στην επιφάνειά τους µεγαλύτερα ποσά του αντιγόνου Α και µικρότερα ποσά του αντιγόνου Μ. Το αντίθετο συµβαίνει µε τη Β. melitensis. Τα αντιγόνα αυτά είναι συµπλέγµατα πρωτεϊνών και λιποπολυσακχαρίτη. Η λοίµωξη του ανθρώπου ή των ζώων µε ένα είδος βρουκέλλας έχει ως αποτέλεσµα την ανάπτυξη στον ορό του αίµατος αντισωµάτων (συγκολλητινών). Οι συγκολλητίνες αυτές προκαλούν τη συγκόλληση των κυττάρων και των τριών ειδών βρουκελλών, ανεξάρτητα από το είδος που προκάλεσε την παραγωγή τους. Αυτό εξηγείται από το γεγονός ότι τα αντιγόνα Α και Μ είναι κοινά στα τρία είδη βρουκελλών. Κατά συνέπεια η συγκολλητινοαντίδραση που χρησιµοποιείται συχνά στο διαγνωστικό εργαστήριο για την ανίχνευση αντισωµάτων έναντι των βρουκελλών µας πληροφορεί µόνο για την ύπαρξη βρουκελλώσεως και όχι για το είδος της βρουκέλλας η οποία προκάλεσε τη νόσο ( ηµητρακόπουλος, 1993; Mandell et al., 2010). 2.5 Λοιμώξεις από βρουκέλλες Ο χρόνος επωάσεως των βρουκελλώσεων είναι µεγάλος, από εβδοµάδες µέχρι µήνες. Η θνητότητα από τη νόσο είναι πολύ µικρή και ο θάνατος στις περισσότερες περιπτώσεις οφείλεται στην προσβολή των βαλβίδων της καρδιάς. Η οξεία βρουκέλλωση είναι επαγγελµατική κυρίως νόσος. Ο χρόνος επωάσεως κυµαίνεται από 7-21 ηµέρες. Παρατηρείται µικροβιαιµία χωρίς εντόπιση του µικροοργανισµού σε κάποιο όργανο. Τα άτοµα εµφανίζουν στην πλειονότητα των περιπτώσεων κακουχία, ρίγη, εφιδρώσεις, αδυναµία και αύξηση της θερµοκρασίας το απόγευµα ή το βράδυ. Τα 2/3 των ασθενών παραπονούνται για πονοκεφάλους, άλγη στην πλάτη και ανορεξία. Οι µισοί από τους ασθενείς παραπονούνται για απώλεια βάρους. Ένα ποσοστό των ασθενών εµφανίζει ξερό βήχα, άλλοι ασθενείς εµφανίζουν αρθραλγίες, ιδίως στην άρθρωση του γόνατος, στον ώµο, στον αστράγαλο ή τον αγκώνα. Ένα µικρό ποσοστό των ασθενών εµφανίζουν αθυµία, απάθεια, σύγχυση ή παραπονούνται για αϋπνία. Στα παιδιά η νόσος είναι συνήθως ασυµπτωµατική. Η λοίµωξη µε τη Β. abortus είναι ελαφρότερη από τις λοιµώξεις µε τη Β. suis ή τη Β. melitensis.
57 ΒΡΟΥΚΕΛΛΑ 57 Οι λεµφαδένες είναι διογκωµένοι σε ποσοστό 14% των ασθενών, ιδίως οι αυχενικοί και οι µασχαλιαίοι. Σπληνοµεγαλία παρατηρείται σε ποσοστό 10-20% και ηπατοµεγαλία σε ποσοστό 5%. Στους άνδρες είναι δυνατό να εµφανισθεί ευαισθησία στους όρχεις και οξεία επιδιδυµίτιδα. Σε ορισµένες περιπτώσεις το µικρόβιο µπορεί να εντοπιστεί σε ένα όργανο και επικρατεί η συµπτωµατολογία από το συγκεκριµένο όργανο. Η εντόπιση στους πνεύµονες εκδηλώνεται µε βήχα και δύσπνοια στο 15% των περιπτώσεων. Έχουν αναφερθεί, επίσης, διάµεσος πνευµονίτιδα, πνευµονικά οζίδια, εµπύηµα και πλευριτική συλλογή. Σπανίως αποµονώνεται από τα πτύελα, ενώ έχει αποµονωθεί από πλευριτικό υγρό και υλικό βιοψίας. Η εντόπιση στο ουρογεννητικό σύστηµα έχει ως κύρια συµπτωµατολογία την οξεία ορχίτιδα ή επιδιδυµοορχίτιδα. Η B. melitensis έχει αποµονωθεί από σπέρµα που αποθηκεύεται σε τράπεζες σπέρµατος, αλλά δεν έχει αποδειχθεί µετάδοση του µικροβίου µε τη σεξουαλική επαφή. Η εντόπιση στα οστά και τις αρθρώσεις αφορά το 40% των περιπτώσεων και χαρακτηρίζεται από αρθρίτιδα (γόνατα, αγκώνες, ισχίο), σπονδυλίτιδα (6% των περιπτώσεων), οστεοµυελίτιδα και τενοντίτιδα. Σε χώρες όπου επικρατεί η λοίµωξη από B. melitensis, είναι συχνότερη η εντόπιση στην ιερολαγόνιο άρθρωση (ιερολαγονίτιδα). Η εντόπιση στο ήπαρ και το σπλήνα εκδηλώνεται µε αποστήµατα τα οποία είναι συνηθέστερα στη λοίµωξη µε B. suis. Από το κεντρικό νευρικό σύστηµα συνήθη συµπτώµατα της βρουκελλώσεως είναι η κατάθλιψη και η διανοητική κόπωση. Σε ποσοστό µικρότερο του 2% των περιπτώσεων το µικρόβιο εισέρχεται στο ΕΝΥ και συνοδεύεται από οξεία ή χρόνια µηνιγγίτιδα. Η εντόπιση στο καρδιαγγειακό σύστηµα απαντάται στο 1% των περιπτώσεων, αφορά συνήθως την αορτική βαλβίδα και είναι υπεύθυνη για τους περισσότερους θανάτους. Σπανίως προκαλείται µυοκαρδίτιδα, περικαρδίτιδα, και ανεύρυσµα της αορτής και των εγκεφαλικών αγγείων. Η εντοπισµένη βρουκέλλωση παρατηρείται κυρίως στις γυναίκες. Οι ασθενείς που πάσχουν από εντοπισµένη βρουκέλλωση εµφανίζουν πυρετό σε ποσοστό 30% και ένα 10-15% των ασθενών εµφανίζουν εφιδρώσεις, αδυναµία και απώλεια βάρους. Η αύξηση του τίτλου των αντισωµάτων στον ορό του αίµατος είναι µικρή, ενώ σε άλλες περιπτώσεις δεν παρατηρείται αύξηση του τίτλου των αντισωµάτων. Στις περιπτώσεις αυτές η διάγνωση της νόσου γίνεται µε βιοψία ή µε καλλιέργεια από το υλικό της βλάβης ( ηµητρακόπουλος, 1993; Mandell et al., 2010; Longo & M.D, 2011).
58 58 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 2.6 Εργαστηριακή διάγνωση Καλλιέργεια Σε υποψία βρουκελλώσεως ο µικροοργανισµός αποµονώνεται κυρίως µετά από καλλιέργεια αίµατος. Η αποµόνωση του µικροοργανισµού µπορεί επίσης να γίνει µετά από καλλιέργεια υλικού αποστηµάτων ή υλικoύ παρακεντήσεως του µυελού των οστών. Σπάνια ο µικροοργανισµός αναζητείται στο εγκεφαλονωτιαίο υγρό, πλευριτικό υγρό, περιτοναϊκό υγρό ή στα ούρα. Από τον ασθενή λαµβάνονται αρκετά δείγµατα αίµατος σε διαφορετικά χρονικά διαστήµατα. Το κάθε δείγµα εµβολιάζεται σε φιάλη αιµατοκαλλιέργειας, η οποία τοποθετείται στους 37 C και σε ατµόσφαιρα 10% CO 2. Η φιάλη εξετάζεται κάθε ηµέρα για να διαπιστωθεί αν ο ζωµός έχει θολώσει. Η θόλωση του ζωµού οφείλεται στην ανάπτυξη µικροβίων. Η φιάλη της αιµατοκαλλιέργειας διατηρείται στους 37 C και σε ατµόσφαιρα 10% CO 2 τουλάχιστον για 28 ήµερες. Αν µετά από αυτό το διάστηµα ο ζωµός δε θολώσει και δεν παρατηρηθεί ανάπτυξη στα στερεά θρεπτικά υλικά, στα οποία έχουν γίνει οι ανακαλλιέργειες, η καλλιέργεια αίµατος για βρουκέλλα θεωρείται αρνητική. Το στέλεχος που έχει αποµονωθεί κατατάσσεται σε ένα από τα είδη της βρουκέλλας µε βάση τις δοκιµασίες που έχουν αναφερθεί, δηλαδή την ανάπτυξη σε ατµόσφαιρα CO 2, ανάπτυξη σε υλικά µε βασική φουξίνη και θειονίνη, παραγωγή υδροθείου και υδρόλυση της ουρίας ( ηµητρακόπουλος, 1993; Mandell et al., 2010). Το ποσοστό των περιπτώσεων βρουκελλώσεως στις οποίες αποµονώνεται ο µικροοργανισµός από το αίµα ανέρχεται στο 20-50%. Από τα ούρα ο µικροοργανισµός αποµονώνεται στο 20% των περιπτώσεων, αλλά σχεδόν πάντοτε οι ουροκαλλιέργειες για βρουκέλλα δεν είναι θετικές εάν οι αιµατοκαλλιέργειες είναι αρνητικές Ορολογικός έλεγχος Η εργαστηριακή διάγνωση της βρουκελλώσεως βασίζεται κυρίως στην ανίχνευση αντισωµάτων εναντίον των βρουκελλών µε τη συγκολλητινοαντίδραση Wright. Ως αντιγόνο χρησιµοποιείται το στέλεχος Β. abortus 1119 το οποίο έχει νεκρωθεί µε θέρµανση. Τα αντισώµατα που αναπτύσσονται στον ορό του αίµατος µετά από λοίµωξη µε τη Β. melitensis, Β. abortus ή Β. suis προκαλούν συγκόλληση των κυττάρων του στελέχους που χρησιµοποιείται ως αντιγόνο. Σε υποψία λοιµώξεως µε Β.
59 ΒΡΟΥΚΕΛΛΑ 59 canis τα αντισώµατα που αναπτύσσονται στον ορό του αίµατος δεν ανιχνεύονται µε το αντιγόνο που έχει αναφερθεί, επειδή τα κύτταρα του µικροοργανισµού δε φέρουν στην επιφάνειά τους τα αντιγόνα Μ και Α. Στην περίπτωση αυτή η ορολογική διάγνωση της νόσου γίνεται µε διαφορετικό αντιγόνο σε εξειδικευµένα εργαστήρια. Τίτλος αντισωµάτων 1 : 160 ή µεγαλύτερος είναι συνήθως ενδεικτικός ενεργού λοιµώξεως, τίτλος αντισωµάτων 1 : 80 είναι ενδεικτικός παλαιάς λοιµώξεως ή πιθανής ενεργού λοιµώξεως. Ποσοστό 1-2% των ατόµων από τους οποίους έχει αποµονωθεί ο µικροοργανισµός έχουν αρνητική συγκολλητινοαντίδραση ή χαµηλό τίτλο αντισωµάτων. Τίτλοι αντισωµάτων 1 : 160 σε άτοµα που εργάζονται σε σφαγεία ή έρχονται σε επαφή µε το µικροοργανισµό δεν έχουν διαγνωστική σηµασία, διότι έχει βρεθεί ότι ποσοστό 40% αυτών των ατόµων έχουν τίτλους αντισωµάτων 1 : 320. Στην οξεία βρουκέλλωση ο τίτλος των αντισωµάτων κυµαίνεται από 1 : 640 µέχρι 1 : 5120 µε µέσο όρο 1 : Σε ασθενείς που έχουν υποστεί την κατάλληλη θεραπεία ο αρχικός τίτλος 1 : 1280 µειώνεται στο 1 : 320 σε 4-5 µήνες και στο 1 : 160 σε ένα χρόνο, ενώ τίτλοι αντισωµάτων 1 : 80 είναι συνήθεις και µετά από αυτό το διάστηµα. Πολύ συχνή είναι η παρουσία ατελών αντισωµάτων τα οποία δηµιουργούν φαινόµενα προζώνης κατά την ορολογική διάγνωση της νόσου και ως εκ τούτου απαιτούνται αραιώσεις του ορού πέραν του 1:320 για να αποφευχθούν ψευδώς αρνητικά αποτελέσµατα στις χαµηλές αραιώσεις ( ηµητρακόπουλος, 1993; Mandell et al., 2010). 2.7 Θεραπεία Η βασική θεραπεία στη βρουκέλλωση των ενηλίκων είναι ο συνδυασµός της στρεπτοµυκίνης µε ενδοµυϊκή χορήγηση (1g ανά ηµέρα για 14 έως 21 ηµέρες) και δοξυκυκλίνης από του στόµατος (100 mg δύο φορές την ηµέρα για 6 εβδοµάδες). Το ποσοστό υποτροπών µε τη συγκεκριµένη θεραπεία είναι 5-10%. Αντί της στρεπτοµυκίνης µπορούν να χορηγηθούν άλλες αµινογλυκοσίδες, όπως η νετυλµικίνη ή η γενταµικίνη. Η εναλλακτική θεραπευτική αγωγή που συνιστάται από τον Παγκόσµιο Οργανισµό Υγείας (ΠΟΥ) είναι ο συνδυασµός ριφαµπικίνης ( mg ανά ηµέρα) και δοξυκυκλίνης (100mg δύο φορές την ηµέρα) από του στόµατος για 6 εβδοµάδες. Η συγκεκριµένη θεραπεία έχει ως αποτέλεσµα υποτροπή της νόσου σε 14% των περιπτώσεων. Σε άτοµα που δεν µπορούν να λάβουν τετρακυκλίνη (παιδιά, έγκυοι) ή είναι αλλεργικά στο αντιµικροβιακό, χορηγούνται υψηλές δόσεις
60 60 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ τριµεθοπρίµης/σουλφοµεθοξαζόλης (κοτριµοξαζόλη, 160mg/800mg τέσσερις φορές την ηµέρα για 6 εβδοµάδες από του στόµατος). Σε παιδιά µικρότερα των 8 ετών χορηγείται κοτριµοξαζόλη σε δοσολογία 5mg/kg βάρους σώµατος κάθε 12 ώρες για 6 εβδοµάδες. Εναλλακτική θεραπεία από του στόµατος αποτελεί η χορήγηση υψηλών δόσεων οφλοξασίνης (400mg δύο φορές την ηµέρα) ή σιπροφλοξασίνης (500mg δύο φορές την ηµέρα) σε συνδυασµό µε ριφαµπικίνη για 6 εβδοµάδες. Σε συµµετοχή του κεντρικού νευρικού συστήµατος η θεραπεία παρατείνεται για 6-12 µήνες και συνήθως συµπληρώνεται µε κεφτριαξόνη. Η ενδοκαρδίτιδα από βρουκέλλα απαιτεί θεραπεία µε τρία τουλάχιστον αντιµικροβιακά (αµινογλυκοσίδη, τετρακυκλίνη, ριφαµπικίνη) και πολλοί συνιστούν την προσθήκη κεφτριαξόνης και/ή φθοριοκινολόνης για να µειωθεί η ανάγκη αντικατάστασης της βαλβίδας. Η συγκεκριµένη θεραπεία διαρκεί τουλάχιστον για 6 µήνες. Σε περίπτωση µόλυνσης προσθετικής βαλβίδας ή υλικών αρθροπλαστικής, παρά τη θεραπεία, είναι αναγκαία η αντικατάσταση των προσθετικών υλικών στις περισσότερες περιπτώσεις (Mandell et al., 2010; Gilbert, 2010; Longo & M.D, 2011). 2.8 Πρόληψη Η πρόληψη της νόσου στον άνθρωπο δεν επιτυγχάνεται µε εµβόλιο. Για τον περιορισµό της νόσου έχουν αναπτυχθεί δύο εµβόλια µε τα εξασθενηµένα στελέχη B. abortus RB51 και B. melitensis Rev.1, τα οποία χορηγούνται σε αγελάδες και πρόβατα ή αίγες, αντιστοίχως (Mandell et al., 2010; Longo & M.D, 2011). 2.9 Παθογόνος δράση Μηχανισμοί ενδοκυττάριας επιβίωσης Τα τελευταία χρόνια έχει γίνει σηµαντική πρόοδος στην κατανόηση των παθογενετικών παραγόντων που επιτρέπουν στη βρουκέλλα να παραµένει εντός των φαγοκυττάρων και να διαφεύγει από τους µηχανισµούς νέκρωσης. Τα αποτελέσµατα της ενδοκυττάριας επιβίωσης έχουν προκύψει κυρίως από in vitro µελέτες µε καλλιέργειες µακροφάγων. Η βρουκέλλα έχει την ικανότητα να πολλαπλασιάζεται σε µεγάλη έκταση µέσα σε µακροφάγα και σε επιθηλιακά κύτταρα χωρίς να επηρεάζει τις βασικές κυτταρικές λειτουργίες ή να προκαλεί το θάνατό τους. Ο µικροοργανισµός ελέγχει αποτελεσµατικά τη µετακίνησή του µέσα στο κύτταρο ώστε να αποφεύγει την αποδόµησή του στο λυσόσωµα και να καταλήξει σε ένα ενδοκυττάριο διαµέρισµα
61 ΒΡΟΥΚΕΛΛΑ 61 κατάλληλο για τον πολλαπλασιασµό του. Η περιοχή αυτή ονοµάζεται κυστίδιο που περιέχει την βρουκέλλα (Brucella Containing Vacuole BCV). Η αρχική επαφή της βρουκέλλας µε το κύτταρο αποτελεί σηµαντικό παράγοντα που καθορίζει την ενδοκυττάρια επιβίωσή της. Τόσο τα οψωνινοποιηµένα όσο και τα µη οψωνινοποιηµένα βακτήρια φαγοκυτταρώνονται επιτυχώς από τα µακροφάγα, γεγονός που υποδηλώνει ότι το συµπλήρωµα και τα αντισώµατα, όπως και η άµεση επαφή βακτηρίου φαγοκυττάρου, συµβάλλουν στην είσοδο του βακτηρίου (Naroeni & Porte, 2002; Watarai et al., 2002). Όσον αφορά στα µη οψωνινοποιηµένα βακτήρια, η είσοδός τους στα µακροφάγα διαµεσολαβείται από δύο υποδοχείς. Ο πρώτος είναι ο Class A Scavenger Receptor ο οποίος αντιδρά µε το λιπίδιο Α του LPS της βρουκέλλας (Kim et al., 2004), ενώ ο δεύτερος είναι µία κυτταρική πρωτεΐνη, η PrPc, η οποία συνδέεται µε την πρωτεΐνη θερµικής καταπληξίας Hsp60 (Watarai et al., 2003). Εν τούτοις, ο ειδικός ρόλος αυτών των πρωτεϊνών στη λοίµωξη από βρουκέλλα είναι αµφιλεγόµενος (Fontes et al., 2005). Επίσης, οι πλευρικές αλυσίδες του LPS της βρουκέλλας είναι απαραίτητες για την αποτελεσµατική είσοδο του βακτηρίου στα κύτταρα του ξενιστή. Μεταλλαγµένα στελέχη χωρίς τις πλευρικές αλυσίδες (rough LPS) εισέρχονται στο φαγοκύτταρο µε διαφορετική οδό και κατευθύνονται ταχέως προς το λυσόσωµα όπου καταστρέφονται (Porte et al., 2003). Πιθανώς οι πλευρικές αλυσίδες του LPS καθυστερούν τη σύντηξη του πρώιµου BCV µε τα λυσοσώµατα, αφού και νεκρωµένες µε θέρµανση βρουκέλλες µε smooth LPS εµφανίζουν το ίδιο φαινόµενο. Τα αρχικά στάδια της ωρίµανσης του BCV προσδιορίζουν κατά πόσο η βρουκέλλα θα επιβιώσει µέσα στα µακροφάγα. Μελέτες in vitro έχουν αποδείξει ότι ο µεγαλύτερος αριθµός των βακτηρίων που φαγοκυτταρώνονται καταστρέφονται από τους µηχανισµούς του φαγοκυττάρου και µόνο λίγα βακτήρια διαφεύγουν και πολλαπλασιάζονται ενδοκυτταρίως. Τα BCVs µέσα στα οποία επιζεί το βακτήριο, αλληλεπιδρούν µε ειδικές δοµές του µηχανισµού φαγοκυττάρωσης. Είναι γενικώς αποδεκτό ότι σε καλλιέργειες κυττάρων τα BCVs αποκτούν δείκτες των πρώιµων ενδοσωµάτων αµέσως µετά την είσοδο του βακτηρίου, µεταξύ των οποίων περιλαµβάνονται το αντιγόνο πρώιµου ενδοσώµατος EEA1 και η πρωτεΐνη Rab5 (Pizarro-Cerdá et al., 1998; Chaves-Olarte et al., 2002; Celli et al., 2003). Οι συγκεκριµένες αλληλεπιδράσεις είναι ταχύτατες και λαµβάνουν χώρα στα πρώτα λεπτά της ωριµάνσεως του BCV. Έτσι, για παράδειγµα, στην περίπτωση των µακροφάγων από το µυελό των οστών ποντικού οι αρχικοί δείκτες έχουν ήδη
62 62 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ αποβληθεί 30 λεπτά µετά την είσοδο του βακτηρίου (Celli et al., 2003). Σε αντίθεση µε τα σφαιρίδια latex και τα νεκρωµένα µε θέρµανση βακτήρια, τα BCVs δεν αποκτούν τους δείκτες των όψιµων ενδοσωµάτων και λυσοσωµάτων, γεγονός που υποδηλώνει ότι διαφεύγουν από το µηχανισµό της φαγοκυττάρωσης. Είναι ενδιαφέρον να σηµειωθεί ότι καθώς το BCV χάνει τους αρχικούς δείκτες του ενδοσώµατος, αποκτά την πρωτεΐνη της µεµβράνης του όψιµου ενδοσώµατος λυσοσώµατος LAMP1, γεγονός που πιθανώς σηµαίνει ότι υπάρχει αλληλεπίδραση µε τις δοµές του όψιµου ενδοσώµατος (Pizarro-Cerdá et al., 1998; Celli et al., 2003; Starr et al., 2008). Άλλη εξήγηση που έχει προταθεί είναι ότι η πρωτεΐνη LAMP1 παραλαµβάνεται απευθείας από τη συσκευή Golgi (Εικόνα 5). Εικόνα 5: Μηχανισµός ενδοκυττάριας επιβίωσης της Brucella Πρόσφατα έχει περιγραφεί η συµµετοχή των β1,2 γλυκανών της βρουκέλλας στον έλεγχο της µετακίνησης του BCV (Arellano-Reynoso et al., 2005). Οι συγκεκριµένες γλυκάνες αποµακρύνουν τη χοληστερόλη από τη λιπιδιακή διπλοστοιβάδα της µεµβράνης των ευκαρυωτικών κυττάρων και έχει προταθεί ότι τροποποιούν τη µεµβράνη του BCV που είναι πλούσια σε χοληστερόλη για να παρεµποδίσουν τη σύντηξη µε τα λυσοσώµατα. Η διαδικασία της ωρίµανσης του BCV εξελίσσεται για αρκετές ώρες, κατά τη διάρκεια των οποίων αποβάλλεται βαθµιαία η πρωτεΐνη LAMP1. Σε µακροφάγα από
63 ΒΡΟΥΚΕΛΛΑ 63 το µυελό των οστών ποντικών, η πρωτεΐνη LAMP1 των BCVs ελαττώνεται σηµαντικά ως τις δώδεκα ώρες και πολύ λίγα BCVs διατηρούν την LAMP1 στις 24 ώρες, όταν ο ενδοκυττάριος πολλαπλασιασµός του βακτηρίου έχει ήδη αρχίσει. Τα οψωνινοποιηµένα βακτήρια επιζούν και πολλαπλασιάζονται σε κυστίδια που διατηρούν την πρωτεΐνη LAMP1 σε ανθρώπινα µονοκύτταρα, ενώ τα µη οψωνινοποιηµένα ακολουθούν την ωρίµανση που περιγράφεται και στα ποντίκια (Bellaire et al., 2005). Αποτέλεσµα της ωρίµανσης του φαγοσώµατος είναι η ελάττωση του ph του BCV που είναι απαραίτητη για την επιβίωση του βακτηρίου µέσα στα κύτταρα του ξενιστή. Σε καλλιέργειες µακροφάγων που έχουν µολυνθεί µε B. suis, το ph στο εσωτερικό του BCV είναι περίπου 4-4,5 σε διάστηµα µίας ώρας (Porte et al., 1999). Η πτώση του ph στο εσωτερικό του κυστιδίου σηµατοδοτεί την έκφραση γονιδίων της βρουκέλλας που είναι απαραίτητα για τη λοιµογόνο δράση της. Μάλιστα, η αναστολή της οξινίσεως του BCV στα αρχικά στάδια της ωρίµανσής του (στη διάρκεια της πρώτης ώρας) αναστέλλει τελείως τον πολλαπλασιασµό του βακτηρίου. Τρεις ώρες µετά τη λοίµωξη, το όξινο περιβάλλον του BCV επάγει την έκφραση του οπερονίου virb, το οποίο κωδικοποιεί το εκκριτικό σύστηµα τύπου IV που είναι απαραίτητο για την εγκατάσταση του βακτηρίου στην περιοχή όπου προστατεύεται και πολλαπλασιάζεται (Boschiroli et al., 2002). Μετά τα αρχικά στάδια ωρίµανσης, το BCV αντιδρά µε το ενδοπλασµατικό δίκτυο και προσλαµβάνει πολλές πρωτεΐνες από αυτό, όπως είναι η καλνεξίνη, η καλρετικουλίνη και η Sec61 (Pizarro-Cerdá et al., 1998; Celli et al., 2003; Starr et al., 2008). Με συνεχείς αλληλεπιδράσεις µεταξύ του BCV και του ενδοπλασµατικού δικτύου η µεµβράνη του κυστιδίου που περιέχει το βακτήριο επικαλύπτεται µε ριβοσώµατα, τα οποία είναι ορατά µε το ηλεκτρονικό µικροσκόπιο και εν τέλει το BCV ωριµάζει σε ένα κυστίδιο που προκύπτει από το ενδοπλασµατικό δίκτυο. Σ αυτό το στάδιο το BCV έχει συντηχθεί µε το ενδοπλασµατικό δίκτυο και έχει εξασφαλιστεί η περιοχή όπου η βρουκέλλα µπορεί να πολλαπλασιαστεί. Ο σχηµατισµός των συγκεκριµένων κυστιδίων που περιέχουν τη βρουκέλλα συµπίπτει µε την έναρξη του πολλαπλασιασµού του βακτηρίου και απαιτεί εκτεταµένη παραλαβή µεµβράνης από το ενδοπλασµατικό δίκτυο, επειδή κάθε νέο βακτήριο βρίσκεται στο δικό του κυστίδιο. Συνεπώς, το ενδοπλασµατικό δίκτυο αποτελεί σηµαντική πηγή µεµβράνης για τα πολλαπλασιαζόµενα βακτήρια. Επίσης, δηµιουργεί το κατάλληλο περιβάλλον για τη βρουκέλλα επειδή προµηθεύει τις απαραίτητες
64 64 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ θρεπτικές ουσίες. Η βρουκέλλα πολλαπλασιάζεται επιτυχώς στα κυστίδια που προήλθαν από το ενδοπλασµατικό δίκτυο. Ο αριθµός των βακτηριακών κυττάρων φθάνει σε τόσο υψηλά επίπεδα που επηρεάζει τη φυσιολογική δοµή του ενδοπλασµατικού δικτύου, το οποίο αναδιατάσσεται ώστε να εφοδιάσει τα πολλαπλασιαζόµενα κυστίδια µε µεµβράνη. Οι µοριακοί µηχανισµοί που επιτρέπουν στη βρουκέλλα να αρχίσει τη σύντηξη µε το ενδοπλασµατικό δίκτυο δεν έχουν διευκρινιστεί. Είναι γνωστό ότι το εκκριτικό σύστηµα τύπου IV που κωδικοποιείται από το οπερόνιο virb είναι απαραίτητο για την παρατεταµένη αλληλεπίδραση µε το ενδοπλασµατικό δίκτυο (Comerci et al., 2001; Celli et al., 2005). Μεταλλαγµένα στελέχη βρουκέλλας που δε φέρουν συγκεκριµένα γονίδια του οπερονίου virb επιζούν στα αρχικά στάδια της λοιµώξεως και φαίνονται µε το ηλεκτρονικό µικροσκόπιο να βρίσκονται µέσα σε κυστίδια σε στενή επαφή µε το ενδοπλασµατικό δίκτυο. Όµως, τα κυστίδια µε τα µεταλλαγµένα στελέχη σε µεταγενέστερα στάδια αδυνατούν να συντηχθούν µε το ενδοπλασµατικό δίκτυο και τελικά αποκτούν δείκτες λυσοσωµάτων όπως η καθεψίνη D. Αυτό αποδεικνύει ότι βρίσκονται εντός των λυσοσωµάτων όπου και ανευρίσκονται αποδοµηµένα µε το ηλεκτρονικό µικροσκόπιο. Με βάση τη γνώση παρόµοιων εκκριτικών συστηµάτων τύπου IV από άλλα µικρόβια, πιθανολογείται ότι το σύστηµα virb της βρουκέλλας εκκρίνει δραστικά µόρια τα οποία διαµεσολαβούν τη διαδικασία της σύντηξης της µεµβράνης του BCV µε αυτήν του ενδοπλασµατικού δικτύου και τα οποία δεν έχουν ταυτοποιηθεί µέχρι σήµερα Αναγνώριση από τη φυσική ανοσία Στην αναγνώριση διαφόρων παθογόνων βακτηρίων έχει αναφερθεί η συµµετοχή των TLRs. Οι TLRs είναι υποδοχείς που αναγνωρίζουν µεγάλο αριθµό µοριακών δοµών των βακτηρίων όπως λιπίδια, πρωτεΐνες, λιποπρωτεΐνες, γλυκάνες και νουκλεϊνικά οξέα. Η σηµατοδότηση διαµέσου των συγκεκριµένων υποδοχέων καταλήγει στην παραγωγή προφλεγµονωδών κυτταροκινών και στην έκκριση συνδιεγερτικών µορίων στην επιφάνεια των κυττάρων µε τελικό σκοπό τη σύνδεση της φυσικής µε την επίκτητη ανοσία. Η εµπλοκή των TLRs στην ανοσία του ξενιστού έναντι της λοιµώξεως από βρουκέλλα έχει µελετηθεί από διαφορετικές ερευνητικές οµάδες µε τη χρήση ποντικών που δεν εκφράζουν TLR2, TLR4, TLR9 ή MyD88. Ο TLR2 δε διαδραµατίζει ρόλο στον έλεγχο της λοιµώξεως από B. abortus στα ποντίκια (Campos et al., 2004; Weiss et al., 2005), αλλά η σηµατοδότηση διαµέσου αυτού
65 ΒΡΟΥΚΕΛΛΑ 65 συµβάλλει στην παραγωγή προφλεγµονωδών κυτταροκινών από τα κύτταρα της φυσικής ανοσίας. Αυτό έχει τεκµηριωθεί σε µελέτες µε ζωντανά βακτήρια (Weiss et al., 2005), νεκρωµένα µε θέρµανση βακτήρια B. abortus (Heat Killed Brucella abortus HKBa) (Huang et al., 2003) ή λιποπρωτεΐνες της βρουκέλλας (Giambartolomei et al., 2004). Επιπλέον, τα νεκρωµένα µε θέρµανση βακτήρια διήγειραν την παραγωγή IL- 12, IL-23/p40 διαµέσου του TLR2 στα δενδριτικά κύτταρα (Macedo et al., 2008; Zwerdling et al., 2008), ενώ ανέστειλαν την έκφραση των µορίων MHC II σε ανθρώπινα µακροφάγα διαµέσου του ίδιου υποδοχέα (Barrionuevo et al., 2008). Τα αποτελέσµατα για τη σηµασία του TLR4 στην ανθεκτικότητα του ξενιστού στη λοίµωξη από βρουκέλλα παραµένουν αντιφατικά. Οι Campos et al. (Campos et al., 2004) έδειξαν ότι ποντίκια µεταλλαγµένα ως προς τον TLR4 (C3H/HeJ) είναι πιο ευαίσθητα στη λοίµωξη από το παθογόνο πρότυπο στέλεχος B. abortus S2308 σε σχέση µε τα ποντίκια µάρτυρες (C3H/HePas) µε αναφορά στο µικροβιακό φορτίο σε διάφορα όργανα των ποντικών των δύο οµάδων. Οι Weiss et al. (Weiss et al., 2005) αναφέρουν ότι η χορήγηση του εξασθενηµένου στελέχους της B. abortus S19, που χρησιµοποιείται ως εµβόλιο για τις αγελάδες, σε ποντίκια οδηγεί σε παραγωγή του TNF-α διαµέσου του TLR4. Όµως, το µικροβιακό φορτίο στα όργανα των πειραµατοζώων όπου απουσιάζει ο TLR4 δεν αυξάνεται σε σχέση µε τους µάρτυρες. Επιπλέον, οι Barquero-Calvo et al. (Barquero-Calvo et al., 2007) έδειξαν ότι ο πολλαπλασιασµός των στελεχών B. abortus S19 και S2308 in vivo είναι ανεξάρτητος του TLR4. Είναι ενδιαφέρον να αναφερθεί (Pei et al., 2008) ότι ο TLR4 είναι σηµαντικός για την είσοδο των smooth στελεχών B. abortus στα µακροφάγα. Ο TLR9 φαίνεται να παίζει σηµαντικό ρόλο στη µείωση του µικροβιακού φορτίου σε ποντίκια στα οποία χορηγήθηκε B. abortus. Συγκεκριµένα, έχει αναφερθεί ότι ποντίκια knock out ως προς τον TLR9 εµφανίζουν αυξηµένη ευαισθησία στη B. abortus (Macedo et al., 2008) και στη B. melitensis (Copin et al., 2007) συγκριτικά µε φυσιολογικά ποντίκια. Οµοίως, δενδριτικά κύτταρα και µακροφάγα από τα παραπάνω ποντίκια παράγουν µειωµένα ποσά IL-12, IL-23/p40 όταν διεγείρονται µε νεκρωµένα µε θέρµανση βακτήρια B. abortus. Τέλος, οι Huang et al. (Huang et al., 2005) αναφέρουν ότι η διέγερση των κυττάρων από HKBa προς παραγωγή IFNα εξαρτάται από τον TLR9. Η σηµατοδότηση διαµέσου του MyD88 φαίνεται να είναι ουσιαστική για την ενεργοποίηση των κυττάρων που παράγουν IFNγ και των δενδριτικών κυττάρων κατά τη µόλυνση µε βρουκέλλα σε ποντίκια. Οι Copin et al. (Copin et al., 2007) έδειξαν ότι
66 66 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ η έλλειψη του MyD88 περιορίζει σηµαντικά τη συχνότητα των κυττάρων που παράγουν IFNγ στη λοίµωξη µε B. melitensis. Επίσης, οι Macedo et al. (Macedo et al., 2008) αναφέρουν ότι η ωρίµανση των δενδριτικών κυττάρων από την B. abortus εξαρτάται από το MyD88. Επιπλέον, οι δύο ανωτέρω µελέτες συµφωνούν στο ότι ποντίκια knock out για την πρωτεΐνη MyD88 είναι πολύ ευαίσθητα στη λοίµωξη µε βρουκέλλα. Η οικογένεια των πρωτεϊνών IRAK παίζει ρόλο στην ενδοκυττάρια σηµατοδότηση των υποδοχέων TLR και της IL-1 διαµέσου του MyD88. Οι Oliveira et al. (Oliveira et al., 2011) παρατήρησαν ότι ποντίκια knock out για την πρωτεΐνη IRAK4 έφεραν µεγαλύτερο µικροβιακό φορτίο στο σπλήνα τους σε σχέση µε ετερόζυγα για την πρωτεΐνη ποντίκια, όταν µολύνθηκαν µε B. abortus. Επίσης, παρατήρησαν ότι η παραγωγή TNF-α και IL-12, IL-23/p40 εξαρτάται από την IRAK4. Η οδός ενδοκυττάριας σηµατοδότησης που αρχίζει από τους TLRs και είναι ανεξάρτητη από την οδό της πρωτεΐνης MyD88 περιλαµβάνει τις πρωτεΐνες TRAM και TRIF. Η έλλειψη της πρωτεΐνης TRIF δεν επηρέασε τον αριθµό των κυττάρων που παράγουν IFNγ και δε σχετίζεται µε τον έλεγχο της λοιµώξεως από βρουκέλλα (Copin et al., 2007). Πρόσφατα έχει αποδειχθεί ότι τα είδη βρουκέλλας B. abortus και B. melitensis φέρουν στο γονιδίωµά τους ένα γονίδιο το οποίο κωδικοποιεί µία πρωτεΐνη µε µεγάλη οµολογία ως προς την περιοχή TIR της οικογένειας των TLRs και των συνοδών µορίων. Η συγκεκριµένη πρωτεΐνη φέρει την ονοµασία Btp1 ή TcpB και οδηγεί στην αποδόµηση της πρωτεΐνης TIRAP/mal του φαγοκυττάρου µε αποτέλεσµα να καθίσταται αδύνατη η µετάδοση του σήµατος από τον TLR2 στο µόριο MyD88 (Salcedo et al., 2008; Cirl et al., 2008; Radhakrishnan et al., 2009, 2011; Sengupta et al., 2010; Radhakrishnan & Splitter, 2010). Αυτή η παρέµβαση φαίνεται να οδηγεί σε αναστολή της ωρίµανσης των δενδριτικών κυττάρων που έχουν µολυνθεί µε τη βρουκέλλα και έτσι ευνοείται η επιβίωση και ο πολλαπλασιασµός του βακτηρίου (Brodsky & Medzhitov, 2009)
67 ΣΚΟΠΟΣ 67 3 ΣΚΟΠΟΣ Η βρουκέλλωση αποτελεί σηµαντικό πρόβληµα στη χώρα µας, όπως και γενικότερα στις χώρες της Βαλκανικής και της Μεσογείου. Επιδηµιολογικές µελέτες στη χώρα µας αναφέρουν συχνότητα προσβολής 1110 περιστατικών / κατοίκους ενώ σύµφωνα µε στοιχεία του ΠΟΥ εµφανίζονται νέες περιπτώσεις το χρόνο στην Ευρώπη. Το κλινικό φάσµα της νόσου ποικίλλει από ασυµπτωµατική έως οξεία ή υποτροπιάζουσα, ενώ ιδιαίτερη σηµασία έχει το γεγονός ότι µπορεί να µεταπέσει σε χρονιότητα. Η βρουκέλλωση µπορεί να αποβεί θανατηφόρος επί προσβολής του καρδιαγγειακού συστήµατος. Η βρουκέλλα είναι ενδοκυττάριο βακτήριο. Η άµυνα του οργανισµού εξασφαλίζεται από µηχανισµούς κυτταρικής ανοσίας. Οι µηχανισµοί που διέπουν την αλληλεπίδραση του βακτηρίου µε το σύστηµα ανοσίας παραµένουν ελλιπώς χαρακτηρισµένοι. Ο ρόλος της φυσικής ανοσίας και συγκεκριµένα µιας µεγάλης οικογένειας µη ειδικών υποδοχέων, των TLRs, που εµπλέκονται άµεσα στην αναγνώριση των παθογόνων, αποτελεί πεδίο έντονου ερευνητικού ενδιαφέροντος. Συγκεκριµένα, µέλη της οικογένειας των TLRs και διαταραχές στη σηµατοδοτική οδό που ενεργοποιούν έχουν συσχετιστεί µε ευπάθεια σε λοιµώξεις. Η αλληλεπίδραση της βρουκέλλας µε τους TLRs και ο ρόλος τους στην τελική έκβαση της λοιµώξεως και τους µηχανισµούς που ευθύνονται για χρονιότητα αποτελεί στόχο της παρούσης διατριβής. Η πειραµατική προσέγγιση σε ανθρώπινο µοντέλο, το οποίο λείπει µέχρι σήµερα από τη διεθνή βιβλιογραφία, µε τεχνολογία αιχµής που µελετά την ενδοκυττάρια σηµατοδότηση στοχεύει στην αναγνώριση/ταυτοποίηση µέλους των TLRs ή ενδοκυτταρίων στόχων στη σηµατοδοτική οδό της ανοσολογικής αποκρίσεως που µπορεί να γίνουν στόχοι εναλλακτικής θεραπείας. Τα µείζονα ερωτήµατα τα οποία η µελέτη επιχείρησε να απαντήσει είναι: 1. ποιό/ά µέλη της οικογενείας των TLRs αναγνωρίζουν την Brucella; 2. η αναγνώριση του µικροβίου από τον/τους TLRs σχετίζεται µε το σηµατοδοτικό µονοπάτι στο εσωτερικό του µακροφάγου που καταλήγει στην ενεργοποίηση των φαγοκυτταρικών µηχανισµών του µικροβίου; 3. ποιά ενδιάµεσα στάδια ενεργοποίησης στη διαδικασία έκφρασης γονιδίων φλεγµονής που πυροδοτούνται από συγκεκριµένους TLRs είναι
68 68 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ καθοριστικά για την επιβίωση του βακτηρίου στο εσωτερικό του µακροφάγου; 4. πώς η αναγνώριση της Brucella από τον/τους TLRs διαφοροποιεί το πρόγραµµα ενεργοποίησης των µακροφάγων;
69 V. ΕΙΔΙΚΟ ΜΕΡΟΣ
70
71 ΥΛΙΚΑ 71 1 ΥΛΙΚΑ Όλα τα αντιδραστήρια που χρησιµοποιήθηκαν για τη διεξαγωγή των πειραµάτων ήταν καθαρότητας αναλυτικού βαθµού. A Annexin apoptosis kit από MOLECULAR PROBES Aprotinin από SIGMA B BCA Protein Assay Reagent kit από PIERCE D Dual-Luciferase Reporter Assay System από PROMEGA H HCl από MERCK I Igepal CA630 από SIGMA IL-1β, IL-6, IL-10, IL-12/p70, TNF-α ELISA kit από R&D SYSTEMS K
72 72 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ KCl από MERCK KH 2 PO 4 από SIGMA L Leupeptin από SIGMA M McFarland standards από BIOMÉRIEUX MgCl 2 από MERCK milli-q-h 2 O N Na 2 HPO 4 2 H 2 O από MERCK Na 3 VO 4 από SIGMA NaCl από MERCK NaOH από MERCK NucleoBond Plasmid DNA Purification από MACHEREY-NAGEL P Pepstatin-A από SIGMA p-κουµαρικό οξύ από SIGMA R rhil-10 από R&D SYSTEMS
73 ΥΛΙΚΑ 73 T Triton X-100 από SIGMA Trypticase Soy Agar (TSA) από MERCK Trypticase Soy Broth (TSB) από MERCK Tween 20 από SIGMA Α Άγαρ από DIFCO Αγαρόζη από GIBCO BRL Αιθανόλη απόλυτη από MERCK Αιθυλεν-διαµιν-τετρα-οξικό οξύ (EDTA) από SIGMA Ακρυλαµίδη από SIGMA Αλβουµίνη ορού βοός (BSA) από SIGMA Αµπικιλλίνη από SCHERING PLOUGH Ανασταλτικά αντισώµατα έναντι των TLR2, TLR4, IL-1β, IL-18 και IL-10 από R&D SYSTEMS Αναστολείς των MAP κινασών p38, MEK1/2 και JNK από την CALBIOCHEM Αντίσωµα anti-goat, rabbit, mouse HRP-conjugated από SANTA-CRUZ BIOTECHNOLOGY Αντίσωµα anti-pjnk από CELL SIGNALING TECHNOLOGIES Αντίσωµα anti-pp38 MAP kinase από CELL SIGNALING TECHNOLOGIES Αντίσωµα anti-pp42/44 MAP kinase από CELL SIGNALING TECHNOLOGIES Αντίσωµα anti-β-actin από CELL SIGNALING TECHNOLOGIES Β Βλαστισιδίνη (Blasticidin) από INVITROGEN β-µερκαπτοαιθανόλη από MERCK Βορικό οξύ από SERVA Βουτανόλη από MERCK Βρωµιούχο αιθίδιο από SIGMA
74 74 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Γ Γενταµικίνη από SCHERING PLOUGH Γλυκερόλη από SIGMA Γλυκίνη από INVITROGEN Γλυκόζη από SIGMA είκτες µοριακού µεγέθους DNA από GIBCO BRL είκτες µοριακού µεγέθους πρωτεϊνών από BIORAD εσοξυχολικό νάτριο από SIGMA ιακυλο-λιποπεπτίδιο (Pam2CSK4) από INVIVOGEN ιάλυµα Ficol-Hypaque-1077 από SIGMA ιάλυµα PBS (χωρίς Mg +2 /Ca +2 ) GIBCO BRL ιάλυµα TBE από INVITROGEN ιάλυµα TBS από GIBCO BRL ιάλυµα TE από GIBCO BRL ιάλυµα Tris-HCl ph 6,8 από GIBCO BRL ιάλυµα Tris-HCl ph 8,8 από INVITROGEN ιάλυµα TRIzol από INVITROGEN ιάλυµα για µέτρηση πρωτεϊνών κατά BRADFORD από BIORAD ιάλυµα εµφάνισης και στερέωσης φιλµ αυτοραδιογραφίας από KODAK ιάλυµα Η 2 Ο 2 30% από SIGMA ιάλυµα στερέωσης Mowiol 4-88 από CALBIOCHEM ιάλυµα χηµειοφωταύγειας ECL από AMERSHAM BIOSCIENCES ιεθυλπυροκαρβονικό (DEPC) από SIGMA ιηθητικό χαρτί Whattman No 3 ιµεθυλσουλφοξίδη (DMSO) από SIGMA ις-ακρυλαµίδη από SIGMA Ε
75 ΥΛΙΚΑ 75 Εκχύλισµα ζύµης από DIFCO Επιδεκτικά βακτήρια E.coli στελέχους DH5α από INVITROGEN Θ Θειικό δωδεκυλικό νάτριο (SDS) από MERCK Θρεπτικό υλικό D-MEM από GIBCO BRL Θρεπτικό υλικό Opti-MEM από GIBCO BRL Θρεπτικό υλικό RPMI 1640 από GIBCO BRL Θρυψίνη-EDTA από INVITROGEN Ι Ισοπροπυλική Αλκοόλη από MERCK Κ Καναµυκίνη από SIGMA Κατιονικό λιπόσωµα Lipopofectamine 2000 από INVITROGEN Κυανούν της βρωµοφαινόλης από BDH Chemicals Κυανούν του τρυπανίου (Trypan blue) από BIOCHROM Λ Λιποπολυσακχαρίτης του κολοβακτηριδίου (LPS E. coli 055:B5) από SIGMA Λουµινόλη από SIGMA Μ Μεθανόλη από MERCK
76 76 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Μεµβράνες νιτροκυτταρίνης από PIERCE Ο Οξικό νάτριο από MERCK Οξικό οξύ παγόµορφο (glacial) από MERCK Ορός εµβρύου µόσχου (FCS) από GIBCO BRL Π Περιοριστικά ένζυµα από NEW ENGLAND BIOLABS Προσταγλανδίνη Ε2 (PGE2) από SIGMA Τ Τετραµεθυλ-αιθαν-διαµίνη (TEMED) από SIGMA Τριακυλο-λιποπεπτίδιο (Pam3CSK4) από INVIVOGEN Τρις-βάση από SIGMA Τρυπτόνη από DIFCO Υ Υδροµυκίνη (HydroGold) από INVITROGEN Υδροξυ-αιθυλ-πιπεραζιν-αιθαν-σουλφονικό οξύ (HEPES) από SIGMA Υλικό κατάψυξης κυττάρων Freezing medium D-MEM από GIBCO BRL Υλικό κατάψυξης κυττάρων Freezing medium RPMI 1640 από GIBCO BRL Υπερθειικό αµµώνιο (ammonium persulfate, APS) από SIGMA Φ
77 ΥΛΙΚΑ 77 Φαινυλ-µεθυλ-σουλφονυλ-φθορίδιο (PMSF) από SIGMA Φιλµ αυτοραδιογραφίας από KODAK Φορβολικός εστέρας (PMA) από SIGMA Χ Χλωροφόρµιο από SIGMA Χρωστική Xylene cyanol FF από SIGMA Χρωστική Coomassie Brilliant Blue R250 από MERCK Χρωστική Ponceau-S από SERVA Τα πλαστικά φιαλίδια µίας χρήσης 15 και 50mL, οι φιάλες κυτταροκαλλιέργειας, οι πλάκες µικροκαλλιεργειών 96 φρεατίων µε κοίλο και/ή επίπεδο πυθµένα, τα φιαλίδια τύπου eppendorf και τα κρυοάντοχα φιαλίδια των 2mL ήταν της εταιρίας CORNING COSTAR.
78
79 ΣΥΣΚΕΥΕΣ 79 2 ΣΥΣΚΕΥΕΣ Ψυχοµένη φυγόκεντρος τύπου Sorval RC5C Φασµατοφωτόµετρο U.V. GeneQuantII της εταιρείας Pharmacia Biotech Φωτόµετρο ELISA Sirio-S Συσκευή ηλεκτροφόρησης πρωτεϊνών XCell SureLock Mini-Cell της εταιρείας NOVEX Συσκευή αποτύπωσης πρωτεϊνών XCell II Blot Module της εταιρείας NOVEX Συσκευή ηλεκτροφόρησης DNA/RNA Horizon 11-1 της εταιρείας Gibco BRL VORTEX Genie 2 της εταιρείας Scientific Industries Υδατόλουτρο 37 C της εταιρείας BioLine Θάλαµος καλλιέργειας ανθρωπίνων κυττάρων 37 C Model 3250 της εταιρείας Forma Scientific Κλίβανος επώασης βακτηρίων Θάλαµος κάθετης (νηµατικής ροής) HB 2448 της εταιρείας Holten Τροφοδοτικό σταθερής έντασης Power/PAC 300 της εταιρείας Bio Rad Λουµινόµετρο TD20/20 της εταιρείας Turner Designs Ψυχοµένη φυγόκεντρος για φιαλίδια τύπου eppendorf 5417R της εταιρείας Eppendorf Στήλη απιονισµένου νερού και συσκευή απόσταξης Συσκευές αποστείρωσης γυάλινων φιαλών και διαλυµάτων (αυτόκαυστο)
80 80 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Αυτόµατο πλυντήριο µικρο-επωαστικής πλάκας 96-φρεατίων της εταιρείας Sorn Biomedica Ψυχοµένη φυγόκεντρος τύπου Universal 32R της εταιρείας Hettich Κυτταροµετρία ροής FACS Epics XL MCL της εταιρείας Beckman Coulter Μικροσκόπιο Ανοσοφθορισµού HBO 50 Microscope Illuminator της εταιρείας Zeiss Οπτικό µικροσκόπιο Axiostar Plus της εταιρείας Zeiss Φυγόκεντρος 5804R της εταιρείας Eppendorf Συσκευή φωτογράφησης gel MiniBIS της εταιρείας DNR Συσκευή µέτρησης ph Model 215 της εταιρείας Denver Instruments Επιδαπέδιος κλίβανος οριζόντιας ανάδευσης Orbit Environ-Shaker της εταιρείας LabLine Οι συσκευές που αναφέρονται βρίσκονται στο Εργαστήριο Μικροβιολογίας στα Προκλινικά Κτίρια Τµήµατος Ιατρικής του Πανεπιστηµίου Πατρών εκτός από το Beckman Coulter Epics XL MCL, στο οποίο έγινε η FACS ανάλυση, που βρίσκεται στο εργαστήριο Αιµατολογίας στα Προκλινικά Κτίρια Τµήµατος Ιατρικής του Πανεπιστηµίου Πατρών
81 ΜΕΘΟΔΟΙ 81 3 ΜΕΘΟΔΟΙ 3.1 Κύτταρα, αντιδραστήρια Στελέχη βακτηρίων Στην παρούσα εργασία χρησιµοποιήθηκαν στελέχη Brucella melitensis που αποµονώθηκαν από καλλιέργειες αίµατος ασθενών που έπασχαν από οξεία βρουκέλλωση και νοσηλεύθηκαν στο Πανεπιστηµιακό Γενικό Νοσοκοµείο Πατρών. Επιπλέον, χρησιµοποιήθηκε το στέλεχος κτηνιατρικού εµβολίου Brucella melitensis Rev.1. Αποικίες που αναπτύχθηκαν σε Trypticase soy άγαρ (TSA) µετά εµβολιασµό από την υγρή καλλιέργεια ταυτοποιήθηκαν ως B. melitensis µε βάση την ιδιότητα βραδείας ή µη υδρόλυσης της ουρίας, ανάπτυξη απουσία CO 2, αδυναµία παραγωγής υδροθείου και την ανάπτυξη σε υλικό µε βασική φουξίνη (1: ) και θειονίνη (1: ). Τα στελέχη, αφού αποµονώθηκαν και ταυτοποιήθηκαν, ανακαλλιεργήθηκαν σε θρεπτικό ζωµό Trypticase Soy Broth (TSB) και επωάστηκαν στους 37 C υπό συνεχή ανάδευση. Η καλλιέργεια συλλέχθηκε σε λογαριθµική φάση ανάπτυξης (συγκέντρωση 10 8 βακτήρια/ml σύµφωνα µε την κλίµακα McFarland). Τα βακτήρια διατηρήθηκαν στους -80 C, µε προσθήκη 40% γλυκερόλης στο εναιώρηµα. Τα ανωτέρω αποθέµατα γλυκερόλης των στελεχών εµβολιάστηκαν σε TSA και αποικίες δύο έως τριών ηµερών ζωντανών βακτηρίων B. melitensis χρησιµοποιήθηκαν για τη διέγερση ανθρώπινων µονοκυττάρων ή ανθρώπινων κυτταρικών σειρών Ανθρώπινα κύτταρα, κυτταρικές σειρές Διαλύματα Ως θρεπτικά υλικά χρησιµοποιήθηκαν τα RPMI 1640 (+HEPES, + L-Glutamine της GIBCO ) και D-MEM (High glucose της GIBCO ) µε προσθήκη 10% κατ όγκο ορού εµβρύου µόσχου (Fetal Calf Serum, FCS) αδρανοποιηµένου µε θέρµανση και 40µg/mL γενταµικίνης. Τα ανθρώπινα µονοκύτταρα περιφερικού αίµατος καλλιεργήθηκαν σε RPMI 1640, ενώ η κυτταρική σειρά HEK 293 σε D-MEM.
82 82 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Απομόνωση ανθρώπινων μονοπυρήνων κυττάρων από περιφερικό αίμα Αρχή µεθόδου: Ορισµένα πολυσακχαριτιδικά διαλύµατα κατάλληλης πυκνότητας και ωσµοτικότητας µπορούν να διαχωρίζουν σε φάσεις τα συστατικά του αίµατος (Böyum, 1968). Το Ficoll-Hypaque είναι διάλυµα του πολυσακχαρίτη φικόλλη (Ficoll) και µετριζιµίδης (Hypaque) µε πυκνότητα 1077g/mL, το οποίο χρησιµοποιείται για το διαχωρισµό και την αποµόνωση των µονοπύρηνων κυττάρων από ολικό περιφερικό αίµα. Αυτό επιτυγχάνεται όταν ολικό αίµα επιστοιβάζεται σε διάλυµα Ficoll-Hypaque και κατόπιν φυγοκεντρείται σε κλίση πυκνότητας. Κατά τη φυγοκέντρηση, τα ερυθροκύτταρα συσσωµατώνονται και καθιζάνουν, ενώ επάνω τους στοιβάζονται τα κοκκιοκύτταρα τα οποία υπό την ωσµωτική πίεση του διαλύµατος αποκτούν µεγάλη πυκνότητα. Τα µονοπύρηνα κύτταρα, λόγω της µικρότερης πυκνότητάς τους, εντοπίζονται µεταξύ του διαλύµατος φικόλλης και του πλάσµατος, µαζί µε τα αιµοπετάλια. Τέλος, το διάλυµα, το πλάσµα και τα αιµοπετάλια αποµακρύνονται µε φυγοκέντρηση σε χαµηλή βαρυτική δύναµη, ώστε να αποµείνει ο πληθυσµός των µονοπυρήνων κυττάρων (Peripheral Blood Mononuclear Cells- PBMCs) Υλικά: ιάλυµα Ficoll-Hypaque Φυγόκεντρος τύπου Sorval Μικροσκόπιο Ηπαρινισµένο αίµα υγιών αιµοδοτών Πλαστικά φιαλίδια χωρητικότητας 50mL Πιπέττες Παστέρ 10mL Πορεία: Περιφερικό αίµα υγιών αιµοδοτών αραιώνεται (1:1) µε στείρο ρυθµιστικό διάλυµα φωσφορικών απουσία δισθενών ιόντων (Phosphate Buffered Saline, PBS χωρίς Mg +2 /Ca +2 ). Στη συνέχεια επιστοιβάζεται σε φιαλίδιο των 50mL προσεκτικά στην επιφάνεια υγρού στρώµατος 15mL διαλύµατος Ficoll-Hypaque σε θερµοκρασία δωµατίου και αναλογία 1:2. Ακολουθεί φυγοκέντρηση σε 400 g για 30 λεπτά σε θερµοκρασία δωµατίου.
83 ΜΕΘΟΔΟΙ 83 Μετά το πέρας της φυγοκέντρησης, προκύπτει ο σχηµατισµός στιβάδων. Η ανώτερη στιβάδα, που αντιπροσωπεύει το πλάσµα, αποχύνεται προσεκτικά µε τη βοήθεια πιπέττας Παστέρ. Η στιβάδα που έχει δηµιουργηθεί από τα µονοπύρηνα κύτταρα και τα αιµοπετάλια µεταφέρεται σε καινούριο φιαλίδιο χωρητικότητας 50mL. Οι στιβάδες του διαλύµατος φικόλλης και των κοκκιοκυττάρων-ερυθρών απορρίπτονται. Τα µονοπύρηνα κύτταρα επαναδιαλύονται σε PBS φυγοκεντρούνται σε 250 g για 10 λεπτά στους 4 C. Η παραπάνω διαδικασία επαναλαµβάνεται τουλάχιστον τρεις φορές. Σκοπός είναι να αποµακρυνθούν υπολείµµατα πλάσµατος, φικόλλης, κυτταρικά θραύσµατα και τα αιµοπετάλια. Τέλος, τα κύτταρα µικροσκοπούνται σε κυτταροµετρική πλάκα Neubauer ώστε να προσδιοριστεί ο φαινότυπος και ο αριθµός τους Απομόνωση μονοκυττάρων με προσκόλληση σε φιάλες κυτταροκαλλιέργειας Αρχή µεθόδου: Τα µονοκύτταρα έχουν την ιδιότητα να προσκολλώνται σε λείες πλαστικές επιφάνειες όπως είναι ο πυθµένας των φιαλών των κυτταροκαλλιεργειών (Bennett & Breit, 1994). Υλικά: Πορεία: PBMCs Φιάλες κυτταροκαλλιέργειας 75cm 2 Ξέστρα κυττάρων RPMI %FCS PBS (37 C & 4 C) µονοπύρηνα κύτταρα/cm 2 επιφάνειας της φιάλης κυτταροκαλλιέργειας επωάζονται σε προθερµασµένο στους RPMI %FCS για ώρες στους 37 C, 5%CO 2. Μετά την επώαση, τα µονοκύτταρα έχουν προσκολληθεί στον πυθµένα της φιάλης, ενώ τα λεµφοκύτταρα αποµακρύνονται µε απόρριψη του θρεπτικού υλικού και έκπλυση µε θερµό PBS (37 C). Ακολουθεί πρόσθεση κρύου PBS (4 C) και αποκόλληση των µονοκυττάρων από τον πυθµένα µε αποστειρωµένα ξέστρα. Τα µονοκύτταρα που αποµονώθηκαν µε την παραπάνω διαδικασία, διατηρούνται σε θρεπτικό υλικό RPMI 1640 (+10%FCS, 40µg/mL γενταµικίνη) για 24 ώρες στους 37 C, πριν χρησιµοποιηθούν για
84 84 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ πειραµατικούς σκοπούς. Το συγκεκριµένο χρονικό διάστηµα επιτρέπει στα κύτταρα να επανέλθουν σε κατάσταση ηρεµίας, καθώς η διαδικασία της αποµόνωσης τα ενεργοποιεί Καλλιέργεια κυτταρικής σειράς HEK-293 Η κυτταρική σειρά HEK-293 (American Tissue Culture Collection Number CRL- 1573), είναι επιθηλιακά κύτταρα που προέρχονται από ανθρώπινο νεφρό εµβρύου, µετασχηµατισµένα µε DNA του αδενοϊού τύπου 5 (Graham et al., 1977). Τα HEK-293 εκφράζουν ενδογενώς τους υποδοχείς TLR1,3,5 και 6, αλλά όχι τους TLR2 και TLR4. Οι κυτταρικές σειρές 293-TLR4A-MD2-CD14 και 293-TLR2-CD14 (Invivogen) πρoέρχονται από σταθερή διαµόλυνση των HEK-293 ώστε να εκφράζουν στην επιφάνειά τους το σύµπλοκο υποδοχέων TLR4/MD2/CD14 και TLR2/CD14, αντιστοίχως. Τα κύτταρα διατηρούνται σε καλλιεργητικό υγρό D-MEM µε 10%FCS σε ατµόσφαιρα 5%CO 2 στους 37 C. Οι θυγατρικές κυτταρικές σειρές απαιτούν επιπλέον την προσθήκη 10µg/mL βλαστισιδίνης (Blasticidin) και 50µg/mL υδροµυκίνης (HydroGold) για τη διατήρηση της έκφρασης των υποδοχέων. Αρχικά τοποθετούνται από 2 έως κύτταρα ανά cm 2 επιφανείας της φιάλης κυτταροκαλλιέργειας, τα οποία προσκολλώνται στον πυθµένα. Όταν υπερβούν τα /cm 2 αποκολλώνται µε τη χρήση διαλύµατος θρυψίνης-edta. Συγκεκριµένα, αποχύνεται το θρεπτικό υλικό, ακολουθεί µία πλύση των κυττάρων µε PBS, ώστε να αποµακρυνθεί ο ορός, ο οποίος αδρανοποιεί τη θρυψίνη και προστίθενται 5mL διαλύµατος θρυψίνης-edta στη φιάλη των 75cm 2. Η φιάλη επωάζεται 1-5 λεπτά στους 37 C, 5%CO 2, για να δοθεί χρόνος στο ένζυµο να δράσει. Μετά την επώαση, τα κύτταρα αποκολλώνται µε ελαφρό χτύπηµα της φιάλη της κυτταροκαλλιέργειας. Φυσιολογικά, τα υγιή κύτταρα δεν αποκολλώνται από τη φιάλη πριν τη χρήση της θρυψίνης. Κατόπιν, προστίθενται στη φιάλη 15mL D-MEM+FCS, οπότε ο ορός αδρανοποιεί τη θρυψίνη. Τέλος, τα κύτταρα συλλέγονται, πλένονται, καταµετρώνται και µοιράζονται µε νέο θρεπτικό υλικό στις φιάλες της κυτταροκαλλιέργειας στην επιθυµητή συγκέντρωση Μέτρηση κυττάρων-προσδιορισμός βιωσιμότητας Αρχή µεθόδου: Ως κυτταρική βιωσιµότητα ορίζεται ο λόγος του αριθµού ζωντανών κυττάρων προς το συνολικό αριθµό κυττάρων, όπως µετρώνται σε αιµατοκυτταροµετρική πλάκα.
85 ΜΕΘΟΔΟΙ 85 Κύτταρα τα οποία προσλαµβάνουν τη χρωστική κυανούν του τρυπανίου θεωρούνται νεκρά. Υλικά: Πορεία: Αιµατοκυτταροµετρική πλάκα Neubauer ιάλυµα κυανού του τρυπανίου 0,4% w/v σε PBS Στο κυτταρικό εναιώρηµα προστίθεται διάλυµα χρωστικής κυανού του τρυπανίου 0,4% w/v, σε αναλογία εννέα προς ένα, ώστε η τελική συγκέντρωση της χρωστικής να είναι 0,04% w/v. Ακολουθεί επώαση για 5 λεπτά σε θερµοκρασία δωµατίου. Τα κύτταρα τοποθετούνται στο αιµατοκυτταρόµετρο και µετρώνται. Από τον αριθµό των κυττάρων που έχουν βαφεί κυανά λόγω εισόδου της χρωστικής, υπολογίζεται το ποσοστό βιωσιµότητας σύµφωνα µε τη σχέση: αριθµός νεκρών κυττάρων κυανά Ποσοστό βιωσιµότητας % =100 1 αριθµός µετρηθέντων κυττάρων Ο συνολικός αριθµός των κυττάρων στο εναιώρηµα υπολογίζεται από τη σχέση: Σύνολο κυττάρων/ml=αριθµός µετρηθέντων κυττάρων 10 αραίωση Κατάψυξη κυτταρικών σειρών Αρχή µεθόδου: Οι κυτταρικές σειρές που βρίσκονται σε καλλιέργεια γηράσκουν, µεταλλάσσονται και κινδυνεύουν να µολυνθούν. Συνεπώς, είναι απαραίτητη η ψύξη τους για µακροπρόθεσµη φύλαξη. Αυτό επιτυγχάνεται µε αποθήκευσή τους σε ατµούς υγρού αζώτου σε πλήρες θρεπτικό υλικό παρουσία διµεθυλσουλφοξίδης (DMSO). Η DMSO είναι κρυοπροστατευτικός παράγοντας, ο οποίος µειώνει το σηµείο πήξεως του θρεπτικού υλικού. Αυτό έχει ως αποτέλεσµα την αργή πήξη του και άρα την αποφυγή σχηµατισµού κρυστάλλων που είναι βλαβεροί για τα κύτταρα. Πορεία: Κυτταροκαλλιέργεια σε λογαριθµική φάση ανάπτυξης φυγοκεντρείται σε 700 g επί 5 λεπτά. Το υπερκείµενο απορρίπτεται και το κυτταρικό ίζηµα επαναιωρείται σε κρύο καλλιεργητικό υλικό που αποτελείται από RPMI 1640 ή D-MEM µε 20%FCS και 10%DMSO. Η πυκνότητα των κυττάρων ρυθµίζεται στα κύτταρα/ml. Από το κυτταρικό εναιώρηµα, 1 ml φέρεται σε ειδικά κρυοάντοχα σωληνάρια των 2 ml, τα
86 86 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ οποία καταψύχονται σταδιακά σε δοχείο µε ισοπροπανόλη έως τους -80 C. Μετά 24 ώρες µεταφέρονται σε ειδική φιάλη που περιέχει υγρό άζωτο (-196 C) Απόψυξη κυτταρικών σειρών Αρχή µεθόδου: Η απόψυξη των κυττάρων από το υγρό άζωτο για την επαναχρησιµοποίησή τους, είναι µία διαδικασία που τα καταπονεί και προκαλεί το θάνατό τους. Εποµένως, η ταχεία θέρµανση και η αποµάκρυνση της DMSO είναι ουσιώδεις διαδικασίες για την υψηλή αναλογία επιβίωσης των κυττάρων. Πορεία: Το κρυοάντοχο σωληνάριο, στο οποίο είχαν παγώσει τα κύτταρα, αποσύρεται από το υγρό άζωτο και τοποθετείται άµεσα σε υδατόλουτρο στους 37 C. Μόλις το περιεχόµενο υγροποιηθεί, αραιώνεται περίπου δέκα φορές µε προθερµασµένο στους 37 C θρεπτικό υλικό και φυγοκεντρείται για 5 λεπτά σε 700 g. Το υπερκείµενο απορρίπτεται και το ίζηµα επαναιωρείται στην απαιτούµενη ποσότητα θρεπτικού υλικού. Ακολούθως, φέρεται σε φιάλες καλλιέργειας και τοποθετείται στους 37 C, 5%CO Αντιδραστήρια Ανασταλτικά αντισώματα και αναστολείς MAP κινασών Ο αποκλεισµός υποδοχέων έγινε µε αντισώµατα που διατίθενται από την εταιρεία R&D Systems. Ως µάρτυρας, χρησιµοποιήθηκε µη ειδικό αντίσωµα του ίδιου ισοτύπου. Οι συγκεντρώσεις που χρησιµοποιήθηκαν είναι οι ακόλουθες: 10µg/mL πολυκλωνικού αντισώµατος έναντι του υποδοχέα TLR4 1µg/mL µονοκλωνικού αντισώµατος έναντι του υποδοχέα TLR2 1µg/mL πολυκλωνικού αντισώµατος έναντι της κυτταροκίνης IL-1β 10µg/mL πολυκλωνικού αντισώµατος έναντι της κυτταροκίνης IL-10 1µg/mL µονοκλωνικού αντισώµατος έναντι της κυτταροκίνης IL-18 Η αναστολή των MAP κινασών πραγµατοποιήθηκε µε ειδικούς αναστολείς, που διατίθενται από την εταιρεία Calbiochem. Ως µάρτυρας χρησιµοποιήθηκε ο διαλύτης των αναστολέων, η DMSO. Οι συγκεντρώσεις που χρησιµοποιήθηκαν είναι οι ακόλουθες: 50µM του αναστολέα των MEK 1/2, PD µM του αναστολέα της p38, SB203580
87 ΜΕΘΟΔΟΙ 87 20µM του αναστολέα της JNK, SP Πορεία: Ανθρώπινα µονοκύτταρα αναδιαλύονται σε πλήρες θρεπτικό υλικό RPMI, σε συγκέντρωση 10 6 /ml και τοποθετούνται σε καλλιεργητική πλάκα 24 φρεατίων. Στο θρεπτικό υλικό προστίθεται το ανάλογο αντίσωµα ή ο φαρµακευτικός αναστολέας. Ακολουθεί επώαση 1 ώρας σε κλίβανο µε ατµόσφαιρα 5%CO 2. Στη συνέχεια, πραγµατοποιείται η διέγερση των κυττάρων Αντιδραστήρια για τη διέγερση ευκαρυωτικών κυττάρων Για τις ανάγκες των πειραµάτων τα µονοκύτταρα ή οι κυτταρικές σειρές THP-1 και HEK 293 διεγέρθηκαν µε τους κατωτέρω παράγοντες στις ανάλογες συγκεντρώσεις: Ζωντανά βακτήρια B. melitensis ή B. melitensis Rev.1, σε αναλογία 20 βακτηρίων ανά µονοκύτταρο (20:1 Multiplicity of Infection MOI) Λιποπολυσακχαρίτη του κολοβακτηριδίου (LPS E. coli 055:B5), ο οποίος αποτελεί τον πρότυπο διεγέρτη του συµπλόκου υποδοχέων TLR4/MD2/CD14, σε συγκέντρωση 0,5µg/mL Τριακυλο-λιποπεπτίδιο (Pam3CSK4), το οποίο αποτελεί ειδικό διεγέρτη του συµπλόκου υποδοχέων TLR1/TLR2, σε συγκέντρωση 1µg/mL ιακυλο-λιποπεπτίδιο (Pam2CSK4), το οποίο αποτελεί ειδικό διεγέρτη του συµπλόκου υποδοχέων TLR2/TLR6, σε συγκέντρωση 0,5µg/mL Φορβολικός εστέρας (PMA), ο οποίος αποτελεί διεγέρτη των µεταγραφικών παραγόντων AP-1 και NFκB, σε συγκέντρωση 5ng/mL Προσταγλανδίνη Ε2 (PGE2), η οποία ενεργοποιεί το µεταγραφικό παράγοντα CREB, σε συγκέντρωση 10-6 M Μετά το πέρας της διέγερσης και του χρόνου επώασης µε τους αντίστοιχους διεγέρτες, τα κύτταρα συλλέγονται µε φυγοκέντρηση, πλένονται µία φορά µε PBS και ακολουθεί η αποµόνωση πρωτεϊνών ή νουκλεϊνικών οξέων. Το υπερκείµενο της καλλιέργειας µετά τη φυγοκέντρηση φυλάσσεται στους -20 C µέχρι τη χρησιµοποίησή του.
88
89 ΜΕΘΟΔΟΙ Αναλυτικές μέθοδοι Δοκιμασία προστασίας από τη γενταμικίνη Αρχή µεθόδου: Η δοκιµασία προστασίας από τη γενταµικίνη, ή δοκιµασία επιβίωσης, είναι µία µέθοδος που χρησιµοποιείται στη µικροβιολογία ώστε να ποσοτικοποιηθεί η ικανότητα παθογόνων βακτηρίων να εισβάλουν σε ευκαρυωτικά κύτταρα. Τα ενδοκυττάρια βακτήρια πρέπει να εισέλθουν στα κύτταρα του ξενιστή ώστε να πολλαπλασιαστούν και να προκαλέσουν λοίµωξη. Η δοκιµασία επιβίωσης βασίζεται στην ιδιότητα ορισµένων αντιµικροβιακών να µη µπορούν να διαπεράσουν την κυτταροπλασµατική µεµβράνη ευκαρυωτικών κυττάρων. Συνεπώς, τα βακτήρια που βρίσκονται στο εσωτερικό του κυττάρου δε βλάπτονται από το αντιµικροβιακό και µπορούν να διαχωριστούν από αυτά που δεν κατάφεραν να διεισδύσουν, τα οποία φονεύονται. Ακολουθεί λύση των κυττάρων και επίστρωση του εκχυλίσµατος σε στερεό θρεπτικό υλικό. Τα βακτήρια που επιβίωσαν σχηµατίζουν αποικίες, οι οποίες µετρώνται. Πορεία: Ανθρώπινα µονοκύτταρα µολύνονται µε ζωντανά βακτήρια B. melitensis, σε αναλογία 20 βακτηρίων ανά µονοκύτταρο, σε καλλιεργητική πλάκα 24 φρεατίων. Η πλάκα φυγοκεντρείται σε συνθήκες 500 g, 5 λεπτά σε θερµοκρασία δωµατίου, ώστε να ξεκινήσει η µόλυνση. Κατόπιν, τοποθετείται σε επωαστικό κλίβανο για 30 λεπτά, ώστε να ολοκληρωθεί η φαγοκυττάρωση. Ακολουθούν τρείς πλύσεις των κυττάρων µε ρυθµιστικό διάλυµα PBS και προσθήκη πλήρους θρεπτικού υλικού RPMI µε 100µg/mL γενταµικίνης, ώστε να αποµακρυνθούν τα βακτήρια που δε φαγοκυτταρώθηκαν. Μετά από 1 ώρα επώασης σε κλίβανο, το θρεπτικό υλικό αντικαθίσταται από ίδιο υλικό µε 20µg/mL αντιµικροβιακού. Τα κύτταρα που λύονται σε αυτό το χρονικό σηµείο περιέχουν τον αρχικό αριθµό βακτηρίων που κατόρθωσαν να εισέλθουν στο εσωτερικό του κυττάρου, αποτελώντας σηµείο αναφοράς της µεθόδου. Τα υπόλοιπα κύτταρα επωάζονται σε κλίβανο για διάφορα χρονικά διαστήµατα, ανάλογα µε τις πειραµατικές ανάγκες. Μετά το πέρας της επώασης, ακολουθούν τρεις πλύσεις σε PBS και λύση των κυττάρων σε διάλυµα PBS µε 0,1% v/v Triton X-100. Τα εκχυλίσµατα ανακινούνται έντονα και διαδοχικές αραιώσεις τους επιστρώνονται σε TSA.
90 90 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Προσδιορισμός κυτταροκινών σε υπερκείμενα ανθρωπίνων καλλιεργειών με ενζυμική μέθοδο ανοσοπροσρόφησης (Enzyme Linked ImmunoSorbent Assay- ELISA) Αρχή µεθόδου: Η µέθοδος, πρωτοπεριγράφηκε το 1971, ταυτόχρονα από τους Engvall και Perlmann και τους Van Weemen και Schuurs (Engvall & Perlmann, 1971; Van Weemen & Schuurs, 1971). Μονοκλωνικό αντίσωµα µε ειδικότητα έναντι της µετρούµενης κυτταροκίνης έχει ακινητοποιηθεί σε πολυστυρενική µικροπλάκα επώασης. Πρότυπα διαλύµατα γνωστής συγκέντρωσης κυτταροκίνης και τα προς ανίχνευση δείγµατα προστίθενται στην πλάκα. Η υπάρχουσα ποσότητα κυτταροκίνης δεσµεύεται ειδικά στο ακινητοποιηµένο στην πλάκα αντίσωµα. Ακολουθούν πλύσεις για την αποµάκρυνση περίσσειας µη συνδεδεµένης πρωτεΐνης. Στη συνέχεια, προστίθεται στην πλάκα σεσηµασµένο µε ένζυµο αντίσωµα έναντι της κυτταροκίνης. Το ένζυµο στην περίπτωση των TNF-α, IL-1β, IL-6 και IL-10 είναι η υπεροξειδάση της αγριοραπανίδας (HorseRadish Peroxidase, HRP), ενώ στην περίπτωση της IL-12/p70 είναι η αλκαλική φωσφατάση (Alkaline Phosphatase, AP). Κατόπιν, προστίθεται το κατάλληλο υπόστρωµα για το ένζυµο (τετρα-µεθυλ-βενζιδίνη (Tetra-Methyl-Benzidine, TMB) ή Nicotinamide Adenine Dinucleotide Phosphate (NADPH), αντιστοίχως) µε αποτέλεσµα τη δηµιουργία χρώµατος ανάλογου του ποσού πρωτεΐνης. Η δηµιουργία χρώµατος τερµατίζεται µε την προσθήκη αραιού διαλύµατος 2N H 2 SO 4 και η ένταση της οπτικής απορρόφησης µετράται σε φασµατοσκόπιο σε µήκος κύµατος 450nm ή 490nm, αντιστοίχως. Πορεία: Ο προσδιορισµός των επιπέδων TNF-α, IL-1β, IL-6, IL-10 και IL-12/p70 σε υπερκείµενα κυτταροκαλλιεργειών έγινε µε εµπορικά διαθέσιµη ELISA της εταιρείας R&D Systems, σύµφωνα µε τις οδηγίες της κατασκευάστριας εταιρείας Ανίχνευση και διαχωρισμός αποπτωτικών και νεκρών κυττάρων με χρώση αννεξίνης V- ιωδιούχου προπιδίου Αρχή µεθόδου: Η απόπτωση είναι µία διαδικασία προγραµµατισµένου κυτταρικού θανάτου που διαχωρίζεται µορφολογικά και βιοχηµικά από τη νέκρωση. Σε φυσιολογικά ζωντανά κύτταρα η φωσφατιδυλοσερίνη (phosphatidylserine, PS) εντοπίζεται στην
91 ΜΕΘΟΔΟΙ 91 κυτταροπλασµατική επιφάνεια της κυτταρικής µεµβράνης. Σε αποπτωτικά κύτταρα η PS µετατοπίζεται στην εξωτερική πλευρά της κυτταροπλασµατικής µεµβράνης και εκτίθεται στο εξωτερικό περιβάλλον του κυττάρου. Το ανθρώπινο αντιπηκτικό αννεξίνη V είναι µία πρωτεΐνη µε υψηλή συγγένεια για την PS. Συνεπώς, αννεξίνη V σεσηµασµένη µε φθοριόχρωµα µπορεί να επιτρέψει την ανίχνευση αποπτωτικών κυττάρων. Η φθορίζουσα χρωστική ιωδιούχο προπίδιο (Propidium Iodide, PI) έχει την ικανότητα να προσδένεται στα νουκλεϊνικά οξέα, αλλά δε διαπερνά την κυτταροπλασµατική µεµβράνη ζωντανών και αποπτωτικών κυττάρων. Η ταυτόχρονη χρώση κυττάρων µε σεσηµασµένη µε πράσινη χρωστική αννεξίνη V και µε PI θα αποδώσει πράσινο φθορισµό στα αποπτωτικά κύτταρα, πράσινο και κόκκινο φθορισµό στα νεκρά κύτταρα, ενώ τα υγιή κύτταρα δε θα φθορίζουν. Πορεία: Τα κύτταρα πλένονται µία φορά µε στείρο διάλυµα PBS. Ακολουθεί προσθήκη διαλύµατος µε σεσηµασµένη αννεξίνη V και διαλύµατος µε PI. Tα κύτταρα επωάζονται σε θερµοκρασία δωµατίου για 15 λεπτά, προστατευµένα από το ηλιακό φως. Επαναλαµβάνεται µία πλύση µε στείρο διάλυµα PBS. Τα κύτταρα τοποθετούνται σε αντικειµενοφόρο πλάκα και καθηλώνονται µε διάλυµα Mowiol 4-88 ώστε να µικροσκοπηθούν ή αναλύονται µε κυτταροµετρία ροής Απομόνωση πρωτεϊνικών εκχυλισμάτων Αρχή µεθόδου: Το διάλυµα µεθόδου ραδιοανοσοκαθιζήσεως (RadioImmunoPrecipitation Buffer RIPA) είναι από τα πλέον διαδεδοµένα και αξιόπιστα λυτικά διαλύµατα για αποµόνωση ολικών πρωτεϊνικών εκχυλισµάτων και είναι συµβατό µε πλήθος εφαρµογών. Αποτελείται από αποδιατακτικές ουσίες (Igepal) και ιοντικά απορρυπαντικά (SDS, εσοξυχολικό νάτριο) σε διάλυµα µεγάλης ωσµοτικότητας, µε αποτέλεσµα να διασπά την κυτταροπλασµατική και πυρηνική µεµβράνη των κυττάρων. Μετά από φυγοκέντρηση σε υψηλή βαρυτική δύναµη ( g), τα υπολείµµατα µεµβρανών και τα νουκλεϊνικά οξέα καθιζάνουν, ενώ οι πρωτεΐνες παραµένουν στο διάλυµα. Για την ανίχνευση και τη µελέτη της φωσφορυλίωσης των MAP κινασών στο διάλυµα RIPA προστέθηκαν αναστολείς πρωτεασών και φωσφατασών, οι οποίοι προστατεύουν τις πρωτεΐνες από πρωτεόλυση και αποφωσφορυλίωση.
92 92 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ ιαλύµατα: ιάλυµα RIPA Αναστολείς πρωτεασών- φωσφατασών 150mM NaCl 1mM Na 3 VO 4 50mM Tris-HCl 1mM PMSF 1% v/v Igepal 10µg/mL Aprotinin 0,5% w/v εσοξυχολικό νάτριο 10µg/mL Pepstatin 0,1% w/v SDS 10µg/mL Leupeptin Πορεία: Όλες οι διαδικασίες της αποµόνωσης των πρωτεϊνικών εκχυλισµάτων γίνονται στους 4 C (σε παγόλουτρο ή σε ψυχρό θάλαµο). Τα κύτταρα (~10 6 ) συλλέγονται µε φυγοκέντρηση και πλένονται µία φορά µε στείρο ρυθµιστικό διάλυµα φωσφορικών. Στη συνέχεια φυγοκεντρούνται και επαναδιαλύονται σε 100µL διαλύµατος RIPA. Ακολουθεί επώαση σε παγόλουτρο για 15 λεπτά µε ζωηρή ανακίνηση (για να λυθούν τα κύτταρα). Στη συνέχεια, πραγµατοποιείται φυγοκέντρηση για 15 λεπτά στους 4 C στις g. Το υπερκείµενο της φυγοκέντρησης συλλέγεται προσεκτικά (αντιπροσωπεύει το πρωτεϊνικό εκχύλισµα) και µεταφέρεται σε καινούργιο φιαλίδιο. Το ίζηµα απορρίπτεται. Μικρή ποσότητα από το υπερκείµενο συλλέγεται για τον προσδιορισµό της συγκέντρωσης της πρωτεΐνης σε κάθε δείγµα, ενώ το υπόλοιπο εκχύλισµα φυλάσσεται στους -70 C Ποσοτικός προσδιορισμός πρωτεϊνών Μεθοδολογία Smith για προσδιορισμό πρωτεϊνών σε κυτταροπλασματικά εκχυλίσματα Αρχή µεθόδου: Οι πεπτιδικοί δεσµοί πρωτεϊνών ανάγουν σε αλκαλικό περιβάλλον δισθενή ιόντα χαλκού (Cu+ 2 ) σε µονοσθενή (Cu +1 ) (αντίδραση διουρίας). Η ποσότητα χαλκού που ανάγεται είναι ανάλογη της συγκέντρωσης της πρωτεΐνης. Στη συνέχεια, ο µονοσθενής χαλκός αντιδρά µε δύο µόρια αµφικινχονινικού οξέος (Bicinchoninic acid-bca) και το προϊόν της αντίδρασης είναι έγχρωµο (Smith et al., 1985). Το υδατοδιαλυτό σύµπλοκο παρουσιάζει υψηλή οπτική απορρόφηση σε µήκος κύµατος 562nm, και εµφανίζει γραµµικότητα σε αυξανόµενες συγκεντρώσεις πρωτεΐνης σε ένα ευρύ φάσµα από 20µg/mL έως και 2.000µg/mL (Εικόνα 6). Η επιλογή της συγκεκριµένης µεθόδου για την
93 ΜΕΘΟΔΟΙ 93 µέτρηση των πρωτεϊνικών εκχυλισµάτων από διάλυµα RIPA βασίστηκε στο γεγονός ότι το αντιδραστήριο που χρησιµοποιείται είναι συµβατό µε τις συγκεντρώσεις των χηµικών ενώσεων που περιέχονται στο διάλυµα. Τα αντιδραστήρια διατίθενται έτοιµα προς χρήση από την Pierce (Thermo Scientific). Εικόνα 6: Μεθοδολογία προσδιορισµού πρωτεϊνών κατά Smith Πορεία: Παρασκευάζεται αντιδραστήριο εργασίας BCA (BCA working reagent-wr) µε µείξη 49 όγκων διαλύµατος BCA µε 1 όγκο διαλύµατος θειικού χαλκού. Μετά από ήπια ανάδευση το αντιδραστήριο παρουσιάζει απαλό πράσινο χρώµα και είναι σταθερό για µία µέρα αν διατηρηθεί σε κλειστό δοχείο και σε θερµοκρασία δωµατίου. Στη συνέχεια, παρασκευάζονται τα πρότυπα διαλύµατα από αλβουµίνη ορού βοός σε ένα φάσµα υποδιπλάσιων συγκεντρώσεων από 2.000µg/mL έως και 25µg/mL. Τα πρότυπα διαλύµατα και τα δείγµατα προς µέτρηση µέχρι τη στιγµή της αντίδρασης φυλάσσονται σε παγόλουτρο. Στα φρεάτια της πολυπροπυλενικής πλάκας προστίθενται 25 µl πρότυπου διαλύµατος ή του προς ανίχνευση δείγµατος. Ακολουθεί προσθήκη 200µL BCA WR και επώαση στους 37 C για 30 λεπτά. Μετά το πέρας της επώασης, ακολουθεί µερικός τερµατισµός της αντίδρασης µε την επαναφορά της επωαστικής πλάκας σε θερµοκρασία δωµατίου. Τέλος, και µέσα σε διάστηµα µισής ώρας, πραγµατοποιείται φωτοµέτρηση σε µήκος κύµατος 562nm. Το αποτέλεσµα της µέτρησης για κάθε δείγµα υπολογίζεται από την καµπύλη που σχηµατίζεται από τις απορροφήσεις των πρότυπων διαλυµάτων σε συνάρτηση µε τις συγκεντρώσεις τους και εκφράζεται σε µg/ml.
94 94 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Μεθοδολογία Bradford για προσδιορισμό πρωτεϊνών σε κυτταροπλασματικά εκχυλίσματα Αρχή µεθόδου: Η χρωστική Coomassie Brilliant Blue G-250 δεσµεύεται κυρίως σε βασικά και αρωµατικά αµινοξέα, ιδιαιτέρως την αργινίνη. Η χρωστική, σε όξινο διάλυµα έχει µέγιστη απορρόφηση στα 450nm. Το χρώµα της αλλάζει διαδοχικά µετά την προσθήκη αυξανόµενων συγκεντρώσεων πρωτεΐνης µε αποτέλεσµα να µετατοπίζεται η µέγιστη απορρόφηση στα 595nm. Η αύξηση της απορρόφησης στα 595nm, είναι ανάλογη της ποσότητας της δεσµευµένης χρωστικής και συνεπώς της συγκέντρωσης της πρωτεΐνης (Bradford, 1976). Η µέθοδος προσδιορισµού πρωτεϊνικών εκχυλισµάτων από διάλυµα παθητικής λύσης (PLB, Promega) έγινε µε το εµπορικά διαθέσιµο αντιδραστήριο BIORAD Protein Assay. Η επιλογή αυτής της µεθόδου για τη µέτρηση της συγκέντρωσης των πρωτεϊνών που αποµονώθηκαν µε PLB βασίστηκε στη συµβατότητα του αντιδραστηρίου µε τις χηµικές ενώσεις που περιέχονται στo ανωτέρω διάλυµα. Πορεία: Παρασκευάζονται πέντε διαδοχικές αραιώσεις πρότυπου διαλύµατος BSA σε εύρος συγκεντρώσεως αντίστοιχο µε του προς µέτρηση διαλύµατος. Στις συγκεκριµένες συνθήκες η δοκιµασία είναι γραµµική σε εύρος συγκεντρώσεων πρωτεΐνης από 50 έως 500µg/mL. Σε φιαλίδια τύπου Eppendorf τοποθετούνται 800µL κάθε πρότυπου διαλύµατος και δείγµατος προς µέτρηση. Στη συνέχεια, προστίθενται 200µL διαλύµατος BIORAD και το µείγµα αναδεύεται ζωηρά για 15 δευτερόλεπτα. Ακολουθεί επώαση σε θερµοκρασία δωµατίου για 5 λεπτά. Καθώς η απορρόφηση αυξάνεται συνεχώς µε την πάροδο της ώρας, τα δείγµατα φωτοµετρούνται εντός µίας ώρας. Το αποτέλεσµα της µέτρησης για κάθε δείγµα υπολογίζεται από την καµπύλη που σχηµατίζεται από τις απορροφήσεις των πρότυπων διαλυµάτων σε συνάρτηση µε τις συγκεντρώσεις τους και εκφράζεται σε µg/ml Ηλεκτροφόρηση Γενικές αρχές ηλεκτροφόρησης Ηλεκτροφόρηση είναι η µετακίνηση ηλεκτρικά φορτισµένων µορίων υπό την επίδραση ηλεκτρικού πεδίου. Το ηλεκτρικό φορτίο κάθε µορίου εξαρτάται από το
95 ΜΕΘΟΔΟΙ 95 ισοηλεκτρικό σηµείο και το ph του ρυθµιστικού διαλύµατος στο οποίο βρίσκεται. Έτσι, οι πρωτεΐνες, όταν βρίσκονται σε ηλεκτρικό πεδίο, διαχωρίζονται σε ζώνες ανάλογα µε το φορτίο, το µέγεθος, και τη δοµή τους. Η ηλεκτροφορητική κινητικότητα (µ e ) ενός µορίου αποτελεί φυσική σταθερά υπό ορισµένες συνθήκες. Είναι ανάλογη της απόστασης (U) που διανύει η ουσία στη µονάδα του χρόνου (µετρούµενη σε cm/sec) προς την ισχύ του ηλεκτρικού πεδίου (Ε) (µετρούµενη σε V/cm), δηλαδή µ e =U/E (µε µονάδες cm 2 V -1 sec -1 ). Στην πράξη χρησιµοποιείται η έννοια της σχετικής ηλεκτροφορητικής κινητικότητας, που είναι η απόσταση την οποία διανύει ένα µόριο στη µονάδα του χρόνου κάτω από τις ίδιες συνθήκες ηλεκτρικού πεδίου. Έτσι, αν γίνει ταυτόχρονα ηλεκτροφόρηση ενός µείγµατος ουσιών των οποίων τα µόρια έχουν διαφορετικό ηλεκτρικό φορτίο στην επιφάνεια τους, θα κινηθούν σε διαφορετική απόσταση από το σηµείο εκκίνησης µε αποτέλεσµα τον πλήρη διαχωρισµό τους. Η µετανάστευση των φορτισµένων µορίων µπορεί να γίνει µέσα σε διάλυµα ή µε τη χρησιµοποίηση ενός µέσου υποστήριξης όπως είναι το χαρτί, η οξική κυτταρίνη, πήκτωµα ακρυλαµιδίου ή πήκτωµα αγαρόζης. Η ηλεκτροφόρηση σε πήκτωµα προστατεύει τα µακροµόρια από τη µεταγωγή θερµότητας λόγω της εφαρµογής του ηλεκτρικού πεδίου. Παράλληλα, υποβοηθά το διαχωρισµό τους καθώς επιβραδύνει τη µετανάστευσή τους ανάλογα µε το µέγεθός τους. Η ηλεκτροφόρηση σε πήκτωµα αποτελεί διαδεδοµένη µέθοδο µε εφαρµογή στο διαχωρισµό των νουκλεϊνικών οξέων, καθώς και των πρωτεϊνών Ηλεκτροφόρηση πρωτεϊνών Ηλεκτροφόρηση σε πήκτωμα πολυακρυλαμίδης με αποδιατακτικούς παράγοντες Αρχή µεθόδου: Η ηλεκτροφόρηση σε πήκτωµα πολυακρυλαµίδης µε αποδιατακτικούς παράγοντες (Sodium-Dodecyl-Sulphate PolyAcrylamide Gel Electrophoresis, SDS- PAGE) χρησιµοποιείται για το διαχωρισµό πρωτεϊνών σύµφωνα µε την ηλεκτροφορητική τους κινητικότητα. Εξαιτίας της πρόσδεσης του SDS, οι πρωτεΐνες έχουν ταυτόσηµο φορτίο ανά µονάδα βάρους µε αποτέλεσµα να διαχωρίζονται σύµφωνα µε το µήκος της πολυπεπτιδικής αλυσίδας ή το µοριακό τους βάρος.
96 96 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Το πήκτωµα του πολυακρυλαµιδίου χρησιµοποιείται πολύ συχνά στην πράξη επειδή είναι χηµικά αδρανές, και κατασκευάζεται εύκολα. Η διάµετρος των πόρων του πηκτώµατος µπορεί να τροποποιηθεί ελεγχόµενα ανάλογα µε τις εκάστοτε ανάγκες διαχωρισµού. Τα πηκτώµατα σχηµατίζονται µε βινυλικό πολυµερισµό της µονοµερούς ακρυλαµίδης σε µακριές αλυσίδες πολυακρυλαµίδης. Οι τελευταίες, συµπολυµερίζονται µε τη µονοµερή N,N -µεθυλεν- δις-ακρυλαµίδη, µε αποτέλεσµα το σχηµατισµό δικτύου (Εικόνα 7). Οι ελεύθερες ρίζες οξυγόνου για την έναρξη του πολυµερισµού προέρχονται από το υπερθειικό αµµώνιο (Ammonium PerSulfate, APS) και ο καταλύτης του σχηµατισµού ριζών είναι η N,N,N,N τετραµεθυλ-αιθαν-1,2-διαµίνη (N,N,N,N - TEtraMethyl-Ethane-1,2-Diamine, TEMED). Εικόνα 7: Αντίδραση πολυµερισµού της ακρυλαµίδης Η µέθοδος που ακολουθήθηκε στην παρούσα εργασία είναι προτυπωµένη στη διεθνή βιβλιογραφία (Laemmli, 1970). Στα πειράµατα χρησιµοποιήθηκαν τα ρυθµιστικά διαλύµατα του Laemmli µε τη χρήση του ανιοντικού απορρυπαντικού θειικό δωδεκυλικό νάτριο (SDS) σε πήκτωµα διαχωρισµού 10-12% w/v.
97 ΜΕΘΟΔΟΙ 97 Υλικά διαλύµατα: Συµπυκνωµένο 5 διάλυµα δείγµατος (Sample Buffer) : 5mL Tris-HCl 0,5M, ph 6,8 4mL γλυκερόλη 8mL SDS 10% w/v 2mL κυανούν της βρωµοφαινόλης 1% w/v 3,8mL ddh 2 O 2mL β-µερκαπτοαιθανόλη Το διάλυµα φυλάσσεται σε σκοτεινό φιαλίδιο στους 4 C. Η γλυκερόλη προστατεύει την πρωτεΐνη σε χαµηλές θερµοκρασίες και αυξάνει το βάρος του δείγµατος ώστε να επικάθεται στο πήκτωµα. Το SDS αποδιατάσσει την πρωτεΐνη και της προσδίδει οµοιόµορφο αρνητικό ηλεκτρικό φορτίο. Η χρώση µε κυανούν της βρωµοφαινόλης αποσκοπεί στον εντοπισµό του δείγµατος. Η β- µερκαπτοαιθανόλη είναι αποδιατακτικός παράγοντας ο οποίος διασπά τους δισουλφιδικούς δεσµούς ώστε η πρωτεΐνη να αποκτήσει πρωτοταγή δοµή. Συµπυκνωµένο 5 ρυθµιστικό διάλυµα ηλεκτροδίων (Running buffer ph 8,3): 9g Τρις βάση 43,2g Γλυκίνη 3g SDS Προστίθεται ddh 2 O έως τα 600mL και το διάλυµα φυλάσσεται στους 4 C. Το διάλυµα εργασίας προκύπτει µε αραίωση 1/5 του πυκνού αρχικού διαλύµατος µε απεσταγµένο νερό. Η Τρις βάση χρησιµοποιείται ως ρυθµιστικό διάλυµα διότι είναι αβλαβής για τις πρωτεΐνες. Πήκτωµα διαχωρισµού 10% w/v (Resolving or Lower or Separating gel): Η επιλογή της περιεκτικότητας σε ακρυλαµίδη γίνεται µε βάση το µέγεθος των υπό µελέτη πρωτεϊνών. Για τις ανάγκες των πειραµάτων χρησιµοποιήθηκε πήκτωµα ακρυλαµίδης 10% w/v στο οποίο οι υπό µελέτη πρωτεΐνες µε µοριακό βάρος 38-45kDa µεταναστεύουν περίπου στο µέσον του πηκτώµατος διαχωρισµού. Σε γυάλινη κωνική φιάλη των 100mL προστίθενται µε τη σειρά τα ακόλουθα: 8,2mL ddh 2 O
98 98 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 5mL Tris-HCl 1,5M, ph 8,8 6,6mL διαλύµατος ακρυλαµίδης-δις-ακρυλαµίδης (30%/0,8% w/v) 200µL SDS 10% w/v 100µL APS 10% w/v 10µL TEMED Το µείγµα αναδεύεται µε ήπιες κυκλικές κινήσεις και τοποθετείται στη µήτρα σχηµατισµού πηκτώµατος. Στη συνέχεια, καλύπτεται από µία λεπτή στρώση βουτανόλης ώστε να µην έρχεται σε επαφή µε το οξυγόνο, το οποίο αναστέλλει την επιµήκυνση του πολυµερισµού. Πήκτωµα συµπιέσεως 4% w/v (Stacking or Upper gel): Το πήκτωµα συµπιέσεως περιέχει µικρή ποσότητα ακρυλαµίδης, άρα χαρακτηρίζεται από µεγάλους πόρους, ώστε να επιτρέπει την ταχεία διέλευση των πρωτεϊνών. Επιπλέον, το όξινο ph του δηµιουργεί τις κατάλληλες φυσικές συνθήκες για τη συσσώρευση του δείγµατος σε µία λεπτή ζώνη µόλις εισέρχεται στο πήκτωµα διαχωρισµού. Σε γυάλινη κωνική φιάλη των 100mL προστίθενται µε τη σειρά τα ακόλουθα: 6mL ddh 2 O 2,5mL Tris-HCl 0,5M, ph 6,8 1,5mL διαλύµατος ακρυλαµίδης-δις-ακρυλαµίδης (30%/0,8% w/v) 100µL SDS 10% w/v 50µL APS 10% w/v 10µL TEMED Το µείγµα αναδεύεται µε ήπιες κυκλικές κινήσεις και τοποθετείται επάνω στο ήδη πολυµερισµένο πήκτωµα διαχωρισµού. Πορεία: Η συσκευή και όλα τα εξαρτήµατα που πρόκειται να έρθουν σε επαφή µε το πήκτωµα πλένονται µε απεσταγµένο νερό και στη συνέχεια καθαρίζονται µε 70% v/v αιθανόλη. Σε έτοιµες πλαστικές µήτρες εύρους 1,5mm τοποθετείται το πήκτωµα διαχωρισµού και αφήνεται να πολυµεριστεί για 30 λεπτά περίπου σε θερµοκρασία δωµατίου. Κατόπιν προστίθεται το πήκτωµα συµπίεσης ύψους περίπου 2cm. Αµέσως µετά τοποθετείται ειδική µήτρα υποδοχής δειγµάτων µε εσοχές που θα
99 ΜΕΘΟΔΟΙ 99 σχηµατίσουν τις θέσεις για την τοποθέτηση των δειγµάτων. Μετά τον πολυµερισµό και του πηκτώµατος συµπίεσης, αφαιρείται µε προσοχή η µήτρα έτσι ώστε να παραµείνουν σχηµατισµένες οι θέσεις εναπόθεσης των δειγµάτων. Στη συνέχεια, η µήτρα µε το πήκτωµα προσαρµόζεται στην κάθετη συσκευή ηλεκτροφόρησης και προστίθενται 500mL διαλύµατος ηλεκτροδίων. Παράλληλα, όγκος δείγµατος που περιέχει περί τα 30µg πρωτεΐνης αναµιγνύεται µε ανάλογο όγκο διαλύµατος δείγµατος (5 Sample Buffer) και τοποθετείται σε υδατόλουτρο στους 95 C για 5 λεπτά ώστε να αποδιαταχθούν τα µόρια πρωτεΐνης. Μετά την προετοιµασία τους, τα δείγµατα και διάλυµα δεικτών µοριακού βάρους τοποθετούνται σε ξεχωριστά φρεάτια του πηκτώµατος. Η συσκευή συνδέεται µε πηγή συνεχούς ρεύµατος σταθερής τάσης 80V µέχρι τα δείγµατα να διανύσουν το πήκτωµα συµπίεσης και στη συνέχεια η τάση προσαρµόζεται στα 120V. Τα δείγµατα διατρέχουν κατακόρυφα το πήκτωµα και η ηλεκτροφόρηση τερµατίζεται όταν η χρωστική των δειγµάτων φτάσει στο κάτω άκρο του πηκτώµατος διαχωρισµού Μεταφορά πρωτεϊνών σε μεμβράνη νιτροκυτταρίνης (Western Blotting) Το 1979, ο Towbin και συνεργάτες (Towbin et al., 1979) περιέγραψαν µία µέθοδο µεταφοράς πρωτεϊνών από πήκτωµα ακρυλαµίδης σε µεµβράνη νιτροκυτταρίνης µε την εφαρµογή ηλεκτρικού ρεύµατος. Μετά το διαχωρισµό του πρωτεϊνικού εκχυλίσµατος σε πήκτωµα ακρυλαµίδης µε SDS-PAGE, οι πρωτεΐνες µεταφέρονται στη µεµβράνη, όπου ανιχνεύονται µε ειδικά αντισώµατα. ιάλυµα µεταφοράς (1L): Πορεία: 3,03g Τρις βάση 14,4g Γλυκίνη 1L ddh 2 O Κατά το διαχωρισµό των πρωτεϊνών σε πήκτωµα ακρυλαµίδης παρασκευάζεται το διάλυµα µεταφοράς και ψύχεται σε παγόλουτρο. Παράλληλα, η µεµβράνη νιτροκυτταρίνης, σπόγγοι και διηθητικό χαρτί Whattman No3 στις διαστάσεις του πηκτώµατος εµβαπτίζονται σε διάλυµα µεταφοράς για 15 λεπτά µε ήπια ανακίνηση. Αφού ολοκληρωθεί ο διαχωρισµός των πρωτεϊνών στοιβάζονται µε τη σειρά τα ακόλουθα στην πλευρά της καθόδου της κασέτας µεταφοράς:
100 100 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σπόγγος εµποτισµένος µε διάλυµα µεταφοράς 3 χαρτιά Whattman No3 Πήκτωµα ακρυλαµίδης Μεµβράνη νιτροκυτταρίνης 3 χαρτιά Whattman No3 Σπόγγος εµποτισµένος µε διάλυµα µεταφοράς Η κασέτα µεταφοράς ασφαλίζεται, τοποθετείται µέσα στη συσκευή και καλύπτεται πλήρως µε το διάλυµα µεταφοράς. Ολόκληρη η συσκευή βυθίζεται σε υγρό πάγο και συνδέεται µε πηγή τροφοδοσίας ρεύµατος. Εφαρµόζεται ρεύµα σταθερής έντασης 360mA για 1 ώρα ώστε να πραγµατοποιηθεί η µεταφορά των πρωτεϊνών Χρώση πρωτεϊνών ακινητοποιημένων σε πήκτωμα ακρυλαμίδης με Coomassie Brilliant Blue R250 ιάλυµα χρώσης (1L): 450mL ddh 2 O 450mL Μεθανόλη 100mL Οξικό οξύ 2,5g Coomassie Brilliant Blue R250 Μετά την παρασκευή του, το διάλυµα διηθείται µέσω φίλτρου διαµέτρου 0,45µm και φυλάσσεται σε θερµοκρασία δωµατίου. ιάλυµα αποχρωµατισµού (1L): 450mL ddh 2 O 450mL Μεθανόλη 100mL Οξικό οξύ Πορεία: Σε γυάλινο δοχείο τοποθετείται το πήκτωµα του ακρυλαµιδίου και καλύπτεται από 200mL διαλύµατος χρώσης. Ακολουθεί επώαση µε συνεχή ήπια ανάδευση για µία ώρα σε θερµοκρασία δωµατίου. Στη συνέχεια, το πήκτωµα βυθίζεται στο διάλυµα αποχρωµατισµού µε ήπια ανακίνηση µέχρι τον πλήρη αποχρωµατισµό του. Το διάλυµα χρώσης συλλέγεται και επαναχρησιµοποιείται.
101 ΜΕΘΟΔΟΙ Χρώση πρωτεϊνών ακινητοποιημένων σε μεμβράνη νιτροκυτταρίνης με Ponceau-S ιάλυµα χρώσης (500mL): 25mL Οξικό οξύ 0,5g χρωστικής Ponceau-S 475mL ddh 2 O Μετά την παρασκευή του, το διάλυµα διηθείται µέσω φίλτρου διαµέτρου 0,45µm και φυλάσσεται σε θερµοκρασία δωµατίου. Για τον αποχρωµατισµό της µεµβράνης χρησιµοποιείται διάλυµα Τρις βάσης, χλωριούχου νατρίου (Tris base- Sodium chloride, TBS) ιάλυµα TBS (1L): 1L ddh 2 O 2,42g Τρις βάση 8g NaCl Πορεία: Σε γυάλινο δοχείο τοποθετείται η µεµβράνη νιτροκυτταρίνης και καλύπτεται από 100mL διαλύµατος χρώσης Ponceau-S. Ακολουθεί επώαση µε συνεχή ήπια ανάδευση για 15 λεπτά σε θερµοκρασία δωµατίου. Εφόσον οι πρωτεΐνες έχουν µεταφερθεί επιτυχώς, γίνονται ορατές ως ζώνες διαφορετικού µοριακού βάρους. Στη συνέχεια, η µεµβράνη βυθίζεται σε διάλυµα TBS µε ήπια ανακίνηση µέχρι τον πλήρη αποχρωµατισµό της Κάλυψη μεμβράνης νιτροκυτταρίνης (blocking) Μετά τη µεταφορά των πρωτεϊνών, στη µεµβράνη νιτροκυτταρίνης παραµένουν περιοχές ελεύθερες πρωτεϊνών οι οποίες πρέπει να καλυφθούν. Η διαδικασία αυτή αποτρέπει την απευθείας πρόσδεση του πρώτου ή του δευτέρου αντισώµατος στη µεµβράνη, που θα είχε ως αποτέλεσµα την παραγωγή µη ειδικού σήµατος. ιάλυµα κάλυψης (blocking buffer): ιάλυµα TBS 0,1% v/v Tween20 (TBS-T) 5% w/v αποβουτυρωµένο γάλα ή BSA
102 102 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Πορεία: Η µεµβράνη βυθίζεται σε διάλυµα κάλυψης και επωάζεται µε ήπια ανάδευση για 1 ώρα σε θερµοκρασία δωµατίου. Στη συνέχεια ξεπλένεται τρείς φορές µε διάλυµα TBS-T, ώστε να αποµακρυνθεί πλήρως το διάλυµα κάλυψης Επώαση μεμβράνης νιτροκυτταρίνης με πρώτο και δεύτερο αντίσωμα Η καλυµµένη µεµβράνη επωάζεται µε ειδικό αντίσωµα που αναγνωρίζει την πρωτεΐνη ενδιαφέροντος (πρώτο αντίσωµα) και στη συνέχεια µε αντίσωµα που προσδένεται στο πρώτο και είναι σεσηµασµένο µε το ένζυµο HRP (δεύτερο αντίσωµα). Συνεπώς, δηµιουργείται µία γέφυρα µεταξύ της πρωτεΐνης-στόχου και του ενζύµου που καταλύει την αντίδραση ανίχνευσης. Πορεία: Το πρώτο αντίσωµα αραιώνεται σε TBS-T µε 5% w/v αποβουτυρωµένο γάλα και επωάζεται µε τη µεµβράνη για µία ώρα σε θερµοκρασία δωµατίου. Αντισώµατα που αναγνωρίζουν τη φωσφορυλιωµένη µορφή πρωτεϊνών αραιώνονται σε TBS-T µε 5% w/v BSA και επωάζονται µε τη µεµβράνη ολονυκτίως. Κατόπιν, η περίσσεια αντισώµατος αποµακρύνεται µε τρείς πλύσεις µε TBS-T. Το δεύτερο αντίσωµα αραιώνεται σε TBS-T και επωάζεται µε τη µεµβράνη για µία ώρα σε θερµοκρασία δωµατίου. Ακολουθούν τρείς πλύσεις για την αποµάκρυνση του µη συνδεδεµένου αντισώµατος Ανίχνευση πρωτεϊνών ακινητοποιημένων σε μεμβράνη νιτροκυτταρίνης με χημειοφωταύγεια Αρχή µεθόδου: Χηµειοφωταύγεια ονοµάζεται το φαινόµενο εκποµπής φωτός από µία χηµική ουσία σε κατάσταση διέγερσης. Για την ανίχνευση πρωτεϊνών µε χηµειοφωταύγεια χρησιµοποιείται η χηµική ουσία λουµινόλη. Η λουµινόλη σε αλκαλικές συνθήκες σχηµατίζει ένα διανιόν. Η κατάλυση της αποσύνθεσης του H 2 O 2 από την HRP προκαλεί την τοπική παραγωγή O 2 στο σηµείο που βρίσκεται η πρωτεΐνη ενδιαφέροντος. Το O 2 αντιδρά µε το διανιόν λουµινόλης, µε αποτέλεσµα το σχηµατισµό ασταθούς οργανικού υπεροξειδίου. Το υπεροξείδιο επανέρχεται σε κατάσταση ηρεµίας µε την αποβολή ενέργειας µε τη µορφή φωτονίου. Το φαινόµενο ενισχύεται έως 1000 φορές παρουσία ενώσεων φαινόλης (όπως το p-κουµαρικό οξύ) (Whitehead et al., 1979). Η µέγιστη
103 ΜΕΘΟΔΟΙ 103 εκποµπή φωτός γίνεται σε µήκος κύµατος 428nm και ανιχνεύεται µε αυτοραδιογραφικό φιλµ, ευαίσθητο στο γαλάζιο φως (Εικόνα 8). Εικόνα 8: Αντίδραση χηµειοφωταύγειας της λουµινόλης ιαλύµατα: ιάλυµα 1 ιάλυµα 2 9mL ddh 2 O 9mL ddh 2 O 1mL δ/τος 1M Tρις-HCl, ph 8,5 1mL δ/τος 1M Tρις-HCl, ph 8,5 45µL δ/τος 90mM p-κουµαρικού οξέος 6µL δ/τος 30% v/v H 2 O 2 100µL δ/τος 250mM λουµινόλης Τα διαλύµατα είναι σταθερά για ένα µήνα όταν φυλάσσονται στους 4 C. Επίσης, χρησιµοποιήθηκαν εµπορικά διαθέσιµα διαλύµατα της εταιρείας Amersham Biosciences. Πορεία: Όλες οι διαδικασίες εκτελούνται σε σκοτεινό θάλαµο. Αναµειγνύονται ίσοι όγκοι των δύο διαλυµάτων και το µείγµα καλύπτει την µεµβράνη νιτροκυτταρίνης από την πλευρά που βρίσκονται οι πρωτεΐνες. Ακολουθεί επώαση ενός λεπτού και στη συνέχεια η νιτροκυτταρίνη τυλίγεται σε διαφανή µεµβράνη, τοποθετείται σε ακτινολογική κασέτα και καλύπτεται από αυτοραδιογραφικό φιλµ. Το φιλµ εκτίθεται για διάφορα χρονικά διαστήµατα (1-45 λεπτά) και στη συνέχεια εµφανίζεται µε ειδικά φωτογραφικά διαλύµατα.
104 104 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Απομάκρυνση αντισωμάτων από τη μεμβράνη νιτροκυτταρίνης (Stripping off) Τις περισσότερες φορές είναι απαραίτητη η πλήρης αποµάκρυνση των αντισωµάτων ώστε η µεµβράνη νιτροκυτταρίνης να επαναχρησιµοποιηθεί. Με αυτόν τον τρόπο είναι εφικτός ο διαδοχικός έλεγχος πολλαπλών πρωτεϊνών ενδιαφέροντος στην ίδια µεµβράνη. Η αποδέσµευση των αντισωµάτων από τις θέσεις πρόσδεσής τους επιτυγχάνεται µε διάλυµα που περιέχει αποδιατακτικούς παράγοντες. ιάλυµα αποµάκρυνσης αντισωµάτων (Stripping buffer): 2g SDS 0,985g Τρις HCl 0,697mL β-µερκαπτοαιθανόλη Έως 100mL ddh 2 O Πορεία: Η µεµβράνη νιτροκυτταρίνης βυθίζεται σε Stripping buffer και επωάζεται στους 50 C για 30 λεπτά υπό ήπια ανάδευση. Ακολουθούν δύο πλύσεις σε διάλυµα TBS-T και στη συνέχεια η µεµβράνη µπορεί να επαναχρησιµοποιηθεί Hλεκτροφόρηση νουκλεϊνικών οξέων σε πήκτωμα αγαρόζης Αρχή µεθόδου: Η ηλεκτροφόρηση σε πήκτωµα αγαρόζης χρησιµοποιείται για το διαχωρισµό νουκλεϊνικών οξέων µε βάση το φορτίο τους. Καθώς τα νουκλεϊνικά οξέα είναι αρνητικά φορτισµένα µόρια, η κινητικότητά τους στο πήκτωµα καθορίζεται από το µήκος τους και την τριτοταγή δοµή τους. Η τροποποίηση της συγκέντρωσης της αγαρόζης στο πήκτωµα επιτρέπει το διαχωρισµό µορίων µε διαφορετικά µεγέθη. Για την ανίχνευση των νουκλεϊνικών οξέων, χρησιµοποιείται το βρωµιούχο αιθίδιο (Ethidium Bromide- EtBr). Η συγκεκριµένη χηµική ουσία έχει την ικανότητα να φθορίζει υπό το υπεριώδες φώς όταν προσδένεται στη µείζονα αύλακα των νουκλεϊνικών οξέων.
105 ΜΕΘΟΔΟΙ 105 ιαλύµατα: Συµπυκνωµένο 10 διάλυµα Τρις-Βορικό-EDTA (10 TBE) 1L: 108g Τρις βάση 55g Βορικό οξύ 20mL δ/τος 0,5M EDTA ph 8,0 Έως 1L ddh 2 O Συµπυκνωµένο 6x διάλυµα δείγµατος (6 Sample buffer): 25mg χρώσης Bromophenol blue 25mg χρώσης Xylene cyanol FF 3mL γλυκερόλη 7mL ddh 2 O Πήκτωµα αγαρόζης: 10mL 10 TBE 90mL ddh 2 O 1-2g αγαρόζη 2µL δ/τος 5µg/µL βρωµιούχου αιθιδίου Πορεία: Παρασκευάζεται πήκτωµα αγαρόζης µε συγκέντρωση 1-2% w/v και τοποθετείται στη συσκευή βυθισµένο σε 1 διάλυµα ηλεκτροφόρησης TBE. Στα δείγµατα του DNA ή RNA προστίθεται διάλυµα δείγµατος. Στη συνέχεια, τα δείγµατα τοποθετούνται στα φρεάτια του πηκτώµατος και εφαρµόζεται στη συσκευή τάση 120V. Μετά την πάροδο µίας ώρας, το πήκτωµα παρακολουθείται υπό υπεριώδες φώς, σε ειδική συσκευή µε λυχνία UV. Όσον αφορά στο RNA, αξιολογείται η παρουσία των δύο υποµονάδων ριβοσωµατικού RNA 28S και 18S και η ακεραιότητα του µορίου. Όσον αφορά στο DNA, αξιολογείται η παρουσία και το µήκος των εκάστοτε αναµενοµένων ζωνών.
106 106 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Πολλαπλασιασμός πλασμιδίων Μετασχηματισμός στελέχους E. coli με ανασυνδυασμένο πλασμίδιο (transformation) Αρχή Μεθόδου: Τα περισσότερα είδη βακτηρίων έχουν την ιδιότητα να προσλαµβάνουν και να ενσωµατώνουν στο γενετικό τους υλικό µόρια DNA από το θρεπτικό υλικό στο οποίο καλλιεργούνται. Στις περισσότερες περιπτώσεις, το εξωγενές DNA αποδοµείται κατά την ενσωµάτωσή του στο βακτηριακό γονιδίωµα, αλλά, υπό κατάλληλες συνθήκες µπορεί να ενσωµατωθεί επιτυχώς, ιδιαίτερα όταν το DNA είναι πλασµιδιακό. Τα βακτήρια πού έχουν την ικανότητα µετασχηµατισµού, καλούνται επιδεκτικά (competent cells). Οι Cohen και συνεργάτες (Cohen et al., 1972) παρατήρησαν το 1972 ότι τα ιόντα Ca +2, έχουν την ιδιότητα να αλλάζουν την ικανότητα των κολοβακτηριδίων να προσλαµβάνουν πλασµιδιακό DNA. Ο λόγος για τον οποίο το ρυθµιστικό διάλυµα άλατος CaCl 2 επιτυγχάνει την αποτελεσµατικότερη ενσωµάτωση του πλασµιδιακού DNA στα βακτηριακά κύτταρα δεν είναι µέχρι σήµερα πλήρως κατανοητός. Πιστεύεται, ότι προκαλεί την κατακρήµνιση του DNA το οποίο συσσωρεύεται στην εξωτερική επιφάνεια της βακτηριακής µεµβράνης. Επιπλέον, πιθανολογείται ότι αλλάζει τη διαπερατότητα της µεµβράνης του βακτηρίου µε αποτέλεσµα το πλασµιδιακό DNA να εισέρχεται στο εσωτερικό του κυττάρου. Η πλήρης ενσωµάτωσή του φαίνεται ότι επιτυγχάνεται µε την προσωρινή αλλαγή της θερµοκρασίας ανάπτυξης του βακτηρίου από τους 37 C στους 42 C. Για την παραλαβή µεγάλων ποσοτήτων των ανασυνδυασµένων πλασµιδίων πραγµατοποιήθηκε µετασχηµατισµός επιδεκτικών βακτηρίων E.coli στελέχους DH5α. Τα βακτήρια προετοιµάστηκαν µε τροποποίηση της µεθόδου που προτάθηκε από τον Hanahan (Hanahan, 1983) και διατίθενται στο εµπόριο από την Invitrogen. ιαλύµατα: Θρεπτικός ζωµός SOC (1L): 20g τρυπτόνης 5g εκχυλίσµατος ζύµης 0,5g NaCl 0,19g KCl 0,95g MgCl 2
107 ΜΕΘΟΔΟΙ 107 3,6g γλυκόζης Έως 1L ddh 2 O Θρεπτικός ζωµός LB (1L): 10g τρυπτόνης 5g εκχυλίσµατος ζύµης 5g NaCl Έως 1L ddh 2 O Τα διαλύµατα αποστειρώνονται στους 121 C. Για την παρασκευή στερεών θρεπτικών υλικών SOC και LB προστίθεται 1,5% w/v άγαρ στα παραπάνω συστατικά. Πορεία: Τα κολοβακτηρίδια, τα οποία φυλάσσονται στους -80 C, αποψύχονται σε υγρό πάγο. Λαµβάνονται 50µL επιδεκτικών βακτηρίων και ακολουθούν πρόσθεση 10-50ng πλασµιδιακού DNA και ήπια ανάδευση. Το µείγµα επωάζεται για 30 λεπτά σε πάγο, βυθίζεται σε υδατόλουτρο θερµοκρασίας 42 C για 45 δευτερόλεπτα και επαναφέρεται για 2 λεπτά στον πάγο. Στη συνέχεια προστίθενται 450µL θρεπτικού υλικού SOC και τα βακτήρια επωάζονται για 1 ώρα στους 37 C µε έντονη ανάδευση. Τέλος, από το τελικό µείγµα, 50µL επιστρώνονται σε τρυβλίο µε LB-άγαρ παρουσία του αντιβιοτικού επιλογής Καλλιέργεια-πολλαπλασιασμός των μετασχηματισμένων βακτηρίων Το τρυβλίο επωάζεται 16 ώρες στους 37 C, ώστε να σχηµατιστούν αποικίες. Αποµονώνονται 1-2 αποικίες και εµβολιάζονται σε 5mL θρεπτικού ζωµού LB, παρουσία αντιβιοτικού επιλογής. Ακολουθεί επώαση για 8 ώρες στους 37 C µε έντονη ανάδευση. Στη συνέχεια, 1 ml από την προηγούµενη καλλιέργεια εµβολιάζεται σε 200 ml LB παρουσία αντιβιοτικού επιλογής και ακολουθεί ολονύκτια επώαση στους 37 C µε έντονη ανάδευση. Τα µετασχηµατισµένα βακτήρια συλλέγονται µε φυγοκέντρηση για 10 λεπτά σε g, 4 C.
108 108 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Απομόνωση πλασμιδίων με στήλες ιοντοανταλλακτικής ρητίνης Η αποµόνωση των ανασυνδυασµένων πλασµιδίων από την καλλιέργεια µετασχηµατισµένων βακτηρίων E.coli πραγµατοποιήθηκε µε εµπορικά διαθέσιµα αντιδραστήρια (NucleoBond Plasmid DNA Purification), σύµφωνα µε τις οδηγίες της κατασκευάστριας εταιρείας Macherey-Nagel. Αρχή Μεθόδου: Το ίζηµα των βακτηρίων λύεται σε διάλυµα NaOH/SDS (Birnboim & Doly, 1979), ώστε να επιτευχθεί αποδιάταξη των πρωτεϊνών και του χρωµατοσωµικού και πλασµιδιακού DNA. Με την προσθήκη RΝάσης στο διάλυµα, αποδοµείται το RNA. Ακολουθεί προσθήκη οξικού καλίου, το οποίο κατακρηµνίζει το SDS και µαζί µε αυτό, τις πρωτεΐνες και το χρωµατοσωµικό DNA, ενώ το πλασµίδιο παραµένει στο διάλυµα. Στη συνέχεια, το διάλυµα τοποθετείται σε στήλη µε ρητίνη ανταλλαγής ιόντων υπό όξινες συνθήκες, οπότε o αρνητικά φορτισµένος φωσφορικός σκελετός του πλασµιδίου προσδένεται στη θετικά φορτισµένη ρητίνη. Η πρόσθεση διαλύµατος µε ελαφρώς αλκαλικό ph προκαλεί την αποδέσµευση του πλασµιδιακού DNA από τη ρητίνη και την έκλουσή του στο διάλυµα. Η προσθήκη ισοπροπανόλης προκαλεί καθίζηση του πλασµιδίου, το οποίο λαµβάνεται ως ίζηµα µετά από φυγοκέντρηση. Η ισοπροπανόλη αποµακρύνεται µε πλύση του ιζήµατος µε διάλυµα 70% v/v αιθανόλης. Τέλος, το πλασµιδιακό DNA επαναδιαλύεται, ελεύθερο προσµίξεων, σε ddh 2 O ή σε διάλυµα TE (10mM Tris HCl, 1mM EDTA) Έλεγχος προϊόντων καθαρισμού πλασμιδίων Ο ποιοτικός και ποσοτικός έλεγχος των ανασυνδυασµένων πλασµιδίων πραγµατοποιήθηκε µε πέψη τους µε περιοριστικά ένζυµα που αναγνωρίζουν αλληλουχίες παρούσες στα συγκεκριµένα πλασµίδια. Η ηλεκτροφόρηση των προϊόντων της πέψης έγινε σε πήκτωµα αγαρόζης 1% w/v και ελέγχθηκε ο αριθµός και το µέγεθος των DNA θραυσµάτων Πλασμίδια Τα ανασυνδυασµένα πλασµίδια που χρησιµοποιήθηκαν στην παρούσα εργασία φαίνονται στον πίνακα που ακολουθεί (Πίνακας 2).
109 ΜΕΘΟΔΟΙ 109 Πίνακας 2: Πλασµίδια που χρησιµοποιήθηκαν στην παρούσα µελέτη
110 110 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Διαμόλυνση ευκαρυωτικών κυττάρων Γενικές αρχές διαμόλυνσης ευκαρυωτικών κυττάρων Η δυνατότητα εισαγωγής και ενσωµάτωσης ανασυνδυασµένου πλασµιδιακού DNA στο γονιδίωµα των ευκαρυωτικών κυττάρων έχει αποδειχθεί µία ιδιαίτερα σηµαντικής αξίας µέθοδος, καθώς επιτρέπει τη µελέτη της λειτουργίας και της ρύθµισης της έκφρασης των γονιδίων. Η έκφραση του πλασµιδιακού DNA που ενσωµατώνεται στα κύτταρα µπορεί υπό κατάλληλες προϋποθέσεις να είναι µόνιµη ή παροδική. Στις πειραµατικές συνθήκες της παρούσας εργασίας η έκφραση των πλασµιδιακών DNA είναι παροδική. Τα κύτταρα εκφράζουν το DNA που ενσωµατώνουν για 12 έως 72 ώρες από τη στιγµή που διαµολύνονται. Για την επιτυχή εισαγωγή πλασµιδιακού DNA σε κύτταρα θηλαστικών ή φυτών έχουν χρησιµοποιηθεί πολλές τεχνικές, όπως αυτή που χρησιµοποιεί διάλυµα χλωριούχου ασβεστίου, διάλυµα δεξτράνης, η ηλεκτροδιάτρηση και τα λιποσώµατα. Ανεξαρτήτως τεχνικής, η ποιότητα των κυττάρων και του πλασµιδιακού DNA είναι ουσιαστικής σηµασίας για την επιτυχή διαµόλυνση. Τα κύτταρα που πρόκειται να χρησιµοποιηθούν για τα πειράµατα διαµόλυνσης πρέπει να είναι σε λογαριθµική φάση ανάπτυξης, γιατί µόνο τότε ενσωµατώνουν το DNA µε µεγαλύτερη αποτελεσµατικότητα. Το πλασµιδιακό DNA που πρόκειται να χρησιµοποιηθεί πρέπει να είναι ελεύθερο πρωτεϊνών, RNA ή άλλων χηµικών ουσιών. DNA κατακρηµνισµένο µε αιθανόλη πρέπει να ανασυσταθεί σε στείρο διάλυµα ΤΕ ή ddh 2 O σε συγκέντρωση 0,2-1mg/mL. Ένδειξη καθαρότητας του DNA αποτελεί ο λόγος της οπτικής του απορρόφησης στα 260nm προς την απορρόφηση στα 280nm. Τιµές του λόγου µεταξύ 1,7 και 1,9 δηλώνουν ελεύθερο προσµίξεων DNA Διαμόλυνση ευκαρυωτικών κυττάρων με κατιονικά λιποσώματα (Lipofection) Αρχή µεθόδου: Η διαµόλυνση ευκαρυωτικών κυττάρων µε λιποσώµατα περιγράφηκε το 1987 από τους Felgner και συνεργάτες (Felgner et al., 1987). Συνθετικά λιπίδια, µε θετικά φορτισµένη υδρόφιλη κεφαλή, σχηµατίζουν µικκύλια (λιποσώµατα) σε υδατικό διάλυµα. Ο αρνητικά φορτισµένος φωσφορικός σκελετός των νουκλεϊνικών οξέων ενώνεται µε το θετικά φορτισµένο λιπόσωµα, οδηγώντας στο σχηµατισµό συµπλέγµατος. Το νουκλεϊνικό οξύ περιέχεται στο εσωτερικό του συµπλέγµατος και περιβάλλεται από
111 ΜΕΘΟΔΟΙ 111 διπλοστοιβάδα λιπιδίων. Το θετικό φορτίο του συµπλέγµατος διευκολύνει την αλληλεπίδραση µε την αρνητικά φορτισµένη κυτταροπλασµατική µεµβράνη. Το σύµπλεγµα εισέρχεται στο εσωτερικό του κυττάρου µε ενδοκυττάρωση. Εφόσον το νουκλεϊνικό οξύ διαφύγει από το ενδόσωµα, διαχέεται µέσω του κυτταροπλάσµατος στον πυρήνα, όπου και εκφράζεται. Εάν δε διαφύγει, το ενδόσωµα ωριµάζει προς λυσόσωµα και το νουκλεϊνικό οξύ αποδοµείται (Εικόνα 9). Εικόνα 9: Μέθοδος διαµόλυνσης ευκαρυωτικών κυττάρων µε λιποσώµατα Η διαµόλυνση µε λιποσώµατα συνδυάζει υψηλή αποτελεσµατικότητα, αναπαραγωγιµότητα και χαµηλή τοξικότητα. Οι τεχνικές διαµόλυνσης µε δεξτράνη, µε χλωριούχο ασβέστιο και µε ηλεκτροδιάτρηση, παρουσιάζουν συχνά προβλήµατα στους συγκεκριµένους τοµείς. Για τις ανάγκες των πειραµάτων χρησιµοποιήθηκε το κατιονικό λιπόσωµα Lipofectamine 2000 της εταιρείας Invitrogen. Πορεία: Κύτταρα HEK 293 ( /0,5mL) τοποθετούνται σε καλλιεργητική πλάκα 24 φρεατίων και αφήνονται να προσκολληθούν. Σε φιαλίδιο µε 50µL θρεπτικού υλικού Opti-MEM προστίθενται τα ανασυνδυασµένα πλασµίδια, ενώ σε ξεχωριστό φιαλίδιο µε ίδια ποσότητα θρεπτικού υλικού αραιώνεται το λιπόσωµα. Ακολουθεί επώαση 5 λεπτών και ανάµειξη των περιεχοµένων των δύο φιαλιδίων. Μετά από περαιτέρω επώαση 25 λεπτών, ώστε να σχηµατιστούν τα συµπλέγµατα, το µείγµα προστίθεται στα κύτταρα. Μετά πάροδο 4 ωρών, το θρεπτικό υλικό απορρίπτεται και αντικαθίσταται από νέο θρεπτικό υλικό. Ύστερα από 16 ώρες πραγµατοποιείται η διέγερση των κυττάρων.
112 112 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Έλεγχος ενσωμάτωσης πλασμιδίων Ο έλεγχος ενσωµάτωσης των πλασµιδίων στα κύτταρα που διαµολύνθηκαν έγινε µε ανοσοφθορισµό. Συγκεκριµένα, τα κύτταρα συνδιαµολύνθηκαν µε το πλασµίδιο pegfp-c1, το οποίο εκφράζει το γονίδιο της GFPmut1, µίας πρωτεΐνης µε ικανότητα εκποµπής φθορισµού στο µήκος κύµατος του πράσινου φωτός. Τα κύτταρα που έχουν ενσωµατώσει επιτυχώς το συγκεκριµένο πλασµίδιο αναφοράς και έχουν εκφράσει την πρωτεΐνη, διακρίνονται ως πράσινα σε µικροσκόπιο φθορισµού. Κύτταρα τα οποία εκφράζουν το pegfp-c1 θεωρείται ότι έχουν ενσωµατώσει και εκφράσει εξίσου επιτυχώς και το υπό µελέτη πλασµίδιο Έλεγχος δραστικότητας μεταγραφικών παραγόντων : Μέθοδος λουσιφεράσης Αρχή µεθόδου: Τα πειραµατικά πλασµίδια pap1-luc, pcre-luc και pnfκb-luc εκφράζουν το γονίδιο της λουσιφεράσης του είδους Photinus pyralis (Firefly Luciferase), υπό τον έλεγχο συνθετικού υποκινητή µε θέσεις δέσµευσης του οµώνυµου µεταγραφικού παράγοντα. Συνεπώς, κύτταρα διαµολυσµένα µε τα παραπάνω πλασµίδια µπορούν να πρωτεϊνοσυνθέσουν ποσότητες του ενζύµου λουσιφεράση, ανάλογες του βαθµού ενεργοποίησης των αντιστοίχων µεταγραφικών παραγόντων. Η προσθήκη περίσσειας ενζυµικού υποστρώµατος επιτρέπει την ποσοτικοποίηση του ενζύµου και κατ επέκταση, της δραστικότητας του υπό µελέτη µεταγραφικού παράγοντα. Το πλασµίδιο prl-tk, εκφράζει το γονίδιο της λουσιφεράσης του είδους Renilla reniformis (Renilla Luciferase), υπό τον έλεγχο του υποκινητή της θυµιδινικής κινάσης του HSV. Το συγκεκριµένο πλασµίδιο διαµολύνεται συγχρόνως µε το πειραµατικό και χρησιµοποιείται ως µάρτυρας της µεθόδου. Οι δύο λουσιφεράσες καταλύουν διαφορετικά υποστρώµατα, επιτρέποντας το διαχωρισµό της βιοφωταύγειας που προκύπτει από τις δύο διαφορετικές ενζυµικές αντιδράσεις. Η µέτρηση της ενζυµικής ενεργότητας έγινε µε αντιδραστήρια διαθέσιµα στο εµπόριο (Dual-Luciferase Reporter Assay System), σύµφωνα µε τις οδηγίες της κατασκευάστριας εταιρείας, Promega. Η εκποµπή φωτός µετρήθηκε µε συσκευή ανίχνευσης φωταύγειας (TD20/20) της εταιρείας Turner Designs. Το εύρος ανίχνευσης της λουσιφεράσης µε τη συγκεκριµένη µεθοδολογία είναι 10fg-10ng ενζύµου. Η µέθοδος µειονεκτεί στο γεγονός ότι η παραγωγή φωτός είναι παροδική και σχετικά γρήγορη (0,3-
113 ΜΕΘΟΔΟΙ 113 0,5 δευτερόλεπτα) και απαιτεί ταχύτητα στους πειραµατικούς χειρισµούς. H παρουσία ακετυλο-συνενζύµου Α βοηθάει την παρατεταµένη παραγωγή και εκποµπή φωτός. Στη µεθοδολογία της Promega εφαρµόζεται η µέθοδος µε το ακετυλο-συνένζυµο Α. Πορεία: Κύτταρα που έχουν διαµολυνθεί µε τα υπό µελέτη πλασµίδια λύονται σε διάλυµα παθητικής λύσης (Passive Lysis Buffer, PLB), ώστε να αποµονωθούν οι ενδοκυττάριες πρωτεΐνες. Η συγκέντρωση των πρωτεϊνών υπολογίζεται µε τη µέθοδο Bradford. Ποσότητα πρωτεΐνης 40µg, τοποθετείται σε ειδικό φιαλίδιο. Στη συνέχεια, προστίθενται 80µL υποστρώµατος της λουσιφεράσης Firefly και προσδιορίζεται η εκποµπή φωτός. Ακολουθεί η προσθήκη 80µL υποστρώµατος της λουσιφεράσης Renilla και νέα µέτρηση. Τέλος, υπολογίζεται ο λόγος της λουσιφεράσης Firefly προς αυτήν της Renilla και εκφράζεται σε µονάδες σχετικής παραγωγής φωτός (Relative Light Units, RLU).
114
115 ΑΠΟΤΕΛΕΣΜΑΤΑ ΑΠΟΤΕΛΕΣΜΑΤΑ 4.1 Κινητική της παραγωγής προφλεγμονωδών (TNF-α, IL- 1β, IL-6) και αντιφλεγμονωδών (IL-10) κυτταροκινών σε υπερκείμενα καλλιεργειών ανθρωπίνων μονοκυττάρων μετά από μόλυνση με ζωντανά βακτήρια B. melitensis Στα πλαίσια της µελέτης της λοιµώξεως από βρουκέλλα αρχικά εξετάσθηκε η παραγωγή προφλεγµονωδών και αντιφλεγµονωδών κυτταροκινών από ανθρώπινα µονοκύτταρα σε καθορισµένα χρονικά διαστήµατα. Ο έλεγχος κρίθηκε απαραίτητος λόγω του κεντρικού ρόλου που παίζουν τα µονοκύτταρα, µε τις κυτταροκίνες που παράγουν, στην εξέλιξη της λοιµώξεως. Γι αυτόν τον λόγο ανθρώπινα µονοκύτταρα (10 6 /ml) από φυσιολογικούς δότες µολύνθηκαν µε ζωντανά βακτήρια B. melitensis σε αναλογία 20 βακτηρίων ανά µονοκύτταρο (MOI 20:1), ενώ ως µάρτυρας χρησιµοποιήθηκαν µονοκύτταρα στα οποία είχε προστεθεί LPS E. coli σε συγκέντρωση 0,5µg/mL. Τα κύτταρα επωάσθηκαν σε συνθήκες 37 C, 5% CO 2 για διαφορετικά χρονικά διαστήµατα (2, 4, 6, 8, 16, 24, 48 και 72 ώρες). Εν συνεχεία, έγινε συλλογή των υπερκειµένων για τον ποσοτικό προσδιορισµό των προφλεγµονωδών (TNF-α, IL-1β, IL- 6) ή αντιφλεγµονωδών (IL-10) κυτταροκινών µε τη µέθοδο της ELISA. Σχήµα 1: Κινητική της παραγωγής του TNF-α από ανθρώπινα µονοκύτταρα µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis
116 116 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Στο Σχήµα 1 απεικονίζεται η παραγωγή TNF-α µετά από στατιστική επεξεργασία τριών ανεξαρτήτων πειραµάτων. Όπως φαίνεται από το σχήµα, τα ζωντανά βακτήρια B. melitensis, καθώς και ο LPS E. coli, είναι εξίσου σηµαντικοί διεγέρτες της παραγωγής TNF-α από ανθρώπινα µονοκύτταρα. Παρατηρείται, ότι η µέγιστη παραγωγή TNF-α από µονοκύτταρα που µολύνθηκαν µε βρουκέλλα επιτυγχάνεται στις 16 ώρες, ενώ στα µονοκύτταρα στα οποία προστέθηκε LPS E. coli, η κορύφωση της παραγωγής TNF-α σηµειώνεται στις 8 ώρες. Όµως, σε αντίθεση µε την καθυστέρηση στη διέγερση της παραγωγής TNF-α, η διέγερση από ζωντανά βακτήρια B. melitensis παραµένει σηµαντική και µετά την πάροδο 48 ή 72 ωρών, όταν η παραγωγή TNF-α από LPS E. coli τείνει να επανέλθει στα επίπεδα ηρεµίας των µονοκυττάρων. Σχήµα 2: Κινητική της παραγωγής της IL-1β από ανθρώπινα µονοκύτταρα µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis Όπως παρουσιάζεται στο Σχήµα 2, τα ζωντανά βακτήρια B. melitensis, καθώς και ο LPS E. coli, αποτελούν ισχυρούς και άµεσους διεγέρτες της παραγωγής IL-1β από τα ανθρώπινα µονοκύτταρα, ήδη από τις πρώτες 2 ώρες µετά την προσθήκη τους στις κυτταροκαλλιέργειες. Η παραγωγή της IL-1β µετά τη διέγερση µε LPS E. coli παραµένει στα ίδια επίπεδα µέχρι και τις 72 ώρες εξελίξεως του πειράµατος. Αντίθετα, η παραγωγή της IL-1β µετά από διέγερση µε ζωντανά βακτήρια B. melitensis συνεχίζει να αυξάνεται µέχρι και τις 48 ώρες, όπου η τιµή της είναι περίπου διπλάσια από εκείνη των κυττάρων που διεγέρθηκαν µε LPS E. coli και παραµένει σταθερή µέχρι τις 72 ώρες.
117 ΑΠΟΤΕΛΕΣΜΑΤΑ 117 Σχήµα 3: Κινητική της παραγωγής της IL-6 από ανθρώπινα µονοκύτταρα µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis Όσον αφορά στην IL-6 (Σχήµα 3), τα ζωντανά βακτήρια B. melitensis και ο LPS E. coli αποτελούν εξίσου ισχυρούς διεγέρτες της παραγωγής της από ανθρώπινα µονοκύτταρα. Η µέγιστη συγκέντρωση IL-6 παρατηρείται στις 24 ώρες και υψηλές συγκεντρώσεις διατηρούνται στα υπερκείµενα των κυτταροκαλλιεργειών µέχρι και τις 72 ώρες. Από τα ανωτέρω προκύπτει ότι η κινητική της παραγωγής της IL-6 από µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis είναι όµοια µε εκείνη µετά την προσθήκη LPS E. coli.
118 118 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σχήµα 4: Κινητική της παραγωγής της IL-10 από ανθρώπινα µονοκύτταρα µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis Η παραγωγή της IL-10 (Σχήµα 4) από ανθρώπινα µονοκύτταρα αυξάνει ταυτόχρονα και µεγιστοποιείται στις 16 ώρες, είτε αυτά µολύνθηκαν µε ζωντανά βακτήρια B. melitensis ή διεγέρθηκαν µε LPS E. coli. Αξίζει να σηµειωθεί ότι η µέγιστη συγκέντρωση IL-10 στην περίπτωση του LPS E. coli είναι σχεδόν διπλάσια εκείνης της βρουκέλλας. Επίσης, η συγκέντρωση της IL-10 ως απάντηση στον LPS E. coli παραµένει σε υψηλά επίπεδα µέχρι και τις 72 ώρες, ενώ όσον αφορά στην B. melitensis η συγκέντρωσή της µειώνεται σταδιακά κατά το αντίστοιχο χρονικό διάστηµα. Συµπερασµατικά, η B. melitensis διεγείρει τα ανθρώπινα µονοκύτταρα προς έντονη παραγωγή προφλεγµονωδών κυτταροκινών κατά τη µόλυνσή τους.
119 ΑΠΟΤΕΛΕΣΜΑΤΑ Κινητική της φωσφορυλίωσης των MAP κινασών σε ολικά πρωτεϊνικά εκχυλίσματα ανθρωπίνων μονοκυττάρων μετά από μόλυνση με ζωντανά βακτήρια B. melitensis Η οικογένεια των MAP κινασών έχει αποδειχθεί ότι εµπλέκεται στην ανοσολογική απάντηση έναντι λοιµώξεων από µεγάλο αριθµό βακτηρίων. Στην παρούσα µελέτη λοιµώξεως ανθρωπίνων µονοκυττάρων από βρουκέλλα διερευνήθηκε η φωσφορυλίωση των MAP κινασών p38 και ERK ½. Γι αυτόν το λόγο ανθρώπινα µονοκύτταρα (10 6 /ml) από φυσιολογικούς δότες µολύνθηκαν µε ζωντανά βακτήρια B. melitensis σε αναλογία 20 βακτηρίων ανά µονοκύτταρο (MOI 20:1), ενώ ως µάρτυρας χρησιµοποιήθηκαν µονοκύτταρα στα οποία είχε προστεθεί LPS E. coli σε συγκέντρωση 0,5µg/mL. Τα κύτταρα επωάσθηκαν σε συνθήκες 37 C, 5% CO 2 για διαφορετικά χρονικά διαστήµατα (2, 4, 6 και 8 ώρες). Εν συνεχεία, έγινε λύση των κυττάρων µε διάλυµα RIPA, ώστε να παραληφθούν ολικές πρωτεΐνες στα εκχυλίσµατα, στις οποίες ανιχνεύθηκαν οι εν λόγω κινάσες σε κατάσταση φωσφορυλίωσης µε τη µεθοδολογία αποτύπωσης κατά Western. Σχήµα 5: Ενεργοποίηση των MAP κινασών σε ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis, µετά την πάροδο 30 λεπτών Όπως αναδεικνύεται στο Σχήµα 5, τόσο η p38 όσο και η ERK ½ δε φωσφορυλιώνονται, ενώ ο LPS E. coli που αποτελεί το θετικό µάρτυρα προκαλεί την έντονη φωσφορυλίωσή τους στο ίδιο χρονικό σηµείο των 30 λεπτών.
120 120 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σχήµα 6: Κινητική της φωσφορυλίωσης των MAP κινασών σε ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis Το αποτέλεσµα αυτό οδήγησε στον έλεγχο της φωσφορυλίωσης των κινασών σε µεταγενέστερα χρονικά σηµεία (Σχήµα 6). Από τον έλεγχο διαπιστώθηκε ότι η έναρξη της φωσφορυλίωσης της ERK ½ σηµειώνεται στις 2 ώρες, αυξάνεται έως τις 4 ώρες και παραµένει υψηλή έως και τις 8 ώρες. Παράλληλα, διαπιστώθηκε ότι η έναρξη της φωσφορυλίωσης της p38 παρατηρείται στις 2 ώρες, αυξάνεται έως τις 4 ώρες και βαθµιαία ελαττώνεται µέχρι τις 8 ώρες. Η β-ακτίνη χρησιµοποιήθηκε ως µάρτυρας παρουσίας ίσης ποσότητας πρωτεΐνης µεταξύ των δειγµάτων.
121 ΑΠΟΤΕΛΕΣΜΑΤΑ Συμμετοχή των υποδοχέων φυσικής ανοσίας Toll Like (TLRs) στην παραγωγή προφλεγμονωδών (TNF-α, IL-1β, IL-6) και αντιφλεγμονωδών (IL-10) κυτταροκινών από φυσιολογικά ανθρώπινα μονοκύτταρα μετά από μόλυνση με ζωντανά παθογόνα βακτήρια B. melitensis Οι υποδοχείς φυσικής ανοσίας Toll Like (TLRs) αναγνωρίζουν µοριακές δοµές συστατικών των βακτηρίων και προάγουν την παραγωγή κυτταροκινών από τα κύτταρα του ανοσοποιητικού συστήµατος. Για τη µελέτη της συµµετοχής των TLRs στην παραγωγή των προφλεγµονωδών και αντιφλεγµονωδών κυτταροκινών από ανθρώπινα µονοκύτταρα σε in vivo λοίµωξη µε βρουκέλλα χρησιµοποιήθηκαν αντισώµατα που αναστέλλουν τη σηµατοδότηση µέσω των εν λόγω υποδοχέων. Τα µονοκύτταρα (10 6 /ml) επωάστηκαν αρχικά µε αντισώµατα (10µg/mL) που αναστέλλουν τη σηµατοδότηση διαµέσου του TLR2, διαµέσου του TLR4 ή µε ισοτυπικό αντίσωµα για 30 λεπτά σε συνθήκες 37 C, 5% CO 2. Ακολούθησε η µόλυνση των κυττάρων µε ζωντανά βακτήρια B. melitensis σε αναλογία 20 βακτηρίων ανά µονοκύτταρο (MOI 20:1). Ταυτόχρονα, ως µάρτυρας της σηµατοδότησης διαµέσου TLR4 χρησιµοποιήθηκε ο LPS E. coli (0,5µg/mL), ενώ ως µάρτυρας της σηµατοδότησης διαµέσου TLR2 χρησιµοποιήθηκε το λιποπεπτίδιο Pam3CSK4 (1µg/mL). Μετά πάροδο 16 ωρών έγινε συλλογή των υπερκειµένων των κυτταροκαλλιεργειών και προσδιορισµός των προφλεγµονωδών (TNF-α, IL-1β, IL-6) ή αντιφλεγµονωδών (IL-10) κυτταροκινών µε τη µέθοδο της ELISA.
122 122 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σχήµα 7: Παραγωγή TNF-α από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis παρουσία αντισωµάτων έναντι των TLR2 και TLR4 µετά από 16 ώρες επώασης Όπως φαίνεται στο Σχήµα 7, η µόλυνση των µονοκυττάρων µε βρουκέλλα προάγει την παραγωγή TNF-α. Η επώαση µε την παρουσία αντισώµατος που αναστέλλει τη σηµατοδότηση διαµέσου TLR4 δεν επηρεάζει την παραγωγή TNF-α. Αντίθετα, η παρουσία αντισώµατος έναντι του TLR2 προκαλεί τη µείωση της παραγωγής TNF-α από τα µονοκύτταρα κατά 90% περίπου. Το ισοτυπικό αντίσωµα δεν επέδρασε στην συγκέντρωση της κυτταροκίνης. Ο LPS E. coli προκάλεσε αύξηση της παραγωγής TNFα, η οποία ανεστάλη παρουσία αντισώµατος έναντι του TLR4, όπως αναµενόταν. Επίσης, το λιποπεπτίδιο Pam3CSK4 διήγειρε την παραγωγή TNF-α, ενώ η προηγηθείσα επώαση µε αντίσωµα έναντι του TLR2 ανέστειλε τη διέγερση.
123 ΑΠΟΤΕΛΕΣΜΑΤΑ 123 Σχήµα 8: Παραγωγή IL-1β από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis παρουσία αντισωµάτων έναντι των TLR2 και TLR4 µετά από 16 ώρες επώασης Στο Σχήµα 8 γίνεται εµφανές ότι η παραγωγή IL-1β από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε βρουκέλλα δεν επηρεάζεται από τα ανασταλτικά αντισώµατα έναντι των TLR2 και TLR4. Επίσης, η προσθήκη ανασταλτικών αντισωµάτων δεν είχε επίδραση στην παραγωγή IL-1β όταν η διέγερση των µονοκυττάρων έγινε µε LPS E. coli. Αντίθετα, το λιποπεπτίδιο Pam3CSK4 οδήγησε στην παραγωγή IL-1β από τα µονοκύτταρα, η οποία µειώθηκε παρουσία αντισώµατος έναντι του TLR2.
124 124 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σχήµα 9: Παραγωγή IL-6 από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis παρουσία αντισωµάτων έναντι των TLR2 και TLR4 µετά από 16 ώρες επώασης Στο Σχήµα 9 φαίνεται ότι η παραγωγή IL-6 από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε βρουκέλλα µειώθηκε κατά 80% όταν έγινε αναστολή του TLR2, ενώ δεν επηρεάστηκε από την αναστολή του TLR4. Ο LPS E. coli προκάλεσε τη διέγερση των µονοκυττάρων προς παραγωγή IL-6, η οποία ανεστάλη παρουσία αντισώµατος έναντι του TLR4. Αντίθετα, η διέγερση µε Pam3CSK4 ανεστάλη παρουσία αντισώµατος έναντι του TLR2.
125 ΑΠΟΤΕΛΕΣΜΑΤΑ 125 Σχήµα 10: Παραγωγή IL-10 από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis παρουσία αντισωµάτων έναντι των TLR2 και TLR4 µετά από 16 ώρες επώασης Όπως φαίνεται στο Σχήµα 10, η µόλυνση των µονοκυττάρων µε βρουκέλλα προάγει την παραγωγή IL-10. Η επώαση µε την παρουσία αντισώµατος που αναστέλλει τη σηµατοδότηση διαµέσου TLR4 δεν επηρεάζει την παραγωγή IL-10. Αντίθετα, η παρουσία αντισώµατος έναντι του TLR2 προκαλεί µείωση της παραγωγής IL-10 από τα µονοκύτταρα κατά 90% περίπου. Το ισοτυπικό αντίσωµα δεν επέδρασε στην συγκέντρωση της κυτταροκίνης. Ο LPS E. coli προκάλεσε αύξηση της παραγωγής IL-10, η οποία ανεστάλη παρουσία αντισώµατος έναντι του TLR4, όπως αναµενόταν. Επίσης, το λιποπεπτίδιο Pam3CSK4 διήγειρε την παραγωγή IL-10, ενώ η προηγηθείσα επώαση µε αντίσωµα έναντι του TLR2 ανέστειλε τη διέγερση.
126 126 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 4.4 Συμμετοχή των υποδοχέων φυσικής ανοσίας Toll Like (TLRs) στην φωσφορυλίωση των MAP κινασών σε φυσιολογικά ανθρώπινα μονοκύτταρα μετά από μόλυνση με ζωντανά παθογόνα βακτήρια B. melitensis Η ενεργοποίηση των MAP κινασών αποτελεί στάδιο της ενδοκυττάριας σηµατοδότησης διαµέσου των υποδοχέων TLRs. Όπως διαπιστώθηκε, η µόλυνση των µονοκυττάρων µε βρουκέλλα προκαλεί τη φωσφορυλίωση των MAP κινασών. Συνεπώς, το ερώτηµα που προκύπτει είναι η εξακρίβωση του υποδοχέα που ενέχεται στη φωσφορυλίωση. Για το σκοπό αυτό, µονοκύτταρα (10 6 /ml) επωάστηκαν αρχικά µε αντισώµατα (10µg/mL) που αναστέλλουν τη σηµατοδότηση διαµέσου του TLR2, διαµέσου του TLR4 ή µε ισοτυπικό αντίσωµα για 30 λεπτά σε συνθήκες 37 C, 5% CO 2. Ακολούθησε η µόλυνση των κυττάρων µε ζωντανά βακτήρια B. melitensis σε αναλογία 20 βακτηρίων ανά µονοκύτταρο (MOI 20:1). Μετά την πάροδο 4 ωρών, χρονικό σηµείο στο οποίο διαπιστώνεται η εντονότερη φωσφορυλίωση, έγινε λύση των κυττάρων µε διάλυµα RIPA, ώστε να παραληφθούν ολικές πρωτεΐνες στα εκχυλίσµατα, στις οποίες ανιχνεύθηκαν οι εν λόγω κινάσες σε κατάσταση φωσφορυλίωσης µε τη µεθοδολογία αποτύπωσης κατά Western.
127 ΑΠΟΤΕΛΕΣΜΑΤΑ 127 Σχήµα 11: Ενεργοποίηση των MAP κινασών σε ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis παρουσία αντισωµάτων έναντι των TLR2 και TLR4 µετά από 4 ώρες επώασης Στο Σχήµα 11 διαπιστώνεται ότι η βρουκέλλα επάγει τη φωσφορυλίωση της ERK ½ µετά από 4 ώρες διέγερσης. Η παρουσία αντισώµατος που αναστέλλει τη σηµατοδότηση διαµέσου TLR2 διατηρεί τη φωσφορυλίωση της ERK ½ σε επίπεδο ηρεµίας των µονοκυττάρων. Η παρουσία αντισώµατος έναντι του TLR4, όπως και η παρουσία ισοτυπικού αντισώµατος µάρτυρα, δεν αναστέλλουν τη φωσφορυλίωση. Οµοίως, στο ίδιο σχήµα παρατηρείται η επαγωγή της φωσφορυλίωσης της p38 από τη βρουκέλλα. Η προσθήκη αντισώµατος έναντι του TLR2 διατηρεί τη φωσφορυλίωση της p38 περίπου σε επίπεδο ηρεµίας των µονοκυττάρων. Η παρουσία αντισώµατος έναντι του TLR4, όπως και η παρουσία ισοτυπικού αντισώµατος µάρτυρα, δεν αναστέλλουν τη φωσφορυλίωση. Η β- ακτίνη χρησιµοποιήθηκε ως µάρτυρας παρουσίας ίσης ποσότητας πρωτεΐνης µεταξύ των δειγµάτων. Από τα παραπάνω προκύπτει ότι η παραγωγή TNF-α, IL-6 και IL-10, καθώς και η φωσφορυλίωση των MAP κινασών ERK ½ και p38, διαµεσολαβείται από τον TLR2 σε ανθρώπινα µονοκύτταρα που µολύνθηκαν από B. melitensis.
128 128 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 4.5 Συμμετοχή των υποδοχέων φυσικής ανοσίας Toll Like (TLRs) στην ενεργοποίηση του μεταγραφικού παράγοντα NFκB στην κυτταρική σειρά HEK 293 μετά από μόλυνση με ζωντανά παθογόνα βακτήρια B. melitensis Είναι γνωστό ότι ο µεταγραφικοί παράγοντες NFκB και AP-1 επάγουν την παραγωγή των προφλεγµονωδών κυτταροκινών TNF-α, IL-1β και IL-6 ως αποτέλεσµα της ενεργοποίησης των TLRs και ο µεταγραφικός παράγοντας CREB επάγει τη µεταγραφή της IL-10 στα µονοκύτταρα. Όπως διαπιστώθηκε, η βρουκέλλα προκαλεί την έκκριση TNF-α, IL-1β, IL-6 και IL-10 από τα ανθρώπινα µονοκύτταρα, η οποία στην περίπτωση των TNF-α, IL-6 και IL-10 εξαρτάται άµεσα από τη σηµατοδότηση διαµέσου του TLR2. Για να επιβεβαιωθεί η συµµετοχή του TLR2 στην ενεργοποίηση των NFκB, AP-1 και CREB από την B. melitensis εξετάστηκε η µεταγραφική δραστηριότητά τους στην κυτταρική σειρά HEK 293, στην οποία υπερεκφράστηκαν οι υποδοχείς TLR2 ή TLR4 µαζί µε τα συνδιεγερτικά τους µόρια. Συγκεκριµένα, κύτταρα HEK 293 TLR2/CD14 ή HEK 293 TLR4/MD2/CD14 ( /0,5mL) διαµολύνθηκαν µε τα πλασµίδια pnfκb-luc (50ng/0,5mL), pap1-luc (50ng/0,5mL), pcre-luc (50ng/0,5mL) και prl-tk (10ng/0,5mL), τα οποία εκφράζουν την πρωτεΐνη λουσιφεράση του είδους P. pyralis, υπό τον έλεγχο συνθετικού υποκινητή µε πέντε θέσεις δέσµευσης του µεταγραφικού παράγοντα NFκB, µε επτά θέσεις δέσµευσης του AP-1, µε τέσσερις θέσεις δέσµευσης του CREB και την πρωτεΐνη λουσιφεράση του είδους R. reniformis, υπό τον έλεγχο του υποκινητή της θυµιδινικής κινάσης του HSV, αντιστοίχως. Ακολούθησε η µόλυνση µε ζωντανά βακτήρια B. melitensis σε αναλογία 20 βακτηρίων ανά κύτταρο (MOI 20:1). Ως µάρτυρες χρησιµοποιήθηκαν ο LPS E. coli (0,5µg/mL), το λιποπεπτίδιο Pam3CSK4 (1µg/mL), ο φορβολικός εστέρας PMA (5ng/mL), ο οποίος ενεργοποιεί τους µεταγραφικούς παράγοντες NFκB και AP-1 και η προσταγλανδίνη PGE2, η οποία ενεργοποιεί τον µεταγραφικό παράγοντα CREB ανεξάρτητα από τους υποδοχείς επιφανείας TLRs. Μετά από 16 ώρες επώασης σε συνθήκες 37 C, 5% CO 2, τα κύτταρα λύθηκαν σε διάλυµα παθητικής λύσης (PLB) για τον προσδιορισµό της δραστικότητας των NFκB, AP-1 και CREB µε τη µέθοδο της λουσιφεράσης.
129 ΑΠΟΤΕΛΕΣΜΑΤΑ 129 Σχήµα 12: ραστικότητα του µεταγραφικού παράγοντα NFκB στην κυτταρική σειρά HEK 293 που υπερεκφράζει το σύµπλοκο υποδοχέα TLR2/CD14 µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis, µετά από 16 ώρες επώασης Στο Σχήµα 12 διακρίνεται ότι τα ζωντανά βακτήρια B. melitensis αυξάνουν τη δραστικότητα του µεταγραφικού παράγοντα NFκB στα κύτταρα HEK 293 που υπερεκφράζουν τον TLR2 κατά 8 φορές. Οι θετικοί µάρτυρες PMA και Pam3CSK4 αύξησαν τη δραστικότητα του NFκB κατά 16 φορές, ενώ ο αρνητικός µάρτυρας LPS E. coli δεν προκάλεσε στατιστικά σηµαντική µεταβολή της δραστικότητας. Σχήµα 13: ραστικότητα του µεταγραφικού παράγοντα NFκB στην κυτταρική σειρά HEK 293 που υπερεκφράζει το σύµπλοκο υποδοχέα TLR4/MD2/CD14 µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis, µετά από 16 ώρες επώασης
130 130 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Στο Σχήµα 13 φαίνεται ότι τα ζωντανά βακτήρια B. melitensis δεν προκαλούν ενεργοποίηση του NFκB στα κύτταρα HEK 293 στα οποία έχει υπερεκφραστεί το πλήρες σύµπλοκο TLR4/MD2/CD14. Οι θετικοί µάρτυρες PMA και LPS E. coli οδήγησαν σε αύξηση της δραστικότητας του NFκB κατά 10 και 24 φορές, αντιστοίχως. Ο αρνητικός µάρτυρας Pam3CSK4 δεν προκάλεσε µεταβολή στη δραστικότητα του NFκB. Σχήµα 14: ραστικότητα του µεταγραφικού παράγοντα AP-1 στις κυτταρικές σειρές HEK 293 που υπερεκφράζουν το σύµπλοκο υποδοχέα TLR2/CD14 ή TLR4/MD2/CD14 µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis, µετά από 16 ώρες επώασης Από το Σχήµα 14 γίνεται εµφανές ότι η διέγερση µε βρουκέλλα δεν αύξησε τη δραστικότητα του µεταγραφικού παράγοντα AP-1 σε κύτταρα HEK 293 που υπερεκφράζουν το σύµπλοκο TLR2/CD14 ή TLR4/MD2/CD14. Οι θετικοί µάρτυρες PMA, LPS E. coli και Pam3CSK4 αύξησαν τη δραστικότητα του AP-1 κατά 100, 30 και 16 φορές στα αντίστοιχα κύτταρα.
131 ΑΠΟΤΕΛΕΣΜΑΤΑ 131 Σχήµα 15: ραστικότητα του µεταγραφικού παράγοντα CREB στις κυτταρικές σειρές HEK 293 που υπερεκφράζουν το σύµπλοκο υποδοχέα TLR2/CD14 ή TLR4/MD2/CD14 µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis, µετά από 16 ώρες επώασης Στο παραπάνω σχήµα (Σχήµα 15) φαίνεται ότι η διέγερση µε βρουκέλλα κυττάρων HEK 293, τα οποία υπερεκφράζουν το σύµπλοκο TLR2/CD14 ή TLR4/MD2/CD14 δεν οδήγησε σε αύξηση της δραστικότητας του µεταγραφικού παράγοντα CREB, ενώ οι θετικοί µάρτυρες PGE2, LPS E. coli και Pam3CSK4 προκάλεσαν την αύξηση της δραστικότητας του µεταγραφικού παράγοντα στα αντίστοιχα κύτταρα κατά 16, 18 και 8 φορές. Συνολικά από τα παραπάνω αποτελέσµατα προκύπτει το συµπέρασµα ότι η B. melitensis προάγει την ενεργοποίηση του µεταγραφικού παράγοντα NFκB προς παραγωγή προφλεγµονωδών κυτταροκινών διαµέσου του TLR2, ενώ οι µεταγραφικοί παράγοντες AP-1 και CREB δεν ενεργοποιούνται από τους υποδοχείς TLR2 και TLR4.
132 132 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 4.6 Συμμετοχή των υποδοχέων φυσικής ανοσίας Toll Like (TLRs) στη φωσφορυλίωση των MAP κινασών στην κυτταρική σειρά HEK 293 μετά από μόλυνση με ζωντανά παθογόνα βακτήρια B. melitensis Όπως ήδη αποδείχθηκε, η µόλυνση ανθρωπίνων µονοκυττάρων µε ζωντανά βακτήρια B. melitensis προκαλεί τη φωσφορυλίωση των MAP κινασών διαµέσω του TLR2. Είναι γνωστό ότι στη διαδικασία της φαγοκυττάρωσης συµµετέχουν οι MAP κινάσες διαµέσου ποικίλων σηµατοδοτικών µηχανισµών, ανεξάρτητων από τους TLRs. Η κυτταρική σειρά HEK 293 είναι επιθηλιακά κύτταρα εµβρυικού νεφρικού ιστού ανθρώπου, τα οποία δεν επιτελούν τη λειτουργία της φαγοκυττάρωσης. Για τη διερεύνηση της σηµασίας των TLRs στη φωσφορυλίωση των κινασών, ανεξάρτητα από τη διαδικασία της φαγοκυττάρωσης, χρησιµοποιήθηκε η κυτταρική σειρά HEK 293, στην οποία υπερεκφράστηκαν οι υποδοχείς TLR2 ή TLR4 µαζί µε τα συνδιεγερτικά τους µόρια. Συγκεκριµένα, κύτταρα HEK 293 TLR2/CD14 ή HEK 293 TLR4/MD2/CD14 (10 6 /ml) µολύνθηκαν µε ζωντανά βακτήρια B. melitensis σε αναλογία 20 βακτηρίων ανά κύτταρο (MOI 20:1). Τα κύτταρα επωάσθηκαν σε συνθήκες 37 C, 5% CO 2 για διαφορετικά χρονικά διαστήµατα (4, 8, 16 και 24 ώρες). Εν συνεχεία, έγινε λύση των κυττάρων µε διάλυµα RIPA, ώστε να παραληφθούν ολικές πρωτεΐνες στα εκχυλίσµατα, στις οποίες ανιχνεύθηκαν οι εν λόγω κινάσες σε κατάσταση φωσφορυλίωσης µε τη µεθοδολογία αποτύπωσης κατά Western. Σχήµα 16: Κινητική της ενεργοποίησης των MAP κινασών στην κυτταρική σειρά HEK 293 που υπερεκφράζει το σύµπλοκο υποδοχέα TLR2/CD14 µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis
133 ΑΠΟΤΕΛΕΣΜΑΤΑ 133 Όπως φαίνεται στο Σχήµα 16, τα ζωντανά βακτήρια B. melitensis προκαλούν φωσφορυλίωση της ERK ½ σε κύτταρα HEK 293 που υπερεκφράζουν τον TLR2. Η φωσφορυλίωση είναι εντονότερη στις 16 ώρες και ελαττώνεται στο χρονικό σηµείο των 24 ωρών. Στα ίδια κύτταρα, η p38 βρίσκεται σε φωσφορυλιωµένη µορφή στο χρονικό σηµείο των 16 ωρών και παραµένει στην ίδια ένταση ως τις 24 ώρες. Η β-ακτίνη χρησιµοποιήθηκε ως µάρτυρας παρουσίας ίσης ποσότητας πρωτεΐνης µεταξύ των δειγµάτων. Σχήµα 17: Κινητική της ενεργοποίησης των MAP κινασών στην κυτταρική σειρά HEK 293 που υπερεκφράζει το σύµπλοκο υποδοχέα TLR4/MD2/CD14 µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis Στο Σχήµα 17 παρουσιάζεται η φωσφορυλίωση των MAP κινασών σε κύτταρα HEK 293 που υπερεκφράζουν το πλήρες σύµπλοκο TLR4/MD2/CD14, µετά από µόλυνση µε ζωντανά βακτήρια B. melitensis. Στα συγκεκριµένα κύτταρα, τόσο η ERK ½ όσο και η p38, σε ουδένα χρονικό σηµείο εµφανίζουν φωσφορυλίωση. Η β-ακτίνη χρησιµοποιήθηκε ως µάρτυρας παρουσίας ίσης ποσότητας πρωτεΐνης µεταξύ των δειγµάτων. Τα αποτελέσµατα από την κυτταρική σειρά HEK 293 ενισχύουν τη σηµασία του ρόλου του TLR2 στη λοίµωξη από βρουκέλλα, όπως διαπιστώθηκε και στα πειράµατα µε ανθρώπινα µονοκύτταρα.
134 134 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ 4.7 Συμμετοχή των μελών της οικογένειας των MAP κινασών στην παραγωγή προφλεγμονωδών (TNF-α, IL- 1β, IL-6) και αντιφλεγμονωδών (IL-10) κυτταροκινών από φυσιολογικά ανθρώπινα μονοκύτταρα μετά από μόλυνση με ζωντανά παθογόνα βακτήρια B. melitensis Είναι γνωστό ότι η οικογένεια των MAP κινασών εµπλέκεται στην παραγωγή προφλεγµονωδών και αντιφλεγµονωδών κυτταροκινών από κύτταρα του ανοσοποιητικού συστήµατος. Στα µονοκύτταρα οι MAP κινάσες αποτελούν στάδιο της ενδοκυττάριας σηµατοδότησης διαµέσου των TLRs. Έχει ήδη καταδειχθεί από τα προηγούµενα αποτελέσµατα ότι η βρουκέλλα, αφενός µεν διεγείρει την παραγωγή κυτταροκινών από τα µονοκύτταρα διαµέσου TLR2, αφετέρου δε οδηγεί στη φωσφορυλίωση των MAP κινασών ERK ½ και p38. Το επόµενο ερώτηµα που προέκυψε ήταν ποιό µέλος της οικογένειας των MAP κινασών πρωταγωνιστεί στη ρύθµιση της παραγωγής των συγκεκριµένων κυτταροκινών από µονοκύτταρα που µολύνονται µε B. melitensis. Για το σκοπό αυτό, σε ανθρώπινα µονοκύτταρα (10 6 /ml) προστέθηκαν οι ειδικοί φαρµακευτικοί αναστολείς των MAP κινασών PD98059, SB και SP και ακολούθησε επώαση των κυττάρων σε συνθήκες 37 C, 5% CO 2 για µία ώρα. Στη συνέχεια, τα µονοκύτταρα µολύνθηκαν µε ζωντανά βακτήρια B. melitensis σε αναλογία 20 βακτηρίων ανά µονοκύτταρο (MOI 20:1) ή µε τον LPS E. coli (0,5µg/mL) ως θετικό µάρτυρα και επωάστηκαν στις ίδιες συνθήκες για 16 ώρες. Ακολούθησε συλλογή των υπερκειµένων των κυτταροκαλλιεργειών για τη µέτρηση των κυτταροκινών µε τη µέθοδο ELISA.
135 ΑΠΟΤΕΛΕΣΜΑΤΑ 135 Σχήµα 18: Παραγωγή TNF-α από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών, µετά από 16 ώρες επώασης Στο Σχήµα 18 φαίνεται ότι ο αναστολέας της ERK ½ PD98059 προκαλεί µείωση της παραγωγής TNF-α από τα µονοκύτταρα που µολύνθηκαν µε βρουκέλλα κατά 60% περίπου. Ο αναστολέας της p38 SB ελαττώνει την παραγωγή TNF-α κατά 90% περίπου, ενώ ο αναστολέας της JNK SP δεν προκαλεί στατιστικά σηµαντική µείωση του TNF-α. Ο οργανικός διαλύτης DMSO, στον οποίο έχουν αναδιαλυθεί οι αναστολείς, δεν επηρεάζει την παραγωγή TNF-α. Και οι τρείς αναστολείς των MAP κινασών προκάλεσαν τη µείωση της παραγωγής TNF-α από τα µονοκύτταρα που διεγέρθηκαν µε LPS E. coli.
136 136 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σχήµα 19: Παραγωγή IL-1β από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών, µετά από 16 ώρες επώασης Στο Σχήµα 19 διακρίνεται ότι µόνο ο αναστολέας της p38 προκαλεί στατιστικά σηµαντική µείωση της παραγωγής IL-1β από ανθρώπινα µονοκύτταρα που έχουν µολυνθεί µε ζωντανά βακτήρια B. melitensis. Ο οργανικός διαλύτης DMSO δεν επηρεάζει την παραγωγή IL-1β. Κατά τη διέγερση µε LPS E. coli, η παραγωγή IL-1β µειώθηκε κατά 65% και 80% παρουσία των αναστολέων της p38 και JNK, αντιστοίχως, ενώ ο αναστολέας της ERK ½ δεν την επηρέασε.
137 ΑΠΟΤΕΛΕΣΜΑΤΑ 137 Σχήµα 20: Παραγωγή IL-6 από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών, µετά από 16 ώρες επώασης Στο Σχήµα 20 είναι εµφανές ότι οι αναστολείς των ERK ½ και p38 οδηγούν σε µείωση της IL-6 που εκκρίνεται από µονοκύτταρα που µολύνθηκαν µε βρουκέλλα κατά 50% και 65% περίπου, αντιστοίχως. Αντιθέτως, ο αναστολέας της JNK δεν παρεµβαίνει στην παραγωγή της IL-6. Η DMSO δεν επηρέασε την παραγωγή IL-6, ενώ και οι τρείς αναστολείς µείωσαν την παραγωγή της όταν τα µονοκύτταρα επωάστηκαν µε LPS E. coli.
138 138 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σχήµα 21: Παραγωγή IL-10 από ανθρώπινα µονοκύτταρα που µολύνθηκαν µε ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών, µετά από 16 ώρες επώασης Τέλος, στο Σχήµα 21 παρατηρείται ότι οι αναστολείς των p38 και JNK MAP κινασών µειώνουν την παραγωγή IL-10 από µολυσµένα µε βρουκέλλα µονοκύτταρα κατά 80% και 65%, αντιστοίχως. Ο αναστολέας της ERK ½ δεν επηρεάζει την παραγωγή IL-10 από τα µονοκύτταρα. Ο διαλύτης DMSO δεν παρεµβαίνει στην παραγωγή IL-10. Όταν τα µονοκύτταρα διεγέρθηκαν µε LPS E. coli η παραγωγή IL-10 επηρεάστηκε κατά τον ίδιο τρόπο όπως και στην περίπτωση της µολύνσεως µε B. melitensis. Συµπερασµατικά, τα ανθρώπινα µονοκύτταρα που µολύνονται µε B. melitensis παράγουν προφλεγµονώδεις και αντιφλεγµονώδεις κυτταροκίνες µε τη συµµετοχή των MAP κινασών.
139 ΑΠΟΤΕΛΕΣΜΑΤΑ Η ενδοκυττάρια επιβίωση ζωντανών βακτηρίων B. melitensis σε ανθρώπινα μονοκύτταρα παρουσία αναστολέων των MAP κινασών Η φωσφορυλίωση των MAP κινασών ως απάντηση στην παρουσία ξένου παράγοντα έχει ως σκοπό την επαγωγή της µεταγραφής πρωτεϊνών που θα προστατεύσουν το κύτταρο. Η βρουκέλλα, όπως έχει αναφερθεί, προκαλεί επιβραδυνόµενη (µετά την πάροδο 4 ωρών) φωσφορυλίωση των MAP κινασών. Η συγκεκριµένη παρατήρηση οδήγησε στον έλεγχο της ενδοκυττάριας επιβίωσης των βακτηρίων B. melitensis σε ανθρώπινα µονοκύτταρα παρουσία αναστολέων των MAP κινασών. Για τις ανάγκες του πειράµατος, σε ανθρώπινα µονοκύτταρα (10 6 /ml) προστέθηκαν οι ειδικοί φαρµακευτικοί αναστολείς των MAP κινασών PD98059, SB και SP και ακολούθησε επώαση των κυττάρων σε συνθήκες 37 C, 5% CO 2 για 1 ώρα. Στη συνέχεια, τα µονοκύτταρα µολύνθηκαν µε ζωντανά βακτήρια B. melitensis σε αναλογία 20 βακτηρίων ανά µονοκύτταρο (MOI 20:1). Ακολουθεί η δοκιµασία προστασίας από τη γενταµικίνη, κατά τη διάρκεια της οποίας επαναπροστίθενται οι αναστολείς των MAP κινασών. Η γενταµικίνη φονεύει τα βακτήρια που δεν έχουν φαγοκυτταρωθεί, ενώ αφήνει ανέπαφα τα βακτήρια που βρίσκονται στο εσωτερικό των µονοκυττάρων, λόγω της αδυναµίας της να διαπεράσει την κυτταροπλασµατική µεµβράνη. Στη συνέχεια, τα µονοκύτταρα λύονται στις µηδέν, 24 και 48 ώρες σε διάλυµα 0,1% v/v Triton X-100. Το εκχύλισµα που περιέχει τα ενδοκυττάρια βακτήρια επιστρώνεται σε TSB θρεπτικό υλικό.
140 140 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σχήµα 22: Ενδοκυττάρια επιβίωση της B. melitensis σε ανθρώπινα µονοκύτταρα, παρουσία αναστολέων των MAP κινασών Όπως φαίνεται στο Σχήµα 22, τα ζωντανά βακτήρια B. melitensis φαγοκυτταρώνονται από τα µονοκύτταρα στο χρονικό σηµείο µηδέν, κατά το οποίο η προσθήκη αναστολέων των MAP κινασών δεν επηρεάζει τον αριθµό των βακτηρίων που φαγοκυτταρώθηκαν. Στις 24 ώρες ο αριθµός τους παραµένει σταθερός, ενώ στις 48 ώρες ο αριθµός τους πενταπλασιάζεται. Παρουσία των αναστολέων των MAP κινασών p38 και JNK, τα ζωντανά βακτήρια δεν πολλαπλασιάζονται περαιτέρω στο διάστηµα µεταξύ 24 και 48 ωρών. Η προσθήκη αναστολέα της ERK ½ στα µονοκύτταρα οδηγεί σε µη στατιστικά σηµαντική µείωση της επιβίωσης των ενδοκυτταρίων βακτηρίων κατά το διάστηµα του δευτέρου 24ώρου. Ο οργανικός διαλύτης DMSO δεν επηρεάζει την ενδοκυττάρια επιβίωση της B. melitensis στα ανθρώπινα µονοκύτταρα. Άρα, η επιβίωση της B. melitensis εντός του µονοκυττάρου ευνοείται από τα µέλη της οικογένειας των MAP κινασών p38 και JNK.
141 ΑΠΟΤΕΛΕΣΜΑΤΑ Έλεγχος της συμμετοχής της απόπτωσης ή του κυτταρικού θανάτου των μονοκυττάρων από τους χημικούς αναστολείς των MAP κινασών στην ενδοκυττάρια επιβίωση ζωντανών βακτηρίων B. melitensis Οι χηµικοί αναστολείς, σε µεγάλες συγκεντρώσεις, µπορούν να προκαλέσουν βλάβη των κυττάρων. Για την επιβεβαίωση της ακεραιότητας της λειτουργίας των µονοκυττάρων ελέγχθηκε το ποσοστό των αποπτωτικών ή των νεκρών κυττάρων. Σε ανθρώπινα µονοκύτταρα (10 6 /ml) προστέθηκαν οι ειδικοί φαρµακευτικοί αναστολείς των MAP κινασών PD98059, SB και SP και ακολούθησε επώαση των κυττάρων σε συνθήκες 37 C, 5% CO 2 για µία ώρα. Στη συνέχεια, τα µονοκύτταρα µολύνθηκαν µε ζωντανά βακτήρια B. melitensis σε αναλογία 20 βακτηρίων ανά µονοκύτταρο (MOI 20:1) για 48 ώρες. Ακολούθησε χρώση των µονοκυττάρων µε διάλυµα αννεξίνης και PI και ανάλυση µε κυτταροµετρία ροής. Σχήµα 23: Απόπτωση και νέκρωση των µονοκυττάρων µετά από 48 ώρες µόλυνσης µε ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών Όπως φαίνεται στο Σχήµα 23, τα υγιή µονοκύτταρα αντιπροσωπεύουν ποσοστό µεγαλύτερο του 75% περίπου, σ όλες τις συνθήκες. Τα αποπτωτικά κύτταρα αποτελούν το 6-8% περίπου, ενώ τα νεκρά το 10-15% περίπου επί του συνόλου των µονοκυττάρων.
142 142 ΑΝΟΣΙΑ ΣΤΗ ΒΡΟΥΚΕΛΛΩΣΗ Σχήµα 24: Κυτταροτοξικότητα των µονοκυττάρων µετά από 48 ώρες µόλυνσης µε ζωντανά βακτήρια B. melitensis παρουσία αναστολέων των MAP κινασών Οµοίως, στο Σχήµα 24 γίνεται εµφανές ότι η κυτταροτοξικότητα σε κύτταρα στα οποία προστέθηκαν φαρµακευτικοί αναστολείς των MAP κινασών αντιπροσωπεύει ποσοστό 10-14% και δε διαφέρει από αυτή των εν ηρεµία κυττάρων. Από τα παραπάνω προκύπτει το συµπέρασµα ότι οι φαρµακευτικοί αναστολείς δεν προκαλούν την απόπτωση ή τον κυτταρικό θάνατο των µονοκυττάρων στις συνθήκες που χρησιµοποιήθηκαν στην παρούσα εργασία.
ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ. Εργαστήριο Γενετικής, ΓΠΑ
 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ Στάδια μικροβιακής λοίμωξης δημιουργία αποικίας σε εξωτερική επιφάνεια διείσδυση στον οργανισμό τοπική μόλυνση συστηματική (γενικευμένη) μόλυνση H σημασία
ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ Στάδια μικροβιακής λοίμωξης δημιουργία αποικίας σε εξωτερική επιφάνεια διείσδυση στον οργανισμό τοπική μόλυνση συστηματική (γενικευμένη) μόλυνση H σημασία
Αυτοφαγία & Ανοσολογικό Σύστημα. Χαράλαμπος Μ. Μουτσόπουλος
 Αυτοφαγία & Ανοσολογικό Σύστημα Χαράλαμπος Μ. Μουτσόπουλος Απρίλιος 2018 Αυτοφαγία & Ανοσολογικό Σύστημα Ευκαρυωτικά κύτταρα: Δυο μηχανισμούς αποδόμησης και ανακύκλωσης κυτταροπλασματικών αποβλήτων Πρωτεάσες
Αυτοφαγία & Ανοσολογικό Σύστημα Χαράλαμπος Μ. Μουτσόπουλος Απρίλιος 2018 Αυτοφαγία & Ανοσολογικό Σύστημα Ευκαρυωτικά κύτταρα: Δυο μηχανισμούς αποδόμησης και ανακύκλωσης κυτταροπλασματικών αποβλήτων Πρωτεάσες
Μοριακή κυτταρική βιοχημεία Ανοσοποιητικό σύστημα
 Μοριακή κυτταρική βιοχημεία Ανοσοποιητικό σύστημα κωδικός μαθήματος: ETY-335 Χειμερινό εξάμηνο 2014 / 2015 Μαρία Χατζηνικολαΐδου mchatzin@materials.uoc.gr Έμφυτο και προσαρμοστικό ανοσοποιητικό σύστημα
Μοριακή κυτταρική βιοχημεία Ανοσοποιητικό σύστημα κωδικός μαθήματος: ETY-335 Χειμερινό εξάμηνο 2014 / 2015 Μαρία Χατζηνικολαΐδου mchatzin@materials.uoc.gr Έμφυτο και προσαρμοστικό ανοσοποιητικό σύστημα
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ Η πρώτη γραπτή αναφορά στο φαινόμενο της ανοσίας μπορεί να αναζητηθεί στον Θουκυδίδη, τον μεγάλο ιστορικό του Πελοποννησιακού Πολέμου Ανάπτυξη και επιβίωση o
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ Η πρώτη γραπτή αναφορά στο φαινόμενο της ανοσίας μπορεί να αναζητηθεί στον Θουκυδίδη, τον μεγάλο ιστορικό του Πελοποννησιακού Πολέμου Ανάπτυξη και επιβίωση o
Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα
 Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα φυσική ή μη ειδική ανοσία δεν απαιτεί προηγούμενη έκθεση στο παθογόνο και δεν διαθέτει μνήμη. σε επίκτητη ή ειδική ανοσία χυμική ανοσία με παραγωγή
Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα φυσική ή μη ειδική ανοσία δεν απαιτεί προηγούμενη έκθεση στο παθογόνο και δεν διαθέτει μνήμη. σε επίκτητη ή ειδική ανοσία χυμική ανοσία με παραγωγή
όλοι αναπνευστική οδός στομάχι στόμα
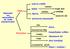 κεράτινη στιβάδα περιέχει σμήγμα λιπαρά οξέα Μηχανισμοί που παρεμποδίζουν την είσοδο Δέρμα περιέχει ιδρώτας φυσιολογική μικροχλωρίδα λυσοζύμη γαλακτικό οξύ μικροοργανισμών Βλεννογόνοι όλοι αναπνευστική
κεράτινη στιβάδα περιέχει σμήγμα λιπαρά οξέα Μηχανισμοί που παρεμποδίζουν την είσοδο Δέρμα περιέχει ιδρώτας φυσιολογική μικροχλωρίδα λυσοζύμη γαλακτικό οξύ μικροοργανισμών Βλεννογόνοι όλοι αναπνευστική
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς. Οι φάσεις των Τ κυτταρικών απαντήσεων
 ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
ΕΡΩΤΗΣΕΙΣ 1 ου ΚΕΦΑΛΑΙΟΥ
 ΕΡΩΤΗΣΕΙΣ 1 ου ΚΕΦΑΛΑΙΟΥ Επιλέξτε τη σωστή απάντηση: Το τρυπανόσωμα προκαλεί α. δυσεντερία β. ελονοσία γ. ασθένεια του ύπνου δ. χολέρα Τα ενδοσπόρια σχηματίζονται από β. φυτά γ. ιούς δ. πρωτόζωα Η σύφιλη
ΕΡΩΤΗΣΕΙΣ 1 ου ΚΕΦΑΛΑΙΟΥ Επιλέξτε τη σωστή απάντηση: Το τρυπανόσωμα προκαλεί α. δυσεντερία β. ελονοσία γ. ασθένεια του ύπνου δ. χολέρα Τα ενδοσπόρια σχηματίζονται από β. φυτά γ. ιούς δ. πρωτόζωα Η σύφιλη
ΦΡΟΝΤΙΣΤΗΡΙΑ ΠΡΟΟΠΤΙΚΗ
 Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
να ταράξουν την λειτουργία των ιστών και των οργάνων του; α. τη θέση τους στο ανθρώπινο σώμα β. την γενικευμένη ή εξειδικευμένη δράση
 Ερωτήσεις κατανόησης της θεωρίας του 1 ο κεφαλαίου (συνέχεια) 1. Από τι εξαρτάται η επιβίωση του ανθρώπου και ποιοι εξωτερικοί παράγοντες θα μπορούσαν να ταράξουν την λειτουργία των ιστών και των οργάνων
Ερωτήσεις κατανόησης της θεωρίας του 1 ο κεφαλαίου (συνέχεια) 1. Από τι εξαρτάται η επιβίωση του ανθρώπου και ποιοι εξωτερικοί παράγοντες θα μπορούσαν να ταράξουν την λειτουργία των ιστών και των οργάνων
ΣΤΗΛΗ Α Αντιβιοτικό Αντισώματα ιντερφερόνες Τ- Τ- (αντιγόνα) κυτταροτοξικά βοηθητικά Τοξίνες Vibrio cholera
 Α1. 1. β Βιολογία ΘΕΜΑ Α γενιικής παιιδείίας 2. γ 3. γ 4. γ 5. δ Α2. ΣΤΗΛΗ Α Αντιβιοτικό Αντισώματα ιντερφερόνες Τ- Τ- (αντιγόνα) κυτταροτοξικά βοηθητικά Τοξίνες Vibrio cholera Ηπατίτιδα C + Candida albicans
Α1. 1. β Βιολογία ΘΕΜΑ Α γενιικής παιιδείίας 2. γ 3. γ 4. γ 5. δ Α2. ΣΤΗΛΗ Α Αντιβιοτικό Αντισώματα ιντερφερόνες Τ- Τ- (αντιγόνα) κυτταροτοξικά βοηθητικά Τοξίνες Vibrio cholera Ηπατίτιδα C + Candida albicans
Βιολογία γενικής παιδείας τάξη Γ
 Βιολογία γενικής παιδείας τάξη Γ Παραδόσεις του μαθήματος Επιμέλεια: Γιάννης Αργύρης Βιολόγος M.Sc. Καθηγητής 3 ου Γεν. Λυκ. Ηλιούπολης Κεφάλαιο 1ο Άνθρωπος και υγεία 2. Μηχανισμοί Άμυνας του Ανθρώπινου
Βιολογία γενικής παιδείας τάξη Γ Παραδόσεις του μαθήματος Επιμέλεια: Γιάννης Αργύρης Βιολόγος M.Sc. Καθηγητής 3 ου Γεν. Λυκ. Ηλιούπολης Κεφάλαιο 1ο Άνθρωπος και υγεία 2. Μηχανισμοί Άμυνας του Ανθρώπινου
ΦΡΟΝΤΙΣΤΗΡΙΑ ΜΗΤΑΛΑΣ ΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ
 ΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΚΕΦΑΛΑΙΟ 1.3 : ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΑΝΟΣΙΑΣ ΘΕΜΑ 1 Χαρακτηρίστε τις προτάσεις ως σωστές ή λανθασµένες. 1. Οι βλεννογόνοι
ΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΚΕΦΑΛΑΙΟ 1.3 : ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΑΝΟΣΙΑΣ ΘΕΜΑ 1 Χαρακτηρίστε τις προτάσεις ως σωστές ή λανθασµένες. 1. Οι βλεννογόνοι
Εισαγωγή στην Ανοσολογία Επίκτητη Ανοσία I. Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ.
 Εισαγωγή στην Ανοσολογία Επίκτητη Ανοσία I Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 14/10/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Γενικά στοιχεία
Εισαγωγή στην Ανοσολογία Επίκτητη Ανοσία I Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 14/10/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Γενικά στοιχεία
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ. ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΕΡΩΤΗΣΕΙΣ ΣΩΣΤΟΥ - ΛΑΘΟΥΣ. ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ
 ΕΡΩΤΗΣΕΙΣ ΣΩΣΤΟΥ - ΛΑΘΟΥΣ. ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ 1. Η πήξη του αίματος συμβάλλει στην άμυνα του οργανισμού 2. Η φαγοκυττάρωση είναι αποτελεσματική μόνο έναντι των βακτηρίων 3. Οι ιντερφερόνες δρουν άμεσα
ΕΡΩΤΗΣΕΙΣ ΣΩΣΤΟΥ - ΛΑΘΟΥΣ. ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ 1. Η πήξη του αίματος συμβάλλει στην άμυνα του οργανισμού 2. Η φαγοκυττάρωση είναι αποτελεσματική μόνο έναντι των βακτηρίων 3. Οι ιντερφερόνες δρουν άμεσα
Θέµατα Πανελληνίων Βιολογίας Γ.Π Άµυνα - Ανοσία
 2012 Α2. Τα φαγοκύτταρα παράγονται α. στο νωτιαίο µυελό β. στο θύµο αδένα γ. στους λεµφαδένες δ. στον ερυθρό µυελό των οστών. Α3. Το συµπλήρωµα και η προπερδίνη συµβάλλουν στην καταπολέµηση α. των ιών
2012 Α2. Τα φαγοκύτταρα παράγονται α. στο νωτιαίο µυελό β. στο θύµο αδένα γ. στους λεµφαδένες δ. στον ερυθρό µυελό των οστών. Α3. Το συµπλήρωµα και η προπερδίνη συµβάλλουν στην καταπολέµηση α. των ιών
Μεταβολικές ανάγκες ανοσοκυττάρων
 Μεταβολικές ανάγκες ανοσοκυττάρων Στέργιος Κατσιουγιάννης PhD Μεταδιδακτορικός συνεργάτης Χαροκόπειο Πανεπιστήµιο Τµήµα Επιστήµης ιαιτολογίας και ιατροφής Μεταβολισµός και Ανοσολογία Ιστορικά το καλύτερο
Μεταβολικές ανάγκες ανοσοκυττάρων Στέργιος Κατσιουγιάννης PhD Μεταδιδακτορικός συνεργάτης Χαροκόπειο Πανεπιστήµιο Τµήµα Επιστήµης ιαιτολογίας και ιατροφής Μεταβολισµός και Ανοσολογία Ιστορικά το καλύτερο
 Μελέτη του ρόλου ανοσο-τροποποιητικής δράσεως της p38 µιτογονο-ενεργοποιηµένης κινάσης ( p38 MAPK ) Μαυρόπουλος Αθανάσιος, PhD ΕΙΣΑΓΩΓΗ-Ι H p38 MAPK ενεργοποιείται από τις ιντερλευκίνες IL-12 και IL-18
Μελέτη του ρόλου ανοσο-τροποποιητικής δράσεως της p38 µιτογονο-ενεργοποιηµένης κινάσης ( p38 MAPK ) Μαυρόπουλος Αθανάσιος, PhD ΕΙΣΑΓΩΓΗ-Ι H p38 MAPK ενεργοποιείται από τις ιντερλευκίνες IL-12 και IL-18
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΕΦΑΡΜΟΓΕΣ ΑΣΚΗΣΕΙΣ ΣΤΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΑΜΥΝΑΣ
 ΕΦΑΡΜΟΓΕΣ ΑΣΚΗΣΕΙΣ ΣΤΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΑΜΥΝΑΣ Ερωτήσεις πολλαπλής επιλογής: επιλέξτε το γράμμα που αντιστοιχεί στη σωστή συνέχεια της πρότασης. 1. Δυσμενές χημικό περιβάλλον στην επιδερμίδα προκαλείται από:
ΕΦΑΡΜΟΓΕΣ ΑΣΚΗΣΕΙΣ ΣΤΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΑΜΥΝΑΣ Ερωτήσεις πολλαπλής επιλογής: επιλέξτε το γράμμα που αντιστοιχεί στη σωστή συνέχεια της πρότασης. 1. Δυσμενές χημικό περιβάλλον στην επιδερμίδα προκαλείται από:
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ
 23-10-11 ΘΕΡΙΝΑ ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Όλα τα βακτήρια: Α. διαθέτουν κυτταρικό
23-10-11 ΘΕΡΙΝΑ ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Όλα τα βακτήρια: Α. διαθέτουν κυτταρικό
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΙ ΠΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΙ ΠΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ Αλληλεπιδράσεις πρωτεϊνών του ενδοσυμβιωτικού ιού του παρασιτοειδούς υμενόπτερου Cotesia congregata
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΙ ΠΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ Αλληλεπιδράσεις πρωτεϊνών του ενδοσυμβιωτικού ιού του παρασιτοειδούς υμενόπτερου Cotesia congregata
2. Τα πρωτόζωα α. δεν έχουν πυρήνα. β. είναι μονοκύτταροι ευκαρυωτικοί οργανισμοί. γ. είναι πολυκύτταρα παράσιτα. δ. είναι αυτότροφοι οργανισμοί.
 1 ΘΕΜΑΤΑ κεφ 1. Α. Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή στη φράση η οποία συμπληρώνει σωστά την ημιτελή πρόταση.
1 ΘΕΜΑΤΑ κεφ 1. Α. Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή στη φράση η οποία συμπληρώνει σωστά την ημιτελή πρόταση.
Ποιες είναι οι προϋποθέσεις που πρέπει να τηρούνται για την αποφυγή µετάδοσης ασθενειών που οφείλονται σε παθογόνους µικροοργανισµούς;
 ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Ποιες είναι οι προϋποθέσεις που πρέπει να τηρούνται για την αποφυγή µετάδοσης ασθενειών που οφείλονται σε παθογόνους µικροοργανισµούς; ΘΕΜΑ Β ίνεται το παρακάτω
ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Ποιες είναι οι προϋποθέσεις που πρέπει να τηρούνται για την αποφυγή µετάδοσης ασθενειών που οφείλονται σε παθογόνους µικροοργανισµούς; ΘΕΜΑ Β ίνεται το παρακάτω
ΑΝΟΣΟΛΟΓΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΡΑΣΗΣ ΕΜΒΟΛΙΩΝ. Μαρία Χατζηστυλιανού Σιδηροπούλου Ομότιμη Καθηγήτρια Παιδιατρικής Ανοσολογίας Τμήματος Ιατρικής, ΣΕΥ, ΑΠΘ
 ΑΝΟΣΟΛΟΓΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΡΑΣΗΣ ΕΜΒΟΛΙΩΝ. Μαρία Χατζηστυλιανού Σιδηροπούλου Ομότιμη Καθηγήτρια Παιδιατρικής Ανοσολογίας Τμήματος Ιατρικής, ΣΕΥ, ΑΠΘ ΑΝΟΣΟΠΟΙΗΣΗ ΕΝΕΡΓΗΤΙΚΗ ΠΑΘΗΤΙΚΗ ΦΥΣΙΚΗ (ΝΟΣΗΣΗ) ΤΕΧΝΗΤΗ
ΑΝΟΣΟΛΟΓΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΡΑΣΗΣ ΕΜΒΟΛΙΩΝ. Μαρία Χατζηστυλιανού Σιδηροπούλου Ομότιμη Καθηγήτρια Παιδιατρικής Ανοσολογίας Τμήματος Ιατρικής, ΣΕΥ, ΑΠΘ ΑΝΟΣΟΠΟΙΗΣΗ ΕΝΕΡΓΗΤΙΚΗ ΠΑΘΗΤΙΚΗ ΦΥΣΙΚΗ (ΝΟΣΗΣΗ) ΤΕΧΝΗΤΗ
Μικροοργανισμοί. Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς
 Μικροοργανισμοί Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς Παθογόνοι μικροοργανισμοί Παθογόνοι μικροοργανισμοί ονομάζονται οι μικροοργανισμοί που χρησιμοποιούν τον άνθρωπο ως ξενιστή
Μικροοργανισμοί Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς Παθογόνοι μικροοργανισμοί Παθογόνοι μικροοργανισμοί ονομάζονται οι μικροοργανισμοί που χρησιμοποιούν τον άνθρωπο ως ξενιστή
ΑΝΟΣΟΒΙΟΛΟΓΙΑ. Εξεταστική Ιανουαρίου 2010
 Εξεταστική Ιανουαρίου 2010 Ποιες είναι οι διαφορές μιας πρωτογενούς από μια δευτερογενή χυμική ανοσολογική απόκριση; Περιγράψετε τους μηχανισμούς ενεργοποίησης στις δυο περιπτώσεις. ΘΕΜΑ 2 (1 μονάδα) Περιγράψετε
Εξεταστική Ιανουαρίου 2010 Ποιες είναι οι διαφορές μιας πρωτογενούς από μια δευτερογενή χυμική ανοσολογική απόκριση; Περιγράψετε τους μηχανισμούς ενεργοποίησης στις δυο περιπτώσεις. ΘΕΜΑ 2 (1 μονάδα) Περιγράψετε
ΘΕΜΑ 1 Ο ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10/11/2013
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10/11/2013 ΘΕΜΑ 1 Ο Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Οι αποικοδομητές είναι:
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10/11/2013 ΘΕΜΑ 1 Ο Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Οι αποικοδομητές είναι:
Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος
 MOPIAKH BIOΛOΓIA ΦAPMAKEYTIKHΣ ΔIAΛEΞΕΙΣ 10-12 Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Δρ. Xρήστος Παναγιωτίδης, Tµήµα Φαρµακευτικής
MOPIAKH BIOΛOΓIA ΦAPMAKEYTIKHΣ ΔIAΛEΞΕΙΣ 10-12 Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Δρ. Xρήστος Παναγιωτίδης, Tµήµα Φαρµακευτικής
ΑΝΟΣΟΛΟΓΙΑ. 1. Εισαγωγή (κυρίως στην επίκτητη ανοσία) 2. Φυσική ανοσία ΕΠΙΚΤΗΤΗ ΑΝΟΣΙΑ
 ΑΝΟΣΟΛΟΓΙΑ 1. Εισαγωγή (κυρίως στην επίκτητη ανοσία) 2. Φυσική ανοσία ΕΠΙΚΤΗΤΗ ΑΝΟΣΙΑ ΑΝΤΙΓΟΝΟ 3. Η πρόσληψη του αντιγόνου και η παρουσίασή του στα λεμφοκύτταρα 4. Η αναγνώριση του αντιγόνου. Αντιγονικοί
ΑΝΟΣΟΛΟΓΙΑ 1. Εισαγωγή (κυρίως στην επίκτητη ανοσία) 2. Φυσική ανοσία ΕΠΙΚΤΗΤΗ ΑΝΟΣΙΑ ΑΝΤΙΓΟΝΟ 3. Η πρόσληψη του αντιγόνου και η παρουσίασή του στα λεμφοκύτταρα 4. Η αναγνώριση του αντιγόνου. Αντιγονικοί
οµή Ανοσιακού Συστήµατος Ελένη Φωτιάδου-Παππά Τµήµα Ανοσολογίας Γ.Ν. Νίκαιας-Πειραιά
 οµή Ανοσιακού Συστήµατος Ελένη Φωτιάδου-Παππά Τµήµα Ανοσολογίας Γ.Ν. Νίκαιας-Πειραιά Ανοσολογικό σύστηµα Βασικό σύστηµα του οργανισµού Λειτουργικές µονάδες του ανοσολογικού συστήµατος Οργανωµένος λεµφικός
οµή Ανοσιακού Συστήµατος Ελένη Φωτιάδου-Παππά Τµήµα Ανοσολογίας Γ.Ν. Νίκαιας-Πειραιά Ανοσολογικό σύστηµα Βασικό σύστηµα του οργανισµού Λειτουργικές µονάδες του ανοσολογικού συστήµατος Οργανωµένος λεµφικός
Ανοσιακή απάντηση (immune response)
 Ανοσιακή απάντηση (immune response) Το σύνολο των μηχανισμών που καθιστούν τον οργανισμό ικανό να αναγνωρίζει,να εξουδετερώνει και να απομακρύνει κάθε ξένη ουσία προς αυτόν χαρακτηρίζεται ως ανοσία. Αποτέλεσμα
Ανοσιακή απάντηση (immune response) Το σύνολο των μηχανισμών που καθιστούν τον οργανισμό ικανό να αναγνωρίζει,να εξουδετερώνει και να απομακρύνει κάθε ξένη ουσία προς αυτόν χαρακτηρίζεται ως ανοσία. Αποτέλεσμα
2 Ο ΜΑΘΗΜΑ ΣΥΣΤΗΜΑ ΣΥΜΠΛΗΡΩΜΑΤΟΣ ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 2 Ο ΜΑΘΗΜΑ ΣΥΣΤΗΜΑ ΣΥΜΠΛΗΡΩΜΑΤΟΣ ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις μεμβράνες 2. Φυσιολογικοί φραγμοί
2 Ο ΜΑΘΗΜΑ ΣΥΣΤΗΜΑ ΣΥΜΠΛΗΡΩΜΑΤΟΣ ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις μεμβράνες 2. Φυσιολογικοί φραγμοί
προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι.
 σύγχρονο Φάσµα & Group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. μαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 210 50 51 557 210 50 56 296 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 210 50 20 990 210 50 27 990 25ης Μαρτίου 74 ΠΕΤΡΟΥΠΟΛΗ
σύγχρονο Φάσµα & Group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. μαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 210 50 51 557 210 50 56 296 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 210 50 20 990 210 50 27 990 25ης Μαρτίου 74 ΠΕΤΡΟΥΠΟΛΗ
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ Με βάση τη θέση στο ανθρώπινο σώμα Με βάση την ιδιότητα για γενικευμένη ή εξειδικευμένη δράση Εξωτερικοί εσωτερικοί μη ειδικοί μηχανισμοί ειδικοί
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ Με βάση τη θέση στο ανθρώπινο σώμα Με βάση την ιδιότητα για γενικευμένη ή εξειδικευμένη δράση Εξωτερικοί εσωτερικοί μη ειδικοί μηχανισμοί ειδικοί
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΚΕΦΑΛΑΙΟ 15. Κυτταρική ρύθμιση. Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1
 ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ. Εξειδίκευση: προϊόντα (κύτταρα ή αντισώματα) ειδικά για το αντιγόνο. Μνήμη: κύτταρα
 ΕΙΔΙΚΗ ΑΜΥΝΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ Εξειδίκευση: προϊόντα (κύτταρα ή αντισώματα) ειδικά για το αντιγόνο Μνήμη: κύτταρα ΑΝΤΙΓΟΝΟ ΜΙΚΡΟΟΡΓΑΝΙΣΜΟΣ ΤΜΗΜΑ ΜΙΚΡΟΟΡΓΑΝΙΣΜΟΥ ΤΟΞΙΚΕΣ ΟΥΣΙΕΣ ΜΙΚΡΟΟΡΓΑΝΙΣΜΟΥ ΓΥΡΗ, ΦΑΡΜΑΚΕΥΤΙΚΕΣ
ΕΙΔΙΚΗ ΑΜΥΝΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ Εξειδίκευση: προϊόντα (κύτταρα ή αντισώματα) ειδικά για το αντιγόνο Μνήμη: κύτταρα ΑΝΤΙΓΟΝΟ ΜΙΚΡΟΟΡΓΑΝΙΣΜΟΣ ΤΜΗΜΑ ΜΙΚΡΟΟΡΓΑΝΙΣΜΟΥ ΤΟΞΙΚΕΣ ΟΥΣΙΕΣ ΜΙΚΡΟΟΡΓΑΝΙΣΜΟΥ ΓΥΡΗ, ΦΑΡΜΑΚΕΥΤΙΚΕΣ
Η πρωτογενής ανοσοβιολογική απόκριση ενεργοποιείται κατά την πρώτη επαφή του οργανισμού με ένα αντιγόνο. Περιλαμβάνει τα εξής στάδια:
 Εικόνα 1.24: α) Σύνδεση αντισώματος - αντιγόνου, β) συμπληρωματικότητα αντισώματος - αντιγόνου, γ) ένα αντίσωμα συνδέεται με περισσότερα από ένα αντιγόνα. Στάδια ανοσοβιολογικής απόκρισης Η αντίδραση του
Εικόνα 1.24: α) Σύνδεση αντισώματος - αντιγόνου, β) συμπληρωματικότητα αντισώματος - αντιγόνου, γ) ένα αντίσωμα συνδέεται με περισσότερα από ένα αντιγόνα. Στάδια ανοσοβιολογικής απόκρισης Η αντίδραση του
ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙAΣ Γ ΛΥΚΕΙΟΥ (Ιανουάριος 2014)
 ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙAΣ Γ ΛΥΚΕΙΟΥ (Ιανουάριος 2014) ΘΕΜΑ 1 ο Στις ερωτήσεις 1-5, να επιλέξετε το γράμμα που αντιστοιχεί στη σωστή απάντηση. 1. Το συμπλήρωμα και η προπερδίνη είναι πρωτεΐνες
ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙAΣ Γ ΛΥΚΕΙΟΥ (Ιανουάριος 2014) ΘΕΜΑ 1 ο Στις ερωτήσεις 1-5, να επιλέξετε το γράμμα που αντιστοιχεί στη σωστή απάντηση. 1. Το συμπλήρωμα και η προπερδίνη είναι πρωτεΐνες
ΕΝΟΤΗΤΑ 4: ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ - ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΑΝΟΣΙΑΣ - ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΜΥΝΑΣ ΕΡΩΤΗΣΕΙΣ-ΑΣΚΗΣΕΙΣ ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ
 ΚΕΦΑΛΑΙΟ 1 Ο : ΑΝΘΡΩΠΟΣ ΚΑΙ ΥΓΕΙΑ ΕΝΟΤΗΤΑ 4: ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ - ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΑΝΟΣΙΑΣ - ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΜΥΝΑΣ ΕΡΩΤΗΣΕΙΣ-ΑΣΚΗΣΕΙΣ ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ Ερώτηση 1 Από ποιούς
ΚΕΦΑΛΑΙΟ 1 Ο : ΑΝΘΡΩΠΟΣ ΚΑΙ ΥΓΕΙΑ ΕΝΟΤΗΤΑ 4: ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ - ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΑΝΟΣΙΑΣ - ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΜΥΝΑΣ ΕΡΩΤΗΣΕΙΣ-ΑΣΚΗΣΕΙΣ ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ Ερώτηση 1 Από ποιούς
Κεφ. 8. ραστικοί µηχανισµοί της χυµικής ανοσίας: Η εξάλειψη των εξωκυττάριων µικροοργανισµών και τοξινών
 Κεφ. 8. ραστικοί µηχανισµοί της χυµικής ανοσίας: Η εξάλειψη των εξωκυττάριων µικροοργανισµών και τοξινών Οι ιδιότητες των αντισωµάτων που καθορίζουν τις δραστικές τους λειτουργίες Οι δραστικές λειτουργίες
Κεφ. 8. ραστικοί µηχανισµοί της χυµικής ανοσίας: Η εξάλειψη των εξωκυττάριων µικροοργανισµών και τοξινών Οι ιδιότητες των αντισωµάτων που καθορίζουν τις δραστικές τους λειτουργίες Οι δραστικές λειτουργίες
6. ΡΑΣΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΗΣ ΚΥΤΤΑΡΙΚΗΣ ΑΝΟΣΙΑΣ: Εξάλειψη των ενδοκυττάριων µικροοργανισµών
 6. ΡΑΣΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΗΣ ΚΥΤΤΑΡΙΚΗΣ ΑΝΟΣΙΑΣ: Εξάλειψη των ενδοκυττάριων µικροοργανισµών Οι δύο τύποι της κυτταρικής ανοσίας Η µετανάστευση των δραστικών Τ κυττάρων στις εστίες της λοίµωξης (εντόπιση
6. ΡΑΣΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΗΣ ΚΥΤΤΑΡΙΚΗΣ ΑΝΟΣΙΑΣ: Εξάλειψη των ενδοκυττάριων µικροοργανισµών Οι δύο τύποι της κυτταρικής ανοσίας Η µετανάστευση των δραστικών Τ κυττάρων στις εστίες της λοίµωξης (εντόπιση
4. Η κίρρωση του ήπατος προκαλείται εξαιτίας της αποθήκευσης στα ηπατικά κύτταρα: Πρωτεϊνών Υδατανθράκων Λιπών Αλκοόλ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
Σάββατο, 25 Μαΐου 2002 Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗ ΠΑΙ ΕΙΑ. Βιολογία
 Σάββατο, 25 Μαΐου 2002 Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗ ΠΑΙ ΕΙΑ Βιολογία ΘΕΜΑ 1 Στις ερωτήσεις 1 5, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα του το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Ποιο
Σάββατο, 25 Μαΐου 2002 Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗ ΠΑΙ ΕΙΑ Βιολογία ΘΕΜΑ 1 Στις ερωτήσεις 1 5, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα του το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Ποιο
Ανοσολογικοί μηχανισμοί άμυνας
 Ανοσολογικοί μηχανισμοί άμυνας Τύποι κυττάρων του ανοσοποιητικού Ουδετερόφιλα Βασεόφιλα Ηωσινόφιλα Μονοκύτταρα Φαγοκυττάρωση Απελευθερώνουν χημικές ουσίες που εμπλέκονται στη φλεγμονή (αγγειοδιαστολή,
Ανοσολογικοί μηχανισμοί άμυνας Τύποι κυττάρων του ανοσοποιητικού Ουδετερόφιλα Βασεόφιλα Ηωσινόφιλα Μονοκύτταρα Φαγοκυττάρωση Απελευθερώνουν χημικές ουσίες που εμπλέκονται στη φλεγμονή (αγγειοδιαστολή,
ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1: ΑΝΘΡΩΠΟΣ ΚΑΙ ΥΓΕΙΑ
 ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1: ΑΝΘΡΩΠΟΣ ΚΑΙ ΥΓΕΙΑ 1.3, 1.4 Μηχανισμοί άμυνας του ανθρώπινου οργανισμού, AIDS ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση:
ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1: ΑΝΘΡΩΠΟΣ ΚΑΙ ΥΓΕΙΑ 1.3, 1.4 Μηχανισμοί άμυνας του ανθρώπινου οργανισμού, AIDS ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση:
Οταν επώασαν σε Ιn vitro σύστηµα πρωτεϊνοσυνθέσεως
 Οι Ενδείξεις οι οποίες υποστηρίζουν οτι η αναστολή της πρωτεϊνοσυνθέσεως από τους αναστολείς HCR και DAI εξασφαλίζεται µέσω της αντεπίδρασης µε τον eif-2 είναι πολλές η σηµαντικότερη οµως είναι µία Οταν
Οι Ενδείξεις οι οποίες υποστηρίζουν οτι η αναστολή της πρωτεϊνοσυνθέσεως από τους αναστολείς HCR και DAI εξασφαλίζεται µέσω της αντεπίδρασης µε τον eif-2 είναι πολλές η σηµαντικότερη οµως είναι µία Οταν
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
µικροοργανισµών στον οργανισµό µας
 Η ENA ENAΡΞΗ ΡΞΗ ΤΗΣ ΖΩΗΣ Ξεκινά µε τη δηµιουργία του ζυγωτού κατά τη γονιµοποίηση του ωαρίου από το σπερµατοζωάριο Το ζυγωτό είναι το πρώτο κύτταρο του νέου οργανισµού Περνά από διάφορα στάδια διαφοροποίησης
Η ENA ENAΡΞΗ ΡΞΗ ΤΗΣ ΖΩΗΣ Ξεκινά µε τη δηµιουργία του ζυγωτού κατά τη γονιµοποίηση του ωαρίου από το σπερµατοζωάριο Το ζυγωτό είναι το πρώτο κύτταρο του νέου οργανισµού Περνά από διάφορα στάδια διαφοροποίησης
Χρόνια φλεγμονή. Βαλεντίνη Τζιούφα-Ασημακοπούλου. Νοέμβριος 2018
 Χρόνια φλεγμονή Βαλεντίνη Τζιούφα-Ασημακοπούλου Νοέμβριος 2018 Οξεία φλεγμονή Ταχεία εισβολή και λύση Εξιδρωματικά στοιχεία Πολυμορφοπύρηνα Χρόνια φλεγμονή Ύπουλη εισβολήπαρατεταμένη πορείαβραδεία λύση
Χρόνια φλεγμονή Βαλεντίνη Τζιούφα-Ασημακοπούλου Νοέμβριος 2018 Οξεία φλεγμονή Ταχεία εισβολή και λύση Εξιδρωματικά στοιχεία Πολυμορφοπύρηνα Χρόνια φλεγμονή Ύπουλη εισβολήπαρατεταμένη πορείαβραδεία λύση
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 5 ΣΕΛΙΔΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΑΠΑΝΤΗΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΣΑΒΒΑΤΟ 26 ΟΚΤΩΒΡΙΟΥ 2013 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΠΕΝΤΕ (5) Θέμα Α Μονάδες 25 Α1.
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΑΠΑΝΤΗΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΣΑΒΒΑΤΟ 26 ΟΚΤΩΒΡΙΟΥ 2013 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΠΕΝΤΕ (5) Θέμα Α Μονάδες 25 Α1.
Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C.
 Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
3. Η ΠΡΟΣΛΗΨΗΤΟΥ ΑΝΤΙΓΟΝΟΥ ΚΑΙ Η ΠΑΡΟΥΣΙΑΣΗ ΤΟΥ ΣΤΑ ΛΕΜΦΟΚΥΤΤΑΡΑ
 3. Η ΠΡΟΣΛΗΨΗΤΟΥ ΑΝΤΙΓΟΝΟΥ ΚΑΙ Η ΠΑΡΟΥΣΙΑΣΗ ΤΟΥ ΣΤΑ ΛΕΜΦΟΚΥΤΤΑΡΑ ΤΙ ΒΛΕΠΟΥΝ ΤΑ ΛΕΜΦΟΚΥΤΤΑΡΑ Τα αντιγόνα που αναγνωρίζονται από τα Τ λεµφοκύτταρα Πρόσληψη των πρωτεϊνικών αντιγόνων από τα αντιγονοπαρουσιαστικά
3. Η ΠΡΟΣΛΗΨΗΤΟΥ ΑΝΤΙΓΟΝΟΥ ΚΑΙ Η ΠΑΡΟΥΣΙΑΣΗ ΤΟΥ ΣΤΑ ΛΕΜΦΟΚΥΤΤΑΡΑ ΤΙ ΒΛΕΠΟΥΝ ΤΑ ΛΕΜΦΟΚΥΤΤΑΡΑ Τα αντιγόνα που αναγνωρίζονται από τα Τ λεµφοκύτταρα Πρόσληψη των πρωτεϊνικών αντιγόνων από τα αντιγονοπαρουσιαστικά
Φλεγμονή. Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ
 Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015 ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Η φαγοκυττάρωση
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015 ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Η φαγοκυττάρωση
Εισαγωγή στην Ανοσολογία Φυσική Ανοσία. Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ.
 Εισαγωγή στην Ανοσολογία Φυσική Ανοσία Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 11/10/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Ανοσολογία Η
Εισαγωγή στην Ανοσολογία Φυσική Ανοσία Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 11/10/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Ανοσολογία Η
Κυτταρική Βιολογία. Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής ΑΠΘ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος
 Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Κυτταρικός κύκλος Φάσεις του κυτταρικού κύκλου G1:Αύξηση του κυττάρου και προετοιμασία
Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Κυτταρικός κύκλος Φάσεις του κυτταρικού κύκλου G1:Αύξηση του κυττάρου και προετοιμασία
ΘΕΜΑ Α Α1. γ Α2. γ Α3. α Α4. β Α5. β ΘΕΜΑ B B1. B2.
 ΘΕΜΑ Α Α1. γ (το πριμόσωμα) Α2. γ (οι υποκινητές και οι μεταγραφικοί παράγοντες κάθε γονιδίου) Α3. α (μεταφέρει ένα συγκεκριμένο αμινοξύ στο ριβόσωμα) Α4. β (αποδιάταξη των δύο συμπληρωματικών αλυσίδων)
ΘΕΜΑ Α Α1. γ (το πριμόσωμα) Α2. γ (οι υποκινητές και οι μεταγραφικοί παράγοντες κάθε γονιδίου) Α3. α (μεταφέρει ένα συγκεκριμένο αμινοξύ στο ριβόσωμα) Α4. β (αποδιάταξη των δύο συμπληρωματικών αλυσίδων)
- Θεωρία- Δρ. ΠέτρουΚαρκαλούσου
 - Θεωρία- Έκδοση2008 Πρόλογος Αγαπητοίσπουδαστέςοισημειώσειςπουκρατάτεσταχέριασαςέχουνσκοπόνασας εισαγάγουνστιςβασικέςγνώσειςμιαςαπότιςσημαντικότερεςβιοιατρικέςεπιστήμες, της ανοσολογίας. Η ανοσολογίαείναιμιασχετικάνέαεπιστήμηηοποίαεμφανίστηκεστοτέλοςτου
- Θεωρία- Έκδοση2008 Πρόλογος Αγαπητοίσπουδαστέςοισημειώσειςπουκρατάτεσταχέριασαςέχουνσκοπόνασας εισαγάγουνστιςβασικέςγνώσειςμιαςαπότιςσημαντικότερεςβιοιατρικέςεπιστήμες, της ανοσολογίας. Η ανοσολογίαείναιμιασχετικάνέαεπιστήμηηοποίαεμφανίστηκεστοτέλοςτου
Βιολογία Γ Ενιαίου Λυκείου Γενικής Παιδείας
 Ερωτήσεις κλειστού τύπου που τέθηκαν στις πανελλήνιες εξετάσεις (2000-2014) και αφορούν το 1 ο κεφάλαιο ΑΝΘΡΩΠΟΣ ΚΑΙ ΥΓΕΙΑ. (σελ. 31-49) Α. Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση
Ερωτήσεις κλειστού τύπου που τέθηκαν στις πανελλήνιες εξετάσεις (2000-2014) και αφορούν το 1 ο κεφάλαιο ΑΝΘΡΩΠΟΣ ΚΑΙ ΥΓΕΙΑ. (σελ. 31-49) Α. Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση
ΑΡΧΕΣ ΑΝΟΣΟΛΟΓΙΑΣ ΕΙΣΑΓΩΓΗ ΣΤΟ ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ
 ΑΡΧΕΣ ΑΝΟΣΟΛΟΓΙΑΣ ΕΙΣΑΓΩΓΗ ΣΤΟ ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Χρειάζεται η µελέτη της ανοσολογία; Εµβόλια Άµυνα κατά µικροοργανισµών Ανοσολογικές ασθένειες Αλλεργίες - υπερευαισθησίες, αυτοανοσίες, ανοσοανεπάρκειες,
ΑΡΧΕΣ ΑΝΟΣΟΛΟΓΙΑΣ ΕΙΣΑΓΩΓΗ ΣΤΟ ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Χρειάζεται η µελέτη της ανοσολογία; Εµβόλια Άµυνα κατά µικροοργανισµών Ανοσολογικές ασθένειες Αλλεργίες - υπερευαισθησίες, αυτοανοσίες, ανοσοανεπάρκειες,
ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ 1 ο ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ
 ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ 1 ο ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΘΕΜΑ 1 ο Α. Ερωτήσεις πολλαπλής επιλογής 1. γ 2. α 3. β 4. δ 5. δ Β. Ερωτήσεις σωστού - λάθους 1. Σωστό 2. Λάθος 3. Λάθος 4. Λάθος 5. Σωστό ΘΕΜΑ
ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ 1 ο ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΘΕΜΑ 1 ο Α. Ερωτήσεις πολλαπλής επιλογής 1. γ 2. α 3. β 4. δ 5. δ Β. Ερωτήσεις σωστού - λάθους 1. Σωστό 2. Λάθος 3. Λάθος 4. Λάθος 5. Σωστό ΘΕΜΑ
Ανοσοποιητικό σύστημα
 Ανοσοποιητικό σύστημα κωδικός μαθήματος: ETY- 335 Χειμερινό εξάμηνο 2016 Μαρία Χατζηνικολαΐδου mchatzin@materials.uoc.gr Έμφυτο και προσαρμοστικό ανοσοποιητικό σύστημα Η ανοσία είναι η κατάσταση προστασίας
Ανοσοποιητικό σύστημα κωδικός μαθήματος: ETY- 335 Χειμερινό εξάμηνο 2016 Μαρία Χατζηνικολαΐδου mchatzin@materials.uoc.gr Έμφυτο και προσαρμοστικό ανοσοποιητικό σύστημα Η ανοσία είναι η κατάσταση προστασίας
ΑΝΟΣΟΛΟΓΙΑ ΘΕΩΡΙΑ 1 Ο ΜΑΘΗΜΑ
 ΑΝΟΣΟΛΟΓΙΑ ΘΕΩΡΙΑ 1 Ο ΜΑΘΗΜΑ ΑΝΟΣΙΑ Η ανοσία (α- στερητικό + νόσος) είναι η ικανότητα ενός οργανισμού να αμύνεται ενάντια σε κάποιον εξωτερικό βλαπτικό παράγοντα και να μην υφίσταται τις συνέπειές του.
ΑΝΟΣΟΛΟΓΙΑ ΘΕΩΡΙΑ 1 Ο ΜΑΘΗΜΑ ΑΝΟΣΙΑ Η ανοσία (α- στερητικό + νόσος) είναι η ικανότητα ενός οργανισμού να αμύνεται ενάντια σε κάποιον εξωτερικό βλαπτικό παράγοντα και να μην υφίσταται τις συνέπειές του.
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015 ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Η φαγοκυττάρωση
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015 ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Η φαγοκυττάρωση
ΒΙΟΛΟΓΙΑ Γ Λυκείου Γενικής Παιδείας
 1.3 Μηχανισμοί άμυνας του ανθρώπινου οργανισμού Βασικές αρχές ανοσίας Μ1 ΒΙΟΛΟΓΙΑ Γ Λυκείου Γενικής Παιδείας Κεφάλαιο 1 - Άνθρωπος και Υγεία (2) 1.3 ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΒΑΣΙΚΕΣ
1.3 Μηχανισμοί άμυνας του ανθρώπινου οργανισμού Βασικές αρχές ανοσίας Μ1 ΒΙΟΛΟΓΙΑ Γ Λυκείου Γενικής Παιδείας Κεφάλαιο 1 - Άνθρωπος και Υγεία (2) 1.3 ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΒΑΣΙΚΕΣ
ΚΕΦΑΛΑΙΟ 5 ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ ΑΜΕΣΗ COOMBS
 ΚΕΦΑΛΑΙΟ 5 ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ ΑΜΕΣΗ COOMBS ΑΜΕΣΗ COOMBS Θεμελιώδες γνώρισμα του κάθε οργανισμού είναι ότι αναγνωρίζει τα κύτταρα των άλλων οργανισμών ως ξένα Αντιδρά με σκοπό την καταστροφή ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ
ΚΕΦΑΛΑΙΟ 5 ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ ΑΜΕΣΗ COOMBS ΑΜΕΣΗ COOMBS Θεμελιώδες γνώρισμα του κάθε οργανισμού είναι ότι αναγνωρίζει τα κύτταρα των άλλων οργανισμών ως ξένα Αντιδρά με σκοπό την καταστροφή ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ
Καραπέτσας Θανάσης. Διπλωματική Εργασία:
 Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ ΕΞΕΤΑΣΗΣ: ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: 16 / 06 / 2017 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ Θέμα Α Α1: δ Α2:
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ ΕΞΕΤΑΣΗΣ: ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: 16 / 06 / 2017 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ Θέμα Α Α1: δ Α2:
Ανοσιακή απάντηση Αικατερίνη Ταράση
 Ανοσιακή απάντηση Αικατερίνη Ταράση ιευθύντρια Τµ. Ανοσολογίας- Ιστοσυµβατότητας Γ.Ν.Α.. " Ο Ευαγγελισµός" ανοσιακή απάντηση είναι το σύνολο των πολύπλοκων διεργασιών µε τις οποίες ο οργανισµός (ξενιστής)
Ανοσιακή απάντηση Αικατερίνη Ταράση ιευθύντρια Τµ. Ανοσολογίας- Ιστοσυµβατότητας Γ.Ν.Α.. " Ο Ευαγγελισµός" ανοσιακή απάντηση είναι το σύνολο των πολύπλοκων διεργασιών µε τις οποίες ο οργανισµός (ξενιστής)
Εισαγωγή στην Ανοσολογία
 Εισαγωγή στην Ανοσολογία ρ. Γιώργος Κρασιάς Ινστιτούτο Νευρολογίας και Γενετικής Κύπρου Τµήµα Μοριακής Ιολογίας Τι είναι το Ανοσοποιητικό Σύστηµα (ΑΣ)? Το ΑΣ (Immune System) είναι ένα σύστηµα άµυνας του
Εισαγωγή στην Ανοσολογία ρ. Γιώργος Κρασιάς Ινστιτούτο Νευρολογίας και Γενετικής Κύπρου Τµήµα Μοριακής Ιολογίας Τι είναι το Ανοσοποιητικό Σύστηµα (ΑΣ)? Το ΑΣ (Immune System) είναι ένα σύστηµα άµυνας του
Συστήματα επικοινωνίας Ανθρωπίνου σώματος. ενδοκρινολογικό νευρικό σύστημα
 Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
μαθητικό φροντιστήριο
 σύγχρονο Φάσμα group προπαρασκευή για μαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 50.51.557 50.56.296 25ης Μαρτίου 74 ΠΛ.ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990 50.20.990 Πρωτεσιλάου
σύγχρονο Φάσμα group προπαρασκευή για μαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 50.51.557 50.56.296 25ης Μαρτίου 74 ΠΛ.ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990 50.20.990 Πρωτεσιλάου
ΚΕΦΑΛΑΙΟ 7 Χυμικές ανοσοαπαντήσεις Ενεργοποίηση των Β λεμφοκυττάρων και παραγωγή των αντισωμάτων
 ΚΕΦΑΛΑΙΟ 7 Χυμικές ανοσοαπαντήσεις Ενεργοποίηση των Β λεμφοκυττάρων και παραγωγή των αντισωμάτων Φάσεις και τύποι των χυμικών ανοσοαπαντήσεων Διέγερση των Β λεμφοκυττάρων από το αντιγόνο Μεταβίβαση σήματος
ΚΕΦΑΛΑΙΟ 7 Χυμικές ανοσοαπαντήσεις Ενεργοποίηση των Β λεμφοκυττάρων και παραγωγή των αντισωμάτων Φάσεις και τύποι των χυμικών ανοσοαπαντήσεων Διέγερση των Β λεμφοκυττάρων από το αντιγόνο Μεταβίβαση σήματος
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών
 Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
ΛΕΜΦΟΚΥΤΤΑΡΑ. Τ λεµφοκύτταρα:
 ΛΕΜΦΟΚΥΤΤΑΡΑ Προέλευση: µυελός των οστών. Μερικά µεταναστεύουν στο θύµο, όπου παραµένουν για ποικίλες περιόδους πριν διασκορπισθούν στο σώµα. Βίος: η ζωή τους ποικίλει. Τα µνηµοκύτταρα ζουν για πολλά χρόνια
ΛΕΜΦΟΚΥΤΤΑΡΑ Προέλευση: µυελός των οστών. Μερικά µεταναστεύουν στο θύµο, όπου παραµένουν για ποικίλες περιόδους πριν διασκορπισθούν στο σώµα. Βίος: η ζωή τους ποικίλει. Τα µνηµοκύτταρα ζουν για πολλά χρόνια
ΑΝΟΣΟΛΟΓΙΑ. 1. Εισαγωγή (κυρίως στην επίκτητη ανοσία) 2. Φυσική ανοσία
 ΑΝΟΣΟΛΟΓΙΑ 1. Εισαγωγή (κυρίως στην επίκτητη ανοσία) 2. Φυσική ανοσία ΕΠΙΚΤΗΤΗ ΑΝΟΣΙΑ ΑΝΤΙΓΟΝΟ και ΥΠΟ ΟΧΕΙΣ ΑΝΤΙΓΟΝΟΥ 3. Η πρόσληψη του αντιγόνου και η παρουσίασή του στα λεµφοκύτταρα 4. Η αναγνώριση
ΑΝΟΣΟΛΟΓΙΑ 1. Εισαγωγή (κυρίως στην επίκτητη ανοσία) 2. Φυσική ανοσία ΕΠΙΚΤΗΤΗ ΑΝΟΣΙΑ ΑΝΤΙΓΟΝΟ και ΥΠΟ ΟΧΕΙΣ ΑΝΤΙΓΟΝΟΥ 3. Η πρόσληψη του αντιγόνου και η παρουσίασή του στα λεµφοκύτταρα 4. Η αναγνώριση
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ
 23 10 2011 ΘΕΡΙΝΑ ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Όλα τα βακτήρια: Α. διαθέτουν
23 10 2011 ΘΕΡΙΝΑ ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Όλα τα βακτήρια: Α. διαθέτουν
4. Η κίρρωση του ήπατος προκαλείται εξαιτίας της αποθήκευσης στα ηπατικά κύτταρα: Πρωτεϊνών Υδατανθράκων Λιπών Αλκοόλ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1(ΥΓΕΙΑ-ΑΝΘΡΩΠΟΣ)
 ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1(ΥΓΕΙΑ-ΑΝΘΡΩΠΟΣ) Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση ή στη φράση που συμπληρώνει σωστά την πρόταση: 1. Οι ιοί αποτελούνται
ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1(ΥΓΕΙΑ-ΑΝΘΡΩΠΟΣ) Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση ή στη φράση που συμπληρώνει σωστά την πρόταση: 1. Οι ιοί αποτελούνται
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ (ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ) ΘΕΜΑ Α Α1. α Α2. γ Α3. α Α4. γ Α5. δ ΘΕΜΑ Β Β1. α) Λάθος
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ (ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ) ΘΕΜΑ Α Α1. α Α2. γ Α3. α Α4. γ Α5. δ ΘΕΜΑ Β Β1. α) Λάθος
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 18 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ: ΒΙΟΛΟΓΙΑ
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 18 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ: ΒΙΟΛΟΓΙΑ ΘΕΜΑ 1ο Α. Στις ερωτήσεις 1-3, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 18 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ: ΒΙΟΛΟΓΙΑ ΘΕΜΑ 1ο Α. Στις ερωτήσεις 1-3, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και
04/11/2018 ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΝΟΤΑ ΛΑΖΑΡΑΚΗ ΘΕΜΑ Α
 ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ 04/11/2018 ΝΟΤΑ ΛΑΖΑΡΑΚΗ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Πυρηνική περιοχή διαθέτει: Α. Ο ιός της
ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ 04/11/2018 ΝΟΤΑ ΛΑΖΑΡΑΚΗ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Πυρηνική περιοχή διαθέτει: Α. Ο ιός της
Μοριακή Βιολογία. Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μοριακή Βιολογία Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος Παναγιωτίδης Χρήστος Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μοριακή Βιολογία Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος Παναγιωτίδης Χρήστος Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΠΑΝΕΛΛΗΝΙΕ 2017 ΑΠΑΝΣΗΕΙ ΣΟ ΜΑΘΗΜΑ ΣΗ ΒΙΟΛΟΓΙΑ ΠΡΟΑΝΑΣΟΛΙΜΟΤ
 ΠΑΝΕΛΛΗΝΙΕ 2017 ΑΠΑΝΣΗΕΙ ΣΟ ΜΑΘΗΜΑ ΣΗ ΒΙΟΛΟΓΙΑ ΠΡΟΑΝΑΣΟΛΙΜΟΤ 16/06/2017 ΕΠΙΜΕΛΕΙΑ: ΑΝΔΡΙΑΝΗ ΠΑΡΑΧΗ ΘΕΜΑ Α A1. Δ Α2. Δ Α3. Β Α4. Γ Α5.Α ΘΕΜΑ Β Β1) I A II E III Σ IV Β V Ζ VI Γ VII Δ Β2) ε προκαρυωτικό γιατί
ΠΑΝΕΛΛΗΝΙΕ 2017 ΑΠΑΝΣΗΕΙ ΣΟ ΜΑΘΗΜΑ ΣΗ ΒΙΟΛΟΓΙΑ ΠΡΟΑΝΑΣΟΛΙΜΟΤ 16/06/2017 ΕΠΙΜΕΛΕΙΑ: ΑΝΔΡΙΑΝΗ ΠΑΡΑΧΗ ΘΕΜΑ Α A1. Δ Α2. Δ Α3. Β Α4. Γ Α5.Α ΘΕΜΑ Β Β1) I A II E III Σ IV Β V Ζ VI Γ VII Δ Β2) ε προκαρυωτικό γιατί
ΠΑΡΑΓΟΝΤΕΣ ΜΗ ΕΙ ΙΚΗΣ ΑΝΟΣΙΑΣ
 ΠΑΡΑΓΟΝΤΕΣ ΜΗ ΕΙ ΙΚΗΣ ΑΝΟΣΙΑΣ Θεοδώρα Κεραµιτσόγλου Ανοσοβιολογικό Τµήµα Π.Γ.Ν.-Μ. «Έλενα Βενιζέλου» Βενιζέλου» Μό Ανατοµικοί (Φυσικοί) Φραγµοί Τ ο ξ ίν ε ς λ υ ν σ η Μη ειδική ΑνοσίαTLRs Ανοσιακό Σύστηµα
ΠΑΡΑΓΟΝΤΕΣ ΜΗ ΕΙ ΙΚΗΣ ΑΝΟΣΙΑΣ Θεοδώρα Κεραµιτσόγλου Ανοσοβιολογικό Τµήµα Π.Γ.Ν.-Μ. «Έλενα Βενιζέλου» Βενιζέλου» Μό Ανατοµικοί (Φυσικοί) Φραγµοί Τ ο ξ ίν ε ς λ υ ν σ η Μη ειδική ΑνοσίαTLRs Ανοσιακό Σύστηµα
Η µελέτη της ρύθµισης της πρωτεινοσύνθεσης στο επίπεδο του Ριβοσώµατος εντοπίζεται σε τρία επίπεδα
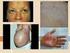 Η µελέτη της ρύθµισης της πρωτεινοσύνθεσης στο επίπεδο του Ριβοσώµατος εντοπίζεται σε τρία επίπεδα ΣτονΣτον ρόλο των διαφόρων οµάδων των ριβοσωµικών πρωτεινών. Κατά πόσο δηλαδή υπάρχει ετερογένεια στις
Η µελέτη της ρύθµισης της πρωτεινοσύνθεσης στο επίπεδο του Ριβοσώµατος εντοπίζεται σε τρία επίπεδα ΣτονΣτον ρόλο των διαφόρων οµάδων των ριβοσωµικών πρωτεινών. Κατά πόσο δηλαδή υπάρχει ετερογένεια στις
ΜΕΛΕΤΗ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ
 ΜΕΛΕΤΗ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ 1. Αναφέρετε ονομαστικά όλα τα μικρόβια και τις ασθένειες που αυτά προκαλούν. 2. Φτιάξτε ένα πίνακα που να φαίνονται οι δομικές κ λειτουργικές διαφορές μεταξύ
ΜΕΛΕΤΗ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ 1. Αναφέρετε ονομαστικά όλα τα μικρόβια και τις ασθένειες που αυτά προκαλούν. 2. Φτιάξτε ένα πίνακα που να φαίνονται οι δομικές κ λειτουργικές διαφορές μεταξύ
Ανοσολογικοί μηχανισμοί άμυνας
 Ανοσολογικοί μηχανισμοί άμυνας Τύποι κυττάρων του ανοσοποιητικού Ουδετερόφιλα Βασεόφιλα Ηωσινόφιλα Μονοκύτταρα Φαγοκυττάρωση Απελευθερώνουν χημικές ουσίες που εμπλέκονται στη φλεγμονή (αγγειοδιαστολή,
Ανοσολογικοί μηχανισμοί άμυνας Τύποι κυττάρων του ανοσοποιητικού Ουδετερόφιλα Βασεόφιλα Ηωσινόφιλα Μονοκύτταρα Φαγοκυττάρωση Απελευθερώνουν χημικές ουσίες που εμπλέκονται στη φλεγμονή (αγγειοδιαστολή,
Φάσμα. προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝ.ΠΑΙΔΕΙΑΣ
 σύγχρονο Φάσμα προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. μαθητικό φροντιστήριο 25ης Μαρτίου 111 - ΠΕΤΡΟΥΠΟΛΗ - 210 50 20 990-210 50 27 990 25ης Μαρτίου 74 - ΠΕΤΡΟΥΠΟΛΗ - 210 50 50 658-210 50 60 845 Γραβιάς 85 -
σύγχρονο Φάσμα προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. μαθητικό φροντιστήριο 25ης Μαρτίου 111 - ΠΕΤΡΟΥΠΟΛΗ - 210 50 20 990-210 50 27 990 25ης Μαρτίου 74 - ΠΕΤΡΟΥΠΟΛΗ - 210 50 50 658-210 50 60 845 Γραβιάς 85 -
Kυτταρική Bιολογία. Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος ΔIAΛEΞΗ 20 (9/5/2017) Δρ. Xρήστος Παναγιωτίδης, Τμήμα Φαρμακευτικής Α.Π.Θ.
 Kυτταρική Bιολογία ΔIAΛEΞΗ 20 (9/5/2017) Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος Τι είναι απόπτωση; Απόπτωση είναι ο προγραμματισμένος κυτταρικός θάνατος Η καταστροφή του κυττάρου γίνεται «ήπια»
Kυτταρική Bιολογία ΔIAΛEΞΗ 20 (9/5/2017) Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος Τι είναι απόπτωση; Απόπτωση είναι ο προγραμματισμένος κυτταρικός θάνατος Η καταστροφή του κυττάρου γίνεται «ήπια»
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
 ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΠΑΝΕΛΛΗΝΙΩΝ 2017 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII Δ Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Στους προκαρυωτικούς
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΠΑΝΕΛΛΗΝΙΩΝ 2017 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII Δ Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Στους προκαρυωτικούς
Γιάννης Δρακόπουλος 1. ΚΕΦ.1.3 ΘΕΜΑΤΑ (ομάδα Δ)
 Γιάννης Δρακόπουλος 1 1. ΚΕΦ.1.3 ΘΕΜΑΤΑ (ομάδα Δ) 2. Το διάγραµµα α δείχνει ότι τα αντιγόνα είναι αρχικά πολλά και εν συνεχεία ελαττώνονται διαρκώς. Δεν µεσολαβεί στάδιο αύξησης τους, επομένως δεν παρατηρείται
Γιάννης Δρακόπουλος 1 1. ΚΕΦ.1.3 ΘΕΜΑΤΑ (ομάδα Δ) 2. Το διάγραµµα α δείχνει ότι τα αντιγόνα είναι αρχικά πολλά και εν συνεχεία ελαττώνονται διαρκώς. Δεν µεσολαβεί στάδιο αύξησης τους, επομένως δεν παρατηρείται
4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ. περιλαμβάνονται ο σπλήνας και ο θύμος αδένας (εικ.4.1). Το λεμφικό σύστημα είναι πολύ σημαντικό γιατί:
 ΚΕΦΑΛΑΙΟ 4 4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ Το λεμφικό σύστημα αποτελείται από τα λεμφαγγεία, τη λέμφο και τους λεμφαδένες. Οι λεμφαδένες είναι δομές που αποτελούνται από εξειδικευμένη μορφή συνδετικού ιστού, το λεμφικό
ΚΕΦΑΛΑΙΟ 4 4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ Το λεμφικό σύστημα αποτελείται από τα λεμφαγγεία, τη λέμφο και τους λεμφαδένες. Οι λεμφαδένες είναι δομές που αποτελούνται από εξειδικευμένη μορφή συνδετικού ιστού, το λεμφικό
