ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Η ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ V. ΑΡΧΕΣ ΔΟΜΗΣΗΣ ΤΩΝ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ
|
|
|
- Ἀδάμ Αποστόλου
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Η ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ V. ΑΡΧΕΣ ΔΟΜΗΣΗΣ ΤΩΝ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Στο άτομο του υδρογόνου, το μοναδικό ηλεκτρόνιο τοποθετείται στο τροχιακό 1s. Στην περίπτωση αυτή λέμε πως το άτομο βρίσκεται στη θεμελιώδη του κατάσταση. Η τοποθέτηση του σε οποιοδήποτε άλλο τροχιακό είναι δυνατή μετά από διέγερση του ατόμου. Στα πολυηλεκτρονικά άτομα προφανώς τα πράγματα είναι πιο πολυ πλοκα. Η συμπλήρωση των τροχιακών με ηλεκτρόνια, η λεγόμενη ηλεκτρονιακη δόμηση, ακολουθεί ορισμένους κανόνες (αρχές). Η ηλεκτρονιακή δόμηση έχει θεμελιώδη σημασία, γιατί με βάση αυτή διαμορφώνεται η ηλεκτρονιακή δομή των ατόμων και κατ επέκταση η χημική συμπεριφορά τους
2 Η ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗΣΗ Η ηλεκτρονιακή δόμηση βασίζεται σε τρεις αρχές. Απαγορευτικη αρχη του Pauli Αρχη ελάχιστης ενέργειας Κανόνας του Hund Απαγορευτική αρχή του Pauli Σύμφωνα με την απαγορευτική αρχή του Pauli είναι αδύνατο να υπάρχουν στο ίδιο άτομο δύο ηλεκτρόνια με ίδια τετράδα κβαντικών αριθμών (n, l, m l, m s ). Συνεπώς, δεν μπορεί ένα τροχιακό να χωρέσει πάνω από δύο ηλεκτρόνια. H απαγορευτική αρχή του Pauli καθορίζει ένα μέγιστο αριθμό ηλεκτρονίων σε κάθε τροχιακό, υποστιβάδα και στιβάδα
3 Ο μέγιστος αριθμός ηλεκτρονίων (ανά τροχιακό, υποστιβάδα και στιβάδα) Σε κάθε τροχιακό [ 2 e ] Σε υποστοιβάδα [ (4l + 2) e ] l = 0 s 2 l = 1 p 6 l = 2 d 10 l = 3 f 14 Ηλεκτρόνια ανά υποστοιβάδα Σε στοιβάδα [ 2n 2 e ] n= 1 K 2 n = 2 L 8 n = 3 M 18 n = 4 N 32 Ηλεκτρόνια ανά στοιβάδα Αρχή ελάχιστης ενέργειας Σ ένα πολυηλεκτρονικό άτομο, πλην των ελκτικών δυνάμεων πυρήνα - ηλεκτρονίου (που καθορίζονται από τον κυ ριο κβαντικό αριθμό), ασκου νται απώσεις ηλεκτρονίου - ηλεκτρονίου (που καθορίζονται από το δευτερευ οντα κβαντικό αριθμό). Για το λόγο αυτό διαφοροποιου νται οι ενεργειακές στάθμες των υποστιβάδων της ίδιας στιβάδας. Σύμφωνα με την αρχή της ελάχιστης ενέργειας, κατά την ηλεκτρονιακή δόμηση ενός πολυηλεκτρονικού ατόμου, τα ηλεκτρόνια οφείλουν να καταλάβουν τροχιακά με τη μικρότερη ενέργεια, ώστε να αποκτήσουν τη μεγίστη σταθερότητα στη θεμελιώδη κατάσταση. Όσο μικρότερο είναι το άθροισμα (n+l) τόσο μικρότερη είναι η ενεργειακή στάθμη του τροχιακου. Αν δυ ο τροχιακά έχουν το ίδιο (n+l), τότε μικρότερη ενεργειακή στάθμη έχει το τροχιακό με το μικρότερο 1ο κβαντικό αριθμό (n). Τα τροχιακά στην ίδια υποστιβάδα έχουν την ίδια ενέργεια (εκφυλισμένα τροχιακά) - 3 -
4 Παράδειγμα 2s n + l = = 2 3p n + l = = 4 4s n + l = = 4 3d n + l = = 5 Άρα για τα τροχιακά αυτά η σειρά αυξανόμενης ενέργειας είναι: 2s < 3p < 4s < 3d Διαγράμματα αυξανόμενης ενέργειας τροχιακών Σειρά πλήρωσης τροχιακών 1s,2s,2p,3s,3p,4s,3d,4p,5s,4d,5p,6s,4f,5d,6p,7s,5f,6d,7p,8s,5g,6f,... 1η παρατήρηση στην ενέργεια των τροχιακών Στο άτομο του υδρογόνου η ενέργεια εξαρτάται μόνο από τον 1ο κβαντικό αριθμό n. Έτσι τα τροχιακά της ίδιας στιβάδας του υδρογόνου έχουν την ίδια ενέργεια (εκφυλισμένα) και δεν διαφοροποιου νται ενεργειακά όπως τα τροχιακά των πολυηλεκτρονικών ατόμων
5 2η παρατήρηση στην ενέργεια των τροχιακών. Από τους κανόνες δόμησης είδαμε ότι το ns τροχιακό έχει μικρότερη ενέργεια από τα (n-1)d τροχιακά και γι αυτό συμπληρώνεται πρώτα το ns και μετά τα (n-1)d. Όταν όμως τοποθετου νται τα ηλεκτρόνια στα (n-1)d τροχιακά, αυτά αποκτου ν μικρότερη ενέργεια από τα ηλεκτρόνια στο ns. Συ μφωνα με τα παραπάνω είναι δυνατόν να γράφουμε της ηλεκτρονικές διαμορφώσεις με δυ ο τρόπους: π.χ. Fe (Z=26) Με αυ ξουσα ενέργεια τροχιακών 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Με αυ ξουσα ενέργεια ηλεκτρονίων 2 1s 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2 Καλό είναι να γράφουμε την ηλεκτρονική διαμόρφωση με αυ ξουσα ενέργεια ηλεκτρονίων γιατί διευκολυ νει στην διαμόρφωση των κατιόντων: π.χ. για τον Fe 2+ γράφουμε: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 ενώ για τον Fe 3+ γράφουμε: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 3η παρατήρηση στην ενέργεια των τροχιακών Την αρχή της μεγίστης σταθερότητας των συμπληρωμένων και ημισυμπληρωμένων υποστιβάδων συ μφωνα με την οποία αυξημένη σταθερότητα επιδεικνυ ουν οι συμπληρωμένες και ημισυμπληρωμένες υποστιβάδες. Cr: [Ar]3d 5 4s 1 και όχι [Ar]3d 4 4s 2 Cu: [Ar]3d 10 4s 1 και όχι [Ar]3d 9 4s 2-5 -
6 Κανόνας του Hund Ηλεκτρόνια που καταλαμβάνουν τροχιακά της ίδιας ενέργειας (της ίδιας υποστιβάδας), έχουν κατά προτίμηση παράλληλα spin, ώστε τα ηλεκτρόνια να αποκτήσουν το μέγιστο άθροισμα των κβαντικών αριθμών spin. π. χ. στο άτομο του οξυγόνου με δομή 1s 2, 2s 2, 2p 4, τα 4 ηλεκτρόνια στην υποστιβάδα (2p) έχουν δυνατότητα να έχουν δυ ο διαμορφώσεις: - 6 -
Η δοµή του ατόµου. Ηλεκτρονική δόµηση. Από τον Δ ηµόκριτο µέχρι το σύγχρονο κβαντικό άτοµο. W. Heisenberg. E. Schrödinger W. Pauli. N. Bohr. M.
 Η δοµή του ατόµου Ηλεκτρονική δόµηση E. Schrödinger W. Pauli W. Heisenberg N. Bohr M. Planck Από τον Δ ηµόκριτο µέχρι το σύγχρονο κβαντικό άτοµο 1 Αρχές ηλεκτρονικής δόµησης Η ηλεκτρονική δόµηση βασίζεται
Η δοµή του ατόµου Ηλεκτρονική δόµηση E. Schrödinger W. Pauli W. Heisenberg N. Bohr M. Planck Από τον Δ ηµόκριτο µέχρι το σύγχρονο κβαντικό άτοµο 1 Αρχές ηλεκτρονικής δόµησης Η ηλεκτρονική δόµηση βασίζεται
Αρχές δόμησης πολυηλεκτρονικών ατόμων.
 Αρχές δόμησης πολυηλεκτρονικών ατόμων. Η συμπλήρωση των τροχιακών των ατόμων με ηλεκτρόνια γίνεται με βάση τους εξής κανόνες: Απαγορευτική αρχή του Pauli. Αρχή ελάχιστης ενέργειας. Κανόνας του Hund. Η
Αρχές δόμησης πολυηλεκτρονικών ατόμων. Η συμπλήρωση των τροχιακών των ατόμων με ηλεκτρόνια γίνεται με βάση τους εξής κανόνες: Απαγορευτική αρχή του Pauli. Αρχή ελάχιστης ενέργειας. Κανόνας του Hund. Η
 http://mathesis.cup.gr/courses/physics/phys1.1/2016_t3/about http://mathesis.cup.gr/courses/course-v1:physics+phys1.2+2016_t4/about f atomic orbitals http://www.orbitals.com/orb/orbtable.htm g atomic orbitals
http://mathesis.cup.gr/courses/physics/phys1.1/2016_t3/about http://mathesis.cup.gr/courses/course-v1:physics+phys1.2+2016_t4/about f atomic orbitals http://www.orbitals.com/orb/orbtable.htm g atomic orbitals
Αφορά τη συμπλήρωση των τροχιακών με ηλεκτρόνια, στα πολυηλεκτρονικά άτομα. Γίνεται λαμβάνοντας υπόψη μας τρεις αρχές (aufbeau)
 Ηλεκτρονιακή δόμηση Αφορά τη συμπλήρωση των τροχιακών με ηλεκτρόνια, στα πολυηλεκτρονικά άτομα. Γίνεται λαμβάνοντας υπόψη μας τρεις αρχές (aufbeau) Απαγορευτική αρχή Pauli Αρχή ελάχιστης ενέργειας Κανόνας
Ηλεκτρονιακή δόμηση Αφορά τη συμπλήρωση των τροχιακών με ηλεκτρόνια, στα πολυηλεκτρονικά άτομα. Γίνεται λαμβάνοντας υπόψη μας τρεις αρχές (aufbeau) Απαγορευτική αρχή Pauli Αρχή ελάχιστης ενέργειας Κανόνας
1.2 Αρχές δόμησης πολυηλεκτρονικών ατόμων
 1.2 Αρχές δόμησης πολυηλεκτρονικών ατόμων 1. Ερώτηση: Τι είναι η ηλεκτρονική δόμηση ή ηλεκτρονική κατανομή; Η συμπλήρωση των τροχιακών με ηλεκτρόνια, λέγεται ηλεκτρονική δόμηση ή ηλεκτρονική κατανομή.
1.2 Αρχές δόμησης πολυηλεκτρονικών ατόμων 1. Ερώτηση: Τι είναι η ηλεκτρονική δόμηση ή ηλεκτρονική κατανομή; Η συμπλήρωση των τροχιακών με ηλεκτρόνια, λέγεται ηλεκτρονική δόμηση ή ηλεκτρονική κατανομή.
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 08 / 09 /2013 ΑΠΑΝΤΗΣΕΙΣ
 ΔΙΑΓΩΝΙΣΜΑ ΕΚΠ. ΕΤΟΥΣ 03-0 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 08 / 09 /03 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α έως και Α να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα
ΔΙΑΓΩΝΙΣΜΑ ΕΚΠ. ΕΤΟΥΣ 03-0 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 08 / 09 /03 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α έως και Α να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα
ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ
 Αρχές δόµησης πολυηλεκτρονιακών ατόµων 39. 2 o Αρχές δόµησης Πολυηλεκτρονιακών ατόµων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Η συµπλήρωση των τροχιακών ενός ατόµου µε ηλεκτρόνια γίνεται µε βάση την αρχή ηλεκτρονιακής
Αρχές δόµησης πολυηλεκτρονιακών ατόµων 39. 2 o Αρχές δόµησης Πολυηλεκτρονιακών ατόµων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Η συµπλήρωση των τροχιακών ενός ατόµου µε ηλεκτρόνια γίνεται µε βάση την αρχή ηλεκτρονιακής
ΧΗΜΕΙΑ θετικής κατεύθυνσης
 ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ Γ ΓΕΛ Οκτώβριος 014 ΧΗΜΕΙΑ θετικής κατεύθυνσης Α1. β Α. δ Α3. δ Α4. γ Α5. γ ΘΕΜΑ Α ΘΕΜΑ Β Β1α) Λάθος Η πιθανότητα εύρεσης του ηλεκτρονίου είναι μέγιστη κοντά στον πυρήνα άρα στο
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ Γ ΓΕΛ Οκτώβριος 014 ΧΗΜΕΙΑ θετικής κατεύθυνσης Α1. β Α. δ Α3. δ Α4. γ Α5. γ ΘΕΜΑ Α ΘΕΜΑ Β Β1α) Λάθος Η πιθανότητα εύρεσης του ηλεκτρονίου είναι μέγιστη κοντά στον πυρήνα άρα στο
Ασκήσεις στην ηλεκτρονιακή δόμηση των ατόμων
 Ασκήσεις στην ηλεκτρονιακή δόμηση των ατόμων Στις παρακάτω ερωτήσεις επιλέξτε τη σωστή απάντηση. Ο μέγιστος αριθμός ηλεκτρονίων για κάθε στιβάδα προκύπτει με εφαρμογή: α. της αρχής της ελάχιστης ενέργειας
Ασκήσεις στην ηλεκτρονιακή δόμηση των ατόμων Στις παρακάτω ερωτήσεις επιλέξτε τη σωστή απάντηση. Ο μέγιστος αριθμός ηλεκτρονίων για κάθε στιβάδα προκύπτει με εφαρμογή: α. της αρχής της ελάχιστης ενέργειας
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 07 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 07 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 07 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί
Κεφάλαιο 8. Ηλεκτρονικές Διατάξεις και Περιοδικό Σύστημα
 Κεφάλαιο 8 Ηλεκτρονικές Διατάξεις και Περιοδικό Σύστημα 1. H απαγορευτική αρχή του Pauli 2. Η αρχή της ελάχιστης ενέργειας 3. Ο κανόνας του Hund H απαγορευτική αρχή του Pauli «Είναι αδύνατο να υπάρχουν
Κεφάλαιο 8 Ηλεκτρονικές Διατάξεις και Περιοδικό Σύστημα 1. H απαγορευτική αρχή του Pauli 2. Η αρχή της ελάχιστης ενέργειας 3. Ο κανόνας του Hund H απαγορευτική αρχή του Pauli «Είναι αδύνατο να υπάρχουν
Πρωτόνια, νετρόνια και ηλεκτρόνια. πρωτόνιο 1 (1,67X10-24 g) +1 νετρόνιο 1 0 1,6X10-19 Cb ηλεκτρόνιο 1/1836 (9X10-28 g) -1
 Πρωτόνια, νετρόνια και ηλεκτρόνια. σχετική μάζα σχετικό φορτίο πρωτόνιο 1 (1,67X10-24 g) +1 νετρόνιο 1 0 1,6X10-19 Cb ηλεκτρόνιο 1/1836 (9X10-28 g) -1 Ο πυρήνας βρίσκεται στο κέντρο του ατόμου και περιέχει
Πρωτόνια, νετρόνια και ηλεκτρόνια. σχετική μάζα σχετικό φορτίο πρωτόνιο 1 (1,67X10-24 g) +1 νετρόνιο 1 0 1,6X10-19 Cb ηλεκτρόνιο 1/1836 (9X10-28 g) -1 Ο πυρήνας βρίσκεται στο κέντρο του ατόμου και περιέχει
Κομβικές επιφάνειες. Από τη γνωστή σχέση: Ψ(r, θ, φ) = R(r).Θ(θ).Φ(φ) για Ψ = 0 θα πρέπει είτε R(r) = 0 ή Θ(θ).Φ(φ) = 0
 Κομβικές επιφάνειες Από τα σχήματα των ατομικών τροχιακών αλλά και από τις μαθηματικές εκφράσεις είναι φανερό ότι υπάρχουν επιφάνειες όπου το Ψ 2 μηδενίζεται, πάνω στις οποίες δηλαδή είναι αδύνατο να βρεθεί
Κομβικές επιφάνειες Από τα σχήματα των ατομικών τροχιακών αλλά και από τις μαθηματικές εκφράσεις είναι φανερό ότι υπάρχουν επιφάνειες όπου το Ψ 2 μηδενίζεται, πάνω στις οποίες δηλαδή είναι αδύνατο να βρεθεί
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 3: Ηλεκτρονική διαμόρφωση των ατόμων
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 3: Ηλεκτρονική διαμόρφωση των ατόμων Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 3: Ηλεκτρονική διαμόρφωση των ατόμων Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε
Α ΚΥΚΛΟΣ ΣΥΓΧΡΟΝΩΝ ΠΡΟΣΟΜΟΙΩΤΙΚΩΝ ΔΙΑΓΩΝΙΣΜΑΤΩΝ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ Γ ΓΕΛ ΣΕΠΤΕΜΒΡΙΟΣ Χημεία ΘΕΜΑ Β
 ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ Γ ΓΕΛ ΣΕΠΤΕΜΒΡΙΟΣ 04 Χημεία ΘΕΜΑ Α Α. β. Α. γ. Α.3 δ. Α.4 γ. Α.5 δ. ΘΕΜΑ Β Β. α. Λάθος. Στα πολυηλεκτρονιακά άτομα η σύγκριση των υποστιβάδων γίνεται με βάση το Θετικής Κατεύθυνσης
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ Γ ΓΕΛ ΣΕΠΤΕΜΒΡΙΟΣ 04 Χημεία ΘΕΜΑ Α Α. β. Α. γ. Α.3 δ. Α.4 γ. Α.5 δ. ΘΕΜΑ Β Β. α. Λάθος. Στα πολυηλεκτρονιακά άτομα η σύγκριση των υποστιβάδων γίνεται με βάση το Θετικής Κατεύθυνσης
1o Kριτήριο Αξιολόγησης
 1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
ΑΠΑΝΤΗΣΕΙΣ. A2. Ο μέγιστος αριθμός ηλεκτρονίων σε ένα άτομο που χαρακτηρίζεται από τους κβαντικούς αριθμούς n = 2 και m l = 0 είναι: α. 4 β.3 γ.2 δ.
 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστ απάντηση. Α1. Ένα τροχιακό χαρακτηρίζεται από τους κβαντικούς
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστ απάντηση. Α1. Ένα τροχιακό χαρακτηρίζεται από τους κβαντικούς
ΑΤΟΜΙΚΑ ΤΟΜΙΚΑ ΠΡΟΤΥΠΑ
 ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
Μετά το τέλος της µελέτης του 1ου κεφαλαίου, ο µαθητής θα πρέπει να είναι σε θέση:
 Μετά το τέλος της µελέτης του 1ου κεφαλαίου, ο µαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει το ατοµικό πρότυπο του Bohr καθώς και τα µειονεκτήµατά του. Να υπολογίζει την ενέργεια που εκπέµπεται ή απορροφάται
Μετά το τέλος της µελέτης του 1ου κεφαλαίου, ο µαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει το ατοµικό πρότυπο του Bohr καθώς και τα µειονεκτήµατά του. Να υπολογίζει την ενέργεια που εκπέµπεται ή απορροφάται
Ζαχαριάδου Φωτεινή Σελίδα 1 από 21. Γ Λυκείου Κατεύθυνσης Κεφάλαιο 1: Ηλεκτρονιακή δοµή του ατόµου
 Ζαχαριάδου Φωτεινή Σελίδα 1 από 21 Γ Λυκείου Κατεύθυνσης Κεφάλαιο 1: Ηλεκτρονιακή δοµή του ατόµου Θέµατα Σωστού/Λάθους και Πολλαπλής επιλογής Πανελληνίων, ΟΕΦΕ, ΠΜ Χ Το 17Cl σχηµατίζει ενώσεις µε ένα µόνο
Ζαχαριάδου Φωτεινή Σελίδα 1 από 21 Γ Λυκείου Κατεύθυνσης Κεφάλαιο 1: Ηλεκτρονιακή δοµή του ατόµου Θέµατα Σωστού/Λάθους και Πολλαπλής επιλογής Πανελληνίων, ΟΕΦΕ, ΠΜ Χ Το 17Cl σχηµατίζει ενώσεις µε ένα µόνο
ΕΙΣΑΓΩΓΗ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Η ΔΟΜΗ ΠΙΝΑΚΑ I. ΠΕΡΙΟΧΕΣ ΟΜΑΔΕΣ - ΠΕΡΙΟΔΟΙ
 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Η ΔΟΜΗ ΠΙΝΑΚΑ I. ΠΕΡΙΟΧΕΣ ΟΜΑΔΕΣ - ΠΕΡΙΟΔΟΙ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Το 1868 ο Ρώσος χημικός Μεντελέγιεφ, στηριζόμενος σε μία παλαιότερη ιδέα των Τζων Νιούλαντς (John Newlands) και Μέγιερ
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Η ΔΟΜΗ ΠΙΝΑΚΑ I. ΠΕΡΙΟΧΕΣ ΟΜΑΔΕΣ - ΠΕΡΙΟΔΟΙ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Το 1868 ο Ρώσος χημικός Μεντελέγιεφ, στηριζόμενος σε μία παλαιότερη ιδέα των Τζων Νιούλαντς (John Newlands) και Μέγιερ
ΔΙΑΓΩΝΙΣΜΑ ΘΕΜΑΤΑ. a. Ο μέγιστος αριθμός ηλεκτρονίων σε ένα άτομο τα οποία χαρακτηρίζονται με n=2 και m l =0
 ΔΙΑΓΩΝΙΣΜΑ Μάθημα : ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΗΜ/ΝIΑ: 2-10-2011 Καθηγητής/τρια: Ονοματεπώνυμο: Χρόνος: Τμήμα: ΘΕΜΑ 1 0 Επιλέξτε το σωστό. ΘΕΜΑΤΑ a. Ο μέγιστος αριθμός ηλεκτρονίων σε ένα άτομο τα οποία χαρακτηρίζονται
ΔΙΑΓΩΝΙΣΜΑ Μάθημα : ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΗΜ/ΝIΑ: 2-10-2011 Καθηγητής/τρια: Ονοματεπώνυμο: Χρόνος: Τμήμα: ΘΕΜΑ 1 0 Επιλέξτε το σωστό. ΘΕΜΑΤΑ a. Ο μέγιστος αριθμός ηλεκτρονίων σε ένα άτομο τα οποία χαρακτηρίζονται
ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου. Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη
 Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου Α) Να επιλέξετε σε κάθε μία από τις παρακάτω προτάσεις τη σωστή απάντηση: 1. To στοιχείο που περιέχει
Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου Α) Να επιλέξετε σε κάθε μία από τις παρακάτω προτάσεις τη σωστή απάντηση: 1. To στοιχείο που περιέχει
Κβαντικοί αριθμοί. l =0 υποφλοιός S σφαίρα m l =0 ένα τροχιακό με σφαιρική συμμετρία
 Κβαντικοί αριθμοί Η θεωρία του Bohr χρειάζεται μόνο τον κύριο κβαντικό αριθμό η, για να καθορίσει ενέργεια για το άτομο του υδρογόνου Ε η =-2,18.10-18 /η 2 κυκλική τροχιά. και επιτρεπτή Στην κβαντομηχανική
Κβαντικοί αριθμοί Η θεωρία του Bohr χρειάζεται μόνο τον κύριο κβαντικό αριθμό η, για να καθορίσει ενέργεια για το άτομο του υδρογόνου Ε η =-2,18.10-18 /η 2 κυκλική τροχιά. και επιτρεπτή Στην κβαντομηχανική
Χημεία Γ Λυκείου Θετικής Κατεύθυνσης
 Χημεία Γ Λυκείου Θετικής Κατεύθυνσης Κεφάλαιο 1 Ηλεκτρονιακή δομή των ατόμων 1 Εισαγωγή Δομή του ατόμου Δημόκριτος Αριστοτέλης Dalton Thomson 400 π.χ. 350π.χ. 1808 1897 Απειροελάχιστα τεμάχια ύλης (τα
Χημεία Γ Λυκείου Θετικής Κατεύθυνσης Κεφάλαιο 1 Ηλεκτρονιακή δομή των ατόμων 1 Εισαγωγή Δομή του ατόμου Δημόκριτος Αριστοτέλης Dalton Thomson 400 π.χ. 350π.χ. 1808 1897 Απειροελάχιστα τεμάχια ύλης (τα
1.3 Δομή περιοδικού πίνακα (τομείς s, p, d, f) στοιχεία μετάπτωσης
 1.3 Δομή περιοδικού πίνακα (τομείς s, p, d, f) στοιχεία μετάπτωσης Τι γνωρίζουμε από τις προηγούμενες τάξεις για τον περιοδικό πίνακα 1. Τα χημικά στοιχεία τοποθετούνται στον περιοδικό πίνακα κατά σειρά
1.3 Δομή περιοδικού πίνακα (τομείς s, p, d, f) στοιχεία μετάπτωσης Τι γνωρίζουμε από τις προηγούμενες τάξεις για τον περιοδικό πίνακα 1. Τα χημικά στοιχεία τοποθετούνται στον περιοδικό πίνακα κατά σειρά
ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ. ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ 1 ου ΚΕΦΑΛΑΙΟΥ
 ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1 ο ΓΕΛ ΕΛΕΥΘΕΡΙΟΥ-ΚΟΡΔΕΛΙΟΥ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ 1 ου ΚΕΦΑΛΑΙΟΥ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: 1 2 1. ΣΩΣΤΟ (Σ) ή ΛΑΘΟΣ (Λ); Αιτιολογήστε σύντομα. 1.1 Ένα ηλεκτρόνιο σθένους του ατόμου
ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1 ο ΓΕΛ ΕΛΕΥΘΕΡΙΟΥ-ΚΟΡΔΕΛΙΟΥ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ 1 ου ΚΕΦΑΛΑΙΟΥ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: 1 2 1. ΣΩΣΤΟ (Σ) ή ΛΑΘΟΣ (Λ); Αιτιολογήστε σύντομα. 1.1 Ένα ηλεκτρόνιο σθένους του ατόμου
ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΑ ΑΤΟΜΑ ΣΥΝΟΠΤΙΚΗ ΘΕΩΡΙΑ
 4Α ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΑ ΑΤΟΜΑ ΣΥΝΟΠΤΙΚΗ ΘΕΩΡΙΑ Σύνοψη Στο Α μέρος του κεφαλαίου καταγράφονται οι παράγοντες που καθορίζουν την ενέργεια των τροχιακών των πολυηλεκτρονιακών ατόμων. Δίνονται οι κανόνες που καθορίζουν
4Α ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΑ ΑΤΟΜΑ ΣΥΝΟΠΤΙΚΗ ΘΕΩΡΙΑ Σύνοψη Στο Α μέρος του κεφαλαίου καταγράφονται οι παράγοντες που καθορίζουν την ενέργεια των τροχιακών των πολυηλεκτρονιακών ατόμων. Δίνονται οι κανόνες που καθορίζουν
Κβαντική θεωρία και ηλεκτρονιακή δομή των ατόμων
 Κβαντική θεωρία και ηλεκτρονιακή δομή των ατόμων Κβαντικοί αριθμοί Κύριος κβαντικός αριθμός (n) Αζιμουθιακός κβαντικός αριθμός (l) Μαγνητικός κβαντικός αριθμός (ml) Στροφορμή (Spin) ηλεκτρονίου κβαντικός
Κβαντική θεωρία και ηλεκτρονιακή δομή των ατόμων Κβαντικοί αριθμοί Κύριος κβαντικός αριθμός (n) Αζιμουθιακός κβαντικός αριθμός (l) Μαγνητικός κβαντικός αριθμός (ml) Στροφορμή (Spin) ηλεκτρονίου κβαντικός
ΕΙΣΑΓΩΓΗ ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Η ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ IV. ΟΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ ΚΑΙ ΤΑ ΤΡΟΧΙΑΚΑ
 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Η ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ IV. ΟΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ ΚΑΙ ΤΑ ΤΡΟΧΙΑΚΑ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Στο ατομικό πρότυπο του Bohr ο κύριος κβαντικός αριθμός (n) εισάγεται αυθαίρετα, για τον καθορισμό
ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Η ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ IV. ΟΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ ΚΑΙ ΤΑ ΤΡΟΧΙΑΚΑ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Στο ατομικό πρότυπο του Bohr ο κύριος κβαντικός αριθμός (n) εισάγεται αυθαίρετα, για τον καθορισμό
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ 1 ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ
 ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
Εξαιρέσεις στις ηλεκτρονιακές διαμορφώσεις
 Εξαιρέσεις στις ηλεκτρονιακές διαμορφώσεις Ακολουθώντας τους κανόνες δόμησης των πολυηλεκτρονιακών ατόμων που αναπτύχθηκαν παραπάνω, θα διαπιστώσουμε ότι σε ορισμένες περιπτώσεις παρατηρούνται αποκλίσεις
Εξαιρέσεις στις ηλεκτρονιακές διαμορφώσεις Ακολουθώντας τους κανόνες δόμησης των πολυηλεκτρονιακών ατόμων που αναπτύχθηκαν παραπάνω, θα διαπιστώσουμε ότι σε ορισμένες περιπτώσεις παρατηρούνται αποκλίσεις
Κεφάλαιο 8. Ηλεκτρονικές Διατάξεις και Περιοδικό Σύστημα
 Κεφάλαιο 8 Ηλεκτρονικές Διατάξεις και Περιοδικό Σύστημα Αρχές δόμησης πολυηλεκτρονικών ατόμων Η ηλεκτρονική (ή ηλεκτρονιακή) δομή ενός ατόμου είναι η κατανομή των ηλεκτρονίων στους υποφλοιούς (ο υποφλοιός
Κεφάλαιο 8 Ηλεκτρονικές Διατάξεις και Περιοδικό Σύστημα Αρχές δόμησης πολυηλεκτρονικών ατόμων Η ηλεκτρονική (ή ηλεκτρονιακή) δομή ενός ατόμου είναι η κατανομή των ηλεκτρονίων στους υποφλοιούς (ο υποφλοιός
τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n, l)
 ΑΤΟΜΙΚΑ ΤΡΟΧΙΑΚΑ Σχέση κβαντικών αριθµών µε στιβάδες υποστιβάδες - τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n,
ΑΤΟΜΙΚΑ ΤΡΟΧΙΑΚΑ Σχέση κβαντικών αριθµών µε στιβάδες υποστιβάδες - τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n,
ΑΣΚΗΣΕΙΣ ΣΤΟ 1ο ΚΕΦΑΛΑΙΟ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ
 ΑΣΚΗΣΕΙΣ ΣΤΟ 1ο ΚΕΦΑΛΑΙΟ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ 1.1. ΤΡΟΧΙΑΚΑ ΚΑΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ 1.1. Ποιες είναι οι πιθανές τιµές : α) του l για : i) n = 1, ii) n = 3, β) του m l για : i) n = 2, ii) l = 2. 1.2. Να βρείτε
ΑΣΚΗΣΕΙΣ ΣΤΟ 1ο ΚΕΦΑΛΑΙΟ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ 1.1. ΤΡΟΧΙΑΚΑ ΚΑΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ 1.1. Ποιες είναι οι πιθανές τιµές : α) του l για : i) n = 1, ii) n = 3, β) του m l για : i) n = 2, ii) l = 2. 1.2. Να βρείτε
) σχηματίζονται : α. Ένας σ και δύο π δεσμοί β. Τρεις σ δεσμοί γ. Ένας π και δύο σ δεσμοί δ. Τρεις π δεσμοί.
 ΘΕΜΑΤΑ Θγ 1 0 ΚΕΦΑΛΑΙΟ 1.1. Σε ένα πολυηλεκτρονιακό άτομο ο μέγιστος αριθμός ηλεκτρονίων με κβαντικούς αριθμούς n= και m s = -½ είναι : α. οκτώ β. τέσσερα γ. δύο δ. ένα 1.. Από τα επόμενα χημικά στοιχεία
ΘΕΜΑΤΑ Θγ 1 0 ΚΕΦΑΛΑΙΟ 1.1. Σε ένα πολυηλεκτρονιακό άτομο ο μέγιστος αριθμός ηλεκτρονίων με κβαντικούς αριθμούς n= και m s = -½ είναι : α. οκτώ β. τέσσερα γ. δύο δ. ένα 1.. Από τα επόμενα χημικά στοιχεία
Ασκήσεις. 5Β: 1s 2 2s 2 2p 2, β) 10 Νe: 1s 2 2s 2 2p 4 3s 2, γ) 19 Κ: 1s 2 2s 2 2p 6 3s 2 3p 6,
 Ασκήσεις 1. Να γίνει η ηλεκτρονιακή δόμηση για τα ακόλουθα άτομα στη θεμελιώδη τους κατάσταση: 29Cu, 33As, 38Sr, 42Mo, 55Cs. Πόσα ηλεκτρόνια έχει η εξωτερική τους στιβάδα και πόσα ασύζευκτα ηλεκτρόνια
Ασκήσεις 1. Να γίνει η ηλεκτρονιακή δόμηση για τα ακόλουθα άτομα στη θεμελιώδη τους κατάσταση: 29Cu, 33As, 38Sr, 42Mo, 55Cs. Πόσα ηλεκτρόνια έχει η εξωτερική τους στιβάδα και πόσα ασύζευκτα ηλεκτρόνια
Κβαντικοί αριθμοί τρεις κβαντικοί αριθμοί
 Κβαντικοί αριθμοί Στην κβαντομηχανική εισάγονται τρεις κβαντικοί αριθμοί για τον καθορισμό της κατανομής του ηλεκτρονιακού νέφους (ατομικού τροχιακού). Οι κβαντικοί αυτοί αριθμοί προκύπτουν από την επίλυση
Κβαντικοί αριθμοί Στην κβαντομηχανική εισάγονται τρεις κβαντικοί αριθμοί για τον καθορισμό της κατανομής του ηλεκτρονιακού νέφους (ατομικού τροχιακού). Οι κβαντικοί αυτοί αριθμοί προκύπτουν από την επίλυση
Μετά το τέλος της µελέτης του 1ου κεφαλαίου, ο µαθητής θα πρέπει να είναι σε θέση:
 Μετά το τέλος της µελέτης του 1ου κεφαλαίου, ο µαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει το ατοµικό πρότυπο του Bohr καθώς και τα µειονεκτήµατά του. Να υπολογίζει την ενέργεια που εκπέµπεται ή απορροφάται
Μετά το τέλος της µελέτης του 1ου κεφαλαίου, ο µαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει το ατοµικό πρότυπο του Bohr καθώς και τα µειονεκτήµατά του. Να υπολογίζει την ενέργεια που εκπέµπεται ή απορροφάται
Μάθημα 11ο. Ηλεκτρονιακή διαμόρφωση Πολυηλεκτρονιακών ατόμων-b
 Μάθημα 11ο Ηλεκτρονιακή διαμόρφωση Πολυηλεκτρονιακών ατόμων-b Παράδειγμα εφαρμογής κανόνα Slater Να επιβεβαιωθεί ότι η πειραματικά επιβεβαιωμένη ηλεκτρονιακή διαμόρφωση του Κ: 1s 2 2s 2 2p 6 3s 2 3p 6
Μάθημα 11ο Ηλεκτρονιακή διαμόρφωση Πολυηλεκτρονιακών ατόμων-b Παράδειγμα εφαρμογής κανόνα Slater Να επιβεβαιωθεί ότι η πειραματικά επιβεβαιωμένη ηλεκτρονιακή διαμόρφωση του Κ: 1s 2 2s 2 2p 6 3s 2 3p 6
Χηµεία Θετικής Κατεύθυνσης
 Χηµεία Θετικής Κατεύθυνσης Γ Λυκείου 1 ο Κεφάλαιο Ηλεκτρονιακή δοµή των ατόµων Περιοδικός πίνακας Ηλεκτρονιακοί τύποι Lewis kostasctheos@yahoo.gr 1 1 ο παράδειγµα Πως υπολογίζουµε τη συχνότητα και το µήκος
Χηµεία Θετικής Κατεύθυνσης Γ Λυκείου 1 ο Κεφάλαιο Ηλεκτρονιακή δοµή των ατόµων Περιοδικός πίνακας Ηλεκτρονιακοί τύποι Lewis kostasctheos@yahoo.gr 1 1 ο παράδειγµα Πως υπολογίζουµε τη συχνότητα και το µήκος
Διάλεξη 6: Ατομική Δομή Συμμετρία Εναλλαγής
 Συμμετρία Εναλλαγής Σε μονοηλεκτρονιακά άτομα ιόντα η κατάσταση του ηλεκτρονίου καθορίζεται από τέσσερις κβαντικούς αριθμούς {n, l, m l, m s } ή {n, l, j, m j }. Σε πολυηλεκτρονιακά άτομα πόσα ηλεκτρόνια
Συμμετρία Εναλλαγής Σε μονοηλεκτρονιακά άτομα ιόντα η κατάσταση του ηλεκτρονίου καθορίζεται από τέσσερις κβαντικούς αριθμούς {n, l, m l, m s } ή {n, l, j, m j }. Σε πολυηλεκτρονιακά άτομα πόσα ηλεκτρόνια
ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 1 ΚΕΦ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ
 ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 1 ΚΕΦ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ Α θεωρία Bohr-σύγχρονη ατομική θεωρία Β περιοδικός πίνακας Γ ηλεκτρονικοί τύποι Δ υβριδικά τροχιακά- μοριακά τροχιακά Α θεωρία Bohr-σύγχρονη ατομική θεωρία Α1. Να
ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 1 ΚΕΦ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ Α θεωρία Bohr-σύγχρονη ατομική θεωρία Β περιοδικός πίνακας Γ ηλεκτρονικοί τύποι Δ υβριδικά τροχιακά- μοριακά τροχιακά Α θεωρία Bohr-σύγχρονη ατομική θεωρία Α1. Να
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Ερωτήσεις από πανελλήνιες εξετάσεις από το 2001 ως το 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ.
ΚΕΦΑΛΑΙΟ 1 ο Ερωτήσεις από πανελλήνιες εξετάσεις από το 2001 ως το 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ.
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΟ 1 Ο : ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΚΑΙ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΚΕΦΑΛΑΙΟ 3 Ο : ΙΟΝΤΙΚΗ ΙΣΟΡΡΟΠΙΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΒΑΘΜΟΣ :. % Θέμα 1 Ο 1. Ατομικό τροχιακό είναι
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΟ 1 Ο : ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΚΑΙ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΚΕΦΑΛΑΙΟ 3 Ο : ΙΟΝΤΙΚΗ ΙΣΟΡΡΟΠΙΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΒΑΘΜΟΣ :. % Θέμα 1 Ο 1. Ατομικό τροχιακό είναι
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Γιώργος Καντώνης
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 02 11-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Γιώργος Καντώνης ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α A1. Tα τροχιακά 2p και 2p y ενός ατόμου διαφέρουν:
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 02 11-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Γιώργος Καντώνης ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α A1. Tα τροχιακά 2p και 2p y ενός ατόμου διαφέρουν:
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 03 / 11 /2013
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 03 / 11 /2013 ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 03 / 11 /2013 ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΣΗΜΕΙΩΣΕΙΣ ΚΕΦΑΛΑΙΟΥ 1 ΣΤΗ ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟ ΚΕΦΑΙΛΑΙΟ 1. Α) Μηχανική συνθήκη ( βελάκι σελ 3) Β) Οπτική συνθήκη (1 ο βελάκι σελ 4 )
 ΣΗΜΕΙΩΣΕΙΣ ΚΕΦΑΛΑΙΟΥ 1 ΣΤΗ ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟ ΚΕΦΑΙΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚOΣ ΠΙΝΑΚΑΣ 1)Ατομικό πρότυπο του Bohr ( πυρήνας,..., περιστρεφόμενα ηλεκτρόνια) περιγράφεται
ΣΗΜΕΙΩΣΕΙΣ ΚΕΦΑΛΑΙΟΥ 1 ΣΤΗ ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟ ΚΕΦΑΙΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚOΣ ΠΙΝΑΚΑΣ 1)Ατομικό πρότυπο του Bohr ( πυρήνας,..., περιστρεφόμενα ηλεκτρόνια) περιγράφεται
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Σύγxρονη Φυσική II. Ατομική Δομή ΙΙΙ Διδάσκων : Επίκ. Καθ. Μ. Μπενής
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Ατομική Δομή ΙΙΙ Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Cetive Commons.
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Ατομική Δομή ΙΙΙ Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Cetive Commons.
Λύνουµε περισσότερες ασκήσεις
 Χηµεία Γ Λυκείου - Θετικής Κατεύθυνσης Βήµα 3 ο Λύνουµε περισσότερες ασκήσεις 17. Λύνουµε περισσότερες ασκήσεις 1. Ηλεκτρόνιο ατόµου του υδρογόνου που βρίσκεται στη θεµελιώδη κατάσταση απορροφά ένα φωτόνιο
Χηµεία Γ Λυκείου - Θετικής Κατεύθυνσης Βήµα 3 ο Λύνουµε περισσότερες ασκήσεις 17. Λύνουµε περισσότερες ασκήσεις 1. Ηλεκτρόνιο ατόµου του υδρογόνου που βρίσκεται στη θεµελιώδη κατάσταση απορροφά ένα φωτόνιο
Ζαχαριάδου Φωτεινή Σελίδα 1 από 9
 Ζαχαριάδου Φωτεινή Σελίδα 1 από 9 Χηµεία Γ Λυκείου - Κεφάλαιο 1: Ηλεκτρονιακή δοµή των ατόµων Ενέργεια που µεταφέρει ένα φωτόνιο: Ε φωτονίου = h f f: συχνότητα φωτονίου h: σταθερά του Planck Ενέργεια ηλεκτρονίου:
Ζαχαριάδου Φωτεινή Σελίδα 1 από 9 Χηµεία Γ Λυκείου - Κεφάλαιο 1: Ηλεκτρονιακή δοµή των ατόµων Ενέργεια που µεταφέρει ένα φωτόνιο: Ε φωτονίου = h f f: συχνότητα φωτονίου h: σταθερά του Planck Ενέργεια ηλεκτρονίου:
A.3 Ποια από τις παρακάτω ηλεκτρονιακές δομές παραβιάζει την αρχή του Pauli:
 Θέμα Α ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ A.1 Να διατυπώσετε την 1 η συνθήκη του Bohr για το ατομικό μοντέλο (μηχανική συνθήκη). (5 μονάδες) A.2 Να διατυπώσετε την 2 η συνθήκη του Bohr για το
Θέμα Α ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ A.1 Να διατυπώσετε την 1 η συνθήκη του Bohr για το ατομικό μοντέλο (μηχανική συνθήκη). (5 μονάδες) A.2 Να διατυπώσετε την 2 η συνθήκη του Bohr για το
Χημεία Γ Λυκείου Διαγώνισμα 2 ο 1 ο Κεφ. :μέχρι και περιοδικός πίνακας. 5 ο Κεφ. : μέχρι και απόσπαση. Θέμα 1 ο
 Χημεία Γ Λυκείου Διαγώνισμα ο 1 ο Κεφ. :μέχρι και περιοδικός πίνακας. 5 ο Κεφ. : μέχρι και απόσπαση. Θέμα 1 ο Σημειώστε πάνω στα θέματα την σωστή απάντηση στις ερωτήσεις 1.1 έως 1.6 1.1. Η ηλεκτρονιακή
Χημεία Γ Λυκείου Διαγώνισμα ο 1 ο Κεφ. :μέχρι και περιοδικός πίνακας. 5 ο Κεφ. : μέχρι και απόσπαση. Θέμα 1 ο Σημειώστε πάνω στα θέματα την σωστή απάντηση στις ερωτήσεις 1.1 έως 1.6 1.1. Η ηλεκτρονιακή
Χημεία Γ Λυκείου Διαγώνισμα 1 ο 1 ο Κεφ. :μέχρι και περιοδικός πίνακας. 5 ο Κεφ. : μέχρι και απόσπαση. Θέμα 1 ο
 Χημεία Γ Λυκείου Διαγώνισμα 1 ο 1 ο Κεφ. :μέχρι και περιοδικός πίνακας. 5 ο Κεφ. : μέχρι και απόσπαση. Θέμα 1 ο Σημειώστε πάνω στα θέματα την σωστή απάντηση στις ερωτήσεις 1.1 έως 1.5 1.1. Κατά τις μεταπτώσεις:
Χημεία Γ Λυκείου Διαγώνισμα 1 ο 1 ο Κεφ. :μέχρι και περιοδικός πίνακας. 5 ο Κεφ. : μέχρι και απόσπαση. Θέμα 1 ο Σημειώστε πάνω στα θέματα την σωστή απάντηση στις ερωτήσεις 1.1 έως 1.5 1.1. Κατά τις μεταπτώσεις:
ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ Ο ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ
 ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ Ο ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Θέμα 1 ο 1. Η θεωρία De Brooglie υποστήριξε: i. Ότι το φως έχει σωματιδιακή φύση. ii. Ότι είναι αδύνατον να προσδιοριστούν ταυτόχρονα η
ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ Ο ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Θέμα 1 ο 1. Η θεωρία De Brooglie υποστήριξε: i. Ότι το φως έχει σωματιδιακή φύση. ii. Ότι είναι αδύνατον να προσδιοριστούν ταυτόχρονα η
Ατομικά τροχιακά. Γνωστικό αντικείμενο: Χημεία. Δημιουργός: Αριστοτέλης Λεβεντέας
 Ατομικά τροχιακά Επαρκές Σενάριο Γνωστικό αντικείμενο: Χημεία Δημιουργός: Αριστοτέλης Λεβεντέας ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ, ΕΡΕΥΝΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ Σημείωση Το παρόν έγγραφο
Ατομικά τροχιακά Επαρκές Σενάριο Γνωστικό αντικείμενο: Χημεία Δημιουργός: Αριστοτέλης Λεβεντέας ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ, ΕΡΕΥΝΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ Σημείωση Το παρόν έγγραφο
Ατομικά τροχιακά. Γνωστικό αντικείμενο: Χημεία. Δημιουργός: Αριστοτέλης Λεβεντέας
 Ατομικά τροχιακά Επαρκές Σενάριο Γνωστικό αντικείμενο: Χημεία Δημιουργός: Αριστοτέλης Λεβεντέας ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ, ΕΡΕΥΝΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ Σημείωση Το παρόν έγγραφο
Ατομικά τροχιακά Επαρκές Σενάριο Γνωστικό αντικείμενο: Χημεία Δημιουργός: Αριστοτέλης Λεβεντέας ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ, ΕΡΕΥΝΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ Σημείωση Το παρόν έγγραφο
Ατομικά τροχιακά. Γνωστικό αντικείμενο: Χημεία. Δημιουργός: Αριστοτέλης Λεβεντέας
 Ατομικά τροχιακά Επαρκές Σενάριο Γνωστικό αντικείμενο: Χημεία Δημιουργός: Αριστοτέλης Λεβεντέας ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ, ΕΡΕΥΝΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ Σημείωση Το παρόν έγγραφο
Ατομικά τροχιακά Επαρκές Σενάριο Γνωστικό αντικείμενο: Χημεία Δημιουργός: Αριστοτέλης Λεβεντέας ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ, ΕΡΕΥΝΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ Σημείωση Το παρόν έγγραφο
Μαγνητικές ιδιότητες Υλικών με βαση τις αντίστοιχες των στοιχείων
 Μαγνητικές ιδιότητες Υλικών με βαση τις αντίστοιχες των στοιχείων Τα υλικά ανάλογα με τη μαγνητική τους συμπεριφορά διακρίνονται σε: 1. ιαμαγνητικά που δεν διαθέτουν μαγνητικά άτομα, δηλαδή άτομα με μονήρη
Μαγνητικές ιδιότητες Υλικών με βαση τις αντίστοιχες των στοιχείων Τα υλικά ανάλογα με τη μαγνητική τους συμπεριφορά διακρίνονται σε: 1. ιαμαγνητικά που δεν διαθέτουν μαγνητικά άτομα, δηλαδή άτομα με μονήρη
ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ
 ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ 1.1 Ερωτήσεις πολλαπλής επιλογής Στις ερωτήσεις 1-54 βάλτε σε ένα κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Η θεωρία των κβάντα:
ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ 1.1 Ερωτήσεις πολλαπλής επιλογής Στις ερωτήσεις 1-54 βάλτε σε ένα κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Η θεωρία των κβάντα:
Δομή ενεργειακών ζωνών
 Ατομικό πρότυπο του Bohr Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Βασικές αρχές του προτύπου Bohr Θετικά φορτισμένος
Ατομικό πρότυπο του Bohr Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Βασικές αρχές του προτύπου Bohr Θετικά φορτισμένος
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Γενική & Ανόργανη Χημεία
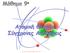 Το άτομο του υδρογόνου Προκειμένου να ευρεθούν οι τιμές της ενέργειας και οι ενεργειακές στάθμες για το ηλεκτρόνιο στο άτομο του υδρογόνου, είναι απαραίτητο να λυθεί η κατάλληλη εξίσωση Schrödinger. Για
Το άτομο του υδρογόνου Προκειμένου να ευρεθούν οι τιμές της ενέργειας και οι ενεργειακές στάθμες για το ηλεκτρόνιο στο άτομο του υδρογόνου, είναι απαραίτητο να λυθεί η κατάλληλη εξίσωση Schrödinger. Για
ΙΑΓΩΝΙΣΜΑ ΣΤΗ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΕΠΩΝΥΜΟ:... ΟΝΟΜΑ:... ΤΜΗΜΑ:... ΤΣΙΜΙΣΚΗ &ΚΑΡΟΛΟΥ ΝΤΗΛ ΓΩΝΙΑ THΛ: 270727 222594 ΑΡΤΑΚΗΣ 12 Κ. ΤΟΥΜΠΑ THΛ: 919113 949422 ΗΜΕΡΟΜΗΝΙΑ:... ΙΑΓΩΝΙΣΜΑ ΣΤΗ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΖΗΤΗΜΑ 1 Ο : Μονάδες
ΕΠΩΝΥΜΟ:... ΟΝΟΜΑ:... ΤΜΗΜΑ:... ΤΣΙΜΙΣΚΗ &ΚΑΡΟΛΟΥ ΝΤΗΛ ΓΩΝΙΑ THΛ: 270727 222594 ΑΡΤΑΚΗΣ 12 Κ. ΤΟΥΜΠΑ THΛ: 919113 949422 ΗΜΕΡΟΜΗΝΙΑ:... ΙΑΓΩΝΙΣΜΑ ΣΤΗ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΖΗΤΗΜΑ 1 Ο : Μονάδες
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις
 1 ο Κεφάλαιο Χημείας Θετικής Κατεύθυνσης Γ Λυκείου 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις 1. Η εξίσωση E = h v μας δίνει την ενέργεια μιας ηλεκτρομαγνητικής ακτινοβολίας 2. H κβαντική
1 ο Κεφάλαιο Χημείας Θετικής Κατεύθυνσης Γ Λυκείου 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις 1. Η εξίσωση E = h v μας δίνει την ενέργεια μιας ηλεκτρομαγνητικής ακτινοβολίας 2. H κβαντική
1.3 Δομή περιοδικού πίνακα (τομείς s, p, d, f) - στοιχεία μετάπτωσης
 1.3 Δομή περιοδικού πίνακα (τομείς s, p, d, f) - στοιχεία μετάπτωσης 1. Ερώτηση: Τι λέει ο νόμος περιοδικότητας του Moseley; «H χημική συμπεριφορά των στοιχείων είναι περιοδική συνάρτηση του ατομικού τους
1.3 Δομή περιοδικού πίνακα (τομείς s, p, d, f) - στοιχεία μετάπτωσης 1. Ερώτηση: Τι λέει ο νόμος περιοδικότητας του Moseley; «H χημική συμπεριφορά των στοιχείων είναι περιοδική συνάρτηση του ατομικού τους
Ατομικός αριθμός = Αριθμός πρωτονίων. Μαζικός αριθμός = Αριθμός πρωτονίων + Αριθμός νετρονίων (nucleon number)
 Δομή Ατόμου και Ατομικά Τροχιακά Ατομικός και μαζικός αριθμός Ατομικός αριθμός = Αριθμός πρωτονίων (proton number) Μαζικός αριθμός = Αριθμός πρωτονίων + Αριθμός νετρονίων (nucleon number) 2 Ισότοπα Ισοβαρή
Δομή Ατόμου και Ατομικά Τροχιακά Ατομικός και μαζικός αριθμός Ατομικός αριθμός = Αριθμός πρωτονίων (proton number) Μαζικός αριθμός = Αριθμός πρωτονίων + Αριθμός νετρονίων (nucleon number) 2 Ισότοπα Ισοβαρή
ΦΥΣΙΚΟΧΗΜΕΙΑ I Ασκήσεις
 ΦΥΣΙΚΟΧΗΜΕΙΑ I Ασκήσεις Ενότητα 9 Πολυηλεκτρονιακά Άτομα Δημήτρης Κονταρίδης Αναπληρωτής Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Άσκηση 1 Να προσδιοριστούν τα επίπεδα, τα οποία μπορεί να προκύψουν
ΦΥΣΙΚΟΧΗΜΕΙΑ I Ασκήσεις Ενότητα 9 Πολυηλεκτρονιακά Άτομα Δημήτρης Κονταρίδης Αναπληρωτής Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Άσκηση 1 Να προσδιοριστούν τα επίπεδα, τα οποία μπορεί να προκύψουν
H εικόνα του ατόμου έχει αλλάξει δραστικά
 Δομή Ατόμου και Ατομικά Τροχιακά Α Τα κλασσικά πρότυπα Η ιστορία της δομής του ατόμου (1/2) ατομική θεωρία Δημόκριτου (άτομοι) ατομική θεωρία Dalton Πλανητικό πρότυπο Rutherford πρότυπο Schrodinger 460
Δομή Ατόμου και Ατομικά Τροχιακά Α Τα κλασσικά πρότυπα Η ιστορία της δομής του ατόμου (1/2) ατομική θεωρία Δημόκριτου (άτομοι) ατομική θεωρία Dalton Πλανητικό πρότυπο Rutherford πρότυπο Schrodinger 460
Σημειώστε τη σωστή απάντηση στις ερωτήσεις 1.1 έως 1.7
 Διαγώνισμα Χημείας Γ Λυκείου. 1 ο Κεφάλαιο: μέχρι και Περιοδικός Πίνακας 5 ο Κεφάλαιο: μέχρι και αντιδράσεις Απόσπασης. Θέμα 1 ο... Σημειώστε τη σωστή απάντηση στις ερωτήσεις 1.1 έως 1.7 1.1. Κατά τη μετάπτωση
Διαγώνισμα Χημείας Γ Λυκείου. 1 ο Κεφάλαιο: μέχρι και Περιοδικός Πίνακας 5 ο Κεφάλαιο: μέχρι και αντιδράσεις Απόσπασης. Θέμα 1 ο... Σημειώστε τη σωστή απάντηση στις ερωτήσεις 1.1 έως 1.7 1.1. Κατά τη μετάπτωση
ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ
 ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ EΠIMEΛEIA BAMNIEΣ ΔHMHTΡHΣ 1.1 Ερωτήσεις πολλαπλής επιλογής Στις ερωτήσεις 1-54 βάλτε σε ένα κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση.
ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ EΠIMEΛEIA BAMNIEΣ ΔHMHTΡHΣ 1.1 Ερωτήσεις πολλαπλής επιλογής Στις ερωτήσεις 1-54 βάλτε σε ένα κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση.
Γεωργίου Κομελίδη. Χημεία Γ Λυκείου Θετικής Ηλεκτρονιακή δομή - Περιοδικός πίνακας - Δομές Lewis
 Γεωργίου Κομελίδη Χημεία Γ Λυκείου Θετικής Ηλεκτρονιακή δομή - Περιοδικός πίνακας - Δομές Lewis komelidis 1/8/2013 Ατομικό πρότυπο του Βοhr: Το 1913 ο Δανός Φυσικός Νιλς Μπορ (Niels Bohr) για να εξηγήσει
Γεωργίου Κομελίδη Χημεία Γ Λυκείου Θετικής Ηλεκτρονιακή δομή - Περιοδικός πίνακας - Δομές Lewis komelidis 1/8/2013 Ατομικό πρότυπο του Βοhr: Το 1913 ο Δανός Φυσικός Νιλς Μπορ (Niels Bohr) για να εξηγήσει
ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ. Ενότητα 1: ΑΤΟΜΑ ΚΑΙ ΔΕΣΜΟΙ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 1: ΑΤΟΜΑ ΚΑΙ ΔΕΣΜΟΙ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 1: ΑΤΟΜΑ ΚΑΙ ΔΕΣΜΟΙ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ
 ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: 01 / 06 /2012 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1. γ ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ Α2. β Α3. β Α4. γ Α5. α. Η απαγορευτική
ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: 01 / 06 /2012 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1. γ ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ Α2. β Α3. β Α4. γ Α5. α. Η απαγορευτική
ΤΕΤΡΑΚΤΥΣ ΦΡΟΝΤΙΣΤΗΡΙΟ ΜΕΣΗΣ ΕΚΠΑΙ ΕΥΣΗΣ Αµυραδάκη 20, Νίκαια ( ) ΘΕΜΑ 1 Ο. 1. Να σηµειώσετε κάτω από κάθε ουσία - σώµα τη λέξη οξύ ή βάση.
 ΜΑΘΗΜΑ...ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ... ΘΕΜΑ 1 Ο ΙΑΝΟΥΑΡΙΟΣ 2012 1. Να σηµειώσετε κάτω από κάθε ουσία - σώµα τη λέξη οξύ ή βάση. NH + HCl NH + Cl + 3 4 H 0+ HCOOH H + HCOO + 2 3 NH + H O NH + H O + + 4 2 3 3 HPO
ΜΑΘΗΜΑ...ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ... ΘΕΜΑ 1 Ο ΙΑΝΟΥΑΡΙΟΣ 2012 1. Να σηµειώσετε κάτω από κάθε ουσία - σώµα τη λέξη οξύ ή βάση. NH + HCl NH + Cl + 3 4 H 0+ HCOOH H + HCOO + 2 3 NH + H O NH + H O + + 4 2 3 3 HPO
Όνομα & Επώνυμο: Ημερομηνία: ΒΑΘΜΟΣ: /100, /20. Διαγώνισμα (2019) στη Χημεία Γ Λυκείου - Ομάδας Προσανατολισμού Θετικών Σπουδών στο Κεφάλαιο 6
 Σελίδα: 1 Επαναληπτικό Διαγώνισμα στη Χημεία Γ Λυκείου στο Κεφάλαιο (19) Διαγώνισμα (19) στη Χημεία Γ Λυκείου - Ομάδας Προσανατολισμού Θετικών Σπουδών στο Κεφάλαιο Όνομα & Επώνυμο: Ημερομηνία: ΒΑΘΜΟΣ:
Σελίδα: 1 Επαναληπτικό Διαγώνισμα στη Χημεία Γ Λυκείου στο Κεφάλαιο (19) Διαγώνισμα (19) στη Χημεία Γ Λυκείου - Ομάδας Προσανατολισμού Θετικών Σπουδών στο Κεφάλαιο Όνομα & Επώνυμο: Ημερομηνία: ΒΑΘΜΟΣ:
Περιοδικό Σύστημα Ιστορική Εξέλιξη
 Περιοδικό Σύστημα Ιστορική Εξέλιξη Newlands (1864): ταξινόμηση στοιχείων κατά αύξουσα ατομική μάζα και σε οκτάβες H Li Be B C N O F Na Mg Al Si P S Cl K Ca Cr Ti Mn Fe Meyer (1865): σχέση ιδιοτήτων και
Περιοδικό Σύστημα Ιστορική Εξέλιξη Newlands (1864): ταξινόμηση στοιχείων κατά αύξουσα ατομική μάζα και σε οκτάβες H Li Be B C N O F Na Mg Al Si P S Cl K Ca Cr Ti Mn Fe Meyer (1865): σχέση ιδιοτήτων και
κυματικής συνάρτησης (Ψ) κυματική συνάρτηση
 Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Μάθημα 10 ο. Ο Περιοδικός Πίνακας και ο Νόμος της Περιοδικότητας. Μέγεθος ατόμων Ενέργεια Ιοντισμού Ηλεκτρονιακή συγγένεια Ηλεκτραρνητικότητα
 Μάθημα 10 ο Ο Περιοδικός Πίνακας και ο Νόμος της Περιοδικότητας Μέγεθος ατόμων Ενέργεια Ιοντισμού Ηλεκτρονιακή συγγένεια Ηλεκτραρνητικότητα Σχέση σειράς συμπλήρωσης τροχιακών και ΠΠ Μνημονικός κανόνας
Μάθημα 10 ο Ο Περιοδικός Πίνακας και ο Νόμος της Περιοδικότητας Μέγεθος ατόμων Ενέργεια Ιοντισμού Ηλεκτρονιακή συγγένεια Ηλεκτραρνητικότητα Σχέση σειράς συμπλήρωσης τροχιακών και ΠΠ Μνημονικός κανόνας
ΗΛΕΚΤΡΟΝΙΚΗ ΔΟΜΗ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ
 1ο ο ΚΕΦΑΛΑΙΟ ΗΛΕΚΤΡΟΝΙΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Σημαντικοί σταθμοί στην εξέλιξη της γνώσης για τη δομή του ατόμου ανακάλυψη e μηχανική μητρών - ατομική θεωρία Δημόκριτου ~450 π.χ ατομικό
1ο ο ΚΕΦΑΛΑΙΟ ΗΛΕΚΤΡΟΝΙΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Σημαντικοί σταθμοί στην εξέλιξη της γνώσης για τη δομή του ατόμου ανακάλυψη e μηχανική μητρών - ατομική θεωρία Δημόκριτου ~450 π.χ ατομικό
Κβαντομηχανική εικόνα του ατομικού μοντέλου
 Κβαντομηχανική εικόνα του ατομικού μοντέλου 1. Ερώτηση: Τι είναι η κβαντομηχανική; H κβαντομηχανική, είναι η σύγχρονη αντίληψη μιας νέας μηχανικής που μπορεί να εφαρμοστεί στο μικρόκοσμο του ατόμου. Σήμερα
Κβαντομηχανική εικόνα του ατομικού μοντέλου 1. Ερώτηση: Τι είναι η κβαντομηχανική; H κβαντομηχανική, είναι η σύγχρονη αντίληψη μιας νέας μηχανικής που μπορεί να εφαρμοστεί στο μικρόκοσμο του ατόμου. Σήμερα
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
3 o. Περιοδικός πίνακας Μεταβολή ορισµένων περιοδικών ιδιοτήτων ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ 59.
 Περιοδικός πίνακας - Μεταβολή ορισµένων περιοδικών ιδιοτήτων 59. 3 o Περιοδικός πίνακας Μεταβολή ορισµένων περιοδικών ιδιοτήτων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Περιοδικός πίνακας: Σύµφωνα µε τον νόµο περιοδικότητας
Περιοδικός πίνακας - Μεταβολή ορισµένων περιοδικών ιδιοτήτων 59. 3 o Περιοδικός πίνακας Μεταβολή ορισµένων περιοδικών ιδιοτήτων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Περιοδικός πίνακας: Σύµφωνα µε τον νόµο περιοδικότητας
2.Η τελευταία στιβάδα οποιουδήποτε ατόμου δεν μπορεί να έχει περισσότερα από 8 ηλεκτρόνια. Εκτός αν είναι η Κ που συμπληρώνεται με 2 ηλεκτρόνια.
 ΗΛΕΚΤΡΟΝΙAΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Το άτομο αποτελείται από τον πυρήνα, που περιέχει τα θετικά φορτισμένα πρωτόνια και τα ουδέτερα νετρόνια. Στον πυρήνα είναι πρακτικά συγκεντρωμένη η μάζα του ατόμου. Γύρω από
ΗΛΕΚΤΡΟΝΙAΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Το άτομο αποτελείται από τον πυρήνα, που περιέχει τα θετικά φορτισμένα πρωτόνια και τα ουδέτερα νετρόνια. Στον πυρήνα είναι πρακτικά συγκεντρωμένη η μάζα του ατόμου. Γύρω από
A2. Ποια τετράδα κβαντικών αριθμών είναι αδύνατη: α. (4, 2, -1, +½) β. (2, 0, 1, -½) γ. (3, 1, 0, -½) δ. (4, 3, -2, +½) Μονάδες 5
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 02 2016 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Στέφανος Γεροντόπουλος, Μαρία Ρήγα, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α A1. Σύμφωνα με τη μηχανική
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 02 2016 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Στέφανος Γεροντόπουλος, Μαρία Ρήγα, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α A1. Σύμφωνα με τη μηχανική
Ατομική δομή. Το άτομο του υδρογόνου Σφαιρικά συμμετρικές λύσεις ψ = ψ(r) Εξίσωση Schrodinger (σφαιρικές συντεταγμένες) ħ2. Εξίσωση Schrodinger (1D)
 Ατομική δομή Το άτομο του υδρογόνου Σφαιρικά συμμετρικές λύσεις ψ = ψ(r) Εξίσωση Schrodinger (1D) Εξίσωση Schrodinger (σφαιρικές συντεταγμένες) ħ2 2m 2 ψ + V r ψ = Εψ Τελεστής Λαπλασιανής για σφαιρικές
Ατομική δομή Το άτομο του υδρογόνου Σφαιρικά συμμετρικές λύσεις ψ = ψ(r) Εξίσωση Schrodinger (1D) Εξίσωση Schrodinger (σφαιρικές συντεταγμένες) ħ2 2m 2 ψ + V r ψ = Εψ Τελεστής Λαπλασιανής για σφαιρικές
ΟΜΗ ΑΤΟΜΟΥ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ
 ΟΜΗ ΑΤΟΜΟΥ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Παππάς Χρήστος - Επίκουρος Καθηγητής Κβαντισμένα μεγέθη Ένα μέγεθος λέγεται κβαντισμένο όταν παίρνει ορισμένες μόνο διακριτές τιμές, δηλαδή το σύνολο των τιμών του δεν
ΟΜΗ ΑΤΟΜΟΥ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Παππάς Χρήστος - Επίκουρος Καθηγητής Κβαντισμένα μεγέθη Ένα μέγεθος λέγεται κβαντισμένο όταν παίρνει ορισμένες μόνο διακριτές τιμές, δηλαδή το σύνολο των τιμών του δεν
Γενική & Ανόργανη Χημεία
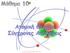 Γενική & Ανόργανη Χημεία 2017-18 Στα στοιχεία μεταπτώσεως τα ηλεκτρόνια προστίθενται στα d τροχιακά Εξαιρέσεις στις διαμορφώσεις d 5, d 10 Δομή ψευδοευγενούς αερίου Με μεταφορά ενός 4s ηλεκτρονίου Cr:
Γενική & Ανόργανη Χημεία 2017-18 Στα στοιχεία μεταπτώσεως τα ηλεκτρόνια προστίθενται στα d τροχιακά Εξαιρέσεις στις διαμορφώσεις d 5, d 10 Δομή ψευδοευγενούς αερίου Με μεταφορά ενός 4s ηλεκτρονίου Cr:
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α. Α1. α. Α2. α. Α3. β. Α4. δ. Α5. α. Σωστό β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β
 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. α Α2. α Α3. β Α4. δ Α5. α. Σωστό β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β Β1. i) Οι πιθανές ηλεκτρονιακές διαμορφώσεις θα είναι: και 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1, Z=24 1s
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. α Α2. α Α3. β Α4. δ Α5. α. Σωστό β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β Β1. i) Οι πιθανές ηλεκτρονιακές διαμορφώσεις θα είναι: και 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1, Z=24 1s
ΦΥΣΙΚΟΧΗΜΕΙΑ I Ενότητα 9 Πολυηλεκτρονιακά Άτομα Δημήτρης Κονταρίδης Αναπληρωτής Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών
 ΦΥΣΙΚΟΧΗΜΕΙΑ I Ενότητα 9 Πολυηλεκτρονιακά Άτομα Δημήτρης Κονταρίδης Αναπληρωτής Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Ενδεικτική βιβλιογραφία 1. ATKINS, ΦΥΣΙΚΟΧΗΜΕΙΑ P.W. Atkins, J. De Paula
ΦΥΣΙΚΟΧΗΜΕΙΑ I Ενότητα 9 Πολυηλεκτρονιακά Άτομα Δημήτρης Κονταρίδης Αναπληρωτής Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Ενδεικτική βιβλιογραφία 1. ATKINS, ΦΥΣΙΚΟΧΗΜΕΙΑ P.W. Atkins, J. De Paula
ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ Άτομο Στοιχείο Χημική ένωση Χημική αντίδραση
 ΕΙΣΑΓΩΓΙΚΕΣ ΕΝΝΟΙΕΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ Άτομο: το μικρότερο σωματίδιο της ύλης που διατηρεί την ταυτότητά του κατά τη διάρκεια των χημικών αντιδράσεων Στοιχείο: αποτελείται από ένα είδος ατόμων Χημική ένωση:
ΕΙΣΑΓΩΓΙΚΕΣ ΕΝΝΟΙΕΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ Άτομο: το μικρότερο σωματίδιο της ύλης που διατηρεί την ταυτότητά του κατά τη διάρκεια των χημικών αντιδράσεων Στοιχείο: αποτελείται από ένα είδος ατόμων Χημική ένωση:
ΤΟ ΚΒΑΝΤΟΜΗΧΑΝΙΚΟ ΜΟΝΤΕΛΟ ΤΟΥ ΑΤΟΜΟΥ
 682 ΤΟ ΚΒΑΝΤΟΜΗΧΑΝΙΚΟ ΜΟΝΤΕΛΟ ΤΟΥ ΑΤΟΜΟΥ Παπαχρήστου Βασίλειος Χημικός, MSc στη διδακτική της Χημείας vasipa@in.gr ΠΕΡΙΛΗΨΗ Το παρόν CD-Rom αποτελείται από τέσσερις ενότητες: Η πρώτη ενότητα αναφέρεται
682 ΤΟ ΚΒΑΝΤΟΜΗΧΑΝΙΚΟ ΜΟΝΤΕΛΟ ΤΟΥ ΑΤΟΜΟΥ Παπαχρήστου Βασίλειος Χημικός, MSc στη διδακτική της Χημείας vasipa@in.gr ΠΕΡΙΛΗΨΗ Το παρόν CD-Rom αποτελείται από τέσσερις ενότητες: Η πρώτη ενότητα αναφέρεται
ΜΟΡΙΑΚΗ ΦΑΣΜΑΤΟΣΚΟΠΙΑ
 ΜΟΡΙΑΚΗ ΦΑΣΜΑΤΟΣΚΟΠΙΑ Ενότητα 9 Ηλεκτρονική Φασματοσκοπία Δημήτρης Κονταρίδης Αναπληρωτής Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Ενδεικτική βιβλιογραφία 1. ATKINS, ΦΥΣΙΚΟΧΗΜΕΙΑ P.W. Atkins,
ΜΟΡΙΑΚΗ ΦΑΣΜΑΤΟΣΚΟΠΙΑ Ενότητα 9 Ηλεκτρονική Φασματοσκοπία Δημήτρης Κονταρίδης Αναπληρωτής Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Ενδεικτική βιβλιογραφία 1. ATKINS, ΦΥΣΙΚΟΧΗΜΕΙΑ P.W. Atkins,
ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ (4)
 ΘΕΜΑ Α Α1. α Α2. α Α3. β Α4. δ Α5. α. Σωστό ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ (4) β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β Β1. i) Οι πιθανές ηλεκτρονιακές διαμορφώσεις θα
ΘΕΜΑ Α Α1. α Α2. α Α3. β Α4. δ Α5. α. Σωστό ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ (4) β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β Β1. i) Οι πιθανές ηλεκτρονιακές διαμορφώσεις θα
Το άτομο του Υδρογόνου- Υδρογονοειδή άτομα
 Το άτομο του Υδρογόνου- Υδρογονοειδή άτομα Το πιο απλό κβαντομηχανικό ρεαλιστικό σύστημα, το οποίο λύνεται ακριβώς, είναι το άτομο του Υδρογόνου (1 πρωτόνιο και 1 ηλεκτρόνιο) Το δυναμικό στην περίπτωση
Το άτομο του Υδρογόνου- Υδρογονοειδή άτομα Το πιο απλό κβαντομηχανικό ρεαλιστικό σύστημα, το οποίο λύνεται ακριβώς, είναι το άτομο του Υδρογόνου (1 πρωτόνιο και 1 ηλεκτρόνιο) Το δυναμικό στην περίπτωση
Κύριος κβαντικός αριθμός (n)
 Κύριος κβαντικός αριθμός (n) Επιτρεπτές τιμές: n = 1, 2, 3, Καθορίζει: το μέγεθος του ηλεκτρονιακού νέφους κατά μεγάλο μέρος, την ενέργεια του τροχιακού τη στιβάδα στην οποία κινείται το ηλεκτρόνιο Όσομεγαλύτερηείναιητιμήτουn
Κύριος κβαντικός αριθμός (n) Επιτρεπτές τιμές: n = 1, 2, 3, Καθορίζει: το μέγεθος του ηλεκτρονιακού νέφους κατά μεγάλο μέρος, την ενέργεια του τροχιακού τη στιβάδα στην οποία κινείται το ηλεκτρόνιο Όσομεγαλύτερηείναιητιμήτουn
Η ΓΕΝΝΗΣΗ ΤΗΣ ΚΒΑΝΤΙΚΗΣ ΧΗΜΕΙΑΣ ΚΑΙ ΤΟΥ ΣΥΓΧΡΟΝΟΥ ΑΤΟΜΙΚΟΥ ΠΡΟΤΥΠΟΥ
 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Με τον όρο ηλεκτρονιακή δοµή εννοούµε τον αριθµό και την κατανοµή των ηλεκτρονίων γύρω από έναν κεντρικό πυρήνα. Ο πυρήνας αυτός αποτελείται από έναν συγκεκριµένο
ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Με τον όρο ηλεκτρονιακή δοµή εννοούµε τον αριθµό και την κατανοµή των ηλεκτρονίων γύρω από έναν κεντρικό πυρήνα. Ο πυρήνας αυτός αποτελείται από έναν συγκεκριµένο
Να βρείτε και να δικαιολογήσετε προς ποια κατεύθυνση είναι μετατοπισμένη η ισορροπία: CH 3 COO (aq) +ΝΗ 4
 Θέ μα 1 ο Επιλέξτε τη σωστή απάντηση σε καθεμιά από τις παρακάτω ερωτήσεις: 1) Τα ατομικά τροχιακά 1s και 2p διαφέρουν α. κατά το σχήμα. β. κατά το μέγεθος. γ. κατά τον προσανατολισμό στο χώρο. δ. σε όλα
Θέ μα 1 ο Επιλέξτε τη σωστή απάντηση σε καθεμιά από τις παρακάτω ερωτήσεις: 1) Τα ατομικά τροχιακά 1s και 2p διαφέρουν α. κατά το σχήμα. β. κατά το μέγεθος. γ. κατά τον προσανατολισμό στο χώρο. δ. σε όλα
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 3 η : Περιοδικότητα & Ατομική Δομή. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 3 η : Περιοδικότητα & Ατομική Δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Φως & Ηλεκτρομαγνητικό Φάσμα 2 Το ορατό φως, η υπεριώδης
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 3 η : Περιοδικότητα & Ατομική Δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Φως & Ηλεκτρομαγνητικό Φάσμα 2 Το ορατό φως, η υπεριώδης
