οµικά στοιχεία βιοµορίων
|
|
|
- Ἰωακείμ Κόρακας
- 8 χρόνια πριν
- Προβολές:
Transcript
1 2-1 Κεφάλαιο 2 οµικά στοιχεία βιοµορίων 2.1. ιαστάσεις των Βιοµορίων Οι διαστάσεις των βιοµορίων κυµαίνονται από µερικά Ångströms (10-10 m) έως µερικές εκατοντάδες Ångströms (10-8 m). (εικόνα 2.1, 2.2) Εικόνα 2.1 Κλίµακα διαστάσεων στο βιολογικό και µοριακό επίπεδο.
2 2-2 Εικόνα 2.2. Μία αίσθηση της κλίµακας µεταξύ οργάνου, κυττάρου, µορίων και ατόµων.
3 Περιβάλλον των βιοµορίων Το φυσικό περιβάλλον των βιοµορίων είναι πολικό ή υδρόφιλο και λιπόφιλο ή υδρόφοβο. Στο πολικό περιβάλλον, κυρίως υδατικό, κυριαρχούν αλληλεπιδράσεις όπως υδρογονικοί δεσµοί, ιοντικές αλληλεπιδράσεις µεταξύ των µορίων του διαλύτη και των βιοµορίων που βρίσκονται µέσα στο διαλύτη (εικόνα 2.3). Εικόνα 2.3 Βιοµόρια σε υδατικό περιβάλλον. Η άνιση κατανοµή ηλεκτρονικού φορτίου στο µόριο του νερού, µε ηλεκτραρνητικότερο το άτοµο του οξυγόνου δηµιουργεί ηλεκτροστατικές έλξεις και τον σχηµατισµό ασθενών δεσµών των υδρογονικών δεσµών (εικόνα 2.2). Εικόνα 2.4. Ο σχηµατισµός υδρογονικών δεσµών µεταξύ των µορίων νερού σε υδατικό διάλυµα και η τετραεδρική οργάνωση των.
4 2-4 Στο λιπόφιλο περιβάλλον (π.χ. κυτταρικές µεµβράνες και µικκύλια) που αποτελείται κυρίως από ασύµµετρα λιπιδικά µόρια µε πολικές οµάδες που συνδέονται µε υδρόφοβες αλυσίδες (εικόνα 2.5)κυριαρχούν οι υδρόφοβες αλληλεπιδράσεις (εικόνα 2.6). Εικόνα 2.5. Ένα µόριο λιπαρού οξέως είναι υδρόφιλο στο ένα άκρο και υδρόφοβο στο άλλο. Σε ένα υδατικό περιβάλλον αυτά τα µόρια φτιάχνουν µικκύλια ή διλιπιδικές στοιβάδες. Εικόνα 2.6. Το υδρόφοβο περιβάλλον που βρίσκεται µία µεµβρανική πρωτείνη. Οι περιοχές της πρωτείνης εκτός της διλιπιδικής στοιβάδας είναι πολικές ενώ αυτές εντός υδρόφοβες.
5 Πρωτοταγής πρωτεϊνική δοµή, δευτεροταγής δοµικές ενότητες, τριτοταγής αρχιτεκτονική και τεταρτοταγής οργάνωση Η πρωτοταγής δοµή της πρωτεΐνης Τα αµινοξικά κατάλοιπα Οι πρωτείνες είναι πολυµερικές αλυσίδες που αποτελούνται από µονοµερή που καλούνται αµινοξέα (εικόνα 2.7). Όλες οι δοµικές και λειτουργικές ιδιότητες των πρωτεϊνών είναι άµεσα συνδεδεµένες µε τις χηµικές ιδιότητες της πολυπεπτιδικής αλυσίδας. Υπάρχουν τέσσερα επίπεδα δοµικής οργάνωσης στις πρωτείνες: Η πρωτοταγής, η δευτεροταγής, η τριτοταγής και η τεταρτοταγής. Ως πρωτοταγής δοµή ορίζεται η γραµµική ακολουθία των αµινοξέων στην πολυπεπτιδική αλυσίδα. Η δευτεροταγής δοµή αναφέρεται σε συγκεκριµένες κανονικές γεωµετρικές στερεοδιατάξεις της αλυσίδας. Η τριτοταγής δοµή αναφέρεται στην στερεοδιάταξη της αλυσίδας στο χώρο και είναι αποτέλεσµα των αλληλεπιδράσεων µεταξύ των ατόµων της αλυσίδας. Η τεταρτοταγής δοµή είναι η οργάνωση των πρωτεϊνικών υποµονάδων, δηλ δύο ή και περισσοτέρων πολυπεπτιδικών αλυσίδων. Εικόνα 2.7. Ένα αµινοξύ αποτελείται από την πεπτιδική οµάδα που είναι επίπεδη και τον ασύµµετρο άνθρακα. Όλες οι αποστάσεις των δεσµών είναι σε Angströms (10-10 m). Τα αµινοξέα είναι οι χηµικές µονάδες που συνθέτουν τις πρωτεΐνες και χαρακτηρίζονται από ένα κεντρικό ασύµµετρο άτοµο άνθρακα (α-άνθρακας). Το α υποδεικνύει την θέση από όπου αρχίζει η αρίθµηση για όλα τις υπόλοιπες συνδεδεµένες σε αυτόν χηµικές υποοµάδες. Τέσσερις υποκαταστάτες είναι συνδεδεµένοι σε αυτό τον α-άνθρακα (Cα): Ένας υποκαταστάτης είναι το α πρωτόνιο (Ηα), ένας άλλος η πλευρική αλυσίδα (-R) που δίνει την χηµική ποικιλοµορφία των αµινοξέων, ο τρίτος είναι η καρβοξυλική οµάδα (- COOH) και η τέταρτη η αµινοµάδα (-ΝΗ). Ο α-άνθρακας είναι το ασύµµετρο κέντρο του αµινοξέος για τα 19 από τα 20 αµινοξέα εκτός της γλυκίνης που έχει ένα πρωτόνιο ως πλευρική αλυσίδα. Η στερεοδιάταξη γύρω από τον α-άνθρακα πρέπει να είναι το L- ισοµερές για πρωτείνες που συντίθενται στο ριβόσωµα. Αυτό πιθανόν να οφείλεται σε µία τυχαία επιλογή της χηµικής εξέλιξης όπου το L-ισοµερές να επιλέχθηκε από τα πρωτόγονα προβιωτικά συστήµατα και παρέµεινε στην εξελικτική ιστορία στον πλανήτη µας.
6 2-6 Εικόνα 2.8. Τα οπτικά στερεοϊσοµερή του α-άνθρακα στις πρωτείνες. Οι πλευρικές αλυσίδες έχουν µεγάλη χηµική ποικιλοµορφία που είναι απαραίτητη για τις µοναδικές λειτουργίες των πρωτεϊνών. Οι πλευρικές αλυσίδες µπορούν να ταξινοµηθούν σε τρεις κατηγορίες: µη-πολικές, αφόρτιστες πολικές και φορτισµένες πολικές. Το απλούστερο αµινοξύ είναι η γλυκίνη. Η αλανίνη, βαλίνη, λευκίνη, ισολευκίνη και προλίνη είναι αµινοξέα µε αποκλειστικά αλειφατικές πλευρικές αλυσίδες. Η αλανίνη έχει ένα µεθύλιο ως πλευρική αλυσίδα. Η βαλίνη έχει δύο µεθύλοµάδες που συνδέονται στον β- άνθρακα και αυτό το αµινοξύ έχει β-διακλάδωση. Η λευκίνη έχει ένα επιπλέον άτοµο άνθρακα στην πλευρική αλυσίδα από την βαλίνη ώστε οι δύο µεθυλοµάδες να συνδέονται µε τον γ-άνθρακα. Η λευκίνη και η ισολευκίνη είναι ισοµερή µε µόνη δοµική διαφορά στην θέση των µεθυλοµάδων. Η ισολευκίνη έχει β-διακλάδωση και ένα δεύτερο ασύµµετρο άνθρακα στην β-θέση. Η προλίνη περιέχει µία αλιφατική αλυσίδα που είναι οµοιπολικά συνδεδεµένη µε το άτοµο αζώτου της α-αµινοµάδας, σχηµατίζοντας ένα αµιδικό δεσµό και την δηµιουργία ενός πενταµελούς δακτυλίου. Οι πλευρικές αλυσίδες που είναι γενικά µη-πολικές, έχουν χαµηλή διαλυτότητα στο νερό γιατί µπορούν να αλληλεπιδρούν µόνο µε δυνάµεις Van der Waals µε τα άτοµα νερού. Αντίθετα τα υπόλοιπα αµινοξέα περιέχουν ετεροάτοµα στις πλευρικές τους αλυσίδες και έτσι έχουν περισσότερες δυνατότητες αλληλεπίδρασης. Τα µη φορτισµένα µέλη της οµάδας των πολικών αµινοξέων περιέχουν: την σερίνη, θρεονίνη, ασπαραγίνη, γλουταµίνη, τυροσίνη και τρυπτοφάνη. Η σερίνη, θρεονίνη και τυροσίνη περιέχουν υδροξυλοµάδες ώστε να συµπεριφέρονται και σαν δότες και δέκτες πρωτονίων. Η θρεονίνη έχει επίσης µία µεθυλοµάδα σε β-διακλάδωση. Ο βενζολικός δακτύλιος της τυροσίνης επιτρέπει την σταθεροποίηση του ανιονικού φαινυλίου µε την απώλεια του πρωτονίου του υδροξυλίου, το οποίο έχει µια σταθερά pk περίπου 10. Η σερίνη και η θρεονίνη δεν µπορούν να αποπρωτονιοθούν σε συνηθισµένες τιµές ph. Η ασπαραγίνη και η γλουταµίνη είναι σχετικά πολικές και µπορούν να είναι δότες και δέκτες πρωτονίων σε υδρογονικούς δεσµούς. Το άζωτο και το πρωτόνιο του ινδολικού δακτυλίου της τρυπτοφάνης µπορεί επίσης να συµµετέχει σε αλληλεπιδράσεις µε υδρογονικούς δεσµούς. Μία άλλη οµάδα πολικών αµινοξέων µπορεί να φέρει πλήρες φορτίο ανάλογα µε το ph αλλά οι τιµές του pka αυτών είναι έτσι διαµορφωµένες ώστε η φορτισµένη µορφή των να παρατηρείται στην περιοχή του ουδέτερου ph (ph=7). Αυτή η οµάδα των αµινοξέων περιέχει τα θετικά φορτισµένα αµινοξέα λυσίνη, αργινίνη και ιστιδίνη και τα αρνητικά φορτισµένα αµινοξέα ασπαρτικό και γλουταµικό οξύ και την κυστείνη. Η λυσίνη και η αργινίνη είναι δύο βασικά αµινοξέα που φέρουν θετικό φορτίο στο τέλος της πλευρικής τους αλυσίδας. Η α-αµινοµάδα της λυσίνης έχει µια τιµή pka κοντά στο 10 ενώ η γουανιδοµάδα της αργινίνης έχει µία τιµή pka περίπου 12. Η ιστιδίνη είναι επίσης βασικό αµινοξύ, µε πλευρική οµάδα ένα πενταµελή δακτύλιο που περιέχει δύο άτοµα αζώτου. Ένα από τα άτοµα αζώτου είναι πρωτονιωµένο αλλά το άλλο έχει µία διαθέσιµη θέση όπου µπορεί να δεχθεί ένα επιπλέον πρωτόνιο και να σχηµατίσει µία φορτισµένη οµάδα µε pka περίπου 6. Το ασπαρτικό και το γλουταµικό οξύ διαφέρουν µόνο στον αριθµό των µεθυλενίων (-CH2-) στην πλευρική αλυσίδα µε µία ή δύο µεθυλενοµόδες αντίστοιχα. Οι
7 2-7 καρβοξυλοµάδες τους είναι πολύ πολικές και µπορούν να δρουν ως δότες και δέκτες πρωτονίων σε υδρογονικούς δεσµούς µε τιµές pka περίπου 4.5. Πίνακας 2.1
8 2-8 Εικόνα 2.9. Οι 20 πλευρικές αλυσίδες των αµινοξέων.
9 2-9 Το σουλφιδρίλιο της κυστείνης µπορεί να ιονίζεται σε σχεtικά αλκαλικές τιµές ph µε pka κοντά στο 9. Στην θειολική µορφή µπορεί να αντιδρά µε άλλο ένα σουλφιδρίλιο για να σχηµατίζει ένα δισουλφιδικό δεµό που είναι αντιστρεπτός µε αναγωγή. Η µεθειονίνη έχει µία µακρυά αλκυλική αλυσίδα που περιέχει ένα ετεροάτοµο θείου αλλά είναι υδρόφοβη. Αυτό το άτοµο θείου είναι αδρανές και δεν δρα ως δέκτης υδρογονικών δεσµών. Τα αµινοξέα µπορούν να οµαδοποιηθούν και µε άλλους τρόπους. Μία οµάδα τριών αµινοξέων που περιέχουν αρωµατικούς δακτυλίους είναι η φαινυλαλανίνη, η ιστιδίνη, η τρυπτοφάνη και η τυροσίνη. Ο αρωµατικός δακτύλιος της φαινυλαλανίνης είναι όµοιος µε αυτό του βενζολίου ή του τολουενίου. Είναι πολύ υδρόφοβος και χηµικά ενεργός µόνο σε ακραίες συνθήκες, αλλά τα ηλεκτρόνια του δακτυλίου µπορούν εύκολα να πολωθούν. Οι πλευρική αλυσίδα της ιστιδίνης µπορεί να θεωρηθεί αρωµατική. Ακολουθεί τους ηλεκτρονικούς κανόνες στην πρωτονιωµένη της κατάσταση αλλά δεν παρουσιάζει την χαρακτηριστική απορρόφηση στην εγγύτερη υπεριώδη περιοχή του φάσµατος όπως τα άλλα τρία αρωµατικά αµινοξέα. Το υπεριώδες φάσµα των τριών άλλων αρωµατικών αµινοξέων είναι χαρακτηριστικό όπως και οι συντελεστές απαλοιφής και αυτές οι ιδιότητες αντικατοπτρίζονται στο ηλεκτρονικό φάσµα των πολυπεπτιδίων που τα περιέχουν. Τέλος η α-άµινο και η α-καρβοξυλοµάδα των αµινοξέων µπορούν επίσης να ιονίζονται, κατέχοντας τιµές pkα και αντίστοιχα για τα αλιφατικά αµινοξέα ενώ οι γειτονικές φορτισµένες οµάδες των πολικών αµινοξέων µπορούν να τροποποιούν τις τιµές pkα αυτών των οµάδων. Κάθε αµινοξύ που ενσωµατώνεται στην πολυπεπτιδική αλυσίδα αναφέρεται ως αµινοξικό κατάλοιπο. Ετσι µόνο τα αµινοτελικά και τα καρβοξυλοτελικά κατάλοιπα κατέχουν α-άµινο και α-καρβόξυ οµάδες που είναι διαθέσιµες Η πολυπεπτιδική αλυσίδα Για να σχηµατισθεί η πολυµερική πρωτεϊνική αλυσίδα από τα µονοµερή αµινοξέα, αυτα συνδέονται µεταξύ τους µε την απώλεια ενός µορίου νερού. Η αντίδραση λαµβάνει χώρα όταν ενα µόριο νερού χάνεται µεταξύ της καρβοξυλοµάδας ενός αµινοξέος και της αµινοµάδας του εποµένου µε την δηµιουργία ενός δεσµού C-N. Αυτές οι αντιδράσεις πολυµερισµού συµβαίνουν στο ριβόσωµα και απαιτούν ενέργεια. Τα ριβοσώµατα, σύµπλοκα πρωτεϊνών και RNA, µεταφράζουν µία νουκλεοτιδική ακολουθία, ένα γονίδιο, σε πρωτεϊνική. Τα 20 αµινοξέα κωδικοποιούνται µε από το γονίδιο και προστίθενται από τον ριβοσωµικό µηχανισµό κατά την διάρκεια της πρωτεϊνοσύνθεσης. Άλλες τροποποιήσεις στην αµινοξική ακολουθία συµβαίνουν µε τις µεταβιοσυνθετικές αλλαγές. Εικόνα Ο σχηµατισµός του πεπτιδικού δεσµού µε την απώλεια ενός µορίου νερού. Η αντίθετη αντίδραση της υδρόλυσης του πεπτιδικού δεσµού δεν συµβαίνει επίσης από µόνη της. Μπορεί να επιτευχθεί χηµικά, αλλά µόνο µε ακραίες συνθήκες. Για παράδειγµα, η επεξεργασία µε ισχυρά οξειδωτικά (1Μ HCl) και βρασµό στους 100 ο C για µερικές ώρες µπορεί να επιτύχει την υδρόλυση των πεπτιδικών δεσµών. Ετσι φαίνεται ότι οι πρωτεΐνες είναι χηµικά και βιολογικά σταθερές εκτός εάν αποπολυµερίζονται (υδρολύονται) επί τούτου. Η αποδόµηση των πολυπεπτιδίων σε ξεχωριστά αµινοξέα µπορεί να υποβοηθηθεί από υδρολυτικά ένζυµα.
10 2-10 Πολλές πρωτεΐνες είναι ετεροπολυµερή (δηλαδή περιέχουν τα περισσότερα ή και όλα τα διαφορετικά αµινοξέα). Σπανιώτερα περιοχές πρωτεϊνών αποτελούνται από συγκεκριµένα αµινοξέα. Συνεπώς κάθε περιοχή µιας τυπικής πρωτεΐνης θα δηµιουργεί ένα ετερόλογο χηµικά περιβάλλον. Αυτό ενισχύεται περισσότερο µε τα υψηλότερα επίπεδα οργάνωσης της πρωτεϊνικής δοµής, δευτεροταγή, τριτοταγή και τεταρτοταγή Ο πεπτιδικός δεσµός. Ο πεπτιδικός δεσµός µεταξύ δύο αµινοξέων είναι µιά ιδιαίτερη περίπτωση αµιδικού δεσµού που περιβάλλεται εκατέρωθεν από α-άνθρακες. Οι γωνίες και τα µήκη δεσµών είναι γνωστά από πολλές παρατηρήσεις σε πρωτεϊνοδοµές. Ο πεπτιδικός δεσµός (C-N) έχει µήκος 1.33Α, λίγο µικρότερος από ένα απλό δεσµό (όχι πεπτιδικό) C-N, αλλά µακρύτερος από ένα διπλό δεσµό όπως C=O µε µήκος 1.23Α (εικόνα 2.7). Τα µήκη των δεσµών όπως και οι γωνίες αντικατοπτρίζουν την κατανοµή ηλεκτρονίων µεταξύ ατόµων, εξ αιτίας της διαφορετικής πολικότητας των ατόµων και του υβριδισµού των δεσµικών τροχιακών. Τα περισσότερο ηλεκτραρνητικά άτοµα, Ο και Ν, µπορούν να φέρουν µερικά αρνητικά φορτία και τα δύο λιγότερο ηλεκτραρνητικά άτοµα, C και Η, µπορούν να φέρουν µερικά θετικά φορτία. Η πεπτιδική οµάδα που αποτελείται από αυτά τα τέσσερα άτοµα µπορεί να θεωρηθεί ως µία δοµή σε κατάσταση συντονισµού. Έτσι ο πεπτιδικός δεσµός έχει χαρακτήρα µερικού διπλού δεσµού που δικαιολογεί και το ενδιάµεσο µήκος δεσµού. Όπως σε κάθε διπλό δεσµό, η περιστροφή γύρω από τον πεπτιδικό δεσµό (δίεδρη γωνία ω) είναι περιορισµένη µε ένα ενεργειακό φράγµα ~3 Kcal/mole µεταξύ cis και trans µορφές. Τα δύο ισοµερή ορίζονται από την κατεύθυνση της πολυπεπτιδικής αλυσίδας εκατέρωθεν του άξονα του δεσµού. ιαδοχικοί α-άνθρακες στη αλυσίδα (ν,ν+1) βρίσκονται στην ίδια πλευρά του δεσµού στο cis ισοµερές και εκατέρωθεν στο trans ισοµερές. Για όλα τα αµινοξέα εκτός από την προλίνη η cis µορφή δεν ευνοείται στις πρωτείνες εξ αιτίας στερικών παρεµποδίσεων µεταξύ διαδοχικών πλευρικών αλυσίδων. Το κλείσιµο του δακτυλίου στην πλευρική αλυσίδα της προλίνης φέρνει το β-άνθρακα µακριά από το προηγούµενο αµινοξύ, οδηγώντας σε ασθενέστερες στερικές παρεµποδίσεις κατά µήκος του πεπτιδικού δεσµού. Για τα περισσότερα αµινοξέα η αναλογία trans-cis είναι ενώ για την προλίνη Επίσης όπως και για κάθε διπλό δεσµό, ορισµένα άτοµα βρίσκονται στο ίδιο επίπεδο που ορίζεται από τον πεπτιδικό δεσµό. Η οµάδα των έξη ατόµων µεταξύ διαδοχικών α- ανθράκων, βρίσκονται στο ίδιο επίπεδο όπως τα έξη άτοµα του αιθυλενίου. Στην trans στερεοδιάταξη του πεπτιδικού δεσµού η πολικότητα των ατόµων οδηγεί στην δηµιουργία µιας µόνιµης διπολικής ροπής κατά µήκος του πεπτιδικού δεσµού µε το αρνητικό άκρο στην πλευρά του καρβονυλικού οξυγόνου. Το επίπεδο του πεπτιδικού δεσµού έχει σηµαντικές συνέπειες στην πολυπεπτιδική δοµή Περιορισµοί στις περιστροφές δίεδρων γωνιών Ενώ η περιστροφή γύρω από τον πεπτιδικό δεσµό είναι περιορισµένη, η περιστροφή γύρω από τους τέσσερις απλούς δεσµούς του α-άνθρακα κάθε αµινοξικού καταλοίπου µπορεί να γίνει ελεύθερα. ύο από αυτές τις περιστροφές σχετίζονται άµεσα µε την στερεοδοµή της πολυπεπτιδικής αλυσίδας. Η δίεδρη γωνία µε κεντρικό δεσµό α- άνθρακα καρβονυλικό άνθρακα ονοµάζεται Ψ. Η δίεδρη γωνία µε κεντρικό δεσµό α- άνθρακα άζωτο της αµινοµάδας ονοµάζεται Φ. Επειδή ο α-άνθρακας είναι ένα από τα έξη άτοµα που σχηµατίζουν το επίπεδο του πεπτιδικού δεσµού, περιστροφές γύρω από τις γωνίες φ και ψ εκατέρωθεν του α-άνθρακα Cα περιστρέφουν ολόκληρο το επίπεδο της πεπτιδικής οµάδας.
11 2-11 Εικόνα Ο ορισµός των δίεδρων γωνιών φ και ψ γύρω από τον α-άνθρακα. Μερικές τιµές των διέδρων γωνιών φ και ψ δεν είναι δυνατές εξ αιτίας στερικών παρεµποδίσεων. Οι επιτρεπτές περιοχές των τιµών φ και ψ διαφέρουν για κάθε αµινοξύ λόγω των διαφορετικών υποκαταστάσεων στην πλευρική αλυσίδα. Ακόµα και για την γλυκίνη (R=H) ορισµένες τιµές δεν είναι επιτρεπτές. Το διάγραµµα των επιτρεπτών τιµών των γωνιών φ και ψ λέγεται διάγραµµα Ramachandran. Οι επιτρεπτές περιοχές µπορούν να οριστούν σαν τιµές ενεργειακού κόστους που απαιτείται για την είσοδο στις µή επιτρεπτές περιοχές. Για αµινοξέα µε διακλάδωση στο β-άνθρακα οι περιορισµοί είναι µεγάλοι και µόνον µικρές περιοχές του χώρου τιµών (φ-ψ) είναι επιτρεπτές. Για την βαλίνη και την ισολευκίνη µόλις το 5% του χώρου (φ-ψ) είναι επιτρεπτό. Όλα τα αµινοξικά κατάλοιπα µπορούν να πάρουν τιµές από την άνω και κάτω αριστερή περιοχή του διαγράµµατος Ramachandran (εικόνα 2.12). Αυτές οι περιοχές αντιστοιχούν σε συνδυασµούς τιµών των γωνιών φ και ψ που χαρακτηρίζουν τις δύο περισσότερο κοινές δευτεροταγείς στερεοδοµές που µπορεί να πάρει η πολυπεπτιδική αλυσίδα, την α-έλικα και την β-πτυχωτή επιφάνεια. Μεταξύ της περιοχής της α-έλικας και της περιοχής της β- πτυχωτής επιφάνειας υπάρχει ένα ενεργειακό φράγµα. Έτσι η εναλλαγή στεροδοµών από α-έλικα σε β-πτυχωτή επιφάνεια παρεµποδίζεται παρ ότι τα περισσότερα αµινοξέα µπορούν να πάρουν και τις δύο στερεοδοµές. Εικόνα Το διάγραµµα Ramachandran των γωνιών φ και ψ. Η κόκκινη περιοχή υποδεικνύει την β-πτυχωτή επιφάνεια και η µπλε την α-έλικα (δεξιόστροφη). Πράσινη είναι η περιοχή της αριστερόστροφης έλικας (για γλυκίνες).
12 2-12 Από πρόσφατες δοµικές αναλύσεις προκύπτουν τα ακόλουθα συµπεράσµατα: Πρώτα ότι υπάρχει απόκλιση από τον επίπεδο πεπτιδικό δεσµό σε µεγάλο ποσοστό. Αυτό επιτρέπει την αύξηση των επιτρεπτών περιοχών τιµών φ και ψ και την ελάττωση του ενεργειακού φράγµατος µεταξύ α-έλικας και β-πτυχωτής επιφάνειας. Κατά δεύτερο λόγο για συγκεκριµένα αµινοξέα, κυρίως µικρά πολικά αµινοξέα, παρατηρούνται πληθώρα τιµών φ/ψ εκτός των επιτρεπτών περιοχών. Πιθανώς αυτά να σχηµατίζουν τοπικές αλληλεπιδράσεις που να αντισταθµίζουν ενεργειακά την συνεισφορά που απαιτείται για αυτές τις περιοχές φ/ψ Η κλίµακα υδροφοβικότητας / πολικότητας των αµινοξέων Η κλίµακα υδροφοβικότητας / πολικότητας των αµινοξέων είναι απαραίτητη για την κατανόηση των ενεργειακών µεγεθών στο δίπλωµα της πρωτείνης αλλά και στην αλληλεπίδραση της πρωτείνης µε άλλες ή και το περιβάλλον (πολικό ή υδρόφοβο) που βρίσκεται (εικόνα 2.13). Εικόνα ιάγραµµα της ολικής ελεύθερης ενέργειας (που εκφράζει την υδροφοβικότητα της πολυπεπτιδικής αλυσίδας) κατά µήκος της αµινοξικής ακολουθίας µεµβρανικής πρωτεΐνης.
13 2-13 Οι κλίµακες υδροφοβικότητας αποτελούνται από πειραµατικές µετρήσεις της ελεύθερης ενέργειας µεταφοράς για κάθε αµινοξύ. ύο κλίµακες είναι απαραίτητες: Μία για την µεταφορά ξεδιπλωµένων αλυσίδων από νερό σε διλιπιδική επιφάνεια και µία για την µεταφορά διπλωµένων αλυσίδων από νερό σε λιπόφιλο διαλύτη. Η συµµετοχή του πεπτιδικού δεσµού στον υπολογισµό είναι απαραίτητη γιατί ολόκληρα αµινοξικά κατάλοιπα και όχι µόνο πλευρικές αλυσίδες συµµετέχουν στις πραγµατικές αλληλεπιδράσεις. Οι κλίµακες που παρατίθενται είναι για POPC διλιπιδική επιφάνεια και n-οκτανόλη σε δύο οικογένειες πεπτιδίων : πενταπεπτίδια της µορφής AcWL-X-LL για τον καθορισµό της υδροφοβικότητας της πλευρικής αλυσίδας και της οµόλογης σειράς AcWLm (m=1-6) για τον καθορισµό της υδροφοβικότητας του πεπτιδικού δεσµού (Εικόνα 2.14). Εικόνα Οι δύο κλίµακες επιτρέπουν την σύγκριση µεταξύ διλιπιδικής στοιβάδας και υδρόφοβου διαλύτη. Η ολική ελεύθερη ενέργεια µεταφοράς αµινοξικών καταλοίπων δίνεται στην εικόνα 2.15 και τον πίνακα 2.2.
14 2-14 Εικόνα Η ολική ελεύθερη ενέργεια µεταφοράς αµινοξικών καταλοίπων για POPC διλιπιδική επιφάνεια και n-οκτανόλη.
15 2-15 Πίνακας 2.2. Κλίµακα υδροφοβικότητας που δίνει την ελεύθερη ενέργεια µεταφοράς G (kcal/mol) από νερό σε POPC στοιβάδα (wif) και n-octanol (woct). Amino Acid Interface Scale G wif (kcal/mol) Octanol Scale G woct (kcal/mol) Octanol - Interface Scale Ala 0.17 ± ± ± 0.12 Arg ± ± ± 0.17 Asn 0.42 ± ± ± 0.13 Asp 1.23 ± ± ± 0.18 Asp ± ± ± 0.17 Cys 0.24 ± ± ± 0.14 Gln 0.58 ± ± ± 0.14 Glu 2.02 ± ± ± 0.21 Glu ± ± ± 0.19 Gly 0.01 ± ± ± 0.12 His ± ± ± 0.16 His ± ± ± 0.13 Ile 0.31 ± ± ± 0.13 Leu 0.56 ± ± ± 0.12 Lys ± ± ± 0.16 Met 0.23 ± ± ± 0.13 Phe 1.13 ± ± ± 0.12 Pro 0.45 ± ± ± 0.16 Ser 0.13 ± ± ± 0.14 Thr 0.14 ± ± ± 0.13 Trp 1.85 ± ± ± 0.13 Tyr 0.94 ± ± ± 0.13 Val 0.07 ± ± ± 0.12
16 Οι δευτεροταγείς δοµές της πρωτείνης. Οι περιορισµοί που προκύπτουν από την στερεοχηµική παρεµπόδιση µεταξύ ατόµων της κύριας και της πλευρικής αλυσίδας είναι ο κυρίως λόγος δηµιουργίας των α και β στερεοδοµών. Επειδή οι περιορισµοί στις τιµές φ/ψ προκύπτουν για κάθε αµινοξύ δεν υπάρχει άµεση σύνδεση στερεοχηµικών παρεµποδίσεων της α/β στερεοδοµής και του τύπου του αµινοξέος (εκτός της προλίνης). Όµως µία ακολουθία αµινοξέων µε παρόµοιες τιµές φ/ψ δηµιουργεί µία α-έλικα ή β-πτυχωτή επιφάνεια σε ένα τµήµα της πολυπεπτιδικής αλυσίδας. Εποµένως οι δευτεροταγείς δοµές οφείλουν την δηµιουργία τους και στις παρεµποδίσεις της κύριας αλλά και της πλευρικής αλυσίδας. Αυτό το συµπέρασµα βοηθά σηµαντικά στην κατανόηση της προέλευσης των πρωτεϊνικών δευτεροταγών δοµών. Οι στερεοδοµές αυτές είναι ενεργειακά επιθυµητές για την πολυπεπτιδική αλυσίδα κάτω από όλες τις συνθήκες ανεξάρτητα της σύνθεσης της α- Ελικα Η στερεοδοµή της έλικας µοιάζει µε ελατήριο (εικόνα 2.16Α). Η δεξιόστροφη α-έλικα που ορίζεται µε ένα µήκος επανάληψης 3.6 αµινοξέα και βήµα 5.4Α ανά στροφή είναι η πλέον συνηθισµένη µορφή έλικας στις πρωτείνες. Σε αυτή τα κατάλοιπα ν+3 και ν+4 βρίσκονται πλησιέστερα στο κατάλοιπο ν. Οι διαστάσεις και το βήµα της έλικας φέρνουν κοντά επίσης τις διπολικές ροπές διαδοχικών πεπτιδίων ώστε τα ετερώνυµα φορτία να εξουδετερώνονται σηµαντικά στο µέσον της έλικας. Στα άκρα της έλικας η διπολική ροπή δεν εξουδετερώνεται δηµιουργώντας µία µακροδιπολική ροπή περίπου ½ ηλεκτρονικού φορτίου σε κάθε άκρο. Η ιδιότητα αυτή χρησιµοποιείται από ορισµένες πρωτείνες αλλά µπορεί και να απαλειφθεί µε την κατανοµή γειτονικών φορτισµένων πλευρικών αλυσίδων. Εικόνα Η δεξιόστροφη α-έλικα (Α) Σχηµατικά µε τους α-άνθρακες, (Β) µόνον Ν-Cα- C της κύριας αλυσίδας, και (C) µε όλα τα άτοµα της κύριας αλυσίδας.
17 2-17 Το βήµα και οι διαστάσεις της έλικας επίσης φέρνουν το πρωτόνιο του αµιδίου του αµινοξέος ν+3 ή ν+4 κοντά στο καρβονυλικό οξυγόνο του αµινοξέος ν (εικόνα 2.16C) ώστε να υπάρχει η δυνατότητα δηµιουργίας υδρογονικού δεσµού. Στην έλικα όλοι οι δότες και οι δέκτες πρωτονίων των πεπτιδικών οµάδων συµµετέχουν στη δηµιουργία υδρογονικών δεσµών εκτός από τα ακραία πεπτίδια και στα δύο άκρα. Οι υδρογονικοί δεσµοί συµµετέχουν στην δηµιουργία µιας σταθερής ελικοειδούς στερεοδοµής. Εικόνα Προβολή της α-έλικας κάθετα στον άξονά της. Με πράσινο αναπαρίστανται οι θέσεις των πλευρικών αλυσίδων β-κλώνοι και β-πτυχωτές επιφάνειες. Οι β-κλώνοι είναι το άλλο στοιχείο κανονικής δευτεροταγούς στερεοδοµής που παρατηρούνται στις πρωτείνες. Είναι εκτεταµένες στερεοδοµές όπου οι διαδοχικές διπολικές ροπές των πεπτιδίων εναλλάσσονται σε κατεύθυνση κατά µήκος της αλυσίδας. Εικόνα Η β-πτυχωτή επιφάνεια αποτελείται από β-κλώνους σε παράλληλη ή αντιπαράλληλη διάταξη.
18 2-18 Επειδή η δοµή είναι εκτεταµένη η στερεοχηµική παρεµπόδιση των οµάδων είναι µικρότερη και έτσι οι περιορισµοί των φ/ψ δίεδρων γωνιών µικρότεροι από την α-έλικα. ύο ή περισσότερα τµήµατα β-κλώνων µπορούν να αλληλεπιδρούν µεταξύ τους µε εναλλασσόµενους υδρογονικούς δεσµούς µεταξύ του πρωτονίου του αµιδίου ενός κλώνου και του καρβονυλικού οξυγόνου του άλλου κλώνου και να σχηµατίζουν µία β- πτυχωτή επιφάνεια. Αντίθετα µε τις ελικοειδείς στερεοδοµές στους υδρογονικούς δεσµούς όλοι οι δότες και οι δέκτες πρωτονίων των πεπτιδικών οµάδων που συµµετέχουν ανήκουν σε γειτονικούς στο χώρο β-κλώνους που όµως µπορεί να βρίσκονται µακριά στην αµινοξική ακολουθία. Έτσι οι β-κλώνοι δεν υπάρχουν ανεξάρτητα αλλά σε οµάδες (δύο ή και περισσότερα). Η κατεύθυνση της κύριας αλυσίδας γειτονικών β-κλώνων µπορεί να είναι παράλληλη οπότε σχηµατίζονται παράλληλες β-πτυχωτές επιφάνειες ή αντιπαράλληλη οπότε σχηµατίζονται αντιπαράλληλες β-πτυχωτές επιφάνειες. Στην ίδια β- πτυχωτή επιφάνεια µπορεί να παρατηρούνται και οι δύο περιπτώσεις. Η αντιπαράλληλη διάταξη των β-κλώνων είναι ενεργειακά περισσότερο σταθερή γιατί οι υδρογονικοί δεσµοί που σχηµατίζονται είναι περισσότερο γραµµικοί (εικόνα 19α,β). Εικόνα Αντιπαράλληλες (Α) και παράλληλες (Β) πτυχωτές επιφάνειες Στροφές και βρόγχοι. Οι στροφές ή βρόγχοι µπορούν να θεωρηθούν επίσης ως στοιχεία δευτεροταγούς δοµής αλλά αντίθετα µε τις έλικες και τους β-κλώνους δεν έχουν κανονική επαναλαµβανόµενη γεωµετρία. Η στερεοδοµή των στροφών χαρακτηρίζεται από ορισµένες τιµές φ/ψ και συχνά απαιτούνται συγκεκριµένοι τύποι αµινοξικών ακολουθιών και σχήµατα υδρογονικών δεσµών. Οι περισσότερες στροφές έχουν τοπικό χαρακτήρα στην πρωτοταγή δοµή, αλλά υπάρχουν και βρόγχοι όπου µεταξύ των αµινοξέων που σχηµατίζουν την αλληλεπίδραση και που η στερεοδοµή τους και συχνά ο τύπος τους είναι καθορισµένος, µεσολαβούν και άλλα αµινοξέα.
19 2-19 Οι στροφές επιτρέπουν στην πολυπεπτιδική αλυσίδα να αναδιπλώνεται δηµιουργώντας τριτοταγείς αλληλεπιδράσεις. Συνήθως αυτές οι αλληλεπιδράσεις είναι µακράς εµβέλειας και έχουν ως αποτέλεσµα την σύµπτυξη της πρωτείνης σε µία σφαιρική µορφή. Οι περιοχές των στροφών γενικά βρίσκονται στην επιφάνεια της σφαιροειδούς µορφής µε τις έλικες και τις β-πτυχωτές επιφάνειες στο εσωτερικό. Οι περιοχές στροφής στην επιφάνεια των πρωτεϊνών µπορεί να είναι περισσότερο ή λιγότερο κινητικές ανάλογα µε την θέση τους και τις αλληλεπιδράσεις που συµµετέχουν Τοπολογικά διαγράµµατα Τοπολογικά διαγράµµατα ονοµάζονται οι επίπεδες αναπαραστάσεις της τριτοταγούς δοµής των πρωτεϊνών µε σύµβολα (κύλινδροι για τις α-έλικες, βέλη για τους β- κλώνους) και βοηθούν στην κατανόηση της συνδετικότητας των στοιχείων της δευτεροταγούς δοµής της πρωτείνης (εικόνες 2.22, 2.23 και 2.24) Απλοί συνδυασµοί µερικών στοιχείων δευτεροταγούς δοµής µε καθορισµένες γεωµετρικές θέσεις ονοµάζονται µοτίφ και εµφανίζονται συχνά στις πρωτεϊνικές δοµές µε συγκεκριµένη λειτουργικότητα. Ορισµένα χαρακτηριστικά µοτίφ είναι: Εικόνα β-κλώνος στροφή β-κλώνος Εικόνα α-έλικα -- στροφή -- α-έλικα (α) το µοτίφ δέσµευσης του DNA (β) το µοτίφ δέσµευσης ιόντων ασβεστίου.
20 2-20 Εικόνα κύλινδρος β-πτυχωτών επιφανειών (jelly roll barrel) Εικόνα Το Ελληνικό κλειδί µε τέσσερις αντιπαράλληλους β-κλώνους
21 2-21 Εικόνα β-κλώνος α-έλικα β-κλώνος που χρησιµοποιείται για την σύνδεση παράλληλων β-κλώνων. Συχνά απλά µοτίφ συνδυάζονται για να σχηµατίσουν πολύπλοκα µοτίφ ( εικόνα 2.25). Εικόνα Ο συνδυασµός τεσσάρων β-α-β-α µοτίφ σχηµατίζει το ΤΙΜ (Triose phοsphate Isomerase) κύλινδρο, µοτίφ που παρατηρείται σε πολλά ένζυµα Η τριτοταγής δοµή της πρωτεΐνης Οι πλευρικές αλυσίδες που προεξέχουν από τις α-ελικοειδείς δοµές και τους β- κλώνους είναι διαθέσιµες για αλληλεπιδράσεις µε άλλες περιοχές της πρωτεϊνικής αλυσίδας µε υδρόφοβες επαφές, ηλεκτροστατικές δυνάµεις ή και οµοιοπολικούς ή υδρογονικούς δεσµούς. Όταν τα στοιχεία δευτεροταγούς δοµής της πρωτείνης
22 2-22 αλληλεπιδράσουν µεταξύ τους τότε η πρωτεϊνική αλυσίδα διπλώνει στην τελική στερεοδοµή της στο χώρο που λέγεται και τριτοταγής δοµή της πρωτείνης. Εικόνα Στοιχεία δευτεροταγούς δοµής σχηµατίζουν δοµικές ενότητες και αυτές συµπτύσσονται µεταξύ τους για να σχηµατίσουν την τριτοταγή δοµή της πρωτείνης. Συνδυασµός στοιχείων δευτεροταγών δοµών και µοτίφ δίνουν ανεξάρτητες δοµικές µονάδες σε µία πρωτείνη και λέγονται δοµικές ενότητες (Domains) (εικόνα 2.27). Εικόνα Τρεις διαφορετικές δοµικές ενότητες (domains) που παρατηρούνται σε πρωτείνες (δέσµη α-ελίκων, β-α-β-α και β-σάντουιτς).
23 2-23 Εάν τα στοιχεία της δευτεροταγούς δοµής (α-έλικες, β-κλώνοι) προκύπτουν εξ αιτίας των στερεοχηµικών περιορισµών στο χώρο των φ και ψ, δεν είναι άµεσα ορατό γιατί σχηµατίζονται οι τριτοταγείς δοµές. Πρωτείνες µε καλά οργανωµένη τριτοταγή δοµή έχουν ένα εσωτερικό υδρόφοβο κέντρο όπου τα αµινοξέα ανήκουν σε πολλά διαφορετικά στοιχεία δευτεροταγούς δοµής. Έτσι οι δευτεροταγείς και η τριτοταγής δοµή είναι γενικά αλληλένδετες. Τα εσωτερικά αµινοξέα είναι πολύ καλά πακεταρισµένα ώστε οι δυνατότητες περιστροφής των πλευρικών αλυσίδων να είναι πολύ περιορισµένες. Σε πολικούς διαλύτες η υδροφοβικότητα οδηγεί την αµινοξική αλυσίδα σε συµπαγή οργάνωση για την αποφυγή αλληλεπιδράσεων του πολικού διαλύτη και των υδρόφοβων πλευρικών αλυσίδων αλλά και ο περιορισµός των βαθµών ελευθερίας της αλυσίδας που διπλώνει έχει εντροπικό κόστος ώστε τα δύο φαινόµενα να αναιρούνται ενεργειακά µεταξύ τους. Η αµοιβαία εξάρτηση δευτεροταγούς και τριτοταγούς δοµής είναι το κύριο αίτιο σε µοριακό επίπεδο της δοµικής σταθερότητας των πρωτεϊνών. Αυτό αντικατοπτρίζεται στο γεγονός της έλλειψης δευτεροταγούς και τριτοταγούς δοµής συγχρόνως όταν στο περιβάλλον της πρωτείνης προκύψουν αλλαγές που δεν ευνοούν το δίπλωµα της όπως υψηλή θερµοκρασία ή ορισµένοι διαλύτες (ουρία κλπ.) Σύµφωνα µε τα στοιχεία δευτεροταγούς δοµής και τα µοτίφ πρωτείνες κατατάσσονται σε: που περιέχουν οι α- δοµές (µόνον α-έλικες) α/β δοµές (α-ελικες και β-πτυχωτές επιφάνειες) β-αντιπαράλληλες δοµές (β-αντιπαράλληλες πτυχωτές επιφάνειες) Η τεταρτοταγής δοµή της πρωτείνης Το υψηλότερο επίπεδο οργάνωσης είναι η τεταρτοταγής δοµή. Οι υποµονάδες που συνενώνονται µπορεί να είναι ακριβώς όµοιες (π.χ. δισµουτάσες), ή τελείως διαφορετικές (π.χ. φωτοσύστηµα) και η οργάνωση τους συµµετρική (π.χ. αιµοσφαιρίνη) ή όχι (ακετυλοχολινικός υποδοχέας). Γενικά η τεταρτοταγής δοµή είναι αποτέλεσµα των αλληλεπιδράσεων της επιφάνειας των ανεξαρτήτων τριτοταγών δοµικών µονάδων (εικόνα 2.28). Εικόνα Παραδείγµατα σχηµατισµού τεταρτοταγούς δοµής.
24 2-24 Υπάρχει ένας µεγάλος αριθµός πρωτεϊνικών δοµών όπου η τριτοταγής δοµή διαµορφώνεται ταυτόχρονα µε την τεταρτοταγή. Έτσι στο διµερές του καταστολέα της τρυπτοφάνης (εικόνα 2.29) οι περισσότερες αλληλεπιδράσεις µεταξύ των στοιχείων της δευτεροταγούς δοµής σχηµατίζονται στην επιφάνεια διεπαφής των δύο πολυπεπτιδικών αλυσίδων. Αυτό δείχνει την συχνή εξάρτηση µεταξύ τριτοταγούς και τεταρτοταγούς δοµής και υποδεικνύει ότι τα όρια διαφοροποίησης µεταξύ των επιπέδων οργάνωσης της πολυπεπτιδικής αλυσίδας είναι µάλλον ασαφή. Εικόνα 2.29 Σχηµατικό διάγραµµα του καταστολέα της τρυπτοφάνης.
25 Η δοµή των τεσσάρων πυρηνικών βάσεων και η στερεοδοµές του DNA Οι τέσσερις πυρηνικές βάσεις. Οι τέσσερις πυρηνικές βάσεις είναι οι βασικές δοµικές µονάδες του DNA και ταιριάζουν ανά ζεύγη. Ο γενετικός κώδικας µεταγραφής µας δίνει τις τριπλέτες βάσεων (κωδικόνια) για κάθε αµινοξύ. Εικόνα 2.30.
26 Οι στερεοδοµές του DNA (Α,Β,Ζ). Τα πυρηνικά οξέα είναι γραµµικά µόρια που αποτελούνται από δύο αντιπαράλληλες αλυσίδες. Η διάµετρος τους είναι περίπου 20Α. Αποτελούνται από δύο χηµικά συστατικά. Την όξυ ή δεσοξυ-ριβοζι-φωσφορική αλυσίδα που µε τους βαθµούς ελευθερίας της δίνει την ευκαµψία στα πυρηνικά οξέα (εικ.2.31) και τα ζευγάρια των πυρηνικών βάσεων (εικόνα 2.32). Εικόνα Οι γωνίες περιστροφής της δεσοξυ-ριβοζι-φωσφορικής αλυσίδας του DNA.
27 2-27 Εικόνα Η διπλή έλικα του DNA σχηµατίζεται από 2 αντιπαράλληλες αλυσίδες που περιέχουν δεσοξυριβονουκλεϊνικές βάσεις συνδεδεµένες µε φωσφοδιεστερικούς δεσµούς και συνδέονται µεταξύ τους µε υδρογονικούς δεσµούς. Το DNA υπάρχει σε τρεiς κυρίως δοµικές µορφές, την Α, Β και Ζ (εικ. 2.33,2.34). In vivo το Β-DNA είναι η ενεργειακά προτιµούµενη στερεοδοµή. Στο Α-DNA υπάρχουν 10.9 ζευγάρια βάσεων για κάθε στροφή της διπλής έλικας µε µία µεταξύ τους απόσταση 2.9Α (εικ.2.33) ενώ για το Β- DNA υπάρχουν 10.0 ζευγάρια βάσεων για κάθε στροφή της διπλής έλικας µε µία µεταξύ τους απόσταση 3.4Ǻ. Εικόνα Χωροπληρωτικά µοντέλα Α,Β, και Ζ DNA. Στο Β- DNA ο άξονας της έλικας περνά από το κέντρο κάθε ζευγαριού βάσεων που είναι κάθετες σε αυτόν, ενώ στο Α- DNA είναι µετατοπισµένος προς την µείζονα κοιλότητα και οι βάσεις έχουν µία κλίση 13 ο -19 ο (εικ.2.33).
28 2-28 Εικόνα Σχηµατική αναπαράσταση των Α και Β DNA. ιακρίνεται η µετατόπιση του άξονα της διπλής έλικας και ο σχηµατισµός της µεγάλης και µικρής κοιλότητας (major και minor groove).
Κεφάλαιο 1. Οι δομικοί λίθοι
 Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν;
 Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
Δομικές κατηγορίες πρωτεϊνών
 3-1 Κεφάλαι ο Δομικές κατηγορίες πρωτεϊνών 3.1. α-δομές πρωτεϊνών Οι α-έλικες είναι δομικά στοιχεία που μπορούν να σχηματίσουν πολλές κατηγορίες στερεοδομών και με πολλές διαφορετικές λειτουργίες. Εκτός
3-1 Κεφάλαι ο Δομικές κατηγορίες πρωτεϊνών 3.1. α-δομές πρωτεϊνών Οι α-έλικες είναι δομικά στοιχεία που μπορούν να σχηματίσουν πολλές κατηγορίες στερεοδομών και με πολλές διαφορετικές λειτουργίες. Εκτός
Μοριακή Αναγνώριση ΗΛΙΑΣ ΗΛΙΟΠΟΥΛΟΣ ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ
 Μοριακή Αναγνώριση ΗΛΙΑΣ ΗΛΙΟΠΟΥΛΟΣ ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΑΘΗΝΑ 2001 ΠΕΡΙΕΧΟΜΕΝΑ Κεφάλαιο 1. Εισαγωγή στην Μοριακή Αναγνώριση 1.1. Εισαγωγή 1.2. Παραδείγματα Κεφάλαιο 2. Δομικά στοιχεία βιομορίων
Μοριακή Αναγνώριση ΗΛΙΑΣ ΗΛΙΟΠΟΥΛΟΣ ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΑΘΗΝΑ 2001 ΠΕΡΙΕΧΟΜΕΝΑ Κεφάλαιο 1. Εισαγωγή στην Μοριακή Αναγνώριση 1.1. Εισαγωγή 1.2. Παραδείγματα Κεφάλαιο 2. Δομικά στοιχεία βιομορίων
Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες
 Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες Γένωμα vs Πρωτέωμα Όλη η αλληλουχία βάσεων στο DNA Τι είναι δυνατόν Συγκεκριμένο Στατικό Οι πρωτεΐνες που κωδικοποιούνται από το γένωμα Τι είναι
Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες Γένωμα vs Πρωτέωμα Όλη η αλληλουχία βάσεων στο DNA Τι είναι δυνατόν Συγκεκριμένο Στατικό Οι πρωτεΐνες που κωδικοποιούνται από το γένωμα Τι είναι
Δευτεροταγής Δομή Πρωτεϊνών
 Δευτεροταγής Δομή Πρωτεϊνών Πρωτεϊνικό δίπλωμα Oι στόχοι μιας πρωτεΐνης όταν διπλωθεί είναι: 1. H xαμηλή ενέργεια διαμόρφωσης του κάθε αμινοξέος 2. Να επιτευχθούν υδρογονικοί δεσμοί από πολικά αμινοξέα
Δευτεροταγής Δομή Πρωτεϊνών Πρωτεϊνικό δίπλωμα Oι στόχοι μιας πρωτεΐνης όταν διπλωθεί είναι: 1. H xαμηλή ενέργεια διαμόρφωσης του κάθε αμινοξέος 2. Να επιτευχθούν υδρογονικοί δεσμοί από πολικά αμινοξέα
Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων. 1/10/2015 Δ.Δ. Λεωνίδας
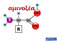 αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
MAΘΗΜΑ 4 ο AMINOΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ
 MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ
 ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
COOH R 2. H α-αμινοξύ 2
 7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
Στοιχεία Φυσικοχηµείας και Βιοφυσικής
 Στοιχεία Φυσικοχηµείας και Βιοφυσικής Β. Φαδούλογλου 2008 Στοιχεία Φυσικοχηµείας και Βιοφυσικής Εργαστήρια Βιβλίο Εξετάσεις Ύλη Στοιχεία Φυσικοχηµείας και Βιοφυσικής Εργαστήρια Βιβλίο Εξετάσεις Ύλη Στοιχεία
Στοιχεία Φυσικοχηµείας και Βιοφυσικής Β. Φαδούλογλου 2008 Στοιχεία Φυσικοχηµείας και Βιοφυσικής Εργαστήρια Βιβλίο Εξετάσεις Ύλη Στοιχεία Φυσικοχηµείας και Βιοφυσικής Εργαστήρια Βιβλίο Εξετάσεις Ύλη Στοιχεία
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
Μικρά αμινοξέα. Βιοχημεία Ι Β-3
 Βιοχημεία Ι Β-2 Μικρά αμινοξέα Βιοχημεία Ι Β-3 Aλειφατικά αμινοξέα Βιοχημεία Ι Β-4 Ιμινοξύ Βιοχημεία Ι Β-5 Αρωματικά αμινοξέα Βιοχημεία Ι Β-6 Βιοχημεία Ι Β-7 Η Tyr και η Trp απορροφούν στα 280nm-έτσι μετράται
Βιοχημεία Ι Β-2 Μικρά αμινοξέα Βιοχημεία Ι Β-3 Aλειφατικά αμινοξέα Βιοχημεία Ι Β-4 Ιμινοξύ Βιοχημεία Ι Β-5 Αρωματικά αμινοξέα Βιοχημεία Ι Β-6 Βιοχημεία Ι Β-7 Η Tyr και η Trp απορροφούν στα 280nm-έτσι μετράται
Μοριακή Αναγνώριση. 5.1. Εισαγωγή. 5.2. Σταθερές σύνδεσης και αποχωρισµού. [A][B] k d = ----------- [AB] [ΑΒ] k i = ---------- [Α][Β] Κεφάλαιο
![Μοριακή Αναγνώριση. 5.1. Εισαγωγή. 5.2. Σταθερές σύνδεσης και αποχωρισµού. [A][B] k d = ----------- [AB] [ΑΒ] k i = ---------- [Α][Β] Κεφάλαιο Μοριακή Αναγνώριση. 5.1. Εισαγωγή. 5.2. Σταθερές σύνδεσης και αποχωρισµού. [A][B] k d = ----------- [AB] [ΑΒ] k i = ---------- [Α][Β] Κεφάλαιο](/thumbs/24/3785169.jpg) Κεφάλαιο 5-1 5 Μοριακή Αναγνώριση 5.1. Εισαγωγή Ένα από τα σηµαντικότερα χαρακτηριστικά των ζωντανών οργανισµών είναι ότι τα µακροµόρια που περιέχουν κάνουν πολύ εξειδικευµένες αλληλεπιδράσεις µε άλλα
Κεφάλαιο 5-1 5 Μοριακή Αναγνώριση 5.1. Εισαγωγή Ένα από τα σηµαντικότερα χαρακτηριστικά των ζωντανών οργανισµών είναι ότι τα µακροµόρια που περιέχουν κάνουν πολύ εξειδικευµένες αλληλεπιδράσεις µε άλλα
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ
 ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
Αρχιτεκτονική της τρισδιάστατης δομής πρωτεϊνών
 Αρχιτεκτονική της τρισδιάστατης δομής πρωτεϊνών Βασίλης Προμπονάς, PhD Ερευνητικό Εργαστήριο Βιοπληροφορικής Τμήμα Βιολογικών Επιστημών Νέα Παν/πολη, Γραφείο B161 Πανεπιστήμιο Κύπρου Ταχ.Κιβ. 20537 1678,
Αρχιτεκτονική της τρισδιάστατης δομής πρωτεϊνών Βασίλης Προμπονάς, PhD Ερευνητικό Εργαστήριο Βιοπληροφορικής Τμήμα Βιολογικών Επιστημών Νέα Παν/πολη, Γραφείο B161 Πανεπιστήμιο Κύπρου Ταχ.Κιβ. 20537 1678,
οµή και Αναδίπλωση πρωτεϊνών
 οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
Κεφάλαιο 22 Πρωτεΐνες
 Κεφάλαιο 22 Πρωτεΐνες Σύνοψη Οι πρωτεΐνες είναι μακρομόρια που προκύπτουν από την ένωση α-αμινοξέων. Τα α-αμινοξέα είναι οργανικές ενώσεις που έχουν μία αμινομάδα (ΝΗ 2 ) και καρβοξύλιο (COOH) συνδεδεμένα
Κεφάλαιο 22 Πρωτεΐνες Σύνοψη Οι πρωτεΐνες είναι μακρομόρια που προκύπτουν από την ένωση α-αμινοξέων. Τα α-αμινοξέα είναι οργανικές ενώσεις που έχουν μία αμινομάδα (ΝΗ 2 ) και καρβοξύλιο (COOH) συνδεδεμένα
Δομή και λειτουργία πρωτεϊνών. Το κύριο δομικό συστατικό των κυττάρων. Το κύριο λειτουργικό μόριο
 Δομή και λειτουργία πρωτεϊνών Το κύριο δομικό συστατικό των κυττάρων. Το κύριο λειτουργικό μόριο Πρωτεΐνες Κύριο συστατικό κυττάρου Δομικοί λίθοι αλλά και επιτελεστές λειτουργίας κυττάρου ένζυμα, μεταφορά,
Δομή και λειτουργία πρωτεϊνών Το κύριο δομικό συστατικό των κυττάρων. Το κύριο λειτουργικό μόριο Πρωτεΐνες Κύριο συστατικό κυττάρου Δομικοί λίθοι αλλά και επιτελεστές λειτουργίας κυττάρου ένζυμα, μεταφορά,
Διαλέξεις Χημείας Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων
 Διαλέξεις Χημείας -2014 Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων 1. Κατάταξη 2. Λειτουργίες 1. Πεπτιδικές ορμόνες 3. Πεπτιδικός δεσμός 1. Χαρακτηριστικά
Διαλέξεις Χημείας -2014 Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων 1. Κατάταξη 2. Λειτουργίες 1. Πεπτιδικές ορμόνες 3. Πεπτιδικός δεσμός 1. Χαρακτηριστικά
Δομές (Διαμορφώσεις) Πρωτεινικών μορίων
 Δομές (Διαμορφώσεις) Πρωτεινικών μορίων Πρωτοταγής δομή (αλληλουχία αμινοξέων) Δευτεροταγής δομή Η διάταξη της πεπτιδικής αλυσίδας στον χωρο αυτής καθ αυτής (χωρίς να ληφθούν υπ όψη οι ομάδες R) Τριτοταγής
Δομές (Διαμορφώσεις) Πρωτεινικών μορίων Πρωτοταγής δομή (αλληλουχία αμινοξέων) Δευτεροταγής δομή Η διάταξη της πεπτιδικής αλυσίδας στον χωρο αυτής καθ αυτής (χωρίς να ληφθούν υπ όψη οι ομάδες R) Τριτοταγής
ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
 ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
Δευτεροταγής Δομή Πρωτεϊνών
 Δευτεροταγής Δομή Πρωτεϊνών Πρωτεϊνικό δίπλωμα Η κινητήρια δύναμη για την αναδίπλωση μιας πρωτεΐνης είναι η επίτευξη των εξής: 1. xαμηλή ενέργεια διαμόρφωσης του κάθε αμινοξέος 2. δημιουργία μιας συμπαγούς
Δευτεροταγής Δομή Πρωτεϊνών Πρωτεϊνικό δίπλωμα Η κινητήρια δύναμη για την αναδίπλωση μιας πρωτεΐνης είναι η επίτευξη των εξής: 1. xαμηλή ενέργεια διαμόρφωσης του κάθε αμινοξέος 2. δημιουργία μιας συμπαγούς
Εισαγωγή στη Δομή Βιομορίων
 Εισαγωγή στη Δομή Βιομορίων Μαρία Παυλάκη mpavlaki@alex.duth.gr Oργάνωση μαθήματος (εξετάσεις) Tο μάθημα έχει συντελεστή 70% του τελικού βαθμού Tο εργαστήριο 30% Θα πρέπει να πάρετε 5 στο μάθημα και ο
Εισαγωγή στη Δομή Βιομορίων Μαρία Παυλάκη mpavlaki@alex.duth.gr Oργάνωση μαθήματος (εξετάσεις) Tο μάθημα έχει συντελεστή 70% του τελικού βαθμού Tο εργαστήριο 30% Θα πρέπει να πάρετε 5 στο μάθημα και ο
 1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
τα βιβλία των επιτυχιών
 Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
Τάξη. Γνωστικό αντικείµενο: Ειδικοί διδακτικοί στόχοι
 Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
Τα χημικά στοιχεία που είναι επικρατέστερα στους οργανισμούς είναι: i..
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
Βιολογία Γενικής Παιδείας Β Λυκείου
 Απρίλιος Μάιος 12 Βιολογία Γενικής Παιδείας Β Λυκείου Βιολογία Γενικής Παιδείας Β Λυκείου (Ερωτήσεις που παρουσιάζουν ενδιαφέρον) 1. Τι είναι τα βιομόρια και ποια είναι τα βασικά χαρακτηριστικά τους; Βιομόρια
Απρίλιος Μάιος 12 Βιολογία Γενικής Παιδείας Β Λυκείου Βιολογία Γενικής Παιδείας Β Λυκείου (Ερωτήσεις που παρουσιάζουν ενδιαφέρον) 1. Τι είναι τα βιομόρια και ποια είναι τα βασικά χαρακτηριστικά τους; Βιομόρια
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής
 Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τμήμα Βιοτεχνολογίας, Γεωπονικό Πανεπιστήμιο Αθηνών
 Μοριακή Αναγνώριση Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τμήμα Βιοτεχνολογίας, Γεωπονικό Πανεπιστήμιο Αθηνών 1 Μοριακή Αναγνώριση Με τον όρο μοριακή αναγνώριση περιγράφουμε την αλληλεπίδραση μεταξύ δύο
Μοριακή Αναγνώριση Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τμήμα Βιοτεχνολογίας, Γεωπονικό Πανεπιστήμιο Αθηνών 1 Μοριακή Αναγνώριση Με τον όρο μοριακή αναγνώριση περιγράφουμε την αλληλεπίδραση μεταξύ δύο
Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ
 Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Θεωρητικό μέρος ΠΡΩΤΕΪΝΕΣ ΚΑΖΕΪΝΗ Πρωτεΐνες Είναι μεγάλα σύνθετα βιομόρια. Έχουν μοριακό βάρος από 10.000 μέχρι πάνω από 1 εκατομμύριο.
Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Θεωρητικό μέρος ΠΡΩΤΕΪΝΕΣ ΚΑΖΕΪΝΗ Πρωτεΐνες Είναι μεγάλα σύνθετα βιομόρια. Έχουν μοριακό βάρος από 10.000 μέχρι πάνω από 1 εκατομμύριο.
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια
 πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια Περιγραφή μαθήματος Επανάληψη σημαντικών εννοιών από την Οργανική Χημεία Χημική σύσταση των κυττάρων Μονοσακχαρίτες Αμινοξέα Νουκλεοτίδια
πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια Περιγραφή μαθήματος Επανάληψη σημαντικών εννοιών από την Οργανική Χημεία Χημική σύσταση των κυττάρων Μονοσακχαρίτες Αμινοξέα Νουκλεοτίδια
ΑΣΚΗΣΗ 1 Δύο αμινοξέα Α, και Β, συνιστούν ένα διπεπτίδιο. Το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του. Ποια είναι η δομή του;
 ΑΣΚΗΣΗ 1 Δύο αμινοξέα Α, και Β, συνιστούν ένα διπεπτίδιο. Το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του. Ποια είναι η δομή του; Β-Α γιατί το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του άρα θα γράφεται
ΑΣΚΗΣΗ 1 Δύο αμινοξέα Α, και Β, συνιστούν ένα διπεπτίδιο. Το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του. Ποια είναι η δομή του; Β-Α γιατί το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του άρα θα γράφεται
Ενεργειακή ανάλυση βιομορίων
 Ενεργειακή ανάλυση βιομορίων Τα βιομόρια ως φυσικά συστήματα πρωτεΐνες, DNA, πεπτίδια, μικρά μόρια (ligands, φάρμακα) Αλληλεπιδράσεις μεταξύ των ατόμων + επίδραση του περιβάλλοντος νερού σταθεροποίηση
Ενεργειακή ανάλυση βιομορίων Τα βιομόρια ως φυσικά συστήματα πρωτεΐνες, DNA, πεπτίδια, μικρά μόρια (ligands, φάρμακα) Αλληλεπιδράσεις μεταξύ των ατόμων + επίδραση του περιβάλλοντος νερού σταθεροποίηση
Το ένζυμο Καρβοξυπεπτιδάση Α έχει τα εξής χαρακτηριστικά
 Το ένζυμο Καρβοξυπεπτιδάση Α έχει τα εξής χαρακτηριστικά Είναι απλή πολυπεπτιδική αλυσίδα 307 αμινοξέων Είναι συμπαγής και έχει σχήμα ελλειψοειδές διαστάσεων 50 x 42 x 38 A Περιέχει περιοχές α-έλικος 38%
Το ένζυμο Καρβοξυπεπτιδάση Α έχει τα εξής χαρακτηριστικά Είναι απλή πολυπεπτιδική αλυσίδα 307 αμινοξέων Είναι συμπαγής και έχει σχήμα ελλειψοειδές διαστάσεων 50 x 42 x 38 A Περιέχει περιοχές α-έλικος 38%
πρωτεΐνες πολυμερείς ουσίες δομούν λειτουργούν λευκώματα 1.Απλές πρωτεΐνες 2.Σύνθετες πρωτεΐνες πρωτεΐδια μη πρωτεϊνικό μεταλλοπρωτεΐνες
 ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α
 Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
Περίληψη 1 ου Κεφαλαίου
 Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Η πλειοψηφία των αμινοξέων είναι του τύπου :
 ΚΕΦΑΛΑΙΟ 5 Η πλειοψηφία των αμινοξέων είναι του τύπου : H 2 NCHCOOH R O συνδυασμός καρβοξυλίου και αμινομάδας στο μόριό τους έχει ως αποτέλεσμα να συμπεριφέρονται είτε ως οξέα είτε ως βάσεις (αμφολύτες).
ΚΕΦΑΛΑΙΟ 5 Η πλειοψηφία των αμινοξέων είναι του τύπου : H 2 NCHCOOH R O συνδυασμός καρβοξυλίου και αμινομάδας στο μόριό τους έχει ως αποτέλεσμα να συμπεριφέρονται είτε ως οξέα είτε ως βάσεις (αμφολύτες).
Αλληλεπιδράσεις μεταξύ βιομορίων
 Αλληλεπιδράσεις μεταξύ βιομορίων Το αντικείμενο των αλληλεπιδράσεων μεταξύ των βιομορίων καλύπτει ένα τεράστιο σύνολο περιπτώσεων με αποτελέσματα από βιολογικές, βιοχημικές και βιοφυσικές μελέτες που δεν
Αλληλεπιδράσεις μεταξύ βιομορίων Το αντικείμενο των αλληλεπιδράσεων μεταξύ των βιομορίων καλύπτει ένα τεράστιο σύνολο περιπτώσεων με αποτελέσματα από βιολογικές, βιοχημικές και βιοφυσικές μελέτες που δεν
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΠΡΩΤΕΪΝΕΣ. Φατούρος Ιωάννης Αναπληρωτής Καθηγητής
 ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1)Πώς το φαινόμενο Bohr επηρεάζει την πρόσδεση οξυγόνου στην αιμοσφαιρίνη; Που συνδέονται τα ιόντα
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1)Πώς το φαινόμενο Bohr επηρεάζει την πρόσδεση οξυγόνου στην αιμοσφαιρίνη; Που συνδέονται τα ιόντα
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ
 ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
Τα αμινοξέα αποτελούν τις δομικές μονάδες των πρωτεϊνών και αποτελούν βασικό στοιχείο των οργανισμών.
 ΑΜΙΝΟΞΕΑ Τα αμινοξέα αποτελούν τις δομικές μονάδες των πρωτεϊνών και αποτελούν βασικό στοιχείο των οργανισμών. Ο γενικός μοριακός τύπος ενός α- αμινοξέος παρουσιάζεται στο διπλανό σχήμα και συνίσταται
ΑΜΙΝΟΞΕΑ Τα αμινοξέα αποτελούν τις δομικές μονάδες των πρωτεϊνών και αποτελούν βασικό στοιχείο των οργανισμών. Ο γενικός μοριακός τύπος ενός α- αμινοξέος παρουσιάζεται στο διπλανό σχήμα και συνίσταται
ΑΜΙΝΟΞΕΑ ΠΕΠΤΙΔΙΑ ΠΡΩΤΕΪΝΕΣ
 ΑΜΙΝΟΞΕΑ ΠΕΠΤΙΔΙΑ ΠΡΩΤΕΪΝΕΣ Παππάς Χρήστος Επίκουρος καθηγητής ΑΜΙΝΟΞΕΑ Αμινοξέα είναι οργανικά μόρια που διαθέτουν καρβοξύλιο (-α) και αμινομάδα (-ες). Πλευρική αλυσίδα R NH 2 α O α- αμινοξύ OH Είναι
ΑΜΙΝΟΞΕΑ ΠΕΠΤΙΔΙΑ ΠΡΩΤΕΪΝΕΣ Παππάς Χρήστος Επίκουρος καθηγητής ΑΜΙΝΟΞΕΑ Αμινοξέα είναι οργανικά μόρια που διαθέτουν καρβοξύλιο (-α) και αμινομάδα (-ες). Πλευρική αλυσίδα R NH 2 α O α- αμινοξύ OH Είναι
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 6 ΣΕΛΙΔΕΣ
 ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Δ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Δ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
Kυτταρική Bιολογία ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΕΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ ΔIAΛEΞΗ 3 (7/3/2012) Δρ. Xρήστος Παναγιωτίδης, Τμήμα Φαρμακευτικής Α.Π.Θ.
 Kυτταρική Bιολογία ΔIAΛEΞΗ 3 (7/3/2012) ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΕΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ AΣ ΘYMHΘOYME Στην προηγούμενη διάλεξη μιλήσαμε για τη χημική σύσταση των κυττάρων και για τα βιολογικά πολυμερή που αποτελούν
Kυτταρική Bιολογία ΔIAΛEΞΗ 3 (7/3/2012) ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΕΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ AΣ ΘYMHΘOYME Στην προηγούμενη διάλεξη μιλήσαμε για τη χημική σύσταση των κυττάρων και για τα βιολογικά πολυμερή που αποτελούν
Φυσική Στερεών στις Πρωτεΐνες
 Φυσική Στερεών στις Πρωτεΐνες Νίκος Απ. Παπανδρέου Τ.Ε.Ι. Πειραιά Φεβρουάριος 2010 Ένα ελικοϊδές μονοπάτι Χημική δομή μίας πρωτεΐνης Μήκος αλυσίδας ~30 έως ~1000 αµινοξέα Συνολικός αριθµός ατόµων έως ~
Φυσική Στερεών στις Πρωτεΐνες Νίκος Απ. Παπανδρέου Τ.Ε.Ι. Πειραιά Φεβρουάριος 2010 Ένα ελικοϊδές μονοπάτι Χημική δομή μίας πρωτεΐνης Μήκος αλυσίδας ~30 έως ~1000 αµινοξέα Συνολικός αριθµός ατόµων έως ~
Εισαγωγή στη Μοριακή Προσοµοίωση
 Κεφάλαιο 6 Εισαγωγή στη Μοριακή Προσοµοίωση 6.1. Μοριακή Μηχανική 6.1.1. Εισαγωγή στη µεθοδολογία του «απ αρχής» διπλώµατος της πρωτείνης. Η ενέργεια κάθε µορίου µπορεί θεωρητικά να υπολογιστεί µε την
Κεφάλαιο 6 Εισαγωγή στη Μοριακή Προσοµοίωση 6.1. Μοριακή Μηχανική 6.1.1. Εισαγωγή στη µεθοδολογία του «απ αρχής» διπλώµατος της πρωτείνης. Η ενέργεια κάθε µορίου µπορεί θεωρητικά να υπολογιστεί µε την
Οργανική Χημεία. Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια
 Οργανική Χημεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν ομάδες υδροξυλίου συνδεδεμένες με κορεσμένα άτομα άνθρακα υβριδισμού sp 3 Βάσει παραπάνω ορισμού,
Οργανική Χημεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν ομάδες υδροξυλίου συνδεδεμένες με κορεσμένα άτομα άνθρακα υβριδισμού sp 3 Βάσει παραπάνω ορισμού,
Περίληψη Κεφαλαίου 2
 Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου. Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση:
 KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
Η κυτταρική µετατόπιση των πρωτεϊνών
 9-1 Κεφάλαιο 9 Η κυτταρική µετατόπιση των πρωτεϊνών Εισαγωγή Στο κύτταρο η έκφραση των πρωτεϊνών γίνεται από µόνο ένα τύπο ριβοσώµατος (εκτός των µιτοχονδριακών και των χλωροπλαστικών που µοιάζουν µε αυτά
9-1 Κεφάλαιο 9 Η κυτταρική µετατόπιση των πρωτεϊνών Εισαγωγή Στο κύτταρο η έκφραση των πρωτεϊνών γίνεται από µόνο ένα τύπο ριβοσώµατος (εκτός των µιτοχονδριακών και των χλωροπλαστικών που µοιάζουν µε αυτά
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
Οργανική Χημεία. Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες
 Οργανική Χημεία Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες 1. Γενικά Πρωτεΐνες: μεγάλα βιομόρια που απαντούν σε όλους τους ζωντανούς οργανισμούς Διαφορετικά είδη πρωτεϊνών με ποικίλη βιολογική
Οργανική Χημεία Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες 1. Γενικά Πρωτεΐνες: μεγάλα βιομόρια που απαντούν σε όλους τους ζωντανούς οργανισμούς Διαφορετικά είδη πρωτεϊνών με ποικίλη βιολογική
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης
 Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ. Καρβουντζή Ηλιάνα Βιολόγος
 Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημικά στοιχεία που συνθέτουν τους οργανισμούς Ο C, το H 2, το O 2 και το N 2 είναι τα επικρατέστερα στους οργανισμούς σε ποσοστό 96% κ.β. Γιατί; Συμμετέχουν σε σημαντικό βαθμό στη σύνθεση
Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημικά στοιχεία που συνθέτουν τους οργανισμούς Ο C, το H 2, το O 2 και το N 2 είναι τα επικρατέστερα στους οργανισμούς σε ποσοστό 96% κ.β. Γιατί; Συμμετέχουν σε σημαντικό βαθμό στη σύνθεση
Μεταβολισμός πρωτεϊνών και των αμινοξέων
 Μεταβολισμός πρωτεϊνών και των αμινοξέων Πρωτεΐνες Πολυσακχαρίτες Λίπη Γαλακτικό Γλυκόζη Αμινοξέα Πρωτεΐνες οργανισμού Δεξαμενή Αζώτου Πυροστα φυλικό Γλυκονεογένεση Γλυκόλυση Acetyl-CoA 6- φωσφορική Γλυκόζη
Μεταβολισμός πρωτεϊνών και των αμινοξέων Πρωτεΐνες Πολυσακχαρίτες Λίπη Γαλακτικό Γλυκόζη Αμινοξέα Πρωτεΐνες οργανισμού Δεξαμενή Αζώτου Πυροστα φυλικό Γλυκονεογένεση Γλυκόλυση Acetyl-CoA 6- φωσφορική Γλυκόζη
Τύποι νουκλεϊκών οξέων
 Τύποι νουκλεϊκών οξέων DNA ένας τύπος, μια λειτουργία RNA - 4 τύποι, 4 λειτουργίες Ριβοσωμικό RNA Αγγελιαφόρο RNA Μεταφορικό RNA Καταλυτικό RNA Βιοχημεία Ι Δ-1 Βιοχημεία Ι Δ-2 3 5 φωσφοδιεστερικός δεσμός
Τύποι νουκλεϊκών οξέων DNA ένας τύπος, μια λειτουργία RNA - 4 τύποι, 4 λειτουργίες Ριβοσωμικό RNA Αγγελιαφόρο RNA Μεταφορικό RNA Καταλυτικό RNA Βιοχημεία Ι Δ-1 Βιοχημεία Ι Δ-2 3 5 φωσφοδιεστερικός δεσμός
ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ, ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΕΙΚΟΝΑ 2.4 ΣΤΑΔΙΑ ΜΕΤΑΦΡΑΣΗΣ σ ε λ ί δ α 1 ΕΙΚΟΝΑ 4.2β ΕΡΩΤΗΣΕΙΣ 1. Να συμπληρώσετε τα κενά πλαίσια της εικόνας με την κατάλληλη λέξη ή φράση 2. Να γράψετε τον προσανατολισμό της μετακίνησης του ριβοσώματος
ΕΙΚΟΝΑ 2.4 ΣΤΑΔΙΑ ΜΕΤΑΦΡΑΣΗΣ σ ε λ ί δ α 1 ΕΙΚΟΝΑ 4.2β ΕΡΩΤΗΣΕΙΣ 1. Να συμπληρώσετε τα κενά πλαίσια της εικόνας με την κατάλληλη λέξη ή φράση 2. Να γράψετε τον προσανατολισμό της μετακίνησης του ριβοσώματος
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 24 ΜΑΪΟΥ 2013 ΕΚΦΩΝΗΣΕΙΣ
 ΘΕΜΑ A ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 24 ΜΑΪΟΥ 2013 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το
ΘΕΜΑ A ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 24 ΜΑΪΟΥ 2013 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το
Οργανική Χηµεία. Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια
 Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
οµή και λειτουργία των πρωτεϊνών TÚÈÙÔÙ Á ÔÌ
 οµή και λειτουργία των πρωτεϊνών Κρύσταλλοι ανθρώπινης ινσουλίνης. Η ινσουλίνη είναι µια πρωτεϊνική ορ- µόνη, απολύτως απαραίτητη για τη διατήρηση των επιπέδων του σακχάρου στο αίµα. (Κάτω) Αυτό που προσδιορίζει
οµή και λειτουργία των πρωτεϊνών Κρύσταλλοι ανθρώπινης ινσουλίνης. Η ινσουλίνη είναι µια πρωτεϊνική ορ- µόνη, απολύτως απαραίτητη για τη διατήρηση των επιπέδων του σακχάρου στο αίµα. (Κάτω) Αυτό που προσδιορίζει
20/3/2017. βουταναμίνη ή βούτυλ-αμίνη. 2-μέθυλ-προπαναμίνη ή ισό-βούτυλ-αμίνη. 1-μέθυλ-προπαναμίνη ή δευτεροταγής βούτυλ-αμίνη
 3 η ΣΕΙΡΑ ΑΣΚΗΣΕΩΝ 20/3/2017 1. Να γράψετε τη σκελετική δομή και να δώσετε το όνομα σε όλες τις πρωτοταγείς και δευτεροταγείς αμίνες με μοριακό τύπο 411 (1.5 μονάδα) Πρωτοταγείς αμίνες Η 2 βουταναμίνη
3 η ΣΕΙΡΑ ΑΣΚΗΣΕΩΝ 20/3/2017 1. Να γράψετε τη σκελετική δομή και να δώσετε το όνομα σε όλες τις πρωτοταγείς και δευτεροταγείς αμίνες με μοριακό τύπο 411 (1.5 μονάδα) Πρωτοταγείς αμίνες Η 2 βουταναμίνη
ΒΙΟΛΟΓΙΑ Β ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ
 ΕΚΠΑΙΔΕΥΤΗΡΙΑ ΣΥΓΧΡΟΝΗ ΠΑΙΔΕΙΑ ΒΙΟΛΟΓΙΑ Β ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΕΠΙΜΕΛΕΙΑ:Ν.ΠΑΠΑΓΙΑΝΝΗΣ 2 Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ 3 1. Ποια είναι τα επίπεδα οργάνωσης της ζωής και ποια τα χημικά χαρακτηριστικά της; Στην
ΕΚΠΑΙΔΕΥΤΗΡΙΑ ΣΥΓΧΡΟΝΗ ΠΑΙΔΕΙΑ ΒΙΟΛΟΓΙΑ Β ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΕΠΙΜΕΛΕΙΑ:Ν.ΠΑΠΑΓΙΑΝΝΗΣ 2 Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ 3 1. Ποια είναι τα επίπεδα οργάνωσης της ζωής και ποια τα χημικά χαρακτηριστικά της; Στην
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής
 ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ. Τα χημικά μόρια που οικοδομούν τους οργανισμούς
 ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ Τα χημικά μόρια που οικοδομούν τους οργανισμούς Μελέτη φαινομένου της ζωής o Η μελέτη του φαινομένου της ζωής ξεκινά από το μοριακό επίπεδο δηλαδή από τα χημικά μόρια που οικοδομούν
ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ Τα χημικά μόρια που οικοδομούν τους οργανισμούς Μελέτη φαινομένου της ζωής o Η μελέτη του φαινομένου της ζωής ξεκινά από το μοριακό επίπεδο δηλαδή από τα χημικά μόρια που οικοδομούν
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ. ΑΣΚΗΣΗ ΠΡΑΞΗΣ 10η ΕΙΣΑΓΩΓΗ ΣΤΙΣ ΠΡΩΤΕΪΝΕΣ
 ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΑΣΚΗΣΗ ΠΡΑΞΗΣ 10η ΕΙΣΑΓΩΓΗ ΣΤΙΣ ΠΡΩΤΕΪΝΕΣ 1 Δομή των αμινοξέων Τα αμινοξέα περιέχουν στο μόριο τους: Καρβοξύλιο και αμινομάδα. Τα αμινοξέα των πρωτεϊνών είναι α-αμινοξέα. Συνέπειες:
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΑΣΚΗΣΗ ΠΡΑΞΗΣ 10η ΕΙΣΑΓΩΓΗ ΣΤΙΣ ΠΡΩΤΕΪΝΕΣ 1 Δομή των αμινοξέων Τα αμινοξέα περιέχουν στο μόριο τους: Καρβοξύλιο και αμινομάδα. Τα αμινοξέα των πρωτεϊνών είναι α-αμινοξέα. Συνέπειες:
ΒΙΟΤΕΧΝΟΛΟΓΙΑ 1 ο ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΒΟΛΟΥ ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ
 ΚΕΦΑΛΑΙΟ 1ο ΒΙΟΤΕΧΝΟΛΟΓΙΑ 1 ο ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΒΟΛΟΥ 2010-11 ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 1 ο : ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΚΑΙ ΒΙΟΧΗΜΕΙΑ 1. Τι είναι η Βιοχημεία και με ποιες ενώσεις ασχολείται. 2. Πόσα και ποια στοιχεία
ΚΕΦΑΛΑΙΟ 1ο ΒΙΟΤΕΧΝΟΛΟΓΙΑ 1 ο ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΒΟΛΟΥ 2010-11 ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 1 ο : ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΚΑΙ ΒΙΟΧΗΜΕΙΑ 1. Τι είναι η Βιοχημεία και με ποιες ενώσεις ασχολείται. 2. Πόσα και ποια στοιχεία
Βιοφυσική. ΦΥΣ 415 Διδάσκων Σ. Σκούρτης (χειμερινό εξάμηνο ) 2 η διάλεξη
 Βιοφυσική ΦΥΣ 415 Διδάσκων Σ. Σκούρτης (χειμερινό εξάμηνο 2009-10) 2 η διάλεξη Πρωτεΐνες Πρωτεΐνη: πολυμερές από αμινοξέα 20 διαφορετικά αμινοξέα CH 2 Pro Ένα από αυτά είναι η Προλίνη CH 2 CH 2 NH C α
Βιοφυσική ΦΥΣ 415 Διδάσκων Σ. Σκούρτης (χειμερινό εξάμηνο 2009-10) 2 η διάλεξη Πρωτεΐνες Πρωτεΐνη: πολυμερές από αμινοξέα 20 διαφορετικά αμινοξέα CH 2 Pro Ένα από αυτά είναι η Προλίνη CH 2 CH 2 NH C α
 ΘΕΜΑ Α ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ' ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΛΑ Β ) ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από
ΘΕΜΑ Α ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ' ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΛΑ Β ) ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από
ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ
 Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Βιολογία Β Λυκείου θέματα
 Ι. Οι υδατάνθρακες διακρίνονται σε μονοσακχαρίτες, δισακχαρίτες και πολυσακχαρίτες. α) Να αναφέρετε από δύο παραδείγματα μονοσακχαριτών, δισακχαριτών και πολυσακχαριτών. (6μ) β) Σε ένα κύτταρο συναντώνται
Ι. Οι υδατάνθρακες διακρίνονται σε μονοσακχαρίτες, δισακχαρίτες και πολυσακχαρίτες. α) Να αναφέρετε από δύο παραδείγματα μονοσακχαριτών, δισακχαριτών και πολυσακχαριτών. (6μ) β) Σε ένα κύτταρο συναντώνται
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ
 ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράμμα που αντιστοιχεί στη σωστή απάντηση:
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΒΙΟΛΟΓΙΑ Ηµεροµηνία: Παρασκευή 25 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΒΙΟΛΟΓΙΑ Ηµεροµηνία: Παρασκευή 25 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
Δοµή και ιδιότητες του DNA. 09/04/2014 1 Μοριακή Βιολογία Κεφ. 1 Καθηγητής Δρ. Κ. Ε. Βοργιάς
 Δοµή και ιδιότητες του DNA 09/04/2014 1 Ορίζεται η γραµµική αλληλουχία των 4 βάσεων damp, dcmp, dgmp, dtmp που είναι συνδεδεµένες µε 3-5 φωσφοδιεστερικό δεσµό. AGCTCGCGTCGCTCACTCTCTGCAT! TCGAGCGCAGCGAGTGAGAGACGTA!
Δοµή και ιδιότητες του DNA 09/04/2014 1 Ορίζεται η γραµµική αλληλουχία των 4 βάσεων damp, dcmp, dgmp, dtmp που είναι συνδεδεµένες µε 3-5 φωσφοδιεστερικό δεσµό. AGCTCGCGTCGCTCACTCTCTGCAT! TCGAGCGCAGCGAGTGAGAGACGTA!
Από το Ελληνικό ρήµα «πρωτεύω» που αποδεικνύει τη σηµασία των πρωτεϊνών στην διατροφή του ανθρώπου
 Πρωτεΐνες 1 Από το Ελληνικό ρήµα «πρωτεύω» που αποδεικνύει τη σηµασία των πρωτεϊνών στην διατροφή του ανθρώπου Οι πρωτεΐνες είναι πολύπλοκα µόρια που περιέχουν 2 Είναι πηγές αµινοξέων (απαραίτητα, µη απαραίτητα)
Πρωτεΐνες 1 Από το Ελληνικό ρήµα «πρωτεύω» που αποδεικνύει τη σηµασία των πρωτεϊνών στην διατροφή του ανθρώπου Οι πρωτεΐνες είναι πολύπλοκα µόρια που περιέχουν 2 Είναι πηγές αµινοξέων (απαραίτητα, µη απαραίτητα)
Ανάλυση Τροφίμων. Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ. Τμήμα Τεχνολογίας Τροφίμων. Ακαδημαϊκό Έτος
 Ανάλυση Τροφίμων Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση:
Ανάλυση Τροφίμων Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση:
ΠΕΠΤΙΔΙΑ. Αναπ. Καθ. Γεράσιμος Μαλανδρίνος
 ΣΥΜΠΛΟΚΑ ΜΕΤΑΛΛΙΚΩΝ ΙΟΝΤΩΝ ΜΕ ΠΕΠΤΙΔΙΑ Αναπ. Καθ. Γεράσιμος Μαλανδρίνος Εισαγωγή Σπουδαιότητα μεταλλικών ιόντων σε βιολογικά συστήματα Πρωτείνες-ένζυμα μοντέλα τους πεπτίδια Βιοανόργανη Χημεία Εισαγωγή
ΣΥΜΠΛΟΚΑ ΜΕΤΑΛΛΙΚΩΝ ΙΟΝΤΩΝ ΜΕ ΠΕΠΤΙΔΙΑ Αναπ. Καθ. Γεράσιμος Μαλανδρίνος Εισαγωγή Σπουδαιότητα μεταλλικών ιόντων σε βιολογικά συστήματα Πρωτείνες-ένζυμα μοντέλα τους πεπτίδια Βιοανόργανη Χημεία Εισαγωγή
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1.Πώς οι κινητικές παράμετροι Κ m και K cat χρησιμεύουν για να συγκριθεί η ανακύκλωση διαφορετικών
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1.Πώς οι κινητικές παράμετροι Κ m και K cat χρησιμεύουν για να συγκριθεί η ανακύκλωση διαφορετικών
Κεφάλαιο 2. Μοτίβα πρωτεϊνικής δομής
 Κεφάλαιο 2 Μοτίβα πρωτεϊνικής δομής Εικόνα 2.1 Το μοντέλο του Kendrew για τη δομή χαμηλής διακριτικότητας της μυοσφαιρίνης όπως φαίνεται από τρεις διαφορετικές οπτικές γωνίες. Οι επιμήκεις περιοχές αντιπροσωπεύουν
Κεφάλαιο 2 Μοτίβα πρωτεϊνικής δομής Εικόνα 2.1 Το μοντέλο του Kendrew για τη δομή χαμηλής διακριτικότητας της μυοσφαιρίνης όπως φαίνεται από τρεις διαφορετικές οπτικές γωνίες. Οι επιμήκεις περιοχές αντιπροσωπεύουν
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001
 Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 6 ΣΕΛΙΔΕΣ
 ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΗΜΕΡΗΣΙΩΝ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΥ ΓΕΝΙΚΥ ΛΥΚΕΙΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΥ 2013 ΕΞΕΤΑΖΜΕΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΧΗΜΕΙΑ ΤΕΧΝΛΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΣ ΤΕΧΝΛΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΛ ΣΕΛΙΔΩΝ:
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΥ ΓΕΝΙΚΥ ΛΥΚΕΙΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΥ 2013 ΕΞΕΤΑΖΜΕΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΧΗΜΕΙΑ ΤΕΧΝΛΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΣ ΤΕΧΝΛΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΛ ΣΕΛΙΔΩΝ:
Διδάσκων: Καθηγητής Εμμανουήλ Μ. Παπαμιχαήλ
 Τίτλος Μαθήματος: Ενζυμολογία Ενότητα: Εισαγωγή Διδάσκων: Καθηγητής Εμμανουήλ Μ. Παπαμιχαήλ Τμήμα: Χημείας 8 1. EIΣAΓΩΓH Tα ένζυμα είναι οι καταλύτες της ζώσης ύλης. Καταλύουν τις χημικές αντιδράσεις,
Τίτλος Μαθήματος: Ενζυμολογία Ενότητα: Εισαγωγή Διδάσκων: Καθηγητής Εμμανουήλ Μ. Παπαμιχαήλ Τμήμα: Χημείας 8 1. EIΣAΓΩΓH Tα ένζυμα είναι οι καταλύτες της ζώσης ύλης. Καταλύουν τις χημικές αντιδράσεις,
