ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΜΕΑΣ ΥΓΕΙΑΣ ΤΟΥ ΠΑΙΔΙΟΥ Γ ΠΑΙΔΙΑΤΡΙΚΗ ΚΛΙΝΙΚΗ ΔΙΕΥΘΥΝΤΗΣ : ΚΑΘΗΓΗΤΗΣ ΙΩΑΝΝΗΣ Ι.
|
|
|
- Ζαρά Λαμπρόπουλος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΜΕΑΣ ΥΓΕΙΑΣ ΤΟΥ ΠΑΙΔΙΟΥ Γ ΠΑΙΔΙΑΤΡΙΚΗ ΚΛΙΝΙΚΗ ΔΙΕΥΘΥΝΤΗΣ : ΚΑΘΗΓΗΤΗΣ ΙΩΑΝΝΗΣ Ι. ΤΣΑΝΑΚΑΣ ΠΑΝΕΠ. ΕΤΟΣ: Αριθμός: 3116 ΘΕΜΑ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΣΥΣΧΕΤΙΣΗ ΤΗΣ ΚΑΤΑΝΑΛΩΣΗΣ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ ΦΑΡΜΑΚΩΝ ΚΑΙ ΜΙΚΡΟΒΙΑΚΗΣ ΑΝΤΟΧΗΣ ΣΕ ΤΡΙΤΟΒΑΘΜΙΟ ΝΟΣΟΚΟΜΕΙΟ. ΜΕΛΕΤΗ ΤΗΣ ΕΠΙΔΡΑΣΗΣ ΘΕΡΑΠΕΥΤΙΚΩΝ ΟΔΗΓΙΩΝ ΠΑΡΕΜΒΑΣΗΣ ΗΛΙΑ ΙΩΣΗΦΙΔΗ ΠΑΙΔΙΑΤΡΟΥ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΥΠΟΒΛΗΘΗΚΕ ΣΤΗΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΥ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΘΕΣΣΑΛΟΝΙΚΗ 2013
2 Η ΤΡΙΜΕΛΗΣ ΣΥΜΒΟΥΛΕΥΤΙΚΗ ΕΠΙΤΡΟΠΗ ΕΜΜΑΝΟΥΗΛ ΡΟΗΛΙΔΗΣ, ΚΑΘΗΓΗΤΗΣ ΠΑΥΛΟΣ ΝΙΚΟΛΑΪΔΗΣ, ΚΑΘΗΓΗΤΗΣ ΜΑΛΑΜΑΤΕΝΙΑ ΑΡΒΑΝΙΤΙΔΟΥ-ΒΑΓΙΩΝΑ, ΚΑΘΗΓΗΤΡΙΑ Η ΕΠΤΑΜΕΛΗΣ ΕΞΕΤΑΣΤΙΚΗ ΕΠΙΤΡΟΠΗ ΕΜΜΑΝΟΥΗΛ ΡΟΗΛΙΔΗΣ, ΚΑΘΗΓΗΤΗΣ ΠΑΥΛΟΣ ΝΙΚΟΛΑΪΔΗΣ, ΚΑΘΗΓΗΤΗΣ ΜΑΛΑΜΑΤΕΝΙΑ ΑΡΒΑΝΙΤΙΔΟΥ-ΒΑΓΙΩΝΑ, ΚΑΘΗΓΗΤΡΙΑ ΙΩΑΝΝΗΣ ΤΣΑΝΑΚΑΣ, ΚΑΘΗΓΗΤΗΣ ΝΙΚΟΛΑΟΣ ΜΑΛΙΣΙΟΒΑΣ, ΚΑΘΗΓΗΤΗΣ ΠΑΡΑΣΚΕΥΗ ΠΑΠΑΪΩΑΝΝΙΔΟΥ, ΚΑΘΗΓΗΤΡΙΑ ΧΑΡΑΛΑΜΠΟΣ ΑΝΤΑΧΟΠΟΥΛΟΣ, ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ «Ἡ ἔγκρισις τῆς Διδακτορικῆς Διατριβῆς ὑπό τῆς Ἰατρικῆς Σχολῆς τοῦ Ἀριστοτελείου Πανεπιστημίου Θεσσαλονίκης δεν ὑποδηλοῖ ἀποδοχήν τῶν γνωμῶν τοῦ συγγραφέως». (Νόμος 5343/32, ἄρθρ και ν. 1268/82. ἄρθρ. 50 8) 2
3 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΠΡΟΕΔΡΟΣ ΤΗΣ ΣΧΟΛΗΣ ΒΑΣΙΛΕΙΟΣ Κ. ΤΑΡΛΑΤΖΗΣ 3
4 Στον Πρόδρομό μου και στην Ελένη μου με αγάπη Στο δάσκαλό μου Ε. Ροηλίδη με σεβασμό 4
5 Στους γονείς μου με σεβασμό Στα αδέρφια και τα ανήψια μου με αγάπη 5
6 Περιεχόμενα ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ 9 ΠΡΟΛΟΓΟΣ ΓΕΝΙΚΟ ΜΕΡΟΣ Εισαγωγή Μικροβιακή αντοχή Ανάπτυξη αντοχής και υποκείμενοι μηχανισμοί στα Gram θετικά μικρόβια Ανάπτυξη αντοχής και υποκείμενοι μηχανισμοί στα εντεροβακτηριοειδή Ανάπτυξη αντοχής και υποκείμενοι μηχανισμοί στα αζυμωτικά Gram αρνητικά μικρόβια (Pseudomonas aeruginosa και Acinetobacter baumannii) Κλινική σημασία των λοιμώξεων από πολυανθεκτικά μικρόβια Συσχέτιση κατανάλωσης αντιμικροβιακών φαρμάκων και μικροβιακής αντοχής Αθροιστικά δεδομένα, διαχρονική συσχέτιση Αθροιστικά δεδομένα, γεωγραφική συσχέτιση Δεδομένα σε επίπεδο ασθενούς (μελέτες ασθενών μαρτύρων, μελέτες φάλαγγας) Παρέμβαση Ορθολογική χρήση αντιμικροβιακών Πρόληψη της οριζόντιας μετάδοσης μικροβίων Ο ρόλος της οριζόντιας μετάδοσης πολυανθεκτικών μικροβίων Τρόποι ελέγχου της οριζόντιας μετάδοσης πολυανθεκτικών μικροβίων.. 50 Α. Διοικητικά μέτρα- Τήρηση των κατευθυντήριων οδηγιών 51 Β1. Υγιεινή χεριών.. 52 Β2. Προφυλάξεις και απομόνωση ασθενών 54 6
7 Γ. Υγιεινή περιβάλλοντος Δ. Επιδημιολογική επιτήρηση των πολυανθεκτικών μικροβίων 56 Ε. Εκπαίδευση. 57 ΕΙΔΙΚΟ ΜΕΡΟΣ Σκοπός Μεθοδολογία Είδος μελέτης Χώρος και χρόνος μελέτης Μικροβιολογικά δεδομένα Κατανάλωση αντιμικροβιακών Αναδρομική μελέτη Παρέμβαση Παρέμβαση στο σύνολο του νοσοκομείου για τις λοιμώξεις από στελέχη K. pneumoniae ανθεκτικά στις καρβαπενέμες Παρέμβαση στη ΜΕΘ ενηλίκων Παρέμβαση στη ΜΕΘ παίδων Παρέμβαση στο παιδογκολογικό Παρέμβαση στη ΜΕΝ νεογνών Μικροβιολογία και μοριακές τεχνικές που χρησιμοποιήθηκαν στην παρέμβαση Στατιστική Αποτελέσματα Συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής: αθροιστικά δεδομένα, διατμηματική σύγκριση Κατανάλωση αντιμικροβιακών φαρμάκων Μικροβιακή αντοχή Συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής στις κλινικές του νοσοκομείου Συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής: 7
8 αθροιστικά δεδομένα, διαχρονική καταγραφή Αντοχές μικροβίων Κατανάλωση αντιμικροβιακών Συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής διαχρονικά Παρέμβαση στο σύνολο του νοσοκομείου για την K. pneumoniae Παρέμβαση στη ΜΕΘ ενηλίκων Παρέμβαση στη ΜΕΘ Παίδων Παρέμβαση στην παιδοογκολογική κλινική Παρέμβαση στη μονάδα εντατικής νοσηλείας νεογνών Συζήτηση Περίληψη Abstract Βιβλιογραφία
9 Συντομογραφίες AmpC : AmpC β lactamase, Ambler class C, Bush group 1 APACHE II : Acute Physiology and Chronic Health Evaluation II score CDC : Centers for Disease Control CLSI : Clinical and Laboratory Standards Institute CTX-M : Cefotaximase-M (ESBL) DDD : Defined Daily Doses DNA : Deoxyribonucleic acid DOT : Days Of Therapy ERIC-PCR : Enterobacterial Repetitive Intergenic Consensus PCR (ERIC-PCR) ESBL : Extended spectrum beta lactamase gyr A : Subunit of DNA gyrase IDSA : Infectious Disease Society of America IMP : Imipenemase (carbapenemase) IRAB : Imipenem resistant Acinetobacter baumannii KPC : Klebsiella pneumoniae carbapenemase KΕΕΛΠΝΟ : Κέντρο ελέγχου και πρόληψης νοσημάτων MATE : Multidrug efflux transporters MBL : Metallo-beta-lactamase MRSA : Methicillin Resistant Staphylococcus aureus OXA : Oxacillinase carbapenemase Par C : Subunit of DNA topoisomerase IV PCR : Polymerase Chain Reaction PFGE : Pulse Field Gel Electrophoresis Qnr : Plasmid-encoded quinolone resistance protein Qnr SIM : Seoul imipenemase SOFA : Sequential Organ Failure Assessment VIM : Verona imipenemase VRE : Vancomycin Resistant Enterococci WHO : World Health Organization 9
10 ΜΕΘ ΜΕΘΠΔ ΜΕΝΝ : Μονάδα Εντατικής Θεραπείας : Μονάδα Εντατικής Θεραπείας Παίδων : Μονάδα Εντατικής Νοσηλείας Νεογνών 10
11 Πρόλογος Η ανακάλυψη των αντιμικροβιακών φαρμάκων αποτέλεσε ορόσημο στην ιστορία της ιατρικής. Η χρήση τους στην αντιμετώπιση των βακτηριακών λοιμώξεων ξεκίνησε τη δεκαετία του 1930 με τις σουλφοναμίδες και συνέχισε στις δεκαετίες , που ονομάστηκε μάλιστα χρυσή εποχή των αντιμικροβιακών. Την εποχή εκείνη ανακαλύφθηκαν οι περισσότερες κατηγορίες αντιμικροβιακών φαρμάκων που χρησιμοποιούνται σήμερα και παρασκευάστηκαν οι περισσότερες συνθετικές μορφές τους. Από το 1990 και έπειτα, η παραγωγή νέων αντιμικροβιακών μειώθηκε δραστικά, και πλέον πολύ λίγα νέα αντιμικροβιακά φάρμακα έχουν εγκριθεί για χρήση τα τελευταία χρόνια. Παράλληλα, η εμφάνιση και εξάπλωση της μικροβιακής αντοχής ξεκίνησε λίγα χρόνια μετά τη χρήση των πρώτων αντιμικροβιακών φαρμάκων ώστε σήμερα να αποτελεί σημαντικό πρόβλημα δημόσιας υγείας. Μάλιστα, από το 2004 η διεθνής κοινότητα με γραπτές αναφορές σε άρθρα προμηνύει τον κίνδυνο έναρξης μιας νέας εποχής στην ιατρική, μιας εποχής χωρίς δραστικά αντιμικροβιακά. Το πρόβλημα της εμφάνισης λοιμώξεων από ανθεκτικά μικρόβια στη σύγχρονη ιατρική είναι ακόμη πιο έντονο και ίσως η κατάσταση να είναι χειρότερη με αυτήν της εποχής πριν την ανακάλυψη των αντιμικροβιακών. Τα αντιμικροβιακά φάρμακα έχουν ελαττώσει τη νοσηρότητα και θνητότητα των μικροβιακών λοιμώξεων ιδίως σε ειδικές ομάδες ασθενών της σύγχρονης ιατρικής πράξης όπως είναι οι βαρέως πάσχοντες ασθενείς των μονάδων εντατικής θεραπείας, οι μεταμοσχευμένοι ασθενείς, οι ογκολογικοί και αιματολογικοί ασθενείς και άλλες ειδικές κατηγορίες ασθενών. Πλέον, έχει αποδειχθεί ότι κινητήρια δύναμη στην εμφάνιση και εξάπλωση της αντοχής στα μικρόβια αποτελεί η αλόγιστη χρήση των αντιμικροβιακών φαρμάκων. Παρότι αυτή η συσχέτιση έχει βρεθεί σε μελέτες τόσο σε ανθρώπους -εντός και εκτός νοσοκομείου- όσο και σε ζώα, η άμεση ποσοτική σχέση μεταξύ της κατανάλωσης αντιμικροβιακών και εμφάνισης αντοχής δεν έχει ακόμη προσδιορισθεί. Είναι επομένως επιτακτική ανάγκη η παρέμβαση με τη λήψη κατάλληλων μέτρων για την αντιμετώπιση του προβλήματος της μικροβιακής αντοχής. Τα μέτρα αυτά θα πρέπει να κατευθύνονται τόσο στο θέμα της ορθολογικής χρήσης των αντιμικροβιακών φαρμάκων όσο και στην πρόληψη της οριζόντιας μετάδοσης ανθεκτικών μικροβίων μεταξύ των ασθενών. Για το λόγο αυτό, ιδίως στα νοσοκομεία, χρειάζεται η εφαρμογή πολιτικών για την καθοδήγηση στη σωστή χρήση των αντιμικροβιακών φαρμάκων και μείωση της άσκοπης και αλόγιστης χρήσης 11
12 τους. Επιπλέον, η εφαρμογή πολιτικών συμμόρφωσης με την υγιεινή των χεριών, τις προφυλάξεις επαφής και άλλων πιο εξειδικευμένων μέτρων, έχει καθοριστική σημασία στην πρόληψη της οριζόντιας μετάδοσης μικροβίων. Σκοπός της διατριβής αυτής ήταν η διερεύνηση της σχέσης μεταξύ κατανάλωσης αντιμικροβιακών και εμφάνισης αντοχής σε συνδυασμό με την εφαρμογή μέτρων παρέμβασης, ώστε να αντιμετωπισθεί το σοβαρό πρόβλημα της αντοχής των μικροβίων που προκαλούν λοιμώξεις σε νοσηλευόμενους ασθενείς σε τριτοβάθμιο νοσοκομείο. Η διατριβή αυτή αποτελείται από το γενικό και το ειδικό μέρος. Στο γενικό μέρος, αναφέρεται το πρόβλημα της αντοχής στα συχνότερα νοσοκομειακά παθογόνα και οι μηχανισμοί ανάπτυξής της. Επιπλέον, επισημαίνεται η κλινική σημασία της απομόνωσης ανθεκτικών μικροβίων στις νοσοκομειακές λοιμώξεις. Στη συνέχεια, αναφέρονται τα δεδομένα της συσχέτισης μεταξύ κατανάλωσης και αντιμικροβιακών φαρμάκων. Ακολουθεί η αναφορά στην παρέμβαση για την αντιμετώπιση του προβλήματος της μικροβιακής αντοχής και αναλυτικότερα στην ορθολογική χρήση των αντιμικροβιακών φαρμάκων και στην πρόληψη της οριζόντιας μετάδοσης ανθεκτικών μικροβίων. Στα πλαίσια υλοποίησης της παρούσας διδακτορικής διατριβής, μετά από επιτυχή συμμετοχή στους διαγνωνισμούς του προγράμματος υποτροφιών για μεταπτυχιακές σπουδές στην Ελλάδα στην ειδίκευση «Ιατρική», έλαβα υποτροφία από το Ίδρυμα Κρατικών Υποτροφιών (ΙΚΥ, σύμβαση αριθμός 5337). Στο συγκεκριμένο σημείο, νιώθω την ανάγκη να εκφράσω τις ευχαριστίες μου από καρδιάς, σε όλους αυτούς που συνέβαλαν, ώστε η εκπόνηση και η υλοποίηση της συγκεκριμένης διατριβής να γίνει πραγματικότητα. Πρωτίστως, θα ήθελα να εκφράσω την ευγνωμοσύνη μου στον Καθηγητή κ. Εμμανουήλ Ροηλίδη για την ανάθεση του θέματος της διδακτορικής διατριβής και την αμέριστη καθοδήγησή του. Η συνεχής επίβλεψη και η συνεργασία μαζί του ήταν πολύτιμες, όχι μόνο για την αξιολόγηση των ευρημάτων και την τελική διαμόρφωση του κειμένου της διατριβής αυτής, αλλά και για περαιτέρω επιστημονικές αναζητήσεις που υπήρξαν καθοριστικές για μένα. Ευχαριστώ θερμά τον Καθηγητή κ. Νικολαΐδη Παύλο, μέλος της τριμελούς επιτροπής, για το ενδιαφέρον του, τη συμπαράσταση και την εμπιστοσύνη που έδειξε σε όλα τα στάδια της παρούσας διδακτορικής διατριβής. Την Καθηγήτρια κ. Αρβανιτίδου-Βαγιωνά, μέλος της τριμελούς επιτροπής, ευχαριστώ από καρδιάς για το ειλικρινές ενδιαφέρον για την ολοκλήρωση 12
13 της προσπάθειας αυτής, καθώς και τις πολύτιμες υποδείξεις της για τη βαθύτερη κατανόηση των αρχών της επιδημιολογίας των νοσοκομειακών λοιμώξεων. Τον Καθηγητή και Διευθυντή της Γ Παιδιατρικής Κλινικής του ΑΠΘ κ. Ιωάννη Τσανάκα, ευχαριστώ θερμά για την άμεση συμπαράστασή του για την ολοκλήρωση της παρούσας διδακτορικής διατριβής. Την Καθηγήτρια και πρώην Διευθύντρια της Γ Παιδιατρικής Κλινικής του ΑΠΘ κ. Θεοδούλη Παπασταύρου-Μαυρουδή, για την ευκαιρία που μου έδωσε μαζί με τον πρώτο επιβλέποντα, να εκπονήσω την διδακτορική μου διατριβή στη Γ Παιδιατρική Κλινική. Θα ήθελα να απευθύνω τις ευχαριστίες μου προς τον Επίκουρο Καθηγητή κ. Χαράλαμπο Ανταχόπουλο για την ουσιαστική του βοήθεια, τις πολύτιμες υποδείξεις και την αμέριστη συμπαράστασή του καθόλη τη διάρκεια της υλοποίησης της παρούσας διατριβής. Εκ βαθέων ευχαριστώ την Καθηγήτρια και πρώην Διευθύντρια του Μικροβιολογικού εργαστηρίου του Ιπποκρατείου νοσοκομείου Θεσσαλονίκης κ. Δανάη Σοφιανού, για τη συνεργασία και τις πολύτιμες συμβουλές της στα μικροβιολογικά δεδομένα της διατριβής, καθώς και τις εύστοχες παρατηρήσεις και την ουσιαστική καθοδήγησή της στην μελέτη των μηχανισμών αντοχής των μικροβίων. Παράλληλα, θα ήθελα να εκφράσω τις ευχαριστίες μου στην κ. Μαρία Μαλλογιάννη και στην κ. Γεωργία Κυθρεώτου, καθώς και στους συναδέλφους μικροβιολόγους κ. Ευσταθία Πρωτονοταρίου, κ. Αλεξία Ζαγοριανού, και σε όλο το προσωπικό του μικροβιολογικού εργαστηρίου που με βοήθησαν σημαντικά κατά τη διάρκεια της διδακτορικής διατριβής. Ιδιαίτερα θα ήθελα να ευχαριστήσω τον Καθηγητή κ. Σπύρο Πουρνάρα, από το Πανεπιστημιακό Νοσοκομείο Λάρισας του Πανεπιστημίου Θεσσαλίας, για την πολύτιμη βοήθειά του στη μοριακή τυποποίηση ανθεκτικών μικροβίων. Ένα μεγάλο ευχαριστώ στους Διευθυντές των κλινικών που συνεργαστήκαμε, για την υλοποίηση της παρέμβασης για την καταπολέμηση των λοιμώξεων από πολυανθεκτικά μικρόβια. Ευχαριστώ πολύ την Καθηγήτρια και Διευθύντρια της Α Μοναδας εντατικής νοσηλείας νεογνών του ΑΠΘ κ. Βασιλική Δρόσου-Αγακίδου, όπως επίσης και το προσωπικό της κλινικής της Α ΜΕΝΝ για την πολύτιμη συνεργασία τους στην αντιμετώπιση του προβλήματος των πολυανθεκτικών μικροβίων στα νεογνά. Τη Διευθύντρια της ΜΕΘ ενηλίκων κ. Νικολέτα Γρίτση-Γερογιάννη και την κ. Ελένη Μουλούδη, ευχαριστώ θερμά για την ουσιαστική βοήθεια στην επίλυση των προβλημάτων αντοχής στη μονάδα. Τη Διευθύντρια της ΜΕΘ παίδων κ. Μαρία Σδούγκα, ευχαριστώ πολύ για τη συμπαράστασή της που μαζί με το προσωπικό της 13
14 κλινικής συνέβαλε στην προσπάθεια αντιμετώπισης των νοσοκομειακών λοιμώξεων στα νοσηλευόμενα παιδιά. Τον Διευθυντή της Παιδοογκολογικής Κλινικής κ. Δημήτρη Κολιούσκα ιδιαίτερα τον ευχαριστώ για την άριστη συνεργασία και συμπαράσταση, στην αντιμετώπιση λοιμώξεων από πολυανθεκτικά μικρόβια σε παιδιατρικούς ογκολογικούς ασθενείς. Θα ήθελα επίσης, να εκφράσω τις ευχαριστίες μου στους νοσηλευτές νοσοκομειακών λοιμώξεων κ. Ιωάννη Στάθη, κ. Βασιλική Πέντσογλου, κ. Μαρία Καπερώνη και κ. Χρύσα Τσιγγαροπούλου για την πολύ καλή συνεργασία καθόλη τη διάρκεια της παρούσας διδακτορικής διατριβής και ιδίως στην αντιμετώπιση της οριζόντιας μετάδοσης ανθεκτικών μικροβίων μεταξύ νοσηλευόμενων ασθενών. Ιδιαίτερα ευχαριστώ τη νυν Διευθύντρια του Φαρμακείου κ. Ιφιγένεια Χρήστου, καθώς και τις πρώην Διευθύντριες κ. Θεανώ Κυριαζή και κ. Αναστασία Αργυρίου για την παροχή των δεδομένων του Φαρμακείου και το προσωπικό της στατιστικής υπηρεσίας του νοσοκομείου κ. Γιαννούλα Εμμανουηλίδου και Χριστίνα Γεωργακοπούλου για τη σημαντική βοήθειά τους στην παροχή των στατιστικών δεδομένων του νοσοκομείου. Θερμές ευχαριστίες θα ήθελα να εκφράσω στον Καθηγητή κ. Θεοκλή Ζαούτη και την Καθηγήρια κ. Susan Coffin, παιδιάτρων-λοιμωξιολόγων στο Νοσοκομείο Παίδων της Φιλαδέλφειας, Πενσυλβάνια, ΗΠΑ, για την καθοδήγηση και τις πολύτιμες συμβουλές τους σε θέματα ορθολογικής χρήσης αντιμικροβιακών και πρόληψης οριζόντιας μετάδοσης μικροβίων, κατά την παραμονή μου στο νοσοκομείο παίδων της Φιλαδέλφειας (Children s Hospital of Philadelphia). Επίσης, ιδιαίτερα ευχαριστώ τους συναδέλφους της παιδιατρικής λοιμωξιολογίας κ. Ασπασία Κατράγκου και κ. Όλγα Τσιάτσιου για τη βοήθειά τους στην αντιμετώπιση των επιδημιών από ανθεκτικά μικρόβια. Το προσωπικό του ερευνητικού εργαστηρίου Λοιμώξεων της Γ Παιδιατρικής Κλινικής και ιδιαίτερα την Διδάκτορα βιολόγο κ. Μαρία Σιμιτσοπούλου την ευχαριστώ πολύ για το συνεχές ενδιαφέρον και τη συμπαράσταση κατά τη διάρκεια υλοποίησης της παρούσας διδακτορικής διατριβής. Τις φοιτήτριες της ιατρικής κ. Βασιλική Μπαρμπαρούση, Σταυρούλα Μπουκουβάλα και Θεοδώρα Παπανικολάου τις ευχαριστώ πολύ για τη συνεργασία στην καταγραφή δεδομένων από το Φαρμακείο του νοσοκομείου. 14
15 ΓΕΝΙΚΟ ΜΕΡΟΣ 15
16 1. Εισαγωγή Η εμφάνιση και εξάπλωση των μικροβίων ανθεκτικών στα διαθέσιμα αντιμικροβιακά φάρμακα στα νοσοκομεία δημιουργεί σοβαρά προβλήματα στην αντιμετώπιση των μικροβιακών λοιμώξεων και επηρεάζει δυσμενώς τη νοσηρότητα, τη διάρκεια νοσηλείας, καθώς και τη θνητότητα των ασθενών (Giamarellos-Bourboulis και συν 2006). Είναι γεγονός ότι τα τελευταία χρόνια, έχει σημειωθεί σημαντική αύξηση στην κατανάλωση αντιμικροβιακών τόσο σε επίπεδο νοσοκομείου όσο και στην κοινότητα (Goossens και συν 2005, Ferech και συν 2006, Kritsotakis και συν 2006). Η ευρεία κατανάλωση των αντιμικροβιακών φαρμάκων, και ιδίως η μη ορθολογική χρήση τους, έχει ως αποτέλεσμα την αύξηση του κόστους, αλλά κατά κύριο λόγο την ανάπτυξη ανθεκτικών μικροβίων (Goossens και συν 2005, Ferech και συν 2006, Levy 2002, Gaynes και συν 1997). Σύμφωνα με τις έως τώρα ενδείξεις, η κατανάλωση των αντιμικροβιακών φαρμάκων αποτελεί έναν από τους παράγοντες που επηρεάζουν την εμφάνιση και επικράτηση ανθεκτικών μικροβίων. Παρόλα αυτά, η ακριβής σχέση μεταξύ της κατανάλωσης αντιμικροβιακών φαρμάκων και της ανάπτυξης αντοχής παραμένει πολύπλοκη και δύσκολη στην κατανόησή της (Levy 2002, Gaynes και συν 1997, Austin και συν 1999). Οι μελέτες που εξετάζουν αυτήν τη σχέση έχουν πολλές φορές διαφορετική μεθοδολογία και καταλήγουν σε ποικίλα συμπεράσματα, πολλές φορές διαφορετικά μεταξύ τους (Goossens και συν 2005, Neuhauser και συν 2003, Kern και συν 2005a, Ena και συν 1998, Boccia και συν 2004, Bassetti και συν 2006, Jacobson και συν 1995, Hsueh και συν 2005). Πιο συγκεκριμένα, η συσχέτιση αυτή έχει μελετηθεί χρησιμοποιώντας αθροιστικά δεδομένα σε σχέση με το χρόνο και το χώρο, αλλά και δεδομένα σε επίπεδο ασθενούς. Αναλυτικά, σε ό,τι αφορά το χρόνο, έχει μελετηθεί κατά πόσο οι μεταβολές στην κατανάλωση αντιμικροβιακών φαρμάκων επηρεάζουν την ανάπτυξη μικροβιακής αντοχής σε διάφορα χρονικά διαστήματα. Αντίστοιχα για το χώρο, υπάρχουν μελέτες που αναλύουν τη σχέση μεταξύ κατανάλωσης αντιμικροβιακών φαρμάκων σε ορισμένες περιοχές (κλινικές, νοσοκομεία, σύνολο μιας χώρας, κ.λπ.) με την εμφάνιση ανθεκτικών μικροβίων. Τέλος, σε επίπεδο ασθενούς, υπάρχουν μελέτες ασθενών-μαρτύρων στις οποίες διερευνάται κατά πόσο προηγούμενη έκθεση σε αντιμικροβιακά αυξάνει τον κίνδυνο εμφάνισης ανθεκτικών μικροβίων (Neuhauser και συν 2003, Kern και συν 2005b, Boccia και συν 2004, Hsueh και συν 2005, Katragkou και συν 2006, Vander Stichele και συν 2006). 16
17 Με εξαίρεση τις μελέτες ασθενών-μαρτύρων, οι υπόλοιπες μελέτες έχουν γίνει σε επίπεδο διακρατικό και εθνικό χρησιμοποιώντας δεδομένα είτε μόνο από τα νοσοκομεία είτε μόνο από την κοινότητα ή συνδυασμό αυτών. Παρά τη μεγάλη αξία των συμπερασμάτων που προκύπτουν από τις παραπάνω μελέτες, πολύ συχνά αναφέρεται ότι η ανάπτυξη αντοχής αφορά κυρίως στο τι γίνεται σε τοπικό επίπεδο και ιδίως σε επίπεδο κλινικής. Επομένως, η μελέτη της κατανάλωσης των αντιμικροβιακών φαρμάκων και της αντοχής των μικροβίων χρειάζεται να γίνεται όχι μόνο σε επίπεδο συνόλου του νοσοκομείου, αλλά και στην κάθε κλινική ξεχωριστά. Υπάρχουν μελέτες που αναφέρονται στη συσχέτιση αυτή σε επίπεδο νοσοκομειακών κλινικών. Ωστόσο, τις περισσότερες φορές αναφέρονται σε συγκεκριμένες μόνο κλινικές, κυρίως μονάδες εντατικής θεραπείας ενηλίκων. Η καλύτερη κατανόηση της σχέσης μεταξύ κατανάλωσης αντιμικροβιακών φαρμάκων και αντοχής σε όλα τα επίπεδα, αποτελεί ουσιαστικά το πρώτο βήμα για την προσπάθεια ελέγχου και στη συνέχεια μείωσης της μικροβιακής αντοχής. Όπως πρόσφατα ανακοινώθηκε από το Κέντρο Ελέγχου Λοιμώξεων στις ΗΠΑ (Centers for Disease Control and Prevention, CDC), η πρόληψη της ανάπτυξης μικροβιακής αντοχής ουσιαστικά κατευθύνεται σε τέσσερις κύριους τομείς, ένας εκ των οποίων είναι και η ορθολογική χρήση των αντιμικροβιακών φαρμάκων. Οι άλλοι τομείς περιλαμβάνουν την πρόληψη των λοιμώξεων, τη σωστή διάγνωση και θεραπεία των λοιμώξεων, και την αποφυγή μετάδοσής τους (Dellit και συν 2007, Siegel και συν 2007a, Hay 2006, French 1993, Solomon και συν 2001, Davey και συν 2005). Ο τρόπος εφαρμογής αλλά και η πραγματική αποτελεσματικότητα των παραπάνω μέτρων αποτελεί σημαντικό πεδίο μελέτης. Η εκπαίδευση του προσωπικού και οι γραπτές κατευθυντήριες οδηγίες αποτελούν βασικούς τρόπους εφαρμογής των μέτρων, όμως δεν αρκούν για την πλήρη αποτελεσματικότητά τους. Η συστηματική και λεπτομερής εξέταση της εφαρμογής των μέτρων και η ενσωμάτωση των απαραίτητων αλλαγών με απώτερο σκοπό την πρόληψη της μικροβιακής αντοχής, είναι ο μόνος τρόπος που έχει αποδειχθεί ότι είναι αποτελεσματικός. Μέχρι σήμερα λίγα είναι τα δεδομένα που είναι δημοσιευμένα και τεκμηριωμένα με τη σωστή μεθοδολογία. Με βάση τα δεδομένα αυτά, μπορούν να εφαρμοστούν όλα τα παραπάνω μέτρα, και ιδιαίτερα σε ορισμένες ομάδες ασθενών, μεταξύ των οποίων και μονάδες εντατικής θεραπείας ενηλίκων και παιδιών (Dellit και συν 2007, Siegel και συν 2007a, Hay 2006, French 1993, Solomon και συν 2001, Davey και συν 2005). 17
18 2. Μικροβιακή αντοχή Η ανάπτυξη αντοχής των παθογόνων στα αντιμικροβιακά φάρμακα αποτελεί πλέον ένα συνηθισμένο φαινόμενο. Ανάλογα με το είδος της αντοχής και τις λοιμώξεις που προκαλεί ο μικροοργανισμός, μπορεί να προκαλεί σημαντικά κλινικά προβλήματα, όπως είναι η αποτυχία της θεραπευτικής επιλογής, ο περιορισμός του θεραπευτικού σχήματος και άλλα προβλήματα που θα αναλυθούν στη συνέχεια (Livermore και συν 2001a, Strateva και συν 2009). Η ανάπτυξη αντοχής στα μικρόβια μπορεί να είναι είτε ενδογενής είτε επίκτητη. Η επίκτητη ανάπτυξη αντοχής μπορεί να γίνει μετά από αυτόματες μεταλλάξεις στο γονιδίωμα του μικροβίου (μεταλλαγές του χρωμοσωματικού DNA, mutations) ή μετά από μεταφορά εξωγενούς γενετικού υλικού από άλλα μικρόβια (οριζόντια μετάδοση γονιδίων). Ο πρώτος τρόπος που αφορά τις μεταλλαγές στο χρωμοσωματικό DNA συμβαίνει σπανιότερα. Όταν όμως δημιουργούνται τα ανθεκτικά γονίδια, και εφόσον υπάρχει έκθεση στον αντιμικροβιακό παράγοντα τότε μέσω της φυσικής επιλογής έχουμε επικράτηση και κλωνική διασπορά της αντοχής. Ο δεύτερος τρόπος, που είναι και ο συχνότερος, αφορά την οριζόντια μετάδοση γονιδίων αντοχής, η οποία γίνεται με τρεις τρόπους: μεταγωγή, σύζευξη και μεταμόρφωση. Στη μεταγωγή έχουμε μεταφορά γονιδίων με τη μεσολάβηση φάγων, στη σύζευξη έχουμε απευθείας μεταφορά γονιδίων μεταξύ δύο μικροβίων και τέλος στη μεταμόρφωση έχουμε πρόσληψη γονιδίου από το περιβάλλον. Η τελευταία είναι ιδιαίτερη συχνή στους πνευμονιοκόκκους, ενώ η σύζευξη είναι πολύ συχνή στα Gram αρνητικά μικρόβια (σχήμα 1). Φορείς των ανθεκτικών γονιδίων μπορεί να είναι τα πλασμίδια, εξωχρωμοσωματικά και κυκλικά, διπλής έλικας μόρια DNA, ή να είναι μικρότερες γονιδιακές μονάδες, τα μεταθετά στοιχεία ή ιντεγκρόνια (integrons), καθώς και τα τρανσποζόνια (transponsons, σχήμα 1). 18
19 Σχήμα 1: Τρόποι μεταφοράς γονιδίων και φορείς γονιδίων αντοχής. Η επίκτητη αντοχή ενός μικροβίου στα αντιμικροβιακά, συνήθως εμφανίζεται μετά την ευρεία χρήση τους. Μάλιστα, αυτή η σχέση τις περισσότερες φορές αφορά συγκεκριμένο συνδυασμό αντιμικροβιακού και μικροβίου, όπως φαίνεται στον πίνακα 1. Ανεξάρτητα όμως από τον τρόπο που αποκτούν τα μικρόβια τα γονίδια αντοχής, οι μηχανισμοί (βιοχημικοί) μέσω των οποίων εμφανίζουν αυτήν την αντοχή συνήθως είναι κοινοί στα διάφορα μικρόβια, όπως φαίνεται στο παρακάτω σχήμα 2 (Livermore και συν 2001a, Strateva και συν 2009, Lipsitch και συν 2002) Ανάπτυξη αντοχής και υποκείμενοι μηχανισμοί στα Gram θετικά μικρόβια Από τα Gram θετικά μικρόβια, τέσσερις μικροοργανισμοί εμφανίζουν κυρίως κλινικό ενδιαφέρον: οι σταφυλόκοκκοι, οι εντερόκοκκοι, ο πνευμονιόκοκκος και ο πυογόνος στρεπτόκοκκος. Οι δύο πρώτοι μικροοργανισμοί αποτελούν και τα συχνότερα Gram θετικά νοσοκομειακά παθογόνα και η αναφορά θα περιοριστεί στους δύο αυτούς μικροοργανισμούς. 19
20 Σχήμα 2: Κοινοί και ειδικοί βιοχημικοί μηχανισμοί αντοχής των μικροβίων: Α) αδρανοποίηση του αντιμικροβιακού φαρμάκου, Β) τροποποίηση του αντιμικροβιακού φαρμάκου, οπότε και καθίσταται ανενεργό, Γ) ενεργητική και γρήγορη απομάκρυνσή του -μηχανισμός αντλίας-, Δ) μειωμένη διαπερατότητα του μικροβίου στο αντιμικροβιακό, Ε) ενίσχυση του στόχου του αντιμικροβιακού φαρμάκου, Ζ) τροποποίηση του στόχου δράσης του αντιμικροβιακού φαρμάκου έτσι ώστε να είναι αδύνατη η δράση του, Η) παράκαμψη του μηχανισμού που επηρεάζει το αντιμικροβιακό φάρμακο (Τροποποιημένο, Livermore και συν 2001a, Strateva και συν 2009, Lipsitch και συν 2002). Από τους σταφυλόκοκκους σημαντικό νοσοκομειακό παθογόνο αποτελεί ο χρυσίζων σταφυλόκοκκος (Staphylococcus aureus). Η αντοχή στη μεθικιλλίνη των στελεχών S. aureus (methicillin resistant S. aureus) καθορίζεται είτε από την ελάχιστη ανασταλτική συγκέντρωση (Minimal Inhibitory Concentration, MIC >2 mg/l) είτε από την παρουσία του ειδικού γονιδίου meca (CLSI 2007) και ουσιαστικά σημαίνει ταυτόχρονα αντοχή σε όλα τα β-λακταμικά αντιμικροβιακά. Μετά την πρώτη εμφάνιση των στελεχών MRSA στη δεκαετία του 1960, πρόσφατες επίσημες καταγραφές στις ΗΠΑ αναφέρουν ότι σε ασθενείς που νοσηλεύονται σε μονάδες εντατικής θεραπείας (ΜΕΘ), πάνω από το 60% των χρυσιζόντων σταφυλόκοκκων είναι MRSA (NNIS 2004). Πλέον, υπάρχουν στελέχη MRSA που εμφανίζονται σε λοιμώξεις της κοινότητας, με συχνότερες τις λοιμώξεις δέρματος, του μυοσκελετικού συστήματος, και της πνευμονίας (εικόνα 1). Το γεγονός αυτό, αποτελεί ένα ιδιαίτερο θεραπευτικό πρόβλημα, καθώς περιορίζονται οι δυνατότητες για αποτελεσματική αντιμικροβιακή θεραπεία (Nygaard και συν 20
21 Πίνακας 1: Μικροβιακή αντοχή: η ανακάλυψη αντιμικροβιακών (δράση) και η ανάπτυξη αντοχής (αντίδραση). Αντιμικροβιακός παράγοντας Ανακάλυψη (κυκλοφορία) 1 η αναφορά αντοχής Μηχανισμός αντοχής Μικροοργανισμός Πενικιλλίνη G 1940 (1943) 1940 Πενικιλλινάση Staphylococcus aureus Τετρακυκλίνη 1948 (1952) 1952 Αντλία εξώθησης Shigella dysenteriae Ερυθρομυκίνη 1952 (1955) S rrna μεθυλίωση S. aureus Βανκομυκίνη 1956 (1972) 1988, 2004 D-Ala-D-Ala ανταλλαγή Enterococcus faecalis, S. aureus Μεθικιλλίνη 1959 (1961) 1961 MecA (PPP2a) S. aureus Γενταμικίνη 1963 (1967) 1969 Τροποποιητικά ένζυμα Ναλιδιξικό οξύ 1962 (1964) 1966 Μεταλλάξεις τοποϊσομεράσης S. aureus Esherichia coli Κεφοταξίμη 1975 (1981) 1981, 1983 AmpC β- λακταμάσες, ESBL Enterobacteriaceae Ιμιπενέμη 1976 (1987) 1986 Επίκτητες καρβαπενεμάσες Λινεζολίδη 1979 (2000) S RNA μεταλλάξεις Δαπτομυκίνη 1980 (2004) 2005 Δεν έχουν καθοριστεί σαφώς Pseudomonas aeruginosa, Serratia marcescens S. aureus, E. faecalis S. aureus, E. faecalis Livermore και συν 2001a, Strateva και συν 2009, Lipsitch και συν
22 2008, Diep 2008). Ένα άλλο πρόβλημα που έχει προκύψει είναι η εμφάνιση μειωμένης ευαισθησίας του χρυσίζοντα σταφυλόκοκκου στα γλυκοπεπτίδια. Η εμφάνιση πλήρους αντοχής στα γλυκοπεπτίδια εξακολουθεί να είναι σπάνια, και μέχρι σήμερα έχουν απομονωθεί πολύ λίγα στελέχη με αντοχή στη βανκομυκίνη (MIC 16 mg/l). Για την περίοδο αναφέρεται ότι 6 κλινικά στελέχη VRSA είχαν απομονωθεί στις ΗΠΑ και ότι όλα τα στελέχη είχαν το γονίδιο της αντοχής van A (Sung και συν 2007). Παράλληλα, σύμφωνα με τις κατευθυντήριες οδηγίες, έχουν βρεθεί και κατατάσσονται διαφορετικά τα στελέχη του χρυσίζοντα σταφυλόκοκκου που έχουν ενδιάμεση αντοχή (MIC 4-8 mg/l) ή ετεροαντοχή στα γλυκοπεπτίδια (CLSI 2007). Ο μηχανισμός αντοχής στα στελέχη με ενδιάμεση αντοχή, φαίνεται να οφείλεται στην πάχυνση του κυτταρικού τοιχώματος, ενώ δεν φέρουν το γονίδιο vana (Appelbaum 2006). Η ετεροαντοχή στα γλυκοπεπτίδια αναφέρεται σε φαινοτυπική ευαισθησία στη βανκομυκίνη του σταφυλόκοκκου, αλλά με υποπληθυσμούς που έχουν MIC στα όρια της ενδιάμεσης αντοχής. Η αξιόπιστη ανίχνευσή τους είναι δύσκολη, καθώς απαιτούνται εξειδικευμένες εξετάσεις που είναι δύσκολο να γίνουν, και για το λόγο αυτό δε συνιστάται ο συστηματικός έλεγχος για την εντόπισή τους (Liu και συν 2011). Παρότι υπάρχουν αναφορές για την αυξημένη ανίχνευση αυτών των στελεχών και πιθανή σχέση με αυξημένη κλινική αποτυχία κατά τη θεραπεία με βανκομυκίνη, λίγα είναι τα δεδομένα σε ό,τι αφορά την πραγματική κλινική σημασία τους (Cosgrove και συν 2004, Soriano και συν 2008). Για το λόγο αυτό, σύμφωνα με τις κατευθυντήριες οδηγίες της Εταιρείας Λοιμώξεων των ΗΠΑ (Infection Disease Society of America, IDSA) που εκδόθηκαν το 2011, στην αντιμετώπιση λοιμώξεων από MRSA στελέχη που έχουν MIC 2mg/L στη βανκομυκίνη, η συνέχιση της αγωγής με βανκομυκίνη καθορίζεται από την κλινική πορεία του ασθενούς και όχι με βάση την MIC (Liu 22
23 και συν 2011). Αντίθετα για MIC >2mg/L συστήνεται η θεραπεία με εναλλακτικά αντιμικροβιακά φάρμακα (Liu και συν 2011). Εικόνα 1: Παγκόσμια διασπορά των στελεχών MRSA και ποσοστά απομόνωσής τους (Grundmann και συν 2006). Από τα διάφορα είδη εντερόκοκκων τα στελέχη Enterococcus faecalis και E. faecium αποτελούν τα πιο συχνά νοσοκομειακά είδη που απομονώνονται. Το είδος των νοσοκομειακών λοιμώξεων που μπορεί να προκαλέσουν ποικίλλει από ουρολοίμωξη έως βακτηριαιμία, ενδοκαρδίτιδα και λοίμωξη ΚΝΣ (Woodford και συν 2009). Σε ό,τι αφορά την επίκτητη αντοχή, αυτή μπορεί να αποκτηθεί έναντι των αμινοπενικιλλινών, αμινογλυκοσιδών (υψηλού βαθμού αντοχή) και των γλυκοπεπτιδίων. Συγκεκριμένα, η αντοχή στα γλυκοπεπτίδια (βανκομυκίνη, τεϊκοπλανίνη) έχει σημαντικό κλινικό ενδιαφέρον, καθώς περιορίζονται στο ελάχιστο οι εναλλακτικές αντιμικροβιακές θεραπείες. Από το 1986 που αναφέρθηκε η πρώτη λοίμωξη από VRE έχουν σημειωθεί κατά καιρούς πολλαπλές επιδημίες είτε από ένα και μοναδικό κλώνο είτε από περισσότερους κλώνους (Pournaras και συν 2004, Hayden 2000). Η αντοχή στα γλυκοπεπτίδια οφείλεται σε συγκεκριμένο γονίδιο και μέχρι σήμερα έχουν τυποποιηθεί 7 διαφορετικά είδη του με τους αντίστοιχους φαινότυπους αντοχής, όπως φαίνεται στον πίνακα 2. Από αυτούς τους 7 φαινότυπους, οι πιο σημαντικοί από άποψη κλινικής είναι οι Van A και Van B (Boyd και συν 2008, Werner και συν 2008). 23
24 Πίνακας 2: Φαινότυποι αντοχής των εντερόκοκκων στα γλυκοπεπτίδια. Φαινότυπος Αντοχή Είδος και επίπεδο αντοχής Αντοχή έναντι Van A E. faecium, E. Επίκτητη Βανκομυκίνη, faecalis, E. Υψηλή Τεικοπλανίνη avium Van B E. faecalis, E. Επίκτητη Βανκομυκίνη Faecium Ποικίλη Van C E. gallinarum, E. Ενδογενής Βανκομυκίνη Casseliflavus Χαμηλή Van D E. faecium Επίκτητη Βανκομυκίνη Ενδιάμεση Τεικοπλανίνη Van E E. faecium Επίκτητη Βανκομυκίνη Ενδιάμεση Van G E. faecium Επίκτητη Βανκομυκίνη Χαμηλή Van L E. faecalis Επίκτητη Βανκομυκίνη Χαμηλή Boyd και συν 2008, Werner και συν 2008 Φορείς της αντοχής Πλασμιδιακή Πλασμιδιακή Χρωμοσωμική Χρωμοσωμική Χρωμοσωμική Χρωμοσωμική Χρωμοσωμική 2.2. Ανάπτυξη αντοχής και υποκείμενοι μηχανισμοί στα εντεροβακτηριοειδή Τα συνήθη αντιμικροβιακά που χρησιμοποιούνται στην αντιμετώπιση των λοιμώξεων από εντεροβακτηριοειδή, τόσο στην κοινότητα όσο και νοσοκομειακών, περιλαμβάνουν τα β- λακταμικά, τις αμινογλυκοσίδες και τις φθοροκινολόνες, και σε ειδικές περιπτώσεις την κοτριμοξαζόλη και τη νιτροφουραντοΐνη. Άλλα φάρμακα που χρησιμοποιούνται είναι η τιγκεκυκλίνη, η οποία ανήκει σε σχετικά νέα κατηγορία αντιμικροβιακών, τις γλυκυλκυκλίνες, η κολιμυκίνη, η φωσφομυκίνη και η χλωραμφενικόλη που είναι παλιότερα φάρμακα. H κολιμυκίνη ανήκει στις πολυμυξίνες. Η εμφάνιση αντοχής των εντεροβακτηριοειδών στα συνήθη αντιμικροβιακά, αλλά πρόσφατα και στα νεότερα, έχει συνδυαστεί ουσιαστικά με την αυξημένη χρήση τους στην κλινική πράξη. Τα εντεροβακτηριοειδή χρησιμοποιούν κοινούς μηχανισμούς για την ανάπτυξη αντοχής, όπως αναγράφεται παραπάνω: α) παραγωγή ειδικών ενζύμων, που αδρανοποιούν τα αντιμικροβιακά β) ελάττωση της συγκέντρωσης του αντιμικροβιακού μέσα στο μικρόβιο και γ) αλλαγή του στόχου δράσης του (Hawkey και συν 2009, Giamarellou 2005). Αναλυτικότερα, η ανάπτυξη αντοχής των εντεροβακτηριοειδών στα β-λακταμικά αντιμικροβιακά οφείλεται κυρίως στην παραγωγή ειδικών ενζύμων, των β-λακταμασών. Οι άλλοι μηχανισμοί αντοχής, που είναι η ελαττωμένη διαπερατότητα στα β-λακταμικά, η προς τα 24
25 έξω εξώθησή τους με μηχανισμό αντλίας και η αλλαγή στόχου δράσης τους με τις πενικιλλινοδεσμευτικές πρωτεΐνες, σπανιότερα, είναι λιγότερο συχνοί (σχήμα 3). Σχήμα 3: Σχηματική απεικόνιση Α) των συχνότερων β-λακταμικών αντιμικροβιακών φαρμάκων, Β) του μηχανισμού δράσης τους και Γ) των μηχανισμών αντοχής των Gramαρνητικών μικροβίων σε αυτά. PBP: Πενικιλλινοδεσμευτικές πρωτεΐνες. Ανάλογα με το είδος των β-λακταμασών που παράγονται από τα εντεροβακτηριοειδή καθορίζεται και η αντοχή τους στα διάφορα β-λακταμικά αντιμικροβιακά φάρμακα. Έτσι, από τις «απλές» β-λακταμάσες που προκαλούν αντοχή στις αμινοπενικιλλίνες και ίσως στις πρώτης γενιάς κεφαλοσπορίνες, τις τελευταίες δεκαετίες εμφανίσθηκαν «νεότερα» ένζυμα με ευρύ φάσμα δράσης, που περιλαμβάνει πολλά και διαφορετικά β-λακταμικά αντιμικροβιακά (πίνακας 3) (Giamarellou 2005, Bush 1999, Helfand 2003, Livermore 2009). 25
26 Πίνακας 3. Συχνότεροι τύποι β-λακταμασών που παράγονται από ανθεκτικά εντεροβακτηριοειδή Ένζυμα (β-λακταμάσες) Παραδείγματα β-λακταμασών Μικροοργανισμοί Φάσμα αντοχής Αναστολή της δράσης τους Ευρέως φάσματος β-λακταμάσες (Extended spectrum b-lactamases, ESBL) TEM, SHV, CTX-M Klebsiella pneumoniae, Escherichia coli, Proteus mirabilis Πενικιλλίνες Κεφαλοσπορίνες Μονομπακτάμες Κλαβουλανικό Ταζομπακτάμη Σουλμπακτάμη Πλασμιδιακή AmpC β- λακταμάση Καρβαπενεμάσες α) Μεταλλοένζυμα (Metallo- -lactamases, MBL) β) Ένζυμα τύπου KPC (K. pneumoniae carbapenemase) CMY, FOX, ACT, MOX IMP, VIM KPC K. pneumoniae, E. coli Εντεροβακτηριοειδή (λιγότερο συχνή) K. pneumoniae E. coli Πενικιλλίνες Κεφαλοσπορίνες Μονομπακτάμες Κεφαμυκίνες Πενικιλλίνες Κεφαλοσπορίνες Κεφαμυκίνες Καρμπαπενέμες Πενικιλλίνες Κεφαλοσπορίνες Κεφαμυκίνες Καρμπαπενέμες Κλοξακιλλίνη Βορονικό οξύ Χηλικές ενώσεις (π.χ. EDTA) Κλαβουλανικό οξύ Ταζομπακτάμη Βορονικό οξύ Η αντοχή στις κεφαλοσπορίνες 3 ης γενιάς των εντεροβακτηριοειδών ολοένα και αυξάνει. Αυτό έχει ως συνέπεια, η κατηγορία αυτή των αντιμικροβιακών να μην είναι ουσιαστικά χρήσιμη στην εμπειρική αντιμετώπιση νοσοκομειακών λοιμώξεων σε πολλά νοσοκομεία. Η αντοχή αυτή, όπως φαίνεται και στον πίνακα 3, οφείλεται κυρίως στην παραγωγή των λεγόμενων ευρέως φάσματος β-λακταμασών (Extended spectrum β-lactamases, ESBL) ή λιγότερο συχνά στις β-λακταμάσες τύπου AmpC. Οι τελευταίες μπορεί να είναι είτε πλασμιδιακά μεταφερόμενες ή χρωμοσωμιακές που υπερπαράγονται. Μετά την πρώτη αναφορά τους το 1983, τα ένζυμα τύπου ESBL εμφάνισαν ραγδαία εξάπλωση σε όλα τα εντεροβακτηριοειδή, αλλά και σε πολλά άλλα Gram-αρνητικά μικρόβια (Giamarellou 2005, Bush 1999, Helfand 2003, Paterson 2006). Τα ένζυμα αυτά (ESBL), όπως επίσης και τα ένζυμα τύπου AmpC, εμφανίζουν ιδιαίτερο κλινικό ενδιαφέρον, καθώς η θεραπεία σοβαρών λοιμώξεων από μικρόβια που τα παράγουν περιορίζεται σημαντικά έχοντας ως μόνη δραστική ουσία από τα β-λακταμικά τις καρβαπενέμες (Giamarellou 2005, Graffunder και συν 2002, Zaoutis και συν 2005). Στο διάγραμμα 1 απεικονίζεται η ποσοστιαία αύξηση των στελεχών E. coli που απομονώθηκαν από ασθενείς με βακτηριαιμία, από το 1990 έως και το 2007 στο Ηνωμένο Βασίλειο. Χαρακτηριστική είναι η σταδιακή αύξηση της αντοχής στις κεφαλοσπορίνες 3 ης 26
27 γενιάς (μέσω παραγωγής ESBL), καθώς και στις φθοροκινολόνες. Η συνύπαρξη αντοχής σε διαφορετικές ομάδες αντιμικροβιακών κάνει ακόμη πιο δύσκολη τη σωστή επιλογή αντιμικροβιακού. Διάγραμμα 1: Ποσοστό στελεχών E. coli που απομονώθηκαν στο αίμα με αντοχή στην σιπροφλοξασίνη (άσπρο χρώμα), στις κεφαλοσπορίνες 3 ης γενιάς (γκρι χρώμα) και στο συνδυασμό τους (μαύρο χρώμα). Τροποποιημένο από Livermore 2009). Η συνεχής χρήση των καρβαπενεμών, ως αντιμικροβιακών φαρμάκων επιλογής για τα ανθεκτικά μικρόβια, είχε ως αποτέλεσμα την εμφάνιση νέων β-λακταμασών που έχουν ευρύτερο φάσμα δράσης και περιλαμβάνουν ακόμη και τις καρβαπενέμες (Bush 1999, Helfand 2003, Poirel και συν 2007). Οι λεγόμενες καρβαπενεμάσες είναι ένζυμα που ουσιαστικά υδρολύουν την πλειονότητα των β-λακταμικών αντιμικροβιακών (Poirel και συν 2007). Οι δύο συχνότερες κατηγορίες ενζύμων που ανήκουν σε αυτήν την ομάδα είναι τα μεταλλοένζυμα (Metallo-βlactamases, MBL) και οι KPC (Klebsiella pneumoniae carbapenemase) β-λακταμάσες (Paterson 2006, Poirel και συν 2007). Η πρώτη κατηγορία, τα μεταλλοένζυμα, αν και εμφανίζονται συχνότερα σε στελέχη Pseudomonas aeruginosa και Acinetobacter baumannii, έχουν περιγραφεί σε αρκετά είδη της οικογένειας των εντεροβακτηριοειδών, όπως K. pneumoniae, Escherichia coli, Proteus mirabilis, Morganella morganii, Citrobacter κ.ά. (εικόνα 2). Στην Ελλάδα έχουν ήδη καταγραφεί επιδημίες από πολυανθεκτικά στελέχη K. pneumoniae που παράγουν 27
28 μεταλλοένζυμα της κατηγορίας VIM (Poirel και συν 2007). Το πρόβλημα με αυτήν την κατηγορία των β-λακταμασών είναι ότι συνήθως συνυπάρχει αντοχή σχεδόν σε όλες τις άλλες κατηγορίες των αντιμικροβιακών (αμινογλυκοσίδες, φθοροκινολόνες). Αυτό έχει ως αποτέλεσμα να υπάρχουν ελάχιστες εναλλακτικές θεραπείες των λοιμώξεων από τα μικρόβια αυτά και ουσιαστικά μόνο η κολιμυκίνη και ίσως η τιγκεκυκλίνη να αποτελούν τα φάρμακα εκλογής (Paterson 2006, Poirel και συν 2007). Εικόνα 2: Παγκόσμια και ευρωπαϊκή κατανομή των εντεροβακτηριοειδών με παραγωγή μεταλο-β-λακταμάσης τύπου IMP και VIM (Nordmann και συν 2011). Το ίδιο πρόβλημα υπάρχει και στην άλλη κατηγορία β-λακταμασών που διασπούν τις καρβαπενέμες, αλλά είναι τύπου KPC και έχουν κοινά χαρακτηριστικά με τις ESBL (Nordmann και συν 2009). Τα ένζυμα αυτά έχουν βρεθεί κατά κύριο λόγο σε στελέχη K. pneumoniae (εικόνα 3), αν και τον τελευταίο καιρό έχουν απομονωθεί και σε άλλα εντεροβακτηριοειδή, όπως στο E. coli και στο Enterobacter spp. (Nordmann και συν 2009). Μετά την πρώτη αναφορά επιδημίας από στελέχη K. pneumoniae, που παρήγαγαν KPC το 2000 στη Νέα Υόρκη, ακολούθησαν αναφορές από αρκετές χώρες μεταξύ των οποίων και η Ελλάδα (Paterson 2006, Nordmann και συν 2009). Οι παράγοντες κινδύνου για την λοίμωξη από αυτά τα στελέχη είναι 28
29 κοινοί, όπως είναι η παραμονή σε ΜΕΘ, ο επεμβατικός μηχανικός αερισμός, η ουδετεροπενία και η μεταμόσχευση (Nordmann και συν 2009). Μάλιστα, εκτός από τις ελάχιστες εναλλακτικές θεραπείες που απομένουν για την αντιμετώπιση των λοιμώξεων από αυτά τα στελέχη, ιδιαίτερο πρόβλημα υπάρχει και στην ανίχνευσή τους, καθώς πολλές φορές δεν είναι δυνατή η αναγνώρισή τους στα συνήθη αντιβιογράμματα που χρησιμοποιούνται στην κλινική πράξη (Nordmann και συν 2009). Εικόνα 3: Παγκόσμια διασπορά στελεχών K. pneumoniae με παραγωγή KPC (Τροποποιημένο, Nordmann και συν 2011). Εκτός από τα β-λακταμικά αντιμικροβιακά, η ανάπτυξη αντοχής των εντεροβακτηριοειδών στις υπόλοιπες ομάδες αντιμικροβιακών αποτελεί εξίσου σημαντικό πρόβλημα για την επιλογή της σωστής αντιμικροβιακής θεραπείας. Η αντοχή στις φθοροκινολόνες συνήθως αφορά όλα τα μέλη της κατηγορίας αυτής, όπως είναι η σιπροφλοξασίνη, οφλοξασίνη, νορφλοξασίνη και μοξιφλοξασίνη, και τις περισσότερες φορές συνυπάρχει με την αντοχή στα β-λακταμικά. Ο υποκείμενος μηχανισμός μπορεί να περιλαμβάνει μεταλλάξεις στο χρωμόσωμα, απόκτηση γονιδίων αντοχής μέσω πλασμιδίων ή συχνότερα μέσω της απομάκρυνσης (αντλίας εξώθησης) των αντιμικροβιακών. Ο τελευταίος μηχανισμός ουσιαστικά προσδίδει αντοχή, εκτός από τις φθοροκινολόνες, και σε άλλα αντιμικροβιακά 29
30 (Paterson 2006, Denton 2007). Τελευταία έχουν αναφερθεί επιπρόσθετοι μηχανισμοί αντοχής στις φθοροκινολόνες (Robicsek και συν 2006α). Ένας από αυτούς είναι και οι πλασμιδιακά μεταφερόμενες πρωτεΐνες τύπου Qnr που παρέχουν προστασία στα ένζυμα στόχου των κινολονών τοποϊσομεράσες του DNA- και επομένως, καθιστούν τα μικρόβια ανθεκτικά σε αυτά τα αντιμικροβιακά (Martinez-Martinez και συν 1998). Επιπλέον, έχει περιγραφεί η εμφάνιση ενζύμου που τροποποιεί τις κινολόνες. Προέρχεται από τα τροποποιητικά ένζυμα των αμινογλυκοσιδών, αλλά με την ιδιότητα να τροποποιεί και συγκεκριμένες φθοροκινολόνες, όπως είναι η σιπροφλοξασίνη και η νορφλοξασίνη (Robicsek και συν 2006b). Η αντοχή των εντεροβακτηριοειδών στις αμινογλυκοσίδες δημιουργεί επίσης πρόβλημα στην θεραπεία των λοιμώξεων. Συνήθως οφείλεται στην ύπαρξη ειδικών τροποποιητικών ενζύμων που ακετυλιώνουν, φωσφορυλιώνουν ή μεθυλιώνουν τις αμινογλυκοσίδες ή και στην εμφάνιση αντλιών εξώθησης (Livermore και συν 2001b). Η αντοχή και εδώ μπορεί να συνδυάζεται με αντοχή σε άλλες κατηγορίες αντιμικροβιακών. Η αντοχή στην κοτριμοξαζόλη, τις περισσότερες φορές, είναι άμεσα συνδεδεμένη με την αντοχή στις άλλες κατηγορίες των αντιμικροβιακών και κυρίως των β-λακταμικών (Livermore και συν 2001b). Το ίδιο και η αντοχή στη νιτροφουραντοΐνη, η οποία είναι πολύ συχνή. Παρόλα αυτά η αντοχή στη νιτροφουραντοΐνη δεν έχει ιδιαίτερα κλινική σημασία για τις νοσοκομειακές λοιμώξεις, καθώς είναι απαγορευτική η χρήση της λόγω των χαμηλών συγκεντρώσεων στο αίμα και στους ιστούς (Livermore και συν 2001b). Η αντοχή στην τιγκεκυκλίνη, αν και ακόμη είναι πολύ περιορισμένη, έχει αναφερθεί σε ορισμένα στελέχη της οικογένειας των εντεροβακτηριοειδών και οφείλεται κυρίως στους μηχανισμούς αντλίας (Giamarellou και συν 2009). Τέλος, αντοχή ή ετεροαντοχή στην κολιμυκίνη, ένα φάρμακο που πολλές φορές αποτελεί το μόνο εναλλακτικό αντιμικροβιακό, έχει βρεθεί σε πολυανθεκτικά στελέχη κυρίως K. pneumoniae και αποτελεί ιδιαίτερα ανησυχητικό φαινόμενο (Meletis και συν 2011, Mammina και συν 2012). Σε αυτήν την περίπτωση έχουμε συνήθως πλήρη αντοχή σε όλα τα αντιμικροβιακά φάρμακα που μπορούν να χρησιμοποιηθούν (Livermore 2009, Giamarellou και συν 2009). Στο σημείο αυτό, είναι ανάγκη να διευκρινιστεί ότι ο όρος πολυανθεκτικά μικρόβια περιλαμβάνει εκείνα τα μικρόβια που εμφανίζουν αντοχή σε 3 αντιμικροβιακά φάρμακα. Ειδικά για τα εντεροβακτηριοειδή, και πιο συγκεκριμένα για τα στελέχη E. coli και K. pneumoniae, εξ ορισμού θεωρούνται πολυανθεκτικά αυτά που παράγουν ευρέως φάσματος β- λακταμάσες (ESBL, πλασμιδιακές AmpC), καθώς και καρβαπενεμάσες. Όπως αναφέρθηκε 30
31 παραπάνω, τα περισσότερα από αυτά τα στελέχη έχουν ταυτόχρονη αντοχή και σε άλλες κατηγορίες αντιμικροβιακών (Giamarellou 2005, Poirel και συν 2007, Nordmann και συν 2009, Giamarellou και συν 2009) Ανάπτυξη αντοχής και υποκείμενοι μηχανισμοί στα αζυμωτικά Gram αρνητικά μικρόβια (Pseudomonas aeruginosa και Acinetobacter baumannii). Τόσο τα στελέχη Pseudomonas spp. όσο και Acinetobacter spp. αποτελούν σημαντικούς παράγοντες σοβαρών νοσοκομειακών λοιμώξεων, ιδίως σε άτομα που νοσηλεύονται σε ΜΕΘ. Όπως φαίνεται στον πίνακα 4, τα στελέχη Pseudomonas και Acinetobacter εμφανίζουν ενδογενή αντοχή σε αρκετά αντιμικροβιακά. Πίνακας 4. Ενδογενείς μηχανισμοί αντοχής Αντιμικροβιακό Pseudomonas aeruginosa Acinetobacter baumannii Πενικιλλίνες AmpC AmpC Κεφαλοσπορίνες AmpC AmpC υπερέκφραση OXA-50 OXA-51 Απώλεια πορίνης Καρβαπενέμες Αντλία εξώθησης Αλλαγή στις πενικιλλινοδεσμευτικές πρωτεΐνες Απώλεια πορίνης Αντλία εξώθησης Φθοροκινολόνες Μεταλλάξεις στο γονίδιο gyra (+parc) Αντλία Πορίνη Κολιμυκίνη, Πολυμυξίνη Β Μεταλλάξεις, αλλαγές στη μεμβράνη Γλυκυλκυκλίνη Αντλία Αντλία Peleg και συν 2008 Αντλία εξώθησης Αλλαγή στις πενικιλλινοδεσμευτικές πρωτεΐνες OXA-51 Μεταλλάξεις στο γονίδιο gyra (+parc) Αντλία +Απώλεια πορίνης Μεταλλάξεις, αλλαγές στη μεμβράνη Η αντοχή των στελεχών A. baumannii στα β-λακταμικά περιλαμβάνει κυρίως την παραγωγή β-λακταμασών. Οι β-λακταμάσες που έχουν βρεθεί σε στελέχη A. baumannii προέρχονται ουσιαστικά από όλες τις κατηγορίες ταξινόμησης των β-λακταμασών κατά Ambler: ESBL τύπου PER, VEB, και CTX-M (κατηγορία Α), MBL τύπου VIM, IMP, SIM, κεφαλοσπορινάσες τύπου AmpC (κατηγορία C, που μάλιστα είναι γνωστές και ως Acinetobacter 31
32 derived Cephalosporins, ADCs ) και τέλος οξακιλλινάσες τύπου OXA (κατηγορία D) (Segal και συν 2004, Poirel και συν 2005). Είναι καλό να τονιστεί ότι λόγω της ιδιαιτερότητας του συγκεκριμένου μικροοργανισμού, πολλές φορές διαφορετικοί μηχανισμοί αντοχής συμμετέχουν και προκαλούν τελικά τον ίδιο φαινότυπο (Peleg και συν 2008). Μη ενζυματικοί μηχανισμοί αντοχής έχουν περιγραφεί στην εμφάνιση αντοχής στα β-λακταμικά και περιλαμβάνουν αλλαγές στις πορίνες της εξωτερικής κυτταρικής μεμβράνης του τοιχώματος, αντλίες εξώθησης και αλλαγή στις πενικιλλινοδεσμευτικές πρωτεΐνες (Peleg και συν 2008). Η αντοχή σε μη β-λακταμικά περιλαμβάνει τόσο την αντοχή στις αμινογλυκοσίδες, που μπορεί να συμβεί με όλους τους γνωστούς μηχανισμούς αντοχής (τροποποιητικά ένζυμα, που αποτελεί τον συχνότερο μηχανισμό, μεθυλίωση και ειδική αντλία εξώθησης) όσο και στις κινολόνες (Livermore 2001b). Η αντοχή στις κινολόνες περιλαμβάνει επίσης την τροποποίηση του ενζύμου-στόχου των κινολονών (DNA γυράση ή τοποϊσομεράση ΙV), καθώς και ειδικές αντλίες εξώθησης, όπως είναι για παράδειγμα οι αντλίες AdeM (MATE pump) και AdeABC (Livermore 2001b). Η αντοχή στις τετρακυκλίνες επιτυγχάνεται είτε με την ύπαρξη ειδικής αντλίας, π.χ. teta-tete, είτε με την προστασία των ριβοσωμάτων, π.χ. tetm και teto. Ειδικά για την τιγκεκυκλίνη που, όπως προαναφέρθηκε, ανήκει στην κατηγορία των γλυκυλκυκλινών, ο μηχανισμός αντοχής περιλαμβάνει την αντλία AdeABC (Giamarellou και συν 2009). Τέλος, η αντοχή στην κολιμυκίνη έχει επίσης αναφερθεί. Παράλληλα, σημαντική είναι η εμφάνιση στελεχών που εμφανίζουν ετεροαντοχή στην κολιμυκίνη. Τα στελέχη αυτά φαινοτυπικά είναι ευαίσθητα, αλλά έχουν πληθυσμούς που εμφανίζουν αντοχή στην κολιμυκίνη (Giamarellou και συν 2009). Η αντοχή της P. aeruginosa στα β-λακταμικά περιλαμβάνει τόσο την παραγωγή β- λακταμασών όσο και τους άλλους γνωστούς μηχανισμούς. Συγκεκριμένα, ένας τρόπος αντοχής στις καρβαπενέμες, και συγκεκριμένα μόνο στην ιμιπενέμη, είναι η απώλεια μιας πορίνης από την εξωτερική κυτταρική μεμβράνη (OprD). Ένας άλλος τρόπος είναι οι αντλίες εξώθησης (Aeschlimann 2003, Schweizer 2003). Οι β-λακταμάσες επίσης, αποτελούν σημαντικό μέρος στην αντοχή της P. aeruginosa στα β-λακταμικά: υπερπαραγωγή (stable derepression) της χρωμοσωμιακής AmpC β-λακταμάσης (κατηγορία C κατά Ambler), απόκτηση νέων β- λακταμασών της κατηγορίας Α (με στενό φάσμα όπως καρβενικιλλινάση PSE-1, CARB-3, CARB-4, και με ευρύ φάσμα δράσης όπως ESBL τύπου ΤΕΜ, SHV, PER, VEB, GES, IBC, BEL), της κατηγορίας B (MBL, τύπου VIM, IMP, SPM, GIM, AIM), καθώς και της κατηγορίας 32
33 D (OXA) (Strateva και συν 2009, Livermore 2009, Rodriguez-Martinez και συν 2009). Μηχανισμοί ενεργητικής απομάκρυνσης των αντιμικροβιακών (MexAB OprM, MexCD OprJ, MexEF OprN) μέσω σταθερής έκφρασης ή υπερέκφρασης προκαλούν αντοχή σε πολλά αντιψευδομοναδικά αντιμικροβιακά (Strateva και συν 2009). Η αντοχή στις αμινογλυκοσίδες περιλαμβάνει πάνω από 80 διαφορετικούς μηχανισμούς. Ο πιο κοινός τρόπος είναι μέσω των τροποποιητικών ενζύμων (AAC(6 )II, ANT (2 )I) (Livermore 2009). Η αντοχή στις φθοροκινολόνες περιλαμβάνει γνωστούς μηχανισμούς αντοχής, όπως είναι οι αντλίες εξώθησης, η τροποποίηση της γυράσης/τοποϊσομεράσης και αλλαγές στην διαπερατότητά τους (Strateva και συν 2009). 3. Κλινική σημασία των λοιμώξεων από πολυανθεκτικά μικρόβια Στις περισσότερες περιπτώσεις, οι λοιμώξεις που προκαλούνται από πολυανθεκτικά μικρόβια είναι όμοιες με αυτές που προκαλούνται από τα ευαίσθητα στελέχη. Με λίγα λόγια, τα πολυανθεκτικά μικρόβια προκαλούν νοσοκομειακές λοιμώξεις όπως είναι η βακτηριαιμία, πνευμονία, ουρολοίμωξη, λοίμωξη χειρουργικών τραυμάτων, κ.λπ.. Παρόλα αυτά, οι επιλογές που υπάρχουν, σε ό,τι αφορά τη θεραπεία των συγκεκριμένων λοιμώξεων από πολυανθεκτικά μικρόβια, είναι πολύ περιορισμένες έως και ανύπαρκτες. Μελέτες που έχουν γίνει έχουν αποδείξει ότι υπάρχει αύξηση της διάρκειας νοσηλείας, του κόστους νοσηλείας, αλλά το κυριότερο αύξηση της θνητότητας, όταν η λοίμωξη οφείλεται σε πολυανθεκτικά μικρόβια (πίνακας 5) (Giske και συν 2008, DiazGranados και συν 2005, Engemann και συν 2003). Ειδικά για τα Gram αρνητικά μικρόβια υπάρχουν αρκετές μελέτες, όπως για παράδειγμα μελέτες ασθενών-μαρτύρων και φάλαγγας/κοόρτης, που αποδεικνύουν αυτήν την σχέση μεταξύ λοίμωξης από πολυανθεκτικά μικρόβια και αυξημένης θνητότητας (Giske και συν 2008). Πρόσφατα, μια μετα-ανάλυση ανέδειξε σημαντική αύξηση της θνητότητας στους ασθενείς με εντεροβακτηριοειδή που παρήγαγαν ESBL με έναν σχετικό κίνδυνο (relative risk, RR) της τάξης του 1,85 (95% διάστημα αξιοπιστίας: 1,39 έως 2,47) (Giske και συν 2008). Παρόμοια αποτελέσματα αναφέρονται και σε λοιμώξεις από πολυανθεκτκά στελέχη P. aeruginosa και A. baumannii. Πιο συγκεκριμένα, η παρουσία αντοχής στελεχών P. aeruginosa σε πολλά αντιμικροβιακά (όπως π.χ. καρβαπενεμών, κεφταζιδίμης, πιπερακιλλίνης/ταζομπακτάμης, τομπραμυκίνης, σιπροφλοξασίνης) επηρεάζει σημαντικά την επιβίωση των ασθενών που εμφανίζουν λοίμωξη από τα στελέχη αυτά, όπως αυτό καταγράφεται σε μελέτες ασθενών- 33
34 μαρτύρων (Cao και συν 2004, Lautenbach και συν 2006, Lautenbach και συν 2010, Hirakata και συν 2003). Βέβαια, υπάρχουν σε κάποιες από τις μελέτες αυτές περιορισμοί, όπως είναι η αδυναμία διάκρισης μεταξύ λοίμωξης και αποικισμού. Πίνακας 5. Συνέπειες της παρουσίας πολυανθεκτικών μικροοργανισμών Αύξηση θνητότητας Υψηλότερη σε ασθενείς με λοιμώξεις από ανθεκτικά μικρόβια σε σύγκριση με ασθενείς χωρίς λοίμωξη Υψηλότερη σε ασθενείς με λοιμώξεις από ανθεκτικά μικρόβια σε σύγκριση με ασθενείς που έχουν λοίμωξη από ευαίσθητα μικρόβια Υψηλότερη σε περίπτωση που η αντοχή αυξάνει την πιθανότητα ακατάλληλης αρχικής θεραπείας Παράταση χρόνου νοσηλείας Στο νοσοκομείο ή στη μονάδα εντατικής θεραπείας μετά την εμφάνιση της λοίμωξης Ανάγκη για θεραπεία που έχει αυξημένο κόστος Αντιμικροβιακά: ακριβότερα αντιμικροβιακά, συνδυασμό πολλών αντιμικροβιακών σε έναν άρρωστο, παρατεταμένη διάρκεια χορήγησής τους Χειρουργική αντιμετώπιση λοιμώξεων που δεν ανταποκρίνονται στη θεραπεία (παροχέτευση αποστημάτων/εμπυημάτων, αλλαγή ξένων σωμάτων κ.λπ.) Υπερκατανάλωση αντιμικροβιακών, που μπορεί να οδηγήσει στην εμφάνιση αντοχής γρηγορότερα Ανάγκη για μεγαλύτερο κόστος Απομόνωση ασθενών: αποκλειστικά δωμάτια για απομόνωση με ή χωρίς αρνητική πίεση, ατομικός προστατευτικός εξοπλισμός (γάντια, ποδιές, μάσκες), εντατικοποίηση των μέτρων υγιεινής κ.ά. Μεγαλύτερη διάρκεια παραμονής στο νοσοκομείο Μεγαλύτερη διάρκεια μηχανικού αερισμού Επιπλοκές που σχετίζονται με την ιατρική πράξη Αποτέλεσμα της παρατεταμένης διαμονής στη ΜΕΘ: τραχειοστομία Αποτέλεσμα της σήψης, η ινότροπη υποστήριξη, καθώς και η νεφρική ανεπάρκεια Αποτέλεσμα της επίμονης και/ή μη ανταποκρινόμενης στη θεραπεία λοίμωξης είναι η καθυστέρηση στην επανάκτηση των φυσιολογικών λειτουργιών Παρόλα αυτά, υπάρχουν μελέτες όπου η λοίμωξη από P. aeruginosa είναι αδιαμφισβήτητη και η αντοχή επηρεάζει δυσμενώς την επιβίωση. O Micek et al, αναφέρουν ότι σε μια αναδρομική μελέτη ασθενών με βακτηριαιμία από P. aeruginosa, η νοσοκομειακή θνητότητα επηρεαζόταν στατιστικώς σημαντικά από την ακατάλληλη αρχική αντιμικροβιακή αγωγή, που σε ποσοστό 88% οφειλόταν σε αντοχή της P. aeruginosa στα αντιψευδομοναδικά αντιμικροβιακά (Micek και συν 2005). Αντίστοιχη μελέτη σε ασθενείς με βακτηριαιμία από A. 34
35 baumannii, έδειξε ότι η αντοχή στην ιμιπενέμη ήταν στατιστικά σημαντικός παράγοντας για κακή έκβαση στις 30 ημέρες (Kwon και συν 2007). Εκτός από τη θνητότητα, την αύξηση της νοσηρότητας και το κόστος νοσηλείας, μια άλλη συνέπεια της εμφάνισης πολυανθεκτικών μικροβίων είναι η μεταβολή της αντιμικροβιακής πολιτικής που χρησιμοποιείται σε μια μονάδα, γεγονός που επηρεάζει τελικά δυσμενώς τη φυσιολογική μικροβιακή χλωρίδα των ασθενών. Απαιτείται η χρήση όλο και περισσότερων αντιμικροβιακών με ευρύ φάσμα ή συνδυασμός αντιμικροβιακών για τη θεραπεία των πολυανθεκτικών μικροβίων. Με τον τρόπο αυτόν, δημιουργείται ένας φαύλος κύκλος που με τη σειρά του δημιουργεί τις κατάλληλες προϋποθέσεις, για τη διευκόλυνση του αποικισμού με ανθεκτικά μικρόβια όλων των ασθενών που βρίσκονται σε αντιμικροβιακή αγωγή (Giske και συν 2008). 4. Συσχέτιση κατανάλωσης αντιμικροβιακών φαρμάκων και εμφάνισης μικροβιακής αντοχής Η εξάπλωση των ανθεκτικών μικροβίων επηρεάζεται άμεσα από τα μέτρα ελέγχου οριζόντιας μετάδοσης ανθεκτικών μικροβίων μεταξύ ασθενών, όπως επίσης και από την ακατάλληλη και αλόγιστη χρήση των αντιμικροβιακών. Η σχέση αυτή μεταξύ χορήγησης αντιμικροβιακών και εμφάνισης αντοχής, έχει διαπιστωθεί τόσο στο νοσοκομείο (και ιδίως σε ορισμένες κλινικές, όπως είναι οι ΜΕΘ), καθώς και στην κοινότητα. Επιπλέον, αυτή η σχέση έχει αποδειχθεί και στην κτηνοτροφία (Smith και συν 2002). Βέβαια, λόγω της ύπαρξης ποικίλων μηχανισμών αντοχής στα μικρόβια, αλλά και του διαφορετικού χρόνου για την εμφάνιση και εξάπλωσή της (πίνακας 1), η συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και εμφάνισης αντοχής, γίνεται πολύ πιο πολύπλοκη. Πολλές φορές καταγράφεται αυτή η συσχέτιση, ωστόσο είναι δύσκολο να αποδειχθεί στην κάθε περίπτωση. Ακόμη πιο περίπλοκη είναι η ποσοτικοποίηση αυτής της συσχέτισης, που ως τώρα δεν έχει μελετηθεί σε βάθος. Οι μελέτες που έχουν ασχοληθεί με την συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και εμφάνισης αντοχής αντιμετωπίζουν συχνά στατιστικά προβλήματα, που έχουν κυρίως σχέση με συγχυτικούς παράγοντες. Ο λόγος είναι ότι υπάρχουν και άλλοι παράγοντες που συνεισφέρουν στην εξάπλωση της αντοχής (οριζόντια μετάδοση, μεταφορά ασθενών), που θα πρέπει να ελέγχονται και να σταθμίζονται. Λαμβάνοντας μάλιστα υπόψη ότι δεν γίνονται προοπτικές τυχαιοποιημένες ελεγχόμενες μελέτες για την εμφάνιση αντοχής, είναι 35
36 λογικό ότι οι μελέτες αυτές είναι κυρίως μελέτες παρατήρησης και στην πλειονότητα αναδρομικές. Η χρήση μαθηματικών και στατιστικών μοντέλων στην επεξεργασία των σχέσεων μεταξύ κατανάλωσης αντιμικροβιακών και εμφάνισης αντοχής φαίνεται να βοηθάει στην κατανόηση της πολυπλοκότητας της σχέσης αυτής (Austin 1999, Austin 1999, Levin 1997, Liptich 2000). Συνοπτικά, οι μελέτες που εξετάζουν τη συσχέτιση αυτή μπορούν να διακριθούν σε δύο μεγάλες κατηγορίες, σε αυτές που χρησιμοποιούν αθροιστικά δεδομένα κατανάλωσης αντιμικροβιακών και αντοχής σε έναν χώρο (νοσοκομείο, κοινότητα) και σε αυτές που χρησιμοποιούν δεδομένα σε επίπεδο ασθενούς. Τα αθροιστικά δεδομένα συνήθως, όπου υπάρχουν οργανωμένα συστήματα καταγραφής, είναι πιο εύκολο να συγκεντρωθούν και να αναλυθούν. Συνήθως οι αντίστοιχες μελέτες διεξάγονται σε επίπεδο κλινικής (για παράδειγμα ΜΕΘ), νοσοκομείου ή δικτύου νοσοκομείων, κοινότητας ή ακόμη και σε επίπεδο εθνικό/διεθνές. Εκτός από τον τρόπο συλλογής αυτών των δεδομένων στις παραπάνω μελέτες, η ανάλυση της συσχέτισης μεταξύ κατανάλωσης και αντοχής γίνεται στη συνέχεια είτε σε σχέση με το χρόνο (διαχρονική συσχέτιση) είτε σε σχέση με το χώρο (γεωγραφική συσχέτιση) Αθροιστικά δεδομένα, διαχρονική συσχέτιση Οι Lepper και συν έδειξαν ότι κατά την 3ετή μελέτη τους υπήρχε σημαντική συσχέτιση του μηνιαίου επιπολασμού της ανθεκτικής P. aeruginosa στην ιμιπενέμη και στη συνταγογράφηση της ιμιπενέμης κατά τον ίδιο ή τον προηγούμενο μήνα (Lepper και συν 2002). Παρόμοια χρονική συσχέτιση της αντοχής στις καρβαπενέμες με την κατανάλωση των αντιμικροβιακών έχει καταγραφεί και για τα στελέχη A. baumannii (Hsueh και συν 2005, Goel 2011). Συσχέτιση μεταξύ της κατανάλωσης αντιμικροβιακών (κεφαλοσπορίνες 3 ης γενιάς, φθοροκινολόνες) και αντοχής έχει παρατηρηθεί και για στελέχη K. pneumoniae σε μια αναδρομική μελέτη διάρκειας 4 ετών σε μια ΜΕΘ στην Ιταλία (Bassetti και συν 2006). Βέβαια, σε μια πολύ πρόσφατη μελέτη, δεν βρέθηκε συσχέτιση μεταξύ αυξημένης κατανάλωσης καρβαπενεμών και ανθεκτικών στις καρβαπενέμες εντεροβακτηριοειδών που απομονώθηκαν σε ενδοκοιλιακές λοιμώξεις (Ho 2012). Οι Mutnick και συν σε μια πολυκεντρική μελέτη, που έγινε από το 1999 έως και το 2001, βρήκαν ότι η αυξημένη χρήση κινολονών συνδυαζόταν με υψηλή αντοχή των εντεροβακτηριοειδών στις κινολόνες, και της ψευδομονάδας σε άλλες κατηγορίες αντιμικροβιακών (Mutnick και συν 2004). Παρόμοια ευρήματα, για τη σχέση μεταξύ 36
37 κατανάλωσης κινολονών και αντοχής των Gram αρνητικών μικροβίων, έδειξαν σε μια 7ετή μελέτη σε ασθενείς που νοσηλεύτηκαν σε ΜΕΘ στις ΗΠΑ οι Neuhauser και συν, όπως επίσης και στην Ταϊβάν οι Wu και συν (Neuhauser και συν 2003, Wu και συν 2012). Η κατανάλωση των φθοροκινολονών έχει συσχετισθεί όχι μόνο με την εμφάνιση αντοχής στα Gram αρνητικά, αλλά και στα Gram θετικά. Σε μια επίσης, πολυκεντρική μελέτη στη Γαλλία, όπου συμμετείχαν 47 νοσοκομεία, βρέθηκε σημαντική συσχέτιση μεταξύ της χρήσης φθοροκινολονών και της αντοχής του χρυσίζοντα σταφυλόκοκκου (MRSA) (Rogues και συν 2007). Εκτός από τις φθοροκινολόνες η κατανάλωση κεφαλοσπορινών 3 ης γενιάς, αμινογλυκοσιδών, καθώς και γλυκοπεπτιδίων έχει συσχετισθεί με την εμφάνιση στελεχών MRSA (Meyer και συν 2006a). Σε μια μελέτη με πολύ καλή μεθοδολογία (χρονοσειρές-time series) από τους Aldeyab και συν, φάνηκε ότι υπήρχε χρονική συσχέτιση της εμφάνισης στελεχών MRSA και της κατανάλωσης φθοροκινολονών, 3 ης γενιάς κεφαλοσπορινών, μακρολιδών και αμοξυκιλλίνης/κλαβουλανικού οξέος. Επίσης, το χαρακτηριστικό της μελέτης αυτής ήταν ότι βρέθηκε χρονική συσχέτιση μεταξύ του επιπολασμού του MRSA και της χρήσης των μέτρων πρόληψης οριζόντιας μετάδοσης μικροβίων, όπως η χρήση αλκοολούχων σκευασμάτων, ο έλεγχος φορείας στους ασθενείς για MRSA κ.ά. (Aldeyab και συν 2008). Τα δεδομένα αυτά έχουν επαληθευτεί και από άλλες μελέτες που χρησιμοποίησαν χρονοσειρές για τη μελέτη του MRSA (Kaier και συν 2009, Vernaz και συν 2008). Σε μια ελληνική μελέτη έγινε διαχρονική συσχέτιση μεταξύ της χρήσης αντιμικροβιακών φαρμάκων και εμφάνισης στελεχών VRE. Αποδείχθηκε με ποσοτικό τρόπο ότι η αύξηση της χρήσης γλυκοπεπτιδίων, φθοροκινολονών, κεφαλοσπορινών με ευρύ φάσμα δράσης και συνδυασμών β-λακταμικών με αναστολείς β-λακταμασών σχετίζεται άμεσα με την αύξηση της αντοχής των εντερόκοκκων στη βανκομυκίνη. Ο χρόνος μάλιστα που μεσολάβησε από τη χορήγηση των αντιμικροβιακών αυτών ήταν διαφορετικός: 2 μήνες για τα γλυκοπεπτίδια και τις κεφαλοσπορίνες με ευρύ φάσμα δράσης, 4 μήνες για τις φθοροκινολόνες και 6 μήνες για τους συνδυασμούς β-λακταμικών με αναστολείς β-λακταμασών (Kritsotakis και συν 2008). Παρόμοια σχέση μεταξύ της συχνότητας του VRE και της κατανάλωσης γλυκοπεπτιδίων και κεφαλοσπορινών 3 ης γενιάς έχει καταγραφεί και σε ειδικές κλινικές, μεταξύ των οποίων είναι η μελέτη των Kolar και συν που περιλαμβάνουν ασθενείς που νοσηλεύονται σε αιματολογικές/ογκολογικές κλινικές (Kolar και συν 2006). 37
38 4.2. Αθροιστικά δεδομένα, γεωγραφική συσχέτιση Σε δύο πολυκεντρικές ευρωπαϊκές μελέτες, έγινε συσχέτιση των δεδομένων που αφορούσαν τον επιπολασμό του MRSA και 2001 αντίστοιχα- και της κατανάλωσης αντιμικροβιακών (MacKenzie και συν 2007, Westh 2004). Στην καταγραφή που έγινε το 2001 μελετήθηκε, μεταξύ των άλλων, και η εφαρμογή των προγραμμάτων πρόληψης της οριζόντιας μετάδοσης μικροβίων σε διάφορες ευρωπαϊκές χώρες. Βρέθηκε μια γεωγραφική σχέση, όπου χώρες με υψηλή κατανάλωση αντιμικροβιακών είχαν και υψηλά ποσοστά MRSA. Αντίστοιχα, νοσοκομεία που είχαν εφαρμόσει μέτρα ελέγχου της οριζόντιας μετάδοσης μικροβίων (υγιεινή χεριών, απομόνωση ασθενών με MRSA) φάνηκε ότι είχαν χαμηλότερα ποσοστά MRSA (MacKenzie και συν 2007). Παρόμοια μελέτη που έγινε στην Ευρώπη από το 1997 έως το 2002, και αφορούσε την καταγραφή της εξωνοσοκομειακής κατανάλωσης αντιμικροβιακών και της εμφάνισης αντοχής, έδειξε ότι υπήρχε γεωγραφική συσχέτιση μεταξύ μικροβιακής αντοχής και κατανάλωσης αντιμικροβιακών φαρμάκων. Συγκεκριμένα, χώρες με υψηλα ποσοστά μικροβιακής αντοχής είχαν ταυτόχρονα υψηλή κατανάλωση αντιμικροβιακών. Μάλιστα οι χώρες αυτές ανήκαν στη νότια και ανατολική Ευρώπη (Goossens 2005). Σε εθνικό επίπεδο, έχει καταγραφεί η συσχέτιση της αντοχής του πνευμονιόκοκκου στις μακρολίδες και β-λακταμικά, και της κατανάλωσης αντιμικροβιακών σε διάφορες περιοχές της Ιταλίας. Η χρήση της πενικιλλίνης συσχετιζόταν με την εμφάνιση αντοχής του πνευμονιόκοκκου στην πενικιλλίνη (r=0,85, p=0,002) (Boccia 2004). Η συσχέτιση της κατανάλωσης αντιμικροβιακών και της εμφάνισης αντοχής σε επίπεδο κλινικών ενός τριτοβάθμιου νοσοκομείου έχει διερευνηθεί μόνο σε ελάχιστες μελέτες. Σε μια τέτοια μελέτη, η διαφορετική κατανάλωση αντιμικροβιακών στις κλινικές ενός νοσοκομείου είχε ως αποτέλεσμα τη διαφορά στη συχνότητα εμφάνισης ανθεκτικών στελεχών εντεροβακτηριοειδών σε ασθενείς που νοσηλεύτηκαν στις κλινικές αυτές (Leibovici και συν 2001) Δεδομένα σε επίπεδο ασθενούς (μελέτες ασθενών μαρτύρων, μελέτες φάλαγγας) Στα Gram-θετικά μικρόβια, αρκετές μελέτες έχουν αποδείξει τη συσχέτιση της προηγηθείσας χορήγησης αντιμικροβιακών και της εμφάνισης λοίμωξης από στελέχη MRSA. Πιο συγκεκριμένα, η χρήση φθοροκινολονών, μακρολιδών, καθώς και β-λακταμικών αντιμικροβιακών έχουν συσχετισθεί με λοίμωξη από MRSA (Graffunder και συν 2002, Monnet 38
39 1998b). Η προηγούμενη έκθεση σε φθοροκινολόνες, κεφαλοσπορίνες 3 ης γενιάς και σε αντιμικροβιακά με αντιαναερόβια δράση, αποτελεί προδιαθεσικό παράγοντα για την εμφάνιση λοίμωξης από VRE (Sakka και συν 2008, Ghanem και συν 2007). Από τα ανθεκτικά Gram αρνητικά μικρόβια, υπάρχουν επίσης αρκετές μελέτες για τη συσχέτιση μεταξύ προηγηθείσας χορήγησης αντιμικροβιακών και εμφάνισης αντοχής τύπου ESBL, κυρίως στα εντεροβακτηριοειδή (MacAdam και συν 2006). Η προηγούμενη έκθεση σε κεφαλοσπορίνες 3 ης γενιάς αποτελεί συχνό παράγοντα κινδύνου ανάπτυξης λοίμωξης από μικρόβια που παράγουν ESBL, και αυτό έχει αποδειχθεί εκτός από τους ενήλικες, σε νεογνά και παιδιά (Huang και συν 2007, Hussein και συν 2009). Εκτός από τις κεφαλοσπορίνες 3 ης γενιάς, και τα υπόλοιπα αντιμικροβιακά της κατηγορίας των β-λακταμικών έχουν συσχετισθεί με την εμφάνιση μικροβίων που παράγουν ESBL, καθώς επίσης και διάφορες κατηγορίες όπως είναι οι αμινογλυκοσίδες, οι φθοροκινολόνες και ο συνδυασμός τριμεθοπρίμης/σουλφομεθοξαζόλης (Zaoutis και συν 2005, Graffunder και συν 2002, Rodriguez-Bano και συν 2008). Η εμφάνιση στελεχών εντεροβακτηριοειδών (κυρίως K. pneumoniae) με αντοχή στις καρβαπενέμες έχει μελετηθεί πρόσφατα, όπου επίσης φαίνεται συσχέτιση μεταξύ της εμφάνισης αυτών των στελεχών και της κατανάλωσης διαφόρων αντιμικροβιακών παραγόντων όπως οι καρβαπενέμες, οι κεφαλοσπορίνες 3 ης γενιάς και οι φθοροκινολόνες (Nordmann και συν 2009, Hussein και συν 2009, Daikos και συν 2009). Παρομοίως, η κατανάλωση ιδίως των καρβαπενεμών, κινολονών και κεφαλοσπορινών 3 ης γενιάς έχει συσχετισθεί σε μελέτες ασθενών-μαρτύρων με την εμφάνιση πολυανθεκτικών στελεχών A. baumannii και P.aeruginosa (Giamarellou και συν 2008, Pena και συν 2009). Στο σημείο αυτό, αξίζει να σημειωθεί ότι ενώ οι μελέτες σε επίπεδο ασθενών φαίνεται να προσεγγίζουν καλύτερα τη συσχέτιση μεταξύ κατανάλωσης και εμφάνισης αντοχής, υπάρχουν μεθοδολογικά προβλήματα που επηρεάζουν τα αποτελέσματα (Harris και συν 2000, Wacholder και συν 1992). Πιο συγκεκριμένα, αυτό που προβληματίζει στις μελέτες ασθενών-μαρτύρων είναι η σωστή επιλογή της ομάδας των μαρτύρων (controls). Συνήθως επιλέγονται στην ομάδα των μαρτύρων άτομα που έχουν την ίδια λοίμωξη με την ομάδα των ασθενών, αλλά με ευαίσθητα μικρόβια (αν εξετάζεται η αντοχή σε ένα αντιμικροβιακό, η μια ομάδα έχει το ανθεκτικό μικρόβιο και η άλλη το ευαίσθητο). Σε αυτήν την περίπτωση όμως, έχει αποδειχθεί ότι συνήθως υπερεκτιμάται ο κίνδυνος της έκθεσης στο υπό μελέτη αντιμικροβιακό (Harris και συν 2002). 39
40 Αντοχή μικροβίου 5. Παρέμβαση Όπως φαίνεται από τις μελέτες συσχέτισης μεταξύ κατανάλωσης αντιμικροβιακών και εμφάνισης αντοχής, υπάρχει γενικά μια ειδική σχέση μεταξύ του εκάστοτε μικροβίου και του αντιμικροβιακού. Για το λόγο αυτό, χρειάζεται γνώση της σχέσης αυτής για κάθε μικρόβιο και αντιμικροβιακό φάρμακο, ώστε να είναι περισσότερο αποτελεσματική η οποιαδήποτε παρέμβαση, αλλά ταυτόχρονα να καθορισθεί και το είδος αυτής της παρέμβασης. Όπως φαίνεται στο σχήμα 2, ανάλογα με το ποσοστό αντοχής ενός μικροβίου σε ένα αντιμικροβιακό και την κατανάλωση αυτού του αντιμικροβιακού σε μια κλινική/νοσοκομείο, καθορίζεται καλύτερα η παρέμβαση εκείνη που είναι απαραίτητη. Α. Β. Γ. Δ. Κατανάλωση αντιμικροβιακών σε Συμβατικές Ημερήσιες Δόσεις (DDDs) ανα 100 κρεβάτια ημέρες Σχήμα 4: Σχέση κατανάλωσης αντιμικροβιακών και ανάπτυξης αντοχής: Α. Υψηλή αντοχή με χαμηλή κατανάλωση αντιμικροβιακών Β. Υψηλή κατανάλωση αντιμικροβιακών και μεγάλα ποσοστά αντοχής Γ. Χαμηλή κατανάλωση αντιμικροβιακών και χαμηλή αντοχή Δ. Υψηλή κατανάλωση αντιμικροβιακών και χαμηλή αντοχή (Τροποποιημένο, Monnet συν 1998a). Πιο συγκεκριμένα, ο τρόπος παρέμβασης καθορίζεται σύμφωνα με τα παρακάτω: 40
41 Α. Υψηλή αντοχή, χαμηλή κατανάλωση αντιμικροβιακών: Πιθανές κατευθύνσεις προς βελτίωση είναι ο έλεγχος των λοιμώξεων, εύρεση των αποικισμένων ασθενών με την εισαγωγή, σωστή δοσολογία αντιμικροβιακών, χρήση εναλλακτικών αντιμικροβιακών. Β. Υψηλή αντοχή και μεγάλη κατανάλωση αντιμικροβιακών: Κατεύθυνση τόσο προς βελτίωση της κατανάλωσης αντιμικροβιακών, αλλά και αυστηρότερη τήρηση των μέτρων οριζόντιας μετάδοσης μικροβίων. Γ. Χαμηλή αντοχή, χαμηλή κατανάλωση: Επαγρύπνηση για είσοδο ανθεκτικών μικροβίων, συνέχιση της ορθολογικής χρήσης αντιμικροβιακών. Δ. Χαμηλή αντοχή, σχετικά υψηλή κατανάλωση: Κατεύθυνση προς βελτίωση των μεθόδων ανίχνευσης της αντοχής στο εργαστήριο. Πιθανή εξήγηση γιατί ανθεκτικά μικρόβια δεν έχουν εισαχθεί στην κλινική. Προσπάθεια παρέμβασης για ορθολογική χρήση αντιμικροβιακών. Βέβαια, η πιο συχνή περίπτωση που καταγράφεται στις περισσότερες κλινικές, και ιδίως στα τριτοβάθμια νοσοκομεία, είναι η μεγάλη κατανάλωση αντιμικροβιακών, καθώς και η οριζόντια μετάδοση ανθεκτικών μικροβίων. Συνεπώς, η παρέμβαση χρειάζεται να γίνει ταυτόχρονα και στα δύο επίπεδα. Σε μια πρόσφατη εκστρατεία, για την πρόληψη της εμφάνισης αντοχής στα μικρόβια, το CDC στις ΗΠΑ ανέπτυξε ένα πρόγραμμα με 4 στρατηγικές και 12 τομείς παρέμβασης -12 βήματα-, όπως φαίνεται στον πίνακα 6 ( Οι στρατηγικές αυτές, απευθύνονται σε νοσηλευόμενους ενήλικες ασθενείς, ασθενείς με αιμοκάθαρση, χειρουργικούς ασθενείς, νοσηλευόμενα παιδιά, καθώς και σε ασθενείς που νοσηλεύονται σε θεραπευτήρια για μακρό χρονικό διάστημα ( Είναι ενδιαφέρον ότι, μεταξύ των στρατηγικών, αναφέρεται η ορθολογική χρήση αντιμικροβιακών και ο έλεγχος της οριζόντιας μετάδοσης μικροβίων. Παραθέτει όμως, και δύο ακόμη στρατηγικές που έχουν μεγάλη σημασία. Αυτές είναι η πρόληψη της εμφάνισης νοσοκομειακών λοιμώξεων και η σωστή διάγνωση. Όταν δεν υπάρχει μέριμνα για πρόληψη ή και σωστή διάγνωση των λοιμώξεων, συνήθως οδηγούμαστε σε χρήση και κατάχρηση των αντιμικροβιακών και κατ επέκταση σε εμφάνιση αντοχής. Παρά τη 41
42 δημοσίευση αυτών των στρατηγικών, μέχρι σήμερα ελάχιστη είναι η εμπειρία από δημοσιεύσεις πάνω στον τομέα αυτόν. Πρόσφατα, η εφαρμογή αυτών των μέτρων μελετήθηκε σε 4 μονάδες εντατικής νοσηλείας νεογνών στις ΗΠΑ, όπου απλά διαπιστώθηκε ότι η ακατάλληλη συνταγογράφηση αντιμικροβιακών ήταν αρκετά συχνή (Patel και συν 2009). Αξίζει να σημειωθεί ότι, όταν πρόκειται για παρέμβαση είτε στο επίπεδο ελέγχου της οριζόντιας μετάδοσης πολυανθεκτικών μικροβίων είτε στο επίπεδο της ορθολογικής χρήσης των αντιβιοτικών, συνήθως ακολουθείται η τακτική του λεγόμενου κλινικού ελέγχου ή «audit» (Hay 2006). Σύμφωνα με τον ορισμό κλινικό «audit» θεωρείται εκείνη η διαδικασία που αποσκοπεί στην βελτίωση της παροχής φροντίδας του ασθενούς μέσα από συστηματική ανασκόπηση όλων των δεδομένων, σύγκριση με την υπάρχουσα κλινική πράξη και εφαρμογή των όποιων απαραίτητων αλλαγών (Hay 2006). Σχήμα 5: Κύκλος «audit» ελέγχου και ανατροφοδότησης μιας παρέμβασης, για τη βελτίωση της ποιότητας στην παροχή φροντίδας των ασθενών. 42
43 Πίνακας 6: Δώδεκα βήματα που προτείνονται από το CDC, για την πρόληψη εμφάνισης αντοχής στα αντιμικροβιακά για ενήλικες και παιδιά ( ) Στρατηγική: Πρόληψη των λοιμώξεων Βήμα 1 Εμβολιασμός νοσηλευόμενων ασθενών και προσωπικού Βήμα 2 Απομάκρυνση των ξένων σωμάτων, όταν αυτό είναι εφικτό Τοποθέτηση καθετήρων και εξαρτημάτων μόνο όταν είναι απαραίτητα Χρήση κατάλληλων διαδικασιών, για την τοποθέτηση και περιποίησή τους Απομάκρυνσή τους, όταν πλέον δεν είναι αναγκαίοι Στρατηγική: Διάγνωση και Θεραπεία της λοίμωξης αποτελεσματικά Βήμα 3 Χρήση κατάλληλων μεθόδων για την έγκυρη διάγνωση Βήμα 4 Στόχευση στο παθογόνο αίτιο Κατεύθυνση της εμπειρικής θεραπείας στο πιο πιθανό παθογόνο Κατεύθυνση της οριστικής θεραπείας έναντι των γνωστών παθογόνων Βήμα 5 Συμβουλή από ειδικούς λοιμωξιολόγους Ιδίως σε επιπλεγμένες και δύσκολες στην αντιμετώπιση λοιμώξεις Στρατηγική: Ορθολογική χρήση των αντιμικροβιακών Βήμα 6 Έλεγχος της πρακτικής χορήγησης αντιμικροβιακών Βελτίωση του χρόνου έναρξης, του σχήματος, της δοσολογίας, του τρόπου και της διάρκειας χορήγησης της αντιμικροβιακής αγωγής και προφύλαξης Τήρηση των πολιτικών ορθολογικής χρήσης αντιμικροβιακών και πρωτοκόλλων στην κάθε κλινική Βήμα 7 Χρήση τοπικών δεδομένων Γνώση της ευαισθησίας των μικροοργανισμών σε επίπεδο τοπικό (του νοσοκομείου και της κλινικής) Γνώση των ιδιαιτεροτήτων των ασθενών κάθε κλινικής Βήμα 8 Αντιμετώπιση της λοίμωξης και όχι του αποικισμού ή της επιμόλυνσης Χρήση σωστού τρόπου αντισηψίας του δέρματος για τη λήψη αιμοκαλλιεργειών Αποφυγή καλλιέργειας άκρων καθετήρων Θεραπεία της βακτηριαιμίας, όχι του αποικισμού του καθετήρα ή της επιμόλυνσης της καλλιέργειας Βήμα 9 Εκπαίδευση στην άρνηση Υπερκατανάλωσης βανκομυκίνης, ευρέως φάσματος κεφαλοσπορινών, καρβαπενεμών, φθοροκινολονών από το στόμα και λινεζολίδης Βήμα 10 Διακοπή θεραπείας Όταν η λοίμωξη είναι σχεδόν απίθανη Όταν, βάσει του αποτελέσματος των καλλιεργειών, δεν υπάρχει ένδειξη για χρήση αντιμικροβιακών Όταν η λοίμωξη θεραπεύτηκε Στρατηγική: Πρόληψη της οριζόντιας μετάδοσης Βήμα 11 Εφαρμογή των μέτρων οριζόντιας μετάδοσης Βήμα 12 Εφαρμογή της υγιεινής των χεριών 43
44 6. Ορθολογική χρήση των αντιμικροβιακών Η ορθολογική χρήση των αντιμικροβιακών αποτελεί ένα ξεχωριστό θέμα άμεσα συνδεδεμένο με την επιλογή και εμφάνιση πολυανθεκτικών μικροβίων. Να σημειωθεί ότι μια πολιτική ορθολογικής χρήσης αντιμικροβιακών περιλαμβάνει τόσο την έννοια της κατάλληλης θεραπείας -αιτιολογικός παράγων και ευαισθησία στα αντιμικροβιακά, κλινική εμπειρία στον άνθρωπο και στα ζώα, φαρμακολογία και τοξικότητα φαρμάκων- όσο και την σωστή επιλογή ενός συγκεκριμένου αντιμικροβιακού που είναι κατάλληλο με βάση τα προηγούμενα. Επιπλέον όμως, λαμβάνεται υπόψη και η απλότητα του σχήματος, η πιθανότητα ανάπτυξης αντοχής αλλά και το κόστος. Σύμφωνα με το CDC από τα 12 συγκεκριμένα βήματα για τη μείωση της εμφάνισης της αντοχής στο θέμα της ορθολογικής χρήσης των αντιμικροβιακών, περιλαμβάνεται η κατάλληλη και αποτελεσματική θεραπεία των λοιμώξεων, η χρήση αντιμικροβιακών παραγόντων με όσο το δυνατόν στενότερο φάσμα δράσης, θεραπεία των λοιμώξεων και όχι της επιμόλυνσης ή του αποικισμού, αποφυγή της παρατεταμένης διάρκειας χορήγησης των αντιμικροβιακών και ιδιαίτερη προσοχή στη χρήση ευρέως φάσματος αντιμικροβιακών. Πιστεύεται ότι με την επίτευξη των μέτρων αυτών για την ορθολογική χρήση των αντιμικροβιακών, θα μπορούσε να ελαττωθεί η πίεση επιλογής για τον πολλαπλασιασμό των πολυανθεκτικών μικροβίων και να επηρεαστεί με αυτόν τον τρόπο, η δυναμική της μετάδοσής τους. Για την εφαρμογή της ορθολογικής χρήσης των αντιμικροβιακών έχουν δημοσιευθεί συγκεκριμένες κατευθυντήριες οδηγίες (Dellit και συν 2007). Στις οδηγίες αυτές, χρησιμοποιείται ο όρος «καθοδήγηση στη χρήση των αντιμικροβιακών» (antimicrobial stewardship). Ουσιαστικά, η καθοδήγηση αυτή (Πίνακας 7) αποτελεί ένα σύστημα πληροφοριών, συλλογής δεδομένων και διαδικασιών που συμβάλλουν στην ορθολογική επιλογή, δοσολογία και διάρκεια της θεραπείας με τα αντιμικροβιακά φάρμακα (Owens 2008, Hersh συν 2009). Σκοπός της καθοδήγησης αυτής είναι η πρόληψη ή η καθυστέρηση στην εμφάνιση αντοχής στα μικρόβια, μείωση της συχνότητας των ανεπιθύμητων ενεργειών από τη χρήση των αντιμικροβιακών, που όλα αυτά μαζί οδηγούν σε μείωση της νοσηρότητας και θνητότητας των ασθενών, μείωση της διάρκειας παραμονής τους και ασφαλώς μείωση του κόστους νοσηλείας τους (Owens 2008, Buising και συν 2008, Patel και συν 2007). 44
45 Πίνακας 7: Στρατηγικές για την εφαρμογή ορθολογικής χρήσης αντιμικροβιακών και πιθανά εμπόδια. Στρατηγική ορθολογικής χρήσης αντιμικροβιακών Εμπόδια στην εφαρμογή 1. Προοπτικός κλινικός έλεγχος (audit) με παρέμβαση 1. Έλλειψη χρηματοδότησης και στην χορήγηση συγκεκριμένων αντιμικροβιακών και προσωπικού συνεχή ανατροφοδότηση (feedback) προς τους θεράποντες ιατρούς 2. Χρήση ειδικής λίστας περιορισμένων 2. Άγνοια του ρόλου, αλλά και της αντιμικροβιακών, που χορηγούνται μόνο κατόπιν πραγματικής ανάγκης ενός έγκρισης και για συγκεκριμένους λόγους προγράμματος ορθολογικής χρήσης αντιμικροβιακών τόσο από τη διοίκηση των νοσοκομείων όσο και από τους κλινικούς ιατρούς 3. Εκπαίδευση 3. Άρνηση από τους κλινικούς, καθώς φαίνεται ως παρέμβαση στην αυτονομία της ιατρικής πράξης τους 4. Δημιουργία και εφαρμογή κατευθυντήριων οδηγιών, 4. Έλλειψη τεχνολογικής υποστήριξης που αφορούν τη διάγνωση και αντιμετώπιση μέσα από για τη συγκέντρωση των δεδομένων, που αλγορίθμους είναι απαραίτητα για την αξιολόγηση της αντιμικροβιακής αγωγής των ασθενών 5. Ενίσχυση ή αποκλιμάκωση της αντιμικροβιακής 5. Έλλειψη γνώσης των κατευθυντήριων αγωγής, όπου χρειάζεται οδηγιών για την ορθολογική χρήση των αντιμικροβιακών 6. Αλλαγή, όταν πρέπει, της αντιμικροβιακής αγωγής από παρεντερική σε από του στόματος 7. Χορήγηση σωστού δοσολογικού σχήματος 8. Χρήση πληροφορικής για διασύνδεση των κλινικών και δυνατότητα συλλογής δεδομένων σε επίπεδο ασθενών 9. Χρήση δεδομένων από τη μικροβιολογική και επιδημιολογική επιτήρηση 45
46 Παρόλα αυτά, η αποτελεσματικότητα των οδηγιών αυτών όταν εκδόθηκαν δεν εμπεριείχε δεδομένα για ειδικούς πληθυσμούς ασθενών όπως είναι τα νεογνά στη ΜΕΝΝ, τα μεγάλα βρέφη και παιδιά στη ΜΕΘ, καθώς και τους ανοσοκατασταλμένους ασθενείς όπως για παράδειγμα αυτούς σε ογκολογικές κλινικές. Επίσης, ένας άλλος περιορισμός των συγκεκριμένων οδηγιών ήταν η έλλειψη δεδομένων για την αποτελεσματικότητα του συνδυασμού της ορθολογικής χρήσης αντιμικροβιακών και μέτρων πρόληψης της εμφάνισης νοσοκομειακών λοιμώξεων (Owens 2008). Σε πρόσφατη μελέτη από νοσοκομείο του Καναδά εφαρμόστηκε το πρόγραμμα ορθολογικής χρήσης αντιμικροβιακών στις μονάδες εντατικής νοσηλείας (Elligsen 2012a). Το χαρακτηριστικό του προγράμματος αυτού ήταν ο συστηματικός έλεγχος με ενδεχόμενη αναθεώρηση της αντιμικροβιακής αγωγής την 3 η και 10 η ημέρα χορήγησης στους ασθενείς που νοσηλεύονταν στις ΜΕΘ. Στη συγκεκριμένη μελέτη, κύριο ρόλο διαδραμάτιζαν οι δύο κλινικοί φαρμακοποιοί με εξειδίκευση στις λοιμώξεις, σε συνεργασία πάντοτε με τους λοιμωξιολόγους του νοσοκομείου. Με βάση αυτό το πρόγραμμα, που ξεκίνησε το 2009, πολύ πρόσφατα δημοσιεύθηκαν τα αποτελέσματα από την ίδια ομάδα, όπου διαγράφεται η στατιστικά σημαντική ελάττωση της κατανάλωσης των αντιμικροβιακών στις ΜΕΘ του νοσοκομείου, όπως επίσης και η ελάττωση της επίπτωσης της λοίμωξης από Clostridium difficile (Elligsen 2012b). Παρόμοια ευρήματα σε ό,τι αφορά την αποτελεσματικότητα των πολιτικών ορθολογικής χρήσης αντιμικροβιακών καταγράφηκαν σε μια συστηματική ανασκόπηση της βιβλιογραφίας που έγινε από το 1996 έως το 2010 και αφορούσε δεδομένα που προέρχονταν αποκλειστικά από ΜΕΘ (Kaki 2011). Μόνο 24 μελέτες είχαν τα απαραίτητα κριτήρια για να ενταχθούν στη μελέτη αυτή, αλλά με αρκετά μεγάλη ετερογένεια στη μεθοδολογία τους. Οι περισσότερες είχαν διεξαχθεί σε ΜΕΘ ενηλίκων (μικτές, παθολογικές, χειρουργικές, τραύματος, εγκαυμάτων) και 2 σε παιδιά (1 ΜΕΘ παίδων, 1 ΜΕΝΝ)-, με διάρκεια παρακολούθησης από 1 έως 54 μήνες. Από άποψη μεθοδολογίας, οι περισσότερες ήταν μη τυχαιοποιημένες μελέτες με δεδομένα καταγραφής προ και μετά την παρέμβαση, και μόνο δύο μελέτες ήταν τυχαιοποιημένες. Παρόλα αυτά καταγράφεται σαφώς η αποτελεσματικότητα των πολιτικών αυτών, κυρίως στην ελάττωση της κατανάλωσης των αντιμικροβιακών, αλλά και στη μείωση της αντοχής των παθογόνων μετά από τουλάχιστον 6 μήνες παρέμβασης (Kaki 2011). Στα παιδιά έχουν δημοσιευθεί πολύ λίγες μελέτες που αφορούν την εφαρμογή της ορθολογικής χρήσης των αντιμικροβιακών (Bradley και συν 2007; Metjian και συν 2008, Hersh 46
47 και συν 2009). Από τους πρώτους ερευνητές που αξιολόγησαν την εφαρμογή προγράμματος ορθολογικής χρήσης αντιμικροβιακών σε νοσοκομείο παίδων ήταν οι Metjian και συν, και η μελέτη έλαβε χώρα σε ένα τριτοβάθμιο νοσοκομείο παίδων στη Φιλαδέλφεια των ΗΠΑ (Metjian και συν 2008). Το πρόγραμμα αυτό ουσιαστικά περιελάμβανε προοπτικά την αξιολόγηση της χρήσης των υπό περιορισμό αντιμικροβιακών, δηλαδή αντιμικροβιακά για τα οποία υποχρεωτικά έπρεπε να ληφθεί έγκριση από το πρόγραμμα, και την παρέμβαση για την ορθολογική χρήση τους. Τα αποτελέσματα της εφαρμογής ενός παρόμοιου προγράμματος καθοδήγησης της χρήσης των αντιμικροβιακών σε νοσοκομείο παίδων δημοσιεύθηκαν πρόσφατα από τους Di Pentima και συν (Di Pentima και συν 2011). Σύμφωνα με τους ερευνητές, η εφαρμογή του προγράμματος συνετέλεσε στη δραστική μείωση της κατανάλωσης όλων των υπό περιορισμό και μη αντιμικροβιακών και συγχρόνως, η μικροβιακή αντοχή ήταν και παρέμεινε σταθερά σε χαμηλά ποσοστά. Ακόμη περισσότερο ενδιαφέρον παρουσιάζουν τα πολύ πρόσφατα αποτελέσματα μιας μελέτης, στην οποία εφαρμόστηκαν οι κατευθυντήριες οδηγίες της ορθολογικής χρήσης αντιμικροβιακών σε τριτοβάθμιο νοσοκομείο παίδων στις ΗΠΑ για χρονικό διάστημα 34 μηνών και συγκρίθηκαν τα αποτελέσματα με νοσοκομεία στα οποία δεν είχε εφαρμοσθεί η παρέμβαση (Saiman και συν 2012, Newland και συν 2012). Η μελέτη απέδειξε ότι όταν η παρέμβαση για τη σωστή χρήση των αντιμικροβιακών γίνεται προοπτικά με συστηματικό κλινικό έλεγχο (audit) και συνεχή ανατροφοδότηση προς τους θεράποντες ιατρούς, μπορεί να ελαττώσει σημαντικά τόσο την κατανάλωση των αντιμικροβιακών όσο και τη διάρκεια χορήγησής τους σε επίπεδο ασθενούς (Newland και συν 2012). Να σημειωθεί ότι στη συγκρεκιμένη μελέτη, η συχνότερη μορφή παρέμβασης ήταν η διακοπή της τρέχουσας αντιμικροβιακής αγωγής. Αν και η εφαρμογή αυτών των κατευθυντήριων οδηγιών, αποδεδειγμένα μειώνει σημαντικά το ποσοστό της συνταγογράφησης ακατάλληλης αντιμικροβιακής αγωγής, ένα από τα κύρια προβλήματά της είναι ακριβώς η συμμόρφωση των θεραπόντων ιατρών με αυτές τις οδηγίες (Dellit και συν 2007). Γίνεται αρκετή έρευνα για τη βελτίωση του τρόπου προώθησης των πολιτικών αυτών στους θεράποντες ιατρούς, είτε αυτές αφορούν την ορθολογική συνταγογράφηση αντιμικροβιακών είτε την τήρηση των μέτρων ελέγχου των λοιμώξεων (Mah και συν 2009). Σύμφωνα με μια ανασκόπηση της βιβλιογραφίας, ελάχιστες είναι οι μελέτες εκείνες που χρησιμοποιούν τεκμηριωμένες μεθόδους των κοινωνικών και ψυχολογικών επιστημών για την προώθηση της εφαρμογής των πολιτικών ορθολογικής χρήσης 47
48 αντιμικροβιακών και προτείνουν τρόπους που μπορεί να γίνει αυτό καλύτερα (Πίνακας 8) (Charani και συν 2011). Ενθαρρυντικά είναι τα απότελέσματα των πρόσφατων μελετών σε νοσοκομείο παίδων, όπου η συμμόρφωση στην εφαρμογή των κατευθυντήριων οδηγιών για τη χρήση των αντιμικροβιακών ήταν πολύ καλή (Metjian και συν 2008). Πίνακας 8: Συστάσεις για την εφαρμογή μεθόδων κοινωνικών και ψυχολογικών επιστημών, για την προώθηση και εφαρμογή των μέτρων ορθολογικής χρήσης των αντιμικροβιακών από τους θεράποντες ιατρούς. Σύσταση Περιγραφή Διεξαγωγή πρωτογενούς έρευνας Διακλινική πρωτογενής έρευνα. Χρήση των γνώσεων των κοινωνικών και ψυχολογικών επιστημών για την ανεύρεση των καθοριστικών κλειδιών που αφορούν την αλλαγή της συμπεριφοράς των θεραπόντων ιατρών Διαμόρφωση της παρέμβασης Χρήση των δεδομένων της πρωτογενούς έρευνας για την προσαρμογή και διαμόρφωση της παρέμβασης με τέτοιον τρόπο, ώστε να αναγνωρίζονται τα προβλήματα και να ενισχύεται η όποια θετική αλλαγή της συμπεριφοράς Αξιολόγηση των αποτελεσμάτων Αξιολόγηση της παρέμβασης στην αλλαγή συμπεριφοράς της παρέμβασης των θεραπόντων ιατρών, ως προς την ορθολογική επιλογή των αντιμικροβιακών Συνέχιση της αξιολόγησης για Καταγραφή της μακροχρόνιας εφαρμογής των μέτρων της επίτευξη μακροχρόνιων παρέμβασης αποτελεσμάτων Ένα άλλο σημαντικό θέμα των πολιτικών ορθολογικής χρήσης αντιμικροβιακών είναι η ιδιότητα του ατόμου που είναι υπεύθυνο για την καθοδήγηση και τις συστάσεις. Αυτό που ορίζεται είναι ότι η καθοδήγηση για την ορθολογική χρήση των αντιμικροβιακών μπορεί να παρέχεται είτε από λοιμωξιολόγο είτε από κλινικό φαρμακοποιό με εξειδίκευση στις λοιμώξεις (Dellit συν 2007, Saiman και συν 2012). Μάλιστα, ο όρος καθοδήγηση στην ορθολογική χρήση των αντιμικροβιακών (antimicrobial stewardship) δεν πρέπει να συγχέεται με τον όρο 48
49 λοιμωξιολογική εκτίμηση και καθοδήγηση (infectious disease consultation) (Saiman και συν 2012). Αξίζει να σημειωθεί ότι από το 2008 ο ευρωπαϊκός οργανισμός European Centre for Disease Prevention and Control (ECDC) έχει ορίσει την 18 η Νοεμβρίου ώς την ημέρα για την επαγρύπνηση στη χρήση των αντιμικροβιακών ( 7. Πρόληψη της οριζόντιας μετάδοσης μικροβίων 7.1. Ο ρόλος της οριζόντιας μετάδοσης πολυανθεκτικών μικροβίων Η εμφάνιση των πολυανθεκτικών μικροβίων σε μια μονάδα είτε λόγω της μη ορθολογικής χρήσης αντιμικροβιακών είτε λόγω της νοσηλείας ενός ασθενούς που έχει λοίμωξη ή είναι αποικισμένος με πολυανθεκτικό μικρόβιο από άλλο νοσοκομείο, δεν προδικάζει την εμφάνιση επιδημίας. Αντίθετα, η μετάδοση και η παραμονή των μικροβίων αυτών καθορίζεται από ποικίλους παράγοντες. Οι παράγοντες αυτοί μπορούν να διακριθούν σε αυτούς που σχετίζονται με τη νοσηλεία του ασθενούς και σε αυτούς που σχετίζονται με τον ίδιο τον ασθενή. Η χαμηλή συμμόρφωση του ιατρονοσηλευτικού προσωπικού στην υγιεινή των χεριών, η ελλιπής χρήση γαντιών, ποδιάς και μάσκας, η μη τήρηση της υγιεινής του περιβάλλοντος, ο συνωστισμός, ο αυξημένος δείκτης αποικισμού σε μια μονάδα, και ασφαλώς ο χαμηλός δείκτης νοσηλευτριών/ασθενών αποτελούν μερικούς από τους παράγοντες αυτούς. Από την πλευρά του αρρώστου, παράγοντες που σχετίζονται με τη λοίμωξη με ανθεκτικά μικρόβια είναι η έκθεση στα αντιμικροβιακά, η σοβαρότητα της νόσου, συνυπάρχουσες παθολογικές καταστάσεις, η ηλικία και η κατάσταση του ανοσιακού του συστήματος (Siegel και συν 2007a, Kane και συν 2007, Beggs και συν 2006). Πιο αναλυτικά, υπάρχουν πλέον σαφή δεδομένα για τη μετάδοση των πολυανθεκτικών μικροβίων από ασθενή σε ασθενή μέσω των χεριών του ιατρικού και νοσηλευτικού προσωπικού. Τα χέρια εύκολα αποικίζονται κατά τη διάρκεια της φροντίδας του ασθενούς, αλλά και κατά την επαφή με αντικείμενα και επιφάνειες που βρίσκονται σε άμεση γειτνίαση με τον ασθενή. Ιδίως τα εντεροβακτηριοειδή και ο εντερόκοκκος, που έχουν σχέση με το γαστρεντερικό σύστημα του ασθενούς, μπορούν πολύ εύκολα να αποικίσουν τον περιβάλλοντα χώρο του ασθενούς. Αντικείμενα για τη φροντίδα του ασθενούς, όπως για παράδειγμα, ηλεκτρονικά ή υδραργυρικά θερμόμετρα και μετρητές γλυκόζης, μπορεί να έχουν αποικισθεί με αυτά τα πολυανθεκτικά 49
50 μικρόβια εάν έρθουν σε επαφή με βιολογικά υγρά του ασθενούς και χρησιμοποιηθούν χωρίς να έχουν καθαρισθεί και απολυμανθεί κατάλληλα μεταξύ των ασθενών. Ιατρικά εργαλεία και συσκευές, όπως επίσης και τα παιχνίδια που μπορεί να υπάρχουν, καθώς και άλλα άψυχα αντικείμενα του περιβάλλοντος μπορούν να μολυνθούν και να αποικισθούν με πολυανθεκτικά μικρόβια (Siegel και συν 2007a, Kane και συν 2007, Beggs και συν 2006). Σπάνια, έχουν περιγραφεί περιπτώσεις στις οποίες το προσωπικό του νοσοκομείου είναι αυτό που εισάγει ένα πολυανθεκτικό μικρόβιο σε μια μονάδα. Σε αυτήν την περίπτωση όμως, πρέπει να συντρέχουν και άλλοι λόγοι για να μπορέσει να γίνει αυτή η μετάδοση και ο αποικισμός, με ή χωρίς λοίμωξη, των ασθενών. Ιδιαίτερο ενδιαφέρον παρουσιάζει στη μελέτη της οριζόντιας μετάδοσης πολυανθεκτικών μικροβίων η λεγόμενη «πίεση αποικισμού» (colonization pressure) ή αλλιώς το μέγεθος (επιπολασμός) του αποικισμού. Αυτό σε μια μονάδα σχετίζεται με τον αριθμό των νέων περιστατικών που θα αποικισθούν. Ένας ασθενής που εισάγεται σε μια μονάδα που έχει 10 ασθενείς έχει μεγαλύτερες πιθανότητες να αποικισθεί από πολυανθεκτικό μικρόβιο, όταν οι υπόλοιποι 6 είναι ήδη αποικισμένοι από ό,τι αν ήταν 2 μόνο οι αποικισμένοι. Ως συνέχεια αυτής της λογικής, σημασία έχει και η διάρκεια παραμονής σε έναν χώρο, όπου υπάρχουν ασθενείς αποικισμένοι με πολυανθεκτικά μικρόβια (Kane και συν 2007, Foglia και συν 2007, Arvaniti και συν 2012) Τρόποι ελέγχου της οριζόντιας μετάδοσης πολυανθεκτικών μικροβίων Η αύξηση της συχνότητας πολυανθεκτικών μικροβίων, η έλλειψη νέων αντιμικροβιακών παραγόντων για την καταπολέμησή τους και οι δυνατότητες μετάδοσης μεταξύ των ασθενών, καθιστούν επιτακτική τη χρήση μέτρων μείωσης της διασποράς τους (πίνακας 7). Η λήψη μέτρων για την πρόληψη της μετάδοσης των παθογόνων αυτών απαιτεί συντονισμένες ενέργειες και συνεργασία όλου του προσωπικού σε ένα νοσοκομείο περιλαμβάνοντας τόσο το ιατρικό όσο και το νοσηλευτικό, παραϊατρικό και διοικητικό προσωπικό (Kolar και συν 2006, Shlaes 1997). 50
51 Πίνακας 9. Βασικά μέτρα για την πρόληψη μετάδοσης παθογόνων μικροοργανισμών στα νοσοκομεία Α: Διοικητικά μέτρα- Τήρηση των κατευθυντήριων οδηγιών Β: Υγιεινή χεριών- Βασικές προφυλάξεις και προφυλάξεις επαφής Γ : Υγιεινή του περιβάλλοντος Δ: Εκπαίδευση Ε: Επιδημιολογική επιτήρηση (κλασσική και ενισχυμένη) Ζ: Ορθολογική χρήση των αντιμικροβιακών Α. Διοικητικά μέτρα- Τήρηση των κατευθυντήριων οδηγιών Θα πρέπει καταρχήν η διοίκηση του νοσοκομείου να μεριμνά για τη σύσταση και λειτουργία επιτροπής νοσοκομειακών λοιμώξεων, με την οποία θα έχει άριστη συνεργασία για την επίλυση των προβλημάτων που τυχόν προκύπτουν. Η διοίκηση, σε αυτήν την περίπτωση, θα πρέπει να παρέχει πλήρη υποστήριξη των μέτρων για τη διακοπή της μετάδοσης των πολυανθεκτικών μικροβίων και την πρόληψη για την εμφάνιση επιδημίας. Η υποστήριξη αυτή πρέπει να είναι τόσο οικονομική όσο και σε ανθρώπινο δυναμικό. Πολλά από τα προγράμματα, όπως αναφέρεται παρακάτω, όπως για παράδειγμα, η ενεργητική επιτήρηση της φορείας πολυανθεκτικών μικροβίων, χρειάζονται επιπρόσθετες διαδικασίες, αναλώσιμα και περισσότερες ώρες εργασίας, που σημαίνει περισσότερο προσωπικό. Τομείς, στους οποίους μπορεί η διοίκηση να παρέχει βοήθεια σε συνδυασμό με την επιτροπή λοιμώξεων, είναι η διατήρηση ικανοποιητικού αριθμού νοσηλευτριών ανά ασθενή, ιδίως για τις ΜΕΘ ενηλίκων, παίδων και νεογνών, παροχή του απαραίτητου εξοπλισμού και υλικοτεχνικής υποδομής για τις βασικές και ειδικές προφυλάξεις και απομονώσεις ασθενών, καθώς και δυναμική συμμετοχή στην ενδυνάμωση της συμμόρφωσης όλου του προσωπικού με τις κατευθυντήριες οδηγίες, που αφορούν τον έλεγχο των λοιμώξεων. Επίσης, η βοήθεια της διοίκησης είναι ιδιαίτερα σημαντική στην εγκατάσταση πληροφοριακών συστημάτων για την έγκαιρη και συνεχή ενημέρωση για την κατάσταση αποικισμού ή λοίμωξης των ασθενών με πολυανθεκτικά μικρόβια. Έχουν αναφερθεί επιδημίες από πολυανθεκτικά μικρόβια εξαιτίας της έλλειψης επικοινωνίας μεταξύ των διαφόρων τμημάτων που μετακινούνται οι ασθενείς, όπως το χειρουργείο, το ακτινολογικό εργαστήριο και το εργαστήριο πυρηνικής ιατρικής (Kane και συν 2007, Beggs και συν 2006, Siegel και συν 2007a, Foglia και συν 2007, Pitout και συν 2008a, Pitout 2008b). Ειδικά στην Ελλάδα, το 2010 λόγω του προβλήματος της μικροβιακής αντοχής, συστάθηκε Εθνικό Σχέδιο Δράσης με την ονομασία «Προκρούστης». Βασικός σκοπός του στρατηγικού αυτού σχεδίου είναι η ελάττωση της αντιμικροβιακής αντοχής και κυρίως, η 51
52 μείωση της οριζόντιας μετάδοσης πολυανθεκτικών μικροβίων (στελέχη P. aeruginosa, K. pneumoniae και A. baumannii ανθεκτικά στις καρβαπενέμες). Βασικό μέρος αυτού του προγράμματος είναι η ευαισθητοποίηση και συμμετοχή της διοίκησης του νοσοκομείου. Β1. Υγιεινή χεριών Η υγιεινή των χεριών συχνά χαρακτηρίζεται ως ο μόνος και σημαντικότερος παράγοντας για την ελάττωση της μετάδοσης των παθογόνων μικροοργανισμών μεταξύ των ασθενών. Αποτελεί άλλωστε, και το κυριότερο στοιχείο των βασικών μέτρων προφύλαξης, όπως θα δούμε παρακάτω. Ο όρος «υγιεινή των χεριών» περιλαμβάνει το πλύσιμο των χεριών με τη χρήση απλού σαπουνιού και νερού, αντισηπτικό πλύσιμο των χεριών, επάλειψη με αντισηπτικό παράγοντα και τη χειρουργική αντισηψία των χεριών. Η υγιεινή των χεριών πρέπει να εφαρμόζεται από όλους και προς όλους τους ασθενείς και πρέπει να γίνεται (σχήμα 6): Πριν από επαφή με τον άρρωστο (βήμα 1 ο ). Εδώ συμπεριλαμβάνεται εκτός από την κλινική εξέταση, όπως για παράδειγμα, η σφυγμομέτρηση, η μέτρηση αρτηριακής πίεσης, η στηθοσκόπηση, η ψηλάφηση, και η απλή χειραψία, η τοποθέτηση μάσκας οξυγόνου, η βοήθεια στον ασθενή να σηκωθεί, και άλλα που συνήθως δεν λαμβάνονται υπόψη για να προηγηθεί η υγιεινή των χεριών. Με τον τρόπο αυτό, προστατεύεται ο ασθενής από τα παθογόνα μικρόβια που βρίσκονται στα χέρια του εξεταστή. Πριν από κάθε καθαρό ή άσηπτο χειρισμό (βήμα 2 ο ). Εδώ περιλαμβάνεται η επαφή με βλεννογόνους, για παράδειγμα στόμα, επιπεφυκότες, τοποθέτηση καθετήρων, ενδοφλέβια χορήγηση φαρμάκων, αναρρόφηση εκκρίσεων αναπνευστικού συστήματος, περιποίηση τραχειοστόματος, φροντίδα κεντρικού φλεβικού καθετήρα. Με τον τρόπο αυτό, προστατεύεται ο ασθενής από τα μικρόβια που αποικίζουν τον ίδιο ή τα χέρια του ιατρού/νοσηλευτή και μπορούν να γίνουν παθογόνα, εάν εισέλθουν στη συστηματική κυλοφορία του ασθενούς. Μετά από έκθεση σε σωματικά υγρά του ασθενή (βήμα 3 ο ). Δηλαδή, μετά από επαφή με βλεννογόνους του ασθενή, φροντίδα τραυμάτων, τοποθέτηση ενδοτραχειακού καθετήρα, αιμοληψία, λήψη δείγματος ούρων, επαφή με 52
53 εκκρίσεις του αναπνευστικού και γαστρεντερικού. Με το βήμα αυτό προστατεύεται ο ίδιος ο εξεταστής από τα παθογόνα μικρόβια του ασθενούς. Μετά από επαφή με τον ασθενή (βήμα 4 ο ). Δηλαδή μετά από χειραψία, κλινική εξέταση και άλλες ενέργειες, όπως περιγράφηκαν στο 1 ο βήμα. Με τον τρόπο αυτό, προστατεύεται ο εξεταστής και το επαγγελματικό του περιβάλλον από τα παθογόνα μικρόβια του ασθενούς. Μετά από επαφή με το άμεσο άψυχο περιβάλλον του ασθενή (βήμα 5 ο ). Εδώ περιλαμβάνονται η αλλαγή κλινοσκεπασμάτων, η ρύθμιση συσκευής έγχυσης ορού, η επαφή με το κομοδίνο, το κρεβάτι, διακόπτες ή άλλες συσκευές στην περιοχή του ασθενούς. Ο λόγος είναι ότι προστατεύεται ο εξεταστής από τα παθογόνα μικρόβια του ασθενούς. Βήμα 2 ο Βήμα 1 ο Βήμα 4 ο Βήμα 3 ο Βήμα 5 ο Σχήμα 6: Τα 5 βήματα για την υγιεινή των χεριών (Τροποποιημένο, ΚΕΕΛΠΝΟ, WHO). Ιδιαίτερη προσπάθεια πρέπει να καταβάλλεται για την αύξηση της συμμόρφωσης του προσωπικού με την υγιεινή των χεριών. Η εκπαίδευση, ο κλινικός έλεγχος (audit), αφίσες υπενθύμισης, εξασφάλιση απαραίτητου και άμεσα προσβάσιμου εξοπλισμού, επιβράβευση της συμμόρφωσης και επαρκής στελέχωση των τμημάτων με νοσηλευτές αποτελούν βασικούς τομείς για τη συμμόρφωση του προσωπικού στην υγιεινή των χεριών (Kane και συν 2007, Beggs και συν 2006, 53
54 Β2. Προφυλάξεις και απομόνωση ασθενών Οι προφυλάξεις διακρίνονται σε βασικές και ειδικές, σύμφωνα με τον τρόπο μετάδοσης του λοιμογόνου παράγοντα (πίνακας 8 και 9). Οι βασικές προφυλάξεις πρέπει να λαμβάνονται από όλο το προσωπικό και αφορούν την επαφή/φροντίδα με όλους τους ασθενείς. Οι ειδικές προφυλάξεις περιλαμβάνουν τις προφυλάξεις επαφής που έχουν άμεση σχέση με τα πολυανθεκτικά μικρόβια, τις αερογενείς προφυλάξεις (κυρίως για φυματίωση και ανευμευλογιά) και τις προφυλάξεις σταγονιδίων (κυρίως για γρίπη και μηνιγγιτιδόκοκκο). Για την πρόληψη της μετάδοσης πολυανθεκτικών μικροβίων πρέπει όλοι οι ασθενείς, που έχουν λοίμωξη ή είναι φορείς, να αντιμετωπίζονται με βάση τις προφυλάξεις επαφής ως προσθήκη στις βασικές προφυλάξεις ( Siegel και συν 2007a, Pratt και συν 2007). Σε αυτήν την περίπτωση, συνιστάται η τοποθέτηση ασθενών με πολυανθεκτικά μικρόβια σε μονόκλινα δωμάτια σε συνδυασμό με τις προφυλάξεις επαφής. Αν δεν είναι εφικτό κάτι τέτοιο, χρειάζεται η τοποθέτηση των ασθενών κατά ομάδες, να γίνεται δηλαδή χωροτακτικός διαχωρισμός (cohorting) όλων των ασθενών που έχουν το ίδιο πολυανθεκτικό μικρόβιο. Σε αυτήν την περίπτωση, είναι απαραίτητη η αποκλειστική απασχόληση του νοσηλευτικού προσωπικού χωριστά με τους ασθενείς αυτούς (Siegel και συν 2007a, Pratt και συν 2007). Γ. Υγιεινή περιβάλλοντος Με τον όρο «υγιεινή του περιβάλλοντος χώρου» του ασθενούς, εννοούμε όλα τα άψυχα αντικείμενα που βρίσκονται είτε στο άμεσο είτε στο ευρύτερο περιβάλλον του ασθενούς. Η διαχείριση των ιατρικών συσκευών και οργάνων του ασθενούς περιλαμβάνει το σωστό καθαρισμό και την απολύμανσή τους, ιδίως όταν έχουν έρθει σε επαφή είτε με το δέρμα του ασθενούς είτε με βιολογικά υγρά. Για το λόγο αυτό, ιδίως σε μονάδες εντατικής θεραπείας, συνιστάται η αποκλειστική χρήση ιατρικών εργαλείων και συσκευών, όπως για παράδειγμα τα στηθοσκόπια, περιχειρίδες του πιεσόμετρου και θερμόμετρα. Σε περίπτωση που αναπόφευκτα χρησιμοποιούνται όργανα πολλαπλών χρήσεων, όπως ζυγαριά, μηχανές μέτρησης σακχάρου, κεφαλή υπερηχογραφήματος, πρέπει οπωσδήποτε πρώτα να καθαρισθούν και να απολυμανθούν επαρκώς πριν από τη χρήση τους σε άλλους ασθενείς (Siegel και συν 2007a, Siegel και συν 2007b, Pratt και συν 2007). 54
55 Πίνακας 10. Βασικές προφυλάξεις Υγιεινή χεριών Πριν και μετά την επαφή (φροντίδα) με τον ασθενή Πριν και μετά τη χρήση γαντιών Αντισηψία χεριών με αλκοολούχο σκεύασμα, όταν τα χέρια δεν είναι εμφανώς λερωμένα Χρήση γαντιών Πριν την πιθανή έκθεση σε βιολογικά υγρά του σώματος (αίμα, υγρά παροχετεύσεων, εκκρίσεις κ.λπ.) και μολυσμένα αντικείμενα Πριν την πιθανή έκθεση σε βλεννογόνους και περιοχές του σώματος με λύση συνέχειας του δέρματος Χρήση μάσκας και προστατευτικών γυαλιών Για την προστασία ματιών, μύτης και στόματος, όταν υπάρχει κίνδυνος εκτίναξης βιολογικών υγρών ή διαλυμάτων Χρήση μπλούζας Για την προστασία του δέρματος και των ενδυμάτων κατά τη διάρκεια νοσηλείας ή παρεμβατικής πράξης, όπου υπάρχει κίνδυνος εκτίναξης βιολογικών υγρών ή διαλυμάτων Πίνακας 11. Προφυλάξεις επαφής που χρησιμοποιούνται επιπλέον των βασικών προφυλάξεων Γάντια Καθαρά γάντια, μη αποστειρωμένα, είναι αρκετά για την επαφή (φροντίδα) με τον ασθενή ή τον περιβάλλοντα χώρο. Η αφαίρεση των γαντιών γίνεται σωστά μετά την χρήση τους, χωρίς να έρθουν σε επαφή με άλλα αντικείμενα ή επιφάνειες και πριν την φροντίδα/εξέταση άλλου ασθενούς. Τα χέρια πλένονται αμέσως μετά την αφαίρεση των γαντιών προς αποφυγή μετάδοσης μικροοργανισμών σε άλλους ασθενείς ή στο περιβάλλον όπως επίσης και πριν την τοποθέτηση των γαντιών Μπλούζα Χρήση καθαρής, μη αποστειρωμένης μπλούζας συνιστάται σε κάθε περίπτωση που θα υπάρξει επαφή με τον ασθενή ή τον περιβάλλοντα χώρο του. Αφαίρεση της μπλούζας μετά την ολοκλήρωση της φροντίδας του ασθενούς. Τοποθέτηση του ασθενούς Συνιστάται η τοποθέτηση του ασθενούς σε μονόκλινο δωμάτιο εκεί όπου είναι εφικτό ή ο διαχωρισμός (cohort) των ασθενών που έχουν τον ίδιο ανθεκτικό μικροοργανισμό. Αντικείμενα ατομικής φροντίδας ασθενούς Συνιστάται η αποκλειστική χρήση μη κριτικών αντικειμένων (περιχειρίδες πιεσόμετρου, ηλεκτρόδια, ζυγαριά κ.λπ.) Σειρά αφαίρεσης του ατομικού προστατευτικού εξοπλισμού Πρώτα τα γάντια και μετά η ποδιά και η μάσκα Aboelela και συν
56 Οριζόντιες επιφάνειες εντός της κλινικής, χειρολαβές, επιφάνειες και πλήκτρα ιατρικών μηχανημάτων (monitors) χρειάζεται να καθαρίζονται τακτικά, ώστε να μην αποτελούν πηγή συνεχούς μόλυνσης των χεριών του προσωπικού. Επίσης οι φάκελοι των ασθενών, διαγράμματα και χαρτικά που βρίσκονται πολύ κοντά στον ασθενή, μπορεί να αποτελέσουν πρόβλημα. Στις ΜΕΘ παίδων, όπου νοσηλεύονται παιδιά διαφόρων ηλικιακών ομάδων, είναι δυνατό να υπάρχουν παιχνίδια. Υπάρχουν ειδικοί τρόποι πλυσίματος για πολλά από τα παιχνίδια αυτά, ώστε να αποφευχθεί ο αποικισμός τους (Siegel και συν 2007a). Δ. Επιδημιολογική επιτήρηση πολυανθεκτικών μικροβίων Με τη βοήθεια της επιδημιολογικής επιτήρησης είναι δυνατή η ανίχνευση νέων πολυανθεκτικών μικροβίων, παρακολούθηση του επιπολασμού και της επίπτωσης των πολυανθεκτικών μικροβίων και τέλος καταγραφή της αποτελεσματικότητας των διαφόρων παρεμβάσεων. Η επιδημιολογική επιτήρηση μπορεί να είναι είτε παθητική είτε ενεργητική. Με τον όρο «παθητική επιδημιολογική επιτήρηση» εννοούμε ότι μελετώνται όλα τα κλινικά δείγματα που αποστέλλονται στο μικροβιολογικό εργαστήριο και προέρχονται από ασθενείς με κάποια μορφή λοίμωξης. Υπάρχει έτσι η δυνατότητα παρακολούθησης της αντοχής, καθώς και εύρεσης νέων μηχανισμών αντοχής, που είναι πιθανό να προκύψουν (Siegel και συν 2007b, Filius και συν 2005, Shlaes και συν 1997, Aboelela και συν 2006, Pratt και συν 2007). Στην ενεργητική επιδημιολογική επιτήρηση γίνεται συστηματική λήψη καλλιεργειών από όλους τους νοσηλευόμενους ασθενείς, ή από συγκεκριμένους ορισμένες φορές, για την ανίχνευση εκείνων των ασθενών που είναι αποικισμένοι με πολυανθεκτικά μικρόβια. Τα συνήθη σημεία που καλλιεργούνται είναι ο φάρυγγας, το γαστρικό υγρό, το περίνεο και το δέρμα. Σκοπός αυτής της ενεργητικής επιτήρησης, με τον εντοπισμό των αποικισμένων ασθενών, είναι η πρωτογενής προφύλαξη των ασθενών που δεν έχουν αποικισθεί για να αποφευχθεί ο αποικισμός και η λοίμωξή τους, καθώς και η δευτερογενής προφύλαξη για τους ήδη αποικισμένους ασθενείς, προφύλαξη από την ενδογενή λοίμωξη. Απώτερος σκοπός είναι η μείωση της νοσηρότητας και θνητότητας που σχετίζονται με τη λοίμωξη από τους συγκεκριμένους μικροοργανισμούς (Siegel και συν 2007b, Filius και συν 2005, Shlaes και συν 1997, Aboelela και συν 2006, Pratt και συν 2007). Στα στελέχη που προκύπτουν από την επιδημιολογική επιτήρηση, πολλές φορές έχει μεγάλη σημασία να γίνει προσδιορισμός της μεταξύ τους συσχέτισης. Η γνώση αυτή παρέχει 56
57 πληροφορίες ουσιαστικά για την οριζόντια μετάδοση των πολυανθεκτικών μικροβίων και μπορεί να βοηθήσει στην εντόπιση της αρχικής πηγής. Για τον σκοπό αυτό σήμερα, χρησιμοποιούνται διάφορες μέθοδοι τυποποίησης είτε φαινοτυπικές είτε γονοτυπικές (μοριακές). Από τις φαινοτυπικές μεθόδους η πιο απλή και καθημερινά χρησιμοποιούμενη μέθοδος είναι η χρήση του αντιβιογράμματος, η μελέτη δηλαδή της ευαισθησίας των στελεχών σε έναν αριθμό αντιμικροβιακών παραγόντων. Δύο διαφορετικά μεταξύ τους αντιβιογράμματα έχουν λιγότερη πιθανότητα να προέρχονται από τον ίδιο κλώνο. Άλλες λιγότερο συχνές μέθοδοι που χρησιμοποιούνται είναι η βιοτυπία, λυσιτυπία και η οροτυπία. Σε ό,τι αφορά τις μοριακές μεθόδους, η ηλεκτροφόρηση σε παλλόμενο ηλεκτρικό πεδίο (pulse field gel electrophoresis, PFGE) θεωρείται η πιο αξιόπιστη μέθοδος και είναι αυτή που συνήθως χρησιμοποιείται στις μελέτες ως μέθοδος αναφοράς (gold standard). Άλλες μέθοδοι που χρησιμοποιούνται βασίζονται κυρίως στη τεχνική της PCR (polymerase chain reaction) και είναι οι παρακάτω: random amplification of polymorphic DNA (RAPD, or AP-PCR), PCR-Restriction Fragment Length polymorphism (PCR-RFLP), Amplified Fragment Length Polymorphism (AFLP). Παλιότερες μέθοδοι που χρησιμοποιήθηκαν, χωρίς όμως καλά αποτελέσματα, ήταν η πλασμιδιακή ανάλυση όπως επίσης και η απλή ανάλυση όλου του βακτηριακού DNA με τη χρήση ενδονουκλεασών. Αντίθετα, πρόσφατα μια άλλη μέθοδος που επίσης χρησιμοποιεί την τεχνολογία της PCR, αλλά εφαρμόζεται κυρίως για ερευνητικούς σκοπούς, είναι η μέθοδος Multilocus sequence typing (MLST) ( Singh και συν 2006). Ε. Εκπαίδευση Η εκπαίδευση αποτελεί ένα από τα βασικά στοιχεία μιας παρέμβασης που στόχο έχει τη μείωση της επίπτωσης των πολυανθεκτικών μικροβίων. Σκοπός της εκπαίδευσης ουσιαστικά, είναι η ενθάρρυνση της αλλαγής συμπεριφοράς μέσω της κατανόησης του προβλήματος που δημιουργεί η παρουσία πολυανθεκτικών μικροβίων σε μια κλινική. Ιδιαίτερα σημαντική είναι η εκπαίδευση του προσωπικού στα θέματα υγιεινής των χεριών και του περιβάλλοντος, καθώς επίσης και στα μέτρα προφύλαξης και απομόνωσης ασθενών. Η συνεχής εκπαίδευση με επιτήρηση και ανατροφοδότηση φαίνεται να έχει πολύ καλά αποτελέσματα στη συμμόρφωση με τις κατευθυντήριες οδηγίες για τον έλεγχο των λοιμώξεων. Επίσης, η συμμετοχή ατόμων του ίδιου του προσωπικού μιας κλινικής στην εκπαίδευση των συναδέλφων βοηθάει στην καλύτερη 57
58 ευαισθητοποίηση και συνεργασία για την αντιμετώπιση της εξάπλωσης των πολυανθεκτικών μικροβίων (Siegel και συν 2007b, Kane και συν 2007, Filius και συν 2005, Shlaes και συν 1997). Να σημειωθεί ότι η συνεχής εκπαίδευση στην πρόληψη της εμφάνισης αντοχής καλό είναι να γίνεται σε όλους όσους εργάζονται στο νοσοκομείο και περιλαμβάνει, εκτός από το μόνιμο ιατρο-νοσηλευτικό προσωπικό, τους φοιτητές της ιατρικής, τους νοσηλευτές και φυσιοθεραπευτές που κάνουν πρακτική εξάσκηση, τις αποκλειστικές νοσηλεύτριες, καθαριστές, ακόμη δε και τους μάγειρες και εργάτες πλυντηρίων. 58
59 ΕΙΔΙΚΟ ΜΕΡΟΣ 59
60 8. Σκοπός της μελέτης Σκοπός της διδακτορικής αυτής διατριβής ήταν η βαθύτερη κατανόηση της σχέσης μεταξύ κατανάλωσης αντιμικροβιακών και ανάπτυξης ανθεκτικών μικροβίων, και η μελέτη επίδρασης της παρέμβασης στη μείωση της μικροβιακής αντοχής. Συγκεκριμένα διερευνήθηκαν Αναδρομικά και προοπτικά: o Η μικροβιακή αντοχή και η κατανάλωση ομάδων αντιμικροβιακών στο σύνολο ενός τριτοβάθμιου νοσοκομείου, αλλά και ειδικότερα στις κλινικές του. o Η σχέση μεταξύ μικροβιακής αντοχής και κατανάλωσης αντιμικροβιακών στο σύνολο και για κάθε ζεύγος μικροβίου/αντιμικροβιακού παράγοντα χωριστά. Προοπτικά, η παρέμβαση σε ειδικές κλινικές του Ιπποκρατείου Νοσοκομείου, και ιδίως εκεί όπου υπάρχει σοβαρό πρόβλημα αντοχής μικροβίων: o Αναγνώριση των προβλημάτων αντοχής στις κλινικές και ορισμός του θέματος της παρέμβασης στην αντιμετώπιση των λοιμώξεων από πολυανθεκτικά μικρόβια. o Ενημέρωση και εκπαίδευση για την ορθολογική χρήση των αντιμικροβιακών και τον έλεγχο της οριζόντιας μετάδοσης μικροβίων, καθώς και την πρόληψη της εμφάνισης νοσοκομειακών λοιμώξεων. o Εφαρμογή στην κλινική πράξη των οδηγιών για την ορθολογική χρήση των αντιμικροβιακών και την πρόληψη της οριζόντιας μετάδοσης μικροβίων με συνεχή παρέμβαση και ανατροφοδότηση. o Καταγραφή της μικροβιακής αντοχής πριν, κατά και μετά την παρέμβαση. 60
61 9. Μεθοδολογία 9.1. Είδος μελέτης Το πρώτο μέρος της διδακτορικής διατριβής έχει καθαρά αναδρομικό χαρακτήρα και αφορά την κατανάλωση αντιμικροβιακών και τη μικροβιακή αντοχή στις κλινικές του Νοσοκομείου για τα έτη Στην αναδρομική αυτή μελέτη έγινε συσχέτιση μεταξύ κατανάλωσης και αντοχής, χρησιμοποιώντας αθροιστικά δεδομένα, τόσο διαχρονικά (longitudinal) όσο και για ορισμένα χρονικά διαστήματα (cross sectional) μεταξύ των διαφόρων κλινικών της μελέτης. Το δεύτερο μέρος της διδακτορικής διατριβής έχει προοπτικό χαρακτήρα. Περιλαμβάνει τη συνέχιση του πρώτου μέρους της μελέτης, δηλαδή καταγραφή της αντοχής, της κατανάλωσης και της συσχέτισης μεταξύ τους τόσο στο σύνολο του νοσοκομείου όσο και σε ειδικές κλινικές για την εντόπιση του προβλήματος. Στη συνέχεια, περιλαμβάνει τη μελέτη της επίδρασης μέτρων παρέμβασης για την ορθολογική χρήση των αντιμικροβιακών και την εφαρμογή των μέτρων της πρόληψης της οριζόντιας μετάδοσης ανθεκτικών μικροβίων. Στo δεύτερο μέρος της μελέτης και στα πλαίσια της παρέμβασης σε ορισμένες κλινικές έγινε μελέτη ασθενώνμαρτύρων για την καλύτερη κατανόηση των παραγόντων κινδύνου για την εμφάνιση ανθεκτικών στελεχών (case-control study), καθώς και μελέτη έκβασης (outcome study) για την μελέτη των παραγόντων θνητότητας από πολυανθεκτικά μικρόβια Χώρος και χρόνος μελέτης Η αναδρομική και προοπτική μελέτη έγινε στο Ιπποκράτειο Νοσοκομείο Θεσσαλονίκης. Πρόκειται για ένα τριτοβάθμιο νοσοκομείο με 981 ανεπτυγμένες κλίνες. Περιλαμβάνει 7 παθολογικές κλινικές ενηλίκων, από τις οποίες οι 4 ήταν γενικές, η μία καρδιολογική, η μία νεφρολογική και η μία νευρολογική. Επίσης περιλαμάνει 11 χειρουργικές κλινικές ενηλίκων, μεταξύ των οποίων 3 γενικές, μία ορθοπεδική, μία νευροχειρουργική, μία ουρολογική, μία ωτορινολαρυγγολογική, μία οφθαλμολογική, και 3 μαυετικές/γυναικολογικές. Στο νοσοκομείο υπάρχει μία ΜΕΘ ενηλίκων, μία κλινική μεταμοσχεύσεων, 7 παιδιατρικές κλινικές. Οι παιδιατρικές κλινικές περιλαμβάνουν δύο γενικές κλινικές, δύο μονάδες εντατικής νοσηλείας νεογνών (ΜΕΝΝ), μία παιδοογκολογική, μία παιδοχειρουργική και μία ΜΕΘ παίδων. 61
62 Το χρονικό διάστημα της μελέτης περιλαμβάνει στο αναδρομικό τμήμα της τα έτη 2001 έως 2011, ενώ στο προοπτικό της τμήμα ξεκινάει από το 2008 και συνεχίζει, ανάλογα με την κλινική όπου έγινε η παρέμβαση, έως και το Μικροβιολογικά δεδομένα Η καταγραφή της αντοχής των μικροβίων που έχουν απομονωθεί στο χρονικό διάστημα της μελέτης έγινε από το μικροβιολογικό εργαστήριο του Ιπποκρατείου Νοσοκομείου Θεσσαλονίκης. Τα μικρόβια αυτά προέρχονται από καλλιέργειες αίματος, ούρων, ΕΝΥ και άλλα βιολογικά υγρά καθώς και από τραύματα. Σύμφωνα με τα πρωτόκολλα του μικροβιολογικού εργαστηρίου, μελέτη της αντοχής (αντιβιόγραμμα) γίνεται μία φορά σε κάθε επεισόδιο λοίμωξης σε έναν ασθενή -αποκλείοντας τα διπλότυπα και τις συνεχόμενες απομονώσεις του ίδιου μικροβίου σε έναν ασθενή. Η τυποποίηση και η ευαισθησία των μικροβίων γίνεται με τον αυτοματοποιημένο αναλυτή VITEK 2 (Biomerieux) (Solomon και συν 2001). Η καταγραφή της αντοχής γίνεται για κάθε μικρόβιο για το χρονικό διάστημα που απαιτείται και υπολογίζεται με τον εξής τύπο: 9.4. Κατανάλωση αντιμικροβιακών Τα δεδομένα για την κατανάλωση των αντιμικροβιακών προέρχονται από το φαρμακείο του νοσοκομείου. Τα δεδομένα αυτά ήταν ετήσιες αναφορές του φαρμακείου, σε έντυπη και στη συνέχεια και σε ηλεκτρονική μορφή, στις οποίες ήταν καταγεγραμμένα χωριστά όλα τα αντιμικροβιακά φάρμακα που χρησιμοποιήθηκαν στην κάθε κλινική του νοσοκομείου σε μηνιαία βάση. Η ποσότητα των αντιμικροβιακών αυτών στις ετήσεις αναφορές ήταν η πραγματική ποσότητα που χρησιμοποιήθηκε και όχι αυτή που ζητήθηκε από το φαρμακείο Για την ποσοτική έκφραση της κατανάλωσης των διαφορετικών ομάδων αντιμικροβιακών στο νοσοκομείο χρησιμοποιήθηκε η μεθοδολογία της συμβατικής ημερήσιας δόσης (Defined Daily Dose, DDD), όπως αυτή έχει ορισθεί πρόσφατα από τον Παγκόσμιο Οργανισμό Υγείας (World Health Organization). Σύμφωνα με τον ΠΟΥ, ως συμβατική ημερήσια δόση ορίζεται η γενικά αποδεκτή μέση ημερήσια δόση θεραπείας για ένα φάρμακο (αντιμικροβιακό), που χορηγείται για την κύρια ένδειξή του στους ενήλικες (Davey και συν 2005). 62
63 Για τον υπολογισμό της κατανάλωσης των αντιμικροβιακών σε DDD χρησιμοποιήθηκε το λογισμικό ABC calc (εικόνα 4) (Antibiotic Consumption Calculator, Microsoft Excel application, version 3.1, Copenhagen, Denmark, Statens Serum Institut, 2006). Το λογισμικό αυτό χρησιμοποιεί την ταξινόμηση των αντιμικροβιακών σύμφωνα με το σύστημα ATC (Anatomical Therapeutic Chemical) (Davey και συν 2005, Monnet 2003, Monnet 2007). Εικόνα 4: Α: ATC κωδικός, Β: Εμπορική ονομασία αντιμικροβιακού, Γ: ποσότητα σε γραμμάρια της δραστικής ουσίας που έχει ένα εμβαλάγιο (φιαλίδιο ή ένα δισκίο) του αντιμικροβιακού φαρμάκου, Δ: δραστική ουσία του αντιμικροβιακού, Ε: μοναδικός κωδικός ATC του αντιμικροβιακού, Ζ: οδός χορήγησης (παρεντερική οδός, από του στόματος), Η: συμβατική ημερήσια δόση που καθορίζεται για το κάθε αντιμικροβιακό από τον ΠΟΥ, Θ: αριθμός DDD ανά εμβαλάγιο, Ι: αριθμός φιαλιδίων ή δισκίων που καταναλώθηκαν από το κάθε αντιμικροβιακό για ένα ορισμένο χρονικό διάστημα, Κ: υπολογιζόμενη κατανάλωση του αντιμικροβιακού σε DDD, Λ: υπολογιζόμενη κατανάλωση του αντιμικροβιακού σε γραμμάρια. Αναλυτικά, για κάθε αντιμικροβιακό ή ομάδα αντιμικροβιακών υπολογίζεται αρχικά η συνολική δόση (σε γραμμάρια) που καταναλώθηκε σε μια κλινική για ένα ορισμένο χρονικό διάστημα, συνήθως έτος. Στη συνέχεια, η ποσότητα αυτή διαιρείται με τη συμβατική ημερήσια δόση που έχει ορισθεί για το κάθε αντιμικροβιακό υπό μελέτη και το αποτέλεσμα εκφράζεται σε DDD σύμφωνα με τον τύπο: 63
64 Για να γίνει στάθμιση ανάλογα με τον αριθμό των ασθενών και την πληρότητα της κλινικής στο χρόνο, χρησιμοποιείται το μέγεθος «ημέρες νοσηλείας» που υπολογίζεται από τον αριθμό των κρεβατιών μιας κλινικής, τη μέση πληρότητά τους για ένα χρονικό διάστημα - συνήθως ένα έτος, και το χρονικό αυτό διάστημα σε ημέρες, συνήθως ένα έτος. Στο τέλος, η κατανάλωση των αντιμικροβιακών για κάθε κλινική για το χρονικό διάστημα γίνεται με τη διαίρεση των DDD που υπολογίστηκαν, όπως παραπάνω, με τον αριθμό ημερών νοσηλείας και το αποτέλεσμα εκφράζεται σε DDD ανά 100 ημέρες νοσηλείας: Εκτός από τις συμβατικές ημερήσιες δόσεις (DDD) υπάρχουν και άλλα συστήματα για την καταγραφή της κατανάλωσης των αντιβιοτικών. Μεταξύ αυτών χρησιμοποιήθηκε στην παρούσα μελέτη η μεθοδολογία που στηρίζεται στον αριθμό των ημερών της θεραπείας (Days Of Therapy, DOT) και χρησιμοποιεί δεδομένα από τον κάθε ασθενή χωριστά (Giamarellou 2005, Polk και συν 2007). Συγκεκριμένα, ο υπολογισμός του μεγέθους DOT ανά 100 ημέρες νοσηλείας, για ένα αντιμικροβιακό φάρμακο, σε μια κλινική, για έναν μήνα, υπολογίζεται από τον παρακάτω τύπο: 9.5. Αναδρομική μελέτη Για τη διατμηματική ανάλυση ( ) μελετήθηκαν τα παρακάτω 5 μικρόβια: E. coli, K. pneumoniae, P. aeruginosa, A. baumannii and E. faecium. Πιο συγκεκριμένα, έγινε καταγραφή της αντοχής των 4 Gram αρνητικών μικροβίων στην ιμιπενέμη, κεφταζιδίμη, αμικασίνη, σιπροφλοξασίνη και του E. faecium στη βανκομυκίνη συνολικά για τα 4 χρόνια της μελέτης και ξεχωριστά για την κάθε κλινική. Στη ίδια μελέτη μελετήθηκε η ετήσια κατανάλωση των παρακάτω πέντε αντιμικροβιακών: κεφαλοσπορίνες 3 ης γενιάς, αμινογλυκοσίδες, φθοροκινολόνες, καρβαπενέμες και γλυκοπεπτίδια. Μελετήθηκε στη συνέχεια η συσχέτιση α) μεταξύ της κατανάλωσης των αντιμικροβιακών στις διάφορες κλινικές του νοσοκομείου, β) της αντοχής των μικροβίων μεταξύ 64
65 των κλινικών και γ) μεταξύ της κατανάλωσης αντιμικροβιακών και αντοχής διακλινικά στο νοσοκομείο. Για τη διαχρονική μελέτη έγινε συνολικά για όλο το νοσοκομείο καταγραφή της αντοχής των συχνότερων μικροβίων και της κατανάλωσης όλων των αντιμικροβιακών φαρμάκων. Στη συνέχεια η κατανάλωση αντιμικροβιακών σε ένα έτος συσχετίσθηκε με την μικροβιακή αντοχή στο επόμενο έτος. Μέσα στο χρονικό αυτό διάστημα που επιλέχθηκε είναι δυνατό να αποτυπωθεί οποιαδήποτε αλλαγή στη μικροβιακή αντοχή οφείλεται σε προηγούμενη μεταβολή στην κατανάλωση των αντιμικροβιακών Παρέμβαση Η παρέμβαση έγινε τόσο στο σύνολο του νοσοκομείου για συγκεκριμένα παθογόνα όσο και σε επιλεγμένες κλινικές (μονάδα εντατικής θεραπείας νεογνών, παίδων και ενηλίκων και παιδοογκολογική κλινική) και αφορούσε την ορθολογική χορήγηση αντιμικροβιακών και τα μέτρα ελέγχου της οριζόντιας μετάδοσης λοιμώξεων. Σε όλες τις περιπτώσεις, κατά τη διάρκεια της παρέμβασης, υπήρχε προοπτικά συνεχής έλεγχος και καταγραφή της χρήσης αντιμικροβιακών από τους κλινικούς ιατρούς και άμεση επικοινωνία και ανταλλαγή απόψεων με την ομάδα που ασχολείται με τις νοσοκομειακές λοιμώξεις, με κύριο εκπρόσωπο τον λοιμωξιολόγο. Παράλληλα, εντατικοποιήθηκε το εθνικό πρόγραμμα με στόχο τον περιορισμό των αντιμικροβιακών, που εφαρμόζεται βάσει νόμου σε όλα τα ελληνικά νοσοκομεία. Το πρόγραμμα αυτό, περιλαμβάνει τη συμπλήρωση ειδικού εντύπου για την παροχή από το φαρμακείο προωθημένων αντιμικροβιακών, το οποίο πρέπει να συνοδεύει τα συνταγολόγια προς το φαρμακείο του νοσοκομείου. Στα προωθημένα αντιμικροβιακά ανήκουν οι κεφαλοσπορίνες 3 ης γενιάς και 4 ης γενιάς, η αζτρεονάμη, οι καρβαπενέμες, οι φθοροκινολόνες, τα γλυκοπεπτίδα, η λινεζολίδη, η δαπτομυκίνη και η κινουπριστίνη/ νταλφοπριστίνη (εικόνα 5). Συμπληρωματικά, στην παραπάνω παρέμβαση συμπεριλήφθηκαν η διεξαγωγή μαθημάτων για την ορθολογική χρήση των αντιμικροβιακών, καθώς και η ενημέρωση και συνεχής σύσταση για εφαρμογή των κατευθυντήριων οδηγιών για τη διάγνωση και θεραπεία των λοιμώξεων που έχουν εκδοθεί από την Ελληνική Εταιρεία Λοιμώξεων, για τις οποίες υπάρχει διαθέσιμο και έντυπο υλικό σε όλες τις κλινικές. 65
66 Στον τομέα του ελέγχου των λοιμώξεων, έγινε αρχικά ενημέρωση και εκπαίδευση του προσωπικού για θέματα όπως είναι η υγιεινή των χεριών, οι βασικές και ειδικές προφυλάξεις με έμφαση στις προφυλάξεις επαφής, καθώς και η πρόληψη εμφάνισης λοιμώξεων. Παράλληλα, έγινε προσπάθεια καταγραφής της εφαρμογής αυτών των μέτρων. Επιπλέον, ενισχύθηκε η ομάδα των νοσηλευτών πρόληψης των λοιμώξεων με έναν ακόμη νοσηλευτή (συνολικά 3 άτομα) για την καλύτερη εφαρμογή των μέτρων. Εικόνα 5: Απεικόνιση τμήματος του ειδικού εντύπου παροχής προωθημένων αντιβιοτικών. Ιδιαίτερα για το θέμα των βασικών και ειδικών προφυλάξεων, σχεδιάστηκαν και εκτυπώθηκαν ειδικά σήματα-πινακίδες, ώστε να τοποθετούνται στον κάθε ασθενή ή θάλαμο 66
67 ασθενών, για να είναι δυνατή η συνεχής ενημέρωση και υπενθύμιση του προσωπικού για τα μέτρα που πρέπει να λαμβάνουν κάθε φορά (εικόνα 6). Εικόνα 6: Πινακίδες τοποθέτησης στους θαλάμους ασθενών για την επισήμανση των μέτρων που πρέπει να λαμβάνονται. Α: Βασικές προφυλάξεις, Β: Προφυλάξεις επαφής. Οι κύριοι δείκτες της αποτελεσματικότητας της παρέμβασης ήταν τα ποσοστά αντοχής των μικροβίων. Επιπλέον, καταγράφηκαν και μελετήθηκαν και άλλοι δείκτες όπως η κατανάλωση αντιμικροβιακών, η θνητότητα, η συχνότητα και το είδος των νοσοκομειακών λοιμώξεων, η νοσηρότητα, η μοριακή επιδημιολογία, και η διάρκεια νοσηλείας (Helfand και συν 2003). 67
68 Από το 2011 το νοσοκομείο μας συμμετείχε στο εθνικό σχέδιο δράσης «Προκρούστης». Πρόκειται για ένα σχέδιο δράσης που εκπονήθηκε από την επιχειρησιακή ομάδα του ΚΕΕΛΠΝΟ για την ανάγκη αντιμετώπισης της αυξημένης επίπτωσης λοιμώξεων από Gram αρνητικά πολυανθεκτικά παθογόνα σε χώρους παροχής υπηρεσιών υγείας. Έτσι, ενσωματτώθηκαν στους στόχους της παρέμβασής μας και οι στόχοι του σχεδίου αυτού που είναι: α) η συστηματική επιτήρηση των λοιμώξεων από τρία πολυανθεκτικά Gram αρνητικά μικρόβια (K. pneumoniae. A. baumannii, P. aeruginosa) με αντοχή στις καρβαπενέμες, μέσω της υποχρεωτικής δήλωσής τους στο ΚΕΕΛΠΝΟ, για τον υπολογισμό και τη διαχρονική παρακολούθηση της επίπτωσης των λοιμώξεων αυτών στα ελληνικά νοσοκομεία και β) η εφαρμογή μέτρων ελέγχου λοιμώξεων, με έμφαση στην τήρηση των αρχών νοσηλείας σε συνθήκες απομόνωσης (μονόκλινους θαλάμους ή συν-νοσηλεία) και στη συστηματική εφαρμογή υγιεινής των χεριών και προφυλάξεων επαφής. Να αναφερθεί ότι για τα δεδομένα του προγράμματος «Προκρούστης» ήταν απαραίτητη η ύπαρξη νοσοκομειακής λοίμωξης και όχι απλά η παρουσία του μικροβίου στους ασθενείς. Επομένως, εκτός από την απομόνωση των μικροβίων, στη δική μας καταγραφή εμφανίζονται τα αποτελέσματα σε ασθενείς με τεκμηριωμένη λοίμωξη Παρέμβαση στο σύνολο του νοσοκομείου για τις λοιμώξεις από στελέχη K. pneumoniae ανθεκτικά στις καρβαπενέμες. Για την πρόληψη της εμφάνισης λοίμωξης από στελέχη K. pneumoniae ανθεκτικών στις καρβαπενέμες, έγινε παρέμβαση τόσο για τη μείωση της οριζόντιας μετάδοσης όσο και την ορθολογική χρήση των αντιμικροβιακών. Να σημειωθεί ότι ειδικά για την παρέμβαση αυτή στο σύνολο του νοσοκομείου, η ομάδα των νοσηλευτών πρόληψης των νοσοκομειακών λοιμώξεων ενισχύθηκε με έναν ακόμη νοσηλευτή (συνολικά 3 άτομα) για την καλύτερη εφαρμογή των μέτρων. Πιο συγκεκριμένα η παρέμβαση στην πρόληψη της μετάδοσης ανθεκτικών μικροβίων μεταξύ ασθενών περιελάμβανε τα παρακάτω μέτρα: Εντοπισμό των περιστατικών με καλλιέργεια θετική για K. pneumoniae (συνεργασία μεταξύ της ομάδας των λοιμωξιολόγων, των νοσηλευτών των λοιμώξεων, των μικροβιολόγων και των θεραπόντων ιατρών). Ενημέρωση της κλινικής του ασθενούς 68
69 Απομόνωση ασθενούς ή σε αδυναμία αποκλειστικού θαλάμου, συν-νοσηλεία με άλλους ασθενείς που είχαν το ίδιο μικρόβιο. Διανομή ενημερωτικών εντύπων, με γραπτές οδηγίες και εικόνες Καθημερινή επιτήρηση των κλινικών, όπου νοσηλεύονταν ασθενείς με πολυανθεκτικό στέλεχος, σε ό,τι αφορά την υγιεινή των χεριών: o οδηγίες πλυσίματος/υγιεινής των χεριών έλεγχος της πρόσβασης σε αλκοολούχα διαλύματα έλεγχος εύκολης πρόσβασης από το προσωπικό επάρκεια αλκοολούχων διαλυμάτων (έλεγχος καταστροφής, έλεγχος ανεφοδιασμού) έλεγχος τήρησης των μέτρων o προφυλάξεις επαφής που προαναφέρθηκαν, o υγιεινή του περιβάλλοντος χώρου: έλεγχος για καθημερινή καθαριότητα σε επιφάνειες εντός του χώρου: κάγκελα κρεβατιού τραπεζάκια αντλίες φαρμάκων μόνιτορ στατό αντικείμενα και εργαλεία νοσηλείας: στηθοσκόπιο, σακχαρόμετρο, αναπνευστήρες, μηχάνημα αιμοκάθαρσης. Καταγραφή της συμμόρφωσης στις προφυλάξεις επαφής για το κάθε περιστατικό. Στη βάση δεδομένων για τους ασθενείς με λοίμωξη από στελέχη K. pneumoniae με αντοχή στις καρβαπενέμες, σε κάθε ασθενή στο τέλος της νοσηλείας καταγραφόταν η συνολική συμμόρφωση του προσωπικού στις προφυλάξεις επαφής. Η συμμόρφωση αυτή χαρακτηριζόταν με 3 κατηγορίες: άψογη, μέτρια και όχι ανάλογα με την εφαρμογή των μέτρων. o Άψογη: Ο άρρωστος σε απομόνωση και ταυτόχρονα σωστή χρήση των γαντιών και της ποδιάς ως πρόσθετων μέτρων των βασικών προφυλάξεων. o Μέτρια: Εφαρμογή των μέτρων προφυλάξεων επαφής χωρίς την δυνατότηα απομόνωσης του ασθενούς. 69
70 o Όχι: Καμία εφαρμογή των προφυλάξεων επαφής. Ενημέρωση για τις ενδονοσοκομειακές μετακινήσεις των ασθενών. Ενημέρωση του προσωπικού των εργαστηρίων (ακτινολογικό εργαστήριο, εργαστήριο πυρηνικής), του χειρουργείου και των φυσιοθεραπευτών για το πρόβλημα της επιδημίας από πολυανθεκτική K. pneumoniae, ώστε οποιαδήποτε ενασχόληση με τους αρρώστους αυτούς να προϋποθέτει την τήρηση των προφυλάξεων επαφής. Η άρση των παραπάνω μέτρων αποφασιζόταν μόνο από την επιτροπή νοσοκομειακών λοιμώξεων. Παράλληλα, γινόταν έλεγχος για την καθαριότητα και απολύμανση του χώρου μετά την απομάκρυνση του ασθενή, και σε περίπτωση μεταφοράς σε άλλο νοσοκομείο επικοινωνία και ενημέρωση με το εκεί προσωπικό. Παρουσίαση και συζήτηση της καταγραφής των περιστατικών με K. pneumoniae στις συνεδριάσεις της επιτροπής νοσοκομειακών λοιμώξεων και ενημέρωση της διοίκησης του νοσοκομείου. Σε ό,τι αφορά τα αντιμικροβιακά, ειδικά στο θέμα της K. pneumoniae, εκτός από τις γενικές αρχές ορθολογικής χρήσης αντιμικροβιακών που συζητήθηκαν προηγουμένως, γινόταν σε κάθε περιστατικό συζήτηση για την αντιμικροβιακή αγωγή του ασθενούς και αποτροπή της χρήσης, εμπειρικά και χωρίς να υπάρχει λόγος, καρβαπενεμών στην κλινική, εξαιτίας της πίεσης επιλογής και της εύκολης οριζόντιας μετάδοσης του μικροβίου. Η σύσταση ήταν η διακοπή της χορήγησης καρβαπενεμών με εξαίρεση την σπάνια περίπτωση όπου το στέλεχος είχε οριακή ευαισθησία ( 4mg/L) στις καρβαπενέμες (μεροπενέμη) οπότε και συνεχιζόταν η αγωγή με καρβαπενέμη αλλά πάντα σε συνδυασμό με άλλο in vitro δραστικό αντιμικροβιακό Παρέμβαση στη ΜΕΘ ενηλίκων Στη ΜΕΘ ενηλίκων αρχικά έγινε αναδρομική καταγραφή της μικροβιολογίας της κλινικής καθώς και της κατανάλωσης των αντιμικροβιακών για την καλύτερη κατανόηση του προβλήματος της αντοχής των μικροβίων και στην αναζήτηση του καλύτερου τρόπου παρέμβασης. Η διαπίστωση του αναδυόμενου προβλήματος της εμφάνισης λοιμώξεων (κυρίως βακτηριαιμιών) από K. pneumoniae ανθεκτική στην ιμιπενέμη μας οδήγησε στην εντατικοποίηση των μέτρων για την αντιμετώπιση του προβλήματος αυτού. 70
71 Στα πλαίσια της παρέμβασης έγιναν οι παρακάτω ενέργειες: Εντοπισμός, ενημέρωση και εφαρμογή των προφυλάξεων επαφής σε όσους ασθενείς της μονάδας είχαν θετική καλλιέργεια από K. pneumoniae Εύκολη πρόσβαση στα αλκοολούχα διαλύματα. Ορθολογική χρήση των αντιμικροβιακών. Διακοπή της χορήγησης καρβαπενεμών στους ασθενείς με πολυανθεκτικό στέλεχος K. pneumoniae. Αποφυγή χορήγησης καρβαπενεμών ως εμπειρική θεραπεία. Διερεύνηση των περιστατικών βακτηριαιμίας για 2 έτη ώστε να προσδιορισθούν οι πιθανοί παράγοντες κινδύνου, καθώς και η έκβασή τους. Συγκεκριμένα, έγινε μελέτη ασθενών-μαρτύρων (case-control). Στη μελέτη αυτή, συμπεριλήφθηκαν όλοι οι ασθενείς που νοσηλεύονταν στη ΜΕΘ και είχαν θετική αιμοκαλλιέργεια από K. pneumoniae, κατά το χρονικο διάστημα Στο πρώτο μέρος της μελέτης για την ανάδειξη των παραγόντων κινδύνου, όλοι οι ασθενείς χωρίστηκαν σε 3 ομάδες: o (α) ασθενείς με βακτηριαιμία από στέλεχος K. pneumoniae, που ήταν ευαίσθητο στις καρβαπενέμες (ομάδα ελέγχου), o (β) ασθενείς με βακτηριαιμία από K. pneumoniae με παραγωγή καρβαπενεμάσης τύπου KPC και o (γ) ασθενείς με βακτηριαιμία από K. pneumoniae με παραγωγή καρβαπενεμάσης τύπου VIM. Στην ανάλυση για τους παράγοντες κινδύνου συγκρίθηκαν οι δύο ομάδες με παραγωγή KPC ή VIM με την ομάδα ελέγχου. Για τον σκοπό αυτόν, ανασκοπήθηκαν οι ιατρικοί φάκελοι των ασθενών και καταγράφηκαν τα παρακάτω δεδομένα: δημογραφικά (ηλικία και φύλο), υποκείμενα νοσήματα (σακχαρώδης διαβήτης, καρδιαγγειακή νόσος, πνευμονοπάθεια, νεφρική νόσος, ηπατική νόσος, πρόσφατο χειρουργείο ή τραύμα, μεταμόσχευση συμπαγούς οργάνου), αγωγή πριν την εμφάνιση της βακτηριαιμίας από K. pneumoniae (αντιμικροβιακά φάρμακα, ανοσοκαταστολή) και διάρκεια παραμονής στη ΜΕΘ πριν το επεισόδιο της βακτηριαιμίας. Για τη στάθμιση της σοβαρότητας της νόσου χρησιμοποιήθηκε το Acute Physiology and Chronic Health Evaluation (APACHE) II score κατά την είσοδο στην ΜΕΘ (Vander και συν 2006). Στο 71
72 δεύτερο μέρος της μελέτης (μελέτη έκβασης) έγινε σύγκριση των ασθενών με βακτηριαιμία από K. pneumoniae που κατέληξαν και αυτών που επέζησαν. Υπολογίσθηκε η θνητότητα η αποδιδόμενη στη λοίμωξη, καθώς και η θνητότητα εντός ΜΕΘ και εντός νοσοκομείου. Aποδιδόμενος στη λοίμωξη θάνατος, ορίσθηκε ως ο θάνατος που συνέβη σε έναν ασθενή της ΜΕΘ εντός 24ώρου από την απομόνωση K. pneumoniae στην καλλιέργεια αίματος και με κλινική εικόνα συμβατή με λοίμωξη, όπως εμμένουσα λευκοκυττάρωση ή λευκοπενία, επιμονή του εμπυρέτου ή υποθερμία και/ή ανεπάρκεια πολλαπλών οργάνων, που δε βελτιώθηκε με τη χορήγηση κατάλληλης εμπειρικής αντιμικροβιακής αγωγής. Οι μεταβλητές που μελετήθηκαν ήταν, όπως και στο πρώτο μέρος της μελέτης, δημογραφικά χαρακτηριστικά και υποκείμενα νοσήματα, αλλά επιπλέον υπολογίσθηκε εκτός από το score APACHE II και το score Sequential Organ Failure Assessment (SOFA) την πρώτη ημέρα της εμφάνισης της βακτηριαιμίας (Dellit και συν 2007). Επίσης, ελέγχθηκε, εάν η παραγωγή καρβαπενεμάσης τύπου VIM ή KPC από τα στελέχη K. pneumoniae επηρέαζε τη θνητότητα. Τέλος, στη μελέτη για την έκβαση των ασθενών αυτών συμπεριλήφθηκε και η καταλληλότητα της χορηγούμενης αντιμικροβιακής αγωγής. Καταγραφή της επίπτωσης νέων περιστατικών με K. pneumoniae, καθώς και της κατανάλωσης αντιμικροβιακών. Εντατικοποίηση των μέτρων μετά το 2011 και εφαρμογή τους και σε 2 ακόμη μικρόβια (P. aeruginosa και A. baumannii, ανθεκτικά στις καρβαπενέμες). Καταγραφή της επίπτωσης 4 νοσοκομειακών λοιμώξεων (νοσοκομειακής βακτηριαιμίας, πνευμονίας, ουρολοίμωξης και χειρουργικού τραύματος) από τα μικρόβια K. pneumoniae, P. aeruginosa και A. baumannii που ήταν ανθεκτικά στις καρβαπενέμες Παρέμβαση στη ΜΕΘ παίδων Στη ΜΕΘ παίδων έγινε αρχικά αναδρομική καταγραφή λοιμώξεων από ανθεκτικά μικρόβια (2008). Το κύριο πρόβλημα στη ΜΕΘ παίδων ήταν η συχνή απομόνωση πολυανθεκτικών στελεχών A. baumannii και P. aeruginosa από τις βρογχικές εκκρίσεις. 72
73 Η παρέμβαση στη μονάδα αυτή περιέλαβε τα παρακάτω μέτρα: Ορθολογική χρήση αντιμικροβιακών, ιδίως στο θέμα της εμπειρικής αγωγής για λοιμώξεις αναπνευστικού. Έγινε ενημέρωση, συζήτηση, καθώς και μαθήματα για τη χρήση των αντιμικροβιακών στη ΜΕΘ παίδων. Ο κυριότερος όμως τρόπος παρέμβασης ήταν η καθημερινή συμμετοχή ενός μέλους της ομάδας λοιμώξεων στην επίσκεψη των ιατρών της ΜΕΘ παίδων. Με τον τρόπο αυτό γινόταν συνεχής συζήτηση με ανατροφοδότηση για τη σωστή χρήση των αντιμικροβιακών. Παρέμβαση και καταγραφή των μέτρων οριζόντιας μετάδοσης μικροβίων. Καθημερινά γινόταν άμεση ενημέρωση για τα αποτελέσματα των καλλιεργειών, τόσο των κλινικών όσο και των καλλιεργειών αποικισμού, στο προσωπικό της κλινικής. Ειδικά στο θέμα της υγιεινής των χεριών σε συνεργασία με μια νοσηλεύτρια και δύο ιατρούς, εντατικολόγο και λοιμωξιολόγο, έγινε άμεση επιτήρηση της συμμόρφωσης με τις οδηγίες για την υγιεινή των χεριών και συμπληρωνόταν ειδικό ερωτηματολόγιο (εικόνα 7). Στο ερωτηματολόγιο αυτό έγινε κατηγοριοποίηση της συμμόρφωσης στην υγιεινή των χεριών σε 4 κατηγορίες: άψογη, μέτρια, μικρή και άψογη. Οι ορισμοί που δόθηκαν στις 4 αυτές κατηγορίες στο ερωτηματολόγιο ήταν οι εξής: o Άψογη: Σωστός τρόπος και χρόνος υγιεινής των χεριών. o Μέτρια: Υγιεινή χεριών αλλά σε μικρότερο χρονικό διάστημα από το προβλεπόμενο (15 δευτερόλεπτα για αντισηπτικό). o Μικρή: Χρήση αντισηπτικού ή πλύσιμο χεριών με λάθος τρόπο ή σε πολύ σύντομο χρόνο ή μια από τις παρακάτω καταστάσεις: αμέσως πριν την επαφή με τον ασθενή χρήση τηλεφώνου/χρήση κομπιούτερ/επαφή με ρούχα, μαλλιά του εξεταστή. o Όχι: Καμία εφαρμογή υγιεινής των χεριών. Επίσης, η καταγραφή της κατανάλωσης των αντιμικροβιακών έγινε με δεδομένα σε επίπεδο ασθενούς χρησιμοποιώντας τη μεθοδολογία των DOT. Λόγω της ιδιαιτερότητας των λοιμώξεων του αναπνευστικού από πολυανθεκτικά στελέχη P. aeruginosa και A. baumannii, έγινε καταγραφή της επίπτωσης της 73
74 Εικόνα 7: Φόρμα καταγραφής της συμμόρφωσης στην υγιεινή των χεριών που χρησιμοποιήθηκε στη ΜΕΘ παίδων. εμφάνισής τους στις βρογχικές εκκρίσεις σε σχέση με την πληρότητα της κλινικής (αυξημένο φόρτο εργασίας), καθώς και με την κατανάλωση αντιμικροβιακών φαρμάκων. 74
75 Παρέμβαση στο παιδοογκολογικό τμήμα Αρχικά έγινε αναδρομική καταγραφή του προβλήματος της αντοχής, ειδικότερα στις βακτηριαιμίες που αποτελούν και το κυριότερο πρόβλημα στους ασθενείς που νοσηλεύονται σε παιδιατρικά ογκολογικά τμήματα. Το πρόβλημα στην κλινική αυτή προέκυψε με την εμφάνιση 2 περιστατικών βακτηριαιμίας από VRE. Πιο συγκεκριμένα, η παιδοογκολογική κλινική είχε 16 κλίνες, κατά το διάστημα της παρέμβασης, και υπήρχαν 7 δωμάτια (με 2 ή 3 κρεβάτια το καθένα), ένας χώρος με χρήση παιδότοπου γενικά αλλά και σχολείου για συγκεκριμένες ώρες, και μια κοινόχρηστη κουζίνα. Αμέσως πριν την εμφάνιση της επιδημίας από VRE η κλινική είχε πληρότητα 80%, η οποία τον μήνα που εμφανίστηκαν τα περιστατικά ήταν 100%. Σε ό,τι αφορά την παρέμβαση για τη μείωση των περιστατικών VRE πάρθηκαν τα παρακάτω μέτρα από την ομάδα λοιμώξεων. Έναρξη ενεργητικής επιδημιολογικής επιτήρησης για τον έλεγχο φορείας VRE σε όλα τα νοσηλευόμενα παιδιά της κλινικής για 6 μήνες. Ο έλεγχος της φορείας γινόταν σε δείγμα κοπράνων, που συλλέγονταν από όλα τα παιδιά με την είσοδό τους στην κλινική και στη συνέχεια κάθε 15 ημέρες, ανεξάρτητα του προηγούμενου αποτελέσματος. Άμεση ενημέρωση του προσωπικού της κλινικής για τα παιδιά με θετική καλλιέργεια για VRE. Εφαρμογή των προφυλάξεων επαφής στα παιδιά με λοίμωξη ή αποικισμό από VRE και γενικές προφυλάξεις στα υπόλοιπα μη αποικισμένα παιδιά. Λόγω της αδυναμίας απομόνωσης όλων των περιστατικών εφαρμόστηκε η συννοσηλεία (cohorting) των ήδη γνωστών αποικισμένων παιδιών, όταν δεν υπήρχε δυνατότητα απομόνωσης. Σχολαστική υγιεινή του περιβάλλοντος, όπως σχολιάστηκε και παραπάνω, στα πλαίσια εμφάνισης πολυανθεκτικού μικροβίου Ενημέρωση των γονιών για την εμφάνιση του συγκεκριμένου μικροβίου στην κλινική και συνεργασία μαζί τους για τη μείωση της οριζόντιας μετάδοσής του. Αναστολή της χρήσης του κοινόχρηστου χώρου (παιδότοπου/σχολείου). Καθαρισμός των παιχνιδιών και αποφυγή κοινής χρήσης. 75
76 Αναστολή των εισαγωγών νέων περιστατικών στην κλινική μετά τη δεύτερη εβδομάδα της επιδημιολογικής επιτήρησης για 2,5 μήνες Αλλαγή της αντιμικροβιακής πολιτικής της κλινικής με καθημερινή συζήτηση για την ορθολογική χρήση όλων των αντιμικροβιακών, και περιορισμό στο ελάχιστο της χρήσης των γλυκοπεπτιδίων (βανκομυκίνης και τεϊκοπλανίνης), ιδίως στις περιπτώσεις της εμπειρικής αγωγής. Ειδικά για την εμπειρική αντιμικροβιακή αγωγή σε εμπύρετη ουδετεροπενία γινόταν συζήτηση για την αναγκαιότητα, στην κάθε περίπτωση, της κάλυψης με αντιμικροβιακό με δράση έναντι των Gram θετικών, ενώ ασφαλώς λαμβανόταν υπόψη και η κατάσταση φορείας VRE στην τελική επιλογή του αντιμικροβιακού. Εντατικοποίηση της συμμόρφωσης στην υγιεινή των χεριών. Διενέργεια μελέτης ασθενών-μαρτύρων. Στη μελέτη αυτή συμπεριλήφθησαν παιδιά της παιδοογκολογικής κλινικής που είχαν ελεγχθεί για αποικισμό με VRE και είχαν νοσηλευθεί στο πρώτο τρίμηνο της επιτήρησης, πριν ανοίξει εκ νέου η κλινική. Τη μια ομάδα την αποτελούσαν παιδιά που ήταν αποικισμένα και την άλλη ομάδα παιδιά που είχαν μόνο αρνητικές καλλιέργειες κοπράνων για VRE. Επιπλέον, ανασκοπήθηκαν οι φάκελοι των ασθενών, καθώς και τα βιβλία κίνησης των νοσηλευτών. Έγινε καταγραφή των δημογραφικών στοιχείων (φύλου, ηλικίας), υποκείμενης νόσου, διάρκειας νοσηλείας, έκβασης, προηγούμενης έκθεσης σε αντιμικροβιακά [γλυκοπεπτίδια (βανκομυκίνη, τεϊκοπλανίνη), κεφαλοσπορίνες 3 ης γενιάς (κεφταζιδίμη, κεφοταξίμη, κεφτριαξόνη, κεφεπίμη), και αντιμικροβιακά με αντιαναερόβια δράση (καρβαπενέμες, μετρονιδαζόλη, κλινδαμυκίνη, συνδυασμούς β-λακταμικών αντιμικροβιακών με αναστολέα β-λακταμάσης)], καθώς και της μεταφοράς σε άλλο εργαστήριο του νοσοκομείου για τη διενέργεια εξετάσεων (πυρηνική ιατρική, αξονικός ή μαγνητικός τομογράφος). Καταγραφή της επίπτωσης και επιπολασμού της φορείας και λοίμωξης από VRE στην κλινική. Καταγραφή της κατανάλωσης των αντιμικροβιακών. Η καταγραφή έγινε έναν χρόνο πριν, έως και έναν χρόνο μετά την επιδημία. Χρησιμοποιήθηκε η μεθοδολογία των DDD, όπως περιγράφηκε παραπάνω. Καταγράφηκε η μηνιαία 76
77 κατανάλωση των γλυκοπεπτιδίων (βανκομυκίνη και τεϊκοπλανίνη), λινεζολίδης, κεφαλοσπορινών (3 ης γενιάς), καρβαπενεμών και άλλων αντιμικροβιακών με αντι-αναερόβια δράση (μετρονιδαζόλη, κλινδαμυκίνη, συνδυασμοί β- λακταμικών αντιμικροβιακών με αναστολέα β-λακταμάσης), και υπολογίσθηκε ο δείκτης DDD ανά 100 ημέρες νοσηλείας για 3 χρόνια ( ) Παρέμβαση στη ΜΕΝ νεογνών Αρχικά, αξιολογήθηκε το πρόβλημα της αντοχής στη μονάδα. Στη συνέχεια, έγινε παρέμβαση το 2008 μετά την εμφάνιση πολυανθεκτικού στελέχους VRE και στη συνέχεια το 2011 νέα παρέμβαση εξαιτίας της εμφάνισης πολυανθεκτικού στελέχους A. bauamannii. Κατά το χρονικό διάστημα εκπόνησης της παροούσας διδακτορικής διατριβής η ΜΕΝ νεογνών στο νοσοκομείο είχε τη δυνατότητα νοσηλείας 44 νεογνών, και σε ό,τι αφορά τη διαρρύθμιση του χώρου υπήρχαν 4 κύριοι θάλαμοι για τη νοσηλεία των νεογνών (θερμοκοιτίδες και κλινίδια, εικόνα 8). Εικόνα 8: Κάτοψη της ΜΕΝ νεογνών Κατά τη διάρκεια της επιδημίας με VRE η παρέμβαση περιελάμβανε: Διενέργεια ενεργητικής επιδημιολογικής επιτήρησης της φορείας του VRE. Σε κάθε νεογνό με παραμονή τουλάχιστον 5 ημερών, γινόταν κάθε εβδομάδα λήψη κοπράνων και έλεγχος για παρουσία VRE. Άμεση ενημέρωση των αποτελεσμάτων της επιτήρησης στο προσωπικό της κλινικής (προφορικά και γραπτά). Τοποθέτηση των αποικισμένων νεογνών σε προφυλάξεις επαφής Συν-νοσηλεία των αποικισμένων νεογνών, καθώς δεν υπήρχε δυνατότητα απομόνωσης του κάθε νεογνού. Για τον σκοπό αυτό, χρησιμοποιήθηκε ο θάλαμος 77
78 3 ως χώρος συγέντρωσης των αποικισμένων νεογνών, ενώ σε όσα νεογνά δεν υπήρχε αυτή η δυνατότητα, υπήρξε χωροταξικός διαχωρισμός των αποικισμένων από τα μη αποικισμένα νεογνά. Ανάρτηση σε κάθε θάλαμο της κάτοψης της κλινικής με τα νεογνά που ήταν αποικισμένα σε καθημερινή βάση, καθώς υπήρχε μεταφορά νεογνών και εισαγωγή νέων περιστατικών. Ενημέρωση και εντατικοποίηση των μέτρων αποφυγής οριζόντιας μετάδοσης μικροβίων, όπως συζητήθηκαν και προηγουμένως. Συζήτηση για την ορθολογική χρήση των αντιμικροβιακών στη μονάδα με τους νεογνολόγους. Προσοχή στη χορήγηση γλυκοπεπτιδίων, αλλά και κεφαλοσπορινών 3 ης γενιάς. Τροποποίηση της εμπειρικής αγωγής και ιδίως διακοπή της αντιμικροβιακής αγωγής όταν οι καλλιέργειες ήταν αρνητικές και υπήρχε βελτίωση της κλινικής εικόνας του νεογνού. Διενέργεια μελέτης ασθενών-μαρτύρων για εντοπισμό των πιθανών παραγόντων κινδύνου. Στη μελέτη αυτή συμπεριλήφθηκαν όλα τα νεογνά που ελέγχθηκαν για αποικισμό με VRE, και νοσηλεύθηκαν στην κλινική το πρώτο τρίμηνο της διενέργειας της επιδημιολογικής επιτήρησης. Η μια ομάδα (ασθενείς) περιελάμβανε τα νεογνά που ήταν αποικισμένα, και η άλλη (μάρτυρες) νεογνά που νοσηλεύθηκαν στο ίδιο διάστημα αλλά είχαν αρνητικές καλλιέργειες αποικισμού στα κόπρανα. Τα δεδομένα που συλλέχθηκαν αφορούσαν όλη τη διάρκεια παραμονής των νεογνών στη ΜΕΝ που δεν ήταν αποικισμένα και το διάστημα μέχρι την πρώτη θετική VRE καλλιέργεια στα αποικισμένα νεογνά. Ανασκοπήθηκαν οι ιατρικοί και νοσηλευτικοί φάκελοι των νεογνών αυτών και έγινε καταγραφή των παρακάτω παραμέτρων: ημερομηνία γέννησης, φύλο, διάρκεια κύησης, βάρος γέννησης, τόπος γέννησης, υποκείμενα νοσήματα, μηχανική υποστήριξη της αναπνοής, παρουσία κεντρικής φλεβικής γραμμής, ρινογαστρικού καθετήρα, παρεντερικής διατροφής, θέση και μεταφορά εντός της ΜΕΝΝ, λοιμώξεις, αντιμικροβιακή αγωγή και μεταφορά εκτός κλινικής αλλά εντός νοσοκομείου για τη διενέργεια εξετάσεων (π.χ. πυρηνική ιατρική, ακτινολογικό εργαστήριο, κ.λπ.). 78
79 Καταγραφή της χρήσης των αντιμικροβιακών, ένα χρόνο πριν έως και ένα χρόνο μετά την επιδημία από VRE. Καταγραφή της επίπτωσης και του επιπολασμού της φορείας ή λοίμωξης από VRE. Το δεύτερο πρόβλημα αντοχής που εμφανίστηκε στην κλινική, για το οποίο χρειάστηκε παρέμβαση, ήταν η εμφάνιση το 2011 επεισοδίων βακτηριαιμίας σε νεογνά από στελέχη A. baumannii ανθεκτικά στην ιμιπενέμη. Τα μέτρα που πάρθηκαν ήταν ίδια όπως και την προηγούμενη φορά, και αφορούσαν τα μέτρα πρόληψης της οριζόντιας μετάδοσης πολυανθεκτικών μικροβίων, καθώς και την ορθολογική χρήση των αντιμικροβιακών. Έγινε ενεργητική επιδημιολογική επιτήρηση για τον εντοπισμό των αποικισμένων νεογνών. Τα επιπλέον μέτρα που πάρθηκαν αυτήν τη φορά ήταν: Αναστολή νέων εισαγωγών στην κλινική για 2 εβδομάδες. Αναθεώρηση της προσβασιμότητας στα αλκοολούχα διαλύματα (τοποθέτηση αλκοολούχων διαλυμάτων σε κάθε θερμοκοιτίδα και σε σημείο με πολύ καλύτερη πρόσβαση στο προσωπικό) Μικροβιολογία και μοριακές τεχνικές που χρησιμοποιήθηκαν στην παρέμβαση Σε ό,τι αφορά τα στελέχη K. pneumoniae (σύνολο του νοσοκομείου και ειδικά στη ΜΕΘ) όλα τα στελέχη από το 2004 με MIC στην ιμιπενέμη > 1 mg/l από όλα τα κλινικά δείγματα (ένα για κάθε ασθενή) συλλέχθηκαν και διατηρήθηκαν στους -74 o C σε ειδικό υλικό συντήρησης (1% proteose-peptone που περιείχε 7% γλυκερόλη) για περαιτέρω ανάλυση. Η αρχική ταυτοποίηση και ο έλεγχος στα αντιμικροβιακά έγινε, όπως σε όλα τα κλινικά δείγματα που προαναφέραμε, με το αυτοματοποιημένο σύστημα VITEK2 (biomérieux, Marcy l Etoile, Γαλλία). Ο έλεγχος της ευαισθησίας στην τιγκεκυκλίνη και κολιμυκίνη έγινε χρησιμοποιώντας Etest (AB Biodisk, Solna, Σουηδία) σύμφωνα με τις οδηγίες του κατασκευαστή και τα όρια ευαισθησίας (breakpoints) που προτείνει ο οργανισμός US FDA για την τιγκεκυκλίνη (ευαισθησία, MIC 2mg/L, αντοχή, MIC 8 mg/l), και ο οργανισμός Clinical Laboratory Standards Institute (CLSI) για τα στελέχη Acinetobacter spp. για την κολιμυκίνη (ευαισθησία, MIC 2mg/L, αντοχή, MIC 4 mg/l). Όλα τα στελέχη ελέγχθηκαν φαινοτυπικά για την παραγωγή καρβαπενεμάσης τύπου VIM και KPC, με τη χρήση των ειδικών δοκιμασιών: ιμιπενέμη και EDTA [δοκιμασία συνέργειας με διπλό δίσκο (double-disk synergy test)] (Boccia και συν 2004) και ιμιπενέμη και 79
80 βορονικό οξύ [συνδυασμένη δοκιμασία με δίσκο (combined-disc test)] (Bassetti και συν 2006, Tsakris και συν 2008b), αντίστοιχα. Μετά τον καθορισμό του φαινότυπου, τα στελέχη K. pneumoniae με παραγωγή VIM και KPC ομαδοποιήθηκαν σύμφωνα με την ευαισθησία τους στα υπόλοιπα αντιμικροβιακά. Σε τυχαία (1 από 4) επιλεγμένα στελέχη (σύνολο 152) από κάθε ομάδα και από όλη την περίοδο της επιδημίας έγινε μοριακή ανάλυση με PCR για την εντόπιση γονιδίων αντοχής στα β-λακταμικά. Χρησιμοποιήθηκαν εκκινητές για τα γονίδια bla VIM, bla IMP and bla KPC (Jacobson και συν 1995, Hsueh και συν 2005). Η κλωνική σχέση μεταξύ των στελεχών έγινε με τη χρήση PCR και συγκεκριμένα με τη μέθοδο Enterobacterial Repetitive Intergenic Consensus (ERIC) PCR και χρησιμοποιώντας τους εκκινητές ERIC-2 (Versalovic και συν 1991). Σε ό,τι αφορά τους εντερόκοκκους (επιδημία στα νεογνά και στην παιδοογκολογική κλινική), η ανίχνευσή τους στα κόπρανα έγινε χρησιμοποιώντας εξειδικευμένα θρεπτικά υλικά. Συγκεκριμένα, τα δείγματα κοπράνων ενοφθαλμίζονταν σε ειδικό ζωμό (Enterococcosel broth) που ήταν εμπλουτισμένος με βανκομυκίνη (15 mg/l). Στη συνέχεια, στα πιθανά στελέχη Enterococcus γινόταν ανακαλλιέργεια σε κοινά θρεπτικά υλικά (αιματούχο άγαρ), απομόνωση του μικροβίου και στη συνέχεια έλεγχος αντοχής στη βανκομυκίνη και στην τεϊκοπλανίνη με τη μέθοδο της διάχυσης του δίσκου. Η τελική ταυτοποίηση και ο έλεγχος της ευαισθησίας στα αντιμικροβιακά γίνονταν με το αυτοματοποιημένο σύστημα Vitek 2. Η παρουσία του γονιδίου van υπεύθυνου για την αντοχή στη βανκομυκίνη πιστοποιήθηκε με τη διενέργεια PCR (Woodford και συν 1998a, Woodford και συν 1998b). Η μοριακή τυποποίηση για την ύπαρξη κλωνικής σχέσης μεταξύ των στελεχών VRE έγινε με την PFGE και τα αποτελέσματα αξιολογήθηκαν με βάση τα διεθνή δημοσιευμένα κριτήρια (Vander και συν 2006). Στην περίπτωση του πολυανθεκτικού A. baumannii (επιδημία στη ΜΕΝ νεογνών) όλα τα δείγματα αποικισμού των νεογνών (από το ορθό ή κόπρανα που λαμβάνονταν από τα νεογνά κάθε εβδομάδα) αλλά και τα δείγματα από τον έλεγχο του περιβάλλοντος, ενοφθαλμίζονταν σε ειδικό καλλιεργητικό υλικό (McConkey agar) που ήταν εμπλουτισμένο με ιμιπενέμη (1 mg/l). Μετά την επώαση, οι πιθανές αποικίες Acinetobacter spp. ελέγχονταν περαιτέρω. Η τυποποίηση και ο έλεγχος της ευαισθησίας γινόταν με το αυτοματοποιημένο σύστημα VITEK2. Για την ανίχνευση των γονιδίων αντοχής στις καρβαπενέμες και συγκεκριμένα για την ανίχνευση των καρβαπενεμασών τύπου OXA, χρησιμοποιήθηκε PCR σύμφωνα με τη 80
81 βιβλιογραφία (Woodford και συν 2006). Η PFGE χρησιμοποιήθηκε για τη μοριακή τυποποίηση και την κλωνική συσχέτιση, σύμφωνα με τη βιβλιογραφία (Tenover και συν 1995) Στατιστική Η στατιστική επεξεργασία των δεδομένων έγινε με το στατιστικό πακέτο SPSS (statistical package for social sciences, SPPS version 17 th Inc. Illinois). Η κατανάλωση των αντιμικροβιακών και η αντοχή των μικροβίων είναι ποσοτικές μεταβλητές. Μελετήθηκε η κανονικότητα των παραπάνω μεταβλητών για την περαιτέρω στατιστική επεξεργασία. Η συσχέτιση μεταξύ της κατανάλωσης και της αντοχής έγινε χρησιμοποιώντας είτε τους παραμετρικούς (Pearson correlation coefficient) είτε τους μη παραμετρικούς συντελεστές (Spearman correlation). Επίσης, για τη διαχρονική μεταβολή της κατανάλωσης και της αντοχής στην αναδρομική και προοπτική μελέτη χρησιμοποιείται ο όρος «κυλιόμενος μέσος όρος». Πρόκειται για τη βασική αρχή της μεθοδολογίας των χρονοσειρών, βάσει της οποίας όταν έχουμε ένα σύνολο τιμών μιας μεταβλητής στον χρόνο, υπολογίζουμε κάθε φορά τον μέσο όρο (συνήθως για 4-12 μήνες). Για παράδειγμα, όταν έχουμε μηνιαία καταγραφή ενός μεγέθους για αρκετά χρόνια, υπολογίζουμε το μέσο όρο των πρώτων 12 μηνών της καταγραφής. Στη συνέχεια υπολογίζουμε τον μέσο όρο από τον 2 ο μήνα έως και τον 13 ο μήνα της καταγραφής κ.ο.κ. Με τον τρόπο αυτό, εξομαλύνονται οι μικρές διακυμάνσεις στον χρόνο και είναι πιο ορατές οι διαχρονικές τάσεις (Helfand και συν 2003). Στις μελέτες ασθενών μαρτύρων, στην μονοπαραγοντική ανάλυση, χρησιμοποιήθηκαν: για τις συνεχείς ποσοτικές μεταβλητές η παραμετρική δοκιμασία Student s t test ή η μη παραμετρική δοκιμασία Mann-Whitney test, ανάλογα με την κανονικότητά τους. Για τις κατηγορικές μεταβλητές χρησιμοποιήθηκε η δοκιμασία Fisher s exact test. Για τον έλεγχο της κανονικότητας των συνεχών ποσοτικών μεταβλητών χρησιμοποιηθηκε η δοκιμασία Kolmogorov-Smirnofh. Το όριο στατιστικής σημαντικότητας ορίσθηκε στο p<0,05. 81
82 10. Αποτελέσματα Συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής: αθροιστικά δεδομένα, διατμηματική σύγκριση. Στη διατμηματική μελέτη της κατανάλωσης αντιμικροβιακών και αντοχής των μικροβίων, συμπεριλήφθησαν 14 κλινικές του νοσοκομείου. Αποκλείστηκαν από τη συγκεκριμένη μελέτη 7 κλινικές (6 χειρουργικές και 1 παθολογική κλινική), καθώς απομονώθηκαν λιγότερο από 10 στελέχη των υπό μελέτη παθογόνων. Οι κλινικές που συμπεριλήφθησαν ήταν οι παρακάτω: ΜΕΘ ενηλίκων, κλινική μεταμοσχεύσεων συμπαγών οργάνων, 6 παθολογικές κλινικές (4 γενικές παθολογικές, 1 νεφρολογική και 1 νευρολογική) και 6 χειρουργικές κλινικές (3 γενικές χειρουργικές, 1 νευροχειρουργική, 1 ουρολογική και 1 ορθοπαιδική κλινική). Να αναφερθεί στο σημείο αυτό, ότι οι παραπάνω κλινικές λειτουργούν αυτόνομα με ξεχωριστό ιατρονοσηλευτικό προσωπικό και σε διαφορετική τοποθεσία στο ίδιο νοσοκομείο. Η διατμηματική μεταφορά ασθενών είναι σπάνια και έχει υπολογισθεί περίπου σε 1-5% των εισαγωγών στις παθολογικές και 1-10% των εισαγωγών στις χειρουργικές κλινικές. Σε περίπτωση μεταφοράς ασθενών με πολυανθεκτικά μικρόβια υπάρχει ενημέρωση, ώστε να παρθούν τα σωστά μέτρα πρόληψης της οριζόντιας μετάδοσης των λοιμώξεων. Σε ό,τι αφορά την κατανάλωση των αντιμικροβιακών, δεν υπάρχει σημαντική διαφορά των πολιτικών ορθολογικής χρήσης αντιμικροβιακών μεταξύ των κλινικών του νοσοκομείου. Η κάθε κλινική έχει ασθενείς με διαφορετικά χαρακτηριστικά ανάλογα με τα επιστημονικά πεδία που εξειδικεύεται Κατανάλωση αντιμικροβιακών φαρμάκων Κατά το χρονικό διάστημα βρέθηκε ότι δεν υπήρχε στατιστικά σημαντική διαφορά στην ταξινόμηση των 14 υπό μελέτη κλινικών με βάση την ετήσια συνολική κατανάλωση αντιμικροβιακών φαρμάκων (πίνακας 12, p>0,05). Για τον λόγο αυτό, για τη σύγκριση των καταναλώσεων των αντιμικροβιακών φαρμάκων στη μελέτη αυτή, χρησιμοποιήθηκε η διάμεση τιμή της ετήσιας κατανάλωσης αντιμικροβιακών φαρμάκων. Οι διάμεσες τιμές της κατανάλωσης των 5 υπό μελέτη αντιμικροβιακών, κατά το χρονικό διάστημα της μελέτης ( ), φαίνονται στον πίνακα 13. Η ΜΕΘ ενηλίκων είχε τη μεγαλύτερη 82
83 κατανάλωση αντιμικροβιακών σε όλα τα υπό μελέτη αντιμικροβιακά εκτός από μια κατηγορία (3 ης γενιάς κεφαλοσπορίνες). Η κλινική μεταμοσχεύσεων συμπαγών οργάνων επίσης 83
84 Πίνακας 12: Ποσοστιαία ταξινόμηση (percent rank) των κλινικών του νοσοκομείου ανάλογα με την κατανάλωση των αντιμικροβιακών για κάθε έτος της μελέτης ( ). 84
85 Πίνακας 13: Διάμεση τιμή της ετήσιας κατανάλωσης αντιμικροβιακών φαρμάκων σε 14 υπό μελέτη κλινικές του νοσοκομείου κατά το χρονικό διάστημα Μονάδα μέτρησης DDD/100 ημέρες-νοσηλείας. Κλινική AMG 3GC FQL CBP GLY ΜΕΘ 58,8 34,9 24,1 27,7 18,1 ΚΛΜ 8,3 11,4 14,6 9,2 3,6 ΠΘ1 4,1 4,1 7,9 0,6 0,3 ΠΘ2 7,1 8,4 16,1 3,3 3,8 ΠΘ3 6,4 12,8 10,4 4,0 3,0 ΠΘ4 2,4 10,4 25,5 2,4 1,7 ΠΘ5 3,0 2,9 4,3 1,1 0,9 ΠΘ6 4,2 8,6 9,1 1,7 2,2 Παθολογικές Διάμεση τιμή (εύρος) 4,2 (2,4-7,1) 8,5 (2,9-12,8) 9,8 (4,3-25,5) 2,1 (0,6-4) 1,9 (0,3-3,8) ΧΚ1 4,1 9,5 10,4 3,7 0,9 ΧΚ2 2,9 1,0 3,6 1,3 1,2 ΧΚ3 5,6 7,4 7,8 1,5 2,4 ΧΚ4 21,5 39,4 3,9 6,4 5,3 ΧΚ5 26,8 1,4 4,5 2,0 3,4 ΧΚ6 20,4 2,7 4,4 0,5 0,1 Χειρουργικές Διάμεση τιμή (εύρος) 13 (2,9-26,8) 5,05 (1,0-39,4) 4,43 (3,6-10,4) 1,73 (0,5-6,4) 1,75 (0,1-5,3) Σύνολο Διάμεση τιμή (εύρος) 6 (2,4-58,8) 8,5 (1-39,4) 8,5 (3,6-25,5) 2,2 (0,5-27,7) 2,3 (0,1-8,1) ΠΘ: παθολογική, ΧΚ: χειρουργική, AMG: αμινογλυκοσίδες, 3GC: Κεφαλοσπορίνες 3 ης γενιάς, FQL: φθοροκινολόνες, CBP: Καρβαπενέμες, GLY: Γλυκοπεπτίδια 85
86 είχε υψηλή κατανάλωση στα περισσότερα αντιμικροβιακά φάρμακα. Σημαντική διαφορά στην κατανάλωση των αντιμικροβιακών δεν βρέθηκε μεταξύ των παθολογικών και χειρουργικών κλινικών. Οι αμινογλυκοσίδες και οι κεφαλοσπορίνες 3 ης γενιάς ήταν οι συχνότερα χρησιμοποιούμενες ομάδες αντιμικροβιακών στη ΜΕΘ ενηλίκων και τις χειρουργικές κλινικές. Οι φθοροκινολόνες και οι κεφαλοσπορίνες 3 ης γενιάς από την άλλη, ήταν αυτές οι κυρίαρχες ομάδες αντιμικροβιακών που χρησιμοποιήθηκαν στην κλινική μεταμοσχεύσεων συμπαγών οργάνων και στις παθολογικές κλινικές. Μεταξύ των κλινικών βρέθηκε υψηλού βαθμού συσχέτιση μεταξύ κατανάλωσης καρβαπενεμών και γλυκοπεπτιδίων (r>0,8, p<0,5). Άλλες σημαντικές συσχετίσεις βρέθηκαν μεταξύ κατανάλωσης καρβαπενεμών και κεφαλοσπορινών 3 ης γενιάς (r=0,73, p<0,5), καθώς και κατανάλωσης καρβαπενεμών και φθοροκινολονών (r=0,59, p<0,05) Μικροβιακή αντοχή Συνολικά, κατά τα χρονικό διάστημα , απομονώθηκαν στελέχη από ασθενείς στις 14 κλινικές του νοσοκομείου και από αυτά τα στελέχη ανήκαν στα 5 μικρόβια της μελέτης. Στο σύνολο, το E. coli ήταν το συχνότερο παθογόνο (1.486 στελέχη, 22%), και ακολουθούσαν η P. aeruginosa (1.331 στελέχη, 20%), A. baumannii (1.216 στελέχη, 18%), K. pneumoniae (553 στελέχη, 8%) και E. faecium (204 στελέχη, 3%). Το συχνότερο από τα μικρόβια της μελέτης ήταν το E. coli. Εξαίρεση αποτελεί η ΜΕΘ ενηλίκων και η κλινική μεταμοσχεύσεων συμπαγών οργάνων, όπου τα στελέχη A. baumannii ήταν τα συχνότερα, και άλλες 3 κλινικές (δύο χειρουργικές και μια παθολογική) όπου η P. aeruginosa είχε τη συχνότερη απομόνωση. Υψηλά ποσοστά αντοχής των στελεχών A. baumannii στην κεφταζιδίμη (πάνω από 80%) βρέθηκαν σε όλες τις κλινικές στις οποίες το A. baumannii απομονώθηκε. Αντίθετα, υψηλού βαθμού αντοχή στην ιμιπενέμη (πάνω από 50%) ανιχνεύθηκε μόνο στην ΜΕΘ ενηλίκων και σε μια παθολογική κλινική (διάγραμμα 2, σχέδιο A). Σε 4 κλινικές (ΜΕΘ ενηλίκων, κλινική μεταμοσχεύσεων συμπαγών οργάνων, μια χειρουργική και μια παθολογική κλινική) η αντοχή της P. aeruginosa στην κεφταζιδίμη, ιμιπενέμη και σιπροφλοξασίνη ήταν πάνω από 60%. Ειδικά στη ΜΕΘ ενηλίκων, 74% των στελεχών P. aeruginosa ήταν ανθεκτικά στις καρβαπενέμες (διάγραμμα 2, σχέδιο B). 86
87 Σε πάνω από τις μισές κλινικές της μελέτης, η αντοχή των στελεχών K. pneumoniae στην κεφταζιδίμη ήταν >40% (διάγραμμα 2, σχέδιο Γ). Συγκεκριμένα, στη ΜΕΘ ενηλίκων και σε μια χειρουργική κλινική, η αντοχή ήταν πάνω από 90%. Σε λίγες μόνο κλινικές βρέθηκαν υψηλά ποσοστά αντοχής στην αμικασίνη σε στελέχη K. pneumoniae. Η σιπροφλοξασίνη ήταν δραστική σε πάνω από 50% των στελεχών K. pneumoniae σε όλες τις κλινικές, συμπεριλαμβανομένης και της ΜΕΘ ενηλίκων. Στελέχη K. pneumoniae ανθεκτικά στις καρβαπενέμες βρέθηκαν σε 3 χειρουργικές κλινικές, στην κλινική μεταμοσχεύσεων συμπαγών οργάνων και στη ΜΕΘ ενηλίκων (η αντοχή κυμαινόταν από 4-8%). Σε όλες τις κλινικές, τα περισσότερα στελέχη E. coli ήταν ευαίσθητα στην αμικασίνη. Παρόλα αυτά, στελέχη ανθεκτικά στη σιπροφλοξασίνη βρέθηκαν με αυξημένη μάλιστα αντοχή (20-26%) σε 5 από τις 14 κλινικές (διάγραμμα 2, σχέδιο Δ). Αντοχή στις κεφαλοσπορίνες 3 ης γενιάς (κεφταζιδίμη) βρέθηκε σε υψηλά ποσοστά σε μια χειρουργική κλινική (29%) καθώς και στη ΜΕΘ ενηλίκων (19%). Στελέχη E. coli ανθεκτικά στην ιμιπενέμη βρέθηκαν σε δύο κλινικές (μία παθολογική και μία χειρουργική) με συχνότητα περίπου 1%. Στελέχη E. faecium ανθεκτικά στη βανκομυκίνη (vancomycin-resistant E. faecium, VRE) βρέθηκαν στη ΜΕΘ ενηλίκων, στην κλινική μεταμοσχεύσεων συμπαγών οργάνων και σε 3 χειρουργικές κλινικές με μέγιστη συχνότητα απομόνωσης στην κλινική μεταμοσχεύσεων (18,5%). Παρόλα αυτά, η αντοχή των στελεχών E. faecium στην βανκομυκίνη ήταν περισσότερο περιστασιακή και όχι σταθερό εύρημα. Σε ό,τι αφορά τις συσχετίσεις μεταξύ των αντοχών των μικροβίων της μελέτης καταγράφηκαν τα παρακάτω ευρήματα. Η αντοχή των στελεχών P. aeruginosa στην κεφταζιδίμη συσχετιζόταν με την αντοχή στην ιμιπενέμη (r=0,97, p<0,0001), στην αμικασίνη (r=0,92, p<0,0001) και στην σιπροφλοξασίνη (r=0,93, p<0,0001). Στα στελέχη K. pneumoniae βρέθηκε συσχέτιση μεταξύ της αντοχής στην κεφταζιδίμη και στην αμικασίνη (r=0,95, p<0,0001). Ενώ αντίθετα, δεν βρέθηκε συσχέτιση στα στελέχη E. coli μεταξύ της αντοχής στην αμικασίνη και της αντοχής στην κεφταζιδίμη ή σιπροφλοξασίνη. Οι συσχετίσεις αυτές απεικονίζονται στο διάγραμμα 2. 87
88 Διάγραμμα 2. Διακύμανση της αντοχής 4 παθογόνων στα τμήματα του νοσοκομείου. Α. A. baumanii, B. P. aeruginosa, Γ. K. pneumoniae, Δ. E. coli. ΚΛΜ: Κλινική μεταμοσχεύσεων, ΠΘ: Παθολογική κλινική, ΧΚ: Χειρουργική κλινική. AMK: Αμικασίνη, TAZ: Κεφταζιδίμη, CIP: Σιπροφλοξασίνη, IPM: Ιμιπενέμη. 88
89 Συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής στις κλινικές του νοσοκομείου Μεταξύ των κλινικών του νοσοκομείου, η κατανάλωση ορισμένων κατηγοριών αντιμικροβιακών φαρμάκων συσχετιζόταν με την αντοχή των μικροβίων στα ίδια ή άλλα αντιμικροβιακά φάρμακα (Πίνακας 14). Πιο συγκεκριμένα, η κατανάλωση καρβαπενεμών συσχετιζόταν με την αντοχή των στελεχών A. baumannii και P. aeruginosa στην ιμιπενέμη. Στο παρακάτω διάγραμμα (διάγραμμα 3) απεικονίζεται η διακύμανση της αντοχής των στελεχών P. aeruginosa ανθεκτικών στην ιμιπενέμη σύμφωνα με την κατανάλωση καρβαπενεμών στις διάφορες κλινικές του νοσοκομείου. Διάγραμμα 3. Σχέση μεταξύ κατανάλωσης καρβαπενεμών (log DDD/100ΗΝ) και αντοχής της P. aeruginosa στις διάφορες κλινικές του νοσοκομείου. log DDDs/100 ΗΝ: δεκαδικός λογάριθμος της κατανάλωσης εκφραζόμενης σε DDD ανά 100 ημέρες νοσηλείας. Επιπλέον, συσχέτιση βρέθηκε μεταξύ της κατανάλωσης αμινογλυκοσιδών και αντοχής των E. coli, P. aeruginosa και K. pneumoniae στην αμικασίνη. Δεν βρέθηκαν στατιστικά σημαντικές συσχετίσεις μεταξύ της κατανάλωσης γλυκοπεπτιδίων και ποσοστών εμφάνισης του εντερόκοκκου ανθεκτικού στη βανκομυκίνη. Επιπλέον, δεν βρέθηκαν συσχετίσεις μεταξύ της κατανάλωσης φθοροκινολονών ή κεφαλοσπορινών 3 ης γενιάς και αντοχής των Gram αρνητικών μικροβίων της μελέτης στη σιπροφλοξασίνη και κεφταζιδίμη, αντίστοιχα. Αξιοσημείωτο πάντως είναι το γεγονός ότι η κατανάλωση καρβαπενεμών, αμινογλυκοσιδών και γλυκοπεπτιδίων συσχετίζεται με την αντοχή των στελεχών P. aeruginosa, E. coli και A. baumannii σε διαφορετικούς αντιμικροβιακούς παράγοντες (Πίνακας 14). 89
90 Πίνακας 14. Στατιστικώς σημαντικές συσχετίσεις μεταξύ της κατανάλωσης αντιμικροβιακών και αντοχής σε διαφορετικές κλινικές του νοσοκομείου Κατανάλωση αντιμικροβιακών Ανθεκτικό μικρόβιο (συντελεστής συσχέτισης Pearson s) Καρβαπενέμες IPMRAB (0,62*) IPMRPA (0,67 ) AMKRPA (0,61*) CAZRPA (0,7 ) CIPRPA (0,6*) Αμινογλυκοσίδες AMKRPA (0,54*) AMKRKP (0,57*) AMKREC (0,67 ) CIPRPA (0,61*) Γλυκοπεπτίδια IPMRAB (0,56*) CAZRPA (0,56*) AMKREC (0,57*) IPMRPA: P. aeruginosa ανθεκτική στην ιμιπενέμη (imipenem-resistant P. aeruginosa), IPMRAB: A. baumannii ανθεκτικό στην ιμιπενέμη (imipenem-resistant A. baumannii), AMKRPA: P. aeruginosa ανθεκτική στην αμικασίνη (amikacin-resistant P. aeruginosa), CAZRPA: P. aeruginosa ανθεκτική στην κεφταζιδίμη (ceftazidime-resistant P. aeruginosa), CIPRPA: P.aeruginosa ανθεκτική στην σιπροφλοξασίνη, (ciprofloxacin-resistant P. aeruginosa), AMKRKP: K. pneumoniae ανθεκτική στην αμικασίνη (amikacin-resistant K. pneumoniae), AMKREC: E. coli ανθεκτικό στην αμικασίνη (amikacin-resistant E. coli), * p μεταξύ 0,05 και 0,01, p<0,01 Χρησιμοποιώντας τα δεδομένα από τις 7 κλινικές με τη μεγαλύτερη ή χαμηλότερη κατανάλωση αντιμικροβιακών, υπολογίσθηκε εκ νέου η συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής των μικροβίων (πίνακας 15). Συγκρίνοντας τα δεδομένα μεταξύ των δύο πινάκων γίνεται φανερό ότι ο συντελεστής συσχέτισης γινόταν μεγαλύτερος, όταν συμπεριλαμβάνονταν οι κλινικές με τη μεγαλύτερη κατανάλωση από ό,τι αν συμπεριλαμβάνονταν όλες οι κλινικές ανεξάρτητα με την κατανάλωση. Σε αντίθεση, όταν συμπεριλήφθησαν οι κλινικές με τη μικρότερη κατανάλωση αντιμικροβιακών δεν βρέθηκε στατιστικώς σημαντική συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής. 90
91 Πίνακας 15: Συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής μικροβίων, όταν συμπεριλαμβάνονται μόνο οι 7 κλινικές με τη μεγαλύτερη κατανάλωση αντιμικροβιακών Κατανάλωση αντιμικροβιακών Καρβαπεμένες IPMRAB 0,93 Αμινογλυκοσίδες AMKREC 0,81* Κεφαλοσπορίνες CAZRPA 3ης γενιάς 0,76* Γλυκοπεπτίδια CAZRAB 0,85* Ανθεκτικά μικρόβια (Spearman s correlation coefficient) IPMRPA 0,76* CAZRPA 0,93 CIPRKP CAZRKP 0,82* 0,83* AMKRPA CAZRPA IPMRPA 0,89 0,79* 0,85* CIPRPA 0,89 CAZRAB: ceftazidime resistant A. baumannii, AMKRPA: amikacin resistant P. aeruginosa, CAZRPA: ceftazidime resistant P. aeruginosa, IPMRPA: imipenem resistant P. aeruginosa, CIPRPA: ciprofloxacin resistant P. aeruginosa, IPMRAB: imipenem resistant A. baumannii, AMKREC: amikacin resistant E. coli, CIPRKP: ciprofloxacin resistant K. pneumoniae, * p μεταξύ 0,05 και 0,01, p<0, Συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής: αθροιστικά δεδομένα, διαχρονική καταγραφή Αντοχές μικροβίων Το σύνολο των υπό μελέτη μικροβίων που απομονώθηκαν στο διάστημα της μελέτης, αναγράφεται στον πίνακα 16 για τα Gram αρνητικά και στον πίνακα 17 για τα Gram θετικά. Στα διαγράμματα 4 και 5 απεικονίζεται η διαχρονική πορεία της συχνότητας απομόνωσης (στελέχη ανά 1000 ημέρες νοσηλείας) των συχνότερων Gram αρνητικών και θετικών παθογόνων, αντίστοιχα. Πίνακας 16: Αριθμός αντιπροσωπευτικών Gram αρνητικών μικροβίων που απομονώθηκαν κατά το διάστημα στο σύνολο του νοσοκομείου Μικρόβιο
92 P. aeruginosa A. baumannii K. pneumoniae E. coli P. mirabilis Διάγραμμα 4: Διαχρονική μεταβολή της απομόνωσης Gram αρνητικών μικροβίων σταθμισμένη ανά 1000 ημέρες νοσηλείας. Πίνακας 17: Αριθμός αντιπροσωπευτικών Gram θετικών μικροβίων που απομονώθηκαν κατά το διάστημα Μικρόβιο S. aureus E. faecium
93 Διάγραμμα 5: Διαχρονική μεταβολή της απομόνωσης Gram θετικών μικροβίων σταθμισμένη ανά 1000 ημέρες νοσηλείας. Η αντοχή των στελεχών P. aeruginosa στην ιμιπενέμη, κεφταζιδίμη, αμικασίνη, σιπροφλοξασίνη και κολιμυκίνη απεικονίζεται στο διάγραμμα 6. Στατιστικώς σημαντική ήταν η μείωση της αντοχής στην αμικασίνη (p=0,01). Διάγραμμα 6: Διαχρονική μεταβολή της αντοχής στελεχών P. aeruginosa σε 5 αντιμικροβιακά. Η αντοχή των στελεχών A. baumannii στην ιμιπενέμη, κεφταζιδίμη, αμικασίνη, σιπροφλοξασίνη και κολιμυκίνη απεικονίζεται στο διάγραμμα 7. Χαρακτηριστική είναι η μεγάλη αύξηση της αντοχής στην ιμιπενέμη μεταξύ 2002 και 2004 και στη συνέχεια η παραμονή σε σταθερά επίπεδα περίπου στο 80% των στελεχών (p=0,058). Αντίθετα, στατιστικώς 93
94 σημαντική υπήρξε η μείωση της αντοχής των στελεχών A. baumannii στην αμικασίνη (p<0,001). Επιπλέον, φαίνεται ότι ήδη από το 2009 εμφανίστηκαν στελέχη ανθεκτικά στην κολιμυκίνη. Διάγραμμα 7: Διαχρονική μεταβολή του ποσοστού αντοχής στελεχών A. baumannii σε 5 αντιμικροβιακά. Η αντοχή των στελεχών K. pneumoniae στην ιμιπενέμη, κεφταζιδίμη, αμικασίνη και σιπροφλοξασίνη απεικονίζονται στο διάγραμμα 8. Χαρακτηριστική είναι η σημαντική και μεγάλη σε ποσοστό αύξηση της αντοχής των στελεχών K. pneumoniae στην ιμιπενέμη (p<0,001), καθώς και στην σιπροφλοξασίνη (p<0,001). Σταθερή, με μικρές διακυμάνσεις, ήταν η αντοχή των στελεχών αυτών στην κεφταζιδίμη και αμικασίνη. 94
95 Διάγραμμα 8: Διαχρονική μεταβολή της αντοχής στελεχών K. pneumoniae σε 4 αντιμικροβιακά. Στο διάγραμμα 9 απεικονίζεται η διαχρονική μεταβολή της ευαισθησίας του E. coli στα αντιμικροβιακά φάρμακα. Με εξαίρεση την υψηλού βαθμού αντοχή στην αμοξυκιλλίνη (>50%) η αντοχή στα υπόλοιπα αντιμικροβιακά ήταν τις περισσότερες φορές μικρότερη από 20% και ιδίως στην αμικασίνη και ιμιπενέμη ουσιαστικά αμελητέα. Διάγραμμα 9: Διαχρονική μεταβολή της αντοχής στελεχών E. coli σε 4 αντιμικροβιακά. 95
96 Διαχρονικά παρατηρήθηκε αύξηση της αντοχής στον συνδυασμό αμοξυκιλλίνης με κλαβουλανικό οξύ (p=0,005), στην κεφταζιδίμη (p=0,005, πιθανός φαινότυπος με παραγωγή ESBL), και στην σιπροφλοξασίνη (p<0,001). Χωρίς ιδιαίτερη μεταβολή ήταν η αντοχή στην αμικασίνη. Η αντοχή του S. aureus στα β-λακταμικά, που ουσιαστικά χαρακτηρίζεται από την αντοχή του στην οξακιλλίνη (που χρησιμοποιείται αντί της μεθικιλλίνης in vitro), καταγράφεται στο διάγραμμα 10. Το ποσοστό του MRSA εμφάνισε στατιστικώς σημαντική μείωση στο σύνολο του νοσοκομείου (p=0,011). Τα ποσοστά αντοχής του S. aureus στην σιπροφλοξασίνη, κλινδαμυκίνη και ερυθρομυκίνη καταγράφονται στο διάγραμμα 10. Διάγραμμα 10: Διαχρονική πορεία της αντοχής του S. aureus σε 4 αντιμικροβιακά. Ειδικά, λόγω αυτής της σημαντικής μείωσης του MRSA υπολογίσθηκαν τα επιμέρους ποσοστά MRSA σε όλες τις κλινικές του νοσοκομείου για να δούμε αν αυτή η μείωση είναι καθολική ή επηρεάζεται από κάποιες κλινικές. Όπως φαίνεται από το διάγραμμα 11, το ποσοστό του MRSA μειώθηκε σημαντικά στη ΜΕΘ ενηλίκων (από 89% σε 25%, p =0,001) και στις χειρουργικές κλινικές (από 67% σε 41%, p=0,016). Στις παθολογικές κλινικές υπήρχε μια αύξηση της εμφάνισης του MRSA ως το 2005, όμως στη συνέχεια υπήρξε σημαντική μείωση (από 43% σε 34%, p=0,004). 96
97 Διάγραμμα 11: Διαχρονική μεταβολή του ποσοστού MRSA στις χειρουργικές και παθολογικές κλινικές και στη ΜΕΘ ενηλίκων. Η αντοχή των στελεχών E. faecium στα γλυκοπεπτίδια φαίνεται στο διάγραμμα 12. Όπως φαίνεται το ποσοστό του VRE ήταν αρκετά χαμηλό σε όλο το χρονικό διάστημα της μελέτης. Διάγραμμα 12: Διαχρονική μεταβολή του ποσοστού αντοχής στα γλυκοπεπτίδια των στελεχών E. faecium Κατανάλωση αντιμικροβιακών Η κατανάλωση των αντιμικροβιακών φαρμάκων εκφραζόμενη σε DDD/100 ημέρες νοσηλείας στο σύνολο του νοσοκομείου και διαχρονικά από το 2001 έως και το 2009, απεικονίζεται στο διάγραμμα
98 DDD/100BD Μέση ετήσια κατανάλωση αντιμικροβιακών Διάγραμμα 13: Διαχρονική μεταβολή της μέσης ετήσιας κατανάλωσης αντιμικροβιακών στο νοσοκομείο. 100BD: 100 bed-days (ημέρες νοσηλείας). Στατιστικά σημαντική υπήρξε η αύξηση στο σύνολο των πενικιλλινών (p=0,002) και κυρίως στον συνδυασμό των πενικιλλινών με αναστολέα (p<0,01). Συγκεκριμένα, αυξήθηκε τόσο ο συνδυασμός πενικιλλινών με αντιψευδομοναδική δράση και αναστολέα (τικαρκιλλίνη/κλαβουλανικό και πιπερακιλλίνη/ταζομπακτάμη, p=0,002) όσο και ο συνδυασμός των πενικιλλινών χωρίς αντιψευδομοναδική δράση και αναστολέα (αμοξυκιλλίνη/κλαβουλανικό και αμπικιλλίνη/σουλμπακτάμη, p<0,001). Αντίθετα, η κατανάλωση πενικιλλινών με ευρύ φάσμα δράσης, όπως είναι η αμοξυκιλλίνη και η αμπικιλλίνη, σημείωσε σημαντική ελάττωση (p=0,002). Διάγραμμα 14: Διαχρονική μεταβολή της κατανάλωσης πενικιλλινών. 100BD: bed-days (ημέρες νοσηλείας). 98
99 Η κατανάλωση των κεφαλοσπορινών εμφάνισε στο σύνολο σημαντική μείωση (p<0,001). Τη μεγαλύτερη μείωση στην κατανάλωση εμφάνισαν οι κεφαλοσπορίνες 3 ης γενιάς (p<0,001) και ακολούθησαν οι κεφαλοσπορίνες 2 ης γενιάς (p=0,012, διάγραμμα 15). Διάραμμα 15: Διαχρονική μεταβολή της κατανάλωσης κεφαλοσπορινών. 100BD: bed-days (ημέρες νοσηλείας). Η κατανάλωση καρβαπενεμών σημείωσε αντίθετα σημαντική αύξηση κατά το χρονικό διάστημα της μελέτης (p<0,001, διάγραμμα 16). Διάγραμμα 16: Διαχρονική μεταβολή της κατανάλωσης καρβαπενεμών. 100BD: bed-days (ημέρες νοσηλείας). Η διαχρονική κατανάλωση των αμινογλυκοσιδών, φθοροκινολονών και κολιμυκίνης φαίνεται στον διάγραμμα 17. Στατιστικά σημαντική αύξηση στην κατανάλωση εμφάνισαν οι 99
100 φθοροκινολόνες (p=0,002) και η κολιμυκίνη (p<0,0001). Αντίθετα, σημαντική μείωση στην κατανάλωση εμφάνισε η κατανάλωση αμινογλυκοσιδών (p=0,01, διάγραμμα 17). Διάγραμμα 17: Διαχρονική μεταβολή της κατανάλωσης φθοροκινολονών, αμινογλυκοσιδών και κολιμυκίνης. 100BD: bed-days, ημέρες νοσηλείας Οι καταναλώσεις των γλυκοπεπτιδίων, καθώς και των μακρολιδών φαίνονται στο διάγραμμα 18. Παρά τις ετήσιες διακυμάνσεις σημαντική μεταβολή δεν υπήρξε κατά τη διάρκεια της μελέτης. Διάγραμμα 18: Διαχρονική μεταβολή της κατανάλωσης γλυκοπεπτιδίων και μακρολιδών. 100BD: bed-days, ημέρες νοσηλείας 100
101 Συσχέτιση μεταξύ κατανάλωσης αντιμικροβιακών και αντοχής διαχρονικά Όπως φαίνεται στον πίνακα 18, υπήρξαν σημαντικές συσχετίσεις μεταξύ της κατανάλωσης ομάδας αντιμικροβιακών και εμφάνισης αντοχής στα διάφορα υπό μελέτη μικρόβια. Λαμβάνοντας υπόψη ότι μελετήθηκε κατά πόσο επηρεάζει η κατανάλωση της προηγούμενης χρονιάς στην εμφάνιση της αντοχής, βρέθηκε ότι η αύξηση στην κατανάλωση των καρβαπενεμών είχε στατιστικώς σημαντική επίδραση στην αυξημένη αντοχή των στελεχών A. baumannii και K. pneumoniae στην ιμιπενέμη. Αντίστοιχα, σημαντική επίδραση είχε και η μείωση της χρήσης των αμινογλυκοσιδών στα στελέχη A. baumannii και P. aeruginosa, καθώς μειώθηκε σημαντικά η αντοχή τους στην αμικασίνη. Σε ό,τι αφορά την αντοχή των στελεχών S. aureus στη μεθικιλλίνη (MRSA), φαίνεται ότι η μείωσή της σχετιζόταν σημαντικά με τη μείωση της χρήσης κεφαλοσπορινών και ιδίως κεφαλοσπορινών 3 ης γενιάς (r=0,9, p=0,01). Η αντοχή του E. faecium στα γλυκοπεπτίδια, σχετιζόταν με την κατανάλωση των κεφαλοσπορινών. Πίνακας 18: Διαχρονική συσχέτιση μεταξύ της κατανάλωσης αντιμικροβιακών ( ) και εμφάνισης αντοχής ( ) συγκεκριμένων μικροβίων στα αντίστοιχα αντιμικροβιακά Αντιμικροβιακά (μεταβολή) P. aeruginosa A. baumannii K. pneumoniae E. coli S. aureus E. faecium Πενικιλλίνες (αύξηση) ΑΜ/CL R r=0,95 Κεφαλοσπορίνες (μείωση) ΤΑΖ R r=-0,75 OXA R r=0,76 VAN R r=0,72 Καρβαπενέμες (αύξηση) IPM R r=0,7 ΙPM R r=0,89 OXA R r=-0,8 Αμινογλυκοσίδες (μείωση) ΑΜΚ R r=0,84 ΑΜΚ R r=0,78 Φθοροκινολόνες (αύξηση) CIP R r=0,82 p<0,05. R: αντοχή, ΑΜK: Αμικασίνη, ΙPM: Ιμιπενέμη, ΤΑΖ: Κεφταζιδίμη, CIP: Σιπροφλοξασίνη, ΑΜ/CL: Αμοξυκιλλίνη/κλαβουλανικό οξύ, OXA: Οξακιλλίνη, VAN: Βανκομυκίνη 101
102 Ιαν-04 Απρ-04 Ιουλ-04 Οκτ-04 Ιαν-05 Απρ-05 Ιουλ-05 Οκτ-05 Ιαν-06 Απρ-06 Ιουλ-06 Οκτ-06 Ιαν-07 Απρ-07 Ιουλ-07 Οκτ-07 Ιαν-08 Απρ-08 Ιουλ-08 Οκτ-08 Ιαν Παρέμβαση στο σύνολο του νοσοκομείου για τη K. pneumoniae Τα πρώτα στελέχη K. pneumoniae ανθεκτικά στις καρβαπενέμες εμφανίστηκαν το Τα περισσότερα από αυτά τα στελέχη εμφανίζονταν σποραδικά σε λίγες μόνο κλινικές του νοσοκομείου. Στη συνέχεια όμως, και όπως φαίνεται στο διάγραμμα 19, υπήρξε σταδιακή αύξηση των περιστατικών με ανθεκτική στις καρβαπενέμες K. pneumoniae Νέα περιστατικά με K. pneumoniae ανθεκτική στις καρβαπεμένες Διάγραμμα 19: Νέα περιστατικά απομόνωσης K. pneumoniae στο νοσοκομείο μεταξύ Ιανουαρίου 2004-Ιανουάριου Συνολικά, απομονώθηκαν κατά το χρονικό διάστημα μεταξύ Ιανουαρίου 2004 και Φεβρουαρίου 2009, 325 στελέχη K. pneumoniae ανθεκτικά στις καρβαπενέμες. Τα στελέχη αυτά προέρχονταν από καλλιέργειες αίματος (28%), ούρων (26%), βρογχικών εκκρίσεων (7%) και άλλων βιολογικών υγρών (τραύμα, απόστημα, κ.ά.). Οι κλινικές με τη συχνότερη απομόνωση της ανθεκτικής στις καρβαπενέμες K. pneumoniae ήταν η ΜΕΘ ενηλίκων και η κλινική μεταμοσχεύσεων συμπαγών οργάνων. Λιγότερο συχνή αλλά με τάση αύξησης ήταν η εμφάνισή της στις παθολογικές, χειρουργικές και παιδιατρικές κλινικές του νοσοκομείου (πίνακας 19). Η μοριακή ανάλυση (PCR) έδειξε ότι υπήρχαν δύο διαφορετικοί μηχανισμοί ανάπτυξης αντοχής στις καρβαπενέμες. Ποσοστό 65% (211 στελέχη) εμφάνιζαν αντοχή στις καρβαπενέμες με την παραγωγή μεταλο-β-λακταμάσης (Metallo-beta-lactamase, MBL και συγκεκριμένα τύπου VIM), καθώς βρέθηκαν θετικά στο γονίδιο bla VIM, ενώ το υπόλοιπο 35% (114 στελέχη) είχαν 102
103 αντοχή στις καρβαπενέμες λόγω παραγωγής μια νέας σερινο-καρβαπενεμάσης (ομάδα A κατά Ambler), της KPC, όπως πιστοποιήθηκε με παρουσία του γονιδίου bla KPC. Πίνακας 19: Εμφάνιση περιστατικών με K. pneumoniae ανθεκτική στις καρβαπενέμες ανά κλινική. Στη παρένθεση αναγράφεται για κάθε έτος η ποσοστιαία κατανομή των ανθεκτικών στελεχών ανά κλινική Έτος* ΜΕΘ ενηλίκων Κλινική μεταμοσχεύσεων Παθολογικές κλινικές Χειρουργικές κλινικές Παιδιατρικές κλινικές Σύνολο (49,1) 7 (12,7) 9 (16,4) 10 (18,4) 2 (3,6) (25,5) 23 (23,5) 21 (21,4) 26 (26,5) 3 (3,1) (30,2) 23 (19,8) 30 (29,5) 23 (19,8) 5 (4,3) 116 *Το 2009 απομονώθηκαν 44 στελέχη τους δύο πρώτους μήνες, με συχνότερη εμφάνιση τις χειρουργικές (28%) και παθολογικές κλινικές (26%) και στη συνέχεια τη ΜΕΘ ενηλίκων (24%), την κλινική μεταμοσχεύσεων (17%) και τις παιδιατρικές κλινικές (5%) Τα πρώτα στελέχη K. pneumoniae που ήταν ανθεκτικά στις καρβαπενέμες (Σεπτέμβριος 2004) έφεραν το γονίδιο αντοχής bla VIM. Τον Αύγουστο του 2007 απομονώθηκε ένα νέο στέλεχος K. pneumoniae ανθεκτικό στις καρβαπενέμες που είχε διαφορετικό φαινότυπο στο αντιβιόγραμμα και η μοριακή ανάλυση έδειξε ότι η αντοχή στις καρβαπενέμες οφειλόταν στην παρουσία του γονιδίου bla KPC. Στη συνέχεια, τα στελέχη αυτά με παραγωγή καρβαπενεμάσης τύπου KPC επικράτησαν ενώ παράλληλα μειώθηκε η απομόνωση στελεχών που είχαν φαινότυπο και γονότυπο παραγωγής VIM (διάγραμμα 20). 103
104 Διάγραμμα 20: Νέα περιστατικά με απομόνωση ανθεκτικής στις καρβαπενέμες K. pneumoniae ανάλογα με τον υποκείμενο μηχανισμό αντοχής. VIM: στελέχη με παραγωγή VIM καρβαπενεμάσης, KPC: στελέχη με παραγωγή KPC καρβαπενεμάσης Η μοριακή ανάλυση των στελεχών K. pneumoniae με ERIC PCR (σχήμα 8) έδειξε ότι υπήρχαν περισσότεροι του ενός κλώνοι τόσο στα στελέχη με παραγωγή VIM όσο και με παραγωγή KPC β-λακταμάσης. Ιδιαίτερα όμως τα στελέχη που είχαν το φαινότυπο VIM φάνηκε ότι ανήκαν σε πολλούς κλώνους (πολυκλωνική εμφάνιση). Σχήμα 8: Αποτελέσματα της ERIC PCR των στελεχών K. pneumoniae με παραγωγή VIM και KPC β-λακταμάσης. L: DNA μάρτυρας. Η ανάλυση αυτή δείχνει ότι πράγματι η οριζόντια μετάδοση του ίδιου κλώνου K. pneumoniae ήταν σημαντική για την εξάπλωση των ανθεκτικών στελεχών, αλλά υπήρξε και μετάδοση του γονιδίου αντοχής σε διαφορετικά στελέχη K. pneumoniae. 104
105 Εκτός όμως από το επιδημιολογικό ενδιαφέρον, τα στελέχη αυτά διέφεραν σημαντικά και στην αντοχή τους σε άλλες κατηγορίες αντιμικροβιακών, και τα στελέχη με παραγωγή KPC ήταν πολύ πιο ανθεκτικά και στις υπόλοιπες κατηγορίες αντιμικροβιακών (Πίνακας 20). Πίνακας 20: Ευαισθησία στελεχών K. pneumoniae με αντοχή στις καρβαπενέμες στα υπόλοιπα αντιμικροβιακά K. pneumoniae Γενταμικίνη Αμικασίνη Κολιμυκίνη Τιγκεκυκλίνξασίνξαζόλη Σιπροφλο- Κοτριμο- (Αρ. στελεχών) Παραγωγή VIM 76%* 66%* 100% 100% 3% 2%* (211) Παραγωγή KPC 85%* 11%* 98% 98% 3% 10%* (114) *p<0,05, VIM: Verona imipenemase, KPC: Klebsiella pneumoniae carbapenemase Για την καλύτερη κατανόηση της επιδημίας μελετήθηκε η κατανάλωση των αντιμικροβιακών (συγκεκριμένα καρβαπενεμών) για το ίδιο χρονικό διάστημα, και η σχέση με την εμφάνιση της K. pneumoniae ανθεκτικής στις καρβαπενέμες. Στο διάγραμμα 21 απεικονίζεται η κατανάλωση καρβαπενεμών στο νοσοκομείο (εκφραζόμενη σε DDD/100 ημέρες νοσηλείας) σε σχέση με την εμφάνιση νέων περιστατικών στα οποία απομονώθηκε K. pneumoniae ανθεκτική στις καρβαπενέμες (νέα περιστατικά/1000 ημέρες νοσηλείας). Τόσο η αύξηση της επίπτωσης της K. pneumoniae είναι στατιστικώς σημαντική (p<0,001), όσο και η αύξηση της κατανάλωσης καρβαπενεμών σε μηνιαία βάση (p=0,001). Στο σύνολο των 62 μηνών η κατανάλωση καρβαπενεμών συσχετιζόταν με την εμφάνιση ανθεκτικής στις καρβαπενέμες K. pneumoniae (r=0,3, p=0,029). Η συσχέτιση αυτή ήταν ακόμη πιο ισχυρή όταν σχετιζόταν ειδικά με την K. pneumoniae με παραγωγή VIM (r=0,4, p<0,001) και όχι με την K. pneumoniae με παραγωγή KPC. 105
106 Διάγραμμα 21: Μηνιαία κατανάλωση καρβαπενεμών και μηνιαία επίπτωση περιστατικών όπου απομονώθηκε K. pneumoniae ανθεκτική στις καρβαπενέμες. Για να εξομαλυνθούν οι μηνιαίες διακυμάνσεις χρησιμοποιήθηκε ο κυλιόμενος μέσος όρος (μέσος όρος 12 μηνών) οπότε και προέκυψε το διάγραμμα 22. Με τη νέα αυτή απεικόνιση φαίνεται ακόμη πιο έντονα η συσχέτιση μεταξύ κατανάλωσης καρβαπενεμών και εμφάνισης ανθεκτικής στις καρβαπενέμες K. pneumoniae (r=0,8, p<0,0001). Στο ίδιο διάγραμμα απεικονίζεται ξεχωριστά η επίπτωση της K. pneumoniae με παραγωγή VIM και αυτής με παραγωγή KPC. Η συσχέτιση και εδώ είναι πολύ καλύτερη μεταξύ κατανάλωσης καρβαπενεμών και K. pneumoniae με παραγωγή VIM (r=0,8, p<0,001) σε σχέση με την παραγωγή KPC (r=0,6, p<0,001). Στο σημείο αυτό να σημειωθεί ότι τα στελέχη με παραγωγή VIM είχαν πολυκλωνική εμφάνιση όπως συζητήθηκε προηγουμένως (οριζόντια μεταφορά γονιδίων), ενώ αυτά με παραγωγή KPC είχαν ολιγοκλωνική εμφάνιση (κυρίως μετάδοση από ασθενή σε ασθενή). Αναλύοντας ξεχωριστά τη κάθε μια καρβαπενέμη (ιμιπενέμη, μεροπενέμη, ερταπενέμη) προέκυψε ότι υπήρχαν διαφορετικές μεταβολές στην κατανάλωσή τους στη διάρκεια της μελέτης. Όπως φαίνεται και στο διάγραμμα 23, η αύξηση της κατανάλωσης μεροπενέμης σχετιζόταν με την εμφάνιση της K. pneumoniae ανθεκτικής στις καρβαπενέμες (r=0,42, p<0,001). Επιπλέον η κατανάλωση μεροπενέμης συσχετιζόταν με την εμφάνιση K. pneumoniae με παραγωγή VIM (r=0,42, p<0,001), αλλά και με την παραγωγή KPC (r=0,29, p=0,01). 106
107 Διάγραμμα 22: 12μηνος κυλιόμενος μέσος όρος της επίπτωσης K. pneumoniae με παραγωγή KPC, VIM και 12μηνος κυλιόμενος μέσος όρος της συνολικής κατανάλωσης καρβαπενεμών. Κάθε ένα σημείο αντιστοιχεί σε 12 μήνες (1 ο σημείο μέσος όρος από Ιανουάριο 2004 έως Δεκέμβριο 2004, 2 ο σημείο μέσος όρος από Φεβρουάριο 2004 έως και Ιανουάριος 2005 κ.ο.κ). Διάγραμμα 23: Ταυτόχρονη καταγραφή κατανάλωσης μεροπενέμης, ιμιπενέμης και ερταπενέμης σε σχέση με την εμφάνιση ανθεκτικής στις καρβαπενέμες K. pneumoniae. 107
108 Με τη χρήση της μεθοδολογίας του κυλιόμενου μέσου όρου αναδείχθηκε καλύτερα η συσχέτιση μεταξύ κατανάλωσης μεροπενέμης και εμφάνισης στελεχών με παραγωγή VIM (r=0,7, p<0,001) καθώς και στελεχών με παραγωγή KPC (r=0,6, p<0,001). Παρόμοια συσχέτιση είχε και η κατανάλωση ερταπενέμης και στελεχών με VIM (r=0,8, p<0,0001) και KPC (r=0,3, p=0,023). Ενώ η κατανάλωση ιμιπενέμης δεν είχε θετική συσχέτιση με την εμφάνιση ανθεκτικών στελεχών K. pneumoniae (διάγραμμα 24). Διάγραμμα 24: Κυλιόμενος μέσος όρος της επίπτωσης K. pneumoniae με παραγωγή KPC καρβαπενεμάσης σε σχέση με τους κυλιόμενους μέσους όρους της κατανάλωσης καρβαπενεμών, μεροπενέμης και ερταπενέμης. Επομένως η παρέμβαση για την K. pneumoniae έπρεπε να στοχεύει τόσο στα μέτρα πρόληψης της οριζόντιας μετάδοσης πολυανθεκτικών μικροβίων (αποδεδειγμένη μετάδοση από ασθενή σε ασθενή με την ύπαρξη ίδιου κλώνου σε πολλούς ασθενείς) αλλά και στην αντιμικροβιακή αγωγή που φάνηκε ότι συσχετιζόταν άμεσα (και κυρίως στην κατανάλωση μεροπενέμης). Ξεκινώντας από την εφαρμογή των μέτρων πρόληψης της οριζόντιας μετάδοσης μικροβίων, τα αποτελέσματα της καταγραφής της συμμόρφωσης στα μέτρα φαίνονται στις παρακάτω εικόνες. Στην πρώτη εικόνα παρουσιάζεται συνολικά στα 3 χρόνια της μελέτης η συμμόρφωση στα μέτρα, ενώ στην δεύτερη εικόνα παρουσιάζεται η διαχρονική πορεία της 108
109 συμμόρφωσης στα μέτρα. Φαίνεται ότι υπήρξε βελτίωση στη συμμόρφωση (μείωση του ποσοστού της ελλιπούς συμμόρφωσης). Να σημειωθεί ότι υπήρχε συνεχής ανατροφοδότηση και επίβλεψη των μέτρων πρόληψης οριζοντιας μετάδοσης μικροβίων (διάγραμματα 25α και 25β). Διάγραμμα 25α: Συμμόρφωση στις οδηγίες για την πρόληψη της μετάδοσης της πολυανθεκτικης K. pneumoniae στο σύνολο του νοσοκομείου και για τα 3 χρόνια της καταγραφής. Διάγραμμα 25β: Συμμόρφωση στις οδηγίες για την πρόληψης της μετάδοσης της πολυανθεκτικης K. pneumoniae στο σύνολο του νοσοκομείου ανά 6 μήνες. 109
110 Σε ό, τι αφορά την ορθολογική χρήση των αντιμικροβιακών, η σύσταση ήταν η διακοπή των καρβαπενεμών στους ασθενείς που είχε απομονωθεί η πολυανθεκτική K. pneumoniae. Η καταγραφή της χρήσης καρβαπενεμών από το 2009 έως και το 2011 φαίνεται στο διάγραμμα 26. Ουσιαστικά υπήρξε σημαντική μείωση της κατανάλωσης ιμιπενέμης (p<0,001) και σταδιακή αύξηση της κατανάλωσης της μεροπενέμης (p<0,001). Η συνολικη κατανάλωση καρβαπενεμών παρουσίασε αύξηση (p<0,001). Διάγραμμα 26: Κατανάλωση καρβαπενεμών και ειδικά της μεροπενέμης και ιμιπενέμης στο σύνολο του νοσοκομείου από το 2009 έως 2011 Τελικά η επίπτωση της K. pneumonaie πριν και κατά τη διάρκεια της παρέμβασης απεικονίζεται στο διάγραμμα 27. Η μηνιαία επίπτωση της απομόνωσης K. pneumoniae ανθεκτικής στις καρβαπενέμες αυξήθηκε σημαντικά (p<0,001) από το 2004 στο 2009 (διάμεση τιμή, 95 νέα περιστατικά ανά 100,000 ημέρες νοσηλείας) και στη συνέχεια παρατηρήθηκε σημαντική μείωση (p=0,025, διάμεση τιμή, 41 νέα περιστατικά ανά 100,000 ημέρες νοσηλείας κατά τους τελευταίους μήνες). Επιπλέον, από το 2009 και έπειτα που γινόταν η συστηματική καταγραφή των ασθενών με λοίμωξη από K. pneumoniae, η θνητότητα εντός νοσοκομείου ήταν 35%. 110
111 Διάγραμμα 27: Διαχρονική πορεία της επίπτωσης της απομόνωσης K. pneumoniae ανθεκτικής στις καρβαπενέμες. Καταγραφή των μέτρων παρέμβασης Στον πίνακα 21 καταγράφεται η επίπτωση συκεκριμένων νοσοκομειακών λοιμώξεων (βακτηριαιμίας, πνευμονίας, ουρολοίμωξης και λοίμωξης χειρουργικού πεδίου) από τα 3 πολυανθετικά μικρόβια (A. baumannii, P. aeruginosa και K. pneumoniae). Πίνακας 21: Καταγραφή λοιμώξεων από στελέχη A. baumannii, K. pneumoniae, P. aeruginosa ανθεκτικών στις καρβαπενέμες κατά το A. baumannii K. pneumoniae P. aeruginosa Επίπτωση Επίπτωση ανά 100 Αριθμός ανά 100 Αριθμός ημέρες ασθενών ημέρες ασθενών Επίπτωση ανά 100 ημέρες Αριθμός Ημ/νια ασθενών Ιαν ,24 4 2,24 2 1,12 Φεβ ,46 8 4,85 3 1,82 Μαρ , ,11 4 2,22 Απρ ,18 6 3,91 3 1,96 Μαϊ ,87 8 4,42 2 1,11 Ιουν , ,31 1 0,56 Ιουλ , ,61 1 0,60 Αυγ , ,99 7 4,50 Σεπ ,18 9 5,26 3 1,75 Οκτ ,73 5 2,76 2 1,10 Νοε ,75 7 3,94 3 1,69 Δεκ ,76 4 2,44 2 1,22 111
112 10.4. Παρέμβαση στη ΜΕΘ ενηλίκων Το κυριότερο πρόβλημα στη ΜΕΘ όπως φαίνεται και από τα προαναφερθέντα δεδομένα ήταν τα πολυανθεκτικά Gram-αρνητικά μικρόβια. Η αντοχή των A. baumannii και P. aeruginosa (διάγραμμα 28) στις καρβαπενέμες ήταν αρκετά συχνή, ενώ αναδυόμενο πρόβλημα ήταν η αντοχή των στελεχών K. pneumoniae στις καρβαπενέμες (όπως είδαμε και στο σύνολο του νοσοκομείου). Διάγραμμα 28: Διαχρονικές μεταβολές της αντοχής των στελεχών P. aeruginosa στη ΜΕΘ ενηλίκων. Το χαρακτηριστικό των στελεχών A. baumannii ήταν η αντοχή σε πολλά αντιμικροβιακά. Έτσι, η αντοχή ήταν >90% σε πρώτης γραμμής αντιμικροβιακά φάρμακα όπως είναι η κεφταζιδίμη, η κεφεπίμη, η ιμιπενέμη αλλά και οι συνδυασμοί τικαρκιλλίνης/κλαβουλανικού και πιπερακιλλίνης/ταζομπακτάμης. Η διαχρονική πορεία της αντοχής φαίνεται στο διάγραμμα
113 Διάγραμμα 29: Διαχρονική μεταβολή της αντοχής των στελεχών A. baumannii στη ΜΕΘ ενηλίκων. Η πορεία της αντοχής των στελεχών K. pneumoniae στη ΜΕΘ ενηλίκων φαίνεται στον πίνακα 22. Όπως καταγράφεται ήδη από το 2006 τα περισσότερα στελέχη K. pneumoniae ήταν στο σύνολό τους ανθεκτικά στις κεφαλοσπορίνες 3 ης γενιάς (αντοχή 88%, φαινότυπος συμβατός με παραγωγή ESBL). Χαρακτηριστική είναι η αύξηση της αντοχής στην ιμιπενέμη, που αποτέλεσε και σημαντικό πρόβλημα στις νοσοκομειακές λοιμώξεις όπως θα δούμε παρακάτω, αλλά και στα υπόλοιπα αντιμικροβιακά. Ενθαρρυντική φαίνεται η σταδιακή μείωση της αντοχής στη γενταμικίνη αλλά και στην αμικασίνη. Επιπλέον, ανησυχητική είναι η συνεχώς αυξανόμενη αντοχή στην κολιμυκίνη (30% στο σύνολο για το 2010) αλλά και στην τιγκεκυκλίνη, που είναι και τα μόνα in vitro δραστικά αντιμικροβιακά για τη θεραπεία της πολυανθεκτικής K. pneumoniae. 113
114 Πίνακας 22. Διαχρονική πορεία της αντοχής στελεχών K. pneumoniae στη ΜΕΘ ενηλίκων p Αντιμικροβιακά % αντοχή στο σύνολο των καλλιεργειών Αμικασίνη ,4 Τομπραμυκίνη Γενταμικίνη ,04 Κεφταζιδίμη ,8 Σιπροφλοξασίνη ,09 Ιμιπενέμη ,04 Πιπερακιλλίνη/ 1,7 Ταζομπακτάμη Κολιμυκίνη ,007 Τιγκεκυκλίνη ΔΕ ΔΕ ΔΕ 0 12 ΔΕ: Δεν ελέγχθηκε. Η πορεία του ποσοστού του MRSA από όλα τα κλινικά δείγματα φαίνεται στο διάγραμμα 30. Διάγραμμα 30: Ποσοστό MRSA στη ΜΕΘ ενηλίκων. 114
115 Στο διάγραμμα 31 καταγράφεται η κατανάλωση αντιμικροβιακών στη ΜΕΘ ενηλίκων. Διάγραμμα 31: Διαχρονική καταγραφή της κατανάλωσης αντιμικροβιακών στη ΜΕΘ ενηλίκων Συσχέτιση κατανάλωσης αντιμικροβιακών και εμφάνισης αντοχής στο σύνολο των μικροβίων. Σε ό,τι αφορά την αντοχή της P. aeruginosa στη ΜΕΘ ενηλίκων και την κατανάλωση αντιμικροβιακών, υπήρχε θετική διαχρονική συσχέτιση μεταξύ της κατανάλωσης πιπερακιλλίνης/ταζομπακτάμης και αντοχής της P. aeruginosa σε αυτό το αντιμικροβιακό (r=0,9, p=0,044). Συσχέτιση μεταξύ της εμφάνισης αντοχής σε στελέχη A. baumannii και κατανάλωσης αντιμικροβιακών δεν βρέθηκε κατά τη συγκεκριμένη χρονική διάρκεια της μελέτης στη ΜΕΘ ενηλίκων. Έχοντας υπόψη τα παραπάνω δεδομένα που αφορούν καλλιέργειες από όλα τα κλινικά δείγματα, και την πρωτοφανή αύξηση της αντοχής των στελεχών K. pneumoniae στην ιμιπενέμη, επικεντρωθήκαμε στα δεδομένα των αιμοκαλλιεργειών και κυρίως στα στελέχη K. pneumoniae. Έτσι, έγινε αρχικά καταγραφή των βακτηριαιμιών από στελέχη K. pneumoniae στη ΜΕΘ ενηλίκων με βάση την ευαισθησία τους στην ιμιπενέμη. Τα αποτελέσματα φαίνονται στο διάγραμμα
116 Διάγραμμα 32: Περιστατικά και επίπτωση βακτηριαιμίας από στελέχη K. pneumoniae στη ΜΕΘ ενηλίκων (ISKP: Κ. pneumoniae ευαίσθητη στην ιμιπενέμη, IRKP: K. pneumoniae ανθεκτική στην ιμιπενέμη). Έχοντας αυτά τα δεδομένα υπόψη έγινε καταγραφή όλων των βακτηριαιμιών από K. pneumoniae για το χρονικό διάστημα Συνολικά βρέθηκαν 59 ασθενείς (μέση ηλικία 53 έτη, εύρος έτη) με βακτηριαιμία από K. pneumoniae. Όλοι οι ασθενείς είχαν μηχανική υποστήριξη της αναπνοής, κεντρικό φλεβικό καθετήρα και ουροκαθετήρα και διάμεση τιμή APACHE II 21 (εύρος 4-37) την ημέρα της εισόδου στη ΜΕΘ ενηλίκων. Η βακτηριαιμία από K. pneumoniae εμφανίστηκε μετά από 13 ημέρες (εύρος, 5-52). Την ημέρα της εμφάνισης της λοίμωξης το SOFA score ήταν 11 (διάμεση τιμή, με εύρος 2 έως 20). Συνολικά η διάρκεια νοσηλείας στη ΜΕΘ των περιστατικών αυτών ήταν 8 έως 90 ημέρες (διάμεση τιμή 26 ημέρες). Συνολικά 22 ασθενείς είχαν στέλεχος K. pneumoniae ευαίσθητο στις καρβαπενέμες (77% ESBL) και 37 ασθενείς στέλεχος ανθεκτικό. Από τους 37 ασθενείς με ανθεκτικό στέλεχος στις καρβαπενέμες οι 18 είχαν K. pneumoniae με παραγωγή MBL (VIM τύπου) ενώ στα υπόλοιπα άτομα απομονώθηκαν στελέχη K. pneumoniae με παραγωγή KPC β-λακταμάσης. Τα περισσότερα από τα ανθεκτικά στελέχη ήταν ανθεκτικά και σε άλλα αντιμικροβιακά (φθοροκινολόνες, κοτριμοξαζόλη, αμινογλυκοσίδες). Όλα τα στελέχη ήταν ευαίσθητα στην κολιμυκίνη (MIC εύρος, 0,19-0,5 mg/l) και τιγκεκυκλίνη (MIC εύρος, 0,25-3 mg/l). 116
117 Τα δημογραφικά και κλινικά χαρακτηριστικά των ασθενών με βακτηριαιμία από K. pneumoniae φαίνονται στον πίνακα 23. Η μονοπαραγοντική ανάλυση (πίνακας 23) έδειξε ότι η εμφάνιση βακτηριαιμίας από K. pneumoniae με παραγωγή KPC συσχετιζόταν με το APACHE II (p=0,016), ενώ δεν σχετιζόταν σημαντικά με τις άλλες μεταβλητές. Στη πολυπαραγοντική ανάλυση, το APACHE II (OR, 1.13; 95% CI, 1.03 to 1.25; p=0.015) παρέμεινε ο μόνος ανεξάρτητος παράγοντας κινδύνου για βακτηριαιμία από K. pneumoniae με παραγωγή KPC. Επιπλέον μελετήθηκε και η έκβαση των ασθενών αυτών για να διαπιστωθεί κατά πόσο η αντοχή στις καρβαπενέμες επηρεάζει τη θνητότητα. Μελετήθηκε τόσο η αποδιδόμενη στη λοίμωξη θνητότητα όσο και η θνητότητα κατά την παραμονή στη ΜΕΘ ενηλίκων αλλά και στο νοσοκομείο. Η αποδιδόμενη στη λοίμωξη θνητότητα ήταν 13,6% (3/22) στην ομάδα ελέγχου, 16,6% (3/18) στην ομάδα με παραγωγή VIM και 36,8% (7/19) στην ομάδα με παραγωγή KPC. Στην μονοπαραγοντική ανάλυση το SOFA score (p=0,001) και το APACHE II (p=0,007) σχετιζόταν με αυξημένο κίνδυνο θνητότητας. Στην πολυπαραγοντική ανάλυση μόνο το SOFA ήταν ανεξάρτητος παράγοντας κινδύνου για θάνατο από τη λοίμωξη (OR: 1,3, 95% CI: 1,03-1,7, p=0,03). Η θνητότητα κατά την παραμονή στη ΜΕΘ των ασθενών αυτών ήταν 40,9% για την ομάδα ελέγχου, 44,4% για την ομάδα VIM και 68,4% για την ομάδα KPC. Ο πίνακας παρουσιάζει την μονοπαραγοντική ανάλυση με τους παράγοντες κινδύνου για θνητότητα εντός της ΜΕΘ. Η ηλικία, το APACHE II score και το SOFA score συσχετίζονταν με τη θνητότητα στη ΜΕΘ. Σε ό,τι αφορά τα υποκείμενα νοσήματα, η πρόσφατη μεταμόσχευση συμπαγούς οργάνου, η χειρουργική επέμβαση, τα πολλαπλά τραύματα, διέφεραν σημαντικά μεταξύ των ασθενών που επέζησαν και αυτών που κατέληξαν. Η πολυπαραγοντική ανάλυση έδειξε ότι η ηλικία, το SOFA score, η μεταμόσχευση συμπαγών οργάνων αλλά και η παραγωγή KPC ήταν ανεξάρτητοι παράγοντες για την κακή έκβαση (θάνατο) (πίνακας 24). 117
118 Πίνακας 23: Παράγοντες κινδύνου για την εμφάνιση βακτηριαιμίας από ανθεκτικά στις καρβαπενέμες στελέχη K. pneumoniae λόγω παραγωγής καρβαπενεμάσης τύπου VIM ή KPC. Ευαισθησία στις Αντοχή στις καρβαπενέμες καρβαπενέμες Μονοπαραγοντική ανάλυση VIM KPC VIM vs Ευαίσθητα KPC vs Ευαίσθητα N=22 N=18 N=19 OR (95% CI) p OR (95% CI) P Ηλικία (δμ, εύρος, έτη) 50,5 (15-78) 56 (17-81) 47 (25-79) 0,25 0,89 Φύλο (άρρεν) ,76 (0,18-3,2) 0,7 1,1 (0,25-4,8) 0,89 APACHE II score (δμ, εύρος) 17,5 (10-37) 20 (4-33) 26 (10-36) 0,67 0,02 Διάρκεια νοσηλείας πριν τη λοίμωξη 12 (5-52) 13 (7-36) 18 (6-29) 0,92 0,74 (δμ, εύρος, ημέρες) Υποκείμενη νόσος Μεταμόσχευση ,3 (0,3-5,6) 0,71 1,4 (0,3-5,9) 0,64 οργάνου Χειρουργείο ,04 (0,29-3,64) 0,6 0,93 (0,27-3,1) 0,57 Τραύμα ,97 (0,22-4,3) 0,64 0,19 (0,02-1,8) 0,13 Νεφρική νόσος ,28 (0,27-6) 0,53 0,84 (0,16-4,3) 0,58 Ηπατική νόσος ,56 (0,09-3,49) 0,44 0,84 (0,16-4,36) 0,58 Αναπνευστική νόσος ,25 (0,15-9,9) 0,6 0,56 (0,046-6,7 0,56 Καρδιαγγειακή νόσος ,9 (0,17-4,66) 0,6 1,2 (0,3-5,6) 0,56 Ανοσοκαταστολή ,3 (0,34-5,2) 0,47 1,2 (0,3-4,7) 0,5 Σακχαρώδης διαβήτης ,56 (0,09-3,5 0,43 0,53 (0,08-3,3) 0,4 Προηγούμενη αντιμικροβιακή αγωγή Αμινογλυκοσίδες ,7 (0,17-3,2) 0,7 2,93 (0,8-10,87) 0,1 Φθοροκινολόνες (0,3-13,5) 0,47 1,17(0,149-9,266) 0,88 Καρβαπενέμες ,8 (0,5-6,4) 0,36 1,98 (0,57-6,9) 0,28 Κεφαλοσπορίνες ,34 (0,085-1,38) 0,125 0,3 (0,08-1,28) 0,1 λακτάμη/αναστολέα β-λακτάμης ,93 (0,247-3,524) 0,9 1,01 (0,27-3,78) 0,99 118
119 K. pneumoniae Πίνακας 24: Παράγοντες κινδύνου που επηρεάζουν τη θνητότητα στη ΜΕΘ ενηλίκων σε ασθενείς με επεισόδια βακτηριαιμίας από στελέχη Θνητότητα εντός ΜΕΘ Ζώντες Θανόντες Μονοπαραγοντική ανάλυση Πολυπαραγοντική ανάλυση N=29 N=30 OR (95% CI) P OR (95% CI) P Ηλικία (δμ, εύρος, έτη) 45 (15-78) 55 (28-81) 0,035 1,1 (1,008-1,23) 0,035 Φύλο (άρρεν) ,4 (0,4-4,7) 0,76 APACHE II score (δμ, εύρος) 18 (4-33) 23 (10-37) 0,008 1,1 (0,9-1,4) 0,1 SOFA score (δμ, εύρος) 9 (2-14) 13,5 (9-20) <0,0001 2,5 (1,2-4,96) 0,01 Διάγνωση Μεταμόσχευση οργάνου (1,2-20,5) 0,03 44,5 (1,1-1,7e3) 0,042 Χειρουργείο ,8 (1,3-11,2) 0,019 2 (0,2-19) 0,5 Τραύμα 10 0 <0, Νεφρική νόσος 3 8 3,1(0,7-13,3) 0,18 Ηπατική νόσος 2 7 4,1 (0,8-21,7) 0,14 Αναπνευστική νόσος 3 2 0,6 (0,1-4) 0,67 Καρδιαγγειακή νόσος 4 7 1,9 (0,5-7,3) 0,5 Ανοσοκαταστολή ,6 (0,8-8) 0,15 Σακχαρώδης διαβήτης 2 6 3,4 (0,6-18,3) 0,25 Διάρκεια νοσηλείας πριν τη βακτηριαιμία (δμ, εύρος, ημέρες) 12 (6-52) 13,5 (5-36) 0,94 Κατάλληλη αρχική εμπειρική θεραπεία (Ναι) Ευαισθησία K, pneumoniae στις καρβαπενέμες Ευαίσθητο ,58 (0,2-1,5) 0,29 Παραγωγή VIM ,7 (0,2-2,1) 0,58 Παραγωγή KPC ,9 (0,9-9,2) 0,094 21,5 (1, ) 0,044 Θεραπεία Μόνο κολιμυκίνη ,7 (0,21-1,7) 0,43 κολιμυκίνη και γενταμικίνη 9 9 0,95 (0,3-2,8) 1 119
120 Τέλος η θνητότητα συνολικά κατά την παραμονή στο νοσοκομείο (ΜΕΘ ή και άλλη κλινική) ήταν 40,9% για την ομάδα ελέγχου, 55,5% για την ομάδα των ασθενών με K. pneumoniae με παραγωγή VIM και 78,9% για τους ασθενείς με παραγωγή KPC. Στην πολυπαραγοντική ανάλυση η ηλικία (p=0,04), το SOFA score (p=0,01), η μεταμόσχευση οργάνου (p=0,04) και η παραγωγή KPC (p=0,04) ήταν ανεξάρτητοι παράγοντες κινδύνου. Έχοντας υπόψη αυτά τα δεδομένα, από το 2009 ξεκίνησε η εντατικοποίηση των μέτρων με σκοπό τη μείωση της εμφάνισης νέων περιστατικών με πολυανθεκτική K. pneumoniae. Στο διάγραμμα 33 απεικονίζεται η πορεία της επίπτωσης της λοίμωξης από K. pneumoniae ανθεκτικής στις καρβαπενέμες στη ΜΕΘ ενηλίκων. Διαχρονικά υπήρξαν μεγάλες διακυμάνσεις, φαίνεται όμως ότι το τελευταίο χρονικό διάστημα του 2011 υπήρξε μείωση των περιστατικών. Παράλληλα καταγράφτηκε και η συμμόρφωση στα μέτρα της οριζόντιας μετάδοσης. Χρησιμοποιήθηκαν τρεις χαρακτηρισμοί: καλή, μέτρια και ελλιπής συμμόρφωση. Τέλος, καταγράφτηκε και η κατανάλωση των καρβαπενεμών στο σύνολο (μεροπενέμης, ιμιπενέμης, ερταπενέμης, δοριπενέμης) καθώς και μεμονωμένων αντιμικροβιακών όπως της μεροπενέμης και της δοριπενέμης. Όπως φαίνεται υπάρχει μια μικρή και σταθερή αύξηση τουλάχιστον τους πρώτους μήνες. 120
121 Διάγραμμα 33: Διαχρονική καταγραφή της: Α) εφαρμογής των μέτρων πρόληψης της οριζόντιας μετάδοσης ανθεκτικών μικροβίων (6μηνιαία καταγραφή) στους ασθενείς της ΜΕΘ με λοίμωξη από K. pneumoniae (108 συνολικά ασθενείς στην τριετία), (Β) επίπτωσης της λοίμωξης από K. pneumoniae ανθεκτικής στις καρβαπενέμες, και Γ) κατανάλωσης καρβαπενεμών (συνολικά) και ειδικά της μεροπενέμης και δοριπενέμης στη ΜΕΘ ενηλίκων, για το χρονικό διάστημα
122 Από το 2011 και έπειτα εκτός από την πολυανθεκτική K. pneumoniae έγινε προσπάθεια για ταυτόχρονη στόχευση στην μείωση των περιστατικών από στελέχη A. baumannii και P. aeruginosa ανθεκτικών στην καρβαπενέμη (σύμφωνα και με το πανελλήνιο πρόγραμμα δράσης για την πρόληψη της μετάδοσης πολυανθεκτικών μικροβίων, Προκρούστης πίνακας 25). Στην παρακάτω καταγραφή να σημειωθεί ότι συμπεριλαμβάνονται μόνο οι ειδικές νοσοκομειακές λοιμώξεις (που βέβαια είναι συχνές και σοβαρές) όπως είναι η βακτηριαιμία, η πνευμονία (με ή χωρίς αναπνευστήρα), η ουρολοίμωξη και η λοίμωξη του χειρουργικού πεδίου. Πίνακας 25: Καταγραφή των συγκεκριμένων νοσοκομειακών λοιμώξεων (βακτηριαιμία, πνευμονία, ουρολοίμωξη και λοιμώξεις χειρουργικού τραύματος) από 3 πολυανθεκτικά μικρόβια και συγκεκριμένα από στελέχη A. baumannii, P. aeruginosa, K. pneumoniae ανθεκτικά στις καρβαπενέμες (πρόγραμμα Προκρούστης) για το διάστημα από Ιανουάριο 2011 έως και Δεκέμβριο 2011 σε μηνιαία βάση. A. baumannii K. pneumoniae P. aeruginosa Επίπτωση Επίπτωση ανά 100 Αριθμός ανά 100 Αριθμός ημέρες ασθενών ημέρες ασθενών Επίπτωση ανά 100 ημέρες Αριθμός Ημ/νια ασθενών Ιαν ,93 3 1,45 1 0,70 Φεβ ,27 1 0,57 1 0,32 Μαρ ,96 4 1,92 2 0,92 Απρ ,62 5 2,62 2 1,37 Μαϊ ,39 2 0,96 2 0,46 Ιουν ,83 5 3,05 0 1,86 Ιουλ ,43 5 2,43 0 1,18 Αυγ ,43 8 3,81 2 1,81 Σεπ ,30 2 1,15 2 0,66 Οκτ ,04 0 0,00 0 0,00 Νοε ,54 4 2,02 2 1,02 Δεκ ,35 0 0,00 0 0,00 Λαμβάνοντας υπόψη συνολικά την επίπτωση των 4 συγκεκριμένων λοιμώξεων από τα 3 πολυανθεκτικά μικρόβια, καταγράφηκε η διαχρονική τους πορεία (διάγραμμα 34). Φαίνεται ότι το συχνότερο παθογόνο στις συγκεκριμένες περιπτώσεις είναι το A. baumannii και ακολουθεί η K. pneumoniae και η P. aeruginosa. Συνολικά καταγράφεται μια τάση μείωσης της επίπτωσης των λοιμώξεων αυτών από τα συγκεκριμένα μικρόβια (διάγραμμα 34). 122
123 Διάγραμμα 34: Μηνιαία επίπτωση και κυλιόμενος μέσος όρος νοσοκομειακών λοιμώξεων (βακτηριαιμία, πνευμονία, ουρολοίμωξη, λοίμωξη χειρουργικού τραύματος) από 3 πολυανθεκτικά μικρόβια (A. baumannii, K. pneumoniae, P. aeruginosa ανθεκτικά στις καρβαπενέμες). 123
124 10.5. Παρέμβαση στη ΜΕΘ παίδων Στη ΜΕΘ παίδων η καταγραφή για τον εντοπισμό των κύριων προβλημάτων αντοχής ξεκίνησε με τον υπολογισμό της συχνότητας των κυριότερων παθογόνων και των ποσοστών αντοχής στα συνήθη αντιμικροβιακά (πίνακας 26). Όπως φαίνεται από τον πίνακα αυτό, τα συχνότερα παθογόνα στη μονάδα είναι η P. aeruginosa και το A. baumannii. Η συχνότερη εστία απομόνωσης είναι το κατώτερο αναπνευστικό σύστημα των νοσηλευόμενων ασθενών. Επιπλέον, φαίνεται ότι τα στελέχη αυτά είχαν αυξημένη αντοχή στα περισσότερα αντιμικροβιακά. Πίνακας 26: Συχνότερα παθογόνα που απομονώθηκαν σε νοσηλευόμενους ασθενείς της ΜΕΘ παίδων το 2008 και οι αντοχές τους. A. baumannii P. aeruginosa K. pneumoniae E. coli Σύνολο καλλιεργειών Αριθμός (Ν) % απομόνωση στις καλλιέργειες αίματος 20,3 15, % απομόνωση στις καλλιέργειες βρογχικών εκκρίσεων 76,6 84,5 31,3 0 Αντοχή στα αντιμικροβιακά (βρογχικές εκκρίσεις) Αμικασίνη 23% 11% 0% - Κεφταζιδίμη 100% 54% 94% - Ιμιπενέμη 90% 54% 7% - Σιπροφλοξασίνη 93% 27% 80% - Επιπλέον, εκτός από το στιγμιότυπο της μικροβιολογίας και αντοχής το 2008, ανατρέχοντας στα προηγούμενα 3 χρόνια βρέθηκε ότι υπήρχε σταδιακή αύξηση τόσο της αντοχής των μικροβίων, φτάνοντας να έχουμε τις προαναφερθείσες αντοχές (ιδίως για A. baumannii και P. aeruginosa) όσο και της κατανάλωσης των αντιμικροβιακών που αυξήθηκε μέσα σε 3 χρόνια κατά 29% φτάνοντας τα 212 DDD/100 ημέρες-νοσηλείας ήδη από το Επομένως, ο ρόλος της παρέμβασης έπρεπε να είναι τόσο στο θέμα της οριζόντιας μετάδοσης ανθεκτικών μικροβίων όσο και στη χρήση των αντιμικροβιακών. Ήδη από το 2008 και κυρίως από το 2009 και έπειτα ξεκίνησε συστηματική προσπάθεια και προς τις δύο κατευθύνσεις. Στο θέμα του ελέγχου της μετάδοσης των μικροβίων γινόταν καθημερινά άμεση 124
125 ενημέρωση και καταγραφή των ασθενών που είχαν πολυανθεκτικά μικρόβια (κυρίως στις βρογχικές εκκρίσεις) και επιμονή στην εφαρμογή εντατικών μέτρων πρόληψης της μετάδοσής τους από ασθενή σε ασθενή. Ειδικά για την υγιεινή των χεριών υπήρξε καταγραφή της συμμόρφωσης του προσωπικού. Μάλιστα στο θέμα αυτό υπήρξε πολύ καλή ανταπόκριση από το προσωπικό της κλινικής και ταυτόχρονα καλή συμμόρφωση στο θέμα της υγιεινής των χεριών από το προσωπικό κυρίως της ΜΕΘ παίδων. Για την καλύτερη καταγραφή διακρίναμε 4 κατηγορίες συμμόρφωσης: καθόλου, μικρή, μέτρια και άψογη. Όπως φαίνεται στο διάγραμμα 35, τη χειρότερη συμμόρφωση στην υγιεινή των χεριών τόσο πριν όσο και μετά την επαφή με τον ασθενή, είχαν οι ιατροί εκτός ΜΕΘ παίδων (ιατροί άλλων ειδικοτήτων που προσήλθαν στην κλινική για εξέταση-χειρισμό στα νοσηλευόμενα παιδιά). Διάγραμμα 35: Συμμόρφωση στην υγιεινή των χεριών (άμεση παρακολούθηση) από 4 ομάδες προσωπικού (ιατροί ΜΕΘ, νοσηλευτές ΜΕΘ, φυσιοθεραπευτές, χειριστές μηχανημάτων, ιατροί εκτός ΜΕΘ) πριν και μετά την επαφή με τον ασθενή. Συνολικά όπως φαίνεται στον πίνακα 27 και ανεξάρτητα από το προσωπικό που ήρθε σε επαφή με το περιστατικό καταγράφεται η συμμόρφωση στην υγιεινή των χεριών ανάλαγα με την πράξη. 125
126 Πίνακας 27: Συμμόρφωση με την υγιεινή των χεριών ανάλογα με την πράξη. Πράξη Όχι Μικρή Μέτρια Άψογη 1) Πριν την φροντίδα 27% 19% 49% 6% 2) Μετά την ολοκλήρωση της φροντίδας 20% 25% 41% 14% 3) Μετακίνηση χεριών από μη-καθαρή σε καθαρή 29% - 57% 14% 4) Πριν την επεμβατική διαδικασία 10% 11% 67% 12% 5) Μετά την επαφή με επιφάνειες του σώματος 19% 19% 57% 4% 6) Μετά την αφαίρεση γαντιών 8% 20% 48% 24% Διαχρονικά παρατηρήθηκε αύξηση της συμμόρφωσης στην υγιεινή των χεριών. Στο διάγραμμα 36 φαίνεται η μεταβολή της συμμόρφωσης στο πρώτο βήμα που είναι η εφαρμογή της υγιεινής των χεριών πριν την επαφή με τον ασθενή. Διάγραμμα 36: Μεταβολή της συμμόρφωσης στην υγιεινή των χεριών πριν την επαφή με τον ασθενή. Ταυτόχρονα με την παρακολούθηση της συμμόρφωσης στην υγιεινή των χεριών γινόταν καθημερινή συζήτηση για τα περιστατικά που προβλημάτιζαν από λοιμωξιολογική άποψη. Για την καλύτερη καταγραφή της κατανάλωσης των αντιμικροβιακών χρησιμοποιήθηκε ο δείκτης ημέρες θεραπείας (Days of therapy, DOT). Με τα δεδομένα αυτά γίνονταν συνεχείς συζητήσεις για τη βελτίωση της χορήγησης αντιμικροβιακών κυρίως στο θέμα της διάρκειας της θεραπείας ή στην αποκλιμάκωση όταν ήταν γνωστό το παθογόνο και η ευαισθησία του στα 126
127 αντιμικροβιακά. Στο διάγραμμα 37 αποτυπώνεται η κατανάλωση των αντιμικροβιακών για το χρονικό διάστημα Στο διάστημα αυτό προσκομίσθηκαν 403 παιδιά στη ΜΕΘ παίδων. Ο μέσος μηνιαίος δείκτης της κατανάλωσης αντιμικροβιακών ήταν 225 DOTs/100 ημέρες νοσηλείας (εύρος από 138 έως 336 DOTs/100 ημέρες). Οι δείκτες αυτοί φανερώνουν ότι ουσιαστικά κατά μέσο όρο κάθε παιδί στην ΜΕΘ παίδων λαμβάνει 2-3 αντιμικροβιακά φάρμακα κατά την νοσηλεία του. Σε ό,τι αφορά το είδος των νοσηλευόμενων ασθενών, πάνω από 90% είναι διασωληνομένοι και έχουν κεντρικούς φλεβικούς καθετήρες. Διάγραμμα 37: Ετήσια και συνολική κατανάλωση αντιμικροβιακών ανάλογα με την κατηγορία. Οι αμινογλυκοσίδες ήταν το πιο συχνά χρησιμοποιούμενο αντιμικροβιακό φάρμακο στην ΜΕΘ παίδων. Μεταξύ των αμινογλυκοσιδών η αμικασίνη είχε τη μεγαλύτερη χρήση. Με την παρουσίαση αυτών των δεδομένων στους ιατρούς της ΜΕΘ παίδων και τη συνεχή ανατροφοδότηση στο θέμα της ορθολογικής αντιμικροβιακής αγωγής, υπήρξε σταδιακή αλλά σημαντική μείωση στην κατανάλωση των αμινογλυκοσιδών (πίνακας 28). Μετά την κατανάλωση των αμινογλυκοσιδών ακολουθούσε η κατανάλωση των κεφαλοσπορινών και των γλυκοπεπτιδίων χωρίς όμως να καταγράφονται σημαντικές διακυμάνσεις της κατανάλωσής τους στη διάρκεια του χρόνου. Να σημειωθεί στο σημείο αυτό ότι ποτέ δεν υπήρξε επιδημία από VRE στη συγκεκριμένη κλινική παρά το γεγονός ότι νοσηλεύθηκαν ασθενείς (λίγοι σε αριθμό) με γνωστό αποικισμό με VRE. 127
128 Πίνακας 28: Μηνιαία καταγραφή της κατανάλωσης αντιμικροβιακών φαρμάκων και διαχρονική τάση. ΜΜR: median monthly rate: διάμεση τιμή μηνιαίας κατανάλωσης εκφραζόμενη σε DOT/100 ημέρες νοσηλείας, ΜΣ: μη σημαντικό. Κατανάλωση αντιμικροβιακών MMR Διαχρονική τάση P Σύνολο 255 Σταθερή ΜΣ Αμινογλυκοσίδες 64 Μείωση 0,002 Αμικασίνη 52 Μείωση <0,0001 Γενταμικίνη 9 Σταθερή ΜΣ Καρβαπενέμες 23 Σταθερή ΜΣ Μεροπενέμη 22 Σταθερή ΜΣ Γλυκοπεπτίδια 32 Σταθερή ΜΣ Βανκομυκίνη 14 Σταθερή ΜΣ Τεϊκοπλανίνη 16 Σταθερή ΜΣ Κεφαλοσπορίνες 40 Σταθερή ΜΣ Κεφεπίμη 1 Αύξηση 0,005 Κεφουροξίμη 8 Μείωση 0,046 Πενικιλλίνες 15 Σταθερή ΜΣ Πιπερακιλλίνη/ 15 Σταθερή ΜΣ Ταζομπακτάμη Πολυμυξίνες 15 Σταθερή ΜΣ Κολιμυκίνη 15 Σταθερή ΜΣ Λινκοζαμίδες 12 Μείωση 0,014 Κλινδαμυκίνη 12 Μείωση 0,014 Μετρονιδαζόλη 12 Σταθερή ΜΣ Κοτριμοξαζόλη 5 Σταθερή ΜΣ Μακρολιδες 6 Σταθερή ΜΣ Κλαριθρομυκίνη 6 Σταθερή ΜΣ Μεταξύ των β-λακταμικών αντιμικροβιακών, η μεροπενέμη (η πιο συχνά χρησιμοποιούμενη καρβαπενέμη), η κεφτριαξόνη και ο συνδυασμός πιπερακιλλίνης/ταζομπακτάμης (ο μόνος συνδυασμός πενικιλλινών με αναστολέα που χρησιμοποιήθηκε) ήταν τα πιο συχνά αντιμικροβιακά της κατηγορίας αυτής. Επιπλέον, και η κεφουροξίμη (η μόνη κεφαλοσπορίνη 2 ης γενιάς) είχε σημαντικά αυξημένη κατανάλωση κατά τη διάρκεια της καταγραφής (διάγραμμα 38). 128
129 Διάγραμμα 38: Ποσοστιαία κατανάλωση β-λακταμικών αντιμικροβιακών ανά μήνα στη ΜΕΘ παίδων Η χρήση της κολιμυκίνης ήταν αρκετά συχνή (πάντοτε όμως με την καθοδήγηση των λοιμωξιολόγων), ώστε να είναι το 5 ο πιο συχνό αντιμικροβιακό. Ο λόγος της χρήσης της ήταν σε ειδικές περιπτώσεις πολυανθεκτικών μικροβίων (A. baumanni, P. aeruginosa) και πάντοτε ως στοχευμένη αγωγή (όχι εμπειρική ή προφυλακτική). Μάλιστα για την βελτίωση της φαρμακοκινητικής και φαρμακοδυναμικής της κολιμυκίνης στα παιδιά που νοσηλεύονταν στην ΜΕΘ έγινε μικρής κλίμακας μελέτη φαρμακοκινητικής και τα αποτελέσματα χρησιμοποιήθηκαν για την ορθολογική χρήση του αντιμικροβιακού αυτού στους επόμενους ασθενείς (Antachopoulos και συν 2010). Διαχρονικά πάντως φαίνεται να υπάρχει σημαντική μείωση στην κατανάλωση της κολιμυκίνης και αυτό είναι ενθαρρυντικό (p<0,001). Στο διάγραμμα 39 απεικονίζεται η διαχρονική μεταβολή της κατανάλωσης της κολιμυκίνης, των β-λακταμικών αντιμικροβιακών και των αμινογλυκοσιδών. 129
130 Διάγραμμα 39: Διαχρονική μεταβολή της μηνιαίας κατανάλωσης κολιμυκίνης, β-λακταμικών αντιμικροβιακών και αμινογλυκοσιδών. Η χρήση των άλλων αντιμικροβιακών μεταξύ των οποίων της κλινδαμυκίνης, της μετρονιδαζόλης, της κοτριμοξαζόλης, και της κλαριθρομυκίνης δεν ήταν πολύ συχνή. Η χρήση της λινεζολίδης και της σιπροφλοξασίνης (η μόνη φθοροκινολόνη) δεν ήταν συστηματική. Παρόλα αυτά η χρήση της λινεζολίδης διαχρονικά εμφάνισε σημαντική αύξηση (p=0,002). Στη συνέχεια, ξεκινώνοντας με το συχνότερο μικρόβιο που ήταν η P. aeruginosa καταγράφεται η πορεία της αντοχής στα αντιμικροβιακά φάρμακα αλλά και η σχέση της απομόνωσής της στις βρογχικές εκκρίσεις, με την πληρότητα της κλινικής και τη χρήση των αντιμικροβιακών (διάγραμμα 40 και 41). Διάγραμμα 40: Μεταβολή της αντοχής των στελεχών P. aeruginosa που απομονώθηκαν στις βρογχικές εκκρίσεις σε σχέση με τις παρεμβάσεις. Χρησιμοποιώντας τη μεθοδολογία των κυλιόμενων μέσων όρων βρέθηκε ότι η επίπτωση της απομόνωσης της ανθεκτικής P. aeruginosa από τις βρογχικές εκκρίσεις στα διασωληνομένα παιδιά στη ΜΕΘ παίδων συσχετίζεται άμεσα με τον επιπολασμό της απομόνωσης P. aeruginosa στις βρογχικές εκκρίσεις (r=0,9, p<0,001), την πληρότητα της κλινικής (r=0,6, p<0,001) και αντιστρόφως ανάλογα με την κατανάλωση των αντιμικροβιακών (r=0,5, p=0,001). 130
131 Διάγραμμα 41: Διαχρονική καταγραφή της απομόνωσης στελεχών P. aeruginosa από τις βρογχικές εκκρίσεις (επίπτωση και επιπολασμός) σε σχέση με το δείκτη πληρότητας της κλινικής και την συνολική κατανάλωση αντιμικροβιακών. Ο επιπολασμός, η επίπτωση και ο δείκτης πληρότητας αναφέρονται ως % στον πρωτεύοντα κάθετο άξονα (αριστερά). Παρομοίως στα διαγράμματα 42 και 43 φαίνεται η μεταβολή της αντοχής των στελεχών A. baumannii στις βρογχικές εκκρίσεις και η σχέση της απομόνωσης των στελεχών αυτών από τις βρογχικές εκκρίσεις με την πληρότητα της κλινικής και τη χρήση των αντιμικροβιακών. 131
132 Διάγραμμα 42: Μεταβολή αντοχής των στελεχών A. baumannii που απομονώθηκαν στις βρογχικές εκκρίσεις σε σχέση με τις παρεμβάσεις. Χρησιμοποιώντας τη μεθοδολογία των κυλιόμενων μέσων όρων βρέθηκε ότι η επίπτωση της εμφάνισης A. baumannii στις βρογχικές εκκρίσεις (που ήταν όλα πολυανθεκτικά στελέχη, με αντοχή σε >3 αντιμικροβιακά, ανεξάρτητα από την αντοχή στις καρβαπενέμες) επηρεάζεται άμεσα από τον επιπολασμό του A. baumannii στην κλινική (r=0,95, p<0,001), τον δείκτη πληρότητας (r=0,6, p=0,002), και είναι αντιστρόφως ανάλογη της κατανάλωσης αντιμικροβιακών (r=-0,89, p<0,001). Διάγραμμα 43: Διαχρονική καταγραφή της απομόνωσης στελεχών A. baumannii από τις βρογχικές εκκρίσεις (επίπτωση και επιπολασμός) σε σχέση με το δείκτη πληρότητας της 132
133 κλινικής και την συνολική κατανάλωση αντιμικροβικών. Ο επιπολασμός, η επίπτωση και ο δείκτης πληρότητας αναφέρονται ως % στον πρωτεύοντα κάθετο άξονα (αριστερά). Ειδικά για συγκεκριμένες λοιμώξεις (βακτηριαιμία, πνευμονία, ουρολοίμωξη, λοίμωξη χειρουργικού τραύματος) από στελέχη A. baumannii, K. pneumoniae και P. aeruginosa με αντοχή στις καρβαπενέμες τα στοιχεία είναι ακόμη καλύτερα. Συνολικά, το 2011 η επίπτωση αυτών των λοιμώξεων ήταν 7 επεισόδια ανά 1000 ημέρες νοσηλείας. Πίνακας 29: Ασθενείς με νοσοκομειακή λοίμωξη (βακτηριαιμία, πνευμονία, ουρολοίμωξη, λοίμωξη χειρουργικού πεδίου) από A. baumannii, K. pneumoniae και P. aeruginosa, με αντοχή στις καρβαπενέμες κατά το Ημ/νια A. baumannii Αρ. ασθενών K. pneumoniae Αρ. ασθενών P. aeruginosa Αρ. ασθενών Σύνολο ασθενών Επίπτωση ανά 100 ημέρες Ιαν ,00 Φεβ ,94 Μαρ ,08 Απρ ,01 Μαϊ ,00 Ιουν ,00 Ιουλ ,65 Αυγ ,42 Σεπ ,79 Οκτ ,00 Νοε ,00 Δεκ ,90 133
134 10.6. Παρέμβαση στην παιδοογκολογική κλινική Στην παιδοογκολογική κλινική έγινε καταγραφή των βακτηριαιμιών που αποτελούν σημαντικό αίτιο νοσηρότητας και θνητότητας στους παιδοογκολογικούς ασθενείς. Κατά το χρονικό διάστημα , απομονώθηκαν 157 μικρόβια (69% Gram θετικά, 31% Gram αρνητικά μικρόβια). Το συχνότερο αίτιο βακτηριαιμίας ήταν οι σταφυλόκοκκοι πηκτάσηαρνητικοί (67%) και κυρίως ο S. epidermidis, και ακολουθούσε η K. pneumoniae (9,6%), E. coli (8%) και P. aeruginosa (7%). Σε ό,τι αφορά τα Gram αρνητικά μικρόβια, η αντοχή στις καρβαπενέμες υπήρχε μόνο στα στελέχη P. aeruginosa σε πολύ χαμηλό ποσοστό (<10%), ενώ αρκετά μικρόβια εμφάνιζαν αντοχή στις κεφαλοσπορίνες 3 ης γενιάς (20-50%) και στις αμινογλυκοσίδες (15-63%). Σε ό,τι αφορά τα Gram θετικά μικρόβια το ποσοστό του MRSA ήταν <10%, ενώ όλα τα στελέχη εντεροκόκκου ήταν ευαίσθητα στα γλυκοπεπτίδια (βανκομυκίνη και τεϊκοπλανίνη). Τον Μάιο όμως του 2008, 2 νοσηλευόμενοι ασθενείς εμφάνισαν βακτηριαιμία από E. faecium που ήταν ανθεκτικός στην βανκομυκίνη και τεϊκοπλανίνη (Vancomycin resistant Εnterococcus faecium, VRE). Ο πρώτος από αυτούς τους ασθενείς είχε οξεία μυελογενή λευχαιμία και απεβίωσε μετά από σύντομο χρονικό διάστημα από την απομόνωση στην καλλιέργεια αίματός του δύο μικροβίων, VRE και P. aeruginosa. Ο δεύτερος ασθενής είχε διαγνωσθεί με μυεολοβλάστωμα ένα χρόνο πριν το επεισόδιο της βακτηριαιμίας. Εμφάνισε βακτηριαιμία από VRE 10 ημέρες μετά τον πρώτο ασθενή. Η θεραπεία των ασθενών αυτών ήταν αρκετά δύσκολη καθώς τα δραστικά αντιμικροβιακά φάρμακα για βακτηριαιμία από VRE είναι πολύ λίγα και ιδίως για τα παιδιά τα δεδομένα είναι ανεπαρκή. Ιδίως για το δεύτερο ασθενή για τη θεραπεία χρησιμοποιήθηκε λινεζολίδη αλλά και δαπτομυκίνη, δύο in vitro δραστικά αντιμικροβιακά αλλά με λίγα διεθνή δεδομένα ιδίως σε ότι αφορά την ένδειξη (και τα δύο) και τη δοσολογία (δαπτομυκίνη) στα παιδιά (Antachopoulos και συν 2012). Λόγω της σοβαρότητας της εκδήλωσης βακτηριαιμίας από VRE σε παιδιά με ογκολογικό νόσημα αποφασίσθηκε να γίνει παρέμβαση στο θέμα τόσο της οριζόντιας μετάδοσης μικροβίων αλλά και στη χρήση των αντιμικροβιακών (και συγκεκριμένα των γλυκοπεπτιδίων) στην κλινική. Σε ό,τι αφορά το θέμα του ελέγχου της οριζόντιας μετάδοσης μικροβίων, χρησιμοποιήθηκε η ενεργητική επιδημιολογική επιτήρηση για να μπορέσουμε να βρούμε τα 134
135 παιδιά εκείνα που ήταν αποικισμένα με VRE και ήταν σε κίνδυνο για εμφάνιση λοίμωξης, αλλά και να διασπείρουν το στέλεχος σε άλλους ασθενείς. Κατά τη διάρκεια των πρώτων 3 μηνών της ενεργητικής επιδημιολογικής επιτήρησης 26 ασθενείς ελέγχθηκαν (μεταξύ των οποίων και ο δεύτερος ασθενής με τη βακτηριαιμία) για την ύπαρξη VRE στο γαστρεντερικό σύστημα τους (κόπρανα). Έντεκα (42%) ασθενείς βρέθηκαν αποικισμένοι με VRE κατά τη διάρκεια του πρώτου επιδημιολογικού ελέγχου. Μεταξύ των υπόλοιπων 15 νοσηλευόμενων παιδιών, που είχαν πρώτη αρνητική καλλιέργεια για VRE, 7 ασθενείς απέκτησαν φορεία με VRE πριν από το τέλος του 2 ου μήνα. Κατά τη διάρκεια του 3 ου μήνα δεν υπήρχε νέο περιστατικό απόκτησης (διάγραμμα 44). Η μηνιαία επίπτωση του αποικισμού με VRE, με τα μέτρα που πάρθηκαν, ελαττώθηκε σταδιακά από 2,5 σε 1,5 και τελικά σε 0 νέα περιστατικά ανά 100 ημέρες νοσηλείας κατά το πρώτο, δεύτερο και τρίτο μήνα, αντίστοιχα. Παρόλα αυτά ο ημερήσιος επιπολασμός της φορείας VRE μεταξύ των νοσηλευόμενων ασθενών παρέμεινε υψηλός (40-70%) κατά το ίδιο χρονικό διάστημα, καθώς η διάρκεια παραμονής των παιδιών ήταν πολύ μεγάλη. Σε ότι αφορά την πληρότητα της κλινικής, και λόγω της αναστολής εισαγωγών νέων ασθενών παρατηρήθηκε σημαντική μείωσή της κατά το πρώτο τρίμηνο της ενεργητικής επιδημιολογικής επιτήρησης (από 94% πληρότητα τον Ιούνιο σε 73% τον Αύγουστο 2008). Τρεις μήνες μετά την εμφάνιση της επιδημίας και την μείωση της οριζόντιας μετάδοσης στελεχών VRE, η κλινική δεχόταν πλέον νέα περιστατικά, με συνέχιση όμως της επιδημιολογικής επιτήρησης (για άλλους τρεις μήνες). Ένα νέο περιστατικό με απόκτηση VRE εντοπίστηκε τον 4 ο μήνα σε ένα ασθενή που είχε πρόφατα προσκομισθεί για νοσηλεία στην κλινική. Κατά τη διάρκεια του 5 ου μήνα, 5 νέα άτομα νοσηλεύτηκαν αλλά κανένα δεν βρέθηκε θετικό για VRE. Παρόλα αυτά τον τελευταίο μήνα της επιτήρησης, δύο νέα περιστατικά φορείας με VRE ανιχνεύθηκαν (και τα 2 περιστατικά ήταν στους 5 ασθενείς που είχαν προσκομισθεί τον προηγούμενο μήνα). Σε αυτόν το μήνα η επίπτωση των περιστατικών με VRE ήταν 0,6 περιστατικά ανά 100 ημέρες νοσηλείας. 135
136 . Διάγραμμα 44: Χρονοδιάγραμμα εμφάνισης λοίμωξης/αποικισμού σε παιδιά της παιδοογκολογικής κλινικής από VRE, και τα μέτρα που ελήφθησαν. Η αναστολή της εισαγωγής νέων περιστατικών έγινε για 3 μήνες, ενώ τα εντατικοποιημένα μέτρα πρόληψης της οριζόντιας μετάδοσης συνεχίστηκαν για όλο το χρονικό διάστημα. Ο δείκτης πληρότητας εμφάνισε περαιτέρω μείωση κατά τη διάρκεια του 4 ου έως και 6 ου μήνα της επιτήρησης (65% τον τελευταίο μήνα). Κατά τη διάρκεια της ενεργητικής επιδημιολογικής επιτήρησης από τα 32 νοσηλευόμενα παιδιά στην παιδοογκολογική κλινική, τα 21 (66%) βρέθηκαν θετικά για VRE στα κόπρανα τουλάχιστον μια φορά. Παρόλα αυτά, έως το τέλος της ενεργητικής επιδημιολογικής επιτήρησης δεν υπήρξε νέο περιστατικό με λοίμωξη από VRE σε κανένα από τα αποικισμένα παιδιά. Μέχρι και τέσσερα χρόνια αργότερα δεν υπήρξε νέο περιστατικό με λοίμωξη από VRE. Συνολικά η θνητότητα ήταν 12%. Η φορεία με VRΕ δεν σχετίστηκε με υψηλότερη θνητότητα ούτε στο πρώτο τρίμηνο της μελέτης, ούτε στο σύνολο των 6 μηνών της επιτήρησης (2/21 VRE αποικισμένα παιδιά σε σχέση με 1/11 μη αποικισμένα παιδιά, p=1). Για την καλύτερη κατανόηση της επιδημίας από VRE στελέχη στο παιδοογκολογικό, και στα πλαίσια της παρέμβασης έγινε μελέτη σύγκρισης ομάδας ασθενών με ομάδα ελέγχου (case control). Τα δημογραφικά και άλλα κλινικά χαρακτηριστικά των 26 παιδιών που νοσηλεύτηκαν το πρώτο τρίμηνο αυτής της επιτήρησης φαίνονται στον πίνακα 45. Η προηγούμενη έκθεση στα γλυκοπεπτίδια, στις κεφαλοσπορίνες 3 ης γενιάς και στα αντιμικροβιακά με αναερόβια δράση, 136
137 ήταν συχνή και στις δύο ομάδες της μελέτης (αποικισμένοι ασθενείς ή μη από VRE). Παρομοίως, η μεταφορά σε κλινικές και εργαστήρια του νοσοκομείου εκτός της παιδοογκολογικής κλινικής, (π.χ. ακτινολογικό εργαστήριο, πυρηνική ιατρική, παιδοχειρουργική κλινική) δεν είχε επίπτωση στην απόκτηση ή όχι φορείας από VRE. Η θνητότητα ήταν ίδια και στις δύο ομάδες. Εξαιτίας του μικρού αριθμού των περιστατικών κατά τη διάρκεια του 4 ου και 6 ου μήνα, δεν συμπεριλήφθησαν αυτά στην μελέτη αυτή. Πίνακας 45: Χαρακτηριστικά των νοσηλευόμενων παιδιών της παιδοογκολογικής κλινικής κατά τους 3 πρώτους μήνες της ενεργητικής επιδημιολογικής επιτήρησης. Χαρακτηριστικό Σύνολο N=26 VRE θετικά N=18 VRE αρνητικά N=8 p τιμή Ηλικία [διάμεση τιμή (εύρος)] Άρρενα/θήλεα Λευχαιμία Ημέρες νοσηλείας 6 (1-16) 6,5 (2-14) 4 (1-16) 0,53 21/5 15/3 6/2 0,63 13/26 7/18 6/8 0,2 23 (5-90) 30 (8-90) 17,5 (5-65) 0,3 Προηγούμενη έκθεση σε αντιμικροβιακά Γλυκοπεπτίδια Κεφαλοσπορίνες Αντιαναερόβια* 22/26 22/26 20/26 17/18 17/18 15/18 5/8 5/8 5/8 0,07 0,07 0,3 Μεταφορά σε άλλο τμήμα του νοσοκομείου Πυρηνική ιατρική 16/26 12/18 4/8 0,67 Μαγνητικός τομογράφος 8/26 6/18 2/8 1 Αξονικός τομογράφος 9/26 6/18 3/8 1 Θνητότητα 3/26 2/18 1/8 1 *καρβεπενέμες, πιπερακιλλίνη/ταζομπακτάμη, αμοξυκιλλίνη/κλαβουλανικό, μετρονιδαζόλη 137
138 Σε ό,τι αφορά τα επιδημιολογικά και μικροβιολογικά δεδομένα, από τα 21 αποικισμένα παιδιά, 3 είχαν συνεχώς θετικούς ελέγχους με VRE. Μάλιστα οι ασθενείς αυτοί είχαν επαναλαμβανόμενες θετικές καλλιέργειες αποικισμού, παρά το γεγονός ότι είχαν λάβει στο ενδιάμεσο διάστημα λινεζολίδη εμπειρικά για κάποιο εμπύρετο επεισόδιο, που τελικά δεν αποδείχθηκε ότι ήταν λοίμωξη από VRE. Η μελέτη με PCR έδειξε ότι όλα τα στελέχη VRE είχαν το γονίδιο αντοχής vana που είναι υπεύθυνο για την αντοχή στα γλυκοπεπτίδια. Η μοριακή τυποποίηση 10 τυχαία επιλεγμένων στελεχών (2 από το αίμα και 8 από καλλιέργειες αποικισμού) από 10 διαφορετικά παιδιά έδειξε ότι υπήρχαν πολλαπλοί κλώνοι VRE (εικόνα 9). Παρόλα αυτά, δύο ασθενείς είχαν ακριβώς τον ίδιο κλώνο. Ο πρώτος από αυτούς τους ασθενείς που είχαν τον ίδιο κλώνο είχε αποικισθεί τον 2 ο μήνα της επιτήρησης, ενώ ο δεύτερος τον 6 ο μήνα της επιτήρησης. Και οι δύο ασθενείς είχαν νοσηλευθεί το ίδιο χρονικό διάστημα (5 ος μήνας) στην κλινική σε ξεχωριστά δωμάτια. Το χρονικό εκείνο διάστημα, ο πρώτος ασθενής ήταν ήδη αποικισμένος αλλά ο δεύτερος όχι (είχε πρώτη καλλιέργεια ελέγχου αρνητική για VRE τον 5 ο μήνα). Εικόνα 9. PFGE ανάλυση επιλεγμένων στελεχών VRE από παιδιά της παιδοογκολογικής κλινικής. Ladder: DNA μάρτυρας Στο θέμα της ορθολογικής χρήσης αντιμικροβιακών, καθημερινά γινόταν συζήτηση για την αναγκαιότητα της χρήσης των γλυκοπεπτιδίων στα διάφορα περιστατικά. Επιπλέον, σε συνεργασία με τους λοιμωξιολόγους καθοριζόταν η αρχική εμπειρική αγωγή σε εμπύρετα επεισόδια των παιδιών της κλινικής, η διάρκεια της αγωγής αλλά και η αποκλιμάκωση σε περίπτωση απομόνωσης ενός μικροβίου με αντιβιόγραμμα. Για να γίνει καλύτερα αντιληπτή η παρέμβαση στο θέμα της ορθολογικής χρήσης των αντιμικροβιακών και σε σχέση πάντοτε με την εμφάνιση των περιστατικών με VRE έγινε καταγραφή σε μηνιαία βάση των αντιμικροβιακών φαρμάκων στην κλινική ένα χρόνο πριν την επιδημία έως και ένα χρόνο μετά. Όπως φαίνεται στο διάγραμμα 45, η τεϊκοπλανίνη ήταν το 138
139 συχνότερο γλυκοπεπτίδιο που χρησιμοποιούσε η κλινική (25-35 DDD/100 ημέρες νοσηλείας) κατά τη διάρκεια των 3 ετών, Σημαντική μείωση στην κατανάλωση των γλυκοπεπτιδίων σημειώθηκε το πρώτο 3μηνο της επιδημίας και υπό την καθοδήγηση της ομάδας των λοιμωξιολόγων. Παράλληλα αυξήθηκε, όπως αναμενόταν, η χρήση της λινεζολίδης. Όπως προαναφέρθηκε η λινεζολίδη χρησιμοποιήθηκε ως στοχευμένη θεραπεία για τα περιστατικά με τη βακτηριαιμία από VRE αλλά και ως εμπειρική αγωγή σε επεισόδια εμπύρετης ουδετεροπενίας σε ασθενείς που ήταν αποικισμένοι με VRE. Η λινεζολίδη δεν χρησιμοποιήθηκε ως φάρμακο χημειοπροφύλαξης σε κανένα παιδί. Η τεϊκοπλανίνη σταδιακά εμφάνισε αύξηση της χρήσης της μετά τους πρώτους μήνες της επιτήρησης για να επιστρέψει στα βασικά επίπεδα κατανάλωσής της λίγους μήνες αργότερα. Η χρήση άλλων αντιμικροβιακών με δράση στα Gramθετικά, όπως είναι η βανκομυκίνη και η δαπτομυκίνη, ήταν σε γενικές γραμμές περιορισμένη καθόλη τη διάρκεια της επιτήρησης. Συνολικά, και λαμβάνοντας υπόψη και τα υπόλοιπα αντιμικροβιακά φάρμακα, η χρήση των κεφαλοσπορινών 3 ης γενιάς ήταν αρκετά συχνή, ενώ λιγότερο συχνή ήταν η χρήση των καρβαπενεμών. Μόνο κατά τη διάρκεια της επιτήρησης υπήρξε μείωση της κατανάλωσης κεφαλοσπορινών 3 ης γενιάς και αύξηση των καρβαπενεμών. Η χρήση άλλων φαρμάκων με αντιαναερόβια δράση δεν είχε σημαντικές διακυμάνσεις (διάγραμμα 45 ). Διάγραμμα 45. Μηνιαία κατανάλωση αντιμικροβιακών φαρμάκων στην παιδοογκολογική κλινική. Κατά το χρονικό διάστημα , δεν καταγράφηκε κανένα νέο περιστατικό λοίμωξης από VRE, και από την καταγραφή λοιμώξεων από ανθεκτικά στις καρβαπενέμες A. 139
140 baumannii, P. aeruginosa και K. pneumoniae δεν βρέθηκε κάποιο περιστατικό. Το πρόβλημα της αντοχής εντοπίζεται κυρίως στις κεφαλοσπορίνες 3 ης γενιάς Παρέμβαση στη μονάδα εντατικής νοσηλείας νεογνών Στη μονάδα εντατικής νοσηλείας νεογνών (ΜΕΝΝ) η βακτηριαιμία αποτελεί σημαντικό αίτιο νοσηρότητας και θνησιμότητας. Η αρχική εμπειρική αγωγή πρέπει να στηρίζεται στην επιδημιολογία της μονάδας. Η αρχική αξιολόγηση των δεδομένων από τη μικροβιολογία των βακτηριαιμιών για το διάστημα έδειξε ότι τα Gram θετικά παθογόνα ήταν συχνότερα με ποσοστό 79,6%. Ο S. epidermidis ήταν το συχνότερο Gram θετικό παθογόνο, ενώ από τα Gram αρνητικά κυριαρχούσαν τα εντεροβακτηριοειδή (K. pneumoniae, E. cloacae και E. coli). Σε ότι αφορά στο θέμα της αντοχής, στα Gram αρνητικά συχνή ήταν η αντοχή στις κεφαλοσπορίνες 3 ης γενιάς, κυρίως σε στελέχη K. pneumoniae. Στα Gram θετικά μικρόβια δεν υπήρχε αντοχή στα γλυκοπεπτίδια μέχρι τον Ιούνιο του 2008 οπότε και παρουσιάστηκε ένα επεισόδιο βακτηριαιμίας σε νεογνό με E. faecium ανθεκτικό στη βανκομυκίνη. Στο ίδιο χρονικό διάστημα ένα ακόμη νεογνό εμφάνισε λοίμωξη του κοιλιοπεριτοναϊκού καθετήρα (shunt) που είχε τοποθετηθεί για αντιμετώπιση υδροκεφαλίας. Μετά από τα δύο αυτά περιστατικά λοίμωξης με VRE, έγινε αρχικά δειγματοληψία στον θάλαμο που νοσηλεύονταν τα νεογνά που εμφάνισαν τη λοίμωξη. Η δειγματοληψία έδειξε ότι αρκετά νεογνά που μοιράζονταν τον ίδιο χώρο ήταν ήδη αποικισμένα. Για το λόγο αυτό ξεκίνησε άμεσα η ενεργητική επιδημιολογική επιτήρηση της φορείας όλων των νοσηλευόμενων νεογνών μετά την 7 η ημέρα παραμονής στην κλινική. Σύμφωνα με τα αποτελέσματα της επιδημιολογικής επιτήρησης, τον πρώτο μήνα στην κλινική ο ημερήσιος επιπολασμός της φορείας VRE έφτασε ως και 85%. Σε ό,τι αφορά την επίπτωση, 4 περιστατικά ανά 1000 ημέρες νοσηλείας (που αντιστοιχούν με νέα περιστατικά αποικισμού με VRE την εβδομάδα) καταγράφηκαν τις πρώτες 4 εβδομάδες της επιδημίας. Τις επόμενες εβδομάδες (5 η ως και 9 η ) και με τα μέτρα που πάρθηκαν, σημειώθηκε μείωση στον αριθμό των νέων περιπτώσεων αποικισμού (εικόνα 10, διάγραμμα 46). Ειδικά κατά την 10 η έως και 12 η εβδομάδα δεν υπήρχε νέο περιστατικό VRE αποικισμού στην μονάδα (εικόνα 10). Παράλληλα, ο επιπολασμός της φορείας με VRE μειώθηκε στο 32% (8 η εβδομάδα) και μετά στο 13% στο τέλος της 12 ης εβδομάδας. 140
141 . Εικόνα 10: Κάτοψη της μονάδας και θέση των αποικισμένων νεογνών κατά τη διάρκεια της επιτήρησης Κατά τη διάρκεια της 13 ης εβδομάδας και ενώ υπήρχε μόνο ένα νεογνό με γνωστή φορεία VRE, βρέθηκαν 4 νέα περιστατικά. Έκτοτε, η επίπτωση της φορείας VRE αυξήθηκε πάλι και 42 νέα περιστατικά φορείας VRE βρέθηκαν τις επόμενες 13 εβδομάδες (διάγραμμα 46). Συνολικά, μεταξύ 389 νεογνών που νοσηλεύτηκαν στη ΜΕΝΝ κατά τη διάρκεια της μελέτης, 253 νεογνά ελέγχθηκαν και 101 (39,9%) βρέθηκαν αποικισμένα με VRE. Η κλινική συνέχισε να δέχεται νέες εισαγωγές με τον καθιερωμένο τρόπο εφημεριών (μέσος αριθμός εισαγωγών 60 νεογνά τον μήνα). Ο μέσος αριθμός των ημερών νοσηλείας κατά τη μελέτη ήταν 1180 ανά μήνα και η πληρότητα 90%. Κατά τη διάρκεια των πρώτων 5 μηνών της επιτήρησης καμία νέα λοίμωξη από VRE δεν υπήρξε. Παρόλα αυτά, τον τελευταίο μήνα απομονώθηκε στέλεχος VRE από καλλιέργεια ούρων νεογνού χωρίς όμως σημεία λοίμωξης. Επεισόδιο βακτηριαιμίας από VRE δεν παρατηρήθηκε εκ νέου. 141
142 Διάγραμμα 46: Καταγραφή της διαχρονικής πορείας της επιδημίας από VRE στη ΜΕΝΝ και των μέτρων που πάρθηκαν. Πρέπει να αναφερθεί ότι η ενεργητική επιδημιολογική επιτήρηση έγινε και σε άλλες κλινικές του νοσοκομείου (λαμβάνοντας υπόψη και την ταυτόχρονη επιδημία στην παιδοογκολογική κλινική). Στη ΜΕΘ ενηλίκων, στην κλινική μεταμοσχεύσεων συμπαγών οργάνων, στις χειρουργικές κλινικές και στη ΜΕΘ παίδων ο έλεγχος έδειξε ότι δεν υπήρχε άλλο περιστατικό με VRE. Μεταξύ των δύο κλινικών (ΜΕΝΝ και παιδοογκολογικό), 2 ασθενείς από τις δύο κλινικές είχαν τον ίδιο κλώνο. Αναφορικά με τα μικροβιολογικά δεδομένα, συνολικά 591 δείγματα κοπράνων ελέγχθηκαν για VRE. Όλα τα στελέχη VRE είχαν παρόμοιο αντιβιόγραμμα και ήταν ανθεκτικά στην βανκομυκίνη και τεϊκοπλανίνη, ενώ ήταν ευαίσθητα στην λινεζολίδη και στη δαπτομυκίνη. Όλα τα στελέχη VRE ήταν E. faecium και η μοριακή ανάλυση έδειξε ότι όλα είχαν το γονίδιο vana, υπεύθυνο για την αντοχή στα γλυκοπεπτίδια. Η μοριακή τυποποίηση (PFGE) συνολικά 27 στελεχών (ένα ανά ασθενή) που επιλέχθηκαν τυχαία από τα 101 αποικισμένα νεογνά και καθόλη 142
143 τη διάρκεια της επιδημιολογικής μελέτης έδειξε ότι στο πρώτο κύμα της επιδημίας κυριαρχούσε ένας κλώνος ενώ στο δεύτερο κύμα βρέθηκαν συνολικά 4 κλώνοι (διάγραμμα 47). Διάγραμμα 47: PFGE αποτυπώματα από 29 στελέχη VRE που απομονώθηκαν από αντίστοιχο αριθμό νεογνών που νοσηλεύθηκαν στη ΜΕΝΝ το ίδιο χρονικό διάστημα. Για την καλύτερη κατανόηση των παραγόντων που οδήγησαν στον αποικισμό των παραπάνω νεογνών έγινε μελέτη ασθενών-μαρτύρων. Κατά τη διάρκεια της μελέτης αναλύθηκαν τα δεδομένα από 33 αποικισμένα νεογνά και 33 νεογνά που δεν αποικίσθηκαν καθόλου κατά την παραμονή τους στην κλινική. Η μονοπαραγοντική ανάλυση έδειξε ότι δεν υπήρχε στατιστικώς σημαντική διαφορά μεταξύ των δύο ομάδων σε ό,τι αφορά το φύλο, τη διάρκεια κύησης, το βάρος γέννησης, το νοσοκομείο γέννησης (εντός του Ιπποκρατείου Νοσοκομείου ή διακομιδή από άλλο νοσοκομείο/μαιευτήριο), την μηχανική υποστήριξη της αναπνοής, την παρεντερική διατροφή, την παρουσία κεντρικού φλεβικού καθετήρα, την παρουσία ρινογαστρικού καθετήρα και τη μεταφορά εκτός της κλινικής σε άλλη κλινική ή εργαστήριο του νοσοκομείου στα πλαίσια εξετάσεων (απεικονιστικός έλεγχος κλπ). Η χορήγηση αντιμικροβιακών φαρμάκων ευρύτερου φάσματος αντιμικροβιακή θεραπεία 2ης γραμμής- για την όψιμη σήψη, ήταν πιο συχνή στα αποικισμένα νεογνά (p<0,05). Επιπλέον, τα περισσότερα από τα αποικισμένα νεογνά νοσηλεύτηκαν την πρώτο μήνα της μελέτης οπότε και ο επιπολασμός της φορείας VRE στη ΜΕΝΝ ήταν υψηλός (Πίνακας 30). Στην πολυπαραγοντική ανάλυση, η χορήγηση τουλάχιστον μια φορά αντιμικροβιακής αγωγής 2 ης γραμμής (p=0,008) και νοσηλεία κατά το πρώτο μήνα της μελέτης (p=0,002), ήταν ανεξάρτητοι παράγοντες για τον αποικισμό με VRE. 143
144 Στα πλαίσια ελέγχου της επιδημίας από VRE ήταν ο περιορισμός της χρήσης των γλυκοπεπτιδίων στη μονάδα και η ενίσχυση της ορθολογικής χρήσης αντιμικροβιακών. Για την παρακολούθηση των αλλαγών στην πολιτική της χρήσης αντιμικροβιακών στην κλινική έγινε μηνιαία καταγραφή της κατανάλωσης γλυκοπεπτιδίων και λινεζολίδης ένα χρόνο πριν έως και ένα χρόνο μετά τη επιδημία. Σύμφωνα με τα αποτελέσματα της καταγραφής της κατανάλωσης των παραπάνω αντιμικροβιακών υπήρχε μια σταθερή χρήση της βανκομυκίνης μέχρι την έναρξη της επιδημίας, ακολούθησε μείωση της χρήσης των γλυκοπεπτιδίων και στη συνέχεια αντικαταστάθηκε η χρήση της βανκομυκίνης από τεϊκοπλανίνη. Η χρήση της λινεζολίδης δεν ήταν συχνή παρά μόνο στη διάρκεια της επιδημίας και αφορούσε την εμπειρική αγωγή νεογνών που ήταν αποικισμένα με VRE και εικόνα σήψης. Χρησιμοποιώντας τη μεθοδολογία του κυλιόμενου μέσου όρου, καταγράφηκε μια σημαντική μείωση στη χρήση των γλυκοπεπτιδίων (p<0,001) και σημαντική αύξηση στη χρήση της λινεζολίδης (p<0,0001) κατά τη διάρκεια της επιδημιολογικής επιτήρησης και των συχνών συναντήσεων της ομάδας των λοιμωξιολόγων με τους νεογνολόγους για τις πολιτικές χορήγησης αντιμικροβιακών. Βέβαια μετά το τέλος της επιτήρησης και της εμφάνισης νέων περιστατικών με VRE η κατανάλωση γλυκοπεπτιδίων εμφάνισε αύξηση στα προηγούμενα της επιδημίας επίπεδα (p<0,001). Μετά την αντιμετώπιση της επιδημίας από VRE, το κύριο πρόβλημα της αντοχής στις βακτηριαιμίες στα νεογνά ήταν η αντοχή στις κεφαλοσπορίνες 3 ης γενιάς (>90%). Έχοντας επαγρύπνηση για την εμφάνιση πολυανθεκτικών στελεχών, τον Σεπτέμβριο και Οκτώβριο του 2011 εμφανίστηκαν περιστατικά με βακτηριαιμία από A. baumannii ανθεκτικό στην ιμιπενέμη, κεφαλοσπορίνες, πενικιλλίνες, φθοροκινολόνες, καθώς και στις περισσότερες αμινογλυκοσίδες. Ήταν η πρώτη φορά που εμφανιζόταν τέτοιο πολυανθεκτικό στέλεχος στη ΜΕΝΝ. Τα μέτρα έπρεπε να στοχεύουν τόσο στον περιορισμό της εξάπλωσης του παθογόνου αυτού αλλά και στην ορθολογική θεραπεία των προσβεβλημένων νεογνών καθώς υπάρχουν πλέον ελάχιστες θεραπευτικές λύσεις (με κυριότερο αντιπρόσωπο την κολιμυκίνη, για την οποία όμως υπάρχουν ελάχιστα δεδομένα φαρμακοκινητικής και φαρμακοδυναμικής στα νεογνά). 144
145 Πίνακας 30: Χαρακτηριστικά των παιδιών που νοσηλεύθηκαν στη μονάδα νεογνών και ελέχθηκαν για αποικισμό με VRE Χαρακτηριστικά Αποικισμένα νεογνά (N=33) Μη αποικισμένα νεογνά (N=33) p Φύλο (Άρρεν, N) ,8 Μέση Διάρκεια Κύησης (SD) 35 εβδ (3,2) 35 εβδ (2,9) 0,9 Βάρος Γέννησης (SD) Εύρος 2563 gr (880) gr 2408 gr (724) gr 0,4 Γέννηση στο Ιπποκράτειο (N) Αναπνευστική ανεπάρκεια (N) Μηχανικός αερισμός CPAP Χορήγηση οξυγόνου ,8 0,4 1 1 Ολική Παρεντερική διατροφή (N) Διάρκεια (διάμεσος) 29 8 ημέρες 28 5 ημέρες 1 0,5 Ρινογαστρικός καθετήρας (N) Διάρκεια (διάμεσος) 32 6 ημέρες 32 7 ημέρες 1 0,6 Κεντρική αγγειακή γραμμή (N) (ΚΦΚ, ΟΚ) 9 5 0,4 Βακτηριαιμία (N) 8 2 0,08 Αντιμικροβιακή αγωγή (N) 1 η γραμμή (AMP +/- GEN) 2 η γραμμή (GLY/MEM/ FEP/ CIP/AZT) ,6 0,02 Αντιμικροβιακό φάρμακο Γλυκοπεπτίδια Βανκομυκίνη Τεϊκοπλανίνη Κεφεπίμη Μεροπενέμη Αζτρεονάμη Σιπροφλοξασίνη ,8 0,8 1 0,4 0,5 0,5 1 Περίοδος νοσηλείας στη ΜΕΝΝ 1 ος μήνας 2 ος μήνας 3 ος μήνας ,01 0,8 0,03 CPAP: συνεχής θετική πίεση στον αεραγωγό, ΚΦΚ: Κεντρικός Φλεβικός Καθετήρας, ΟΚ: Ομφαλικός Καθετήρας, AMP: Αμπικιλλίνη, GEN: Γενταμικίνη, GLY: Γλυκοπεπτίδια, MEM: Μεροπενέμη, FEP: Κεφεπίμη, CIP: Σιπροφλοξασίνη, AZT: Αζτρεονάμη 145
146 Η επιδημία από A. baumannii ανθεκτικό στην ιμιπενέμη (imipenem resistant A. baumannii, IRAB) ξεκίνησε λίγο πριν τις διαδικασίες ανακαίνισης της κλινικής. Ο πρώτος ασθενής εμφάνισε βακτηριαιμία από IRAB τον Σεπτέμβριο και στη συνέχεια άλλα 7 νεογνά εμφάνισαν λοίμωξη από IRAB τους επόμενους 2 μήνες (διάγραμμα 48). Πέντε νεογνά εμφάνισαν βακτηριαιμία, τέσσερα εμφάνισαν λοίμωξη του κατώτερου αναπνευστικού συστήματος και ένα οφθαλμία. Όλα τα νεογνά με εξαίρεση ένα ήταν πρόωρα (μέσος όρος και τυπική απόκλιση της διάρκειας κύησης 30,8 1,7 εβδομάδες, εύρος εβδομάδες). Η μέση χρονολογική ηλικία (και τυπική αποκλιση) εμφάνισης της λοίμωξης ήταν 4,8 0,9 εβδομάδες. Όλα τα νεογνά αυτά είχαν υποβληθεί σε πολλές επεμβατικές διαδικασίες όπως είναι η διασωλήνωση, τοποθέτηση κεντρικού φλεβικού καθετήρα και ρινογαστρικού καθετήρα. Όλα τα νεογνά είχαν λάβει ευρέως φάσματος αντιμικροβιακή αγωγή πριν την εμφάνιση της λοίμωξης από IRAB. Όλα τα νεογνά θεραπεύτηκαν επιτυχώς με τη χορηγηση μεροπενέμης και σε κάποια με προσθήκη κολιμυκίνης. Ένα νεογνό κατέληξε εξαιτίας της συνύπαρξης άλλων υποκείμενων νοσημάτων μεταξύ των οποίων και βαριά νεφρική ανεπάρκεια. Παρά το μικρό αριθμό των περιστατικών σε μελέτη ασθενών-μαρτύρων για τον προσδιορισμό των πιθανών παραγόντων εμφάνισης λοίμωξης από IRAB φάνηκε ότι τα νεογνά με IRAB λοίμωξη είχαν τάση να είναι περισσότερο πρόωρα (30,8 1,7 vs 34 1,8 εβδομάδες κύησης), είχαν μικρότερο βάρος γέννησης (1431,2 265,2 vs ,2 gr), είχαν περισσότερους κεντρικούς αγγειακούς καθετήρες (9 vs 5) και παρατεταμένη νοσηλεία στη ΜΕΝΝ πριν την λοίμωξη από ΙRAB (4,8 0,9 vs 2 1,5 εβδομάδες) σε σχέση με την ομάδα χωρίς λοίμωξη από IRAB, αλλά χωρίς στατιστική σημαντικότητα (p >0,05). Από τις άμεσες ενέργειες για την μείωση της μετάδοσης του IRAB ήταν να απομονωθούν όλα τα περιστατικά με λοίμωξη, να γίνει στενή παρακολούθηση της χορήγησης των αντιμικροβιακών φαρμάκων (εμπειρική και κατευθυνόμενη αγωγή) και η έναρξη προγράμματος ενεργητικής επιδημιολογικής επιτήρησης για την ανίχνευση των φορέων του IRAB. Ξεκινώντας την 10 η εβδομάδα από το πρώτο κρούσμα (Νοέμβριος 2011), και για 10 εβδομάδες, ελέχθηκαν συνολικά 216 δείγματα από 96 νεογνά (43% των νεογνών είχαν τουλάχιστον 2 δείγματα). Κατά τη διάρκεια της 1 ης, 5 ης και 6 ης εβδομάδας της επιδημιολογικής επιτήρησης, 5, 2 και 2 νέα περιστατικά IRAB ανιχνεύθηκαν, αντίστοιχα (διάγραμμα 48). Ο 146
147 επιπολασμός της φορείας IRAB μειώθηκε από 19% (1 η εβδομάδα της επιτήρησης) σε 4% (7 η εβδομάδα) και τελικά στο 0% (8 η,9 η και 10 η εβδομάδα, διάγραμμα 48). Επιπλέον των καλλιεργειών αποικισμού στα νεογνά, έγιναν καλλιέργειες στο περιβάλλον της ΜΕΝΝ, συμπεριλαμβάνοντας καλλιέργειες από μόνιτορς, επιφάνειες γραφείων, διαγράμματα πορείας ασθενών και από τον αναπνευστήρα, που όλες ήταν αρνητικές για IRAB. Με την επιδημιολογική επιτήρηση καταγράφηκε ότι σε 3 νεογνά ο αποικισμός από IRAB είχε μεγάλη διάρκεια (τουλάχιστον 5 εβδομάδες). Ένα νεογνό που είχε αρχικά λοίμωξη αναπνευστικού από IRAB, μετά από 44 ημέρες εμφάνισε επίμονη βακτηριαιμία από IRAB και τελικά κατέληξε. Μετά την έναρξη της επιδημιολογικής επιτήρησης και την εφαρμογή των μέτρων, δύο λοιμώξεις από IRAB εμφανίστηκαν σε νεογνά (1 λοίμωξη αναπνευστικού συστήματος και μια βακτηριαιμία σε πολύ κοντινά διαστήματα, διάγραμμα 48). Έκτοτε και για 12 μήνες δεν υπήρξε νέο περιστατικό λοίμωξης από IRAB. Διάγραμμα 48: Χρονική καταγραφή των νέων περιστατικών με λοίμωξη ή αποικισμό από ανθεκτικό στην ιμιπενέμη A. baumannii και των μέτρων που πάρθηκαν. IRAB: Imipenem resistant A. baumannii Με τη βοήθεια της μοριακής τυποποιησης (PFGE) όλα τα A. baumannii στελέχη που απομονώθηκαν από τα νεογνά με λοίμωξη ή αποικισμό είχαν πανομοιότυπο PFGE αποτύπωμα, υποδηλώνοντας ότι πρόκειται για έναν και μοναδικό κλώνο (εικόνα 11). Σε ό,τι αφορά τον 147
148 μηχανισμό αντοχής στις καρβαπενέμες, ανιχνεύθηκαν με PCR 2 γονίδια υπεύθυνα για την παραγωγή καρβαπενεμασών της κατηγορίας OXA (Ambler τάξη D) και συγκεκριμένα τα γονίδια bla OXA-58 και bla OXA-51. Εικόνα 11: PFGE αποτυπώματα στελεχών IRAB που απομονώθηκαν από νεογνά με λοίμωξη ή αποικισμό. Η διαχρονική μεταβολή της κατανάλωσης καρβαπενεμών (κυρίως μεροπενέμης) και κεφαλοσπορίνης 4 η γενιάς (κεφεπίμη) στα νεογνά φαίνεται στο διάγραμμα 49. Διάγραμμα 49: Μηναία κατανάλωση μεροπενέμης και κεφεπίμης στη ΜΕΝΝ 148
pneumoniae ΣΤΟ ΠΑΝΕΠΙΣΤΗΜΙΑΚΟ ΓΕΝΙΚΟ ΝΟΣΟΚΟΜΕΙΟ
 ΕΜΦΑΝΙΣΗ OXA-8 ΚΑΡΒΑΠΕΝΕΜΑΣΩΝ ΣΕ ΣΤΕΛΕΧΗ Klebsiella pneumoniae ΣΤΟ ΠΑΝΕΠΙΣΤΗΜΙΑΚΟ ΓΕΝΙΚΟ ΝΟΣΟΚΟΜΕΙΟ ΙΩΑΝΝΙΝΩΝ (ΠΓΝΙ) Γ. Καπνίση, Ε. Πριάβαλη, Α. Γιαννάκη, Α. Παπαδημητρίου, Π. Παπαδιώτη, Α. Καλλιντέρη,
ΕΜΦΑΝΙΣΗ OXA-8 ΚΑΡΒΑΠΕΝΕΜΑΣΩΝ ΣΕ ΣΤΕΛΕΧΗ Klebsiella pneumoniae ΣΤΟ ΠΑΝΕΠΙΣΤΗΜΙΑΚΟ ΓΕΝΙΚΟ ΝΟΣΟΚΟΜΕΙΟ ΙΩΑΝΝΙΝΩΝ (ΠΓΝΙ) Γ. Καπνίση, Ε. Πριάβαλη, Α. Γιαννάκη, Α. Παπαδημητρίου, Π. Παπαδιώτη, Α. Καλλιντέρη,
Αντιβιοτικά Μηχανισμοί δράσης και μηχανισμοί αντοχής
 Αντιβιοτικά Μηχανισμοί δράσης και μηχανισμοί αντοχής Ιωσήφ Παπαπαρασκευάς Εργαστήριο Μικροβιολογίας, Ιατρική Σχολή Εθνικό και Καποδιστριακό Πανεπιστήμιο Αθηνών, ipapapar@med.uoa.gr Ομάδες αντιβιοτικών
Αντιβιοτικά Μηχανισμοί δράσης και μηχανισμοί αντοχής Ιωσήφ Παπαπαρασκευάς Εργαστήριο Μικροβιολογίας, Ιατρική Σχολή Εθνικό και Καποδιστριακό Πανεπιστήμιο Αθηνών, ipapapar@med.uoa.gr Ομάδες αντιβιοτικών
Βερανζέρου 50 Αθήνα ΤΚ10438 Φ. Καλύβα (210) 5236948 (210) 5233563 ddy@yyka.gov.gr fkaliva@yyka.gov.gr ΠΡΟΣ :
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ ΑΝΑΡΤΗΤΕΑ ΣΤΟ ΔΙΑΔΙΚΤΥΟ ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ Αθήνα 18/ 4/2013 ΓΕΝΙΚΗ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΕΙΑΣ & Αριθ.Πρωτ.Υ1/Γ.Π.οικ. 35566 ΠΟΙΟΤΗΤΑΣ ΖΩΗΣ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΙΕΙΝΗΣ ΤΜΗΜΑ ΕΠΙΔΗΜΙΟΛΟΓΙΑΣ ΝΟΣΗΜΑΤΩΝ
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ ΑΝΑΡΤΗΤΕΑ ΣΤΟ ΔΙΑΔΙΚΤΥΟ ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ Αθήνα 18/ 4/2013 ΓΕΝΙΚΗ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΕΙΑΣ & Αριθ.Πρωτ.Υ1/Γ.Π.οικ. 35566 ΠΟΙΟΤΗΤΑΣ ΖΩΗΣ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΙΕΙΝΗΣ ΤΜΗΜΑ ΕΠΙΔΗΜΙΟΛΟΓΙΑΣ ΝΟΣΗΜΑΤΩΝ
ΜΟΡΙΑΚΗ ΑΝΙΧΝΕΥΣΗ ΚΑΙ ΔΙΕΡΕΥΝΗΣΗ ΤΗΣ ΜΙΚΡΟΒΙΑΚΗΣ ΑΝΤΟΧΗΣ
 ΗΜΕΡΙΔΑ ΕΦΑΡΜΟΣΜΕΝΗΣ ΚΛΙΝΙΚΗΣ ΚΑΙ ΔΙΑΓΝΩΣΤΙΚΗΣ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ 24 ΙΑΝΟΥΑΡΙΟΥ 2009 ΜΟΡΙΑΚΗ ΑΝΙΧΝΕΥΣΗ ΚΑΙ ΔΙΕΡΕΥΝΗΣΗ ΤΗΣ ΜΙΚΡΟΒΙΑΚΗΣ ΑΝΤΟΧΗΣ Ε. ΠΕΤΕΙΝΑΚΗ ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ
ΗΜΕΡΙΔΑ ΕΦΑΡΜΟΣΜΕΝΗΣ ΚΛΙΝΙΚΗΣ ΚΑΙ ΔΙΑΓΝΩΣΤΙΚΗΣ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ 24 ΙΑΝΟΥΑΡΙΟΥ 2009 ΜΟΡΙΑΚΗ ΑΝΙΧΝΕΥΣΗ ΚΑΙ ΔΙΕΡΕΥΝΗΣΗ ΤΗΣ ΜΙΚΡΟΒΙΑΚΗΣ ΑΝΤΟΧΗΣ Ε. ΠΕΤΕΙΝΑΚΗ ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ
ΤΟ ΕΡΓΑΣΤΗΡΙΟ ΚΛΙΝΙΚΗΣ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ ΣΤΟΝ ΕΛΕΓΧΟ ΤΩΝ ΝΟΣΟΚΟΜΕΙΑΚΩΝ ΛΟΙΜΩΞΕΩΝ
 1η ΕΠΙΣΤΗΜΟΝΙΚΗ ΔΙΗΜΕΡΙΔΑ «ΕΛΕΓΧΟΣ ΤΩΝ ΝΟΣΟΚΟΜΕΙΑΚΩΝ ΛΟΙΜΩΞΕΩΝ ΕΦΑΡΜΟΓΕΣ ΣΤΗ ΚΑΘΗΜΕΡΙΝΗ ΠΡΑΞΗ ΔΥΝΑΤΟΤΗΤΕΣ ΠΡΟΟΠΤΙΚΕΣ» ΛΑΜΙΑ 21 22 22 ΟΚΤΩΒΡΙΟΥ 2005 ΤΟ ΕΡΓΑΣΤΗΡΙΟ ΚΛΙΝΙΚΗΣ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ ΣΤΟΝ ΕΛΕΓΧΟ ΤΩΝ
1η ΕΠΙΣΤΗΜΟΝΙΚΗ ΔΙΗΜΕΡΙΔΑ «ΕΛΕΓΧΟΣ ΤΩΝ ΝΟΣΟΚΟΜΕΙΑΚΩΝ ΛΟΙΜΩΞΕΩΝ ΕΦΑΡΜΟΓΕΣ ΣΤΗ ΚΑΘΗΜΕΡΙΝΗ ΠΡΑΞΗ ΔΥΝΑΤΟΤΗΤΕΣ ΠΡΟΟΠΤΙΚΕΣ» ΛΑΜΙΑ 21 22 22 ΟΚΤΩΒΡΙΟΥ 2005 ΤΟ ΕΡΓΑΣΤΗΡΙΟ ΚΛΙΝΙΚΗΣ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ ΣΤΟΝ ΕΛΕΓΧΟ ΤΩΝ
Genus Klebsiella. Ταξινόμηση. Λοιμογόνοι παράγοντες 3/12/2014
 ΔΙΕΡΕΥΝΗΣΗ ΤΗΣ ΑΝΘΕΚΤΙΚΟΤΗΤΑΣ ΣΤΙΣ ΚΑΡΒΑΠΕΝΕΜΕΣ ΠΟΛΥΑΝΘΕΚΤΙΚΩΝ ΣΤΕΛΕΧΩΝ KLEBSIELLA PNEUMONIAE ΜΠΑΚΑΛΗ ΣΤΑΜΑΤΙΑ Ειδικευόμενη Ιατρικής Βιοπαθολογίας Αλεξανδρούπολη Ιούνιος 2014 Kingdom: Phylum: Class: Order:
ΔΙΕΡΕΥΝΗΣΗ ΤΗΣ ΑΝΘΕΚΤΙΚΟΤΗΤΑΣ ΣΤΙΣ ΚΑΡΒΑΠΕΝΕΜΕΣ ΠΟΛΥΑΝΘΕΚΤΙΚΩΝ ΣΤΕΛΕΧΩΝ KLEBSIELLA PNEUMONIAE ΜΠΑΚΑΛΗ ΣΤΑΜΑΤΙΑ Ειδικευόμενη Ιατρικής Βιοπαθολογίας Αλεξανδρούπολη Ιούνιος 2014 Kingdom: Phylum: Class: Order:
Η ΣΗΜΑΣΙΑ ΤΗΣ ΕΠΙΤΗΡΗΣΗΣ ΤΗΣ ΚΑΤΑΝΑΛΩΣΗΣ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ ΟΥΣΙΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΑΚΟ ΧΩΡΟ
 Η ΣΗΜΑΣΙΑ ΤΗΣ ΕΠΙΤΗΡΗΣΗΣ ΤΗΣ ΚΑΤΑΝΑΛΩΣΗΣ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ ΟΥΣΙΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΑΚΟ ΧΩΡΟ ΜΑΡΚΟΓΙΑΝΝΑΚΗΣ ΑΝΤΩΝΙΟΣ BPharm, MPH, PhD ΝΟΣΟΚΟΜΕΙΑΚΟΣ ΦΑΡΜΑΚΟΠΟΙΟΣ ΔΙΕΥΘΥΝΤΗΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΤΜΗΜΑΤΟΣ ΓΝΑ «ΛΑΪΚΟ»
Η ΣΗΜΑΣΙΑ ΤΗΣ ΕΠΙΤΗΡΗΣΗΣ ΤΗΣ ΚΑΤΑΝΑΛΩΣΗΣ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ ΟΥΣΙΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΑΚΟ ΧΩΡΟ ΜΑΡΚΟΓΙΑΝΝΑΚΗΣ ΑΝΤΩΝΙΟΣ BPharm, MPH, PhD ΝΟΣΟΚΟΜΕΙΑΚΟΣ ΦΑΡΜΑΚΟΠΟΙΟΣ ΔΙΕΥΘΥΝΤΗΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΤΜΗΜΑΤΟΣ ΓΝΑ «ΛΑΪΚΟ»
Τι πρέπει να γνωρίζει ο κλινικός για τη σωστή ανάγνωση του αντιβιογράμματος. Γεώργος Λ. Δαΐκος Ομ. Καθηγητής Ιατρικής Σχολής ΕΚΠΑ
 Τι πρέπει να γνωρίζει ο κλινικός για τη σωστή ανάγνωση του αντιβιογράμματος Γεώργος Λ. Δαΐκος Ομ. Καθηγητής Ιατρικής Σχολής ΚΠ Minimal Inhibitory Concentration (MIC) vs. Minimal Bactericidal Concentration
Τι πρέπει να γνωρίζει ο κλινικός για τη σωστή ανάγνωση του αντιβιογράμματος Γεώργος Λ. Δαΐκος Ομ. Καθηγητής Ιατρικής Σχολής ΚΠ Minimal Inhibitory Concentration (MIC) vs. Minimal Bactericidal Concentration
ΔΕΙΚΤΗΣ ΣΥΜΜΟΡΦΩΣΗΣ ΣΤΙΣ ΠΡΟΦΥΛΑΞΕΙΣ ΕΠΑΦΗΣ
 ΔΕΙΚΤΗΣ ΣΥΜΜΟΡΦΩΣΗΣ ΣΤΙΣ ΠΡΟΦΥΛΑΞΕΙΣ ΕΠΑΦΗΣ Α. Σκοπός μέτρησης του δείκτη Ο δείκτης αυτός ανήκει στην κατηγορία των δεικτών επιτήρησης διαδικασιών (process indicator). Αποσκοπεί στην επιτήρηση της εφαρμογής
ΔΕΙΚΤΗΣ ΣΥΜΜΟΡΦΩΣΗΣ ΣΤΙΣ ΠΡΟΦΥΛΑΞΕΙΣ ΕΠΑΦΗΣ Α. Σκοπός μέτρησης του δείκτη Ο δείκτης αυτός ανήκει στην κατηγορία των δεικτών επιτήρησης διαδικασιών (process indicator). Αποσκοπεί στην επιτήρηση της εφαρμογής
ΣΧΕΔΙΟ ΔΡΑΣΗΣ ΓΙΑ ΤΟΝ ΕΛΕΓΧΟ ΤΗΣ ΔΙΑΣΠΟΡΑΣ ΤΩΝ ΠΟΛΥΑΝΘΕΚΤΙΚΩΝ ΜΙΚΡΟΟΡΓΑΝΙΣΜΩΝ ΣΤΑ ΕΛΛΗΝΙΚΑ ΝΟΣΟΚΟΜΕΙΑ
 ΣΧΕΔΙΟ ΔΡΑΣΗΣ ΓΙΑ ΤΟΝ ΕΛΕΓΧΟ ΤΗΣ ΔΙΑΣΠΟΡΑΣ ΤΩΝ ΠΟΛΥΑΝΘΕΚΤΙΚΩΝ ΜΙΚΡΟΟΡΓΑΝΙΣΜΩΝ ΣΤΑ ΕΛΛΗΝΙΚΑ ΝΟΣΟΚΟΜΕΙΑ ΠΡΟΚΡΟΥΣΤΗΣ Φλώρα Κοντοπίδου Παθολόγος- Λοιμωξιολόγος (Phd) Υπεύθυνη Γραφείου Μικροβιακής Αντοχής ΚΕΕΛΠΝΟ
ΣΧΕΔΙΟ ΔΡΑΣΗΣ ΓΙΑ ΤΟΝ ΕΛΕΓΧΟ ΤΗΣ ΔΙΑΣΠΟΡΑΣ ΤΩΝ ΠΟΛΥΑΝΘΕΚΤΙΚΩΝ ΜΙΚΡΟΟΡΓΑΝΙΣΜΩΝ ΣΤΑ ΕΛΛΗΝΙΚΑ ΝΟΣΟΚΟΜΕΙΑ ΠΡΟΚΡΟΥΣΤΗΣ Φλώρα Κοντοπίδου Παθολόγος- Λοιμωξιολόγος (Phd) Υπεύθυνη Γραφείου Μικροβιακής Αντοχής ΚΕΕΛΠΝΟ
Νοσοκομειακή πνευμονία(hap)
 Νοσοκομειακή πνευμονία(hap) Περιγραφή περίπτωσης Άνδρας 78 ετών, νοσηλεύεται στην παθολογική κλινική από 3ημέρου για ΑΕΕ ισχαιμικού τύπου με δεξιά ημιπάρεση και δυσαρθρία. Από το ατομικό αναμνηστικό, πάσχει
Νοσοκομειακή πνευμονία(hap) Περιγραφή περίπτωσης Άνδρας 78 ετών, νοσηλεύεται στην παθολογική κλινική από 3ημέρου για ΑΕΕ ισχαιμικού τύπου με δεξιά ημιπάρεση και δυσαρθρία. Από το ατομικό αναμνηστικό, πάσχει
Γενικοί μηχανισμοί αντοχής βακτηρίων στα αντιβιοτικά
 Γενικοί μηχανισμοί αντοχής βακτηρίων στα αντιβιοτικά Αλκιβιάδης Βατόπουλος Εθνική Σχολή Δημόσιας Υγείας 1 Μικροβιακή Αντοχή Βασικοί ορισμοί Δραστικότητα αντιβιοτικού Αντοχή Μικροοργανισμού Μικροβιολογική
Γενικοί μηχανισμοί αντοχής βακτηρίων στα αντιβιοτικά Αλκιβιάδης Βατόπουλος Εθνική Σχολή Δημόσιας Υγείας 1 Μικροβιακή Αντοχή Βασικοί ορισμοί Δραστικότητα αντιβιοτικού Αντοχή Μικροοργανισμού Μικροβιολογική
20/11/2013. Παλαιότερα αντιβιοτικά για πολυανθεκτικά Gram αρνητικά βακτήρια. Παλαιότερα αντιβιοτικά για πολυανθεκτικά. Πολυανθεκτικά Gram( ) βακτήρια
 Παλαιότερα αντιβιοτικά για πολυανθεκτικά Gram αρνητικά βακτήρια Αθανάσιος Γ. Μίχος Eπίκουρος Καθηγητής Παιδιατρικής Λοιμωξιολογίας Α Παιδιατρική Κλινική Πανεπιστημίου Αθηνών Παλαιότερα αντιβιοτικά για
Παλαιότερα αντιβιοτικά για πολυανθεκτικά Gram αρνητικά βακτήρια Αθανάσιος Γ. Μίχος Eπίκουρος Καθηγητής Παιδιατρικής Λοιμωξιολογίας Α Παιδιατρική Κλινική Πανεπιστημίου Αθηνών Παλαιότερα αντιβιοτικά για
«Εθνική Επιτροπή Αντιβιογράμματος και Ορίων Ευαισθησίας στα Αντιβιοτικά»
 Ελληνική Μικροβιολογική Εταιρεία «Εθνική Επιτροπή Αντιβιογράμματος και Ορίων Ευαισθησίας στα Αντιβιοτικά» Προτάσεις για όρια Ευαισθησίας στις Καρμπαπενέμες. Θεραπευτικές Οδηγίες Πρόταση Απόφαση: Με βάση
Ελληνική Μικροβιολογική Εταιρεία «Εθνική Επιτροπή Αντιβιογράμματος και Ορίων Ευαισθησίας στα Αντιβιοτικά» Προτάσεις για όρια Ευαισθησίας στις Καρμπαπενέμες. Θεραπευτικές Οδηγίες Πρόταση Απόφαση: Με βάση
Φλώρα Κοντοπίδου Παθολόγος-Λοιμωξιολόγος (Phd) Υπεύθυνη Γραφείου Μικροβιακής Αντοχής ΚΕΕΛΠΝΟ
 Φλώρα Κοντοπίδου Παθολόγος-Λοιμωξιολόγος (Phd) Υπεύθυνη Γραφείου Μικροβιακής Αντοχής ΚΕΕΛΠΝΟ ΗΠΑ SENIC 1975-1985 Βασικά στοιχεία προγράμματος 1. Επιδημιολογική επιτήρηση- feedback 2. Εφαρμογή συγκεκριμένων
Φλώρα Κοντοπίδου Παθολόγος-Λοιμωξιολόγος (Phd) Υπεύθυνη Γραφείου Μικροβιακής Αντοχής ΚΕΕΛΠΝΟ ΗΠΑ SENIC 1975-1985 Βασικά στοιχεία προγράμματος 1. Επιδημιολογική επιτήρηση- feedback 2. Εφαρμογή συγκεκριμένων
Καρβαπενεμάσες τάξης Α - Ταξινόμηση
 Καρβαπενεμάσες τάξης Α - Ταξινόμηση Χρωμοσωματικές SME NMC/ΙΜΙ Πλασμιδιακές KPC!!! GES SFC-1 SHV-38 Οι χρωμοσωματικές πρωτοεμφανίστηκαν στις αρχές της δεκαετίας του 80, πριν την κλινική χρήση της ιμιπενέμης
Καρβαπενεμάσες τάξης Α - Ταξινόμηση Χρωμοσωματικές SME NMC/ΙΜΙ Πλασμιδιακές KPC!!! GES SFC-1 SHV-38 Οι χρωμοσωματικές πρωτοεμφανίστηκαν στις αρχές της δεκαετίας του 80, πριν την κλινική χρήση της ιμιπενέμης
Επιδημιολογία Λοιμώξεων Βασικά στοιχεία. Ιωσήφ Παπαπαρασκευάς Εργαστήριο Μικροβιολογίας Ιατρική Σχολή ΕΚΠΑ
 Επιδημιολογία Λοιμώξεων Βασικά στοιχεία Ιωσήφ Παπαπαρασκευάς Εργαστήριο Μικροβιολογίας Ιατρική Σχολή ΕΚΠΑ Επιδημία είναι κάθε κατάσταση στην οποία παρατηρείται αυξημένη συχνότητα (επίπτωση) ενός νοσήματος
Επιδημιολογία Λοιμώξεων Βασικά στοιχεία Ιωσήφ Παπαπαρασκευάς Εργαστήριο Μικροβιολογίας Ιατρική Σχολή ΕΚΠΑ Επιδημία είναι κάθε κατάσταση στην οποία παρατηρείται αυξημένη συχνότητα (επίπτωση) ενός νοσήματος
Μικροβιακή Αντοχή Η ικανότητα των βακτηρίων να παραµένουν ζωντανά µετά από χορήγηση κατάλληλου αντιβιοτικού σε συγκέντρωση που κανονικά θα έπρεπε να τ
 PART VΙ.. Μικροβιακή Αντοχή Η ικανότητα των βακτηρίων να παραµένουν ζωντανά µετά από χορήγηση κατάλληλου αντιβιοτικού σε συγκέντρωση που κανονικά θα έπρεπε να το έχει σκοτώσει!! Μικροβιακή Αντοχή Η ικανότητα
PART VΙ.. Μικροβιακή Αντοχή Η ικανότητα των βακτηρίων να παραµένουν ζωντανά µετά από χορήγηση κατάλληλου αντιβιοτικού σε συγκέντρωση που κανονικά θα έπρεπε να το έχει σκοτώσει!! Μικροβιακή Αντοχή Η ικανότητα
Νεότερα αντιβιοτικά για Gram-αρνητικά βακτήρια. Χαράλαμπος Ανταχόπουλος 3 η Παιδιατρική Κλινική ΑΠΘ
 Νεότερα αντιβιοτικά για Gram-αρνητικά βακτήρια Χαράλαμπος Ανταχόπουλος 3 η Παιδιατρική Κλινική ΑΠΘ 1 2 3 4 Υπάρχοντα αντιβιοτικά έναντι ανθεκτικών στις καρβαπενέμες Gram (-) Αμινογλυκοσίδες: τοξικότητα,
Νεότερα αντιβιοτικά για Gram-αρνητικά βακτήρια Χαράλαμπος Ανταχόπουλος 3 η Παιδιατρική Κλινική ΑΠΘ 1 2 3 4 Υπάρχοντα αντιβιοτικά έναντι ανθεκτικών στις καρβαπενέμες Gram (-) Αμινογλυκοσίδες: τοξικότητα,
«ΠΡΟΚΡΟΥΣΤΗΣ» για τη λήψη άμεσων μέτρων
 ΕΝΔΟΝΟΣΟΚΟΜΟΚΕΙΑΚΕΣ ΛΟΙΜΩΞΕΙΣ ΑΠΟ ΠΟΛΥΑΝΘΕΚΤΙΚΑ Gram ΑΡΝΗΤΙΚΑ ΠΑΘΟΓΟΝΑ: για τη λήψη άμεσων μέτρων Χρ. Παπανικολάου Διοικητής Β Υ.Π.Ε Πειραιά κ Αιγαίου Βιοπαθολόγος Πειραιάς 19-10-2010 ΓΕΝΙΚΕΣ ΠΑΡΑΔΟΧΕΣ
ΕΝΔΟΝΟΣΟΚΟΜΟΚΕΙΑΚΕΣ ΛΟΙΜΩΞΕΙΣ ΑΠΟ ΠΟΛΥΑΝΘΕΚΤΙΚΑ Gram ΑΡΝΗΤΙΚΑ ΠΑΘΟΓΟΝΑ: για τη λήψη άμεσων μέτρων Χρ. Παπανικολάου Διοικητής Β Υ.Π.Ε Πειραιά κ Αιγαίου Βιοπαθολόγος Πειραιάς 19-10-2010 ΓΕΝΙΚΕΣ ΠΑΡΑΔΟΧΕΣ
ΠΝΕΥΜΟΝΙΕΣ. Αικατερίνη Κ. Μασγάλα. Επιμελήτρια Α Α Παθολογικής Κλινικής
 ΠΝΕΥΜΟΝΙΕΣ Αικατερίνη Κ. Μασγάλα Επιμελήτρια Α Α Παθολογικής Κλινικής Ορισμοί Πνευμονία της κοινότητας: Λοίμωξη του πνευμονικού παρεγχύματος που αποκτήθηκε στην κοινότητα. Ενδονοσοκομειακή πνευμονία: Η
ΠΝΕΥΜΟΝΙΕΣ Αικατερίνη Κ. Μασγάλα Επιμελήτρια Α Α Παθολογικής Κλινικής Ορισμοί Πνευμονία της κοινότητας: Λοίμωξη του πνευμονικού παρεγχύματος που αποκτήθηκε στην κοινότητα. Ενδονοσοκομειακή πνευμονία: Η
ΑΞΙΟΛΟΓΗΣΗ ΤΟΥ RAPID POLYMYXIN NP TEST ΣΤΗΝ ΑΝΙΧΝΕΥΣΗ COLISTIN ΑΝΘΕΚΤΙΚΩΝ (ColR) KLEBSIELLA PNEUMONIAE
 ΑΞΙΟΛΟΓΗΣΗ ΤΟΥ RAPID POLYMYXIN NP TEST ΣΤΗΝ ΑΝΙΧΝΕΥΣΗ COLISTIN ΑΝΘΕΚΤΙΚΩΝ (ColR) KLEBSIELLA PNEUMONIAE Ε.Μάλλη 1, Ι.Βουλγαρίδη 1, Κ.Τσιλιπουνιδάκη 1, Ζ.Φλώρου 1, Α.Στέφος 3, Σ.Ξύτσας 1, Π.Πυρίδου 1, Κ.Παπαγιαννίτσης
ΑΞΙΟΛΟΓΗΣΗ ΤΟΥ RAPID POLYMYXIN NP TEST ΣΤΗΝ ΑΝΙΧΝΕΥΣΗ COLISTIN ΑΝΘΕΚΤΙΚΩΝ (ColR) KLEBSIELLA PNEUMONIAE Ε.Μάλλη 1, Ι.Βουλγαρίδη 1, Κ.Τσιλιπουνιδάκη 1, Ζ.Φλώρου 1, Α.Στέφος 3, Σ.Ξύτσας 1, Π.Πυρίδου 1, Κ.Παπαγιαννίτσης
AMS-Net ΕΚΠΑΙΔΕΥΤΙΚΑ ΣΕΜΙΝΑΡΙΑ ΓΙΑ ΤΗΝ ΕΠΙΜΕΛΗΤΕΙΑ ΤΗΣ ΧΡΗΣΗΣ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΑΚΟ ΧΩΡΟ
 AMS-Net ΕΚΠΑΙΔΕΥΤΙΚΑ ΣΕΜΙΝΑΡΙΑ ΓΙΑ ΤΗΝ ΕΠΙΜΕΛΗΤΕΙΑ ΤΗΣ ΧΡΗΣΗΣ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΑΚΟ ΧΩΡΟ ΜΕΡΟΣ 1 ο ΝΟΜΟΘΕΤΙΚΟ ΠΛΑΙΣΙΟ ΔΙΑΔΙΑΚΑΣΙΕΣ ΑΛΓΟΡΙΘΜΟΙ Γραφείο Νοσοκομειακών Λοιμώξεων και
AMS-Net ΕΚΠΑΙΔΕΥΤΙΚΑ ΣΕΜΙΝΑΡΙΑ ΓΙΑ ΤΗΝ ΕΠΙΜΕΛΗΤΕΙΑ ΤΗΣ ΧΡΗΣΗΣ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΑΚΟ ΧΩΡΟ ΜΕΡΟΣ 1 ο ΝΟΜΟΘΕΤΙΚΟ ΠΛΑΙΣΙΟ ΔΙΑΔΙΑΚΑΣΙΕΣ ΑΛΓΟΡΙΘΜΟΙ Γραφείο Νοσοκομειακών Λοιμώξεων και
Μηχανισμοί Αντοχής των Gram-θετικών και Gramαρνητικών. στα β-λακταμικά αντιβιοτικά
 Μηχανισμοί Αντοχής των Gram-θετικών και Gramαρνητικών βακτηρίων στα β-λακταμικά αντιβιοτικά Ευαγγελία Λεμπέση Διευθύντρια ΕΣΥ Μικροβιολογικό Εργαστήριο Ν. Παίδων Αθηνών Π. & Α. Κυριακού Πρόγραμμα Μετεκπαιδευτικών
Μηχανισμοί Αντοχής των Gram-θετικών και Gramαρνητικών βακτηρίων στα β-λακταμικά αντιβιοτικά Ευαγγελία Λεμπέση Διευθύντρια ΕΣΥ Μικροβιολογικό Εργαστήριο Ν. Παίδων Αθηνών Π. & Α. Κυριακού Πρόγραμμα Μετεκπαιδευτικών
Μικροβιακή αντοχή και τρόποι πρόληψης. Ιωσηφίδης Ηλίας Εξειδικευόμενος λοιμωξιολογίας Γ Παιδιατρική Ιπποκράτειο Νοσοκομείο Θεσσαλονίκης
 Μικροβιακή αντοχή και τρόποι πρόληψης Ιωσηφίδης Ηλίας Εξειδικευόμενος λοιμωξιολογίας Γ Παιδιατρική Ιπποκράτειο Νοσοκομείο Θεσσαλονίκης Αντοχή: πού βρισκόμαστε σήμερα Νεαρός ασθενής εμφανίζει επίμονη μικροβιακή
Μικροβιακή αντοχή και τρόποι πρόληψης Ιωσηφίδης Ηλίας Εξειδικευόμενος λοιμωξιολογίας Γ Παιδιατρική Ιπποκράτειο Νοσοκομείο Θεσσαλονίκης Αντοχή: πού βρισκόμαστε σήμερα Νεαρός ασθενής εμφανίζει επίμονη μικροβιακή
Αντιμετώπιση οξείας ουρολοίμωξης. Δέσποινα Τράμμα Επίκουρη Καθηγήτρια Παιδιατρικής- Παιδιατρικής Νεφρολογίας Δ Παιδιατρική Κλινική ΑΠΘ
 Αντιμετώπιση οξείας ουρολοίμωξης Δέσποινα Τράμμα Επίκουρη Καθηγήτρια Παιδιατρικής- Παιδιατρικής Νεφρολογίας Δ Παιδιατρική Κλινική ΑΠΘ Θεραπεία Στόχοι : Περιορισμός της οξείας λοίμωξης Πρόληψη άμεσων επιπλοκών
Αντιμετώπιση οξείας ουρολοίμωξης Δέσποινα Τράμμα Επίκουρη Καθηγήτρια Παιδιατρικής- Παιδιατρικής Νεφρολογίας Δ Παιδιατρική Κλινική ΑΠΘ Θεραπεία Στόχοι : Περιορισμός της οξείας λοίμωξης Πρόληψη άμεσων επιπλοκών
Ελληνική Εταιρεία Χημειοθεραπείας
 20 Η ΗΜΡΙΔΑ ΓΙΑ ΤΗΝ ΟΡΘΟΛΟΓΙΚΗ ΧΡΗΣΗ ΤΩΝ ΑΝΤΙΒΙΟΤΙΚΩΝ ΑΠΟ ΤΟΝ ΝΟΣΟΚΟΜΙΑΚΟ ΙΑΤΡΟ ΟΛΥΜΠΙΑ- 21 Οκτωβρίου 2017 H ερμηνεία του αντιβιογράμματος από τον νοσοκομειακό Ιατρό λληνική ταιρεία Χημειοθεραπείας Αθηνά
20 Η ΗΜΡΙΔΑ ΓΙΑ ΤΗΝ ΟΡΘΟΛΟΓΙΚΗ ΧΡΗΣΗ ΤΩΝ ΑΝΤΙΒΙΟΤΙΚΩΝ ΑΠΟ ΤΟΝ ΝΟΣΟΚΟΜΙΑΚΟ ΙΑΤΡΟ ΟΛΥΜΠΙΑ- 21 Οκτωβρίου 2017 H ερμηνεία του αντιβιογράμματος από τον νοσοκομειακό Ιατρό λληνική ταιρεία Χημειοθεραπείας Αθηνά
Πρόγραμμα Παρακολούθησης της Αντοχής στις Αντιμικροβιακές Ουσίες Ζωονοσογόνων & Συμβιωτικών Βακτηρίων του ΥΠΑΑΤ, για τα έτη
 Πρόγραμμα Παρακολούθησης της Αντοχής στις Αντιμικροβιακές Ουσίες Ζωονοσογόνων & Συμβιωτικών Βακτηρίων του ΥΠΑΑΤ, για τα έτη -2015 Ελένη Βαλκάνου Κτηνίατρος Κτηνιατρικό Εργαστήριο Χαλκίδας ΥΠΑΑΤ Νομικό
Πρόγραμμα Παρακολούθησης της Αντοχής στις Αντιμικροβιακές Ουσίες Ζωονοσογόνων & Συμβιωτικών Βακτηρίων του ΥΠΑΑΤ, για τα έτη -2015 Ελένη Βαλκάνου Κτηνίατρος Κτηνιατρικό Εργαστήριο Χαλκίδας ΥΠΑΑΤ Νομικό
Αντιβιοτικά Αρχές αντιμικροβιακής θεραπείας. Χ. Ανταχόπουλος
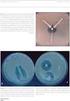 Αντιβιοτικά Αρχές αντιμικροβιακής θεραπείας Χ. Ανταχόπουλος Εμπειρική αντιμικροβιακή εξωνοσοκομειακή θεραπεία για εμπύρετη πνευμονία της κοινότητας σε υγιή, μη καπνιστή, άνδρα 45 ετών που δεν έχει πάρει
Αντιβιοτικά Αρχές αντιμικροβιακής θεραπείας Χ. Ανταχόπουλος Εμπειρική αντιμικροβιακή εξωνοσοκομειακή θεραπεία για εμπύρετη πνευμονία της κοινότητας σε υγιή, μη καπνιστή, άνδρα 45 ετών που δεν έχει πάρει
Η συμβολή του μικροβιολογικού εργαστηρίου στον έλεγχο των νοσοκομειακών λοιμώξεων. Παναγέα Θεοφανώ Βιοπαθολόγος Λέκτορας ΕΚΠΑ
 Η συμβολή του μικροβιολογικού εργαστηρίου στον έλεγχο των νοσοκομειακών λοιμώξεων Παναγέα Θεοφανώ Βιοπαθολόγος Λέκτορας ΕΚΠΑ Ορισμός νοσοκομειακών λοιμώξεων Οι λοιμώξεις που εκδηλώνονται 48h μετά την εισαγωγή
Η συμβολή του μικροβιολογικού εργαστηρίου στον έλεγχο των νοσοκομειακών λοιμώξεων Παναγέα Θεοφανώ Βιοπαθολόγος Λέκτορας ΕΚΠΑ Ορισμός νοσοκομειακών λοιμώξεων Οι λοιμώξεις που εκδηλώνονται 48h μετά την εισαγωγή
Αντιβιοτικά Αρχές αντιμικροβιακής θεραπείας. Χ. Ανταχόπουλος 3 η Παιδιατρική Κλινική ΑΠΘ
 Αντιβιοτικά Αρχές αντιμικροβιακής θεραπείας Χ. Ανταχόπουλος 3 η Παιδιατρική Κλινική ΑΠΘ Εμπειρική αντιμικροβιακή εξωνοσοκομειακή θεραπεία για εμπύρετη πνευμονία της κοινότητας σε υγιή άνδρα 45 ετών που
Αντιβιοτικά Αρχές αντιμικροβιακής θεραπείας Χ. Ανταχόπουλος 3 η Παιδιατρική Κλινική ΑΠΘ Εμπειρική αντιμικροβιακή εξωνοσοκομειακή θεραπεία για εμπύρετη πνευμονία της κοινότητας σε υγιή άνδρα 45 ετών που
ΑΝΤΙΜΙΚΡΟΒΙΑΚΗ ΘΕΡΑΠΕΙΑ ΣΤΙΣ ΛΟΙΜΩΞΕΙΣ ΤΗΣ ΟΡΘΟΠΑΙΔΙΚΗΣ
 ΑΝΤΙΜΙΚΡΟΒΙΑΚΗ ΘΕΡΑΠΕΙΑ ΣΤΙΣ ΛΟΙΜΩΞΕΙΣ ΤΗΣ ΟΡΘΟΠΑΙΔΙΚΗΣ Ιωάννης Π.Κιουμής Αναπληρωτής Καθηγητής Α.Π.Θ. Για την καλύτερη κατανόηση της δέουσας αντιμικροβιακής θεραπείας στις λοιμώξεις της Ορθοπαιδικής ουσιαστική
ΑΝΤΙΜΙΚΡΟΒΙΑΚΗ ΘΕΡΑΠΕΙΑ ΣΤΙΣ ΛΟΙΜΩΞΕΙΣ ΤΗΣ ΟΡΘΟΠΑΙΔΙΚΗΣ Ιωάννης Π.Κιουμής Αναπληρωτής Καθηγητής Α.Π.Θ. Για την καλύτερη κατανόηση της δέουσας αντιμικροβιακής θεραπείας στις λοιμώξεις της Ορθοπαιδικής ουσιαστική
ΚΟΚΚΙΝΗΣ ΦΟΙΒΟΣ ΠΑΝΑΓΙΩΤΗΣ ΕΠΙΜΕΛΗΤΗΣ Β. ΠΝΕΥΜΟΝΟΛΟΓΟΣ ΦΥΜΑΤΙΟΛΟΓΟΣ ΠΝΕΥΜΟΝΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΓΝΝ ΛΑΜΙΑΣ
 ΕΝΔΟΝΟΣΟΚΟΜΕΙΑΚΕΣ ΛΟΙΜΩΞΕΙΣ ΣΤΟΝ ΧΡΟΝΙΟ ΑΠΟΦΡΑΚΤΙΚΟ ΠΝΕΥΜΟΝΟΠΑΘΗ ΑΣΘΕΝΗ ΚΟΚΚΙΝΗΣ ΦΟΙΒΟΣ ΠΑΝΑΓΙΩΤΗΣ ΕΠΙΜΕΛΗΤΗΣ Β. ΠΝΕΥΜΟΝΟΛΟΓΟΣ ΦΥΜΑΤΙΟΛΟΓΟΣ ΠΝΕΥΜΟΝΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΓΝΝ ΛΑΜΙΑΣ ΠΑΡΑΓΟΝΤΕΣ ΚΙΝΔΥΝΟΥ ΓΙΑ ΠΟΛΥΑΝΘΕΚΤΙΚΑ
ΕΝΔΟΝΟΣΟΚΟΜΕΙΑΚΕΣ ΛΟΙΜΩΞΕΙΣ ΣΤΟΝ ΧΡΟΝΙΟ ΑΠΟΦΡΑΚΤΙΚΟ ΠΝΕΥΜΟΝΟΠΑΘΗ ΑΣΘΕΝΗ ΚΟΚΚΙΝΗΣ ΦΟΙΒΟΣ ΠΑΝΑΓΙΩΤΗΣ ΕΠΙΜΕΛΗΤΗΣ Β. ΠΝΕΥΜΟΝΟΛΟΓΟΣ ΦΥΜΑΤΙΟΛΟΓΟΣ ΠΝΕΥΜΟΝΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΓΝΝ ΛΑΜΙΑΣ ΠΑΡΑΓΟΝΤΕΣ ΚΙΝΔΥΝΟΥ ΓΙΑ ΠΟΛΥΑΝΘΕΚΤΙΚΑ
ΜΕΤΕΓΧΕΙΡΗΤΙΚΗ ΝΟΣΟΚΟΜΕΙΑΚΗ ΜΗΝΙΓΓΙΤΙΔΑ
 ΕΚΠΑΙΔΕΥΤΙΚΑ ΣΕΜΙΝΑΡΙΑ ΣΥΝΔΕΣΜΩΝ ΕΠΙΤΡΟΠΩΝ ΛΟΙΜΩΞΕΩΝ ΓΙΑ ΤΗΝ ΧΡΗΣΗ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΑΚΟ ΧΩΡΟ Τιτλος ΜΕΤΕΓΧΕΙΡΗΤΙΚΗ ΝΟΣΟΚΟΜΕΙΑΚΗ ΜΗΝΙΓΓΙΤΙΔΑ 20/2/2018 AMS.net ΕΚΠΑΙΔΕΥΣΗ ΣΥΝΔΕΣΜΩΝ
ΕΚΠΑΙΔΕΥΤΙΚΑ ΣΕΜΙΝΑΡΙΑ ΣΥΝΔΕΣΜΩΝ ΕΠΙΤΡΟΠΩΝ ΛΟΙΜΩΞΕΩΝ ΓΙΑ ΤΗΝ ΧΡΗΣΗ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΑΚΟ ΧΩΡΟ Τιτλος ΜΕΤΕΓΧΕΙΡΗΤΙΚΗ ΝΟΣΟΚΟΜΕΙΑΚΗ ΜΗΝΙΓΓΙΤΙΔΑ 20/2/2018 AMS.net ΕΚΠΑΙΔΕΥΣΗ ΣΥΝΔΕΣΜΩΝ
Αντιβιοτικά- Χρήση και κατάχρηση
 Αντιβιοτικά- Χρήση και κατάχρηση Παιδί 4 χρόνων Πυρετό για 24 ώρες Εξέταση από παιδίατρο λαιμός-αυτιά λ ίγο κόκκινα cefuroxime Δ ρ Μαρκέλλα Μάρκου Ειδική Μικροβιολόγος-Λοιμωξιολόγος Παιδί 4 χρόνων Πυρετό
Αντιβιοτικά- Χρήση και κατάχρηση Παιδί 4 χρόνων Πυρετό για 24 ώρες Εξέταση από παιδίατρο λαιμός-αυτιά λ ίγο κόκκινα cefuroxime Δ ρ Μαρκέλλα Μάρκου Ειδική Μικροβιολόγος-Λοιμωξιολόγος Παιδί 4 χρόνων Πυρετό
ΚΟΝΤΟΥ ΠΑΣΧΑΛΙΝΑ ΠΝΕΥΜΟΝΟΛΟΓΟΣ ΕΝΤΑΤΙΚΟΛΟΓΟΣ ΕΠΙΜΕΛΗΤΡΙΑ Β Α ΜΕΘ «Γ. ΠΑΠΑΝΙΚΟΛΑΟΥ»
 ΚΟΝΤΟΥ ΠΑΣΧΑΛΙΝΑ ΠΝΕΥΜΟΝΟΛΟΓΟΣ ΕΝΤΑΤΙΚΟΛΟΓΟΣ ΕΠΙΜΕΛΗΤΡΙΑ Β Α ΜΕΘ «Γ. ΠΑΠΑΝΙΚΟΛΑΟΥ» Am J Respir Crit Care Med 2005 Ενδονοσοκομειακή πνευμονία (HAP): ηπνευμονία που εκδηλώνεται σε >48 ώρες από την εισαγωγή
ΚΟΝΤΟΥ ΠΑΣΧΑΛΙΝΑ ΠΝΕΥΜΟΝΟΛΟΓΟΣ ΕΝΤΑΤΙΚΟΛΟΓΟΣ ΕΠΙΜΕΛΗΤΡΙΑ Β Α ΜΕΘ «Γ. ΠΑΠΑΝΙΚΟΛΑΟΥ» Am J Respir Crit Care Med 2005 Ενδονοσοκομειακή πνευμονία (HAP): ηπνευμονία που εκδηλώνεται σε >48 ώρες από την εισαγωγή
ΟΡΘΟΛΟΓΙΚΗ ΕΠΙΛΟΓΗ ΑΝΤΙΒΙΟΤΙΚΩΝ ΓΙΑ ΤΗΝ ΘΕΡΑΠΕΙΑ ΤΩΝ ΟΥΡΟΛΟΙΜΩΞΕΩΝ
 ΟΡΘΟΛΟΓΙΚΗ ΕΠΙΛΟΓΗ ΑΝΤΙΒΙΟΤΙΚΩΝ ΓΙΑ ΤΗΝ ΘΕΡΑΠΕΙΑ ΤΩΝ ΟΥΡΟΛΟΙΜΩΞΕΩΝ Μαρία Σουλή Επ. Καθηγήτρια Παθολογίας-Λοιμώξεων Πανεπιστημιακό Γενικό Νοσοκομείο ΑΤΤΙΚΟΝ Γυναίκα 25 ετών προσέρχεται λόγω δυσουρίας και
ΟΡΘΟΛΟΓΙΚΗ ΕΠΙΛΟΓΗ ΑΝΤΙΒΙΟΤΙΚΩΝ ΓΙΑ ΤΗΝ ΘΕΡΑΠΕΙΑ ΤΩΝ ΟΥΡΟΛΟΙΜΩΞΕΩΝ Μαρία Σουλή Επ. Καθηγήτρια Παθολογίας-Λοιμώξεων Πανεπιστημιακό Γενικό Νοσοκομείο ΑΤΤΙΚΟΝ Γυναίκα 25 ετών προσέρχεται λόγω δυσουρίας και
«Η Ορθολογική Χρήση των Αντιβιοτικών από το Νοσοκομειακό Ιατρό» Ελληνική Εταιρεία Χημειοθεραπείας. Καρβαπενέμες. Ελένη Γιαμαρέλλου 31/3/2018
 «Η Ορθολογική Χρήση των Αντιβιοτικών από το Νοσοκομειακό Ιατρό» Καρβαπενέμες Ελένη Γιαμαρέλλου 31/3/2018 β-λακτάμες Πενικιλλίνες Ιμιπεμένη/ σιλαστατίνη Κεφαλοσπορίνες Μεροπενέμη Καρβαπενέμες Ερταπενέμη
«Η Ορθολογική Χρήση των Αντιβιοτικών από το Νοσοκομειακό Ιατρό» Καρβαπενέμες Ελένη Γιαμαρέλλου 31/3/2018 β-λακτάμες Πενικιλλίνες Ιμιπεμένη/ σιλαστατίνη Κεφαλοσπορίνες Μεροπενέμη Καρβαπενέμες Ερταπενέμη
ΑΝΤΙΒΙΟΤΙΚΑ ΟΡΘΗ ΧΡΗΣΗ ΑΝΤΙΒΙΟΤΙΚΩΝ
 ΑΝΤΙΒΙΟΤΙΚΑ ΟΡΘΗ ΧΡΗΣΗ ΑΝΤΙΒΙΟΤΙΚΩΝ Διονυσία Κουτραφούρη Ειδικ. Παθολόγος, Γ.Ν.Θ.Π. «Η Παμμακάριστος» Τα αντιβιοτικά είναι φυσικά παράγωγα μικροοργανισμών και δρουν εναντίον άλλων μικροοργανισμών (αντιβιοτικά).
ΑΝΤΙΒΙΟΤΙΚΑ ΟΡΘΗ ΧΡΗΣΗ ΑΝΤΙΒΙΟΤΙΚΩΝ Διονυσία Κουτραφούρη Ειδικ. Παθολόγος, Γ.Ν.Θ.Π. «Η Παμμακάριστος» Τα αντιβιοτικά είναι φυσικά παράγωγα μικροοργανισμών και δρουν εναντίον άλλων μικροοργανισμών (αντιβιοτικά).
ΟΙ ΠΡΩΤΕΣ ΕΜΠΕΙΡΙΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΚΑΛΛΙΕΡΓΕΙΩΝ ΤΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΛΑΜΙΑΣ
 ΟΙ ΠΡΩΤΕΣ ΕΜΠΕΙΡΙΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΚΑΛΛΙΕΡΓΕΙΩΝ ΤΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΛΑΜΙΑΣ Τούμπα Ίλντικο, Ζούνη Παναγιώτα 3, Δημοπούλου Ειρήνη 4, Λεμονή Αλεξάνδρα 4, Χριστοπούλου Ανδρονίκη 5, Μπακόλα Δήμητρα Δντρια Βιοπαθολόγος,
ΟΙ ΠΡΩΤΕΣ ΕΜΠΕΙΡΙΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΚΑΛΛΙΕΡΓΕΙΩΝ ΤΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΛΑΜΙΑΣ Τούμπα Ίλντικο, Ζούνη Παναγιώτα 3, Δημοπούλου Ειρήνη 4, Λεμονή Αλεξάνδρα 4, Χριστοπούλου Ανδρονίκη 5, Μπακόλα Δήμητρα Δντρια Βιοπαθολόγος,
Θεραπευτικές εξελίξεις στις λοιμώξεις. Ε. Κωστής 2018
 Θεραπευτικές εξελίξεις στις λοιμώξεις Ε. Κωστής 2018 Βακτηριδιακές λοιμώξεις Ένα νέο αντιβιοτικό η λεφαμουλίνη(lefamulin), μια πλευρομουτιλίνη, δρα στο επίπεδο του ριβοσώματος, αναστέλλοντας έτσι την παραγωγή
Θεραπευτικές εξελίξεις στις λοιμώξεις Ε. Κωστής 2018 Βακτηριδιακές λοιμώξεις Ένα νέο αντιβιοτικό η λεφαμουλίνη(lefamulin), μια πλευρομουτιλίνη, δρα στο επίπεδο του ριβοσώματος, αναστέλλοντας έτσι την παραγωγή
Αντιμικροβιακά Χαρακτηριστικά
 ΚΕΦΑΛΟΣΠΟΡΙΝΕΣ Αντιμικροβιακά Χαρακτηριστικά Εξαιρετικά υψηλή ενδογενής δραστικότητα έναντι των εντεροβακτηριακών: Δεν είναι εξ ορισμού δραστικές: - στους εντεροκόκκους - στους MRSA και MRSE - στα αναερόβια
ΚΕΦΑΛΟΣΠΟΡΙΝΕΣ Αντιμικροβιακά Χαρακτηριστικά Εξαιρετικά υψηλή ενδογενής δραστικότητα έναντι των εντεροβακτηριακών: Δεν είναι εξ ορισμού δραστικές: - στους εντεροκόκκους - στους MRSA και MRSE - στα αναερόβια
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ. ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «Ιατρική Ερευνητική Μεθοδολογία» ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «Ιατρική Ερευνητική Μεθοδολογία» ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ ΕΠΙΔΗΜΙΟΛΟΓΙΚΗ ΕΠΙΤΗΡΗΣΗ ΛΟΙΜΩΞΕΩΝ ΑΠΟ ΠΟΛΥΑΝΘΕΚΤΙΚΑ GRAM-ΑΡΝΗΤΙΚΑ
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «Ιατρική Ερευνητική Μεθοδολογία» ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ ΕΠΙΔΗΜΙΟΛΟΓΙΚΗ ΕΠΙΤΗΡΗΣΗ ΛΟΙΜΩΞΕΩΝ ΑΠΟ ΠΟΛΥΑΝΘΕΚΤΙΚΑ GRAM-ΑΡΝΗΤΙΚΑ
Φαρμακολογία Τμήμα Ιατρικής Α.Π.Θ.
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΧΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Α.Π.Θ. Ενότητα 6: Αντιμικροβιακά χημειοθεραπευτικά φάρμακα Μαρία Μυρωνίδου-Τζουβελέκη Α.Π.Θ. Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΧΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Α.Π.Θ. Ενότητα 6: Αντιμικροβιακά χημειοθεραπευτικά φάρμακα Μαρία Μυρωνίδου-Τζουβελέκη Α.Π.Θ. Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό
In vitro δραστικότητα των ceftaroline, ceftobiprole και telavancin έναντι κλινικών στελεχών Staphylococcus aureus στη Θεσσαλία
 In vitro δραστικότητα των ceftaroline, ceftobiprole και telavancin έναντι κλινικών στελεχών Staphylococcus aureus στη Θεσσαλία Ε.Μάλλη 1, Κ.Τσιλιπουνιδάκη 1, Σ.Ξύτσας 1, Π.Πυρίδου 1,Σ. Σάρρου 1, Α.Στέφος
In vitro δραστικότητα των ceftaroline, ceftobiprole και telavancin έναντι κλινικών στελεχών Staphylococcus aureus στη Θεσσαλία Ε.Μάλλη 1, Κ.Τσιλιπουνιδάκη 1, Σ.Ξύτσας 1, Π.Πυρίδου 1,Σ. Σάρρου 1, Α.Στέφος
μηχανισμοί ανάπτυξης αντοχής των μικροοργανισμών στα αντιβιοτικά πολυανθεκτικοί μικροοργανισμοί
 μηχανισμοί ανάπτυξης αντοχής των μικροοργανισμών στα αντιβιοτικά πολυανθεκτικοί μικροοργανισμοί Περιβολιώτη Ευσταθία, MD, PhD Διευθύντρια, Μικροβιολογικό τμήμα ΓΝΑ Ευαγγελισμός Πέμπτη, 11/10/2018, 19:00-21:00
μηχανισμοί ανάπτυξης αντοχής των μικροοργανισμών στα αντιβιοτικά πολυανθεκτικοί μικροοργανισμοί Περιβολιώτη Ευσταθία, MD, PhD Διευθύντρια, Μικροβιολογικό τμήμα ΓΝΑ Ευαγγελισμός Πέμπτη, 11/10/2018, 19:00-21:00
Η ΚΛΙΝΙΚΗ ΧΡΗΣΗ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ. Άγγελος Πεφάνης ΓΝΝΘΑ «Η Σωτηρία»
 Η ΚΛΙΝΙΚΗ ΧΡΗΣΗ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ Άγγελος Πεφάνης ΓΝΝΘΑ «Η Σωτηρία» Αντιμικροβιακή θεραπεία Τι θέλει ο κλινικός ; Αντιβιοτικό Το καλύτερο θεραπευτικό αποτέλεσμα STOP Όχι τοξική δράση STOP Όχι ανάπτυξη
Η ΚΛΙΝΙΚΗ ΧΡΗΣΗ ΤΩΝ ΑΝΤΙΜΙΚΡΟΒΙΑΚΩΝ Άγγελος Πεφάνης ΓΝΝΘΑ «Η Σωτηρία» Αντιμικροβιακή θεραπεία Τι θέλει ο κλινικός ; Αντιβιοτικό Το καλύτερο θεραπευτικό αποτέλεσμα STOP Όχι τοξική δράση STOP Όχι ανάπτυξη
Επιδημιολογική μελέτη Ευρωπαϊκή Ένωση 6,1-9,9 % των νοσηλευομένων ασθενών έχουν ενδονοσοκομειακή λοίμωξη
 Επιδημιολογική μελέτη Ευρωπαϊκή Ένωση 6,1-9,9 % των νοσηλευομένων ασθενών έχουν ενδονοσοκομειακή λοίμωξη α ί τ ι ο Πολυανθεκτικά στελέχη Ανοσοκαταστολή Πολυανθεκτικά παθογόνα βακτήρια: MRSA / CA-MRSA MR-CNS
Επιδημιολογική μελέτη Ευρωπαϊκή Ένωση 6,1-9,9 % των νοσηλευομένων ασθενών έχουν ενδονοσοκομειακή λοίμωξη α ί τ ι ο Πολυανθεκτικά στελέχη Ανοσοκαταστολή Πολυανθεκτικά παθογόνα βακτήρια: MRSA / CA-MRSA MR-CNS
Γ.Ν.Α «Ο ΕΥΑΓΓΕΛΙΣΜΟΣ- ΟΦΘΑΛΜΙΑΤΡΕΙΟ ΑΘΗΝΩΝ ΠΟΛΥΚΛΙΝΙΚΗ» ΜΙΚΡΟΒΙΟΛΟΓΙΚΟΥ ΤΜΗΜΑΤΟΣ - ΒΙΟΙΑΤΡΙΚΗΣ ΥΠΗΡΕΣΙΑΣ. ΘΕΟΔΩΡΟ ΝΙΑΡΧΑΚΟ (Διευθυντή Πωλήσεων)
 ΠΡΟΣ: ΥΠΟΨΗ: ΑΠΟ: Γ.Ν.Α «Ο ΕΥΑΓΓΕΛΙΣΜΟΣ- ΟΦΘΑΛΜΙΑΤΡΕΙΟ ΑΘΗΝΩΝ ΠΟΛΥΚΛΙΝΙΚΗ» ΜΙΚΡΟΒΙΟΛΟΓΙΚΟΥ ΤΜΗΜΑΤΟΣ - ΒΙΟΙΑΤΡΙΚΗΣ ΥΠΗΡΕΣΙΑΣ ΘΕΟΔΩΡΟ ΝΙΑΡΧΑΚΟ (Διευθυντή Πωλήσεων) ΗΜΕΡΟΜΗΝΙΑ: 5/4/2018 ΘΕΜΑ: Διαβούλευση
ΠΡΟΣ: ΥΠΟΨΗ: ΑΠΟ: Γ.Ν.Α «Ο ΕΥΑΓΓΕΛΙΣΜΟΣ- ΟΦΘΑΛΜΙΑΤΡΕΙΟ ΑΘΗΝΩΝ ΠΟΛΥΚΛΙΝΙΚΗ» ΜΙΚΡΟΒΙΟΛΟΓΙΚΟΥ ΤΜΗΜΑΤΟΣ - ΒΙΟΙΑΤΡΙΚΗΣ ΥΠΗΡΕΣΙΑΣ ΘΕΟΔΩΡΟ ΝΙΑΡΧΑΚΟ (Διευθυντή Πωλήσεων) ΗΜΕΡΟΜΗΝΙΑ: 5/4/2018 ΘΕΜΑ: Διαβούλευση
Σχολή Επιστημών Υγείας Τμήμα Νοσηλευτικής
 Σχολή Επιστημών Υγείας Τμήμα Νοσηλευτικής Τρίτη 19 Φεβρουαρίου 2019 12.00 14.00 2 η Θεματική Ενότητα Μάθημα: ΝΟΣΗΛΕΥΤΙΚΗ ΛΟΙΜΩΞΕΩΝ Ακαδ. Έτος: 2018 2019 Νομοθεσία και Εσωτερικοί Κανονισμοί ελέγχου λοιμώξεων.
Σχολή Επιστημών Υγείας Τμήμα Νοσηλευτικής Τρίτη 19 Φεβρουαρίου 2019 12.00 14.00 2 η Θεματική Ενότητα Μάθημα: ΝΟΣΗΛΕΥΤΙΚΗ ΛΟΙΜΩΞΕΩΝ Ακαδ. Έτος: 2018 2019 Νομοθεσία και Εσωτερικοί Κανονισμοί ελέγχου λοιμώξεων.
Πρόγραμμα εξειδίκευσης στη λοιμωξιολογία στη Γʹ Παιδιατρική Κλινική ΑΠΘ
 1 Πρόγραμμα εξειδίκευσης στη λοιμωξιολογία στη Γʹ Παιδιατρική Κλινική ΑΠΘ Υπεύθυνοι για την εκπαίδευση των εξειδικευομένων είναι οι: Εμμανουήλ Ροηλίδης, Καθηγητής Παιδιατρικής Λοιμωξιολογίας Χαράλαμπος
1 Πρόγραμμα εξειδίκευσης στη λοιμωξιολογία στη Γʹ Παιδιατρική Κλινική ΑΠΘ Υπεύθυνοι για την εκπαίδευση των εξειδικευομένων είναι οι: Εμμανουήλ Ροηλίδης, Καθηγητής Παιδιατρικής Λοιμωξιολογίας Χαράλαμπος
Τα παθογόνα μικρόβια στο ιαβητικό πόδι σε ασθενείς που παρακολουθούνται στο ιατρείο ιαβητικού ποδιού και θεραπεύονται εκτός νοσοκομείου.
 Τα παθογόνα μικρόβια στο ιαβητικό πόδι σε ασθενείς που παρακολουθούνται στο ιατρείο ιαβητικού ποδιού και θεραπεύονται εκτός νοσοκομείου..σκούτας¹,.καραγιάννη¹, Ε.Ρηγάδη¹, Κ.Μικούδη¹, Κ.Σιώμος¹, Ο.Γουλή¹,
Τα παθογόνα μικρόβια στο ιαβητικό πόδι σε ασθενείς που παρακολουθούνται στο ιατρείο ιαβητικού ποδιού και θεραπεύονται εκτός νοσοκομείου..σκούτας¹,.καραγιάννη¹, Ε.Ρηγάδη¹, Κ.Μικούδη¹, Κ.Σιώμος¹, Ο.Γουλή¹,
Ανθεκτικός στη μεθικιλλίνη χρυσίζων σταφυλόκοκκος (MRSA)
 ΕΚΠΑΙΔΕΥΣΗ ΑΣΘΕΝΟΥΣ & ΦΡΟΝΤΙΣΤΗ Ανθεκτικός στη μεθικιλλίνη χρυσίζων σταφυλόκοκκος (MRSA) Οι πληροφορίες αυτές παρέχουν εξηγήσεις σχετικά με τον ανθεκτικό στη μεθικιλλίνη χρυσίζοντα σταφυλόκοκκο (MRSA),
ΕΚΠΑΙΔΕΥΣΗ ΑΣΘΕΝΟΥΣ & ΦΡΟΝΤΙΣΤΗ Ανθεκτικός στη μεθικιλλίνη χρυσίζων σταφυλόκοκκος (MRSA) Οι πληροφορίες αυτές παρέχουν εξηγήσεις σχετικά με τον ανθεκτικό στη μεθικιλλίνη χρυσίζοντα σταφυλόκοκκο (MRSA),
Αντιβιοτικά. Ίρις Σπηλιοπούλου Εργαστήριο Μικροβιολογίας Ιατρική Σχολή Πανεπιστήμιο Πατρών
 Αντιβιοτικά Ίρις Σπηλιοπούλου Εργαστήριο Μικροβιολογίας Ιατρική Σχολή Πανεπιστήμιο Πατρών Αντι-βιοτικό ή αντι-μικροβιακό φάρμακο ποιος είναι ο καταλληλότερος όρος??? Τι είναι αντιβιοτικό;;; Αντιβιοτικά
Αντιβιοτικά Ίρις Σπηλιοπούλου Εργαστήριο Μικροβιολογίας Ιατρική Σχολή Πανεπιστήμιο Πατρών Αντι-βιοτικό ή αντι-μικροβιακό φάρμακο ποιος είναι ο καταλληλότερος όρος??? Τι είναι αντιβιοτικό;;; Αντιβιοτικά
Νεότερες παρεµβάσεις στην πρόληψη και θεραπεία του διαβητικού ποδιού
 Στρογγυλό τραπέζι Νεότερες παρεµβάσεις στην πρόληψη και θεραπεία του διαβητικού ποδιού Συντονιστής: Η. Ν. Μυγδάλης Β Παθολογική Κλινική και ιαβητολογικό Κέντρο, Γενικό Νοσοκοµείο ΝΙΜΤΣ, Αθήνα Οι διαταραχές
Στρογγυλό τραπέζι Νεότερες παρεµβάσεις στην πρόληψη και θεραπεία του διαβητικού ποδιού Συντονιστής: Η. Ν. Μυγδάλης Β Παθολογική Κλινική και ιαβητολογικό Κέντρο, Γενικό Νοσοκοµείο ΝΙΜΤΣ, Αθήνα Οι διαταραχές
ΟΡΘΟΛΟΓΙΚΗ ΕΠΙΛΟΓΗ ΑΝΤΙΒΙΟΤΙΚΩΝ ΓΙΑ ΤΗΝ ΘΕΡΑΠΕΙΑ ΤΩΝ ΟΥΡΟΛΟΙΜΩΞΕΩΝ. Μαρία Σουλή, Επ. Καθηγήτρια Μίνα Ψυχογιού, Επ. Καθηγήτρια
 ΟΡΘΟΛΟΓΙΚΗ ΕΠΙΛΟΓΗ ΑΝΤΙΒΙΟΤΙΚΩΝ ΓΙΑ ΤΗΝ ΘΕΡΑΠΕΙΑ ΤΩΝ ΟΥΡΟΛΟΙΜΩΞΕΩΝ Μαρία Σουλή, Επ. Καθηγήτρια Μίνα Ψυχογιού, Επ. Καθηγήτρια Γυναίκα 25 ετών προσέρχεται λόγω δυσουρίας και υπερηβικού άλγους από 24ώρου.
ΟΡΘΟΛΟΓΙΚΗ ΕΠΙΛΟΓΗ ΑΝΤΙΒΙΟΤΙΚΩΝ ΓΙΑ ΤΗΝ ΘΕΡΑΠΕΙΑ ΤΩΝ ΟΥΡΟΛΟΙΜΩΞΕΩΝ Μαρία Σουλή, Επ. Καθηγήτρια Μίνα Ψυχογιού, Επ. Καθηγήτρια Γυναίκα 25 ετών προσέρχεται λόγω δυσουρίας και υπερηβικού άλγους από 24ώρου.
ΛΟΙΜΩΞΕΙΣ ΣΤΟ ΔΙΑΒΗΤΙΚΟ ΠΟΔΙ Επιδημιολογία των παθογόνων στελεχών στην Ελλάδα
 ΛΟΙΜΩΞΕΙΣ ΣΤΟ ΔΙΑΒΗΤΙΚΟ ΠΟΔΙ Επιδημιολογία των παθογόνων στελεχών στην Ελλάδα Μαρία Δημητρίου Ειδικευόμενη Βιοπαθολόγος, Επιστημονική Συνεργάτης Ιατρείου Διαβητικού Ποδιού Διαβητολογικού Κέντρου Β Παθολογικής
ΛΟΙΜΩΞΕΙΣ ΣΤΟ ΔΙΑΒΗΤΙΚΟ ΠΟΔΙ Επιδημιολογία των παθογόνων στελεχών στην Ελλάδα Μαρία Δημητρίου Ειδικευόμενη Βιοπαθολόγος, Επιστημονική Συνεργάτης Ιατρείου Διαβητικού Ποδιού Διαβητολογικού Κέντρου Β Παθολογικής
ΕΞ. ΕΠΕΙΓΟΝ ΑΝΑΡΤΗΤΕΟ ΣΤΟ ΔΙΑΔΙΚΤΥΟ Αθήνα 30 / 05 /2019 Αριθ. Πρωτ.Δ1α/Γ.Π.οικ.24815
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΓΕΝΙΚΗ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΕΙΑΣ ΚΑΙ ΠΟΙΟΤΗΤΑΣ ΖΩΗΣ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΕΙΑΣ ΤΜΗΜΑ ΜΕΤΑΔΟΤΙΚΩΝ ΚΑΙ ΜΗ ΜΕΤΑΔΟΤΙΚΩΝ ΝΟΣΗΜΑΤΩΝ Πληροφορίες : Ο. Παντελά Ταχ. Δ/νση : Αριστοτέλους
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΓΕΝΙΚΗ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΕΙΑΣ ΚΑΙ ΠΟΙΟΤΗΤΑΣ ΖΩΗΣ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΕΙΑΣ ΤΜΗΜΑ ΜΕΤΑΔΟΤΙΚΩΝ ΚΑΙ ΜΗ ΜΕΤΑΔΟΤΙΚΩΝ ΝΟΣΗΜΑΤΩΝ Πληροφορίες : Ο. Παντελά Ταχ. Δ/νση : Αριστοτέλους
Αντοχή τροφιμογενών βακτηρίων στα αντιβιοτικά
 Δρ. Παναγιώτα Γούσια Κτηνίατρος Ενιαίος Φορέας Ελέγχου Τροφίμων Περιφερειακή Διεύθυνση Κεντρικής Μακεδονίας pgousia@efet.gr Αντοχή τροφιμογενών βακτηρίων στα αντιβιοτικά Αντοχή στα αντιβιοτικά Η ικανότητα
Δρ. Παναγιώτα Γούσια Κτηνίατρος Ενιαίος Φορέας Ελέγχου Τροφίμων Περιφερειακή Διεύθυνση Κεντρικής Μακεδονίας pgousia@efet.gr Αντοχή τροφιμογενών βακτηρίων στα αντιβιοτικά Αντοχή στα αντιβιοτικά Η ικανότητα
Δέσμες Μέτρων για την Πρόληψη των Αναπνευστικών Λοιμώξεων
 Σχολή Επιστημών Υγείας Τμήμα Νοσηλευτικής Τρίτη 19 Μαρτίου 2019 12.00 14.00 6 η Θεματική Ενότητα Μάθημα: ΝΟΣΗΛΕΥΤΙΚΗ ΛΟΙΜΩΞΕΩΝ Ακαδ. Έτος: 2018 2019 Δέσμες Μέτρων για την Πρόληψη των Αναπνευστικών Λοιμώξεων
Σχολή Επιστημών Υγείας Τμήμα Νοσηλευτικής Τρίτη 19 Μαρτίου 2019 12.00 14.00 6 η Θεματική Ενότητα Μάθημα: ΝΟΣΗΛΕΥΤΙΚΗ ΛΟΙΜΩΞΕΩΝ Ακαδ. Έτος: 2018 2019 Δέσμες Μέτρων για την Πρόληψη των Αναπνευστικών Λοιμώξεων
ΝΟΜΟΘΕΤΙΚΕΣ ΑΛΛΑΓΕΣ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΤΗΣ ΜΙΚΡΟΒΙΑΚΗΣ ΑΝΤΟΧΗΣ, ΤΗΝ ΠΡΟΛΗΨΗ ΚΑΙ ΤΟΝ ΕΛΕΓΧΟ ΤΩΝ ΝΟΣΟΚΟΜΕΙΚΩΝ ΛΟΙΜΩΞΕΩΝ
 ΝΟΜΟΘΕΤΙΚΕΣ ΑΛΛΑΓΕΣ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΤΗΣ ΜΙΚΡΟΒΙΑΚΗΣ ΑΝΤΟΧΗΣ, ΤΗΝ ΠΡΟΛΗΨΗ ΚΑΙ ΤΟΝ ΕΛΕΓΧΟ ΤΩΝ ΝΟΣΟΚΟΜΕΙΚΩΝ ΛΟΙΜΩΞΕΩΝ Φ. ΚΑΛΥΒΑ ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΙΕΙΝΗΣ Παιδίατρος- Ιατρός Δημόσιας Υγείας
ΝΟΜΟΘΕΤΙΚΕΣ ΑΛΛΑΓΕΣ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΤΗΣ ΜΙΚΡΟΒΙΑΚΗΣ ΑΝΤΟΧΗΣ, ΤΗΝ ΠΡΟΛΗΨΗ ΚΑΙ ΤΟΝ ΕΛΕΓΧΟ ΤΩΝ ΝΟΣΟΚΟΜΕΙΚΩΝ ΛΟΙΜΩΞΕΩΝ Φ. ΚΑΛΥΒΑ ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ Δ/ΝΣΗ ΔΗΜΟΣΙΑΣ ΥΓΙΕΙΝΗΣ Παιδίατρος- Ιατρός Δημόσιας Υγείας
Νοσοκομειακές Λοιμώξεις Επιδημιολογία και επιτήρηση
 Νοσοκομειακές Λοιμώξεις Επιδημιολογία και επιτήρηση Ποια είναι η αναγκαιότητα της επιτήρησης των νοσοκομειακών λοιμώξεων Οι νοσοκομειακές λοιμώξεις είναι άμεσα συνδεόμενες με Την ασφάλεια των ασθενών Την
Νοσοκομειακές Λοιμώξεις Επιδημιολογία και επιτήρηση Ποια είναι η αναγκαιότητα της επιτήρησης των νοσοκομειακών λοιμώξεων Οι νοσοκομειακές λοιμώξεις είναι άμεσα συνδεόμενες με Την ασφάλεια των ασθενών Την
Αθηνά Αργυροπούλου Βιοπαθολόγος Κλινικός Μικροβιολόγος Γ.Ν.Α «Ο Ευαγγελισμός»
 ΡΜΗΝΙΑ ΑΝΤΙΒΙΟΓΡΑΜΜΑΤΟΣ: τι πρέπει να ξέρει ο κλινικός ιατρός Αθηνά Αργυροπούλου Βιοπαθολόγος Κλινικός Μικροβιολόγος Γ.Ν.Α «Ο υαγγελισμός» Η ομιλία αυτή δεν χρηματοδοτήθηκε από καμία φαρμακευτική εταιρεία
ΡΜΗΝΙΑ ΑΝΤΙΒΙΟΓΡΑΜΜΑΤΟΣ: τι πρέπει να ξέρει ο κλινικός ιατρός Αθηνά Αργυροπούλου Βιοπαθολόγος Κλινικός Μικροβιολόγος Γ.Ν.Α «Ο υαγγελισμός» Η ομιλία αυτή δεν χρηματοδοτήθηκε από καμία φαρμακευτική εταιρεία
Επιδημιολογική Επιτήρηση Μικροβιακής Αντοχής στα νοσοκομεία
 Επιδημιολογική Επιτήρηση Μικροβιακής Αντοχής στα νοσοκομεία Αλκ Βατόπουλος Εθνική Σχολή Δημόσιας Υγείας (Ιατρική) Μικροβιολογία Κλινική Μικροβιολογία: Απαντά στα ερωτήματα: Ποιό είναι το (μικροβιακό) αίτιο
Επιδημιολογική Επιτήρηση Μικροβιακής Αντοχής στα νοσοκομεία Αλκ Βατόπουλος Εθνική Σχολή Δημόσιας Υγείας (Ιατρική) Μικροβιολογία Κλινική Μικροβιολογία: Απαντά στα ερωτήματα: Ποιό είναι το (μικροβιακό) αίτιο
Πανδής Σ., Αραμπατζής Μ. & Α. Βελεγράκη. Ειδικό Εργαστήριο Μυκητολογίας (Κ.Α 70/4/5905, Κ.Α 70/3/6915)
 Αξιολόγηση της in vitro αποτελεσματικότητας υφασμάτων οξειδωτικού καταλύτη επί της επιβίωσης παθογόνων βακτηρίων και ευκαιριακά παθογόνων μυκήτων του νοσοκομειακού περιβάλλοντος Πανδής Σ., Αραμπατζής Μ.
Αξιολόγηση της in vitro αποτελεσματικότητας υφασμάτων οξειδωτικού καταλύτη επί της επιβίωσης παθογόνων βακτηρίων και ευκαιριακά παθογόνων μυκήτων του νοσοκομειακού περιβάλλοντος Πανδής Σ., Αραμπατζής Μ.
Ελληνική Εταιρεία Χημειοθεραπείας
 Τί κερδίζεται in Vitro? Δραστικότητα έναντι: ESBLs ενζύμων (Εντεροβακτηριακά) KPC ενζύμων (Εντεροβακτηριακά) AmpC ενζύμων (Pseudomonas aeruginosa) OXA-48 ενζύμων (Εντεροβακτηριακά) Στελεχών ανθεκτικών
Τί κερδίζεται in Vitro? Δραστικότητα έναντι: ESBLs ενζύμων (Εντεροβακτηριακά) KPC ενζύμων (Εντεροβακτηριακά) AmpC ενζύμων (Pseudomonas aeruginosa) OXA-48 ενζύμων (Εντεροβακτηριακά) Στελεχών ανθεκτικών
Ο ρόλος και η σημασία των μοριακών τεχνικών στον έλεγχο των. μικροβιολογικών παραμέτρων σε περιβαλλοντικά δείγματα για την προστασία
 Ο ρόλος και η σημασία των μοριακών τεχνικών στον έλεγχο των μικροβιολογικών παραμέτρων σε περιβαλλοντικά δείγματα για την προστασία της Δημόσιας Υγείας Α. Βανταράκης Εργαστήριο Υγιεινής, Ιατρική Σχολή,
Ο ρόλος και η σημασία των μοριακών τεχνικών στον έλεγχο των μικροβιολογικών παραμέτρων σε περιβαλλοντικά δείγματα για την προστασία της Δημόσιας Υγείας Α. Βανταράκης Εργαστήριο Υγιεινής, Ιατρική Σχολή,
ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ. Ιατρική Σχολή Πανεπιστημίου Θεσσαλίας
 ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ Ιατρική Σχολή Πανεπιστημίου Θεσσαλίας Ε. ΠΕΤΕΙΝΑΚΗ Aναπληρώτρια Καθηγήτρια Μικροβιολογίας Διευθύντρια Εργαστηρίου Μικροβιολογίας ΜΙΚΡΟΒΙΟΛΟΓΙΑ φάση της κλινικής ιατρικής Η μικροβιολογία
ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ Ιατρική Σχολή Πανεπιστημίου Θεσσαλίας Ε. ΠΕΤΕΙΝΑΚΗ Aναπληρώτρια Καθηγήτρια Μικροβιολογίας Διευθύντρια Εργαστηρίου Μικροβιολογίας ΜΙΚΡΟΒΙΟΛΟΓΙΑ φάση της κλινικής ιατρικής Η μικροβιολογία
ΒΑΚΤΗΡΙΑΙΜΙΑ ΣΗΠΤΙΚΟ ΣΥΝΔΡΟΜΟ
 ΒΑΚΤΗΡΙΑΙΜΙΑ ΣΗΠΤΙΚΟ ΣΥΝΔΡΟΜΟ Ε. Ι. Γιαμαρέλλος-Μπουρμπούλης Αναπληρωτής Καθηγητής Παθολογίας Δ Παθολογική Κλινική Ιατρική Σχολή Πανεπιστημίου Αθηνών Ιστορικό (1) Άνδρας 65 ετών Εισαγωγή στα ΤΕΠ λόγω δύσπνοιας
ΒΑΚΤΗΡΙΑΙΜΙΑ ΣΗΠΤΙΚΟ ΣΥΝΔΡΟΜΟ Ε. Ι. Γιαμαρέλλος-Μπουρμπούλης Αναπληρωτής Καθηγητής Παθολογίας Δ Παθολογική Κλινική Ιατρική Σχολή Πανεπιστημίου Αθηνών Ιστορικό (1) Άνδρας 65 ετών Εισαγωγή στα ΤΕΠ λόγω δύσπνοιας
Αντιβιοτικών στις. 12 ο. Ορθολογική Χρήση. Συνήθεις Λοιμώξεις. Πρόγραμμα. Μετεκπαιδευτικό Σεμινάριο Λοιμώξεων 04-05
 Διοργάνωση Μεσογειακό Ινστιτούτο Μελέτης & Εκπαίδευσης στην Πρόληψη & Αντιμετώπιση των Λοιμώξεων Δ Παθολογική Κλινική Ιατρικής Σχολής Εθνικού & Καποδιστριακού Πανεπιστημίου Αθηνών 12 ο Μετεκπαιδευτικό
Διοργάνωση Μεσογειακό Ινστιτούτο Μελέτης & Εκπαίδευσης στην Πρόληψη & Αντιμετώπιση των Λοιμώξεων Δ Παθολογική Κλινική Ιατρικής Σχολής Εθνικού & Καποδιστριακού Πανεπιστημίου Αθηνών 12 ο Μετεκπαιδευτικό
Πρόληψη των ενδονοσοκομειακών λοιμώξεων
 Πρόληψη των ενδονοσοκομειακών λοιμώξεων Αικατερίνη Μασγάλα Παθολόγος-Λοιμωξιολόγος Επιμελήτρια Α Α Παθολογικής Κλινικής Aικατερίνη Κωνσταντοπούλειο Κ. Μασγάλα ΓΝΝΙ Παθολόγος- Λοιμωξιολόγος Επιμελήτρια
Πρόληψη των ενδονοσοκομειακών λοιμώξεων Αικατερίνη Μασγάλα Παθολόγος-Λοιμωξιολόγος Επιμελήτρια Α Α Παθολογικής Κλινικής Aικατερίνη Κωνσταντοπούλειο Κ. Μασγάλα ΓΝΝΙ Παθολόγος- Λοιμωξιολόγος Επιμελήτρια
Ελληνική Εταιρεία Λοιμώξεων
 Ελληνική Εταιρεία Λοιμώξεων ΕΤΗΣΙΟ ΠΑΝΕΛΛΑΔΙΚΟ ΕΚΠΑΙΔΕΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΣΤΙΣ ΛΟΙΜΩΞΕΙΣ 2008-2009 Μάθημα 3 ο 16 Δεκεμβρίου 2008 ΕΙΣΗΓΗΤΕΣ: Χαράλαμπος Α Γώγος Καθηγητής Παθολογίας Πανεπιστημίου Πατρών Με την
Ελληνική Εταιρεία Λοιμώξεων ΕΤΗΣΙΟ ΠΑΝΕΛΛΑΔΙΚΟ ΕΚΠΑΙΔΕΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΣΤΙΣ ΛΟΙΜΩΞΕΙΣ 2008-2009 Μάθημα 3 ο 16 Δεκεμβρίου 2008 ΕΙΣΗΓΗΤΕΣ: Χαράλαμπος Α Γώγος Καθηγητής Παθολογίας Πανεπιστημίου Πατρών Με την
ΕΡΜΗΝΕΙΑ ΑΝΤΙΒΙΟΓΡΑΜΜΑΤΟΣ, ΦΑΙΝΟΤΥΠΙΚΕΣ ΔΟΚΙΜΑΣΙΕΣ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΑΝΤΟΧΗΣ INTERPRETATION OF ANTIBIOGRAM, PHENOTYPIC TESTS AND RESISTANCE MECHANISMS
 ΑΝΑΣΚΟΠΗΣΗ REVIEW ΕΡΜΗΝΕΙΑ ΑΝΤΙΒΙΟΓΡΑΜΜΑΤΟΣ, ΦΑΙΝΟΤΥΠΙΚΕΣ ΔΟΚΙΜΑΣΙΕΣ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΑΝΤΟΧΗΣ INTERPRETATION OF ANTIBIOGRAM, PHENOTYPIC TESTS AND RESISTANCE MECHANISMS Kωνσταντίνα Τζανέτου Konstantina Tzanetou
ΑΝΑΣΚΟΠΗΣΗ REVIEW ΕΡΜΗΝΕΙΑ ΑΝΤΙΒΙΟΓΡΑΜΜΑΤΟΣ, ΦΑΙΝΟΤΥΠΙΚΕΣ ΔΟΚΙΜΑΣΙΕΣ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΑΝΤΟΧΗΣ INTERPRETATION OF ANTIBIOGRAM, PHENOTYPIC TESTS AND RESISTANCE MECHANISMS Kωνσταντίνα Τζανέτου Konstantina Tzanetou
Επιδηµιολογία νοσοκοµειακών λοιµώξεων
 Επιδηµιολογία νοσοκοµειακών λοιµώξεων Η επιδηµιολογία των νοσοκοµειακών λοιµώξεων παρουσιάζει πολλές ιδιαιτερότητες σε σχέση µε αυτήν των λοιµωδών νοσηµάτων που εκδηλώνονται στην κοινότητα. Αφορά ένα ευρύ
Επιδηµιολογία νοσοκοµειακών λοιµώξεων Η επιδηµιολογία των νοσοκοµειακών λοιµώξεων παρουσιάζει πολλές ιδιαιτερότητες σε σχέση µε αυτήν των λοιµωδών νοσηµάτων που εκδηλώνονται στην κοινότητα. Αφορά ένα ευρύ
ΝΟΣΟΚΟΜΕΙΑΚΕΣ ΛΟΙΜΩΞΕΙΣ ΣΑΝ ΔΕΙΚΤΗΣ ΠΟΙΟΤΗΤΑΣ Παναγιώτου Χρυσούλα Ανώτερη Νοσηλευτικός Λειτουργός Νοσηλεύτρια Ελέγχου Λοιμώξεων ΝΟΣΟΚΟΜΕΙΟ ΠΑΦΟΥ
 ΝΟΣΟΚΟΜΕΙΑΚΕΣ ΛΟΙΜΩΞΕΙΣ ΣΑΝ ΔΕΙΚΤΗΣ ΠΟΙΟΤΗΤΑΣ Παναγιώτου Χρυσούλα Ανώτερη Νοσηλευτικός Λειτουργός Νοσηλεύτρια Ελέγχου Λοιμώξεων ΝΟΣΟΚΟΜΕΙΟ ΠΑΦΟΥ ΝΟΣΟΚΟΜΕΙΑΚΕΣ ΛΟΙΜΩΞΕΙΣ ΣΑΝ ΔΕΙΚΤΗΣ ΠΟΙΟΤΗΤΑΣ Φτάνοντας
ΝΟΣΟΚΟΜΕΙΑΚΕΣ ΛΟΙΜΩΞΕΙΣ ΣΑΝ ΔΕΙΚΤΗΣ ΠΟΙΟΤΗΤΑΣ Παναγιώτου Χρυσούλα Ανώτερη Νοσηλευτικός Λειτουργός Νοσηλεύτρια Ελέγχου Λοιμώξεων ΝΟΣΟΚΟΜΕΙΟ ΠΑΦΟΥ ΝΟΣΟΚΟΜΕΙΑΚΕΣ ΛΟΙΜΩΞΕΙΣ ΣΑΝ ΔΕΙΚΤΗΣ ΠΟΙΟΤΗΤΑΣ Φτάνοντας
Δράμα Πνευμονία από την κοινότητα Κ.Κανελλακοπούλου
 Δράμα 14 12 2018 Πνευμονία από την κοινότητα Κ.Κανελλακοπούλου 1 Ασθενής ηλικίας 40 ετών καπνιστής με ελεύθερο ατομικό αναμνηστικό προσέρχεται στο Κέντρο Υγείας με πυρετό 40 Ο C από 10ώρου, ρίγος και κακουχία.
Δράμα 14 12 2018 Πνευμονία από την κοινότητα Κ.Κανελλακοπούλου 1 Ασθενής ηλικίας 40 ετών καπνιστής με ελεύθερο ατομικό αναμνηστικό προσέρχεται στο Κέντρο Υγείας με πυρετό 40 Ο C από 10ώρου, ρίγος και κακουχία.
Αντιμετώπιση Επιδημιών από Ιογενείς Παράγοντες
 Αντιμετώπιση Επιδημιών από Ιογενείς Παράγοντες Δρ. Έλενα Μαλτέζου Τμήμα Παρεμβάσεων σε Χώρους Παροχής Υπηρεσιών Υγείας Κέντρο Ελέγχου & Πρόληψης Νοσημάτων 1 ο Πανελλήνιο Συνέδριο Παιδιατρικών Λοιμώξεων
Αντιμετώπιση Επιδημιών από Ιογενείς Παράγοντες Δρ. Έλενα Μαλτέζου Τμήμα Παρεμβάσεων σε Χώρους Παροχής Υπηρεσιών Υγείας Κέντρο Ελέγχου & Πρόληψης Νοσημάτων 1 ο Πανελλήνιο Συνέδριο Παιδιατρικών Λοιμώξεων
ΟΞΕΙΑ ΠΥΕΛΟΝΕΦΡΙΤΙΔΑ
 ΠΥΕΛΟΝΕΦΡΙΤΙΔΑ ΟΞΕΙΑ ΠΥΕΛΟΝΕΦΡΙΤΙΔΑ Πυελονεφρίτιδα είναι η φλεγμονή του νεφρικού παρεγχύματος και της νεφρικής πυέλου. Η διάγνωση τίθεται με βάση τα σημεία και τα συμπτώματα. Πόνος στην πλάτη, στο πλευρό
ΠΥΕΛΟΝΕΦΡΙΤΙΔΑ ΟΞΕΙΑ ΠΥΕΛΟΝΕΦΡΙΤΙΔΑ Πυελονεφρίτιδα είναι η φλεγμονή του νεφρικού παρεγχύματος και της νεφρικής πυέλου. Η διάγνωση τίθεται με βάση τα σημεία και τα συμπτώματα. Πόνος στην πλάτη, στο πλευρό
ΝΕΕΣ MΟΡΙΑΚΕΣ ΤΕΧΝΙΚΕΣ ΓΙΑ ΤΗΝ ΤΥΠΟΠΟΙΗΣΗ ΤΩΝ ΒΑΚΤΗΡΙΩΝ
 ΝΕΕΣ MΟΡΙΑΚΕΣ ΤΕΧΝΙΚΕΣ ΓΙΑ ΤΗΝ ΤΥΠΟΠΟΙΗΣΗ ΤΩΝ ΒΑΚΤΗΡΙΩΝ ΑΠΟΣΤΟΛΟΣ ΒΑΝΤΑΡΑΚΗΣ ΒΙΟΛΟΓΟΣ (M.Sc, Ph.D) Επιδημίες μολυσματικών ασθενειών συχνά οφείλονται σε έκθεση σε μία κοινή πηγή ενός αιτιολογικού παράγοντα.
ΝΕΕΣ MΟΡΙΑΚΕΣ ΤΕΧΝΙΚΕΣ ΓΙΑ ΤΗΝ ΤΥΠΟΠΟΙΗΣΗ ΤΩΝ ΒΑΚΤΗΡΙΩΝ ΑΠΟΣΤΟΛΟΣ ΒΑΝΤΑΡΑΚΗΣ ΒΙΟΛΟΓΟΣ (M.Sc, Ph.D) Επιδημίες μολυσματικών ασθενειών συχνά οφείλονται σε έκθεση σε μία κοινή πηγή ενός αιτιολογικού παράγοντα.
ΟΙ ΜΟΡΙΑΚΕΣ ΤΕΧΝΙΚΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ. Eφη. Πετεινάκη
 ΟΙ ΜΟΡΙΑΚΕΣ ΤΕΧΝΙΚΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ Eφη Πετεινάκη ΠΡΟΒΛΗΜΑΤΑ ΡΟΥΤΙΝΑΣ ΕΝΟΣ ΚΛΙΝΙΚΟΥ ΜΙΚΡΟΒΙΟΛΟΓΙΚΟΥ ΕΡΓΑΣΤΗΡΙΟΥ ταυτοποίηση κάποιων βακτηρίων ο έλεγχος ευαισθησίας διάγνωση λοιμώξεων από μικροοργανισμούς
ΟΙ ΜΟΡΙΑΚΕΣ ΤΕΧΝΙΚΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ Eφη Πετεινάκη ΠΡΟΒΛΗΜΑΤΑ ΡΟΥΤΙΝΑΣ ΕΝΟΣ ΚΛΙΝΙΚΟΥ ΜΙΚΡΟΒΙΟΛΟΓΙΚΟΥ ΕΡΓΑΣΤΗΡΙΟΥ ταυτοποίηση κάποιων βακτηρίων ο έλεγχος ευαισθησίας διάγνωση λοιμώξεων από μικροοργανισμούς
Λοιμώξεις ουροποιητικού. Αικατερίνη Κ. Μασγάλα
 Λοιμώξεις ουροποιητικού Αικατερίνη Κ. Μασγάλα Ταξινόμηση-Ορισμοί Λοιμώξεις ανώτερου ουροποιητικού Πυελονεφρίτιδα με ή χωρίς νεφρικό ή παρανεφρικό απόστημα. Λοιμώξεις κατώτερου ουροποιητικού Κυστίτιδα,
Λοιμώξεις ουροποιητικού Αικατερίνη Κ. Μασγάλα Ταξινόμηση-Ορισμοί Λοιμώξεις ανώτερου ουροποιητικού Πυελονεφρίτιδα με ή χωρίς νεφρικό ή παρανεφρικό απόστημα. Λοιμώξεις κατώτερου ουροποιητικού Κυστίτιδα,
2/12/2013. Νοσοκομειακές λοιμώξεις. Επιδημιολογία νοσοκομειακών λοιμώξεων από Gramαρνητικά παθογόνα Μέτρα ελέγχου. Ορισμοί. Νοσοκομειακή λοίμωξη
 Επιδημιολογία νοσοκομειακών λοιμώξεων από Gramαρνητικά παθογόνα Μέτρα ελέγχου Νοσοκομειακές λοιμώξεις Welcome to the hospital! Bugs are waiting for you!!! Ξανθή Δεδούκου Γραφείο Νοσοκομειακών Λοιμώξεων
Επιδημιολογία νοσοκομειακών λοιμώξεων από Gramαρνητικά παθογόνα Μέτρα ελέγχου Νοσοκομειακές λοιμώξεις Welcome to the hospital! Bugs are waiting for you!!! Ξανθή Δεδούκου Γραφείο Νοσοκομειακών Λοιμώξεων
ΠΡΩΤΟΚΟΛΛΑ ΣΥΝΤΑΓΟΓΡΑΦΗΣΗΣ ΣΕ ΛΟΙΜΩΞΕΙΣ ΟΥΡΟΠΟΙΗΤΙΚΟΥ ( Υπεύθυνος: Γ Πετρίκκος, Συνεργάτες: M Σουλή, Δ Πλαχούρας )
 ΠΡΩΤΟΚΟΛΛΑ ΣΥΝΤΑΓΟΓΡΑΦΗΣΗΣ ΣΕ ΛΟΙΜΩΞΕΙΣ ΟΥΡΟΠΟΙΗΤΙΚΟΥ ( Υπεύθυνος: Γ Πετρίκκος, Συνεργάτες: M Σουλ, Δ Πλαχούρας ) Οι λοιμώξεις του ουροποιητικού συστματος είναι από τις πλέον συχνές βακτηριακές λοιμώξεις,
ΠΡΩΤΟΚΟΛΛΑ ΣΥΝΤΑΓΟΓΡΑΦΗΣΗΣ ΣΕ ΛΟΙΜΩΞΕΙΣ ΟΥΡΟΠΟΙΗΤΙΚΟΥ ( Υπεύθυνος: Γ Πετρίκκος, Συνεργάτες: M Σουλ, Δ Πλαχούρας ) Οι λοιμώξεις του ουροποιητικού συστματος είναι από τις πλέον συχνές βακτηριακές λοιμώξεις,
ΥΓΙΕΙΝΗ ΤΩΝ ΧΕΡΙΩΝ. Aγγελική Διπλού Νοσηλεύτρια Επιτήρησης Λοιμώξεων Γ.Ν. «Ασκληπιείο Βούλας»
 ΥΓΙΕΙΝΗ ΤΩΝ ΧΕΡΙΩΝ Aγγελική Διπλού Νοσηλεύτρια Επιτήρησης Λοιμώξεων Γ.Ν. «Ασκληπιείο Βούλας» Η ΣΗΜΑΣΙΑ ΤΗΣ ΥΓΙΕΙΝΗΣ ΤΩΝ ΧΕΡΙΩΝ Η υγιεινή των χεριών αποτελεί βασικό παράγοντα για την: Ασφάλεια ασθενών Πρόληψη
ΥΓΙΕΙΝΗ ΤΩΝ ΧΕΡΙΩΝ Aγγελική Διπλού Νοσηλεύτρια Επιτήρησης Λοιμώξεων Γ.Ν. «Ασκληπιείο Βούλας» Η ΣΗΜΑΣΙΑ ΤΗΣ ΥΓΙΕΙΝΗΣ ΤΩΝ ΧΕΡΙΩΝ Η υγιεινή των χεριών αποτελεί βασικό παράγοντα για την: Ασφάλεια ασθενών Πρόληψη
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Φαρμακολογία ΙI. Χημειοθεραπεία. Διδάσκοντες: Μ. Μαρσέλος, Μ. Κωνσταντή, Π. Παππάς, Κ.
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Φαρμακολογία ΙI Χημειοθεραπεία Διδάσκοντες: Μ. Μαρσέλος, Μ. Κωνσταντή, Π. Παππάς, Κ. Αντωνίου Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Φαρμακολογία ΙI Χημειοθεραπεία Διδάσκοντες: Μ. Μαρσέλος, Μ. Κωνσταντή, Π. Παππάς, Κ. Αντωνίου Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Eρωτήσεις Εξέτασης στη Φαρµακολογία IΙ
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟ ΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Πανεπιστηµιούπολη, Ζωγράφου 157 71, Αθήνα Πρόεδρος: Καθηγητής Παναγιώτης Μαχαίρας Τηλ.: 210 7274367, Φαξ: 210 7274027 Ονοµατεπώνυµο: Eρωτήσεις
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟ ΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Πανεπιστηµιούπολη, Ζωγράφου 157 71, Αθήνα Πρόεδρος: Καθηγητής Παναγιώτης Μαχαίρας Τηλ.: 210 7274367, Φαξ: 210 7274027 Ονοµατεπώνυµο: Eρωτήσεις
«Λοιμώξεις και Αντιμικροβιακη Θεραπεία στην Πρωτοβάθμια Περίθαλψη» Πενικιλλίνες Αρχαία Ολυμπία 2017 Κ.Κανελλακοπούλου
 «Λοιμώξεις και Αντιμικροβιακη Θεραπεία στην Πρωτοβάθμια Περίθαλψη» Πενικιλλίνες Αρχαία Ολυμπία 2017 Κ.Κανελλακοπούλου Η χημική δομή της πενικιλλίνης G. 1. Δακτύλιος β-λακτάμης 2. Δακτύλιος θειαζολιδίνης.
«Λοιμώξεις και Αντιμικροβιακη Θεραπεία στην Πρωτοβάθμια Περίθαλψη» Πενικιλλίνες Αρχαία Ολυμπία 2017 Κ.Κανελλακοπούλου Η χημική δομή της πενικιλλίνης G. 1. Δακτύλιος β-λακτάμης 2. Δακτύλιος θειαζολιδίνης.
ΣΗΨΗ Η ΕΝΝΟΙΑ ΤΗΣ ΑΝΟΣΟΘΕΡΑΠΕΙΑΣ
 ΣΗΨΗ Η ΕΝΝΟΙΑ ΤΗΣ ΑΝΟΣΟΘΕΡΑΠΕΙΑΣ Ευάγγελος Ι. Γιαμαρέλλος-Μπουρμπούλης Αναπλ. Καθηγητής Παθολογίας, Δ Παθολογική Κλινική, Ιατρική Σχολή Πανεπιστημίου Αθηνών Professor Center for Sepsis Control and Care,
ΣΗΨΗ Η ΕΝΝΟΙΑ ΤΗΣ ΑΝΟΣΟΘΕΡΑΠΕΙΑΣ Ευάγγελος Ι. Γιαμαρέλλος-Μπουρμπούλης Αναπλ. Καθηγητής Παθολογίας, Δ Παθολογική Κλινική, Ιατρική Σχολή Πανεπιστημίου Αθηνών Professor Center for Sepsis Control and Care,
ΛΟΙΜΩΞΕΙΣ ΚΑΤΩΤΕΡΟΥ ΑΝΑΠΝΕΥΣΤΙΚΟΥ (Υπεύθυνος : M Λαζανάς. 1.Εμπειρική θεραπεία πνευμονίας από την κοινότητα
 ΛΟΙΜΩΞΕΙΣ ΚΑΤΩΤΕΡΟΥ ΑΝΑΠΝΕΥΣΤΙΚΟΥ (Υπεύθυνος : M Λαζανάς 1.Εμπειρική θεραπεία πνευμονίας από την κοινότητα Η πνευμονία από την κοινότητα είναι η οξεία λοίμωξη του πνευμονικού παρεγχύματος σε ασθενή που
ΛΟΙΜΩΞΕΙΣ ΚΑΤΩΤΕΡΟΥ ΑΝΑΠΝΕΥΣΤΙΚΟΥ (Υπεύθυνος : M Λαζανάς 1.Εμπειρική θεραπεία πνευμονίας από την κοινότητα Η πνευμονία από την κοινότητα είναι η οξεία λοίμωξη του πνευμονικού παρεγχύματος σε ασθενή που
ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΚΑΙ ΚΟΙΝΩΝΙΚΗΣ ΑΛΛΗΛΕΓΓΥΗΣ ΓΡΙΠΗ ΕΝΗΜΕΡΩΣΗ ΓΙΑ ΤΗΝ ΠΕΡΙΟ Ο ΓΡΙΠΗΣ
 ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΚΑΙ ΚΟΙΝΩΝΙΚΗΣ ΑΛΛΗΛΕΓΓΥΗΣ ΓΡΙΠΗ 2010-2011 ΕΝΗΜΕΡΩΣΗ ΓΙΑ ΤΗΝ ΠΕΡΙΟ Ο ΓΡΙΠΗΣ 2010-2011 ΣΤΡΑΤΗΓΙΚΗ ΧΡΗΣΗΣ ΑΝΤΙ-ΙΙΚΩΝ ΚΑΤΑ ΤΗΣ ΓΡΙΠΗΣ 15 ΙΑΝΟΥΑΡΙΟΥ 2011 ΣΗΜΑΝΤΙΚΑ ΣΗΜΕΙΑ Κατά την περίοδο
ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΚΑΙ ΚΟΙΝΩΝΙΚΗΣ ΑΛΛΗΛΕΓΓΥΗΣ ΓΡΙΠΗ 2010-2011 ΕΝΗΜΕΡΩΣΗ ΓΙΑ ΤΗΝ ΠΕΡΙΟ Ο ΓΡΙΠΗΣ 2010-2011 ΣΤΡΑΤΗΓΙΚΗ ΧΡΗΣΗΣ ΑΝΤΙ-ΙΙΚΩΝ ΚΑΤΑ ΤΗΣ ΓΡΙΠΗΣ 15 ΙΑΝΟΥΑΡΙΟΥ 2011 ΣΗΜΑΝΤΙΚΑ ΣΗΜΕΙΑ Κατά την περίοδο
Διερεύνηση μιας υδατογενούς ή τροφικής επιδημικής έκρηξης
 Watermicro Πρόγραμμα Κατάρτισης Εξ αποστάσεως (Distance learning course) Διερεύνηση μιας υδατογενούς ή τροφικής επιδημικής έκρηξης Τάνια Αρβανιτίδου-Βαγιωνά Καθηγήτρια, ΑΠΘ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ
Watermicro Πρόγραμμα Κατάρτισης Εξ αποστάσεως (Distance learning course) Διερεύνηση μιας υδατογενούς ή τροφικής επιδημικής έκρηξης Τάνια Αρβανιτίδου-Βαγιωνά Καθηγήτρια, ΑΠΘ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ
ΜΕΛΕΤΗ ΜΗΧΑΝΙΣΜΩΝ ΑΝΤΟΧΗΣ ΠΟΛΥΑΝΘΕΚΤΙΚΩΝ ΣΤΕΛΕΧΩΝ PSEUDOMONAS AERUGINOSA ΣΤΙΣ ΚΑΡΜΠΑΠΕΝΕΜΕΣ ΜΕ ΦΑΙΝΟΤΥΠΙΚΕΣ ΚΑΙ ΜΟΡΙΑΚΕΣ ΜΕΘΟ ΟΥΣ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΤΟΜΕΑΣ ΒΙΟΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΠΡΟΛΗΠΤΙΚΗΣ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ ΠΑΝΕΠΙΣΤΗΜΙΑΚΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΑΧΕΠΑ ΙΕΥΘΥΝΤΡΙΑ:
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΤΟΜΕΑΣ ΒΙΟΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΠΡΟΛΗΠΤΙΚΗΣ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ ΠΑΝΕΠΙΣΤΗΜΙΑΚΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΑΧΕΠΑ ΙΕΥΘΥΝΤΡΙΑ:
«Κατανάλωση Αντιβιοτικών και Αντοχή: Μπορεί να Λυθεί το Πρόβλημα?»
 Ημερίδα Νοσοκομειακών Λοιμώξεων: Το Πρόβλημα και η Αντιμετώπισή του «Κατανάλωση Αντιβιοτικών και Αντοχή: Μπορεί να Λυθεί το Πρόβλημα?» 21 Ιουλίου 2014 Αίθουσα τελετών Υπουργείου Υγείας Ελένη Γιαμαρέλλου
Ημερίδα Νοσοκομειακών Λοιμώξεων: Το Πρόβλημα και η Αντιμετώπισή του «Κατανάλωση Αντιβιοτικών και Αντοχή: Μπορεί να Λυθεί το Πρόβλημα?» 21 Ιουλίου 2014 Αίθουσα τελετών Υπουργείου Υγείας Ελένη Γιαμαρέλλου
Κεφτολοζάνη/Ταζομπακτάμη:
 Κεφτολοζάνη/Ταζομπακτάμη: Μια νέα κεφαλοσπορίνη με έναν αναστολέα β λακταμασών Άγγελος Πεφάνης Παθολόγος Λοιμωξιολόγος Παθολογική Κλινική ΓΝΝΘΑ «Η Σωτηρία» Μικρή εισαγωγή β λακταμάσες και άλλοι μηχανισμοί
Κεφτολοζάνη/Ταζομπακτάμη: Μια νέα κεφαλοσπορίνη με έναν αναστολέα β λακταμασών Άγγελος Πεφάνης Παθολόγος Λοιμωξιολόγος Παθολογική Κλινική ΓΝΝΘΑ «Η Σωτηρία» Μικρή εισαγωγή β λακταμάσες και άλλοι μηχανισμοί
Ελληνική Εταιρεία Χημειοθεραπείας
 «Λοιμώξεις και Αντιμικροβιακη Θεραπεία στην Πρωτοβάθμια Περίθαλψη» Τριμεθοπρίμη/σουλφaμεθοξαζόλη Αρχαία Ολυμπία 2017 Κ.Κανελλακοπούλου Γυναίκα 24 ετών προσέρχεται στο ΚΥ για δυσουρικά ενοχλήματα Αναφέρει
«Λοιμώξεις και Αντιμικροβιακη Θεραπεία στην Πρωτοβάθμια Περίθαλψη» Τριμεθοπρίμη/σουλφaμεθοξαζόλη Αρχαία Ολυμπία 2017 Κ.Κανελλακοπούλου Γυναίκα 24 ετών προσέρχεται στο ΚΥ για δυσουρικά ενοχλήματα Αναφέρει
Αναγκαιότητα για όλους; Μάμαλη Β. Επιμ.Β ΕΣΥ «Τζάνειο» Νοσ.Πειραιά
 «Ερμηνευτικό» ιάβασμα του Αντιβιογράμματος: Νοητική Άσκηση για λίγους ή Κλινική Αναγκαιότητα για όλους; Μάμαλη Β. Επιμ.Β ΕΣΥ «Τζάνειο» Νοσ.Πειραιά «Ερμηνεία» αντιβιογράμματος Από το φαινότυπο Στο μηχανισμό
«Ερμηνευτικό» ιάβασμα του Αντιβιογράμματος: Νοητική Άσκηση για λίγους ή Κλινική Αναγκαιότητα για όλους; Μάμαλη Β. Επιμ.Β ΕΣΥ «Τζάνειο» Νοσ.Πειραιά «Ερμηνεία» αντιβιογράμματος Από το φαινότυπο Στο μηχανισμό
Οι νέες τεχνολογίες στο σύγχρονο κλινικό εργαστήριο- Diagnostic stewardship
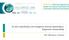 ΕΝΟΤΗΤΑ 5 Πολιτικές διαχείρισης κα Ελέγχου της Ιατρικής Τεχνολογίας: Νέε δυνατότητες-καλύτερα Αποτελέσματα Οι νέες τεχνολογίες στο σύγχρονο κλινικό εργαστήριο- Diagnostic stewardship Καθ. Αθανάσιος Τσακρής
ΕΝΟΤΗΤΑ 5 Πολιτικές διαχείρισης κα Ελέγχου της Ιατρικής Τεχνολογίας: Νέε δυνατότητες-καλύτερα Αποτελέσματα Οι νέες τεχνολογίες στο σύγχρονο κλινικό εργαστήριο- Diagnostic stewardship Καθ. Αθανάσιος Τσακρής
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ Α.Π.Θ. ΣΕΜΙΝΑΡΙΟ. «ΣΧΟΛΕΙΟ ΙΑΤΡΙΚΗΣ ΜΥΚΗΤΟΛΟΓΙΑΣ (εργαστηριακή διάγνωση-κλινικές προεκτάσεις)»
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ Α ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ Διευθύντρια: Καθηγήτρια Α. Παπά ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ Α.Π.Θ. Επιστημονικά υπεύθυνος: Τ. Α. Βυζαντιάδης Αναπληρωτής
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ Α ΕΡΓΑΣΤΗΡΙΟ ΜΙΚΡΟΒΙΟΛΟΓΙΑΣ Διευθύντρια: Καθηγήτρια Α. Παπά ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ Α.Π.Θ. Επιστημονικά υπεύθυνος: Τ. Α. Βυζαντιάδης Αναπληρωτής
Μια ενημέρωση για ασθενείς και παρόχους φροντίδας
 Μια ενημέρωση για ασθενείς και παρόχους φροντίδας Τι είναι το FoundationOne ; Το FoundationOne είναι μια εξέταση που ανιχνεύει γενωμικές μεταβολές (π.χ. μεταλλάξεις) που είναι γνωστό ότι σχετίζονται με
Μια ενημέρωση για ασθενείς και παρόχους φροντίδας Τι είναι το FoundationOne ; Το FoundationOne είναι μια εξέταση που ανιχνεύει γενωμικές μεταβολές (π.χ. μεταλλάξεις) που είναι γνωστό ότι σχετίζονται με
