ΚΕΦΑΛΑΙΟ 2 ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΚΑΘΑΡΩΝ ΟΥΣΙΩΝ.
|
|
|
- Ὅμηρος Μπλέτσας
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΚΕΦΑΛΑΙΟ 2 ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΚΑΘΑΡΩΝ ΟΥΣΙΩΝ. 2.1 Η ΕΝΝΟΙΑ ΤΗΣ ΚΑΘΑΡΗΣ ΟΥΣΙΑΣ. Μια ουσία της οποίας η χημική σύσταση παραμένει σταθερή σε όλη της την έκταση ονομάζεται καθαρή ουσία. Δεν είναι υποχρεωτικό να είναι ένα χημικό στοιχείο ή μια χημική ένωση. Ένα μίγμα χημικών στοιχείων ή ενώσεων μπορεί επίσης να είναι καθαρή ουσία εφόσον είναι ομογενές. Για παράδειγμα ο αέρας είναι καθαρή ουσία ενώ είναι μίγμα διαφόρων αερίων, έχει όμως ομοιόμορφη χημική σύσταση. Το μίγμα του νερού με το λάδι δεν είναι καθαρή ουσία, γιατί το λάδι δεν είναι διαλυτό στο νερό και συγκεντρώνεται πάνω από το νερό σχηματίζοντας δύο χημικά ανόμοιες περιοχές (ετερογενές μίγμα). Το μίγμα δύο ή περισσοτέρων φάσεων μιας καθαρής ουσίας είναι επίσης καθαρή ουσία, γιατί όλες οι φάσεις έχουν την ίδια χημική σύσταση. Το μίγμα πάγου και νερού είναι επίσης καθαρή ουσία, γιατί και οι δύο φάσεις έχουν την ίδια χημική σύσταση. Το μίγμα όμως της υγρής και της αέριας φάσης του αέρα δεν είναι καθαρή ουσία, γιατί η σύσταση του υγρού είναι διαφορετική από αυτή του αερίου και έτσι το μίγμα δεν είναι πλέον χημικά ομογενές. Αυτό οφείλεται στο ότι τα διάφορα συστατικά του αέρα σε συγκεκριμένη πίεση έχουν διαφορετικές θερμοκρασίες συμπύκνωσης. Σχήμα 10_Το άζωτο και ο αέρας είναι καθαρές ουσίες. Ένα μίγμα νερού στην υγρή και στην αέρια φάση είναι μια καθαρή ουσία (α), ενώ ένα μίγμα αέρα στην υγρή και στην αέρια φάση δεν είναι καθαρή ουσία (β). 1
2 2.2 ΔΙΕΡΓΑΣΙΕΣ ΑΛΛΑΓΗΣ ΦΑΣΗΣ ΤΩΝ ΚΑΘΑΡΩΝ ΟΥΣΙΩΝ. Σε πολλά παραδείγματα από την καθημερινότητα, δύο φάσεις μιας καθαρής ουσίας συνυπάρχουν σε ισορροπία. Στο βραστήρα και στο συμπυκνωτή μιας μονάδας παραγωγής ισχύος με υδρατμό, το νερό βρίσκεται με τη μορφή μίγματος υγρού και ατμού. Το ψυκτικό υγρό στα ψυγεία και στους κύκλους ψύξης μετατρέπεται από υγρό σε ατμό και αντίστροφα. Στη συνέχεια για την παρουσίαση των βασικών αρχών της διεργασίας εξάτμισης θα χρησιμοποιηθεί το παράδειγμα του νερού που είναι οικείο Συμπιεσμένο Υγρό και Κορεσμένο Υγρό. Θεωρούμε ένα σύστημα εμβόλου κυλίνδρου το οποίο περιέχει νερό σε θερμοκρασία 20 ο C. Υπό τις συνθήκες αυτές, το νερό βρίσκεται στην υγρή φάση και ονομάζεται συμπιεσμένο ή υπόψυκτο υγρό, υποδηλώνοντας ότι το υγρό δεν είναι έτοιμο να εξατμιστεί. Στη συνέχεια ζεσταίνουμε μέχρι να αυξηθεί η θερμοκρασία του για παράδειγμα στους 40 ο C. Σχήμα 11: Σε πίεση 1 atm και σε θερμοκρασία 20 ο C, το νερό βρίσκεται στην υγρή φάση (συμπιεσμένο υγρό). Σε πίεση 1 atm και στους 100 ο C, το νερό βρίσκεται στην κατάσταση του υγρού που είναι έτοιμο να εξατμιστεί (κορεσμένο υγρό). 2
3 Καθώς αυξάνεται η θερμοκρασία, ο όγκος του νερού στην υγρή φάση αυξάνεται, γεγονός που σημαίνει αύξηση του ειδικού όγκου του νερού. Το έμβολο, παρακολουθώντας την αύξηση του όγκου, θα μετακινηθεί ελαφρά προς τα πάνω. Η πίεση στο εσωτερικό του κυλίνδρου θα παραμείνει ίση με 1 atm, αφού εξαρτάται μόνο από την εξωτερική βαρομετρική πίεση και το βάρος του εμβόλου, τα οποία παραμένουν σταθερά. Το νερό συνεχίζει να βρίσκεται στην κατάσταση του συμπιεσμένου υγρού, αφού στις συνθήκες αυτές δεν έχει αρχίσει η εξάτμιση. Καθώς μεταφέρεται περισσότερη θερμότητα στο υγρό, η θερμοκρασία συνεχίζει να αυξάνεται ως τους 100 ο C (κατάσταση 2). Στο σημείο αυτό, το νερό συνεχίζει να είναι υγρό, αλλά οποιαδήποτε επιπλέον προσθήκη θερμότητας, όσο μικρή και αν είναι θα οδηγήσει σε εξάτμιση ενός μέρους του υγρού. Αυτό σημαίνει ότι η διεργασία αλλαγής φάσης είναι έτοιμη να αρχίσει. Το υγρό που είναι έτοιμο να εξατμιστεί ονομάζεται κορεσμένο υγρό (κατάσταση 2) Κορεσμένος Ατμός και Υπέρθερμος Ατμός. Όταν αρχίσει ο βρασμός, η θερμοκρασία παύει να αυξάνεται μέχρι να εξατμιστεί όλο το υγρό. Δηλαδή η θερμοκρασία παραμένει σταθερή σε όλη τη διεργασία αλλαγής φάσης, εάν η πίεση παραμείνει σταθερή. Κατά τη διάρκεια της διεργασίας εξάτμισης (βρασμός), οι μόνες μεταβολές που παρατηρούνται είναι η μεγάλη αύξηση του όγκου και η σταθερή πτώση της στάθμης του υγρού. Στο ενδιάμεσο περίπου της διεργασίας εξάτμισης (κατάσταση 3), ο κύλινδρος περιέχει ίσες ποσότητες υγρού και ατμού. Με την προσθήκη επιπλέον θερμότητας, η εξάτμιση θα συνεχιστεί μέχρι να εξατμιστεί και η τελευταία σταγόνα του υγρού (κατάσταση 4). Στο σημείο αυτό ολόκληρος ο κύλινδρος είναι γεμάτος με ατμό και βρίσκεται στο όριο να υγροποιηθεί. Οποιαδήποτε επιπλέον απώλεια θερμότητας από τον ατμό αυτό θα προκαλέσει συμπύκνωση μέρους του ατμού (αλλαγή φάσης από ατμό σε υγρό). Ο ατμός που είναι έτοιμος να υγροποιηθεί ονομάζεται κορεσμένος ατμός. Μια ουσία μεταξύ των καταστάσεων 2 και 4 αναφέρεται ως μίγμα κορεσμένου υγρού ατμού, γιατί στις καταστάσεις αυτές η υγρή και η αέρια φάση συνυπάρχουν σε ισορροπία. Όταν ολοκληρωθεί η διεργασία αλλαγής φάσης, το σύστημα θα βρεθεί στη φάση του ατμού και οποιαδήποτε νέα προσθήκη θερμότητας, θα προκαλέσει αύξηση της θερμοκρασίας και του ειδικού όγκου. 3
4 Σχήμα 12: Καθώς μεταφέρεται περισσότερη θερμότητα (κατάσταση 3), ένα μέρος του κορεσμένου υγρού εξατμίζεται (μίγμα κορεσμένου υγρού και ατμού). Σε πίεση 1 atm, η θερμοκρασία παραμένει σταθερή στους 100 ο C (κατάσταση 4) μέχρι να εξατμιστεί και η τελευταία σταγόνα υγρού (κορεσμένος ατμός). Στην κατάσταση 5 η θερμοκρασία του ατμού είναι για παράδειγμα 300 ο C. Εάν ένα ποσό θερμότητας απομακρυνθεί από τον ατμό, τότε η θερμοκρασία του θα ελαττωθεί αλλά δεν θα λάβει χώρα συμπύκνωση, εφόσον η θερμοκρασία παραμένει πάνω από τους 100 ο C (για πίεση 1 atm). O ατμός που δεν είναι έτοιμος να συμπυκνωθεί (ο ατμός που δεν είναι κορεσμένος) ονομάζεται υπέρθερμος ατμός. Σχήμα 13: (α)καθώς μεταφέρεται περισσότερη θερμότητα προς τον ατμό, η θερμοκρασία του αρχίζει να αυξάνεται (υπέρθερμος ατμός). (β) Διάγραμμα T υ για τη διεργασία προσθήκης θερμότητας στο νερό σε σταθερή πίεση. 4
5 Αν η παραπάνω διαδικασία επαναληφθεί αντίστροφα, ψύχοντας το νερό ενώ η πίεση διατηρείται παράλληλα σταθερή, τότε το νερό θα επιστρέψει στην κατάσταση 1 ακολουθώντας την ίδια διαδρομή. Κατά την αντίστροφη πορεία, το ποσό θερμότητας που εκλύεται είναι ακριβώς ίσο με το ποσό θερμότητας που προσδόθηκε στο νερό κατά τη διεργασία της θέρμανσης Θερμοκρασία Κορεσμού και Πίεση Κορεσμού. Η θερμοκρασία στην οποία το νερό αρχίζει να βράζει εξαρτάται από την πίεση, γεγονός που σημαίνει ότι εάν η πίεση παραμείνει σταθερή, το ίδιο θα συμβεί και με τη θερμοκρασία βρασμού. Σε μια δεδομένη πίεση, η θερμοκρασία στην οποία μια καθαρή ουσία αρχίζει να βράζει ονομάζεται θερμοκρασία κορεσμού T sat. Όμοια, σε μια δεδομένη θερμοκρασία, η πίεση στην οποία μια καθαρή ουσία αρχίζει να βράζει ονομάζεται πίεση κορεσμού P sat. Για όλες τις ουσίες υπάρχουν πίνακες κορεσμού, που περιέχουν τις τιμές της πίεσης κορεσμού σε διάφορες θερμοκρασίες (ή της θερμοκρασίας κορεσμού σε διάφορες πιέσεις). ΠΙΝΑΚΑΣ 2-1_Πίεση κορεσμού (βρασμού) του νερού σε διάφορες θερμοκρασίες. Σύμφωνα με τον παραπάνω πίνακα, η πίεση του νερού που αλλάζει φάση (βράζει ή συμπυκνώνεται) στους 25 ο C θα πρέπει να είναι 3.17 kpa, ενώ για να βράσει το νερό στους 250 ο C 5
6 η πίεση θα πρέπει να διατηρείται στα 3973 kpa (περίπου 40 atm). Ακόμα το νερό μπορεί να παγώσει αν η πίεσή του γίνει μικρότερη από 0.61 kpa. Για να λιώσει ένα στερεό ή για να εξατμιστεί ένα υγρό χρειάζεται μεγάλο ποσό ενέργειας. To ποσό της ενέργειας, που απορροφάται ή απελευθερώνεται, κατά τη διάρκεια της μετάβασης μιας ουσίας από τη μία φάση στην άλλη, ονομάζεται λανθάνουσα θερμότητα. Ειδικότερα το ποσό της ενέργειας που απορροφάται κατά την τήξη ονομάζεται λανθάνουσα θερμότητα τήξης και είναι ισοδύναμο με το ποσό της ενέργειας που αποβάλλεται κατά την πήξη. Το ποσό της ενέργειας που απορροφάται κατά την εξάτμιση ονομάζεται λανθάνουσα θερμότητα εξάτμισης και είναι ισοδύναμο με το ποσό της ενέργειας που απελευθερώνεται κατά την συμπύκνωση. Το μέγεθος της λανθάνουσας θερμότητας εξαρτάται από τη θερμοκρασία ή την πίεση στην οποία λαμβάνει χώρα η αλλαγή φάσης. Όταν πραγματοποιείται αλλαγή φάσης, η θερμοκρασία και η πίεση είναι εξαρτημένες μεταβλητές και συνδέονται (T sat = f(p sat )). H σχέση αυτή περιγράφεται από την καμπύλη κορεσμού αερίου υγρού. Οι καμπύλες αυτού του είδους είναι χαρακτηριστικές για κάθε καθαρή ουσία. Σχήμα 14: Καμπύλη κορεσμού αερίου υγρού για καθαρή ουσία (οι τιμές αναφέρονται στο νερό). 6
7 2.2.4 Συνέπειες της εξάρτησης από τη Θερμοκρασία Κορεσμού (Tsat )και Πίεση Κορεσμού (Psat.). Σύμφωνα με τα παραπάνω σε μια συγκεκριμένη πίεση μια ουσία θα βράσει στη θερμοκρασία κορεσμού που αντιστοιχεί στην πίεση αυτή. Για την καλύτερη αντίληψη των φαινομένων θεωρείται ένα σφραγισμένο κουτί που περιέχει ψυκτικό υγρό R134 α σε ένα δωμάτιο θερμοκρασίας 25 ο C. Αν το κουτί βρίσκεται αρκετή ώρα στο δωμάτιο η θερμοκρασία του ψυκτικού μέσα στο κουτί θα είναι επίσης 25 ο C. Αν ανοίξουμε το καπάκι αργά και αφήσουμε να διαφύγει μια ποσότητα ψυκτικού, η πίεση μέσα στο κουτί θα αρχίσει να μειώνεται μέχρι να γίνει ίση με την ατμοσφαιρική. Αν κάποιος κρατάει το κουτί θα παρατηρήσει ότι η θερμοκρασία του μειώνεται γρήγορα και ότι σχηματίζεται πάγος στο εξωτερικό του (αν ο αέρας περιέχει υγρασία). Αν εισαχθεί ένα θερμόμετρο στο κουτί, θα δείξει την τιμή - 26 ο C σε πίεση μιας ατμόσφαιρας, που είναι η θερμοκρασία κορεσμού του ψυκτικού R134 α στη συγκεκριμένη πίεση. Η θερμοκρασία του υγρού ψυκτικού θα παραμείνει στους - 26 ο C μέχρι να εξατμιστεί και η τελευταία σταγόνα του. Πρέπει να σημειωθεί ότι το υγρό δεν μπορεί να εξατμιστεί παρά μόνο αν απορροφήσει ενέργεια ίση με την λανθάνουσα θερμότητα εξάτμισης, που στην περίπτωση του ψυκτικού R134 α είναι ίση με 217 KJ/Kg σε πίεση 1 atm. Άρα ο ρυθμός εξάτμισης του ψυκτικού εξαρτάται από το ρυθμό μεταφοράς θερμότητας στο κουτί, δηλαδή όσο μεγαλύτερος είναι ο ρυθμός μεταφοράς θερμότητας, τόσο μεγαλύτερος είναι ο ρυθμός εξάτμισης. Οι ρυθμοί αυτοί μπορούν να ελαχιστοποιηθούν μονώνοντας κατάλληλα το κουτί. Στην οριακή περίπτωση μηδενικής μεταφοράς θερμότητας το ψυκτικό θα παραμείνει στο κουτί σε υγρή κατάσταση και σε θερμοκρασία - 26 ο C. 2.3 ΔΙAΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ. Στη διεργασία εμβόλου κυλίνδρου προσθέτουμε βάρος στο έμβολο μέχρι η πίεση στο εσωτερικό του κυλίνδρου να γίνει 1 MPa. Στην πίεση αυτή, το νερό θα έχει ειδικό όγκο λίγο μικρότερο από αυτόν που είχε σε πίεση 1 atm. Στη νέα αυτή πίεση, καθώς μεταφέρεται θερμότητα προς το νερό, η όλη διεργασία θα ακολουθήσει μια διαδρομή ανάλογη με την πρώτη όπως φαίνεται και στο Σχήμα 15 αλλά με ορισμένες αξιοσημείωτες διαφορές. 7
8 Το νερό θα αρχίσει να βράζει σε πολύ υψηλότερη θερμοκρασία (179.9 ο C). Ο ειδικός όγκος του κορεσμένου υγρού θα είναι μεγαλύτερος και ο ειδικός όγκος του κορεσμένου ατμού μικρότερος από τις αντίστοιχες τιμές στην πίεση 1 atm. Αυτό σημαίνει ότι η οριζόντια γραμμή που ενώνει τις καμπύλες του κορεσμένου υγρού και του κορεσμένου ατμού θα είναι μικρότερη. Καθώς η πίεση συνεχίζει να αυξάνει, η γραμμή κορεσμού γίνεται όλο και μικρότερη, όπως φαίνεται και στο σχήμα παρακάτω και καταλήγει να γίνει ένα σημείο, συγκεκριμένα για το νερό σε P = MPa. To σημείο αυτό λέγεται κρίσιμο σημείο και ορίζεται ως το σημείο εκείνο στο οποίο, οι καταστάσεις του κορεσμένου υγρού και του κορεσμένου ατμού, γίνονται ίδιες μεταξύ τους. Σχήμα 15_Διάγραμμα T υ για ισοβαρείς διεργασίες αλλαγής φάσης μιας καθαρής ουσίας, σε διάφορες πιέσεις (οι αριθμητικές τιμές αναφέρονται στο νερό). 8
9 Σε πιέσεις μεγαλύτερης της κρίσιμης πίεσης δεν υπάρχει διακριτή διαδικασία αλλαγής φάσης. Στις πιέσεις αυτές, ο ειδικός όγκος της ουσίας αυξάνεται συνεχώς και σε κάθε χρονική στιγμή είναι παρούσα μόνο μια φάση της ουσίας. Η τελική φάση θα είναι ατμός αλλά δεν είναι διακριτό το πότε συνέβη η αλλαγή. Πάνω από την κρίσιμη κατάσταση δεν υπάρχει γραμμή που να ξεχωρίζει τη φάση του συμπιεσμένου υγρού από τη φάση του υπέρθερμου ατμού. Μια ουσία όμως συνηθίζεται να λέγεται υπέρθερμος ατμός σε θερμοκρασίες μεγαλύτερες της κρίσιμης θερμοκρασίας και συμπιεσμένο υγρό σε θερμοκρασίες χαμηλότερες της κρίσιμης θερμοκρασίας. Στο Σχήμα 15 οι καταστάσεις κορεσμένου υγρού στις διάφορες πιέσεις μπορούν να ενωθούν με μια γραμμή που λέγεται καμπύλη κορεσμένου υγρού. Ανάλογα οι καταστάσεις κορεσμένου ατμού μπορούν να συνδεθούν με την καμπύλη κορεσμένου ατμού. Οι δύο αυτές καμπύλες συναντώνται στο κρίσιμο σημείο σχηματίζοντας ένα θόλο, όπως φαίνεται και στο Σχήμα 16. Όλες οι καταστάσεις συμπιεσμένου υγρού βρίσκονται αριστερά της καμπύλης κορεσμένου υγρού και η περιοχή αυτή ονομάζεται περιοχή συμπιεσμένου υγρού. Σχήμα 16_Διάγραμμα T υ για μια καθαρή ουσία. υ 9
10 Όλες οι καταστάσεις υπέρθερμου ατμού βρίσκονται στην περιοχή δεξιά της καμπύλης κορεσμένου ατμού και η περιοχή αυτή λέγεται περιοχή υπέρθερμου ατμού. Στις δύο παραπάνω περιοχές η ουσία υφίσταται σε μία μόνο φάση υγρού ή ατμού. Όλες εκείνες οι καταστάσεις που περιέχουν δύο φάσεις σε ισορροπία βρίσκονται στο εσωτερικό του θόλου, που λέγεται περιοχή μίγματος κορεσμένου υγρού και ατμού. H γενική μορφή των διαγραμμάτων P υ είναι σχεδόν ίδια με αυτή των διαγραμμάτων Τ υ, όπως φαίνεται και στο Σχήμα 18, με τη διαφορά ότι οι καμπύλες σταθερής θερμοκρασίας έχουν φορά προς τα κάτω. Θεωρούμε πάλι τη διάταξη εμβόλου κυλίνδρου, η οποία περιέχει νερό σε υγρή κατάσταση σε πίεση 1 MPa και σε θερμοκρασία 25 ο C. Στις συνθήκες αυτές το νερό βρίσκεται σε συνθήκες συμπιεσμένου υγρού. Σχήμα 17_Σε μια διάταξη εμβόλου κυλίνδρου η πίεση μπορεί να ελαττωθεί με την αφαίρεση βάρους από το έμβολο. Στη συνέχεια αφαιρούνται τα βάρη πάνω από το έμβολο, ώστε η πίεση στο εσωτερικό του κυλίνδρου να ελαττωθεί βαθμιαία. Το νερό μπορεί να εναλλάσσει θερμότητα με το περιβάλλον και έτσι η θερμοκρασία του να παραμένει σταθερή. Καθώς η πίεση ελαττώνεται, ο όγκος του υγρού θα αυξηθεί ελαφρά. Όταν η πίεση φτάσει στην τιμή κορεσμού για τη συγκεκριμένη θερμοκρασία ( ΜPa), το υγρό θα αρχίσει να βράζει. Κατά τη διάρκεια της εξάτμισης, η θερμοκρασία και η πίεση θα παραμένουν σταθερές, ο ειδικός όγκος όμως θα αυξηθεί. Από τη 10
11 στιγμή που θα εξατμιστεί και η τελευταία σταγόνα του υγρού, κάθε επιπλέον ελάττωση της πίεσης θα έχει σαν αποτέλεσμα την περαιτέρω αύξηση του ειδικού όγκου. Πρέπει να σημειωθεί ότι κατά τη διάρκεια της αλλαγής φάσης δεν αφαιρέθηκε κανένα βάρος από το έμβολο. Αν κάτι τέτοιο συνέβαινε, θα προκαλούσε πτώση της πίεσης και κατά συνέπεια και της θερμοκρασίας [αφού Tsat = f(psat)] και η διαδικασία δεν θα ήταν πλέον ισόθερμη. Εάν η διαδικασία επαναληφθεί και σε άλλες θερμοκρασίες, οι διαδικασίες αλλαγής φάσης που θα ακολουθήσουν παρόμοιες διαδρομές. Ενώνοντας τα σημεία που αντιστοιχούν,στις καταστάσεις κορεσμένου υγρού και κορεσμένου ατμού με μια καμπύλη, κατασκευάζεται έτσι το διάγραμμα P υ μιας καθαρής ουσίας όπως φαίνεται και στο Σχήμα 18. Σχήμα 18_Διάγραμμα P υ για μια καθαρή ουσία. 11
12 2.4 ΠΙΕΣΗ ΑΤΜΩΝ ΚΑΙ ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ Η πίεση που αναπτύσσεται στο εσωτερικό ενός δοχείου που περιέχει κάποιο αέριο οφείλεται στις συγκρούσεις των μεμονωμένων μορίων με τα τοιχώματα του δοχείου. Αποτέλεσμα αυτών των συγκρούσεων είναι η άσκηση μιας δύναμης στα τοιχώματα ανάλογη της μέσης ταχύτητας των μορίων ανά μονάδα όγκου του δοχείου (δηλ. με τη γραμμομοριακή πυκνότητα). Επομένως, η πίεση που ασκεί ένα αέριο εξαρτάται σε μεγάλο βαθμό από την πυκνότητα και τη θερμοκρασία του αερίου. Η πίεση ενός αερίου μίγματος, είναι το άθροισμα των πιέσεων που ασκούν τα μεμονωμένα αέρια συστατικά του. Οι πιέσεις αυτές ονομάζονται μερικές πιέσεις. Ο ατμοσφαιρικός αέρας μπορεί να θεωρηθεί μίγμα ξηρού αέρα (αέρα με μηδενικό περιεχόμενο υγρασίας) και ατμών νερού (οι οποίοι αναφέρονται και ως υγρασία). Στην περίπτωση αυτή η ατμοσφαιρική πίεση είναι το άθροισμα της πίεσης του ξηρού αέρα P α και της πίεσης των ατμών του νερού, η οποία ονομάζεται πίεση των ατμών P ν ή τάση ατμών. Ισχύει δηλαδή: P atm = P α + P ν (1) To ποσό των ατμών στον αέρα, παίζει σημαντικό ρόλο σε πολλές διεργασίες, όπως στην ξήρανση και στον κλιματισμό ενός χώρου. Ο αέρας μπορεί να συγκρατήσει μόνο ένα συγκεκριμένο ποσό υγρασίας και ο λόγος του ποσού αυτού σε μια δεδομένη θερμοκρασία προς το μέγιστο δυνατό ποσό υγρασίας που μπορεί να περιέχει ο αέρας στη θερμοκρασία αυτή ονομάζεται σχετική υγρασία φ. Οι τιμές της σχετικής υγρασίας κυμαίνονται από 0 (ξηρός αέρας) έως 100 (κορεσμένος αέρας, δηλαδή αέρας που δεν μπορεί να συγκρατήσει περισσότερη υγρασία). Η πίεση των ατμών του κορεσμένου αέρα σε μια δεδομένη θερμοκρασία είναι ίση με την πίεση κορεσμού του νερού στη θερμοκρασία αυτή. Για παράδειγμα η πίεση των ατμών του κορεσμένου αέρα στους 25 0 C είναι 3.17 kpa. To ποσό της υγρασίας στον αέρα καθορίζεται πλήρως, από τη θερμοκρασία και τη σχετική υγρασία. Η πίεση των ατμών συνδέεται με τη σχετική υγρασία με τη σχέση: P ν = P sat,t (2) όπου P sat,t η πίεση κορεσμού του νερού στη συγκεκριμένη θερμοκρασία. 12
13 Για παράδειγμα η πίεση των ατμών του αέρα στους 25 0 C και σε σχετική υγρασία 60% είναι : P ν = P = 0.6 x (3.17 kpa) = 1.9 kpa. (3) 0 sat 25 C Οι επιθυμητές τιμές σχετικής υγρασίας για να υπάρχει ένα θερμικά άνετο περιβάλλον κυμαίνονται σε 40% - 60%. Αξίζει να σημειωθεί ότι το ποσό της υγρασίας που μπορεί να κατακρατήσει ο αέρας είναι ανάλογο της πίεσης κορεσμού που αυξάνεται με τη θερμοκρασία. Άρα ο αέρας μπορεί να κατακρατήσει περισσότερη υγρασία σε υψηλότερες θερμοκρασίες. Η μείωση της θερμοκρασίας του υγρού αέρα έχει ως αποτέλεσμα τη μείωση της χωρητικότητάς του σε υγρασία και μπορεί να οδηγήσει στη συμπύκνωση μέρους της υγρασίας με τη μορφή αιωρούμενων σταγονιδίων νερού (ομίχλη) ή με τη μορφή υγρού στρώματος πάνω σε κρύες επιφάνειες (δροσιά). Η ομίχλη και η δροσιά εμφανίζονται συχνά σε τοποθεσίες με υψηλή υγρασία, ιδιαίτερα τις πρώτες πρωινές ώρες, όταν η θερμοκρασία είναι χαμηλότερη. Εξαφανίζονται (εξατμίζονται) μετά την ανατολή του ήλιου, καθώς αυξάνεται η θερμοκρασία του αέρα. Γενικά όποτε υπάρχει μια ανισορροπία μιας ποσότητας σε ένα μέσο, η φύση τείνει να την ανακατανέμει μέχρι να επιτευχθεί ισορροπία ή ισότητα. Η τάση αυτή συχνά χαρακτηρίζεται ως κινητήρια ή ωθούσα δύναμη. Πρόκειται για το μηχανισμό που ευθύνεται για πολλά φυσικά φαινόμενα μεταφοράς, όπως η μεταφορά θερμότητας, μάζας, ενέργειας, Αν η ποσότητα που μεταφέρεται ανά μονάδα όγκου οριστεί ως συγκέντρωση, η ροή της ποσότητας αυτής έχει πάντα την κατεύθυνση εκείνη προς την οποία μειώνεται η συγκέντρωση, δηλαδή η ροή κατευθύνεται από την περιοχή υψηλής συγκέντρωσης προς την περιοχή χαμηλής συγκέντρωσης. Η ροή αυτή είναι μια διεργασία διάχυσης. Η ύπαρξη μιας κινητήριας δύναμης ανάμεσα στις δύο φάσεις μιας ουσίας προκαλεί τη μετάβαση της μάζας από τη μία φάση στην άλλη. Το μέγεθος αυτής της δύναμης εξαρτάται από τις σχετικές συγκεντρώσεις των δύο φάσεων. Μια βρεγμένη μπλούζα θα στεγνώσει πολύ πιο γρήγορα σε ξηρό αέρα παρά σε υγρό. Αν η σχετική υγρασία του περιβάλλοντος είναι 100% (δηλαδή ο αέρας είναι κορεσμένος με υδρατμούς) δεν πρόκειται να στεγνώσει καθόλου. Στην περίπτωση αυτή δεν θα υπάρξει μετάβαση από την υγρή φάση στη φάση των ατμών, αλλά το σύστημα θα βρίσκεται σε ισορροπία φάσεων. Στην περίπτωση του υγρού νερού που είναι ανοικτό στην ατμόσφαιρα, το κριτήριο της ισορροπίας φάσεων διατυπώνεται ως εξής: 13
14 H πίεση των ατμών στον αέρα θα πρέπει να είναι ίση με την πίεση κορεσμού του νερού, στη θερμοκρασία του νερού. Ή αλλιώς: To κριτήριο ισορροπίας φάσεων για νερό που εκτίθεται στον αέρα: P ν = P sat,water, T Eπομένως, εάν η πίεση των ατμών στον αέρα είναι μικρότερη από την πίεση κορεσμού του νερού στη θερμοκρασία του νερού, τότε μέρος του υγρού θα εξατμιστεί. Όσο μεγαλύτερη είναι η διαφορά ανάμεσα στην πίεση των ατμών και στην πίεση κορεσμού τόσο μεγαλύτερος είναι ο ρυθμός εξάτμισης. Η εξάτμιση θα έχει ψυκτική επίδραση στο νερό και θα μειώσει τη θερμοκρασία του. Κατά συνέπεια θα μειωθεί η πίεση κορεσμού του νερού και άρα ο ρυθμός εξάτμισης, μέχρι να επιτευχθεί κάποια σταθερή κατάσταση. Έτσι εξηγείται το γεγονός ότι το νερό βρίσκεται συνήθως σε αρκετά χαμηλότερη θερμοκρασία από τον αέρα, ιδιαίτερα σε ξηρά κλίματα. Για τον ίδιο λόγο μπορεί να αυξηθεί ο ρυθμός εξάτμισης του νερού αυξάνοντας τη θερμοκρασία του νερού και άρα την πίεση κορεσμού του νερού. Στο σημείο αυτό θα πρέπει να σημειωθεί ότι ο αέρας που βρίσκεται στην επιφάνεια του νερού θα είναι πάντα κορεσμένος, εξαιτίας της άμεσης επαφής του με το νερό και της πίεσης των ατμών. Έτσι η πίεση των ατμών στην επιφάνεια μιας λίμνης θα είναι η πίεση κορεσμού του νερού στην επιφάνεια. Αν ο αέρας δεν είναι κορεσμένος, η πίεση των ατμών θα μειωθεί και θα γίνει ίση με την πίεση στον αέρα σε κάποια απόσταση από την επιφάνεια του νερού. Η διαφορά ανάμεσα στις δύο αυτές πιέσεις ατμών θα είναι η κινητήρια δύναμη της εξάτμισης του νερού Παράδειγμα: Πτώση Πίεσης της Θερμοκρασίας μιας λίμνης λόγω εξάτμισης. Μια καλοκαιρινή μέρα η θερμοκρασία του αέρα πάνω από μια λίμνη είναι 25 0 C. Να υπολογιστεί η θερμοκρασία του νερού της λίμνης όταν επιτευχθεί ισορροπία φάσεων ανάμεσα στο νερό της λίμνης και τους ατμούς στον αέρα, αν η σχετική υγρασία στον αέρα είναι 10%, 80% και 100%. 14
15 Λύση: Η πίεση κορεσμού του νερού στους 25 0 C είναι 3.17 kpa. (Πίνακας 2-1). Οι πιέσεις των ατμών με δεδομένη τη σχετική υγρασία υπολογίζονται από τη σχέση (2) ως εξής: Σχετική υγρασία = 10% P ν1 = 1 P 0 = 0.1 x (3.17 kpa) = kpa. (4) sat 25 C Σχετική υγρασία = 80% P ν2 = 2 P 0 = 0.8 x (3.17 kpa) = kpa. (5) sat 25 C Σχετική υγρασία = 100% P ν3 = 3 P 0 = 1.0 x (3.17 kpa) = 3.17 kpa. (6) sat 25 C Οι θερμοκρασίες κορεσμού που αντιστοιχούν σε αυτές τις πιέσεις προσδιορίζονται με βάση τον πίνακα 2-1 με παρεμβολή. Τ 1 = -8 0 C, Τ 2 = C, Τ 3 = 25 0 C (7) Άρα, στην πρώτη περίπτωση το νερό θα παγώσει, παρά το γεγονός ότι ο αέρας του περιβάλλοντος είναι θερμός. Η θερμοκρασία του νερού θα πέσει στους -8 0 C στην οριακή περίπτωση της μηδενικής μεταφοράς θερμότητας στην επιφάνεια του νερού. Πρακτικά η θερμοκρασία του νερού θα μειωθεί και θα γίνει μικρότερη από τη θερμοκρασία του αέρα, χωρίς όμως να κατέβει κάτω από τους -8 0 C για δύο λόγους: (1) είναι απίθανο να είναι τόσο ξηρός ο αέρας στην επιφάνεια της λίμνης (σχετική υγρασία μόλις 10%), (2) καθώς μειώνεται η θερμοκρασία του νερού κοντά στην επιφάνειά του, η μεταφορά θερμότητας από τον αέρα και τα κατώτερα στρώματα του όγκου του νερού θα τείνει να αναπληρώσει αυτή την απώλεια θερμότητας και να εμποδίσει την υπερβολική μείωση της θερμοκρασίας του νερού. Η θερμοκρασία του νερού θα σταθεροποιηθεί όταν η θερμότητα, που προσδίδουν ο αέρας και ο όγκος του νερού, εξισωθεί με τη θερμότητα που χάνεται λόγω εξάτμισης, δηλαδή όταν επιτευχθεί μια δυναμική ισορροπία ανάμεσα στη μεταφορά θερμότητας και μάζας (αντί για ισορροπία φάσεων). Στην τρίτη περίπτωση το νερό θα έχει την ίδια θερμοκρασία με τον αέρα του περιβάλλοντος. Οι όροι βρασμός και εξάτμιση χρησιμοποιούνται συχνά για να δηλώσουν τη μετάβαση από την υγρή φάση στη φάση των ατμών. Αν και αναφέρονται στην ίδια φυσική διεργασία, διαφέρουν σε κάποια σημεία. 15
16 Η εξάτμιση λαμβάνει χώρα στη διεπιφάνεια υγρού ατμών όταν η πίεση των ατμών είναι μικρότερη από την πίεση κορεσμού του υγρού σε μια δεδομένη θερμοκρασία. Για παράδειγμα το νερό μιας λίμνης θερμοκρασίας 20 0 C θα εξατμιστεί στον αέρα στους 20 0 C και σε σχετική υγρασία 60%, αφού η πίεση κορεσμού του νερού στη θερμοκρασία αυτή είναι 2.34 kpa και η πίεση των ατμών του αέρα στις ίδιες συνθήκες θερμοκρασίας και σχετικής υγρασίας είναι 1.4 kpa. Πρέπει να σημειωθεί ότι κατά την εξάτμιση δεν σχηματίζονται ούτε μετακινούνται φυσαλίδες. O βρασμός λαμβάνει χώρα στη διεπιφάνεια στερεού υγρού, όταν το υγρό φέρεται σε επαφή με μια επιφάνεια που διατηρείται σε θερμοκρασία Τ S η οποία είναι αρκετά μεγαλύτερη από τη θερμοκρασία κορεσμού του υγρού Τ Sat. Για παράδειγμα σε πίεση 1 atm το υγρό νερό που βρίσκεται σε επαφή με μια στερεή επιφάνεια στους C θα βράσει, αφού η θερμοκρασία κορεσμού του νερού στην πίεση αυτή είναι C. Η διεργασία του βρασμού χαρακτηρίζεται από τη γρήγορη κίνηση φυσαλίδων του ατμού, οι οποίες σχηματίζονται στη διεπιφάνεια στερεού υγρού, στη συνέχεια αποσπώνται από την επιφάνεια και επιχειρούν να ανέβουν στην ελεύθερη επιφάνεια του υγρού. 2.5 ΕΝΘΑΛΠΙΑ Κατά την ανάλυση ορισμένων διεργασιών, ειδικά των διεργασιών παραγωγής ενέργειας και των διεργασιών ψύξης, συναντάται ο συνδυασμός των ιδιοτήτων U + PV. Ο συνδυασμός αυτός ορίζεται ως μια νέα ιδιότητα που λέγεται ενθαλπία. Δηλαδή Η = U + PV (kj) (8) ή ανά μονάδα μάζας h = u + Pυ (kj /kg ) (9) Η εκτεταμένη χρήση της ενθαλπίας ως θερμοδυναμική ιδιότητα οφείλεται στον Richard Mollier ο οποίος ανακάλυψε τη σημασία της ποσότητας u + Pυ στους στροβίλους υδρατμών και στην καταχώρηση των ιδιοτήτων του ατμού σε μορφή πινάκων και διαγραμμάτων (όπως το περίφημο διάγραμμα Mollier). 16
17 Βιβλιογραφία. 1. Cengel, Boles Θερμοδυναμική για Μηχανικούς Τόμος Β Εκδόσεις Α.Τζιόλα Θεσσαλονίκη Κουρεμένος Α. Δημήτριος Ψυκτικές Μηχανές και Εγκαταστάσεις Ίδρυμα Ευγενίδου Αθήνα Περράκης Κ.Κ Εργαστηριακές Ασκήσεις Τεχνικής Θερμοδυναμικής, Εργαστήριο Τεχνικής Θερμοδυναμικής Τμήμα Μηχανολόγων και Αεροναυπηγών Μηχανικών Πανεπιστήμιο Πατρών
Εφαρμοσμένη Θερμοδυναμική
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εφαρμοσμένη Θερμοδυναμική Ενότητα 2: Ιδιότητες Χατζηαθανασίου Βασίλειος Καδή Στυλιανή Τμήμα Ηλεκτρολόγων Μηχανικών και Μηχανικών Η/Υ Άδειες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εφαρμοσμένη Θερμοδυναμική Ενότητα 2: Ιδιότητες Χατζηαθανασίου Βασίλειος Καδή Στυλιανή Τμήμα Ηλεκτρολόγων Μηχανικών και Μηχανικών Η/Υ Άδειες
Συστήματα Βιομηχανικών Διεργασιών 6ο εξάμηνο
 Συστήματα Βιομηχανικών Διεργασιών 6ο εξάμηνο Μέρος ο : Εισαγωγικά (διαστ., πυκν., θερμ., πίεση, κτλ.) Μέρος 2 ο : Ισοζύγια μάζας Μέρος 3 ο : 9 ο μάθημα Εκτός ύλης ΔΠΘ-ΜΠΔ Συστήματα Βιομηχανικών Διεργασιών
Συστήματα Βιομηχανικών Διεργασιών 6ο εξάμηνο Μέρος ο : Εισαγωγικά (διαστ., πυκν., θερμ., πίεση, κτλ.) Μέρος 2 ο : Ισοζύγια μάζας Μέρος 3 ο : 9 ο μάθημα Εκτός ύλης ΔΠΘ-ΜΠΔ Συστήματα Βιομηχανικών Διεργασιών
Φάσεις μιας καθαρής ουσίας
 Αντικείμενο μαθήματος: ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι ΚΑΘΑΡΕΣ ΟΥΣΙΕΣ. Διαδικασίες αλλαγής φάσης. P-v, T-v, και P-T διαγράμματα ιδιοτήτων και επιφάνειες P-v-T Καθαρών ουσιών. Υπολογισμός θερμοδυναμικών ιδιοτήτων από πίνακες
Αντικείμενο μαθήματος: ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι ΚΑΘΑΡΕΣ ΟΥΣΙΕΣ. Διαδικασίες αλλαγής φάσης. P-v, T-v, και P-T διαγράμματα ιδιοτήτων και επιφάνειες P-v-T Καθαρών ουσιών. Υπολογισμός θερμοδυναμικών ιδιοτήτων από πίνακες
ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΘΕΡΜΟ ΥΝΑΜΙΚΗΣ
 ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΘΕΡΜΟ ΥΝΑΜΙΚΗΣ. Μια νοικοκυρά µαγειρεύει σε χύτρα, η οποία είναι: (α) ακάλυπτη, (β) καλυµµένη µε ελαφρύ καπάκι και (γ) καλυµµένη µε βαρύ καπάκι. Σε ποια περίπτωση ο χρόνος µαγειρέµατος θα
ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΘΕΡΜΟ ΥΝΑΜΙΚΗΣ. Μια νοικοκυρά µαγειρεύει σε χύτρα, η οποία είναι: (α) ακάλυπτη, (β) καλυµµένη µε ελαφρύ καπάκι και (γ) καλυµµένη µε βαρύ καπάκι. Σε ποια περίπτωση ο χρόνος µαγειρέµατος θα
ΠΟΛΥΦΑΣΙΚΑ ΣΥΣΤΗΜΑΤΑ
 . ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΟΛΥΦΑΣΙΚΑ ΣΥΣΤΗΜΑΤΑ ΣΩΤΗΡΗΣ ΤΣΙΒΙΛΗΣ, Καθ. ΕΜΠ 135 ΔΙΑΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ 1 2 3 4 1 στερεό (solid) 2 υγρό (liquid) 3 ατμός (vapor) 4 αέριο (gas) A 1+2+3
. ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΟΛΥΦΑΣΙΚΑ ΣΥΣΤΗΜΑΤΑ ΣΩΤΗΡΗΣ ΤΣΙΒΙΛΗΣ, Καθ. ΕΜΠ 135 ΔΙΑΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ 1 2 3 4 1 στερεό (solid) 2 υγρό (liquid) 3 ατμός (vapor) 4 αέριο (gas) A 1+2+3
Εφηρμοσμένη Θερμοδυναμική
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εφηρμοσμένη Θερμοδυναμική Ενότητα 11: Μίγματα Χατζηαθανασίου Βασίλειος Καδή Στυλιανή Τμήμα Ηλεκτρολόγων Μηχανικών και Μηχανικών Η/Υ Άδειες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εφηρμοσμένη Θερμοδυναμική Ενότητα 11: Μίγματα Χατζηαθανασίου Βασίλειος Καδή Στυλιανή Τμήμα Ηλεκτρολόγων Μηχανικών και Μηχανικών Η/Υ Άδειες
Ο «TRANSCRITICAL» ΨΥΚΤΙΚΟΣ ΚΥΚΛΟΣ ΤΟΥ CO2
 6--5 Ο «TRANSCRITICAL» ΨΥΚΤΙΚΟΣ ΚΥΚΛΟΣ ΤΟΥ CO2 Στα συνηθισμένα ψυκτικά ρευστά, η απόρριψη θερμότητας γίνεται υπό σταθερά θερμοκρασία, που είναι η θερμοκρασία συμπύκνωσης του ψυκτικού ρευστού. Όπως φαίνεται
6--5 Ο «TRANSCRITICAL» ΨΥΚΤΙΚΟΣ ΚΥΚΛΟΣ ΤΟΥ CO2 Στα συνηθισμένα ψυκτικά ρευστά, η απόρριψη θερμότητας γίνεται υπό σταθερά θερμοκρασία, που είναι η θερμοκρασία συμπύκνωσης του ψυκτικού ρευστού. Όπως φαίνεται
ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΚΑΙ ΤΑΣΗ ΑΤΜΩΝ
 ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΚΑΙ ΤΑΣΗ ΑΤΜΩΝ 2 Διεργασίες Πολυφασικών συστημάτων Πολλές διεργασίες στη Χημική Μηχανική στηρίζονται στη μεταφορά μάζας μεταξύ διαφορετικών φάσεων (αέρια, υγρή, στερεή) Εξάτμιση-Εξάχνωση
ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΚΑΙ ΤΑΣΗ ΑΤΜΩΝ 2 Διεργασίες Πολυφασικών συστημάτων Πολλές διεργασίες στη Χημική Μηχανική στηρίζονται στη μεταφορά μάζας μεταξύ διαφορετικών φάσεων (αέρια, υγρή, στερεή) Εξάτμιση-Εξάχνωση
Φάσεις μιας καθαρής ουσίας. Αλλαγές φάσεων καθαρών ουσιών
 ΘΕΡΜΙΚΕΣ ΕΓΚΑΤΑΣΤΑΣΕΙΣ ΚΑΘΑΡΕΣ ΟΥΣΙΕΣ Μια ουσία της οποίας η χημική σύσταση παραμένει σταθερή σε όλη της την έκταση ονομάζεται Καθαρή Ουσία Πχ νερό, άζωτο, ήλιο, διοξείδιο του άνθρακα κλπ. Επίσης θεωρούνται
ΘΕΡΜΙΚΕΣ ΕΓΚΑΤΑΣΤΑΣΕΙΣ ΚΑΘΑΡΕΣ ΟΥΣΙΕΣ Μια ουσία της οποίας η χημική σύσταση παραμένει σταθερή σε όλη της την έκταση ονομάζεται Καθαρή Ουσία Πχ νερό, άζωτο, ήλιο, διοξείδιο του άνθρακα κλπ. Επίσης θεωρούνται
Ειδική Ενθαλπία, Ειδική Θερµότητα και Ειδικός Όγκος Υγρού Αέρα
 θερµοκρασία που αντιπροσωπεύει την θερµοκρασία υγρού βολβού. Το ποσοστό κορεσµού υπολογίζεται από την καµπύλη του σταθερού ποσοστού κορεσµού που διέρχεται από το συγκεκριµένο σηµείο. Η απόλυτη υγρασία
θερµοκρασία που αντιπροσωπεύει την θερµοκρασία υγρού βολβού. Το ποσοστό κορεσµού υπολογίζεται από την καµπύλη του σταθερού ποσοστού κορεσµού που διέρχεται από το συγκεκριµένο σηµείο. Η απόλυτη υγρασία
P. kpa T, C v, m 3 /kg u, kj/kg Περιγραφή κατάστασης και ποιότητα (αν εφαρμόζεται) , ,0 101,
 Ασκήσεις Άσκηση 1 Να συμπληρώσετε τα κενά κελιά στον επόμενο πίνακα των ιδιοτήτων του νερού εάν παρέχονται επαρκή δεδομένα. Στην τελευταία στήλη να περιγράψετε την κατάσταση του νερού ως υπόψυκτο υγρό,
Ασκήσεις Άσκηση 1 Να συμπληρώσετε τα κενά κελιά στον επόμενο πίνακα των ιδιοτήτων του νερού εάν παρέχονται επαρκή δεδομένα. Στην τελευταία στήλη να περιγράψετε την κατάσταση του νερού ως υπόψυκτο υγρό,
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΛΥΜΕΝΑ ΘΕΜΑΤΑ
 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΛΥΜΕΝΑ ΘΕΜΑΤΑ 1 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 Θέμα 1 Επιλέγοντας το κατάλληλο διάγραμμα φάσεων για ένα πραγματικό
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΛΥΜΕΝΑ ΘΕΜΑΤΑ 1 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 Θέμα 1 Επιλέγοντας το κατάλληλο διάγραμμα φάσεων για ένα πραγματικό
ΕΙΣΑΓΩΓΗ ΣΤΗ ΜΗΧΑΝΟΛΟΓΙΑ (7 Ο ΕΞΑΜΗΝΟ)
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΕΙΣΑΓΩΓΗ ΣΤΗ ΜΗΧΑΝΟΛΟΓΙΑ (7 Ο ΕΞΑΜΗΝΟ) Νίκος Μ. Κατσουλάκος Μηχανολόγος Μηχανικός Ε.Μ.Π., PhD, Msc ΜΑΘΗΜΑ 4-1 Ο ΨΥΚΤΙΚΟΣ ΚΥΚΛΟΣ, ΤΟ
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΕΙΣΑΓΩΓΗ ΣΤΗ ΜΗΧΑΝΟΛΟΓΙΑ (7 Ο ΕΞΑΜΗΝΟ) Νίκος Μ. Κατσουλάκος Μηχανολόγος Μηχανικός Ε.Μ.Π., PhD, Msc ΜΑΘΗΜΑ 4-1 Ο ΨΥΚΤΙΚΟΣ ΚΥΚΛΟΣ, ΤΟ
2.6 Αλλαγές κατάστασης
 2.6 Αλλαγές κατάστασης 1. Όταν ένα στερεό θερμαίνεται, σε μια ορισμένη θερμοκρασία μετατρέπεται σε υγρό. Αυτό το φαινόμενο ονομάζεται τήξη. Η σταθερή θερμοκρασία στην οποία τήκεται το στερεό ονομάζεται
2.6 Αλλαγές κατάστασης 1. Όταν ένα στερεό θερμαίνεται, σε μια ορισμένη θερμοκρασία μετατρέπεται σε υγρό. Αυτό το φαινόμενο ονομάζεται τήξη. Η σταθερή θερμοκρασία στην οποία τήκεται το στερεό ονομάζεται
ΦΑΣΕΙΣ ΒΡΑΣΜΟΥ ΚΑΙ ΜΕΤΑΦΟΡΑ ΘΕΡΜΟΤΗΤΑΣ
 Ο εναλλάκτης ψύξης ονομάζεται και εξατμιστής. Τούτο διότι στο εσωτερικό του λαμβάνει χώρα μετατροπή του ψυκτικού ρευστού, από υγρό σε αέριο (εξάτμιση) σε μια κατάλληλη πίεση, ώστε η αντίστοιχη θερμοκρασία
Ο εναλλάκτης ψύξης ονομάζεται και εξατμιστής. Τούτο διότι στο εσωτερικό του λαμβάνει χώρα μετατροπή του ψυκτικού ρευστού, από υγρό σε αέριο (εξάτμιση) σε μια κατάλληλη πίεση, ώστε η αντίστοιχη θερμοκρασία
Φυσικοί μετασχηματισμοί καθαρών ουσιών
 Φυσικοί μετασχηματισμοί καθαρών ουσιών Ή εξάτμιση, η τήξη και η μετατροπή του γραφίτη σε διαμάντι αποτελούν συνηθισμένα παραδείγματα αλλαγών φάσης χωρίς μεταβολή της χημικής σύστασης. Ορισμός φάσης: Μια
Φυσικοί μετασχηματισμοί καθαρών ουσιών Ή εξάτμιση, η τήξη και η μετατροπή του γραφίτη σε διαμάντι αποτελούν συνηθισμένα παραδείγματα αλλαγών φάσης χωρίς μεταβολή της χημικής σύστασης. Ορισμός φάσης: Μια
ΕΞΙΣΩΣΗ CLAUSIUS-CLAPEYRON ΘΕΩΡΙΑ
 ΕΞΙΣΩΣΗ CLAUSIUS-CLAEYRON ΘΕΩΡΙΑ Περιεχόμενα 1. 3D Διάγραμμα Φάσης 2. Λανθάνουσα θερμότητα 3. Εξίσωση Clausius Clapeyron 4. Συμπιεστότητα 5. Θερμική διαστολή 6. Θερμοχωρητικότητα 1 στερεό στερεό+υγρό υγρό
ΕΞΙΣΩΣΗ CLAUSIUS-CLAEYRON ΘΕΩΡΙΑ Περιεχόμενα 1. 3D Διάγραμμα Φάσης 2. Λανθάνουσα θερμότητα 3. Εξίσωση Clausius Clapeyron 4. Συμπιεστότητα 5. Θερμική διαστολή 6. Θερμοχωρητικότητα 1 στερεό στερεό+υγρό υγρό
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 4 ΣΕΛΙ ΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΝΕΟ ΣΥΣΤΗΜΑ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑ ΙΚΕΣ ΕΞΕΤΑΣΕΙΣ HMEΡΗΣΙΩΝ ΕΠΑΓΓΕΛΜΑΤΙΚΩΝ ΛΥΚΕΙΩΝ ΠΕΜΠΤΗ 26 ΜΑΪΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ ΚΑΙ ΚΛΙΜΑΤΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΤΕΣΣΕΡΙΣ (4) ΘΕΜΑ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΝΕΟ ΣΥΣΤΗΜΑ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑ ΙΚΕΣ ΕΞΕΤΑΣΕΙΣ HMEΡΗΣΙΩΝ ΕΠΑΓΓΕΛΜΑΤΙΚΩΝ ΛΥΚΕΙΩΝ ΠΕΜΠΤΗ 26 ΜΑΪΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ ΚΑΙ ΚΛΙΜΑΤΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΤΕΣΣΕΡΙΣ (4) ΘΕΜΑ
ΤΕΙ Καβάλας, Τμήμα Δασοπονίας και Διαχείρισης Φυσικού Περιβάλλοντος Μάθημα: Μετεωρολογία-Κλιματολογία. Υπεύθυνη : Δρ Μάρθα Λαζαρίδου Αθανασιάδου
 7. ΤΟ ΝΕΡΟ ΤΗΣ ΑΤΜΟΣΦΑΙΡΑΣ ΤΕΙ Καβάλας, Τμήμα Δασοπονίας και Διαχείρισης Φυσικού Περιβάλλοντος Μάθημα: Μετεωρολογία-Κλιματολογία. Υπεύθυνη : Δρ Μάρθα Λαζαρίδου Αθανασιάδου 1 7. ΤΟ ΝΕΡΟ ΤΗΣ ΑΤΜΟΣΦΑΙΡΑΣ
7. ΤΟ ΝΕΡΟ ΤΗΣ ΑΤΜΟΣΦΑΙΡΑΣ ΤΕΙ Καβάλας, Τμήμα Δασοπονίας και Διαχείρισης Φυσικού Περιβάλλοντος Μάθημα: Μετεωρολογία-Κλιματολογία. Υπεύθυνη : Δρ Μάρθα Λαζαρίδου Αθανασιάδου 1 7. ΤΟ ΝΕΡΟ ΤΗΣ ΑΤΜΟΣΦΑΙΡΑΣ
ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ - 6 Η ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΗΣ Β ΓΥΜΝΑΣΙΟΥ
 ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ 6 Η ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΗΣ Β ΓΥΜΝΑΣΙΟΥ Κυριακή, 16 Μαΐου 2010 Ώρα : 10:00-12:30 Προτεινόμενες λύσεις ΘΕΜΑ 1 0 (12 μονάδες) Για τη μέτρηση της πυκνότητας ομοιογενούς πέτρας (στερεού
ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ 6 Η ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΗΣ Β ΓΥΜΝΑΣΙΟΥ Κυριακή, 16 Μαΐου 2010 Ώρα : 10:00-12:30 Προτεινόμενες λύσεις ΘΕΜΑ 1 0 (12 μονάδες) Για τη μέτρηση της πυκνότητας ομοιογενούς πέτρας (στερεού
Εφηρμοσμένη Θερμοδυναμική
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εφηρμοσμένη Θερμοδυναμική Ενότητα 8: Θερμοδυναμικά κύκλα Χατζηαθανασίου Βασίλειος Καδή Στυλιανή Τμήμα Ηλεκτρολόγων Μηχανικών και Μηχανικών
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εφηρμοσμένη Θερμοδυναμική Ενότητα 8: Θερμοδυναμικά κύκλα Χατζηαθανασίου Βασίλειος Καδή Στυλιανή Τμήμα Ηλεκτρολόγων Μηχανικών και Μηχανικών
Τμήμα Χημείας Μάθημα: Φυσικοχημεία Ι Εξέταση: Περίοδος Ιουνίου (21/6/2017)
 Τμήμα Χημείας Μάθημα: Φυσικοχημεία Ι Εξέταση: Περίοδος Ιουνίου -7 (//7). Δίνεται η θεμελιώδης εξίσωση για την εσωτερική ενέργεια ενός συστήματος ενός συστατικού όπου κατάλληλη σταθερά. Να προσδιορίσετε
Τμήμα Χημείας Μάθημα: Φυσικοχημεία Ι Εξέταση: Περίοδος Ιουνίου -7 (//7). Δίνεται η θεμελιώδης εξίσωση για την εσωτερική ενέργεια ενός συστήματος ενός συστατικού όπου κατάλληλη σταθερά. Να προσδιορίσετε
ΘΕΡΜΟΧΗΜΕΙΑ. Είδη ενέργειας ΘΕΡΜΟΔΥΝΑΜΙΚΟΙ ΟΡΙΣΜΟΙ
 ΘΕΡΜΟΧΗΜΕΙΑ Όλες οι χημικές αντιδράσεις περιλαμβάνουν έκλυση ή απορρόφηση ενέργειας υπό μορφή θερμότητας. Η γνώση του ποσού θερμότητας που συνδέεται με μια χημική αντίδραση έχει και πρακτική και θεωρητική
ΘΕΡΜΟΧΗΜΕΙΑ Όλες οι χημικές αντιδράσεις περιλαμβάνουν έκλυση ή απορρόφηση ενέργειας υπό μορφή θερμότητας. Η γνώση του ποσού θερμότητας που συνδέεται με μια χημική αντίδραση έχει και πρακτική και θεωρητική
Παράγοντες που επηρεάζουν τη θέση της χημικής ισορροπίας. Αρχή Le Chatelier.
 Παράγοντες που επηρεάζουν τη θέση της χημικής ισορροπίας. Αρχή Le Chatelier. H θέση ισορροπίας επηρεάζεται από τους εξής παράγοντες χημικής ισορροπίας: Τη συγκέντρωση των αντιδρώντων ή των προϊόντων. Την
Παράγοντες που επηρεάζουν τη θέση της χημικής ισορροπίας. Αρχή Le Chatelier. H θέση ισορροπίας επηρεάζεται από τους εξής παράγοντες χημικής ισορροπίας: Τη συγκέντρωση των αντιδρώντων ή των προϊόντων. Την
6.2. ΤΗΞΗ ΚΑΙ ΠΗΞΗ, ΛΑΝΘΑΝΟΥΣΕΣ ΘΕΡΜΟΤΗΤΕΣ
 45 6.1. ΓΕΝΙΚΑ ΠΕΡΙ ΦΑΣΕΩΝ ΜΕΤΑΤΡΟΠΕΣ ΦΑΣΕΩΝ Όλα τα σώµατα,στερεά -ά-αέρια, που υπάρχουν στη φύση βρίσκονται σε µια από τις τρεις φάσεις ή σε δύο ή και τις τρεις. Όλα τα σώµατα µπορεί να αλλάξουν φάση
45 6.1. ΓΕΝΙΚΑ ΠΕΡΙ ΦΑΣΕΩΝ ΜΕΤΑΤΡΟΠΕΣ ΦΑΣΕΩΝ Όλα τα σώµατα,στερεά -ά-αέρια, που υπάρχουν στη φύση βρίσκονται σε µια από τις τρεις φάσεις ή σε δύο ή και τις τρεις. Όλα τα σώµατα µπορεί να αλλάξουν φάση
ΥΠΟΔΕΙΓΜΑ ΘΕΩΡΗΤΙΚΩΝ ΕΡΩΤΗΣΕΩΝ ΕΞΕΤΑΣΕΩΝ
 ΥΠΟΔΕΙΓΜΑ ΘΕΩΡΗΤΙΚΩΝ ΕΡΩΤΗΣΕΩΝ ΕΞΕΤΑΣΕΩΝ 1. Πώς ορίζεται η περίσσεια αέρα και η ισχύς μίγματος σε μία καύση; 2. Σε ποιές περιπτώσεις παρατηρείται μή μόνιμη μετάδοση της θερμότητας; 3. Τί είναι η αντλία
ΥΠΟΔΕΙΓΜΑ ΘΕΩΡΗΤΙΚΩΝ ΕΡΩΤΗΣΕΩΝ ΕΞΕΤΑΣΕΩΝ 1. Πώς ορίζεται η περίσσεια αέρα και η ισχύς μίγματος σε μία καύση; 2. Σε ποιές περιπτώσεις παρατηρείται μή μόνιμη μετάδοση της θερμότητας; 3. Τί είναι η αντλία
Συστήματα Βιομηχανικών Διεργασιών 6ο εξάμηνο
 Συστήματα Βιομηχανικών Διεργασιών 6ο εξάμηνο Μέρος 1 ο : Εισαγωγικά (διαστ., πυκν., θερμ., πίεση, κτλ.) Μέρος 2 ο : Ισοζύγια μάζας Μέρος 3 ο : 8 ο μάθημα Εκτός ύλης ΔΠΘ-ΜΠΔ Συστήματα Βιομηχανικών Διεργασιών
Συστήματα Βιομηχανικών Διεργασιών 6ο εξάμηνο Μέρος 1 ο : Εισαγωγικά (διαστ., πυκν., θερμ., πίεση, κτλ.) Μέρος 2 ο : Ισοζύγια μάζας Μέρος 3 ο : 8 ο μάθημα Εκτός ύλης ΔΠΘ-ΜΠΔ Συστήματα Βιομηχανικών Διεργασιών
ΥΠΟΔΕΙΓΜΑ ΑΣΚΗΣΕΩΝ ΓΡΑΠΤΩΝ ΕΞΕΤΑΣΕΩΝ
 ΥΠΟΔΕΙΓΜΑ ΑΣΚΗΣΕΩΝ ΓΡΑΠΤΩΝ ΕΞΕΤΑΣΕΩΝ 1. Να υπολογιστεί η μαζική παροχή του ατμού σε (kg/h) που χρησιμοποιείται σε ένα θερμαντήρα χυμού με τα παρακάτω στοιχεία: αρχική θερμοκρασία χυμού 20 C, τελική θερμοκρασία
ΥΠΟΔΕΙΓΜΑ ΑΣΚΗΣΕΩΝ ΓΡΑΠΤΩΝ ΕΞΕΤΑΣΕΩΝ 1. Να υπολογιστεί η μαζική παροχή του ατμού σε (kg/h) που χρησιμοποιείται σε ένα θερμαντήρα χυμού με τα παρακάτω στοιχεία: αρχική θερμοκρασία χυμού 20 C, τελική θερμοκρασία
Κεφάλαιο 20. Θερμότητα
 Κεφάλαιο 20 Θερμότητα Εισαγωγή Για να περιγράψουμε τα θερμικά φαινόμενα, πρέπει να ορίσουμε με προσοχή τις εξής έννοιες: Θερμοκρασία Θερμότητα Θερμοκρασία Συχνά συνδέουμε την έννοια της θερμοκρασίας με
Κεφάλαιο 20 Θερμότητα Εισαγωγή Για να περιγράψουμε τα θερμικά φαινόμενα, πρέπει να ορίσουμε με προσοχή τις εξής έννοιες: Θερμοκρασία Θερμότητα Θερμοκρασία Συχνά συνδέουμε την έννοια της θερμοκρασίας με
ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ & ΚΛΙΜΑΤΙΣΜΟΥ ΕΠΑΛ
 ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ & ΚΛΙΜΑΤΙΣΜΟΥ ΕΠΑΛ Απαντήσεις Πανελλήνιων Εξετάσεων 2017-2018 ΕΚΠΑΙΔΕΥΤΙΚΟΣ: ΒΑΝΤΣΗΣ Β. ΓΕΩΡΓΙΟΣ ΜΗΧΑΝΟΛΟΓΟΣ ΜΗΧΑΝΙΚΟΣ ΠΕ17 ΘΕΜΑ Α. Α1. Να χαρακτηρίσετε τις προτάσεις που ακολουθούν, γράφοντας
ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ & ΚΛΙΜΑΤΙΣΜΟΥ ΕΠΑΛ Απαντήσεις Πανελλήνιων Εξετάσεων 2017-2018 ΕΚΠΑΙΔΕΥΤΙΚΟΣ: ΒΑΝΤΣΗΣ Β. ΓΕΩΡΓΙΟΣ ΜΗΧΑΝΟΛΟΓΟΣ ΜΗΧΑΝΙΚΟΣ ΠΕ17 ΘΕΜΑ Α. Α1. Να χαρακτηρίσετε τις προτάσεις που ακολουθούν, γράφοντας
panagiotisathanasopoulos.gr
 Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΙΑΧΕΙΡΙΣΗΣ ΕΝΕΡΓΕΙΑΚΩΝ ΠΟΡΩΝ ΘΕΡΜΟ ΥΝΑΜΙΚΗ Ι 1
 ΘΕΡΜΟ ΥΝΑΜΙΚΗ Ι ιδάσκων: Καθ. Α.Γ.Τοµπουλίδης ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΙΑΧΕΙΡΙΣΗΣ ΕΝΕΡΓΕΙΑΚΩΝ ΠΟΡΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΥΤΙΚΗΣ ΜΑΚΕ ΟΝΙΑΣ, ΚΟΖΑΝΗ Εαρινό εξάµηνο 2003-2004 Άσκηση 1: Κυλινδρικό έµβολο περιέχει αέριο το
ΘΕΡΜΟ ΥΝΑΜΙΚΗ Ι ιδάσκων: Καθ. Α.Γ.Τοµπουλίδης ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΙΑΧΕΙΡΙΣΗΣ ΕΝΕΡΓΕΙΑΚΩΝ ΠΟΡΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΥΤΙΚΗΣ ΜΑΚΕ ΟΝΙΑΣ, ΚΟΖΑΝΗ Εαρινό εξάµηνο 2003-2004 Άσκηση 1: Κυλινδρικό έµβολο περιέχει αέριο το
ΤΜΗΜΑ ΜΗΧΑΝΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΚΛΙΜΑΤΙΣΜΟΥ ΨΥΧΡΟΜΕΤΡΙΑ
 ΤΕΙ - ΧΑΛΚΙ ΑΣ Τµήµα Μηχανολογίας Εργαστ:Ψύξη-Κλιµατισµός- Θέρµανση & Α.Π.Ε. 34400 ΨΑΧΝΑ ΕΥΒΟΙΑΣ TEI - CHALKIDOS Department of Mecanical Engineering Cooling, Air Condit., Heating and R.E. Lab. 34400 PSACHNA
ΤΕΙ - ΧΑΛΚΙ ΑΣ Τµήµα Μηχανολογίας Εργαστ:Ψύξη-Κλιµατισµός- Θέρµανση & Α.Π.Ε. 34400 ΨΑΧΝΑ ΕΥΒΟΙΑΣ TEI - CHALKIDOS Department of Mecanical Engineering Cooling, Air Condit., Heating and R.E. Lab. 34400 PSACHNA
6.1 Θερμόμετρα και μέτρηση θερμοκρασίας
 ΚΕΦΑΛΑΙΟ 6 ο ΘΕΡΜΟΤΗΤΑ 6.1 Θερμόμετρα και μέτρηση θερμοκρασίας 1. Τι ονομάζεται θερμοκρασία; Το φυσικό μέγεθος που εκφράζει πόσο ζεστό ή κρύο είναι ένα σώμα ονομάζεται θερμοκρασία. 2. Πως μετράμε τη θερμοκρασία;
ΚΕΦΑΛΑΙΟ 6 ο ΘΕΡΜΟΤΗΤΑ 6.1 Θερμόμετρα και μέτρηση θερμοκρασίας 1. Τι ονομάζεται θερμοκρασία; Το φυσικό μέγεθος που εκφράζει πόσο ζεστό ή κρύο είναι ένα σώμα ονομάζεται θερμοκρασία. 2. Πως μετράμε τη θερμοκρασία;
ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ ΚΛΙΜΑΤΙΣΜΟΥ
 ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ ΚΛΙΜΑΤΙΣΜΟΥ 2/12/2018 ΚΑΡΑΓΚΙΑΟΥΡΗΣ ΝΙΚΟΛΑΟΣ ΘΕΜΑ 1 ο 1. Να γράψετε στο τετράδιό σας το γράμμα καθεμιάς από τις παρακάτω προτάσεις και δίπλα τη λέξη ΣΩΣΤΟ, αν είναι σωστή ή τη λέξη ΛΑΘΟΣ,
ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ ΚΛΙΜΑΤΙΣΜΟΥ 2/12/2018 ΚΑΡΑΓΚΙΑΟΥΡΗΣ ΝΙΚΟΛΑΟΣ ΘΕΜΑ 1 ο 1. Να γράψετε στο τετράδιό σας το γράμμα καθεμιάς από τις παρακάτω προτάσεις και δίπλα τη λέξη ΣΩΣΤΟ, αν είναι σωστή ή τη λέξη ΛΑΘΟΣ,
διαιρούμε με το εμβαδό Α 2 του εμβόλου (1)
 1)Συνήθως οι πτήσεις των αεροσκαφών γίνονται στο ύψος των 15000 m, όπου η θερμοκρασία του αέρα είναι 210 Κ και η ατμοσφαιρική πίεση 10000 N / m 2. Σε αεροδρόμιο που βρίσκεται στο ίδιο ύψος με την επιφάνεια
1)Συνήθως οι πτήσεις των αεροσκαφών γίνονται στο ύψος των 15000 m, όπου η θερμοκρασία του αέρα είναι 210 Κ και η ατμοσφαιρική πίεση 10000 N / m 2. Σε αεροδρόμιο που βρίσκεται στο ίδιο ύψος με την επιφάνεια
ΘΕΡΜΟΤΗΤΑ Πρόκειται για τρόπο μεταφοράς ενέργειας από ένα σώμα σε ένα άλλο λόγω διαφοράς θερμοκρασίας. Είναι διαφορετική από την εσωτερική (θερμική)
 ΘΕΡΜΙΔΟΜΕΤΡΙΑ ΘΕΡΜΟΤΗΤΑ Πρόκειται για τρόπο μεταφοράς ενέργειας από ένα σώμα σε ένα άλλο λόγω διαφοράς θερμοκρασίας. Είναι διαφορετική από την εσωτερική (θερμική) ενέργεια που έχει ένα σώμα. Συμβολίζεται
ΘΕΡΜΙΔΟΜΕΤΡΙΑ ΘΕΡΜΟΤΗΤΑ Πρόκειται για τρόπο μεταφοράς ενέργειας από ένα σώμα σε ένα άλλο λόγω διαφοράς θερμοκρασίας. Είναι διαφορετική από την εσωτερική (θερμική) ενέργεια που έχει ένα σώμα. Συμβολίζεται
Πείραμα 2 Αν αντίθετα, στο δοχείο εισαχθούν 20 mol ΗΙ στους 440 ºC, τότε το ΗΙ διασπάται σύμφωνα με τη χημική εξίσωση: 2ΗΙ(g) H 2 (g) + I 2 (g)
 Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
ΟΙ ΑΛΛΑΓΕΣ ΚΑΤΑΣΤΑΣΗΣ ΤΟΥ ΝΕΡΟΥ Ο «ΚΥΚΛΟΣ» ΤΟΥ ΝΕΡΟΥ
 ΟΙ ΑΛΛΑΓΕΣ ΚΑΤΑΣΤΑΣΗΣ ΤΟΥ ΝΕΡΟΥ Ο «ΚΥΚΛΟΣ» ΤΟΥ ΝΕΡΟΥ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 6 Τι πρέπει να γνωρίζεις Θεωρία 6.1 Να αναφέρεις τις τρεις φυσικές καταστάσεις στις οποίες μπορεί να βρεθεί ένα υλικό σώμα. Όπως και
ΟΙ ΑΛΛΑΓΕΣ ΚΑΤΑΣΤΑΣΗΣ ΤΟΥ ΝΕΡΟΥ Ο «ΚΥΚΛΟΣ» ΤΟΥ ΝΕΡΟΥ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 6 Τι πρέπει να γνωρίζεις Θεωρία 6.1 Να αναφέρεις τις τρεις φυσικές καταστάσεις στις οποίες μπορεί να βρεθεί ένα υλικό σώμα. Όπως και
Μελέτη και κατανόηση των διαφόρων φάσεων του υδρολογικού κύκλου.
 Ζαΐμης Γεώργιος Κλάδος της Υδρολογίας. Μελέτη και κατανόηση των διαφόρων φάσεων του υδρολογικού κύκλου. Η απόκτηση βασικών γνώσεων της ατμόσφαιρας και των μετεωρολογικών παραμέτρων που διαμορφώνουν το
Ζαΐμης Γεώργιος Κλάδος της Υδρολογίας. Μελέτη και κατανόηση των διαφόρων φάσεων του υδρολογικού κύκλου. Η απόκτηση βασικών γνώσεων της ατμόσφαιρας και των μετεωρολογικών παραμέτρων που διαμορφώνουν το
ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ
 ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ 2 Η ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑ Α ΦΥΣΙΚΗΣ Β ΓΥΜΝΑΣΙΟΥ Κυριακή, 16 Απριλίου 2006 Ώρα: 10:30 13.00 Προτεινόµενες Λύσεις ΜΕΡΟΣ Α 1. α) Η πυκνότητα του υλικού υπολογίζεται από τη m m m σχέση d
ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ 2 Η ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑ Α ΦΥΣΙΚΗΣ Β ΓΥΜΝΑΣΙΟΥ Κυριακή, 16 Απριλίου 2006 Ώρα: 10:30 13.00 Προτεινόµενες Λύσεις ΜΕΡΟΣ Α 1. α) Η πυκνότητα του υλικού υπολογίζεται από τη m m m σχέση d
Ψυχρομετρία. Εισαγωγή
 Ψυχρομετρία. Εισαγωγή Η Ψυχρομετρία ασχολείται με τη μελέτη και τη μέτρηση των περιεχόμενων υδρατμών (υγρασία) στον ατμοσφαιρικό αέρα. Κατ επέκταση, ο όρος χρησιμοποιείται συνήθως για να περιγράψει τη
Ψυχρομετρία. Εισαγωγή Η Ψυχρομετρία ασχολείται με τη μελέτη και τη μέτρηση των περιεχόμενων υδρατμών (υγρασία) στον ατμοσφαιρικό αέρα. Κατ επέκταση, ο όρος χρησιμοποιείται συνήθως για να περιγράψει τη
Παραγωγή Ηλεκτρικής Ενέργειας 6ο Εξάμηνο Ηλεκτρολόγων Μηχανικών και Μηχανικών Ηλεκτρονικών Υπολογιστών Ροή Ε. 1η Σειρά Ασκήσεων
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ Σχολή Ηλεκτρολόγων Μηχ. και Μηχ. Υπολογιστών Ακαδ. Έτος 0- Τομέας Ηλεκτρικής Ισχύος Αθήνα, 0 Μαρτίου 0 Καθηγητής Κ.Βουρνάς Παράδοση,,5: 8// Λέκτωρ Σ. Καβατζά 6,,4: /4/ Παραγωγή
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ Σχολή Ηλεκτρολόγων Μηχ. και Μηχ. Υπολογιστών Ακαδ. Έτος 0- Τομέας Ηλεκτρικής Ισχύος Αθήνα, 0 Μαρτίου 0 Καθηγητής Κ.Βουρνάς Παράδοση,,5: 8// Λέκτωρ Σ. Καβατζά 6,,4: /4/ Παραγωγή
Θερμοκρασία - Θερμότητα. (Θερμοκρασία / Θερμική διαστολή / Ποσότητα θερμότητας / Θερμοχωρητικότητα / Θερμιδομετρία / Αλλαγή φάσης)
 Θερμοκρασία - Θερμότητα (Θερμοκρασία / Θερμική διαστολή / Ποσότητα θερμότητας / Θερμοχωρητικότητα / Θερμιδομετρία / Αλλαγή φάσης) Θερμοκρασία Ποσοτικοποιεί την αντίληψή μας για το πόσο ζεστό ή κρύο είναι
Θερμοκρασία - Θερμότητα (Θερμοκρασία / Θερμική διαστολή / Ποσότητα θερμότητας / Θερμοχωρητικότητα / Θερμιδομετρία / Αλλαγή φάσης) Θερμοκρασία Ποσοτικοποιεί την αντίληψή μας για το πόσο ζεστό ή κρύο είναι
ΠΡΟΛΟΓΟΣ. ΜΕΡΟΣ Α : Βασικές αρχές Ψυχρομετρίας. Νίκος Χαριτωνίδης
 ΠΡΟΛΟΓΟΣ ΜΕΡΟΣ Α : Βασικές αρχές Ψυχρομετρίας 1. Γενικά 2. Μερικές βασικές Θερμοδυναμικές ιδιότητες του νερού 3. Η σύσταση του Αέρα 4. Ο νόμος των μερικών πιέσεων του Dalton 5. Ο Γενικός Νόμος των αερίων
ΠΡΟΛΟΓΟΣ ΜΕΡΟΣ Α : Βασικές αρχές Ψυχρομετρίας 1. Γενικά 2. Μερικές βασικές Θερμοδυναμικές ιδιότητες του νερού 3. Η σύσταση του Αέρα 4. Ο νόμος των μερικών πιέσεων του Dalton 5. Ο Γενικός Νόμος των αερίων
Ανάλυση Τροφίμων. Ενότητα 4: Θερμοχημεία Χημική Ενέργεια Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ. Τμήμα Τεχνολογίας Τροφίμων. Ακαδημαϊκό Έτος
 Ανάλυση Τροφίμων Ενότητα 4: Θερμοχημεία Χημική Ενέργεια Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Εσωτερική Ενέργεια & Καταστατικές
Ανάλυση Τροφίμων Ενότητα 4: Θερμοχημεία Χημική Ενέργεια Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Εσωτερική Ενέργεια & Καταστατικές
P (Torr) 4,6 A 0 0,
 ΑΕΝ ΜΑΚΕΟΝΙΑΣ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΕΞΕΤΑΣΕΙΣ ΦΕΡΟΥΑΡΙΟΥ 2013 Μάθηµα: ΦΥΣΙΚΗ Α ΕΞΑΜΗΝΟΥ Καθηγητής: Ι. Π. ΠΑΠΑΠΑΝΑΟΥ Ονοµ/µo σπουδαστή: αθµολογία: Αριθµητικά: Ολογράφως: Α) ΕΡΩΤΗΣΕΙΣ ΣΩΣΤΟΥ-ΛΑΘΟΥΣ (µονάδες 20)
ΑΕΝ ΜΑΚΕΟΝΙΑΣ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΕΞΕΤΑΣΕΙΣ ΦΕΡΟΥΑΡΙΟΥ 2013 Μάθηµα: ΦΥΣΙΚΗ Α ΕΞΑΜΗΝΟΥ Καθηγητής: Ι. Π. ΠΑΠΑΠΑΝΑΟΥ Ονοµ/µo σπουδαστή: αθµολογία: Αριθµητικά: Ολογράφως: Α) ΕΡΩΤΗΣΕΙΣ ΣΩΣΤΟΥ-ΛΑΘΟΥΣ (µονάδες 20)
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 4 ΣΕΛΙ ΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΝΕΟ ΣΥΣΤΗΜΑ Γ ΗΜΕΡΗΣΙΩΝ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑ ΙΚΕΣ ΕΞΕΤΑΣΕΙΣ HMEΡΗΣΙΩΝ ΕΠΑΓΓΕΛΜΑΤΙΚΩΝ ΛΥΚΕΙΩΝ ΤΕΤΑΡΤΗ 22 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ ΚΑΙ ΚΛΙΜΑΤΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ:
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΝΕΟ ΣΥΣΤΗΜΑ Γ ΗΜΕΡΗΣΙΩΝ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑ ΙΚΕΣ ΕΞΕΤΑΣΕΙΣ HMEΡΗΣΙΩΝ ΕΠΑΓΓΕΛΜΑΤΙΚΩΝ ΛΥΚΕΙΩΝ ΤΕΤΑΡΤΗ 22 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΣΤΟΙΧΕΙΑ ΨΥΞΗΣ ΚΑΙ ΚΛΙΜΑΤΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ:
8. Θερμοκρασία και θερμότητα - Μεταβολές καταστάσεων της ύλης
 8. Θερμοκρασία και θερμότητα - Μεταβολές καταστάσεων της ύλης Φύλλο Εργασίας Τίτλος: Μεταβολές καταστάσεων της ύλης Γνωστικό Αντικείμενο: Μελέτη Περιβάλλοντος Διδακτική Ενότητα: Μεταβολές καταστάσεων της
8. Θερμοκρασία και θερμότητα - Μεταβολές καταστάσεων της ύλης Φύλλο Εργασίας Τίτλος: Μεταβολές καταστάσεων της ύλης Γνωστικό Αντικείμενο: Μελέτη Περιβάλλοντος Διδακτική Ενότητα: Μεταβολές καταστάσεων της
ηµήτρης Τσίνογλου ρ. Μηχανολόγος Μηχανικός
 ηµήτρης Τσίνογλου ρ. Μηχανολόγος Μηχανικός 1 Φυσική (ελεύθερη) συναγωγή Κεφάλαιο 8 2 Ορισµός του προβλήµατος Μηχανισµός µετάδοσης θερµότητας ανάµεσα σε ένα στερεό και σε ένα ρευστό, το οποίο βρίσκεται
ηµήτρης Τσίνογλου ρ. Μηχανολόγος Μηχανικός 1 Φυσική (ελεύθερη) συναγωγή Κεφάλαιο 8 2 Ορισµός του προβλήµατος Μηχανισµός µετάδοσης θερµότητας ανάµεσα σε ένα στερεό και σε ένα ρευστό, το οποίο βρίσκεται
ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΘΕΩΡΙΑ
 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΘΕΩΡΙΑ Περιεχόμενα 1. Όρια καταστατικής εξίσωσης ιδανικού αερίου 2. Αποκλίσεις των Ιδιοτήτων των πραγματικών αερίων από τους Νόμους
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΘΕΩΡΙΑ Περιεχόμενα 1. Όρια καταστατικής εξίσωσης ιδανικού αερίου 2. Αποκλίσεις των Ιδιοτήτων των πραγματικών αερίων από τους Νόμους
ΑΕΝ ΜΑΚΕ ΟΝΙΑΣ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2013 ΨΥΚΤΙΚΕΣ ΚΑΙ ΚΛΙΜΑΤΙΣΤΙΚΕΣ ΕΓΚΑΤΑΣΤΑΣΕΙΣ ΠΛΟΙΩΝ ΣΤ ΕΞΑΜΗΝΟΥ ΑΣΚΗΣΕΙΣ.
 ΑΕΝ ΜΑΚΕ ΟΝΙΑΣ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2013 ΨΥΚΤΙΚΕΣ ΚΑΙ ΚΛΙΜΑΤΙΣΤΙΚΕΣ ΕΓΚΑΤΑΣΤΑΣΕΙΣ ΠΛΟΙΩΝ ΣΤ ΕΞΑΜΗΝΟΥ ΑΣΚΗΣΕΙΣ. 1. Παροχη αερα 600kg/h περναει από ένα ψυχρο εναλλακτη. Η αρχικη θερμοκρασια
ΑΕΝ ΜΑΚΕ ΟΝΙΑΣ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2013 ΨΥΚΤΙΚΕΣ ΚΑΙ ΚΛΙΜΑΤΙΣΤΙΚΕΣ ΕΓΚΑΤΑΣΤΑΣΕΙΣ ΠΛΟΙΩΝ ΣΤ ΕΞΑΜΗΝΟΥ ΑΣΚΗΣΕΙΣ. 1. Παροχη αερα 600kg/h περναει από ένα ψυχρο εναλλακτη. Η αρχικη θερμοκρασια
1. Περιγράψτε τι συμβαίνει με την εξάτμιση, την υγροποίηση και τη συμπύκνωση στον Κύκλο του Νερού.
 1. Περιγράψτε τι συμβαίνει με την εξάτμιση, την υγροποίηση και τη συμπύκνωση στον Κύκλο του Νερού. Άσκηση 1 2. Καθώς το νερό συνεχώς κάνει τον κύκλο του («κύκλος του νερού»), η συνολική ποσότητα του νερού
1. Περιγράψτε τι συμβαίνει με την εξάτμιση, την υγροποίηση και τη συμπύκνωση στον Κύκλο του Νερού. Άσκηση 1 2. Καθώς το νερό συνεχώς κάνει τον κύκλο του («κύκλος του νερού»), η συνολική ποσότητα του νερού
ΕΓΚΑΤΑΣΤΑΣΕΙΣ ΨΥΚΤΙΚΟΣ ΚΥΚΛΟΣ. Θεωρία - Λυμένα Παραδείγματα. Νικόλαος Χονδράκης (Εκπαιδευτικός)
 ΕΓΚΑΤΑΣΤΑΣΕΙΣ ΨΥΞΗΣ ΨΥΚΤΙΚΟΣ ΚΥΚΛΟΣ Θεωρία - Λυμένα Παραδείγματα Νικόλαος Χονδράκης (Εκπαιδευτικός) ... Νικόλαος Γ. Χονδράκης ( chonniko@gmail.com) Διπλωματούχος Μηχανολόγος Μηχανικός Copyright Νικόλαος
ΕΓΚΑΤΑΣΤΑΣΕΙΣ ΨΥΞΗΣ ΨΥΚΤΙΚΟΣ ΚΥΚΛΟΣ Θεωρία - Λυμένα Παραδείγματα Νικόλαος Χονδράκης (Εκπαιδευτικός) ... Νικόλαος Γ. Χονδράκης ( chonniko@gmail.com) Διπλωματούχος Μηχανολόγος Μηχανικός Copyright Νικόλαος
ΕΡΓΑΣΙΑ ΤΕΧΝΟΛΟΓΙΑΣ Γ Γυμνασίου. «Μείωση των θερμικών απωλειών από κλειστό χώρο με τη χρήση διπλών τζαμιών»
 3 ο ΓΥΜΝΑΣΙΟ ΒΡΙΛΗΣΣΙΩΝ ΣΧΟΛΙΚΟ ΕΤΟΣ 2016 2017 ΕΡΓΑΣΙΑ ΤΕΧΝΟΛΟΓΙΑΣ Γ Γυμνασίου «Μείωση των θερμικών απωλειών από κλειστό χώρο με τη χρήση διπλών τζαμιών» του μαθητή Διονύση Κλαδά Μάιος 2017 1 Περιεχόμενα
3 ο ΓΥΜΝΑΣΙΟ ΒΡΙΛΗΣΣΙΩΝ ΣΧΟΛΙΚΟ ΕΤΟΣ 2016 2017 ΕΡΓΑΣΙΑ ΤΕΧΝΟΛΟΓΙΑΣ Γ Γυμνασίου «Μείωση των θερμικών απωλειών από κλειστό χώρο με τη χρήση διπλών τζαμιών» του μαθητή Διονύση Κλαδά Μάιος 2017 1 Περιεχόμενα
Η ψύξη ενός αερίου ρεύματος είναι δυνατή με αδιαβατική εκτόνωση του. Μπορεί να συμβεί:
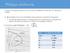 Ψύξη με εκτόνωση Η ψύξη ενός αερίου ρεύματος είναι δυνατή με αδιαβατική εκτόνωση του. Μπορεί να συμβεί: A. Mε ελεύθερη εκτόνωση σε βαλβίδα στραγγαλισμού: ισενθαλπική διεργασία σε χαμηλές θερμοκρασίες,
Ψύξη με εκτόνωση Η ψύξη ενός αερίου ρεύματος είναι δυνατή με αδιαβατική εκτόνωση του. Μπορεί να συμβεί: A. Mε ελεύθερη εκτόνωση σε βαλβίδα στραγγαλισμού: ισενθαλπική διεργασία σε χαμηλές θερμοκρασίες,
Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις
 Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις Άσκηση 1β: Ενθαλπία εξατμίσεως Αθανάσιος Τσεκούρας Τμήμα Χημείας 1. Θεωρία... 3 2. Μετρήσεις... 4 3. Επεξεργασία Μετρήσεων... 5 Σελίδα 2 1. Θεωρία Σύμφωνα με τον κανόνα
Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις Άσκηση 1β: Ενθαλπία εξατμίσεως Αθανάσιος Τσεκούρας Τμήμα Χημείας 1. Θεωρία... 3 2. Μετρήσεις... 4 3. Επεξεργασία Μετρήσεων... 5 Σελίδα 2 1. Θεωρία Σύμφωνα με τον κανόνα
ΑΣΚΗΣΗ 5 ΑΤΜΟΣΦΑΙΡΙΚΗ ΥΓΡΑΣΙΑ
 ΑΣΚΗΣΗ 5 ΑΤΜΟΣΦΑΙΡΙΚΗ ΥΓΡΑΣΙΑ Με τον όρο ατμοσφαιρική υγρασία περιγράφουμε την ποσότητα των υδρατμών που περιέχονται σε ορισμένο όγκο ατμοσφαιρικού αέρα. Η περιεκτικότητα της ατμόσφαιρας σε υδρατμούς μπορεί
ΑΣΚΗΣΗ 5 ΑΤΜΟΣΦΑΙΡΙΚΗ ΥΓΡΑΣΙΑ Με τον όρο ατμοσφαιρική υγρασία περιγράφουμε την ποσότητα των υδρατμών που περιέχονται σε ορισμένο όγκο ατμοσφαιρικού αέρα. Η περιεκτικότητα της ατμόσφαιρας σε υδρατμούς μπορεί
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ. Τράπεζα θεμάτων. Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ
 ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ 16111 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ 16111 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ ΕΝΤΡΟΠΙΑ ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ
 ΕΝΤΡΟΠΙΑ ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ 1 ΑΣΚΗΣΗ 1 Το δοχείο του σχήματος είναι απομονωμένο (αδιαβατικά τοιχώματα). Το διάφραγμα χωρίζει το δοχείο σε δύο μέρη. Το αριστερό μέρος έχει όγκο 1 και περιέχει ιδανικό αέριο
ΕΝΤΡΟΠΙΑ ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ 1 ΑΣΚΗΣΗ 1 Το δοχείο του σχήματος είναι απομονωμένο (αδιαβατικά τοιχώματα). Το διάφραγμα χωρίζει το δοχείο σε δύο μέρη. Το αριστερό μέρος έχει όγκο 1 και περιέχει ιδανικό αέριο
ΜΕΡΟΣ Α ΝΟΜΟΙ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ-ΜΕΤΑΤΡΟΠΕΣ ΦΑΣΗΣ ΥΓΡΟΣΚΟΠΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΙΝΩΝ
 ΜΕΡΟΣ Α ΝΟΜΟΙ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ-ΜΕΤΑΤΡΟΠΕΣ ΦΑΣΗΣ ΥΓΡΟΣΚΟΠΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΙΝΩΝ Εισαγωγή Τα περισσότερα είδη ινών είναι υγροσκοπικά, έχουν δηλαδή την ιδιότητα να απορροφούν υγρασία (υδρατμούς) όταν η ατμόσφαιρα
ΜΕΡΟΣ Α ΝΟΜΟΙ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ-ΜΕΤΑΤΡΟΠΕΣ ΦΑΣΗΣ ΥΓΡΟΣΚΟΠΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΙΝΩΝ Εισαγωγή Τα περισσότερα είδη ινών είναι υγροσκοπικά, έχουν δηλαδή την ιδιότητα να απορροφούν υγρασία (υδρατμούς) όταν η ατμόσφαιρα
Η φυσική με πειράματα Α Γυμνασίου
 Εργαστήριο Φυσικών Επιστημών Γυμνασίου Δρεπάνου Η φυσική με πειράματα Α Γυμνασίου Φύλλο Εργασίας 5 Από τη Θερμότητα στη θερμοκρασία Η θερμική Ισορροπία Επεξεργασία-Απαντήσεις των δραστηριοτήτων και των
Εργαστήριο Φυσικών Επιστημών Γυμνασίου Δρεπάνου Η φυσική με πειράματα Α Γυμνασίου Φύλλο Εργασίας 5 Από τη Θερμότητα στη θερμοκρασία Η θερμική Ισορροπία Επεξεργασία-Απαντήσεις των δραστηριοτήτων και των
1bar. bar; = = y2. mol. mol. mol. P (bar)
 Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξέταση: Περίοδος Σεπτεµβρίου -3 (7//4). Σηµειώστε µέσα στην παρένθεση δίπλα σε κάθε µέγεθος αν είναι εντατικό (Ν) ή εκτατικό (Κ): όγκος (Κ), θερµοκρασία (Ν), πυκνότητα
Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξέταση: Περίοδος Σεπτεµβρίου -3 (7//4). Σηµειώστε µέσα στην παρένθεση δίπλα σε κάθε µέγεθος αν είναι εντατικό (Ν) ή εκτατικό (Κ): όγκος (Κ), θερµοκρασία (Ν), πυκνότητα
Όνομα και Επώνυμο:.. Όνομα Πατέρα: Όνομα Μητέρας:.. Δημοτικό Σχολείο:.. Τάξη/Τμήμα:.. Εξεταστικό Κέντρο:...
 Όνομα και Επώνυμο:.. Όνομα Πατέρα: Όνομα Μητέρας:.. Δημοτικό Σχολείο:.. Τάξη/Τμήμα:.. Εξεταστικό Κέντρο:.... Παρατήρησε τα διάφορα φαινόμενα αλλαγής της φυσικής κατάστασης του νερού που σημειώνονται με
Όνομα και Επώνυμο:.. Όνομα Πατέρα: Όνομα Μητέρας:.. Δημοτικό Σχολείο:.. Τάξη/Τμήμα:.. Εξεταστικό Κέντρο:.... Παρατήρησε τα διάφορα φαινόμενα αλλαγής της φυσικής κατάστασης του νερού που σημειώνονται με
ΥΛΙΚΑ ΓΙΑ ΕΝΕΡΓΕΙΑΚΕΣ ΕΦΑΡΜΟΓΕΣ
 ΥΛΙΚΑ ΓΙΑ ΕΝΕΡΓΕΙΑΚΕΣ ΕΦΑΡΜΟΓΕΣ ΑΤΜΟΣΤΡΟΒΙΛΟΙ Σημειώσεις Δ. Κουζούδη Εαρινό Εξάμηνο 2017 ΑΤΜΟ-ΣΤΡΟΒΙΛΟΙ (ΑΤΜΟ-ΤΟΥΡΜΠΙΝΕΣ) Που χρησιμοποιούνται; Για παραγωγή ηλεκτρικής ς σε μεγάλη κλίμακα. Εκτός από τα
ΥΛΙΚΑ ΓΙΑ ΕΝΕΡΓΕΙΑΚΕΣ ΕΦΑΡΜΟΓΕΣ ΑΤΜΟΣΤΡΟΒΙΛΟΙ Σημειώσεις Δ. Κουζούδη Εαρινό Εξάμηνο 2017 ΑΤΜΟ-ΣΤΡΟΒΙΛΟΙ (ΑΤΜΟ-ΤΟΥΡΜΠΙΝΕΣ) Που χρησιμοποιούνται; Για παραγωγή ηλεκτρικής ς σε μεγάλη κλίμακα. Εκτός από τα
2 ΕΙΣΑΓΩΓΙΚΕΣ ΕΝΝΟΙΕΣ
 ΙΣΟΖΥΓΙΑ ΕΝΕΡΓΕΙΑΣ ΕΙΣΑΓΩΓΙΚΕΣ ΕΝΝΟΙΕΣ 2 ΣΗΜΑΝΤΙΚΟΙ ΟΡΟΙ Αδιαβατικό σύστημα Ισοβαρές σύστημα Ισόχωρο σύστημα Ισοθερμοκρασιακό σύστημα Μεταβλητή διαδρομής (συνάρτηση μετάβασης) Καταστατική μεταβολή (σημειακή
ΙΣΟΖΥΓΙΑ ΕΝΕΡΓΕΙΑΣ ΕΙΣΑΓΩΓΙΚΕΣ ΕΝΝΟΙΕΣ 2 ΣΗΜΑΝΤΙΚΟΙ ΟΡΟΙ Αδιαβατικό σύστημα Ισοβαρές σύστημα Ισόχωρο σύστημα Ισοθερμοκρασιακό σύστημα Μεταβλητή διαδρομής (συνάρτηση μετάβασης) Καταστατική μεταβολή (σημειακή
Θερμοδυναμική. Ενότητα 3: Ασκήσεις στη Θερμοδυναμική. Κυρατζής Νικόλαος Τμήμα Μηχανικών Περιβάλλοντος και Μηχανικών Αντιρρύπανσης ΤΕ
 Θερμοδυναμική Ενότητα 3: Ασκήσεις στη Θερμοδυναμική Κυρατζής Νικόλαος Τμήμα Μηχανικών Περιβάλλοντος και Μηχανικών Αντιρρύπανσης ΤΕ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Θερμοδυναμική Ενότητα 3: Ασκήσεις στη Θερμοδυναμική Κυρατζής Νικόλαος Τμήμα Μηχανικών Περιβάλλοντος και Μηχανικών Αντιρρύπανσης ΤΕ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ
 5 Η ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΗΣ B ΓΥΜΝΑΣΙΟΥ Κυριακή, 17 Μαΐου 2009 Ώρα: 10:00 12:30 Προτεινόμενες Λύσεις θεμα - 1 (5 μον.) Στον πίνακα υπάρχουν δύο στήλες με ασυμπλήρωτες προτάσεις. Στο τετράδιο των απαντήσεών
5 Η ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΗΣ B ΓΥΜΝΑΣΙΟΥ Κυριακή, 17 Μαΐου 2009 Ώρα: 10:00 12:30 Προτεινόμενες Λύσεις θεμα - 1 (5 μον.) Στον πίνακα υπάρχουν δύο στήλες με ασυμπλήρωτες προτάσεις. Στο τετράδιο των απαντήσεών
Λύση: α) Χρησιµοποιούµε την εξίσωση Clausius Clapeyron για να υπολογίσουµε το σηµείο ζέσεως του αζώτου υπό πίεση 2 atm. 1 P1
 Το άζωτο αποθηκεύεται ως υγρό σε θερµικά µονωµένα δοχεία υπό πίεση. Η πίεση ρυθµίζεται µε βαλβίδα διαφυγής σε τιµή atm επιπλέον της ατµοσφαιρικής πιέσεως. α) Να εκτιµηθεί η θερµοκρασία στην οποία βρίσκεται
Το άζωτο αποθηκεύεται ως υγρό σε θερµικά µονωµένα δοχεία υπό πίεση. Η πίεση ρυθµίζεται µε βαλβίδα διαφυγής σε τιµή atm επιπλέον της ατµοσφαιρικής πιέσεως. α) Να εκτιµηθεί η θερµοκρασία στην οποία βρίσκεται
Παραγωγή Ηλεκτρικής Ενέργειας. 6ο Εξάμηνο Ηλεκτρολόγων Μηχανικών και Μηχανικών Ηλεκτρονικών Υπολογιστών. 1η Σειρά Ασκήσεων.
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ Σχολή Ηλεκτρολόγων Μηχ. και Μηχ. Υπολογιστών Ακαδ. Έτος 00- Τομέας Ηλεκτρικής Ισχύος Αθήνα 5//0 Κ. Βουρνάς, Κ. Ντελκής, Π. Γεωργιλάκης Παράδοση,,,4: //0 Παράδοση 5, 6: 5/4/0
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ Σχολή Ηλεκτρολόγων Μηχ. και Μηχ. Υπολογιστών Ακαδ. Έτος 00- Τομέας Ηλεκτρικής Ισχύος Αθήνα 5//0 Κ. Βουρνάς, Κ. Ντελκής, Π. Γεωργιλάκης Παράδοση,,,4: //0 Παράδοση 5, 6: 5/4/0
ΒΙΟΚΛΙΜΑΤΟΛΟΓΙΑ ΘΕΡΜΟΚΗΠΙΩΝ ΤΕΙ ΔΥΤΙΚΗΣ ΕΛΛΑΔΑΣ
 ΒΙΟΚΛΙΜΑΤΟΛΟΓΙΑ ΘΕΡΜΟΚΗΠΙΩΝ ΥΓΡΑΣΙΑ Δρ.Ι. Λυκοσκούφης ΤΕΙ ΔΥΤΙΚΗΣ ΕΛΛΑΔΑΣ 1 Η ΥΓΡΑΣΙΑ Ο ατμοσφαιρικός αέρας στη φυσική του κατάσταση είναι μίγμα αερίων, οξυγόνου, αζώτου, διοξειδίου του άνθρακα, αργού,
ΒΙΟΚΛΙΜΑΤΟΛΟΓΙΑ ΘΕΡΜΟΚΗΠΙΩΝ ΥΓΡΑΣΙΑ Δρ.Ι. Λυκοσκούφης ΤΕΙ ΔΥΤΙΚΗΣ ΕΛΛΑΔΑΣ 1 Η ΥΓΡΑΣΙΑ Ο ατμοσφαιρικός αέρας στη φυσική του κατάσταση είναι μίγμα αερίων, οξυγόνου, αζώτου, διοξειδίου του άνθρακα, αργού,
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 6 η : Θερμοχημεία Χημική ενέργεια. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 6 η : Θερμοχημεία Χημική ενέργεια Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Εσωτερική Ενέργεια & Καταστατικές Συναρτήσεις 2 1 ος Νόμος
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 6 η : Θερμοχημεία Χημική ενέργεια Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Εσωτερική Ενέργεια & Καταστατικές Συναρτήσεις 2 1 ος Νόμος
ΣΤΑΘΜΟΙ ΠΑΡΑΓΩΓΗΣ ΗΛΕΚΤΡΙΚΗΣ ΕΝΕΡΓΕΙΑΣ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΣΤΑΘΜΟΙ ΠΑΡΑΓΩΓΗΣ ΗΛΕΚΤΡΙΚΗΣ ΕΝΕΡΓΕΙΑΣ Ενότητα 11: Κύκλα ατμού Χατζηαθανασίου Βασίλειος Καδή Στυλιανή Τμήμα Ηλεκτρολόγων Μηχανικών και
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΣΤΑΘΜΟΙ ΠΑΡΑΓΩΓΗΣ ΗΛΕΚΤΡΙΚΗΣ ΕΝΕΡΓΕΙΑΣ Ενότητα 11: Κύκλα ατμού Χατζηαθανασίου Βασίλειος Καδή Στυλιανή Τμήμα Ηλεκτρολόγων Μηχανικών και
Βασικές Διεργασίες Μηχανικής Τροφίμων
 Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 4: Ψύξη - Κατάψυξη (/3), ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Συντελεστής
Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 4: Ψύξη - Κατάψυξη (/3), ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Συντελεστής
4.2 Παρα γοντες που επηρεα ζουν τη θε ση χημικη ς ισορροπι ας - Αρχη Le Chatelier
 Χημικός Διδάκτωρ Παν. Πατρών 4.2 Παρα γοντες που επηρεα ζουν τη θε ση χημικη ς ισορροπι ας - Αρχη Le Chatelier Τι ονομάζεται θέση χημικής ισορροπίας; Από ποιους παράγοντες επηρεάζεται η θέση της χημικής
Χημικός Διδάκτωρ Παν. Πατρών 4.2 Παρα γοντες που επηρεα ζουν τη θε ση χημικη ς ισορροπι ας - Αρχη Le Chatelier Τι ονομάζεται θέση χημικής ισορροπίας; Από ποιους παράγοντες επηρεάζεται η θέση της χημικής
ΦΥΣΙΚΗ Α ΓΥΜΝΑΣΙΟΥ. Φύλλο Εργασίας 5 ο Από τη Θερμότητα στη Θερμοκρασία Η Θερμική Ισορροπία
 ΦΥΣΙΚΗ Α ΓΥΜΝΑΣΙΟΥ Φύλλο Εργασίας 5 ο Από τη Θερμότητα στη Θερμοκρασία Η Θερμική Ισορροπία Φύλλο Εργασίας 5ο: Από τη Θερμότητα στη Θερμοκρασία Η Θερμική Ισορροπία Στόχος μας είναι: να διακρίνουμε τη διαφορά
ΦΥΣΙΚΗ Α ΓΥΜΝΑΣΙΟΥ Φύλλο Εργασίας 5 ο Από τη Θερμότητα στη Θερμοκρασία Η Θερμική Ισορροπία Φύλλο Εργασίας 5ο: Από τη Θερμότητα στη Θερμοκρασία Η Θερμική Ισορροπία Στόχος μας είναι: να διακρίνουμε τη διαφορά
ΘΕΡΜΙΚΕΣ & ΨΥΚΤΙΚΕΣ ΜΗΧΑΝΕΣ ΘΕΩΡΙΑ
 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 www.pmoiras.weebly.om ΘΕΡΜΙΚΕΣ & ΨΥΚΤΙΚΕΣ ΜΗΧΑΝΕΣ ΘΕΩΡΙΑ Περιεχόμενα 1. Κυκλικές διαδικασίες 2. O 2ος Θερμοδυναμικός Νόμος- Φυσική Ερμηνεία 2.1 Ισοδυναμία
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 www.pmoiras.weebly.om ΘΕΡΜΙΚΕΣ & ΨΥΚΤΙΚΕΣ ΜΗΧΑΝΕΣ ΘΕΩΡΙΑ Περιεχόμενα 1. Κυκλικές διαδικασίες 2. O 2ος Θερμοδυναμικός Νόμος- Φυσική Ερμηνεία 2.1 Ισοδυναμία
Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου /3
 Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου 2014 1/3 Πρόβλημα 2. Καταστατική Εξίσωση Van der Waals (11 ) Σε ένα πολύ γνωστό μοντέλο του ιδανικού αερίου, του οποίου η καταστατική εξίσωση περιγράφεται από το νόμο
Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου 2014 1/3 Πρόβλημα 2. Καταστατική Εξίσωση Van der Waals (11 ) Σε ένα πολύ γνωστό μοντέλο του ιδανικού αερίου, του οποίου η καταστατική εξίσωση περιγράφεται από το νόμο
ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ
 ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ 1 Η ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑ Α ΦΥΣΙΚΗΣ B ΓΥΜΝΑΣΙΟΥ Κυριακή, 17 Απριλίου, 2005 Ώρα: 10:00-12:30 Προτεινόµενες Λύσεις ΜΕΡΟΣ Α 1. (α) Από το δεύτερο σχήµα, επειδή ο ζυγός ισορροπεί, προκύπτει
ΕΝΩΣΗ ΚΥΠΡΙΩΝ ΦΥΣΙΚΩΝ 1 Η ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑ Α ΦΥΣΙΚΗΣ B ΓΥΜΝΑΣΙΟΥ Κυριακή, 17 Απριλίου, 2005 Ώρα: 10:00-12:30 Προτεινόµενες Λύσεις ΜΕΡΟΣ Α 1. (α) Από το δεύτερο σχήµα, επειδή ο ζυγός ισορροπεί, προκύπτει
Ψυκτικές Μηχανές 21/10/2012. Υποπλοίαρχος (Μ) Α.Δένδης ΠΝ 1. Ψυκτικές Μηχανές (6.2) Ψυκτικές Μηχανές (6.2) Ψυκτικές Μηχανές (6.2)
 Ψυκτικές Μηχανές Εξατμιστές Επανάληψη - Εισαγωγή 1. Ποιός είναι ο σκοπός λειτουργίας του εξατμιστή; 4 3 1 2 Υποπλοίαρχος (Μ) Α.Δένδης Π.Ν. 1 2 Ρόλος Τύποι Εξατμιστών Ψύξης αέρα ( φυσικής εξαναγκασμένης
Ψυκτικές Μηχανές Εξατμιστές Επανάληψη - Εισαγωγή 1. Ποιός είναι ο σκοπός λειτουργίας του εξατμιστή; 4 3 1 2 Υποπλοίαρχος (Μ) Α.Δένδης Π.Ν. 1 2 Ρόλος Τύποι Εξατμιστών Ψύξης αέρα ( φυσικής εξαναγκασμένης
6 ο Εργαστήριο Τεχνολογία αερισμού
 6 ο Εργαστήριο Τεχνολογία αερισμού 1 Στόχος του εργαστηρίου Στόχος του εργαστηρίου είναι να γνωρίσουν οι φοιτητές: - μεθόδους ελέγχου υγρασίας εντός του κτηνοτροφικού κτηρίου - τεχνικές αερισμού - εξοπλισμό
6 ο Εργαστήριο Τεχνολογία αερισμού 1 Στόχος του εργαστηρίου Στόχος του εργαστηρίου είναι να γνωρίσουν οι φοιτητές: - μεθόδους ελέγχου υγρασίας εντός του κτηνοτροφικού κτηρίου - τεχνικές αερισμού - εξοπλισμό
σημείο ζέσεως, σημείο τήξεως, σημείο πήξεως, εξάτμιση, εξάχνωση, συμπύκνωση, απόθεση
 1.2 Καταστάσεις των υλικών Πρώτες σκέψεις: Η διπλανή φωτογραφία δείχνει ένα υδάτινο τοπίο. Το νερό βρίσκεται σε τρεις διαφορετικές καταστάσεις: ως αέριο, ως υγρό και ως στερεό. Τα διάφορα υλικά μπορούν
1.2 Καταστάσεις των υλικών Πρώτες σκέψεις: Η διπλανή φωτογραφία δείχνει ένα υδάτινο τοπίο. Το νερό βρίσκεται σε τρεις διαφορετικές καταστάσεις: ως αέριο, ως υγρό και ως στερεό. Τα διάφορα υλικά μπορούν
ΚΕΦΑΛΑΙΟ 4 Ο ΘΕΡΜΟΔΥΝΑΜΙΚΗ
 103 Α. ΠΡΩΤΟΣ ΘΕΡΜΟΔΥΝΑΜΙΚΟΣ ΝΟΜΟΣ ΚΕΦΑΛΑΙΟ 4 Ο ΘΕΡΜΟΔΥΝΑΜΙΚΗ 1. Ιδανικό αέριο εκτελεί διαδοχικά τις αντιστρεπτές μεταβολές ΑΒ, ΒΓ, ΓΑ που παριστάνονται στο ακόλουθο διάγραμμα P-V. α. Αν δίνονται Q ΑΒΓ
103 Α. ΠΡΩΤΟΣ ΘΕΡΜΟΔΥΝΑΜΙΚΟΣ ΝΟΜΟΣ ΚΕΦΑΛΑΙΟ 4 Ο ΘΕΡΜΟΔΥΝΑΜΙΚΗ 1. Ιδανικό αέριο εκτελεί διαδοχικά τις αντιστρεπτές μεταβολές ΑΒ, ΒΓ, ΓΑ που παριστάνονται στο ακόλουθο διάγραμμα P-V. α. Αν δίνονται Q ΑΒΓ
ΦΕ6 α. παρατηρώ, πληροφορούμαι, ενδιαφέρομαι / έναυσμα ενδιαφέροντος
 4ο ΓΥΜΝΑΣΙΟ ΛΑΜΙΑΣ 1 ΦΕ6 α. παρατηρώ, πληροφορούμαι, ενδιαφέρομαι / έναυσμα ενδιαφέροντος Το νερό βράζει στο καζάνι και μετατρέπεται σε υδρατμούς. Το νερό εξατμίζεται από την επιφάνεια της λίμνης και του
4ο ΓΥΜΝΑΣΙΟ ΛΑΜΙΑΣ 1 ΦΕ6 α. παρατηρώ, πληροφορούμαι, ενδιαφέρομαι / έναυσμα ενδιαφέροντος Το νερό βράζει στο καζάνι και μετατρέπεται σε υδρατμούς. Το νερό εξατμίζεται από την επιφάνεια της λίμνης και του
Σημειώσεις. Επιλεγμένα θέματα Κλωστοϋφαντουργικής Φυσικής
 ΤΕΙ ΠΕΙΡΑΙΑ Τμήμα Φυσικής Χημείας και Τεχνολογίας Υλικών Σημειώσεις για τους σπουδαστές του τμήματος Κλωστοϋφαντουργίας Επιλεγμένα θέματα Κλωστοϋφαντουργικής Φυσικής ΑΘΗΝΑ 2007 Δρ. Ζαχαριάδου Αικατερίνη
ΤΕΙ ΠΕΙΡΑΙΑ Τμήμα Φυσικής Χημείας και Τεχνολογίας Υλικών Σημειώσεις για τους σπουδαστές του τμήματος Κλωστοϋφαντουργίας Επιλεγμένα θέματα Κλωστοϋφαντουργικής Φυσικής ΑΘΗΝΑ 2007 Δρ. Ζαχαριάδου Αικατερίνη
Μεταφορά Θερμότητας. Βρασμός και συμπύκνωση (boiling and condensation)
 ΜΜK 312 Τμήμα Μηχανολόγων Μηχανικών και Μηχανικών Παραγωγής γής MMK 312 1 Βρασμός και συμπύκνωση (boiing and condenion Όταν η θερμοκρασία ενός υγρού (σε συγκεκριμένη πίεση αυξάνεται μέχρι τη θερμοκρασία
ΜΜK 312 Τμήμα Μηχανολόγων Μηχανικών και Μηχανικών Παραγωγής γής MMK 312 1 Βρασμός και συμπύκνωση (boiing and condenion Όταν η θερμοκρασία ενός υγρού (σε συγκεκριμένη πίεση αυξάνεται μέχρι τη θερμοκρασία
ΕΙΣΑΓΩΓΗ ΣΤΗ ΜΕΤΑΔΟΣΗ ΘΕΡΜΟΤΗΤΑΣ
 ΕΙΣΑΓΩΓΗ ΣΤΗ ΜΕΤΑΔΟΣΗ ΘΕΡΜΟΤΗΤΑΣ Η Επιστήμη της Θερμοδυναμικής ασχολείται με την ποσότητα της θερμότητας που μεταφέρεται σε ένα κλειστό και απομονωμένο σύστημα από μια κατάσταση ισορροπίας σε μια άλλη
ΕΙΣΑΓΩΓΗ ΣΤΗ ΜΕΤΑΔΟΣΗ ΘΕΡΜΟΤΗΤΑΣ Η Επιστήμη της Θερμοδυναμικής ασχολείται με την ποσότητα της θερμότητας που μεταφέρεται σε ένα κλειστό και απομονωμένο σύστημα από μια κατάσταση ισορροπίας σε μια άλλη
ΤΥΠΟΛΟΓΙΟ ΟΡΙΣΜΟΙ ΦΥΣΙΚΗΣ Β ΓΥΜΝΑΣΙΟΥ
 ΤΥΠΟΛΟΓΙΟ ΟΡΙΣΜΟΙ ΦΥΣΙΚΗΣ Β ΓΥΜΝΑΣΙΟΥ Τα σημαντικότερα στοιχεία της επιστημονικής μεθόδου είναι η παρατήρηση, η υπόθεση, το πείραμα, η γενίκευση και η πρόβλεψη νέων φαινομένων. Για να μελετήσουμε πλήρως
ΤΥΠΟΛΟΓΙΟ ΟΡΙΣΜΟΙ ΦΥΣΙΚΗΣ Β ΓΥΜΝΑΣΙΟΥ Τα σημαντικότερα στοιχεία της επιστημονικής μεθόδου είναι η παρατήρηση, η υπόθεση, το πείραμα, η γενίκευση και η πρόβλεψη νέων φαινομένων. Για να μελετήσουμε πλήρως
ΘΕΡΜΑΝΣΗ-ΨΥΞΗ-ΚΛΙΜΑΤΙΣΜΟΣ Ι ΑΣΚΗΣΕΙΣ
 ΘΕΡΜΑΝΣΗ-ΨΥΞΗ-ΚΛΙΜΑΤΙΣΜΟΣ Ι ΑΣΚΗΣΕΙΣ 1. Ψυκτική εγκατάσταση που ακολουθεί στοιχειώδη ψυκτικό κύκλο συμπίεσης ατμών με ψυκτικό μέσο R134a, εργάζεται μεταξύ των ορίων πίεσης 0,12 MΡa και 1 MΡa. Αν η παροχή
ΘΕΡΜΑΝΣΗ-ΨΥΞΗ-ΚΛΙΜΑΤΙΣΜΟΣ Ι ΑΣΚΗΣΕΙΣ 1. Ψυκτική εγκατάσταση που ακολουθεί στοιχειώδη ψυκτικό κύκλο συμπίεσης ατμών με ψυκτικό μέσο R134a, εργάζεται μεταξύ των ορίων πίεσης 0,12 MΡa και 1 MΡa. Αν η παροχή
V (β) Αν κατά τη μεταβολή ΓΑ μεταφέρεται θερμότητα 22J από το αέριο στο περιβάλλον, να βρεθεί το έργο W ΓA.
 Άσκηση 1 Ιδανικό αέριο εκτελεί διαδοχικά τις αντιστρεπτές μεταβολές ΑΒ, ΒΓ, ΓΑ που παριστάνονται στο διάγραμμα p V του σχήματος. (α) Αν δίνονται Q ΑΒΓ = 30J και W BΓ = 20J, να βρεθεί η μεταβολή της εσωτερικής
Άσκηση 1 Ιδανικό αέριο εκτελεί διαδοχικά τις αντιστρεπτές μεταβολές ΑΒ, ΒΓ, ΓΑ που παριστάνονται στο διάγραμμα p V του σχήματος. (α) Αν δίνονται Q ΑΒΓ = 30J και W BΓ = 20J, να βρεθεί η μεταβολή της εσωτερικής
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ ΕΝΤΡΟΠΙΑ ΛΥΜΕΝΑ ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ
 ΕΝΤΡΟΠΙΑ ΛΥΜΕΝΑ ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ Θέμα Απομονωμένο σύστημα περνάει από κατάσταση με εντροπία S σε κατάσταση με εντροπία S. Αποδείξτε και σχολιάστε ότι ισχύει S S. Για οποιαδήποτε μηχανή (σύστημα που εκτελεί
ΕΝΤΡΟΠΙΑ ΛΥΜΕΝΑ ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ Θέμα Απομονωμένο σύστημα περνάει από κατάσταση με εντροπία S σε κατάσταση με εντροπία S. Αποδείξτε και σχολιάστε ότι ισχύει S S. Για οποιαδήποτε μηχανή (σύστημα που εκτελεί
ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι. Ενότητα 10: Ισορροπίες φάσεων. Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών
 ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι Ενότητα 0: Ισορροπίες φάσεων Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοποί ενότητας Σκοπός της ενότητας αυτής είναι η παρουσίαση και η εξέταση της ισορροπίας ανάμεσα
ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι Ενότητα 0: Ισορροπίες φάσεων Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοποί ενότητας Σκοπός της ενότητας αυτής είναι η παρουσίαση και η εξέταση της ισορροπίας ανάμεσα
3. Έχουμε δύο ποτήρια, το ένα γεμάτο πάγο και το άλλο γεμάτο με νερό 80 C. Τα αφήνουμε πάνω σε ένα τραπέζι. Τι θα συμβεί καθώς περνά ο χρόνος;
 1. Τι είναι θερμότητα; Θερμότητα είναι η ενέργεια που μεταφέρεται από ένα θερμό σώμα σε ένα ψυχρό ώσπου να αποκτήσουν την ίδια θερμοκρασία. Μονάδα μέτρησης της θερμότητας είναι το 1 Joule. 2. Τι είναι
1. Τι είναι θερμότητα; Θερμότητα είναι η ενέργεια που μεταφέρεται από ένα θερμό σώμα σε ένα ψυχρό ώσπου να αποκτήσουν την ίδια θερμοκρασία. Μονάδα μέτρησης της θερμότητας είναι το 1 Joule. 2. Τι είναι
Τ.Ε.Ι. ΠΕΙΡΑΙΑ ΤΜΗΜΑ ΜΗΧΑΝΟΛΟΓΙΑΣ ΜΑΘΗΜΑ: ΕΦΑΡΜΟΣΜΕΝΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ (Ασκήσεις πράξης) ΙΔΑΝΙΚΑ ΑΕΡΙΑ - ΕΡΓΟ
 ΙΔΑΝΙΚΑ ΑΕΡΙΑ - ΕΡΓΟ 1. Να υπολογιστεί η πυκνότητα του αέρα σε πίεση 0,1 MPa και θερμοκρασία 20 ο C. (R air =0,287 kj/kgk) 2. Ποσότητα αέρα 1 kg εκτελεί τις παρακάτω διεργασίες: Διεργασία 1-2: Αδιαβατική
ΙΔΑΝΙΚΑ ΑΕΡΙΑ - ΕΡΓΟ 1. Να υπολογιστεί η πυκνότητα του αέρα σε πίεση 0,1 MPa και θερμοκρασία 20 ο C. (R air =0,287 kj/kgk) 2. Ποσότητα αέρα 1 kg εκτελεί τις παρακάτω διεργασίες: Διεργασία 1-2: Αδιαβατική
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις. Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι
 Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
ΛΥΣΕΙΣ. ΘΕΜΑ A Να γράψετε στο τετράδιο σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
 ΜΑΘΗΜΑ / ΤΑΞΗ: ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ / B ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1η ΗΜΕΡΟΜΗΝΙΑ: 04/11/1 ΛΥΣΕΙΣ ΘΕΜΑ A Να γράψετε στο τετράδιο σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράμμα που αντιστοιχεί
ΜΑΘΗΜΑ / ΤΑΞΗ: ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ / B ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1η ΗΜΕΡΟΜΗΝΙΑ: 04/11/1 ΛΥΣΕΙΣ ΘΕΜΑ A Να γράψετε στο τετράδιο σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράμμα που αντιστοιχεί
2. Ασκήσεις Θερμοδυναμικής. Ομάδα Γ.
 . σκήσεις ς. Ομάδα..1. Ισοβαρής θέρμανση και έργο. Ένα αέριο θερμαίνεται ισοβαρώς από θερμοκρασία Τ 1 σε θερμοκρασία Τ, είτε κατά την μεταβολή, είτε κατά την μεταβολή Δ. i) Σε ποια μεταβολή παράγεται περισσότερο
. σκήσεις ς. Ομάδα..1. Ισοβαρής θέρμανση και έργο. Ένα αέριο θερμαίνεται ισοβαρώς από θερμοκρασία Τ 1 σε θερμοκρασία Τ, είτε κατά την μεταβολή, είτε κατά την μεταβολή Δ. i) Σε ποια μεταβολή παράγεται περισσότερο
Προσανατολισμού Θερμοδυναμική
 ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ 60 Ον/μο:.. Β Λυκείου Ύλη: Κινητική θεωρία αερίων Προσανατολισμού Θερμοδυναμική 8-2-2015 Θέμα 1 ο : 1. Η απόλυτη θερμοκρασία ορισμένης ποσότητας αερίου διπλασιάζεται υπό σταθερό όγκο.
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ 60 Ον/μο:.. Β Λυκείου Ύλη: Κινητική θεωρία αερίων Προσανατολισμού Θερμοδυναμική 8-2-2015 Θέμα 1 ο : 1. Η απόλυτη θερμοκρασία ορισμένης ποσότητας αερίου διπλασιάζεται υπό σταθερό όγκο.
ΘΕΡΜΙΔΟΜΕΤΡΙΑ ΘΕΡΜΟΚΡΑΣΙΑ ΜΗΔΕΝΙΚΟΣ ΝΟΜΟΣ. Μονάδες - Τάξεις μεγέθους
 ΘΕΡΜΙΔΟΜΕΤΡΙΑ ΘΕΡΜΟΚΡΑΣΙΑ ΜΗΔΕΝΙΚΟΣ ΝΟΜΟΣ Μονάδες - Τάξεις μεγέθους Μονάδες ενέργειας 1 cal = 4,19 J Πυκνότητα νερού 1 g/cm 3 = 1000 Kg/m 3. Ειδική θερμότητα νερού c = 4190 J/Kg.K = 1Kcal/Kg.K = 1 cal/g.k
ΘΕΡΜΙΔΟΜΕΤΡΙΑ ΘΕΡΜΟΚΡΑΣΙΑ ΜΗΔΕΝΙΚΟΣ ΝΟΜΟΣ Μονάδες - Τάξεις μεγέθους Μονάδες ενέργειας 1 cal = 4,19 J Πυκνότητα νερού 1 g/cm 3 = 1000 Kg/m 3. Ειδική θερμότητα νερού c = 4190 J/Kg.K = 1Kcal/Kg.K = 1 cal/g.k
ΜΟΡΦΕΣ ΕΝΕΡΓΕΙΑΣ. ΕΝΕΡΓΕΙΑ ΔΙΕΡΓΑΣΙΩΝ (Μεταβατικές) ΕΝΕΡΓΕΙΑ ΣΥΣΤΗΜΑΤΟΣ ΕΡΓΟ ΘΕΡΜΟΤΗΤΑ
 Έργο - Θερμότητα ΜΟΡΦΕΣ ΕΝΕΡΓΕΙΑΣ ΕΝΕΡΓΕΙΑ ΔΙΕΡΓΑΣΙΩΝ (Μεταβατικές) ΕΡΓΟ ΘΕΡΜΟΤΗΤΑ ΕΝΕΡΓΕΙΑ ΣΥΣΤΗΜΑΤΟΣ ΕΞΩΤΕΡΙΚΗ (Κινητική, Δυναμική) ΕΣΩΤΕΡΙΚΗ (Εσωτερική [U], Ενθαλπία [Η]) Χαρακτηριστικά και Σύμβαση
Έργο - Θερμότητα ΜΟΡΦΕΣ ΕΝΕΡΓΕΙΑΣ ΕΝΕΡΓΕΙΑ ΔΙΕΡΓΑΣΙΩΝ (Μεταβατικές) ΕΡΓΟ ΘΕΡΜΟΤΗΤΑ ΕΝΕΡΓΕΙΑ ΣΥΣΤΗΜΑΤΟΣ ΕΞΩΤΕΡΙΚΗ (Κινητική, Δυναμική) ΕΣΩΤΕΡΙΚΗ (Εσωτερική [U], Ενθαλπία [Η]) Χαρακτηριστικά και Σύμβαση
