OSNOVNA ŠOLA VOJNIK. Raziskovalna naloga: KRISTALI MORSKE SOLI
|
|
|
- Νάρκισσα Μανωλάς
- 6 χρόνια πριν
- Προβολές:
Transcript
1 OSNOVNA ŠOLA VOJNIK Raziskovalna naloga: KRISTALI MORSKE SOLI Vojnik 2009
2 OSNOVNA ŠOLA VOJNIK Raziskovalna naloga: KRISTALI MORSKE SOLI Mentor: Katja Selčan Avtorja: Ula Selčan, 1996 Lektor: g. Gregor Palčnik Tilen Marčič, 1995 Vojnik
3 KAZALA KAZALO VSEBINE POVZETEK 5 ZAHVALA 6 1. UVOD Namen Hipoteze Raziskovalne metode 8 2. TEORETIČNI DEL KAJ JE SOL? ZGODOVINA SOLI PRIDOBIVANJE SOLI VRSTE SOLI SLANOST ZVEZA MED SLANOSTJO IN GOSTOTO LASTNOSTI MORSKE VODE Raztopine Raztapljanje kuhinjske soli ali natrijevega klorida v vodi Izparevanje izhlapevanje in utekočinjanje Ionska vez Ionski kristali EKSPERIMENTALNI DEL ZBIRANJE VZORCEV Izhlapevanje morske vode Gostota morske vode vzorca Vsebnost soli Mikroskopiranje ZAKLJUČEK VIRI IN LITERATURA 24 3
4 KAZALO TABEL Tabela 1: Odjemni vzorci 17 Tabela 2: Podatki o masi 19 Tabela 3: Podatki o gostoti 20 KAZALO SLIK IN GRAFIKONOV Slika1: Shema nastanka NaCl 15 Slika2: Prerez kristala natrijevega klorida 16 Slika 3: Merilni valj s 50 ml morske vode 18 Slika 4: Tehtanje čaš 18 Slika 5: Tehtanje morske vode 18 Slika 6: Izhlapevanje morske vode 18 Slika 7: Izhlapevanje po 6 dneh 19 Slika 8: Izhlapevanje po 14 dneh 19 Slika 9: Kristal morske soli najmanjša povečava- Koper 22 Slika 10: Kristal morske soli srednja povečava- Koper 22 4
5 POVZETEK KEMIJA Naslov naloge: KRISTALI MORSKE SOLI Avtorja: Ula Selčan, Tilen Marčič Mentorica: ga. Katja Selčan Lektor: g. Gregor Palčnik Šola: OŠ Vojnik Namen najine raziskovalne naloge je bil ugotoviti, koliko kristalov soli bo nastalo pri izhlapevanju morske vode. Najino delo se je začelo z zbiranjem podatkov o morski vodi, vsebnosti soli in zgradbi kristalov. Veliko podatkov in informacij sva dobila v šolski knjižnici in na internetu. Sledilo je eksperimentalno delo v domačem labolatoriju. Za metodo ločevanja sva uporabila izhlapevanje. Morsko vodo sva pustila izhlapeti, da so nastali kristali morske soli. Zanimalo naju je, v katerem vzorcu morske vode bo ostalo največ kristalov soli. Zanimala naju je tudi gostota morske vode v najinih vzorcih. Kristale soli, ki so nastali pri izhlapevanju morske vode, sva si ogledala z mikroskopom preko digitalne kamere. Pri izhlapevanju morske vode sva dobila različno količino kristalov morske soli, vsi pa so pod mikroskopom imeli enako strukturo. 5
6 ZAHVALA Zahvaljujeva se: - svoji mentorici gospe Katji Selčan za usmerjanje na raziskovalni poti, - vsem, ki so nama prinesli vzorce morske vode iz različnih krajev ob obali Jadranskega morja, - lektorju gospodu Gregorju Palčniku, ki je nalogo jezikovno pregledal in - vsem učiteljem za spodbudo pri raziskovalnem delu. 6
7 1. UVOD V našem življenju je zelo pomembna snov sol (NaCl natrijev klorid). Za nemoteno delovanje organizma je v ustreznih količinah nepogrešljiva. Natrijev klorid je glavna sestavina kuhinjske soli, ki jo uporabljamo tudi pri pripravi mnogih jedi. Uporabljamo morsko sol, ki jo pridobivamo iz morske vode in ki vsebuje magnezijeve in kalcijeve spojine ter elementarni jod. Sol pa vsebuje tudi še sredstva, ki preprečujejo strjevanje, npr. magnezijev karbonat MgCO 3. Jod je zelo pomemben za organizem, kajti preprečuje nastanek bolezni (golšavost). Tega kamena sol, ki jo kopljejo v solnih rudnikih, ne vsebuje. Kameni soli morajo zato jod dodajati v obliki kalijevega ali natrijevega jodida. Pretirana uporaba soli je lahko tudi zdravju škodljiva, saj zvišuje krvni tlak. Sol je bila izjemno pomembna v preteklosti, pred iznajdbo hladilnikov, ker je bila edino poznano sredstvo za konzerviranje živil. Dodatek soli prepreči rast in razvoj bakterij oziroma kvarjenje živil. Sicer pa je sol je prisotna vsepovsod okoli nas. Z njo se srečujemo v prehrambeni industriji, v medicini in doma pri kuhanju, na morju, ko se potimo itd. 1.1 Namen naloge Namen najine raziskovalne naloge je, da ugotoviva s pomočjo eksperimenta, koliko gramov soli je v enem litru morske vode, kolikšna je gostota morske vode najinih vzorcev ter kakšna je sestava kristalov morske soli. V teoretičnem delu bova najprej ugotovila, kaj sploh je sol, kako nastane in iz česa je sestavljena. V eksperimentalnem delu pa bova izvedla nekaj poskusov ločevanja soli iz morske vode, s katerimi bova potrdila ali ovrgla svoje hipoteze. Morsko vodo bova izparevala in kristalizirala, nato pa primerjala dobljene rezultate. 7
8 1.2 Hipoteze Predvidevava: - da bo vsebnost soli v morski vodi vzorcev približno enaka; - da bo približno 35 gramov soli na 1 liter morske vode; - da bo gostota morske vode približno 1035 kg/m 3 ; - da bodo nastali kristali enaki in - da bo največ kristalov soli ostalo pri izhlapevanju morske vode iz Turčije, ki je edini vzorec, ki ni iz Jadranskega morja. 1.3 Raziskovalne metode Raziskovalna naloga je nastajala na osnovi kabinetnega dela, kjer sva proučevala obstoječo literaturo, podatke in risala tabele. Terensko delo je zajemalo zbiranje vzorcev morske vode. Izvedla sva eksperiment ločevanje soli iz morske vode z izhlapevanjem le-te. Eksperiment je obsegal opazovanje in beleženje ter zapisovanje podatkov v tabele. Na osnovi poskusa sva izračunala gostoto in vsebnost soli v danih vzorcih. Laboratorijsko delo je potekalo doma, pa tudi v šolskem laboratoriju. Prav tako tudi mikroskopiranje. 8
9 2. TEORETIČNI DEL 2.1 KAJ JE SOL? Je kemijska spojina natrijevega klorida. Sol pridelujemo na solnih poljih. Morska voda je speljana iz izparilnih bazenov v kristalizacijske. Po tem postopku pridobivajo morsko sol. V 1l morske vode je približno 30g soli. Kristali soli so kockasti in so, kadar so čisti in brez primesi, brezbarvni. Sol je zelo težka in občutljiva na vlago. Je tudi zelo škodljiva. Človek naj bi na dan zaužil le 6 gramov soli. Glede na to, da vsa živila vsebujejo sol, moramo biti skrajno pazljivi in disciplinirani, da te meje ne presežemo. Zaradi prevelikih količin soli lahko pride do različnih obolenj: raka na želodcu, povečanja krvnega pritiska, ledvičnih kamnov. Prevelika količina zaužite soli lahko vpliva tudi na trdoto naših kosti. 2.2 ZGODOVINA SOLI Sol je bila zelo cenjena že daleč nazaj. V predzgodovinskem času so jo uporabljali že kot začimbo, za konzerviranje živil in strojenje kož. Egipčani so jo uporabljali pri balzamiranju mumij, veliki uporabniki so bili Rimljani. V industriji je sol tudi danes pomembna surovina. Prvi zapis o piranskih solinah je znan iz leta 804, sol se je prodajala Beneški republiki, ki se je bojevala za ekonomsko prevlado v Sredozemlju. Pozneje so soline prešle pod avstrijsko upravo, avstro-ogrska monarhija pa je razglasila sol za državni monopol. Lastniki solnih fondov in solinarji so si prizadevali povečevati proizvodnjo in porabo soli. Ob pomoči trgovcev so solinarji velike količine soli pretihotapili v slovensko zaledje. Po razpadu avstro-ogrske monarhije je piranske soline prevzela Italija. V bližini Slovenije je bilo tudi nekaj pomembnih rudnikov kamene soli (Tuzla, Salzburg), kar je pomenilo lažjo dostopnost soli in omogočilo razcvet trgovanja z njo. V Sloveniji je uporaba soli prevelika. Težko bo spremeniti zakoreninjeno razvado. 9
10 2.2.1 PRIDOBIVANJE SOLI Že davno pred našim štetjem je bilo znano pridelovanje in trgovanje s soljo. Prebivalci Bretanije pa tudi Galci in Normani so že pred našim štetjem s pridom izkoriščali ugodnosti soli. V preprostih pečeh so v glinenih ali bronastih posodah greli slano vodo iz močvar in na ta način dobili sol v kockah. Tak način je bil primeren za hrambo in prevoz v druge kraje. Plimovanje in ostanki morske soli v kotanjah kamnitih morskih obal so ljudi privedli do zamisli o gradnji sistema zapornic, kanalov in bazenov, kjer bi bilo pridobivanje morske soli enostavno, izdatno, predvsem pa bolj donosno. Glede na način pridobivanja delimo sol na evaporirano, kameno in morsko sol VRSTE SOLI Sol delimo glede na način pridobivanja na evaporirano, kameno in morsko sol. Evaporirana sol Pridobiva se z industrijskim izparevanjem slane vode v industrijskih kristalizatorjih. Kristali evaporirane soli so kockaste ali okrogle oblike, velikosti okoli 1 mm in izredno homogeni. Kamena sol S predelavo solne rude pridobivajo kameno sol. Običajno vsebuje kamena sol dodatke ostalih kamenin, ki se nahajajo v nahajališčih soli. Granulacija zrn je lahko zelo različna, enakomerne granulacije lahko dosežemo z mletjem in sejanjem. Morska sol Z naravno kristalizacijo soli v solnih bazenih pridobivajo morsko sol. Granulacijska sestava morske soli je različna. Morska sol poleg NaCl vsebuje tudi bogastvo ostalih mineralov (Ca, Mg, K, Br, F, I), ki se skupaj z NaCl kristalizirajo v solnih bazenih. 10
11 Nastajanje soli v solinah Morska sol nastaja v solinah, kjer je pridobljena z naravno kristalizacijo. Takšna vsebuje največ telesu potrebnih mineralov. Rafinirano sol, ki jo uporabljajo za kemično industrijo, pa očistijo mineralov, da dosežejo čim bolj čist natrijev klorid. Iz kristalov na površini slanice nastaja solni cvet, ki dopolnjuje hrano s svojim okusom in vonjem. 2.3 SLANOST Slanost nam pove količino soli, raztopljene v enem litru vode. Med solmi je največ natrijevega klorida (78 %), ostali delež pa predstavljajo druge snovi. Povprečna slanost je 35, kar pomeni, da je v 1 litru vode 35g soli. Slanost povečujejo visoke temperature in s tem stalno izparevanje. Zmanjšujejo jo pritoki sladke vode, nizke temperature, stalne padavine. 2.4 ZVEZA MED SLANOSTJO IN GOSTOTO m Gostota je količnik med maso in prostornino. ρ =. V Gostota (ρ) čiste vode je približno 1000 kg/m³. Zaradi raztopljene soli ima morska voda večjo gostoto; povprečna gostota na gladini je približno 1027 kg/m³. Na odstopanje gostote morske vode od te vrednosti vplivata dva dejavnika: - temperatura in - slanost. Gostota morske vode se zmanjša, če se poveča temperatura. Gostota morske vode se poveča z večanjem slanosti. V primeru, da imamo dve plasti vode z enako slanostjo, bo plast toplejše vode plavala na plasti hladnejše vode. Vendar ni vse tako enostavno, kajti temperatura ima večji vpliv na gostoto od slanosti. Tako se lahko zgodi, da plast toplejše vode z večjo slanostjo plava na plasti hladnejše vode z manjšo slanostjo. Temperatura vode v oceanih 11
12 je z naraščajočo globino vse nižja, kar posledično pomeni, da je na oceanskem dnu gostota vode največja, na gladini pa najmanjša. 2.5 LASTNOSTI MORSKE VODE Temperatura Morsko vodo segreva izključno sonce. Le-to segreje samo površinski sloj vode, globlje pa se temperatura poviša zaradi kroženja vode. Najhladnejša so morja na polih, najtoplejša pa so tropska morja (direkten kot sončnih žarkov). Hladni in topli morski tokovi vplivajo na temperaturo. Največje je letno nihanje temperatur morske vode v zmerno toplem pasu, v tropskih in polarnih morjih pa zelo skromno,. Morska voda se počasneje ogreva in ohlaja kot kopno. Gibanje Valovanje nastane kot posledica delovanja vetrov, izjema so tsunamiji, ki jih sprožijo potresi ali vulkani na morskem dnu. Plimovanje ali bibavica je izmenjavanje višje ali nižje morske gladine oziroma plime in oseke, ki ju povzročata privlačni sili lune in sonca. Morska gladina se dvigne dvakrat na dan in tudi zniža. Razlika na odprtem morju je 1m, v Jadranskem morju pa cm. Morski tokovi so najobsežnejše gibanje morske vode. Delimo jih na: - tople tokove (stran od ekvatorja), - hladne tokove (proti ekvatorju). Na smer vplivata tudi odklonska sila in oblika obale, najmanjši vpliv pa imajo stalni vetrovi. 12
13 2.6 Raztopine Raztopine so zmesi. Da dobimo raztopino, potrebujemo topilo in topljenec. Topljenec je lahko trdna, tekoča ali plinasta snov. Raztopine imajo drugačne lastnosti kot čiste snovi, ki jih sestavljajo. Tako raztopina kuhinjske soli v vodi kasneje zavre kot voda. Slana voda ima višje vrelišče kot neslana voda. V raztopinah so delci raztopljene snovi pomešani med delci topila. RAZTOPINA = TOPILO + TOPLJENEC 2.7 Raztapljanje kuhinjske soli ali natrijevega klorida v vodi Natrijev klorid je ionska spojina. V trdnem natrijevem kloridu so v kristalni mreži ioni natrija in klora. V vodni raztopini so ioni obdani z molekulami vode. Vodna raztopina natrijevega klorida prevaja električni tok, ker so v njej gibljivi ioni. Če voda iz raztopine izhlapi, preostane trden natrijev klorid. 2.8 Izparevanje, izhlapevanje in utekočinjanje Izparevanje je postopek, pri katerem tekočina, ki jo segrevamo, preide iz tekočega v plinasto agregatno stanje. Izparevanje tekočine poteka pri temperaturi vrelišča. Pri segrevanju raztopin, topilo izpari, preostane pa trdna snov, ki je bila raztopljena v topilu. Pri segrevanju slane vode voda izpari. Preostane sol, ki je bila v vodi raztopljena. Prehod tekočine v plin pri temperaturah, nižjih od vrelišča, imenujemo izhlapevanje. Iz tekočine izhajajo hlapi tekočine. 13
14 K hitrosti izhlapevanja močno vplivata zunanja temperatura in veter. Če želimo primerjati hitrost izhlapevanja različnih tekočin, moramo poskrbeti, da so pogoji pri poskusu enaki. Kapljevina lahko preide v plinasto stanje, če molekule prejmejo dovolj toplote. Kadar se jim notranja energija tako poveča, da premagajo medsebojne privlačne sile, kapljevina preide v plin. Temperaturo, pri kateri snov izpareva, imenujemo temperatura vrelišča (vrelišče). Prehod kapljevine v plin pri tej temperaturi imenujemo izparevanje. Prehod kapljevine v plin pa je možen tudi pri nižjih temperaturah. Nekateri gradniki na površini kapljevine imajo dovolj energije, da premagajo privlačne sile, ki jih vežejo na sosednje gradnike, zapustijo kapljevino in preidejo v plinasto stanje. Takšen prehod imenujemo izhlapevanje. Izhlapevanje je izrazitejše pri višjih temperaturah. Toplota, ki je potrebna za spremembo stanja, prihaja iz kapljevine in iz okolice. Zato se kapljevina in okolica hladita. Tako lahko razložimo, zakaj se telo pri potenju hladi. Ko pot izhlapeva, se telo (okolica kapljevine) ohlaja. Glede na izparevanje in izhlapevanje ločimo med paro in hlapi. Kadar je plin v okoliščinah, ki se ne razlikujejo znatno od okoliščin izparevanja, ga navadno imenujemo para. Plin pri pogojih, ko poteka izhlapevanje, imenujemo hlapi. Tako poimenovanje je zelo nazorno in pomaga pri razumevanju pojavov, posebno tistih, ki potekajo v naravi. Utekočinjanje ali kondenzacija je prehod iz plinastega stanja v kapljevinsko. Pri kondenzaciji plin toploto odda. Pri izhlapevanju vode prehajajo v zrak vodni hlapi, ki pa jih ne vidimo. Če se vodni hlapi v atmosferi utekočinijo (kondenzirajo), nastanejo oblaki ali megla. 2.9 Ionska vez Ionska vez nastane, ko atomi kovin oddajo svoje zunanje elektrone atomom nekovin. Atomi kovin postanejo takrat pozitivno nabiti ioni (kationi), atomi nekovin pa negativno nabiti (anioni). Kationi in anioni se med seboj privlačijo, saj imajo nasprotne naboje. Privlačno silo med ioni imenujemo ionska vez. Ioni so delci, ki imajo električni naboj. Imamo pozitivne in negativne ione. Nasprotno nabiti se privlačijo, medtem ko se enako 14
15 nabiti odbijajo. Pozitivno nabiti ion se imenuje tudi kation, negativno nabiti ion pa anion. Nastanek ionske vezi, ko atom natrija odda svoj zunanji elektron atomu klora. Slika1: Shema nastanka NaCl Vir: Pri reakciji natrija s klorom nastane natrijev klorid. Pri tem natrijevi atomi oddajajo elektrone klorovim atomom in nastajajo natrijevi in kloridni ioni. Atom klora ima na zadnji lupini sedem elektronov. Ko atom klora sprejme elektron in postane negativno nabiti ion ali anion. Na ta način doseže stabilno zunanjo lupino. Atom natrija ima en zunanji elektron, ki ga odda iz zunanje lupine atomu klora. Tako oba dosežeta oktet elektronov na zunanji lupini Ionski kristali Med natrijevimi ioni in ioni klora vlada močan elektrostatični privlak. Posledica privlačnih sil med nasprotno nabitimi ioni je pravilno razporejanje natrijevih in klorovih ionov v prostoru, saj se okoli pozitivno nabitega natrijevega iona razporedijo negativno nabiti kloridni ioni in obratno. Nastane ionski kristal, katerega gradniki so ioni. Delci v kristalih so razporejeni na urejen in periodičen način. 15
16 Slika 2: Prerez kristala natrijevega klorida Vir: Plasti ionov potekajo v vseh smereh. Okrog enega natrijevega iona je 6 kloridnih ionov in obratno. Spojina natrijevega klorida je električno nevtralna, to pomeni, da je število kationov enako številu anionov. Razmerje med anioni in kationi nam prikazuje empirična formula. NaCl empirična formula natrijevega klorida S kemijskim zapisom lahko empirično formulo NaCl razložimo takole: Na Na + + 1e Cl + 1e Cl Na + + Cl NaCl 16
17 3. EKSPERIMENTALNI DEL 3.1 ZBIRANJE VZORCEV Morsko vodo sva dobila s pomočjo sošolcev in očeta od Ule, ki je bil službeno v Albaniji in Črni Gori. Sošolka Jerneja nama je prinesla morsko vodo s Korčule, sošolec Alen pa iz Turčije. Sama sva prinesla vzorec morske vode iz Kopra. 4 vzorci so bili iz Jadranskega morja, eden pa iz Sredozemskega morja. Za izhlapevanje morske vode sva imela 5 vzorcev morske vode: Tabela 1: Odjemni vzorci Mesto odjema vzorca Čas odjema vzorca Morje Koper oktober Jadransko morje Korčula oktober Jadransko morje Turčija oktober Sredozemsko morje Albanija januar Jadransko morje Črna gora januar Jadransko morje 3.2 Izhlapevanje morske vode Priprava eksperimenta Morsko vodo sva pripravila za izhlapevanje. Potrebni pripomočki in laboratorijski pribor, ki sva ga potrebovala: - 5 čaš, - tehtnica in - merilni valj. Potek eksperimenta Začetek eksperimentiranja: 13. januar 2009 Najprej sva stehtala vse prazne čaše. V menzuri sva odmerila 50 ml morske vode, ki sva jo nato nalila v čaše. V vsako 50 ml. Čaše sva označila z imenom vzorca. Nato sva še enkrat stehtala 50 ml morske vode s 17
18 čašo. Čaše sva postavila na okensko polico. Čaše sva pustila na polici in vsake 3 dni ugotavljala, koliko vode je že izhlapelo. Podatke o merjenju sva zapisala v tabelo. Slika 3: Merilni valj s 50 ml morske vode Slika 4: Tehtanje čaš (foto: Ula Selčan, ) (foto: Ula Selčan, ) Slika 5: Tehtanje morske vode Slika 6: Izhlapevanje morske vode (foto: Ula Selčan, ) (foto: Ula Selčan, ) 18
19 Kaj je masa? Masa je osnovna fizikalna količina. Vse snovi oz. telesa imajo maso. Izmerimo jo s tehtnico in označimo z majhno pisano črko m. Osnovna enota za maso je kilogram (kg). Zelo sva bila presenečena, ko sva stehtala vseh 5 čaš, kajti nobena čaša ni imela enake mase. Tabela 2: Podatki o masi Vzorec Masa čaše v [g] Masa čaše + morska voda v [g] Masa čaše + kristali v [g] Masa kristalov v [g] Albanija 108,0 154,5 110,0 2,0 Črna gora 98,0 147,8 101,0 3,0 Koper 98,8 148,5 101,2 2,4 Korčula 103,0 154,2 105,6 2,6 Turčija 102,5 152,5 104,8 2,3 Ugotovila sva, da je največja količina kristalov morske soli v čaši, kjer je bila morska voda iz Črne Gore, najmanj soli, pa je bilo v čaši, kjer je bila morska voda iz Albanije. Nad rezultati sva bila zelo presenečena. Stanje čaš o 6 dneh, Slika 7: Izhlapevanje po 6 dneh Slika 8: Izhlapevanje po 14 dneh (foto: Ula Selčan, ) (foto: Ula Selčan, ) 19
20 3.3 Gostota morske vode vzorca Zanimala naju je gostota morske vode. Izračunala sva jo po enačbi: ρ= V m ρ: gostota snovi m: masa snovi V: prostornina ali volumen snovi Tabela 3: Podatki o gostoti Vzorec Masa čaše Masa čaše + Masa vode Prostornina Gostota v [g] morska voda v [g] v [g] vode v ml vode v ml Albanija 108,0 154,5 46,5 50 0,930 Črna gora 98,0 147,8 49,8 50 0,996 Koper 98,8 148,5 49,7 50 0,994 Korčula 103,0 154,2 51,2 50 1,024 Turčija 102,5 152,5 50,0 50 1,000 Nad dobljenimi podatki sva bila nemalo presenečena. Vendar ne smemo pozabiti, da ima temperatura večji vpliv na gostoto od slanosti. Temperatura vode v oceanih je z naraščajočo globino vse nižja, kar posledično pomeni, da je na oceanskem dnu gostota vode največja, na gladini pa najmanjša. Najina voda pa je seveda bila odvzeta na gladini, ob obali. Ugotavljava, da se gostota snovi pri višji temperaturi zmanjša. Primer: Izračun gostote morske vode iz Korčule. V = 50 ml m = 51,2 g ρ =? ρ = V m ρ = 51,2 g 50ml Gostota vode je 1,024 kg/l, kar pomeni: ρ = 1,024 g/ml= 1,024 kg/l 1 liter morske vode iz Korčule tehta 1,024 kilograma. 20
21 3.4 Vsebnost soli Izračun vsebnosti soli v vzorcih morske vode. Vzorec: Koper Vzorec: Albanija V 50 ml slane vode _2,4 g soli V 1000 ml slane vode x g soli V 50 ml slane vode _2 g soli V 1000 ml slane vode x g soli X = 1000 ml 2,4g 50ml = 48 g soli X = 1000 ml 2,0g 50ml = 40 g soli Vzorec: Črna Gora Vzorec: Turčija V 50 ml slane vode 3,0 g soli V 1000 ml slane vode x g soli V 50 ml slane vode 2,3 g soli V 1000 ml slane vode x g soli X = 1000 ml 3,0 g 50ml = 60 g soli X = 1000 ml 2,3g 50ml = 46 g soli Vzorec: Korčula V 50 ml slane vode _2,6 g soli V 1000 ml slane vode x g soli X = 1000 ml 2,6g 50ml = 52 g soli Slanost najine morske vode se giblje od 40 g do 60 g, oziroma promíle ( ) ta je tisoči del celote, kar se nama zdi veliko. Ugotavljava, da je vsebnost soli zelo močna. 3.5 Mikroskopiranje Kristale, ki so nastali po izhlapevanju vode, sva pogledala pod mikroskopom. Najprej pri najmanjši povečavi, potem pa še pri srednji povečavi. 21
22 Pogledala sva vse kristale iz vseh čaš in ugotovila, da je pri vseh kristalih morske soli struktura enaka. Slika 9: Kristal morske soli najmanjša povečava Koper (foto: Ula Selčan, ) Slika 10: Kristal morske soli srednja povečava Koper (foto: Ula Selčan, ) 22
23 4. ZAKLJUČEK Z izhlapevanjem morske vode sva dobila kristale morske soli. Uporabila sva torej metodo ločevanja: izhlapevanje. Pripomočki, ki sva jih potrebovala, so bili: menzura ali merilni valj, tehtnica in pet čaš. Po približno treh tednih sva dobila kristalčke. Kristali iz Kopra in Korčule so si zelo podobni, po barvi ter po obliki iz Turčije pa so malce večji, nekateri pa celo beli. Kristalčke sva s pomočjo digitalne kamere pogledala tudi pod mikroskopom in dobila zelo lepo sliko strukture kristala. Vsebnost soli se zelo razlikuje med vzorci in naju je zelo presenetila; takega rezultata nisva pričakovala. Pri najinih vzorcih je več kot 35 g soli na 1 l morske vode. Gostota morske vode je bila pri najinem izračunu malo manjša, vendar minimalno. Prav tako se najina hipoteza, da bo največ kristalčkov v čaši, kjer je bila morska voda iz Turčije ni potrdila. Največ kristalčkov je bilo v čaši z morsko vodo iz Črne gore. Prav sva predvidevala, da bodo nastali kristali enaki. Pri raziskovalnem delu sva se veliko naučila in spoznala eksperimentalno delo, svoje rezultate bova predstavila svojim sošolcem in na dnevu odprtih vrat, ki bo v mesecu marcu, si bodo lahko najine kristalčke vsi ogledali z mikroskopom in digitalno kamero. 23
24 5. VIRI IN LITERATURA Enciklopedija znanosti. Naravoslovje. Ljubljana: Slovenska knjiga. 2. Lawrie Ryan Preproste razlage kemijskih poskusov. Ljubljana: Tehniška založba Slovenije. 3. Bukovec N., Brenčič J Kemija za gimnazije 1: Učbenik. Ljubljana: DZS. 4. Pucelj Vesna Kuhinjska sol [Online]. Ljubljana: Institut za varovanje zdravja Republike Slovenije. [Članek dobljen ]. Dostopno na naslovu: 5. Gabrič Alenka Kemija danes 1, učbenik 8/9. Ljubljana: DZS 6. Boh B., Devetak I Ionska vez [Online]. [Članek dobljen ]. Dostopno na naslovu: view.php?id= _. Vse o soli [Online]. [Članek dobljen ]. Dostopno na naslovu: 8. _ Ionski kristali [Online]. [Članek dobljen ]. Dostopno na naslovu: sklop/ionski_kristali.html. 9. _. Kaj je masa? [Online]. [Članek dobljen ]. Dostopno na naslovu: sklop/kaj_je_masa_znanje_iz_naravoslovja.html 10. _. Nastanek vezi [Online]. [Članek dobljen ]. Dostopno na naslovu: sklop/nastanek_vezi.html 24
Diferencialna enačba, v kateri nastopata neznana funkcija in njen odvod v prvi potenci
 Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 5. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Funkcijske vrste. Matematika 2. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 2. april Gregor Dolinar Matematika 2
 Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 22. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
Tretja vaja iz matematike 1
 Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Osnove elektrotehnike uvod
 Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 14. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
Kontrolne karte uporabljamo za sprotno spremljanje kakovosti izdelka, ki ga izdelujemo v proizvodnem procesu.
 Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 21. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
NEPARAMETRIČNI TESTI. pregledovanje tabel hi-kvadrat test. as. dr. Nino RODE
 NEPARAMETRIČNI TESTI pregledovanje tabel hi-kvadrat test as. dr. Nino RODE Parametrični in neparametrični testi S pomočjo z-testa in t-testa preizkušamo domneve o parametrih na vzorcih izračunamo statistike,
NEPARAMETRIČNI TESTI pregledovanje tabel hi-kvadrat test as. dr. Nino RODE Parametrični in neparametrični testi S pomočjo z-testa in t-testa preizkušamo domneve o parametrih na vzorcih izračunamo statistike,
Tabele termodinamskih lastnosti vode in vodne pare
 Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
PONOVITEV SNOVI ZA 4. TEST
 PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK
 1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
1. Trikotniki hitrosti
 . Trikotniki hitrosti. Z radialno črpalko želimo črpati vodo pri pogojih okolice z nazivnim pretokom 0 m 3 /h. Notranji premer rotorja je 4 cm, zunanji premer 8 cm, širina rotorja pa je,5 cm. Frekvenca
. Trikotniki hitrosti. Z radialno črpalko želimo črpati vodo pri pogojih okolice z nazivnim pretokom 0 m 3 /h. Notranji premer rotorja je 4 cm, zunanji premer 8 cm, širina rotorja pa je,5 cm. Frekvenca
MATEMATIČNI IZRAZI V MAFIRA WIKIJU
 I FAKULTETA ZA MATEMATIKO IN FIZIKO Jadranska cesta 19 1000 Ljubljan Ljubljana, 25. marec 2011 MATEMATIČNI IZRAZI V MAFIRA WIKIJU KOMUNICIRANJE V MATEMATIKI Darja Celcer II KAZALO: 1 VSTAVLJANJE MATEMATIČNIH
I FAKULTETA ZA MATEMATIKO IN FIZIKO Jadranska cesta 19 1000 Ljubljan Ljubljana, 25. marec 2011 MATEMATIČNI IZRAZI V MAFIRA WIKIJU KOMUNICIRANJE V MATEMATIKI Darja Celcer II KAZALO: 1 VSTAVLJANJE MATEMATIČNIH
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * NAVODILA ZA OCENJEVANJE. Sreda, 3. junij 2015 SPLOŠNA MATURA
 Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
IZPIT IZ ANALIZE II Maribor,
 Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 15. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 15. oktober 2013 Oglejmo si, kako množimo dve kompleksni števili, dani v polarni obliki. Naj bo z 1 = r 1 (cosϕ 1 +isinϕ 1 )
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 15. oktober 2013 Oglejmo si, kako množimo dve kompleksni števili, dani v polarni obliki. Naj bo z 1 = r 1 (cosϕ 1 +isinϕ 1 )
Slika, vir: http://www.manataka.org
 KEMIJA Slika, vir: http://www.manataka.org RAZTOPINE SPLOŠNE INFORMACIJE O GRADIVU Učno gradivo je nastalo v okviru projekta Munus 2. Njegovo izdajo je omogočilo sofinanciranje Evropskega socialnega sklada
KEMIJA Slika, vir: http://www.manataka.org RAZTOPINE SPLOŠNE INFORMACIJE O GRADIVU Učno gradivo je nastalo v okviru projekta Munus 2. Njegovo izdajo je omogočilo sofinanciranje Evropskega socialnega sklada
Kotne in krožne funkcije
 Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 10. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
p 1 ENTROPIJSKI ZAKON
 ENROPIJSKI ZAKON REERZIBILNA srememba: moža je obrjea srememba reko eakih vmesih staj kot rvota srememba. Po obeh sremembah e sme biti obeih trajih srememb v bližji i dalji okolici. IREERZIBILNA srememba:
ENROPIJSKI ZAKON REERZIBILNA srememba: moža je obrjea srememba reko eakih vmesih staj kot rvota srememba. Po obeh sremembah e sme biti obeih trajih srememb v bližji i dalji okolici. IREERZIBILNA srememba:
Simbolni zapis in množina snovi
 Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
SEMINAR IZ KOLEGIJA ANALITIČKA KEMIJA I. Studij Primijenjena kemija
 SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
Numerično reševanje. diferencialnih enačb II
 Numerčno reševanje dferencaln enačb I Dferencalne enačbe al ssteme dferencaln enačb rešujemo numerčno z več razlogov:. Ne znamo j rešt analtčno.. Posamezn del dferencalne enačbe podan tabelarčno. 3. Podatke
Numerčno reševanje dferencaln enačb I Dferencalne enačbe al ssteme dferencaln enačb rešujemo numerčno z več razlogov:. Ne znamo j rešt analtčno.. Posamezn del dferencalne enačbe podan tabelarčno. 3. Podatke
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * FIZIKA NAVODILA ZA OCENJEVANJE. Petek, 10. junij 2016 SPLOŠNA MATURA
 Državni izpitni center *M16141113* SPOMLADANSKI IZPITNI ROK FIZIKA NAVODILA ZA OCENJEVANJE Petek, 1. junij 16 SPLOŠNA MATURA RIC 16 M161-411-3 M161-411-3 3 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor
Državni izpitni center *M16141113* SPOMLADANSKI IZPITNI ROK FIZIKA NAVODILA ZA OCENJEVANJE Petek, 1. junij 16 SPLOŠNA MATURA RIC 16 M161-411-3 M161-411-3 3 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor
Integralni račun. Nedoločeni integral in integracijske metrode. 1. Izračunaj naslednje nedoločene integrale: (a) dx. (b) x 3 +3+x 2 dx, (c) (d)
 Integralni račun Nedoločeni integral in integracijske metrode. Izračunaj naslednje nedoločene integrale: d 3 +3+ 2 d, (f) (g) (h) (i) (j) (k) (l) + 3 4d, 3 +e +3d, 2 +4+4 d, 3 2 2 + 4 d, d, 6 2 +4 d, 2
Integralni račun Nedoločeni integral in integracijske metrode. Izračunaj naslednje nedoločene integrale: d 3 +3+ 2 d, (f) (g) (h) (i) (j) (k) (l) + 3 4d, 3 +e +3d, 2 +4+4 d, 3 2 2 + 4 d, d, 6 2 +4 d, 2
SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK
 SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
Booleova algebra. Izjave in Booleove spremenljivke
 Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
8. Diskretni LTI sistemi
 8. Diskreti LI sistemi. Naloga Določite odziv diskretega LI sistema s podaim odzivom a eoti impulz, a podai vhodi sigal. h[] x[] - - 5 6 7 - - 5 6 7 LI sistem se a vsak eoti impulz δ[] a vhodu odzove z
8. Diskreti LI sistemi. Naloga Določite odziv diskretega LI sistema s podaim odzivom a eoti impulz, a podai vhodi sigal. h[] x[] - - 5 6 7 - - 5 6 7 LI sistem se a vsak eoti impulz δ[] a vhodu odzove z
1. Έντυπα αιτήσεων αποζημίωσης... 2 1.1. Αξίωση αποζημίωσης... 2 1.1.1. Έντυπο... 2 1.1.2. Πίνακας μεταφράσεων των όρων του εντύπου...
 ΑΠΟΖΗΜΙΩΣΗ ΘΥΜΑΤΩΝ ΕΓΚΛΗΜΑΤΙΚΩΝ ΠΡΑΞΕΩΝ ΣΛΟΒΕΝΙΑ 1. Έντυπα αιτήσεων αποζημίωσης... 2 1.1. Αξίωση αποζημίωσης... 2 1.1.1. Έντυπο... 2 1.1.2. Πίνακας μεταφράσεων των όρων του εντύπου... 3 1 1. Έντυπα αιτήσεων
ΑΠΟΖΗΜΙΩΣΗ ΘΥΜΑΤΩΝ ΕΓΚΛΗΜΑΤΙΚΩΝ ΠΡΑΞΕΩΝ ΣΛΟΒΕΝΙΑ 1. Έντυπα αιτήσεων αποζημίωσης... 2 1.1. Αξίωση αποζημίωσης... 2 1.1.1. Έντυπο... 2 1.1.2. Πίνακας μεταφράσεων των όρων του εντύπου... 3 1 1. Έντυπα αιτήσεων
Delovna točka in napajalna vezja bipolarnih tranzistorjev
 KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
Logatherm WPL 14 AR T A ++ A + A B C D E F G A B C D E F G. kw kw /2013
 WP 14 R T d 9 10 11 53 d 2015 811/2013 WP 14 R T 2015 811/2013 WP 14 R T Naslednji podatki o izdelku izpolnjujejo zahteve uredb U 811/2013, 812/2013, 813/2013 in 814/2013 o dopolnitvi smernice 2010/30/U.
WP 14 R T d 9 10 11 53 d 2015 811/2013 WP 14 R T 2015 811/2013 WP 14 R T Naslednji podatki o izdelku izpolnjujejo zahteve uredb U 811/2013, 812/2013, 813/2013 in 814/2013 o dopolnitvi smernice 2010/30/U.
II. gimnazija Maribor PROJEKTNA NALOGA. Mentor oblike: Mirko Pešec, prof. Predmet: kemija - informatika
 II. gimnazija Maribor PROJEKTNA NALOGA Mentor vsebine: Irena Ilc, prof. Avtor: Andreja Urlaub Mentor oblike: Mirko Pešec, prof. Predmet: kemija - informatika Selnica ob Dravi, januar 2005 KAZALO VSEBINE
II. gimnazija Maribor PROJEKTNA NALOGA Mentor vsebine: Irena Ilc, prof. Avtor: Andreja Urlaub Mentor oblike: Mirko Pešec, prof. Predmet: kemija - informatika Selnica ob Dravi, januar 2005 KAZALO VSEBINE
Frekvenčna analiza neperiodičnih signalov. Analiza signalov prof. France Mihelič
 Frekvenčna analiza neperiodičnih signalov Analiza signalov prof. France Mihelič Vpliv postopka daljšanja periode na spekter periodičnega signala Opazujmo družino sodih periodičnih pravokotnih impulzov
Frekvenčna analiza neperiodičnih signalov Analiza signalov prof. France Mihelič Vpliv postopka daljšanja periode na spekter periodičnega signala Opazujmo družino sodih periodičnih pravokotnih impulzov
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * NAVODILA ZA OCENJEVANJE. Petek, 12. junij 2015 SPLOŠNA MATURA
 Državni izpitni center *M543* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Petek,. junij 05 SPLOŠNA MATURA RIC 05 M543 M543 3 IZPITNA POLA Naloga Odgovor Naloga Odgovor Naloga Odgovor Naloga Odgovor
Državni izpitni center *M543* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Petek,. junij 05 SPLOŠNA MATURA RIC 05 M543 M543 3 IZPITNA POLA Naloga Odgovor Naloga Odgovor Naloga Odgovor Naloga Odgovor
matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):
![matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij): matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):](/thumbs/87/96579490.jpg) 4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
1. Definicijsko območje, zaloga vrednosti. 2. Naraščanje in padanje, ekstremi. 3. Ukrivljenost. 4. Trend na robu definicijskega območja
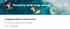
 ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
Splošno o interpolaciji
 Splošno o interpolaciji J.Kozak Numerične metode II (FM) 2011-2012 1 / 18 O funkciji f poznamo ali hočemo uporabiti le posamezne podatke, na primer vrednosti r i = f (x i ) v danih točkah x i Izberemo
Splošno o interpolaciji J.Kozak Numerične metode II (FM) 2011-2012 1 / 18 O funkciji f poznamo ali hočemo uporabiti le posamezne podatke, na primer vrednosti r i = f (x i ) v danih točkah x i Izberemo
Če je električni tok konstanten (se ne spreminja s časom), poenostavimo enačbo (1) in dobimo enačbo (2):
 ELEKTRIČNI TOK TEOR IJA 1. Definicija enote električnega toka Električni tok je gibanje električno nabitih delcev v trdnih snoveh (kovine, polprevodniki), tekočinah ali plinih. V kovinah se gibljejo prosti
ELEKTRIČNI TOK TEOR IJA 1. Definicija enote električnega toka Električni tok je gibanje električno nabitih delcev v trdnih snoveh (kovine, polprevodniki), tekočinah ali plinih. V kovinah se gibljejo prosti
vaja Kvan*ta*vno določanje proteinov. 6. vaja Kvan*ta*vno določanje proteinov. 6. vaja Kvan*ta*vno določanje proteinov
 28. 3. 11 UV- spektrofotometrija Biuretska metoda Absorbanca pri λ=28 nm (A28) UV- spektrofotometrija Biuretska metoda vstopni žarek intenziteta I Lowrijeva metoda Bradfordova metoda Bradfordova metoda
28. 3. 11 UV- spektrofotometrija Biuretska metoda Absorbanca pri λ=28 nm (A28) UV- spektrofotometrija Biuretska metoda vstopni žarek intenziteta I Lowrijeva metoda Bradfordova metoda Bradfordova metoda
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 12. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 12. november 2013 Graf funkcije f : D R, D R, je množica Γ(f) = {(x,f(x)) : x D} R R, torej podmnožica ravnine R 2. Grafi funkcij,
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 12. november 2013 Graf funkcije f : D R, D R, je množica Γ(f) = {(x,f(x)) : x D} R R, torej podmnožica ravnine R 2. Grafi funkcij,
13. poglavje: Energija
 13. poglavje: Energija 1. (Naloga 3) Koliko kilovatna je peč za hišno centralno kurjavo, ki daje 126 MJ toplote na uro? Podatki: Q = 126 MJ, t = 3600 s; P =? Če peč z močjo P enakomerno oddaja toploto,
13. poglavje: Energija 1. (Naloga 3) Koliko kilovatna je peč za hišno centralno kurjavo, ki daje 126 MJ toplote na uro? Podatki: Q = 126 MJ, t = 3600 s; P =? Če peč z močjo P enakomerno oddaja toploto,
Effect of Fibre Fineness on Colour and Reflectance Value of Dyed Filament Polyester Fabrics after Abrasion Process Izvirni znanstveni članek
 Učinek finosti filamentov na barvne vrednosti in odbojnost svetlobe 8 Učinek finosti filamentov na barvne vrednosti in odbojnost svetlobe barvanih poliestrskih filamentnih tkanin po drgnjenju July November
Učinek finosti filamentov na barvne vrednosti in odbojnost svetlobe 8 Učinek finosti filamentov na barvne vrednosti in odbojnost svetlobe barvanih poliestrskih filamentnih tkanin po drgnjenju July November
Srednja šola za gostinstvo in turizem v Ljubljani NARAVOSLOVJE I
 Srednja šola za gostinstvo in turizem v Ljubljani NARAVOSLOVJE I Interno nelektorirano gradivo Izobraževanje odraslih Gastronomske in hotelske storitve (1. letnik) Pripravil: Jernej Grdun, prof Ljubljana,
Srednja šola za gostinstvo in turizem v Ljubljani NARAVOSLOVJE I Interno nelektorirano gradivo Izobraževanje odraslih Gastronomske in hotelske storitve (1. letnik) Pripravil: Jernej Grdun, prof Ljubljana,
[ ]... je oznaka za koncentracijo
![[ ]... je oznaka za koncentracijo [ ]... je oznaka za koncentracijo](/thumbs/62/48148191.jpg) 9. Vaja: Elektrolitska disociacija a) Osnove: Elektroliti so snovi, ki prevajajo električni tok; to so raztopine kislin, baz in soli. Elektrolitska disociacija je razpad elektrolita na ione. Stopnja elektrolitske
9. Vaja: Elektrolitska disociacija a) Osnove: Elektroliti so snovi, ki prevajajo električni tok; to so raztopine kislin, baz in soli. Elektrolitska disociacija je razpad elektrolita na ione. Stopnja elektrolitske
VPLIV REAKCIJSKIH SPREMENLJIVK NA POTEK IN HITROST MODELNE REAKCIJE NATRIJEVEGA TIOSULFATA S KLOROVODIKOVO KISLINO
 OSNOVNA ŠOLA PRIMOŽA TRUBARJA LAŠKO VPLIV REAKCIJSKIH SPREMENLJIVK NA POTEK IN HITROST MODELNE REAKCIJE NATRIJEVEGA TIOSULFATA S KLOROVODIKOVO KISLINO (RAZISKOVALNO DELO) Avtorici: Lea Lešek Povšič in
OSNOVNA ŠOLA PRIMOŽA TRUBARJA LAŠKO VPLIV REAKCIJSKIH SPREMENLJIVK NA POTEK IN HITROST MODELNE REAKCIJE NATRIJEVEGA TIOSULFATA S KLOROVODIKOVO KISLINO (RAZISKOVALNO DELO) Avtorici: Lea Lešek Povšič in
Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih
 Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih različne Postopki ločevanja zmesi:iz zmesi je mogoče ločiti
Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih različne Postopki ločevanja zmesi:iz zmesi je mogoče ločiti
VPLIV RAZLIČNIH PARAMETROV PRANJA NA ODSTRANJEVANJE STANDARDNE UMAZANIJE Z BOMBAŽNE TKANINE
 Univerza v Ljubljani Naravoslovnotehniška fakulteta Oddelek za tekstilstvo VPLIV RAZLIČNIH PARAMETROV PRANJA NA ODSTRANJEVANJE STANDARDNE UMAZANIJE Z BOMBAŽNE TKANINE Avtorica: M. P. Študijska smer: Načrtovanje
Univerza v Ljubljani Naravoslovnotehniška fakulteta Oddelek za tekstilstvo VPLIV RAZLIČNIH PARAMETROV PRANJA NA ODSTRANJEVANJE STANDARDNE UMAZANIJE Z BOMBAŽNE TKANINE Avtorica: M. P. Študijska smer: Načrtovanje
Fazni diagram binarne tekočine
 Fazni diagram binarne tekočine Žiga Kos 5. junij 203 Binarno tekočino predstavljajo delci A in B. Ti se med seboj lahko mešajo v različnih razmerjih. V nalogi želimo izračunati fazni diagram take tekočine,
Fazni diagram binarne tekočine Žiga Kos 5. junij 203 Binarno tekočino predstavljajo delci A in B. Ti se med seboj lahko mešajo v različnih razmerjih. V nalogi želimo izračunati fazni diagram take tekočine,
MLADI ZA CELJE RAZISKOVALNA NALOGA
 MLADI ZA CELJE RAZISKOVALNA NALOGA MAGNUSOV UČINEK AVTORJA: Gašper Bračun, 8. r Luka Marič, 8. r MENTOR: Jože Berk, prof. Osnovna šola Hudinja Področje: FIZIKA Celje, 2016 1 KAZALO KAZALO. 2 KAZALO SLIK...
MLADI ZA CELJE RAZISKOVALNA NALOGA MAGNUSOV UČINEK AVTORJA: Gašper Bračun, 8. r Luka Marič, 8. r MENTOR: Jože Berk, prof. Osnovna šola Hudinja Področje: FIZIKA Celje, 2016 1 KAZALO KAZALO. 2 KAZALO SLIK...
Univerza v Novi Gorici Fakulteta za znanosti o okolju Okolje (I. stopnja) Meteorologija 2013/2014. Energijska bilanca pregled
 Univerza v Novi Gorici Fakulteta za znanosti o okolu Okole (I. stopna) Meteorologia 013/014 Energiska bilanca pregled 1 Osnovni pomi energiski tok: P [W = J/s] gostota energiskega toka: [W/m ] toplota:q
Univerza v Novi Gorici Fakulteta za znanosti o okolu Okole (I. stopna) Meteorologia 013/014 Energiska bilanca pregled 1 Osnovni pomi energiski tok: P [W = J/s] gostota energiskega toka: [W/m ] toplota:q
*M * Osnovna in višja raven MATEMATIKA NAVODILA ZA OCENJEVANJE. Sobota, 4. junij 2011 SPOMLADANSKI IZPITNI ROK. Državni izpitni center
 Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
Ponovi in utrdi svoje znanje Rešitve
 1. poglavje: Kakšne so lastnosti vode? 10. Ni dosežena, saj podgana zaužije 188,8 mg/kg. 11. LD 50 = 0,480 mg/kg 2. poglavje: Kaj je največje čudo na Zemlji? 5. Edini stabilni izotop natrija ima masno
1. poglavje: Kakšne so lastnosti vode? 10. Ni dosežena, saj podgana zaužije 188,8 mg/kg. 11. LD 50 = 0,480 mg/kg 2. poglavje: Kaj je največje čudo na Zemlji? 5. Edini stabilni izotop natrija ima masno
Transformator. Delovanje transformatorja I. Delovanje transformatorja II
 Transformator Transformator je naprava, ki v osnovi pretvarja napetost iz enega nivoja v drugega. Poznamo vrsto različnih izvedb transformatorjev, glede na njihovo specifičnost uporabe:. Energetski transformator.
Transformator Transformator je naprava, ki v osnovi pretvarja napetost iz enega nivoja v drugega. Poznamo vrsto različnih izvedb transformatorjev, glede na njihovo specifičnost uporabe:. Energetski transformator.
= 3. Fizika 8. primer: s= 23,56 m, zaokroženo na eno decimalno vejico s=23,6 m. Povprečna vrednost meritve izračuna povprečno vrednost meritve
 Fizika 8 Merjenje Pojasniti namen in pomen meritev pri fiziki našteje nekaj fizikalnih količin in navede enote zanje, ter priprave s katerimi jih merimo Merska Merska enota Merska priprava količina Dolžina
Fizika 8 Merjenje Pojasniti namen in pomen meritev pri fiziki našteje nekaj fizikalnih količin in navede enote zanje, ter priprave s katerimi jih merimo Merska Merska enota Merska priprava količina Dolžina
13. Jacobijeva metoda za računanje singularnega razcepa
 13. Jacobijeva metoda za računanje singularnega razcepa Bor Plestenjak NLA 25. maj 2010 Bor Plestenjak (NLA) 13. Jacobijeva metoda za računanje singularnega razcepa 25. maj 2010 1 / 12 Enostranska Jacobijeva
13. Jacobijeva metoda za računanje singularnega razcepa Bor Plestenjak NLA 25. maj 2010 Bor Plestenjak (NLA) 13. Jacobijeva metoda za računanje singularnega razcepa 25. maj 2010 1 / 12 Enostranska Jacobijeva
- Geodetske točke in geodetske mreže
 - Geodetske točke in geodetske mreže 15 Geodetske točke in geodetske mreže Materializacija koordinatnih sistemov 2 Geodetske točke Geodetska točka je točka, označena na fizični površini Zemlje z izbrano
- Geodetske točke in geodetske mreže 15 Geodetske točke in geodetske mreže Materializacija koordinatnih sistemov 2 Geodetske točke Geodetska točka je točka, označena na fizični površini Zemlje z izbrano
Katedra za farmacevtsko kemijo. Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks. 25/11/2010 Vaje iz Farmacevtske kemije 3 1
 Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
SEKUNDARNE VEZE međumolekulske veze
 PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
POROČILO. št.: P 1100/ Preskus jeklenih profilov za spuščen strop po točki 5.2 standarda SIST EN 13964:2004
 Oddelek za konstrkcije Laboratorij za konstrkcije Ljbljana, 12.11.2012 POROČILO št.: P 1100/12 680 01 Presks jeklenih profilov za spščen strop po točki 5.2 standarda SIST EN 13964:2004 Naročnik: STEEL
Oddelek za konstrkcije Laboratorij za konstrkcije Ljbljana, 12.11.2012 POROČILO št.: P 1100/12 680 01 Presks jeklenih profilov za spščen strop po točki 5.2 standarda SIST EN 13964:2004 Naročnik: STEEL
VEKTORJI. Operacije z vektorji
 VEKTORJI Vektorji so matematični objekti, s katerimi opisujemo določene fizikalne količine. V tisku jih označujemo s krepko natisnjenimi črkami (npr. a), pri pisanju pa s puščico ( a). Fizikalne količine,
VEKTORJI Vektorji so matematični objekti, s katerimi opisujemo določene fizikalne količine. V tisku jih označujemo s krepko natisnjenimi črkami (npr. a), pri pisanju pa s puščico ( a). Fizikalne količine,
+105 C (plošče in trakovi +85 C) -50 C ( C)* * Za temperature pod C se posvetujte z našo tehnično službo. ϑ m *20 *40 +70
 KAIFLEX ST Tehnični podatki Material Izjemno fleksibilna zaprtocelična izolacija, fleksibilna elastomerna pena (FEF) Opis Uporaba Temperaturno območje Toplotna prevodnost W/(m K ) pri različnih srednjih
KAIFLEX ST Tehnični podatki Material Izjemno fleksibilna zaprtocelična izolacija, fleksibilna elastomerna pena (FEF) Opis Uporaba Temperaturno območje Toplotna prevodnost W/(m K ) pri različnih srednjih
KEMIJA PRVEGA LETNIKA
 KEMIJA naravoslovna znanost oz. veda, ki proučuje zakonitosti v naravi družboslovje proučuje zakonitosti v medčloveških odnosih matematika je veda, ki služi kot pripomoček k drugim naravoslovnim in družboslovnim
KEMIJA naravoslovna znanost oz. veda, ki proučuje zakonitosti v naravi družboslovje proučuje zakonitosti v medčloveških odnosih matematika je veda, ki služi kot pripomoček k drugim naravoslovnim in družboslovnim
Sestava topil Topila s šibkimi vodikovimi vezmi:
 TOPILA Večina premazov vsebuje hlapne komponente, ki izhlapijo tekom aplikacije (nanosa) in nastanka filma. Hlapne komponente premaza s skupnim imenom imenujemo topila, kljub temu, da se smola v določenih
TOPILA Večina premazov vsebuje hlapne komponente, ki izhlapijo tekom aplikacije (nanosa) in nastanka filma. Hlapne komponente premaza s skupnim imenom imenujemo topila, kljub temu, da se smola v določenih
2.1. MOLEKULARNA ABSORPCIJSKA SPEKTROMETRIJA
 2.1. MOLEKULARNA ABSORPCJSKA SPEKTROMETRJA Molekularna absorpcijska spektrometrija (kolorimetrija, fotometrija, spektrofotometrija) temelji na merjenju absorpcije svetlobe, ki prehaja skozi preiskovano
2.1. MOLEKULARNA ABSORPCJSKA SPEKTROMETRJA Molekularna absorpcijska spektrometrija (kolorimetrija, fotometrija, spektrofotometrija) temelji na merjenju absorpcije svetlobe, ki prehaja skozi preiskovano
POROČILO 3.VAJA DOLOČANJE REZULTANTE SIL
 POROČILO 3.VAJA DOLOČANJE REZULTANTE SIL Izdba aje: Ljubjana, 11. 1. 007, 10.00 Jan OMAHNE, 1.M Namen: 1.Preeri paraeogramsko praio za doočanje rezutante nezporedni si s skupnim prijemaiščem (grafično)..dooči
POROČILO 3.VAJA DOLOČANJE REZULTANTE SIL Izdba aje: Ljubjana, 11. 1. 007, 10.00 Jan OMAHNE, 1.M Namen: 1.Preeri paraeogramsko praio za doočanje rezutante nezporedni si s skupnim prijemaiščem (grafično)..dooči
0,00275 cm3 = = 0,35 cm = 3,5 mm.
 1. Za koliko se bo dvignil alkohol v cevki termometra s premerom 1 mm, če se segreje za 5 stopinj? Prostorninski temperaturni razteznostni koeficient alkohola je 11 10 4 K 1. Volumen alkohola v termometru
1. Za koliko se bo dvignil alkohol v cevki termometra s premerom 1 mm, če se segreje za 5 stopinj? Prostorninski temperaturni razteznostni koeficient alkohola je 11 10 4 K 1. Volumen alkohola v termometru
u ê ê ê ê ê : ê ê ê } ê ê ê ê ê ê ê ê
 kemija 1_2.qxd 26.6.2009 7:56 Page 123 y u ê ê ê ê ê : ê ê ê } ê ê ê ê ê ê ê ê ê } ê ê ê ê ê ê ê ê w ê êr ê ê r ê ê ê 7. 1 Vodne raztopine so v nas in okoli nas Z raztopinami se sre~ujemo vsak dan. Pri
kemija 1_2.qxd 26.6.2009 7:56 Page 123 y u ê ê ê ê ê : ê ê ê } ê ê ê ê ê ê ê ê ê } ê ê ê ê ê ê ê ê w ê êr ê ê r ê ê ê 7. 1 Vodne raztopine so v nas in okoli nas Z raztopinami se sre~ujemo vsak dan. Pri
fosfat fosfat H deoksiriboza H O KEMIJA Z BIOKEMIJO učbenik za študente visokošolskega strokovnega študija kmetijstva
 Cl Cl Na + Cl Na + Na + Cl Na + O H H Cl Cl O H H Na + O H H fosfat H deoksiriboza N C N fosfat H H N C C C N N C H H O H C C C N N C N deoksiriboza CH 3 C O C N O C C N fosfat H deoksiriboza H H N C H
Cl Cl Na + Cl Na + Na + Cl Na + O H H Cl Cl O H H Na + O H H fosfat H deoksiriboza N C N fosfat H H N C C C N N C H H O H C C C N N C N deoksiriboza CH 3 C O C N O C C N fosfat H deoksiriboza H H N C H
1 Fibonaccijeva stevila
 1 Fibonaccijeva stevila Fibonaccijevo število F n, kjer je n N, lahko definiramo kot število načinov zapisa števila n kot vsoto sumandov, enakih 1 ali Na primer, število 4 lahko zapišemo v obliki naslednjih
1 Fibonaccijeva stevila Fibonaccijevo število F n, kjer je n N, lahko definiramo kot število načinov zapisa števila n kot vsoto sumandov, enakih 1 ali Na primer, število 4 lahko zapišemo v obliki naslednjih
Poglavje 7. Poglavje 7. Poglavje 7. Regulacijski sistemi. Regulacijski sistemi. Slika 7. 1: Normirana blokovna shema regulacije EM
 Slika 7. 1: Normirana blokovna shema regulacije EM Fakulteta za elektrotehniko 1 Slika 7. 2: Principielna shema regulacije AM v KSP Fakulteta za elektrotehniko 2 Slika 7. 3: Merjenje komponent fluksa s
Slika 7. 1: Normirana blokovna shema regulacije EM Fakulteta za elektrotehniko 1 Slika 7. 2: Principielna shema regulacije AM v KSP Fakulteta za elektrotehniko 2 Slika 7. 3: Merjenje komponent fluksa s
Osnovne stehiometrijske veličine
 Osnovne stehiometrijske veličine Stehiometrija (grško: stoiheion snov, metron merilo) obravnava količinske odnose pri kemijskih reakcijah. Fizikalne veličine, s katerimi kemik najpogosteje izraža količino
Osnovne stehiometrijske veličine Stehiometrija (grško: stoiheion snov, metron merilo) obravnava količinske odnose pri kemijskih reakcijah. Fizikalne veličine, s katerimi kemik najpogosteje izraža količino
Stehiometrija za študente veterine
 Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
REŠITVE LABORATORIJSKE VAJE ZA KEMIJO V GIMNAZIJI. Marjeta Prašnikar
 REŠITVE LABORATORIJSKE VAJE ZA KEMIJO V GIMNAZIJI Andrej Nika Cebin Godec Manica Ivan Perdan Leban - Ocepek Marjeta Prašnikar 2 Rešitve VARNO EKSPERIMENTALNO DELO Kemija je eksperimentalna veda (str. 8)
REŠITVE LABORATORIJSKE VAJE ZA KEMIJO V GIMNAZIJI Andrej Nika Cebin Godec Manica Ivan Perdan Leban - Ocepek Marjeta Prašnikar 2 Rešitve VARNO EKSPERIMENTALNO DELO Kemija je eksperimentalna veda (str. 8)
6 Trdno in tekoče. 6.1 Tlak in gostota 6.2 Tekočine 6.3 Plavanje 6.4 Ozračje in vreme
 6 Trdno in tekoče 6.1 Tlak in gostota 6.2 Tekočine 6.3 Plavanje 6.4 Ozračje in vreme Aprila 1912 se je Titanik podal na svojo prvo plovbo. Z dolžino treh nogometnih igrišč in višino Ljubljanskega nebotičnika
6 Trdno in tekoče 6.1 Tlak in gostota 6.2 Tekočine 6.3 Plavanje 6.4 Ozračje in vreme Aprila 1912 se je Titanik podal na svojo prvo plovbo. Z dolžino treh nogometnih igrišč in višino Ljubljanskega nebotičnika
Univerza v Ljubljani Fakulteta za strojništvo. Vrstični elektronski mikroskop - Scanning electron microscope. Poročilo laboratorijske vaje
 Univerza v Ljubljani Fakulteta za strojništvo Vrstični elektronski mikroskop - Scanning electron microscope Poročilo laboratorijske vaje Rok oddaje: Ponedeljek, 16. 5. 2016 Uroš R 15. junij 2016 KAZALO
Univerza v Ljubljani Fakulteta za strojništvo Vrstični elektronski mikroskop - Scanning electron microscope Poročilo laboratorijske vaje Rok oddaje: Ponedeljek, 16. 5. 2016 Uroš R 15. junij 2016 KAZALO
ZGRADBA ATOMA IN PERIODNI SISTEM
 ZGRADBA ATOMA IN PERIODNI SISTEM Kemijske lastnosti elementov se periodično spreminjajo z naraščajočo relativno atomsko maso oziroma kot vemo danes z naraščajočim vrstnim številom. Dmitrij I. Mendeljejev,
ZGRADBA ATOMA IN PERIODNI SISTEM Kemijske lastnosti elementov se periodično spreminjajo z naraščajočo relativno atomsko maso oziroma kot vemo danes z naraščajočim vrstnim številom. Dmitrij I. Mendeljejev,
CM707. GR Οδηγός χρήσης... 2-7. SLO Uporabniški priročnik... 8-13. CR Korisnički priručnik... 14-19. TR Kullanım Kılavuzu... 20-25
 1 2 3 4 5 6 7 OFFMANAUTO CM707 GR Οδηγός χρήσης... 2-7 SLO Uporabniški priročnik... 8-13 CR Korisnički priručnik... 14-19 TR Kullanım Kılavuzu... 20-25 ENG User Guide... 26-31 GR CM707 ΟΔΗΓΟΣ ΧΡΗΣΗΣ Περιγραφή
1 2 3 4 5 6 7 OFFMANAUTO CM707 GR Οδηγός χρήσης... 2-7 SLO Uporabniški priročnik... 8-13 CR Korisnički priručnik... 14-19 TR Kullanım Kılavuzu... 20-25 ENG User Guide... 26-31 GR CM707 ΟΔΗΓΟΣ ΧΡΗΣΗΣ Περιγραφή
diferencialne enačbe - nadaljevanje
 12. vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 diferencialne enačbe - nadaljevanje Ortogonalne trajektorije Dana je 1-parametrična družina krivulj F(x, y, C) = 0. Ortogonalne
12. vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 diferencialne enačbe - nadaljevanje Ortogonalne trajektorije Dana je 1-parametrična družina krivulj F(x, y, C) = 0. Ortogonalne
PROCESIRANJE SIGNALOV
 Rešive pisega izpia PROCESIRANJE SIGNALOV Daum: 7... aloga Kolikša je ampliuda reje harmoske kompoee arisaega periodičega sigala? f() - -3 - - 3 Rešiev: Časova fukcija a iervalu ( /,/) je lieara fukcija:
Rešive pisega izpia PROCESIRANJE SIGNALOV Daum: 7... aloga Kolikša je ampliuda reje harmoske kompoee arisaega periodičega sigala? f() - -3 - - 3 Rešiev: Časova fukcija a iervalu ( /,/) je lieara fukcija:
IZZIVI DRUŽINSKE MEDICINE. U no gradivo zbornik seminarjev
 IZZIVI DRUŽINSKE MEDICINE Uno gradivo zbornik seminarjev študentov Medicinske fakultete Univerze v Mariboru 4. letnik 2008/2009 Uredniki: Alenka Bizjak, Viktorija Janar, Maša Krajnc, Jasmina Rehar, Mateja
IZZIVI DRUŽINSKE MEDICINE Uno gradivo zbornik seminarjev študentov Medicinske fakultete Univerze v Mariboru 4. letnik 2008/2009 Uredniki: Alenka Bizjak, Viktorija Janar, Maša Krajnc, Jasmina Rehar, Mateja
SATCITANANDA. F = e E sila na naboj. = ΔW e. Rudolf Kladnik: Fizika za srednješolce 3. Svet elektronov in atomov
 Ruolf Klnik: Fizik z srenješolce Set elektrono in too Električno olje (11), gibnje elce električne olju Strn 55, nlog 1 Kolikšno netost or releteti elektron, se njego kinetičn energij oeč z 1 kev? Δ W
Ruolf Klnik: Fizik z srenješolce Set elektrono in too Električno olje (11), gibnje elce električne olju Strn 55, nlog 1 Kolikšno netost or releteti elektron, se njego kinetičn energij oeč z 1 kev? Δ W
1A skupina alkalijske kovine
 1. NALOGA: KATERA IZMED SPOJIN JE NAJBOLJ TOPNA V VODI? NaCl, KBr, RbBr ALI NaF? ZAKAJ? 1. NALOGA: ODGOVOR Topnost je odvisna od mrežne entalpije ΔH mr (energija, potrebna za razgradnjo kristala na anione
1. NALOGA: KATERA IZMED SPOJIN JE NAJBOLJ TOPNA V VODI? NaCl, KBr, RbBr ALI NaF? ZAKAJ? 1. NALOGA: ODGOVOR Topnost je odvisna od mrežne entalpije ΔH mr (energija, potrebna za razgradnjo kristala na anione
1. TVORBA ŠIBKEGA (SIGMATNEGA) AORISTA: Največ grških glagolov ima tako imenovani šibki (sigmatni) aorist. Osnova se tvori s. γραψ
 TVORBA AORISTA: Grški aorist (dovršnik) izraža dovršno dejanje; v indikativu izraža poleg dovršnosti tudi preteklost. Za razliko od prezenta ima aorist posebne aktivne, medialne in pasivne oblike. Pri
TVORBA AORISTA: Grški aorist (dovršnik) izraža dovršno dejanje; v indikativu izraža poleg dovršnosti tudi preteklost. Za razliko od prezenta ima aorist posebne aktivne, medialne in pasivne oblike. Pri
Matematika 1. Gregor Dolinar. 2. januar Fakulteta za elektrotehniko Univerza v Ljubljani. Gregor Dolinar Matematika 1
 Mtemtik 1 Gregor Dolinr Fkultet z elektrotehniko Univerz v Ljubljni 2. jnur 2014 Gregor Dolinr Mtemtik 1 Izrek (Izrek o povprečni vrednosti) Nj bo m ntnčn spodnj mej in M ntnčn zgornj mej integrbilne funkcije
Mtemtik 1 Gregor Dolinr Fkultet z elektrotehniko Univerz v Ljubljni 2. jnur 2014 Gregor Dolinr Mtemtik 1 Izrek (Izrek o povprečni vrednosti) Nj bo m ntnčn spodnj mej in M ntnčn zgornj mej integrbilne funkcije
Kvantni delec na potencialnem skoku
 Kvantni delec na potencialnem skoku Delec, ki se giblje premo enakomerno, pride na mejo, kjer potencial naraste s potenciala 0 na potencial. Takšno potencialno funkcijo zapišemo kot 0, 0 0,0. Slika 1:
Kvantni delec na potencialnem skoku Delec, ki se giblje premo enakomerno, pride na mejo, kjer potencial naraste s potenciala 0 na potencial. Takšno potencialno funkcijo zapišemo kot 0, 0 0,0. Slika 1:
ODGOVORI NA VPRAŠANJA V UČBENIKU. Margareta Vrtačnik Katarina S. Wissiak Grm Saša A. Glažar Andrej Godec
 ODGOVORI NA VPRAŠANJA V UČBENIKU Margareta Vrtačnik Katarina S. Wissiak Grm Saša A. Glažar Andrej Godec 1. KAJ JE KEMIJA KEMIJA JE EKSPERIMENTALNA VEDA (str. 14) 1. Kemija je nauk o snovi in njenih spremembah.
ODGOVORI NA VPRAŠANJA V UČBENIKU Margareta Vrtačnik Katarina S. Wissiak Grm Saša A. Glažar Andrej Godec 1. KAJ JE KEMIJA KEMIJA JE EKSPERIMENTALNA VEDA (str. 14) 1. Kemija je nauk o snovi in njenih spremembah.
Avto na vodik in gorivne celice
 OSNOVNA ŠOLA ŽELEZNIKI Avto na vodik in gorivne celice Raziskovalna naloga Področje: naravoslovno - tehniško Avtorji: Matija Rihtaršič, Vid Šolar, Gašper Potočnik, Jakob Bernik, Luka Galjot, 9. razred
OSNOVNA ŠOLA ŽELEZNIKI Avto na vodik in gorivne celice Raziskovalna naloga Področje: naravoslovno - tehniško Avtorji: Matija Rihtaršič, Vid Šolar, Gašper Potočnik, Jakob Bernik, Luka Galjot, 9. razred
Ovrednotenje vzorca naravne vode
 Ovrednotenje vzorca naravne vode Esej Katja Kunčič, 1. letnik Laboratorijske biomedicine Analizna kemija Mentorica: Prof. dr. Nataša Gros Ljubljana, 14.5.2013 1 Uvod Pri vaji analiza vod bi želela analizirati
Ovrednotenje vzorca naravne vode Esej Katja Kunčič, 1. letnik Laboratorijske biomedicine Analizna kemija Mentorica: Prof. dr. Nataša Gros Ljubljana, 14.5.2013 1 Uvod Pri vaji analiza vod bi želela analizirati
Zemlja in njeno ozračje
 Zemlja in njeno ozračje Pojavi v ozračju se dogajajo na zelo različnih časovnih in prostorskih skalah Prostorska skala Pojav 1 cm Turbulenca, sunki vetra 1 m 1 km 10 km 100 km 1000 in več km Tornadi Poplave,
Zemlja in njeno ozračje Pojavi v ozračju se dogajajo na zelo različnih časovnih in prostorskih skalah Prostorska skala Pojav 1 cm Turbulenca, sunki vetra 1 m 1 km 10 km 100 km 1000 in več km Tornadi Poplave,
Univerza v Ljubljani Fakulteta za matematiko in fiziko Oddelek za fiziko
 Univerza v Ljubljani Fakulteta za matematiko in fiziko Oddelek za fiziko Seminar HIDRODINAMIKA OBALNIH VALOV Mateja Erjavec Mentor: prof. dr. Rudolf Podgornik Februar 2010 Povzetek V začetnem delu seminarja
Univerza v Ljubljani Fakulteta za matematiko in fiziko Oddelek za fiziko Seminar HIDRODINAMIKA OBALNIH VALOV Mateja Erjavec Mentor: prof. dr. Rudolf Podgornik Februar 2010 Povzetek V začetnem delu seminarja
DISKRETNA FOURIERJEVA TRANSFORMACIJA
 29.03.2004 Definicija DFT Outline DFT je linearna transformacija nekega vektorskega prostora dimenzije n nad obsegom K, ki ga označujemo z V K, pri čemer ima slednji lastnost, da vsebuje nek poseben element,
29.03.2004 Definicija DFT Outline DFT je linearna transformacija nekega vektorskega prostora dimenzije n nad obsegom K, ki ga označujemo z V K, pri čemer ima slednji lastnost, da vsebuje nek poseben element,
Kotni funkciji sinus in kosinus
 Kotni funkciji sinus in kosinus Oznake: sinus kota x označujemo z oznako sin x, kosinus kota x označujemo z oznako cos x, DEFINICIJA V PRAVOKOTNEM TRIKOTNIKU: Kotna funkcija sinus je definirana kot razmerje
Kotni funkciji sinus in kosinus Oznake: sinus kota x označujemo z oznako sin x, kosinus kota x označujemo z oznako cos x, DEFINICIJA V PRAVOKOTNEM TRIKOTNIKU: Kotna funkcija sinus je definirana kot razmerje
SEMINARSKA NALOGA Funkciji sin(x) in cos(x)
 FAKULTETA ZA MATEMATIKO IN FIZIKO Praktična Matematika-VSŠ(BO) Komuniciranje v matematiki SEMINARSKA NALOGA Funkciji sin(x) in cos(x) Avtorica: Špela Marinčič Ljubljana, maj 2011 KAZALO: 1.Uvod...1 2.
FAKULTETA ZA MATEMATIKO IN FIZIKO Praktična Matematika-VSŠ(BO) Komuniciranje v matematiki SEMINARSKA NALOGA Funkciji sin(x) in cos(x) Avtorica: Špela Marinčič Ljubljana, maj 2011 KAZALO: 1.Uvod...1 2.
KOLI»INSKI ODNOSI. Kemik mora vedeti, koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane.
 KOLI»INSKI ODNOSI Kemik mora vedeti koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane 4 Mase atomov in molekul 42 tevilo delcev masa in mnoæina snovi 43 RaËunajmo maso mnoæino in πtevilo
KOLI»INSKI ODNOSI Kemik mora vedeti koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane 4 Mase atomov in molekul 42 tevilo delcev masa in mnoæina snovi 43 RaËunajmo maso mnoæino in πtevilo
Podobnost matrik. Matematika II (FKKT Kemijsko inženirstvo) Diagonalizacija matrik
 Podobnost matrik Matematika II (FKKT Kemijsko inženirstvo) Matjaž Željko FKKT Kemijsko inženirstvo 14 teden (Zadnja sprememba: 23 maj 213) Matrika A R n n je podobna matriki B R n n, če obstaja obrnljiva
Podobnost matrik Matematika II (FKKT Kemijsko inženirstvo) Matjaž Željko FKKT Kemijsko inženirstvo 14 teden (Zadnja sprememba: 23 maj 213) Matrika A R n n je podobna matriki B R n n, če obstaja obrnljiva
UPOR NA PADANJE SONDE V ZRAKU
 UPOR NA PADANJE SONDE V ZRAKU 1. Hitrost in opravljena pot sonde pri padanju v zraku Za padanje v zraku je odgovorna sila teže. Poleg sile teže na padajoče telo deluje tudi sila vzgona, ki je enaka teži
UPOR NA PADANJE SONDE V ZRAKU 1. Hitrost in opravljena pot sonde pri padanju v zraku Za padanje v zraku je odgovorna sila teže. Poleg sile teže na padajoče telo deluje tudi sila vzgona, ki je enaka teži
Gimnazija Krˇsko. vektorji - naloge
 Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
I.13. Koliki je napon između neke tačke A čiji je potencijal 5 V i referentne tačke u odnosu na koju se taj potencijal računa?
 TET I.1. Šta je Kulonova sila? elektrostatička sila magnetna sila c) gravitaciona sila I.. Šta je elektrostatička sila? sila kojom međusobno eluju naelektrisanja u mirovanju sila kojom eluju naelektrisanja
TET I.1. Šta je Kulonova sila? elektrostatička sila magnetna sila c) gravitaciona sila I.. Šta je elektrostatička sila? sila kojom međusobno eluju naelektrisanja u mirovanju sila kojom eluju naelektrisanja
