ιαστερεοεκλεκτικότητα σε κυκλικά δικυκλικά µόρια. Πενταµελείς και εξαµελείς συµπυκνωµένοι δακτύλιοι.
|
|
|
- Βαρβάρα Κομνηνός
- 8 χρόνια πριν
- Προβολές:
Transcript
1 diabicy1 1 ιαστερεοεκλεκτικότητα σε κυκλικά δικυκλικά µόρια. Πενταµελείς και εξαµελείς συµπυκνωµένοι δακτύλιοι. Cis-συµπυκνωµένοι πενταµελείς δακτύλιοι. Ένα δικυκλικό σύστηµα µε δυο συµπυκνωµένους πενταµελείς δακτυλίους, όπως το [3,3,0] δικυκλοοκτάνιο, (σχήµα 1) είναι σχεδόν πάντα σταθερότερο όταν η ένωση των δακτυλίων είναι cis. Η συνολική µορφή τέτοιων cis µορίων εµφανίζει µια κυρτή, εξωτερική πλευρά προς την οποία βρίσκονται οι δυο cis υποκαταστάτες της ένωσης των δακτυλίων και µια κοίλη ή εσωτερική πλευρά. Σχήµα 1. Οι όποιοι υποκαταστάτες των δυο δακτυλίων είναι λιγότερο συνωστισµένοι όταν βρίσκονται στην εξωτερική πλευρά. Με τον ίδιο τρόπο η προσέγγιση ενός αντιδραστηρίου γίνεται γενικά ευκολότερα από την έξω πλευρά δηλαδή προς την πλευρά των δυο υποκαταστατών της ένωσης των δακτυλίων (τα δυο άτοµα Η για το µητρικό σκελετό cis δικυκλοεξανίου). κυρτþ εξωτερικþ πλευρü εýκολη προσýγγιση Ξ κοßλο εσωτερικü παρεìπüδιση Σχήµα 1. Τα διαµορφωτικά εναντιοµερή και οι δυο πλευρές του µορίου του cis [3,3,0]- δικυκλοοκτανίου. Η εξωτερική πλευρά του διπλού δεσµού στο ακόρεστο δικυκλικό µόριο του σχήµατος 2 προσεγγίζει (και προσροφάται) ευκολότερα στην επιφάνεια ενός καταλύτη υδρογόνωσης και είναι αυτή η πλευρά του δ. δεσµού που υποδέχεται τα δυο άτοµα υδρογόνου (στερεοειδική cis προσθήκη υδρογόνου µε προτίµηση προς την έξω πλευρά του δ.δ). 2 (M) C 3 Σχήµα 2. ιαστερεοεκλεκτική υδρογόνωση ενός ακόρεστου δικυκλικού µορίου. Η διαφορά αυτή στην προσέγγιση των δυο πλευρών του δικυκλικού είναι εντελώς ανάλογη µε αυτή που παρατηρείται σε απλούς πενταµελείς δακτυλίους µε δυο cis υποκαταστάτες όπου η προσέγγιση του οποιουδήποτε αντιδραστηρίου γίνεται σχεδόν αποκλειστικά trans. (Σχήµα 3)
2 diabicy1 2 [] Ξ Σχήµα 3. ιαστερεοεκλεκτική εποξειδίωση cis-δισυποκατεστηµένου κυκλοπεντενίου. Η πτύχωση του µορίου που αναφέρθηκε για το καρβοκυκλικό σύστηµα των συµπυκνωµένων πενταµελών δακτυλίων, διατηρείται ακόµα και όταν ένα από τα δυο άτοµα που είναι κοινά στους δακτυλίους είναι άτοµο αζώτου. Όπως είναι γνωστό ένα τέτοιο άζωτο (τύπου αµίνης) είναι τετραεδρικό µεν αλλά συγχρόνως είναι και στερεοχηµικά ευµετάβλητο, λόγω της πυραµιδικής αναστροφής που αντιστρέφει τη στερεοχηµεία του. Μια τέτοια αναστροφή ισοδυναµεί µε cis-trans ισοµερίωση και συνεπώς το µόριο βρίσκεται σε δυναµική ισορροπία µεταξύ δυο διαστερεοµερών διαµορφώσεων. Η cis διαµόρφωση είναι και εδώ πολύ λιγότερο τεταµένη και συνεπώς επικρατεί σε µεγάλο βαθµό (Σχήµα 4). Σχήµα 4. Πυραµιδική αναστροφή του ατόµου αζώτου στην υποκατεστηµένη κινολιζιδίνη (αζαδικυκλοοκτάνιο) που αντιστοιχεί σε cis- trans ισοµερίωση. Ώστε η σχετική στερεοχηµεία του αζώτου είναι καθορισµένη ως cis ως προς το στσθερό στερεογονικό κέντρο του γειτονικού άνθρακα. Η ύπαρξη πτύχωσης γίνεται φανερή από τη µεγάλη διαφορά στη σταθερότητα επιµερών δοµών σε ενδοκυκλικές θέσεις: π.χ. για τον εστέρα του σχήµατος 5 η βάση δίνει τη δυνατότητα θερµοδυναµικής εξισορρόπησης µέσω επιµερίωσης του στερεογονικού κέντρου που φέρει την αιθοξυκαρβονυλοµάδα. Η ακόρεστη αµίνη του σχήµατος 5 φαίνεται να υδρογονώνεται καταλυτικά µε trans γεωµετρία προσθήκης του υδρογόνου προς syn προϊόν. Λόγω της αυξηµένης θερµοκρασίας η αντίδραση µπορεί να θεωρηθεί αντιστρεπτή ώστε συνολικά ως προϊόν να προκύπτει το θερµοδυναµικά σταθερότερο cis ισοµερές.
3 diabicy1 3 anti C 2 Et Et syn C 2 Et βüση cis anti δοìþ ενδιüìεσο ενολικü ιüν cis syn δοìþ C 2 Et 2 / Pd θýρìανση C 2 Et C 2 Et επιìερßωση C 2 Et Σχήµα 5. Εξισορρόπηση επιµερών προς την κατεύθυνση του σταθερότερου, µε τον υποκαταστάτη σε syn γεωµετρία (προς την έξω πλευρά των δακτυλίων). Εάν λοιπόν δεν υπάρχει δυνατότητα θερµοδυναµικής επιµερίωσης τότε το syn στερεοχηµικό αποτέλεσµα τέτοιων αντιδράσεων µπορεί να εξηγηθεί ως κινητικά ελεγχόµενη προσβολή από την εξωτερική (λιγότερο παρεµποδισµένη) πλευρά. Προφανώς µια τέτοια προσβολή οδηγεί αναγκαστικά σε εσωτερική θέση τον προϋπάρχοντα υποκαταστάτη, όπως φαίνεται στα παραδείγµατα των αντιδράσεων του σχήµατος 6. u α) u β) cis κετüνη 2. 1 Br Br 1 2 cis λακτüνη προϊüν syn προσβολþò προϊüν syn προσβολþò
4 diabicy1 4 γ) 2. J cis υδρινδανüνη-2 προϊüν syn προσβολþò Σχήµα 6. ιαστερεοεκλεκτική syn προσβολή σε µόρια µε cis συµπυκνωµένους πενταµελείς δακτυλίους. Όπως φαίνεται από το παράδειγµα γ) του σχήµατος 6 ανάλογα ισχύουν και για το σύστηµα δακτυλίων του cis-υδρινδανίου όπου ο πενταµελής δακτύλιος είναι cis- συµπυκνωµένος µε εξαµελή. cis- συµπυκνωµένοι εξαµελείς δακτύλιοι, cis-δεκαλίνη. Η cis δεκαλίνη είναι τυπικό παράδειγµα cis- συµπυκνωµένων εξαµελών δακτυλίων. Ο σκελετός του µορίου της cis δεκαλίνης παρουσιάζει και αυτό µια κύρτωση ώστε οι δυο πλευρές του να εµφανίζουν διαφορετική ευκολία στην προσέγγιση άλλων µορίων. Το φαινόµενο είναι λιγότερο έντονο απ ότι για τους πενταµελείς δακτυλίους αφού όπως έχει ηδη αναφερθεί ο σκελετός της δεκαλίνης µπορεί εύκολα να µετασχηµατισθεί µε ταυτόχρονη αναστροφή και των δυο ανακλίντρων του προς µια εναντιοµερή διαµόρφωση διατηρώντας όµως την κύρτωση του προς την ίδια πλευρά. Η καταλυτική υδρογόνωση της ακόρεστης κετόνης του σχήµατος 7 οδηγεί σε εισαγωγή των δυο ατόµων Η από την ίδια πλευρά µε τους προϋπάρχοντες υποκαταστάτες ( και ) και συνεπώς το µόριο προσροφάται στην καταλυτική επιφάνεια µε αυτή την πλευρά. Παρ όλο ότι αυτή η πλευρά περιέχει ήδη υποκαταστάτες, είναι η κυρτή / εξωτερική πλευρά του µορίου και είναι η πλέον εκτεθειµένη. αναστροφþ 2 / Pd [] Σχήµα 7. Εκλεκτική syn προσβολή σε δακτυλίους τύπου cis-δεκαλίνης.
5 diabicy1 5 Παρόµοια κύρτωση εµφανίζουν και τα cis συµπυκνωµένα µόρια µε τετραµελείς δακτυλίους και (προφανώς) και µε τριµελείς, απαντώνται όµως σπανιότερα και είναι γενικά ασταθέστερα λόγω της αυξηµένης τάσης γωνιών που χαρακτηρίζει τους πολύ µικρούς δακτυλίους. Ας σηµειωθεί ακόµη ότι οι trans- δεκαλίνες είναι γενικά σταθερότερες από τις αντίστοιχες cis και δεν εµφανίζουν την ίδια συµπεριφορά µε αυτές. Κατά την προσέγγιση αντιδραστηρίων σε µόρια µε σκελετό trans δεκαλίνης η κύρια παρεµπόδιση είναι αυτή από cis-υποκαταστάτες, όπως π.χ. κατά την ακόλουθη αντίδραση αλκυλίωσης της εικονιζόµενης κετόνης µε σκελετό trans δεκαλίνης. 2. EtJ Et Το στερεοχηµικό αποτέλεσµα (εκλεκτικότητα) της παραπάνω αντίδρασης ερµηνεύεται ως 1,3 διαξονική παρεµπόδιση κατά την είσοδο της αιθυλοµάδας cis προς το µεθύλιο της γέφυρας µε αποτέλεσµα η είσοδος να γίνεται trans (από την αντίθετη πλευρά του µορίου).
aldo B 1 Σχήµα 15. Παρουσία κετόνης (πηγή πρωτονίων) προκαλείται σταδιακή µετατροπή του κινητικού µίγµατος ενολικών σε θερµοδυναµικό.
 aldo B 1 ογκώδεις υποκαταστάτες του αζώτου αλλά δηµιουργώντας έτσι αλλυλική τάση Α 1, 2 µε το µεθύλιο της θέσης 1 (τοποθέτηση cis των µεθυλοµάδων στο trans ενολικό). Η ΜΚ του cis-ενολικού µε αξονική µεθυλοµάδα
aldo B 1 ογκώδεις υποκαταστάτες του αζώτου αλλά δηµιουργώντας έτσι αλλυλική τάση Α 1, 2 µε το µεθύλιο της θέσης 1 (τοποθέτηση cis των µεθυλοµάδων στο trans ενολικό). Η ΜΚ του cis-ενολικού µε αξονική µεθυλοµάδα
ΣΤΕΡΕΟΗΛΕΚΤΡΟΝΙΚΑ ΕΛΕΓΧΟΜΕΝΕΙΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΕ ΚΥΚΛΟΕΞΑΝΙΑ ΜΕ ΟΜΗ ΗΜΙΑΝΑΚΛΙΝΤΡΟΥ α. διάνοιξη του οξιρανικού δακτυλίου σε κυκλοεξενοξείδια.
 bstelc ΣΤΕΡΕΟΗΛΕΚΤΡΟΝΙΚΑ ΕΛΕΓΧΟΜΕΝΕΙΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΕ ΚΥΚΛΟΕΞΑΝΙΑ ΜΕ ΟΜΗ ΗΜΙΑΝΑΚΛΙΝΤΡΟΥ α. διάνοιξη του οξιρανικού δακτυλίου σε κυκλοεξενοξείδια. Όπως έχει αναφερθεί κατά τη συζήτηση των διαµορφώσεων των
bstelc ΣΤΕΡΕΟΗΛΕΚΤΡΟΝΙΚΑ ΕΛΕΓΧΟΜΕΝΕΙΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΕ ΚΥΚΛΟΕΞΑΝΙΑ ΜΕ ΟΜΗ ΗΜΙΑΝΑΚΛΙΝΤΡΟΥ α. διάνοιξη του οξιρανικού δακτυλίου σε κυκλοεξενοξείδια. Όπως έχει αναφερθεί κατά τη συζήτηση των διαµορφώσεων των
N Ph + J. Σχήµα 1. Ισορροπία εναντιοµερίωσης ενός ασταθούς χειρικού αµµωνιακού άλατος.
 asrac1 1 Ασύµµετροι µετασχηµατισµοί ρακεµικών µιγµάτων Η απόδοση µιας ανάλυσης ρακεµικού µίγµατος περιορίζεται κατά µέγιστο στο 50% της ποσότητας του ρακεµικού, δηλαδή στο 100% της ποσότητας του ενός εκ
asrac1 1 Ασύµµετροι µετασχηµατισµοί ρακεµικών µιγµάτων Η απόδοση µιας ανάλυσης ρακεµικού µίγµατος περιορίζεται κατά µέγιστο στο 50% της ποσότητας του ρακεµικού, δηλαδή στο 100% της ποσότητας του ενός εκ
7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή
 7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή Στερεοχημεία της προσθήκης στα αλκένια C C + E Y E C C Y Για να μάθετε να κατανοείτε τη στερεοχημεία του προϊόντος, χρειάζεται να γνωρίζετε δυο πράγματα:
7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή Στερεοχημεία της προσθήκης στα αλκένια C C + E Y E C C Y Για να μάθετε να κατανοείτε τη στερεοχημεία του προϊόντος, χρειάζεται να γνωρίζετε δυο πράγματα:
Me O N H C 2. S D 2 χειρική δοµή. R εναντιοµερές
 ΠΡΟΒΛΗΜΑ 1.1 Απάντηση/ ανάλυση Για την επεξεργασία του συγκεκριµένου προβλήµατος είναι κατάλληλες οι απεικονίσεις κατά Newmman κάθετα στο διφαινυλικό δεσµό. Εάν επιπλέον δεχθούµε ότι το αµιδικό σύστηµα
ΠΡΟΒΛΗΜΑ 1.1 Απάντηση/ ανάλυση Για την επεξεργασία του συγκεκριµένου προβλήµατος είναι κατάλληλες οι απεικονίσεις κατά Newmman κάθετα στο διφαινυλικό δεσµό. Εάν επιπλέον δεχθούµε ότι το αµιδικό σύστηµα
Tα λογικά βήματα της λύσης μπορεί να είναι αναλυτικά τα ακόλουθα:
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση-Στερεοχημεία και Μηχανισμοί. Μάθημα 629,Επιλεγόμενο Διδάσκων: Κ. Χ. Φρούσιος Εξεταστική Περίοδος Ιουνίου 2013 Διάρκεια εξέτασης
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση-Στερεοχημεία και Μηχανισμοί. Μάθημα 629,Επιλεγόμενο Διδάσκων: Κ. Χ. Φρούσιος Εξεταστική Περίοδος Ιουνίου 2013 Διάρκεια εξέτασης
ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΗΣ ΣΧΕΤΙΚΗΣ ΣΤΕΡΕΟΧΗΜΕΙΑΣ ΥΠΟΚΑΤΕΣΤΗΜΕΝΩΝ ΚΥΚΛΙΚΩΝ ΕΝΩΣΕΩΝ (cis trans ισοµέρεια)
 relst1 1 ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΗΣ ΣΧΕΤΙΚΗΣ ΣΤΕΡΕΟΧΗΜΕΙΑΣ ΥΠΟΚΑΤΕΣΤΗΜΕΝΩΝ ΚΥΚΛΙΚΩΝ ΕΝΩΣΕΩΝ (cis trans ισοµέρεια) Οι θέσεις των διάφορων υποκαταστατών ενός κυκλικού µορίου µε αναφορά στο επίπεδο του δακτυλίου,
relst1 1 ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΗΣ ΣΧΕΤΙΚΗΣ ΣΤΕΡΕΟΧΗΜΕΙΑΣ ΥΠΟΚΑΤΕΣΤΗΜΕΝΩΝ ΚΥΚΛΙΚΩΝ ΕΝΩΣΕΩΝ (cis trans ισοµέρεια) Οι θέσεις των διάφορων υποκαταστατών ενός κυκλικού µορίου µε αναφορά στο επίπεδο του δακτυλίου,
O H ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση. Στερεοχημεία-Μηχανισμοί (Μάθημα 629, Επιλεγόμενο) Διδάσκων :Κ.Χ.Φρούσιος Τμηματικές Εξετάσεις 08 ΣΕΠ 2010 Διάρκεια εξέτασης
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση. Στερεοχημεία-Μηχανισμοί (Μάθημα 629, Επιλεγόμενο) Διδάσκων :Κ.Χ.Φρούσιος Τμηματικές Εξετάσεις 08 ΣΕΠ 2010 Διάρκεια εξέτασης
7.9 Αντιδράσεις που δηµιουργούν ένα στερεογονικό κέντρο
 7.9 Αντιδράσεις που δηµιουργούν ένα στερεογονικό κέντρο Πολλές αντιδράσεις µετατρέπουν µη χειρόµορφα αντιδρώντα σε χειρόµορφα προϊόντα. Εν τούτοις, είναι σηµαντικό να αναγνωρίσουµε, οτι εάν όλα τα συστατικά
7.9 Αντιδράσεις που δηµιουργούν ένα στερεογονικό κέντρο Πολλές αντιδράσεις µετατρέπουν µη χειρόµορφα αντιδρώντα σε χειρόµορφα προϊόντα. Εν τούτοις, είναι σηµαντικό να αναγνωρίσουµε, οτι εάν όλα τα συστατικά
EtOH. OEt. µοναδικό ισοµερές, cis ή trans ;
 ΠΡΟΒΛΗΜΑ 2.1 2 / i + 3 C Et 3 C ακόρεστη ακετάλη A Et Et ισοµερίωση B µοναδικό ισοµερές, cis ή trans ; Το φάσµα 1 MR της υδρογονωµένης ακετάλης δείχνει σήµατα σε δ 3,95 ( 1 Η, πολύπλοκη, J 0.5, 3.9, 9.5
ΠΡΟΒΛΗΜΑ 2.1 2 / i + 3 C Et 3 C ακόρεστη ακετάλη A Et Et ισοµερίωση B µοναδικό ισοµερές, cis ή trans ; Το φάσµα 1 MR της υδρογονωµένης ακετάλης δείχνει σήµατα σε δ 3,95 ( 1 Η, πολύπλοκη, J 0.5, 3.9, 9.5
Περίληψη Κεφαλαίων 6 & 7
 Περίληψη Κεφαλαίων 6 & 7 Αλκένια: υδρογονάνθρακες µε 1 ή περισσότερους διπλούς δεσµούς Παρεµπόδιση περιστροφής γύρω από δ.δ. cis-trans ισοµέρεια (Ε ή Ζ) Αλκένια δίνουν αντιδράσεις ηλεκτρονιόφιλης προσθήκης
Περίληψη Κεφαλαίων 6 & 7 Αλκένια: υδρογονάνθρακες µε 1 ή περισσότερους διπλούς δεσµούς Παρεµπόδιση περιστροφής γύρω από δ.δ. cis-trans ισοµέρεια (Ε ή Ζ) Αλκένια δίνουν αντιδράσεις ηλεκτρονιόφιλης προσθήκης
Στερεοηλεκτρονικά ελεγχόμενοι μετασχηματισμοί.
 Σελίδα 1 /24 1. ΑΣΚΗΣΗ Η 5-κετοεννεανο-1,9-διόλη, με θέρμανση παρουσία καταλυτικής ποσότητας οξέος, κυκλοποιείται με αφυδάτωση προς την σπειροκετάλη,όπως φαίνεται στο σχήμα που ακολουθεί. Προτείνετε ένα
Σελίδα 1 /24 1. ΑΣΚΗΣΗ Η 5-κετοεννεανο-1,9-διόλη, με θέρμανση παρουσία καταλυτικής ποσότητας οξέος, κυκλοποιείται με αφυδάτωση προς την σπειροκετάλη,όπως φαίνεται στο σχήμα που ακολουθεί. Προτείνετε ένα
Σχεδιάστε τύπους ανακλίντρων για τις ενώσεις Α και Β και εξηγήστε σχετικά. Yπόδειξη : Η αντίδραση Μichael θεωρείται γενικά αντιστρεπτή αντίδραση.
 1 1 H 3 C H 3 C αναγωγή H 3 C H 3 C H H ± A B Η διφαινυλική κετόνη Α εµφανίζει ατροποϊσοµέρεια και σε συνήθη θερµοκρασία µπορεί να αναλυθεί σε δυο σταθερές έναντιοµερικές µορφές. 1. Χαρακτηρίστε τις πλευρές
1 1 H 3 C H 3 C αναγωγή H 3 C H 3 C H H ± A B Η διφαινυλική κετόνη Α εµφανίζει ατροποϊσοµέρεια και σε συνήθη θερµοκρασία µπορεί να αναλυθεί σε δυο σταθερές έναντιοµερικές µορφές. 1. Χαρακτηρίστε τις πλευρές
διπλός δεσμός τριπλός δεσμός
 Ακόρεστοι Υδρογονάνθρακες Αλκένια Αλκίνια Αρωματικές ενώσεις Αλκένια διπλός δεσμός Αλκίνια τριπλός δεσμός Αρωματικοί υδρογονάνθρακες Βενζόλιο Αλκένια-ΑλκίνιαΑλκίνια Μη πολικές ενώσεις Αδιάλυτες στο νερό
Ακόρεστοι Υδρογονάνθρακες Αλκένια Αλκίνια Αρωματικές ενώσεις Αλκένια διπλός δεσμός Αλκίνια τριπλός δεσμός Αρωματικοί υδρογονάνθρακες Βενζόλιο Αλκένια-ΑλκίνιαΑλκίνια Μη πολικές ενώσεις Αδιάλυτες στο νερό
Οργανική Χημεία. Κεφάλαιο 15: Βενζόλιο και αρωματικότητα
 Οργανική Χημεία Κεφάλαιο 15: Βενζόλιο και αρωματικότητα 1. Αρωματικές ενώσεις Αρωματικές ενώσεις: ενώσεις με ευχάριστη οσμή Αρωματικές ενώσεις αναφέρονται συνήθως στο βενζόλιο και σε ενώσεις με συγγενική
Οργανική Χημεία Κεφάλαιο 15: Βενζόλιο και αρωματικότητα 1. Αρωματικές ενώσεις Αρωματικές ενώσεις: ενώσεις με ευχάριστη οσμή Αρωματικές ενώσεις αναφέρονται συνήθως στο βενζόλιο και σε ενώσεις με συγγενική
- H 2 O O - Σχήµα 1. Σχηµατισµός β-υδροξυκαρβονυλικής και α-ακόρεστης καρβονυλικής ένωσης και ο ρόλος της κατάλυσης (όξινης ή βασικής).
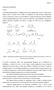 Aldo A 1 ΑΛ ΟΛΙΚΗ ΑΝΤΙ ΡΑΣΗ Γενικά. Ως αλδολική χαρακτηρίζεται η αντίδραση µεταξύ µιας καρβονυλικής ένωσης η οποία υπό τη µορφή ενόλης ή ενολικού ιόντος επιδρά ως πυρηνόφιλο επί µιας δεύτερης καρβονυλικής
Aldo A 1 ΑΛ ΟΛΙΚΗ ΑΝΤΙ ΡΑΣΗ Γενικά. Ως αλδολική χαρακτηρίζεται η αντίδραση µεταξύ µιας καρβονυλικής ένωσης η οποία υπό τη µορφή ενόλης ή ενολικού ιόντος επιδρά ως πυρηνόφιλο επί µιας δεύτερης καρβονυλικής
ΚΙΝΗΤΙΚΑ ΕΛΕΓΧΟΜΕΝΕΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΧΗΜΑΤΙΣΜΟΥ ΣΤΕΡΕΟΪΣΟΜΕΡΩΝ.
 kinss1 1 ΚΙΝΗΤΙΚ ΕΛΕΓΧΜΕΝΕΣ ΝΤΙ ΡΣΕΙΣ ΣΧΗΜΤΙΣΜΥ ΣΤΕΡΕΪΣΜΕΡΩΝ. ταυτόχρονος σχηµατισµός στερεοϊσοµερών κατά τη λειτουργία µιας χηµικής µετατροπής δηµιουργεί µίγµατα προϊόντων µέσω παραλλήλων ανταγωνιστικών
kinss1 1 ΚΙΝΗΤΙΚ ΕΛΕΓΧΜΕΝΕΣ ΝΤΙ ΡΣΕΙΣ ΣΧΗΜΤΙΣΜΥ ΣΤΕΡΕΪΣΜΕΡΩΝ. ταυτόχρονος σχηµατισµός στερεοϊσοµερών κατά τη λειτουργία µιας χηµικής µετατροπής δηµιουργεί µίγµατα προϊόντων µέσω παραλλήλων ανταγωνιστικών
ΣΤΕΡΕΟΧΗΜΕΙΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΑΝΤΙ ΡΑΣΕΩΝ ΤΟΥ ΚΥΚΛΟΥ KREBS.
 krb1 1 ΣΤΕΡΕΟΧΗΜΕΙΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΑΝΤΙ ΡΑΣΕΩΝ ΤΟΥ ΚΥΚΛΟΥ KREBS. Η προσθήκη νερού στο φουµαρικό οξύ. si si re φουìαρüση anti-προσθþκη 2 re φουìαρικü οξý S-ìηλικü οξý anti- προσθήκη νερού στο δ.δ. του φουµαρικού
krb1 1 ΣΤΕΡΕΟΧΗΜΕΙΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΑΝΤΙ ΡΑΣΕΩΝ ΤΟΥ ΚΥΚΛΟΥ KREBS. Η προσθήκη νερού στο φουµαρικό οξύ. si si re φουìαρüση anti-προσθþκη 2 re φουìαρικü οξý S-ìηλικü οξý anti- προσθήκη νερού στο δ.δ. του φουµαρικού
Δομή. Ως συζυγιακά διένια ορίζουμε τους υδρογονάνθρακες που στην. κύριο χαρακτηριστικό την εναλλαγή των δεσμών (απλών και διπλών) στο μόριο.
 ΣΥΖΥΓΙΑΚA ΔΙΕΝΙA Δομή Ως συζυγιακά διένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχουν δυο διπλούς δεσμούς με κύριο χαρακτηριστικό την εναλλαγή των δεσμών (απλών και διπλών)
ΣΥΖΥΓΙΑΚA ΔΙΕΝΙA Δομή Ως συζυγιακά διένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχουν δυο διπλούς δεσμούς με κύριο χαρακτηριστικό την εναλλαγή των δεσμών (απλών και διπλών)
H 2 N CH 2 CH 3 O S. Σχήµα 1. Τα τέσσερα στερεοϊσοµερή µιας ένωσης µε 2 χειρικά κέντρα.
 corlst1 1 Στερεοχηµικοί συσχετισµοί. Απόλυτη και σχετική στερεοχηµεία. Σύγκριση δυο χειρικών κέντρων στο ίδιο µόριο. Έστω για παράδειγµα η διαπίστωση της στερεοχηµείας ενός απλού µορίου µε δυο χειρικά
corlst1 1 Στερεοχηµικοί συσχετισµοί. Απόλυτη και σχετική στερεοχηµεία. Σύγκριση δυο χειρικών κέντρων στο ίδιο µόριο. Έστω για παράδειγµα η διαπίστωση της στερεοχηµείας ενός απλού µορίου µε δυο χειρικά
Εναντιοεκλεκτικότητα κατά την αντίδραση χειρικών ενολικών µε αχειρικά ηλεκτρονιόφιλα. Ενολικά ιόντα εστέρων και αµιδίων.
 enalkb 1 Εναντιοεκλεκτικότητα κατά την αντίδραση χειρικών ενολικών µε αχειρικά ηλεκτρονιόφιλα. Ενολικά ιόντα εστέρων και αµιδίων. Ένα ενολικό µε ένα τυπικό χειρικό κέντρο στο µόριο του εµφανίζει ασφαλώς
enalkb 1 Εναντιοεκλεκτικότητα κατά την αντίδραση χειρικών ενολικών µε αχειρικά ηλεκτρονιόφιλα. Ενολικά ιόντα εστέρων και αµιδίων. Ένα ενολικό µε ένα τυπικό χειρικό κέντρο στο µόριο του εµφανίζει ασφαλώς
Υποδειγματικά Λυμένα Προβλήματα Κεφαλαίου 4
 ΔΟΜΗ, ΔΡΑΣΤΙΚΟΤΗΤΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ STRUTURE, REATIVITY AND MEANISM IN ORGANI EMISTRY Διονύσης Α. Παπαϊωάννου Καθηγητής Οργανικής Χημείας Dionysios A. Papaioannou Professor of Organic
ΔΟΜΗ, ΔΡΑΣΤΙΚΟΤΗΤΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ STRUTURE, REATIVITY AND MEANISM IN ORGANI EMISTRY Διονύσης Α. Παπαϊωάννου Καθηγητής Οργανικής Χημείας Dionysios A. Papaioannou Professor of Organic
Ηλεκτρονιόφιλα Πυρηνόφιλα αντιδραστήρια. Επίκουρος καθηγητής Χρήστος Παππάς
 Ηλεκτρονιόφιλα Πυρηνόφιλα αντιδραστήρια Επίκουρος καθηγητής Χρήστος Παππάς 1 Ηλεκτρονιόφιλα - πυρηνόφιλα αντιδραστήρια Ηλεκτρονιόφιλα λέγονται τα αντιδραστήρια τα οποία δέχονται ένα ή δύο ηλεκτρόνια σε
Ηλεκτρονιόφιλα Πυρηνόφιλα αντιδραστήρια Επίκουρος καθηγητής Χρήστος Παππάς 1 Ηλεκτρονιόφιλα - πυρηνόφιλα αντιδραστήρια Ηλεκτρονιόφιλα λέγονται τα αντιδραστήρια τα οποία δέχονται ένα ή δύο ηλεκτρόνια σε
Περίληψη Κεφαλαίου 3
 Περίληψη Κεφαλαίου 3 Λειτουργική οµάδα: άτοµο ή σύνολο ατόµων ενός µορίου που προσδίδει χαρακτηριστική χηµική συµπεριφορά στο µόριο Αλκάνια: κατηγορία υδρογονανθράκων µε γενικό µοριακό τύπο C v H 2v+2
Περίληψη Κεφαλαίου 3 Λειτουργική οµάδα: άτοµο ή σύνολο ατόµων ενός µορίου που προσδίδει χαρακτηριστική χηµική συµπεριφορά στο µόριο Αλκάνια: κατηγορία υδρογονανθράκων µε γενικό µοριακό τύπο C v H 2v+2
Μηχανισµός και στερεοχηµεία των ενζυµατικών οξειδοαναγωγών µε συνένζυµα νουκλεοτίδια της πυριδίνης. Εφαρµογή σε οργανικές συνθέσεις.
 nad 1 Μηχανισµός και στερεοχηµεία των ενζυµατικών οξειδοαναγωγών µε συνένζυµα νουκλεοτίδια της πυριδίνης. Εφαρµογή σε οργανικές συνθέσεις. Οι αφυδρογονάσες που καταλύουν την αντιστρεπτή µετατροπή διάφορων
nad 1 Μηχανισµός και στερεοχηµεία των ενζυµατικών οξειδοαναγωγών µε συνένζυµα νουκλεοτίδια της πυριδίνης. Εφαρµογή σε οργανικές συνθέσεις. Οι αφυδρογονάσες που καταλύουν την αντιστρεπτή µετατροπή διάφορων
O Ε + S N 2. Σχήµα 1. Ηλεκτρονιόφιλη α-αλκυλίωση κετόνης παρουσία ισχυρής βάσης.
 enalka 1 α-αλκυλίωση των κετονών Όπως έχει ηδη αναφερθεί τα α-υδρογόνα των καρβονυλικών ενώσεων παρουσιάζουν αυξηµένη οξύτητα και είναι δυνατόν να πραγµατοποιηθεί η αποµάκρυνση ενός τέτοιου πρωτονίου σχετικά
enalka 1 α-αλκυλίωση των κετονών Όπως έχει ηδη αναφερθεί τα α-υδρογόνα των καρβονυλικών ενώσεων παρουσιάζουν αυξηµένη οξύτητα και είναι δυνατόν να πραγµατοποιηθεί η αποµάκρυνση ενός τέτοιου πρωτονίου σχετικά
ιαµορφώσεις και χηµική συµπεριφορά των κυκλικών ενώσεων µε εξαµελή δακτύλιο. Κυκλοεξάνιο.
 confrx1 1 ιαµορφώσεις και χηµική συµπεριφορά των κυκλικών ενώσεων µε εξαµελή δακτύλιο. Κυκλοεξάνιο. Η αρχική ιδέα του Baeyer για το κυκλοεξάνιο ήταν αυτή ενός επίπεδου δακτυλίου µε τάση γωνιών (τάση Baeyer),
confrx1 1 ιαµορφώσεις και χηµική συµπεριφορά των κυκλικών ενώσεων µε εξαµελή δακτύλιο. Κυκλοεξάνιο. Η αρχική ιδέα του Baeyer για το κυκλοεξάνιο ήταν αυτή ενός επίπεδου δακτυλίου µε τάση γωνιών (τάση Baeyer),
ΕΝΟΤΗΤΑ 1: ΙΣΟΜΕΡΕΙΑ
 ΕΝΟΤΗΤΑ 1: ΙΣΟΜΕΡΕΙΑ 1 Ισομέρεια, ή ισομερισμός (ως αποτέλεσμα επιδράσεων), λέγεται το φαινόμενο κατά το οποίο δύο ή περισσότερες χημικές ενώσεις αν και αποτελούνται από τα ίδια χημικά στοιχεία, του αυτού
ΕΝΟΤΗΤΑ 1: ΙΣΟΜΕΡΕΙΑ 1 Ισομέρεια, ή ισομερισμός (ως αποτέλεσμα επιδράσεων), λέγεται το φαινόμενο κατά το οποίο δύο ή περισσότερες χημικές ενώσεις αν και αποτελούνται από τα ίδια χημικά στοιχεία, του αυτού
2
 1 2 3 4 5 6 7 8 9 Η μικρότερη σταθερότητα της βινυλικής ρίζας (για παράδειγμα σε σχέση με τη μεθυλική) θα μπορούσε να εξηγηθεί στη βάση του πόσο ισχυρά έλκονται τα ηλεκτρόνια από το κάθε άτομο άνθρακα.
1 2 3 4 5 6 7 8 9 Η μικρότερη σταθερότητα της βινυλικής ρίζας (για παράδειγμα σε σχέση με τη μεθυλική) θα μπορούσε να εξηγηθεί στη βάση του πόσο ισχυρά έλκονται τα ηλεκτρόνια από το κάθε άτομο άνθρακα.
3.4 Τα σχήματα των Κυκλοεξανίων: Επίπεδα ή όχι
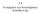 3.4 Τα σχήματα των Κυκλοεξανίων: Επίπεδα ή όχι Adolf von Baeyer (19ος αιώνας) Υπέθεσε οτι τα κυκλοαλκάνια είναι επίπεδα πολύγωνα Η παραμόρφωση των γωνιών δεσμού από τις 109.5 δίνει γωνιακή τάση στα κυκλοαλκάνια
3.4 Τα σχήματα των Κυκλοεξανίων: Επίπεδα ή όχι Adolf von Baeyer (19ος αιώνας) Υπέθεσε οτι τα κυκλοαλκάνια είναι επίπεδα πολύγωνα Η παραμόρφωση των γωνιών δεσμού από τις 109.5 δίνει γωνιακή τάση στα κυκλοαλκάνια
C n (H 2 O) ν 22/11/2016 2
 22/11/2016 1 1 C n (H 2 O) ν 22/11/2016 2 Εκτιμάται πως ετησίως παράγονται 100 δισεκατομμύρια τόνοι υδατανθράκων με τη διαδικασία της φωτοσύνθεσης 22/11/2016 3 δεν μπορούν να υδρολυθούν σε άλλα μικρότερα
22/11/2016 1 1 C n (H 2 O) ν 22/11/2016 2 Εκτιμάται πως ετησίως παράγονται 100 δισεκατομμύρια τόνοι υδατανθράκων με τη διαδικασία της φωτοσύνθεσης 22/11/2016 3 δεν μπορούν να υδρολυθούν σε άλλα μικρότερα
Διαμόρφωση-διαμορφωμερή
 Οργανική Χημεία Πέτρος Ταραντίλης Αναπληρωτής Καθηγητής Εργαστήριο Χημείας, Τμήμα Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax:
Οργανική Χημεία Πέτρος Ταραντίλης Αναπληρωτής Καθηγητής Εργαστήριο Χημείας, Τμήμα Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax:
Ε. Μαλαμίδου-Ξενικάκη
 Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 Ηλεκτρονιόφιλη προσβολή σε παράγωγα του βενζολίου Ασπιρίνη Η ασπιρίνη παρασκευάζεται βιομηχανικά με εκλεκτική ηλεκτρονιόφιλη αρωματική υποκατάσταση της φαινόλης.
Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 Ηλεκτρονιόφιλη προσβολή σε παράγωγα του βενζολίου Ασπιρίνη Η ασπιρίνη παρασκευάζεται βιομηχανικά με εκλεκτική ηλεκτρονιόφιλη αρωματική υποκατάσταση της φαινόλης.
ΑΝΑΓΩΓΗ ΚΑΡΒΟΝΥΛΙΟΥ. O Me 3 SiCl. Μόνο σε κυκλοεξανικά παράγωγα R 2 C R 3. R 1 H p-tosyl = p-ts + H 2 NHN SO 2 CH 3. 2RLi. - Ts.
 ΑΝΑΓΩΓΗ ΚΑΡΒΟΝΥΛΙΟΥ Me 3 Sil Zn Μόνο σε κυκλοεξανικά παράγωγα R 2 R 3 + 2 S 2 3 R 1 p-tosyl = p-ts R 2 R 3 2RLi R 2 R 3 - Ts R 1 Ts R 1 Ts R 2 R 3 R 2 R 3 R 2-2 2 R 3 R 1 Li R 1 Li R 1 Κ. Τσολερίδης Τμ.
ΑΝΑΓΩΓΗ ΚΑΡΒΟΝΥΛΙΟΥ Me 3 Sil Zn Μόνο σε κυκλοεξανικά παράγωγα R 2 R 3 + 2 S 2 3 R 1 p-tosyl = p-ts R 2 R 3 2RLi R 2 R 3 - Ts R 1 Ts R 1 Ts R 2 R 3 R 2 R 3 R 2-2 2 R 3 R 1 Li R 1 Li R 1 Κ. Τσολερίδης Τμ.
Κυκλικοί υδρογονάνθρακες
 Κυκλικοί υδρογονάνθρακες C 2 Y C 2 Y C 2 C 2 C n 2n+2 C n 2n : Κορεσμένοι = Ισομερή των αλκενίων C n 2n C n 2n-2 : Μονοακόρεστοι = ισομερή των αλκινίων 1 1. Καύση Αντιδράσεις Αλκανίων C 3 -C 2 -C 3 + 5
Κυκλικοί υδρογονάνθρακες C 2 Y C 2 Y C 2 C 2 C n 2n+2 C n 2n : Κορεσμένοι = Ισομερή των αλκενίων C n 2n C n 2n-2 : Μονοακόρεστοι = ισομερή των αλκινίων 1 1. Καύση Αντιδράσεις Αλκανίων C 3 -C 2 -C 3 + 5
ΑΝΤΙ ΡΑΣΕΙΣ Β-ΑΠΟΣΠΑΣΗΣ ΣΕ ΑΛΚΥΛΑΛΟΓΟΝΙ ΙΑ ΚΑΙ ΣΟΥΛΦΟΝΙΚΟΥΣ ΕΣΤΕΡΕΣ (ΑΝΤΙ ΡΑΣΕΙΣ Ε).
 elim 1 ΑΝΤΙ ΡΑΣΕΙΣ Β-ΑΠΟΣΠΑΣΗΣ ΣΕ ΑΛΚΥΛΑΛΟΓΟΝΙ ΙΑ ΚΑΙ ΣΟΥΛΦΟΝΙΚΟΥΣ ΕΣΤΕΡΕΣ (ΑΝΤΙ ΡΑΣΕΙΣ Ε). Κατά την εξέταση της συµπεριφοράς τριτοταγών αλογονιδίων σε πολικούς διαλύτες θεωρήθηκε ότι το προϊόν της αντίδρασης
elim 1 ΑΝΤΙ ΡΑΣΕΙΣ Β-ΑΠΟΣΠΑΣΗΣ ΣΕ ΑΛΚΥΛΑΛΟΓΟΝΙ ΙΑ ΚΑΙ ΣΟΥΛΦΟΝΙΚΟΥΣ ΕΣΤΕΡΕΣ (ΑΝΤΙ ΡΑΣΕΙΣ Ε). Κατά την εξέταση της συµπεριφοράς τριτοταγών αλογονιδίων σε πολικούς διαλύτες θεωρήθηκε ότι το προϊόν της αντίδρασης
Εισαγωγή στις βασικές έννοιες που αφορούν τις οργανομεταλλικές ενώσεις, την κατάλυση και τις βασικές αρχές της, καθώς και τη χρησιμότητα των
 124 Εισαγωγή στις βασικές έννοιες που αφορούν τις οργανομεταλλικές ενώσεις, την κατάλυση και τις βασικές αρχές της, καθώς και τη χρησιμότητα των καταλυτών των μετάλλων μεταπτώσεως στην οργανική σύνθεση.
124 Εισαγωγή στις βασικές έννοιες που αφορούν τις οργανομεταλλικές ενώσεις, την κατάλυση και τις βασικές αρχές της, καθώς και τη χρησιμότητα των καταλυτών των μετάλλων μεταπτώσεως στην οργανική σύνθεση.
Αλκένια. Τα άτομα άνθρακα του διπλού δεσμού έχουν sp 2 υβριδίωση, με
 Αλκένια Ως αλκένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχεται τουλάχιστον ένας διπλός δεσμός =. Είναι δυνατόν να υπάρξουν ως άκυκλα ή κυκλικά αλκένια. Τα άτομα άνθρακα του
Αλκένια Ως αλκένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχεται τουλάχιστον ένας διπλός δεσμός =. Είναι δυνατόν να υπάρξουν ως άκυκλα ή κυκλικά αλκένια. Τα άτομα άνθρακα του
Α.Π.Α.Υ. ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ
 Α.Π.Α.Υ. ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ Όλα τα παράγωγα καρβοξυλικών οξέων µπορούν να συντεθούν από καρβοξυλικά οξέα, µέσω αντίδρασης πυρηνόφιλης άκυλο υποκατάστασης (ΑΠΥΑ). ΠΑΡΑΣΚΕΥΗ ΧΛΩΡΙΔΙΩΝ ΟΞΕΩΝ ΜΕ SCl 2 ΑΝΤΙΔΡΑΣΗ:
Α.Π.Α.Υ. ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ Όλα τα παράγωγα καρβοξυλικών οξέων µπορούν να συντεθούν από καρβοξυλικά οξέα, µέσω αντίδρασης πυρηνόφιλης άκυλο υποκατάστασης (ΑΠΥΑ). ΠΑΡΑΣΚΕΥΗ ΧΛΩΡΙΔΙΩΝ ΟΞΕΩΝ ΜΕ SCl 2 ΑΝΤΙΔΡΑΣΗ:
καρβονυλική ένωση pk α ( )
 enol1 1 ΕΝΟΛΙΚΑ ΑΝΙΟΝΤΑ ΚΑΙ ΕΝΑΜΙΝΕΣ. Παρασκευές και αντιδράσεις µε αλκυλιωτικά αντιδραστήρια. Ο γενικότερος τρόπος δηµιουργίας πυρηνόφιλου άνθρακα είναι η αποπρωτονίωση του µε βάση, ώστε να δηµιουργηθεί
enol1 1 ΕΝΟΛΙΚΑ ΑΝΙΟΝΤΑ ΚΑΙ ΕΝΑΜΙΝΕΣ. Παρασκευές και αντιδράσεις µε αλκυλιωτικά αντιδραστήρια. Ο γενικότερος τρόπος δηµιουργίας πυρηνόφιλου άνθρακα είναι η αποπρωτονίωση του µε βάση, ώστε να δηµιουργηθεί
1. Να δείξετε πως τα παρακάτω μόρια μπορούν να παρασκευαστούν με αντίδρασεις Mannich
 1. Να δείξετε πως τα παρακάτω μόρια μπορούν να παρασκευαστούν με αντίδρασεις Mannich (!) (") (C 3 ) 2 (#) ($) 2. αντίδραση της τριτοταγούς αμίνης τροπινόνη με βρωμομεθυλο βενζόλιο (βενζυλο βρωμίδιο) δίνει
1. Να δείξετε πως τα παρακάτω μόρια μπορούν να παρασκευαστούν με αντίδρασεις Mannich (!) (") (C 3 ) 2 (#) ($) 2. αντίδραση της τριτοταγούς αμίνης τροπινόνη με βρωμομεθυλο βενζόλιο (βενζυλο βρωμίδιο) δίνει
Οργανική Χημεία. Κεφάλαιο 4: Στερεοχημεία αλκανίων και κυκλοαλκανίων
 Οργανική Χημεία Κεφάλαιο 4: Στερεοχημεία αλκανίων και κυκλοαλκανίων 1. Διατάξεις μορίων στο χώρο Η μορφή των μορίων στο χώρο εξαρτάται από πολλές δυνάμεις Μόριο μπορεί να λάβει διαφορετικές μορφές στο
Οργανική Χημεία Κεφάλαιο 4: Στερεοχημεία αλκανίων και κυκλοαλκανίων 1. Διατάξεις μορίων στο χώρο Η μορφή των μορίων στο χώρο εξαρτάται από πολλές δυνάμεις Μόριο μπορεί να λάβει διαφορετικές μορφές στο
Περίληψη Κεφαλαίου 5
 Περίληψη Κεφαλαίου 5 Είδη αντιδράσεων: προσθήκης, απόσπασης, υποκατάστασης & αναδιάταξης Μηχανισµός αντίδρασης: πλήρης περιγραφή τρόπου πραγµατοποίησης Μηχανισµοί µέσω ριζών ή πολικοί Πολική αντίδράση
Περίληψη Κεφαλαίου 5 Είδη αντιδράσεων: προσθήκης, απόσπασης, υποκατάστασης & αναδιάταξης Μηχανισµός αντίδρασης: πλήρης περιγραφή τρόπου πραγµατοποίησης Μηχανισµοί µέσω ριζών ή πολικοί Πολική αντίδράση
Οργανική Χημεία. Κεφάλαιο 26: Βιομόρια: υδατάνθρακες
 Οργανική Χημεία Κεφάλαιο 26: Βιομόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισμό Άμυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαμβάκι είναι καθαροί υδατάνθρακες
Οργανική Χημεία Κεφάλαιο 26: Βιομόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισμό Άμυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαμβάκι είναι καθαροί υδατάνθρακες
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 7 η θεματική ενότητα: Οι αντιδράσεις του διπλού δεσμού
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 7 η θεματική ενότητα: Οι αντιδράσεις του διπλού δεσμού Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 7 η θεματική ενότητα: Οι αντιδράσεις του διπλού δεσμού Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
MAΘΗΜΑ 3 ο Υ ΑΤΑΝΘΡΑΚΕΣ
 MAΘΗΜΑ ο Υ ΑΤΑΝΘΡΑΚΕΣ Γλυκόζη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr Απλοί υδατάνθρακες ή Μονοσακχαρίτες Σύνθετοι υδατάνθρακες γλυκόζη σακχαρόζη φρουκτόζη
MAΘΗΜΑ ο Υ ΑΤΑΝΘΡΑΚΕΣ Γλυκόζη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr Απλοί υδατάνθρακες ή Μονοσακχαρίτες Σύνθετοι υδατάνθρακες γλυκόζη σακχαρόζη φρουκτόζη
ΑΝΟΡΓΑΝΗ ΙΙΙ. Prof. Dr. Maria Louloudi. Laboratory of Biomimetic Catalysis & Biomimetic Materials. Chemistry Department. University of Ioannina
 Prof. Dr. Maria Louloudi Laboratory of Biomimetic Catalysis & Biomimetic Materials Chemistry Department University of Ioannina ΑΝΟΡΓΑΝΗ ΙΙΙ Μηχανισµοί Ανόργανων Αντιδράσεων (στοιχειοµετρικές αντιδράσεις)
Prof. Dr. Maria Louloudi Laboratory of Biomimetic Catalysis & Biomimetic Materials Chemistry Department University of Ioannina ΑΝΟΡΓΑΝΗ ΙΙΙ Μηχανισµοί Ανόργανων Αντιδράσεων (στοιχειοµετρικές αντιδράσεις)
ΟΜΟ- ΚΑΙ ΕΤΕΡΟΤΟΠΙΚΟΤΗΤΑ. ΠΡΟΣΤΕΡΕΟΪΣΟΜΕΡΕΙΑ, ΠΡΟΧΕΙΡΙΚΟΤΗΤΑ.
 topct1 1 ΟΜΟ- ΚΑΙ ΕΤΕΡΟΤΟΠΙΚΟΤΗΤΑ. ΠΡΟΣΤΕΡΕΟΪΣΟΜΕΡΕΙΑ, ΠΡΟΧΕΙΡΙΚΟΤΗΤΑ. Σε ένα µόριο όπως π.χ. το προπιονικό οξύ ο τετραεδρικός άνθρακας στη θέση 2 (µεθυλενοµάδα Η Α και Η Β ) φέρει δύο ίδιους υποκαταστάτες
topct1 1 ΟΜΟ- ΚΑΙ ΕΤΕΡΟΤΟΠΙΚΟΤΗΤΑ. ΠΡΟΣΤΕΡΕΟΪΣΟΜΕΡΕΙΑ, ΠΡΟΧΕΙΡΙΚΟΤΗΤΑ. Σε ένα µόριο όπως π.χ. το προπιονικό οξύ ο τετραεδρικός άνθρακας στη θέση 2 (µεθυλενοµάδα Η Α και Η Β ) φέρει δύο ίδιους υποκαταστάτες
υναµική ισορροπία Περιορισµένη περιστροφή Αναστροφή δακτυλίου Αναστροφή διάταξης Ταυτοµέρεια
 υναµική ισορροπία Η φασµατοσκοπία MR µπορεί να µελετήσει φυσικές και χηµικές διεργασίες, οι οποίες µεταβάλλονται µε το χρόνο. Μπορεί, για παράδειγµα, να µελετήσει την αλληλοµετατροπή δύο ή περισσότερων
υναµική ισορροπία Η φασµατοσκοπία MR µπορεί να µελετήσει φυσικές και χηµικές διεργασίες, οι οποίες µεταβάλλονται µε το χρόνο. Μπορεί, για παράδειγµα, να µελετήσει την αλληλοµετατροπή δύο ή περισσότερων
Ε. Μαλαμίδου-Ξενικάκη
 Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 ΑΛΚΥΝΙΑ: C ν H 2ν-2 Ο τριπλός δεσμός άνθρακα άνθρακα Τριπλός δεσμός αλκυνίου ΑΛΚΥΝΙΑ Μόρια πρότυπα για «μοριακούς διακόπτες» Μικροσκοπία σάρωσης σήραγγας (Scanning
Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 ΑΛΚΥΝΙΑ: C ν H 2ν-2 Ο τριπλός δεσμός άνθρακα άνθρακα Τριπλός δεσμός αλκυνίου ΑΛΚΥΝΙΑ Μόρια πρότυπα για «μοριακούς διακόπτες» Μικροσκοπία σάρωσης σήραγγας (Scanning
Οργανική Χηµεία. Κεφάλαιο 26: Βιοµόρια: υδατάνθρακες
 Οργανική Χηµεία Κεφάλαιο 26: Βιοµόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισµό Άµυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαµβάκι είναι καθαροί υδατάνθρακες
Οργανική Χηµεία Κεφάλαιο 26: Βιοµόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισµό Άµυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαµβάκι είναι καθαροί υδατάνθρακες
Κεφάλαιο 7 Στερεοχηµεία
 Κεφάλαιο 7 Στερεοχηµεία 7.1 Μοριακή χειροµορφία: Εναντιοµερή Χειροµορφία Ένα µόριο είναι χειρόµορφο εάν οι δυο µορφές του που έχουν σχέση ειδώλου-αντικειµένου δεν συµπίπτουν η µια πάνω στην άλλη. Ένα µόριο
Κεφάλαιο 7 Στερεοχηµεία 7.1 Μοριακή χειροµορφία: Εναντιοµερή Χειροµορφία Ένα µόριο είναι χειρόµορφο εάν οι δυο µορφές του που έχουν σχέση ειδώλου-αντικειµένου δεν συµπίπτουν η µια πάνω στην άλλη. Ένα µόριο
Η ολεφινική μετάθεση είναι σήμερα η αποτελεσματικότερη μέθοδος δημιουργίας διπλών δεσμών C-C. Το σημαντικότερο χαρακτηριστικό της, είναι η μεγάλη
 Η ολεφινική μετάθεση είναι σήμερα η αποτελεσματικότερη μέθοδος δημιουργίας διπλών δεσμών C-C. Το σημαντικότερο χαρακτηριστικό της, είναι η μεγάλη ανεκτικότητα και σταθερότητα των χρησιμοποιούμενων καταλυτών
Η ολεφινική μετάθεση είναι σήμερα η αποτελεσματικότερη μέθοδος δημιουργίας διπλών δεσμών C-C. Το σημαντικότερο χαρακτηριστικό της, είναι η μεγάλη ανεκτικότητα και σταθερότητα των χρησιμοποιούμενων καταλυτών
Κατάλυση σε διαλύµατα Συµπλόκων των Στοιχείων Μετάπτωσης. Βασίλης Ταγκούλης
 Κατάλυση σε διαλύµατα Συµπλόκων των Στοιχείων Μετάπτωσης Βασίλης Ταγκούλης vtango@upatras.gr στοιχειώδεις έννοιες στην κατάλυση η κατάλυση και η σπουδαιότητά της η έννοια της κατάλυσης καταλυτικός κύκλος
Κατάλυση σε διαλύµατα Συµπλόκων των Στοιχείων Μετάπτωσης Βασίλης Ταγκούλης vtango@upatras.gr στοιχειώδεις έννοιες στην κατάλυση η κατάλυση και η σπουδαιότητά της η έννοια της κατάλυσης καταλυτικός κύκλος
ΕΝΟΤΗΤΑ
 Παρασκευές Αλδεϋδών - Κετονών 17.9 ΕΝΟΤΗΤΑ 17.9 7.8 7.8 8.5 8.5 16.4 Μηχανισµός Ενυδάτωσης Αλκυνίων µε άλατα υδραργύρου ΕΝΟΤΗΤΑ 8.5 Υδροβορίωση τελικών Αλκυνίων και οξείδωση δίνει αλδεΰδες Παρασκευές Αλδεϋδών
Παρασκευές Αλδεϋδών - Κετονών 17.9 ΕΝΟΤΗΤΑ 17.9 7.8 7.8 8.5 8.5 16.4 Μηχανισµός Ενυδάτωσης Αλκυνίων µε άλατα υδραργύρου ΕΝΟΤΗΤΑ 8.5 Υδροβορίωση τελικών Αλκυνίων και οξείδωση δίνει αλδεΰδες Παρασκευές Αλδεϋδών
Επιφανειακή οξεοβασική κατάλυση
 Επιφανειακή οξεοβασική κατάλυση Μια μεγάλη κατηγορία στερεών καταλυτών εκδηλώνουν επιφανειακή οξεοβασική συμπεριφορά γ-αl 2 O 3, SiO 2, TiO 2, MgO, SiO 2 -Al 2 O 3, ζεόλιθοι Στην επιφάνεια τέτοιων οξειδίων
Επιφανειακή οξεοβασική κατάλυση Μια μεγάλη κατηγορία στερεών καταλυτών εκδηλώνουν επιφανειακή οξεοβασική συμπεριφορά γ-αl 2 O 3, SiO 2, TiO 2, MgO, SiO 2 -Al 2 O 3, ζεόλιθοι Στην επιφάνεια τέτοιων οξειδίων
Ο ιοντισµός σε υδατικό διάλυµα ενός οξέος Bronsted δηµιουργεί την ισορροπία:
 abpoc1 ΟΞΙΝΕΣ ΚΑΙ ΒΑΣΙΚΕΣ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΟΡΓΑΝΙΚΩΝ ΕΝΩΣΕΩΝ. Γενικά. Ο ιοντισµός σε υδατικό διάλυµα ενός οξέος Bronsted δηµιουργεί την ισορροπία: ΧΗ + ΗΟΗ Χ - + Η 3 Ο + Κeq= ( 3 + )(X - ) (X)() οπου (ΗΟΗ)=55,5mol
abpoc1 ΟΞΙΝΕΣ ΚΑΙ ΒΑΣΙΚΕΣ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΟΡΓΑΝΙΚΩΝ ΕΝΩΣΕΩΝ. Γενικά. Ο ιοντισµός σε υδατικό διάλυµα ενός οξέος Bronsted δηµιουργεί την ισορροπία: ΧΗ + ΗΟΗ Χ - + Η 3 Ο + Κeq= ( 3 + )(X - ) (X)() οπου (ΗΟΗ)=55,5mol
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C;
 Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ
 ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr ΠΥΡΗΝΟΦΙΛΗ ΠΡΟΣΒΟΛΗ ΣΕ ΚΑΡΒΟΝΥΛΙΚΕΣ
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr ΠΥΡΗΝΟΦΙΛΗ ΠΡΟΣΒΟΛΗ ΣΕ ΚΑΡΒΟΝΥΛΙΚΕΣ
5.3 Κατηγορίες οργανικών αντιδράσεων και μερικοί μηχανισμοί οργανικών αντιδράσεων
 5. Κατηγορίες οργανικών αντιδράσεων και μερικοί μηχανισμοί οργανικών αντιδράσεων Κατηγορίες οργανικών αντιδράσεων Η ταξινόμηση των οργανικών αντιδράσεων μπορεί να γίνει με δύο διαφορετικούς τρόπους : α.
5. Κατηγορίες οργανικών αντιδράσεων και μερικοί μηχανισμοί οργανικών αντιδράσεων Κατηγορίες οργανικών αντιδράσεων Η ταξινόμηση των οργανικών αντιδράσεων μπορεί να γίνει με δύο διαφορετικούς τρόπους : α.
4.15 Αλογόνωση των αλκανίων RH + X 2 RX + HX
 4.15 Αλογόνωση των αλκανίων R + X 2 RX + X Ενεργειακό περιεχόμενο R + X 2 RX + X εκρηκτική για το F 2 εξώθερμη για το Cl 2 και το Br 2 ενδόθερμη για το I 2 4.16 Χλωρίωση του Μεθανίου Χλωρίωση του Μεθανίου
4.15 Αλογόνωση των αλκανίων R + X 2 RX + X Ενεργειακό περιεχόμενο R + X 2 RX + X εκρηκτική για το F 2 εξώθερμη για το Cl 2 και το Br 2 ενδόθερμη για το I 2 4.16 Χλωρίωση του Μεθανίου Χλωρίωση του Μεθανίου
Οργανική Χημεία ΕΝΟΤΗΤΑ 8: ΑΛΚΑΝΙΑ ΚΥΚΛΟΑΛΚΑΝΙΑ ΣΥΝΘΕΣΗ ΔΙΑΜΟΡΦΩΣΕΙΣ ΜΟΡΙΩΝ ΠΕΡΙΣΤΡΟΦΕΣ ΔΕΣΜΩΝ - ΙΣΟΜΕΡΙΣΜΟΣ
 Οργανική Χημεία ΕΝΟΤΗΤΑ 8: ΑΛΚΑΝΙΑ ΚΥΚΛΟΑΛΚΑΝΙΑ ΣΥΝΘΕΣΗ ΔΙΑΜΟΡΦΩΣΕΙΣ ΜΟΡΙΩΝ ΠΕΡΙΣΤΡΟΦΕΣ ΔΕΣΜΩΝ - ΙΣΟΜΕΡΙΣΜΟΣ Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περίληψη ΑΛΚΑΝΙΑ ΚΥΚΛΟΑΛΚΑΝΙΑ - ΑΝΤΙΔΡΑΣΕΙΣ
Οργανική Χημεία ΕΝΟΤΗΤΑ 8: ΑΛΚΑΝΙΑ ΚΥΚΛΟΑΛΚΑΝΙΑ ΣΥΝΘΕΣΗ ΔΙΑΜΟΡΦΩΣΕΙΣ ΜΟΡΙΩΝ ΠΕΡΙΣΤΡΟΦΕΣ ΔΕΣΜΩΝ - ΙΣΟΜΕΡΙΣΜΟΣ Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περίληψη ΑΛΚΑΝΙΑ ΚΥΚΛΟΑΛΚΑΝΙΑ - ΑΝΤΙΔΡΑΣΕΙΣ
ΣΤΟΙΧΕΙΑ ΣΤΕΡΕΟΪΣΟΜΕΡΕΙΑΣ ΜΕ ΧΡΗΣΗ ΠΟΛΥΜΕΣΩΝ
 2 Ο ΣΥΝΕΔΡΙΟ ΣΤΗ ΣΥΡΟ ΤΠΕ ΣΤΗΝ ΕΚΠΑΙΔΕΥΣΗ 405 ΣΤΟΙΧΕΙΑ ΣΤΕΡΕΟΪΣΟΜΕΡΕΙΑΣ ΜΕ ΧΡΗΣΗ ΠΟΛΥΜΕΣΩΝ Κορακάκης Γώργιος Τεχνολόγος γραφικών τεχνών-χημικός- Msc ΔιΧηΝΕΤ gk1966@yahoo.com Μουτεβέλη- Μηνακάκη Παναγιώτα
2 Ο ΣΥΝΕΔΡΙΟ ΣΤΗ ΣΥΡΟ ΤΠΕ ΣΤΗΝ ΕΚΠΑΙΔΕΥΣΗ 405 ΣΤΟΙΧΕΙΑ ΣΤΕΡΕΟΪΣΟΜΕΡΕΙΑΣ ΜΕ ΧΡΗΣΗ ΠΟΛΥΜΕΣΩΝ Κορακάκης Γώργιος Τεχνολόγος γραφικών τεχνών-χημικός- Msc ΔιΧηΝΕΤ gk1966@yahoo.com Μουτεβέλη- Μηνακάκη Παναγιώτα
4 o Μάθημα. Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους
 Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους 2017-2018 4 o Μάθημα Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό Προσωπικό,
Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους 2017-2018 4 o Μάθημα Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό Προσωπικό,
Οργανική Χημεία. Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες
 Οργανική Χημεία Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες 1. Καρβονυλικές ενώσεις Καρβονυλική ομάδα C=O σημαντικότερη λειτουργική ομάδα οργανικής χημείας Καρβονυλικές ομάδες βρίσκονται
Οργανική Χημεία Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες 1. Καρβονυλικές ενώσεις Καρβονυλική ομάδα C=O σημαντικότερη λειτουργική ομάδα οργανικής χημείας Καρβονυλικές ομάδες βρίσκονται
Οργανική Χημεία. Κεφάλαιο 16: Χημεία του βενζολίου: ηλεκτρονιόφιλη αρωματική υποκατάσταση
 Οργανική Χημεία Κεφάλαιο 16: Χημεία του βενζολίου: ηλεκτρονιόφιλη αρωματική υποκατάσταση 1. Αντιδράσεις αρωματικών ενώσεων Σημαντικότερη αντίδραση αρωματικών ενώσεων: ηλεκτρονιόφιλη αρωματική υποκατάσταση
Οργανική Χημεία Κεφάλαιο 16: Χημεία του βενζολίου: ηλεκτρονιόφιλη αρωματική υποκατάσταση 1. Αντιδράσεις αρωματικών ενώσεων Σημαντικότερη αντίδραση αρωματικών ενώσεων: ηλεκτρονιόφιλη αρωματική υποκατάσταση
Αλκυλαλογονίδια. Επίκουρος καθηγητής Χρήστος Παππάς
 Αλκυλαλογονίδια Επίκουρος καθηγητής Χρήστος Παππάς 1 Αλκυλαλογονίδια Αλκυλαλογονίδια ονομάζονται οι οργανικές ενώσεις οι οποίες, ως λειτουργική ομάδα, διαθέτουν την ομάδα C-X: -X= -F, -Cl, -Br, -I. Η ισχύς
Αλκυλαλογονίδια Επίκουρος καθηγητής Χρήστος Παππάς 1 Αλκυλαλογονίδια Αλκυλαλογονίδια ονομάζονται οι οργανικές ενώσεις οι οποίες, ως λειτουργική ομάδα, διαθέτουν την ομάδα C-X: -X= -F, -Cl, -Br, -I. Η ισχύς
astelc1 1 Στερεοηλεκτρονικά φαινόµενα
 astelc1 1 Στερεοηλεκτρονικά φαινόµενα Οι διάφοροι δεσµοί που συγκρατούν τα άτοµα σε ένα µόριο είναι το αποτέλεσµα της αλληλεπίδρασης των δεσµικών ηλεκτρονίων και συνολικά απαρτίζουν το µοριακό σκελετό
astelc1 1 Στερεοηλεκτρονικά φαινόµενα Οι διάφοροι δεσµοί που συγκρατούν τα άτοµα σε ένα µόριο είναι το αποτέλεσµα της αλληλεπίδρασης των δεσµικών ηλεκτρονίων και συνολικά απαρτίζουν το µοριακό σκελετό
ΠΡΟΣΘΗΚΗ. Προσθήκη ή ανόρθωση διπλού δεσµού στα αλκένια.
 ΠΡΟΣΘΗΚΗ Σε µία αντίδραση προσθήκης δύο µόρια ενώνονται και δίνουν ένα άλλο µόριο. Η προσθήκη συνήθως λαµβάνει χώρα σε ένα πολλαπλό δεσµό (διπλό ή τριπλό) µε αποτέλεσµα την µετατροπή της «ακόρεστης» ένωσης
ΠΡΟΣΘΗΚΗ Σε µία αντίδραση προσθήκης δύο µόρια ενώνονται και δίνουν ένα άλλο µόριο. Η προσθήκη συνήθως λαµβάνει χώρα σε ένα πολλαπλό δεσµό (διπλό ή τριπλό) µε αποτέλεσµα την µετατροπή της «ακόρεστης» ένωσης
Οργανική Χηµεία. Κεφάλαιο 29: Βιοµόρια: ετεροκυκλικές ενώσεις και νουκλεϊκά οξέα
 Οργανική Χηµεία Κεφάλαιο 29: Βιοµόρια: ετεροκυκλικές ενώσεις και νουκλεϊκά οξέα 1. Γενικά-ιδιότητες Κυκλικές οργανικές ενώσεις: καρβοκυκλικές (δακτύλιος περιέχει µόνο άτοµα C) και ετεροκυκλικές (δακτύλιος
Οργανική Χηµεία Κεφάλαιο 29: Βιοµόρια: ετεροκυκλικές ενώσεις και νουκλεϊκά οξέα 1. Γενικά-ιδιότητες Κυκλικές οργανικές ενώσεις: καρβοκυκλικές (δακτύλιος περιέχει µόνο άτοµα C) και ετεροκυκλικές (δακτύλιος
διακλαδισμένο αλκάνιο γραμμικό αλκάνιο ΑΛΚΑΝΙΑ
 ΑΛΚΑΝΙΑ Ως αλκάνια ορίζουμε τις κορεσμένες οργανικές ενώσεις που αποτελούνται αποκλειστικά από άτομα άνθρακα και υδρογόνου και περιέχουν μόνο απλούς δεσμούς τύπου C C και C. Διακρίνονται δε σε άκυκλα αλκάνια
ΑΛΚΑΝΙΑ Ως αλκάνια ορίζουμε τις κορεσμένες οργανικές ενώσεις που αποτελούνται αποκλειστικά από άτομα άνθρακα και υδρογόνου και περιέχουν μόνο απλούς δεσμούς τύπου C C και C. Διακρίνονται δε σε άκυκλα αλκάνια
στην ανθρακική τους αλυσίδα τουλάχιστον έναν τριπλό δεσμό τύπου C C.
 AΛΚΥΝΙΑ Ως αλκύνια ορίζουμε τους υδρογονάνθρακες που περιέχουν στην ανθρακική τους αλυσίδα τουλάχιστον έναν τριπλό δεσμό τύπου C C. Οι τρεις δεσμοί ενός αλκυνίου σχηματίζονται από την επικάλυψη δυο sp-υβριδισμένων
AΛΚΥΝΙΑ Ως αλκύνια ορίζουμε τους υδρογονάνθρακες που περιέχουν στην ανθρακική τους αλυσίδα τουλάχιστον έναν τριπλό δεσμό τύπου C C. Οι τρεις δεσμοί ενός αλκυνίου σχηματίζονται από την επικάλυψη δυο sp-υβριδισμένων
Οργανική Χημεία. Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια
 Οργανική Χημεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν ομάδες υδροξυλίου συνδεδεμένες με κορεσμένα άτομα άνθρακα υβριδισμού sp 3 Βάσει παραπάνω ορισμού,
Οργανική Χημεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν ομάδες υδροξυλίου συνδεδεμένες με κορεσμένα άτομα άνθρακα υβριδισμού sp 3 Βάσει παραπάνω ορισμού,
Answers to Homework Set
 Answers to Homework Set 3 12-8-2017 1. Χρησιμοποιώντας επιχειρήματα με τυπικό φορτίο εξηγήστε για ποιο λόγο το μονοξείδιο του άνθρακα έχει πολύ μικρότερη διπολική ροπή από ότι αναμένεται με βάση την ηλεκτραρνητικότητα.
Answers to Homework Set 3 12-8-2017 1. Χρησιμοποιώντας επιχειρήματα με τυπικό φορτίο εξηγήστε για ποιο λόγο το μονοξείδιο του άνθρακα έχει πολύ μικρότερη διπολική ροπή από ότι αναμένεται με βάση την ηλεκτραρνητικότητα.
Μάθημα 20 ο. Το σχήμα των μορίων
 Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
Πυρηνόφιλα του Άνθρακα: ΥΛΙΔΙΑ ΦΩΣΦΟΡΟΥ Αντίδραση WITTIG
 Georg Wittig Νόµπελ Χηµείας 1979 Πυρηνόφιλα του Άνθρακα: ΥΛΙΔΙΑ ΦΩΣΦΟΡΟΥ Αντίδραση WITTIG Υλίδιο: Ουδέτερη ένωση µε αρνητικά φορτισµένο άτοµο (C-) ενωµένο µε θετικά φορτισµένο ετεροάτοµο (P+) Υβρίδιο Δοµών
Georg Wittig Νόµπελ Χηµείας 1979 Πυρηνόφιλα του Άνθρακα: ΥΛΙΔΙΑ ΦΩΣΦΟΡΟΥ Αντίδραση WITTIG Υλίδιο: Ουδέτερη ένωση µε αρνητικά φορτισµένο άτοµο (C-) ενωµένο µε θετικά φορτισµένο ετεροάτοµο (P+) Υβρίδιο Δοµών
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ
 ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
Αλκάνια. κορεσμένοι υδρογονάνθρακες. αποτελούνται μόνο από C και H συνδεδεμένα με απλούς δεσμούς. έχουν το γενικό τύπο: C n H 2n+2 (γραμμικά αλκάνια)
 Υδρογονάνθρακες Αλκάνια Alkanes Αλκάνια κορεσμένοι υδρογονάνθρακες αποτελούνται μόνο από C και H συνδεδεμένα με απλούς δεσμούς έχουν το γενικό τύπο: C n H 2n+2 (γραμμικά αλκάνια) Αλκάνια Φυσικές ιδιότητες
Υδρογονάνθρακες Αλκάνια Alkanes Αλκάνια κορεσμένοι υδρογονάνθρακες αποτελούνται μόνο από C και H συνδεδεμένα με απλούς δεσμούς έχουν το γενικό τύπο: C n H 2n+2 (γραμμικά αλκάνια) Αλκάνια Φυσικές ιδιότητες
ΣΤΕΡΕΟΧΗΜΕΙΑ. Καθηγητής Μόσχος Πολυσίου, / Εργαστήριο Γενικής Χημείας Γ.Π.Α.
 ΣΤΕΡΕΟΧΗΜΕΙΑ Καθηγητής Μόσχος Πολυσίου, / Εργαστήριο Γενικής Χημείας Γ.Π.Α. ΙΣΟΜΕΡΕΙΑ Ισομερείς είναι οι ενώσεις με ίδιο μοριακό αλλά διαφορετικό συντακτικό τύπο (συντακτικά ισομερείς) ή με ίδιο μοριακό,
ΣΤΕΡΕΟΧΗΜΕΙΑ Καθηγητής Μόσχος Πολυσίου, / Εργαστήριο Γενικής Χημείας Γ.Π.Α. ΙΣΟΜΕΡΕΙΑ Ισομερείς είναι οι ενώσεις με ίδιο μοριακό αλλά διαφορετικό συντακτικό τύπο (συντακτικά ισομερείς) ή με ίδιο μοριακό,
Αντιδράσεις πυρηνόφιλης υποκατάστασης µε συµµετοχή γειτονικής οµάδας. Αγχιµερής υποβοήθηση.
 ngp 1 Αντιδράσεις πυρηνόφιλης υποκατάστασης µε συµµετοχή γειτονικής οµάδας. Αγχιµερής υποβοήθηση. Είδαµε σε προηγούµενο κεφάλαιο ότι η ύπαρξη ατόµων οξυγόνου (ή και αζώτου) καθώς και διπλών δεσµών ή αρωµατικών
ngp 1 Αντιδράσεις πυρηνόφιλης υποκατάστασης µε συµµετοχή γειτονικής οµάδας. Αγχιµερής υποβοήθηση. Είδαµε σε προηγούµενο κεφάλαιο ότι η ύπαρξη ατόµων οξυγόνου (ή και αζώτου) καθώς και διπλών δεσµών ή αρωµατικών
Οργανική Χηµεία. Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια
 Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
60
 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 Η (συνήθης) αύξηση του πυρηνόφιλου χαρακτήρα όσο κατερχόμαστε σε μία ομάδα του περιοδικού πίνακα οφείλεται στην αντίστοιχη μείωση της ηλεκτραρνητικότητας
59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 Η (συνήθης) αύξηση του πυρηνόφιλου χαρακτήρα όσο κατερχόμαστε σε μία ομάδα του περιοδικού πίνακα οφείλεται στην αντίστοιχη μείωση της ηλεκτραρνητικότητας
Οργανική Χημεία. Κεφάλαια 20 & 21: Καρβοξυλικά οξέα, παράγωγα τους και αντιδράσεις ακυλο υποκατάστασης
 Οργανική Χημεία Κεφάλαια 20 & 21: Καρβοξυλικά οξέα, παράγωγα τους και αντιδράσεις ακυλο υποκατάστασης 1. Καρβοξυλικά οξέα Σημαντικά ακυλο (-COR) παράγωγα Πλήθος καρβοξυλικών ενώσεων στη φύση, π.χ. οξικό
Οργανική Χημεία Κεφάλαια 20 & 21: Καρβοξυλικά οξέα, παράγωγα τους και αντιδράσεις ακυλο υποκατάστασης 1. Καρβοξυλικά οξέα Σημαντικά ακυλο (-COR) παράγωγα Πλήθος καρβοξυλικών ενώσεων στη φύση, π.χ. οξικό
ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΚΟ ΦΑΣΜΑ
 ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΚΟ ΦΑΣΜΑ ΤΥΠΟΙ ΔΟΝΗΣΗΣ Δόνηση τάσης Δονήσεις τάσης Δονήσεις επί του επιπέδου Δονήσεις κάμψης Δονήσεις εκτός επιπέδου συμμετρική (sym) ~1465 cm -1 συμμετρική (scissoring) συμμετρική (twisting)
ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΚΟ ΦΑΣΜΑ ΤΥΠΟΙ ΔΟΝΗΣΗΣ Δόνηση τάσης Δονήσεις τάσης Δονήσεις επί του επιπέδου Δονήσεις κάμψης Δονήσεις εκτός επιπέδου συμμετρική (sym) ~1465 cm -1 συμμετρική (scissoring) συμμετρική (twisting)
13.6 Η ερμηνεία των φασμάτων NMR πρωτονίου
 13.6 Η ερμηνεία των φασμάτων NMR πρωτονίου Η πληροφορία που περιέχεται σ ένα φάσμα NMR περιλαμβάνει: 1. Αριθμό σημάτων 2. Την έντασή τους (ως μετρούμενη επιφάνεια κάτω από την κορυφή) 3. Τύπος σχάσης (πολλαπλότητα)
13.6 Η ερμηνεία των φασμάτων NMR πρωτονίου Η πληροφορία που περιέχεται σ ένα φάσμα NMR περιλαμβάνει: 1. Αριθμό σημάτων 2. Την έντασή τους (ως μετρούμενη επιφάνεια κάτω από την κορυφή) 3. Τύπος σχάσης (πολλαπλότητα)
Κεφάλαιο 2. Οι μεταβλητές των οργανικών αντιδράσεων
 Κεφάλαιο 2 Οι μεταβλητές των οργανικών αντιδράσεων Σύνοψη Στο κεφάλαιο αυτό αναφέρονται οι αντιδράσεις χωρίς τους μηχανισμούς τους, με στόχο να δοθεί έμφαση στις συνέπειες από τις μεταβολές ορισμένων χαρακτηριστικών
Κεφάλαιο 2 Οι μεταβλητές των οργανικών αντιδράσεων Σύνοψη Στο κεφάλαιο αυτό αναφέρονται οι αντιδράσεις χωρίς τους μηχανισμούς τους, με στόχο να δοθεί έμφαση στις συνέπειες από τις μεταβολές ορισμένων χαρακτηριστικών
Πυρηνόφιλη Προσθήκη Αµινών: Ιµίνες και Εναµίνες
 Πυρηνόφιλη Προσθήκη Αµινών: Ιµίνες και Εναµίνες Πυρηνόφιλα Αζώτου - Πρωτοταγείς Αµίνες: ΜΗΧΑΝΙΣΜΟΣ Σχηµατισµός Ιµινών ΣΗΜΑΝΤΙΚΕΣ ΛΕΠΤΟΜΕΡΕΙΕΣ Η ταχύτητα σχηµατισµού ιµίνης εξαρτάται από το ph: Σε υψηλό
Πυρηνόφιλη Προσθήκη Αµινών: Ιµίνες και Εναµίνες Πυρηνόφιλα Αζώτου - Πρωτοταγείς Αµίνες: ΜΗΧΑΝΙΣΜΟΣ Σχηµατισµός Ιµινών ΣΗΜΑΝΤΙΚΕΣ ΛΕΠΤΟΜΕΡΕΙΕΣ Η ταχύτητα σχηµατισµού ιµίνης εξαρτάται από το ph: Σε υψηλό
Οργανική Χημεία. Κεφάλαιο 29: Βιομόρια: ετεροκυκλικές ενώσεις και νουκλεϊκά οξέα
 Οργανική Χημεία Κεφάλαιο 29: Βιομόρια: ετεροκυκλικές ενώσεις και νουκλεϊκά οξέα 1. Γενικά-ιδιότητες Κυκλικές οργανικές ενώσεις: καρβοκυκλικές (δακτύλιος περιέχει μόνο άτομα C) και ετεροκυκλικές (δακτύλιος
Οργανική Χημεία Κεφάλαιο 29: Βιομόρια: ετεροκυκλικές ενώσεις και νουκλεϊκά οξέα 1. Γενικά-ιδιότητες Κυκλικές οργανικές ενώσεις: καρβοκυκλικές (δακτύλιος περιέχει μόνο άτομα C) και ετεροκυκλικές (δακτύλιος
Aντιδράσεις Καρβονυλίου C=O (1)
 Aντιδράσεις Καρβονυλίου = (1) Πυρηνόφιλη προσθήκη (αλδεΰδες, κετόνες) Πυρηνόφιλη ακυλο-υποκατάσταση (καρβοξυλικά οξέα και παράγωγα) α-υποκατάσταση (καρβονυλοενώσεις: αλδεΰδες, κετόνες, καρβοξυλικά οξέα
Aντιδράσεις Καρβονυλίου = (1) Πυρηνόφιλη προσθήκη (αλδεΰδες, κετόνες) Πυρηνόφιλη ακυλο-υποκατάσταση (καρβοξυλικά οξέα και παράγωγα) α-υποκατάσταση (καρβονυλοενώσεις: αλδεΰδες, κετόνες, καρβοξυλικά οξέα
Οργανική Χημεία. Κεφάλαιο 28: Βιομόρια-λιπίδια
 Οργανική Χημεία Κεφάλαιο 28: Βιομόρια-λιπίδια 1. Γενικά Λιπίδια: οργανικά μόρια που απαντούν στη φύση και απομονώνονται κατά την εκχύληση κυττάρων ή ιστών με άπολους οργανικούς διαλύτες Δύο γενικές κατηγορίες
Οργανική Χημεία Κεφάλαιο 28: Βιομόρια-λιπίδια 1. Γενικά Λιπίδια: οργανικά μόρια που απαντούν στη φύση και απομονώνονται κατά την εκχύληση κυττάρων ή ιστών με άπολους οργανικούς διαλύτες Δύο γενικές κατηγορίες
ΣΤΕΡΕΟΧΗΜΕΙΑ: Κλάδος της Χημείας που μελετά τη
 ΣΤΕΡΕΟΧΗΜΕΙΑ: Κλάδος της Χημείας που μελετά τη διάταξη στο χώρο (τρισδιάστατη δομή) των δομικών στοιχείων των ενώσεων Στερεοϊσομερή: Ισομερείς ενώσεις που διαφέρουν στηστερεοχημικήτουςδομή Παραδείγματα
ΣΤΕΡΕΟΧΗΜΕΙΑ: Κλάδος της Χημείας που μελετά τη διάταξη στο χώρο (τρισδιάστατη δομή) των δομικών στοιχείων των ενώσεων Στερεοϊσομερή: Ισομερείς ενώσεις που διαφέρουν στηστερεοχημικήτουςδομή Παραδείγματα
Κεφάλαιο 6: Αντιδράσεις ενολών και ενολικών ανιόντων
 Κεφάλαιο 6: Αντιδράσεις ενολών και ενολικών ανιόντων Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων των ενολών και των ενολικών ανιόντων εστιάζοντας κυρίως σε εκείνα που προέρχονται από
Κεφάλαιο 6: Αντιδράσεις ενολών και ενολικών ανιόντων Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων των ενολών και των ενολικών ανιόντων εστιάζοντας κυρίως σε εκείνα που προέρχονται από
4.3 Οργανομεταλλικές ενώσεις των στοιχείων της Ομάδας 3Α (13)
 4.3 Οργανομεταλλικές ενώσεις των στοιχείων της Ομάδας 3Α (13) Bορίου και αργιλίου οι πλέον ενδιαφέρουσες Ενώσεις οργανοβορίου (οργανοβοράνια), ΒR 3 Πώς παρασκευάζονται οι ενώσεις BR 3 ; (α) Υδροβορίωση
4.3 Οργανομεταλλικές ενώσεις των στοιχείων της Ομάδας 3Α (13) Bορίου και αργιλίου οι πλέον ενδιαφέρουσες Ενώσεις οργανοβορίου (οργανοβοράνια), ΒR 3 Πώς παρασκευάζονται οι ενώσεις BR 3 ; (α) Υδροβορίωση
ΘΕΜΑ 1. ΘΕΜΑ 2. NH 2 H 2. Σχηματίζεται γρήγορα. Σταθερότερο
 ΘΕΜΑ 1. Πείραμα Α. Ενα μείγμα ισομοριακών ποσοτήτων κυκλοεξανόνης,φουρφουράλης και σεμικαρβαζιδίου βράζεται με αναρροή σε διαλύτη αιθανόλη επι εξι ώρες,ψύχεται και η σεμικαρβαζόνη που αποβάλεται απομονώνεται
ΘΕΜΑ 1. Πείραμα Α. Ενα μείγμα ισομοριακών ποσοτήτων κυκλοεξανόνης,φουρφουράλης και σεμικαρβαζιδίου βράζεται με αναρροή σε διαλύτη αιθανόλη επι εξι ώρες,ψύχεται και η σεμικαρβαζόνη που αποβάλεται απομονώνεται
1.5 Αλκένια - αιθένιο ή αιθυλένιο
 19 1.5 Αλκένια - αιθένιο ή αιθυλένιο Γενικά Αλκένια ονομάζονται οι άκυκλοι ακόρεστοι υδρογονάνθρακες, οι οποίοι περιέχουν ένα διπλό δεσμό στο μόριο. O γενικός τύπος των αλκενίων είναι C ν Η 2ν (ν 2). Στον
19 1.5 Αλκένια - αιθένιο ή αιθυλένιο Γενικά Αλκένια ονομάζονται οι άκυκλοι ακόρεστοι υδρογονάνθρακες, οι οποίοι περιέχουν ένα διπλό δεσμό στο μόριο. O γενικός τύπος των αλκενίων είναι C ν Η 2ν (ν 2). Στον
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
7.6 Το συµβολικό σύστηµα R-S των Cahn, Ingold, Prelog
 7.6 Το συµβολικό σύστηµα R-S των ahn, Ingold, Prelog ρ Χάρης Ε. Σεµιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Για να καθοριστεί η απόλυτη στερεοαπεικόνιση ενός συστήµατος απαιτούνται δυο προϋποθέσεις: 1. Χρειάζονται
7.6 Το συµβολικό σύστηµα R-S των ahn, Ingold, Prelog ρ Χάρης Ε. Σεµιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Για να καθοριστεί η απόλυτη στερεοαπεικόνιση ενός συστήµατος απαιτούνται δυο προϋποθέσεις: 1. Χρειάζονται
Εισαγωγή οµάδων σε αρωµατικούς δακτύλιους που εµπεριέχουν περισσότερους από έναν υποκαταστάτες
 1 Χρήσιµες Αντιδράσεις Για το σχεδιασµό, και τελικά στην επιτυχία της παρασκευής νέων φαρµακοµορίων, πρέπει να συνυπολογίζεται το εφικτό µιας συνθετικής στρατηγικής. Έτσι, θα γίνει µια συνοπτική αναφορά
1 Χρήσιµες Αντιδράσεις Για το σχεδιασµό, και τελικά στην επιτυχία της παρασκευής νέων φαρµακοµορίων, πρέπει να συνυπολογίζεται το εφικτό µιας συνθετικής στρατηγικής. Έτσι, θα γίνει µια συνοπτική αναφορά
5.5 Φυσικές ιδιότητες των αλκενίων. ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας
 5.5 Φυσικές ιδιότητες των αλκενίων ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας ιπολικές ροπές Ποια είναι η κατεύθυνση της διπολικής ροπής; Μια μεθυλομάδα προσφέρει ηλεκτρόνια στο διπλό δεσμό,
5.5 Φυσικές ιδιότητες των αλκενίων ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας ιπολικές ροπές Ποια είναι η κατεύθυνση της διπολικής ροπής; Μια μεθυλομάδα προσφέρει ηλεκτρόνια στο διπλό δεσμό,
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις
 Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις Βιβλίο McMurry: σελ. 3-22 Διδάσκων: Στ. Μπογιατζής Επίκουρος
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις Βιβλίο McMurry: σελ. 3-22 Διδάσκων: Στ. Μπογιατζής Επίκουρος
