1-TS. Partea generală IV
|
|
|
- Στυλιανός Αντωνοπούλου
- 8 χρόνια πριν
- Προβολές:
Transcript
1 1-TS. Partea generală IV 1. M himia farmaceutică este ştiinţa care bazându-se pe legile fundamentale ale ştiinţelor chimice: a) Elaborează metodele de obţinere a substanţelor medicamentoase, studiază proprietăţile lor chimice şi fizice b) Studiază corelaţia dintre structura chimică a substanţelor medicamentoase şi acţiunea lor asupra organismului c) Elaborează metodele de determinare a calităţii substanţelor medicamentoase d) Studiază modificările ce au loc la păstrarea substanţelor medicamentoase e) Studiază compoziţia chimică a produsului vegetal 2. M himia farmaceutică are legătură strânsă cu alte discipline de profil: a) himia analitică b) himia toxicologică c) Farmacia socială d) Tehnologia medicamentelor e) Farmacognozia 3. M himia farmaceutică se bazează pe legităţile comune ale disciplinelor: a) himia anorganică b) himia analitică c) himia organică d) himia fizică şi coloidală e) Farmacologia 4. M ăile de elaborare a substanţelor medicamentoase noi sunt: a) Studierea metabolismului compuşilor chimici b) Screening farmacologic ale substanţelor chimice c) Reproducerea compuşilor naturali biologic activi d) Studierea efectelor adverse ale substanţelor medicamentoase cunoscute e) Modificarea structurii compuşilor biologic naturali activi 5. M riteriile analizei farmaceutice sânt: a) Reproductibilitatea b) oncentraţia reagentilor c) Selectivitatea d) Exactitatea e) Sensibilitatea 6. M Monografii unificate la analiză substanţelor medicamentoase în Farmacopeea sunt: a) Solubilitatea b) Reacţiile comune pentru determinarea identităţii c) Determinarea conţinutului de substanţă d) ontrolul purităţii şi limita admisibilă de impurităţi e) Determinarea p-ului 7. M Monografii unificate la analiză substanţelor medicamentoase în Farmacopeea sunt: 1
2 a) Determinarea culorii substanţelor b) Determinarea apei şi a substanţelor volatile c) Dozarea nitrogenului din combinaţiile organice d) Determinarea temperaturii de topire e) Metoda de ardere în balonul cu oxigen 8. M riteriile de apreciere a calităţii medicamentelor sunt: a) uloarea b) Mirosul c) Indicele de refracţie d) Aspectul exterior (descrierea) e) Temperatura de topire 9. M Metodele de obţinere ale substanţelor medicamentoase sânt: a) Sinteza organică completă b) Semisinteza pe baza substanţelor naturale de origine vegetală c) bţinerea din materie primă vegetală d) Screening biologic e) Sinteza microbiologică 10. M Se supun oxidării la păstrarea incorectă a substanţelor medicamentoase grupările funcţionale: a) idroxil fenolic b) Aldehidă c) α-cetolică d) Esterică e) Lactonică 11. S La păstrarea incorectă a substanţelor medicamentoase, care conţin în molecule hidroxil fenolic, au loc procesele chimice de: a) idroliză b) Reducere c) xidare d) ondensare e) Polimerizare 12. S La păstrarea incorectă a substanţelor, ce conţin în molecule grupări esterice, au loc procese chimice de: a) Descompunere b) xidare c) Reducere d) idroliză e) ondensare 13. S Substanţele, care interacţionează cu oxidul de carbon (IV) din aer sunt: a) Preparatele enzimatice b) rganopreparatele c) Sărurile alcaloizilor 2
3 d) Glicozidele e) Sărurile metalelor alcaline şi a acizilor organici slabi 14. M Factorii, sub acţiunea cărora substanţele degradează la păstrare, sunt: a) Temperatura b) Umiditatea c) Presiunea atmosferică d) Alcalinitatea sticlei ambalajului e) xidul de carbon din aer 15. M În monografiile farmacopeice se consideră constante fizice: a) Solubilitatea b) Puterea rotatorie specifică c) Temperatura de topire d) uloarea soluţiei e) Absorbanţa specifica 16. M La controlul purităţii substanţelor medicamentoase după DA se determină: a) enuşa de sulfaţi b) Impurităţile comune (cloruri, sulfaţi, etc.) c) Impurităţile specifice d) Temperatura de topire e) Pierderea în masă la uscare 17. M La criteriile obiective de apreciere a calităţii medicamentelor se referă: a) Valoarea p-lui b) Temperatura de fierbere c) Aspectul exterior (descriere) d) Indicele de refracţie e) Temperatura de topire 18. M Esterii se obţin la interacţiunea alcoolilor cu: a) Acizi carboxilici b) Anhidridele acizilor c) Alcooli poliatomici. d) Amidele acizilor carboxilici e) Acizi anorganici 19. M Pentru sinteza substanţelor medicamentoase se folosesc următoarele reacţii chimice: a) Reacţii de substituţie b) Reacţii de transformare a substituenţilor c) Reacţii de reducere d) Reacţii de oxidare e) Reacţii de polimerizare 20. M La sinteza substanţelor medicamentoase se folosesc pe larg reacţiile de substituţie: a) R x + х Н 2 S 4 R(S 3 ) x + x 2 b) R x + x Нal 2 Ral x + x al 3
4 c) R x + x 3 R( 2 ) x + x 2 d) R - R - R 1-2 R - = - R R 1 - R R 1 2 e) 21. M La sinteza substanţelor medicamentoase se folosesc reacţiile de transformare a substituenţilor: R - = 2 + al 2 R a) b) al al R a X R - + ax + 2 X 2 c) d) R - R - I I [] R - + R 1 - R R e) 22. M La sinteza substanţelor medicamentoase se folosesc reacţiile de oxidare: a) R R R - - R b) R - 3 c) R - d) R - R R R 1 R - = - R 1 + R - R - e) 23. M În Farmacopee sunt descrise metodele de identificare a impurităţilor la cationii: a) Zincului b) Ferului c) alciului d) Potasiului e) Metalelor grele 24. S Impurităţile, care sunt determinate în concentraţii admisibile, trebuie comparate cu: a) Solventul b) Soluţia etalon de tulbureală c) Soluţia etalon la impuritatea ce se determină 2
5 d) Soluţia etalon, care constă din soluţia etalon a impurităţii ce se determină şi reactivul de bază e) Soluţia etalon de culoare 25. S Treo- şi eritro- stereoizomeria e legată de prezenţa în structura moleculei a: a) idroxilului alcoolic secundar b) Radicalului de ciclohexan c) Atomului chiralic de carbon d) âtorva atomi chiralici de carbon, care sânt situaţi la distanţă unul faţă de altul e) Doi atomi chiralici de carbon vecini 26. M Procesele chimice de degradare, ce au loc la păstrare, sunt: a) xidarea b) idroliza c) ondensarea d) Polimerizarea e) Interacţiunea cu dioxidul de carbon 27. S Pentru obţinerea eterului, la alcool e necesar de adăugat: a) Amină primară b) idrazină c) Uree d) Alcool e) Acid carbonic 28. M ătre constantele fizice, care caracterizează gradul relativ de puritate a substanţelor medicamentoase se referă: a) Temperatura de topire b) Gradul de albeaţă a pulberilor c) Vâscozitatea d) Temperatura de descompunere e) Temperatura de solidificare 29. M În analiza farmaceutică, pentru determinarea identităţii substanţelor medicamentoase se folosesc următoarele constante fizice: a) Puterea rotatorie specifică b) Solubilitatea c) Absorbanţa specifică d) Indicele de refracţie e) Temperatura de topire 30. S La alcaloizi se referă compuşii organici de origine vegetală, care au în structura chimică grupele funcţionale: a) - С b) c) Ar - 2 d) = - e) R 31. M Substanţele medicamentoase se clasifică după următoarele criterii: 5
6 a) După aspectul lor b) După structura chimică c) După condiţiile de păstrare d) După acţiunea asupra organismului e) După grupările funcţionale 32. S lasificarea chimică a substanţelor medicamentoase pe grupe se efectuează în corespundere: a) u metodele chimice de analiză b) atura substanţelor c) Metodele fizico-chimice de analiză d) Structura chimică e) Analiza funcţională 33. S În monografiile farmacopeice în calitate de constante fizico-chimice serveşte: a) Solubilitatea b) uloarea soluţiei c) Determinarea substanţelor volatile d) Tulbureala soluţiei e) Puterea rotatorie specifică 2-TS. Analiza funcţională IV 34. S Pentru obţinerea eterului, la alcool e necesar de adăugat: a) Amină primară b) idrazină c) Uree d) Alcool e) Acid carbonic 35. M Pentru identificarea compuşilor carbonilici pot fi folosite următoarele reacţii: a) b) c) 2 - R = = - R +... = = R 2 - = - - R +... = = = d) [] = e)
7 36. M loramină B poate fi folosită pentru analiza calitativă, ca oxidant pentru următoarele grupe de preparate: a) Fenoli b) Preparatele sulfanilamide c) Ioduri d) Derivaţii pirazolonului-5 e) Derivaţii a 5-nitrofuranului 37. M Pentru identificarea grupei amine terţiare în molecula substanţelor se folosesc reactivii: a) Lugol b) Marquis c) Dragendorff d) Erdman e) Mayer 38. M Dehalogenarea din molecula organică e posibilă sub influenţa: a) Soluţiei de hidroxid de sodiu b) Soluţiei de nitrat de argint c) Descompunerea termică d) idrolizei e) Zincului în mediu bazic 39. M Reacţia de formare a azocoloranţilor se foloseşte pentru identificarea substanţelor medicamentoase, derivaţi de: a) Fenol b) Anilină c) Acid para-aminobenzoic d) Pirazol e) Sulfanilamide 40. M La reactivii comuni de precipitare se referă: a) Reactivul Bouchardat, reactivul Marquis b) Acidul picric, tanic c) Reactivul Dragendorff, reactivul Fehling d) Reactivul Marquis, reactivul Bouchardat e) Reactivul Lugol, reactivul Mayer 41. S u clorură ferică nu interacţionează: a a) b) 7
8 a c) d) 2. l e) 42. M Reacţie hidroxamică dau: a) Sulfacetamid sodic (sulfacilul sodic) b) Acetatul de hidrocortizon c) lorhidratul de procaină (novocaină) d) Propionatul de testosteron e) lorhidratul de morfină 43. S Grupa aminică aromatică a sulfanilamidelor poate fi identificată cu reacţia: a) De reducere b) De esterificare c) De diazotare d) De diazotare şi cuplare cu fenol e) Sulfonare 44. M Reacţia de formare a azocoloranţilor în anumite condiţii este posibilă pentru: a) b) a 2. l c) 8
9 2 3 d) e) 45. M u ionul de fier (III) pot fi identificate substanţele medicamentoase: a) Ftivazida b) Paracetamol c) lorhidrat de morfină d) Fosfat de codeină e) Aminofillina (eufillina) 46. M ătre grupele funcţionale care se pot oxida sau autooxida se referă: R - a) R b) R R 1 c) d) R -S e) R M Identificarea substanţelor medicamentoase, care au în moleculă hidroxil fenolic, se efectuează după formarea: a) olorantului aurinic b) Sării de amoniu a acidului tetrametilpurpuric c) Bromderivaţilor d) olorantului indofenolic e) Azocolorantului 48. M Azocolorantul se va forma în condiţiile: - R a 2 ; l a) 9
10 + 2 [Ar - ] l - b) - - R l ; + [Ar - - ] l c) a + [Ar - - ] l d) 2 a 2 ; l; a e) 49. M u scopul identificării substanţelor medicamentoase, ce conţin în moleculă grupa amină aromatică primară, se efectuează reacţia de obţinere a: a) Taleiochininei b) olorantului aurinic c) Azocolorantului d) Bromderivaţilor e) Periodurilor 50. M Proprietăţile amfotere sunt condiţionate de următoarele perechi de grupe funcţionale: a) Aldehidă şi cetonă b) Aminică şi imidă c) arboxil şi amină d) Esterică şi aldehidă e) idroxil alcoolic şi fenol 51. M Proprietăţile bazice sunt condiţionate de următoarele grupe funcţionale: a) b) c) d) e) 2 10
11 52. M Reacţiile de interacţiune a substanţelor medicamentoase cu bazele sunt condiţionate de grupele funcţionale: a) b) R - R R 1 R R 1 c) d) R R e) 53. S Pirimidina este: a) b) c) d) e) 54. S eterociclul care conţine oxigen este: a) hinolina b) Pirol c) Furan d) hinuclidina e) Tiofen 11
12 55. M Sisteme condensate sunt: a) hinuclidina b) Purina c) Piperidina d) Pteridina e) Imidazol 56. M Reactivi de precipitare alcaloidali sunt: a) Reactivul Marquis b) Reactivul Dragendorff c) Reactivul Fehling d) Reactivul Bouchardat e) Soluţia de tanină 57. M Reactivi pentru determinarea azotului terţiar sunt: a) Soluţia de nitrat de argint b) Soluţia de acid picric c) Reactivul Mayer d) Reactivul Erdman e) Reactivul Lugol 58. S Reactivul Mayer este: a) Soluţie de K 2 gi 4 b) Soluţie de BiI 3 KI c) K 2 gi 4 în soluţie de a d) I 2 în soluţie de KI e) 2 în 2 S 4 conc 59. S Reactivul Marquis este: a) 3 conc. b) Amestec 3 conc. şi 2 S 4 conc. c) K 2 gi 4 în soluţie de a d) 2 în 2 S 4 conc. e) I 2 în soluţie de KI 60. M La reactivii de culoare se referă: a) Reactivul Marquis b) Reactivul essler c) Reactivul Erdman d) 2 S 4 conc. e) 3 conc. 61. M Interacţiunea cu reactivii de precipitare comuni se bazează pe următoarele reacţii de: a) ondensare b) xidare c) Formare de săruri d) Formare de complecşi 12
13 e) Deshidratare 62. S Reactivul Dragendorff este: a) Soluţie de iod în iodură de potasiu b) Soluţie de iodură de mercur în iodură de potasiu c) Soluţie de iodură de bismut în iodură de potasiu d) Soluţie de iodură de cadmiu în iodură de potasiu e) Soluţie de acid fosforomolibdenic 63. M idroxil fenolic este prezent în structura chimică a substanţilor: a) Fosfat de codeină b) lorhidrat de morfină c) Bromură de butilscopolamină d) itroxolină e) afeină 64. M Reacţia pozitivă cu soluţie amoniacală de nitrat de argint dau preparatele: a) odeina b) Izoniazida c) lorhidrat de papaverină d) Glucoza e) Fenobarbital 65. M Reacţia hidroxamică se efectuează la identificarea preparatelor: a) idrotartrat de platifilină b) itrazepam c) lorhidrat de morfină d) Benzilpenicilina sodică e) Diazepam 66. M Grupă esterică conţin preparatele: a) Quifenadin (fencarol) b) Benzocaină (anestezina) c) Ftivazid d) Bromură de butilscopolamină e) idrotartrat de platifilină 67. M u soluţia de sulfat de cupru interacţionează preparatele: a) lorură de sodiu b) Sulfatiazol (norsulfazol) c) Sulfat de atropină d) Fenilbutazonă (butadionă) e) Metamizol sodic (analgină) 68. M Flacăra se colorează în verde la arderea pe sîrma de cupru a preparatelor: a) Sulfacetamida sodica (sulfacil de sodiu) b) loramfenicol (levomecitină) c) icotinamid d) lorhidrat de bendazol (dibazol) 13
14 e) lorhidrat de trimeperidină (promedol) 69. S La încălzirea cu acizii minerali degajă anhidrida sulfurică preparatul: a) Sulfanilamid (streptocida) b) Оfloxacin c) Quifenadin (fencarol) d) Metamizol sodic (analgină) e) lorhidrat de drotaverină (o-şpa) 70. M Efect pozitiv a reacţiei hidroxamice dau preparatele: a) Benzilpenicilina b) Trimeperidină (promedol) c) Fenilbutazona (butadiona) d) Sulfat de atropină e) Quifenadin (fencarol) 71. M u clorura de fer (III) interacţionează preparatele: a) lorhidrat de pilocaprină b) Fenazonă (antipirina) c) idrotartrat de epinefrină (adrenalină) d) lotrimazol e) lorhidrat de trimeperidină (promedol) 72. S u clorura de fer (III) formează compuşi complecşi: a) Sulfat de chinină b) Fenazonă (antipirină) c) Sulfat de atropină d) lorhidrat de papaverină e) lorură de sodiu 73. M Reacţia de formare a azocoloranţilor se efectuează la identificarea preparatelor: a) icotinamida b) lotrimazol c) lonidina (clofelin) d) loramfenicol (levomecitină) e) Benzocaina (anestezină) 74. M u soluţia de clorură de fer (III) interacţionează: a) Metamizol sodic (analgină) b) Fosfat de codeină c) Ftivazid d) lorhidrat de morfină e) Tramadol 75. M idroxil fenolic conţin: a) Fosfat de codeină b) lorhidrat de morfină c) Bromură de butilscopolamină d) itroxolină 14
15 e) lorchinaldol 76. M Reacţia cu clorura de fer (III) poate fi utilizată la identificarea preparatelor: a) Fenazonă (antipirină) b) lorhidrat de piridoxină c) Ftivazida d) Rutozid (rutină) e) lorhidrat de papaverină 77. M În structura chimică grupă carbinolă conţin preparatele: a) Quifenadin (fencarol) b) lorhidrat de difenhidramină (dimedrol) c) Sulfat de chinină d) Bromură de butilscopolamină e) Fenilbutazona (butadionă) 78. M Grupa esterică se conţine în structura chimică a preparatelor: a) Sulfat de chinină b) Sulfat de atropină c) lorhidrat de trimeperidină (promedol) d) lorhidrat de papaverină e) idrotartrat de platifilină 79. S u soluţia amoniacală de nitrat de argint (Ag 3 ) interacţionează: a) Fosfat de codeină b) Izoniazida c) lorhidrat de papaverină d) lorhidrat de chinină e) Сlorhidratul de cocaina 80. M Reacţia de formare a azocoloranţilor dau substanţele care conţin grupele funcţionale: a) Alcooli b) Fenoli c) Esteri d) Aldehide e) Amine aromatice primare 81. M La interacţiunea clorhidratului de hidroxilamină în mediu bazic cu acetatul de cupru (II), precipitat verde se formează datorită: a) idroxilului fenolic b) Grupei esterice c) Grupei eterice d) Grupei lactonice e) Grupei lactamice 82. M Reacţia de formare a azocoloranţilor dau substanţele care conţin grupele funcţionale: a) Amino-grupa secundară 15
16 b) Amino-grupa aromatică primară c) idroxil fenolic d) Azotul terţiar e) idroxil alcoolic 83. M u clorura de fer (III) interacţionează fragmentele de structură şi grupele funcţionale: a) idroxil alcoolic b) Salicilat-ion c) Grupa aldehidă d) idroxil fenolic e) Benzoat-ion 84. S Reacţie pozitivă (coloraţie violetă) cu ninhidrina dău: a) Esterii b) Aminoacizii c) Aldehidele d) Fenolii e) Alcoolii 85. M Pentru identificarea grupei aldehide sunt utilizaţi reactivii: a) Reactivul essler b) Soluţiа сlorura de fer (III) c) Soluţia amoniacală de nitrat de argint d) Soluţia nitrat de argint e) Reactivul Fehling 86. M Pentru determinarea grupei carboxilice în structura substanţelor medicamentoase, sunt utilizaţi reactivii: a) Acizii alifatici b) Alcooli c) Soluţia de clorură de fer (III) d) Soluţia de sulfat de cupru (II) e) Soluţia de ninhidrină 87. M idroxilul fenolic în substanţele medicamentoase se determină cu ajutorul reactivilor: a) Apa de brom b) Soluţia sulfat de cupru (II) c) Diazoreactiv d) Reactiv Marquis e) Soluţia de сloramină şi amoniac 88. M eterociclii ce conţin azot sunt: a) Purina b) Furan c) hinolina d) Tiofen e) Pirimidina 16
17 89. S Purinei îi corespunde formula: a) b) c) d) e) 90. S Formula de structură a pirimidinei este: a) b) c) d) e) 17
18 91. S Formula de structură a indolului este: a) b) c) d) e) 92. S Formula de structură a chinolinei este: a) b) c) d) e) 93. M Interacţiunea cu reactivii de coloraţie se bazează pe următoarele reacţii de: a) Formare de săruri b) xidare 18
19 c) Formare de complecşi d) ondensare e) Deshidratare 3 - TS. Metodele titrimetrice IV 94. M Pentru determinarea cantitativă a substanţelor medicamentoase se folosesc următoarele metode: a) Analiza gravimetrică b) Analiza biologică c) Analiza titrimetrică d) Analiza elementelor e) Analiza funcţională 95. M La titrarea complexonometrică se folosesc următorii indicatori: a) Fenolftalina b) Murexidul c) Metiloranj d) egru de eroicrom e) Xilenoloranj 96. M La titrarea în mediu anhidru au loc reacţiile: a) R + 3 [R ] b) 3 + l 4 l c) 3 + a 3 a + 2 d) e) [R ] + + l 4 [R ] +. l M Folosirea metodei nitritometrice pentru analiza cantitativă este condiţionată de prezenţa în moleculele substanţelor a grupelor funcţionale: a) Grupa amină alifatică primară b) Grupa amină aromatică primară c) Grupa amină aromatică secundară d) itro-grupele în ciclul aromatic după reducere e) idroxilul fenolic 98. M Pentru analiza cantitativă a clorhidraţilor substanţelor şi conţin grupa imidă, se poate folosi metoda: a) itritometrică b) eutralizarea în mediu anhidru c) Argentometrică d) Alcalimetrică e) Acidimetrică 99. M Stabilirea punctului de echivalenţă în metoda nitritometrică la analiza substanţelor medicamentoase se efectuează: 19
20 a) Spectrofotometric b) Potenţiometric c) Fără indicator d) u ajutorul indicatorului extern e) u ajutorul indicatorului intern 100. S Mediul reacţiei la dozarea halogenului după metoda Mohr trebuie să fie: a) Acid b) Bazic c) eutru d) Puternic bazic e) Puternic acid 101. M Metoda Kjeldahl poate fi folosită la determinarea cantitativă a: a) Uretanilor b) Aminoacizilor c) Amidelor acizilor d) Aldehidelor e) eterociclelor cu conţinut de azot 102. M are noţiuni se recomandă de folosit la efectuarea analizei titrimetice: a) Factorul de echivalenţă b) Masa molară echivalentă c) Titrul titrantului după substanţa determinată d) Unitate convenţională e) Soluţie standard 103. S Indicatorii de adsorbţie se folosesc la metoda de analiză cantitativă: a) omplexonometria b) Bromatometria c) Titrarea acido-bazică în mediu anhidru d) Argentometria e) Titrarea acido-bazică în mediu apos 104. S Metoda argentometrică de titrare poate fi folosită la identificarea substanţelor, ce conţin în moleculă ionii şi grupele funcţionale indicate în afară de: a) Ionii de clor b) Ionii de brom c) Grupa imidă d) alogen legat organic e) Grupa alcoolică 105. СМ alcularea conţinutului substanţei de analizat după metoda titrimetrică, la titrarea directă, se efectuează după formula: V TB / A K Vb. c. 100 X % a V a) p. 20
21 V TB / A K 100 X % b) a ( V1K 1 V2K 2 ) TB / A 100 X % c) a V TB / A K X % d) a (100 b) ( V V p. c. ) TB / A K 100 X % e) a 106. M La determinarea cantitativă a clorurii de sodiu prin metoda argentometrică Mohr, se referă următoarele reacţii: a) Ag S AgS b) al + Ag 3 Agl+a 3 c) 2Ag 3 + K 2 r 4 Ag 2 r 4 + 2K 3 d) al +Zn[(U 2 ) 3 ( 3 ) 8 ] azn[(u 2 ) 3 ( 3 ) 9 ] l e) 3 4 S + Fe 4 (S 4 ) 2 Fe(S) 3 + 2( 4 ) 2 S M Pentru metoda bromatometrică de dozare sunt caracteristice reacţiile chimice: a) xidare b) Substituţie c) Formare de compuşi complecşi d) Reducere e) De neutralizare 108. S ondiţiile necesare pentru titrarea clorurilor şi bromurilor după metoda Mohr sunt: a) Mediul acid al reacţiei b) Mediul alcalin c) Prezenţa acidului azotic d) Mediul reacţiei trebuie să fie aproape neutru e) Mediul reacţiei nu are importanţă 109. S La titrarea argentometrică prin metoda Mohr se folosesc indicatorii: a) К 2 r 2 7 b) К 2 r 4 c) 4 S d) Fe 4 (S 4 ) 2 e) KMn M În calitate de indicatori la titrarea argentometrică prin metoda Volhard se pot folosi: a) Fe 4 (S 4 ) 2 b) Fel 3 c) Fe( 3 ) 3 21
22 d) К 2 r 4 e) 4 S 111. M La titrarea argentometrică prin metoda Fajans se folosesc indicatorii: a) Eozionată b) Fluoresceina c) Albastru de bromfenol d) Fenolftaleina e) Murexid 112. M Prin metoda nitritometrică se determină preparatele: a) lorpomazina (aminazina) b) loramfenicol (levomicetina) c) Benzocaina (аnestezina) d) Difenhidramina (dimedrol) e) Тramadol 113. M În calitate de solvenţi protogeni la titrarea în mediu anhidru se folosesc: a) Benzen b) Acid formic c) Acid clorhidric d) Acid acetic glacial e) Dimetilformamida 114. M În calitate de solvenţi protofili la titrarea în mediu anhidru se folosesc: a) Acidul acetic glacial b) Anhidrida acetică c) Dimetilformamida d) Metanolul e) Piridin 115. S În prezenţa cărui acid şi în ce limite trebuie să se afle mărimea p la titrarea halogenurilor după metoda Volhard: a) Mediu acid sulfuric, p nu mai mare de 2 b) Mediu acid azotic, p nu mai mare de 2 c) Mediu acid azotic, p nu mai mare de 8 d) Mediu acid acetic, p nu mai mare de 4 e) Mediu acid acetic, p nu mai mare de S Pentru determinarea cantitativă a clorurilor după metoda Fajans se utilizează albastru de bromfenol în mediu: a) eutru b) Reacţia mediului nu are importanţă c) Acid azotic d) Acid acetic e) Bazic 117. S Metoda de titrare în mediul solvenţilor protofili poate fi aplicată la dozarea: a) Fenobarbitalului 22
23 b) lorhidratului de clorpromazină (aminazina) c) lorhidratului de papaverină d) afeinei e) lorhidratului de glaucină 118. S La titrarea indirectă conţinutul substanţei de analizat se calculează după formula: V TB / A K 100 X % a) a ( V1K 1 V2K 2 ) TB / A 100 X % b) a V TB / A K X % c) a (100 b) V TB / A K Vb. c. 100 X % a V d) p. ( V V p. c. ) TB / A K 100 X % e) a 119. S a indicator la titrarea iodurilor dupa metoda argentometrică, varianta Fajans, serveşte: a) Metiloranj b) Albastru de bromfenol c) Fenolftaleina d) Eozina e) Murexid 120. S La titrarea argentometrică a clorurilor după metoda Fajans ca indicator serveşte: a) Fluoresceina b) Eozina c) Murexid d) Albastru de bromfenol e) Albastru de metilen 121. S Metoda cerimetrică de dozare a substanţelor medicamentoase este o metodă de: a) eutralizare în mediu apos b) eutralizare în mediu anhidru c) De precipitare d) omplexonometric e) xidare-reducere 122. M Metoda iodometrică în condiţii corespunzătoare se poate utiliza pentru determinarea cantitativă a: a) a
24 3 a 3 S b) = c) 3 3 d) e) 4-ТS. Metodele fizico-chimice IV 123. S Metoda fotometrică de analiză se bazează pe: a) Determinarea unghiului de rotaţie a luminii poralizate b) Separarea între două faze c) Determinarea spectrelor de emisie d) Absorbţia selectivă a radiaţiei electromagnetice e) Măsurarea indicelui de refracţie 124. S Absorbanţa este: a) A= k b b) A= lg I/I 0 c) A= 10 -kb d) A= sin α /sin β e) A= lg I 0 / I 125. M Alegeţi expresile corecte a legii Bugher-Lambert-Beer: 1% A1 A c l a) cm I 0 1% lg A A1 c l cm b) I I 0 lg A c l c) I 1% A A1 1/ c d) cm kb e) I / I
25 126. S umim spectru de absorbţie: a) Dependenţa lungimii de undă de concentraţie b) Dependenţa absorbanţei de concentraţie c) Dependenţa absorbanţei de lungimea de undă d) Dependenţa absorbanţei de grosimea stratului e) Dependenţa absorbanţei specifice de concentraţie 127. M În determinările fotometrice se folosesc aparatele: a) Polarimetre b) Spectrofotometre c) Refractometre d) olorimetre e) Fotoelectrocolorimetre 128. M Pentru determinarea concentraţiei prin metoda spectrofotometrică folosim formula: a) l / A b) A/ l 1% A A l c) / 1cm A l d) 1 % 1 cm A A l e) % / 1 1cm 129. M Pentru determinările cantitative spectrele de absorbţie trebuie să respecte condiţiile: a) Banda aleasă să nu fie suprapusă de o altă bandă a altor componenţi b) Spectrul de absorbţie trebuie să fie în limita nm c) Absorbanţa în λ max trebuie să fie destul de mare pentru un compus individual d) Absorbanţa să fie direct proporţională cu concentraţia e) oncentraţia soluţiei analizate să fie 1% 130. M Spectrul în IR este caracterizat de: a) Lungimea de undă b) Serii de benzi de absorbţie c) umăr de undă d) Transmitanţa în % e) Absorbanţa spicifică 131. M Metoda fotocolorimetrică de analiză se bazează pe: a) Determinarea absorbanţei luminii policromatice de către substanţa analizată b) Determinarea absorbanţei unei soluţii, obţinute în urma unei reacţii de culoare c) Determinarea lungimii de undă a unei soluţii în dependenţă de concentraţie d) Determinarea concentraţiei soluţiei în dependenţă de absorbanţa e) Determinarea absorbanţei soluţiilor colorate 25
26 132. M Spectrul RM (rezonanţei magnetice nucleare) este caracterizat de: a) Deplasarea chimică b) Multiplitate c) Suprafaţa rezonanţei d) Interacţiune de spin e) Interacţiune magnetică 133. M Separarea substanţelor pe strat subţire poate fi efectuată prin următoarele mecanisme: a) u schimb de ioni b) De precipitare c) De repartiţie d) De adsorbţie e) De excluziune moleculară 134. M Indicaţi constantele optice, folosite la identificarea substanţelor prin metoda spectrofotometrică: a) Raportul absorbanţei către grosimea stratului de substanţă analizată b) Lungimea de undă, corespunzătoare maximului de adsorbţie c) Raportul absorbanţei către lungimea de undă d) Raportul absorbanţelor la diferite lungimi de undă e) Raportul absorbanţei către concentraţie şi grosimea stratului 135. M În spectroscopia IR la pregătirea substanţelor pentru analiză se folosesc: a) Vazelină b) Ulei de vazelină c) Bromură de potasiu d) loroform e) Alcool etilic 136. M Indicaţi factorii care determină condiţiile optime de dozare a substanţelor medicamentoase prin metoda spectrofotometrică: a) Solventul b) Valoarea p-ului c) Lungimea de undă d) Structura chimică a substanţei e) Temperatura 137. M Spectrofotometria în IR se deosebeşte de spectrofotometria în UV prin: a) aracterul spectrului de absorbţie b) Diapazonul spectrului electromagnetic c) Dependenţa absorbţiei de concentraţie d) atura absorbţiei e) Metodele de calcul a concentraţiei 138. M Deosebirea între spectroscopia în UV şi fotocolorimetria constă în: a) Dependenţa absorbţiei de grosimea stratului b) Metodele de calcul a concentraţiei c) Regiunea spectrului electromagnetic folosit 26
27 d) Dependenţa absorbţiei de concentraţia soluţiei e) Dependenţa de culoarea soluţiilor 139. M Metodele bazate pe determinarea absorbţiei electromagnetice sunt: a) Refractometria b) romatografia c) Spectrofotometria UV d) Polarimetria e) Fotocolorimetria 140. S La metoda optică nespectrale se refera: a) Polarografia b) romatografia c) Polarimetria d) Potenţiometria e) Spectroscopia IR 141. M Mărimea absorbanţei este direct proporţională cu: a) Lungimea de undă b) oncentraţia soluţiei c) Masa molară a substanţei dizolvate d) Grosimea stratului e) Transmitanţa în % 142. M Metoda fotocolorimetrică este bazată pe măsurarea intensităţii culorii produşilor reacţiilor de obţinere a: a) Azocolorantului b) olorantului aurinic c) Tiocromului d) olorantului indofenolic e) Murexidului 143. M Puterea rotatorie specifică depinde de: a) atura substanţei b) Lungimea de undă c) oncentraţia soluţiei d) Grosimea stratului e) atura solventului 144. M Absorbanţă specifică depinde de: a) Absorbanţă b) Lungime de undă c) oncentraţia soluţiei (1g în 100 ml) d) oncentraţia soluţiei (g/mol în 1 l) e) Grosimea stratului 145. M alculul conţinutului de substanţă analizată prin metoda fotometrică, se efectuează conform formulelor: 27
28 A / A a) st st st A / A b) an st st 1% Aan / A1 1 c) A an / cm d) st A 1% A e) / 1cm 146. M Faţă de produşii reacţiilor, folosiţi la determinarea cantitativă prin metoda fotocolorimetrică, se înaintează următoarele cerinţe: a) Stabilitatea culorii soluţiei b) Stabilitatea în timp (fără a se schima) a culorii soluţiei c) Dependenţa proporţională între absorbanţă şi concentraţie d) Dependenţa proporţională între absorbanţă şi lungimea de undă e) Dependenţa proporţională între absorbanţă şi grosimea stratului de soluţie analizată 147. M romatografia pe hârtie poate avea mecanism de: a) Repartiţie b) Precipitare c) Adsorbţie d) Schimb cationic e) Schimb anionic 148. M Pentru legea Bugher-Lambert-Beer, alegeţi expresiile corecte: I 0 lg A c l a) I I c b) 0 I 0 lg A c l c) I I 0 1% lg A A1 c l cm d) I n n c F e) M Fotometria de extracţie este bazată pe interacţiunea preparatelor, ca baze slabe cu indicatorii: a) Metiloranj b) Albastru de bromtimol c) Albastru de bromfenol d) Murexid e) Tropeolină M Factorii ce determină condiţile optime de dozare a substanţelor medicamentoas prin metoda spectofotometrică sunt: a) Temperatura b) Solventul c) p 28
29 d) Lungimea de undă, ce corespunde minimului de absorbţie a luminii e) Structura chimică a substanţelor 151. S La metode optice nespectrale se refera: a) Refractometria b) romatografia c) Potenţiometria d) Polarografia e) Spectrofotometria 152. M Absorbtivitatea molară depinde: a) Lungimea de undă b) Absorbanţa c) oncentraţia soluţiei (1 g în 100 ml) d) oncentraţia soluţiei (g/mol în 1 l) e) Grosimea stratului soluţiei 153. S Metoda bazată pe refracţia luminii este: a) romatografia b) Spectrofotometria în UV c) Refractometria d) Polarimetria e) Fotocolorimetria 154. M Indicele de refracţie a soluţiei depinde de: a) atura solventului b) Temperatura c) Lungimea de undă d) oncentraţie e) Grosimea stratului 155. S onţinutul de substanţă prin metoda refractometrica se calculează conform formulei: ( n1 n2 ) c a) n n2 n n0 b) F F c) n n0 F ( n n d) ) 0 F ( n n0 ) e) F S Metoda bazată pe proprietatea substanţelor optic active de a roti planul luminii 29
30 polarizate este: a) Spectrofotometria în UV b) romatografia c) Refractometria d) Polarimetria e) Fotocolorimetria 157. S Puterea rotatorie specifică pentru substanţe în soluţie se calculează conform formulei: 20 a) [ ] D 100/ l c 20 b) [ ] D / l 20 c) [ ] D 100/ l 20 d) [ ] D / l e) [ ] D S Puterea rotatorie specifică pentru substanţe lichide se calculează conform formulei: 20 a) [ ] D 100/ l c 20 b) [ ] D 100/ l 20 c) [ ] D / l 20 d) [ ] D / l e) [ ] D TS. Derivaţii hidroxifenilalchilaminelor IV 159. СS lorhidratul de epinefrin[ (adrenalina) după structura chimică este: l a) lorhidrat de l-1-fenil-2-metilaminopropanol-1 b) lorhidrat de l-izopropilamin-3-(1-naftoxi)-propanol-2 c) α-metil-β-(3,4-dihidroxifenil)-alanina d) n-aminobenzolsulfonilacetamid de sodiu e) lorhidrat de l-(3,4-dihidroxifenil)-2-metilaminoetanol hidroclorid 160. M După structura chimică clorhidratul de epinefrină (adrenalina) este: l 30
31 a) Alcool poliatomic b) Derivat heterociclic c) Amină alifatică d) Fenol e) Aldehidă 161. M Identificarea izadrinei se poate efectua cu ajutorul următoarelor reacţii: a) Reacţia murexindă b) u clorură de fer (III) c) Formarea colorantului aurinic d) 4-nitrobenzilclorură e) u nitrat de argint 162. M Identificarea clorhidratului de propranolol (anaprilina) se poate efectua cu ajutorul următoarelor reacţii: a) Determinarea punctului de topire a basei propranololului b) u reactivul Fehling c) u soluţie nitrat de argint d) Determinarea maximului de absorbţie în UV e) Formarea oglinzii de argint 163. M Derivaţii fenilalchilaminelor sunt: a) loramfenicolul (levomicetina) b) idrotartratul de epinefrina (adrenalina) c) lorhidratul de efedrina d) lorochina (chingamina) e) Ibuprofenul 164. M Identificarea metildofei se poate efectua conform următoarelor reacţii: a) Proba murexidă b) u clorură de fer (III) c) Formarea hidroxamatului de fer d) u ninhidrină e) Formarea indofenolului 165. M Identificarea clorhidratului de epinefrină (adrenalină) se poate efectua cu ajutorul următoarelor reacţii: a) Formarea tiocromului b) u clorură de fer c) Formarea adrenocromului d) u difenilamina e) u nitrat de argint 166. M Dozarea levodopei se efectuiază prin următoarele metode: a) Metoda Kjeldahl b) Bromatometrică c) Titrarea în solvenţi protofili d) Spectrofotometrică e) Titrarea în solvenţi protogeni 31
32 167. СS Substanţa iniţială pentru obţinerea clorhidratului de efedrină este: a) Pirocatechina b) Piridina c) Aldehida succinică d) Benzaldehida e) Acidul р-aminobenzoic 168. СS Substanţa iniţială pentru obţinerea epinefrinei (adrenalina) este: a) Izatina b) Toluen c) Pirocatechina d) itrobenzen e) Aldehida succinică 169. СS Activitatea optică a clorhidratului de efedrină este determinată de segmentul structural: a) l b) c) d) - e) M Sub formă de treo- şi eritroizomeri pot exista: a) lorhidratul de efedrină b) Prazosina c) idrotartratul de epinefrina (adrenalina) d) Metildopa e) loramfenicolul (levomicetina) 171. M Reacţia de obţinere a azocolorantului este posibilă pentru: a) 32
33 b) c) l l d) e) 172. СS idrotartratul de norepinefrină (adrenalină) formează compuşi coloraţi la p=6,5 cu reactivii: a) Iodura de potasiu b) Iodul c) idroxidul de sodiu d) Iodatul de potasiu e) itritul de sodiu 173. M Pentru determinarea cantitativă a clorhidratului de efedrină prin metoda acidobazică în mediu anhidru se folosesc ca reactivi: a) Dimetilformamida b) Acidul acetic glacial c) Acetatul de mercur d) Piridina e) Acidul percloric 174. СS Metildopa după structura chimică este: a) Izopropilnoradrenalină b) L-1-metil-β-(3,4-dioxifenil)-alanină c) L-1-amino- β-(3-oxifenil)-acid propionic d) 1-fenil-2-metilamino- propan e) lorhidratul de l-1-(3,4-dihidroxifenil)-2-metilaminoetanol 175. M După structura chimică clorhidratul de epinefrină (adrenalină) este: l a) itro-derivat b) Alcool poliatomic 33
34 c) Amină aromatică d) Fenol e) Amină alifatică 176. M Identificarea hidrotartratului de epinefrină după reacţia de obţinere a adrenocromului este posibilă cu: a) Soluţie de iod 0,1 mol/l b) Soluţie tampon cu рн 3,56 c) Soluţie de iodură de potasiu 0,1 mol/l d) Soluţie tampon cu рн 6,5 e) Soluţie tampon cu рн 9, M Reacţia de obţinere a azocolorantului în anumite condiţii este posibilă pentru: Br l a) b) c) d) a 2 Br l l 2. l e) 178. СS Efect mucolitic posedă: a) lorhidratul de efedrină b) lorhidratul de ambroxol c) lorhidratul de papaverină d) Metoxamina e) loramfenicol (levomicetina) 179. СS În ambroxol reacţia de obţinere a azocolorantului este determinata de fragmentul 34
35 structural: Br 2 Br 2 -. l a) b) 2 - Br c) Br 2 d) e) 6-TS. Diuretice - IV M După structura chimică idroclortiazida este: 2 S l S a) Amină aromatică b) Fenol c) ompus heterociclic d) Derivat al sulfamidei e) Eter 181. M După structura chimică Indapamida este: 2 S l a) Acid carboxilic b) ompus heterociclic 3 si enantiomer 35
36 c) Aldehidă d) Derivat ai sulfamidei e) Ester 182. M După structura chimică Furosemida este: 2 S l a) Ester b) Acid carboxilic c) Aldehidă d) ompus heterociclic e) Derivat ai sulfamidei 183. M Derivaţi ai amidei acidului clorbenzensulfonic sunt: a) lorhidrat de amilorid b) Furosemid c) Indapamidă d) idroclortiazid (hipotiazida) e) Spironolacton 184. M Acţiune diuretică au: a) Metenamina (hexametilentetramina) b) lorhidratul de difenhidramină (dimedrol) c) Furosemid d) Sulfametoxazol e) idroclortiazid (hipotiazida) 185. СS Din remedii diuretice fac parte: a) Metenamina (exametilentetramina) b) lorhidrat de difenhidramina (lorhidrat de dimedrol) c) Furosemid d) Sulfadimetoxină e) Salbutamol 7-TS. Antidiabetice - IV 186. M Determinarea cantitativă a derivaţilor amidei acidului sulfanilic poate fi efectuată prin metodele: a) Argentometrică b) Bromatometrică c) Iodoclorimetrică d) itritometrică e) Spectrofotometrică 36
37 187. M Sarea de sodiu a preparatelor sulfanilamide poate fi determinată cantitativ prin metodele: a) itritometrică b) Spectrofotometrică c) omplexonometrică d) Acidimetrică e) Alcalimetrică 188. S Substanţele medicamentoase din grupa sulfanilamidelor nu se standardizează conform indicelui: a) Solubilitate b) Transparenţă şi coloraţie c) Aciditate şi bazicitate d) Puterea rotatorie specifică e) Metale grele 189. M Prezenţa amino-grupei aromatice primare în preparatele sulfanilamide condiţionazează reacţiile de: a) xidare b) Diazotare şi cuplare cu fenoli c) Bromurare d) Formare a sărurilor complexe e) Formare a tiocromului 190. M Metodele utilizate la determinarea cantitativă a preparatelor sulfanilamide sunt condiţionate de reacţiile de: a) eutralizare b) Diazotare c) Bromurare d) Formare a sărurilor e) ondensare 191. M Alterarea proprietăţilor fizice şi chimice a derivaţilor benzensulfanilamidelor la păstrare sunt condiţionate de: a) Lumină b) Umiditate c) xigenul aerului d) Azotul aerului e) De temperatura joaşă 192. M Sulfanilamidele se identifică prin metodele: a) Spectrofotometria în IR b) Refractometria c) RM d) Spectrofotometria în UV e) Fotocolorimetria 193. M Dozarea sulfanilamidelor se efectuează prin metodele: 37
38 a) Fotocolorimetrie b) Spectrofotometrie în IR c) PL d) Polarimetric e) Spectrofotometrie în UV 194. M Derivaţi ai benzensulfonilureei cu acţiunea antidiabetică sunt: a) Gliquidon b) Insulină c) Glibenclamida d) Metformin e) Furosemid 195. S Derivaţi ai biguanidei cu acţiunea antidiabetică sunt: a) Spironolacton b) Metformin c) Glibenclamida d) Furosemid e) Glipizid (minidiab) 196. S Antidiabetice de substituţie sunt: a) Furosemid b) idroclortiazida c) Metformin d) Glibenclamida e) Insulina 8 TS. Derivaţii bezopiranului IV 197. S Folosirea metodei cerimetrice, ca metoda de determinare cantitativă a tocoferolului acetat, este bazată pe proprietatea lui de a se: a) Reduce b) De a forma săruri c) ondensa d) xida e) De a forma compuşi complecşi 198. M ompuşi coloraţi cu hidroxidul de sodiu formează: a) Fenilbutazona (butadionul) b) Acidul benzoic c) itrofurantoin (furadonina) d) Rezorcina e) Rutozida (rutina) 199. S Denumirea chimică a neodicumarini este: 38
39 - 2 5 a) 3-α-fenil-β-propioniletil -4-oxicumarină b) Esterul etilic al di-(4-hidroxicumarinil-3) acidului acetic c) Di-(4-oxicumarinil-3) acid acetic d) 3-(α-para-nitrofenil-β-propionil-etil)-4-oxicumarină e) Eterul etilic al acidului p-aminobenzoic 200. M 1,4-benzopiranul constă din ciclurile: a) Benzenic b) Fenolic c) α-piranic d) γ-piranic e) Furanic 201. M După structura chimică etilbiscumacetatul (neodicumarina) este: a) Derivat heterociclic b) Ester c) Alcool d) Derivat lactonic e) Derivat lactamic 202. M Identificarea etilbiscumacetatului (neodicumarina), se efectuează cu ajutorul: a) Topirea cu hidrogenocarbonat de sodiu b) Soluţiei de clorură de fer (III) c) Reactivilor de precipitare ai alcaloizilor d) Determinarea temperaturii de topire a diacetatului e) Înregistrarea spectrului în UV 203. M La derivaţii benzopiranului se referă: a) Furosemidul b) lorhidratul de epinefrină (adrenalină) c) Acenocumarol d) Acetat de tocoferol e) Rutozida (rutina) 204. M Sistema heterociclică a 1,2-benzopiranului constă din: a) Furan b) Fenol c) Benzen 39
40 d) α-piran e) γ- Piran 205. S La derivaţii indandionei-1,3 se referă: a) Furosemid b) Fenindion (fenilin) c) Acid cromoglicic d) Tocoferol acetat e) Rutozida (rutina) 206. S După structură chimică la glicozid se referă: a) Amiodaron b) Fenindion (fenilin) c) Griseofulvin d) Tocoferol acetat e) Rutozida (rutina) 207. S Reacţia comună pentru etilbiscumacetat (neodicumarina) şi ampicilină este: S a) Proba hidroxamică b) u reactivi de precipitare a alcaloizilor c) Formarea colorantului indofenolic d) Proba murexidă e) Formarea de compuşi complecşi cu clorura de fer (III) 208. S Identificarea acenocumarolului după gruparea nitro- se poate de efectuat după reacţiile: a) Formarea colorantului aurinic b) Diazotare c) Formarea azocolorantului d) Formarea azocolorantului după reducere e) Formarea azocolorantului cu oxidarea în prealabil 209. M Metoda alcalimetrică în mediu de acetonă se aplică la dozarea: a) Etilbiscumacetatului (neodicumarina) b) Acenocumarol c) Tocoferol acetat d) Rutozida (rutina) e) Sulfacetamida sodică (sulfacil sodic) 40
41 210. S Reacţia comună caracteristică pentru rutozidă (rutină) şi troxerutină (troxevazină) este: a) Formarea sărurilor de oxoniu b) Reacţia cianinei c) Proba ninhidrinică d) Formarea sărurilor de diazoniu e) Formarea bazelor Şiff 211. M Dozarea acetatului de tocoferol se poate de efectuat prin metodele: a) erimetrică b) Titrarea în mediu abhidru c) PL d) GL e) Polarimetria 9 TS. Derivaţii pirolului şi indolului IV 212. S Formula de structura a Pirolulului este: a) b) c) d) e) 213. M Produşii de reducere a pirolului sunt: a) Pirolina b) Piperidina c) Pirolidin d) Pirolizidin e) Pirimidina 41
42 214. S Denumirea chimică a pirolidon-2-acetamidei corespunde cu: a) Rutozidă (rutină) b) Furosemid c) aptopril d) Acetatul de tocoferol e) Piracetam 215. M Identificarea piracetamului se efectuează prin reacţiile de: a) Degajare a amoniacului după încălzire cu hidroxid de sodiu b) Înregistrare a spectrului de absorbţie în IR c) Formare a azocoloranţilor d) Înregistrare a spectrului de absorbţie în UV e) Formare a hidroxamatului de fer 216. S Metoda de determinare cantitativă a piracetamului este: a) Titrarea anhidră b) Argentometrică c) Bromatometrică d) omplexonometrică e) Dozarea nitrogenului din combinaţiile organice (metoda Kjheldahl) 217. S Utilizarea metodei Kjeldahl pentru determinarea cantitativă a piracetamului este condiţionată de structura fragmentului din formula: 2-2 a) b) c) 2 d) 2 - e) M La derivaţii pirolidon-2 se referă: 42
43 a) Glibenclamida b) Polivinilpirolidona c) Piracetamul d) Etilbiscumacetat (neodicumarina) e) idrotartraetul de platifilină 219. S Derivaţi ai pirolului sunt vitaminele: a) Rutozid (rutină) b) Acidul ascorbic c) Acetatul de tocoferol d) ianocobalamina e) Filochinona 220. M ompuşi coloraţi sunt: a) ianocobalanima b) itrofural (furacilina) c) idroclortiazida (diclotiazida) d) Sulfadimetoxin e) Indometacină 221. S Identificarea şi determinarea cantitativă a cianocobalaminei se efectuează prin metoda: a) Refarctometrică b) Polarometrică c) romatografia cu schimb de ioni d) Spectrofotometria în UV e) Potenţiometrică 222. S Derivaţii pirolizidinei sunt: a) ianocobalamina b) Piracetamul c) Acetatul de tocoferol d) idrotartrat de platifilină e) lorhidrat de propanolol (anaprilina) 223. M idrotartratul de platifilină se determină cu ajutorul: a) Reactivului Mayer b) Soluţiei de clorură de potasiu c) Soluţiei de β-naftol d) Reacţiei hidroxamice e) De formare a azocoloranţilor 224. M ompuşi optic activi sunt: a) loramfenicolul (levomicetina). 43
44 b) lorhidratul de efedrină c) idrotartratul de platifilină d) lorhidratul de epinefrină (adrenalină) e) ianocobalamina 225. M Metodele posibile de determinare cantitativă a hidrotartratului de platifilină sunt: a) eutralizarea (alcalimetria) b) Titrarea anhidră în mediu de acid acetic glacial c) Titrarea anhidră în mediu de dimetilformamidă d) eutralizare (acidimetria) e) Fotocolorimetria 226. apitol: Pirolului si indol Punctajul: 10S Ester dublu este: a) aptopril b) Reserpina c) Metilsulfat de neostigmină d) Tocoferol acetat e) Piracetam 227. M În formula structurală a piracetamului se conţin următoarele grupele funcţionale: 2-2 a) Grupa aldehidă b) Inel lactonic c) Grupa amină terţiară d) Grupa carboxilă e) Grupa amidă 228. S Piracetamul posedă acţiunea farmacologică: a) Antihipertensivă b) Antivirală c) ootropă d) Diuretică e) Antiseptică 229. M Piracetamul se eliberează în formele medicamentoase: a) Сomprimate b) Сomprimate filmate c) apsule d) Aerozole e) Soluţii injectabile 230. S Sistemul corinic se găseşte în structura preparatului: 44
45 B A D a) ianocobalaminei b) Acidului cromoglicic (intal) c) Metforminei d) lorhidratului de ambroxol e) idrotartratului de platifilină 231. M În formula structurală a platifilinei se conţin următoarele grupele funcţionale: a) Grupa eter b) grupă esterică c) Grupa amină terţiară d) Grupa carbonilică e) Două grupe esterice 10 - TS. Derivaţii pirazolului IV 232. M Reacţie pozitivă cu clorura de fer (III) dau: a) itrofural (furacilina) b) Fenazona (antipirina) c) Acidul salicilic d) Metamizol sodic (analgina) e) Fenilbutazona (butadionă) 233. S Fenazona (antipirina) este derivat de: a) Pirazolinei b) Pirazolidinei c) Pirazolonei-5 d) Pirazolidonei 45
46 e) Pirazolidindionei-3, S Proprietăţile chimice şi farmacologice a derivaţilor pirazolonei sunt condiţionate de substituenţii din: a) Рoziţia - 1 b) Рoziţia - 2 c) Рoziţia - 3 d) Рoziţia - 4 e) Рoziţia S Fenazona (antipirina) în poziţia 4 conţine: a) Grupa carbonilică b) Grupa carboxilică c) idrogen d) Radical metilic e) Radical n-butilic 236. M Derivaţi de pirazol sunt: a) Metamizol sodic (analgină) b) Fenazona (antipirină) c) Piracetam (nootropil) d) Fenilbutazona (butadionă) e) Gliquidon (glurenom) 237. S Solubilitatea uşoară a fenazonei (antipirinei) în apă este condiţionată de formarea formelor: a) Iminice b) Enolice c) Metilenice d) Betainice e) etonice 238. S Denumirea chimică care corespunde fenazonei (antipirinei) este: a) 1,2-difenil-4-n-butilpirazolidin-dionă-3,5 b) 1-fenil-2,3-dimetil-4-metilaminopirazolon-5,-metilensulfoxid de sodiu c) 1-fenil-2,3-dimetil-4-dimetilaminopirazolon-5 d) 1-fenil-2,3-dimetil-pirazolon-5 e) 1-fenil-2,3-dimetil-4-izopropin.pirazolon-5 46
47 239. M Identitatea fenazonei (antipirinei) se determină prin reacţiile cu: a) Acidul azotic b) itritul de sodiu în mediu acid c) Sulfatul de cupru d) lorura de fier (III) e) Acidul picric 240. M Determinarea cantitativă a fenazonei (antipirină) se poate de efectuat prin metodele: a) eutralizare b) Argentometrică c) Bromatometrică d) Iodometrică e) Permanganatometrică 241. M Identificarea fenazonei (antipirina) se efectuează prin reacţiile de formare a: a) itrozo-derivaţilor b) Feripirinei c) olorantului aurinic d) Azocoloranţilor e) itro-derivaţilor 242. S La baza determinării cantitative prin metoda iodometrică a fenazonei (antipirinei) stă reacţia de: a) xidare b) Adiţie c) Reducere d) Substituţie e) Formare a sărurilor 243. M Pentru efectuarea determinării cantitative a fenazonei (antipirina) prin metoda iodometrică sunt necesari reactivii: a) Soluţie de iod 0,1 mol/l b) Soluţie tiosulfat de sodiu 0,1 mol/l c) loroform d) itrat de sodiu e) Soluţie de amidon 47
48 244. S Produsul comun la descompunerea hidrolitică a metamizolului sodic (analgină) şi metenaminei (hexametilentetraminei) este: a) Amoniacul b) Dioxidul de carbon c) Azot d) Dioxidul de sulf e) Formaldehida 245. S Pentru substanţele medicamentoase cu structura chimică reacţia comună este de formare a: a) Periodurii b) olorantului aurinic c) Brom-derivatului d) idroxamatului de fier (III) e) Azocoloranţului 246. M Fenazona (antipirina) se poate de determinat cu ajutorul reactivilor: a) Reinecat de amoniu b) lorură de fier (III) c) Tanină d) itritul de sodiu e) itratul de argint 247. S Proprietăţi reducătoare mai puternice posedă: a) Metamizol sodic (analgină) b) Fenazona (antipirină) c) Propifenazona d) Benzilpenicilina sodică e) Fenilbutazona (butadiona) 248. S Tipul reacţiei de interacţiune a substanţei medicamentoase cu soluţia de nitrit de sodiu 1% în mediu acid este de: 3 2 S 3 a a) Precipitare b) xidare c) Diazotare d) Formare de săruri e) Substituţie electrofilă 249. S La baza determinării cantitative a metamizolului sodic (analgină) prin metoda iodometrică stă reacţia: a) De formare a compuşilor complexi b) De substituţie electrofilă c) De oxidare S +4 pînă la S +6 48
49 d) De oxidare a formaldehidei e) De oxidare a ciclului pirazolic 250. S Masa molară a echivalentului pentru metamizol sodic (analgină) prin titrarea iodometrică este: a) 1 Mm metamizol sodic b) 1/2 Mm metamizol sodic c) 1/4 Mm metamizol sodic d) 2 Mm metamizol sodic e) 4 Mm metamizol sodic 251. M Derivaţii hidrogenaţi ai pirazolului sunt: a) Pirimidina b) Pirazolina Pirazolidina c) d) Pirazina e) Pirolul 252. M Săruri complexe cu sulfatul de cupru formează: a) Metamizol sodic (analgină) b) Acidul glutamic c) Acidul benzoic d) Ftalilsulfatiazolul (ftalazol) e) Fenilbutazona (butadiona) 253. M u soluţia de clorură de fier (III) nu se oxidează substanţele medicamentoase: a) Metamizol sodic (analgina) b) Fenilbutazona (butadiona) c) Acidul ascorbic d) Fenazona (antipirina) e) idrotartratul de platifilină 254. M Reacţia de hidroliză acidă se utilizează pentru determinarea identităţii 49
50 substanţelor: a) Acidul acetilsalicilic b) Rutozida (rutina) c) Metamizol sodic (analgina) d) Acidul ascorbic e) lorhidratul de norepinefrină 255. S Proprietăţile acide a fenilbutazonei (butadion) sunt determinate de: a) Gruparea carboxilă b) Gruparea carbonilică c) Gruparea amidă d) Tautomeria lactam-lactimică e) Tautomeria ceto-enolă 256. M După DA prin metoda iodometrică se determină preparatele: a) Izoniazida b) Metamizol-sodic (analgina) c) itrofural (furacilina) d) Iindometacină e) Acidul benzoic 257. M La reagenţii cu care putem diferenţa metamizolul sodic de fenazonă (antipirină) se referă: a) Soluţie de iod b) Soluţie de nitrat de argint c) Reactivul Dragendorff d) Soluţie de nitrat de sodiu în mediu acid e) Soluţie de iodat de potasiu 11 - TS. Derivaţii imidazolului IV 258. S Formula de structură a imidazolul este: a) b) S c) d) 50
Acizi carboxilici heterofuncționali.
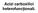 Acizi carboxilici heterofuncționali. 1. Acizi carboxilici halogenați. R R 2 l l R 2 R l Acizi α-halogenați Acizi β-halogenați l R 2 2 l Acizi γ-halogenați Metode de obținere. 1. alogenarea directă a acizilor
Acizi carboxilici heterofuncționali. 1. Acizi carboxilici halogenați. R R 2 l l R 2 R l Acizi α-halogenați Acizi β-halogenați l R 2 2 l Acizi γ-halogenați Metode de obținere. 1. alogenarea directă a acizilor
a. 0,1; 0,1; 0,1; b. 1, ; 5, ; 8, ; c. 4,87; 6,15; 8,04; d. 7; 7; 7; e. 9,74; 12,30;1 6,08.
 1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
REACŢII DE ADIŢIE NUCLEOFILĂ (AN-REACŢII) (ALDEHIDE ŞI CETONE)
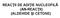 EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
Tema 5 (S N -REACŢII) REACŢII DE SUBSTITUŢIE NUCLEOFILĂ. ŞI DE ELIMINARE (E - REACŢII) LA ATOMULDE CARBON HIBRIDIZAT sp 3
 Tema 5 REACŢII DE SUBSTITUŢIE NUCLEOFILĂ (S N -REACŢII) ŞI DE ELIMINARE (E - REACŢII) LA ATOMULDE CARBON IBRIDIZAT sp 3 1. Reacții de substituție nucleofilă (SN reacții) Reacţiile de substituţie nucleofilă
Tema 5 REACŢII DE SUBSTITUŢIE NUCLEOFILĂ (S N -REACŢII) ŞI DE ELIMINARE (E - REACŢII) LA ATOMULDE CARBON IBRIDIZAT sp 3 1. Reacții de substituție nucleofilă (SN reacții) Reacţiile de substituţie nucleofilă
I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare.
 Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
T e m a PROPRIETĂŢILE ACIDE ŞI BAZICE ALE COMPUŞILOR ORGANICI.
 T e m a PROPRIETĂŢILE ACIDE ŞI BAZICE ALE COMPUŞILOR ORGANICI. Cele mai importante grupe funcţionale, care se întâlnesc în componenţa compuşilor naturali biologic activi sunt: -ОН, -SH, NH 2, -COH, -COOH
T e m a PROPRIETĂŢILE ACIDE ŞI BAZICE ALE COMPUŞILOR ORGANICI. Cele mai importante grupe funcţionale, care se întâlnesc în componenţa compuşilor naturali biologic activi sunt: -ОН, -SH, NH 2, -COH, -COOH
ANALIZE FIZICO-CHIMICE MATRICE APA. Tip analiza Tip proba Metoda de analiza/document de referinta/acreditare
 ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
5.1. Noţiuni introductive
 ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
Capitolul 4-COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ-
 Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Aplicaţii ale principiului I al termodinamicii la gazul ideal
 Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
Capitolul 1-INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme
 Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Testele (întrebările) oferă 3 (trei) răspunsuri diferite din care se alege un singur răspuns corect.
 Testele (întrebările) oferă 3 (trei) răspunsuri diferite din care se alege un singur răspuns corect. 1) Compușii care fac parte din clasa alchenelor sunt: a) Etan și propan; b) Acetilenă și benzen; c)
Testele (întrebările) oferă 3 (trei) răspunsuri diferite din care se alege un singur răspuns corect. 1) Compușii care fac parte din clasa alchenelor sunt: a) Etan și propan; b) Acetilenă și benzen; c)
ANALIZA SPECTROFOTOMETRICĂ CALITATIVĂ ŞI CANTITATIVĂ
 ANALIZA SPECTROFOTOMETRICĂ CALITATIVĂ ŞI CANTITATIVĂ Spectrometria de absorbţie moleculară are aplicaţii atât în analiza cantitativă cât şi în cea calitativă. Spectrometria de absorbţie moleculară efctuată
ANALIZA SPECTROFOTOMETRICĂ CALITATIVĂ ŞI CANTITATIVĂ Spectrometria de absorbţie moleculară are aplicaţii atât în analiza cantitativă cât şi în cea calitativă. Spectrometria de absorbţie moleculară efctuată
31. Aplicaţiile metodelor cromatografice în controlul medicamentelor
 31. Aplicaţiile metodelor cromatografice în controlul medicamentelor 31. 1. In funcţie de procesele care stau la baza separărilor cromatografice există următoarele metode: A. cromatografie de adsorbţie
31. Aplicaţiile metodelor cromatografice în controlul medicamentelor 31. 1. In funcţie de procesele care stau la baza separărilor cromatografice există următoarele metode: A. cromatografie de adsorbţie
Planul determinat de normală şi un punct Ecuaţia generală Plane paralele Unghi diedru Planul determinat de 3 puncte necoliniare
 1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
TESTE DE CHIMIE ORGANICĂ
 UNIVERSITATEA DE MEDICINA ŞI FARMACIE TÂRGU MUREŞ TESTE DE CHIMIE ORGANICĂ Pentru admiterea la Facultatea de Farmacie Specializarea ASISTENŢĂ DE FARMACIE 2013 Având în vedere că la elaborarea şi multiplicarea
UNIVERSITATEA DE MEDICINA ŞI FARMACIE TÂRGU MUREŞ TESTE DE CHIMIE ORGANICĂ Pentru admiterea la Facultatea de Farmacie Specializarea ASISTENŢĂ DE FARMACIE 2013 Având în vedere că la elaborarea şi multiplicarea
Capitolul 2-HIDROCARBURI-2.5.-ARENE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.5.ARENE Exerciţii şi probleme E.P.2.5. 1. Denumeşte conform IUPAC următoarele hidrocarburi aromatice mononucleare: Determină formula generală a hidrocarburilor aromatice mononucleare
Capitolul 2 - HIDROCARBURI 2.5.ARENE Exerciţii şi probleme E.P.2.5. 1. Denumeşte conform IUPAC următoarele hidrocarburi aromatice mononucleare: Determină formula generală a hidrocarburilor aromatice mononucleare
a. 11 % b. 12 % c. 13 % d. 14 %
 1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate.
 Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Reactia de amfoterizare a aluminiului
 Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
5.5. REZOLVAREA CIRCUITELOR CU TRANZISTOARE BIPOLARE
 5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
MARCAREA REZISTOARELOR
 1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
GRILE ORIENTATIVE PENTRU EXAMENUL DE LICENȚĂ FARMACIE 2014
 GRILE ORIENTATIVE PENTRU EXAMENUL DE LICENȚĂ FARMACIE 2014 1. [M] Grad de dificultate: scazut Punctajul: 5Selectaţi enunţul corect referitor la substanţele chimice de referinţă: a) [x] prezintă un înalt
GRILE ORIENTATIVE PENTRU EXAMENUL DE LICENȚĂ FARMACIE 2014 1. [M] Grad de dificultate: scazut Punctajul: 5Selectaţi enunţul corect referitor la substanţele chimice de referinţă: a) [x] prezintă un înalt
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM 1 electronica.geniu.ro
 Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Metode iterative pentru probleme neliniare - contractii
 Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Subiecte Clasa a VII-a
 lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
Sisteme diferenţiale liniare de ordinul 1
 1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
14. Se dă următorul compus:
 CLASA a XI-a 1. Care din următorii compuşi este un derivat halogenat vicinal: a) 1,2-dicloropropanul; b) 1,1-dicloropropanul; c) 1-bromopropanul; d) 2-bromo-2-metilpropanul; e) 1,3,5-tricloropropanul.
CLASA a XI-a 1. Care din următorii compuşi este un derivat halogenat vicinal: a) 1,2-dicloropropanul; b) 1,1-dicloropropanul; c) 1-bromopropanul; d) 2-bromo-2-metilpropanul; e) 1,3,5-tricloropropanul.
DETERMINAREA INDICATORILOR DE CALITATE PENTRU CARACTERIZAREA APELOR DE SUPRAFAŢĂ. CARACTERISTICI CHIMICE
 DETERMINAREA INDICATORILOR DE CALITATE PENTRU CARACTERIZAREA APELOR DE SUPRAFAŢĂ. CARACTERISTICI CHIMICE Conform legislaţiei naţionale şi internaţionale indicatorii chimici se impart în: Indicatori generali:
DETERMINAREA INDICATORILOR DE CALITATE PENTRU CARACTERIZAREA APELOR DE SUPRAFAŢĂ. CARACTERISTICI CHIMICE Conform legislaţiei naţionale şi internaţionale indicatorii chimici se impart în: Indicatori generali:
II. 5. Probleme. 20 c 100 c = 10,52 % Câte grame sodă caustică se găsesc în 300 g soluţie de concentraţie 10%? Rezolvare m g.
 II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
NANOCOMPOSITES BASED ON MAGNETITE NANOPARTICLES FOR BIO-APPLICATIONS NANOCOMPOZITE PE BAZA DE NANOPARTICULE DE MAGNETITA PENTRU BIO-APLICATII
 A 8-a ediţie a Seminarului Naţional de Nanoştiinţă şi Nanotehnologie Academia Română, 27 aprilie 2009 NANOCOMPOSITES BASED ON MAGNETITE NANOPARTICLES FOR BIO-APPLICATIONS NANOCOMPOZITE PE BAZA DE NANOPARTICULE
A 8-a ediţie a Seminarului Naţional de Nanoştiinţă şi Nanotehnologie Academia Română, 27 aprilie 2009 NANOCOMPOSITES BASED ON MAGNETITE NANOPARTICLES FOR BIO-APPLICATIONS NANOCOMPOZITE PE BAZA DE NANOPARTICULE
ITEMI MODEL PENTRU UNITATEA DE ÎNVĂŢARE: Alcooli
 LIEUL TEORETI GRIGORE ANTIPA BOTOŞANI - ITEMI MODEL PENTRU UNITATEA DE ÎNVĂŢARE: Alcooli Subiectul A: Indicaţi care dintre afirmaţiile de mai jos sunt adevărate şi care sunt false, completând cu litera
LIEUL TEORETI GRIGORE ANTIPA BOTOŞANI - ITEMI MODEL PENTRU UNITATEA DE ÎNVĂŢARE: Alcooli Subiectul A: Indicaţi care dintre afirmaţiile de mai jos sunt adevărate şi care sunt false, completând cu litera
Clasa a VII-a. Noțiuni teoretice așteptate să fie cunoscute de către concurenți. Noțiuni teoretice studiate conform curriculum
 Clasa a VII-a Proprietăţile fizice, chimice şi fiziologice ale substanţelor. Fenomene fizice şi chimice în jurul nostru. Reacţie chimică. Semnele reacţiilor chimice. Atomul. Molecula. Substanţe simple
Clasa a VII-a Proprietăţile fizice, chimice şi fiziologice ale substanţelor. Fenomene fizice şi chimice în jurul nostru. Reacţie chimică. Semnele reacţiilor chimice. Atomul. Molecula. Substanţe simple
Capitolul 2-HIDROCARBURI-2.3.-ALCHINE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
Universitatea de Stat de Medicină și Farmacie Nicolae Testemițanu
 Universitatea de Stat de Medicină și Farmacie Nicolae Testemițanu Programul analitic pentru examenul de admitere. Chimie Introducere Cunoștințele în chimie sunt necesare pentru a înțelege concepțiile bazice
Universitatea de Stat de Medicină și Farmacie Nicolae Testemițanu Programul analitic pentru examenul de admitere. Chimie Introducere Cunoștințele în chimie sunt necesare pentru a înțelege concepțiile bazice
CURS XI II.3. AMINE 1. II.3.1. Clasificarea si nomenclatura 1. II.3.2. Structura de baza 2
 CURS XI II.3. AMIE 1 II.3.1. Clasificarea si nomenclatura 1 II.3.2. Structura de baza 2 II.3.3. Metode de obtinere a aminelor 2 II.3.3.1. Aminarea compusilor halogenati 2 II.3.3.1.1. Amine alifatice 2
CURS XI II.3. AMIE 1 II.3.1. Clasificarea si nomenclatura 1 II.3.2. Structura de baza 2 II.3.3. Metode de obtinere a aminelor 2 II.3.3.1. Aminarea compusilor halogenati 2 II.3.3.1.1. Amine alifatice 2
CATIONI Grupa I. Pb II : -reacția cu reactivul de grupă (dizolvarea în apă, la cald) -reacția cu iodurile alcaline (dizolvarea în apă, la cald)
 CATIONI Grupa I Ag I : -reacția cu reactivul de grupă (dizolvarea în NH 3 ) -reacția cu halogenurile alcaline (dizolvarea în NH 3 ) -reacția cu S II- -reacția cu ditizona -(se completează pe parcurs cu
CATIONI Grupa I Ag I : -reacția cu reactivul de grupă (dizolvarea în NH 3 ) -reacția cu halogenurile alcaline (dizolvarea în NH 3 ) -reacția cu S II- -reacția cu ditizona -(se completează pe parcurs cu
LUCRARI PRACTICE CHIMIE ORGANICĂ
 LUAI PATIE IMIE GANIĂ 1 Programare şedinţe lucrări practice IMIE GANIĂ 1. Protecţia muncii şi prezentarea laboratorului Analiza elementară calitativă organică 2. eacţii de identificarea elementelor carbon,
LUAI PATIE IMIE GANIĂ 1 Programare şedinţe lucrări practice IMIE GANIĂ 1. Protecţia muncii şi prezentarea laboratorului Analiza elementară calitativă organică 2. eacţii de identificarea elementelor carbon,
ECHILIBRE ACIDO BAZICE - 1
 ECHILIBRE ACIDO-BAZICE 1 DISOCIEREA APEI 2 H 2 O H 3 O + + OH - H 3 O + H + PRODUS IONIC AL APEI: + c P H K = [ H ] [ OH ] = 2 O P H O = 2 = 10 14 M 2 (25 o C ) ÎN APA PURĂ + [ H ] = [ OH ] = PH 2 O =
ECHILIBRE ACIDO-BAZICE 1 DISOCIEREA APEI 2 H 2 O H 3 O + + OH - H 3 O + H + PRODUS IONIC AL APEI: + c P H K = [ H ] [ OH ] = 2 O P H O = 2 = 10 14 M 2 (25 o C ) ÎN APA PURĂ + [ H ] = [ OH ] = PH 2 O =
SYLLABUS ichemist, EDIȚIA A IV-A
 Clasa a VIII-a Proprietăţile fizice, chimice şi fiziologice ale substanţelor. Fenomene fizice şi chimice în jurul nostru. Reacţie chimică. Semnele reacţiilor chimice. Atomul. Molecula. Substanţe simple
Clasa a VIII-a Proprietăţile fizice, chimice şi fiziologice ale substanţelor. Fenomene fizice şi chimice în jurul nostru. Reacţie chimică. Semnele reacţiilor chimice. Atomul. Molecula. Substanţe simple
V O. = v I v stabilizator
 Stabilizatoare de tensiune continuă Un stabilizator de tensiune este un circuit electronic care păstrează (aproape) constantă tensiunea de ieșire la variaţia între anumite limite a tensiunii de intrare,
Stabilizatoare de tensiune continuă Un stabilizator de tensiune este un circuit electronic care păstrează (aproape) constantă tensiunea de ieșire la variaţia între anumite limite a tensiunii de intrare,
TEST VI CHIMIE ORGANICA
 TEST VI CHIMIE ORGANICA 1. AlegeŃi afirmańia adevărată: A. prin analiza elementală calitativă nu se pot determina elementele prezente într-un compus organic B. în compuşii organici sunt preponderente legăturile
TEST VI CHIMIE ORGANICA 1. AlegeŃi afirmańia adevărată: A. prin analiza elementală calitativă nu se pot determina elementele prezente într-un compus organic B. în compuşii organici sunt preponderente legăturile
II.5. COMPUSI CARBOXILICI SI DERIVATI FUNCTIONALI AI ACESTORA 8
 URS XIII II..6. ompusi carbonilici nesaturati 1 II..6.1. Definitie. lasificare 1 II..6.. etene 1 II..6..1. Sinteze 1 II..6... Reactivitatea generala II..6.. Reactivitatea compusilor carbonilici α,β-nesaturati
URS XIII II..6. ompusi carbonilici nesaturati 1 II..6.1. Definitie. lasificare 1 II..6.. etene 1 II..6..1. Sinteze 1 II..6... Reactivitatea generala II..6.. Reactivitatea compusilor carbonilici α,β-nesaturati
Seminariile Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reziduurilor
 Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Curs 1 Şiruri de numere reale
 Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Valori limită privind SO2, NOx şi emisiile de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili
 Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
CHIMIE ORGANICĂ NUTRIȚIE ȘI DIETETICĂ TEHNICĂ DENTARĂ VARIANTA A
 CHIMIE ORGANICĂ NUTRIȚIE ȘI DIETETICĂ TEHNICĂ DENTARĂ VARIANTA A 1. Alegeți afirmația corectă : A. pirogalolul este un fenol ce conține două grupări OH B. fenolii au caracter acid mai pronunțat decât alcolii
CHIMIE ORGANICĂ NUTRIȚIE ȘI DIETETICĂ TEHNICĂ DENTARĂ VARIANTA A 1. Alegeți afirmația corectă : A. pirogalolul este un fenol ce conține două grupări OH B. fenolii au caracter acid mai pronunțat decât alcolii
Metode optice de analiza instrumentala. Cursul 11
 Metode optice de analiza instrumentala Cursul 11 1 OBIECTIVE Prezentarea tipurilor de metode optice Principiile fundamentale ale metodelor optice Spectroscopia moleculara UV VIS Principii generale Variante
Metode optice de analiza instrumentala Cursul 11 1 OBIECTIVE Prezentarea tipurilor de metode optice Principiile fundamentale ale metodelor optice Spectroscopia moleculara UV VIS Principii generale Variante
Cuprins. Hidrocarburi... 1
 Cuprins Hidrocarburi... 1 Alcani (Parafine)... 1 Definiţie... 1 Formula generală... 1 Denumirea... 2 Denumirea radicalilor... 3 Denumirea alcanilor cu catenă ramificată... 3 Izomeria alcanilor... 4 Metode
Cuprins Hidrocarburi... 1 Alcani (Parafine)... 1 Definiţie... 1 Formula generală... 1 Denumirea... 2 Denumirea radicalilor... 3 Denumirea alcanilor cu catenă ramificată... 3 Izomeria alcanilor... 4 Metode
Integrala nedefinită (primitive)
 nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
Mase atomice C 12, H 1, O 16, S 32, Cl 35,5, Na 23, Cu 64,
 Mase atomice C 12, H 1, O 16, S 32, Cl 35,5, Na 23, Cu 64, Intrebari cu 1 raspuns corect: 1. Caracterul electronegativ reprezintă: a. tendinţa atomilor de a ceda electroni şi de a forma ioni pozitivi b.
Mase atomice C 12, H 1, O 16, S 32, Cl 35,5, Na 23, Cu 64, Intrebari cu 1 raspuns corect: 1. Caracterul electronegativ reprezintă: a. tendinţa atomilor de a ceda electroni şi de a forma ioni pozitivi b.
ASISTENȚĂ MEDICALĂ GENERALĂ Chimie Organică Varianta A
 ASISTENȚĂ MEDICALĂ GENERALĂ Chimie Organică Varianta A 1. Alegeți afirmația corectă : A. pirogalolul este un fenol ce contine doua grupari OH B. fenolii au caracter acid mai pronuntat decat alcolii C.
ASISTENȚĂ MEDICALĂ GENERALĂ Chimie Organică Varianta A 1. Alegeți afirmația corectă : A. pirogalolul este un fenol ce contine doua grupari OH B. fenolii au caracter acid mai pronuntat decat alcolii C.
Curs 4 Serii de numere reale
 Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
STUDIUL PROCESULUI DE CARAMELIZARE
 Aditivi alimentari Lucrarea practică nr.3. STUDIUL PROCESULUI DE CARAMELIZARE Scopul lucrării: Determinarea particularităţilor procesului de caramelizare a carbohidraţilor din compoziţia produselor alimente.
Aditivi alimentari Lucrarea practică nr.3. STUDIUL PROCESULUI DE CARAMELIZARE Scopul lucrării: Determinarea particularităţilor procesului de caramelizare a carbohidraţilor din compoziţia produselor alimente.
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE
 DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
R R, f ( x) = x 7x+ 6. Determinați distanța dintre punctele de. B=, unde x și y sunt numere reale.
 5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
Universitatea Dunărea de Jos din Galaţi MODELE DE TESTE GRILĂ PENTRU ADMITEREA 2018 DISCIPLINA: CHIMIE ORGANICĂ
 Universitatea Dunărea de Jos din Galaţi MODELE DE TESTE GRILĂ PENTRU ADMITEREA 2018 DISCIPLINA: CHIMIE ORGANICĂ ACESTE MODELE DE TESTE SUNT RECOMANDATE PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE
Universitatea Dunărea de Jos din Galaţi MODELE DE TESTE GRILĂ PENTRU ADMITEREA 2018 DISCIPLINA: CHIMIE ORGANICĂ ACESTE MODELE DE TESTE SUNT RECOMANDATE PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE
Capitolul 2-HIDROCARBURI-2.2.-ALCHENE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.2.ALCHENE Exerciţii şi probleme E.P.2.2.1. Denumeşte conform IUPAC următoarele alchene: A CH 3 CH 3 CH 2 C 3 C 4 H C 5 CH 3 C 2 H CH 3 C 6 H 2 C 1 H 3 C 7 H 3 3-etil-4,5,5-trimetil-2-heptenă
Capitolul 2 - HIDROCARBURI 2.2.ALCHENE Exerciţii şi probleme E.P.2.2.1. Denumeşte conform IUPAC următoarele alchene: A CH 3 CH 3 CH 2 C 3 C 4 H C 5 CH 3 C 2 H CH 3 C 6 H 2 C 1 H 3 C 7 H 3 3-etil-4,5,5-trimetil-2-heptenă
Cuprins Hidrocarburi
 Cuprins Hidrocarburi... 1 22 Alcani (Parafine)... 1 7 Definiţie...1 Formula generală...1 Denumirea...1 Denumirea radicalilor...3 Denumirea alcanilor cu catenă ramificată...3 Izomeria alcanilor...4 Metode
Cuprins Hidrocarburi... 1 22 Alcani (Parafine)... 1 7 Definiţie...1 Formula generală...1 Denumirea...1 Denumirea radicalilor...3 Denumirea alcanilor cu catenă ramificată...3 Izomeria alcanilor...4 Metode
Curs 14 Funcţii implicite. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi"
 Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
Universitatea Dunărea de Jos din Galaţi MODELE DE TESTE GRILĂ PENTRU ADMITEREA 2013 DISCIPLINA: CHIMIE ORGANICĂ. Clasa a X-a și a XI-a
 Universitatea Dunărea de Jos din Galaţi MODELE DE TESTE GRILĂ PENTRU ADMITEREA 2013 DISCIPLINA: CHIMIE ORGANICĂ Clasa a X-a și a XI-a ACESTE MODELE DE TESTE SUNT RECOMANDATE PENTRU CANDIDAȚII CARE VOR
Universitatea Dunărea de Jos din Galaţi MODELE DE TESTE GRILĂ PENTRU ADMITEREA 2013 DISCIPLINA: CHIMIE ORGANICĂ Clasa a X-a și a XI-a ACESTE MODELE DE TESTE SUNT RECOMANDATE PENTRU CANDIDAȚII CARE VOR
CAP. 4. ALCHENE 10. Despre adiţia apei la alchene nesimetrice sunt adevărate afirmaţiile: 1. Referitor la alchene sunt adevărate afirmaţiile:
 CAP. 4. ALCHENE 1. Referitor la alchene sunt adevărate afirmaţiile: A. se mai numesc şi parafine B. se mai numesc şi olefine C. au formula generală C nh 2n D. se mai numesc şi acetilene E. au structură
CAP. 4. ALCHENE 1. Referitor la alchene sunt adevărate afirmaţiile: A. se mai numesc şi parafine B. se mai numesc şi olefine C. au formula generală C nh 2n D. se mai numesc şi acetilene E. au structură
Curs 2 DIODE. CIRCUITE DR
 Curs 2 OE. CRCUTE R E CUPRN tructură. imbol Relația curent-tensiune Regimuri de funcționare Punct static de funcționare Parametrii diodei Modelul cu cădere de tensiune constantă Analiza circuitelor cu
Curs 2 OE. CRCUTE R E CUPRN tructură. imbol Relația curent-tensiune Regimuri de funcționare Punct static de funcționare Parametrii diodei Modelul cu cădere de tensiune constantă Analiza circuitelor cu
CHIMIE ORGANICĂ CLASA a XII-a
 CHIMIE ORGANICĂ CLASA a XII-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea
CHIMIE ORGANICĂ CLASA a XII-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea
Bazele Chimiei Organice
 Bazele Chimiei Organice An universitar 2016-2017 Lector dr. Adriana Urdă Partea a 8a Alți compuși organici: nomenclatură, structură, reacții caracteristice Obiectivele cursului: În această partea a cursului
Bazele Chimiei Organice An universitar 2016-2017 Lector dr. Adriana Urdă Partea a 8a Alți compuși organici: nomenclatură, structură, reacții caracteristice Obiectivele cursului: În această partea a cursului
Bazele Chimiei Organice
 Bazele Chimiei Organice An universitar 2017-2018 Lector dr. Adriana Urdă Partea 1. Scurt istoric; definiții; principii de bază în purificarea și investigarea compușilor organici. Obiectivele acestei părți:
Bazele Chimiei Organice An universitar 2017-2018 Lector dr. Adriana Urdă Partea 1. Scurt istoric; definiții; principii de bază în purificarea și investigarea compușilor organici. Obiectivele acestei părți:
TEBEL SINOPTIC CU REPARTIŢIA TESTELOR GRILĂ DE CHIMIE ORGANICĂ PENTRU EXAMENUL DE ADMITERE, SESIUNEA IULIE 2011 SPECIALIZAREA FARMACIE
 TEBEL SINOPTIC CU REPARTIŢIA TESTELOR GRILĂ DE CHIMIE ORGANICĂ PENTRU EXAMENUL DE ADMITERE, SESIUNEA IULIE 2011 SPECIALIZAREA FARMACIE TEMATICA AUTORI DE CARTE CHIMIE Manual pentru clasa a 10 a Luminiţa
TEBEL SINOPTIC CU REPARTIŢIA TESTELOR GRILĂ DE CHIMIE ORGANICĂ PENTRU EXAMENUL DE ADMITERE, SESIUNEA IULIE 2011 SPECIALIZAREA FARMACIE TEMATICA AUTORI DE CARTE CHIMIE Manual pentru clasa a 10 a Luminiţa
Componente şi Circuite Electronice Pasive. Laborator 3. Divizorul de tensiune. Divizorul de curent
 Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Capitolul 4-COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ-
 Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. TEST 4.1.2. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare
Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. TEST 4.1.2. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare
Metode de interpolare bazate pe diferenţe divizate
 Metode de interpolare bazate pe diferenţe divizate Radu Trîmbiţaş 4 octombrie 2005 1 Forma Newton a polinomului de interpolare Lagrange Algoritmul nostru se bazează pe forma Newton a polinomului de interpolare
Metode de interpolare bazate pe diferenţe divizate Radu Trîmbiţaş 4 octombrie 2005 1 Forma Newton a polinomului de interpolare Lagrange Algoritmul nostru se bazează pe forma Newton a polinomului de interpolare
V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile
 Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Unitatea atomică de masă (u.a.m.) = a 12-a parte din masa izotopului de carbon
 ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
CURSUL 3 ECHILIBRE DE DIZOLVARE
 CURSUL 3 ECHILIBRE DE DIZOLVARE Soluţii: ţ definiţie, ţ compoziţie, ţ exemple Soluţia mediu dispersant (solvent) fază dispersată (solut, solvit) Importanţa soluţiilor: olocul de desfăşurare a majorităţii
CURSUL 3 ECHILIBRE DE DIZOLVARE Soluţii: ţ definiţie, ţ compoziţie, ţ exemple Soluţia mediu dispersant (solvent) fază dispersată (solut, solvit) Importanţa soluţiilor: olocul de desfăşurare a majorităţii
CLASIFICAREA REACŢIILOR CHIMICE
 CLASIFICAREA REACŢIILOR CHIMICE 1. Reacţii de combinare Reacţia de combinare este reacţia chimică ce are loc între două sau mai multe substanţe chimice, simple sau compuse, cu obţinerea unei singure substanţe
CLASIFICAREA REACŢIILOR CHIMICE 1. Reacţii de combinare Reacţia de combinare este reacţia chimică ce are loc între două sau mai multe substanţe chimice, simple sau compuse, cu obţinerea unei singure substanţe
Studiu privind soluţii de climatizare eficiente energetic
 Studiu privind soluţii de climatizare eficiente energetic Varianta iniţială O schemă constructivă posibilă, a unei centrale de tratare a aerului, este prezentată în figura alăturată. Baterie încălzire/răcire
Studiu privind soluţii de climatizare eficiente energetic Varianta iniţială O schemă constructivă posibilă, a unei centrale de tratare a aerului, este prezentată în figura alăturată. Baterie încălzire/răcire
Proprietăţile pulberilor metalice
 3 Proprietăţile pulberilor metalice Pulberea reprezintă principala componentă din materia primă folosită la elaborarea pieselor prin tehnologia M.P. (alături de aditivi, lubrefianţi, etc.) Pulberea se
3 Proprietăţile pulberilor metalice Pulberea reprezintă principala componentă din materia primă folosită la elaborarea pieselor prin tehnologia M.P. (alături de aditivi, lubrefianţi, etc.) Pulberea se
Seria Balmer. Determinarea constantei lui Rydberg
 Seria Balmer. Determinarea constantei lui Rydberg Obiectivele lucrarii analiza spectrului in vizibil emis de atomii de hidrogen si determinarea lungimii de unda a liniilor serie Balmer; determinarea constantei
Seria Balmer. Determinarea constantei lui Rydberg Obiectivele lucrarii analiza spectrului in vizibil emis de atomii de hidrogen si determinarea lungimii de unda a liniilor serie Balmer; determinarea constantei
Subiecte Clasa a VIII-a
 Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
FARMACIE CHIMIE ORGANICĂ 2016, SIMULARE. La întrebările de mai jos 1-18 alegeți un singur răspuns corect
 FARMACIE CHIMIE ORGANICĂ 2016, SIMULARE La întrebările de mai jos 1-18 alegeți un singur răspuns corect 1. Referitor la valină sunt adevărate afirmaţiile, cu excepţia: A. prezintă activitate optică B.
FARMACIE CHIMIE ORGANICĂ 2016, SIMULARE La întrebările de mai jos 1-18 alegeți un singur răspuns corect 1. Referitor la valină sunt adevărate afirmaţiile, cu excepţia: A. prezintă activitate optică B.
III. Serii absolut convergente. Serii semiconvergente. ii) semiconvergentă dacă este convergentă iar seria modulelor divergentă.
 III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
LICEUL TEORETIC TRAIAN CONSTANŢA CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM
 LICEUL TEORETIC TRAIAN CONSTANŢA CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 Clasa a XI-a Varianta 2 La întrebările de la 1-30, alege un singur răspuns: 1.Câți enantiomeri prezintă 4,5 dimetil
LICEUL TEORETIC TRAIAN CONSTANŢA CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 Clasa a XI-a Varianta 2 La întrebările de la 1-30, alege un singur răspuns: 1.Câți enantiomeri prezintă 4,5 dimetil
ŞTIINŢA ŞI INGINERIA. conf.dr.ing. Liana Balteş curs 7
 ŞTIINŢA ŞI INGINERIA MATERIALELOR conf.dr.ing. Liana Balteş baltes@unitbv.ro curs 7 DIAGRAMA Fe-Fe 3 C Utilizarea oţelului în rândul majorităţii aplicaţiilor a determinat studiul intens al sistemului metalic
ŞTIINŢA ŞI INGINERIA MATERIALELOR conf.dr.ing. Liana Balteş baltes@unitbv.ro curs 7 DIAGRAMA Fe-Fe 3 C Utilizarea oţelului în rândul majorităţii aplicaţiilor a determinat studiul intens al sistemului metalic
Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II)
 Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II) Varianta 9 Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL
Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II) Varianta 9 Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL
Liceul de Ştiinţe ale Naturii Grigore Antipa Botoşani
 Fişă de lucru RANDAMENT. CONVERSIE UTILĂ. CONVERSIE TOTALĂ 1. Randament A. Hidrocarburile alifatice pot fi utilizate drept combustibili, sau pot fi transformate în compuşi cu aplicaţii practice. 1. Scrieţi
Fişă de lucru RANDAMENT. CONVERSIE UTILĂ. CONVERSIE TOTALĂ 1. Randament A. Hidrocarburile alifatice pot fi utilizate drept combustibili, sau pot fi transformate în compuşi cu aplicaţii practice. 1. Scrieţi
STUDIUL COMPARATIV AL CURBELOR DE TITRARE A UNOR ACIZI
 REACŢIA CHIMICĂ STUDIUL COMPARATIV AL CURBELOR DE TITRARE A UNOR ACIZI Reacţia de titrare a unui acid tare respectiv a unui acid slab (notat în general HA) cu o bază tare se reprezintă prin echilibrul:
REACŢIA CHIMICĂ STUDIUL COMPARATIV AL CURBELOR DE TITRARE A UNOR ACIZI Reacţia de titrare a unui acid tare respectiv a unui acid slab (notat în general HA) cu o bază tare se reprezintă prin echilibrul:
Subiectul III (30 puncte) Varianta 001
 Subiectul III (30 puncte) Varianta 001 Proteinele şi zaharidele sunt compuşi organici cu acţiune biologică. 1. Scrieţi formula de structură pentru o tripeptidă P care conţine glicină, valină şi serină
Subiectul III (30 puncte) Varianta 001 Proteinele şi zaharidele sunt compuşi organici cu acţiune biologică. 1. Scrieţi formula de structură pentru o tripeptidă P care conţine glicină, valină şi serină
Ecuaţia generală Probleme de tangenţă Sfera prin 4 puncte necoplanare. Elipsoidul Hiperboloizi Paraboloizi Conul Cilindrul. 1 Sfera.
 pe ecuaţii generale 1 Sfera Ecuaţia generală Probleme de tangenţă 2 pe ecuaţii generale Sfera pe ecuaţii generale Ecuaţia generală Probleme de tangenţă Numim sferă locul geometric al punctelor din spaţiu
pe ecuaţii generale 1 Sfera Ecuaţia generală Probleme de tangenţă 2 pe ecuaţii generale Sfera pe ecuaţii generale Ecuaţia generală Probleme de tangenţă Numim sferă locul geometric al punctelor din spaţiu
CHIMIE. Asistență Medicală Generală. Varianta A
 CHIMIE Asistență Medicală Generală Varianta A 1. Un alcool primar se poate obține prin: 1. hidroliza oleatului de etil 2. hidroliza clorurii de benzoil 3. hidroliza clorurii de metilen 4. hidroliza clorurii
CHIMIE Asistență Medicală Generală Varianta A 1. Un alcool primar se poate obține prin: 1. hidroliza oleatului de etil 2. hidroliza clorurii de benzoil 3. hidroliza clorurii de metilen 4. hidroliza clorurii
CAP. 16. ZAHARIDE COOH + C 6 H 5 CH OH. CH 3 COCl. Y + HCl
 + C 2 5 X + 2 O C 6 5 C CO + C 3 COCl Y + Cl Alegeţi răspunsurile corecte: A. compusul X este acetat de fenil B. compusul X este 2-fenil-2-hidroxiacetat de etil C. compusul Y este acid 1-acetil-1-fenilsalicilic
+ C 2 5 X + 2 O C 6 5 C CO + C 3 COCl Y + Cl Alegeţi răspunsurile corecte: A. compusul X este acetat de fenil B. compusul X este 2-fenil-2-hidroxiacetat de etil C. compusul Y este acid 1-acetil-1-fenilsalicilic
Metode de caracterizare structurala in stiinta nanomaterialelor: aplicatii practice
 Metode de caracterizare structurala in stiinta nanomaterialelor: aplicatii practice Utilizare de metode complementare de investigare structurala Proba investigata: SrTiO 3 sub forma de pulbere nanostructurata
Metode de caracterizare structurala in stiinta nanomaterialelor: aplicatii practice Utilizare de metode complementare de investigare structurala Proba investigata: SrTiO 3 sub forma de pulbere nanostructurata
CULEGERE DE PROBLEME pentru Concursul de Chimie Organică din cadrul Facultății de Chimie Industrială și Ingineria Mediului UNIVERSITATEA POLITEHNICA
 Sabina-Violeta NIȚU Sorina RAN CULGR PRLM pentru Concursul de Chimie rganică din cadrul Facultății de Chimie Industrială și Ingineria Mediului UNIVRSITATA PLITHNICA TIMIȘARA Timișoara 2014 1 CUPRINS I.
Sabina-Violeta NIȚU Sorina RAN CULGR PRLM pentru Concursul de Chimie rganică din cadrul Facultății de Chimie Industrială și Ingineria Mediului UNIVRSITATA PLITHNICA TIMIȘARA Timișoara 2014 1 CUPRINS I.
1. PROPRIETĂȚILE FLUIDELOR
 1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
Subiectul II (30 puncte) Varianta 001
 Subiectul II (30 puncte) Varianta 001 Compuşii cloruraţi obţinuţi din hidrocarburile alifatice au importante aplicaţii practice. 1. Scrieţi ecuaţiile reacţiilor chimice, prin care se obţin din metan: monoclorometan,
Subiectul II (30 puncte) Varianta 001 Compuşii cloruraţi obţinuţi din hidrocarburile alifatice au importante aplicaţii practice. 1. Scrieţi ecuaţiile reacţiilor chimice, prin care se obţin din metan: monoclorometan,
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ
 Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii transversale, scrisă faţă de una dintre axele de inerţie principale:,
 REZISTENTA MATERIALELOR 1. Ce este modulul de rezistenţă? Exemplificaţi pentru o secţiune dreptunghiulară, respectiv dublu T. RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii
REZISTENTA MATERIALELOR 1. Ce este modulul de rezistenţă? Exemplificaţi pentru o secţiune dreptunghiulară, respectiv dublu T. RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii
