Capitolul 2-HIDROCARBURI-2.5.-ARENE Exerciţii şi probleme
|
|
|
- Ὀρέστης Διαμαντόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 Capitolul 2 - HIDROCARBURI 2.5.ARENE Exerciţii şi probleme E.P Denumeşte conform IUPAC următoarele hidrocarburi aromatice mononucleare: Determină formula generală a hidrocarburilor aromatice mononucleare cu catenă laterală saturată. Formula generală a alcanilor este C n H 2n+2. Hidrocarburile aromatice mononucleare au un ciclu şi 3 legături duble. La apariţia unui ciclu dispar 2 atomi de hidrogen. De asemenea la apariţia unei duble legături. Deci la apariţia unui ciclu şi a trei legături duble vor dispărea 8 atomi de hidrogen = 8 1
2 Formula generală a hidrocarburilor aromatice mononucleare cu catenă laterală saturată devine: C n H 2n+2-8 adică C n H 2n-6 E.P Scrie formulele de structură şi formulele moleculare ale următoarelor hidrocarburi aromatice: Rezolvare : a) 1,2-dietilbenzen; b) izopropilbenzen; c) 1,3,5,-trimetilbenzen; d) orto-etiltoluen; e) meta-dietilbenzen. Determinarea formulelor moleculare Formula generală C n H 2n-6 a) 1,2-dietilbenzen are = 10 atomi de carbon C 10 H 14 b) izopropilbenzen are = 9 atomi de carbon C 9 H 12 c) 1,3,5,-trimetilbenzen are = 9 atomi de carbon C 9 H 12 d) orto-etiltoluen are = 9 atomi de carbon C 9 H 12 e) meta-dietilbenzen are = 10 atomi de carbon C 10 H 14 unde: metil -CH 3 are 1 atom de carbon; etil CH 2 -CH 3 are 2 atomi de carbon izopropil H 3 C C*H CH 3 are 3 atomi de carbon toluenul este metilbenzen C 6 H 5 -CH 3 are = 7 atomi de carbon benzenul C 6 H 6 are 6 atomi de carbon Formulele de structură sunt: 2
3 E.P O hidrocarbură aromatică, A, mononucleară, disubstituită se arde. Ştiind că hidrocarbura A are catena laterală de tipul C n H 2n+1 şi că prin arderea a 0,05 kmoli hidrocarbură se degajă 10,08 m 3 CO 2, se cere: a) determină formula moleculară a hidrocarburii aromatice A. b) scrie formula de structură a izomerului hidrocarburii A care prin monoclorurare catalitică formează un singur compus. 3
4 Rezolvare a: 0,05 kmoli 10,08 m 3 C n H 2n-6 + 3(n-1)O 2 nco 2 + (n-3)h 2 O A oxigen dioxid de carbon apă 1 kmol n*22,4 m 3 V molar = 22,4 m 3 / kmol n*22,4*0,05 = 1*10,08 n = 10,08/ 1,12 = 9 formula moleculară este C 9 H 12 Hidrocarbura aromatică, A, mononucleară, disubstituită are următorii izomeri: Rezolvare b: 4
5 E.P ,4 g amestec echimasic de orto-xilen şi naftalină se oxidează cu aer., pe catalizator de V 2 O 5 la temperatură ridicată. Calculează masa de anhidridă ftalică obţinută. Care din cele două hidrocarburi din amestec consumă la oxidare un volum mai mare de aer şi cu cât. Rezolvare: Amestec echimasic, adică mase egale de orto-xilen şi nafatalină şi anume 21,2 g orto-xilen, respectiv 21,2 g naftalină: 21,2 + 21,2 = 42,4 g amestec echimasic 21,2 g V1 litri V2O5 m1 g C 8 H O 2 C 8 H 4 O 3 + 3H 2 O orto-xilen oxigen temperatură ridicată anhidridă ftalică apă 106 g 3*22,4 litri 148 g 21,2 g V2 litri V2O5 m2 g C 10 H 8 + 9/2O 2 C 8 H 4 O 3 + 2H 2 O + 2CO 2 naftalină oxigen temperatură ridicată anhidridă ftalică apă dioxid de carbon 128 g 9/2*22,4 litri 148 g 5
6 M C 8 H 10 = 8*12 +10*1 = = 106 g/ mol M C 10 H 8 = 10*12 +8*1 = 128 g/ mol M C 8 H 4 O 3 = 8*12 +4*1 + 3*16 = = 148 g/ mol V molar = 22,4 litri/ mol m1 = 21,2*148/ 106 = 29,6 g anhidridă ftalică m2 = 21,2*148/ 128 = 24,5125 g anhidridă ftalică m1 + m2 = 29,6 + 24,51 = 54,11 g anhidridă ftalică V1 = 21,2*3*22,4/ 106 = 13,44 litri O 2 V2 = 21,2*4,5*22,4/ 128 = 16,695 litri O litri aer.20 litri O 2.80 litri N 2 Vaer1.13,44 litri O 2? litri N 2 Vaer1 = 13,44*100/ 20 = 67,2 litri aer 20 % O 2 necesar arderii orto-xilenului 100 litri aer.20 litri O 2.80 litri N 2 Vaer2.16,695 litri O 2? litri N 2 Vaer2 = 16,695*100/ 20 = 83,475 litri aer 20 % O 2 necesar arderii naftalinei Vaer2 Vaer1 = 83,475 67,2 = 16,275 litri aer 20 % O 2 Naftalina a folosit la oxidare un volum mai mare de aer decât orto-xilenul şi anume cu 16,275 litri aer 20 % O 2 mai mult. E.P Prin alchilarea benzenului cu propenă, în prezenţă de AlCl 3 umedă, se obţine un amestec de izopropilbenzen, diizopropilbenzen şi benzen nereacţionat, în raport molar de 2 : 2: 1. Calculează volumul de benzen, cu ρ = 0,88 g/cm 3, necesar obţinerii a 36 g izopropilbenzen. 6
7 Rezolvare: n1 = 2 moli (1) 2 moli C 6 H 6 + C 3 H 6 C 6 H 5 -C 3 H 7 benzen propenă AlCl 3 umedă izopropilbenzen 1 mol 1 mol n2 = 2 moli (2) 2 moli C 6 H 6 + 2C 3 H 6 C 3 H 7 - C 6 H 4 - C 3 H 7 benzen propenă AlCl 3 umedă 1.4-diizopropilbenzen 1 mol 1 mol n3 = 1 mol (3) 1 mol C 6 H 6 C 6 H 6 benzen benzen nereacţionat 1 mol 1 mol 7
8 Presupunem că amestecul final conţine 2 moli izopropilbenzen, 2 moli diizopropilbenzen şi 1 mol de benzen nereacţionat. n total = n1 + n2 + n3 = = 5 moli benzen M C 6 H 5 -C 3 H 7 = 9* *1 = = 120 g/mol 1 mol C 6 H 5 -C 3 H g C 6 H 5 -C 3 H 7 x1 moli C 6 H 5 -C 3 H 7 36 g C 6 H 5 -C 3 H 7 x1 = 36*1/ 120 = 0,3 moli C 6 H 5 -C 3 H 7 y1 =0,3 moli (1) x1 =0,3 moli C 6 H 6 + C 3 H 6 C 6 H 5 -C 3 H 7 benzen propenă AlCl 3 umedă izopropilbenzen 1 mol 1 mol y2 moli (2) x2 moli C 6 H 6 + 2C 3 H 6 C 3 H 7 - C 6 H 4 - C 3 H 7 benzen propenă AlCl 3 umedă 1.4-diizopropilbenzen 1 mol 1 mol y3 moli (3) x3 moli C 6 H 6 C 6 H 6 benzen benzen nereacţionat 1 mol 1 mol 5 moli.2 moli (1).2 moli (2)..1 mol (3) (y1 +y2 +y3) y1 moli (1).y2 moli (2).y3 moli (3) (y1 + y2 + y3) moli C6H6 = 5*y1/ 2 = 5*0,3/ 2 = 0,75 moli C 6 H 6 introdus 8
9 M C 6 H 6 = 6*12 + 6*1 = 78 g/ mol 1 mol benzen 78 g benzen 0,75 moli benzen m g m = 0,75*78 = 58,5 g benzen ρ = 0,88 g/cm 3 (densitatea benzenului) V = m/ρ = 58,5/ 0,88 = 66,477 cm 3 benzen E.P Se nitrează 400 g benzen de puritate 78 % cu un amestec sulfonitric în care HNO 3 şi H 2 SO 4 se găsesc în raport molar de 1 : 2 şi care conţine 5 % apă (procente de masă). Calculează masa amestecului sulfonitric necesară reacţiei de nitrare. Ştiind că amestecul sulfonitric este format din soluţie de acid sulfuric şi soluţie de acid azotic, iar acidul sulfuric a avut concentraţia procentuală masică de 98 %, calculează care a fost concentraţia procentuală masică a acidului azotic din amestecul sulfonitric. Rezolvare: a = 4*78 g m d1 C 6 H 6 + HO-NO 2 C 6 H 5 -NO 2 + H 2 O benzen acid azotic H 2 SO 4 nitrobenzen apă 78 g 63 g acid sulfuric M C 6 H 6 = 6*12 + 6*1 = 78 g/ mol M HNO 3 = *16 = 63 g/ mol 9
10 M H 2 SO 4 = 2* *16 = 98 g/ mol 100 g benzen impur..78 g benzen pur..22 g impurităţi 400 g benzen impur a g benzen pur..(400 a) g impurităţi a = 400*78/ 100 = 4*78 g benzen pur m d1 = 4*78*63/ 78 = 4*63 g acid azotic = 252 g acid azotic HNO 3 n 1 = 4*63/ 63 = 4 moli acid azotic HNO 3 raport molar HNO 3 : H 2 SO 4 = 1 : 2 = 4 : 8 = n 1 : n 2 n 1 = 4 moli acid azotic HNO 3 n 2 = 8 moli acid sulfuric H 2 SO 4 m d2 = 8*98 = 784 g acid sulfuric notăm cu x masa de apă din amestecul sulfonitric masa amestecului = ( m d1 + m d2 + x) = 252 g HNO g H 2 SO 4 + x g H 2 O ( x) g amestec..252 g HNO g H 2 SO 4 x g H 2 O 100 g amestec % HNO 3 % H 2 SO g H 2 O ( x)*5 = 100*x ( x) = 20x 1036 = 19x x = 1036/19 = 54,52 g apă masa amestecului = ( m d1 + m d2 + x) = 252 g HNO g H 2 SO ,52 g H 2 O 10
11 masa amestecului = ,52 = 1090,52 g amestec sulfonitric Bilanţul apei : m apă1 + m apă2 = g x = 54,52 g apă Soluţia de acid sulfuric (2) : m d2 = 784 g acid sulfuric m apă2 =? m s2 = (784 + m apă2 ) g soluţie de acid sulfuric 98 % c p2 = 98 % acid sulfuric 100 g soluţie 98 g acid sulfuric 2 g apă m s2 g soluţie.784 g acid sulfuric m apă2 g apă m apă2 = 784*2/ 98 = 16 g apă se găseşte în soluţia de acid sulfuric 98 % Soluţia de acid azotic (1) : m d1 = 252 g acid azotic m apă1 =? m s1 = (252 + m apă1 ) g soluţie de acid azotic de concentraţie procentuală necunoscută c p1 =? % acid azotic Bilanţul apei : m apă1 + m apă2 = g 11
12 m apă1 = 54,52-16 = 38,52 g apă 100 g soluţie c p1 g acid azotic (100 - c p1 ) g apă m s1 g soluţie.252 g acid azotic m apă1 g apă c p1 * m apă1 = 252*(100 - c p1 ) 38,52* c p1 = * c p1 (38, )* c p1 = c p1 = 25200/ 290,52 = 86,74 % acid azotic E.P Se consideră schema: AlCl 3 2) A + CH 3 - Cl B + B V 2 O 5 / t 0 C 3) B + O 2 D + H 2 O + CO 2 V 2 O 5 / t 0 C 4) E + 9/2O 2 D + 2H 2 O + 2CO 2 Ştiind că ecuaţia reacţiei chimice 4) este egalată corect, determină substanţele necunoscute A E, denumeşte-le şi scrie corect cele 4 ecuaţii ale reacţiilor chimice. Rezolvare: 12
13 E.P kg de benzen de puritate 89,7 % s-au supus sulfonării cu H 2 SO 4 de concentraţie 98 %. Ştiind că acidul sulfuric a fost în exces, iar concentraţia lui procentuală în soluţia finală este de 57,45 %, se cere: a) scrie ecuaţia reacţiei chimice de sulfonare a benzenului; b) calculează masa de soluţie de acid sulfuric consumată în reacţie; c) calculează masa de soluţie de acid sulfuric introdusă în reacţia de sulfonare. 13
14 Rezolvare: a =1794 g b g c g C 6 H 6 + HO-SO 3 H C 6 H 5 -SO 3 H + H 2 O benzen acid sulfuric acid benzensulfonic apă 78 g 98 g 18 g M C 6 H 6 = 6*12 + 6*1 = 78 g/ mol M H 2 SO 4 = 2* *16 = 98 g/ mol M H 2 O = 2* = 18 g/ mol 2 kg benzen de puritate 89,7 % = 2000 g benzen de puritate 89,7 % 100 g benzen impur.89,7 g benzen pur..10,3 g impurităţi 2000 g benzen impur.a g benzen pur (2000 a) g impurităţi a = 2000*89,7/ 100 =1794 g benzen pur b = 1794*98 / 78 = 2254 g acid sulfuric consumat la sulfonare c = 1794*18/ 78 = 414 g apă rezultată în reacţie Masa soluţiei de acid sulfuric 98 % consumată în reacţie =? 100 g soluţie 98 g acid sulfuric m sc g soluţie g acid sulfuric 14
15 m sc = 2254*100/ 98 = 2300 g soluţie de acid sulfuric 98 % consumată în reacţie Masa soluţiei de acid sulfuric 98 % introdusă în reacţie =? m si =? Notăm cu x masa de acid sulfuric în exces 100 g soluţie 98 g acid sulfuric m si g soluţie..( x) g acid sulfuric 100( x) = 98* m si (1) În reacţie se obţin 414 g apă şi se consumă 2254 g acid sulfuric. Soluţia finală are concentraţia procentuală 57,45 % acid sulfuric m sf =( m si ) g soluţie finală de acid sulfuric 57,45 % 100 g soluţie finală.57,45 g acid sulfuric m sf g sol finală x g acid sulfuric m sf = 100*x/ 57,45 ( m si ) = 100*x/ 57,45 (2) Avem un sistem de două ecuaţii (1) şi (2) cu două necunoscute, m si şi x: Din prima ecuaţie îl scoatem pe m si şi îl introducem în ecuaţia (2) : m si = 100*( x)/98 m si = 1,02* ,02x m si = ,02x 15
16 ( m si ) = 100*x/ 57,45 (2) ( ,02x ) = 1,74x ,02x = 1,74x 459 = 0,72x x = 637,5 g acid sulfuric în exces m si = ,02x m si = ,02*637,5 = 2949,25 g soluţie acid sulfuric 98 % introdusă E.P g amestec de benzen şi toluen, care conţine 8,064 % H, se oxidează cu soluţie de KMnO 4 de concentraţie 0,2 M şi H 2 SO 4. Se cere: Rezolvare: a) calculează compoziţia procentuală, în procente masice a amestecului de hidrocarburi aromatice; b) calculează volumul soluţiei de KMnO 4 consumat în reacţia de oxidare. M C 6 H 6 = 6*12 + 6*1 = 78 g/ mol M C 6 H 5 CH 3 = 7*12 + 8*1 = 92 g/ mol Notăm cu x numărul de moli de benzen şi cu y numărul de moli de toluen. 48 = 78x + 92y (1) Calculăm masa de hidrogen totală (m1 + m2) din amestecul de 48 g. 78 g benzen..6 g H 78x g benzen m1 g H 16
17 m1 = 78x*6/ 78 = 6x g H din benzen 92 g toluen.8 g H 92y g toluen..m2 g H m2 = 92y*8/ 92 = 8y g H din toluen 48 g amestec..(m1 + m2) g H 100 g amestec.8,064 g H (m1 + m2) = 48*8,064/ 100 = 3,87 g H 6x + 8y = 3,87 (2) 48 = 78x + 92y (1) Avem un sistem de două ecuaţii (1) şi (2) şi două necunoscute x şi y. x + 4/3y = 0,645 x = 0,645 4*y/3 48 = 78(0,645 4*y/3) + 92y 48 = 78*0,645-78*4y/3 +92y 48 = 50,31 26*4y +92y 104y-92y = 50, y = 2,31 y = 2,31/ 12 = 0,1925 moli toluen x = 0,645 4*0,1925/3 = 0,645 0,2566 = 0,3884 moli benzen 48 g amestec..78x g benzen..92y g toluen 100 g amestec..% benzen.% toluen 17
18 % benzen = 100*78x/ 48 = 100*78*0,3884/ 48 = 63,11 % benzen % toluen = 100*92y/ 48 = 100*92*0,1925/ 48 = 36,89 % toluen 63,11 % benzen + 36,89 % toluen = 100 0,1925 moli n moli 5C 6 H 5 -CH 3 + 6KMnO 4 + 9H 2 SO 4 5C 6 H 5 -COOH + 3K 2 SO 4 + 6MnSO H 2 O toluen permangan at de potasiu acid sulfuric 5 moli 6 moli C -3-6e - C +3 oxidare *5 Mn e - Mn 2+ reducere *6 5C -3-30e - 5C +3 oxidare 6Mn e - 6Mn 2+ reducere acid benzoic sulfat de potasiu sulfat de mangan Numărul de electroni cedaţi este întotdeauna egal cu numărul electronilor acceptaţi. n = 6*0,1925/ 5 = 0,231 moli KMnO 4 apă 1000 ml soluţie..0,2 moli KMnO 4 V ml soluţie.n moli KMnO 4 V = 1000*n/ 0,2 = 1000*0,231/ 0,2 = 1155 ml soluţie KMnO 4 0,2 M 18
19 V = 1,155 litri soluţie KMnO 4 0,2 M. E.P Se acilează benzenul cu o clorură acidă de forma C n H 2n+1 CO-Cl. Ştiind că prin acilarea masa molară a benzenului creşte cu 71,8 %, se cere: Rezolvare: a) determină clorura acidă cu care s-a realizat acilarea; b) scrie ecuaţia reacţiei chimice de acilare; c) presupunând că s-au acilat total 5 moli de benzen, calculează volumul soluţiei de acid clorhidric, de concentraţie 1 M, care se obţine prin dizolvarea în apă a acidului clorhidric rezultat din reacţia de acilare. C 6 H 6 + C n H 2n+1 CO-Cl C 6 H 5 -CO-C n H 2n+1 + HCl benzen clorură acidă acilbenzen acid clorhidric M C 6 H 6 = 6*12 + 6*1 = 78 g/ mol M C 6 H 5 -CO-C n H 2n+1 = 6*12 + 5* n + 2n + 1 = (14n + 106) g acilbenzen *71,8/ 100 = (14n +106) = 14n = 14n n = 2 C n H 2n+1 CO-Cl C 2 H 5 CO-Cl CH 3 -CH 2 -CO-Cl Clorură de propanoil Clorură de propanoil adică clorura acidă a acidului propanoic CH 3 -CH 2 -COOH 19
20 5 moli 5 moli C 6 H 6 + C 2 H 5 COCl C 6 H 5 -CO-C 2 H 5 + HCl benzen clorură acidă propanoilbenzen sau etil-fenil-cetonă acid clorhidric 1 mol 1 mol 1000 ml soluţie.1 mol HCl V ml soluţie..5 moli HCl V = 5*1000/ 1 = 5000 ml soluţie HCl 1 M V = 5 litri soluţie HCl 1 M. 20
21 CH 3 -CH 2 -CO-Cl Clorură de propanoil etil fenil-cetonă C 6 H 5 - CO- C 2 H 5 21
22 E.P Prin oxidarea a 4 kg antracen de puritate 89 % se obţin 3,12 kg antrachinonă. Calculează randamentul reacţiei de oxidare şi volumul soluţiei de K 2 Cr 2 O 7 de concentraţie 0,5 M consumat în reacţia de oxidare. antracen C 14 H 10 M C 14 H 10 = 14* *1 = 178 g/ mol M C 14 H 8 O 2 = 14*12 + 8*1 + 2*16 = antrachinonă C 14 H 8 O 2 22
23 a=2670 g n moli 3120 g C 14 H 10 + K 2 Cr 2 O 7 + 8CH 3 -COOH C 14 H 8 O 2 + 2CH 3 -COOK + 2(CH 3 -COO) 3 Cr + 5H 2 O antracen dicromat de potsiu acid acetic antrachino nă 178 g 1 mol 208 g acetat de potasiu acetat de crom apă C -1-3e - C +2 oxidare *2 Cr e - Cr 3+ reducere *2 2C -1-6e - 2C +2 oxidare 2Cr e - 2Cr 3+ reducere Numărul de electroni cedaţi este întotdeauna egal cu numărul electronilor acceptaţi. 3,12 kg antrachinonă = 3120 g antrachinonă a = 178*3120/ 208 = 2670 g antracen 3120 g antrachinonă n = 3120*1/ 208 = 15 moli K 2 Cr 2 O 7 1 litru soluţie 0,5 moli K 2 Cr 2 O 7 V litri soluţie 15 moli K 2 Cr 2 O 7 V = 15*1/ 0,5 = 30 litri soluţie K 2 Cr 2 O 7 0,5 M 4 kg antracen de puritate 89 % 4kg = 4000 g antracen de puritate 89 % 100 g antracen impur 89 g antracen pur 11 g impurităţi 4000 g antracen impur (a + b) g antracen pur..[4000 (a +b)] g impurităţi (a +b) = 4000*89/ 100 = 3560 g antracen 23
24 a =2670 g antracen 3120 g antrachinonă (a +b) = 3560 g antracen b = = 890 g antracen 890 g antracen nereacţionat η = a*100/ (a +b) = 2670*100/ 3560 = 75 % E.P Se sulfonează 2 moli de benzen cu 400 g soluţie de acid sulfuric de concentraţie 98 %. Rezolvare: a) Calculează care din cei doi reactanţi se află în exces. b) Calculează concentraţia procentuală a acidului sulfuric rezidual.(h 2 SO 4 în soluţia finală) c) Calculează masa de acid sulfuric oleum (20 % SO 3 ), necesară pentru a readuce acidul sulfuric rezidual la concentraţia procentuală de 98 %. 2 moli x = 196 g y = 36 g C 6 H 6 + HO-SO 3 H C 6 H 5 -SO 3 H + H 2 O benzen acid sulfuric acid benzensulfonic apă 1 mol 98 g 18 g M C 6 H 6 = 6*12 + 6*1 = 78 g/ mol M H 2 SO 4 = 2* *16 = 98 g/ mol 24
25 M H 2 O = 2* = 18 g/ mol x = 2*98/ 1 = 196 g acid sulfuric m s = 400 g soluţie acid sulfuric 98 % c p = 98 % acid sulfuric m d =? g acid sulfuric 100 g soluţie.. c p m s. m d m d = 400*98/ 100 = 392 g acid sulfuric Bilanţul acidului sulfuric: 392 g acid sulfuric = 196 g acid sulfuric consumat g acid sulfuric rămas (în exces) y = 18*2/ 1 = 36 g apă m sr = g acid sulfuric consumat +36 g apă rezultată în reacţie = 240 g soluţie reziduală m dr = 196 g acid sulfuric rămas (în exces) c pr =? 100 g soluţie.. c pr m sr. m dr c pr = 100*196/ 240 = 81,66 % H 2 SO 4 rezidual m sr =240 g soluţie reziduală 25
26 100 g oleum (20 % SO 3 ) = 80 g H 2 SO g SO g oleum (20 % SO 3 ) conţine ( ,5) = 104,5 g acid sulfuric sau 104,5 % H 2 SO 4 20 g 4,5 g 24,5 g SO 3 + H 2 O H 2 SO 4 trioxid de sulf apă acid sulfuric 80 g 18 g 98 g M SO 3 = 32 +3*16 = 80 g/ mol M H 2 O = 2* = 18 g/ mol M H 2 SO 4 = 2* * 16 = 98 g/ mol m sr = 240 g soluţie reziduală c pr = 81,66 % H 2 SO 4 rezidual + m so =? oleum c po = 104,5 % H 2 SO 4 m sf = (m sr +m so ) c pf = 98 % H 2 SO 4 m sr *c pr + m so *c po = (m sr +m so )*98 240*81,66 + m so *104,5 = (240 +m so )*98 (104,5 98)*m so = 240(98 81,66) 26
27 6,5*m so = 240*16,34 m so = 603,32 g oleum (20 % SO 3 ) E.P Prin hidrogenarea naftalinei se obţin tetralină şi decalină, în raport molar de 1 : 3. Ştiind ca doar 80 % din naftalina introdusă se hidrogenează, iar masa amestecului final este cu 68 g mai mare decât masa iniţială a naftalinei, calculează masa de naftalină supusă hidrogenării. Rezolvare : naftalina C 10 H 8 27
28 tetralina C 10 H 12 decalina C 10 H 18 Raport molar tetralina : decalină = 1 : 3 = x : 3x x moli naftalină se hidrogenează cu 2x moli H 2 x moli tetralină 3x moli naftalină se hidrogenează cu 15x moli H 2 3x moli decalină M H 2 = = 2 g/mol (2x + 15x) moli H 2 ce cântăresc 68 g 28
29 17x moli H 2 ce cântăresc 68 g 1 mol H2.2 g H2 17x moli H g H2 x = 68*1/ 17*2 = 2 moli tetralină 3x = 6 moli decalină 2 moli naftalină 2 moli tetralină (1) 6 moli naftalină 6 moli decalină (2) y moli naftalină y moli naftalină nereacţionată (3) ( y) moli 2moli (1)..6 moli (2)..y moli (3) 100 moli..% (1) % (2) % (3) % (1) + % (2) = 80 % din naftalina introdusă se hidrogenează % (3) = 20 % din naftalina introdusă nu se hidrogenează ( y)*20 = 100y ( y) = 5y 8 = 4y y = 2 moli naftalină nu se hidrogenează ( ) = 10 moli naftalină introdusă M C 10 H 8 = 10*12 + 8*1 = 128 g/mol masa de naftalină supusă hidrogenării = 10*128 = 1280 g naftalină E.P La hidrogenarea totală a 89,6 g naftalină se consumă 51,52 litri H 2 măsurat în condiţii normale. Calculează raportul molar decalină : tetralină obţinut în urma hidrogenării. 29
30 Rezolvare : naftalina C 10 H 8 tetralina C 10 H 12 30
31 decalina C 10 H 18 Raport molar tetralina : decalină = x : y x moli naftalină se hidrogenează cu 2x moli H 2 x moli tetralină y moli naftalină se hidrogenează cu 5y moli H 2 5y moli decalină M H 2 = = 2 g/mol M C 10 H 8 = 10*12 + 8*1 = 128 g/mol V molar = 22,4 litri/mol (x + y)*128 = 89,6 (2x + 5y)*22,4 = 51,52 x + y = 0,7 2x +5y = 2,3 x + y = 0,7 2(x + y) + 3y = 2,3 1,4 + 3y = 2,3 31
32 3y = 0,9 y = 0,3 moli naftalină 0,3 moli decalină x = 0,4 moli naftalină 0,4 moli tetralină raportul molar decalină : tetralină = 0,3 : 0,4 = 3 : 4 E.P Prin halogenarea fotochimică a toluenului se obţine un amestec format din doi derivaţi halogenaţi care conţin 28,06 % Cl şi respectiv 44,09 % Cl. Se cere: Rezolvare: a) Determină formulele moleculare ale celor doi derivaţi halogenaţi obţinuţi. b) Calculează volumul de toluen (ρ = 0,9 g/ cm 3 ) supus clorurării, ştiind că cei doi derivaţi se găsesc în rapor molar de 2 : 3, iar în urma procesului s-au degajat 224 litri HCl (c.n.). C 6 H 5 -CH 3-n Cl n C 6 H 5 -CH 3 + ncl 2 C 6 H 5 -CH 3-n Cl n + nhcl M C 6 H 5 -CH 3-n Cl n = 7*12 + 8*1 n*1 + 35,5*n = (92 34,5n) g/ mol (92 34,5n) g 35,5n g Cl 100 g 28,06 g Cl (92 34,5n)*28,06 = 100*35,5n 2581,52 = 3550n 968,07n 2581,52 = 2581,93n n = 1 32
33 C 6 H 5 -CH 3-n Cl n C 6 H 5 -CH 2 Cl clorură de benzil ce conţine 28,06 % Cl C 6 H 5 -CH 3-m Cl m C 6 H 5 -CH 3 + mcl 2 C 6 H 5 -CH 3-m Cl m + mhcl M C 6 H 5 -CH 3-m Cl m = 7*12 + 8*1 m*1 + 35,5*m = (92 34,5m) g/ mol (92 34,5m) g 35,5m g Cl 100 g 44,09 g Cl (92 34,5m)*44,09 =100*35,5m 4056,28 = 3550m 1521,105m 4056,28 = 2028,895m m = 2 C 6 H 5 -CH 3-m Cl m C 6 H 5 -CHCl 2 clorură de benziliden ce conţine 44,09 % Cl 2a moli (1) 2a moli 2a moli C 6 H 5 -CH 3 + Cl 2 C 6 H 5 -CH 2 Cl + HCl toluen clor halogenare fotochimică clorură de benzil acid clorhidric 1 mol 1 mol 1 mol 3a moli (2) 3a moli 6a moli C 6 H 5 -CH 3 + 2Cl 2 C 6 H 5 -CHCl 2 + 2HCl toluen clor halogenare clorură de benziliden acid fotochimică clorhidric 1 mol 1 mol 2 moli 33
34 Raport molar C 6 H 5 -CH 2 Cl : C 6 H 5 -CHCl 2 = 2 : 3 = 2a : 3a V molar = 22,4 litri/mol 224 litri HCl (2a + 6a)*22, 4 = 224 8a = 10 a = 10/8 = 1,25 moli 2a + 3a = 5a moli toluen M C 6 H 5 -CH 3 = 7*12 + 8*1 = 92 g/mol masa de toluen = 5a*92 = 5*1,25*92 = 575 g toluen (cu densitatea ρ = 0,9 g/ cm 3 ) V = m/ρ = 575/ 0,9 = 638,88 cm 3 toluen 34
35 toluen C 6 H 5 -CH 3 clorură de benzil C 6 H 5 -CH 2 Cl 35
36 clorură de benziliden C 6 H 5 -CHCl 2 H C 6 H 5 H C H Cl C Cl H Cl metan fenil-triclormetan 36
37 fenil-triclormetan C 6 H 5 -CCl 3 37
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Capitolul 2-HIDROCARBURI-2.3.-ALCHINE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
Capitolul 2-HIDROCARBURI-2.2.-ALCHENE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.2.ALCHENE Exerciţii şi probleme E.P.2.2.1. Denumeşte conform IUPAC următoarele alchene: A CH 3 CH 3 CH 2 C 3 C 4 H C 5 CH 3 C 2 H CH 3 C 6 H 2 C 1 H 3 C 7 H 3 3-etil-4,5,5-trimetil-2-heptenă
Capitolul 2 - HIDROCARBURI 2.2.ALCHENE Exerciţii şi probleme E.P.2.2.1. Denumeşte conform IUPAC următoarele alchene: A CH 3 CH 3 CH 2 C 3 C 4 H C 5 CH 3 C 2 H CH 3 C 6 H 2 C 1 H 3 C 7 H 3 3-etil-4,5,5-trimetil-2-heptenă
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Capitolul 4-COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ-
 Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Liceul de Ştiinţe ale Naturii Grigore Antipa Botoşani
 Fişă de lucru RANDAMENT. CONVERSIE UTILĂ. CONVERSIE TOTALĂ 1. Randament A. Hidrocarburile alifatice pot fi utilizate drept combustibili, sau pot fi transformate în compuşi cu aplicaţii practice. 1. Scrieţi
Fişă de lucru RANDAMENT. CONVERSIE UTILĂ. CONVERSIE TOTALĂ 1. Randament A. Hidrocarburile alifatice pot fi utilizate drept combustibili, sau pot fi transformate în compuşi cu aplicaţii practice. 1. Scrieţi
I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare.
 Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
Capitolul 1-INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme
 Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2015 DISCIPLINA: CHIMIE ORGANICĂ
 Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2015 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2015 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
CLASA a X a PROBA TEORETICĂ Filiera tehnologică toate profilurile/specializările/calificările
 CLASA a X a PROBA TEORETICĂ Filiera tehnologică toate profilurile/specializările/calificările Subiectul I 20 Fiecare item are un singur răspuns corect. Notaţi în tabel cu X numai răspunsul corect. Pentru
CLASA a X a PROBA TEORETICĂ Filiera tehnologică toate profilurile/specializările/calificările Subiectul I 20 Fiecare item are un singur răspuns corect. Notaţi în tabel cu X numai răspunsul corect. Pentru
Subiectul III (30 puncte) Varianta 001
 Subiectul III (30 puncte) Varianta 001 Proteinele şi zaharidele sunt compuşi organici cu acţiune biologică. 1. Scrieţi formula de structură pentru o tripeptidă P care conţine glicină, valină şi serină
Subiectul III (30 puncte) Varianta 001 Proteinele şi zaharidele sunt compuşi organici cu acţiune biologică. 1. Scrieţi formula de structură pentru o tripeptidă P care conţine glicină, valină şi serină
II. 5. Probleme. 20 c 100 c = 10,52 % Câte grame sodă caustică se găsesc în 300 g soluţie de concentraţie 10%? Rezolvare m g.
 II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
Rezolvarea problemelor la chimie prin metoda algebrică
 Ministerul Educaţiei şi Tineretului al Republicii Moldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă Rezolvarea problemelor la chimie prin metoda algebrică Autor: Postolache Ion,
Ministerul Educaţiei şi Tineretului al Republicii Moldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă Rezolvarea problemelor la chimie prin metoda algebrică Autor: Postolache Ion,
Subiectul II (30 puncte) Varianta 001
 Subiectul II (30 puncte) Varianta 001 Compuşii cloruraţi obţinuţi din hidrocarburile alifatice au importante aplicaţii practice. 1. Scrieţi ecuaţiile reacţiilor chimice, prin care se obţin din metan: monoclorometan,
Subiectul II (30 puncte) Varianta 001 Compuşii cloruraţi obţinuţi din hidrocarburile alifatice au importante aplicaţii practice. 1. Scrieţi ecuaţiile reacţiilor chimice, prin care se obţin din metan: monoclorometan,
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ. Capitolul Hidrocarburi
 Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ Capitolul Hidrocarburi CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ Capitolul Hidrocarburi CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE
14. Se dă următorul compus:
 CLASA a XI-a 1. Care din următorii compuşi este un derivat halogenat vicinal: a) 1,2-dicloropropanul; b) 1,1-dicloropropanul; c) 1-bromopropanul; d) 2-bromo-2-metilpropanul; e) 1,3,5-tricloropropanul.
CLASA a XI-a 1. Care din următorii compuşi este un derivat halogenat vicinal: a) 1,2-dicloropropanul; b) 1,1-dicloropropanul; c) 1-bromopropanul; d) 2-bromo-2-metilpropanul; e) 1,3,5-tricloropropanul.
Curs 14 Funcţii implicite. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi"
 Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
ITEMI MODEL PENTRU UNITATEA DE ÎNVĂŢARE: Alcooli
 LIEUL TEORETI GRIGORE ANTIPA BOTOŞANI - ITEMI MODEL PENTRU UNITATEA DE ÎNVĂŢARE: Alcooli Subiectul A: Indicaţi care dintre afirmaţiile de mai jos sunt adevărate şi care sunt false, completând cu litera
LIEUL TEORETI GRIGORE ANTIPA BOTOŞANI - ITEMI MODEL PENTRU UNITATEA DE ÎNVĂŢARE: Alcooli Subiectul A: Indicaţi care dintre afirmaţiile de mai jos sunt adevărate şi care sunt false, completând cu litera
Aplicaţii ale principiului I al termodinamicii la gazul ideal
 Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM
 LICEUL TEORETIC TRAIAN CONSTANŢA CLAS a X-a VARIANTA II CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 La întrebările de la 1-20, alege un singur răspuns: 1. Sunt adevarate urmatoarele afirmații cu
LICEUL TEORETIC TRAIAN CONSTANŢA CLAS a X-a VARIANTA II CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 La întrebările de la 1-20, alege un singur răspuns: 1. Sunt adevarate urmatoarele afirmații cu
5.1. Noţiuni introductive
 ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
Prefaţă: Lucrarea de faţă se bazează pe asimilarea şi fixarea cunoştinţelor de chimie organică prin intermediul rezolvării de probleme.
 Prefaţă: Lucrarea de faţă se bazează pe asimilarea şi fixarea cunoştinţelor de chimie organică prin intermediul rezolvării de probleme. Soluţiile problemelor sunt explicate pentru a dezvolta gândirea în
Prefaţă: Lucrarea de faţă se bazează pe asimilarea şi fixarea cunoştinţelor de chimie organică prin intermediul rezolvării de probleme. Soluţiile problemelor sunt explicate pentru a dezvolta gândirea în
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM 1 electronica.geniu.ro
 Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Seminariile Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reziduurilor
 Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Sisteme diferenţiale liniare de ordinul 1
 1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
Planul determinat de normală şi un punct Ecuaţia generală Plane paralele Unghi diedru Planul determinat de 3 puncte necoliniare
 1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
(a) se numeşte derivata parţială a funcţiei f în raport cu variabila x i în punctul a.
 Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
Reactia de amfoterizare a aluminiului
 Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
OLIMPIADA DE CHIMIE etapa judeţeană
 Clasa a VIII-a OLIMPIADA DE CHIMIE etapa judeţeană Str. General Berthelot nr. 28-30, Sector 1, Cod 010168, Bucureşti Tel: +40 (0)21 405 62 21 Fax: +40 (0)21 313 55 47 www.edu.ro DIRECȚIA GENERALĂ EDUCAȚIE
Clasa a VIII-a OLIMPIADA DE CHIMIE etapa judeţeană Str. General Berthelot nr. 28-30, Sector 1, Cod 010168, Bucureşti Tel: +40 (0)21 405 62 21 Fax: +40 (0)21 313 55 47 www.edu.ro DIRECȚIA GENERALĂ EDUCAȚIE
5. FUNCŢII IMPLICITE. EXTREME CONDIŢIONATE.
 5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
a. 11 % b. 12 % c. 13 % d. 14 %
 1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
CONCURSUL DE CHIMIE CORIOLAN DRĂGULESCU 2017
 Universitatea Politehnica Timişoara Facultatea de Chimie Industrială şi Ingineria Mediului Clasa a IX-a Chimie anorganică CONCURSUL DE CHIMIE CORIOLAN DRĂGULESCU 2017 1. (2 p) Precizaţi poziţia în sistemul
Universitatea Politehnica Timişoara Facultatea de Chimie Industrială şi Ingineria Mediului Clasa a IX-a Chimie anorganică CONCURSUL DE CHIMIE CORIOLAN DRĂGULESCU 2017 1. (2 p) Precizaţi poziţia în sistemul
Metoda rezolvării problemelor de determinare a formulelor chimice
 inisterul Educaţiei şi Tineretului al Republicii oldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă etoda rezolvării problemelor de determinare a formulelor chimice Autor Postolache
inisterul Educaţiei şi Tineretului al Republicii oldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă etoda rezolvării problemelor de determinare a formulelor chimice Autor Postolache
OLIMPIADA NAȚIONALĂ DE CHIMIE
 MINISTERUL EDUCAȚIEI ȘI CERCETĂRII ȘTIINȚIFICE INSPECTORATUL ȘCOLAR JUDEȚEAN GALAȚI OLIMPIADA NAȚIONALĂ DE CHIMIE EDIȚIA a XLIX-a GALAȚI 5-10 APRILIE 2015 Proba teoretică Clasa a VIII-a Subiectul I (20
MINISTERUL EDUCAȚIEI ȘI CERCETĂRII ȘTIINȚIFICE INSPECTORATUL ȘCOLAR JUDEȚEAN GALAȚI OLIMPIADA NAȚIONALĂ DE CHIMIE EDIȚIA a XLIX-a GALAȚI 5-10 APRILIE 2015 Proba teoretică Clasa a VIII-a Subiectul I (20
Examenul naţional de bacalaureat 2014 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d)
 Examenul naţional de bacalaureat 2014 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d) FILIERĂ TEHNOLOGICĂ profil tehnic, profil resurse naturale şi protecţia mediului SUBIECTUL I (30 puncte)
Examenul naţional de bacalaureat 2014 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d) FILIERĂ TEHNOLOGICĂ profil tehnic, profil resurse naturale şi protecţia mediului SUBIECTUL I (30 puncte)
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate.
 Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Examenul de bacalaureat nańional 2013 Proba E. d) Chimie organică (nivel I/ nivel II)
 Examenul de bacalaureat nańional 2013 Proba E. d) Chimie organică (nivel I/ nivel II) MODEL Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL I Subiectul
Examenul de bacalaureat nańional 2013 Proba E. d) Chimie organică (nivel I/ nivel II) MODEL Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL I Subiectul
Ecuaţia generală Probleme de tangenţă Sfera prin 4 puncte necoplanare. Elipsoidul Hiperboloizi Paraboloizi Conul Cilindrul. 1 Sfera.
 pe ecuaţii generale 1 Sfera Ecuaţia generală Probleme de tangenţă 2 pe ecuaţii generale Sfera pe ecuaţii generale Ecuaţia generală Probleme de tangenţă Numim sferă locul geometric al punctelor din spaţiu
pe ecuaţii generale 1 Sfera Ecuaţia generală Probleme de tangenţă 2 pe ecuaţii generale Sfera pe ecuaţii generale Ecuaţia generală Probleme de tangenţă Numim sferă locul geometric al punctelor din spaţiu
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE
 DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II)
 Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II) Varianta 9 Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL
Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II) Varianta 9 Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL
Definiţia generală Cazul 1. Elipsa şi hiperbola Cercul Cazul 2. Parabola Reprezentari parametrice ale conicelor Tangente la conice
 1 Conice pe ecuaţii reduse 2 Conice pe ecuaţii reduse Definiţie Numim conica locul geometric al punctelor din plan pentru care raportul distantelor la un punct fix F şi la o dreaptă fixă (D) este o constantă
1 Conice pe ecuaţii reduse 2 Conice pe ecuaţii reduse Definiţie Numim conica locul geometric al punctelor din plan pentru care raportul distantelor la un punct fix F şi la o dreaptă fixă (D) este o constantă
Examenul de bacalaureat naţional 2016 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d)
 Examenul de bacalaureat naţional 2016 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d) FILIERĂ TEHNOLOGICĂ profil tehnic, profil resurse naturale şi protecţia mediului SUBIECTUL I (30 puncte)
Examenul de bacalaureat naţional 2016 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d) FILIERĂ TEHNOLOGICĂ profil tehnic, profil resurse naturale şi protecţia mediului SUBIECTUL I (30 puncte)
Mase atomice C 12, H 1, O 16, S 32, Cl 35,5, Na 23, Cu 64,
 Mase atomice C 12, H 1, O 16, S 32, Cl 35,5, Na 23, Cu 64, Intrebari cu 1 raspuns corect: 1. Caracterul electronegativ reprezintă: a. tendinţa atomilor de a ceda electroni şi de a forma ioni pozitivi b.
Mase atomice C 12, H 1, O 16, S 32, Cl 35,5, Na 23, Cu 64, Intrebari cu 1 raspuns corect: 1. Caracterul electronegativ reprezintă: a. tendinţa atomilor de a ceda electroni şi de a forma ioni pozitivi b.
a. 0,1; 0,1; 0,1; b. 1, ; 5, ; 8, ; c. 4,87; 6,15; 8,04; d. 7; 7; 7; e. 9,74; 12,30;1 6,08.
 1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
Metode iterative pentru probleme neliniare - contractii
 Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
CHIMIE ORGANICĂ CLASA a XII-a
 CHIMIE ORGANICĂ CLASA a XII-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea
CHIMIE ORGANICĂ CLASA a XII-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea
ANALIZE FIZICO-CHIMICE MATRICE APA. Tip analiza Tip proba Metoda de analiza/document de referinta/acreditare
 ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
Integrala nedefinită (primitive)
 nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
MODEL DE SUBIECT Chimie organică (nivel I / nivel II)
 Bun venit dragi elevi! Am speranţa, că ciclul de emisiuni destinate pregătirii examenului de Bacalaureat-proba de Chimie organică sau Chimie anorganică şi generală, va fi util pentru alegerea voastră.
Bun venit dragi elevi! Am speranţa, că ciclul de emisiuni destinate pregătirii examenului de Bacalaureat-proba de Chimie organică sau Chimie anorganică şi generală, va fi util pentru alegerea voastră.
5.5. REZOLVAREA CIRCUITELOR CU TRANZISTOARE BIPOLARE
 5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
CLASA a X-a. 3. Albastrul de Berlin are formula: a) PbS; b) [Cu(NH 3 ) 4 ](OH); c) Na 4 [Fe(CN) 6 ]; d) Ag(NH 3 ) 2 OH; e) Fe 4 [Fe(CN) 6 ] 3.
; c) Na 4 [Fe(CN) 6 ]; d) Ag(NH 3 ) 2 OH; e) Fe 4 [Fe(CN) 6 ] 3. CLASA a X-a. 3. Albastrul de Berlin are formula: a) PbS; b) [Cu(NH 3 ) 4 ](OH); c) Na 4 [Fe(CN) 6 ]; d) Ag(NH 3 ) 2 OH; e) Fe 4 [Fe(CN) 6 ] 3.](/thumbs/54/33993973.jpg) CLASA a X-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea solubilităţii;
CLASA a X-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea solubilităţii;
SEMINAR 14. Funcţii de mai multe variabile (continuare) ( = 1 z(x,y) x = 0. x = f. x + f. y = f. = x. = 1 y. y = x ( y = = 0
 Facultatea de Hidrotehnică, Geodezie şi Ingineria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucian MATICIUC SEMINAR 4 Funcţii de mai multe variabile continuare). Să se arate că funcţia z,
Facultatea de Hidrotehnică, Geodezie şi Ingineria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucian MATICIUC SEMINAR 4 Funcţii de mai multe variabile continuare). Să se arate că funcţia z,
LICEUL TEORETIC TRAIAN CONSTANŢA CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM
 LICEUL TEORETIC TRAIAN CONSTANŢA CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 Clasa a XI-a Varianta 2 La întrebările de la 1-30, alege un singur răspuns: 1.Câți enantiomeri prezintă 4,5 dimetil
LICEUL TEORETIC TRAIAN CONSTANŢA CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 Clasa a XI-a Varianta 2 La întrebările de la 1-30, alege un singur răspuns: 1.Câți enantiomeri prezintă 4,5 dimetil
Acizi carboxilici heterofuncționali.
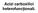 Acizi carboxilici heterofuncționali. 1. Acizi carboxilici halogenați. R R 2 l l R 2 R l Acizi α-halogenați Acizi β-halogenați l R 2 2 l Acizi γ-halogenați Metode de obținere. 1. alogenarea directă a acizilor
Acizi carboxilici heterofuncționali. 1. Acizi carboxilici halogenați. R R 2 l l R 2 R l Acizi α-halogenați Acizi β-halogenați l R 2 2 l Acizi γ-halogenați Metode de obținere. 1. alogenarea directă a acizilor
CULEGERE DE PROBLEME pentru Concursul de Chimie Organică din cadrul Facultății de Chimie Industrială și Ingineria Mediului UNIVERSITATEA POLITEHNICA
 Sabina-Violeta NIȚU Sorina RAN CULGR PRLM pentru Concursul de Chimie rganică din cadrul Facultății de Chimie Industrială și Ingineria Mediului UNIVRSITATA PLITHNICA TIMIȘARA Timișoara 2014 1 CUPRINS I.
Sabina-Violeta NIȚU Sorina RAN CULGR PRLM pentru Concursul de Chimie rganică din cadrul Facultății de Chimie Industrială și Ingineria Mediului UNIVRSITATA PLITHNICA TIMIȘARA Timișoara 2014 1 CUPRINS I.
Curs 4 Serii de numere reale
 Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Modele de teste grilă pentru examenul de admitere la Facultatea de Medicină şi Farmacie, specializarea Farmacie*
 Universitatea UNIVERSITATEA DUNĂREA DE JOS din GALAŢI Facultatea de Medicină şi Farmacie, Specializarea Farmacie Modele de teste grilă pentru examenul de admitere la Facultatea de Medicină şi Farmacie,
Universitatea UNIVERSITATEA DUNĂREA DE JOS din GALAŢI Facultatea de Medicină şi Farmacie, Specializarea Farmacie Modele de teste grilă pentru examenul de admitere la Facultatea de Medicină şi Farmacie,
REACŢII DE ADIŢIE NUCLEOFILĂ (AN-REACŢII) (ALDEHIDE ŞI CETONE)
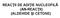 EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
IV. CUADRIPOLI SI FILTRE ELECTRICE CAP. 13. CUADRIPOLI ELECTRICI
 V. POL S FLTE ELETE P. 3. POL ELET reviar a) Forma fundamentala a ecuatiilor cuadripolilor si parametrii fundamentali: Prima forma fundamentala: doua forma fundamentala: b) Parametrii fundamentali au urmatoarele
V. POL S FLTE ELETE P. 3. POL ELET reviar a) Forma fundamentala a ecuatiilor cuadripolilor si parametrii fundamentali: Prima forma fundamentala: doua forma fundamentala: b) Parametrii fundamentali au urmatoarele
Ecuatii trigonometrice
 Ecuatii trigonometrice Ecuatiile ce contin necunoscute sub semnul functiilor trigonometrice se numesc ecuatii trigonometrice. Cele mai simple ecuatii trigonometrice sunt ecuatiile de tipul sin x = a, cos
Ecuatii trigonometrice Ecuatiile ce contin necunoscute sub semnul functiilor trigonometrice se numesc ecuatii trigonometrice. Cele mai simple ecuatii trigonometrice sunt ecuatiile de tipul sin x = a, cos
PROBLEME DE CHIMIE ORGANICĂ
 FNDUL SCIAL EURPEAN Programul peraţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară: 1 Educaţia şi formarea profesională în sprijinul creşterii economice şi dezvoltării societăţii
FNDUL SCIAL EURPEAN Programul peraţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară: 1 Educaţia şi formarea profesională în sprijinul creşterii economice şi dezvoltării societăţii
Tranzistoare bipolare şi cu efect de câmp
 apitolul 3 apitolul 3 26. Pentru circuitul de polarizare din fig. 26 se cunosc: = 5, = 5, = 2KΩ, = 5KΩ, iar pentru tranzistor se cunosc următorii parametrii: β = 200, 0 = 0, μa, = 0,6. a) ă se determine
apitolul 3 apitolul 3 26. Pentru circuitul de polarizare din fig. 26 se cunosc: = 5, = 5, = 2KΩ, = 5KΩ, iar pentru tranzistor se cunosc următorii parametrii: β = 200, 0 = 0, μa, = 0,6. a) ă se determine
Subiectul C. Acidul tartric (A) este folosit ca substanńă acidulantă în industria alimentară şi are formula de structură:
 Ministerul EducaŃiei, Cercetării, Tineretului şi Sportului Centrul NaŃional de Evaluare şi Examinare Examenul de bacalaureat 2012 Proba E. d) Proba scrisă la CHIMIE ORGANICĂ (Nivel I/Nivel II) Model Filiera
Ministerul EducaŃiei, Cercetării, Tineretului şi Sportului Centrul NaŃional de Evaluare şi Examinare Examenul de bacalaureat 2012 Proba E. d) Proba scrisă la CHIMIE ORGANICĂ (Nivel I/Nivel II) Model Filiera
Profesor Blaga Mirela-Gabriela DREAPTA
 DREAPTA Fie punctele A ( xa, ya ), B ( xb, yb ), C ( xc, yc ) şi D ( xd, yd ) în planul xoy. 1)Distanţa AB = (x x ) + (y y ) Ex. Fie punctele A( 1, -3) şi B( -2, 5). Calculaţi distanţa AB. AB = ( 2 1)
DREAPTA Fie punctele A ( xa, ya ), B ( xb, yb ), C ( xc, yc ) şi D ( xd, yd ) în planul xoy. 1)Distanţa AB = (x x ) + (y y ) Ex. Fie punctele A( 1, -3) şi B( -2, 5). Calculaţi distanţa AB. AB = ( 2 1)
Ministerul Educa iei i Cercet rii Serviciul Na ional de Evaluare i Examinare. EXAMENUL DE BACALAUREAT Prob scris la CHIMIE ORGANIC I Proba E/F
 Ministerul Educa iei i Cercet rii Serviciul Na ional de Evaluare i Examinare EXAMENUL DE BACALAUREAT - 2007 Prob scris la CHIMIE ORGANIC I Proba E/F Toate subiectele sunt obligatorii. Se acord din oficiu.
Ministerul Educa iei i Cercet rii Serviciul Na ional de Evaluare i Examinare EXAMENUL DE BACALAUREAT - 2007 Prob scris la CHIMIE ORGANIC I Proba E/F Toate subiectele sunt obligatorii. Se acord din oficiu.
Conice. Lect. dr. Constantin-Cosmin Todea. U.T. Cluj-Napoca
 Conice Lect. dr. Constantin-Cosmin Todea U.T. Cluj-Napoca Definiţie: Se numeşte curbă algebrică plană mulţimea punctelor din plan de ecuaţie implicită de forma (C) : F (x, y) = 0 în care funcţia F este
Conice Lect. dr. Constantin-Cosmin Todea U.T. Cluj-Napoca Definiţie: Se numeşte curbă algebrică plană mulţimea punctelor din plan de ecuaţie implicită de forma (C) : F (x, y) = 0 în care funcţia F este
III. Serii absolut convergente. Serii semiconvergente. ii) semiconvergentă dacă este convergentă iar seria modulelor divergentă.
 III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
Examenul de bacalaureat național 2014 Proba E. d) Chimie organică (nivel I/ nivel II)
 Ministerul Educației Naționale Centrul Național de Evaluare şi Examinare Examenul de bacalaureat național 2014 Proba E. d) Chimie organică (nivel I/ nivel II) Filiera teoretică profil real, specializarea
Ministerul Educației Naționale Centrul Național de Evaluare şi Examinare Examenul de bacalaureat național 2014 Proba E. d) Chimie organică (nivel I/ nivel II) Filiera teoretică profil real, specializarea
Asupra unei inegalităţi date la barajul OBMJ 2006
 Asupra unei inegalităţi date la barajul OBMJ 006 Mircea Lascu şi Cezar Lupu La cel de-al cincilea baraj de Juniori din data de 0 mai 006 a fost dată următoarea inegalitate: Fie x, y, z trei numere reale
Asupra unei inegalităţi date la barajul OBMJ 006 Mircea Lascu şi Cezar Lupu La cel de-al cincilea baraj de Juniori din data de 0 mai 006 a fost dată următoarea inegalitate: Fie x, y, z trei numere reale
Unitatea atomică de masă (u.a.m.) = a 12-a parte din masa izotopului de carbon
 ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
1. PROPRIETĂȚILE FLUIDELOR
 1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
R R, f ( x) = x 7x+ 6. Determinați distanța dintre punctele de. B=, unde x și y sunt numere reale.
 5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
MARCAREA REZISTOARELOR
 1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor X) functia f 1
 Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
Curs 1 Şiruri de numere reale
 Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Subiecte Clasa a VII-a
 lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
TEST VI CHIMIE ORGANICA
 TEST VI CHIMIE ORGANICA 1. AlegeŃi afirmańia adevărată: A. prin analiza elementală calitativă nu se pot determina elementele prezente într-un compus organic B. în compuşii organici sunt preponderente legăturile
TEST VI CHIMIE ORGANICA 1. AlegeŃi afirmańia adevărată: A. prin analiza elementală calitativă nu se pot determina elementele prezente într-un compus organic B. în compuşii organici sunt preponderente legăturile
CAP. 4. ALCHENE 10. Despre adiţia apei la alchene nesimetrice sunt adevărate afirmaţiile: 1. Referitor la alchene sunt adevărate afirmaţiile:
 CAP. 4. ALCHENE 1. Referitor la alchene sunt adevărate afirmaţiile: A. se mai numesc şi parafine B. se mai numesc şi olefine C. au formula generală C nh 2n D. se mai numesc şi acetilene E. au structură
CAP. 4. ALCHENE 1. Referitor la alchene sunt adevărate afirmaţiile: A. se mai numesc şi parafine B. se mai numesc şi olefine C. au formula generală C nh 2n D. se mai numesc şi acetilene E. au structură
Subiecte Clasa a VIII-a
 Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
Activitatea A5. Introducerea unor module specifice de pregătire a studenţilor în vederea asigurării de şanse egale
 Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educaţiaşiformareaprofesionalăînsprijinulcreşteriieconomiceşidezvoltăriisocietăţiibazatepecunoaştere
Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educaţiaşiformareaprofesionalăînsprijinulcreşteriieconomiceşidezvoltăriisocietăţiibazatepecunoaştere
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor
 Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile
 Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
1 C L A S A a I X - a
 9 Clasa Numele și prenumele elevului: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Ediția a V-a, 2017 Formular de concurs Clasa a IX-a, CHIMIE APLICATĂ ÎN PROTECȚIA MEDIULUI Toate
9 Clasa Numele și prenumele elevului: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Ediția a V-a, 2017 Formular de concurs Clasa a IX-a, CHIMIE APLICATĂ ÎN PROTECȚIA MEDIULUI Toate
riptografie şi Securitate
 riptografie şi Securitate - Prelegerea 12 - Scheme de criptare CCA sigure Adela Georgescu, Ruxandra F. Olimid Facultatea de Matematică şi Informatică Universitatea din Bucureşti Cuprins 1. Schemă de criptare
riptografie şi Securitate - Prelegerea 12 - Scheme de criptare CCA sigure Adela Georgescu, Ruxandra F. Olimid Facultatea de Matematică şi Informatică Universitatea din Bucureşti Cuprins 1. Schemă de criptare
a n (ζ z 0 ) n. n=1 se numeste partea principala iar seria a n (z z 0 ) n se numeste partea
 Serii Laurent Definitie. Se numeste serie Laurent o serie de forma Seria n= (z z 0 ) n regulata (tayloriana) = (z z n= 0 ) + n se numeste partea principala iar seria se numeste partea Sa presupunem ca,
Serii Laurent Definitie. Se numeste serie Laurent o serie de forma Seria n= (z z 0 ) n regulata (tayloriana) = (z z n= 0 ) + n se numeste partea principala iar seria se numeste partea Sa presupunem ca,
2. ECHILIBRE CU TRANSFER DE ELECTRONI. 2.1 Aspecte generale. 2.2 Reacţii între oxidanţi şi reducatori. Chimie Analitică
 . ECHILIBRE CU TRANSFER DE ELECTRONI. Aspecte generale În cazul unui echilibru de forma: Donor Acceptor + π (.) Dacă particula π este electron avem un echilibru cu transfer de electroni sau un echililibru
. ECHILIBRE CU TRANSFER DE ELECTRONI. Aspecte generale În cazul unui echilibru de forma: Donor Acceptor + π (.) Dacă particula π este electron avem un echilibru cu transfer de electroni sau un echililibru
Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu
 Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu Ediția a-5-a, 18 noiembrie 2017, Iași Clasa a XII-a, secțiunea a-2-a: Chimie Aplicată în Protecția Mediului Alegeţi răspunsul corect
Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu Ediția a-5-a, 18 noiembrie 2017, Iași Clasa a XII-a, secțiunea a-2-a: Chimie Aplicată în Protecția Mediului Alegeţi răspunsul corect
Curs 2 DIODE. CIRCUITE DR
 Curs 2 OE. CRCUTE R E CUPRN tructură. imbol Relația curent-tensiune Regimuri de funcționare Punct static de funcționare Parametrii diodei Modelul cu cădere de tensiune constantă Analiza circuitelor cu
Curs 2 OE. CRCUTE R E CUPRN tructură. imbol Relația curent-tensiune Regimuri de funcționare Punct static de funcționare Parametrii diodei Modelul cu cădere de tensiune constantă Analiza circuitelor cu
ASISTENȚĂ MEDICALĂ GENERALĂ Chimie Organică Varianta A
 ASISTENȚĂ MEDICALĂ GENERALĂ Chimie Organică Varianta A 1. Alegeți afirmația corectă : A. pirogalolul este un fenol ce contine doua grupari OH B. fenolii au caracter acid mai pronuntat decat alcolii C.
ASISTENȚĂ MEDICALĂ GENERALĂ Chimie Organică Varianta A 1. Alegeți afirmația corectă : A. pirogalolul este un fenol ce contine doua grupari OH B. fenolii au caracter acid mai pronuntat decat alcolii C.
Lectia 4 proiect-17.10.2010 Clasa a VIII-a Grupa de performanta. Mulaje, chituri pentru geamuri FeSO 4.7H 2 0 Calaican Mordant in vopsitorie
 Lectia 4 proiect-17.10.2010 Clasa a VIII-a Grupa de performanta COMPOZITIA PROCENTUALA A UNUI AMESTEC.SOLUTII.CRISTALOHIDRATI. REGULA DREPTUNGIULUI O serie de substante retin un numar de molecule de apa,
Lectia 4 proiect-17.10.2010 Clasa a VIII-a Grupa de performanta COMPOZITIA PROCENTUALA A UNUI AMESTEC.SOLUTII.CRISTALOHIDRATI. REGULA DREPTUNGIULUI O serie de substante retin un numar de molecule de apa,
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2015 DISCIPLINA: CHIMIE ORGANICĂ
 Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2015 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2015 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
VII.2. PROBLEME REZOLVATE
 Teoria Circuitelor Electrice Aplicaţii V PROBEME REOVATE R7 În circuitul din fiura 7R se cunosc: R e t 0 sint [V] C C t 0 sint [A] Se cer: a rezolvarea circuitului cu metoda teoremelor Kirchhoff; rezolvarea
Teoria Circuitelor Electrice Aplicaţii V PROBEME REOVATE R7 În circuitul din fiura 7R se cunosc: R e t 0 sint [V] C C t 0 sint [A] Se cer: a rezolvarea circuitului cu metoda teoremelor Kirchhoff; rezolvarea
Concurs Acad. Cristofor Simionescu Clasa a IX-a - chimie Toate subiectele sunt obligatorii, 1 singur răspuns corect.
 oncurs Acad. ristoor Simionescu lasa a IX-a - chimie Toate subiectele sunt obligatorii, 1 singur răspuns corect. 1. Într-un atom de magneziu, care are Z = 12 şi A = 24: a) numărul protonilor = b) numărul
oncurs Acad. ristoor Simionescu lasa a IX-a - chimie Toate subiectele sunt obligatorii, 1 singur răspuns corect. 1. Într-un atom de magneziu, care are Z = 12 şi A = 24: a) numărul protonilor = b) numărul
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ
 Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
CHIMIE ORGANICĂ NUTRIȚIE ȘI DIETETICĂ TEHNICĂ DENTARĂ VARIANTA A
 CHIMIE ORGANICĂ NUTRIȚIE ȘI DIETETICĂ TEHNICĂ DENTARĂ VARIANTA A 1. Alegeți afirmația corectă : A. pirogalolul este un fenol ce conține două grupări OH B. fenolii au caracter acid mai pronunțat decât alcolii
CHIMIE ORGANICĂ NUTRIȚIE ȘI DIETETICĂ TEHNICĂ DENTARĂ VARIANTA A 1. Alegeți afirmația corectă : A. pirogalolul este un fenol ce conține două grupări OH B. fenolii au caracter acid mai pronunțat decât alcolii
GEOMETRIE PLANĂ TEOREME IMPORTANTE ARII. bh lh 2. abc. abc. formula înălţimii
 GEOMETRIE PLNĂ TEOREME IMPORTNTE suma unghiurilor unui triunghi este 8º suma unghiurilor unui patrulater este 6º unghiurile de la baza unui triunghi isoscel sunt congruente într-un triunghi isoscel liniile
GEOMETRIE PLNĂ TEOREME IMPORTNTE suma unghiurilor unui triunghi este 8º suma unghiurilor unui patrulater este 6º unghiurile de la baza unui triunghi isoscel sunt congruente într-un triunghi isoscel liniile
Algebra si Geometrie Seminar 9
 Algebra si Geometrie Seminar 9 Decembrie 017 ii Equations are just the boring part of mathematics. I attempt to see things in terms of geometry. Stephen Hawking 9 Dreapta si planul in spatiu 1 Notiuni
Algebra si Geometrie Seminar 9 Decembrie 017 ii Equations are just the boring part of mathematics. I attempt to see things in terms of geometry. Stephen Hawking 9 Dreapta si planul in spatiu 1 Notiuni
