a) Kateri tip hibridnih orbital na klorovem atomu uporabimo? a) Kateri tip hibridnih orbital na fosforjevem atomu uporabimo?
|
|
|
- Ευρυδίκη Αντωνιάδης
- 7 χρόνια πριν
- Προβολές:
Transcript
1 76. Narišite strukturo karbonatnega iona. Upoštevajte dejstvo, da so vse vezi enako dolge. Kateri tip hibridizacije na ogljikovem atomu moramo uporabiti? Ogljik je element 4. skupine. a) sp 2 b) sp 3 c) dsp 2 d) dsp Nitratni ion je planaren. Vse vezi v ionu so enako dolge. Narišite resonančne (kanonske) strukture tega iona, če veste, da je dušik element 5. skupine. 78. Narišite strukturo sulfatnega iona. Upoštevajte dejstvo, da so vse vezi enako dolge. Kateri tip hibridizacije na žveplovem atomu moramo uporabiti? a) sp 2 b) sp 3 c) dsp 2 d) dsp Narišite strukturno formulo perkloratnega iona. a) Kateri tip hibridnih orbital na klorovem atomu uporabimo? b) Kako upoštevamo dejstvo, da so vse vezi klor kisik enako dolge? 80. Narišite molekulo ksenonovega difluorida, če veste, da je ksenon žlahtni plin, fluor pa element 7. skupine. 81. Narišite strukturno formulo fosfatnega iona. a) Kateri tip hibridnih orbital na fosforjevem atomu uporabimo? b) Kako upoštevamo dejstvo, da so vse vezi fosfor kisik enako dolge? 82. Kateri tip hibridnih orbital na Xe atomu uporabimo za razlago strukture molekule XeF 4? Narišite strukturno formulo molekule. a) sp 2 b) dsp 2 c) dsp 3 d) d 2 sp 3 19
2 83. Koliko veznih (vez) in neveznih (nevez) elektronskih parov je v Lewisovi strukturi molekule ogljikovega oksida? a) 1 vez in 4 nevez elektronski pari b) 2 vez in 3 nevez elektronski pari c) 3 vez in 2 nevezna elektronska para d) 3 vez in 1 nevezni elektronski par 84. Ocenite kolikšna je dolžina vezi ogljik- kisik v molekuli ogljikovega dioksida. Pomagajte si s podatki: C C: 154 pm, C=C: 120 pm, C O: 143 pm, O O: 145 pm, O=O: 121 pm. a) 120 pm b) >130 pm c) 140 pm d) >150 pm 85. V katerem delcu je trojna vez? a) NH 3 b) HCCl 3 c) NO 3 d) CO 3 2 e) CN 86. Katere vezi so najbolj polarne? a) N H v NH 3 b) O H v H 2 O c) P H v PH 3 d) S H v H 2 S e) C H v CH Katere trditve so pravilne za lastnosti vezi v : a) CsF polarna kovalentna vez b) F 2 polarna kovalentna vez c) NO nepolarna kovalentna vez d) HCl polarna kovalentna vez e) ICl ionska vez 88. Katere molekule moramo predstaviti z več kanonskimi strukturami? Nrišite njihove strukturne formule. a) F 2 b) CO c) OF 2 d) SO 2 e) CO 2 20
3 89. Pri katerih molekulah, pri risanju njihovih strukturnih formul, ne upoštevamo pravilo okteta? a) BF 3 b) OF 2 c) HNO 3 d) PF 5 e) NF Katere molekule imajo dipol? Narišite njihove strukturne formule. a) CO 2 b) SO 2 c) BCl 3 d) NH 3 e) CCl Katere molekule nimajo dipola? Narišite njihove strukturne formule. a) H 2 S b) BeCl 2 c) OF 2 d) SF 6 e) PCl Kateri ion ima piramidalno strukturo? Narišite strukturno formulo tega iona. a) ClO b) ClO 2 c) ClO 3 d) ClO Katera molekula ni polarna? Narišite njeno strukturno formulo. a) HCN b) CHCl 3 c) H 2 O d) IF 5 e) PCl Kakšno obliko ima molekula BrF 5 a) kvadratno-planarno b) trigonalno-bipiramidalno c) kvadratno-piramidalno d) oktaedrično 95. Katera molekula ni linearna? Narišite njeno strukturno formulo. Če je potrebno dodajte še komentar. a) BeH 2 b) C 2 H 2 c) HCN d) O 3 e) CO Katera molekula ali ion je polaren? Narišite strukturno formulo tega delca. a) NBr 3 b) CH 4 c) CS 2 d) NH 4 + e) PF 5 21
4 97. Katere molekule kjub polarnim vezem, nimajo dipola? Narišite njihove strukturne formule. a) BeF 2 b) NH 3 c) CO 2 d) CH 3 Cl e) SF Ocenite kolikšna je dolžina vezi N Br v molekuli NBr 3. Pomagajte si s podatki: N N: 145 pm, N=N: 123 pm, Br Br: 228 pm a) 373 pm b) 351 pm c) 187 pm d) 125 pm 99. Kvadratno-piramidalno obliko molekul lahko opišemo z naslednjim tipom hibridnih orbital na centralnem atomu: a) sp 3 b) sp 3 d c) sp 2 d d) sp 3 d Katere orbitale na dušikovem atomu uporabimo za razlago vezi v ionu NH 4 +? a) s b) p c) sp d) sp 2 e) sp Obkrožite nepravilno trditev za ion AsF 6 in narišite njegovo strukturno formulo. a) Na As- atomu predpostavimo d 2 sp 3 hibridne orbitale. b) Ion ima oktaedrično obliko. c) Ion nima π-vezi. d) Ion ima en nevezni elektronski par. e) Ion ima šest σ-vezi Ena od kanonskih struktur molekule N 2 O je N N O Katere orbitale na centralnem dušikovem atomu uporabimo za razlago te kanonske strukture? a) Štiri sp 3 -orbitale. b) Tri sp 2 -orbitale in eno 2p-orbitalo. c) Dve sp 2 -orbitali in eno 2p-orbitalo. d) Dve sp-orbitali in dve 2p-orbitali e) 2s-orbitalo in dve 2p-orbitali Katere orbitale uporabimo na dušikovem atomu za opis vezi v ionu NO 2? a) sp b) sp 2 c) sp 3 d) sp 2 d 22
5 104. S katerim tipom hibridnih orbital na centralnem atomu lahko razložimo molekule in ione: PF 6 centralni atom tip hibrinih orbital COS SiCl 4 NO 3 AsF 5 Dodatek: Energetski nivoji MO orbital za dvoatomne molekule elementov 2. periode Li 2 N 2 O 2 Ne 2 Li 2 N 2 σ 2s σ 2s * π 2p σ 2p π 2p * σ 2p * O 2 Ne 2 σ 2s σ 2s * σ 2p π 2p π 2p * σ 2p * 23
6 105. Katere MO-orbitale imajo nižjo energijo? a) σ 1s * ali σ 1s b) σ 2s ali σ 2p c) σ * 1s ali σ 2s d) σ 2p ali * σ 2p 106. Izračunajte red vezi in določite magnetizem v molekulah in ionih. red vezi magnetizem a) H + 2 (Z=1) b) H 2 (Z=1) c) He 2 (Z=2) d) Li 2 (Z=3) e) Li 2 + (Z=3) e) Be 2 (Z=4) Obkrožite delce, ki ne obstajajo Katera molekula ima večjo energijo vezi Li 2 ali C 2 Molekula: Ustrezni dokaz: 108. S katero razporeditvijo MO-orbital v energijskem diagramu lahko razložimo dejstvo, da je molekula C 2 diamagnetna? Narišite energijski diagram in izračunajte red vezi molekule C Katere so nepravilne trditve za ion N 2 +? a) Red vezi v ionu je 2,5. b) Ima en samski elektron. c) V MO-orbitali σ 2p je en elektron. d) Ion je diamagneten. e) V MO-orbitalah je devet elektronov. 24
7 110.a) Ustrezno dopolnite manjkajoče energetske nivoje molekulskih orbital (?) in atomskih orbital (?) za ion C 2 2. V molekulske orbitale narišite ustrezno število elektronov iona C 2 2 ter določite red vezi in magnetne lastnosti iona. Vrstno število ogljika je 6. AO(ogljik) MO AO(ogljik) σ * 2p π * 2p? σ 2p? π 2p σ * 2s σ 2s?? Red vezi: Magnetne lastnosti: b) Narišite Lewisovo strukturno formulo za C 2 2 ion 111. Kateri delec je stabilnejši kation NO + ali molekula NO? Narišite energijska diagrama MO-orbital. Kvantitativno utemeljite svojo razlago. NO + Kvantitativna utemeljitev: NO Razlaga: 112. Kateri delec je stabilnejši kation CO + ali molekula CO? Narišite energetske nivoje MO-orbital zunanje lupine. Kvantitativno utemeljite svojo razlago. CO + Kvantitativna utemeljitev: CO Razlaga: 25
8 113. Izračunajte red vezi in določite magnetizem v ionih. red vezi magnetizem a) C 2 + b) O 2 2 c) F 2 + (Z = 6) (Z = 8) (Z = 9) 114. Dolžine vezi v delcih O 2 +, O 2, O 2 in O 2 2 so 112, 121, 128, in 149 pm. Ali so dolžine vezi v skladu z redi vezi? Razporedite elektrone v ustrezen MO-energijski diagram in izračunajte rede vezi. Utemeljite odgovor na gornje vprašanje Uporabite ustrezna MO-energijska diagrama za iona NO + in N 2 + in določite za oba iona: a) red vezi b) magnetne lastnosti c) Kateri ion ima daljšo vez? 116. Uporabite ustrezna MO-energijska diagrama za iona CO + in CN in določite za oba iona: a) red vezi b) magnetne lastnosti c) Kateri ion ima krajšo vez? 117. V katerih molekulah lahko razložimo vezi z delokaliziranimi MO-orbitalami? a) C 2 H 4 b) C 2 H 6 c) B 2 H 6 d) H 2 CO e) SO V katerih ionih lahko razložimo vezi z delokaliziranimi MO-orbitalami? a) NH 4 + b) H 3 O + c) CO 3 2 d) CH 3 COO 26
9 119. Molekule etanojske kisline tvorijo dimere. Narišite strukturno formulo dimera in označite nevezne elektronske pare. Katere vezi povezujejo molekuli v dimeru? Posebej jih označite Pri katerih pogojih se ogljikov dioksid obnaša približno tako kot idealni plin a) T = 100 o C, P = 1000 kpa b) T = 200 o C, P = 50 kpa c) T = 0 o C, P = 50 kpa d) T = 100 o C, P = 1000 kpa 121. Obkrožite pravilne trditve. Tekočina zavre pri višji temperaturi: a) če zvišamo temperaturo tekočine b) če zvišamo tlak nad tekočino c) če povečamo prostornino tekočine d) če sta tekočina in njene pare v ravnotežju 122. Smiselno dopolnite stavek. a) Vpliv tlaka na tališče neke snovi je, kot na vrelišče b) Voda se razlikuje od večine snovi saj je njeno tališče pri temperaturi, kadar tlak povečamo c) Površinska napetost tekočine je pri višji temperaturi Ena od spodaj napisanih snovi je pri sobni temperaturi v tekočem stanju. I) Katera? Obkrožite jo. a) C 2 H 6 b) N 2 c) CO 2 d) C 2 H 5 OH II) Zakaj je spojina, ki ste jo določili, v tekočem stanju? a) Zaradi vodikovih vezi. b) Zaradi van der Waalsovih vezi. c) Zaradi kovalentnih vezi: d) Ker je spojina polarna. e) Ker spojina ni polarna Katera od naslednjih trditev je pravilna, če primerjate 1,0 g vodika in 4 g helija pri tlaku 101,3 kpa in T = 0 o C? Relativna atomska masa vodika je 1, helija pa 4. a) Oba plina nimata enake povprečne kinetične energije. b) Povprečna hitrost molekul je v obeh plinih ni enaka. c) Prostornina obeh plinov je enaka. d) Množina obeh plinov je enaka 27
10 125. V vsaki vrstici obkrožite snov za katero velja trditev napisana v isti vrstici. a) Cl, Ar, K Ima najmanjšo ionizacijsko energijo. b) CO 2, NH 3, CO Nima dipolnega momenta. c) CH 4, HCl, HF Ima najvišje vrelišče. d) Cl 2, Br 2, I 2 Ima najnižje vrelišče. e) HCl, HBr, HI Je najšibkejša kislina Katere trditve so pravilne? a) Ko plin stisnemo se množina plina zmanjša. b) Vsi idealni plini imajo enako gostoto pri istih pogojih. c) Dušik difundira skozi porozno membrano pri isti temperaturi hitreje kot kisik. d) Za vse pline velja, da so pri istih pogojih v enakih prostorninah plinov enake množine plinov. e) V enem gramu vodika je enako število molekul, kot je atomov v 4g helija. f) Totalni tlak plinske zmesi plinov X in Y je 364 kpa. Parcialni tlak plina X je 91 kpa. V posodi je 3-krat večje število molekul plinay kot molekul plina X Tekočina in pare tekočine so v zaprti posodi v ravnotežju, če: a) sta hitrosti izparevanja tekočine in kondenzacija pare v tekočino enaki. b) spemenimo temperaturo v posodi in se parni tlak nič ne spremeni. c) molekule tekočine ne morejo več prehajati v parno fazo. d) dodamo vodno paro v posodo in ta ne kondenzira v tekočino V zaprti izolirani posodi sta tekočina in njena para v ravnotežju. Zelo majhen del prostornine posode zavzema tekočina. Prostornino posode zmanjšamo za polovico. Vzpostavi se novo ravnotežno stanje. Ali se bo spremenila temperatura v posodi? 129. Vrelišče acetona je pri temperaturi 56,2 ºC. Pri kateri temperature bo aceton zavrel pri tlaku 0.50 kpa.? a) 156 ºC b) 82 ºC c) 49 ºC d) 6 ºC 130. Delci spojine A so nepolarne molekule, delci spojine B pa polarne molekule. Obe spojini imata enako molsko maso. Obkrožite pravilno trditev: a) Obe spojini imata vrelišče pri isti temperaturi. b) Spojina A zavre pri nižji temperaturi kot spojina B. c) Spojina A zavre pri višji temperaturi kot spojina B d) Spojina B zavre pri nižji temperaturi kot spojina A Katera spojina ima najvišje vrelišče? a) NH 3 b) HF c) H 2 O d) CH 4 28
11 132. Katere trditve so pravilne? a) Če helij ekspandiramo pri T = 210 C, se plin ohlaja. b) Če kisik ekspandiramo pri T = 500 C se plin ohlaja. c) Žveplov dioksid lahko utekočinimo pri T = 0 C in P = kpa d) Metan lahko utekočinimo pri T = 0 C in P = kpa Helij ima inverzno T pri 36 K kisik pa pri 1034 K Ostale podatke najdete v tabeli Katere od naštetih snovi so pri tlaku 10,13 MPa in 20 C lahko v tekoči fazi? Podatke poiščite v Tabeli 1 N 2, O 3, CO, CO 2, Xe, CCl 4 Odgovor: 134. Katere od naštetih snovi so pri tlaku 10,13 MPa in 100 C lahko samo v plinasti fazi? Podatke poiščite v Tabeli 1. Rn, NO, HBr, NH 3, CH 4, SO 2 Odgovor: 135. Za fazni diagram določene čiste snovi dopolnite naslednji opis. a) Snov je v območju A na faznem diagramu v agregatnem stanju. b) Kritična točka na faznem digramu je. c) Ravnotežje med med trdno in tekočo fazo te snovi predstavlja. d) Tališče te snovi se z naraščajočim tlakom. e) Snov je v območju C na faznem diagramu v agregatnem stanju. f) Ravnotežje med med plinasto in tekočo fazo te snovi predstavlja. g) Vrelišče te snovi se z zmanjšanjem tlaka. 29
12 136. Spojina AB ima trojno točko pri 57 C in 527 kpa in se, pri tlaku 700 kpa stali pri temperaturi 35 C. Kritična temperatura te spojine je 31 C, kritični tlak pa pri 7400 kpa. Pri tlaku 101,3 kpa sublimira pri 78 C. Narišite fazni diagram te spojine. Narišite fazni diagram vode, če je trojna točka pri 0,01 ºC in tlaku 0,77 kpa. Katere podatke boste še uporabili? Tabela 1 Kritična temperatura in tlak za nekatere snovi T c /K P c /MPa Ar 5,19 0,227 CCl 4 556,6 4,516 CH 4 190,56 4,599 C 6 H 6 562,05 4,895 C 2 H 2 308,33 6,139 CO 132,91 3,499 CO 2 304,14 7,375 H 2 32,97 1,293 HBr 363,2 8,55 HCl 324,7 8,31 He 5,19 0,227 NH 3 405,5 11,35 N 2 H ,7 H 2 O 647,14 22,06 H 2 S 373,2 8,94 Kr 209,41 5,50 N 2 126,21 3,39 Ne 44,4 2,76 N 2 O 309,57 7,255 N 2 O ,1 NO 180 6,48 O 2 154,6 5,043 O 3 261,1 5,57 Rn 377 6,28 SO 2 430,8 7,884 Xe 289,73 5,84 30
13 137. Iz preglednih modelov osnovnih celic ugotovite: a) Formulsko enoto ionskega kristala: b) Število formulskih enot v osnovni celici: c) Koordinacijo kationa in aniona: (npr. kvadratno planarna, tetraedrična, v obliki kocke itd..): 31
14 32
15 138. V ZnO je koordinacija 4/4. Opišite strukturo te snovi z enim od najgostejših skladov. Spojina je izostrukturna z ZnS (glej model v nalogi137) Koliko formulskih enot je v osnovni celici? Opis strukture: 139. V FeO kristalizira v NaCl-strukturnem tipu. Opišite strukturo te snovi z enim od najgostejših skladov. Pomagajte si s preglednim modelom v nalogi 137. Koliko formulskih enot je v osnovni celici? Opis strukture: 140. Ionska spojina kristalizira tako, da so anioni elementa X v kubično najgostejšem skladu, kationi elementa M pa zasedajo tetraedrska mesta. Katera je prava formula spojine? a) M 2 X b) MX c) MX 2 d) MX Iz preglednega modela osnovne celice ugotovite: a) Formulsko enoto ionskega kristala: b) Število formulskih enot v osnovni celici: c) Koordinacijo aniona: (n.pr. kvadratno planarna, tetraedrična, itd...): A B 33
16 142. Ionska spojina kristalizira tako, da so anioni elementa X v kubično najgostejšem skladu, kationi elementa M pa zasedajo polovico tetraedrskih mest. Katera je prava formula spojine? a) M 2 X b) MX c) MX 2 d) MX Iz osnovne celice Li 2 S ( a = 5,88 Å) določite: a) koordinacijski števili Li + in S 2 b) število formulskih enot v osnovni celici c) gostoto Li 2 S 144. Vzdolž roba c osnovne celice je dvoštevna vijačna os na polovici roba a. Narišite ekvivalentne in identične lege trikotnika do 2 c. 2c c a 34
17 145. Vzdolž roba a osnovne celice je zrcalno drsna ravnina na višini c/2. Narišite ekvivalentne in identične lege trikotnika do razdalje 2a, če je translacija polovica roba (?) osnovne celice. c/2 a 2a 146. Iz preglednega modela osnovne celice diamanta ugotovite: a) Število atomov ogljika v osnovni celici: b) Koordinacijo ogljikovega atoma (npr. kvadratno planarna, linearna, itd...): c) Opišite položaje atomov v osnovni celici diamanta s KNS: 147. Kakšno je razmerje radijev r(na + )/ r(cl ) v strukturi NaCl? 35
18 148. PtO, PdO, PtS, in PdS kristalizirajo v tetragonalnem kristalnem sistemu. Pri določenih pogojih lahko pripravimo mešane kristale teh spojin. Kakšna bi bila enostavna formula» ionske spojine«, če je množinsko razmerje ionov v mešanem kristalu n(pt 2+ ) : n(pd 2+ ) : n(o 2 ) : n(s 2 ) = 3 : 1 : 2 : 2? Enostavna formula : 149. Narišite shemo enegetskih nivojev v polprevodniku tipa p Obkrožite polprevodnik tip-p a) aluminij s sledovi skandija b) berilij s sledovi barija c) germanij s sledovi arzena d) silicij s sledovi bora 151. Germanij dopiramo z aluminijem. Kakšne vrste je polprevodnik? a) polprevodnik tip-n b) polprevodnik tip-p c) polprevodnik tip p-n-p d) polprevodnik tip n-p-p 152. Diamant je izolator, ker: a) so vsi elektroni ogljikovih atomov v prevodnem pasu b) elektroni iz valenčnega pasu ne morejo preiti v prevodni pas, ker so močno vezani na jedra ogljikovih atomov c) elektroni z valenčnega pasu ne morejo preiti v prevodni pas zaradi širokega prepovedanega pasu 36
19 d) so vezi med atomi v diamantu premočne, da bi atomi prevajali električni tok 153. Obkrožite nepravilno trditev za silicij, ki je dopiran s fosforjem a) Fosfor je donorski atom. b) Fosfor ima 5 valenčnih elektronov. c) To je povprevodnik tip-p. d) Vsak fosforjev atom je vezan s štirimi silicijevimi atomi a) Katere faze tekočih kristalov poznate? b) Narišite orientiranost molekul v posameznih fazah tekočih kristalov Izračunajte standardno entalpijo reakcije za redukcijo Fe 2 O 3 z aluminijem. Al 2 O 3 (s): H o tv = 1676,22 kj/mol Fe 2 O 3 (s): H o tv = 825,30 kj/mol 156. Toplota, ki se sprosti pri gorenju 1 mola etina pri 25 o C je 1304,94 kj/mol. Izračunajte standardno tvorbeno entalpijo etina. CO 2 (g): H o tv = 395,22 kj/mol H 2 O(l): H o tv = 286,86 kj/mol 157. Koliko toplote je potrebno, da pripravimo 1 kg CaC 2 z reakcijo: CaO(s) + 3C(s) CaC 2 (s) + CO(g) CaO(s): H o tv = 637,98 kj/mol CaC 2 (s): H o tv = 63,0 kj/mol CO(g): H o tv = 110,88 kj/mol 158. Pri gorenju 1 mol CH 4 (g) se sprosti 890,3 kj toplote. Napišite in uredite enačbo in izračunajte standardno tvorbeno entalpijo metana. CO 2 (g): H o tv = 393,8 kj/mol H 2 O(l): H o tv = 285,9 kj/mol 37
20 159. Produkcija vodnega plina je endotermna reakcija. C(s) + H 2 O(g) H 2 (g) + CO(g) Toploto, ki se pri reakciji porablja proizvedemo z gorenjem ogljika v zraku. Koliko gramov ogljika moramo sežgati, da dobimo dovolj toplote, da pretvorimo 100 g ogljika v vodni plin? H 2 O(g): H o tv = 242,76 kj/mol CO(g): H o tv = 110,88 kj/mol CO 2 (g): H o tv = 395,22 kj/mol 160. Toplota, ki se sprosti pri gorenju 1 mol C 2 H 6 (etan) je 1566,18 kj ali 1 mol C 2 H 4 (eten) je 1416,66 kj. Izračunajte standardno reakcijsko entalpijo za naslednjo reakcijo: C 2 H 4 (g) + H 2 (g) C 2 H 6 (g) Kateri podatek manjka? Poiščite ga v drugih nalogah Izračunajte standardno tvorbeno entalpijo za H 2 S. Pomagajte si z naslednjo shemo: H 2 (g) + S(g) H 2 S(g) (H 2 O(l)): H o tv= 286 kj/mol (SO 2 (g)): H o tv= 297 kj/mol + 11/2 O 2 (g) H o r = 562 kj/mol H 2 O(l) + SO 2 (g) 162. Izračunajte standardno reakcijsko entalpijo za reakcijo: N 2 O 4 (g) + Cl 2 (g) 2NOCl(g) + O 2 (g) iz podatkov: NOCl(g) NO(g) + ½ Cl 2 (g) NO(g) + 1/2O 2 (g) NO 2 (g) 2NO 2 (g) N 2 O 4 (g) H o r = 37,78 kj/mol H o r = 56,53 kj/mol H o r = 58,03 kj/mol 38
21 163. Izračunajte standardno reakcijsko entalpijo za reakcijo: 2LiH(s) + O 2 (g) Li 2 O(s) + H 2 O(l) iz podatkov: 2LiOH(s) Li 2 O(s) + H 2 O(l) LiH(s) + H 2 O(l) LiOH(s) + H 2 (g) H 2 (g) + 1/2O 2 (g) H 2 O(l) H o r = 379,1 kj/mol H o r = 111,0 kj/mol H o tv = 285,9 kj/mol 39
Osnovne stehiometrijske veličine
 Osnovne stehiometrijske veličine Stehiometrija (grško: stoiheion snov, metron merilo) obravnava količinske odnose pri kemijskih reakcijah. Fizikalne veličine, s katerimi kemik najpogosteje izraža količino
Osnovne stehiometrijske veličine Stehiometrija (grško: stoiheion snov, metron merilo) obravnava količinske odnose pri kemijskih reakcijah. Fizikalne veličine, s katerimi kemik najpogosteje izraža količino
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * NAVODILA ZA OCENJEVANJE. Sreda, 3. junij 2015 SPLOŠNA MATURA
 Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 5. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
4. Z električnim poljem ne moremo vplivati na: a) α-delce b) β-delce c) γ-žarke d) protone e) elektrone
 1. Katera od naslednjih trditev velja za katodne žarke? a) Katodni žarki so odbijajo od katode. b) Katodni žarki izvirajo iz katode c) Katodni žarki so elektromagnetno valovanje z kratko valovno dolžino.
1. Katera od naslednjih trditev velja za katodne žarke? a) Katodni žarki so odbijajo od katode. b) Katodni žarki izvirajo iz katode c) Katodni žarki so elektromagnetno valovanje z kratko valovno dolžino.
HEMIJSKA VEZA TEORIJA VALENTNE VEZE
 TEORIJA VALENTNE VEZE Kovalentna veza nastaje preklapanjem atomskih orbitala valentnih elektrona, pri čemu je region preklapanja između dva jezgra okupiran parom elektrona. - Nastalu kovalentnu vezu opisuje
TEORIJA VALENTNE VEZE Kovalentna veza nastaje preklapanjem atomskih orbitala valentnih elektrona, pri čemu je region preklapanja između dva jezgra okupiran parom elektrona. - Nastalu kovalentnu vezu opisuje
Diferencialna enačba, v kateri nastopata neznana funkcija in njen odvod v prvi potenci
 Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Funkcijske vrste. Matematika 2. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 2. april Gregor Dolinar Matematika 2
 Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Tretja vaja iz matematike 1
 Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
3. Υπολογίστε το μήκος κύματος de Broglie (σε μέτρα) ενός αντικειμένου μάζας 1,00kg που κινείται με ταχύτητα1 km/h.
 1 Ο ΚΕΦΑΛΑΙΟ ΑΣΚΗΣΕΙΣ 1. Ποια είναι η συχνότητα και το μήκος κύματος του φωτός που εκπέμπεται όταν ένα e του ατόμου του υδρογόνου μεταπίπτει από το επίπεδο ενέργειας με: α) n=4 σε n=2 b) n=3 σε n=1 c)
1 Ο ΚΕΦΑΛΑΙΟ ΑΣΚΗΣΕΙΣ 1. Ποια είναι η συχνότητα και το μήκος κύματος του φωτός που εκπέμπεται όταν ένα e του ατόμου του υδρογόνου μεταπίπτει από το επίπεδο ενέργειας με: α) n=4 σε n=2 b) n=3 σε n=1 c)
SEMINAR IZ KOLEGIJA ANALITIČKA KEMIJA I. Studij Primijenjena kemija
 SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 22. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
1. Definicijsko območje, zaloga vrednosti. 2. Naraščanje in padanje, ekstremi. 3. Ukrivljenost. 4. Trend na robu definicijskega območja
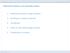 ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
Energije in okolje 1. vaja. Entalpija pri kemijskih reakcijah
 Entalpija pri kemijskih reakcijah Pri obravnavi energijskih pretvorb pri kemijskih reakcijah uvedemo pojem entalpije, ki popisuje spreminjanje energije sistema pri konstantnem tlaku. Sistemu lahko povečamo
Entalpija pri kemijskih reakcijah Pri obravnavi energijskih pretvorb pri kemijskih reakcijah uvedemo pojem entalpije, ki popisuje spreminjanje energije sistema pri konstantnem tlaku. Sistemu lahko povečamo
PONOVITEV SNOVI ZA 4. TEST
 PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
Simbolni zapis in množina snovi
 Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK
 1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
ΓΗ ΚΑΙ ΣΥΜΠΑΝ. Εικόνα 1. Φωτογραφία του γαλαξία μας (από αρχείο της NASA)
 ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
ZGRADBA ATOMA IN PERIODNI SISTEM
 ZGRADBA ATOMA IN PERIODNI SISTEM Kemijske lastnosti elementov se periodično spreminjajo z naraščajočo relativno atomsko maso oziroma kot vemo danes z naraščajočim vrstnim številom. Dmitrij I. Mendeljejev,
ZGRADBA ATOMA IN PERIODNI SISTEM Kemijske lastnosti elementov se periodično spreminjajo z naraščajočo relativno atomsko maso oziroma kot vemo danes z naraščajočim vrstnim številom. Dmitrij I. Mendeljejev,
Osnove elektrotehnike uvod
 Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
Delovna točka in napajalna vezja bipolarnih tranzistorjev
 KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
Na pregledni skici napišite/označite ustrezne točke in paraboli. A) 12 B) 8 C) 4 D) 4 E) 8 F) 12
 Predizpit, Proseminar A, 15.10.2015 1. Točki A(1, 2) in B(2, b) ležita na paraboli y = ax 2. Točka H leži na y osi in BH je pravokotna na y os. Točka C H leži na nosilki BH tako, da je HB = BC. Parabola
Predizpit, Proseminar A, 15.10.2015 1. Točki A(1, 2) in B(2, b) ležita na paraboli y = ax 2. Točka H leži na y osi in BH je pravokotna na y os. Točka C H leži na nosilki BH tako, da je HB = BC. Parabola
1. Trikotniki hitrosti
 . Trikotniki hitrosti. Z radialno črpalko želimo črpati vodo pri pogojih okolice z nazivnim pretokom 0 m 3 /h. Notranji premer rotorja je 4 cm, zunanji premer 8 cm, širina rotorja pa je,5 cm. Frekvenca
. Trikotniki hitrosti. Z radialno črpalko želimo črpati vodo pri pogojih okolice z nazivnim pretokom 0 m 3 /h. Notranji premer rotorja je 4 cm, zunanji premer 8 cm, širina rotorja pa je,5 cm. Frekvenca
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 21. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Katedra za farmacevtsko kemijo. Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks. 25/11/2010 Vaje iz Farmacevtske kemije 3 1
 Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
KOLI»INSKI ODNOSI. Kemik mora vedeti, koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane.
 KOLI»INSKI ODNOSI Kemik mora vedeti koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane 4 Mase atomov in molekul 42 tevilo delcev masa in mnoæina snovi 43 RaËunajmo maso mnoæino in πtevilo
KOLI»INSKI ODNOSI Kemik mora vedeti koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane 4 Mase atomov in molekul 42 tevilo delcev masa in mnoæina snovi 43 RaËunajmo maso mnoæino in πtevilo
Booleova algebra. Izjave in Booleove spremenljivke
 Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
Kotne in krožne funkcije
 Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ
 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
Stehiometrija za študente veterine
 Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
Θέματα Ανόργανης Χημείας Γεωπονικής ΓΟΜΗ ΑΣΟΜΩΝ
 Θέματα Ανόργανης Χημείας Γεωπονικής 1 ΓΟΜΗ ΑΣΟΜΩΝ 1. α) Γχζηε ηζξ ααζζηέξ ανπέξ μζημδυιδζδξ ημο δθεηηνμκζημφ πενζαθήιαημξ ηςκ αηυιςκ Mg (Z=12), K (Z=19), ηαζ Ag (Ε=47). Δλδβήζηε ιε ηδ εεςνία ηςκ ιμνζαηχκ
Θέματα Ανόργανης Χημείας Γεωπονικής 1 ΓΟΜΗ ΑΣΟΜΩΝ 1. α) Γχζηε ηζξ ααζζηέξ ανπέξ μζημδυιδζδξ ημο δθεηηνμκζημφ πενζαθήιαημξ ηςκ αηυιςκ Mg (Z=12), K (Z=19), ηαζ Ag (Ε=47). Δλδβήζηε ιε ηδ εεςνία ηςκ ιμνζαηχκ
Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih
 Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih različne Postopki ločevanja zmesi:iz zmesi je mogoče ločiti
Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih različne Postopki ločevanja zmesi:iz zmesi je mogoče ločiti
Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ. Παππάς Χρήστος Επίκουρος Καθηγητής
 ΗΛΕΚΤΡΟΝΙΚΗ ΟΜΗ ΚΑΙ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ Παππάς Χρήστος Επίκουρος Καθηγητής ΤΟ ΜΕΓΕΘΟΣ ΤΩΝ ΑΤΟΜΩΝ Ατομική ακτίνα (r) : ½ της απόστασης μεταξύ δύο ομοιοπυρηνικών ατόμων, ενωμένων με απλό ομοιοπολικό δεσμό.
ΗΛΕΚΤΡΟΝΙΚΗ ΟΜΗ ΚΑΙ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ Παππάς Χρήστος Επίκουρος Καθηγητής ΤΟ ΜΕΓΕΘΟΣ ΤΩΝ ΑΤΟΜΩΝ Ατομική ακτίνα (r) : ½ της απόστασης μεταξύ δύο ομοιοπυρηνικών ατόμων, ενωμένων με απλό ομοιοπολικό δεσμό.
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 10. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
*M * K E M I J A. Izpitna pola 2. Četrtek, 30. avgust 2007 / 90 minut JESENSKI ROK
 Š i f r a k a n d i d a t a : Državni izpitni center *M07243112* JESENSKI ROK K E M I J A Izpitna pola 2 Četrtek, 30. avgust 2007 / 90 minut Dovoljeno dodatno gradivo in pripomočki: Kandidat prinese s
Š i f r a k a n d i d a t a : Državni izpitni center *M07243112* JESENSKI ROK K E M I J A Izpitna pola 2 Četrtek, 30. avgust 2007 / 90 minut Dovoljeno dodatno gradivo in pripomočki: Kandidat prinese s
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 14. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
Το άτομο του Υδρογόνου
 Το άτομο του Υδρογόνου Δυναμικό Coulomb Εξίσωση Schrödinger h e (, r, ) (, r, ) E (, r, ) m ψ θφ r ψ θφ = ψ θφ Συνθήκες ψ(, r θφ, ) = πεπερασμένη ψ( r ) = 0 ψ(, r θφ, ) =ψ(, r θφ+, ) π Επιτρεπτές ενέργειες
Το άτομο του Υδρογόνου Δυναμικό Coulomb Εξίσωση Schrödinger h e (, r, ) (, r, ) E (, r, ) m ψ θφ r ψ θφ = ψ θφ Συνθήκες ψ(, r θφ, ) = πεπερασμένη ψ( r ) = 0 ψ(, r θφ, ) =ψ(, r θφ+, ) π Επιτρεπτές ενέργειες
SEKUNDARNE VEZE međumolekulske veze
 PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
fosfat fosfat H deoksiriboza H O KEMIJA Z BIOKEMIJO učbenik za študente visokošolskega strokovnega študija kmetijstva
 Cl Cl Na + Cl Na + Na + Cl Na + O H H Cl Cl O H H Na + O H H fosfat H deoksiriboza N C N fosfat H H N C C C N N C H H O H C C C N N C N deoksiriboza CH 3 C O C N O C C N fosfat H deoksiriboza H H N C H
Cl Cl Na + Cl Na + Na + Cl Na + O H H Cl Cl O H H Na + O H H fosfat H deoksiriboza N C N fosfat H H N C C C N N C H H O H C C C N N C N deoksiriboza CH 3 C O C N O C C N fosfat H deoksiriboza H H N C H
1. Arrhenius. Ion equilibrium. ก - (Acid- Base) 2. Bronsted-Lowry *** ก - (conjugate acid-base pairs) HCl (aq) H + (aq) + Cl - (aq)
 Ion equilibrium ก ก 1. ก 2. ก - ก ก ก 3. ก ก 4. (ph) 5. 6. 7. ก 8. ก ก 9. ก 10. 1 2 สารล ลายอ เล กโทรไลต (Electrolyte solution) ก 1. strong electrolyte ก HCl HNO 3 HClO 4 NaOH KOH NH 4 Cl NaCl 2. weak
Ion equilibrium ก ก 1. ก 2. ก - ก ก ก 3. ก ก 4. (ph) 5. 6. 7. ก 8. ก ก 9. ก 10. 1 2 สารล ลายอ เล กโทรไลต (Electrolyte solution) ก 1. strong electrolyte ก HCl HNO 3 HClO 4 NaOH KOH NH 4 Cl NaCl 2. weak
Ponovi in utrdi svoje znanje Rešitve
 1. poglavje: Kakšne so lastnosti vode? 10. Ni dosežena, saj podgana zaužije 188,8 mg/kg. 11. LD 50 = 0,480 mg/kg 2. poglavje: Kaj je največje čudo na Zemlji? 5. Edini stabilni izotop natrija ima masno
1. poglavje: Kakšne so lastnosti vode? 10. Ni dosežena, saj podgana zaužije 188,8 mg/kg. 11. LD 50 = 0,480 mg/kg 2. poglavje: Kaj je največje čudo na Zemlji? 5. Edini stabilni izotop natrija ima masno
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2012. Ηµεροµηνία: Τετάρτη 18 Απριλίου 2012 ΕΚΦΩΝΗΣΕΙΣ
 ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 0 Ε_.ΧλΘ(ε) ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 8 Απριλίου
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 0 Ε_.ΧλΘ(ε) ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 8 Απριλίου
KEMIJA ZA GIMNAZIJE 1
 Nataša Bukovec KEMIJA ZA GIMNAZIJE 1 Zbirka nalog za 1. letnik gimnazij VSEBINA Predgovor 1. VARN DEL V KEMIJSKEM LABRATRIJU 5 Laboratorijski inventar 5 Znaki za nevarnost opozorilne besede stavki o nevarnosti
Nataša Bukovec KEMIJA ZA GIMNAZIJE 1 Zbirka nalog za 1. letnik gimnazij VSEBINA Predgovor 1. VARN DEL V KEMIJSKEM LABRATRIJU 5 Laboratorijski inventar 5 Znaki za nevarnost opozorilne besede stavki o nevarnosti
Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Πανεπιστήμιο Δυτικής Αττικής - ΣΑΕΤ
 Γενική και Ανόργανη Χημεία Περιοδικές ιδιότητες των στοιχείων. Σχηματισμός ιόντων. Στ. Μπογιατζής 1 Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Π Δ Χειμερινό εξάμηνο 2018-2019 Π
Γενική και Ανόργανη Χημεία Περιοδικές ιδιότητες των στοιχείων. Σχηματισμός ιόντων. Στ. Μπογιατζής 1 Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Π Δ Χειμερινό εξάμηνο 2018-2019 Π
Αέρια υψηλής Καθαρότητας 2000. Ο συνεργάτης σας για Αέρια, Εξοπλισµό και Υπηρεσίες
 Αέρια υψηλής Καθαρότητας 2000 Ο συνεργάτης σας για Αέρια, Εξοπλισµό και Υπηρεσίες Αέρια Υψηλής Καθαρότητας από την MESSER Αέρια Υψηλής Καθαρότητας Το παρόν κεφάλαιο δείνει ένα πανόραµα των αερίων υψηλής
Αέρια υψηλής Καθαρότητας 2000 Ο συνεργάτης σας για Αέρια, Εξοπλισµό και Υπηρεσίες Αέρια Υψηλής Καθαρότητας από την MESSER Αέρια Υψηλής Καθαρότητας Το παρόν κεφάλαιο δείνει ένα πανόραµα των αερίων υψηλής
C M. V n: n =, (D): V 0,M : V M P = ρ ρ V V. = ρ
 »»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
»»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
ΝΟΜΟΣ ΤΗΣ ΠΕΡΙΟ ΙΚΟΤΗΤΑΣ : Οι ιδιότητες των χηµικών στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
Αλληλεπίδραση ακτίνων-χ με την ύλη
 Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
IZPIT IZ ANALIZE II Maribor,
 Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
8. Diskretni LTI sistemi
 8. Diskreti LI sistemi. Naloga Določite odziv diskretega LI sistema s podaim odzivom a eoti impulz, a podai vhodi sigal. h[] x[] - - 5 6 7 - - 5 6 7 LI sistem se a vsak eoti impulz δ[] a vhodu odzove z
8. Diskreti LI sistemi. Naloga Določite odziv diskretega LI sistema s podaim odzivom a eoti impulz, a podai vhodi sigal. h[] x[] - - 5 6 7 - - 5 6 7 LI sistem se a vsak eoti impulz δ[] a vhodu odzove z
SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK
 SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΕΡΙΕΧΟΝΤΑΙ ΚΑΙ ΟΙ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ)
 ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΕΡΙΕΧΟΝΤΑΙ ΚΑΙ ΟΙ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ) ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 9 ΙΟΥΝΙΟΥ
ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΕΡΙΕΧΟΝΤΑΙ ΚΑΙ ΟΙ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ) ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 9 ΙΟΥΝΙΟΥ
KEMIJA PRVEGA LETNIKA
 KEMIJA naravoslovna znanost oz. veda, ki proučuje zakonitosti v naravi družboslovje proučuje zakonitosti v medčloveških odnosih matematika je veda, ki služi kot pripomoček k drugim naravoslovnim in družboslovnim
KEMIJA naravoslovna znanost oz. veda, ki proučuje zakonitosti v naravi družboslovje proučuje zakonitosti v medčloveških odnosih matematika je veda, ki služi kot pripomoček k drugim naravoslovnim in družboslovnim
Fazni diagram binarne tekočine
 Fazni diagram binarne tekočine Žiga Kos 5. junij 203 Binarno tekočino predstavljajo delci A in B. Ti se med seboj lahko mešajo v različnih razmerjih. V nalogi želimo izračunati fazni diagram take tekočine,
Fazni diagram binarne tekočine Žiga Kos 5. junij 203 Binarno tekočino predstavljajo delci A in B. Ti se med seboj lahko mešajo v različnih razmerjih. V nalogi želimo izračunati fazni diagram take tekočine,
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * FIZIKA NAVODILA ZA OCENJEVANJE. Petek, 10. junij 2016 SPLOŠNA MATURA
 Državni izpitni center *M16141113* SPOMLADANSKI IZPITNI ROK FIZIKA NAVODILA ZA OCENJEVANJE Petek, 1. junij 16 SPLOŠNA MATURA RIC 16 M161-411-3 M161-411-3 3 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor
Državni izpitni center *M16141113* SPOMLADANSKI IZPITNI ROK FIZIKA NAVODILA ZA OCENJEVANJE Petek, 1. junij 16 SPLOŠNA MATURA RIC 16 M161-411-3 M161-411-3 3 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ 1 ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ
 ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
1A skupina alkalijske kovine
 1. NALOGA: KATERA IZMED SPOJIN JE NAJBOLJ TOPNA V VODI? NaCl, KBr, RbBr ALI NaF? ZAKAJ? 1. NALOGA: ODGOVOR Topnost je odvisna od mrežne entalpije ΔH mr (energija, potrebna za razgradnjo kristala na anione
1. NALOGA: KATERA IZMED SPOJIN JE NAJBOLJ TOPNA V VODI? NaCl, KBr, RbBr ALI NaF? ZAKAJ? 1. NALOGA: ODGOVOR Topnost je odvisna od mrežne entalpije ΔH mr (energija, potrebna za razgradnjo kristala na anione
Χθμικόσ Δεςμόσ (Ομοιοπολικόσ-Ιοντικόσ Δεςμόσ) Οριςμοί, αναπαράςταςη κατά Lewis, ηλεκτραρνητικότητα, εξαιρζςεισ του κανόνα τησ οκτάδασ, ενζργεια δεςμοφ
 Χθμικόσ Δεςμόσ (Ομοιοπολικόσ-Ιοντικόσ Δεςμόσ) Οριςμοί, αναπαράςταςη κατά Lewis, ηλεκτραρνητικότητα, εξαιρζςεισ του κανόνα τησ οκτάδασ, ενζργεια δεςμοφ Τβριδιςμόσ Υβριδικά τροχιακά και γεωμετρίεσ Γηαίξεζε
Χθμικόσ Δεςμόσ (Ομοιοπολικόσ-Ιοντικόσ Δεςμόσ) Οριςμοί, αναπαράςταςη κατά Lewis, ηλεκτραρνητικότητα, εξαιρζςεισ του κανόνα τησ οκτάδασ, ενζργεια δεςμοφ Τβριδιςμόσ Υβριδικά τροχιακά και γεωμετρίεσ Γηαίξεζε
Produkti krekinga so (ravno tako, kot pri radikalski substituciji) zmesi alkanov, alkenov ter cikloalkanov. Alkeni
 Kreking je cepitev daljših verig alkanov v krajše alkane, alkene in cikloalkane. H-C-C-C-C-C-H Nastane: 1) C=C + C-C-C 2) C-C + C=C-C 3) C-C + Produkti krekinga so (ravno tako, kot pri radikalski substituciji)
Kreking je cepitev daljših verig alkanov v krajše alkane, alkene in cikloalkane. H-C-C-C-C-C-H Nastane: 1) C=C + C-C-C 2) C-C + C=C-C 3) C-C + Produkti krekinga so (ravno tako, kot pri radikalski substituciji)
ΛΥΣΕΙΣ. 1. Χαρακτηρίστε τα παρακάτω στοιχεία ως διαµαγνητικά ή. Η ηλεκτρονική δοµή του 38 Sr είναι: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 5s 2
 ΛΥΣΕΙΣ 1. Χαρακτηρίστε τα παρακάτω στοιχεία ως διαµαγνητικά ή παραµαγνητικά: 38 Sr, 13 Al, 32 Ge. Η ηλεκτρονική δοµή του 38 Sr είναι: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 5s 2 Η ηλεκτρονική δοµή του
ΛΥΣΕΙΣ 1. Χαρακτηρίστε τα παρακάτω στοιχεία ως διαµαγνητικά ή παραµαγνητικά: 38 Sr, 13 Al, 32 Ge. Η ηλεκτρονική δοµή του 38 Sr είναι: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 5s 2 Η ηλεκτρονική δοµή του
Gimnazija Krˇsko. vektorji - naloge
 Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
BRONASTE PREGLOVE PLAKETE
 ŠOLSKO TEKMOVNJE IZ ZNNJ KEMIJE Z RONSTE PREGLOVE PLKETE Tekmovalna pola za. letnik. marec 08 Pred vami je deset tekmovalnih nalog, ki so različnega tipa. Pri reševanju lahko uporabljajte le priložen periodni
ŠOLSKO TEKMOVNJE IZ ZNNJ KEMIJE Z RONSTE PREGLOVE PLKETE Tekmovalna pola za. letnik. marec 08 Pred vami je deset tekmovalnih nalog, ki so različnega tipa. Pri reševanju lahko uporabljajte le priložen periodni
Logatherm WPL 14 AR T A ++ A + A B C D E F G A B C D E F G. kw kw /2013
 WP 14 R T d 9 10 11 53 d 2015 811/2013 WP 14 R T 2015 811/2013 WP 14 R T Naslednji podatki o izdelku izpolnjujejo zahteve uredb U 811/2013, 812/2013, 813/2013 in 814/2013 o dopolnitvi smernice 2010/30/U.
WP 14 R T d 9 10 11 53 d 2015 811/2013 WP 14 R T 2015 811/2013 WP 14 R T Naslednji podatki o izdelku izpolnjujejo zahteve uredb U 811/2013, 812/2013, 813/2013 in 814/2013 o dopolnitvi smernice 2010/30/U.
Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design
 Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Termodinamika vlažnega zraka. stanja in spremembe
 Termodinamika vlažnega zraka stanja in spremembe Termodinamika vlažnega zraka Najpogostejši medij v sušilnih procesih konvektivnega sušenja je VLAŽEN ZRAK Obravnavamo ga kot dvokomponentno zmes Suhi zrak
Termodinamika vlažnega zraka stanja in spremembe Termodinamika vlažnega zraka Najpogostejši medij v sušilnih procesih konvektivnega sušenja je VLAŽEN ZRAK Obravnavamo ga kot dvokomponentno zmes Suhi zrak
S t r a n a 1. 1.Povezati jonsku jačinu rastvora: a) MgCl 2 b) Al 2 (SO 4 ) 3 sa njihovim molalitetima, m. za so tipa: M p X q. pa je jonska jačina:
 S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n, l)
 ΑΤΟΜΙΚΑ ΤΡΟΧΙΑΚΑ Σχέση κβαντικών αριθµών µε στιβάδες υποστιβάδες - τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n,
ΑΤΟΜΙΚΑ ΤΡΟΧΙΑΚΑ Σχέση κβαντικών αριθµών µε στιβάδες υποστιβάδες - τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n,
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * NAVODILA ZA OCENJEVANJE. Petek, 12. junij 2015 SPLOŠNA MATURA
 Državni izpitni center *M543* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Petek,. junij 05 SPLOŠNA MATURA RIC 05 M543 M543 3 IZPITNA POLA Naloga Odgovor Naloga Odgovor Naloga Odgovor Naloga Odgovor
Državni izpitni center *M543* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Petek,. junij 05 SPLOŠNA MATURA RIC 05 M543 M543 3 IZPITNA POLA Naloga Odgovor Naloga Odgovor Naloga Odgovor Naloga Odgovor
Tabele termodinamskih lastnosti vode in vodne pare
 Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
ΘΕΜΑΤΑ Β' ΛΥΚΕΙΟΥ ΓΕΝ. ΠΑΙΔΕΙΑΣ
 ΘΕΜΑΤΑ Β' ΛΥΚΕΙΟΥ ΓΕΝ. ΠΑΙΔΕΙΑΣ ΘΕΜΑ 1 ο 1. Γενικό μοριακό τύπο C v H 2v (v 2) έχουν : α. όλοι οι άκυκλοι υδρογονάνθρακες β. τα αλκάνια γ. τα αλκένια δ. τα αλκίνια 2. Η οργανική ένωση CH 3 - CH - CH 3
ΘΕΜΑΤΑ Β' ΛΥΚΕΙΟΥ ΓΕΝ. ΠΑΙΔΕΙΑΣ ΘΕΜΑ 1 ο 1. Γενικό μοριακό τύπο C v H 2v (v 2) έχουν : α. όλοι οι άκυκλοι υδρογονάνθρακες β. τα αλκάνια γ. τα αλκένια δ. τα αλκίνια 2. Η οργανική ένωση CH 3 - CH - CH 3
Državni izpitni center K E M I J A. Izpitna pola 1. Sreda, 28. avgust 2013 / 90 minut
 Š i f r a k a n d i d a t a : ržavni izpitni center *M13243111* JESENSKI IZPITNI RK K E M I J Izpitna pola 1 Sreda, 28. avgust 2013 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno pero
Š i f r a k a n d i d a t a : ržavni izpitni center *M13243111* JESENSKI IZPITNI RK K E M I J Izpitna pola 1 Sreda, 28. avgust 2013 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno pero
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014. ÄÉÁÍüÇÓÇ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
Ισχυροί και ασθενείς ηλεκτρολύτες μέτρα ισχύος οξέων και βάσεων νόμοι Ostwald
 Ισχυροί και ασθενείς ηλεκτρολύτες μέτρα ισχύος οξέων και βάσεων νόμοι Ostwald Ποιους θα ονομάζουμε «ισχυρούς ηλεκτρολύτες»; Τις χημικές ουσίες που όταν διαλύονται στο νερό, ένα μεγάλο ποσοστό των mole
Ισχυροί και ασθενείς ηλεκτρολύτες μέτρα ισχύος οξέων και βάσεων νόμοι Ostwald Ποιους θα ονομάζουμε «ισχυρούς ηλεκτρολύτες»; Τις χημικές ουσίες που όταν διαλύονται στο νερό, ένα μεγάλο ποσοστό των mole
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002
 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
ΑΣΚΗΣΕΙΣ ΣΤΟ 1ο ΚΕΦΑΛΑΙΟ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ
 ΑΣΚΗΣΕΙΣ ΣΤΟ 1ο ΚΕΦΑΛΑΙΟ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ 1.1. ΤΡΟΧΙΑΚΑ ΚΑΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ 1.1. Ποιες είναι οι πιθανές τιµές : α) του l για : i) n = 1, ii) n = 3, β) του m l για : i) n = 2, ii) l = 2. 1.2. Να βρείτε
ΑΣΚΗΣΕΙΣ ΣΤΟ 1ο ΚΕΦΑΛΑΙΟ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ 1.1. ΤΡΟΧΙΑΚΑ ΚΑΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ 1.1. Ποιες είναι οι πιθανές τιµές : α) του l για : i) n = 1, ii) n = 3, β) του m l για : i) n = 2, ii) l = 2. 1.2. Να βρείτε
NEPARAMETRIČNI TESTI. pregledovanje tabel hi-kvadrat test. as. dr. Nino RODE
 NEPARAMETRIČNI TESTI pregledovanje tabel hi-kvadrat test as. dr. Nino RODE Parametrični in neparametrični testi S pomočjo z-testa in t-testa preizkušamo domneve o parametrih na vzorcih izračunamo statistike,
NEPARAMETRIČNI TESTI pregledovanje tabel hi-kvadrat test as. dr. Nino RODE Parametrični in neparametrični testi S pomočjo z-testa in t-testa preizkušamo domneve o parametrih na vzorcih izračunamo statistike,
ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ ΤΩΝ ΣΤΟΙΧΕΙΩΝ (1) Ηλία Σκαλτσά ΠΕ ο Γυμνάσιο Αγ. Παρασκευής
 ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ ΤΩΝ ΣΤΟΙΧΕΙΩΝ (1) Ηλία Σκαλτσά ΠΕ04.01 5 ο Γυμνάσιο Αγ. Παρασκευής Όπως συμβαίνει στη φύση έτσι και ο άνθρωπος θέλει να πετυχαίνει σπουδαία αποτελέσματα καταναλώνοντας το λιγότερο δυνατό
ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ ΤΩΝ ΣΤΟΙΧΕΙΩΝ (1) Ηλία Σκαλτσά ΠΕ04.01 5 ο Γυμνάσιο Αγ. Παρασκευής Όπως συμβαίνει στη φύση έτσι και ο άνθρωπος θέλει να πετυχαίνει σπουδαία αποτελέσματα καταναλώνοντας το λιγότερο δυνατό
matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):
![matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij): matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):](/thumbs/87/96579490.jpg) 4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
0,00275 cm3 = = 0,35 cm = 3,5 mm.
 1. Za koliko se bo dvignil alkohol v cevki termometra s premerom 1 mm, če se segreje za 5 stopinj? Prostorninski temperaturni razteznostni koeficient alkohola je 11 10 4 K 1. Volumen alkohola v termometru
1. Za koliko se bo dvignil alkohol v cevki termometra s premerom 1 mm, če se segreje za 5 stopinj? Prostorninski temperaturni razteznostni koeficient alkohola je 11 10 4 K 1. Volumen alkohola v termometru
panagiotisathanasopoulos.gr
 . Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
. Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
13. poglavje: Energija
 13. poglavje: Energija 1. (Naloga 3) Koliko kilovatna je peč za hišno centralno kurjavo, ki daje 126 MJ toplote na uro? Podatki: Q = 126 MJ, t = 3600 s; P =? Če peč z močjo P enakomerno oddaja toploto,
13. poglavje: Energija 1. (Naloga 3) Koliko kilovatna je peč za hišno centralno kurjavo, ki daje 126 MJ toplote na uro? Podatki: Q = 126 MJ, t = 3600 s; P =? Če peč z močjo P enakomerno oddaja toploto,
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
Γεωμετρία Μορίων Θεωρία VSEPR
 Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 7 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6)
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 7 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ 1ο Στις ερωτήσεις 1.1-1.4, να γράψετε στο
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 7 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ 1ο Στις ερωτήσεις 1.1-1.4, να γράψετε στο
Poglavje 10. Molekule Kovalentna vez
 Poglavje 10 Molekule Atomi se vežejo v molekule. Vezavo med atomi v molkuli posredujejo zunanji - valenčni elektroni. Pri vseh molekularnih vezeh negativni naboj elektronov posreduje med pozitinvimi ioni
Poglavje 10 Molekule Atomi se vežejo v molekule. Vezavo med atomi v molkuli posredujejo zunanji - valenčni elektroni. Pri vseh molekularnih vezeh negativni naboj elektronov posreduje med pozitinvimi ioni
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (Επιλέγετε δέκα από τα δεκατρία θέματα) ΘΕΜΑΤΑ 1. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λάθος; Γιατί; (α) Από τα στοιχεία Mg, Al, Cl, Xe, C και Ρ, τον μεγαλύτερο
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (Επιλέγετε δέκα από τα δεκατρία θέματα) ΘΕΜΑΤΑ 1. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λάθος; Γιατί; (α) Από τα στοιχεία Mg, Al, Cl, Xe, C και Ρ, τον μεγαλύτερο
*M * K E M I J A. Izpitna pola 1. Četrtek, 27. avgust 2009 / 90 minut JESENSKI IZPITNI ROK
 Š i f r a k a n d i d a t a : ržavni izpitni center *M09243111* JESENSKI IZPITNI ROK K E M I J Izpitna pola 1 Četrtek, 27. avgust 2009 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Š i f r a k a n d i d a t a : ržavni izpitni center *M09243111* JESENSKI IZPITNI ROK K E M I J Izpitna pola 1 Četrtek, 27. avgust 2009 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Kontrolne karte uporabljamo za sprotno spremljanje kakovosti izdelka, ki ga izdelujemo v proizvodnem procesu.
 Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
1.Θερμοχημεία. Η έννοια της ενθαλπίας
 1 ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ-Χ.Κ.ΦΙΡΦΙΡΗΣ 1.Θερμοχημεία Η έννοια της ενθαλπίας 1.Δίνεται το παρακάτω σχεδιάγραμμα 2.Να υπολογίσετε το ποσό θερμότητας που εκλύεται ή απορροφάται κατά την πραγματοποίηση της αντίδρασης
1 ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ-Χ.Κ.ΦΙΡΦΙΡΗΣ 1.Θερμοχημεία Η έννοια της ενθαλπίας 1.Δίνεται το παρακάτω σχεδιάγραμμα 2.Να υπολογίσετε το ποσό θερμότητας που εκλύεται ή απορροφάται κατά την πραγματοποίηση της αντίδρασης
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Ι: Ο ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΚΑΙ ΜΙΑ ΠΡΩΤΗ ΠΡΟΣΕΓΓΙΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ. Παππάς Χρήστος Επίκουρος Καθηγητής
 ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Ι: Ο ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΚΑΙ ΜΙΑ ΠΡΩΤΗ ΠΡΟΣΕΓΓΙΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Είδη Δεσμών Ιοντικός δεσμός (Ionic bond), σχηματίζεται πάντα μεταξύ ηλεκτροθετικών
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Ι: Ο ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΚΑΙ ΜΙΑ ΠΡΩΤΗ ΠΡΟΣΕΓΓΙΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Είδη Δεσμών Ιοντικός δεσμός (Ionic bond), σχηματίζεται πάντα μεταξύ ηλεκτροθετικών
V tem poglavju bomo vpeljali pojem determinante matrike, spoznali bomo njene lastnosti in nekaj metod za računanje determinant.
 Poglavje IV Determinanta matrike V tem poglavju bomo vpeljali pojem determinante matrike, spoznali bomo njene lastnosti in nekaj metod za računanje determinant 1 Definicija Preden definiramo determinanto,
Poglavje IV Determinanta matrike V tem poglavju bomo vpeljali pojem determinante matrike, spoznali bomo njene lastnosti in nekaj metod za računanje determinant 1 Definicija Preden definiramo determinanto,
Κεφάλαιο 1. Έννοιες και παράγοντες αντιδράσεων
 Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
Κατανομή μετάλλων και αμετάλλων στον Π.Π.
 Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
antična Grčija - snov zgrajena iz atomov /rezultat razmišljanja/
 ZGRADBA ATOMA 1.1 - DALTON atom (atomos nedeljiv) antična Grčija - snov zgrajena iz atomov /rezultat razmišljanja/ dokaz izpred ~ 200 let Temelj so 3 zakoni: ZAKON O OHRANITVI MASE /Lavoisier, 1774/ ZAKON
ZGRADBA ATOMA 1.1 - DALTON atom (atomos nedeljiv) antična Grčija - snov zgrajena iz atomov /rezultat razmišljanja/ dokaz izpred ~ 200 let Temelj so 3 zakoni: ZAKON O OHRANITVI MASE /Lavoisier, 1774/ ZAKON
ΑΠΑΝΤΗΣΕΙΣ ΤΩΝ ΑΣΚΗΣΕΩΝ
 ΑΠΑΝΤΗΣΕΙΣ ΤΩΝ ΑΣΚΗΣΕΩΝ Ε.1. Γ. Ε.. Β. Ε.. Α. Ε.4. Α. Ε.5. Γ. Ε.6. Β. Ε.7. Δ. Ε.8. Δ. Ε.9. Γ. Ε.1. Γ. Ε.11. Δ. Ε.1. Β. Ε.1. α: Σ, β:σ, γ:σ, δ:σ, ε:λ (είναι σωστό μόνο για ιοντικές ενώσεις, στις ομοιοπολικές
ΑΠΑΝΤΗΣΕΙΣ ΤΩΝ ΑΣΚΗΣΕΩΝ Ε.1. Γ. Ε.. Β. Ε.. Α. Ε.4. Α. Ε.5. Γ. Ε.6. Β. Ε.7. Δ. Ε.8. Δ. Ε.9. Γ. Ε.1. Γ. Ε.11. Δ. Ε.1. Β. Ε.1. α: Σ, β:σ, γ:σ, δ:σ, ε:λ (είναι σωστό μόνο για ιοντικές ενώσεις, στις ομοιοπολικές
Integralni račun. Nedoločeni integral in integracijske metrode. 1. Izračunaj naslednje nedoločene integrale: (a) dx. (b) x 3 +3+x 2 dx, (c) (d)
 Integralni račun Nedoločeni integral in integracijske metrode. Izračunaj naslednje nedoločene integrale: d 3 +3+ 2 d, (f) (g) (h) (i) (j) (k) (l) + 3 4d, 3 +e +3d, 2 +4+4 d, 3 2 2 + 4 d, d, 6 2 +4 d, 2
Integralni račun Nedoločeni integral in integracijske metrode. Izračunaj naslednje nedoločene integrale: d 3 +3+ 2 d, (f) (g) (h) (i) (j) (k) (l) + 3 4d, 3 +e +3d, 2 +4+4 d, 3 2 2 + 4 d, d, 6 2 +4 d, 2
Teorija molekulskoi orbitala linearna kombinacija atomskih orbitala(lcao)
 Teorija molekulskoi orbitala linearna kombinacija atomskih orbitala(lcao) Kada je elektron u blizini jezgre jednog atoma onda njegova valna funkcija sliči atomskoj orbitali tog atoma. Zbrajanjem atomskih
Teorija molekulskoi orbitala linearna kombinacija atomskih orbitala(lcao) Kada je elektron u blizini jezgre jednog atoma onda njegova valna funkcija sliči atomskoj orbitali tog atoma. Zbrajanjem atomskih
Če je električni tok konstanten (se ne spreminja s časom), poenostavimo enačbo (1) in dobimo enačbo (2):
 ELEKTRIČNI TOK TEOR IJA 1. Definicija enote električnega toka Električni tok je gibanje električno nabitih delcev v trdnih snoveh (kovine, polprevodniki), tekočinah ali plinih. V kovinah se gibljejo prosti
ELEKTRIČNI TOK TEOR IJA 1. Definicija enote električnega toka Električni tok je gibanje električno nabitih delcev v trdnih snoveh (kovine, polprevodniki), tekočinah ali plinih. V kovinah se gibljejo prosti
και να υπολογίσετε την ενωτική ενέργεια του κρυσταλλικού πλέγματος του. ίνονται: Ενθαλπία σχηματισμού SrCl 2
 Ποιά από τις ενώσεις NaCl και CaCl 2 είναι περισσότερο ιοντική και γιατί; Να σχεδιαστεί ο κύκλος Born-Haber για την ένωση AlF 3 Να σχεδιάσετε τον κύκλο Born-Haber της ένωσης SrCl 2 και να υπολογίσετε την
Ποιά από τις ενώσεις NaCl και CaCl 2 είναι περισσότερο ιοντική και γιατί; Να σχεδιαστεί ο κύκλος Born-Haber για την ένωση AlF 3 Να σχεδιάσετε τον κύκλο Born-Haber της ένωσης SrCl 2 και να υπολογίσετε την
Appendix B Table of Radionuclides Γ Container 1 Posting Level cm per (mci) mci
 3 H 12.35 Y β Low 80 1 - - Betas: 19 (100%) 11 C 20.38 M β+, EC Low 400 1 5.97 13.7 13 N 9.97 M β+ Low 1 5.97 13.7 Positrons: 960 (99.7%) Gaas: 511 (199.5%) Positrons: 1,199 (99.8%) Gaas: 511 (199.6%)
3 H 12.35 Y β Low 80 1 - - Betas: 19 (100%) 11 C 20.38 M β+, EC Low 400 1 5.97 13.7 13 N 9.97 M β+ Low 1 5.97 13.7 Positrons: 960 (99.7%) Gaas: 511 (199.5%) Positrons: 1,199 (99.8%) Gaas: 511 (199.6%)
