primarni minerali (minerali iz kamnin): plagioklazi, kremen, olivin
|
|
|
- Βερενίκη Αλεξόπουλος
- 6 χρόνια πριν
- Προβολές:
Transcript
1 Komponente tal primarni minerali (minerali iz kamnin): plagioklazi, kremen, olivin sekundarni minerali (preprevanje primarnih mineralov): gline, železovi oksidi, aluminijevi oksidi, sulfidi organska snov (zelo variabilna) kamnine: magmatske, metamorfne, sedimentne
2 Minerali minerali so naravne trdne anorganske snovi imajo določeno kemijsko strukturo (običajno spojine dveh ali več prvin, redko samo ene) imajo urejeno notranjo strukturo in kristalijo na določen način, značilna je ena ali več kristalnih oblik imajo značilne fizikalne lastnosti (trdota, gostota, razkolnost, lom, barva, barva črte, sijaj, prožnost)
3 Kristali kristali so trdne snovi s prostorsko urejeno notranjo strukturo omejeno z ravnimi ploskvami zrna kristaliziranih mineralov so lahko navzven nepravilnih oblik, vendar je njihova notranja zgradba urejena po obliki jih delimo v 7 kristalografskih sistemov (sigonij) z različno stopnjo simetrije
4 Ionske trdne strukture Osnovna enota kristala (enota iz katere je kristal izgrajen) a 1 = a 2 = a 3 α = β = γ = 90 0 kubična (primitivna) kubična (centrirana v kocki) kubična (centrirana na ploskvi) Značilni predstavniki: halit, pirit, granati, magnetit, fluorit, galenit, sfalerit
5 Ionske trdne strukture a 1 = a 2 =a 3 α = β = γ = 90 0 tetragonalna (primitivna) tetragonalna centrirana v tetragonu Značilni predstavniki: cirkon, piroluzit, modra galica
6 Ionske trdne strukture a 1 =a 2 =a 3 rombični (primitivni) rombični (centriran v ortorombu) rombični (centriran na ploskvi) α = β = γ =90 0 Značilni predstavniki: olivin, cojzit, nekateri pirokseni in amfiboli, aragonit, anhidrit, žveplo, barit
7 Ionske trdne strukture a 1 = a 2 =a 3 α = β = 90 0, γ = heksagonalna Značilni predstavniki: apatit
8 Ionske trdne strukture a 1 = a 2 = a 3 α = β = 60 o γ =90 0 rombohedralna Značilni predstavniki: kalcit, kremen, dolomit, hematit, turmalin
9 Ionske trdne strukture monoklinski (primitiven) monoklinski (centriran na ploskvi) a 1 =a 2 =a 3 α = β = 90 o γ =90 0 Značilni predstavniki: K-glinenci, ortoklaz, pirokseni (avgit), amfiboli (rogovača), lojevec, sljude, montmorilionit, vermikulit, ilit, serpentin, epidot, sadra, vivanit
10 Ionske trdne strukture a 1 =a 2 =a 3 triklinski α = β = γ =90 0 Značilni predstavniki: plagioklaz, kaolinit
11 Ionske trdne strukture Kristalne strukture v mineralih nastajajo glede na pravila, ki: - minimizirajo elektrostatske odbojne sile - maksimizirajo privlačne slie Nastanek minerala je opisan s Paulingovimi pravili (Linus Pauling)
12 Paulingova pravila 1. Koordinacijsko število in razmerje radijev 2. Elektrostatski valenčni princip moč valenčne vezi je s = z/cn z je naboj ali valenca kationa, CN je število kisikovih atomov koordiniranih na kation
13 Ionske trdne strukture večina talnih mineralnih struktur nastane z vezjo med O 2- in Si ali kovinskim ionom s Si so vezi kovalentne z ostalimi kovinami so vezi predvsem ionske pakiranje atomov je odvisno od njihove trde sfere Al 3+ O 2-
14 Ionske trdne strukture razporeditev ali koordinacija kationov in anionov je odvisna od razmerja radijev razmerje radijev = radij kationa/radij aniona oktahedron tetrahedron
15 Ionske trdne strukture razmerje radijev koordinacijsko št. geometrija trikotnik tetrahedron oktahedron kocka dodekahedron
16 Ionske trdne strukture Primer: silicijev oksid r c /r a = 0.29 aluminijev oksid r c /r a = 0.36 Oba, silicij in aluminij, bi morala biti v tetrahedralni koordinaciji, vendar samo silikat najdemo v tetrahedralni konformaciji.
17 Paulingova pravila 3. Stabilnost poliedrov točka do točke > rob do roba > ploskev na ploskev > >
18 Paulingova pravila 4. V kristalih, ki imajo različne katione, ostajajo visoko nabiti kationi, kar se le da daleč vsak sebi, kar zniža kristalno potencialno Columbovo energijo. 5. Število različnih konstituent je običajno majhno, kar dodatno zmanjša potencialno energijo minerala.
19 Ionske amorfne strukture Hitro kristaljenje če se nasičena talina hitro ohladi pod temperaturo tališča nastanejo številni drobni delci snov se izloči v želatinasti (amorfni) obliki z redkimi kristalnimi zrni ali brez njih
20 Talni minerali - osnovne enote Si tetrahedron Al oktahedron polimerizacija - zmanjšanje viška negativnega naboja
21 Primarni minerali: silikati so najpomembnejši minerali, ki formirajo tla klasifikacija je zasnovana glede na razporeditev povezanih silicijevih tetraedrov razvijajo se od enostavnih do kompleksnih
22 Primarni minerali: silikati Ortosilikati -otočni razmerje med silicijem in kisikom je 1 : 4 izolirani SiO 4 so med seboj povezani z oktahedralno koordiniranim Mg 2+ in Fe 2+ ubogajo Paulijevo 4 pravilo, vendar imajo kljub temu MgO 6 in FeO 6 skupno ploskev s SiO 4 predstavniki: olivin, granat naboj 4 -
23 Primarni minerali: silikati Pirosilikati -skupinski razmerje med silicijem in kisikom je 2 : 7 izolirani SiO 4 tvorijo dvojne tetrahedralne skupine SiO 4 in SiO 7 skupine so med seboj povezane z AlO 6 verigami predstavniki: epidot, alanit, cojzit naboj 3 -
24 Primarni minerali: silikati Ciklosilikati -obročni razmerje med silicijem in kisikom je 1 : 3 izolirani SiO 4 tvorijo obroče Si 6 O 18 obroči so povezani z različnimi kationi predstavniki: beril, (emerald, aquamarin), turmalin
25 Primarni minerali: silikati Inosilikati - verižni silikati enojni in dvojni inosilikati razmerje med silicijem in kisikom pri enojnih je 1 : 3 razmerje med silicijem in kisikom pri dvojnih je 4 : 11 verige so povezane z alkalijskimi in zemeljsko alkalijskimi kationi pomembni minerali, ki formirajo tla predstavniki: piroksen (enojni), amfiboli (dvojni) naboj na en Si = 2 - naboj na en Si = enojni dvojni
26 Primarni minerali: silikati Filosilikati - listasti silikati razmerje med silicijem in kisikom je pri enojnih 2 : 5 slojasti, velike strukture zaradi izomorfnih substitucij polimerizirani sloji Al-oktahedrov in Si-tetrahedrov, Al in Si plasti med seboj povezane s kisiki, ki si jih delita tvorijo zelo pomembne talne sekundarne minerale predstavniki: sljude, glineni minerali, biotit, lojevec
27 Primarni minerali: silikati Tektosilikati -ogrodni razmerje med silicijem in kisikom je pri enojnih 1 : 2 silikati si delijo kisik zelo malo prostora za nečistoče običajni mineral v zemeljski skorji predstavniki: kremen, plagioklazi (Na, K, Ca)
28 Sekundarni minerali Glineni minerali izgledajo amorfno, vendar imajo zelo drobne kristale (<1 µm) različnih orientacij en kristal je sestavljen iz 10 do 20 lamel osnovno strukturo tvorijo silicijevi tetraedri in aluminijevi oktaedri delci so lahko mešani (sljuda-vermikulit, kaolinit-vermikulit) nastajajo z delnim preperevanjem ali fiksacijo primarnih mineralov vrsto glinenih mineralov določa vrsta izvornega minerala, kemijske značilnosti okolja, klimatski pogoji, stopnja preperelosti kamnine
29 Sekundarni minerali Filosilikati - minerali glin podobni po strukturi primarnim silikatom, prihaja do zamenjave kationov klasificirani glede na število plasti so najpomembnejši minerali za delovanje tal apikalni kisik tetra kation ena plast bazalni kisiki
30 2D struktura sekundarnih mineralov Si tetrahedralna plast Al - oktahedralna plast Al-Si kombiniran sloj
31 Sekundarni minerali oktahedralne plasti kisik ali hidroksil oktahedralni kation kisik ali hidroksil trioktahedralna plast kisik ali hidroksil oktahedralni kation dioktahedralna plast kisik ali hidroksil
32 Sekundarni minerali izomorfne substitucije Silicijev tetraeder postavi dimenzije kletke, v kletko se lahko vgradijo tudi Al, Fe,Mg in drug kationi, ki imajo podobno velikost. Al 3+ Si 4+ (razvije se bolj negativni naboj) Fe 3+ Si 4+ (razvije se bolj negativni naboj) možne so še druge substitucije Mg 2+ Al 3+ (razvije se bolj negativni naboj) Al 3+ Al 3+ Mg 2+ (razvije se bolj pozitivni naboj) Fe 2+ (razvije se bolj pozitivni naboj)
33 Sekundarni minerali izomorfne substitucije do izomorfne substitucije pride med formiranjem minerala pomembne zaradi razvoja permanentnega naboja minerala pomembne za CEC (Cation Exchange Capacity, kationsko izmenjalno kapaciteto) v glineni frakciji predstavljajo mesta reaktivnosti v tleh
34 1:1 tip sekundarnega minerala plast lamela medsloj plast lamela
35 1:1 tip sekundarnega minerala stabilni minerali, ki ne nabrekajo nizek skupni naboj relativno nizko-specifična površina od ph odvisni naboji dobre fizikalne lastnosti za obdelavo tal majhna zadrževalna sposobnost za hranila uporabni za gradnjo cest, stavb, keramike, opeke heksagonalnih oblik
36 Sekundarni minerali 1:1 tip Kaolinit Al 4 Si 4 O 10 (OH) 8 dioktahdralni mineral ne prispeva veliko k CEC običajen v preperelih tleh proton omogoča močne vezi, v medsloju ni vode ali drugih ionov Halojzit podoben kaolinitu, med sloji ima vodo običajen v tleh nastalih iz vulkanskega prahu
37 2:1 tip sekundarnega ne-ekspandirajočega minerala delno ekspandirajoči dobre fizikalne karakteristike za obdelavo srednje nabiti nižje specifična površina kot pri ekspandirajočih 2:1 mineralih rodovitna tla problematični za upravljanje s K + in NH + 4
38 Sekundarni minerali Sljuda (biotit, muskovit) v tleh lahko kot primarni ali sekundarni minerali K 2 Al 4 (Al 2 Si 6 )O 20 (OH) 4 med tetrahedralnimi plastmi se ujame K (pomemben vir K) naboj je 2 - na osnovno celico, ~ 20 % Si zamenjanih z Al oktahedralna plast je lahko di ali trioktohedralna velik neto naboj privlači K + in NH 4 +, ki se optimalno prilegajo heksagonalnim odprtinam
39 Heksagonalne odprtine vezava K +, NH 4 +
40 2:1 tip sekundarnega ekspandirajočega minerala konstantno nabrekanje in krčenje slabe fizikalne karakteristike veliko površinskih nabojev velika površina bogati s hranili rodovitna tla niso občutljivi na spremembe ph predstavniki; vermikulit, smektit, talko, pirofilit
41 Sekundarni minerali Vermikulit podobna struktura kot sljuda, vendar nižji naboj (0.6 do 0.9 na osnovno celico, izomorfne substitucije predvsem v tetrahedralnem sloju zmožnost fiksacije K +, v medsloju veliko Mg 2+, ki povezuje na vsaki strani po eno plast vode oktahedralna plast je lahko di ali trioktohedralna pomemben talni mineral Mg hidratirana plast tetra okta tetra
42 Sekundarni minerali Smektit (montmorilonit) podobna struktura kot sljuda, vendar nižji naboj (0.2 do 0.6 na osnovno celico) izomorfne substitucije predvsem v oktahedralnem sloju, Mg 2+ ali Fe 2+ nezmožnost fiksacije kalija medlamelarne plasti povezane samo z Van der Waalsovimi vezmi oktahedralna plast je lahko di ali trioktohedralna pomemben talni mineral
43 Sekundarni minerali Krčenje in nabrekanje smektita (montmorilionita) manjši naboj ionska moč je v oktahedralnem sloju Columbova sila F ( z )( z d + ) ekspanzija minerala pri hidrataciji
44 2:1:1 tip sekundarnega minerala ne-ekspandirajoči minerali zelo majhno nabrekanje in krčenje dobre fizikalne karakteristike omejeni naboji na površini rodovitna tla niso občutljivi na spremembe ph
45 Sekundarni minerali Klorit podobna struktura kot sljuda, vendar naboj uravnotežen s plastjo hidroksida lahko di ali trioktahedralni manj pomemben talni mineral tetra okta tetra Mg, Fe, Al hidroksid
46 Sekundarni minerali 1:1 tip kaolinit halojzit H 2 O 2:1 tip (neekspandirajoči) sljuda/ilit vermikulit :1:1 tip klorit (2:1:1) H 2 O :1 tip (neekspandirajoči) smektit (montmorilionit) H 2 O + H 2+ O H 2 O
47 Organizacija tetrahedralnih in oktahedralnih slojev 0.7 nm tetrahedralni sloj oktahedralni sloj tetrahedralni sloj oktahedralni sloj kaolinit (1:1) neekspandirajoč 1-2 nm tetrahedralni sloj oktahedralni sloj tetrahedralni sloj H 2 O, Mg 2+, drugi ioni tetrahedralni sloj oktahedralni sloj tetrahedralni sloj smektit (2:1) ekspandirajoč nm tetrahedralni sloj oktahedralni sloj tetrahedralni sloj H 2 O, Mg 2+, drugi ioni tetrahedralni sloj oktahedralni sloj tetrahedralni sloj vermikulit (2:1) ekspandirajoč delno nabrekajoč 1.0 nm tetrahedralni sloj oktahedralni sloj tetrahedralni sloj K K K K K K K tetrahedralni sloj oktahedralni sloj tetrahedralni sloj sljuda (2:1) neekspandirajoč min. nabrekanje 1.4 nm tetrahedralni sloj oktahedralni sloj tetrahedralni sloj hidroksidni sloj tetrahedralni sloj oktahedralni sloj tetrahedralni sloj klorit (2:1:1) neekspandirajoč min.nabrekanje max. nabrekanje
48 Talni koloidi kemijsko najbolj aktivna frakcija v tleh manjši od 2 µm talni koloidi so lahko: -kristalične silikatne gline -nekristalične silikatne gline - železovi in aluminijevi oksidi - organski material (humus) lahko so kristalični (dobro definirana struktura) ali pa amorfni
49 Koloidi Lastnosti koloidov pomembne za funkcioniranje tal kemijske - vir hranil za talne organizme - talna elektronegativnost (CEC) - puferska kapaciteta - kemijski cement fizikalne - velika površina na enoto mase -plastičnost
50 Koloidi glinena micela Al Al 3+ Ca 2+ Mg 2+ Al 3+ Mg 2+ Ca Al 3+ Ca 2+ Ca 2+ H + K + Ca 2+ Mg 2+ Ca 2+ H + K K + K + Ca 2+ K + Ca 2+ H + Ca 2+ Mg 2+ H + Mg 2+ K + Ca 2+ Ca Mg 2+ Al 3+ Na 2+ + zunanja površina Al 3+ K + H + K + H + Ca 2+ SO 2-4 K + notranja površina Ca 2+ Al 3+ H + Al 3+ Mg K + negativni naboj gline Ca 2+ H + v Ca 2+ K + Ca 2+ adsorbirani kationi Ca 2+ Al 3+ v kationi H + Al 3+ Ca 2+ Cl - električni dvosloj v Cl - kationi in anioni v raztopini
51 Površina koloidnih delcev Koloidni delci imajo veliko razmerje med površino in maso npr. kocka s stranico 0.1 m (1 dm, ρ = 1 kg dm -3 ) ima površino 0.06 m 2 kg -1 če kocko razdelimo v kocke s stranico 100 nm dobimo 1 x majhnih kock in je skupna površina majhnih kock m 2 kg -1 Merjenje površine delcev površina = geometrijska površina x hrapavost geometrijska površina predpostavlja ravno površino faktor hrapavosti (r) 1.0 < r < 150
52 Specifična površina mineralov dolžina roba kocke skupna površina specifična površina S S/V (cm 2 /cm 3 ) 1 cm 6 cm mm 60 cm mm 600 cm mm 6000 cm µm 6 m µm 60 m µm 600 m nm 6000 m
53 Specifična površina mineralov talna komponenta celokupna (m 2 /g) specifična površina Zunanja m 2 /g) kaolinit CEC (cmol/kg) montmorillonit ilit goethit / ferihidrit / / huminske k ,
54 Stabilne koloidne suspenzije - sóli Sól se ne sedimentira (je stabilen) zaradi elektrostatskega naboja Sól postane nestabilen v destilirani vodi (če ni ionov, so koloidi nenabiti insedimentirajo)
55 Zbistritev koloidnih suspenzij Soli lahko sedimentirajo z dodatkom visoko valenčnih ionov negativno nabit sol zahteva 2+ ali 3+ nabite ione pozitivno nabit sol zahteva 2- ali 3- nabite ione pri precipitaciji Fe 2 O 3 sola, ki ima pozitivni naboj, se uporabljajo negativni naboji ion relativna koncentracija potrebna za zbistritev Fe(CN) SO CrO NO Br Cl - 400
56 AgI AgI Ag + Na + PO 3-4 NO - 3 Ioni z višjo valenco vodijo do večje gostote naboja in povečane privlačne sile Agregirani (koagulirani) delci izgubijo neto naboj (separacija naboja izgine) in so zaradi gravitacije sedimentirani AgI AgI
57 Sekundarni minerali Oksidi Al, Fe, Mn oksidi spremenljiv in ph odvisen naboj zelo reaktivna površina pomemben silicijev oksid SiO 2 je kremen (npr. kalcedon, opal)
58 Sekundarni minerali Hidroksidi Al, Fe hidroksidi amorfni ali drobno kristalni nastajajo z oksidacijo silikatnih mineralov pomembne rude (npr. limonit, boksit), nastajajo tako, da se kremenica hitro izpira
59 Sekundarni minerali oksidi in hidroksidi element mineral formula Al gibsit Al(OH) 3 bohemit AlOOH korund Al 2 O 3 Fe hematit Fe 2 O 3 geotit FeOOH ferihidrat Fe 5 O 7 (OH) 4 H 2 O Mn birnezit spremenljivo pirulozit MnO 2 manganit MNOOH Ti rutil TiO 2 atanaz TiO 2 ilmenit FeTiO 3
60 Sekundarni minerali Evaporiti nastali z evaporacijo morja ionske vezi zelo topni halit (NaCl), silvin (KCl) in gips ali sadra (CaSO 4 x 2H 2 0)
61 Sekundarni minerali Karbonati najpomembnejša: kalcit (CaCO 3 ) in dolomit CaMg(CO 3 ) 2 soli z ogljikovo kislino tvorijo še simsonit (ZnCO 3 ), siderit (FeCO 3 ), cerusit (PbCO 3 ), soda (Na 2 CO 3 ), malahtit (CuCO 3 ) pomembni v bolj aridnih klimatih (sekundarni precipitati) pri preperevanju se raztopijo (kraški pojavi)
62 Sekundarni minerali Sulfati nastajajo z obarjanjem iz vode so mehki in lahko topni z evaporacijo nastaneta anhidrit (CaSO 4 ) in sadra (CaSO 4 x 2 H 2 O) v tleh nasičenih z vodo lahko nastane barit (BaSO 4 ) s preperevanjem pirita nastaja jarozit (K,Fe sulfat) neprozorni s kovinskim sisjajem, visoka gostota
63 Sekundarni minerali Fosfati najpomebnejši je apatit Ca 5 (PO 4 )F, sestavina sklenine v kamninah kot slučajni minerali v tleh se pojavljajo še variskit Al(PO 4 ) x 2 H 2 O in strengit Fe(PO 4 ) x 2 H 2 O ti minerali so zelo slabo topni
64 Sekundarni minerali Sulfidi pirit(fes 2 ) najdemo jih predvsem v anaerobnih okoljih pri oksidaciji pride do zakisanja (bakterijsko gnan proces) rudninski minerali HgS (cinabarit, Idrija), Cu 2 S (halkozin), PbS (galenit, Mežica), ZnS (halkozit, Mežica) v kamnih se pojavljajo kot slučajni minerali imajo kovinski sijaj
65 Nastanek mineralov na površini bakterijskih celic zaradi velikega razmerja med površino in volumnom in površinskih nabojev so bakterijske celice močni nukleacijski agensi površina je zaradi prisotnosti karboksilnih in fosforilnih skupin negativno nabita v manjšem obsegu najdemo pozitivno nabite aminske skupine nastanek mineralov ni vezan na poseben organizem temveč na njegove fizikalno-kemijske lastnosti (npr. prisotnost EPS, S-sloj)
66 Nastanek mineralov na površini bakterijskih celic Dvostopenjski proces: 1. kovine v okolici celice interagirajo z nabitimi skupinami na površini celice (stoihiometrično) 2. vezava kovine zniža prosto energijo sistema in omogoča vezavo dodatnih kovin, na mestu nukleacije pride do precipitacije (večja koncentracija kovine, kot bi jo pričakovali glede na naboje na površini)
67 Nastanek mineralov v sulfidnih rudnikih zaradi oksidacije pirita pride do nastanka topnega Fe 2+ železa in sulfata (nizek ph) pri pronicanju sulfata v globlje plasti pride do interakcije s karbonatnimi minerali (dvigovanje ph) in precipitacije mineralov (predvsem Fe-oksidov in melanterita FeSO 4 x 7H 2 O) na celičnih nukleacijskih jedrih v anaerobnem okolju je sulfat reduciran do H 2 S, kar omogoča interakcijo s kovinami in njihovo precipitacijo v raztopini in na celični površini (nastanek FeS in drugih sulfidov)
68 Nastanek silikatov s pomočjo bakterijskih celic v rečnih sedimentih, sulfidnih rudnikih, vročih vrelcih in sulfidnih vrelcih lahko nastanejo minerali glin minerali glin lahko nastanejo tudi v okolju z zelo malo silikatov (npr. reke, jezera) struktura takih glin je drugačna od abiotsko nastalih (bolj amorfni), sestava kovin v silikatu je odvisna od okolja v toplih vrelcih lahko nastaja na površini bakterij čisti kremen silicij se veže direktno na amino skupine na površini, ali pa indirektno z mostovnimi povezavami preko divalentnih kationov
69 Nastanek karbonatnih mineralov s pomočjo bakterijskih celic organokarbonatni minerali (mikrobialiti) nastajajo v toplih plitvih morskih okoljih zaščitenih pred delovanjem močnejših fizikalnih sil in predatorji potrebne so cianobakterije in bakterije do mineralizacije pride zaradi povečane alkalizacije mikrookolja ali zaradi izparevanja supersaturirane kalcitne vode mikrobi predstavljajo nukleacijska jedra za nastanek biotskega minerala, poleg tega pa adsorpcijska mesta za vezavo abiotsko nastalega minerala
70 Nastanek karbonatnih mineralov s pomočjo bakterijskih celic Obstajata dva tipa organokarbonatnih mineralov (mikrobialitov): 1. stromatoliti (plastovite strukture z svetlimi karbonatnimi in temnimi organskimi pasovi, po končani aktivni rasti pride do cementacije slojev, filamentozne cianobakterije) 2. tromboliti (globularna struktura, enocelične cianobakterije)
71 Nastanek karbonatnih mineralov s pomočjo bakterijskih celic Stromatolitom podobne strukture najdemo: puščavah (kokoidne cianobakterije naredijo skorje na površini tal iz kalcificirane zemlje, Kalifornija, Sinaj) jame (plastovite strukture, speleotermi) fosforiti (sedimentne kamnine bogate s fosforjem (Ca 10 (PO 4 CO 3 ) 6 F 2, nastajajo kot noduli v oceanskem okolju, ki precipitirajo na organski snovi cianobakterij)
72 Mehanizem nastaneka karbonatnih mineralov s pomočjo bakterijskih celic Celice morajo imeti sposobnost nastanka mikro-alkalnega okolja: nitratni reducenti (nastanek amonija) urea-razkrajoči (nastanek amonija) sulfatni reducenti (sproščanje bikarbonata) oksigeni fotosintetski mikroorganizmi (sproščanje hidroksilnih ionov)
73 Mehanizem nastaneka karbonatnih mineralov s pomočjo Synechococcusa pri Synechococcusu ima zelo pomembno vlogo S-sloj S-sloj je bolj hidrofoben, kot večina bakterijskih površin v porah S-sloja so prisotna negativno nabita mesta, kjer se lahko veže Ca 2+ ko je Ca 2+ vezan se lahko veže sulfat ali karbonat (ph>8.3) do lokalnega povečanja ph pride zaradi sprejema topnega HCO 3- v celico, kjer ga ogljik anhidraza razcepi v CO 2 in OH - celica funkcionira kot celično-mineralni agregat, ki po poropadu potone na dno in tvori kalcitni sediment
74 Mehanizem nastaneka karbonatnih mineralov s pomočjo Synechococcusa v labotratoriju lahko Synechococcus postane v 8 urah popolnoma obdan z gipsom ali kalcitom bakterija se deli vsakih 72 ur da bi preprečila popolni omot celica kontinuirano odmeče S-sloj s prenehanjem rasti se S-sloj ne lušči več in celica odmre, potone in tvori kalcitni sediment
75 Organska snov 0.5 do 5 % v mineralnih tleh amorfna dekompozicija rastlinske in živalske biomase glavni vpliv na fizikalno/kemijske lastnosti tal nehuminske spojine pripadajo znanim molekulam (npr. amino kisline, ogljikovi hidrati, lipidi) huminske spojine imajo visoko molekularno težo so rumene do črne in nastajajo s sekundarno sintezo huminske kisline so bogate s kisikovimi funkcionalnimi skupinami (karboksilne kisline, fenol, enol, alkohol, aldehid, keton)
76 Organska snov vodotopne organske snovi so nizkomolekularne alifatske in aromatske kisline, pomembne kot vir hranil talni encimi (veliko različnih, aktivnost odvisna od okoljskih faktorjev) organska snov je pomembna pri transportu kovin organska snov je pomembna pri vezavi težkih kovin na organsko snov
77 Frakcionacija organske snovi v tleh talna organska snov ne-huminske substance huminske substance topne v kislinah in bazah netopne v kislinah topne v bazah netopne v kislinah netopne v bazah fulvo kisline huminske kisline humin
78 Organska snov elementna sestava huminskih kislin in fulvo kislin fulvo kisline huminske kisline ogljik vodik kisik dušik žveplo
79 Organska snov pomembne funkcionalne organske skupine: karboksilna R-COOH pka=<5 enolna R-CH=CH-OH pka=6-7 fenolna Ar-OH pka=6 kinonska Ar=O pka=6-7 alkoholna R-CH 2 -OH pka=9 eterska R-CH2-O-CH 2 -R ketonska aldehidna esterska R-CO-R R-CHO R-CO-O-R aminska R-CH 2 -NH 2 amidna R-C=NH-R
80 Organska snov visoka specifična površina: m 2 kg -1 visoka CEC: cmoc kg -1 je ph odvisna 50 % CEC iz karboksilnih skupin 30 % CEC iz kinonskh, fenolnih in enolnih skupin prispeva 75 do 95 % CEC v mineralnih peščenih tleh
Nastajanje in preperevanje mineralov
 Nastajanje in preperevanje mineralov endogene sile tektonika: dviganje gubanje eksogene sile sila sonca in gravitacije: preperevanje erozija denudacija nastanek sedimentov Nastajanje in preperevanje mineralov
Nastajanje in preperevanje mineralov endogene sile tektonika: dviganje gubanje eksogene sile sila sonca in gravitacije: preperevanje erozija denudacija nastanek sedimentov Nastajanje in preperevanje mineralov
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * NAVODILA ZA OCENJEVANJE. Sreda, 3. junij 2015 SPLOŠNA MATURA
 Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 21. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
MINERALOGIJA KRISTAL MINERAL. Definicija: - kristalna vrsta, nastala v naravi (tudi umetno)
 MINERALOGIJA KRISTAL Definicija: - trdno telo - periodična prostorska razvrstitev kemičnih sestavin - ravne ploskve - stalni koti - nastanek: naravni, umetni procesi - anorganske, organske spojine MINERAL
MINERALOGIJA KRISTAL Definicija: - trdno telo - periodična prostorska razvrstitev kemičnih sestavin - ravne ploskve - stalni koti - nastanek: naravni, umetni procesi - anorganske, organske spojine MINERAL
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 5. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
II. RAZRED SULFIDI (SELENIDI, TELURIDI, ARZENIDI, ANTIMONIDI) IN SULFOSOLI (KOMPLEKSNI SULFIDI)
 II. RAZRED SULFIDI (SELENIDI, TELURIDI, ARZENIDI, ANTIMONIDI) IN SULFOSOLI (KOMPLEKSNI SULFIDI) Žveplo v litosferi: 470 µg/g kot - S 2- - sulfidi, s kovinskimi kationi. Nastopanje v magmatskih, metamorfnih
II. RAZRED SULFIDI (SELENIDI, TELURIDI, ARZENIDI, ANTIMONIDI) IN SULFOSOLI (KOMPLEKSNI SULFIDI) Žveplo v litosferi: 470 µg/g kot - S 2- - sulfidi, s kovinskimi kationi. Nastopanje v magmatskih, metamorfnih
SEMINAR IZ KOLEGIJA ANALITIČKA KEMIJA I. Studij Primijenjena kemija
 SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
Tla in ioni. naboj mineralov. električni dvojni sloj. adsorpcija. adsorpcijske izoterme. izmenjava ionov. ravnotežje trdno - raztopina
 Tla in ioni naboj mineralov električni dvojni sloj adsorpcija adsorpcijske izoterme izmenjava ionov ravnotežje trdno raztopina Ravnotežje trdno raztopina asimilacija rastlina, mikrobi mineralizacija imobilizacija
Tla in ioni naboj mineralov električni dvojni sloj adsorpcija adsorpcijske izoterme izmenjava ionov ravnotežje trdno raztopina Ravnotežje trdno raztopina asimilacija rastlina, mikrobi mineralizacija imobilizacija
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 22. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
PONOVITEV SNOVI ZA 4. TEST
 PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
ΦΡΟΝΤΙΣΤΗΡΙΟ Μ.Ε. ΣΥΜΒΟΛΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
Funkcijske vrste. Matematika 2. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 2. april Gregor Dolinar Matematika 2
 Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
Zakaj proučevati tla?
 Zakaj proučevati tla? medij za rast rastlin in pridelkov produkcija in absorbcija plinov medij za rast mikroorganizmov habitat za živali veliki integrator vseh delov terestričnega ekosistema vir za proučevanje
Zakaj proučevati tla? medij za rast rastlin in pridelkov produkcija in absorbcija plinov medij za rast mikroorganizmov habitat za živali veliki integrator vseh delov terestričnega ekosistema vir za proučevanje
Osnove elektrotehnike uvod
 Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
1. ΧΗΜΙΚΟΙ ΕΣΜΟΙ ΣΤΑ ΣΤΕΡΕΑ
 1. ΧΗΜΙΚΟΙ ΕΣΜΟΙ ΣΤΑ ΣΤΕΡΕΑ ΓΕΝΙΚΑ Η στερεά, η υγρή και η αέρια κατάσταση αποτελούν τις τρεις, συνήθεις στο γήινο περιβάλλον, καταστάσεις της ύλης. ιαφέρουν η µία από την άλλη σε κάποια απλά γνωρίσµατα:
1. ΧΗΜΙΚΟΙ ΕΣΜΟΙ ΣΤΑ ΣΤΕΡΕΑ ΓΕΝΙΚΑ Η στερεά, η υγρή και η αέρια κατάσταση αποτελούν τις τρεις, συνήθεις στο γήινο περιβάλλον, καταστάσεις της ύλης. ιαφέρουν η µία από την άλλη σε κάποια απλά γνωρίσµατα:
KERAMIKA, BETON I DRVO
 VJEŽBE: četvrtak, 12:15-14:00 KERAMIKA, BETON I DRVO Vježba 1. Ionske i kovalentne strukture Prof.dr.sc. Lidija Ćurković STRUKTURA ČVRSTIH (krutih) TVARI ovisi o: 1. VRSTI VEZA IZMEĐU STRUKTURNIH JEDINICA
VJEŽBE: četvrtak, 12:15-14:00 KERAMIKA, BETON I DRVO Vježba 1. Ionske i kovalentne strukture Prof.dr.sc. Lidija Ćurković STRUKTURA ČVRSTIH (krutih) TVARI ovisi o: 1. VRSTI VEZA IZMEĐU STRUKTURNIH JEDINICA
3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ
 23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
C M. V n: n =, (D): V 0,M : V M P = ρ ρ V V. = ρ
 »»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
»»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
Diferencialna enačba, v kateri nastopata neznana funkcija in njen odvod v prvi potenci
 Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
SEKUNDARNE VEZE međumolekulske veze
 PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
KRISTAL MINERAL: MINERALNA PARAGENEZA: PARAGENETSKI DIAGRAM:
 KRISTAL: trdno telo, periodična prostorska razvrstitev, ravne ploskve, stalni koti, naravni ali umetni nastanek MINERAL: kristalna vrsta, nastala v naravi (tudi umetno) MINERALNA PARAGENEZA: združba mineralov,
KRISTAL: trdno telo, periodična prostorska razvrstitev, ravne ploskve, stalni koti, naravni ali umetni nastanek MINERAL: kristalna vrsta, nastala v naravi (tudi umetno) MINERALNA PARAGENEZA: združba mineralov,
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014. ÄÉÁÍüÇÓÇ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
Kotne in krožne funkcije
 Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
6. ΤΕΛΙΚΗ ΙΑΘΕΣΗ ΤΑΦΗ. 6.1. Γενικά
 6. ΤΕΛΙΚΗ ΙΑΘΕΣΗ ΤΑΦΗ 6.1. Γενικά Είναι γεγονός ότι ανέκαθεν ο τελικός αποδέκτης των υπολειµµάτων της κατανάλωσης και των καταλοίπων της παραγωγικής διαδικασίας υπήρξε το περιβάλλον. Στις παλιότερες κοινωνίες
6. ΤΕΛΙΚΗ ΙΑΘΕΣΗ ΤΑΦΗ 6.1. Γενικά Είναι γεγονός ότι ανέκαθεν ο τελικός αποδέκτης των υπολειµµάτων της κατανάλωσης και των καταλοίπων της παραγωγικής διαδικασίας υπήρξε το περιβάλλον. Στις παλιότερες κοινωνίες
Φασματοσκοπία υπεριώδους-ορατού (UV-Vis)
 Καλαϊτζίδου Κυριακή Φασματοσκοπία υπεριώδους-ορατού (UV-Vis) Μέθοδος κυανού του μολυβδαινίου Προσθήκη SnCl 2 και (NH 4 ) 6 Mo 7 O 24 4H 2 O στο δείγμα Μέτρηση στα 690nm Μέτρηση 10-12min μετά από την προσθήκη
Καλαϊτζίδου Κυριακή Φασματοσκοπία υπεριώδους-ορατού (UV-Vis) Μέθοδος κυανού του μολυβδαινίου Προσθήκη SnCl 2 και (NH 4 ) 6 Mo 7 O 24 4H 2 O στο δείγμα Μέτρηση στα 690nm Μέτρηση 10-12min μετά από την προσθήκη
panagiotisathanasopoulos.gr
 . Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
. Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
Tretja vaja iz matematike 1
 Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK
 1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
1. Arrhenius. Ion equilibrium. ก - (Acid- Base) 2. Bronsted-Lowry *** ก - (conjugate acid-base pairs) HCl (aq) H + (aq) + Cl - (aq)
 Ion equilibrium ก ก 1. ก 2. ก - ก ก ก 3. ก ก 4. (ph) 5. 6. 7. ก 8. ก ก 9. ก 10. 1 2 สารล ลายอ เล กโทรไลต (Electrolyte solution) ก 1. strong electrolyte ก HCl HNO 3 HClO 4 NaOH KOH NH 4 Cl NaCl 2. weak
Ion equilibrium ก ก 1. ก 2. ก - ก ก ก 3. ก ก 4. (ph) 5. 6. 7. ก 8. ก ก 9. ก 10. 1 2 สารล ลายอ เล กโทรไลต (Electrolyte solution) ก 1. strong electrolyte ก HCl HNO 3 HClO 4 NaOH KOH NH 4 Cl NaCl 2. weak
Κανόνες διαλυτότητας για ιοντικές ενώσεις
 Κανόνες διαλυτότητας για ιοντικές ενώσεις 1. Ενώσεις των στοιχείων της Ομάδας 1A και του ιόντος αμμωνίου (Ιόντα: Li +, Na +, K +, Rb +, Cs +, NH 4+ ) είναι ευδιάλυτες, χωρίς εξαίρεση: πχ. NaCl, K 2 S,
Κανόνες διαλυτότητας για ιοντικές ενώσεις 1. Ενώσεις των στοιχείων της Ομάδας 1A και του ιόντος αμμωνίου (Ιόντα: Li +, Na +, K +, Rb +, Cs +, NH 4+ ) είναι ευδιάλυτες, χωρίς εξαίρεση: πχ. NaCl, K 2 S,
ΟΝΟΜΑΣΙΑ F - HF Υδροφθόριο S 2- H 2 S Υδρόθειο Cl - HCl Υδροχλώριο OH - H 2 O Οξείδιο του Υδρογόνου (Νερό) NO 3 HNO 3. Νιτρικό οξύ SO 3 H 2 SO 3
 1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 14. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΙΚΩΝ ΜΕ ΠΡΟΣΡΟΦΗΣΗ ΣΕ ΥΔΡΟΞΥ-ΟΞΕΙΔΙΑ ΣΙΔΗΡΟΥ ΑΠO ΤΗΝ ΕΚΡΟΗ ΒΙΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΛΥΜΑΤΩΝ. Κυριακή Καλαϊτζίδου MSc Χημικός Μηχανικός
 ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΙΚΩΝ ΜΕ ΠΡΟΣΡΟΦΗΣΗ ΣΕ ΥΔΡΟΞΥ-ΟΞΕΙΔΙΑ ΣΙΔΗΡΟΥ ΑΠO ΤΗΝ ΕΚΡΟΗ ΒΙΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΛΥΜΑΤΩΝ Κυριακή Καλαϊτζίδου MSc Χημικός Μηχανικός Φώσφορος Θεωρητικό Μέρος Παρουσιάζεται: Ορυκτά Ανθρώπινα
ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΙΚΩΝ ΜΕ ΠΡΟΣΡΟΦΗΣΗ ΣΕ ΥΔΡΟΞΥ-ΟΞΕΙΔΙΑ ΣΙΔΗΡΟΥ ΑΠO ΤΗΝ ΕΚΡΟΗ ΒΙΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΛΥΜΑΤΩΝ Κυριακή Καλαϊτζίδου MSc Χημικός Μηχανικός Φώσφορος Θεωρητικό Μέρος Παρουσιάζεται: Ορυκτά Ανθρώπινα
Delovna točka in napajalna vezja bipolarnih tranzistorjev
 KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
3. Υπολογίστε το μήκος κύματος de Broglie (σε μέτρα) ενός αντικειμένου μάζας 1,00kg που κινείται με ταχύτητα1 km/h.
 1 Ο ΚΕΦΑΛΑΙΟ ΑΣΚΗΣΕΙΣ 1. Ποια είναι η συχνότητα και το μήκος κύματος του φωτός που εκπέμπεται όταν ένα e του ατόμου του υδρογόνου μεταπίπτει από το επίπεδο ενέργειας με: α) n=4 σε n=2 b) n=3 σε n=1 c)
1 Ο ΚΕΦΑΛΑΙΟ ΑΣΚΗΣΕΙΣ 1. Ποια είναι η συχνότητα και το μήκος κύματος του φωτός που εκπέμπεται όταν ένα e του ατόμου του υδρογόνου μεταπίπτει από το επίπεδο ενέργειας με: α) n=4 σε n=2 b) n=3 σε n=1 c)
Παραδοχές στις οποίες στις οποίες στηρίζεται ο αριθμός οξείδωσης
 Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
Gimnazija Krˇsko. vektorji - naloge
 Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
ΙΑΓΩΝΙΣΜΑ 1 Ο ( 1 Ο ΚΕΦΑΛΑΙΟ)
 ΙΑΓΩΝΙΣΜΑ 1 Ο ( 1 Ο ΚΕΦΑΛΑΙΟ) ΘΕΜΑ 1 Ο Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές και να διορθώσετε τις λανθασµένες: 1. Τα άτοµα όλων των στοιχείων είναι διατοµικά.. Το 16 S έχει ατοµικότητα
ΙΑΓΩΝΙΣΜΑ 1 Ο ( 1 Ο ΚΕΦΑΛΑΙΟ) ΘΕΜΑ 1 Ο Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές και να διορθώσετε τις λανθασµένες: 1. Τα άτοµα όλων των στοιχείων είναι διατοµικά.. Το 16 S έχει ατοµικότητα
1 η Σειρά προβλημάτων στο μάθημα Εισαγωγική Χημεία
 1 η Σειρά προβλημάτων στο μάθημα Εισαγωγική Χημεία Ημ. Παράδοσης: Δευτέρα 25/11/2013 11 πμ 1. Οι αντιδράσεις οξειδοαναγωγής σώζουν ζωές!!! Οι αερόσακοι στα αυτοκίνητα, όταν ανοίγουν γεμίζουν με άζωτο το
1 η Σειρά προβλημάτων στο μάθημα Εισαγωγική Χημεία Ημ. Παράδοσης: Δευτέρα 25/11/2013 11 πμ 1. Οι αντιδράσεις οξειδοαναγωγής σώζουν ζωές!!! Οι αερόσακοι στα αυτοκίνητα, όταν ανοίγουν γεμίζουν με άζωτο το
Booleova algebra. Izjave in Booleove spremenljivke
 Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ
 ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (Επιλέγετε δέκα από τα δεκατρία θέματα) ΘΕΜΑΤΑ 1. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λάθος; Γιατί; (α) Από τα στοιχεία Mg, Al, Cl, Xe, C και Ρ, τον μεγαλύτερο
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (Επιλέγετε δέκα από τα δεκατρία θέματα) ΘΕΜΑΤΑ 1. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λάθος; Γιατί; (α) Από τα στοιχεία Mg, Al, Cl, Xe, C και Ρ, τον μεγαλύτερο
ΓΗ ΚΑΙ ΣΥΜΠΑΝ. Εικόνα 1. Φωτογραφία του γαλαξία μας (από αρχείο της NASA)
 ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) ( ) ΘΕΜΑ Α Α1.
 Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) (5 2 2017) ΘΕΜΑ Α Α1. Επιλέξτε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις : 1. Σε ποια από τις επόμενες ενώσεις το χλώριο έχει μεγαλύτερο αριθμό
Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) (5 2 2017) ΘΕΜΑ Α Α1. Επιλέξτε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις : 1. Σε ποια από τις επόμενες ενώσεις το χλώριο έχει μεγαλύτερο αριθμό
Definiranje okolja mikroorganizmov
 Definiranje okolja mikroorganizmov David Stopar Novi sad 2007 Izr. prof. dr. David Stopar Univerza v Ljubljani, BF Oddelek za živilstvo Katedra za mikrobiologijo Večna pot 111 Email: david.stopar@bf.uni-lj.si
Definiranje okolja mikroorganizmov David Stopar Novi sad 2007 Izr. prof. dr. David Stopar Univerza v Ljubljani, BF Oddelek za živilstvo Katedra za mikrobiologijo Večna pot 111 Email: david.stopar@bf.uni-lj.si
1. Definicijsko območje, zaloga vrednosti. 2. Naraščanje in padanje, ekstremi. 3. Ukrivljenost. 4. Trend na robu definicijskega območja
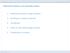 ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
+105 C (plošče in trakovi +85 C) -50 C ( C)* * Za temperature pod C se posvetujte z našo tehnično službo. ϑ m *20 *40 +70
 KAIFLEX ST Tehnični podatki Material Izjemno fleksibilna zaprtocelična izolacija, fleksibilna elastomerna pena (FEF) Opis Uporaba Temperaturno območje Toplotna prevodnost W/(m K ) pri različnih srednjih
KAIFLEX ST Tehnični podatki Material Izjemno fleksibilna zaprtocelična izolacija, fleksibilna elastomerna pena (FEF) Opis Uporaba Temperaturno območje Toplotna prevodnost W/(m K ) pri različnih srednjih
Κεφάλαιο 1. Έννοιες και παράγοντες αντιδράσεων
 Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
Kontrolne karte uporabljamo za sprotno spremljanje kakovosti izdelka, ki ga izdelujemo v proizvodnem procesu.
 Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
ARHITEKTURA DETAJL 1, 1:10
 0.15 0.25 3.56 0.02 0.10 0.12 0.10 SESTV S2 polimer-bitumenska,dvoslojna(po),... 1.0 cm po zahtevah SIST DIN 52133 in nadstandardno, (glej opis v tehn.poročilu), npr.: PHOENIX STR/Super 5 M * GEMINI P
0.15 0.25 3.56 0.02 0.10 0.12 0.10 SESTV S2 polimer-bitumenska,dvoslojna(po),... 1.0 cm po zahtevah SIST DIN 52133 in nadstandardno, (glej opis v tehn.poročilu), npr.: PHOENIX STR/Super 5 M * GEMINI P
- Geodetske točke in geodetske mreže
 - Geodetske točke in geodetske mreže 15 Geodetske točke in geodetske mreže Materializacija koordinatnih sistemov 2 Geodetske točke Geodetska točka je točka, označena na fizični površini Zemlje z izbrano
- Geodetske točke in geodetske mreže 15 Geodetske točke in geodetske mreže Materializacija koordinatnih sistemov 2 Geodetske točke Geodetska točka je točka, označena na fizični površini Zemlje z izbrano
Katedra za farmacevtsko kemijo. Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks. 25/11/2010 Vaje iz Farmacevtske kemije 3 1
 Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
Φημικές αντιδράσεις-α Λυκείου
 Αντιδράςεισ εξουδετζρωςησ. Ουςιαςτικά όλεσ οι αντιδράςεισ εξουδετζρωςθσ είναι θ αντίδραςθ ενόσ κατιόντοσ Η + με ζνα ανιόν ΟΗ - προσ ςχθματιςμό ενόσ μορίου Η 2 Ο (Η-ΟΗ). Αντίδραςη εξουδετζρωςησ. H + + OH
Αντιδράςεισ εξουδετζρωςησ. Ουςιαςτικά όλεσ οι αντιδράςεισ εξουδετζρωςθσ είναι θ αντίδραςθ ενόσ κατιόντοσ Η + με ζνα ανιόν ΟΗ - προσ ςχθματιςμό ενόσ μορίου Η 2 Ο (Η-ΟΗ). Αντίδραςη εξουδετζρωςησ. H + + OH
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 10. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
REGIONALNO-METAMORFNE STENE ( ºC; 2-10 kbar)
 REGIONALNO-METAMORFNE STENE (200-800ºC; 2-10 kbar) PODELA PREMA TEKSTURI 1. ŠKRILJAVE I 2. MASIVNE METAMORFNE STENE PODELA PREMA STEPENU KRISTALINITETA (NE ZAVISI OD STEPENA METAMORFIZMA) 1. STENE VISOKOG
REGIONALNO-METAMORFNE STENE (200-800ºC; 2-10 kbar) PODELA PREMA TEKSTURI 1. ŠKRILJAVE I 2. MASIVNE METAMORFNE STENE PODELA PREMA STEPENU KRISTALINITETA (NE ZAVISI OD STEPENA METAMORFIZMA) 1. STENE VISOKOG
Χημικές Αντιδράσεις. Εισαγωγική Χημεία
 Χημικές Αντιδράσεις Εισαγωγική Χημεία Κατηγορίες Χημικών Αντιδράσεων Πέντε κυρίως κατηγορίες: Σύνθεσης Διάσπασης Απλής αντικατάστασης Διπλής αντικατάστασης Καύσης Αντιδράσεις σύνθεσης Ένωση δύο ή περισσότερων
Χημικές Αντιδράσεις Εισαγωγική Χημεία Κατηγορίες Χημικών Αντιδράσεων Πέντε κυρίως κατηγορίες: Σύνθεσης Διάσπασης Απλής αντικατάστασης Διπλής αντικατάστασης Καύσης Αντιδράσεις σύνθεσης Ένωση δύο ή περισσότερων
SJAJ MINERALA JE OSOBINA KOJA ZAVISI OD KOLIĈINE REFLEKTOVANE SVETLOSTI SA POVRŠINE MINERALA
 SJAJ MINERALA JE OSOBINA KOJA ZAVISI OD KOLIĈINE REFLEKTOVANE SVETLOSTI SA POVRŠINE MINERALA GLATKE POVRŠINE REFLEKTUJU VEĆU KOLIĈINU SVETLOSTI PA IMAJU I VEĆU SJAJNOST MINERALA RAVNE POVRŠINE - REFLEKTUJU
SJAJ MINERALA JE OSOBINA KOJA ZAVISI OD KOLIĈINE REFLEKTOVANE SVETLOSTI SA POVRŠINE MINERALA GLATKE POVRŠINE REFLEKTUJU VEĆU KOLIĈINU SVETLOSTI PA IMAJU I VEĆU SJAJNOST MINERALA RAVNE POVRŠINE - REFLEKTUJU
Ljubljana,
 Ljubljana, 18.10.2005 www.gamelandsports.com/cupmetalb.jpg http://www.meteorite martin.de/images/meteor/odessa.jpg O KOVINAH Kovine so elementi področij s, d in f periodnega sistema. Elemente I. skupine
Ljubljana, 18.10.2005 www.gamelandsports.com/cupmetalb.jpg http://www.meteorite martin.de/images/meteor/odessa.jpg O KOVINAH Kovine so elementi področij s, d in f periodnega sistema. Elemente I. skupine
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2015 Β ΦΑΣΗ Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
Θέμα Α. Ονοματεπώνυμο: Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Διαγώνισμα Χημείας Α Λυκείου Αριθμοί Οξείδωσης & Χημικές Αντιδράσεις 29/03/2015. Στις ερωτήσεις 1.1 έως 1.10 επιλέξτε τη σωστή απάντηση:
 Διαγώνισμα Χημείας Α Λυκείου Αριθμοί Οξείδωσης & Χημικές Αντιδράσεις 29/03/2015 1 ο Θέμα. Στις ερωτήσεις 1.1 έως 1.10 επιλέξτε τη σωστή απάντηση: 1.1. Ο αριθμός οξείδωσης του μαγγανίου (Mn) στην ένωση
Διαγώνισμα Χημείας Α Λυκείου Αριθμοί Οξείδωσης & Χημικές Αντιδράσεις 29/03/2015 1 ο Θέμα. Στις ερωτήσεις 1.1 έως 1.10 επιλέξτε τη σωστή απάντηση: 1.1. Ο αριθμός οξείδωσης του μαγγανίου (Mn) στην ένωση
=DYH]XMRþHELRORãNHPHMQHYUHGQRVWL- BAT vrednosti
![=DYH]XMRþHELRORãNHPHMQHYUHGQRVWL- BAT vrednosti =DYH]XMRþHELRORãNHPHMQHYUHGQRVWL- BAT vrednosti](/thumbs/84/90356170.jpg) PRILOGA II =DYH]XMRþHELRORãNHPHMQHYUHGQRVWL- BAT vrednosti Ime snovi.dudnwhulvwlþql Aceton aceton 0,34 mmol/l (20,0 mg/l) 38,95 mmol/mol kreatinina* (20,0 mg/g kreatinina*) Aluminij aluminij 200µg/l Anilin
PRILOGA II =DYH]XMRþHELRORãNHPHMQHYUHGQRVWL- BAT vrednosti Ime snovi.dudnwhulvwlþql Aceton aceton 0,34 mmol/l (20,0 mg/l) 38,95 mmol/mol kreatinina* (20,0 mg/g kreatinina*) Aluminij aluminij 200µg/l Anilin
IZPIT IZ ANALIZE II Maribor,
 Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
INTELIGENTNO UPRAVLJANJE
 INTELIGENTNO UPRAVLJANJE Fuzzy sistemi zaključivanja Vanr.prof. Dr. Lejla Banjanović-Mehmedović Mehmedović 1 Osnovni elementi fuzzy sistema zaključivanja Fazifikacija Baza znanja Baze podataka Baze pravila
INTELIGENTNO UPRAVLJANJE Fuzzy sistemi zaključivanja Vanr.prof. Dr. Lejla Banjanović-Mehmedović Mehmedović 1 Osnovni elementi fuzzy sistema zaključivanja Fazifikacija Baza znanja Baze podataka Baze pravila
Ονοματολογία ανόργανων χημικών ενώσεων Γραφή ανόργανων χημικών ενώσεων Οξέα, βάσεις, άλατα
 Ονοματολογία ανόργανων χημικών ενώσεων Γραφή ανόργανων χημικών ενώσεων Οξέα, βάσεις, άλατα Βοηθητικές Σημειώσεις Αγγελική Απ. Γαλάνη, Χημικός Ph.D. Εργαστηριακό Διδακτικό Προσωπικό, (Ε.ΔΙ.Π.) Χημείας Γραφή
Ονοματολογία ανόργανων χημικών ενώσεων Γραφή ανόργανων χημικών ενώσεων Οξέα, βάσεις, άλατα Βοηθητικές Σημειώσεις Αγγελική Απ. Γαλάνη, Χημικός Ph.D. Εργαστηριακό Διδακτικό Προσωπικό, (Ε.ΔΙ.Π.) Χημείας Γραφή
Υ ΑΤΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΙΓΑΙΟΥ ΤΟΜΕΑΣ ΠΕΡΙΒΑΛΛΟΝΤΙΚΗΣ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΕΠΙΣΤΗΜΗΣ Κ. Π. ΧΑΛΒΑ ΑΚΗΣ ΜΥΤΙΛΗΝΗ 2004. Καθηγητής Περ.
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΙΓΑΙΟΥ ΤΟΜΕΑΣ ΠΕΡΙΒΑΛΛΟΝΤΙΚΗΣ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΕΠΙΣΤΗΜΗΣ Υ ΑΤΙΚΗ ΧΗΜΕΙΑ ΤΜΗΜΑ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΜΥΤΙΛΗΝΗ 2004 Κ. Π. ΧΑΛΒΑ ΑΚΗΣ Καθηγητής Περ. Μηχανικής ΠΕΡΙΕΧΟΜΕΝΑ ΠΕΡΙΕΧΟΜΕΝΑ...1 1 ΕΙΣΑΓΩΓΗ...3
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΙΓΑΙΟΥ ΤΟΜΕΑΣ ΠΕΡΙΒΑΛΛΟΝΤΙΚΗΣ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΕΠΙΣΤΗΜΗΣ Υ ΑΤΙΚΗ ΧΗΜΕΙΑ ΤΜΗΜΑ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΜΥΤΙΛΗΝΗ 2004 Κ. Π. ΧΑΛΒΑ ΑΚΗΣ Καθηγητής Περ. Μηχανικής ΠΕΡΙΕΧΟΜΕΝΑ ΠΕΡΙΕΧΟΜΕΝΑ...1 1 ΕΙΣΑΓΩΓΗ...3
Pošto pretvaramo iz veće u manju mjernu jedinicu broj 2.5 množimo s 1000,
 PRERAČUNAVANJE MJERNIH JEDINICA PRIMJERI, OSNOVNE PRETVORBE, POTENCIJE I ZNANSTVENI ZAPIS, PREFIKSKI, ZADACI S RJEŠENJIMA Primjeri: 1. 2.5 m = mm Pretvaramo iz veće u manju mjernu jedinicu. 1 m ima dm,
PRERAČUNAVANJE MJERNIH JEDINICA PRIMJERI, OSNOVNE PRETVORBE, POTENCIJE I ZNANSTVENI ZAPIS, PREFIKSKI, ZADACI S RJEŠENJIMA Primjeri: 1. 2.5 m = mm Pretvaramo iz veće u manju mjernu jedinicu. 1 m ima dm,
*M * Osnovna in višja raven MATEMATIKA NAVODILA ZA OCENJEVANJE. Sobota, 4. junij 2011 SPOMLADANSKI IZPITNI ROK. Državni izpitni center
 Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
MINERAL? nema jedinstvenih kriterijuma za odgovor
 Predavanje 1. MINERALI, MINERALOGIJA NAUKA O MINERALIMA minerals (lat.) rudni logos (grč.) nauka Izučava prirodu supstanci koje su vezane za rudnike, rudne žile i Zemljinu koru. MINERAL? nema jedinstvenih
Predavanje 1. MINERALI, MINERALOGIJA NAUKA O MINERALIMA minerals (lat.) rudni logos (grč.) nauka Izučava prirodu supstanci koje su vezane za rudnike, rudne žile i Zemljinu koru. MINERAL? nema jedinstvenih
V kristalu so atomi, ioni ali molekule geometrijsko urejeni po povsem določeni zakonitosti.
 3. KRISTALI IN KRISTALITI Večina trdnih snovi je v kristalnem stanju. V splošnem lahko rečemo, da so kristali periodična prostorska razporeditev atomov, molekul in ionov. V poljubni smeri kristala so enaki
3. KRISTALI IN KRISTALITI Večina trdnih snovi je v kristalnem stanju. V splošnem lahko rečemo, da so kristali periodična prostorska razporeditev atomov, molekul in ionov. V poljubni smeri kristala so enaki
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ
 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
ΦΡΟΝΤΙΣΤΗΡΙΟ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΗΡΑΚΛΕΙΤΟΣ ΚΩΛΕΤΤΗ
 ΚΩΛΕΤΤΗ 9- -068 0 8464 0 847670 www.irakleitos.gr ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 0 ΜΑΙΟΥ 06 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ) ΕΝΔΕΙΚΤΙΚΕΣ
ΚΩΛΕΤΤΗ 9- -068 0 8464 0 847670 www.irakleitos.gr ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 0 ΜΑΙΟΥ 06 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ) ΕΝΔΕΙΚΤΙΚΕΣ
2 η ΕΞΕΤΑΣΤΙΚΗ ΠΕΡΙΟΔΟΣ. Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Α1. Να βρεθεί η δομή των παρακάτω ατόμων: 23 11 Na, 40 20 Ca, 33 16 S, 127 53 I, 108
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Α1. Να βρεθεί η δομή των παρακάτω ατόμων: 23 11 Na, 40 20 Ca, 33 16 S, 127 53 I, 108
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002
 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design
 Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015)
 Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015) 1. Σε ποια απο τις παρακάτω ενώσεις το Ν έχει αριθμό οξέιδωσης +5 A. ΗΝΟ 2 C ΚΝΟ 3 B. ΝΗ 3 D Ν 2 Ο 3 2. Σε ποια απο τις παρακάτω
Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015) 1. Σε ποια απο τις παρακάτω ενώσεις το Ν έχει αριθμό οξέιδωσης +5 A. ΗΝΟ 2 C ΚΝΟ 3 B. ΝΗ 3 D Ν 2 Ο 3 2. Σε ποια απο τις παρακάτω
13. Jacobijeva metoda za računanje singularnega razcepa
 13. Jacobijeva metoda za računanje singularnega razcepa Bor Plestenjak NLA 25. maj 2010 Bor Plestenjak (NLA) 13. Jacobijeva metoda za računanje singularnega razcepa 25. maj 2010 1 / 12 Enostranska Jacobijeva
13. Jacobijeva metoda za računanje singularnega razcepa Bor Plestenjak NLA 25. maj 2010 Bor Plestenjak (NLA) 13. Jacobijeva metoda za računanje singularnega razcepa 25. maj 2010 1 / 12 Enostranska Jacobijeva
Ημερομηνία: Τρίτη 18 Απριλίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
Ονοματεπώνυμο: Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
3. Να συμπληρωθούν οι παρακάτω αντιδράσεις:
 1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
ΑΝΟΡΓΑΝΟΙ ΡΥΠΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΕΣΜΕΥΣΗΣ ΚΥΡΙΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΕΣΜΕΥΣΗΣ ΣΤΟ ΕΔΑΦΟΣ
 ΑΝΟΡΓΑΝΟΙ ΡΥΠΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΕΣΜΕΥΣΗΣ ΚΥΡΙΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΕΣΜΕΥΣΗΣ ΣΤΟ ΕΔΑΦΟΣ ΑΠΟΚΑΤΑΣΤΑΣΗ ΡΥΠΑΣΜΕΝΩΝ ΕΔΑΦΩΝ 2γ-1 ΜΗΧΑΝΙΣΜΟΙ ΔΕΣΜΕΥΣΗΣ ΣΤΟ ΕΔΑΦΟΣ Μη ειδική προσρόφηση (ανταλλαγή ιόντων) Ειδική προσρόφηση
ΑΝΟΡΓΑΝΟΙ ΡΥΠΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΕΣΜΕΥΣΗΣ ΚΥΡΙΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΕΣΜΕΥΣΗΣ ΣΤΟ ΕΔΑΦΟΣ ΑΠΟΚΑΤΑΣΤΑΣΗ ΡΥΠΑΣΜΕΝΩΝ ΕΔΑΦΩΝ 2γ-1 ΜΗΧΑΝΙΣΜΟΙ ΔΕΣΜΕΥΣΗΣ ΣΤΟ ΕΔΑΦΟΣ Μη ειδική προσρόφηση (ανταλλαγή ιόντων) Ειδική προσρόφηση
AΝΑΛΟΓΙΑ ΜΑΖΩΝ ΣΤΟΧΕΙΩΝ ΧΗΜΙΚΗΣ ΕΝΩΣΗΣ
 2 ο Γυμνάσιο Καματερού 1 ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΗΣ ΥΛΗΣ 1. Πόσα γραμμάρια είναι: ι) 0,2 kg, ii) 5,1 kg, iii) 150 mg, iv) 45 mg, v) 0,1 t, vi) 1,2 t; 2. Πόσα λίτρα είναι: i) 0,02 m 3, ii) 15 m 3, iii) 12cm
2 ο Γυμνάσιο Καματερού 1 ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΗΣ ΥΛΗΣ 1. Πόσα γραμμάρια είναι: ι) 0,2 kg, ii) 5,1 kg, iii) 150 mg, iv) 45 mg, v) 0,1 t, vi) 1,2 t; 2. Πόσα λίτρα είναι: i) 0,02 m 3, ii) 15 m 3, iii) 12cm
ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ (ΚΕΦ 2-3 ) ΚΥΡΙΑΚΗ 4 ΔΕΚΕΜΒΡΙΟΥ 2016 ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ 4
 ΑΡΧΗ 1 ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ (ΚΕΦ 2-3 ) ΚΥΡΙΑΚΗ 4 ΔΕΚΕΜΒΡΙΟΥ 2016 ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ 4 ΘΕΜΑ Α Α1. Στον σύγχρονο Περιοδικό Πίνακα τα χημικά στοιχεία έχουν ταξινομηθεί: α. κατ αύξοντα ατομικό
ΑΡΧΗ 1 ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ (ΚΕΦ 2-3 ) ΚΥΡΙΑΚΗ 4 ΔΕΚΕΜΒΡΙΟΥ 2016 ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ 4 ΘΕΜΑ Α Α1. Στον σύγχρονο Περιοδικό Πίνακα τα χημικά στοιχεία έχουν ταξινομηθεί: α. κατ αύξοντα ατομικό
TROŠENJE MINERALA I STIJENA
 Mramor Granit monomineralne kalcit Zbog čega je značajno? polimineralne ortoklas, kvarc, plagioklas, biotit, hornblenda ukupna anorganska tvar tla potječe iz susjednih sfera (litosfere, atmosfere i hidrosfere)
Mramor Granit monomineralne kalcit Zbog čega je značajno? polimineralne ortoklas, kvarc, plagioklas, biotit, hornblenda ukupna anorganska tvar tla potječe iz susjednih sfera (litosfere, atmosfere i hidrosfere)
ZAKLJUČNI PROCESI V BIOTEHNOLOGIJI. Membranski separacijski procesi: diafiltracija, elektrodializa, reverzna osmoza, pervaporacija
 ZAKLJUČNI PROCESI V BIOTEHNOLOGIJI Membranski separacijski procesi: diafiltracija, elektrodializa, reverzna osmoza, pervaporacija Membranski separacijski procesi v biotehnologiji proces mikrofiltracija
ZAKLJUČNI PROCESI V BIOTEHNOLOGIJI Membranski separacijski procesi: diafiltracija, elektrodializa, reverzna osmoza, pervaporacija Membranski separacijski procesi v biotehnologiji proces mikrofiltracija
http://ekfe.chi.sch.gr ΙΑΝΟΥΑΡΙΟΣ 2010 Πειράματα Χημείας Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων
 http://ekfe.chi.sch.g 5 η - 6 η Συνάντηση ΙΑΝΟΥΑΡΙΟΣ 010 Πειράματα Χημείας Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων Παρασκευή διαλύματος ορισμένης συγκέντρωσης αραίωση διαλυμάτων Παρασκευή και ιδιότητες
http://ekfe.chi.sch.g 5 η - 6 η Συνάντηση ΙΑΝΟΥΑΡΙΟΣ 010 Πειράματα Χημείας Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων Παρασκευή διαλύματος ορισμένης συγκέντρωσης αραίωση διαλυμάτων Παρασκευή και ιδιότητες
ΙΑΦΑ Φ ΝΕΙ Ε ΕΣ Ε ΧΗΜΕ Μ Ι Ε ΑΣ ΓΥΜΝ Μ ΑΣΙΟΥ H
 Hταξινόµηση των στοιχείων τάξη Γ γυµνασίου Αναγκαιότητα ταξινόµησης των στοιχείων Μέχρι το 1700 µ.χ. ο άνθρωπος είχε ανακαλύψει µόνο 15 στοιχείακαι το 1860 µ.χ. περίπου 60στοιχεία. Σηµαντικοί Χηµικοί της
Hταξινόµηση των στοιχείων τάξη Γ γυµνασίου Αναγκαιότητα ταξινόµησης των στοιχείων Μέχρι το 1700 µ.χ. ο άνθρωπος είχε ανακαλύψει µόνο 15 στοιχείακαι το 1860 µ.χ. περίπου 60στοιχεία. Σηµαντικοί Χηµικοί της
Talna kemija. Kaj je potrebno poznati:
 Talna kemija Kaj je potrebno poznati: splošno kemijo mol, molaren, normalnost, ekvivalent ionska jakost, aktivnost ravnotežne konstante funkcionalne skupine hidratacija, hidroliza redoks reakcije Redoks
Talna kemija Kaj je potrebno poznati: splošno kemijo mol, molaren, normalnost, ekvivalent ionska jakost, aktivnost ravnotežne konstante funkcionalne skupine hidratacija, hidroliza redoks reakcije Redoks
ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ. β) Να βρεθεί σε ποια οµάδα και σε ποια περίοδο του Περιοδικού Πίνακα ανήκουν.
 ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ: 03490 ΗΜΕΡΟΜΗΝΙΑ: 27/5/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ ΕΚΦΩΝΗΣΕΙΣ Θέμα 2ο Α) Για τα στοιχεία: 12 Μg και 8 Ο α) Να κατανεµηθούν τα ηλεκτρόνιά τους σε στιβάδες. (µονάδες 2) β)
ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ: 03490 ΗΜΕΡΟΜΗΝΙΑ: 27/5/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ ΕΚΦΩΝΗΣΕΙΣ Θέμα 2ο Α) Για τα στοιχεία: 12 Μg και 8 Ο α) Να κατανεµηθούν τα ηλεκτρόνιά τους σε στιβάδες. (µονάδες 2) β)
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 4
 ΚΕΦΑΛΑΙΟ 4 ΣΤΟΙΧΕΙΟΜΕΤΡΙΑ ΕΡΩΤΗΣΕΙΣ ΜΕ ΤΙΣ ΑΠΑΝΤΗΣΕΙΣ: 1. Τι είναι ατομικό και τί μοριακό βάρος; Ατομικό βάρος είναι ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη η μάζα του ατόμου από το 1/12 της
ΚΕΦΑΛΑΙΟ 4 ΣΤΟΙΧΕΙΟΜΕΤΡΙΑ ΕΡΩΤΗΣΕΙΣ ΜΕ ΤΙΣ ΑΠΑΝΤΗΣΕΙΣ: 1. Τι είναι ατομικό και τί μοριακό βάρος; Ατομικό βάρος είναι ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη η μάζα του ατόμου από το 1/12 της
SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK
 SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΔΙΕΠΙΣΤΗΜΟΝΙΚΟ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ (Δ.Π.Μ.Σ.) «ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ»
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΔΙΕΠΙΣΤΗΜΟΝΙΚΟ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ (Δ.Π.Μ.Σ.) «ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ» ΜΑΘΗΜΑ ΚΟΡΜΟΥ «ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ» ΥΔΑΤΙΚΑ ΟΙΚΟΣΥΣΤΗΜΑΤΑ Σημειώσεις
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΔΙΕΠΙΣΤΗΜΟΝΙΚΟ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ (Δ.Π.Μ.Σ.) «ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ» ΜΑΘΗΜΑ ΚΟΡΜΟΥ «ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ» ΥΔΑΤΙΚΑ ΟΙΚΟΣΥΣΤΗΜΑΤΑ Σημειώσεις
S t r a n a 1. 1.Povezati jonsku jačinu rastvora: a) MgCl 2 b) Al 2 (SO 4 ) 3 sa njihovim molalitetima, m. za so tipa: M p X q. pa je jonska jačina:
 S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
Αλληλεπίδραση ακτίνων-χ με την ύλη
 Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
ΜΕΛΕΤΗ ΤΗΣ ΥΝΑΤΟΤΗΤΑΣ ΑΞΙΟΠΟΙΗΣΗΣ ΤΟΥ ΓΕΩΘΕΡΜΙΚΟΥ ΠΕ ΙΟΥ ΘΕΡΜΩΝ ΝΙΓΡΙΤΑΣ (Ν. ΣΕΡΡΩΝ)
 ελτίο της Ελληνικής Γεωλογικής Εταιρίας τοµ. XXXVI, 2004 Πρακτικά 10 ου ιεθνούς Συνεδρίου, Θεσ/νίκη Απρίλιος 2004 Bulletin of the Geological Society of Greece vol. XXXVI, 2004 Proceedings of the 10 th
ελτίο της Ελληνικής Γεωλογικής Εταιρίας τοµ. XXXVI, 2004 Πρακτικά 10 ου ιεθνούς Συνεδρίου, Θεσ/νίκη Απρίλιος 2004 Bulletin of the Geological Society of Greece vol. XXXVI, 2004 Proceedings of the 10 th
Βουκλής Χ. Αλέξανδρος Αριθμός οξείδωσης, χημικοί τύποι, γραφή - ονοματολογία χημικών ενώσεων Παρουσίαση σε μορφή ερωτωαπαντήσεων
 Βουκλής Χ. Αλέξανδρος Αριθμός οξείδωσης, χημικοί τύποι, γραφή ονοματολογία χημικών ενώσεων Παρουσίαση σε μορφή ερωτωαπαντήσεων 1. Τι εννοούμε όταν λέμε «η γλώσσα της Χημείας»; Η χημεία είναι μια συμβολική
Βουκλής Χ. Αλέξανδρος Αριθμός οξείδωσης, χημικοί τύποι, γραφή ονοματολογία χημικών ενώσεων Παρουσίαση σε μορφή ερωτωαπαντήσεων 1. Τι εννοούμε όταν λέμε «η γλώσσα της Χημείας»; Η χημεία είναι μια συμβολική
ΙΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗ. Η 2 SO 4 + BaCl 2 2HCl + BaSO 4. 2HCl + Na 2 CO 3 CO 2 + H 2 O + 2NaCl. 2HCl + Na 2 SO 3 SO 2 + H 2 O + 2NaCl
 ΙΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗ Οι αντιδράσεις διπλής αντικατάστασης γίνονται ανάµεσα σε ηλεκτρολύτες µε ανταλλαγή ιόντων. Για να πραγµατοποιηθεί µια αντίδραση διπλής αντικατάστασης πρέπει ένα τουλάχιστον από τα προϊόντα
ΙΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗ Οι αντιδράσεις διπλής αντικατάστασης γίνονται ανάµεσα σε ηλεκτρολύτες µε ανταλλαγή ιόντων. Για να πραγµατοποιηθεί µια αντίδραση διπλής αντικατάστασης πρέπει ένα τουλάχιστον από τα προϊόντα
Transformator. Delovanje transformatorja I. Delovanje transformatorja II
 Transformator Transformator je naprava, ki v osnovi pretvarja napetost iz enega nivoja v drugega. Poznamo vrsto različnih izvedb transformatorjev, glede na njihovo specifičnost uporabe:. Energetski transformator.
Transformator Transformator je naprava, ki v osnovi pretvarja napetost iz enega nivoja v drugega. Poznamo vrsto različnih izvedb transformatorjev, glede na njihovo specifičnost uporabe:. Energetski transformator.
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
