Γεληθή Φεκεία. Νίθνο Ξεθνπθνπισηάθεο Δπίθνπξνο Καζεγεηήο
|
|
|
- Νομική Τοκατλίδης
- 6 χρόνια πριν
- Προβολές:
Transcript
1 Γεληθή Φεκεία Νίθνο Ξεθνπθνπισηάθεο Δπίθνπξνο Καζεγεηήο Πνιπηερλείν Κξήηεο Τκήκα Μεραληθψλ Πεξηβάιινληνο Γξαθείν Κ2.125, ηει.:
2 Πεξηερφκελα Μνξηαθφ βάξνο θαη ηππηθφ βάξνο Ζ έλλνηα ηνπ mole Σηνηρεηνκεηξία ρεκηθψλ αληηδξάζεσλ 2
3 Πεξηνδηθφο Πίλαθαο ησλ Σηνηρείσλ Αηνκηθφο αξηζκφο 3
4 Μορηαθό βάρος Τν κορηαθό βάρος (molecular weight, MW) κηαο νπζίαο είλαη ην άζξνηζκα ησλ αηνκηθψλ βαξψλ φισλ ησλ αηφκσλ ηα νπνία ππάξρνπλ ζην κφξην ηεο νπζίαο. MW ηνπ H 2 O = 2 1, ,999 = 18,015 amu MW ηεο NH 3 = 14, ,008 = 17,031 amu MW ηνπ H 2 SO 4 = 2 1, , ,999 = 98,07 amu MW ηνπ CHCl 3 = 12, , ,45 = 119,37 amu 4
5 Τσπηθό βάρος Τν ησπηθό βάρος (formula weight, FW) κηαο νπζίαο είλαη ην άζξνηζκα ησλ αηνκηθψλ βαξψλ φισλ ησλ αηφκσλ ηα νπνία ππάξρνπλ ζε κηα ηππηθή κνλάδα ηεο νπζίαο, αλεμάξηεηα αλ ε νπζία είλαη κνξηαθή ή φρη. FW ηνπ NaCl = 22, ,45 = 58,44 amu FW ηνπ Fe 2 (SO 4 ) 3 = 2 55, , ,999 = 399,75 amu FW ηνπ CuSO 4 5H 2 O = 63, , , , ,999 = 249,68 amu 5
6 Μνξηαθφ θαη ηππηθφ βάξνο Παραηήρεζε!!!: ην κνξηαθφ θαη ην ηππηθφ βάξνο κηαο νπζίαο ππνινγίδεηαη κε βάζε ηα αθξηβή αηνκηθά βάξε, φπσο απηά δίλνληαη ζηνλ πεξηνδηθφ πίλαθα ησλ ζηνηρείσλ. Καηά ηελ εθηέιεζε ησλ πξάμεσλ λα εθαξκφδεηε ηνπο θαλφλεο γηα ηα ζεκαληηθά ςεθία. Σπλήζσο ην κνξηαθφ θαη ην ηππηθφ βάξνο ζηξνγγπινπνηείηαη ζην δεχηεξν δεθαδηθφ ςεθίν: Π.ρ. MW ηνπ H 2 = 2,016 amu 2,02 amu Π.ρ. MW ηνπ H 2 O = 18,015 amu 18,02 amu MW ηεο NH 3 = 17,031 amu 17,03 amu 6
7 Άζθεζε 3.1 Υπνινγίζηε ηα ηππηθά βάξε ησλ αθφινπζσλ ελψζεσλ. Σηξνγγπινπνηείζηε ην απνηέιεζκα ζην δεχηεξν δεθαδηθφ ςεθίν. NO 2 C 6 H 12 O 6 NaOH Mg(OH) 2 (NH 4 ) 2 SO 4 Al 2 (SO 4 ) 3 18H 2 O 7
8 Άζθεζε 3.2 Βξείηε ηηο ηππηθέο κάδεο ησλ παξαθάησ ελψζεσλ. Σε θάζε πεξίπησζε λα ζηξνγγπινπνηήζεηε ην απνηέιεζκα ζην δεχηεξν δεθαδηθφ ςεθίν. CH 3 OH N 2 O 5 K 2 CO 3 Ni 3 (PO 4 ) 2 NH 4 Cl Ca(OH) 2 8
9 Η έλλοηα ηοσ mole Οξηζκφο ηνπ mole (ζχκβνιν mol): πνζφηεηα ηεο χιεο ε νπνία πεξηέρεη ηφζα αληηθείκελα (άηνκα, κφξηα, ηφληα, ηππηθέο κνλάδεο ή νπνηαδήπνηε άιια αληηθείκελα) φζα πεξηέρνληαη ζε αθξηβψο 12 g ηνπ ηζνηφπνπ ηνπ 12 C. Σε 12 g ηνπ ηζνηφπνπ ηνπ 12 C πεξηέρνληαη 6, άηνκα. Ο αξηζκφο απηφο νλνκάδεηαη αρηζκός Avogadro, ζχκβνιν Ν Α, θαη έρεη κνλάδεο mol 1. Ν Α = 6, mol 1 9
10 Η έλλοηα ηοσ mole Άξα, 1 mol χιεο πεξηέρεη 6, αληηθείκελα (άηνκα, κφξηα, ηφληα, ηππηθέο κνλάδεο ή νπνηαδήπνηε άιια αληηθείκελα). Γειαδή ην mole νξίδεηαη κε βάζε ηνλ αξηζκφ ησλ αληηθεηκέλσλ. Καη αληηζηνηρία νξίδεηαη θαη ε δσδεθάδα (ληνπδίλα) = πεξηέρεη αθξηβψο 12 αληηθείκελα. π.ρ. 1 δσδεθάδα (ληνπδίλα) απγά = 12 απγά. 10
11 Η έλλοηα ηοσ mole 1 mol αηφκσλ 12 C = 6, άηνκα 12 C 1 mol αηφκσλ Ο = 6, άηνκα Ο 1 mol κνξίσλ Ο 2 = 6, κφξηα Ο 2 1 mol κνξίσλ Ζ 2 Ο = 6, κφξηα Ζ 2 Ο 1 mol ηππηθψλ κνλάδσλ NaCl = 6, ηππηθέο κνλάδεο NaCl 1 mol ηφλησλ ΝΟ 3 = 6, ηφληα ΝΟ 3 1 mol πέηξεο = 6, πέηξεο 1 mol άλζξσπνη = 6, άλζξσπνη 1 mol επξψ = 6, επξψ!!! 11
12 Η έλλοηα ηοσ mole Προζοτή!!!: 1 mol αηφκσλ νμπγφλνπ πεξηέρεη 6, άηνκα νμπγφλνπ. 1 mol κνξίσλ Ο 2 πεξηέρεη 6, κφξηα Ο 2, ηα νπνία είλαη 2 6, άηνκα νμπγφλνπ. Ο φξνο mole γηα ηηο ηνληηθέο ελψζεηο αλαθέξεηαη ζηνλ αξηζκφ ησλ ηππηθψλ κνλάδσλ ηεο νπζίαο, π.ρ. 1 mol ηππηθψλ κνλάδσλ Na 2 CΟ 3 πεξηέρεη 6, ηππηθέο κνλάδεο Na 2 CΟ 3, νη νπνίεο πεξηέρνπλ 2 6, ηφληα Na + θαη 6, ηφληα CO
13 1 mol δηαθφξσλ νπζηψλ 1-Οθηαλφιε C 8 H 17 OH HgI 2 Ο 2 S 8 Μεζαλφιε CH 3 OH Ζ 2 Ο NaCl 13
14 Πόζο δσγίδεη 1 mol??? 1 mol αληηθεηκέλσλ πεξηέρεη πάληα Ν Α = 6, αληηθείκελα. Ωζηφζν, ε κάδα ηνπ 1 mol αληηθεηκέλσλ δελ είλαη πάληνηε ε ίδηα. Πξνθαλψο εμαξηάηαη απφ ην είδνο ησλ αληηθεηκέλσλ. Ζ κάδα ηνπ 1 mol αληηθεηκέλσλ είλαη δηαθνξεηηθή θάζε θνξά, αλάινγα κε ηε κάδα ηνπ θάζε ελφο αληηθεηκέλνπ. 14
15 Πφζν δπγίδεη 1 mol? Έζησ 1 mol θξάνπιεο θαη 1 mol πνξηνθάιηα. Έζησ φηη ε θάζε θξάνπια δπγίδεη 10 g θαη ην θάζε πνξηνθάιη δπγίδεη 200 g (20 θνξέο πεξηζζφηεξν). 1 mol θξάνπιεο δπγίδεη 10 6, g θαη 1 mol πνξηνθάιηα δπγίδεη 200 6, g (20 θνξέο πεξηζζφηεξν). 15
16 Πφζν δπγίδεη 1 mol? Έζησ ηα εμήο άηνκα: Ζ: A r = 1 amu (γηα ηελ αθξίβεηα 1,008 amu) 12 C: A r = 12 amu, εμ νξηζκνχ Mg: A r = 24 amu (γηα ηελ αθξίβεηα 24,3050 amu) 1 mol αηφκσλ 12 C πεξηέρεη Ν Α = 6, άηνκα 12 C θαη δπγίδεη 12 g (εμ νξηζκνχ). Τν θάζε έλα άηνκν πδξνγφλνπ έρεη 12 θνξέο ιηγφηεξε κάδα απφ ην θάζε έλα άηνκν ηνπ 12 C. Καηά ζπλέπεηα, 1 mol αηφκσλ Ζ πεξηέρεη Ν Α = 6, άηνκα Ζ θαη δπγίδεη 1 g (γηα ηελ αθξίβεηα 1,008 g). 16
17 Πφζν δπγίδεη 1 mol? Οκνίσο, ην θάζε έλα άηνκν καγλεζίνπ έρεη 2 θνξέο κεγαιχηεξε κάδα απφ ην θάζε έλα άηνκν ηνπ 12 C. Καηά ζπλέπεηα, 1 mol αηφκσλ Mg πεξηέρεη Ν Α = 6, άηνκα Mg θαη δπγίδεη 24 g (γηα ηελ αθξίβεηα 24,3050 g). θ.ν.θ. Δειαδή, 1 mol αηόκωλ, κορίωλ, ηόληωλ ή ησπηθώλ κολάδωλ δσγίδεη όζο ηο αηοκηθό ή ηο κορηαθό ή ηο ησπηθό βάρος ζε g!!! 17
18 1 mol δπγίδεη φζν ην A r, MW ή FW ζε g 1 mol αηφκσλ H δπγίδεη 1,008 g 1 mol αηφκσλ Ο δπγίδεη 15,999 g 1 mol αηφκσλ Na δπγίδεη 23, g 1 mol κνξίσλ H 2 δπγίδεη 2,016 g 1 mol κνξίσλ Ο 2 δπγίδεη 31,998 g 1 mol κνξίσλ Ζ 2 Ο δπγίδεη 18,015 g 1 mol ηφλησλ ΝΟ 3 δπγίδεη 62,004 g 1 mol ηππηθψλ κνλάδσλ NaCl δπγίδεη 58,44 g 1 mol ηππηθψλ κνλάδσλ CuSO 4 5H 2 O δπγίδεη 249,68 g 18
19 Γρακκοκορηαθή κάδα Ζ γρακκοκορηαθή κάδα (molar mass) κηαο νπζίαο είλαη ε κάδα ελφο mole ηεο νπζίαο. Ζ γξακκνκνξηαθή κάδα κεηξηέηαη ζε g/mol. Η γρακκοκορηαθή κάδα θάζε οσζίας κεηρεκέλε ζε g/mol, είλαη πάληα αρηζκεηηθά ίζε κε ηο κορηαθό ή ηο ησπηθό βάρος ηες οσζίας κεηρεκέλο ζε amu. Σπλήζσο ε γξακκνκνξηαθή κάδα, φπσο ην κνξηαθφ θαη ην ηππηθφ βάξνο, ζηξνγγπινπνηείηαη ζην δεχηεξν δεθαδηθφ ςεθίν. 19
20 Άζθεζε 3.3 i. Πφζε είλαη ε κάδα ζε γξακκάξηα ελφο αηφκνπ ρισξίνπ, Cl; ii. Πφζε είλαη ε κάδα ζε γξακκάξηα ελφο κνξίνπ ρισξηδίνπ ηνπ πδξνγφλνπ, ΖCl; Λύζε: Γηαηξνχκε ηε γξακκνκνξηαθή κάδα κε ηνλ αξηζκφ Avogadro: μάζα ενόρ αηόμος Cl 35,45 g/mol 23 6, mol 1 5, g μάζα ενόρ μοπίος ΗCl 36,46 g/mol 23 6, mol 1 6, g 20
21 Άζθεζε 3.4 i. Πφζε είλαη ε κάδα ζε γξακκάξηα ελφο αηφκνπ αζβεζηίνπ, Ca; ii. Πφζε είλαη ε κάδα ζε γξακκάξηα ελφο κνξίνπ αηζαλφιεο, C 2 H 5 OH; 21
22 Άζθεζε 3.5 Υπνινγίζηε ηε κάδα ζε γξακκάξηα θαζεκηάο απφ ηηο παξαθάησ νληφηεηεο (ζσκαηίδηα): άηνκν Na άηνκν Ν κφξην CH 3 Cl ηππηθή κνλάδα Hg(NO 3 ) 2 κφξην PBr 3 ηππηθή κνλάδα Fe(OH) 2 κφξην (C 2 H 5 ) 2 O κφξην C 3 H 8 O 3 22
23 Υποιογηζκοί κε moles Γηα λα ππνινγίδνπκε ηνλ αξηζκφ ησλ moles κηαο νπζίαο δηαηξνχκε ηε κάδα ηεο νπζίαο κε ηε γξακκνκνξηαθή ηεο κάδα: φπνπ: n m Μ (3.1) n: ν αξηζκφο ησλ moles ηεο νπζίαο, ζε mol m: ε κάδα ηεο νπζίαο, ζε g M: ε γξακκνκνξηαθή κάδα ηεο νπζίαο, ζε g/mol 23
24 Υπνινγηζκνί κε moles Ο αξηζκφο ησλ moles κηαο νπζίαο κπνξεί λα ππνινγηζηεί θαη απφ ηελ αθφινπζε ζρέζε: φπνπ: n N N A (3.2) n: ν αξηζκφο ησλ moles ηεο νπζίαο, ζε mol Ν: ν αξηζκφο ησλ αηφκσλ, κνξίσλ, ή ηππηθψλ κνλάδσλ ηεο νπζίαο Ν Α : ν αξηζκφο Avogadro 6, mol 1 24
25 Άζθεζε 3.6 Να ππνινγίζεηε πφζα γξακκάξηα είλαη ηα 0,0654 mol ZnI 2. Λύζε: Τν κνξηαθφ βάξνο ηνπ ZnI 2 είλαη: 65, ,90447 = 319,18894 amu 319,19 amu Άξα ε γξακκνκνξηαθή κάδα ηνπ ZnI 2 είλαη 319,19 g/mol. n m m Μ n M m 0,0654 mol 319,19 g/mol m 20,9 g 25
26 Άζθεζε 3.7 Ζ αλάιπζε ελφο δηαιχκαηνο Ζ 2 Ο 2 δείρλεη φηη ζε 1,00 L δηαιχκαηνο ππάξρνπλ 0,909 mol H 2 O 2. Πφζε είλαη ε κάδα ηνπ ππεξνμεηδίνπ ηνπ πδξνγφλνπ ζε απηφ ηνλ φγθν δηαιχκαηνο. 26
27 Άζθεζε 3.8 Να ππνινγίζεηε πφζα moles είλαη ηα 45,6 g ρξσκηθνχ κνιχβδνπ(ηη), PbCrO 4. Λύζε: Τν κνξηαθφ βάξνο ηνπ PbCrO 4 είλαη: 207,2 + 51, ,999 = 323,1921 amu 323,2 amu (ην αηνκηθφ βάξνο ηνπ κνιχβδνπ δίλεηαη κε έλα δεθαδηθφ ςεθίν). Άξα ε γξακκνκνξηαθή κάδα ηνπ PbCrO 4 είλαη 323,2 g/mol. n Μ m n 45,6 g 323,2 g/mol 0,141 mol 27
28 Άζθεζε 3.9 Να ππνινγίζεηε πφζα moles είλαη ηα 28,5 g ληηξηθνχ νμένο, ΖΝΟ 3. 28
29 Άζθεζε 3.10 Πφζα κφξηα ππάξρνπλ ζε έλα δείγκα ρισξηδίνπ ηνπ πδξνγφλνπ, HCl, κάδαο 3,46 g. Λύζε: Τν κνξηαθφ βάξνο ηνπ HCl είλαη: 1, ,45 = 36,458 amu 36,46 amu, άξα ε γξακκνκνξηαθή ηνπ κάδα είλαη 36,46 g/mol. Υπνινγίδνπκε ηα moles ηνπ HCl: n N N A n N Μ m n NA n N 5,715 3,46 g 36,46 g/mol 0, mol 6,022 μόπια HCl 0, mol 23 mol 1 29
30 Άζθεζε 3.11 Πφζα κφξηα ππάξρνπλ ζε 56 mg HCN; 30
31 Άζθεζε 3.12 Να ππνινγηζηεί ν αξηζκφο ησλ moles ησλ παξαθάησ νπζηψλ: i. 2,00 g NaOH ii. 4,90 g H 2 SO 4 iii. 3,00 g CH 3 COOH iv. 5,00 g CaCO 3 v. 6,30 g HNO 3 vi. 5,26 g Fe 2 (SO 4 ) 3 7H 2 O vii. 4,74 g KAl(SO 4 ) 2 12H 2 O viii.9,16 g Na 2 SO 4 Al 2 (SO 4 ) 3 24H 2 O 31
32 Υποιογηζκοί κε moles Έζησ ην κφξην ηνπ λεξνχ, H 2 O. 1 κφξην Ζ 2 Ο πεξηέρεη 2 άηνκα Ζ θαη 1 άηνκν Ο. 6, κφξηα Ζ 2 Ο πεξηέρνπλ 2 6, άηνκα Ζ θαη 6, άηνκα Ο. 1 mol κνξίσλ Ζ 2 Ο πεξηέρεη 2 mol αηφκσλ Ζ θαη 1 mol αηφκσλ Ο. 18,015 g H 2 O πεξηέρνπλ 2 1,008 = 2,016 g πδξνγφλνπ θαη 15,999 g νμπγφλνπ. 32
33 Άζθεζε 3.13 Να ππνινγίζεηε πφζα γξακκάξηα πδξνγφλνπ θαη νμπγφλνπ πεξηέρνληαη ζε 0,913 g λεξνχ. Λύζε: 2,016 g ςδπογόνος 0,913 g H2O 18,015 g H O 2 0,102 g ςδπογόνος 15,999 g οξςγόνος 0,913 g H2O 18,015 g H O 2 0,811 g οξςγόνος 33
34 Άζθεζε 3.14 Έζησ 1,000 g απφ ηα αθφινπζα ηφληα: i. ΝΟ 2 ii. ΝΟ 3 iii. ΝΖ 4 + Να ππνινγίζεηε πφζα γξακκάξηα αδψηνπ πεξηέρεη ην θάζε ηφλ. Λύζε: i. ΝΟ 2 : ii. ΝΟ 3 : iii. ΝΖ 4+ : 14,007 g N 46,005 g NO 2 1,000 g NO 2 0,3045 g N 34
35 Άζθεζε 3.15 Να ππνινγίζεηε πφζα γξακκάξηα άλζξαθα πεξηέρνληαη ζε: i. 12,08 g γιπθφδεο, C 6 H 12 O 6. ii. 18,55 g νμηθνχ νμένο, CH 3 COOH. iii. 5,44 g κεζαλφιεο, CH 3 OH. Λύζε: i. C 6 H 12 O 6 : ii. 612,011 g C 12,08 g C6H12O6 180,156 g C6H12O6 4,832 g C CH 3 COOH: iii. CH 3 OH: 35
36 Σηοητεηοκεηρία τεκηθώλ αληηδράζεωλ Πρόβιεκα #1: Πφζε πνζφηεηα πδξνγφλνπ, H 2, ζε kg απαηηείηαη γηα ηελ παξαγσγή 907 kg ακκσλίαο, NH 3, ζχκθσλα κε ηε κέζνδν Haber: Ν 2 (g) + 3H 2 (g) 2NH 3 (g) 36
37 Σηνηρεηνκεηξία ρεκηθψλ αληηδξάζεσλ Σηοητεηοκεηρία (stoichiometry) είλαη ν ππνινγηζκφο ησλ πνζνηήησλ ησλ αληηδξψλησλ θαη πξντφλησλ ηα νπνία ζπκκεηέρνπλ ζε κηα ρεκηθή αληίδξαζε. Ν 2 (g) + 3H 2 (g) 2NH 3 (g) 1 κφξην Ν 2 3 κφξηα Ζ 2 2 κφξηα ΝΖ 3 6, , , κφξηα Ν 2 κφξηα Ζ 2 κφξηα ΝΖ 3 1 mol Ν 2 3 mol Ζ 2 2 mol ΝΖ 3 28,014 g Ν 2 3 2,016 g Ζ ,031 g ΝΖ 3 37
38 Σηνηρεηνκεηξηθνί ζπληειεζηέο θαη mol Σε θάζε ρεκηθή εμίζσζε νη ζηνηρεηνκεηξηθνί ζπληειεζηέο εθθξάδνπλ ηελ αλαιογία ηωλ moles ησλ αληηδξψλησλ θαη ησλ πξντφλησλ ηα νπνία ζπκκεηέρνπλ ζηελ αληίδξαζε. 38
39 Σηνηρεηνκεηξηθνί ζπληειεζηέο θαη mol Ν 2 + 3Ζ 2 2ΝΖ 3 1 mol Ν 2 αληηδξά κε 3 mol Ζ 2 θαη ζρεκαηίδνληαη 2 mol ΝΖ mol Ν 2 αληηδξνχλ κε 30 mol Ζ 2 θαη ζρεκαηίδνληαη 20 mol ΝΖ 3. 0,1 mol Ν 2 αληηδξνχλ κε 0,3 mol Ζ 2 θαη ζρεκαηίδνληαη 0,2 mol ΝΖ 3. θ.ν.θ. 39
40 Σηνηρεηνκεηξηθνί ζπληειεζηέο θαη mol Σηελ πξνεγνχκελε αληίδξαζε έζησ φηη έρνπκε 4,8 mol H 2. Πφζε πνζφηεηα αδψηνπ, Ν 2, απαηηείηαη ψζηε λα αληηδξάζεη πιήξσο ην πδξνγφλν, Ζ 2 ; Σηελ πεξίπησζε απηή, πφζε πνζφηεηα ακκσλίαο, ΝΖ 3, παξάγεηαη; Απάληεζε: Απαηηνχληαη: Παξάγνληαη: 1mol N2 4,8 mol H 2 1,6 mol 3 mol H 2 N 2 2 mol NH3 4,8 mol H 2 3,2 mol 3 mol H 2 NH 3 40
41 Μεζνδνινγία ιχζεο ησλ πξνβιεκάησλ Γεδνκέλα: κάδες ησλ αληηδξψλησλ Α ή/θαη Β ρξήζε ησλ γξακκνκνξηαθψλ καδψλ αα + ββ γγ + δγ Εεηνχκελα: κάδες ησλ πξντφλησλ Γ ή/θαη Γ ρξήζε ησλ γξακκνκνξηαθψλ καδψλ moles ησλ αληηδξψλησλ Α ή/θαη Β ρξήζε ησλ ζηνηρεηνκεηξηθψλ ζπληειεζηψλ ηεο ρεκηθήο εμίζσζεο moles ησλ πξντφλησλ Γ ή/θαη Γ 41
42 Πρόβιεκα #1: Πφζε πνζφηεηα πδξνγφλνπ, H 2, ζε kg απαηηείηαη γηα ηελ παξαγσγή 907 kg ακκσλίαο, NH 3, ζχκθσλα κε ηε κέζνδν Haber: Ν 2 (g) + 3H 2 (g) 2NH 3 (g) Λύζε: Αξρηθά ππνινγίδνπκε ηα moles ηεο ακκσλίαο: 3 m g 4 n 5,3310 mol NH Μ 17,03 g/mol n 3 42
43 Πρόβιεκα #1: Λύζε Σηε ζπλέρεηα ππνινγίδνπκε ηα moles ηνπ Ζ 2 ηα νπνία απαηηνχληαη γηα ηελ παξαζθεπή ηεο παξαπάλσ πνζφηεηαο ΝΖ 3 : 3 mol H 4 2 5,3310 mol NH3 2 mol NH3 8,00 10 Τέινο, ππνινγίδνπκε ηε κάδα ηνπ Ζ 2 : 4 mol H 2 n Μ m m n Μ 8, mol 2,02 g/mol m 1, g H 2 ή 162 kg H 2 43
44 Άζθεζε 3.16 Έζησ ε αληίδξαζε: Fe 2 O 3 (s) + 3CO(g) 2Fe(s) + 3CO 2 (g) Πφζα γξακκάξηα ζηδήξνπ κπνξνχλ λα παξαρζνχλ απφ 1,00 kg Fe 2 O 3 ; Λύζε: Αξρηθά ππνινγίδνπκε ηα moles ηνπ Fe 2 O 3 : 3 m 1,00 10 g n n 6,26 mol Fe Μ 2O3 159,69 g/mol 44
45 Άζθεζε 3.16 Σηε ζπλέρεηα ππνινγίδνπκε ηα moles ηνπ ζηδήξνπ: 6,26 mol Fe O 2 mol Fe ,52 mol Fe 1mol Fe 2 O 3 Τέινο, ππνινγίδνπκε ηε κάδα ηνπ ζηδήξνπ: n Μ m m n Μ 12,52 mol 55,85 g/mol m 699,2 g Fe 45
46 Άζθεζε 3.17 Τν κεηαιιηθφ λάηξην αληηδξά κε ην λεξφ παξάγνληαο αέξην πδξνγφλν θαη δηάιπκα πδξνμεηδίνπ ηνπ λαηξίνπ. Πφζα γξακκάξηα κεηαιιηθνχ λαηξίνπ απαηηνχληαη γηα λα παξαρζνχλ 7,81 g H 2 ; 46
47 Άζθεζε 3.18 Έζησ ε αληίδξαζε: 4HCl(aq) + MnO 2 (s) 2H 2 O(s) + MnCl 2 (aq) + Cl 2 (g) Πφζα γξακκάξηα ΖCl απαηηνχληαη γηα λα αληηδξάζνπλ κε 5,00 g MnO 2 ; Λύζε: Αξρηθά ππνινγίδνπκε ηα moles ηνπ MnO 2 : m 5,00 g n n 0,0575 mol MnO 2 Μ 86,94 g/mol 47
48 Άζθεζε 3.18 Σηε ζπλέρεηα ππνινγίδνπκε ηα moles ηνπ ΖCl: 4 mol HCl 0,0575 mol MnO 2 0,230 mol HCl 1mol MnO 2 Τέινο, ππνινγίδνπκε ηε κάδα ηνπ ΖCl: n Μ m m n Μ 0,230 mol 36,46 g/mol m 8,39 g HCl 48
49 Άζθεζε 3.19 Καηά ηελ ζέξκαλζε ηνπ ζνπιθηδίνπ ηνπ ςεπδαξγχξνπ κε νμπγφλν παξάγεηαη νμείδην ηνπ ςεπδαξγχξνπ θαη δηνμείδην ηνπ ζείνπ. Πφζα ρηιηφγξακκα αεξίνπ νμπγφλνπ ελψλνληαη κε 5, g ζνπιθηδίνπ ηνπ ςεπδαξγχξνπ; 49
50 Άζθεζε 3.20 Καηά ηελ ζέξκαλζε ηνπ νμεηδίνπ ηνπ πδξαξγχξνπ(ηη) παξάγεηαη νμπγφλν θαη κεηαιιηθφο πδξάξγπξνο. Αλ παξαρζνχλ 6,47 g νμπγφλνπ, πφζα γξακκάξηα κεηαιιηθνχ πδξαξγχξνπ έρνπλ ηαπηφρξνλα παξαρζεί; 50
51 Άζθεζε 3.21 Τν βνπηάλην, C 4 H 10, θαίγεηαη απφ ην νμπγφλν ηνπ αέξα πξνο CO 2 θαη H 2 O. Πφζε είλαη ε πνζφηεηα ζε moles ηνπ CO 2 ε νπνία παξάγεηαη θαηά ηελ θαχζε 0,15 mol βνπηαλίνπ, C 4 H 10 ; Λύζε: Αξρηθά γξάθνπκε ηελ ηζνζηαζκηζκέλε εμίζσζε θαχζεο ηνπ βνπηαλίνπ: C 4 H 10 (g) + 13/2O 2 (g) 4CO 2 (g) + 5H 2 O(g) 51
52 Άζθεζε 3.21: Απάληεζε Σχκθσλα κε ηελ ζηνηρεηνκεηξία ηεο αληίδξαζεο έρνπκε: 0,15 mol C H 4 mol CO ,60 1mol C H 4 10 mol CO 2 52
53 Άζθεζε 3.22 Να ππνινγίζεηε ηα γξακκάξηα ηνπ νμπγφλνπ ηα νπνία απαηηνχληαη γηα ηελ πιήξε θαχζε ησλ παξαθάησ νπζηψλ, θαζψο θαη ηα γξακκάξηα ηνπ CO 2 ηα νπνία παξάγνληαη θαηά ηελ θαχζε: i. 3,24 g θαηλφιεο, C 6 H 5 OH. ii. 5,14 g νμηθνχ νμένο, CH 3 COOH. iii. 2,18 g αηζαλφιεο, CH 3 CH 2 OH. Λύζε: i. Αξρηθά γξάθνπκε ηελ ηζνζηαζκηζκέλε εμίζσζε θαχζεο ηεο θαηλφιεο: C 6 H 5 OH + 7Ο 2 6CO 2 + 3H 2 O 53
54 Άζθεζε 3.22 Καηφπηλ ππνινγίδνπκε ηα moles ηεο θαηλφιεο: n Μ m 3,24 g n 0,0344 mol C6H5OH 94,11 g/mol Σηε ζπλέρεηα ππνινγίδνπκε ηα moles ηνπ νμπγφλνπ ζχκθσλα κε ηελ ζηνηρεηνκεηξία ηεο αληίδξαζεο: 7 mol O2 0,0344 mol C6H5OH 0,241 1mol C H OH 6 5 mol Έπεηηα, ππνινγίδνπκε ηα γξακκάξηα ηνπ Ο 2 : O 2 n Μ m m n Μ 0,241 mol 32,00 g/mol 7,71 g O2 54
55 Άζθεζε 3.22 Σηε ζπλέρεηα ππνινγίδνπκε ηα moles ηνπ CO 2 ζχκθσλα κε ηελ ζηνηρεηνκεηξία ηεο αληίδξαζεο: 6 mol CO2 0,0344 mol C6H5OH 1mol C H OH Τέινο ππνινγίδνπκε ηα γξακκάξηα ηνπ CΟ 2 : 6 5 0,206 mol CO 2 n m m n Μ 0,206 mol 44,01 g/mol 9,07 g CO Μ 2 ii. 5,14 g νμηθνχ νμένο, CH 3 COOH. iii. 2,18 g αηζαλφιεο, CH 3 CH 2 OH. 55
56 Περηορηζηηθό αληηδρώλ Πρόβιεκα #2: Σε έλα θιεηζηφ δνρείν ηνπνζεηνχληαη 7,0 γξακκάξηα αδψηνπ, Ν 2, θαη 3,0 γξακκάξηα πδξνγφλνπ, H 2, ζε θαηάιιειεο ζπλζήθεο ψζηε λα πξαγκαηνπνηεζεί ρεκηθή αληίδξαζε. Να βξείηε πφζα γξακκάξηα ακκσλίαο, ΝH 3 ζα ζρεκαηηζηνχλ. 56
57 Πεξηνξηζηηθφ αληηδξψλ Σπρλά ζηηο ρεκηθέο αληηδξάζεηο έλα ή πεξηζζφηεξα αληηδξψληα πξνζηίζεληαη ζε αλαινγίεο κεγαιχηεξεο απφ ηηο ζηνηρεηνκεηξηθά απαηηνχκελεο, π.ρ. Ζ 2 + Η 2 2ΖΗ 0,1 mol 0,5 mol Σχκθσλα κε ηε ζηνηρεηνκεηξία ηεο αληίδξαζεο, ε αλαινγία moles H 2 θαη I 2 είλαη 1:1. 57
58 Πεξηνξηζηηθφ αληηδξψλ Σχκθσλα κε ηε ζηνηρεηνκεηξία ηεο αληίδξαζεο θαη ηα αξρηθά moles ησλ αληηδξψλησλ ζπκπεξαίλνπκε φηη: νιφθιεξε ε πνζφηεηα ηνπ Ζ 2 ζα αληηδξάζεη έλα κέξνο ηεο πνζφηεηαο ηνπ Η 2 (ζπγθεθξηκέλα 0,4 mol) ζα πεξηζζέςεη ζα ζρεκαηηζηνχλ 2 0,1 = 0,2 mol HI 58
59 Πεξηνξηζηηθφ αληηδξψλ Τν αληηδξψλ ην νπνίν θαηαλαιψλεηαη πιήξσο φηαλ ε αληίδξαζε θηάζεη ζην ηέξκα ηεο νλνκάδεηαη περηορηζηηθό αληηδρώλ (limiting reactant), ζην πξνεγνχκελν παξάδεηγκα ην Ζ 2. Έλα αληηδξψλ ην νπνίν δελ θαηαλαιψλεηαη πιήξσο νλνκάδεηαη αληηδρώλ ζε περίζζεηα (excess reactant), ζην πξνεγνχκελν παξάδεηγκα ην Η 2. Τα moles ησλ πξντφλησλ θαζνξίδνληαη πάληνηε απφ ηα αξρηθά moles ηνπ πεξηνξηζηηθνχ αληηδξψληνο, ζην πξνεγνχκελν παξάδεηγκα 0,2 mol HI. 59
60 Πεξηνξηζηηθφ αληηδξψλ Σπρλά θαηαζηξψλνπκε έλα πίλαθα ηηκψλ σο εμήο: moles Ζ 2 + Η 2 2ΖΗ Αξρηθά 0,1 0,5 Αληηδξνχλ Παξάγνληαη πεξηνξηζηηθφ αληηδξψλ αληηδξψλ ζε πεξίζζεηα 0,1 0,1 + 0,2 Τειηθά 0 0,4 0,2 Άξα παξάγνληαη 0,2 mol HI θαη περηζζεύοσλ 0,4 mol I 2 60
61 Πεξηνξηζηηθφ αληηδξψλ 61
62 Πεξηνξηζηηθφ αληηδξψλ Έζησ ε αληίδξαζε: 2Ζ 2 + Ο 2 2Ζ 2 Ο 1 mol 1 mol moles 2Ζ 2 + Ο 2 2Ζ 2 Ο Αξρηθά 1 1 Αληηδξνχλ Παξάγνληαη πεξηνξηζηηθφ αληηδξψλ αληηδξψλ ζε πεξίζζεηα 1 0,5 Τειηθά 0 0,
63 Πεξηνξηζηηθφ αληηδξψλ 2Ζ 2 + Ο 2 2Ζ 2 Ο 1 mol 1 mol 63
64 Περηορηζηηθό αληηδρώλ Πρόβιεκα #2: Σε έλα θιεηζηφ δνρείν ηνπνζεηνχληαη 7,0 γξακκάξηα αδψηνπ, Ν 2, θαη 3,0 γξακκάξηα πδξνγφλνπ, H 2, ζε θαηάιιειεο ζπλζήθεο ψζηε λα πξαγκαηνπνηεζεί ρεκηθή αληίδξαζε. Να βξείηε πφζα γξακκάξηα ακκσλίαο, ΝH 3 ζα ζρεκαηηζηνχλ. 64
65 Λύζε ηοσ προβιήκαηος Αξρηθά κεηαηξέπνπκε ηηο κάδεο ησλ αληηδξψλησλ ζε moles. N 2 : n m M 7,0 g 28,01 g/mol 0,25 mol H 2 : n m M 3,0 g 2,02 g/mol 1,5 mol 65
66 Λύζε ηοσ προβιήκαηος Σηε ζπλέρεηα θαηαζηξψλνπκε ηνλ αθφινπζν πίλαθα ηηκψλ: πεξηνξηζηηθφ αληηδξψλ αληηδξψλ ζε πεξίζζεηα moles N 2 + 3H 2 2NΖ 3 Αξρηθά 0,25 1,5 Αληηδξνχλ Παξάγνληαη 0,25 0,75 + 0,50 Τειηθά 0 0,75 0,50 Άξα παξάγνληαη 0,50 17,03 = 8,5 g ΝH 3 θαη περηζζεύοσλ 0,75 2,02 = 1,5 g H 2 66
67 Άζθεζε 3.23 Μεηαιιηθφο ςεπδάξγπξνο θαη πδξνρισξηθφ νμχ αληηδξνχλ ζχκθσλα κε ηελ εμίζσζε: Zn(s) + 2HCl(aq) ZnCl 2 (aq) + H 2 (g) Αλ πξνζηεζνχλ 0,30 mol Zn ζε πδξνρισξηθφ νμχ ην νπνίν πεξηέρεη 0,52 mol HCl, πφζα moles H 2 ζα παξαρζνχλ; Λύζε: Καηαζηξψλνπκε ηνλ αθφινπζν πίλαθα ηηκψλ: 67
68 Άζθεζε 3.23 moles Zn(s) + 2HCl(aq) ZnCl 2 (aq) + Ζ 2 (g) Αξρηθά 0,30 0,52 Αληηδξνχλ 0,26 0,52 Παξάγνληαη + 0,26 + 0,26 Τειηθά 0,04 0 0,26 0,26 Ζ πνζφηεηα ηνπ Ζ 2 ε νπνία παξάγεηαη είλαη 0,26 mol. 68
69 Άζθεζε 3.24 Έζησ ε αληίδξαζε: 2Al(s) + 6HCl(g) 2AlCl 3 (s) + 3H 2 (g) Έζησ φηη ην δνρείν ηεο αληίδξαζεο πεξηέρεη 0,15 mol Al θαη 0,35 mol HCl. Πφζα mol AlCl 3 κπνξνχλ λα παξαρζνχλ; 69
70 Άζθεζε 3.25 Έζησ ε αληίδξαζε: 2CH 3 CHO(l) + O 2 (g) 2CH 3 COOH(l) Σην δνρείν ηεο αληίδξαζεο ηνπνζεηνχληαη 20,0 g αθεηαιδευδεο, CH 3 CHO, θαη 10,0 g O 2. Πφζα γξακκάξηα νμηθνχ νμένο, CH 3 COOH, παξάγνληαη; Πφζα γξακκάξηα απφ ην αληηδξψλ ζε πεξίζζεηα κέλνπλ κεηά ην ηέινο ηεο αληίδξαζεο; 70
71 Άζθεζε 3.25 Αξρηθά ππνινγίδνπκε ηα moles ησλ αληηδξψλησλ: CH 3 CHO: n m M 20,0 g 44,05 g/mol 0,454 mol O 2 : n m M 10,0 g 32,00 g/mol 0,313 mol 71
72 Άζθεζε 3.25 Σηε ζπλέρεηα θαηαζηξψλνπκε ηνλ αθφινπζν πίλαθα ηηκψλ: moles 2CH 3 CHO + O 2 2CH 3 COOH Αξρηθά 0,454 0,313 Αληηδξνχλ Παξάγνληαη πεξηνξηζηηθφ αληηδξψλ αληηδξψλ ζε πεξίζζεηα 0,454 0, ,454 Τειηθά 0 0,086 0,454 Άξα παράγοληαη 0,454 60,05 = 27,3 g CH 3 COOH θαη περηζζεύοσλ 0,086 32,00 = 2,8 g O 2 72
73 Άζθεζε 3.26 Σε έλα πείξακα ζεξκαίλνληαη 7,36 g ςεπδαξγχξνπ κε 6,45 g ζείνπ, ηα νπνία αληηδξνχλ ζχκθσλα κε ηελ εμίζσζε: 8Zn + S 8 8ZnS Πφζε πνζφηεηα ζνπιθηδίνπ ηνπ ςεπδαξγχξνπ παξάρζεθε; 73
74 Άζθεζε 3.27 Έζησ νη αληηδξάζεηο: 2C(s) + O 2 (g) 2CO(g) ZnO(s) + CO(g) Zn(s) + CO 2 (g) Πφζε είλαη ε κέγηζηε πνζφηεηα ςεπδαξγχξνπ ε νπνία κπνξεί λα ιεθζεί απφ 75,0 g νμεηδίνπ ηνπ ςεπδαξγχξνπ θαη 50,0 g άλζξαθα; Λύζε: Αξρηθά ππνινγίδνπκε ηα moles ηνπ άλζξαθα: m 50,0 g C: n 4,16 mol M 12,01 g/mol 74
75 Άζθεζε 3.27 Με βάζε ηε ζηνηρεηνκεηξία ηεο πξψηεο αληίδξαζεο ηα moles ηνπ CO είλαη: 2 mol CO 4,16 mol C 4,16 mol CO 2 mol C Σηε ζπλέρεηα ππνινγίδνπκε ηα moles ηνπ νμεηδίνπ ηνπ ςεπδαξγχξνπ: ZnO: n m M 75,0 g 81,38 g/mol 0,922 mol Σηε ζπλέρεηα θαηαζηξψλνπκε ηνλ αθφινπζν πίλαθα ηηκψλ: 75
76 Άζθεζε 3.27 πεξηνξηζηηθφ αληηδξψλ αληηδξψλ ζε πεξίζζεηα moles ZnO + CO Zn + CO 2 Αξρηθά 0,922 4,16 Αληηδξνχλ Παξάγνληαη 0,922 0, , ,922 Τειηθά 0 3,238 0,922 0,922 Άξα ε κέγηζηε πνζφηεηα ςεπδαξγχξνπ ε νπνία κπνξεί λα ιεθζεί είλαη 0,922 mol ή 0,922 65,38 = 60,3 g Zn. 76
77 Άζθεζε 3.28 Μίγκα 0,500 g Cu 2 O θαη CuO πεξηέρεη 0,425 g Cu. Πφζε είλαη ε κάδα ηνπ CuO ζην κίγκα; Λύζε: Έζησ x θαη y ε κάδα ηνπ Cu 2 O θαη ηνπ CuO αληίζηνηρα. Θα ηζρχεη φηη: x + y = 0,500 Γηα ην Cu 2 O ηζρχεη φηη: 1 mol Cu 2 O πεξηέρεη 2 mol Cu ή 143,09 g Cu 2 O πεξηέρνπλ 2 63,55 = 127,10 g Cu 77
78 Άζθεζε 3.28 Άξα ε κάδα ηνπ ραιθνχ ζην Cu 2 O ζα είλαη: 127,10 g Cu x g Cu 2O 143,09 g Cu O Οκνίσο, γηα ην CuO ηζρχεη φηη: 2 0,88825x g Cu 1 mol CuO πεξηέρεη 1 mol Cu ή 79,55 g CuO πεξηέρνπλ 63,55 g Cu Άξα ε κάδα ηνπ ραιθνχ ζην CuO ζα είλαη: y g CuO 63,55 g Cu 0,7989y g Cu 79,55 g CuO 78
79 Άζθεζε 3.28 Άξα έρνπκε ην εμήο ζχζηεκα εμηζψζεσλ: x + y = 0,500 0,88825x + 0,7989y = 0,425 Λχλνληαο ην ζχζηεκα έρνπκε: x = 0,286 θαη y = 0,214 Άξα ε κάδα ηνπ CuO ζην κίγκα είλαη 0,214 g. 79
80 Θεσξεηηθή θαη πξαγκαηηθή απφδνζε Ζ ζεωρεηηθή απόδοζε ελφο πξντφληνο είλαη ε κέγηζηε πνζφηεηα πξντφληνο ε νπνία κπνξεί λα ιεθζεί ζε κηα αληίδξαζε απφ δεδνκέλεο πνζφηεηεο αληηδξψλησλ. Ζ πραγκαηηθή απόδοζε ελφο πξντφληνο είλαη απηή ε νπνία πξνζδηνξίδεηαη πεηξακαηηθά. Σπλήζσο ε πξαγκαηηθή απφδνζε είλαη κηθξφηεξε ηεο ζεσξεηηθήο ιφγσ: απσιεηψλ θαηά ην δηαρσξηζκφ ησλ πξντφλησλ παξάιιεισλ αληαγσληζηηθψλ αληηδξάζεσλ ρεκηθήο ηζνξξνπίαο 80
81 Δθαηνζηηαία απφδνζε Ζ εθαηνζηηαία απφδνζε ελφο πξντφληνο είλαη ην επί ηνηο εθαηφ πειίθν ηεο πξαγκαηηθήο απφδνζεο πξνο ηε ζεσξεηηθή απφδνζε: Εκαηοζηιαί α απόδοζη ππαγμαηική απόδοζη θεωπηηική απόδοζη 100 (3.3) Αλ ζην παξάδεηγκα 3.15 ε πξαγκαηηθή απφδνζε ζε CH 3 COOH ήηαλ 23,8 g, ηφηε: 23,8 Εκαηοζηιαί α απόδοζη ζε CH3COOH ,3 87,2% 81
82 Άζθεζε 3.29 Έζησ ε αληίδξαζε ηεο κεζαλφιεο, CH 3 OH, κε κνλνμείδην ηνπ άλζξαθα, CO, πξνο ζρεκαηηζκφ νμηθνχ νμεφο, CH 3 COOH: CH 3 OH(l) + CO(g) CH 3 COOH(l) Σε έλα πείξακα, 15,0 g κεζαλφιεο θαη 10,0 g κνλνμεηδίνπ ηνπ άλζξαθα εηζάγνληαη ζην δνρείν ηεο αληίδξαζεο. Πφζε είλαη ε ζεσξεηηθή απφδνζε ζε νμηθφ νμχ; Αλ ε πξαγκαηηθή απφδνζε είλαη 19,1 g, πφζε είλαη ε εθαηνζηηαία απφδνζε; 82
83 Άζθεζε 3.29 Αξρηθά ππνινγίδνπκε ηα moles ησλ αληηδξψλησλ: CH 3 OH: n m M 15,0 g 32,04 g/mol 0,468 mol CO: n m M 10,0 g 28,01 g/mol 0,357 mol 83
84 Άζθεζε 3.29 Σηε ζπλέρεηα θαηαζηξψλνπκε ηνλ αθφινπζν πίλαθα ηηκψλ: moles CH 3 OH + CO CH 3 COOH Αξρηθά 0,468 0,357 Αληηδξνχλ Παξάγνληαη αληηδξψλ ζε πεξίζζεηα πεξηνξηζηηθφ αληηδξψλ 0,357 0, ,357 Τειηθά 0, ,357 Άξα παράγοληαη 0,357 60,05 = 21,4 g CH 3 COOH θαη περηζζεύοσλ 0,111 32,04 = 3,56 g CO 84
85 Άζθεζε 3.29 Ζ εθαηνζηηαία απφδνζε ζε νμηθφ νμχ είλαη: 19,1 Εκαηοζηιαί α απόδοζη ζε CH3COOH ,4 89,3% 85
86 Άζθεζε 3.30 Να ππνινγίζεηε ηελ πνζφηεηα ηνπ CO 2 εθθξαζκέλε ζε kg, ε νπνία εθιχεηαη θαηά ηελ πιήξε θαχζε 150 L βελδίλεο. Να ζεσξήζεηε φηη ν ρεκηθφο ηχπνο ηεο βελδίλεο είλαη C 8 H 18 θαη φηη ε ππθλφηεηα ηεο βελδίλεο ηζνχηαη κε 735 kg/m 3. Απάληεζε: Αξρηθά γξάθνπκε ηελ αληίδξαζε θαχζεο ηνπ νθηαλίνπ: C 8 H /2Ο 2 8CO 2 + 9H 2 O 86
87 Άζθεζε 3.30: Απάληεζε Σηε ζπλέρεηα ππνινγίδνπκε ηε κάδα ηνπ νθηαλίνπ, απφ ηελ ππθλφηεηά ηνπ. Ηζρχεη φηη ξ = 735 kg/m 3 = 735 g/l. Άξα: π m V m πv m 735 g L 150L g Σηε ζπλέρεηα ππνινγίδνπκε ηα mol ηνπ νθηαλίνπ. Ηζρχεη φηη: Μ(C 8 H 18 ) = 114,23 g/mol 87
88 Άζθεζε 3.30: Απάληεζε Άξα: n m M g 114,23 g/mol Σηε ζπλέρεηα ππνινγίδνπκε ηα mol ηνπ CO 2 : n(co 2 ) = 8 n(c 8 H 18 )= 7721,26 965,158 Τέινο, ππνινγίδνπκε ηε κάδα ηνπ CO 2 : mol m nm m 7721,26 mol 44,01 g/mol Γειαδή, ζα ζρεκαηηζηνχλ 340 kg CO 2. g 88
Γεληθή Φεκεία. Νίθνο Ξεθνπθνπισηάθεο Δπίθνπξνο Καζεγεηήο
 Γεληθή Φεκεία Νίθνο Ξεθνπθνπισηάθεο Δπίθνπξνο Καζεγεηήο Πνιπηερλείν Κξήηεο Τκήκα Μεραληθψλ Πεξηβάιινληνο Γξαθείν Κ2.125, ηει.: 28210-37772 e-mail:nikosxek@gmail.com Πεξηερφκελα Καηαζηάζεηο ηεο χιεο αέξηα
Γεληθή Φεκεία Νίθνο Ξεθνπθνπισηάθεο Δπίθνπξνο Καζεγεηήο Πνιπηερλείν Κξήηεο Τκήκα Μεραληθψλ Πεξηβάιινληνο Γξαθείν Κ2.125, ηει.: 28210-37772 e-mail:nikosxek@gmail.com Πεξηερφκελα Καηαζηάζεηο ηεο χιεο αέξηα
Γενική Χημεία. Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής
 Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Μοριακό βάρος και τυπικό
Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Μοριακό βάρος και τυπικό
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΖΜΔΗΑ / Α ΛΥΚΔΗΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 10/02/2013 ΑΠΑΝΤΖΣΔΗΣ ΘΔΜΑ Α. Σελίδα 1 από 5 ΔΙΑΓΩΝΙΣΜΑ ΕΚΠ. ΕΤΟΥΣ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΖΜΔΗΑ / Α ΛΥΚΔΗΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 10/02/2013 ΘΔΜΑ Α ΑΠΑΝΤΖΣΔΗΣ Γηα ηηο εξσηήζεηο Α.1 έσο Α.4 λα γξάςεηε ην γξάκκα πνπ αληηζηνηρεί ζηε ζσζηή απάληεζε δίπια ζηνλ αξηζκό ηεο εξώηεζεο.
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΖΜΔΗΑ / Α ΛΥΚΔΗΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 10/02/2013 ΘΔΜΑ Α ΑΠΑΝΤΖΣΔΗΣ Γηα ηηο εξσηήζεηο Α.1 έσο Α.4 λα γξάςεηε ην γξάκκα πνπ αληηζηνηρεί ζηε ζσζηή απάληεζε δίπια ζηνλ αξηζκό ηεο εξώηεζεο.
Προτεινόμενα Θέματα Οργανικής Χημείας
 Προτεινόμενα Θέματα Οργανικής Χημείας 1. 3 g θνξεζκέλεο κνλνζζελνύο αιθνόιεο Α αθπδαηώλνληαη κε ζέξκαλζε παξνπζία H 2 SO 4, νπόηε ζρεκαηίδεηαη πδξνγνλάλζξαθαο Β κε απόδνζε 60%. Γηα ηελ πνζόηεηα ηνπ Β πνπ
Προτεινόμενα Θέματα Οργανικής Χημείας 1. 3 g θνξεζκέλεο κνλνζζελνύο αιθνόιεο Α αθπδαηώλνληαη κε ζέξκαλζε παξνπζία H 2 SO 4, νπόηε ζρεκαηίδεηαη πδξνγνλάλζξαθαο Β κε απόδνζε 60%. Γηα ηελ πνζόηεηα ηνπ Β πνπ
ΠΡΟΣΕΙΝΟΜΕΝΕ ΛΤΕΙ. β. Η θαηάιπζε είλαη εηεξνγελήο, αθνύ ν θαηαιύηεο είλαη ζηεξεόο ελώ ηα αληηδξώληα αέξηα (βξίζθνληαη ζε δηαθνξεηηθή θάζε).
 ΔΗΑΓΩΓΗΚΔ ΔΞΔΣΑΔΗ ΣΔΚΝΩΝ ΔΛΛΖΝΩΝ ΔΞΩΣΔΡΗΚΟΤ ΚΑΗ ΣΔΚΝΩΝ ΔΛΛΖΝΩΝ ΤΠΑΛΛΖΛΩΝ ΠΟΤ ΤΠΖΡΔΣΟΤΝ ΣΟ ΔΞΩΣΔΡΗΚΟ ΑΒΒΑΣΟ 8 ΔΠΣΔΜΒΡΗΟΤ 2018 ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΥΖΜΔΗΑ ΠΡΟΑΝΑΣΟΛΗΜΟΤ ΠΡΟΣΕΙΝΟΜΕΝΕ ΛΤΕΙ ΘΔΜΑ Α Α1. α Α2.
ΔΗΑΓΩΓΗΚΔ ΔΞΔΣΑΔΗ ΣΔΚΝΩΝ ΔΛΛΖΝΩΝ ΔΞΩΣΔΡΗΚΟΤ ΚΑΗ ΣΔΚΝΩΝ ΔΛΛΖΝΩΝ ΤΠΑΛΛΖΛΩΝ ΠΟΤ ΤΠΖΡΔΣΟΤΝ ΣΟ ΔΞΩΣΔΡΗΚΟ ΑΒΒΑΣΟ 8 ΔΠΣΔΜΒΡΗΟΤ 2018 ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΥΖΜΔΗΑ ΠΡΟΑΝΑΣΟΛΗΜΟΤ ΠΡΟΣΕΙΝΟΜΕΝΕ ΛΤΕΙ ΘΔΜΑ Α Α1. α Α2.
Θέμα Α. Θέμα Β. Α.1 - γ Α.2 - δ Α.3 - γ Α.4 - α Α.5 α. Σ β. Λ γ. Λ δ. Λ ε. Σ
 ΠΑΝΕΛΛΑΔΘΚΕ ΕΞΕΣΑΕΘ Γ ΣΑΞΗ ΗΜΕΡΗΘΟΤ ΓΕΝΘΚΟΤ ΛΤΚΕΘΟΤ ΔΕΤΣΕΡΑ 30 ΜΑΪΟΤ 016 ΕΞΕΣΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΥΗΜΕΘΑ ΠΡΟΑΝΑΣΟΛΘΜΟΤ (ΝΕΟ ΤΣΗΜΑ) (Ενδεικηικές Απανηήζεις) Θέμα Α Α.1 - γ Α. - δ Α.3 - γ Α.4 - α Α.5 α. Σ β.
ΠΑΝΕΛΛΑΔΘΚΕ ΕΞΕΣΑΕΘ Γ ΣΑΞΗ ΗΜΕΡΗΘΟΤ ΓΕΝΘΚΟΤ ΛΤΚΕΘΟΤ ΔΕΤΣΕΡΑ 30 ΜΑΪΟΤ 016 ΕΞΕΣΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΥΗΜΕΘΑ ΠΡΟΑΝΑΣΟΛΘΜΟΤ (ΝΕΟ ΤΣΗΜΑ) (Ενδεικηικές Απανηήζεις) Θέμα Α Α.1 - γ Α. - δ Α.3 - γ Α.4 - α Α.5 α. Σ β.
Φςζική Πποζαναηολιζμού Γ Λςκείος. Αζκήζειρ Ταλανηώζειρ 1 ο Φςλλάδιο
 Φςζική Πποζαναηολιζμού Γ Λςκείος Αζκήζειρ Ταλανηώζειρ 1 ο Φςλλάδιο Επιμέλεια: Αγκανάκηρ Α. Παναγιώηηρ Επωηήζειρ Σωζηό- Λάθορ Να χαπακηηπίζεηε ηιρ παπακάηω πποηάζειρ ωρ ζωζηέρ ή λάθορ: 1. Η ηαιάλησζε είλαη
Φςζική Πποζαναηολιζμού Γ Λςκείος Αζκήζειρ Ταλανηώζειρ 1 ο Φςλλάδιο Επιμέλεια: Αγκανάκηρ Α. Παναγιώηηρ Επωηήζειρ Σωζηό- Λάθορ Να χαπακηηπίζεηε ηιρ παπακάηω πποηάζειρ ωρ ζωζηέρ ή λάθορ: 1. Η ηαιάλησζε είλαη
x x x x tan(2 x) x 2 2x x 1
 ΘΕΡΙΝΟ ΣΜΗΜΑ ΜΑΘΗΜΑΣΙΚΑ Ι ΕΠΑΝΑΛΗΠΣΙΚΕ ΑΚΗΕΙ ΜΕΡΟ Ι 1. Να γίλνπλ νη γξαθηθέο παξαζηάζεηο ησλ παξαθάησ ζπλαξηήζεσλ. t ( i) e ( ii) ln( ) ( iii). Να βξεζεί ην Π.Ο., ν ηύπνο ηεο αλίζηξνθεο θαη ην Π.Τ. ησλ
ΘΕΡΙΝΟ ΣΜΗΜΑ ΜΑΘΗΜΑΣΙΚΑ Ι ΕΠΑΝΑΛΗΠΣΙΚΕ ΑΚΗΕΙ ΜΕΡΟ Ι 1. Να γίλνπλ νη γξαθηθέο παξαζηάζεηο ησλ παξαθάησ ζπλαξηήζεσλ. t ( i) e ( ii) ln( ) ( iii). Να βξεζεί ην Π.Ο., ν ηύπνο ηεο αλίζηξνθεο θαη ην Π.Τ. ησλ
ΠΑΝΔΛΛΑΓΗΚΔ ΔΞΔΣΑΔΗ Γ ΣΑΞΖ ΖΜΔΡΖΗΟΤ ΓΔΝΗΚΟΤ ΛΤΚΔΗΟΤ ΚΑΗ ΔΠΑΛ ΣΔΣΑΡΣΖ 25 ΜΑΨΟΤ 2016 ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΑΡΥΔ ΟΗΚΟΝΟΜΗΚΖ ΘΔΧΡΗΑ ΠΡΟΑΝΑΣΟΛΗΜΟΤ - ΔΠΗΛΟΓΖ
 ΠΑΝΔΛΛΑΓΗΚΔ ΔΞΔΣΑΔΗ Γ ΣΑΞΖ ΖΜΔΡΖΗΟΤ ΓΔΝΗΚΟΤ ΛΤΚΔΗΟΤ ΚΑΗ ΔΠΑΛ ΣΔΣΑΡΣΖ 25 ΜΑΨΟΤ 2016 ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΑΡΥΔ ΟΗΚΟΝΟΜΗΚΖ ΘΔΧΡΗΑ ΠΡΟΑΝΑΣΟΛΗΜΟΤ - ΔΠΗΛΟΓΖ (Δλδεηθηηθέο Απαληήζεηο) ΘΔΜΑ Α Α1. α. Σωζηό β. Λάζνο
ΠΑΝΔΛΛΑΓΗΚΔ ΔΞΔΣΑΔΗ Γ ΣΑΞΖ ΖΜΔΡΖΗΟΤ ΓΔΝΗΚΟΤ ΛΤΚΔΗΟΤ ΚΑΗ ΔΠΑΛ ΣΔΣΑΡΣΖ 25 ΜΑΨΟΤ 2016 ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΑΡΥΔ ΟΗΚΟΝΟΜΗΚΖ ΘΔΧΡΗΑ ΠΡΟΑΝΑΣΟΛΗΜΟΤ - ΔΠΗΛΟΓΖ (Δλδεηθηηθέο Απαληήζεηο) ΘΔΜΑ Α Α1. α. Σωζηό β. Λάζνο
ΕΡΓΑΣΗΡΙΑΚΕ ΑΚΗΕΙ ΠΟΟΣΙΚΗ ΥΗΜΙΚΗ ΑΝΑΛΤΗ
 ΕΡΓΑΣΗΡΙΑΚΕ ΑΚΗΕΙ ΠΟΟΣΙΚΗ ΥΗΜΙΚΗ ΑΝΑΛΤΗ 1. Τηηινκεηξηθή κέζνδνο αλάιπζεο, Βαζηθέο Αξρέο Τηηινκεηξίαο, Μεζνδνινγία, Αλαιπηηθά Σθεύε θαη Όξγαλα. 2. Αιθαιηκεηξία (Πξνζδηνξηζκόο νιηθήο νμύηεηαο μηδηνύ) 3.
ΕΡΓΑΣΗΡΙΑΚΕ ΑΚΗΕΙ ΠΟΟΣΙΚΗ ΥΗΜΙΚΗ ΑΝΑΛΤΗ 1. Τηηινκεηξηθή κέζνδνο αλάιπζεο, Βαζηθέο Αξρέο Τηηινκεηξίαο, Μεζνδνινγία, Αλαιπηηθά Σθεύε θαη Όξγαλα. 2. Αιθαιηκεηξία (Πξνζδηνξηζκόο νιηθήο νμύηεηαο μηδηνύ) 3.
α) ηε κεηαηόπηζε x όηαλ ην ζώκα έρεη κέγηζην ξπζκό κεηαβνιήο ζέζεο δ) ην κέγηζην ξπζκό κεηαβνιήο ηεο ηαρύηεηαο
 Έξγν ελέξγεηα 3 (Λύζε) Σώκα κάδαο m = 4Kg εξεκεί ζηε βάζε θεθιηκέλνπ επηπέδνπ γσλίαο θιίζεο ζ κε εκζ = 0,6 θαη ζπλζ = 0,8. Τν ζώκα αξρίδεη λα δέρεηαη νξηδόληηα δύλακε θαη μεθηλά λα αλεβαίλεη ζην θεθιηκέλν
Έξγν ελέξγεηα 3 (Λύζε) Σώκα κάδαο m = 4Kg εξεκεί ζηε βάζε θεθιηκέλνπ επηπέδνπ γσλίαο θιίζεο ζ κε εκζ = 0,6 θαη ζπλζ = 0,8. Τν ζώκα αξρίδεη λα δέρεηαη νξηδόληηα δύλακε θαη μεθηλά λα αλεβαίλεη ζην θεθιηκέλν
ΔΦΑΡΜΟΜΔΝΑ ΜΑΘΗΜΑΣΙΚΑ ΣΗ ΧΗΜΔΙΑ Ι ΘΔΜΑΣΑ Α επηέκβξηνο 2009. 1. Να ππνινγηζηνύλ νη κεξηθέο παξάγσγνη πξώηεο ηάμεο ηεο ζπλάξηεζεο f(x,y) =
 ΘΔΜΑΣΑ Α επηέκβξηνο 9. Να ππνινγηζηνύλ νη κεξηθέο παξάγσγνη πξώηεο ηάμεο ηεο ζπλάξηεζεο f(,y) = y.. Να ππνινγηζηνύλ ηα νινθιεξώκαηα: a) ln b) a) 3cos b) e sin 4. Να ππνινγηζηεί ην νινθιήξσκα: S ( y) 3
ΘΔΜΑΣΑ Α επηέκβξηνο 9. Να ππνινγηζηνύλ νη κεξηθέο παξάγσγνη πξώηεο ηάμεο ηεο ζπλάξηεζεο f(,y) = y.. Να ππνινγηζηνύλ ηα νινθιεξώκαηα: a) ln b) a) 3cos b) e sin 4. Να ππνινγηζηεί ην νινθιήξσκα: S ( y) 3
ΚΔΦ. 2.4 ΡΗΕΔ ΠΡΑΓΜΑΣΗΚΩΝ ΑΡΗΘΜΩΝ
 ΚΔΦ.. ΡΗΕΔ ΠΡΑΓΜΑΣΗΚΩΝ ΑΡΗΘΜΩΝ Οξηζκόο ηεηξαγσληθήο ξίδαο: Αλ 0 ηόηε νλνκάδνπκε ηεηξαγσληθή ξίδα ηνπ ηελ κε αξλεηηθή ιύζε ηεο εμίζσζεο:. Γειαδή ηεηξαγσληθή ξίδα ηνπ 0 ιέγεηαη ν αξηζκόο 0 πνπ όηαλ πςσζεί
ΚΔΦ.. ΡΗΕΔ ΠΡΑΓΜΑΣΗΚΩΝ ΑΡΗΘΜΩΝ Οξηζκόο ηεηξαγσληθήο ξίδαο: Αλ 0 ηόηε νλνκάδνπκε ηεηξαγσληθή ξίδα ηνπ ηελ κε αξλεηηθή ιύζε ηεο εμίζσζεο:. Γειαδή ηεηξαγσληθή ξίδα ηνπ 0 ιέγεηαη ν αξηζκόο 0 πνπ όηαλ πςσζεί
ΚΕΦ. 2.3 ΑΠΟΛΤΣΗ ΣΘΜΗ ΠΡΑΓΜΑΣΘΚΟΤ ΑΡΘΘΜΟΤ
 ΚΕΦ..3 ΑΠΟΛΤΣΗ ΣΘΜΗ ΠΡΑΓΜΑΣΘΚΟΤ ΑΡΘΘΜΟΤ Οπιζμόρ απόλςηηρ ηιμήρ: Σηνλ άμνλα ησλ πξαγκαηηθώλ αξηζκώλ ζεσξνύκε έλαλ αξηζκό α πνπ ζπκβνιίδεηαη κε ην ζεκείν Α. Η απόζηαζε ηνπ ζεκείνπ Α από ηελ αξρή Ο, δειαδή
ΚΕΦ..3 ΑΠΟΛΤΣΗ ΣΘΜΗ ΠΡΑΓΜΑΣΘΚΟΤ ΑΡΘΘΜΟΤ Οπιζμόρ απόλςηηρ ηιμήρ: Σηνλ άμνλα ησλ πξαγκαηηθώλ αξηζκώλ ζεσξνύκε έλαλ αξηζκό α πνπ ζπκβνιίδεηαη κε ην ζεκείν Α. Η απόζηαζε ηνπ ζεκείνπ Α από ηελ αξρή Ο, δειαδή
Ονομαηεπώνςμο: Μάθημα: ΥΗΜΙΚΗ ΚΑΙ ΙΟΝΣΙΚΗ ΙΟΡΡΟΠΙΑ ΜΔΥΡΙ ΔΚΙ. Δπιμέλεια διαγωνίζμαηορ: Αξιολόγηζη :
 Ονομαηεπώνςμο: Μάθημα: Τλη: Δπιμέλεια διαγωνίζμαηορ: Αξιολόγηζη : ΥΗΜΙΚΗ ΚΑΙ ΙΟΝΣΙΚΗ ΙΟΡΡΟΠΙΑ ΜΔΥΡΙ ΔΚΙ ΘΔΜΑ Α Για ηις ερφηήζεις Α1 εώς Α4 να γράυεηε ζηο ηεηράδιό ζας ηον αριθμό ηης ερώηηζης και δίπλα
Ονομαηεπώνςμο: Μάθημα: Τλη: Δπιμέλεια διαγωνίζμαηορ: Αξιολόγηζη : ΥΗΜΙΚΗ ΚΑΙ ΙΟΝΣΙΚΗ ΙΟΡΡΟΠΙΑ ΜΔΥΡΙ ΔΚΙ ΘΔΜΑ Α Για ηις ερφηήζεις Α1 εώς Α4 να γράυεηε ζηο ηεηράδιό ζας ηον αριθμό ηης ερώηηζης και δίπλα
Σεκαληηθή Σεκείσζε. Απφ ην θπιιάδην απηφ γίλεηαη ππφδεημε ζηνπο καζεηέο πνηα είλαη ηα απαξαίηεηα πνπ πξέπεη λα κειεηήζνπλ.
 Σεκαληηθή Σεκείσζε Απφ ην θπιιάδην απηφ γίλεηαη ππφδεημε ζηνπο καζεηέο πνηα είλαη ηα απαξαίηεηα πνπ πξέπεη λα κειεηήζνπλ. Όκσο, ηαπηφρξνλα ηνλίδνπκε φηη φζνη ζέινπλ λα αζρνιεζνχλ ζνβαξά κε ην κάζεκα ηεο
Σεκαληηθή Σεκείσζε Απφ ην θπιιάδην απηφ γίλεηαη ππφδεημε ζηνπο καζεηέο πνηα είλαη ηα απαξαίηεηα πνπ πξέπεη λα κειεηήζνπλ. Όκσο, ηαπηφρξνλα ηνλίδνπκε φηη φζνη ζέινπλ λα αζρνιεζνχλ ζνβαξά κε ην κάζεκα ηεο
ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΕΣΑΙΡΕΙΑ ΜΑΘΗΜΑΣΙΚΗ ΚΤΣΑΛΟΓΡΟΜΙΑ 2007 ΓΙΑ ΣΟ ΓΤΜΝΑΙΟ Παπασκευή 26 Ιανουαπίου 2007 Σάξη: Α Γυμνασίου ΥΟΛΕΙΟ..
 ΜΑΘΗΜΑΣΙΚΗ ΚΤΣΑΛΟΓΡΟΜΙΑ 2007 ΓΙΑ ΣΟ ΓΤΜΝΑΙΟ Παπασκευή 26 Ιανουαπίου 2007 Σάξη: Α Γυμνασίου έλαξμεο 09.30 ιήμεο 09.45 Σην παξαθάησ ζρήκα θαίλεηαη ηκήκα ελόο πνιενδνκηθνύ ζρεδίνπ κηαο πόιεο. Οη ζθηαζκέλεο
ΜΑΘΗΜΑΣΙΚΗ ΚΤΣΑΛΟΓΡΟΜΙΑ 2007 ΓΙΑ ΣΟ ΓΤΜΝΑΙΟ Παπασκευή 26 Ιανουαπίου 2007 Σάξη: Α Γυμνασίου έλαξμεο 09.30 ιήμεο 09.45 Σην παξαθάησ ζρήκα θαίλεηαη ηκήκα ελόο πνιενδνκηθνύ ζρεδίνπ κηαο πόιεο. Οη ζθηαζκέλεο
ΔΠΙΣΡΟΠΗ ΓΙΑΓΩΝΙΜΩΝ 74 ος ΠΑΝΔΛΛΗΝΙΟ ΜΑΘΗΣΙΚΟ ΓΙΑΓΩΝΙΜΟ ΣΑ ΜΑΘΗΜΑΣΙΚΑ Ο ΘΑΛΗ 19 Οκηωβρίοσ Δνδεικηικές λύζεις
 ΔΛΛΗΝΙΚΗ ΜΑΘΗΜΑΣΙΚΗ ΔΣΑΙΡΔΙΑ Παλεπηζηεκίνπ (Διεπζεξίνπ Βεληδέινπ) 34 06 79 ΑΘΖΝΑ Τει. 36653-367784 - Fax: 36405 e-mail : info@hms.gr www.hms.gr GREEK MATHEMATICAL SOCIETY 34, Panepistimiou (Δleftheriou
ΔΛΛΗΝΙΚΗ ΜΑΘΗΜΑΣΙΚΗ ΔΣΑΙΡΔΙΑ Παλεπηζηεκίνπ (Διεπζεξίνπ Βεληδέινπ) 34 06 79 ΑΘΖΝΑ Τει. 36653-367784 - Fax: 36405 e-mail : info@hms.gr www.hms.gr GREEK MATHEMATICAL SOCIETY 34, Panepistimiou (Δleftheriou
f '(x)g(x)h(x) g'(x)f (x)h(x) h'(x) f (x)g(x)
 ΓΙΑΓΩΝΙΣΜΑ ΣΤΑ ΜΑΘΗΜΑΤΙΚΑ 54 Υλη: Παράγωγοι Γ Λσκείοσ Ον/μο:.. 6--4 Θεη-Τετν. ΘΔΜΑ Α.. Αλ f, g, h ηξεηο παξαγωγίζηκεο ζπλαξηήζεηο ζην λα απνδείμεηε όηη : f () g() h() ' f '()g()h() g'()f ()h() h'() f ()g()
ΓΙΑΓΩΝΙΣΜΑ ΣΤΑ ΜΑΘΗΜΑΤΙΚΑ 54 Υλη: Παράγωγοι Γ Λσκείοσ Ον/μο:.. 6--4 Θεη-Τετν. ΘΔΜΑ Α.. Αλ f, g, h ηξεηο παξαγωγίζηκεο ζπλαξηήζεηο ζην λα απνδείμεηε όηη : f () g() h() ' f '()g()h() g'()f ()h() h'() f ()g()
ΓΙΑΓΩΝΙΣΜΑ Γ ΛΥΚΔΙΟΥ XHMEIA. Ολνκαηεπώλπκν:... Ζκ/λία:... Τάμε: Φξνληθή Γηάξθεηα:.
 ΓΙΑΓΩΝΙΣΜΑ Γ ΛΥΚΔΙΟΥ XHMEIA Ολνκαηεπώλπκν:.... Ζκ/λία:... Τάμε: Φξνληθή Γηάξθεηα:. Βαζκόο: ΘΔΜΑ Α Γηα ηηο πξνηάζεηο Α1 έσο θαη Α5 λα γξάςεηε ζην ηεηξάδηό ζαο ηνλ αξηζκό ηεο πξόηαζεο θαη, δίπια, ην γξάκκα
ΓΙΑΓΩΝΙΣΜΑ Γ ΛΥΚΔΙΟΥ XHMEIA Ολνκαηεπώλπκν:.... Ζκ/λία:... Τάμε: Φξνληθή Γηάξθεηα:. Βαζκόο: ΘΔΜΑ Α Γηα ηηο πξνηάζεηο Α1 έσο θαη Α5 λα γξάςεηε ζην ηεηξάδηό ζαο ηνλ αξηζκό ηεο πξόηαζεο θαη, δίπια, ην γξάκκα
ΓΗΑΓΩΝΗΣΜΑ ΣΤΑ ΜΑΘΖΜΑΤΗΚΑ. Ύλη: Μιγαδικοί-Σσναρηήζεις-Παράγωγοι Θεη.-Τετν. Καη Εήηημα 1 ο :
 ΓΗΑΓΩΝΗΣΜΑ ΣΤΑ ΜΑΘΖΜΑΤΗΚΑ Ον/μο:.. Γ Λσκείοσ Ύλη: Μιγαδικοί-Σσναρηήζεις-Παράγωγοι Θεη.-Τετν. Καη. 11-1-11 Εήηημα 1 ο : Α. Γηα ηελ ζπλάξηεζε f, λα βξείηε ην δηάζηεκα ζην νπνίν είλαη παξαγσγίζηκε θαζώο θαη
ΓΗΑΓΩΝΗΣΜΑ ΣΤΑ ΜΑΘΖΜΑΤΗΚΑ Ον/μο:.. Γ Λσκείοσ Ύλη: Μιγαδικοί-Σσναρηήζεις-Παράγωγοι Θεη.-Τετν. Καη. 11-1-11 Εήηημα 1 ο : Α. Γηα ηελ ζπλάξηεζε f, λα βξείηε ην δηάζηεκα ζην νπνίν είλαη παξαγσγίζηκε θαζώο θαη
Κευάλαιο 8 Μονοπωλιακή Συμπεριφορά- Πολλαπλή Τιμολόγηση
 Κευάλαιο 8 Μονοπωλιακή Συμπεριφορά- Πολλαπλή Τιμολόγηση Πώς πρέπει να τιμολογεί ένα μονοπώλιο; Μέρξη ζηηγκήο ην κνλνπώιην έρεη ζεσξεζεί ζαλ κηα επηρείξεζε ε νπνία πσιεί ην πξντόλ ηεο ζε θάζε πειάηε ζηελ
Κευάλαιο 8 Μονοπωλιακή Συμπεριφορά- Πολλαπλή Τιμολόγηση Πώς πρέπει να τιμολογεί ένα μονοπώλιο; Μέρξη ζηηγκήο ην κνλνπώιην έρεη ζεσξεζεί ζαλ κηα επηρείξεζε ε νπνία πσιεί ην πξντόλ ηεο ζε θάζε πειάηε ζηελ
Ενδεικτικά Θέματα Στατιστικής ΙΙ
 Ενδεικτικά Θέματα Στατιστικής ΙΙ Θέματα. Έζησ όηη ζε δείγκα 35 θαηνηθηώλ πνπ ελνηθηάδνληαη ζε θνηηεηέο ζηελ Κνδάλε βξέζεθε ην κέζν κεληαίν κίζζσκα ζηα 5 επξώ, ελώ ζην Ζξάθιεην ην κέζν κεληαίν κίζζσκα ζε
Ενδεικτικά Θέματα Στατιστικής ΙΙ Θέματα. Έζησ όηη ζε δείγκα 35 θαηνηθηώλ πνπ ελνηθηάδνληαη ζε θνηηεηέο ζηελ Κνδάλε βξέζεθε ην κέζν κεληαίν κίζζσκα ζηα 5 επξώ, ελώ ζην Ζξάθιεην ην κέζν κεληαίν κίζζσκα ζε
Ονομαηεπώνυμο: Μάθημα: Υλη: Δπιμέλεια διαγωνίζμαηος: Αξιολόγηζη :
 Ονομαηεπώνυμο: Μάθημα: Υλη: Δπιμέλεια διαγωνίζμαηος: Αξιολόγηζη : Θέμα Α. Σηιρ επωηήζειρ πολλαπλήρ επιλογήρ πος ακολοςθούν ζημειώζηε ζηο γπαπηό ζαρ ηον απιθμό ηηρ επώηηζηρ και δίπλα ηην ένδειξη ηηρ ζωζηήρ
Ονομαηεπώνυμο: Μάθημα: Υλη: Δπιμέλεια διαγωνίζμαηος: Αξιολόγηζη : Θέμα Α. Σηιρ επωηήζειρ πολλαπλήρ επιλογήρ πος ακολοςθούν ζημειώζηε ζηο γπαπηό ζαρ ηον απιθμό ηηρ επώηηζηρ και δίπλα ηην ένδειξη ηηρ ζωζηήρ
5 η Δργαζηηριακή Άζκηζη Κσκλώμαηα Γσαδικού Αθροιζηή/Αθαιρέηη
 5 η Δργαζηηριακή Άζκηζη Κσκλώμαηα Γσαδικού Αθροιζηή/Αθαιρέηη Σηα πιαίζηα ηεο πέκπηεο εξγαζηεξηαθήο άζθεζεο ζα ρξεζηκνπνηεζεί απνθιεηζηηθά ην πεξηβάιινλ αλάπηπμεο νινθιεξσκέλσλ θπθισκάησλ IDL-800 Digital
5 η Δργαζηηριακή Άζκηζη Κσκλώμαηα Γσαδικού Αθροιζηή/Αθαιρέηη Σηα πιαίζηα ηεο πέκπηεο εξγαζηεξηαθήο άζθεζεο ζα ρξεζηκνπνηεζεί απνθιεηζηηθά ην πεξηβάιινλ αλάπηπμεο νινθιεξσκέλσλ θπθισκάησλ IDL-800 Digital
Απαντήσεις θέματος 2. Παξαθάησ αθνινπζεί αλαιπηηθή επίιπζε ησλ εξσηεκάησλ.
 Απαντήσεις θέματος 2 Απηά πνπ έπξεπε λα γξάςεηε (δελ ρξεηαδόηαλ δηθαηνιόγεζε εθηόο από ην Γ) Α return a*b; Β 0:acegf2, 1: acegf23, 2: acegf234, 3:acegf2345, 4:acegf23456, 5:acegf234567, 6:acegf2345678,
Απαντήσεις θέματος 2 Απηά πνπ έπξεπε λα γξάςεηε (δελ ρξεηαδόηαλ δηθαηνιόγεζε εθηόο από ην Γ) Α return a*b; Β 0:acegf2, 1: acegf23, 2: acegf234, 3:acegf2345, 4:acegf23456, 5:acegf234567, 6:acegf2345678,
ΔΕΟ 13. Ποσοτικές Μέθοδοι. θαη λα ππνινγίζεηε ην θόζηνο γηα 10000 παξαγόκελα πξντόληα. Να ζρεδηαζηεί γηα εύξνο πξντόλησλ έσο 30000.
 ΔΕΟ 13 Ποσοτικές Μέθοδοι Σσνάρηηζη Κόζηοσς C(), μέζο κόζηος C()/. Παράδειγμα 1 Μηα εηαηξεία δαπαλά γηα θάζε πξντόλ Α πνπ παξάγεη 0.0 λ.κ. Τα πάγηα έμνδα ηεο εηαηξείαο είλαη 800 λ.κ. Ζεηείηαη 1) Να πεξηγξάςεηε
ΔΕΟ 13 Ποσοτικές Μέθοδοι Σσνάρηηζη Κόζηοσς C(), μέζο κόζηος C()/. Παράδειγμα 1 Μηα εηαηξεία δαπαλά γηα θάζε πξντόλ Α πνπ παξάγεη 0.0 λ.κ. Τα πάγηα έμνδα ηεο εηαηξείαο είλαη 800 λ.κ. Ζεηείηαη 1) Να πεξηγξάςεηε
ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΕΣΑΙΡΕΙΑ ΜΑΘΗΜΑΤΙΚΗ ΣΚΥΤΑΛΟΓΡΟΜΙΑ 2015 ΓΙΑ ΤΟ ΓΥΜΝΑΣΙΟ Τεηάπηη 28 Ιανουαπίου 2015 ΛΔΥΚΩΣΙΑ Τάξη: Α Γυμναζίου
 ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΕΣΑΙΡΕΙΑ ΜΑΘΗΜΑΤΙΚΗ ΣΚΥΤΑΛΟΓΡΟΜΙΑ 2015 ΓΙΑ ΤΟ ΓΥΜΝΑΣΙΟ Τεηάπηη 28 Ιανουαπίου 2015 ΛΔΥΚΩΣΙΑ Τάξη: Α Γυμναζίου ΠΡΟΒΛΗΜΑ Σε έλα ηνπξλνπά βόιετ δήισζαλ ζπκκεηνρή νκάδεο Γπκλαζίσλ ηεο Κύπξνπ.
ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΕΣΑΙΡΕΙΑ ΜΑΘΗΜΑΤΙΚΗ ΣΚΥΤΑΛΟΓΡΟΜΙΑ 2015 ΓΙΑ ΤΟ ΓΥΜΝΑΣΙΟ Τεηάπηη 28 Ιανουαπίου 2015 ΛΔΥΚΩΣΙΑ Τάξη: Α Γυμναζίου ΠΡΟΒΛΗΜΑ Σε έλα ηνπξλνπά βόιετ δήισζαλ ζπκκεηνρή νκάδεο Γπκλαζίσλ ηεο Κύπξνπ.
ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΔΣΑΙΡΔΙΑ ΠΑΓΚΤΠΡΙΟ ΓΙΑΓΩΝΙΜΟ Α ΛΤΚΔΙΟΤ. Ημεπομηνία: 10/12/11 Ώπα εξέτασηρ: 09:30-12:30 ΠΡΟΣΔΙΝΟΜΔΝΔ ΛΤΔΙ
 ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΔΣΑΙΡΔΙΑ ΠΑΓΚΤΠΡΙΟ ΓΙΑΓΩΝΙΜΟ Α ΛΤΚΔΙΟΤ Ημεπομηνία: 10/12/11 Ώπα εξέτασηρ: 09:30-12:30 ΠΡΟΣΔΙΝΟΜΔΝΔ ΛΤΔΙ Πρόβλημα 1: α) Να δείμεηε όηη αλ ζεηηθνί πξαγκαηηθνί αξηζκνί ηζρύεη: β) Αλ είλαη
ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΔΣΑΙΡΔΙΑ ΠΑΓΚΤΠΡΙΟ ΓΙΑΓΩΝΙΜΟ Α ΛΤΚΔΙΟΤ Ημεπομηνία: 10/12/11 Ώπα εξέτασηρ: 09:30-12:30 ΠΡΟΣΔΙΝΟΜΔΝΔ ΛΤΔΙ Πρόβλημα 1: α) Να δείμεηε όηη αλ ζεηηθνί πξαγκαηηθνί αξηζκνί ηζρύεη: β) Αλ είλαη
x-1 x (x-1) x 5x 2. Να απινπνηεζνύλ ηα θιάζκαηα, έηζη ώζηε λα κελ ππάξρνπλ ξηδηθά ζηνπο 22, 55, 15, 42, 93, 10 5, 12
 ΑΚΖΔΗ ΤΜΝΑΗΟΤ - ΚΤΚΛΟ ΠΡΩΣΟ - - ηα πνηεο ηηκέο ηνπ ηα παξαθάησ θιάζκαηα δελ νξίδνληαη ; (Τπόδεημε : έλα θιάζκα νξίδεηαη αλ ν παξνλνκαζηήο είλαη δηάθνξνο ηνπ κεδελόο) - (-) - (-) - Να απινπνηεζνύλ ηα θιάζκαηα
ΑΚΖΔΗ ΤΜΝΑΗΟΤ - ΚΤΚΛΟ ΠΡΩΣΟ - - ηα πνηεο ηηκέο ηνπ ηα παξαθάησ θιάζκαηα δελ νξίδνληαη ; (Τπόδεημε : έλα θιάζκα νξίδεηαη αλ ν παξνλνκαζηήο είλαη δηάθνξνο ηνπ κεδελόο) - (-) - (-) - Να απινπνηεζνύλ ηα θιάζκαηα
ΦΡΟΝΤΙΣΤΗΡΙΟ Μ.Ε. ΣΥΜΒΟΛΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
Οργανική χημεία. Όλνκα: Δπίζεην: Ζκ/ληα:
 Οργανική χημεία Όλνκα: Δπίζεην: Ζκ/ληα: Θέμα 1 Α)Ποιερ από ηιρ παπακάηυ πποηάζειρ είναι ζυζηέρ (Σ) και ποιερ λάθορ (Λ); 1. Καηά ηελ νμείδσζε ελόο αηόκνπ άλζξαθα, ε ειεθηξνληαθή ηνπ ππθλόηεηα απμάλεηαη.
Οργανική χημεία Όλνκα: Δπίζεην: Ζκ/ληα: Θέμα 1 Α)Ποιερ από ηιρ παπακάηυ πποηάζειρ είναι ζυζηέρ (Σ) και ποιερ λάθορ (Λ); 1. Καηά ηελ νμείδσζε ελόο αηόκνπ άλζξαθα, ε ειεθηξνληαθή ηνπ ππθλόηεηα απμάλεηαη.
ΦΥΣΙΚΗ ΤΩΝ ΡΕΥΣΤΩΝ. G. Mitsou
 ΦΥΣΙΚΗ ΤΩΝ ΡΕΥΣΤΩΝ ηαηηθή ηωλ ξεπζηώλ (Τδξνζηαηηθή) Ση είλαη ηα ξεπζηά - Γεληθά Ππθλόηεηα Πίεζε Μεηαβνιή ηεο πίεζεο ζπλαξηήζεη ηνπ βάζνπο Αξρή ηνπ Pascal Τδξνζηαηηθή πίεζε Αηκνζθαηξηθή πίεζε Απόιπηε &
ΦΥΣΙΚΗ ΤΩΝ ΡΕΥΣΤΩΝ ηαηηθή ηωλ ξεπζηώλ (Τδξνζηαηηθή) Ση είλαη ηα ξεπζηά - Γεληθά Ππθλόηεηα Πίεζε Μεηαβνιή ηεο πίεζεο ζπλαξηήζεη ηνπ βάζνπο Αξρή ηνπ Pascal Τδξνζηαηηθή πίεζε Αηκνζθαηξηθή πίεζε Απόιπηε &
ΘΔΜΑ 1 ο Μονάδες 5,10,10
 ΟΝΟΜΑΣΔΠΩΝΤΜΟ ΗΜΔΡΟΜΗΝΙΑ ΘΔΜΑ 1 ο Μονάδες 5,1,1 ΓΙΑΓΩΝΙΜΑ 1 ου ΜΔΡΟΤ ΣΗ ΑΝΑΛΤΗ Α Γώζηε ηνλ νξηζκό ηεο αληίζηξνθεο ζπλάξηεζεο Β Γείμηε όηη αλ κηα ζπλάξηεζε είλαη αληηζηξέςηκε ηόηε νη γξαθηθέο παξαζηάζεηο
ΟΝΟΜΑΣΔΠΩΝΤΜΟ ΗΜΔΡΟΜΗΝΙΑ ΘΔΜΑ 1 ο Μονάδες 5,1,1 ΓΙΑΓΩΝΙΜΑ 1 ου ΜΔΡΟΤ ΣΗ ΑΝΑΛΤΗ Α Γώζηε ηνλ νξηζκό ηεο αληίζηξνθεο ζπλάξηεζεο Β Γείμηε όηη αλ κηα ζπλάξηεζε είλαη αληηζηξέςηκε ηόηε νη γξαθηθέο παξαζηάζεηο
H ΜΑΓΕΙΑ ΤΩΝ ΑΡΙΘΜΩΝ
 H ΜΑΓΕΙΑ ΤΩΝ ΑΡΙΘΜΩΝ Φξεζηκόηεηα καζεκαηηθώλ Αξρή θαηακέηξεζεο Όζα έδσζαλ νη Έιιελεο... Τξίγσλνη αξηζκνί Τεηξάγσλνη αξηζκνί Δπηκήθεηο αξηζκνί Πξώηνη αξηζκνί Αξηζκνί κε μερσξηζηέο ηδηόηεηεο Γίδπκνη πξώηνη
H ΜΑΓΕΙΑ ΤΩΝ ΑΡΙΘΜΩΝ Φξεζηκόηεηα καζεκαηηθώλ Αξρή θαηακέηξεζεο Όζα έδσζαλ νη Έιιελεο... Τξίγσλνη αξηζκνί Τεηξάγσλνη αξηζκνί Δπηκήθεηο αξηζκνί Πξώηνη αξηζκνί Αξηζκνί κε μερσξηζηέο ηδηόηεηεο Γίδπκνη πξώηνη
iii. iv. γηα ηελ νπνία ηζρύνπλ: f (1) 2 θαη
 ΔΠΑΝΑΛΗΠΣΙΚΑ ΘΔΜΑΣΑ ΣΟ ΓΙΑΦΟΡΙΚΟ ΛΟΓΙΜΟ Μάρτιος 0 ΘΔΜΑ Να ππνινγίζεηε ηα όξηα: i ii lim 0 0 lim iii iv lim e 0 lim e 0 ΘΔΜΑ Γίλεηαη ε άξηηα ζπλάξηεζε '( ) ( ) γηα θάζε 0 * : R R γηα ηελ νπνία ηζρύνπλ:
ΔΠΑΝΑΛΗΠΣΙΚΑ ΘΔΜΑΣΑ ΣΟ ΓΙΑΦΟΡΙΚΟ ΛΟΓΙΜΟ Μάρτιος 0 ΘΔΜΑ Να ππνινγίζεηε ηα όξηα: i ii lim 0 0 lim iii iv lim e 0 lim e 0 ΘΔΜΑ Γίλεηαη ε άξηηα ζπλάξηεζε '( ) ( ) γηα θάζε 0 * : R R γηα ηελ νπνία ηζρύνπλ:
Δπηιέγνληαο ην «Πξνεπηινγή» θάζε θνξά πνπ ζα ζπλδέεζηε ζηελ εθαξκνγή ζα βξίζθεζηε ζηε λέα ρξήζε.
 ΑΝΟΙΓΜΑ ΝΔΑ ΥΡΗΗ 1. Γεκηνπξγείηε ηε λέα ρξήζε από ηελ επηινγή «Παξάκεηξνη/Παξάκεηξνη Δηαηξίαο/Γηαρείξηζε Δηαηξηώλ». Πιεθηξνινγείηε ηνλ θσδηθό ηεο εηαηξίαο ζαο θαη παηάηε Enter. Σηελ έλδεημε «Υξήζεηο» παηάηε
ΑΝΟΙΓΜΑ ΝΔΑ ΥΡΗΗ 1. Γεκηνπξγείηε ηε λέα ρξήζε από ηελ επηινγή «Παξάκεηξνη/Παξάκεηξνη Δηαηξίαο/Γηαρείξηζε Δηαηξηώλ». Πιεθηξνινγείηε ηνλ θσδηθό ηεο εηαηξίαο ζαο θαη παηάηε Enter. Σηελ έλδεημε «Υξήζεηο» παηάηε
ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΑΣΚΗΣΗ
 ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΑΣΚΗΣΗ 1 η : A) 9,8g H 3 PO 4 αντιδρούν με την κατάλληλη ποσότητα NaCl σύμφωνα με την χημική εξίσωση: H 3 PO 4 + 3NaCl Na 3 PO 4 + 3HCl. Να υπολογίσετε πόσα λίτρα αέριου HCl παράγονται,
ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΑΣΚΗΣΗ 1 η : A) 9,8g H 3 PO 4 αντιδρούν με την κατάλληλη ποσότητα NaCl σύμφωνα με την χημική εξίσωση: H 3 PO 4 + 3NaCl Na 3 PO 4 + 3HCl. Να υπολογίσετε πόσα λίτρα αέριου HCl παράγονται,
ml NaOH 2,0 4,0 6,0 8,0 9,0 9,9 10,0 10,1 11,0 12,0 ph 2,5 2,6 2,8 3,1 3,4 4,4 7,0 9,6 10,6 10,9
 ΘΕΜΑ 1 ο Γηάιπκα κνλνπξσηηθνύ νμένο ΗΑ (δηάιπκα Γ) όγθνπ 50mL νγθνκεηξείηαη κε πξόηππν δηάιπκα NaOH 0,2M. Σεκεηώλεηαη ε κεηαβνιή ηνπ ph ηνπ δηαιύκαηνο θαηά δηαζηήκαηα (βιέπε πίλαθα) ml NaOH 2,0 4,0 6,0
ΘΕΜΑ 1 ο Γηάιπκα κνλνπξσηηθνύ νμένο ΗΑ (δηάιπκα Γ) όγθνπ 50mL νγθνκεηξείηαη κε πξόηππν δηάιπκα NaOH 0,2M. Σεκεηώλεηαη ε κεηαβνιή ηνπ ph ηνπ δηαιύκαηνο θαηά δηαζηήκαηα (βιέπε πίλαθα) ml NaOH 2,0 4,0 6,0
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ. Οξηδόληηα θαη θαηαθόξπθε κεηαηόπηζε παξαβνιήο
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ Οξηδόληηα θαη θαηαθόξπθε κεηαηόπηζε παξαβνιήο 1 ε Δξαζηεξηόηεηα Αλνίμηε ην αξρείν «Μεηαηόπηζε παξαβνιήο.ggb». Με ηε καύξε γξακκή παξηζηάλεηαη ε γξαθηθή παξάζηαζε ηεο f(x)=αx 2 πνπ ζα ηελ
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ Οξηδόληηα θαη θαηαθόξπθε κεηαηόπηζε παξαβνιήο 1 ε Δξαζηεξηόηεηα Αλνίμηε ην αξρείν «Μεηαηόπηζε παξαβνιήο.ggb». Με ηε καύξε γξακκή παξηζηάλεηαη ε γξαθηθή παξάζηαζε ηεο f(x)=αx 2 πνπ ζα ηελ
ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΔΣΑΙΡΔΙΑ ΠΑΓΚΤΠΡΙΟ ΓΙΑΓΩΝΙ ΜΟ
 ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΔΣΑΙΡΔΙΑ ΠΑΓΚΤΠΡΙΟ ΓΙΑΓΩΝΙ ΜΟ Α ΛΤΚΔΙΟΤ Ζμεπομηνία: 18/12/10 Ώπα εξέτασηρ: 09:30-12:30 ΠΡΟΣΕΙΝΟΜΕΝΕ ΛΤ ΕΙ 1. Δίλεηαη ην πνιπώλπκν Αλ θαη., λα βξείηε ην ηειεπηαίν ςεθίν ηνπ αξηζκνύ έρνπκε:
ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΔΣΑΙΡΔΙΑ ΠΑΓΚΤΠΡΙΟ ΓΙΑΓΩΝΙ ΜΟ Α ΛΤΚΔΙΟΤ Ζμεπομηνία: 18/12/10 Ώπα εξέτασηρ: 09:30-12:30 ΠΡΟΣΕΙΝΟΜΕΝΕ ΛΤ ΕΙ 1. Δίλεηαη ην πνιπώλπκν Αλ θαη., λα βξείηε ην ηειεπηαίν ςεθίν ηνπ αξηζκνύ έρνπκε:
ΘΔΜΑΤΑ ΤΔΛΙΚΩΝ ΔΞΔΤΑΣΔΩΝ ΣΤΗ ΦΥΣΙΚΟΦΗΜΔΙΑ - ΘΔΩΡΙΑ ΦΡΟΝΙΚΗ ΓΙΑΡΚΔΙΑ: 1 ώρα (14:00-15:00) Α. Φημική Θερμοδσναμική
 ΘΔΜΑΤΑ ΤΔΛΙΚΩΝ ΔΞΔΤΑΣΔΩΝ ΣΤΗ ΦΥΣΙΚΟΦΗΜΔΙΑ - ΘΔΩΡΙΑ 2011-12 ΦΡΟΝΙΚΗ ΓΙΑΡΚΔΙΑ: 1 ώρα (14:00-15:00) Α. Φημική Θερμοδσναμική Βξείηε κηα εθθξαζε γηα ηνλ παξάγνληα ζπκπηεζηόηεηαο ελόο αεξίνπ πνπ αθνινπζεί ηελ
ΘΔΜΑΤΑ ΤΔΛΙΚΩΝ ΔΞΔΤΑΣΔΩΝ ΣΤΗ ΦΥΣΙΚΟΦΗΜΔΙΑ - ΘΔΩΡΙΑ 2011-12 ΦΡΟΝΙΚΗ ΓΙΑΡΚΔΙΑ: 1 ώρα (14:00-15:00) Α. Φημική Θερμοδσναμική Βξείηε κηα εθθξαζε γηα ηνλ παξάγνληα ζπκπηεζηόηεηαο ελόο αεξίνπ πνπ αθνινπζεί ηελ
ΕΞΙΣΩΣΕΙΣ. (iv) (ii) (ii) (ii) 5. Γηα ηηο δηάθνξεο ηηκέο ηνπ ι λα ιπζνύλ νη εμηζώζεηο : x 6 3 9x
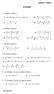 Να ιπζνύλ νη εμηζώζεηο : ( ) 4 ( ) 7 ( )( ) (ii) 5 7 9 4 (iv) 5 6 4 9 6 0 9 6 8 Να ιπζνύλ νη εμηζώζεηο : 7 5 8 (ii) 4 6 8 5 8 ( 6) 4 4 5 (iv) 7 5 4 7 0 7 ( ) 4 8 4 5 8 Να ιπζνύλ νη εμηζώζεηο : ( ) 0 5
Να ιπζνύλ νη εμηζώζεηο : ( ) 4 ( ) 7 ( )( ) (ii) 5 7 9 4 (iv) 5 6 4 9 6 0 9 6 8 Να ιπζνύλ νη εμηζώζεηο : 7 5 8 (ii) 4 6 8 5 8 ( 6) 4 4 5 (iv) 7 5 4 7 0 7 ( ) 4 8 4 5 8 Να ιπζνύλ νη εμηζώζεηο : ( ) 0 5
1. Η απιή αξκνληθή ηαιάλησζε πνπ εθηειεί έλα κηθξό ζώκα κάδαο m = 1 kg έρεη πιάηνο Α = 20 cm θαη
 ΛΤΜΔΝΔ ΑΚΖΔΗ ΣΖΝ ΔΤΡΔΖ ΑΡΥΗΚΖ ΦΑΖ 1. Η αιή αξκνληθή ηαιάλησζε ν εθηειεί έλα κηθξό ζώκα κάδαο m = 1 kg έρεη ιάηνο Α = cm θαη ζρλόηεηα f = 5 Hz. Τε ρξνληθή ζηηγκή = ην κηθξό ζώκα δηέξρεηαη αό ηε ζέζε ανκάθξλζεο
ΛΤΜΔΝΔ ΑΚΖΔΗ ΣΖΝ ΔΤΡΔΖ ΑΡΥΗΚΖ ΦΑΖ 1. Η αιή αξκνληθή ηαιάλησζε ν εθηειεί έλα κηθξό ζώκα κάδαο m = 1 kg έρεη ιάηνο Α = cm θαη ζρλόηεηα f = 5 Hz. Τε ρξνληθή ζηηγκή = ην κηθξό ζώκα δηέξρεηαη αό ηε ζέζε ανκάθξλζεο
ΑΠΑΝΤΗΣΔΙΣ ΘΔΜΑ Α ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Β ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 03/03/2013
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Β ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 03/03/013 ΘΔΜΑ Α ΑΠΑΝΤΗΣΔΙΣ Γηα ηηο εξσηήζεηο Α.1 έσο Α.5 λα γξάςεηε ην γξάκκα πνπ αληηζηνηρεί ζηε ζσζηή απάληεζε δίπια ζηνλ αξηζκό ηεο
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Β ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 03/03/013 ΘΔΜΑ Α ΑΠΑΝΤΗΣΔΙΣ Γηα ηηο εξσηήζεηο Α.1 έσο Α.5 λα γξάςεηε ην γξάκκα πνπ αληηζηνηρεί ζηε ζσζηή απάληεζε δίπια ζηνλ αξηζκό ηεο
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ. Ύλη: Εσθύγραμμη Κίνηζη
 ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ Είμαζηε ηυχεροί που είμαζηε δάζκαλοι Ον/μο:.. A Λσκείοσ Ύλη: Εσθύγραμμη Κίνηζη 8-11-2015 Θέμα 1 ο : 1. Η εμίζωζε θίλεζεο ελόο θηλεηνύ πνπ θηλείηαη επζύγξακκα είλαη ε x = 5t. Πνηα
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ Είμαζηε ηυχεροί που είμαζηε δάζκαλοι Ον/μο:.. A Λσκείοσ Ύλη: Εσθύγραμμη Κίνηζη 8-11-2015 Θέμα 1 ο : 1. Η εμίζωζε θίλεζεο ελόο θηλεηνύ πνπ θηλείηαη επζύγξακκα είλαη ε x = 5t. Πνηα
Άζκηζη ζτέζης κόζηοσς-τρόνοσ (Cost Time trade off) Καηαζκεσαζηική ΑΔ
 Άζκηζη ζτέζης κόζηοσς-τρόνοσ (Cost Time trade off) Καηαζκεσαζηική Δίζηε μησανικόρ διοίκηζηρ μεγάληρ καηαζκεςαζηικήρ εηαιπείαρ και καλείζηε να ςλοποιήζεηε ηο έπγο πος πεπιγπάθεηαι από ηον Πίνακα 1. Κωδ.
Άζκηζη ζτέζης κόζηοσς-τρόνοσ (Cost Time trade off) Καηαζκεσαζηική Δίζηε μησανικόρ διοίκηζηρ μεγάληρ καηαζκεςαζηικήρ εηαιπείαρ και καλείζηε να ςλοποιήζεηε ηο έπγο πος πεπιγπάθεηαι από ηον Πίνακα 1. Κωδ.
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
(γ) Να βξεζεί ε ρξνλνεμαξηώκελε πηζαλόηεηα κέηξεζεο ηεο ζεηηθήο ηδηνηηκήο ηνπ ηειεζηή W.
 ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ Ι Τειηθή Εμέηαζε: 5 Σεπηέκβξε 6 (Δηδάζθσλ: ΑΦ Τεξδήο) ΘΕΜΑ Θεσξνύκε θβαληηθό ζύζηεκα πνπ πεξηγξάθεηαη από Φακηιηνληαλή Η, ε νπνία ζε κνξθή πίλαθα ρξεζηκνπνηώληαο ηηο ηδηνζπλαξηήζεηο, θαη
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ Ι Τειηθή Εμέηαζε: 5 Σεπηέκβξε 6 (Δηδάζθσλ: ΑΦ Τεξδήο) ΘΕΜΑ Θεσξνύκε θβαληηθό ζύζηεκα πνπ πεξηγξάθεηαη από Φακηιηνληαλή Η, ε νπνία ζε κνξθή πίλαθα ρξεζηκνπνηώληαο ηηο ηδηνζπλαξηήζεηο, θαη
ΚΤΠΡΙΑΚΗ ΜΑΘΗΜΑΣΙΚΗ ΕΣΑΙΡΕΙΑ ΜΑΘΗΜΑΣΙΚΗ ΚΤΣΑΛΟΓΡΟΜΙΑ 2007 ΓΙΑ ΣΟ ΓΤΜΝΑΙΟ Παπασκευή 26 Ιανουαπίου 2007 Σάξη: Α Γυμνασίου ΥΟΛΕΙΟ..
 ΜΑΘΗΜΑΣΙΚΗ ΚΤΣΑΛΟΓΡΟΜΙΑ 2007 ΓΙΑ ΣΟ ΓΤΜΝΑΙΟ Παπασκευή 26 Ιανουαπίου 2007 Σάξη: Α Γυμνασίου έλαξμεο 09.30 ιήμεο 09.45 Σην παξαθάησ ζρήκα θαίλεηαη ηκήκα ελόο πνιενδνκηθνύ ζρεδίνπ κηαο πόιεο. Οη ζθηαζκέλεο
ΜΑΘΗΜΑΣΙΚΗ ΚΤΣΑΛΟΓΡΟΜΙΑ 2007 ΓΙΑ ΣΟ ΓΤΜΝΑΙΟ Παπασκευή 26 Ιανουαπίου 2007 Σάξη: Α Γυμνασίου έλαξμεο 09.30 ιήμεο 09.45 Σην παξαθάησ ζρήκα θαίλεηαη ηκήκα ελόο πνιενδνκηθνύ ζρεδίνπ κηαο πόιεο. Οη ζθηαζκέλεο
Ονομαηεπώνςμο: Φημεία Γ Λςκείος. Δπαναληπηικό εθ οληρ ηηρ ύληρ. Ημεπομηνία: Σάββαηο 20 Αππιλίος Αξιολόγηζη : Σχολικό έτος Σελίδα 1
 Ονομαηεπώνςμο: Μάθημα: Υλη: Δπιμέλεια διαγωνίζμαηορ: Φημεία Γ Λςκείος Δπαναληπηικό εθ οληρ ηηρ ύληρ Κακαπώνη Φωηεινή Φημικόρ Ημεπομηνία: Σάββαηο 20 Αππιλίος 2019 Αξιολόγηζη : Σχολικό έτος 2018-2019 Σελίδα
Ονομαηεπώνςμο: Μάθημα: Υλη: Δπιμέλεια διαγωνίζμαηορ: Φημεία Γ Λςκείος Δπαναληπηικό εθ οληρ ηηρ ύληρ Κακαπώνη Φωηεινή Φημικόρ Ημεπομηνία: Σάββαηο 20 Αππιλίος 2019 Αξιολόγηζη : Σχολικό έτος 2018-2019 Σελίδα
66. Ομογενής ράβδος ποσ περιζηρέθεηαι
 1 66. Ομογενής ράβδος ποσ περιζηρέθεηαι Λεπηή νκνγελήο ξάβδνο Α κήθνπο L=1 θαη κάδαο Μ=Kg, κπνξεί λα ζηξέθεηαη ζε θαηαθόξπθν επίπεδν ρωξίο ηξηβέο γύξω από νξηδόληην άμνλα πνπ πεξλά από ην άθξν ηεο Α. Σην
1 66. Ομογενής ράβδος ποσ περιζηρέθεηαι Λεπηή νκνγελήο ξάβδνο Α κήθνπο L=1 θαη κάδαο Μ=Kg, κπνξεί λα ζηξέθεηαη ζε θαηαθόξπθν επίπεδν ρωξίο ηξηβέο γύξω από νξηδόληην άμνλα πνπ πεξλά από ην άθξν ηεο Α. Σην
ΟΠΤΙΚΗ Α. ΑΝΑΚΛΑΣΖ - ΓΗΑΘΛΑΣΖ
 ΟΠΤΙΚΗ Α. ΑΝΑΚΛΑΣΖ - ΓΗΑΘΛΑΣΖ. Μία αθηίλα θωηόο πξνζπίπηεη κε κία γωλία ζ ζηε επάλω επηθάλεηα ελόο θύβνπ από πνιπεζηέξα ν νπνίνο έρεη δείθηε δηάζιαζεο ε =,49 (ζρήκα ). Βξείηε πνηα ζα είλαη ε κέγηζηε γωλία
ΟΠΤΙΚΗ Α. ΑΝΑΚΛΑΣΖ - ΓΗΑΘΛΑΣΖ. Μία αθηίλα θωηόο πξνζπίπηεη κε κία γωλία ζ ζηε επάλω επηθάλεηα ελόο θύβνπ από πνιπεζηέξα ν νπνίνο έρεη δείθηε δηάζιαζεο ε =,49 (ζρήκα ). Βξείηε πνηα ζα είλαη ε κέγηζηε γωλία
ΓΔΧΜΔΣΡΙΑ ΓΙΑ ΟΛΤΜΠΙΑΓΔ
 ΒΑΓΓΔΛΗ ΦΤΥΑ 2009 ελίδα 2 από 9 ΔΤΘΔΙΔ SIMSON 1 ΒΑΙΚΔ ΠΡΟΣΑΔΙ 1.1 ΔΤΘΔΙΑ SIMSON Γίλεηαη ηξίγσλν AB θαη ηπρόλ ζεκείν ηνπ πεξηγεγξακκέλνπ θύθινπ ηνπ. Αλ 1, 1 θαη 1 είλαη νη πξνβνιέο ηνπ ζηηο επζείεο πνπ
ΒΑΓΓΔΛΗ ΦΤΥΑ 2009 ελίδα 2 από 9 ΔΤΘΔΙΔ SIMSON 1 ΒΑΙΚΔ ΠΡΟΣΑΔΙ 1.1 ΔΤΘΔΙΑ SIMSON Γίλεηαη ηξίγσλν AB θαη ηπρόλ ζεκείν ηνπ πεξηγεγξακκέλνπ θύθινπ ηνπ. Αλ 1, 1 θαη 1 είλαη νη πξνβνιέο ηνπ ζηηο επζείεο πνπ
ΜΙΓΑΔΙΚΟΙ ΑΡΙΘΜΟΙ: έζησ
 ΜΙΓΑΔΙΚΙ ΑΡΙΘΜΙ: έζησ έλαο κηγαδηθόο αξηζκόο. αληίζηξνθνο ηνπ κηγαδηθνύ αξηζκνύ a b είλαη ν αξηζκόο Παπάδειγμα: έζησ.αληίζηξνθνο ηνπ αξηζκνύ : Μέηπο μιγαδικού απιθμού: αλ κέηξν δηαλύζκαηνο OM. b ή απόιπηε
ΜΙΓΑΔΙΚΙ ΑΡΙΘΜΙ: έζησ έλαο κηγαδηθόο αξηζκόο. αληίζηξνθνο ηνπ κηγαδηθνύ αξηζκνύ a b είλαη ν αξηζκόο Παπάδειγμα: έζησ.αληίζηξνθνο ηνπ αξηζκνύ : Μέηπο μιγαδικού απιθμού: αλ κέηξν δηαλύζκαηνο OM. b ή απόιπηε
ΕΞΙΣΩΣΕΙΣ. Α. Πρωτοβάθμιεσ Εξιςώςεισ. Β. Διερεφνηςη Εξιςώςεων. 1x είναι αδφνατθ. x 1 x 1. Άλγεβρα Α Λυκείου
 ΕΞΙΣΩΣΕΙΣ Α. Πρωτοβάθμιεσ Εξιςώςεισ. 1. Να λυκεί θ εξίςωςθ (x - 4) (x +5) x -5 5(x +1) - - = - - x 4 6. Να λυκεί θ εξίςωςθ x (x+1)+x(x+1)+x+1=0. Να λυκεί θ εξίςωςθ x(x -4)-x +x =0 4. Να λυκεί θ εξίςωςθ
ΕΞΙΣΩΣΕΙΣ Α. Πρωτοβάθμιεσ Εξιςώςεισ. 1. Να λυκεί θ εξίςωςθ (x - 4) (x +5) x -5 5(x +1) - - = - - x 4 6. Να λυκεί θ εξίςωςθ x (x+1)+x(x+1)+x+1=0. Να λυκεί θ εξίςωςθ x(x -4)-x +x =0 4. Να λυκεί θ εξίςωςθ
Περιβαλλοντική Χημεία - Γεωχημεία
 Περιβαλλοντική Χημεία - Γεωχημεία Διαφάνειεσ 5 ου Μαθήματοσ ακ. Έτοσ 2016-2017 Γαλάνη Απ. Αγγελική, Χημικόσ Ph.D. Εργαςτηριακό Διδακτικό Προςωπικό (Ε.ΔΙ.Π.) Χημείασ Να ππνινγηζηεί ην γηλφκελν δηαιπηφηεηαο
Περιβαλλοντική Χημεία - Γεωχημεία Διαφάνειεσ 5 ου Μαθήματοσ ακ. Έτοσ 2016-2017 Γαλάνη Απ. Αγγελική, Χημικόσ Ph.D. Εργαςτηριακό Διδακτικό Προςωπικό (Ε.ΔΙ.Π.) Χημείασ Να ππνινγηζηεί ην γηλφκελν δηαιπηφηεηαο
Ονοματεπώνυμο:.. Ημερομηνία:. ΔΠΑΝΑΛΗΠΤΙΚΟ ΓΙΑΓΩΝΙΣΜΑ 1 ου ΚΑΙ 3 ου ΚΔΦΑΛΑΙΟ Γ ΛΥΚΔΙΟΥ
 Ονοματεπώνυμο: Ημερομηνία: Γάθηζεο Δκκαλνπήι ΔΠΑΝΑΛΗΠΤΙΚΟ ΓΙΑΓΩΝΙΣΜΑ 1 ου ΚΑΙ 3 ου ΚΔΦΑΛΑΙΟ Γ ΛΥΚΔΙΟΥ ΘΔΜΑ 1 ο Α Να επηιέμεηε ηε ζσζηή απάληεζε 11 Πνην από ηα παξαθάησ άηνκα ή ηόληα έρεη δηαθνξεηηθό αξηζκό
Ονοματεπώνυμο: Ημερομηνία: Γάθηζεο Δκκαλνπήι ΔΠΑΝΑΛΗΠΤΙΚΟ ΓΙΑΓΩΝΙΣΜΑ 1 ου ΚΑΙ 3 ου ΚΔΦΑΛΑΙΟ Γ ΛΥΚΔΙΟΥ ΘΔΜΑ 1 ο Α Να επηιέμεηε ηε ζσζηή απάληεζε 11 Πνην από ηα παξαθάησ άηνκα ή ηόληα έρεη δηαθνξεηηθό αξηζκό
ΜΑΘΗΜΑΤΙΚΑ ΘΔΤΙΚΗΣ ΚΑΙ ΤΔΦΝΟΛΟΓΙΚΗΣ ΚΑΤΔΥΘΥΝΣΗΣ Β ΛΥΚΔΙΟΥ ΤΔΣΤ(1) ΣΤΑ ΓΙΑΝΥΣΜΑΤΑ
 ΜΑΘΗΜΑΤΙΚΑ ΘΔΤΙΚΗΣ ΚΑΙ ΤΔΦΝΟΛΟΓΙΚΗΣ ΚΑΤΔΥΘΥΝΣΗΣ Β ΛΥΚΔΙΟΥ ΤΔΣΤ() ΣΤΑ ΓΙΑΝΥΣΜΑΤΑ ΘΔΜΑ : Αλ ηζρύεη 3 3, λα δείμεηε όηη ηα ζεκεία Μ, Ν ηαπηίδνληαη. ΘΔΜΑ : Α Β Μ Γ Σην παξαπάλσ ζρήκα είλαη 3. α) Γείμηε όηη
ΜΑΘΗΜΑΤΙΚΑ ΘΔΤΙΚΗΣ ΚΑΙ ΤΔΦΝΟΛΟΓΙΚΗΣ ΚΑΤΔΥΘΥΝΣΗΣ Β ΛΥΚΔΙΟΥ ΤΔΣΤ() ΣΤΑ ΓΙΑΝΥΣΜΑΤΑ ΘΔΜΑ : Αλ ηζρύεη 3 3, λα δείμεηε όηη ηα ζεκεία Μ, Ν ηαπηίδνληαη. ΘΔΜΑ : Α Β Μ Γ Σην παξαπάλσ ζρήκα είλαη 3. α) Γείμηε όηη
ΑΛΛΑΓΗ ΟΝΟΜΑΣΟ ΚΑΙ ΟΜΑΔΑ ΕΡΓΑΙΑ, ΚΟΙΝΟΥΡΗΣΟΙ ΦΑΚΕΛΟΙ ΚΑΙ ΕΚΣΤΠΩΣΕ ΣΑ WINDOWS XP
 ΑΛΛΑΓΗ ΟΝΟΜΑΣΟ ΚΑΙ ΟΜΑΔΑ ΕΡΓΑΙΑ, ΚΟΙΝΟΥΡΗΣΟΙ ΦΑΚΕΛΟΙ ΚΑΙ ΕΚΣΤΠΩΣΕ ΣΑ WINDOWS XP ηότοι εργαζηηρίοσ ην πιαίζην ηνπ ζπγθεθξηκέλνπ εξγαζηεξίνπ ζα παξνπζηαζηνύλ βαζηθέο ιεηηνπξγίεο ησλ Windows XP πνπ ζρεηίδνληαη
ΑΛΛΑΓΗ ΟΝΟΜΑΣΟ ΚΑΙ ΟΜΑΔΑ ΕΡΓΑΙΑ, ΚΟΙΝΟΥΡΗΣΟΙ ΦΑΚΕΛΟΙ ΚΑΙ ΕΚΣΤΠΩΣΕ ΣΑ WINDOWS XP ηότοι εργαζηηρίοσ ην πιαίζην ηνπ ζπγθεθξηκέλνπ εξγαζηεξίνπ ζα παξνπζηαζηνύλ βαζηθέο ιεηηνπξγίεο ησλ Windows XP πνπ ζρεηίδνληαη
Σύνθεζη ηαλανηώζεων. Έζησ έλα ζώκα πνπ εθηειεί ηαπηόρξνλα δύν αξκνληθέο ηαιαληώζεηο ηεο ίδηαο ζπρλόηεηαο πνπ πεξηγξάθνληαη από ηηο παξαθάησ εμηζώζεηο:
 Σύνθεζη ηαλανηώζεων Α. Σύλζεζε δύν α.α.η ηεο ίδιας ζστνόηηηας Έζησ έλα ζώκα πνπ εθηειεί ηαπηόρξνλα δύν αξκνληθέο ηαιαληώζεηο ηεο ίδηαο ζπρλόηεηαο πνπ πεξηγξάθνληαη από ηηο παξαθάησ εμηζώζεηο: Η απνκάθξπλζε
Σύνθεζη ηαλανηώζεων Α. Σύλζεζε δύν α.α.η ηεο ίδιας ζστνόηηηας Έζησ έλα ζώκα πνπ εθηειεί ηαπηόρξνλα δύν αξκνληθέο ηαιαληώζεηο ηεο ίδηαο ζπρλόηεηαο πνπ πεξηγξάθνληαη από ηηο παξαθάησ εμηζώζεηο: Η απνκάθξπλζε
Τν εθπαηδεπηηθό πιηθό ηεο Φξνληηζηεξηαθήο Δθπαίδεπζεο Τζηάξα δηαλέκεηαη δωξεάλ απνθιεηζηηθά από ηνλ ψεθηαθό ηόπν ηνπ schooltime.gr
 Τν εθπαηδεπηηθό πιηθό ηεο Φξνηηζηεξηαθήο Δθπαίδεπζεο Τζηάξα δηαέκεηαη δωξεά απνθιεηζηηθά από ην ψεθηαθό ηόπν ηνπ schooltime.gr Η έα ηζηνζειίδα καο : www. Μ ΑΘΗΜ ΑΤΙΚΑ α x +β< 0 Γ ΓΥΜΝΑΣΙΟΥ α.(β +γ )α.
Τν εθπαηδεπηηθό πιηθό ηεο Φξνηηζηεξηαθήο Δθπαίδεπζεο Τζηάξα δηαέκεηαη δωξεά απνθιεηζηηθά από ην ψεθηαθό ηόπν ηνπ schooltime.gr Η έα ηζηνζειίδα καο : www. Μ ΑΘΗΜ ΑΤΙΚΑ α x +β< 0 Γ ΓΥΜΝΑΣΙΟΥ α.(β +γ )α.
Μονοψϊνιο. Αγνξά κε ιίγνπο αγνξαζηέο. Δύναμη μονοψωνίος Η ηθαλόηεηα πνπ έρεη ν αγνξαζηήο λα επεξεάζεη ηελ ηηκή ηνπ αγαζνύ.
 Μονοψϊνιο Ολιγοψώνιο Αγνξά κε ιίγνπο αγνξαζηέο. Δύναμη μονοψωνίος Η ηθαλόηεηα πνπ έρεη ν αγνξαζηήο λα επεξεάζεη ηελ ηηκή ηνπ αγαζνύ. Οπιακή αξία Δπηπξόζζεηα νθέιε από ηελ ρξήζε/θαηαλάισζε κηαο επηπξόζζεηε
Μονοψϊνιο Ολιγοψώνιο Αγνξά κε ιίγνπο αγνξαζηέο. Δύναμη μονοψωνίος Η ηθαλόηεηα πνπ έρεη ν αγνξαζηήο λα επεξεάζεη ηελ ηηκή ηνπ αγαζνύ. Οπιακή αξία Δπηπξόζζεηα νθέιε από ηελ ρξήζε/θαηαλάισζε κηαο επηπξόζζεηε
Q Η ζσνάρηηζη μέζοσ κόζηοσς μας δίνει ηο κόζηος ανά μονάδα παραγωγής. Q Η ζσνάρηηζη μέζοσ κόζηοσς μας δίνει ηο ζηαθερό κόζηος ανά μονάδα παραγωγής
 ΜΙΚΡΟΟΙΚΟΝΟΜΙΚΗ ΘΕΩΡΙΑ ΣΟΜΟ Α Mάθημα 5: To παραγωγής σναρηήζεις κόζηοσς Η ζπλάξηεζε ζπλνιηθνύ θόζηνπο C FC VC Όπνπ FC= ην ζηαζεξό θόζηνο (ην θόζηνο γηα ηνλ ζηαζεξό παξαγσγηθό ζπληειεζηή) θαη VC= ην κεηαβιεηό
ΜΙΚΡΟΟΙΚΟΝΟΜΙΚΗ ΘΕΩΡΙΑ ΣΟΜΟ Α Mάθημα 5: To παραγωγής σναρηήζεις κόζηοσς Η ζπλάξηεζε ζπλνιηθνύ θόζηνπο C FC VC Όπνπ FC= ην ζηαζεξό θόζηνο (ην θόζηνο γηα ηνλ ζηαζεξό παξαγσγηθό ζπληειεζηή) θαη VC= ην κεηαβιεηό
ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
 ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΣΠΟΥΔΕΣ ΣΤΙΣ ΦΥΣΙΚΕΣ ΕΠΙΣΤΗΜΕΣ ΓΕΝΙΚΑ ΜΑΘΗΜΑΤΙΚΑ ΙΙ - ΦΥΕ 0 7 Ινπλίνπ 009 Απαντήσειρ στιρ ασκήσειρ τηρ τελικήρ εξέτασηρ στιρ Σςνήθειρ Διαυοπικέρ Εξισώσειρ Αγαπηηέ θοιηηηή/ηπια,
ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΣΠΟΥΔΕΣ ΣΤΙΣ ΦΥΣΙΚΕΣ ΕΠΙΣΤΗΜΕΣ ΓΕΝΙΚΑ ΜΑΘΗΜΑΤΙΚΑ ΙΙ - ΦΥΕ 0 7 Ινπλίνπ 009 Απαντήσειρ στιρ ασκήσειρ τηρ τελικήρ εξέτασηρ στιρ Σςνήθειρ Διαυοπικέρ Εξισώσειρ Αγαπηηέ θοιηηηή/ηπια,
ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ ΕΚΦΩΝΗΣΕΙΣ. Διάρκεια: 3 ώρες Ημερομηνία: 12/5/2019 Έκδοση: 1 η. Τα sites blogs που συμμετέχουν (σε αλφαβητική σειρά):
 Τα sites blogs που συμμετέχουν (σε αλφαβητική σειρά): blogsschgr/iordaniskos/ Επιμελητής: Ιορδάνης Κόσογλου blogsschgr/pavtryfon/ Επιμελητής: Παύλος Τρύφων eisatoponblogspotgr/ Επιμελητής: Σωκράτης Ρωμανίδης
Τα sites blogs που συμμετέχουν (σε αλφαβητική σειρά): blogsschgr/iordaniskos/ Επιμελητής: Ιορδάνης Κόσογλου blogsschgr/pavtryfon/ Επιμελητής: Παύλος Τρύφων eisatoponblogspotgr/ Επιμελητής: Σωκράτης Ρωμανίδης
ΧΗΜΕΙΑ Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ
 Γιάννης Κεφαλλωνίτης Βύρων Χρηστίδης ΧΗΜΕΙΑ Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΛΥΣΕΙΣ ΣΕ ΕΠΙΛΕΓΜΕΝΑ ΘΕΜΑΤΑ ΑΠΟ ΤΗΝ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ 3996 Θέμα 2 ο 2.1.Να συμπληρώσετε τις χημικές εξισώσεις (προϊόντα και συντελεστές) των
Γιάννης Κεφαλλωνίτης Βύρων Χρηστίδης ΧΗΜΕΙΑ Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΛΥΣΕΙΣ ΣΕ ΕΠΙΛΕΓΜΕΝΑ ΘΕΜΑΤΑ ΑΠΟ ΤΗΝ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ 3996 Θέμα 2 ο 2.1.Να συμπληρώσετε τις χημικές εξισώσεις (προϊόντα και συντελεστές) των
Γ ΣΑΞΖ ΔΝΗΑΗΟΤ ΛΤΚΔΗΟΤ ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΜΑΘΖΜΑΣΗΚΑ ΘΔΣΗΚΩΝ ΚΑΗ ΟΗΚΟΝΟΜΗΚΩΝ ΠΟΤΓΩΝ ΤΝΑΡΣΖΔΗ ΟΡΗΑ ΤΝΔΥΔΗΑ (έως Θ.Bolzano) ΘΔΜΑ Α
 Γ ΣΑΞΖ ΔΝΗΑΗΟΤ ΛΤΚΔΗΟΤ ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΜΑΘΖΜΑΣΗΚΑ ΘΔΣΗΚΩΝ ΚΑΗ ΟΗΚΟΝΟΜΗΚΩΝ ΠΟΤΓΩΝ ΤΝΑΡΣΖΔΗ ΟΡΗΑ ΤΝΔΥΔΗΑ (έως Θ.Bolzano). Να δηαηππώζεηε ην Θ.Bolzano. 5 ΘΔΜΑ Α μονάδες A. Να απνδείμεηε όηη γηα θάζε πνιπωλπκηθή
Γ ΣΑΞΖ ΔΝΗΑΗΟΤ ΛΤΚΔΗΟΤ ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΜΑΘΖΜΑΣΗΚΑ ΘΔΣΗΚΩΝ ΚΑΗ ΟΗΚΟΝΟΜΗΚΩΝ ΠΟΤΓΩΝ ΤΝΑΡΣΖΔΗ ΟΡΗΑ ΤΝΔΥΔΗΑ (έως Θ.Bolzano). Να δηαηππώζεηε ην Θ.Bolzano. 5 ΘΔΜΑ Α μονάδες A. Να απνδείμεηε όηη γηα θάζε πνιπωλπκηθή
Αιγόξηζκνη Γνκή επηινγήο. Πνιιαπιή Δπηινγή Δκθωιεπκέλεο Δπηινγέο. Δηζαγωγή ζηηο Αξρέο ηεο Δπηζηήκεο ηωλ Η/Υ. introcsprinciples.wordpress.
 Αιγόξηζκνη 2.2.7.3 Γνκή επηινγήο Πνιιαπιή Δπηινγή Δκθωιεπκέλεο Δπηινγέο Δηζαγωγή ζηηο Αξρέο ηεο Δπηζηήκεο ηωλ Η/Υ 1 Πνιιαπιή Δληνιή Δπηινγήο Αν ζπλζήθε_1 ηόηε εληνιέο_1 αλλιώς_αν ζπλζήθε_2 ηόηε εληνιέο_2...
Αιγόξηζκνη 2.2.7.3 Γνκή επηινγήο Πνιιαπιή Δπηινγή Δκθωιεπκέλεο Δπηινγέο Δηζαγωγή ζηηο Αξρέο ηεο Δπηζηήκεο ηωλ Η/Υ 1 Πνιιαπιή Δληνιή Δπηινγήο Αν ζπλζήθε_1 ηόηε εληνιέο_1 αλλιώς_αν ζπλζήθε_2 ηόηε εληνιέο_2...
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 4
 ΚΕΦΑΛΑΙΟ 4 ΣΤΟΙΧΕΙΟΜΕΤΡΙΑ ΕΡΩΤΗΣΕΙΣ ΜΕ ΤΙΣ ΑΠΑΝΤΗΣΕΙΣ: 1. Τι είναι ατομικό και τί μοριακό βάρος; Ατομικό βάρος είναι ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη η μάζα του ατόμου από το 1/12 της
ΚΕΦΑΛΑΙΟ 4 ΣΤΟΙΧΕΙΟΜΕΤΡΙΑ ΕΡΩΤΗΣΕΙΣ ΜΕ ΤΙΣ ΑΠΑΝΤΗΣΕΙΣ: 1. Τι είναι ατομικό και τί μοριακό βάρος; Ατομικό βάρος είναι ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη η μάζα του ατόμου από το 1/12 της
Βάσεις Δεδομέμωμ. Εξγαζηήξην V. Τκήκα Πιεξνθνξηθήο ΑΠΘ 2015-2016
 Βάσεις Δεδομέμωμ Εξγαζηήξην V Τκήκα Πιεξνθνξηθήο ΑΠΘ 2015-2016 2 Σκοπός του 5 ου εργαστηρίου Σθνπόο απηνύ ηνπ εξγαζηεξίνπ είλαη: ε κειέηε ζύλζεησλ εξσηεκάησλ ζύλδεζεο ζε δύν ή πεξηζζόηεξεο ζρέζεηο ε κειέηε
Βάσεις Δεδομέμωμ Εξγαζηήξην V Τκήκα Πιεξνθνξηθήο ΑΠΘ 2015-2016 2 Σκοπός του 5 ου εργαστηρίου Σθνπόο απηνύ ηνπ εξγαζηεξίνπ είλαη: ε κειέηε ζύλζεησλ εξσηεκάησλ ζύλδεζεο ζε δύν ή πεξηζζόηεξεο ζρέζεηο ε κειέηε
Αζθήζεηο 5 νπ θεθαιαίνπ Crash course Step by step training. Dipl.Biol.cand.med. Stylianos Kalaitzis
 Αζθήζεηο 5 νπ θεθαιαίνπ Crash course Step by step training Dipl.Biol.cand.med. Stylianos Kalaitzis Stylianos Kalaitzis Μνλνϋβξηδηζκνο 1 Γπν γνλείο, εηεξόδπγνη γηα ηνλ αιθηζκό θάλνπλ παηδηά. Πνία ε πηζαλόηεηα
Αζθήζεηο 5 νπ θεθαιαίνπ Crash course Step by step training Dipl.Biol.cand.med. Stylianos Kalaitzis Stylianos Kalaitzis Μνλνϋβξηδηζκνο 1 Γπν γνλείο, εηεξόδπγνη γηα ηνλ αιθηζκό θάλνπλ παηδηά. Πνία ε πηζαλόηεηα
Αζκήζεις ζτ.βιβλίοσ ζελίδας 13 14
 .1.10 ζκήζεις ζτ.βιβλίοσ ζελίδας 13 14 Ερωηήζεις Καηανόηζης 1. ύν δηαθνξεηηθέο επζείεο κπνξεί λα έρνπλ θαλέλα θνηλό ζεκείν Έλα θνηλό ζεκείν i ύν θνηλά ζεκεία iλ) Άπεηξα θνηλά ζεκεία ηηηνινγήζηε ηελ απάληεζε
.1.10 ζκήζεις ζτ.βιβλίοσ ζελίδας 13 14 Ερωηήζεις Καηανόηζης 1. ύν δηαθνξεηηθέο επζείεο κπνξεί λα έρνπλ θαλέλα θνηλό ζεκείν Έλα θνηλό ζεκείν i ύν θνηλά ζεκεία iλ) Άπεηξα θνηλά ζεκεία ηηηνινγήζηε ηελ απάληεζε
Κεθάιαην 20. Ελαχιστοποίηση του κόστους
 Κεθάιαην 0 Ελαχιστοποίηση του κόστους Ειαρηζηνπνίεζε ηνπ θόζηνπο Μηα επηρείξεζε ειαρηζηνπνηεί ην θόζηνο ηεο αλ παξάγεη νπνηνδήπνηε δεδνκέλν επίπεδν πξντόληνο y 0 ζην κηθξόηεξν δπλαηό ζπλνιηθό θόζηνο. Τν
Κεθάιαην 0 Ελαχιστοποίηση του κόστους Ειαρηζηνπνίεζε ηνπ θόζηνπο Μηα επηρείξεζε ειαρηζηνπνηεί ην θόζηνο ηεο αλ παξάγεη νπνηνδήπνηε δεδνκέλν επίπεδν πξντόληνο y 0 ζην κηθξόηεξν δπλαηό ζπλνιηθό θόζηνο. Τν
ΓΤΜΝΑΙΟ ΚΑΘΟΛΙΚΗ ΥΟΛΙΚΗ ΥΡΟΝΙΑ Γ Ρ Α Π Σ Δ Α Π Ο Λ Τ Σ Η Ρ Ι Δ Δ Ξ Δ Σ Α Δ Ι
 ΓΤΜΝΑΙΟ ΚΑΘΟΛΙΚΗ ΥΟΛΙΚΗ ΥΡΟΝΙΑ 2011 2012 ΜΑΘΗΜΑ: ΥΗΜΔΙΑ ΣΑΞΗ: Γ Γ Ρ Α Π Σ Δ Α Π Ο Λ Τ Σ Η Ρ Ι Δ Δ Ξ Δ Σ Α Δ Ι 2 0 1 2 ΒΑΘΜΟ: ΓΙΑΡΚΔΙΑ: 2 ώξεο (καδί κε Βηνινγία/Αλζξωπνινγία) ΤΠΟΓΡΑΦΗ: ΗΜΔΡΟΜΗΝΙΑ: 05 /
ΓΤΜΝΑΙΟ ΚΑΘΟΛΙΚΗ ΥΟΛΙΚΗ ΥΡΟΝΙΑ 2011 2012 ΜΑΘΗΜΑ: ΥΗΜΔΙΑ ΣΑΞΗ: Γ Γ Ρ Α Π Σ Δ Α Π Ο Λ Τ Σ Η Ρ Ι Δ Δ Ξ Δ Σ Α Δ Ι 2 0 1 2 ΒΑΘΜΟ: ΓΙΑΡΚΔΙΑ: 2 ώξεο (καδί κε Βηνινγία/Αλζξωπνινγία) ΤΠΟΓΡΑΦΗ: ΗΜΔΡΟΜΗΝΙΑ: 05 /
Α. Εηζαγσγή ηεο έλλνηαο ηεο ηξηγσλνκεηξηθήο εμίζσζεο κε αξρηθό παξάδεηγκα ηελ εκx = 2
 ΣΡΙΓΩΝΟΜΔΣΡΙΚΔ EΞΙΩΔΙ Πνηα παξαδείγκαηα εμηζώζεσλ ή θαη πξνβιεκάησλ πηζηεύεηαη όηη είλαη θαηάιιεια γηα ηελ επίιπζε ηνπο θαηά ηελ δηάξθεηα ηεο δηδαθηηθήο δηαδηθαζίαο κέζα ζηελ ηάμε; 1 ε ΓΙΓΑΚΣΙΚΗ ΩΡΑ Α.
ΣΡΙΓΩΝΟΜΔΣΡΙΚΔ EΞΙΩΔΙ Πνηα παξαδείγκαηα εμηζώζεσλ ή θαη πξνβιεκάησλ πηζηεύεηαη όηη είλαη θαηάιιεια γηα ηελ επίιπζε ηνπο θαηά ηελ δηάξθεηα ηεο δηδαθηηθήο δηαδηθαζίαο κέζα ζηελ ηάμε; 1 ε ΓΙΓΑΚΣΙΚΗ ΩΡΑ Α.
1. Οδηγίερ εγκαηάζηαζηρ και σπήζηρ έξςπνυν καπηών και τηθιακών πιζηοποιηηικών με σπήζη ηος λογιζμικού Μοzilla Thunderbird
 1. Οδηγίερ εγκαηάζηαζηρ και σπήζηρ έξςπνυν καπηών και τηθιακών πιζηοποιηηικών με σπήζη ηος λογιζμικού Μοzilla Thunderbird 1.1 Εγκαηάζηαζη ηυν οδηγών ηηρ έξςπνηρ κάπηαρ ζηο λογιζμικό Mozilla Thunderbird
1. Οδηγίερ εγκαηάζηαζηρ και σπήζηρ έξςπνυν καπηών και τηθιακών πιζηοποιηηικών με σπήζη ηος λογιζμικού Μοzilla Thunderbird 1.1 Εγκαηάζηαζη ηυν οδηγών ηηρ έξςπνηρ κάπηαρ ζηο λογιζμικό Mozilla Thunderbird
ΑΠΛΟΠΟΙΗΗ ΛΟΓΙΚΩΝ ΤΝΑΡΣΗΕΩΝ ΜΕ ΠΙΝΑΚΕ KARNAUGH
 ΑΠΛΟΠΟΙΗΗ ΛΟΓΙΚΩΝ ΤΝΑΡΣΗΕΩΝ ΜΕ ΠΙΝΑΚΕ KRNUGH Γηα λα θάλνπκε απινπνίεζε κηαο ινγηθήο ζπλάξηεζεο κε πίλαθα (ή ράξηε) Karnaugh αθνινπζνύκε ηα παξαθάησ βήκαηα:. Η ινγηθή ζπλάξηεζε ζα πξέπεη λα είλαη ζε πιήξε
ΑΠΛΟΠΟΙΗΗ ΛΟΓΙΚΩΝ ΤΝΑΡΣΗΕΩΝ ΜΕ ΠΙΝΑΚΕ KRNUGH Γηα λα θάλνπκε απινπνίεζε κηαο ινγηθήο ζπλάξηεζεο κε πίλαθα (ή ράξηε) Karnaugh αθνινπζνύκε ηα παξαθάησ βήκαηα:. Η ινγηθή ζπλάξηεζε ζα πξέπεη λα είλαη ζε πιήξε
ΜΕΛΕΣΗ E.O.K. ΜΕ ΑΙΘΗΣΗΡΑ ΘΕΗ
 ΜΕΛΕΣΗ E.O.K. ΜΕ ΑΙΘΗΣΗΡΑ ΘΕΗ ΦΤΛΛΟ ΕΡΓΑΙΑ (Θεοδώρα Γιώηη, Νικόλας Καραηάζιος- Τπεύθσνη εκ/κος Λ. Παπαηζίμπα) ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ:.., ΗΜΕΡΟΜΗΝΙΑ:.// Σε ακαμίδην πνπ κπνξεί λα θηλείηαη ρσξίο ηξηβέο πάλσ
ΜΕΛΕΣΗ E.O.K. ΜΕ ΑΙΘΗΣΗΡΑ ΘΕΗ ΦΤΛΛΟ ΕΡΓΑΙΑ (Θεοδώρα Γιώηη, Νικόλας Καραηάζιος- Τπεύθσνη εκ/κος Λ. Παπαηζίμπα) ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ:.., ΗΜΕΡΟΜΗΝΙΑ:.// Σε ακαμίδην πνπ κπνξεί λα θηλείηαη ρσξίο ηξηβέο πάλσ
Μηα ζπλάξηεζε κε πεδίν νξηζκνύ ην Α, ζα ιέκε όηη παξνπζηάδεη ηοπικό μέγιζηο ζην, αλ ππάξρεη δ>0, ηέηνην ώζηε:
 1 ΟΡΙΜΟΙ MONOTONIA AKΡOTATA Μηα ζπλάξηεζε κε πεδίν νξηζκνύ ην Α, ζα ιέκε όηη παξνπζηάδεη ηοπικό μέγιζηο ζην, αλ ππάξρεη δ>0, ηέηνην ώζηε: Σν ιέγεηαη ζέζε ή ζεκείν ηνπ ηνπηθνύ κεγίζηνπ θαη ην ( ηνπηθό κέγηζην.
1 ΟΡΙΜΟΙ MONOTONIA AKΡOTATA Μηα ζπλάξηεζε κε πεδίν νξηζκνύ ην Α, ζα ιέκε όηη παξνπζηάδεη ηοπικό μέγιζηο ζην, αλ ππάξρεη δ>0, ηέηνην ώζηε: Σν ιέγεηαη ζέζε ή ζεκείν ηνπ ηνπηθνύ κεγίζηνπ θαη ην ( ηνπηθό κέγηζην.
ΗΜΔΡΟΜΗΝΙΑ. ΟΝΟΜΑΣΔΠΩΝΤΜΟ.. ΒΑΘΜΟΛΟΓΙΑ..
 ΗΜΔΡΟΜΗΝΙΑ. ΟΝΟΜΑΣΔΠΩΝΤΜΟ.. ΒΑΘΜΟΛΟΓΙΑ.. ΘΔΜΑ Α Σηηο εκηηειείο πξνηάζεηο Α.1 Α.4 λα γξάςεηε ζην ηεηξάδην ζαο ηνλ αξηζκό ηεο πξόηαζεο θαη, δίπια, ην γξάκκα πνπ αληηζηνηρεί ζηε θξάζε ε νπνία ηε ζπκπιεξώλεη
ΗΜΔΡΟΜΗΝΙΑ. ΟΝΟΜΑΣΔΠΩΝΤΜΟ.. ΒΑΘΜΟΛΟΓΙΑ.. ΘΔΜΑ Α Σηηο εκηηειείο πξνηάζεηο Α.1 Α.4 λα γξάςεηε ζην ηεηξάδην ζαο ηνλ αξηζκό ηεο πξόηαζεο θαη, δίπια, ην γξάκκα πνπ αληηζηνηρεί ζηε θξάζε ε νπνία ηε ζπκπιεξώλεη
ΥΡΙΣΟΤΓΔΝΝΙΑΣΙΚΔ ΚΑΣΑΚΔΤΔ
 ΥΡΙΣΟΤΓΔΝΝΙΑΣΙΚΔ ΚΑΣΑΚΔΤΔ 1) Υξηζηνπγελληάηηθα ειαηάθηα θάξηα ή θαδξάθη θάξηα ή θαδξάθη Τιηθά πνπ ζα ρξεηαζηνύκε: Υαξηί θάλζνλ καύξν γηα ην θόλην, πξάζηλν γηα ηα ειαηάθηα, θόθθηλν γηα ηα αζηεξάθηα Απιό
ΥΡΙΣΟΤΓΔΝΝΙΑΣΙΚΔ ΚΑΣΑΚΔΤΔ 1) Υξηζηνπγελληάηηθα ειαηάθηα θάξηα ή θαδξάθη θάξηα ή θαδξάθη Τιηθά πνπ ζα ρξεηαζηνύκε: Υαξηί θάλζνλ καύξν γηα ην θόλην, πξάζηλν γηα ηα ειαηάθηα, θόθθηλν γηα ηα αζηεξάθηα Απιό
(Ενδεικηικές Απανηήζεις) ΘΔΜΑ Α. Α1. Βιέπε απόδεημε Σει. 262, ζρνιηθνύ βηβιίνπ. Α2. Βιέπε νξηζκό Σει. 141, ζρνιηθνύ βηβιίνπ
 ΠΑΝΔΛΛΑΓΗΚΔ ΔΞΔΣΑΔΗ Γ ΣΑΞΖ ΖΜΔΡΖΗΟΤ ΓΔΝΗΚΟΤ ΛΤΚΔΗΟΤ ΚΑΗ ΔΠΑΛ (ΟΜΑΓΑ Β ) ΣΔΣΑΡΣΖ 18 ΜΑΪΟΤ 16 ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΜΑΘΖΜΑΣΗΚΑ ΠΡΟΑΝΑΣΟΛΗΜΟΤ (ΝΔΟ ΤΣΖΜΑ) ΚΑΣΔΤΘΤΝΖ (ΠΑΛΑΗΟ ΤΣΖΜΑ) (Ενδεικηικές Απανηήζεις) ΘΔΜΑ
ΠΑΝΔΛΛΑΓΗΚΔ ΔΞΔΣΑΔΗ Γ ΣΑΞΖ ΖΜΔΡΖΗΟΤ ΓΔΝΗΚΟΤ ΛΤΚΔΗΟΤ ΚΑΗ ΔΠΑΛ (ΟΜΑΓΑ Β ) ΣΔΣΑΡΣΖ 18 ΜΑΪΟΤ 16 ΔΞΔΣΑΕΟΜΔΝΟ ΜΑΘΖΜΑ: ΜΑΘΖΜΑΣΗΚΑ ΠΡΟΑΝΑΣΟΛΗΜΟΤ (ΝΔΟ ΤΣΖΜΑ) ΚΑΣΔΤΘΤΝΖ (ΠΑΛΑΗΟ ΤΣΖΜΑ) (Ενδεικηικές Απανηήζεις) ΘΔΜΑ
Γοκή επαλάιευες Δληοιές Όζο & Μέτρης_όηοσ
 Αιγόξηζκνη 2.2.7.4 Γοκή επαλάιευες Δληοιές Όζο & Μέτρης_όηοσ Εηζαγσγή ζηηο Αξρέο ηεο Επηζηήκεο ησλ Η/Υ 1 Άζθεζε 34 ζει 53 Έλα ςεθηαθό θσηνγξαθηθό άικπνπκ έρεη απνζεθεπηηθό ρώξν N Mbytes. Να αλαπηύμεηε
Αιγόξηζκνη 2.2.7.4 Γοκή επαλάιευες Δληοιές Όζο & Μέτρης_όηοσ Εηζαγσγή ζηηο Αξρέο ηεο Επηζηήκεο ησλ Η/Υ 1 Άζθεζε 34 ζει 53 Έλα ςεθηαθό θσηνγξαθηθό άικπνπκ έρεη απνζεθεπηηθό ρώξν N Mbytes. Να αλαπηύμεηε
Έκδοζη /10/2014. Νέα λειηοσργικόηηηα - Βεληιώζεις
 Έκδοζη 2.89.31 08/10/2014 Η έκδοζη 2.89.31, περιλαμβάνει : Βεληιώζεις Καηάζηαζη Υπερφριών (Ε8) Αναγγελία πρόζληυης (Ε3) 08/10/2014 1 Βεληιώζεις Καηάζηαζη Υπερφριών (Ε8) Επεηδή ζηελ ειεθηξνληθή ππνβνιή
Έκδοζη 2.89.31 08/10/2014 Η έκδοζη 2.89.31, περιλαμβάνει : Βεληιώζεις Καηάζηαζη Υπερφριών (Ε8) Αναγγελία πρόζληυης (Ε3) 08/10/2014 1 Βεληιώζεις Καηάζηαζη Υπερφριών (Ε8) Επεηδή ζηελ ειεθηξνληθή ππνβνιή
3ο Δπαναληπηικό διαγώνιζμα ζηα Μαθημαηικά καηεύθσνζης ηης Γ Λσκείοσ Θέμα A Α1. Έζησ f κηα ζπλερήο ζπλάξηεζε ζ έλα δηάζηεκα
 wwwaskisopolisgr 3ο Δπνληπηικό διγώνιζμ ζη Μθημηικά κηεύθσνζης ηης Γ Λσκείοσ 17-18 Θέμ A Α1 Έζησ κη ζπλερήο ζπλάξηεζε ζ έλ δηάζηεκ β λ πνδείμεηε όηη: t dt G β G Α Πόηε κη ζπλάξηεζε ιέγεηη 1-1; Α3 Πόηε
wwwaskisopolisgr 3ο Δπνληπηικό διγώνιζμ ζη Μθημηικά κηεύθσνζης ηης Γ Λσκείοσ 17-18 Θέμ A Α1 Έζησ κη ζπλερήο ζπλάξηεζε ζ έλ δηάζηεκ β λ πνδείμεηε όηη: t dt G β G Α Πόηε κη ζπλάξηεζε ιέγεηη 1-1; Α3 Πόηε
Σ Δ Υ Ν Ι Κ Η Δ Κ Θ Δ Η Π Ρ Ο Μ Η Θ Δ Ι Α Ο Ι Κ Ο Γ Ο Μ Ι Κ Ω Ν Τ Λ Ι Κ Ω Ν Γ Η Μ Ο Τ Β Ο Λ Β Η
 Σ Δ Υ Ν Ι Κ Η Δ Κ Θ Δ Η Π Ρ Ο Μ Η Θ Δ Ι Α Ο Ι Κ Ο Γ Ο Μ Ι Κ Ω Ν Τ Λ Ι Κ Ω Ν Γ Η Μ Ο Τ Β Ο Λ Β Η ΠΔΡΙΔΥΟΜΔΝΑ 1. Τερληθή Έθζεζε 2. Δλδεηθηηθφο Πξνυπνινγηζκφο 3. Έληππν νηθνλνκηθήο πξνζθνξάο ΘΔΜΑ : Πξνκήζεηα
Σ Δ Υ Ν Ι Κ Η Δ Κ Θ Δ Η Π Ρ Ο Μ Η Θ Δ Ι Α Ο Ι Κ Ο Γ Ο Μ Ι Κ Ω Ν Τ Λ Ι Κ Ω Ν Γ Η Μ Ο Τ Β Ο Λ Β Η ΠΔΡΙΔΥΟΜΔΝΑ 1. Τερληθή Έθζεζε 2. Δλδεηθηηθφο Πξνυπνινγηζκφο 3. Έληππν νηθνλνκηθήο πξνζθνξάο ΘΔΜΑ : Πξνκήζεηα
ΣΥΣΤΗΜΑΤΑ ΑΛΓΕΒΡΑ Α ΛΥΚΕΙΟΥ. 1. Να ιπζνύλ ηα ζπζηήκαηα. 1 0,3x 0,1y x 3 3x 4y 2 4x 2y ( x 1) 6( y 1) (i) (ii)
 . Να ιπζνύλ ηα ζπζηήκαηα.,, 6 4 4 4 5( ) 6( ). Να ιπζνύλ ηα ζπζηήκαηα.,,,6 7. Να ιπζνύλ ηα ζπζηήκαηα. 5 ( )( ) ( ) 4. Να ιπζνύλ ηα ζπζηήκαηα. 5 4 6 7 4. 5. Να ιπζνύλ ηα ζπζηήκαηα. 59 ( )( ) ()( 5) 7 6.
. Να ιπζνύλ ηα ζπζηήκαηα.,, 6 4 4 4 5( ) 6( ). Να ιπζνύλ ηα ζπζηήκαηα.,,,6 7. Να ιπζνύλ ηα ζπζηήκαηα. 5 ( )( ) ( ) 4. Να ιπζνύλ ηα ζπζηήκαηα. 5 4 6 7 4. 5. Να ιπζνύλ ηα ζπζηήκαηα. 59 ( )( ) ()( 5) 7 6.
ΜΑΘΗΜΑ / ΤΑΞΗ : ΗΛΕΚΤΡΟΛΟΓΙΑ/Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 08/09/2014
 ΔΙΑΓΩΝΙΣΜΑ ΕΚΠ. ΕΤΟΥΣ 204-205 ΜΑΘΗΜΑ / ΤΑΞΗ : ΗΛΕΚΤΡΟΛΟΓΙΑ/Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 08/09/204 A ΟΜΑΓΑ Οδηγία: Να γράυεηε ζηο ηεηράδιο ζας ηον αριθμό κάθε μιας από ηις παρακάηφ ερφηήζεις Α.-Α.8 και
ΔΙΑΓΩΝΙΣΜΑ ΕΚΠ. ΕΤΟΥΣ 204-205 ΜΑΘΗΜΑ / ΤΑΞΗ : ΗΛΕΚΤΡΟΛΟΓΙΑ/Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 08/09/204 A ΟΜΑΓΑ Οδηγία: Να γράυεηε ζηο ηεηράδιο ζας ηον αριθμό κάθε μιας από ηις παρακάηφ ερφηήζεις Α.-Α.8 και
ιαχείριση Εφοδιαστικής Αλυσίδας
 ΤΕΧΝΟΛΟΓΙΚΟ ΕΚΠΑΙ ΕΥΤΙΚΟ Ι ΡΥΜΑ ΙΟΝΙΩΝ ΝΗΣΩΝ ΣΧΟΛΗ ΙΟΙΚΗΣΗΣ ΚΑΙ ΟΙΚΟΝΟΜΙΑΣ ΤΜΗΜΑ ΙΟΙΚΗΣΗΣ ΕΠΙΧΕΙΡΗΣΕΩΝ ΕΙΣΑΓΩΓΙΚΗ ΚΑΤΕΥΘΥΝΣΗ: ΙΟΙΚΗΣΗ ΕΠΙΧΕΙΡΗΣΕΩΝ ιαχείριση Εφοδιαστικής Αλυσίδας Ασκήσεις αποθεµάτωνµ Δρ.
ΤΕΧΝΟΛΟΓΙΚΟ ΕΚΠΑΙ ΕΥΤΙΚΟ Ι ΡΥΜΑ ΙΟΝΙΩΝ ΝΗΣΩΝ ΣΧΟΛΗ ΙΟΙΚΗΣΗΣ ΚΑΙ ΟΙΚΟΝΟΜΙΑΣ ΤΜΗΜΑ ΙΟΙΚΗΣΗΣ ΕΠΙΧΕΙΡΗΣΕΩΝ ΕΙΣΑΓΩΓΙΚΗ ΚΑΤΕΥΘΥΝΣΗ: ΙΟΙΚΗΣΗ ΕΠΙΧΕΙΡΗΣΕΩΝ ιαχείριση Εφοδιαστικής Αλυσίδας Ασκήσεις αποθεµάτωνµ Δρ.
Τν Πξόγξακκα ζα αλαθνηλσζεί, ακέζσο κεηά ηηο γηνξηέο ηνπ Πάζρα.
 Οι Πανελλαδικέρ Δξεηάζειρ για ηην ειζαγωγή ζηην ηπιηοβάθμια εκπαίδεςζη θα ππαγμαηοποιηθούν ππιν ηιρ απολςηήπιερ ενδοζσολικέρ εξεηάζειρ ηων μαθηηών και ηων μαθηηπιών. Τν Πξόγξακκα ζα αλαθνηλσζεί, ακέζσο
Οι Πανελλαδικέρ Δξεηάζειρ για ηην ειζαγωγή ζηην ηπιηοβάθμια εκπαίδεςζη θα ππαγμαηοποιηθούν ππιν ηιρ απολςηήπιερ ενδοζσολικέρ εξεηάζειρ ηων μαθηηών και ηων μαθηηπιών. Τν Πξόγξακκα ζα αλαθνηλσζεί, ακέζσο
ηδάζθσλ: εµήηξεο Εετλαιηπνύξ
 ηάιεμε 4: ιάρηζηα ελλεηνξηθά έλδξα Αιγόξηζκνο Kruskal Σηελ ελόηεηα απηή ζα κειεηεζνύλ ηα εμήο επηκέξνπο ζέκαηα: Ο αλγόριθμος ηοσ Kruskal για εύρεζη ζε γράθοσς Παράδειγμα κηέλεζης ηδάζθσλ: εµήηξεο ετλαιηπνύξ
ηάιεμε 4: ιάρηζηα ελλεηνξηθά έλδξα Αιγόξηζκνο Kruskal Σηελ ελόηεηα απηή ζα κειεηεζνύλ ηα εμήο επηκέξνπο ζέκαηα: Ο αλγόριθμος ηοσ Kruskal για εύρεζη ζε γράθοσς Παράδειγμα κηέλεζης ηδάζθσλ: εµήηξεο ετλαιηπνύξ
Σήκαηα Β Α Γ Γ Δ Λ Η Σ Ο Ι Κ Ο Ν Ο Μ Ο Υ Γ Ι Α Λ Δ Ξ Η - ( 2 ) ΕΙΣΑΓΨΓΗ ΣΤΙΣ ΤΗΛΕΠΙΚΟΙΝΨΝΙΕΣ
 Σήκαηα 1 Β Α Γ Γ Δ Λ Η Σ Ο Ι Κ Ο Ν Ο Μ Ο Υ Γ Ι Α Λ Δ Ξ Η - ( 2 ) Σήκαηα Οξηζκόο ζήκαηνο Ταμηλόκεζε ζεκάησλ Σεηξέο Fourier Μεηαζρεκαηηζκόο Fourier Σπλέιημε Σπζρέηηζε θαη Φαζκαηηθή Ππθλόηεηα 2 Οξηζκόο Σήκαηνο
Σήκαηα 1 Β Α Γ Γ Δ Λ Η Σ Ο Ι Κ Ο Ν Ο Μ Ο Υ Γ Ι Α Λ Δ Ξ Η - ( 2 ) Σήκαηα Οξηζκόο ζήκαηνο Ταμηλόκεζε ζεκάησλ Σεηξέο Fourier Μεηαζρεκαηηζκόο Fourier Σπλέιημε Σπζρέηηζε θαη Φαζκαηηθή Ππθλόηεηα 2 Οξηζκόο Σήκαηνο
Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015)
 Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015) 1. Σε ποια απο τις παρακάτω ενώσεις το Ν έχει αριθμό οξέιδωσης +5 A. ΗΝΟ 2 C ΚΝΟ 3 B. ΝΗ 3 D Ν 2 Ο 3 2. Σε ποια απο τις παρακάτω
Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015) 1. Σε ποια απο τις παρακάτω ενώσεις το Ν έχει αριθμό οξέιδωσης +5 A. ΗΝΟ 2 C ΚΝΟ 3 B. ΝΗ 3 D Ν 2 Ο 3 2. Σε ποια απο τις παρακάτω
ΠΟΛΤΜΕΡΙΜΟ - ΠΕΣΡΟΥΗΜΙΚΑ
 ΠΟΛΤΜΕΡΙΜΟ - ΠΕΣΡΟΥΗΜΙΚΑ ΠΑΡΑΔΕΙΓΜΑΣΑ Ο πολσμεριζμός Πολσμεριζμός είναι η τημική ανηίδραζη καηά ηην οποία πολλά μόρια ίδιων ή διαθορεηικών οργανικών ενώζεων, ποσ ονομάζονηαι μονομερή, ενώνονηαι και ζτημαηίζοσν
ΠΟΛΤΜΕΡΙΜΟ - ΠΕΣΡΟΥΗΜΙΚΑ ΠΑΡΑΔΕΙΓΜΑΣΑ Ο πολσμεριζμός Πολσμεριζμός είναι η τημική ανηίδραζη καηά ηην οποία πολλά μόρια ίδιων ή διαθορεηικών οργανικών ενώζεων, ποσ ονομάζονηαι μονομερή, ενώνονηαι και ζτημαηίζοσν
ΣΟ ΤΣΖΜΑ ΔΛΑΣΖΡΗΟ - ΩΜΑ
 ΣΟ ΤΣΖΜΑ ΔΛΑΣΖΡΗΟ - ΩΜΑ Σε όια ηα πξνβιήκαηα πνπ ζα αληηκεηωπίζνπκε, ην ειαηήξην ζα είλαη αβαξέο θαη ζα ηθαλνπνηεί ην λόκν ηνπ Hooke (ηδαληθό ειαηήξην), δειαδή ε δύλακε πνπ αζθεί έλα ηδαληθό ειαηήξην έρεη
ΣΟ ΤΣΖΜΑ ΔΛΑΣΖΡΗΟ - ΩΜΑ Σε όια ηα πξνβιήκαηα πνπ ζα αληηκεηωπίζνπκε, ην ειαηήξην ζα είλαη αβαξέο θαη ζα ηθαλνπνηεί ην λόκν ηνπ Hooke (ηδαληθό ειαηήξην), δειαδή ε δύλακε πνπ αζθεί έλα ηδαληθό ειαηήξην έρεη
ΓΗΜΟΙΑ ΟΙΚΟΝΟΜΙΚΗ ΣΟΜΟ Γ
 1 ΓΗΜΟΙΑ ΟΙΚΟΝΟΜΙΚΗ ΣΟΜΟ Γ Μάθημα 19: Φόροι ΦΟΡΟΛΟΓΙΚΑ ΤΣΗΜΑΣΑ: Προοδεσηικό, Αναλογικά και ανηίζηροθα προοδεσηικό θορολογικό ζύζηημα Μέζος και οριακός θορολογικός ζσνηελεζηής Ο κέζνο θνξνινγηθόο ζπληειεζηήο
1 ΓΗΜΟΙΑ ΟΙΚΟΝΟΜΙΚΗ ΣΟΜΟ Γ Μάθημα 19: Φόροι ΦΟΡΟΛΟΓΙΚΑ ΤΣΗΜΑΣΑ: Προοδεσηικό, Αναλογικά και ανηίζηροθα προοδεσηικό θορολογικό ζύζηημα Μέζος και οριακός θορολογικός ζσνηελεζηής Ο κέζνο θνξνινγηθόο ζπληειεζηήο
Η/Υ A ΤΑΞΕΩΣ ΑΕ 2010-2011. Συστήματα Αρίθμησης. Υποπλοίαρχος Ν. Πετράκος ΠΝ
 Συστήματα Αρίθμησης Υποπλοίαρχος Ν. Πετράκος ΠΝ 1 Ειζαγωγή Τν bit είλαη ε πην βαζηθή κνλάδα κέηξεζεο. Είλαη κία θαηάζηαζε on ή off ζε έλα ςεθηαθό θύθισκα. Άιιεο θνξέο είλαη κία θαηάζηαζε high ή low voltage
Συστήματα Αρίθμησης Υποπλοίαρχος Ν. Πετράκος ΠΝ 1 Ειζαγωγή Τν bit είλαη ε πην βαζηθή κνλάδα κέηξεζεο. Είλαη κία θαηάζηαζε on ή off ζε έλα ςεθηαθό θύθισκα. Άιιεο θνξέο είλαη κία θαηάζηαζε high ή low voltage
ΥΗΜΕΙΑ Γ ΛΤΚΕΙΟΤ ΘΕΣΙΚΩΝ ΠΟΤΔΩΝ 13 ΑΠΡΙΛΙΟΤ 2018 ΤΝΟΛΟ ΕΛΙΔΩΝ: 5
 1 ΥΗΜΕΙΑ Γ ΛΤΚΕΙΟΤ ΘΕΣΙΚΩΝ ΠΟΤΔΩΝ 13 ΑΠΡΙΛΙΟΤ 2018 ΤΝΟΛΟ ΕΛΙΔΩΝ: 5 Θέμα Α Γηα ηηο παξαθάησ εξσηήζεηο λα γξάςεηε ηνλ αξηζκό ηεο εξώηεζεο θαη δίπια ην γξάκκα πνπ αληηζηνηρεί ζηε ζσζηή απάληεζε: Α1. Τν ζηνηρείν
1 ΥΗΜΕΙΑ Γ ΛΤΚΕΙΟΤ ΘΕΣΙΚΩΝ ΠΟΤΔΩΝ 13 ΑΠΡΙΛΙΟΤ 2018 ΤΝΟΛΟ ΕΛΙΔΩΝ: 5 Θέμα Α Γηα ηηο παξαθάησ εξσηήζεηο λα γξάςεηε ηνλ αξηζκό ηεο εξώηεζεο θαη δίπια ην γξάκκα πνπ αληηζηνηρεί ζηε ζσζηή απάληεζε: Α1. Τν ζηνηρείν
Αντισταθμιστική ανάλυση
 Θεσξήζηε έλαλ αιγόξηζκν Α πνπ ρξεζηκνπνηεί κηα δνκή δεδνκέλσλ Γ : Καηά ηε δηάξθεηα εθηέιεζεο ηνπ Α ε Γ πξαγκαηνπνηεί κία αθνινπζία από πξάμεηο. Παξάδεηγκα: Θπκεζείηε ην πξόβιεκα ηεο εύξεζεο-έλσζεο Δίρακε
Θεσξήζηε έλαλ αιγόξηζκν Α πνπ ρξεζηκνπνηεί κηα δνκή δεδνκέλσλ Γ : Καηά ηε δηάξθεηα εθηέιεζεο ηνπ Α ε Γ πξαγκαηνπνηεί κία αθνινπζία από πξάμεηο. Παξάδεηγκα: Θπκεζείηε ην πξόβιεκα ηεο εύξεζεο-έλσζεο Δίρακε
