Titrări acido-bazice
|
|
|
- Σάρρα Αποστόλου
- 7 χρόνια πριν
- Προβολές:
Transcript
1 Titrări acido-bazice Titrări acido-bazice SoluŃii standard Succesul majorităńii metodelor de analiză depinde de modul de alegere a materialului de referinńă utilizat pentru etalonare. De exemplu, pentru determinarea titrimetrică a unui alcaliu este necesar de adăugat un volum măsurat de acid cu concentrańia cunoscută până se ajunge la punctul de echivalenńă. Pentru a putea calcula conńinutul de alcaliu în soluńie, trebuie să se cunoască exact concentrańia soluńiei de acid. O astfel de soluńie este denumită soluńie standard. Dacă pentru prepararea unei asemenea soluńii a fost folosită o substanńă a cărei puritate a fost verificată în prealabil, ea este numită standard primar. O substanńă poate fi utilizată drept standard chimic primar, dacă îndeplineşte următoarele condińii: să aibă o compozińie strict corespunzătoare formulei moleculare; să aibă o puritate cunoscută de cel puńin 99% (de preferat 99,9%); să fie accesibilă şi la un preń convenabil; să fie stabilă în solventul utilizat; să fie stabilă în aer şi nehigroscopică; să participe în reacńii în proporńii stoechiometrice; să posede o masă moleculară cât mai mare. Pentru a prepara o soluńie standard primar, se cântăreşte cu precizie la balanńa analitică o anumită masă de substanńă desemnată drept standard, se dizolvă şi se diluiază până la un volum cunoscut într-un balon cotat. În acest mod se obńine o soluńie de concentrańie cunoscută. Numărul de substanńe ce satisfac cerinńele enumărate anterior este limitat. Să presupunem că se cere o soluńie standard de KOH. Evident că KOH, care absoarbe din aer CO 2 şi H 2 O nu îndeplineşte condińiile enumărate mai sus. În asemenea cazuri se prepară o soluńie de KOH cu o concentrańie aproximativă de ordinul celei cerute. Apoi se prepară o soluńie standard primară de acid (de exemplu H 2 C 2 O. H 2 O) şi se titrează soluńia de KOH. Întrucât concentrańia soluńiei de acid oxalic (standard primar) este cunoscută, cu uşurinńă se poate calcula concentrańia soluńiei de KOH. SoluŃia de KOH este acum etalonată şi poate fi folosită pentru determinarea conńinutului acizilor în soluńii. SoluŃia de KOH este considerată acum drept un standard secundar. SoluŃiile standard primar sunt necesare pentru toate tipurile de reacńii utilizate în titrimetrie. Prepararea unei soluńii de NaOH Hidroxidul de sodiu absoarbe bioxidul de carbon din aer şi întotdeauna conńine o cantitate de Na 2 CO 3. Această impuritate va afecta rezultatele titrării acizilor, dacă se vor folosi indicatori diferińi fenolftaleina sau metiloranjul. În cazul când titrările se efectuează numai cu metiloranj, impurităńile de Na 2 CO 3 nu prezintă interferenńe. Cel mai potrivit procedeu pentru înlăturarea carbonatului de sodiu este adăugarea unei cantităńi mici de BaCl 2 care precipită carbonańii: BaCl 2 + Na 2 CO 3 = BaCO 3 + 2NaCl.
2 Titrări acido-bazice 2 Pentru prepararea unui litru de soluńie 0, mol/l ar trebui să cântărim g de NaOH. Deoarece hidroxidul luat mai conńine apă şi Na 2 CO 3 se va lua o masă mai mare (circa,5-5 g). Hidroxidul de sodiu cântărit se trece într-un păhar şi se spală repede de 2-3 ori cu mici cantităńi de apă distilată. Prin acest procedeu se înlătură pojghińa de Na 2 CO 3 de pe suprafańa hidroxidului de sodiu. Se trece apoi într-un vas mai mare şi se dizolvă în 000 cm 3 de apă distilată. La soluńia obńinută se adaugă 2-3 cm 3 soluńie de BaCl 2 mol/l. Precipitatul format se sedimentează pe fundul vasului. Se controlează plenitudinea sedimentării carbonańilor. În acest scop -2 cm 3 de soluńie limpezită se tratează cu câteva picături de H 2 SO. Formarea precipitatului de BaSO indică prezenńa în soluńie a ionilor de Ba 2+, şi prin urmare o sedimentare completă. Lichidul limpezit se trece în vasul unde urmează să fie păstrat şi să protejează de contactul cu CO 2 introducând în dop un tub cu o bulă umplută cu calciu sodat, care absoarbe bioxidul de carbon. Deseori în laborator sunt preparate şi eliberate de carbonańi soluńii de NaOH de concentrańii mai mari. De exemplu, se cere de preparat 700 cm 3 de soluńie de NaOH aproximativ 0, mol/l plecând de la o soluńie de 2 mol/l. Volumul de soluńie concentrată necesar pentru a fi diluat până la 700 cm 3 calculează din relańia: V NaOH) 700 0, = 35 (cm 3 ). 2 ( = Prin urmare pentru a prepara 700 cm 3 de soluńia NaOH aproximativ 0, mol/l se vor măsura 35 cm 3 de NaOH (2 moli/l) şi se vor dilua cu = 665 (cm 3 ) de apă distilată (eliberată de CO 2 ). SoluŃia obńinută se protejează de acńiunea bioxidului de carbon. Pentru stabilirea titrului soluńiei de NaOH se pot folosi mai multe soluńii standard primar: acidul oxalic (H 2 C 2 O. 2H 2 O), acidul o-clorbenzoic (C 6 H ClCOOH), biiodatul de potasiu (KH(IO 3 ) 2 ), acidul succinic (H 2 C H O ) etc. Mai des este utilizat în acest scop acidul oxalic. Masa echivalentă a acidului oxalic este 63,033 g. ReacŃionează cu hidroxidul de sodiu conform ecuańiei: H 2 C 2 O + 2NaOH = Na 2 C 2 O + 2H 2 O. Indicatorul potrivit pentru stabilirea punctului de echivalenńă este fenolftaleina. se Prepararea unei soluńii standard de acid oxalic În primul rând se face calculul masei de acid oxalic, necesară pentru a prepara 00 cm 3 de soluńie cu concentrańia C(½H 2 C 2 O ) = 0, mol/ l. m(h 2 C 2 O. 2H 2 O) = M(½H 2 C 2 C. 2H 2 O). V. C (½H 2 C 2 O ), m(h 2 C 2 O. 2H 2 O) = 63,033 (g/mol). 0, (l). 0, (mol echiv./l) = 0,6303 g. Prin urmare, dacă se cântăreşte la balanńa analitică o probă de acid oxalic de 0,6303 g şi se dizolvă într-un balon cotat de 00 cm 3, după aducerea nivelului soluńiei cu apă distilată până la cotă, se obńine o soluńie cu concentrańia exactă (½H 2 C 2 O ) = 0, mol echiv./l. Nu este necesar să vă străduińi să cântărińi exact 0,6303 g de H 2 C 2 O. 2H 2 O pentru că această minuńiozitate nu dă nici un avantaj. Se recomandă următorul mod de lucru. CântăriŃi la o balanńă tehnică o probă de H 2 C 2 O. 2H 2 O cu masa (0,63 ±0,02) g. TreceŃi proba într-o fiolă specială sau pe o sticlă de ceas şi cântărińi-o la o balanńă analitică m = m fiol. + m prob. TurnaŃi cu precauńie pe o pâlnie introdusă în balonul cotat solidul din fiolă. CântăriŃi din nou
3 Titrări acido-bazice 3 fiola cu unele cantităńi mici de H 2 C 2 O. 2H 2 O care au rămas lipite de pereńii fiolei m 2 = m fiol + m rămas. Din diferenńa m m 2 = m(h 2 C 2 O. 2H 2 O) determinăm masa exactă de acid oxalic, care a fost trecut pe pâlnie. Cu ajutorul stropitorii proba se trece de pe pâlnie cantitativ în balonul cotat, se dizolvă şi nivelul soluńiei se aduce cu apă distilată până la cotă. Balonul se agită de câteva ori pentru a omogeniza soluńia. ConcentraŃia soluńiei preparate se determină din relańia: C(½H 2 C 2 O ) m(h C O 2H O) =, 63,03 V unde V este volumul (l) balonului cotat. Pentru a determina concentrańia soluńiei preparate de NaOH se umple biureta cu soluńie, respectând modul de lucru cu biuretele descris anterior şi măsurile de precauńie privitoare la soluńia de alcaliu. Nivelul soluńiei în biuretă se stabileşte la cifra 0. Din balonul cotat se trece cu pipeta un volum V(H 2 C 2 O ) de 0 cm 3 (parte alicotă) într-un balon Erlenmayer, se adaugă -5 picături de soluńie de fenolftaleină şi se titrează cu NaOH până la virarea indicatorului (prima nuanńă de roz). Se notează volumul de hidroxid de sodiu consumat V (NaOH). Lichidul se evacuează din balon, se spală cu apă din robinet şi se clăteşte bine cu apă distilată. Din nou se trec din balonul cotat 0 cm 3 de soluńie de H 2 C 2 O şi titrarea se repetă. La titrarea fiecărei părńi alicote de soluńie nivelul titrantului din biuretă se aduce la zero. Nu uitańi să scoateńi pâlnia din biureta după umplere. Pentru a obńine un rezultat bun e necesar să se facă minimum 3 titrări şi măsurătorile de volum V (NaOH); V 2 (NaOH) şi V 3 (NaOH) să fie apropiate (diferenńa maximală a volumelor consumate la titrarea părńilor alicote nu trebuie să depăşească 0,2 cm 3. În caz contrar titrările se repetă de mai multe ori. Pentru calcule se foloseşte volumul mediu sau V (NaOH) + V2 (NaOH) + V(NaOH) = 3 V (NaOH) i= (l) n = V i (NaOH). n V3 (NaOH) ; ConcentraŃia soluńiei de NaOH se calculează folosind formula: V(H C 2O ) C(½H 2C 2O ) C(NaOH) = (moli/ l). V(NaOH) 2 SoluŃia de NaOH este astfel etalonată şi serveşte mai departe pentru dozarea acizilor, fiind denumită standard secundar. Dozări cu ajutorul unei soluńii standardizate de alcaliu Dozarea masei acidului sulfuric Dozarea acidului sulfuric se bazează pe următoarea reacńie de neutralizare: H 2 SO + 2NaOH = Na 2 SO + 2H 2 O. Proba primită pentru analiza se trece cantitativ într-un balon cotat de 00 cm 3, se aduce până la cotă cu apă distilată şi se agită bine. Se ia o parte alicotă cu pipeta (0 cm 3 ) se trece în balonul Erlenmayer, se adaugă -5 picături de fenolftaleină şi se titrează cu soluńia de NaOH standardizată anterior până la virarea culorii indicatorului. Se notează volumul de
4 Titrări acido-bazice soluńie de alcaliu consumat. Titrările se repetă de cel puńin trei ori şi se calculează volumul mediu n V (NaOH) = Vi (NaOH), n unde n este numărul de titrări considerate pentru calcul. Din măsurătorile efectuate se calculează concentrańia C(½H 2 SO ) acidului sulfuric în soluńia din balonul cotat. i= C(NaOH) V(NaOH) C(½H 2SO ) =, V(H SO ) unde V(H 2 SO ) este volumul de acid luat pentru titrare. Titrul soluńiei de acid sulfuric se va calcula din relańia: C(½H 2SO ) M(½H 2SO ) T(H 2SO ) = (g/cm 3 ), 000 unde M(/2 H 2 SO ) reprezintă masa echivalentă a acidului sulfuric, egală cu 9,0 g. Masa acidului sulfuric din balonul cotat, care anterior se găsea în proba propusă pentru analiză va fi: M(H 2 SO ) = T(H 2 SO ). V b, unde V b este volumul balonului cotat în cm 3. În mod analog poate fi determinată şi masa acidului clorhidric. 2 Dozări cu ajutorul unei soluńii standardizate de HCl Prepararea unei soluńii de HCl Pentru a prepara o soluńie de 0, mol/l de acid clorhidric se folosesc soluńii de acid mai concentrate. ConcentraŃia acidului de la care se pleacă trebuie să fie cunoscută. În cazul când concentrańia nu este precizată se măsoară cu ajutorul unui densimetru densitatea soluńiei ρşi din tabele se determină conńinutul de acid fie în părńi de masă (ω) fie în moli/l. Acidul clorhidric concentrat poate atinge un conńinut de circa 0%, ceea ce corespunde molarităńii 3, moli/l (densitatea,98 g/cm 3 ). În scopuri de analiză se prepară o soluńie intermediară cu C(HCl) = 2 moli/l. Pentru a calcula gradul de diluare a acidului concentrat până la 2 moli/l poate fi folosită metoda diagonalelor sau legea maselor echivalente. De exemplu, se cere să fie preparat un volum de 000 cm 3 soluńie diluată de acid HCl cu C(HCl) = 2 moli/l, prin diluare cu apă distilată a acidului concentrat cu densitatea,75 g/cm 3. Din îndreptar se determină că acestei densităńi îi corespunde concentrańia,3 moli/l. Aplicăm legea diagonalelor: Din schemă este evident că la 2 volume de acid cu concentrańia,3 moli/l urmează a fi adăugate 9,3 volume de apă distilată pentru a avea în final,3 volume de soluńie cu concentrańia 2 moli/l. Prin urmare, pentru a prepara 000 volume (cm 3 ) se va consuma volumul V de acid concentrat calculat din relańia:
5 Titrări acido-bazice V(HCl) = = 76,36 (cm 3 ).,3 Acest volum de acid clorhidric concentrat se diluează cu apă distilată până la un litru. Acelaşi rezultat se obńine şi în cazul când se aplică legea maselor echivalente: V. C = V 2. C 2, unde V şi C reprezintă volumul şi concentrańia soluńiei finale, iar V 2 şi C 2 aceiaşi parametri pentru soluńia inińială. V C = ; V = 76,36 (cm 3 ). C,3 V2 2 = 2 Din soluńia intermediară se prepară o soluńie mai diluată, care mai apoi se standardizează. Calculul se efectuează prin una din metodele menńionate. Spre exemplu, pentru a prepara 700 cm 3 de soluńie de HCl cu C = 0, moli/l pornind de la o soluńie cu concentrańia 2 moli/l este necesar un volum V de acid cu concentrańia indicată egal cu ,/2 = 35 cm 3 şi de (cm 3 ). Ambele componente se amestecă şi se agită bine. Standardizarea unei soluńii de HCl Pentru stabilirea concentrańiei unei soluńii de HCl pot fi folosite mai multe substanńe etalon. Mai des se foloseşte boraxul (Na 2 B O 7. 0H 2 O), carbonatul de sodiu (Na 2 CO 3 ), oxalatul de sodiu (Na 2 C 2 O ) etc. Boraxul poate fi uşor recristalizat din soluńii cu temperaturi moderate (60 o C), este suficient de stabil şi are o masă molară a echivalentului destul de mare. Fiind dizolvat în apă boraxul hidrolizează conform ecuańiei: Na 2 B O 7 + 7H 2 O = 2NaOH + H 3 BO 3. Acidul boric H 3 BO 3 este foarte slab (pk = 9,5) şi nu influenńează semnificativ rezultatele titrării. Deoarece fiecare mol de borax produce la hidroliza 2 moli de bază tare, masa echivalentă a etalonului va fi ½M(Na 2 B O 7. 0H 2 O) = 90,67 (g/mol echiv.). Pentru a prepara 00 cm 3 de soluńie de Na 2 B O 7 cu concentrańia C(½Na 2 B O 7 ) = 0, moli/l în primul rând se face calculul masei necesare de borax cu formula: m(na 2 B O 7. 0H 2 O) = ½M(Na 2 B O 7. 0H 2 O). C(½Na 2 B O 7 ). V; m(na 2 B O 7. 0H 2 O) = 90,67 (g/mol echiv.). 0, (mol echiv./l). 0, (l) =,9067 g. Nu se va insista să se cântărească anume,9067 g de borax. Este important ca masa etalonului să fie de acest ordin şi să fie cunoscută exact. Pentru aceasta în fiolă se introduce o probă de borax cântărită la o balanńă tehnică cu masa de circa,9 g. Mai apoi fiola cu borax se cântăreşte exact la balanńa analitică. SubstanŃa cântărită se trece cu precauńie pe o pâlnie uscată în balonul cotat. După trecere se cântăreşte fiola din nou la balanńa analitică. Din diferenńa primei şi a doua cântăriri se determină masa boraxului trecut pe pâlnie. Deoarece boraxul este rău solubil în apă rece, proba de pe pâlnie se trece în balonul cotat cu apă fierbinte. Se spală atent pâlnia de câteva ori cu scopul de a trece cantitativ boraxul în balonul cotat. Dizolvarea probei se face în apă fierbinte, volumul căreia nu va depăşi 2/3 din volumul balonului cotat. Pentru a accelera dizolvarea se recomandă agitarea soluńiei, produsă prin mişcări line circulare a balonului cotat. După dizolvarea totală a boraxului soluńie se răceşte până la temperatura camerei şi se aduce cu apă distilată până la semnul circular şi se omogenizează prin agitare. ConcentraŃia soluńiei preparate se calculează din relańia:
6 Titrări acido-bazice 6 m(na 2BO 7 0H 2O C(½Na 2BO7 ) =. 90,67 0, Pentru a determina concentrańia soluńiei pregătite de HCl se umple biureta cu soluńie de acid respectând modul de lucru cu biureta descris anterior. Nivelul soluńiei de acid se stabileşte la zero. Din balonul cotat ce trece cu pipeta o parte alicotă de soluńie de borax (0 cm 3 ) în balonul Erlenmayer, se adaugă 2 picături de soluńie de metiloranj şi se titrează cu soluńia de acid din biuretă până la virarea indicatorului din galben în roz pal. Pentru fixarea mai exactă a punctului de echivalenńă se foloseşte soluńia martor. Pentru a prepara o asemenea soluńie întrun alt balon Erlenmayer se introduc circa 20 cm 3 de apă distilată, 2 picături de indicator şi o picătură de acid HCl. Volumul de acid necesar pentru atingerea punctului de echivalenńă se va determina prin compararea culorii soluńiei care se titrează cu a soluńiei martor. Este important să fie fixat momentul, când în urma adăugării unei singure picături de acid clorhidric soluńia care se titrează capătă o nuanńă roză, asemenea colorańiei soluńiei martor. Titrarea se repetă de cel puńin 3 ori pentru a obńine rezultate mai exacte. Pentru calculul concentrańiei acidului clorhidric se foloseşte volumul mediu V(HCl), care se determină cu relańia: n V (HCl) = Vi (HCl), n unde n este numărul de titrări, iar V i volumul consumat de acid. ConcentraŃia soluńiei de acid clorhidric se calculează folosind formula: i= 0 C(½Na 2BO 7 ) C(HCl) = (moli/ l). V(HCl) Dacă este necesar se face calcul titrului soluńiei de acid clorhidric T(HCl): C(HCl) 36,6 T(HCl) = (g/cm 3 ). 000 Oxalatul de sodiu se foloseşte pentru stabilirea titrului soluńiei de acid tare în varianta titrării directe a probei. Pentru aceasta se cântăresc exact la o balanńă analitică într-un creuzet de platină 0,2 g de oxalat de sodiu. Creuzetul se acoperă cu un capac puńin înclinat şi se calcinează la flacăra unui bec de gaz până la topire. Are loc reacńia: Na 2 C 2 O = Na 2 CO 3 + CO. ConŃinutul creuzetului se umectează şi se trece într-un balon, se răceşte şi se titrează cu HCl în prezenńa metiloranjului. Masa echivalentă a oxalatului de sodiu este 66,9996 g/mol echiv. ConcentraŃia soluńiei de acid se determină folosind relańia: m(na 2C 2O ) C(HCl) =, 66,9996 V unde V este volumul de acid exprimat în litri, consumat pentru titrare. Carbonatul de sodiu are masa molară a echivalentului 52,99. Pentru a obńine carbonat de o calitate satisfăcătoare pentru a fi folosit ca substanńă etalon se pleacă de la hidrogenocarbonat de sodiu pur NaHCO 3, care în prealabil se calcinează timp de o oră într-un cuptor electric la temperatura o C. Ca şi în cazul oxalatului de sodiu la titrare are loc reacńia: Na 2 CO 3 + 2HCl = 2NaCl + CO 2 + H 2 O.
7 Titrări acido-bazice 7 Pentru a minimiza eroarea produsă de prezenńa bioxidului de carbon dozlvat, se recomandă fierberea soluńiei (2 min.) înainte de a atinge punctul de echivalenńă. Determinarea amoniacului în sărurile de amoniu Există mai multe variante de determinare a conńinutului amoniacului. Unele din ele au fost descrise anterior. Ne vom opri aici la o metodă de titrare inversă în varianta titrării probelor cântărite. Se cântăreşte pe balanńa analitică o probă de sare de amoniu (masa aproximativă a probei variază în funcńie de conńinutul amoniacului, şi în cadrul lucrărilor de laborator este indicată de conducătorul de lucrări). Proba cântărită se trece cantitativ în balonul pentru titrare şi se dizolvă în 50 cm 3 de apă distilată. Se adaugă un volum exact (cu biureta sau pipeta) de soluńie de NaOH cu concentrańia cunoscută (de exemplu 0 cm 3 ) şi se încălzeşte pe un reşou electric până la înlăturarea completă a amoniacului care se produce conform ecuańiei: NH Cl + NaOH t C NaCl + H 2 O + NH 3. Pentru a stabili prezenńa amoniacului se foloseşte o hârtie de filtru umezită cu Hg 2 (NO 3 ) 2. În prezenńa amoniacului hârtia introdusă la ieşirea din balonul de titrare se înnegreşte. Dacă eliminarea amoniacului s-a sfârşit, hârtia umezită nu-şi schimbă culoarea. Poate fi folosită în acest scop şi hârtie roză de turnesol, care, fiind umezită, în contact cu amoniacul devine albastră. După înlăturarea completă a amoniacului soluńia se răceşte şi se titrează cu o soluńie standardizată de HCl în prezenńa metiloranjului. Pentru a efectua calculul conńinutului de amoniac se foloseşte rańionamentul următor. Se exprimă numărul de moli echivalenńi de hidroxid de sodiu n(naoh) introduşi în balonul pentru titrare: C(NaOH) V(NaOH),ml n (NaOH) =, 000 şi numărul de moli echivalenńi de acid clorhidric consumat pentru titrarea hidroxidului de sodiu rămas după eliminarea amoniacului: C(HCl) V(HCl),ml n (HCl) =, 000 Evident că n (HCl) < n (NaOH) pentru că o parte de hidroxid a fost consumat pentru eliminarea amoniacului conform ecuańiei scrise mai sus. Aceeaşi ecuańie indică că numărul de moli de hidroxid de sodiu consumat şi poate fi calculat din diferenńa: va fi: C(NaOH) V(NaOH) C(HCl) V(HCl) n(nh 3 ) = n(naoh) n(hcl) =. 000 Masa molară a amoniacului este 7,03 g/mol. Prin urmare, masa amoniacului m(nh 3 ) m(nh3) = n (NH 3 ) 7,03 (g). Rezultatul poate fi exprimat în părńi de masă ω(nh 3 ) a amoniacului în proba analizată: m(nh ω(nh 3 ) = 3 ) 00%. m(prodei) Metoda este mai puńin precisă ca cele descrise anterior. În timpul încălzirii o parte din NaOH poate reacńiona cu sticla, reducând masa de hidroxid care rămâne şi majorând conńinutul amoniacului. În schimb este mai simplă şi mai rapidă.
8 Titrări acido-bazice 8 Analiza unui amestec de carbonat şi hidroxid de sodiu Fiind în contact cu aerul, soluńiile de alcalii absorb dioxidul de carbon CO 2, transformându-se parńial în carbonańi. De exemplu, hidroxidul de sodiu conńine ca impuritate carbonatul de sodiu, format în urma reacńiei: 2NaOH + CO 2 = Na 2 CO 3 + H 2 O. Pentru a determina conńinutul unui carbonat şi a unui alcaliu în amestec se folosesc mai multe metode. Propunem mai jos una din ele. Este cunoscut că pe curba de titrare a Na 2 CO 3 există două salturi de titrare care corespund celor două puncte de echivalenńă a reacńiilor: Na 2 CO 3 + HCl = NaHCO 3 + H 2 O; Na 2 CO 3 + 2HCl = Na 2 CO 3 + 2H 2 O. Primul punct de echivalenńă poate fi fixat în prezenńă de metiloranj. Din ecuańii este evident că pentru a atinge al doilea punct de echivalenńă consumul de acid va fi dublu, în comparańie cu cel necesar pentru primul punct. Prin urmare se poate afirma că în prezenńă de fenolftaleină se titrează numai o jumătate din cantitatea totală de Na 2 CO 3. Pentru un alcaliu tare (de exemplu NaOH) titrarea va fi totală cu ambii indicatori. Modul de lucru. SoluŃia propusă pentru analiză, care conńine hidroxid şi carbonat de sodiu, se trece cantitativ într-un balon cotat, se aduce până la cota cu apă distilată ce nu conńine CO 2 şi se agită bine. Se măsoară cu pipeta o parte alicotă din soluńia de analizat (V pip. ) se trece în balonul pentru titrare, se adaugă 8-0 picături de fenolftaleină şi se titrează cu HCl până la disparińia culorii roze. Se înregistrează de pe biuretă consumul de HCl V (HCl). Acest volum reprezintă cantitatea de HCl consumată pentru neutralizarea totală a hidroxidului de sodiu şi a unei jumătăńi de carbonat de sodiu. După înregistrarea volumului V (HCl), la soluńia decolorată se adaugă -2 picături de metiloranj. SoluŃia capătă o colorańie galbenă. Titrarea continuă până la aparińia unei colorańii roze. Se înregistrează volumul de HCl (total) V 2 (HCl). Este evident că V 2 (HCl) >> V (HCl) şi diferenńa (V 2 V ) reprezintă cantitatea de Na 2 CO 3 rămase după titrarea în prezenńă de fenolftaleină. Titrările se repetă minimum de 3 ori. Pentru calcul este important să fie corect exprimat volumul de HCl consumat pentru NaOH V 3 (HCl) şi pentru Na 2 CO 3 V (HCl). sau łinând cont de cele spuse mai sus vor fi corecte relańiile: V (HCl) = 2[V 2 (HCl) V (HCl)], V 3 (HCl) = V 2 (HCl) V (HCl ) = V 2 (HCl) 2V 2 (HCl) + 2V 2 (HCl) = 2V (HCl) V 2 (HCl) V 3 (HCl) = V (HCl) 2 V (HCl) = V (HCl) V 2 (HCl) + V (HCl) = 2V (HCl) V 2 (HCl). ConŃinutul hidroxidului de sodiu şi al carbonatului de sodiu în soluńia propusă pentru analiză poate fi calculat folosind expresiile: m(naoh) = T(HCl/NaOH). V 3 (HCl). V bal /V pip ; m(na 2 CO 3 ) = T(HCl/Na 2 CO 3 ). V (HCl). V bal /V pip.
9 Titrări acido-bazice 9 Această metodă poate fi folosită în cazul când conńinutul carbonatului este mic fańă de cel al hidroxidului. Pentru a minimiza erorile este necesar să fie respectate următoarele condińii: a) să se evite sau să se reducă la minimum, contactul cu aerul (se foloseşte apa distilată, care nu conńine CO 2, se lucrează mai repede ca de obicei şi nu se recomandă o amestecare intensă a soluńiei de titrare). b) spre sfârşitul titrării cu fenolftaleină, acidul se adaugă încet, pentru a evita formarea acidului carbonic H 2 CO 3. c) se foloseşte o cantitate destul de mare de fenolftaleină, pentru a evita decolorarea pretimpurie a soluńiei.
a. 0,1; 0,1; 0,1; b. 1, ; 5, ; 8, ; c. 4,87; 6,15; 8,04; d. 7; 7; 7; e. 9,74; 12,30;1 6,08.
 1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
Metode iterative pentru probleme neliniare - contractii
 Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate.
 Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
MARCAREA REZISTOARELOR
 1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
Aplicaţii ale principiului I al termodinamicii la gazul ideal
 Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
STUDIUL COMPARATIV AL CURBELOR DE TITRARE A UNOR ACIZI
 REACŢIA CHIMICĂ STUDIUL COMPARATIV AL CURBELOR DE TITRARE A UNOR ACIZI Reacţia de titrare a unui acid tare respectiv a unui acid slab (notat în general HA) cu o bază tare se reprezintă prin echilibrul:
REACŢIA CHIMICĂ STUDIUL COMPARATIV AL CURBELOR DE TITRARE A UNOR ACIZI Reacţia de titrare a unui acid tare respectiv a unui acid slab (notat în general HA) cu o bază tare se reprezintă prin echilibrul:
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE
 DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
(a) se numeşte derivata parţială a funcţiei f în raport cu variabila x i în punctul a.
 Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
Curs 4 Serii de numere reale
 Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Metode de interpolare bazate pe diferenţe divizate
 Metode de interpolare bazate pe diferenţe divizate Radu Trîmbiţaş 4 octombrie 2005 1 Forma Newton a polinomului de interpolare Lagrange Algoritmul nostru se bazează pe forma Newton a polinomului de interpolare
Metode de interpolare bazate pe diferenţe divizate Radu Trîmbiţaş 4 octombrie 2005 1 Forma Newton a polinomului de interpolare Lagrange Algoritmul nostru se bazează pe forma Newton a polinomului de interpolare
V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile
 Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Planul determinat de normală şi un punct Ecuaţia generală Plane paralele Unghi diedru Planul determinat de 3 puncte necoliniare
 1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM 1 electronica.geniu.ro
 Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
5. FUNCŢII IMPLICITE. EXTREME CONDIŢIONATE.
 5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
II. 5. Probleme. 20 c 100 c = 10,52 % Câte grame sodă caustică se găsesc în 300 g soluţie de concentraţie 10%? Rezolvare m g.
 II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
Curs 14 Funcţii implicite. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi"
 Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
a. 11 % b. 12 % c. 13 % d. 14 %
 1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
5.5. REZOLVAREA CIRCUITELOR CU TRANZISTOARE BIPOLARE
 5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
Componente şi Circuite Electronice Pasive. Laborator 3. Divizorul de tensiune. Divizorul de curent
 Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Asupra unei inegalităţi date la barajul OBMJ 2006
 Asupra unei inegalităţi date la barajul OBMJ 006 Mircea Lascu şi Cezar Lupu La cel de-al cincilea baraj de Juniori din data de 0 mai 006 a fost dată următoarea inegalitate: Fie x, y, z trei numere reale
Asupra unei inegalităţi date la barajul OBMJ 006 Mircea Lascu şi Cezar Lupu La cel de-al cincilea baraj de Juniori din data de 0 mai 006 a fost dată următoarea inegalitate: Fie x, y, z trei numere reale
Seminariile Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reziduurilor
 Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
DETERMINAREA INDICATORILOR DE CALITATE PENTRU CARACTERIZAREA APELOR DE SUPRAFAŢĂ. CARACTERISTICI CHIMICE
 DETERMINAREA INDICATORILOR DE CALITATE PENTRU CARACTERIZAREA APELOR DE SUPRAFAŢĂ. CARACTERISTICI CHIMICE Conform legislaţiei naţionale şi internaţionale indicatorii chimici se impart în: Indicatori generali:
DETERMINAREA INDICATORILOR DE CALITATE PENTRU CARACTERIZAREA APELOR DE SUPRAFAŢĂ. CARACTERISTICI CHIMICE Conform legislaţiei naţionale şi internaţionale indicatorii chimici se impart în: Indicatori generali:
Laborator 11. Mulţimi Julia. Temă
 Laborator 11 Mulţimi Julia. Temă 1. Clasa JuliaGreen. Să considerăm clasa JuliaGreen dată de exemplu la curs pentru metoda locului final şi să schimbăm numărul de iteraţii nriter = 100 în nriter = 101.
Laborator 11 Mulţimi Julia. Temă 1. Clasa JuliaGreen. Să considerăm clasa JuliaGreen dată de exemplu la curs pentru metoda locului final şi să schimbăm numărul de iteraţii nriter = 100 în nriter = 101.
riptografie şi Securitate
 riptografie şi Securitate - Prelegerea 12 - Scheme de criptare CCA sigure Adela Georgescu, Ruxandra F. Olimid Facultatea de Matematică şi Informatică Universitatea din Bucureşti Cuprins 1. Schemă de criptare
riptografie şi Securitate - Prelegerea 12 - Scheme de criptare CCA sigure Adela Georgescu, Ruxandra F. Olimid Facultatea de Matematică şi Informatică Universitatea din Bucureşti Cuprins 1. Schemă de criptare
 4. CIRCUITE LOGICE ELEMENTRE 4.. CIRCUITE LOGICE CU COMPONENTE DISCRETE 4.. PORŢI LOGICE ELEMENTRE CU COMPONENTE PSIVE Componente electronice pasive sunt componente care nu au capacitatea de a amplifica
4. CIRCUITE LOGICE ELEMENTRE 4.. CIRCUITE LOGICE CU COMPONENTE DISCRETE 4.. PORŢI LOGICE ELEMENTRE CU COMPONENTE PSIVE Componente electronice pasive sunt componente care nu au capacitatea de a amplifica
a n (ζ z 0 ) n. n=1 se numeste partea principala iar seria a n (z z 0 ) n se numeste partea
 Serii Laurent Definitie. Se numeste serie Laurent o serie de forma Seria n= (z z 0 ) n regulata (tayloriana) = (z z n= 0 ) + n se numeste partea principala iar seria se numeste partea Sa presupunem ca,
Serii Laurent Definitie. Se numeste serie Laurent o serie de forma Seria n= (z z 0 ) n regulata (tayloriana) = (z z n= 0 ) + n se numeste partea principala iar seria se numeste partea Sa presupunem ca,
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor X) functia f 1
 Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
Problema a II - a (10 puncte) Diferite circuite electrice
 Olimpiada de Fizică - Etapa pe judeţ 15 ianuarie 211 XI Problema a II - a (1 puncte) Diferite circuite electrice A. Un elev utilizează o sursă de tensiune (1), o cutie cu rezistenţe (2), un întrerupător
Olimpiada de Fizică - Etapa pe judeţ 15 ianuarie 211 XI Problema a II - a (1 puncte) Diferite circuite electrice A. Un elev utilizează o sursă de tensiune (1), o cutie cu rezistenţe (2), un întrerupător
5.4. MULTIPLEXOARE A 0 A 1 A 2
 5.4. MULTIPLEXOARE Multiplexoarele (MUX) sunt circuite logice combinaţionale cu m intrări şi o singură ieşire, care permit transferul datelor de la una din intrări spre ieşirea unică. Selecţia intrării
5.4. MULTIPLEXOARE Multiplexoarele (MUX) sunt circuite logice combinaţionale cu m intrări şi o singură ieşire, care permit transferul datelor de la una din intrări spre ieşirea unică. Selecţia intrării
III. Serii absolut convergente. Serii semiconvergente. ii) semiconvergentă dacă este convergentă iar seria modulelor divergentă.
 III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
SEMINAR 14. Funcţii de mai multe variabile (continuare) ( = 1 z(x,y) x = 0. x = f. x + f. y = f. = x. = 1 y. y = x ( y = = 0
 Facultatea de Hidrotehnică, Geodezie şi Ingineria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucian MATICIUC SEMINAR 4 Funcţii de mai multe variabile continuare). Să se arate că funcţia z,
Facultatea de Hidrotehnică, Geodezie şi Ingineria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucian MATICIUC SEMINAR 4 Funcţii de mai multe variabile continuare). Să se arate că funcţia z,
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor
 Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
Curs 1 Şiruri de numere reale
 Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
Fig Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36].
![Fig Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36]. Fig Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36].](/thumbs/72/67648751.jpg) Componente şi circuite pasive Fig.3.85. Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36]. Fig.3.86. Rezistenţa serie echivalentă pierderilor în funcţie
Componente şi circuite pasive Fig.3.85. Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36]. Fig.3.86. Rezistenţa serie echivalentă pierderilor în funcţie
I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare.
 Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
1. PROPRIETĂȚILE FLUIDELOR
 1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
Reactia de amfoterizare a aluminiului
 Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
5.1. Noţiuni introductive
 ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
2. Sisteme de forţe concurente...1 Cuprins...1 Introducere Aspecte teoretice Aplicaţii rezolvate...3
 SEMINAR 2 SISTEME DE FRŢE CNCURENTE CUPRINS 2. Sisteme de forţe concurente...1 Cuprins...1 Introducere...1 2.1. Aspecte teoretice...2 2.2. Aplicaţii rezolvate...3 2. Sisteme de forţe concurente În acest
SEMINAR 2 SISTEME DE FRŢE CNCURENTE CUPRINS 2. Sisteme de forţe concurente...1 Cuprins...1 Introducere...1 2.1. Aspecte teoretice...2 2.2. Aplicaţii rezolvate...3 2. Sisteme de forţe concurente În acest
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
SERII NUMERICE. Definiţia 3.1. Fie (a n ) n n0 (n 0 IN) un şir de numere reale şi (s n ) n n0
 SERII NUMERICE Definiţia 3.1. Fie ( ) n n0 (n 0 IN) un şir de numere reale şi (s n ) n n0 şirul definit prin: s n0 = 0, s n0 +1 = 0 + 0 +1, s n0 +2 = 0 + 0 +1 + 0 +2,.......................................
SERII NUMERICE Definiţia 3.1. Fie ( ) n n0 (n 0 IN) un şir de numere reale şi (s n ) n n0 şirul definit prin: s n0 = 0, s n0 +1 = 0 + 0 +1, s n0 +2 = 0 + 0 +1 + 0 +2,.......................................
VII.2. PROBLEME REZOLVATE
 Teoria Circuitelor Electrice Aplicaţii V PROBEME REOVATE R7 În circuitul din fiura 7R se cunosc: R e t 0 sint [V] C C t 0 sint [A] Se cer: a rezolvarea circuitului cu metoda teoremelor Kirchhoff; rezolvarea
Teoria Circuitelor Electrice Aplicaţii V PROBEME REOVATE R7 În circuitul din fiura 7R se cunosc: R e t 0 sint [V] C C t 0 sint [A] Se cer: a rezolvarea circuitului cu metoda teoremelor Kirchhoff; rezolvarea
Sisteme diferenţiale liniare de ordinul 1
 1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
Ecuaţia generală Probleme de tangenţă Sfera prin 4 puncte necoplanare. Elipsoidul Hiperboloizi Paraboloizi Conul Cilindrul. 1 Sfera.
 pe ecuaţii generale 1 Sfera Ecuaţia generală Probleme de tangenţă 2 pe ecuaţii generale Sfera pe ecuaţii generale Ecuaţia generală Probleme de tangenţă Numim sferă locul geometric al punctelor din spaţiu
pe ecuaţii generale 1 Sfera Ecuaţia generală Probleme de tangenţă 2 pe ecuaţii generale Sfera pe ecuaţii generale Ecuaţia generală Probleme de tangenţă Numim sferă locul geometric al punctelor din spaţiu
Valori limită privind SO2, NOx şi emisiile de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili
 Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
Conice. Lect. dr. Constantin-Cosmin Todea. U.T. Cluj-Napoca
 Conice Lect. dr. Constantin-Cosmin Todea U.T. Cluj-Napoca Definiţie: Se numeşte curbă algebrică plană mulţimea punctelor din plan de ecuaţie implicită de forma (C) : F (x, y) = 0 în care funcţia F este
Conice Lect. dr. Constantin-Cosmin Todea U.T. Cluj-Napoca Definiţie: Se numeşte curbă algebrică plană mulţimea punctelor din plan de ecuaţie implicită de forma (C) : F (x, y) = 0 în care funcţia F este
Subiecte Clasa a VII-a
 lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
Subiecte Clasa a VIII-a
 Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
Integrala nedefinită (primitive)
 nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
Capitolul 14. Asamblari prin pene
 Capitolul 14 Asamblari prin pene T.14.1. Momentul de torsiune este transmis de la arbore la butuc prin intermediul unei pene paralele (figura 14.1). De care din cotele indicate depinde tensiunea superficiala
Capitolul 14 Asamblari prin pene T.14.1. Momentul de torsiune este transmis de la arbore la butuc prin intermediul unei pene paralele (figura 14.1). De care din cotele indicate depinde tensiunea superficiala
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
MINISTERUL SĂNĂTĂȚII AL REPUBLICII MOLDOVA UNIVERSITATEA DE STAT DE MRDICINĂ ȘI FARMACIE NICOLAE TESTEMIȚANU
 MINISTERUL SĂNĂTĂȚII L REPULICII MOLDOV UNIVERSITTE DE STT DE MRDICINĂ ȘI FRMCIE NICOLE TESTEMIȚNU FCULTTE FRMCIE Catedra Chimie Generală Grigore UDU CURS DE CHIMIE NLITICĂ Partea II. naliza chimică cantitativă.
MINISTERUL SĂNĂTĂȚII L REPULICII MOLDOV UNIVERSITTE DE STT DE MRDICINĂ ȘI FRMCIE NICOLE TESTEMIȚNU FCULTTE FRMCIE Catedra Chimie Generală Grigore UDU CURS DE CHIMIE NLITICĂ Partea II. naliza chimică cantitativă.
Definiţia generală Cazul 1. Elipsa şi hiperbola Cercul Cazul 2. Parabola Reprezentari parametrice ale conicelor Tangente la conice
 1 Conice pe ecuaţii reduse 2 Conice pe ecuaţii reduse Definiţie Numim conica locul geometric al punctelor din plan pentru care raportul distantelor la un punct fix F şi la o dreaptă fixă (D) este o constantă
1 Conice pe ecuaţii reduse 2 Conice pe ecuaţii reduse Definiţie Numim conica locul geometric al punctelor din plan pentru care raportul distantelor la un punct fix F şi la o dreaptă fixă (D) este o constantă
RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii transversale, scrisă faţă de una dintre axele de inerţie principale:,
 REZISTENTA MATERIALELOR 1. Ce este modulul de rezistenţă? Exemplificaţi pentru o secţiune dreptunghiulară, respectiv dublu T. RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii
REZISTENTA MATERIALELOR 1. Ce este modulul de rezistenţă? Exemplificaţi pentru o secţiune dreptunghiulară, respectiv dublu T. RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii
Curs 2 Şiruri de numere reale
 Curs 2 Şiruri de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Convergenţă şi mărginire Teoremă Orice şir convergent este mărginit. Demonstraţie Fie (x n ) n 0 un
Curs 2 Şiruri de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Convergenţă şi mărginire Teoremă Orice şir convergent este mărginit. Demonstraţie Fie (x n ) n 0 un
2.1 Sfera. (EGS) ecuaţie care poartă denumirea de ecuaţia generală asferei. (EGS) reprezintă osferă cu centrul în punctul. 2 + p 2
 .1 Sfera Definitia 1.1 Se numeşte sferă mulţimea tuturor punctelor din spaţiu pentru care distanţa la u punct fi numit centrul sferei este egalăcuunnumăr numit raza sferei. Fie centrul sferei C (a, b,
.1 Sfera Definitia 1.1 Se numeşte sferă mulţimea tuturor punctelor din spaţiu pentru care distanţa la u punct fi numit centrul sferei este egalăcuunnumăr numit raza sferei. Fie centrul sferei C (a, b,
R R, f ( x) = x 7x+ 6. Determinați distanța dintre punctele de. B=, unde x și y sunt numere reale.
 5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
COLEGIUL NATIONAL CONSTANTIN CARABELLA TARGOVISTE. CONCURSUL JUDETEAN DE MATEMATICA CEZAR IVANESCU Editia a VI-a 26 februarie 2005.
 SUBIECTUL Editia a VI-a 6 februarie 005 CLASA a V-a Fie A = x N 005 x 007 si B = y N y 003 005 3 3 a) Specificati cel mai mic element al multimii A si cel mai mare element al multimii B. b)stabiliti care
SUBIECTUL Editia a VI-a 6 februarie 005 CLASA a V-a Fie A = x N 005 x 007 si B = y N y 003 005 3 3 a) Specificati cel mai mic element al multimii A si cel mai mare element al multimii B. b)stabiliti care
ANALIZE FIZICO-CHIMICE MATRICE APA. Tip analiza Tip proba Metoda de analiza/document de referinta/acreditare
 ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
Seminar 5 Analiza stabilității sistemelor liniare
 Seminar 5 Analiza stabilității sistemelor liniare Noțiuni teoretice Criteriul Hurwitz de analiză a stabilității sistemelor liniare În cazul sistemelor liniare, stabilitatea este o condiție de localizare
Seminar 5 Analiza stabilității sistemelor liniare Noțiuni teoretice Criteriul Hurwitz de analiză a stabilității sistemelor liniare În cazul sistemelor liniare, stabilitatea este o condiție de localizare
Criptosisteme cu cheie publică III
 Criptosisteme cu cheie publică III Anul II Aprilie 2017 Problema rucsacului ( knapsack problem ) Considerăm un număr natural V > 0 şi o mulţime finită de numere naturale pozitive {v 0, v 1,..., v k 1 }.
Criptosisteme cu cheie publică III Anul II Aprilie 2017 Problema rucsacului ( knapsack problem ) Considerăm un număr natural V > 0 şi o mulţime finită de numere naturale pozitive {v 0, v 1,..., v k 1 }.
4. Măsurarea tensiunilor şi a curenţilor electrici. Voltmetre electronice analogice
 4. Măsurarea tensiunilor şi a curenţilor electrici oltmetre electronice analogice oltmetre de curent continuu Ampl.c.c. x FTJ Protectie Atenuator calibrat Atenuatorul calibrat divizor rezistiv R in const.
4. Măsurarea tensiunilor şi a curenţilor electrici oltmetre electronice analogice oltmetre de curent continuu Ampl.c.c. x FTJ Protectie Atenuator calibrat Atenuatorul calibrat divizor rezistiv R in const.
Aparate de măsurat. Măsurări electronice Rezumatul cursului 2. MEE - prof. dr. ing. Ioan D. Oltean 1
 Aparate de măsurat Măsurări electronice Rezumatul cursului 2 MEE - prof. dr. ing. Ioan D. Oltean 1 1. Aparate cu instrument magnetoelectric 2. Ampermetre şi voltmetre 3. Ohmetre cu instrument magnetoelectric
Aparate de măsurat Măsurări electronice Rezumatul cursului 2 MEE - prof. dr. ing. Ioan D. Oltean 1 1. Aparate cu instrument magnetoelectric 2. Ampermetre şi voltmetre 3. Ohmetre cu instrument magnetoelectric
Ovidiu Gabriel Avădănei, Florin Mihai Tufescu,
 vidiu Gabriel Avădănei, Florin Mihai Tufescu, Capitolul 6 Amplificatoare operaţionale 58. Să se calculeze coeficientul de amplificare în tensiune pentru amplficatorul inversor din fig.58, pentru care se
vidiu Gabriel Avădănei, Florin Mihai Tufescu, Capitolul 6 Amplificatoare operaţionale 58. Să se calculeze coeficientul de amplificare în tensiune pentru amplficatorul inversor din fig.58, pentru care se
Esalonul Redus pe Linii (ERL). Subspatii.
 Seminarul 1 Esalonul Redus pe Linii (ERL). Subspatii. 1.1 Breviar teoretic 1.1.1 Esalonul Redus pe Linii (ERL) Definitia 1. O matrice A L R mxn este in forma de Esalon Redus pe Linii (ERL), daca indeplineste
Seminarul 1 Esalonul Redus pe Linii (ERL). Subspatii. 1.1 Breviar teoretic 1.1.1 Esalonul Redus pe Linii (ERL) Definitia 1. O matrice A L R mxn este in forma de Esalon Redus pe Linii (ERL), daca indeplineste
Măsurări în Electronică şi Telecomunicaţii 4. Măsurarea impedanţelor
 4. Măsurarea impedanţelor 4.2. Măsurarea rezistenţelor în curent continuu Metoda comparaţiei ceastă metodă: se utilizează pentru măsurarea rezistenţelor ~ 0 montaj serie sau paralel. Montajul serie (metoda
4. Măsurarea impedanţelor 4.2. Măsurarea rezistenţelor în curent continuu Metoda comparaţiei ceastă metodă: se utilizează pentru măsurarea rezistenţelor ~ 0 montaj serie sau paralel. Montajul serie (metoda
Curs 2 DIODE. CIRCUITE DR
 Curs 2 OE. CRCUTE R E CUPRN tructură. imbol Relația curent-tensiune Regimuri de funcționare Punct static de funcționare Parametrii diodei Modelul cu cădere de tensiune constantă Analiza circuitelor cu
Curs 2 OE. CRCUTE R E CUPRN tructură. imbol Relația curent-tensiune Regimuri de funcționare Punct static de funcționare Parametrii diodei Modelul cu cădere de tensiune constantă Analiza circuitelor cu
Erori si incertitudini de măsurare. Modele matematice Instrument: proiectare, fabricaţie, Interacţiune măsurand instrument:
 Erori i incertitudini de măurare Sure: Modele matematice Intrument: proiectare, fabricaţie, Interacţiune măurandintrument: (tranfer informaţie tranfer energie) Influente externe: temperatura, preiune,
Erori i incertitudini de măurare Sure: Modele matematice Intrument: proiectare, fabricaţie, Interacţiune măurandintrument: (tranfer informaţie tranfer energie) Influente externe: temperatura, preiune,
Cum folosim cazuri particulare în rezolvarea unor probleme
 Cum folosim cazuri particulare în rezolvarea unor probleme GHEORGHE ECKSTEIN 1 Atunci când întâlnim o problemă pe care nu ştim s-o abordăm, adesea este bine să considerăm cazuri particulare ale acesteia.
Cum folosim cazuri particulare în rezolvarea unor probleme GHEORGHE ECKSTEIN 1 Atunci când întâlnim o problemă pe care nu ştim s-o abordăm, adesea este bine să considerăm cazuri particulare ale acesteia.
Proiectarea filtrelor prin metoda pierderilor de inserţie
 FITRE DE MIROUNDE Proiectarea filtrelor prin metoda pierderilor de inserţie P R Puterea disponibila de la sursa Puterea livrata sarcinii P inc P Γ ( ) Γ I lo P R ( ) ( ) M ( ) ( ) M N P R M N ( ) ( ) Tipuri
FITRE DE MIROUNDE Proiectarea filtrelor prin metoda pierderilor de inserţie P R Puterea disponibila de la sursa Puterea livrata sarcinii P inc P Γ ( ) Γ I lo P R ( ) ( ) M ( ) ( ) M N P R M N ( ) ( ) Tipuri
SEMINARUL 3. Cap. II Serii de numere reale. asociat seriei. (3n 5)(3n 2) + 1. (3n 2)(3n+1) (3n 2) (3n + 1) = a
 Capitolul II: Serii de umere reale. Lect. dr. Lucia Maticiuc Facultatea de Hidrotehică, Geodezie şi Igieria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucia MATICIUC SEMINARUL 3. Cap. II Serii
Capitolul II: Serii de umere reale. Lect. dr. Lucia Maticiuc Facultatea de Hidrotehică, Geodezie şi Igieria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucia MATICIUC SEMINARUL 3. Cap. II Serii
Capitolul ASAMBLAREA LAGĂRELOR LECŢIA 25
 Capitolul ASAMBLAREA LAGĂRELOR LECŢIA 25 LAGĂRELE CU ALUNECARE!" 25.1.Caracteristici.Părţi componente.materiale.!" 25.2.Funcţionarea lagărelor cu alunecare.! 25.1.Caracteristici.Părţi componente.materiale.
Capitolul ASAMBLAREA LAGĂRELOR LECŢIA 25 LAGĂRELE CU ALUNECARE!" 25.1.Caracteristici.Părţi componente.materiale.!" 25.2.Funcţionarea lagărelor cu alunecare.! 25.1.Caracteristici.Părţi componente.materiale.
REACŢII DE ADIŢIE NUCLEOFILĂ (AN-REACŢII) (ALDEHIDE ŞI CETONE)
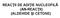 EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
 10. STABILIZATOAE DE TENSIUNE 10.1 STABILIZATOAE DE TENSIUNE CU TANZISTOAE BIPOLAE Stabilizatorul de tensiune cu tranzistor compară în permanenţă valoare tensiunii de ieşire (stabilizate) cu tensiunea
10. STABILIZATOAE DE TENSIUNE 10.1 STABILIZATOAE DE TENSIUNE CU TANZISTOAE BIPOLAE Stabilizatorul de tensiune cu tranzistor compară în permanenţă valoare tensiunii de ieşire (stabilizate) cu tensiunea
BARAJ DE JUNIORI,,Euclid Cipru, 28 mai 2012 (barajul 3)
 BARAJ DE JUNIORI,,Euclid Cipru, 8 mi 0 (brjul ) Problem Arătţi că dcă, b, c sunt numere rele cre verifică + b + c =, tunci re loc ineglitte xy + yz + zx Problem Fie şi b numere nturle nenule Dcă numărul
BARAJ DE JUNIORI,,Euclid Cipru, 8 mi 0 (brjul ) Problem Arătţi că dcă, b, c sunt numere rele cre verifică + b + c =, tunci re loc ineglitte xy + yz + zx Problem Fie şi b numere nturle nenule Dcă numărul
L.2. Verificarea metrologică a aparatelor de măsurare analogice
 L.2. Verificarea metrologică a aparatelor de măsurare analogice 1. Obiectul lucrării Prin verificarea metrologică a unui aparat de măsurat se stabileşte: Dacă acesta se încadrează în limitele erorilor
L.2. Verificarea metrologică a aparatelor de măsurare analogice 1. Obiectul lucrării Prin verificarea metrologică a unui aparat de măsurat se stabileşte: Dacă acesta se încadrează în limitele erorilor
Examenul de bacalaureat nańional 2013 Proba E. d) Chimie organică (nivel I/ nivel II)
 Examenul de bacalaureat nańional 2013 Proba E. d) Chimie organică (nivel I/ nivel II) MODEL Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL I Subiectul
Examenul de bacalaureat nańional 2013 Proba E. d) Chimie organică (nivel I/ nivel II) MODEL Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL I Subiectul
Exemple de probleme rezolvate pentru cursurile DEEA Tranzistoare bipolare cu joncţiuni
 Problema 1. Se dă circuitul de mai jos pentru care se cunosc: VCC10[V], 470[kΩ], RC2,7[kΩ]. Tranzistorul bipolar cu joncţiuni (TBJ) este de tipul BC170 şi are parametrii β100 şi VBE0,6[V]. 1. să se determine
Problema 1. Se dă circuitul de mai jos pentru care se cunosc: VCC10[V], 470[kΩ], RC2,7[kΩ]. Tranzistorul bipolar cu joncţiuni (TBJ) este de tipul BC170 şi are parametrii β100 şi VBE0,6[V]. 1. să se determine
1.7. AMPLIFICATOARE DE PUTERE ÎN CLASA A ŞI AB
 1.7. AMLFCATOARE DE UTERE ÎN CLASA A Ş AB 1.7.1 Amplificatoare în clasa A La amplificatoarele din clasa A, forma de undă a tensiunii de ieşire este aceeaşi ca a tensiunii de intrare, deci întreg semnalul
1.7. AMLFCATOARE DE UTERE ÎN CLASA A Ş AB 1.7.1 Amplificatoare în clasa A La amplificatoarele din clasa A, forma de undă a tensiunii de ieşire este aceeaşi ca a tensiunii de intrare, deci întreg semnalul
FLUXURI MAXIME ÎN REŢELE DE TRANSPORT. x 4
 FLUXURI MAXIME ÎN REŢELE DE TRANSPORT Se numeşte reţea de transport un graf în care fiecărui arc îi este asociat capacitatea arcului şi în care eistă un singur punct de intrare şi un singur punct de ieşire.
FLUXURI MAXIME ÎN REŢELE DE TRANSPORT Se numeşte reţea de transport un graf în care fiecărui arc îi este asociat capacitatea arcului şi în care eistă un singur punct de intrare şi un singur punct de ieşire.
Principiul Inductiei Matematice.
 Principiul Inductiei Matematice. Principiul inductiei matematice constituie un mijloc important de demonstratie in matematica a propozitiilor (afirmatiilor) ce depind de argument natural. Metoda inductiei
Principiul Inductiei Matematice. Principiul inductiei matematice constituie un mijloc important de demonstratie in matematica a propozitiilor (afirmatiilor) ce depind de argument natural. Metoda inductiei
Εμπορική αλληλογραφία Ηλεκτρονική Αλληλογραφία
 - Εισαγωγή Stimate Domnule Preşedinte, Stimate Domnule Preşedinte, Εξαιρετικά επίσημη επιστολή, ο παραλήπτης έχει ένα ειδικό τίτλο ο οποίος πρέπει να χρησιμοποιηθεί αντί του ονόματος του Stimate Domnule,
- Εισαγωγή Stimate Domnule Preşedinte, Stimate Domnule Preşedinte, Εξαιρετικά επίσημη επιστολή, ο παραλήπτης έχει ένα ειδικό τίτλο ο οποίος πρέπει να χρησιμοποιηθεί αντί του ονόματος του Stimate Domnule,
Capitolul 4-COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ-
 Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Ecuatii trigonometrice
 Ecuatii trigonometrice Ecuatiile ce contin necunoscute sub semnul functiilor trigonometrice se numesc ecuatii trigonometrice. Cele mai simple ecuatii trigonometrice sunt ecuatiile de tipul sin x = a, cos
Ecuatii trigonometrice Ecuatiile ce contin necunoscute sub semnul functiilor trigonometrice se numesc ecuatii trigonometrice. Cele mai simple ecuatii trigonometrice sunt ecuatiile de tipul sin x = a, cos
IV. CUADRIPOLI SI FILTRE ELECTRICE CAP. 13. CUADRIPOLI ELECTRICI
 V. POL S FLTE ELETE P. 3. POL ELET reviar a) Forma fundamentala a ecuatiilor cuadripolilor si parametrii fundamentali: Prima forma fundamentala: doua forma fundamentala: b) Parametrii fundamentali au urmatoarele
V. POL S FLTE ELETE P. 3. POL ELET reviar a) Forma fundamentala a ecuatiilor cuadripolilor si parametrii fundamentali: Prima forma fundamentala: doua forma fundamentala: b) Parametrii fundamentali au urmatoarele
Noţiuni introductive
 Metode Numerice Noţiuni introductive Erori. Condiţionare numerică. Stabilitatea algoritmilor. Complexitatea algoritmilor. Metodele numerice reprezintă tehnici prin care problemele matematice sunt reformulate
Metode Numerice Noţiuni introductive Erori. Condiţionare numerică. Stabilitatea algoritmilor. Complexitatea algoritmilor. Metodele numerice reprezintă tehnici prin care problemele matematice sunt reformulate
13. Grinzi cu zăbrele Metoda izolării nodurilor...1 Cuprins...1 Introducere Aspecte teoretice Aplicaţii rezolvate...
 SEMINAR GRINZI CU ZĂBRELE METODA IZOLĂRII NODURILOR CUPRINS. Grinzi cu zăbrele Metoda izolării nodurilor... Cuprins... Introducere..... Aspecte teoretice..... Aplicaţii rezolvate.... Grinzi cu zăbrele
SEMINAR GRINZI CU ZĂBRELE METODA IZOLĂRII NODURILOR CUPRINS. Grinzi cu zăbrele Metoda izolării nodurilor... Cuprins... Introducere..... Aspecte teoretice..... Aplicaţii rezolvate.... Grinzi cu zăbrele
Capitolul 4 PROPRIETĂŢI TOPOLOGICE ŞI DE NUMĂRARE ALE LUI R. 4.1 Proprietăţi topologice ale lui R Puncte de acumulare
 Capitolul 4 PROPRIETĂŢI TOPOLOGICE ŞI DE NUMĂRARE ALE LUI R În cele ce urmează, vom studia unele proprietăţi ale mulţimilor din R. Astfel, vom caracteriza locul" unui punct în cadrul unei mulţimi (în limba
Capitolul 4 PROPRIETĂŢI TOPOLOGICE ŞI DE NUMĂRARE ALE LUI R În cele ce urmează, vom studia unele proprietăţi ale mulţimilor din R. Astfel, vom caracteriza locul" unui punct în cadrul unei mulţimi (în limba
Ακαδημαϊκός Λόγος Κύριο Μέρος
 - Επίδειξη Συμφωνίας În linii mari sunt de acord cu...deoarece... Επίδειξη γενικής συμφωνίας με άποψη άλλου Cineva este de acord cu...deoarece... Επίδειξη γενικής συμφωνίας με άποψη άλλου D'une façon générale,
- Επίδειξη Συμφωνίας În linii mari sunt de acord cu...deoarece... Επίδειξη γενικής συμφωνίας με άποψη άλλου Cineva este de acord cu...deoarece... Επίδειξη γενικής συμφωνίας με άποψη άλλου D'une façon générale,
Metode de rezolvare a problemelor de calcul la chimia analitică
 Metoe e rezolvare a problemelor e calcul la chimia analitică 1 Metoe e rezolvare a problemelor e calcul la chimia analitică Problema este un tip e problematizare, care prouce un conflict intelectual mai
Metoe e rezolvare a problemelor e calcul la chimia analitică 1 Metoe e rezolvare a problemelor e calcul la chimia analitică Problema este un tip e problematizare, care prouce un conflict intelectual mai
riptografie şi Securitate
 riptografie şi Securitate - Prelegerea 21.2 - Sistemul de criptare ElGamal Adela Georgescu, Ruxandra F. Olimid Facultatea de Matematică şi Informatică Universitatea din Bucureşti Cuprins 1. Scurt istoric
riptografie şi Securitate - Prelegerea 21.2 - Sistemul de criptare ElGamal Adela Georgescu, Ruxandra F. Olimid Facultatea de Matematică şi Informatică Universitatea din Bucureşti Cuprins 1. Scurt istoric
II.METODE ELECTROCHIMICE DE ANALIZĂ
 II.METODE ELECTROCHIMICE DE ANALIZĂ Metodele electroanalitice reprezintă totalitatea metodelor analitice care măsoară potenţialul (Volţi) şi/sau intensitatea curentului electric (Amperi) într-o celulă
II.METODE ELECTROCHIMICE DE ANALIZĂ Metodele electroanalitice reprezintă totalitatea metodelor analitice care măsoară potenţialul (Volţi) şi/sau intensitatea curentului electric (Amperi) într-o celulă
Metode Runge-Kutta. 18 ianuarie Probleme scalare, pas constant. Dorim să aproximăm soluţia problemei Cauchy
 Metode Runge-Kutta Radu T. Trîmbiţaş 8 ianuarie 7 Probleme scalare, pas constant Dorim să aproximăm soluţia problemei Cauchy y (t) = f(t, y), a t b, y(a) = α. pe o grilă uniformă de (N + )-puncte din [a,
Metode Runge-Kutta Radu T. Trîmbiţaş 8 ianuarie 7 Probleme scalare, pas constant Dorim să aproximăm soluţia problemei Cauchy y (t) = f(t, y), a t b, y(a) = α. pe o grilă uniformă de (N + )-puncte din [a,
Examen AG. Student:... Grupa:... ianuarie 2011
 Problema 1. Pentru ce valori ale lui n,m N (n,m 1) graful K n,m este eulerian? Problema 2. Să se construiască o funcţie care să recunoască un graf P 3 -free. La intrare aceasta va primi un graf G = ({1,...,n},E)
Problema 1. Pentru ce valori ale lui n,m N (n,m 1) graful K n,m este eulerian? Problema 2. Să se construiască o funcţie care să recunoască un graf P 3 -free. La intrare aceasta va primi un graf G = ({1,...,n},E)
3. Momentul forţei în raport cu un punct...1 Cuprins...1 Introducere Aspecte teoretice Aplicaţii rezolvate...4
 SEMINAR 3 MMENTUL FRŢEI ÎN RAPRT CU UN PUNCT CUPRINS 3. Momentul forţei în raport cu un punct...1 Cuprins...1 Introducere...1 3.1. Aspecte teoretice...2 3.2. Aplicaţii rezolvate...4 3. Momentul forţei
SEMINAR 3 MMENTUL FRŢEI ÎN RAPRT CU UN PUNCT CUPRINS 3. Momentul forţei în raport cu un punct...1 Cuprins...1 Introducere...1 3.1. Aspecte teoretice...2 3.2. Aplicaţii rezolvate...4 3. Momentul forţei
Conice - Câteva proprietǎţi elementare
 Conice - Câteva proprietǎţi elementare lect.dr. Mihai Chiş Facultatea de Matematicǎ şi Informaticǎ Universitatea de Vest din Timişoara Viitori Olimpici ediţia a 5-a, etapa I, clasa a XII-a 1 Definiţii
Conice - Câteva proprietǎţi elementare lect.dr. Mihai Chiş Facultatea de Matematicǎ şi Informaticǎ Universitatea de Vest din Timişoara Viitori Olimpici ediţia a 5-a, etapa I, clasa a XII-a 1 Definiţii
Transformări de frecvenţă
 Lucrarea 22 Tranformări de frecvenţă Scopul lucrării: prezentarea metodei de inteză bazate pe utilizarea tranformărilor de frecvenţă şi exemplificarea aceteia cu ajutorul unui filtru trece-jo de tip Sallen-Key.
Lucrarea 22 Tranformări de frecvenţă Scopul lucrării: prezentarea metodei de inteză bazate pe utilizarea tranformărilor de frecvenţă şi exemplificarea aceteia cu ajutorul unui filtru trece-jo de tip Sallen-Key.
