2017. Rīgas Stradiņa universitāte
|
|
|
- Σίλας Παυλόπουλος
- 5 χρόνια πριν
- Προβολές:
Transcript
1 Termoinmik Siltum kustī:grieķu, Ltīņu vlos U - Iekšējā enerģij; Entlpij, Siltum sturs; S Entropij, uz pārmiņām (ūtī, sturs): Grieķu vlos- en tropos G Brīvā enerģij: Gis enerģij, Free: Angļu; Freie: Vācu Δ A Siltum stnrt sturs vieli kj/mol ΔS A Entropijs stnrt sturs vieli kj/mol ΔG A Brīvās enerģijs stnrt sturs vieli kj/mol Δr,ΔSr,ΔGr Entlpij,Entropij,Gis Enerģijs izmiņs ΔS izklieēt =-Δr/T siltum izkliee; ΔS kopējā =ΔSr+ΔS izklieēt kopējā entropijs izmiņ rekcijā sistīto enerģiju 1 Δr=ΣΔ proukti ΣΔ izejviels ; ΔSr=ΣΔS proukti ΣΔS izejviels ; ΔGr=ΣΔG proukti ΣΔG izejviels ; ΔGr=Δr T ΔSr; prēķin kā ΔS kopējā T=-ΔGr ir negtīv Gis Enerģijs izmiņ rekcijā 1) pozitīv ΔS kopējā T>0 prouktos ir zuēt rīvā Gis Enerģij; 2) negtīv ΔS kopējā T<0 Enerģij ir uzkrāt rekcijs prouktos Ķīmiskis potenciāls µ A vienm molm Δn A =1 mol A viels ir µ A = ΔG A /Δn A =ΔG A + R T ln(x A ) ; kj/mol B,, D vielu misījumā 0<X A <1 vienmēr ir ln(x A )<0 negtīvs lielums un mol ļs koncentrācijs prēķins X A =n A /n totl misījumā Rekcijs līzsvr konstntei K eq = X c X D ir konstnt vērtī XB līzsvr vielu misījum koncentrācijām X, XD, XA, XB. Brīvās enerģijs izmiņ līzsvrā veio minimumu. Ts veio Σ proukti Σ izejviels strpīu nulle 0=ΔG r+r T ln(k eq ). Tā kā Stnrt rīvās enerģijs izmiņu prēķin r negtīvu nturālo logritmu no līzsvr konstntes K eq : ΔG r= R T ln(k eq ) Brīvās enerģijs izmiņ cilvēk homeostāzē nv līzsvrā un tšķirs no nulles un koncentrāciju ttiecī c X XD XB nv konstnt rekcijā tā pēc: ΔGr=ΔG r+r T ln X c X D 0 nv nulle. XB
2 Āris Kksis Ķīmiskis potenciāls un ptvļīgie procesi homeostāze Ķīmiskis potenciāls rā kāu rīvās-gis enerģijs G A uzumu sistēmā-rekcijā ienes 1 mols pievienotās viels A. Fktiski cik uz rīvās enerģijs ir vienm 1 molm viels rekcijs misījumā. Ts prā rīvās enerģijs G A uzumu vienā 1 molā viels A, j viels uzum molu skits ir n A = 1 mol : µ A = G A n A = G A + R T ln(x A ) (1-1) ķīmiskis potenciāls vieli A, kur: G A, kj/mol Ķīmiskis stnrt potenciāls (stnrt pstākļos) T = K, spieiens p = kp; R = J/mol/K universālā gāzu konstnte; ln(x A ) - nturālis logritms no koncentrācijs X A un X A, j viels A koncentrācij molu ļās izteikt kā X A = n A /n kopīgis un pieņem vērtīs strp 0<X A 1 (nulle un tīr) viels A koncentrācij, kur n A, mol molu skits vieli A un n kopīgis, mol - kopējis molu skits visām vielām kopā ieskitot ūeni. Logritm vērtī tīri vieli ir ln(1) = 0, ks o stnrt ķīmiskā potenciāl vērtīu G A = µ A, jo X A = 1 tīrs A viels 1 mol rīvās enerģijs sturs ir G A, lietojot 1 mol viels A stnrt rīvo veiošnās enerģiju G A no elementiem. Rekcij norisinās līz glm vienīgi kmēr rekcijs gl prouktiem neros tieksme pārvērsties tpkļ rekcijs izejvielās. itiem vāriem rekcijs prouktiem ir neievērojmi niecīg vi nulles ķīmiskā potenciāl vērtī µ proukti = 0, tieksme pārvērsties tpkļ rekcijs izejvielās A : A x proukti Ķīmiskā līzsvr (equilirium) termoinmiskie noscījumi un homeostāze J rekcijs prouktiem ir vērā ņemms ķīmiskā potenciāl vērtīs, t rekcij nenorisinās turpinoties līz glm izejvielām simts procentīgi pārvēršoties prouktos, et vr novērot ķīmiskā līzsvr iestāšnos. Līzsvr stāvoklī izejvielu ķīmisko potenciālu summ kļūst vienā r prouktu ķīmisko potenciālu summu, tilstoši rekcijs ķīmiskjm vienāojumm izejviels A + B un proukti c + D: rekcij A + B pretrekcij c + D ; µ izejviels = µ proukti ; A + B = c + D, (1-2) G jo vielu koeficienti,, c, un nozīmē reizināšnu r µ. Svienojumm A A+B +D (A+A+A+ )= A=> A reizes. Svienojumi B,, un D, kā rezms equilirium līzsvr rekcijs vienāojumā, pielās rekcijā reizes, c, : (B+B+B+ )= B=> B ; (+++ )= c=>c ; (D+D+D+ )= D=> D Ķīmiskm potenciālm µ tāpt kā viels uzumm n molos ir itīvs sskitāmo īpšīs, t.i. summējs. Koncentrācij X izejvielām un prouktiem līzsvrā efinē līzsvr konstnti Keq (skt. Ķīmiskis līzsvrs). Ķīmisko potenciālu summ +D izejvielām µ izejviels un prouktiem µ proukti līzsvrā ir vienāi. Tāpēc rīvās enerģijs izmiņ rekcijā ir nulle A+B 100% 50% 0% 0% +D 100% 0= G rekc = µ proukti - µ izejviels un izskitļojmā negtīvā stnrt rīvās enerģijs izmiņ līzsvrā ir - G rekc =R T ln X c X D =R T ln(k eq ) ; K eq = X c X D XB (1-3) XB Āris Kksis Rīgs Striņ universitāte: rection G rekcij = G rekcij + R T ln X c X D XB 0 ; līzsvrā ir nulle 0 = G rekcij +R T ln(k eq ) (1-4) homeostāzē (XD X c )/(XA XB ) K eq tšķirs no līzsvr konstntes K eq = X c X D X A X B Mums precīzi jānol tšķirīs strp iviem 2 žāiem lielumiem: rīvās-enerģijs izmiņu, G un stnrt rīvās-enerģijs izmiņu G. Ktri ķīmiski rekciji ir rksturīg stnrt rīvās-enerģijs izmiņ uz vienu 1 molu izejviels, vi nu pozitīv G >0, negtīv G <0, vi žkārt nulle G =0, kur tkrīg no rekcijs līzsvr konstntes K eq lielum. Stnrt rīvās-enerģijs izmiņ G rā mums, kurā virzienā un cik tālu otā rekcij virzīsies, ssniezot līzsvru, j tempertūr ir 25 kā T o = K, 2
3 un spieiens p ir kp (1 tm) un komponentu koncentrācijs līzsvrā ir X. Tāt G ir konstnte: ti ir rksturīgi, neminīt lielumu otjā rekcijā. Bet ktuālā rīvās-enerģijs izmiņ G ir izejvielu un prouktu koncentrācijs X funkcij cilvēk ķermeņ tempertūrā T = K homeostāzes rekcijās, kur tšķirsies no stnrt pstākļiem kā efinēts iepriekš. Turklāt, ktrs ptvļīgs rekcijs G norises likā virzienā uz līzsvr stāvokli izmiņ G<0 vienmēr ir negtīv, un kļūst mzāk negtīv, j pretrekcij tsāks, ssniezot nulli G=0 līzsvr stāvoklī r konstntes (XD X c )/(XA XB ) = K eq vērtīu, uzrāot nulles ru W= - G =0, jo tiešā rekcij ssniegusi līzsvru: A + B c + D tilstoši vienāojumm G rekcij +R T ln(k eq ) = 0. Stuijs Meicīniskjā ķīmijā ; Bioķīmijā Gis rīvās enerģijs izmiņs ΔG rekc = Δ rekc T ΔS rekc Δ rekc Entlpij izklieētā enerģij T ΔS rekc >0 tiek sistīt pkārtējā viē, ir izlietot un zuētā rīvā enerģij ΔG rekc <0 1. Enotermisk Pozitīv Δ rekc >0 2. Eksotermisk Negtīv Δ rekc <0 3. Dzīvo šunu virošnās un pstāvēšns noscījums Dzīvīi Enotermisk Pozitīv Δ rekc >0 4. Eksotermisk Negtīv Δ rekc <0 ΔS rekc Entropij ΔS rekc >0 Pozitīv entropij plielinās entropijs izmiņ pozitīv Izklieētā enerģij r lielāku hosu ΔS rekc >0 Pozitīv. Ptvļīgās ktolism rekcijs Ptērē rīvo enerģiju ΔG rekc <0 zīvīs uzturēšni orgnismos 37º kā rī norošin siltumu orgnismiem kā Eksotermisk Δ rekc <0 rekcij. ΔS rekc <0 Negtīv entropij smzinās entropijs izmiņ negtīv Sintezētā rīvā enerģij ΔG rekc >0 Pozitīv uzkrājs vielā fotosintēzē, ATF sintēze, polipeptīos je olltumvielās, sintezētjās molekulās, ks norošin šūnu zīvošnu un virošnos T Tempertūr slīšnās rekcij zem T Δ rekc > -T ΔS rekc ugst T Δ rekc < -T ΔS rekc jekurā T sintēzes rekcij jekurā T ugst T Δ rekc < T ΔS rekc zem T Δ rekc > T ΔS rekc 3 ΔG rekc Brīvā enerģij AB A + B veiojs lielāks hoss Pozitīv ΔG rekc >0 Δ rekc T ΔS rekc >0 Negtīv ΔG rekc <0 Δ rekc T ΔS rekc <0 Negtīv ΔG rekc <0 Δ rekc T ΔS rekc <0 A + B AB orgnizējs lielāk skārtotī Pozitīv ΔG rekc >0 Δ rekc T ΔS rekc >0 Pozitīv ΔG rekc >0 Δ rekc T ΔS rekc >0 Negtīv ΔG rekc <0 Δ rekc T ΔS rekc <0 Rekcijs ptvļīgums Ptvļīgjās ioķīmiskjās ktolism rekcijās ptērētā rīvā enerģij ΔG rekc <0 uztur zīvīs procesus orgnismos omeostāzē neptvļīg rekcij zemā tempertūrā ptvļīg rekcij ugstā tempertūrā termoinmiski ptvļīg rekcij jekurā tempertūrā Bioķīmiskjās nolism rekcijās enerģij kumulējs un orgnizējs sintezētjās vielās lielākā kārtīā, jo smzin hos mēru entropiju ΔS rekc <0 Negtīv neptvļīg rekcij termoinmiski izliegt jekurā tempertūrā neptvļīg rekcij ugstā tempertūrā ptvļīg rekcij zemā tempertūrā
4 Dzīvjā ā šūnā sintezējmjās vielās ir ļoti nozīmīg rīvās enerģijs uzkrāšn, plielinot ΔG rekc >0! Rekcijā negtīv izmiņ ΔS rekc <0 entropijā un pozitīv izmiņ ΔG rekc >0 rīvā enerģijā smzin izklieēto enerģiju TΔS un plielin kumulēto pievīto +Q enerģiju, uzkrājot mkroerģisko sišu veiā kā rīvo enerģiju ΔG rekc >0. Δ rekc = ΔG rekc + T ΔS rekc. Pretēji kā ptvļīgjā rekcijā ΔG rec <0 negtīv rīvās enerģijs izmiņ ir izklieētā (zuētā) enerģij. Āris Kksis Rīg Striņ universitāte 4. lps puse Bioķīmisko rekciju piemēri stuentu Meicīniskās ķīmijs stuijām pr omeostāzi 1. Glikozes un skāekļ zļo ugu fotosintēze ilvēk omeostāze srknās un zilās gisms fotonu sorētā enerģij E=hν siltums kumulējs glikozes vielā Δ rec >0= -Q Enotermiski Δ rec == +2805,27 kj / mol Q + G r fotosintēze ΔG r >0 ir Enoerģisks G r =+3040 kj/mol rīvā enerģij kumulējs 1 molā citosol glikozes molekulās ioķīmiski glikolīzē un Kres ciklā seg r skāekli 2 oksitīvās fosforilēšnās pārvērtīu ceļos mitohonrijās. tiešā rekcij E=h FR srkn gism zil foto sinteze segsn pretrekcij Glikolīze; ksitīvā fosforilēšn Enzīms FotoSintetiskis Rekcijs entrs glikoze+skāeklis ioķīmiskā segšn Kres cikls mitohonrijās Memrāns potenciāls 3. Lps puse (lps puse ATPāzes virzīt ATF sintēze (ATF enozīn trifos Vien glikozes molekul proucē glikolītiski un mitohonrijās. Memrānā ieūvētā enzīm ATPāzes nno zinējā līzīgi kā spēkstcijā protonu grient virzītā rekcijā ros kopā 36 ATF molekuls, kumulējoties rīvi enerģiji ΔG rec =+30.5kJ/mol vienā molā ATP 4- molekulu ADP P 4 - fāts ATP 4- njons p=7,36 mitohonrijā) [+] 2290 Protonu grients 1 [+] [+]=10-5 mol/litrs [+]= mol/l p=5 4 + ATPse 4 + p=7.36 telp strpmemrnu mitohonrij ATP Enzīmu kompleks kofktors riosomās ATP 4-3. ir rīvās enerģijs ATP 4- pārnešn un uzkrāšn ΔG rec =+17.2 kj/mol peptīu sitē veiojoties olltumvieli riosomās: l + gly l-gly+ 2. Vienā molā peptīu sites uzkrājs rīvā enerģij ΔG rec =+17.2 kj/mol. Riosom ssist peptīu sintēzi r ATF hirolīzi: rīvā enerģij ΔG hyrilize = kj/mol tļuj pārnest un.. uzkrāt ΔG rec =+17.2 kj/mol rīvo Al [A] Gly [G] enerģiju rekcijā uz vienu molu Alnīns Glicīns 4- Riosom peptīu sišu ATP 3 A DP P 4 - N + 3 N + + pepti u sit es sinteze ATF hirolīze ir ptvļīg ΔG =-30.5kJ/mol un summārā rekcij rī kopumā ir ptvļīg, jo summā ΔG rec <0 negtīv ΔG rec = = kj/mol 3 N + N AlninGlicīns Al-Gly AG 4
5 Sintēzes un ekompozīcijs rekcijs četri veii ioķīmijā Sintēzes un ekompozīcijs: hirolīzes, io oksiēšns rekcijs 1. EKSTERMISKA, EKSERĢISKA SADALĪŠANAS REAKIJA BIKSIDĒŠANA un IDRLĪZE 3. un 4. lp: ksioreuktāzes E.1 klses enzīmi, piemērm, oksitīv fosforilēšn: qu => Q + G rekc ΔG rekc = kj / mol ; Δ rekc = kj / mol 2. un 3. lp : E.2 klses hirolāzes enzīmi gremošn, polimēru egrēšn peptiāzes : glicil-glicīns + 2 peptise => glicīns + glicīns + Q + ΔG rekc ΔG rekc = kj / mol ; Δ rekc = kj / mol Rekciju vispārīgā veiā vr uzrkstīt kā: AB => A + B, Δ<0 un ΔS>0 ΔG = Δ - T ΔS < 0, vr rezēt, k pirmā komponente Δ ir negtīv. ΔS ir pozitīvs, et r mīnus zīmi pirms sskitāmā, otrā komponente - T ΔS rī ir negtīv. Ts nozīmē, k ΔG vienmēr ir negtīvs šī vei rekcijās. Secinājums: eksotermisk slīšnās rekcij ir ptvļīg jekuros pstākļos.. 2. EKSTERMISKA SINTĒZES REAKIJA Eksotermisku sintēzes rekciju vispārīgā veiā vr uzrkstīt kā: A + B => AB, Δ<0 un ΔS<0 ΔG = Δ - T ΔS. Pirmā komponente Δ izteiksmē ir negtīv, et otrā ir pozitīv (ΔS ir negtīvs, et r mīnus zīmi). Tā kā vien komponente ir pozitīv, et otrs negtīvs, rezultāts ΔG ir negtīvs, j negtīvā komponent Δ solūtā vērtī ir lielāks pr pozitīvo komponentu (-TΔS): Δ > T ΔS Ts ir iespējms, j tempertūr ir pietiekoši zem kā cilvēk ķermeņ tempertūrā 310,15 K. Secinājums: sintēzes eksotermisk rekcij ir ptvļīg pietiekmi zemās tempertūrās. 3. ENDTERMISKA, EKSERĢISKA SADALĪŠANĀS REAKIJA Enotermisks slīšnās rekcijs piemērs vispārīgā formā ir : AB => A + B Δ>0 un ΔS>0 ΔG = Δ - T ΔS Pirmā komponente Δ izteiksmē ir pozitīv, et otrā -T ΔS negtīv, jo entropij ir pozitīv, et mīnus zīme izteiksmē pārvērš otro komponenti izteiksmē pr negtīvu. Gis enerģijs izmiņ ΔG vr ūt negtīv (un rekcij vr ūt ptvļīg), j negtīvā komponente ir lielāk pr pozitīvo : T ΔS > Δ Enotermisk ekompozīcijs rekcij ir ptvļīg pietiekoši ugstās tempertūrās. 5
6 4. ENDTERMISKA, ENDERĢISKA SINTĒZES REAKIJA ksioreuktāzes E.1 klses enzīmi, piemērm, fotosintēzē: ΔG rekc = kj / mol ; Δ rekc = kj / mol Q + G rekc => qu lp: lltumvielu peptīu sites sintēzē hirolāzes klses E.2 enzīmi šūnu riosomās: glicīns + glicīns + Q + ΔG rekc => glicil-glicīns + 2 ; ΔG rekc = kj / mol, Δ=60.58 kj / mol 4. lp : Rekciju vispārīgā veiā vr uzrkstīt kā: A + B => AB Δ>0 un ΔS<0 As komponentes ΔG izteiksmē ir pozitīvs tā pēc summ ΔG ir pozitīv jekurā tempertūrā. Šī tip rekcijs nenotiek ptvļīgi - citiem vāriem, Enotermisk, enoerģisk sintēzes rekcij ir termoinmiski izliegt ΔG>0. Piezīme: 1, 4 un 2, 3 ir pretrekcijs. Ppilus ivi secinājumi: 1) J tiešā rekcij ir ptvļīg, t pretrekcij ir termoinmiski izliegt.(1, 4 rekcijs ) 2) J tiešā rekcij ir ptvļīg pie ugstām tempertūrām, pretrekcij ir ptvļīg pie zemām tempertūrām.(2, 3 rekcijs ) 6
rs r r â t át r st tíst Ó P ã t r r r â
 rs r r â t át r st tíst P Ó P ã t r r r â ã t r r P Ó P r sã rs r s t à r çã rs r st tíst r q s t r r t çã r r st tíst r t r ú r s r ú r â rs r r â t át r çã rs r st tíst 1 r r 1 ss rt q çã st tr sã
rs r r â t át r st tíst P Ó P ã t r r r â ã t r r P Ó P r sã rs r s t à r çã rs r st tíst r q s t r r t çã r r st tíst r t r ú r s r ú r â rs r r â t át r çã rs r st tíst 1 r r 1 ss rt q çã st tr sã
Παρασκευή 1 Νοεμβρίου 2013 Ασκηση 1. Λύση. Παρατήρηση. Ασκηση 2. Λύση.
 (, ) =,, = : = = ( ) = = = ( ) = = = ( ) ( ) = = ( ) = = = = (, ) =, = = =,,...,, N, (... ) ( + ) =,, ( + ) (... ) =,. ( ) = ( ) = (, ) = = { } = { } = ( ) = \ = { = } = { = }. \ = \ \ \ \ \ = = = = R
(, ) =,, = : = = ( ) = = = ( ) = = = ( ) ( ) = = ( ) = = = = (, ) =, = = =,,...,, N, (... ) ( + ) =,, ( + ) (... ) =,. ( ) = ( ) = (, ) = = { } = { } = ( ) = \ = { = } = { = }. \ = \ \ \ \ \ = = = = R
M.Jansone, J.Blūms Uzdevumi fizikā sagatavošanas kursiem
 DINAMIKA. Dinmik prkst pātrinājum ršnās cēloħus un plūko tā lielum un virzien noteikšns pħēmienus. Spēks (N) ir vektoriāls lielums; ts ir ėermeħu vi to dĝiħu mijiedrbībs mērs. Inerce ir ėermeħu īpšīb sglbāt
DINAMIKA. Dinmik prkst pātrinājum ršnās cēloħus un plūko tā lielum un virzien noteikšns pħēmienus. Spēks (N) ir vektoriāls lielums; ts ir ėermeħu vi to dĝiħu mijiedrbībs mērs. Inerce ir ėermeħu īpšīb sglbāt
THERMODYNAMICS Exercise 1 6CO 2 gas photosynthesis to 6O 2aqua and C 6 H 12 O 6
 TERMDYNAMIS Exercise 1 6 2 gas photosynthesis to 6 2aqua and 6 12 6 alculate Δ r, ΔS r, ΔG r at standard conditions 298.15 K. Reaction is exothermic, athermic, endothermic? 2 gas assimilation reaction
TERMDYNAMIS Exercise 1 6 2 gas photosynthesis to 6 2aqua and 6 12 6 alculate Δ r, ΔS r, ΔG r at standard conditions 298.15 K. Reaction is exothermic, athermic, endothermic? 2 gas assimilation reaction
P P Ó P. r r t r r r s 1. r r ó t t ó rr r rr r rí st s t s. Pr s t P r s rr. r t r s s s é 3 ñ
 P P Ó P r r t r r r s 1 r r ó t t ó rr r rr r rí st s t s Pr s t P r s rr r t r s s s é 3 ñ í sé 3 ñ 3 é1 r P P Ó P str r r r t é t r r r s 1 t r P r s rr 1 1 s t r r ó s r s st rr t s r t s rr s r q s
P P Ó P r r t r r r s 1 r r ó t t ó rr r rr r rí st s t s Pr s t P r s rr r t r s s s é 3 ñ í sé 3 ñ 3 é1 r P P Ó P str r r r t é t r r r s 1 t r P r s rr 1 1 s t r r ó s r s st rr t s r t s rr s r q s
ss rt çã r s t Pr r Pós r çã ê t çã st t t ê s 1 t s r s r s r s r q s t r r t çã r str ê t çã r t r r r t r s
 P P P P ss rt çã r s t Pr r Pós r çã ê t çã st t t ê s 1 t s r s r s r s r q s t r r t çã r str ê t çã r t r r r t r s r t r 3 2 r r r 3 t r ér t r s s r t s r s r s ér t r r t t q s t s sã s s s ér t
P P P P ss rt çã r s t Pr r Pós r çã ê t çã st t t ê s 1 t s r s r s r s r q s t r r t çã r str ê t çã r t r r r t r s r t r 3 2 r r r 3 t r ér t r s s r t s r s r s ér t r r t t q s t s sã s s s ér t
Alterazioni del sistema cardiovascolare nel volo spaziale
 POLITECNICO DI TORINO Corso di Laurea in Ingegneria Aerospaziale Alterazioni del sistema cardiovascolare nel volo spaziale Relatore Ing. Stefania Scarsoglio Studente Marco Enea Anno accademico 2015 2016
POLITECNICO DI TORINO Corso di Laurea in Ingegneria Aerospaziale Alterazioni del sistema cardiovascolare nel volo spaziale Relatore Ing. Stefania Scarsoglio Studente Marco Enea Anno accademico 2015 2016
r r t r r t t r t P s r t r P s r s r r rs tr t r r t s ss r P s s t r t t tr r r t t r t r r t t s r t rr t Ü rs t 3 r r r 3 rträ 3 röÿ r t
 r t t r t ts r3 s r r t r r t t r t P s r t r P s r s r P s r 1 s r rs tr t r r t s ss r P s s t r t t tr r 2s s r t t r t r r t t s r t rr t Ü rs t 3 r t r 3 s3 Ü rs t 3 r r r 3 rträ 3 röÿ r t r r r rs
r t t r t ts r3 s r r t r r t t r t P s r t r P s r s r P s r 1 s r rs tr t r r t s ss r P s s t r t t tr r 2s s r t t r t r r t t s r t rr t Ü rs t 3 r t r 3 s3 Ü rs t 3 r r r 3 rträ 3 röÿ r t r r r rs
β) ψ τάξης ως προς Β,
 3.3 Νο μος ταχυ τητας - Μηχανισμο ς αντι δρασης αντιδράσεις ονοµάζονται απλές ή στοιχειώδεις; αντιδράσεις ονοµάζονται πολύπλοκες; Τι ονοµάζεται νόµος ταχύτητας µιας χηµικής Πως προσδιορίζεται ο νόµος της
3.3 Νο μος ταχυ τητας - Μηχανισμο ς αντι δρασης αντιδράσεις ονοµάζονται απλές ή στοιχειώδεις; αντιδράσεις ονοµάζονται πολύπλοκες; Τι ονοµάζεται νόµος ταχύτητας µιας χηµικής Πως προσδιορίζεται ο νόµος της
Assessment of otoacoustic emission probe fit at the workfloor
 Assessment of otoacoustic emission probe fit at the workfloor t s st tt r st s s r r t rs t2 t P t rs str t t r 1 t s ér r tr st tr r2 t r r t s t t t r t s r ss r rr t 2 s r r 1 s r r t s s s r t s t
Assessment of otoacoustic emission probe fit at the workfloor t s st tt r st s s r r t rs t2 t P t rs str t t r 1 t s ér r tr st tr r2 t r r t s t t t r t s r ss r rr t 2 s r r 1 s r r t s s s r t s t
ss rt çã r s t à rs r ç s rt s 1 ê s Pr r Pós r çã ís r t çã tít st r t
 ss rt çã r s t à rs r ç s rt s 1 ê s Pr r Pós r çã ís r t çã tít st r t FichaCatalografica :: Fichacatalografica https://www3.dti.ufv.br/bbt/ficha/cadastrarficha/visua... Ficha catalográfica preparada
ss rt çã r s t à rs r ç s rt s 1 ê s Pr r Pós r çã ís r t çã tít st r t FichaCatalografica :: Fichacatalografica https://www3.dti.ufv.br/bbt/ficha/cadastrarficha/visua... Ficha catalográfica preparada
2ο Σύνολο Ασκήσεων. Λύσεις 6C + 7H 2 C 6 H H διαφορά στο θερμικό περιεχόμενο των προϊόντων και των αντιδρώντων καλείται
 1 2ο Σύνολο Ασκήσεων Λύσεις Άσκηση 1: 6C + 7H 2 C 6 H 14 H1 6C + 7H 2 ΔΗ αντίδρασης H2 C 6 + H 14 C + H 2 H αντίδραση είναι εξώθερμη Άσκηση 2 - H διαφορά στο θερμικό περιεχόμενο των προϊόντων και των αντιδρώντων
1 2ο Σύνολο Ασκήσεων Λύσεις Άσκηση 1: 6C + 7H 2 C 6 H 14 H1 6C + 7H 2 ΔΗ αντίδρασης H2 C 6 + H 14 C + H 2 H αντίδραση είναι εξώθερμη Άσκηση 2 - H διαφορά στο θερμικό περιεχόμενο των προϊόντων και των αντιδρώντων
r t t r t t à ré ér t é r t st é é t r s s2stè s t rs ts t s
 r t r r é té tr q tr t q t t q t r t t rrêté stér ût Prés té r ré ér ès r é r r st P t ré r t érô t 2r ré ré s r t r tr q t s s r t t s t r tr q tr t q t t q t r t t r t t r t t à ré ér t é r t st é é
r t r r é té tr q tr t q t t q t r t t rrêté stér ût Prés té r ré ér ès r é r r st P t ré r t érô t 2r ré ré s r t r tr q t s s r t t s t r tr q tr t q t t q t r t t r t t r t t à ré ér t é r t st é é
Rīgas Tehniskā universitāte. Inženiermatemātikas katedra. Uzdevumu risinājumu paraugi. 4. nodarbība
 Rīgas Tehniskā univesitāte Inženiematemātikas kateda Uzdevumu isinājumu paaugi 4 nodabība piemēs pēķināt vektoa a gaumu un viziena kosinusus, ja a = 5 i 6 j + 5k Vektoa a koodinātas i dotas: a 5 ; a =
Rīgas Tehniskā univesitāte Inženiematemātikas kateda Uzdevumu isinājumu paaugi 4 nodabība piemēs pēķināt vektoa a gaumu un viziena kosinusus, ja a = 5 i 6 j + 5k Vektoa a koodinātas i dotas: a 5 ; a =
Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design
 Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
ο ο 3 α. 3"* > ω > d καΐ 'Ενορία όλις ή Χώρί ^ 3 < KN < ^ < 13 > ο_ Μ ^~~ > > > > > Ο to X Η > ο_ ο Ο,2 Σχέδι Γλεγμα Ο Σ Ο Ζ < o w *< Χ χ Χ Χ < < < Ο
 18 ρ * -sf. NO 1 D... 1: - ( ΰ ΐ - ι- *- 2 - UN _ ί=. r t ' \0 y «. _,2. "* co Ι». =; F S " 5 D 0 g H ', ( co* 5. «ΰ ' δ". o θ * * "ΰ 2 Ι o * "- 1 W co o -o1= to»g ι. *ΰ * Ε fc ΰ Ι.. L j to. Ι Q_ " 'T
18 ρ * -sf. NO 1 D... 1: - ( ΰ ΐ - ι- *- 2 - UN _ ί=. r t ' \0 y «. _,2. "* co Ι». =; F S " 5 D 0 g H ', ( co* 5. «ΰ ' δ". o θ * * "ΰ 2 Ι o * "- 1 W co o -o1= to»g ι. *ΰ * Ε fc ΰ Ι.. L j to. Ι Q_ " 'T
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Το άτομο του Υδρογόνου
 Το άτομο του Υδρογόνου Δυναμικό Coulomb Εξίσωση Schrödinger h e (, r, ) (, r, ) E (, r, ) m ψ θφ r ψ θφ = ψ θφ Συνθήκες ψ(, r θφ, ) = πεπερασμένη ψ( r ) = 0 ψ(, r θφ, ) =ψ(, r θφ+, ) π Επιτρεπτές ενέργειες
Το άτομο του Υδρογόνου Δυναμικό Coulomb Εξίσωση Schrödinger h e (, r, ) (, r, ) E (, r, ) m ψ θφ r ψ θφ = ψ θφ Συνθήκες ψ(, r θφ, ) = πεπερασμένη ψ( r ) = 0 ψ(, r θφ, ) =ψ(, r θφ+, ) π Επιτρεπτές ενέργειες
ΓΗ ΚΑΙ ΣΥΜΠΑΝ. Εικόνα 1. Φωτογραφία του γαλαξία μας (από αρχείο της NASA)
 ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
P r s r r t. tr t. r P
 P r s r r t tr t r P r t s rés t t rs s r s r r t é ér s r q s t r r r r t str t q q s r s P rs t s r st r q r P P r s r r t t s rés t t r t s rés t t é ér s r q s t r r r r t r st r q rs s r s r r t str
P r s r r t tr t r P r t s rés t t rs s r s r r t é ér s r q s t r r r r t str t q q s r s P rs t s r st r q r P P r s r r t t s rés t t r t s rés t t é ér s r q s t r r r r t r st r q rs s r s r r t str
Jeux d inondation dans les graphes
 Jeux d inondation dans les graphes Aurélie Lagoutte To cite this version: Aurélie Lagoutte. Jeux d inondation dans les graphes. 2010. HAL Id: hal-00509488 https://hal.archives-ouvertes.fr/hal-00509488
Jeux d inondation dans les graphes Aurélie Lagoutte To cite this version: Aurélie Lagoutte. Jeux d inondation dans les graphes. 2010. HAL Id: hal-00509488 https://hal.archives-ouvertes.fr/hal-00509488
Q π (/) ^ ^ ^ Η φ. <f) c>o. ^ ο. ö ê ω Q. Ο. o 'c. _o _) o U 03. ,,, ω ^ ^ -g'^ ο 0) f ο. Ε. ιη ο Φ. ο 0) κ. ο 03.,Ο. g 2< οο"" ο φ.
 II 4»» «i p û»7'' s V -Ζ G -7 y 1 X s? ' (/) Ζ L. - =! i- Ζ ) Η f) " i L. Û - 1 1 Ι û ( - " - ' t - ' t/î " ι-8. Ι -. : wî ' j 1 Τ J en " il-' - - ö ê., t= ' -; '9 ',,, ) Τ '.,/,. - ϊζ L - (- - s.1 ai
II 4»» «i p û»7'' s V -Ζ G -7 y 1 X s? ' (/) Ζ L. - =! i- Ζ ) Η f) " i L. Û - 1 1 Ι û ( - " - ' t - ' t/î " ι-8. Ι -. : wî ' j 1 Τ J en " il-' - - ö ê., t= ' -; '9 ',,, ) Τ '.,/,. - ϊζ L - (- - s.1 ai
Εντροπία Ελεύθερη Ενέργεια
 Μάθημα Εντροπία Ελεύθερη Ενέργεια Εξαγωγική Μεταλλουργία Καθ. Ι. Πασπαλιάρης Εργαστήριο Μεταλλουργίας ΕΜΠ Αυθόρμητες χημικές αντιδράσεις Ηαντίδρασηοξείδωσηςενόςμετάλλουμπορείναγραφτείστη γενική της μορφή
Μάθημα Εντροπία Ελεύθερη Ενέργεια Εξαγωγική Μεταλλουργία Καθ. Ι. Πασπαλιάρης Εργαστήριο Μεταλλουργίας ΕΜΠ Αυθόρμητες χημικές αντιδράσεις Ηαντίδρασηοξείδωσηςενόςμετάλλουμπορείναγραφτείστη γενική της μορφή
Errata Sheet. 2 k. r 2. ts t. t t ... cos n W. cos nx W. W n x. Page Location Error Correction 2 Eq. (1.3) q dt. W/m K. 100 Last but 6 2.
 Eaa S Pag can E Ccn Eq. (. q q k W/ K k W/ K A A 6 n as bu 6 s q lns s q T k T k Q.. Wall s aus n gvn Wall s aus a an C. 7 n, lf kc cs ( s sn kc cs ( s sn s f cs k sn cs k sn quan C ( s C ( s an ln 6 sn
Eaa S Pag can E Ccn Eq. (. q q k W/ K k W/ K A A 6 n as bu 6 s q lns s q T k T k Q.. Wall s aus n gvn Wall s aus a an C. 7 n, lf kc cs ( s sn kc cs ( s sn s f cs k sn cs k sn quan C ( s C ( s an ln 6 sn
HONDA. Έτος κατασκευής
 Accord + Coupe IV 2.0 16V (CB3) F20A2-A3 81 110 01/90-09/93 0800-0175 11,00 2.0 16V (CB3) F20A6 66 90 01/90-09/93 0800-0175 11,00 2.0i 16V (CB3-CC9) F20A8 98 133 01/90-09/93 0802-9205M 237,40 2.0i 16V
Accord + Coupe IV 2.0 16V (CB3) F20A2-A3 81 110 01/90-09/93 0800-0175 11,00 2.0 16V (CB3) F20A6 66 90 01/90-09/93 0800-0175 11,00 2.0i 16V (CB3-CC9) F20A8 98 133 01/90-09/93 0802-9205M 237,40 2.0i 16V
ΔΗΜΟΤΙΚΕΣ ΕΚΛΟΓΕΣ 18/5/2014 ΑΚΥΡΑ
 ΔΗΜΟΤΙΚΕΣ ΕΚΛΟΓΕΣ 18/5/2014 ΑΚΥΡΑ ΑΔΑΜΗΣ Δ.Κ. / Τ.Κ. E.T. ΕΓΓ/ΝΟΙ ΨΗΦΙΣΑΝ ΕΓΚΥΡΑ ΓΙΟΒΑΣ ΙΩΑΝΝΗΣ ΛΕΥΚΑ ΠΑΝΑΓΙΩΤΗΣ ΜΑΝΤΑΣ ΠΑΝΑΓΙΩΤΗΣ ΔΑΛΙΑΝΗΣ ΓΕΩΡΓΙΟΣ ΑΣΤΡΟΣ 5 2.728 1.860 36 1.825 69 3,8% 152 8,3% 739 40,5%
ΔΗΜΟΤΙΚΕΣ ΕΚΛΟΓΕΣ 18/5/2014 ΑΚΥΡΑ ΑΔΑΜΗΣ Δ.Κ. / Τ.Κ. E.T. ΕΓΓ/ΝΟΙ ΨΗΦΙΣΑΝ ΕΓΚΥΡΑ ΓΙΟΒΑΣ ΙΩΑΝΝΗΣ ΛΕΥΚΑ ΠΑΝΑΓΙΩΤΗΣ ΜΑΝΤΑΣ ΠΑΝΑΓΙΩΤΗΣ ΔΑΛΙΑΝΗΣ ΓΕΩΡΓΙΟΣ ΑΣΤΡΟΣ 5 2.728 1.860 36 1.825 69 3,8% 152 8,3% 739 40,5%
P P Ô. ss rt çã r s t à rs r ç s rt s 1 ê s Pr r Pós r çã ís r t çã tít st r t
 P P Ô P ss rt çã r s t à rs r ç s rt s 1 ê s Pr r Pós r çã ís r t çã tít st r t FELIPE ANDRADE APOLÔNIO UM MODELO PARA DEFEITOS ESTRUTURAIS EM NANOMAGNETOS Dissertação apresentada à Universidade Federal
P P Ô P ss rt çã r s t à rs r ç s rt s 1 ê s Pr r Pós r çã ís r t çã tít st r t FELIPE ANDRADE APOLÔNIO UM MODELO PARA DEFEITOS ESTRUTURAIS EM NANOMAGNETOS Dissertação apresentada à Universidade Federal
ΝΟΜΟΣ ΤΗΣ ΠΕΡΙΟ ΙΚΟΤΗΤΑΣ : Οι ιδιότητες των χηµικών στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
,
 ... 7 1.,... 8 1.1... 8 1.2... 10 1.3-4... 12 1.4,... 13 1.5,... 14 1.6... 14 2... 16 2.1... 16 2.2... 18 2.3... 23 2.4... 24 2.5... 24 2.6... 27 2.7... 29 2.8... 32 2.9... 34 2.10... 40 2.11... 40 2.12...
... 7 1.,... 8 1.1... 8 1.2... 10 1.3-4... 12 1.4,... 13 1.5,... 14 1.6... 14 2... 16 2.1... 16 2.2... 18 2.3... 23 2.4... 24 2.5... 24 2.6... 27 2.7... 29 2.8... 32 2.9... 34 2.10... 40 2.11... 40 2.12...
Υπολογιστικές Μέθοδοι Ανάλυσης και Σχεδιασμού
 EΘNIKO ΜEΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Ανάλυσης, Σχεδιασμού & Ανάπτυξης Διεργασιών & Συστημάτων Υπολογιστικές Μέθοδοι Ανάλυσης και Σχεδιασμού Εργαστηριακές Ασκήσεις Διδάσκων: Α.
EΘNIKO ΜEΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Ανάλυσης, Σχεδιασμού & Ανάπτυξης Διεργασιών & Συστημάτων Υπολογιστικές Μέθοδοι Ανάλυσης και Σχεδιασμού Εργαστηριακές Ασκήσεις Διδάσκων: Α.
!"#$ "%&$ ##%&%'()) *..$ /. 0-1$ )$.'-
 !!" !"# "%& ##%&%',-... /. -1.'- -13-',,'- '-...4 %. -5"'-1.... /..'-1.....-"..'-1.. 78::8
!!" !"# "%& ##%&%',-... /. -1.'- -13-',,'- '-...4 %. -5"'-1.... /..'-1.....-"..'-1.. 78::8
1857 Κ.Δ.Π. 312/9& ; Αριθμός 312 Ο ΠΕΡΙ ΠΟΛΕΟΔΟΜΙΑΣ ΚΑΙ ΧΩΡΟΤΑΞΙΑΣ ΝΟΜΟΣ (ΝΟΜΟΙ 90 ΤΟΥ 1972 ΚΑΙ 56 ΤΟΥ 1982)
 Ε.Ε. Πα. I(I) Α. 292, 1.12.98 1857.Δ.Π. 12/9& ; Αιθμός 12 ΠΕΙ ΠΛΕΔΜΙΑΣ ΑΙ ΩΤΑΞΙΑΣ ΝΜΣ (ΝΜΙ 90 ΤΥ 1972 ΑΙ 56 ΤΥ 1982) Διάταγμα Διατήησης σύμφνα με τ άθ 8(1) Ασκώντας τις εξυσίες πυ ηγύνται σ' αυτόν από
Ε.Ε. Πα. I(I) Α. 292, 1.12.98 1857.Δ.Π. 12/9& ; Αιθμός 12 ΠΕΙ ΠΛΕΔΜΙΑΣ ΑΙ ΩΤΑΞΙΑΣ ΝΜΣ (ΝΜΙ 90 ΤΥ 1972 ΑΙ 56 ΤΥ 1982) Διάταγμα Διατήησης σύμφνα με τ άθ 8(1) Ασκώντας τις εξυσίες πυ ηγύνται σ' αυτόν από
Compress 6000 LW Bosch Compress LW C 35 C A ++ A + A B C D E F G. db kw kw /2013
 Ι 55 C 35 C A A B C D E F G 47 17 21 18 19 19 18 db kw kw db 2015 811/2013 Ι A A B C D E F G 2015 811/2013 Izstrādājuma datu lapa par energopatēriņu Turpmākie izstrādājuma dati atbilst ES regulu 811/2013,
Ι 55 C 35 C A A B C D E F G 47 17 21 18 19 19 18 db kw kw db 2015 811/2013 Ι A A B C D E F G 2015 811/2013 Izstrādājuma datu lapa par energopatēriņu Turpmākie izstrādājuma dati atbilst ES regulu 811/2013,
Radio détection des rayons cosmiques d ultra-haute énergie : mise en oeuvre et analyse des données d un réseau de stations autonomes.
 Radio détection des rayons cosmiques d ultra-haute énergie : mise en oeuvre et analyse des données d un réseau de stations autonomes. Diego Torres Machado To cite this version: Diego Torres Machado. Radio
Radio détection des rayons cosmiques d ultra-haute énergie : mise en oeuvre et analyse des données d un réseau de stations autonomes. Diego Torres Machado To cite this version: Diego Torres Machado. Radio
ο3 3 gs ftffg «5.s LS ό b a. L Μ κ5 =5 5 to w *! .., TJ ο C5 κ .2 '! "c? to C φ io -Ρ (Μ 3 Β Φ Ι <^ ϊ bcp Γί~ eg «to ιο pq ΛΛ g Ό & > I " CD β U3
 I co f - bu. EH T ft Wj. ta -p -Ρ - a &.So f I P ω s Q. ( *! C5 κ u > u.., TJ C φ Γί~ eg «62 gs ftffg «5.s LS ό b a. L κ5 =5 5 W.2 '! "c? io -Ρ ( Β Φ Ι < ϊ bcp «δ ι pq ΛΛ g Ό & > I " CD β U (Ν φ ra., r
I co f - bu. EH T ft Wj. ta -p -Ρ - a &.So f I P ω s Q. ( *! C5 κ u > u.., TJ C φ Γί~ eg «62 gs ftffg «5.s LS ό b a. L κ5 =5 5 W.2 '! "c? io -Ρ ( Β Φ Ι < ϊ bcp «δ ι pq ΛΛ g Ό & > I " CD β U (Ν φ ra., r
ITU-R SF ITU-R SF ( ) GHz 14,5-14,0 1,2.902 (WRC-03) 4.4. MHz GHz 14,5-14 ITU-R SF.1585 ( " " .ITU-R SF.
 1 (008-003) * (ITU-R 54/4 ITU-R 6/9 ). 1. 4. 3. GHz 14,5-14,0 1,.90 (WRC-03) ( 4.4 ( - ) MHz 6 45-5 95 GHz 14,5-14 ( 4.4 " " ( ( ( ( ITU-R SF.1585 ( ( (ATPC) ( (.ITU-R SF.1650-1 " " * ITU-R SM.1448 / (
1 (008-003) * (ITU-R 54/4 ITU-R 6/9 ). 1. 4. 3. GHz 14,5-14,0 1,.90 (WRC-03) ( 4.4 ( - ) MHz 6 45-5 95 GHz 14,5-14 ( 4.4 " " ( ( ( ( ITU-R SF.1585 ( ( (ATPC) ( (.ITU-R SF.1650-1 " " * ITU-R SM.1448 / (
P t s st t t t t2 t s st t t rt t t tt s t t ä ör tt r t r 2ö r t ts t t t t t t st t t t s r s s s t är ä t t t 2ö r t ts rt t t 2 r äärä t r s Pr r
 r s s s t t P t s st t t t t2 t s st t t rt t t tt s t t ä ör tt r t r 2ö r t ts t t t t t t st t t t s r s s s t är ä t t t 2ö r t ts rt t t 2 r äärä t r s Pr r t t s st ä r t str t st t tt2 t s s t st
r s s s t t P t s st t t t t2 t s st t t rt t t tt s t t ä ör tt r t r 2ö r t ts t t t t t t st t t t s r s s s t är ä t t t 2ö r t ts rt t t 2 r äärä t r s Pr r t t s st ä r t str t st t tt2 t s s t st
van der Waals Ν Bohr Ν
 Ν ( )Ν φ ) ( Ν van der Waals Ν Ν Χ Χ Θ Θ Ν ) ( ( ) ( Ν ( ( Bohr Ν ΝΆ (, )Ν Ν,, ) ) Ν ) Ν 1. Γ /,,,. φ. m, Ό V, P, Θ PV=nRT Van der Waals (P+n2a/V2)(V-nb)=nRT = b= : T Ω Γ φ ( Φ 24/10/2012, ) 11.00-13.00
Ν ( )Ν φ ) ( Ν van der Waals Ν Ν Χ Χ Θ Θ Ν ) ( ( ) ( Ν ( ( Bohr Ν ΝΆ (, )Ν Ν,, ) ) Ν ) Ν 1. Γ /,,,. φ. m, Ό V, P, Θ PV=nRT Van der Waals (P+n2a/V2)(V-nb)=nRT = b= : T Ω Γ φ ( Φ 24/10/2012, ) 11.00-13.00
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ
 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
Ax = b. 7x = 21. x = 21 7 = 3.
 3 s st 3 r 3 t r 3 3 t s st t 3t s 3 3 r 3 3 st t t r 3 s t t r r r t st t rr 3t r t 3 3 rt3 3 t 3 3 r st 3 t 3 tr 3 r t3 t 3 s st t Ax = b. s t 3 t 3 3 r r t n r A tr 3 rr t 3 t n ts b 3 t t r r t x 3
3 s st 3 r 3 t r 3 3 t s st t 3t s 3 3 r 3 3 st t t r 3 s t t r r r t st t rr 3t r t 3 3 rt3 3 t 3 3 r st 3 t 3 tr 3 r t3 t 3 s st t Ax = b. s t 3 t 3 3 r r t n r A tr 3 rr t 3 t n ts b 3 t t r r t x 3
Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ. Παππάς Χρήστος Επίκουρος Καθηγητής
 ΗΛΕΚΤΡΟΝΙΚΗ ΟΜΗ ΚΑΙ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ Παππάς Χρήστος Επίκουρος Καθηγητής ΤΟ ΜΕΓΕΘΟΣ ΤΩΝ ΑΤΟΜΩΝ Ατομική ακτίνα (r) : ½ της απόστασης μεταξύ δύο ομοιοπυρηνικών ατόμων, ενωμένων με απλό ομοιοπολικό δεσμό.
ΗΛΕΚΤΡΟΝΙΚΗ ΟΜΗ ΚΑΙ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ Παππάς Χρήστος Επίκουρος Καθηγητής ΤΟ ΜΕΓΕΘΟΣ ΤΩΝ ΑΤΟΜΩΝ Ατομική ακτίνα (r) : ½ της απόστασης μεταξύ δύο ομοιοπυρηνικών ατόμων, ενωμένων με απλό ομοιοπολικό δεσμό.
ELEKTRĪBA UN MAGNĒTISMS. Laboratorijas darbi Uzdevumi patstāvīgai risināšanai
 ELEKTRĪBA UN MAGNĒTISMS Lortorijs dri Uzdevumi ptstāvīgi risināšni RTU Elektrotehniks institūts 1 Krājumā ievietoti priekšmet «Elektrī un mgnētisms» (EuM) lortorijs dru prksti, kurus RTU Elektrotehniks
ELEKTRĪBA UN MAGNĒTISMS Lortorijs dri Uzdevumi ptstāvīgi risināšni RTU Elektrotehniks institūts 1 Krājumā ievietoti priekšmet «Elektrī un mgnētisms» (EuM) lortorijs dru prksti, kurus RTU Elektrotehniks
ΠΑΓΚΥΠΡΙΑ ΕΝΩΣΗ ΕΠΙΣΤΗΜΟΝΩΝ ΧΗΜΙΚΩΝ ΠΡΙΝ ΑΡΧΙΣΕΤΕ ΝΑ ΓΡΑΦΕΤΕ ΝΑ ΜΕΛΕΤΗΣΕΤΕ ΜΕ ΠΡΟΣΟΧΗ ΤΙΣ ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ ΠΟΥ ΑΚΟΛΟΥΘΟΥΝ:
 ΠΑΓΚΥΠΡΙΑ ΕΝΩΣΗ ΕΠΙΣΤΗΜΟΝΩΝ ΧΗΜΙΚΩΝ ΠΑΓΚΥΠΡΙΑ ΕΝΩΣΗ ΕΠΙΣΤΗΜΟΝΩΝ ΧΗΜΙΚΩΝ ΔΙΑΓΩΝΙΣΜΟΣ ΠΑΓΚΥΠΡΙΑΣ ΟΛΥΜΠΙΑΔΑΣ ΧΗΜΕΙΑΣ 2011-2012 Β ΦΑΣΗ ΥΠΟ ΤΗΝ ΑΙΓΙΔΑ ΤΟΥ ΥΠΟΥΡΓΕΙΟΥ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΠΡΙΝ ΑΡΧΙΣΕΤΕ ΝΑ
ΠΑΓΚΥΠΡΙΑ ΕΝΩΣΗ ΕΠΙΣΤΗΜΟΝΩΝ ΧΗΜΙΚΩΝ ΠΑΓΚΥΠΡΙΑ ΕΝΩΣΗ ΕΠΙΣΤΗΜΟΝΩΝ ΧΗΜΙΚΩΝ ΔΙΑΓΩΝΙΣΜΟΣ ΠΑΓΚΥΠΡΙΑΣ ΟΛΥΜΠΙΑΔΑΣ ΧΗΜΕΙΑΣ 2011-2012 Β ΦΑΣΗ ΥΠΟ ΤΗΝ ΑΙΓΙΔΑ ΤΟΥ ΥΠΟΥΡΓΕΙΟΥ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΠΡΙΝ ΑΡΧΙΣΕΤΕ ΝΑ
Rīgas Tehniskā universitāte Enerģētikas un elektrotehnikas fakultāte Vides aizsardzības un siltuma sistēmu institūts
 Rīgas Tehniskā universitāte Enerģētikas un elektrotehnikas fakultāte Vides aizsardzības un siltuma sistēmu institūts www.videszinatne.lv Saules enerģijas izmantošanas iespējas Latvijā / Seminārs "Atjaunojamo
Rīgas Tehniskā universitāte Enerģētikas un elektrotehnikas fakultāte Vides aizsardzības un siltuma sistēmu institūts www.videszinatne.lv Saules enerģijas izmantošanas iespējas Latvijā / Seminārs "Atjaunojamo
 1951 {0, 1} N = N \ {0} n m M n, m N F x i = (x i 1,..., xi m) x j = (x 1 j,..., xn j ) i j M M i j x i j m n M M M M T f : F m F f(m) f M (f(x 1 1,..., x1 m),..., f(x n 1,..., xn m)) T R F M R M R x
1951 {0, 1} N = N \ {0} n m M n, m N F x i = (x i 1,..., xi m) x j = (x 1 j,..., xn j ) i j M M i j x i j m n M M M M T f : F m F f(m) f M (f(x 1 1,..., x1 m),..., f(x n 1,..., xn m)) T R F M R M R x
Physique des réacteurs à eau lourde ou légère en cycle thorium : étude par simulation des performances de conversion et de sûreté
 Physique des réacteurs à eau lourde ou légère en cycle thorium : étude par simulation des performances de conversion et de sûreté Alexis Nuttin To cite this version: Alexis Nuttin. Physique des réacteurs
Physique des réacteurs à eau lourde ou légère en cycle thorium : étude par simulation des performances de conversion et de sûreté Alexis Nuttin To cite this version: Alexis Nuttin. Physique des réacteurs
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2012. Ηµεροµηνία: Τετάρτη 18 Απριλίου 2012 ΕΚΦΩΝΗΣΕΙΣ
 ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 0 Ε_.ΧλΘ(ε) ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 8 Απριλίου
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 0 Ε_.ΧλΘ(ε) ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 8 Απριλίου
Laboratorijas darbs Nr Junga dubultsprauga
 Lbortorijs rbs Nr.3.2.1 Jung ubultsprug Stuent vārs, uzvārs:... Fkultāte, grup:... Stuent pliecībs numurs:... 1 Teorētiskis pmtojums Jung ubultsprug Prāību, k ivi vi virāki viļņi vienlikus ierbojs kāā
Lbortorijs rbs Nr.3.2.1 Jung ubultsprug Stuent vārs, uzvārs:... Fkultāte, grup:... Stuent pliecībs numurs:... 1 Teorētiskis pmtojums Jung ubultsprug Prāību, k ivi vi virāki viļņi vienlikus ierbojs kāā
Résolution de problème inverse et propagation d incertitudes : application à la dynamique des gaz compressibles
 Résolution de problème inverse et propagation d incertitudes : application à la dynamique des gaz compressibles Alexandre Birolleau To cite this version: Alexandre Birolleau. Résolution de problème inverse
Résolution de problème inverse et propagation d incertitudes : application à la dynamique des gaz compressibles Alexandre Birolleau To cite this version: Alexandre Birolleau. Résolution de problème inverse
Υλικά V, Κεραμικά-Διάλεξη 2. Διδακτέα ύλη:
 Υλικά V, Κεραμικά-Διάλεξη 2 Διδακτέα ύλη: Διάλεξη 1: Εισαγωγή στα Κεραμικά Υλικά. Πυροσυσσωμάτωση και ανάπτυξη μικροδομής. Δεσμοί σε Κεραμικά Υλικά. Δομές σε Κεραμικά Υλικά - Πυριτικά πλέγματα. Διάλεξη
Υλικά V, Κεραμικά-Διάλεξη 2 Διδακτέα ύλη: Διάλεξη 1: Εισαγωγή στα Κεραμικά Υλικά. Πυροσυσσωμάτωση και ανάπτυξη μικροδομής. Δεσμοί σε Κεραμικά Υλικά. Δομές σε Κεραμικά Υλικά - Πυριτικά πλέγματα. Διάλεξη
Χηµεία Θετικής Κατεύθυνσης Β Λυκείου 2001
 Χηµεία Θετικής Κατεύθυνσης Β Λυκείου 001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1 ο Στις ερωτήσεις 1.1-1.4, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Η
Χηµεία Θετικής Κατεύθυνσης Β Λυκείου 001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1 ο Στις ερωτήσεις 1.1-1.4, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Η
Couplage dans les applications interactives de grande taille
 Couplage dans les applications interactives de grande taille Jean-Denis Lesage To cite this version: Jean-Denis Lesage. Couplage dans les applications interactives de grande taille. Réseaux et télécommunications
Couplage dans les applications interactives de grande taille Jean-Denis Lesage To cite this version: Jean-Denis Lesage. Couplage dans les applications interactives de grande taille. Réseaux et télécommunications
Για αραιά διαλύματα : x 1 0 : μ i = μ i 0 RTlnx i χ. όπου μ i φ =μ i 0 χ
 Για ιδανικά διαλύματα : μ i = μ i lnx i x= γ=1 Για αραιά διαλύματα : x 1 : μ i = μ i lnx i χ μ i = μ i φ lnx i όπου μ i φ =μ i χ Χημική Ισορροπία λ Από σελ. 7 Χημική Ισορροπία όταν ν i μ i = (T,P σταθερό)
Για ιδανικά διαλύματα : μ i = μ i lnx i x= γ=1 Για αραιά διαλύματα : x 1 : μ i = μ i lnx i χ μ i = μ i φ lnx i όπου μ i φ =μ i χ Χημική Ισορροπία λ Από σελ. 7 Χημική Ισορροπία όταν ν i μ i = (T,P σταθερό)
Vers un assistant à la preuve en langue naturelle
 Vers un assistant à la preuve en langue naturelle Thévenon Patrick To cite this version: Thévenon Patrick. Vers un assistant à la preuve en langue naturelle. Autre [cs.oh]. Université de Savoie, 2006.
Vers un assistant à la preuve en langue naturelle Thévenon Patrick To cite this version: Thévenon Patrick. Vers un assistant à la preuve en langue naturelle. Autre [cs.oh]. Université de Savoie, 2006.
3607 Ν. 7.28/88. E.E., Παρ. I, Αρ. 2371,
 E.E., Παρ. I, Αρ. 271, 16.12. 607 Ν. 7.2/ περί Συμπληρματικύ Πρϋπλγισμύ Νόμς (Αρ. 5) τυ 19 εκδίδεται με δημσίευση στην επίσημη εφημερίδα της Κυπριακής Δημκρατίας σύμφνα με τ Άρθρ 52 τυ Συντάγματς- - Αριθμός
E.E., Παρ. I, Αρ. 271, 16.12. 607 Ν. 7.2/ περί Συμπληρματικύ Πρϋπλγισμύ Νόμς (Αρ. 5) τυ 19 εκδίδεται με δημσίευση στην επίσημη εφημερίδα της Κυπριακής Δημκρατίας σύμφνα με τ Άρθρ 52 τυ Συντάγματς- - Αριθμός
Γεωχημεία. Ενότητα 2: Γεωχημικές διεργασίες στην επιφάνεια της γης. Αριάδνη Αργυράκη Σχολή Θετικών Επιστημών Τμήμα Γεωλογίας και Γεωπεριβάλλοντος
 Γεωχημεία Ενότητα 2: Γεωχημικές διεργασίες στην επιφάνεια της γης Αριάδνη Αργυράκη Σχολή Θετικών Επιστημών Τμήμα Γεωλογίας και Γεωπεριβάλλοντος Περιεχόμενα ενότητας 1. Γεωχημικές διεργασίες ελέγχου χημισμού
Γεωχημεία Ενότητα 2: Γεωχημικές διεργασίες στην επιφάνεια της γης Αριάδνη Αργυράκη Σχολή Θετικών Επιστημών Τμήμα Γεωλογίας και Γεωπεριβάλλοντος Περιεχόμενα ενότητας 1. Γεωχημικές διεργασίες ελέγχου χημισμού
ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ Ενότητα # (16): θερμοδυναμική Ακρίβος Περικλής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ Ενότητα # (16): θερμοδυναμική Ακρίβος Περικλής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
XHMIKH KINHTIKH & ΘΕΡΜΟΔΥΝΑΜΙΚΗ. Γλυκόζη + 6 Ο 2 6CO 2 + 6H 2 O ΔG o =-3310 kj/mol
 XHMIKH KINHTIKH XHMIKH KINHTIKH & ΘΕΡΜΟΔΥΝΑΜΙΚΗ Θερμοδυναμική: Εξετάζει και καθορίζει το κατά πόσο μια αντίδραση ευνοείται ενεργειακά (ΔG
XHMIKH KINHTIKH XHMIKH KINHTIKH & ΘΕΡΜΟΔΥΝΑΜΙΚΗ Θερμοδυναμική: Εξετάζει και καθορίζει το κατά πόσο μια αντίδραση ευνοείται ενεργειακά (ΔG
SUPPLEMENTAL INFORMATION. Fully Automated Total Metals and Chromium Speciation Single Platform Introduction System for ICP-MS
 Electronic Supplementary Material (ESI) for Journal of Analytical Atomic Spectrometry. This journal is The Royal Society of Chemistry 2018 SUPPLEMENTAL INFORMATION Fully Automated Total Metals and Chromium
Electronic Supplementary Material (ESI) for Journal of Analytical Atomic Spectrometry. This journal is The Royal Society of Chemistry 2018 SUPPLEMENTAL INFORMATION Fully Automated Total Metals and Chromium
Μεταβολή ορισμένων περιοδικών ιδιοτήτων
 Μεταβολή ορισμένων περιοδικών ιδιοτήτων 1. Ερώτηση: Ποια θεωρούνται θεμελιώδη χαρακτηριστικά του ατόμου και γιατί; Θεμελιώδη χαρακτηριστικά του ατόμου είναι: η ατομική ακτίνα, η ενέργεια ιοντισμού και
Μεταβολή ορισμένων περιοδικών ιδιοτήτων 1. Ερώτηση: Ποια θεωρούνται θεμελιώδη χαρακτηριστικά του ατόμου και γιατί; Θεμελιώδη χαρακτηριστικά του ατόμου είναι: η ατομική ακτίνα, η ενέργεια ιοντισμού και
5 Ι ^ο 3 X X X. go > 'α. ο. o f Ο > = S 3. > 3 w»a. *= < ^> ^ o,2 l g f ^ 2-3 ο. χ χ. > ω. m > ο ο ο - * * ^r 2 =>^ 3^ =5 b Ο? UJ. > ο ο.
 728!. -θ-cr " -;. '. UW -,2 =*- Os Os rsi Tf co co Os r4 Ι. C Ι m. Ι? U Ι. Ι os ν ) ϋ. Q- o,2 l g f 2-2 CT= ν**? 1? «δ - * * 5 Ι -ΐ j s a* " 'g cn" w *" " 1 cog 'S=o " 1= 2 5 ν s/ O / 0Q Ε!θ Ρ h o."o.
728!. -θ-cr " -;. '. UW -,2 =*- Os Os rsi Tf co co Os r4 Ι. C Ι m. Ι? U Ι. Ι os ν ) ϋ. Q- o,2 l g f 2-2 CT= ν**? 1? «δ - * * 5 Ι -ΐ j s a* " 'g cn" w *" " 1 cog 'S=o " 1= 2 5 ν s/ O / 0Q Ε!θ Ρ h o."o.
2013/2012. m' Z (C) : V= (E): (C) :3,24 m/s. (A) : T= (1-z).g. (D) :4,54 m/s
 ( ) 03/0 - o l P z o M l =.P S. ( ) m' Z l=m m=kg m =,5Kg g=0/kg : : : : Q. (A) : V= (B) : V= () : V= (D) : V= (): : V :Q. (A) :4m/s (B) :0,4 m/s () :5m/s (D) :0,5m/s (): : M T : Q.3 (A) : T=(-z).g (B)
( ) 03/0 - o l P z o M l =.P S. ( ) m' Z l=m m=kg m =,5Kg g=0/kg : : : : Q. (A) : V= (B) : V= () : V= (D) : V= (): : V :Q. (A) :4m/s (B) :0,4 m/s () :5m/s (D) :0,5m/s (): : M T : Q.3 (A) : T=(-z).g (B)
ITU-R P (2009/10)
 ITU-R.38-6 (009/0 $% #! " #( ' * & ' /0,-. # GHz 00 MHz 900 ITU-R.38-6 ii.. (IR (ITU-T/ITU-R/ISO/IEC.ITU-R http://www.itu.int/itu-r/go/patents/en. (http://www.itu.int/publ/r-rec/en ( ( BO BR BS BT F M
ITU-R.38-6 (009/0 $% #! " #( ' * & ' /0,-. # GHz 00 MHz 900 ITU-R.38-6 ii.. (IR (ITU-T/ITU-R/ISO/IEC.ITU-R http://www.itu.int/itu-r/go/patents/en. (http://www.itu.int/publ/r-rec/en ( ( BO BR BS BT F M
Klasificēšanas kritēriji, ņemot vērā fizikāli ķīmiskās īpašības
 , ņemot vērā fizikāli ķīmiskās īpašības Mg.sc.ing. Līga Rubene VSIA "Latvijas Vides, ģeoloģijas un meteoroloģijas centrs" Informācijas analīzes daļa Ķīmisko vielu un bīstamo atkritumu nodaļa 20.04.2017.
, ņemot vērā fizikāli ķīmiskās īpašības Mg.sc.ing. Līga Rubene VSIA "Latvijas Vides, ģeoloģijas un meteoroloģijas centrs" Informācijas analīzes daļa Ķīmisko vielu un bīstamo atkritumu nodaļa 20.04.2017.
Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ
 Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 poulios@chem.auth.gr http://www.chem.auth.gr/index.php?st=84 XHMIKH IΣΟΡΡΟΠΙΑ Σύστημα διαφόρων ουσιών που σε σταθερή θερμοκρασία δεν
Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 poulios@chem.auth.gr http://www.chem.auth.gr/index.php?st=84 XHMIKH IΣΟΡΡΟΠΙΑ Σύστημα διαφόρων ουσιών που σε σταθερή θερμοκρασία δεν
ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ ΤΩΝ ΣΤΟΙΧΕΙΩΝ (1) Ηλία Σκαλτσά ΠΕ ο Γυμνάσιο Αγ. Παρασκευής
 ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ ΤΩΝ ΣΤΟΙΧΕΙΩΝ (1) Ηλία Σκαλτσά ΠΕ04.01 5 ο Γυμνάσιο Αγ. Παρασκευής Όπως συμβαίνει στη φύση έτσι και ο άνθρωπος θέλει να πετυχαίνει σπουδαία αποτελέσματα καταναλώνοντας το λιγότερο δυνατό
ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ ΤΩΝ ΣΤΟΙΧΕΙΩΝ (1) Ηλία Σκαλτσά ΠΕ04.01 5 ο Γυμνάσιο Αγ. Παρασκευής Όπως συμβαίνει στη φύση έτσι και ο άνθρωπος θέλει να πετυχαίνει σπουδαία αποτελέσματα καταναλώνοντας το λιγότερο δυνατό
ΔG o ' = πρότυπη μεταβολή ελέυθερης ενέργειας (ph 7, 1M αντιδρ.& προιόντων ); R = στ. αερίων; T = θερμοκρ. 2 ΔG o ' >0, ΔG<0
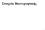 Στοιχεία Βιοενεργητικής 1 Ελεύθερη ενέργεια αντίδρασης Μια αντίδραση είναι αυθόρμητη εάν η μεταβολή ελεύθερης ενέργειας [free energy change (ΔG)] είναι αρνητική, δηλ. εάν η ελεύθερη ενέργεια των προϊόντων
Στοιχεία Βιοενεργητικής 1 Ελεύθερη ενέργεια αντίδρασης Μια αντίδραση είναι αυθόρμητη εάν η μεταβολή ελεύθερης ενέργειας [free energy change (ΔG)] είναι αρνητική, δηλ. εάν η ελεύθερη ενέργεια των προϊόντων
1. Testa nosaukums IMUnOGLOBULĪnS G (IgG) 2. Angļu val. Immunoglobulin G
 1. Testa nosaukums IMUnOGLOBULĪnS G (IgG) 2. Angļu val. Immunoglobulin G 3. Īss raksturojums Imunoglobulīnu G veido 2 vieglās κ vai λ ķēdes un 2 smagās γ ķēdes. IgG iedalās 4 subklasēs: IgG1, IgG2, IgG3,
1. Testa nosaukums IMUnOGLOBULĪnS G (IgG) 2. Angļu val. Immunoglobulin G 3. Īss raksturojums Imunoglobulīnu G veido 2 vieglās κ vai λ ķēdes un 2 smagās γ ķēdes. IgG iedalās 4 subklasēs: IgG1, IgG2, IgG3,
Logatherm WPS 10K A ++ A + A B C D E F G A B C D E F G. kw kw /2013
 51 d 11 11 10 kw kw kw d 2015 811/2013 2015 811/2013 Izstrādājuma datu lapa par energopatēriņu Turpmākie izstrādājuma dati atbilst S regulu 811/2013, 812/2013, 813/2013 un 814/2013 prasībām, ar ko papildina
51 d 11 11 10 kw kw kw d 2015 811/2013 2015 811/2013 Izstrādājuma datu lapa par energopatēriņu Turpmākie izstrādājuma dati atbilst S regulu 811/2013, 812/2013, 813/2013 un 814/2013 prasībām, ar ko papildina
E.E. Παρ. Ill (I) 701 &.Δ.Π. 237/92 Αρ. 2740, Αριθμός 237 Ο ΠΕΡΙ ΠΟΛΕΟΔΟΜΙΑΣ ΚΑΙ ΧΩΡΟΤΑΞΙΑΣ ΝΟΜΟΣ (ΝΟΜΟΙ 90 ΤΟΥ 1972 ΚΑΙ 56 ΤΟΥ 1982)
 E.E. Παρ. Ill (I) 71 &.Δ.Π. 7/9 Αρ. 74, 5.9.9 Αριθμός 7 ΠΕΡΙ ΠΛΕΔΙΑΣ ΑΙ ΧΩΡΤΑΞΙΑΣ ΝΣ (ΝΙ 9 ΤΥ 197 ΑΙ 5 ΤΥ 19) Διάταγμα Διατήρησης σύμφνα μ τ άρθρ (1) Ασκώντας τις ξσίς π χρηγύνται σ' ατόν από τ άφι (Ι)
E.E. Παρ. Ill (I) 71 &.Δ.Π. 7/9 Αρ. 74, 5.9.9 Αριθμός 7 ΠΕΡΙ ΠΛΕΔΙΑΣ ΑΙ ΧΩΡΤΑΞΙΑΣ ΝΣ (ΝΙ 9 ΤΥ 197 ΑΙ 5 ΤΥ 19) Διάταγμα Διατήρησης σύμφνα μ τ άρθρ (1) Ασκώντας τις ξσίς π χρηγύνται σ' ατόν από τ άφι (Ι)
Sarò signor io sol. α α. œ œ. œ œ œ œ µ œ œ. > Bass 2. Domenico Micheli. Canzon, ottava stanza. Soprano 1. Soprano 2. Alto 1
 Sarò signor io sol Canzon, ottava stanza Domenico Micheli Soprano Soprano 2 Alto Alto 2 Α Α Sa rò si gnor io sol del mio pen sie io sol Sa rò si gnor io sol del mio pen sie io µ Tenor Α Tenor 2 Α Sa rò
Sarò signor io sol Canzon, ottava stanza Domenico Micheli Soprano Soprano 2 Alto Alto 2 Α Α Sa rò si gnor io sol del mio pen sie io sol Sa rò si gnor io sol del mio pen sie io µ Tenor Α Tenor 2 Α Sa rò
Solving an Air Conditioning System Problem in an Embodiment Design Context Using Constraint Satisfaction Techniques
 Solving an Air Conditioning System Problem in an Embodiment Design Context Using Constraint Satisfaction Techniques Raphael Chenouard, Patrick Sébastian, Laurent Granvilliers To cite this version: Raphael
Solving an Air Conditioning System Problem in an Embodiment Design Context Using Constraint Satisfaction Techniques Raphael Chenouard, Patrick Sébastian, Laurent Granvilliers To cite this version: Raphael
Γεωχημεία. Ενότητα 1: Γεωχημικές διεργασίες στο εσωτερικό της γης. Χριστίνα Στουραϊτη Σχολή Θετικών Επιστημών Τμήμα Γεωλογίας και Γεωπεριβάλλοντος
 Γεωχημεία Ενότητα 1: Γεωχημικές διεργασίες στο εσωτερικό της γης Χριστίνα Στουραϊτη Σχολή Θετικών Επιστημών Τμήμα Γεωλογίας και Γεωπεριβάλλοντος Γεωχημικές διεργασίες στο εσωτερικό της γης Στοιχεία Θερμοδυναμικής
Γεωχημεία Ενότητα 1: Γεωχημικές διεργασίες στο εσωτερικό της γης Χριστίνα Στουραϊτη Σχολή Θετικών Επιστημών Τμήμα Γεωλογίας και Γεωπεριβάλλοντος Γεωχημικές διεργασίες στο εσωτερικό της γης Στοιχεία Θερμοδυναμικής
ITU-R P (2009/10)
 ITU-R.45-4 (9/) % # GHz,!"# $$ # ITU-R.45-4.. (IR) (ITU-T/ITU-R/ISO/IEC).ITU-R http://www.tu.t/itu-r/go/patets/e. (http://www.tu.t/publ/r-rec/e ) () ( ) BO BR BS BT F M RA S RS SA SF SM SNG TF V.ITU-R
ITU-R.45-4 (9/) % # GHz,!"# $$ # ITU-R.45-4.. (IR) (ITU-T/ITU-R/ISO/IEC).ITU-R http://www.tu.t/itu-r/go/patets/e. (http://www.tu.t/publ/r-rec/e ) () ( ) BO BR BS BT F M RA S RS SA SF SM SNG TF V.ITU-R
... 5 A.. RS-232C ( ) RS-232C ( ) RS-232C-LK & RS-232C-MK RS-232C-JK & RS-232C-KK
 RS-3C WIWM050 014.1.9 P1 :8... 1... 014.0.1 1 A... 014.0. 1... RS-3C()...01.08.03 A.. RS-3C()...01.08.03 3... RS-3C()... 003.11.5 4... RS-3C ()... 00.10.01 5... RS-3C().008.07.16 5 A.. RS-3C().0 1.08.
RS-3C WIWM050 014.1.9 P1 :8... 1... 014.0.1 1 A... 014.0. 1... RS-3C()...01.08.03 A.. RS-3C()...01.08.03 3... RS-3C()... 003.11.5 4... RS-3C ()... 00.10.01 5... RS-3C().008.07.16 5 A.. RS-3C().0 1.08.
Vn 1: NHC LI MT S KIN TH C LP 10
 Vn : NHC LI MT S KIN TH C LP 0 Mc ích ca vn này là nhc li mt s kin thc ã hc lp 0, nhng có liên quan trc tip n vn s hc trng lp. Vì thi gian không nhiu (khng tit) nên chúng ta s không nhc li lý thuyt mà
Vn : NHC LI MT S KIN TH C LP 0 Mc ích ca vn này là nhc li mt s kin thc ã hc lp 0, nhng có liên quan trc tip n vn s hc trng lp. Vì thi gian không nhiu (khng tit) nên chúng ta s không nhc li lý thuyt mà
Π Α Ρ Α Ρ Τ Η Μ Α ΠΑΙΧΝΙΔΙΑ ΜΕ ΤΟΥΣ ΜΟΥΣΙΚΟΥΣ ΣΩΛΗΝΕΣ BOOMWHACKERS
 Π Α Ρ Α Ρ Τ Η Μ Α ΠΑΙΧΝΙΔΙΑ ΜΕ ΤΟΥΣ ΜΟΥΣΙΚΟΥΣ ΣΩΛΗΝΕΣ BOOMWHACKERS Ελισσάβετ Περακάκη & Μαρίνα Μίντζα 1 σελ. 18 Δαχτυλίδι Παιδικό τραγούδι 2 2 σελ. 19 Twinkl Twinkl Παιδικό τραγούδι 3 3 σελ. 20 Frèr Jacqus
Π Α Ρ Α Ρ Τ Η Μ Α ΠΑΙΧΝΙΔΙΑ ΜΕ ΤΟΥΣ ΜΟΥΣΙΚΟΥΣ ΣΩΛΗΝΕΣ BOOMWHACKERS Ελισσάβετ Περακάκη & Μαρίνα Μίντζα 1 σελ. 18 Δαχτυλίδι Παιδικό τραγούδι 2 2 σελ. 19 Twinkl Twinkl Παιδικό τραγούδι 3 3 σελ. 20 Frèr Jacqus
Consommation marchande et contraintes non monétaires au Canada ( )
 Consommation marchande et contraintes non monétaires au Canada (1969-2008) Julien Boelaert, François Gardes To cite this version: Julien Boelaert, François Gardes. Consommation marchande et contraintes
Consommation marchande et contraintes non monétaires au Canada (1969-2008) Julien Boelaert, François Gardes To cite this version: Julien Boelaert, François Gardes. Consommation marchande et contraintes
1 La teoría de Jeans. t + (n v) = 0 (1) b) Navier-Stokes (conservación del impulso) c) Poisson
 1 La teoría de Jeans El caso ás siple de evolución de fluctuaciones es el de un fluído no relativista. las ecuaciones básicas son: a conservación del núero de partículas n t + (n v = 0 (1 b Navier-Stokes
1 La teoría de Jeans El caso ás siple de evolución de fluctuaciones es el de un fluído no relativista. las ecuaciones básicas son: a conservación del núero de partículas n t + (n v = 0 (1 b Navier-Stokes
A hybrid PSTD/DG method to solve the linearized Euler equations
 A hybrid PSTD/ method to solve the linearized Euler equations ú P á ñ 3 rt r 1 rt t t t r t rs t2 2 t r s r2 r r Ps s tr r r P t s s t t 2 r t r r P s s r r 2s s s2 t s s t t t s t r t s t r q t r r t
A hybrid PSTD/ method to solve the linearized Euler equations ú P á ñ 3 rt r 1 rt t t t r t rs t2 2 t r s r2 r r Ps s tr r r P t s s t t 2 r t r r P s s r r 2s s s2 t s s t t t s t r t s t r q t r r t
U unutrašnja energija H entalpija S entropija G 298. G Gibsova energija TERMOHEMIJA I TERMODINAMIKA HEMIJSKA TERMODINAMIKA
 HEMIJSKA TERMODINAMIKA Bavi se energetskim promenama pri odigravanju hemijskih reakcija. TERMODINAMIČKE FUNKCIJE STANJA U unutrašnja energija H entalpija S entropija Ako su određene na standardnom pritisku
HEMIJSKA TERMODINAMIKA Bavi se energetskim promenama pri odigravanju hemijskih reakcija. TERMODINAMIČKE FUNKCIJE STANJA U unutrašnja energija H entalpija S entropija Ako su određene na standardnom pritisku
Εισαγωγή στην πυρηνοποίηση. http://users.auth.gr/~paloura/ Ομο- & ετερογενής πυρηνοποίηση: αρχικά στάδια ανάπτυξης υλικών ή σχηματισμού νέας φάσης.
 Εισαγωγή στην πυρηνοποίηση. http://users.auth.gr/~paloura/ Αντικείμενο Ομο- & ετερογενής πυρηνοποίηση: αρχικά στάδια ανάπτυξης υλικών ή σχηματισμού νέας φάσης. Ομογενής πυρηνοποίηση: αυθόρμητος σχηματισμός
Εισαγωγή στην πυρηνοποίηση. http://users.auth.gr/~paloura/ Αντικείμενο Ομο- & ετερογενής πυρηνοποίηση: αρχικά στάδια ανάπτυξης υλικών ή σχηματισμού νέας φάσης. Ομογενής πυρηνοποίηση: αυθόρμητος σχηματισμός
La naissance de la cohomologie des groupes
 La naissance de la cohomologie des groupes Nicolas Basbois To cite this version: Nicolas Basbois. La naissance de la cohomologie des groupes. Mathématiques [math]. Université Nice Sophia Antipolis, 2009.
La naissance de la cohomologie des groupes Nicolas Basbois To cite this version: Nicolas Basbois. La naissance de la cohomologie des groupes. Mathématiques [math]. Université Nice Sophia Antipolis, 2009.
Tēraudbetona konstrukcijas
 Tēraudbetona konstrukcijas tēraudbetona kolonnu projektēšana pēc EN 1994-1-1 lektors: Gatis Vilks, SIA «BALTIC INTERNATIONAL CONSTRUCTION PARTNERSHIP» Saturs 1. Vispārīga informācija par kompozītām kolonnām
Tēraudbetona konstrukcijas tēraudbetona kolonnu projektēšana pēc EN 1994-1-1 lektors: Gatis Vilks, SIA «BALTIC INTERNATIONAL CONSTRUCTION PARTNERSHIP» Saturs 1. Vispārīga informācija par kompozītām kolonnām
τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n, l)
 ΑΤΟΜΙΚΑ ΤΡΟΧΙΑΚΑ Σχέση κβαντικών αριθµών µε στιβάδες υποστιβάδες - τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n,
ΑΤΟΜΙΚΑ ΤΡΟΧΙΑΚΑ Σχέση κβαντικών αριθµών µε στιβάδες υποστιβάδες - τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n,
Supplementary Data. Engineering, Nanjing University, Nanjing , P. R. China;
 Supplementary Data Synthesis, Chemo-selective Properties of Substituted 9-Aryl-9H-fluorenes from Triarylcarbinols and Enantiomerical Kinetics of Chiral 9-Methoxy-11-(naphthalen-1-yl)-11H-benzo[a]fluorene
Supplementary Data Synthesis, Chemo-selective Properties of Substituted 9-Aryl-9H-fluorenes from Triarylcarbinols and Enantiomerical Kinetics of Chiral 9-Methoxy-11-(naphthalen-1-yl)-11H-benzo[a]fluorene
ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ Ι Θέμα ασκήσεως Αρχή μεθόδου Θεωρία
 3-1 ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ Ι Θέμα ασκήσεως: Προσδιορισμός κανονικού δυναμικού (Ε) ηλεκτροδίου. Προσδιορισμός του θερμικού συντελεστή ( Ε/ Τ) P. Προσδιορισμός του γινομένου διαλυτότητας του Agl. Αρχή μεθόδου:
3-1 ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ Ι Θέμα ασκήσεως: Προσδιορισμός κανονικού δυναμικού (Ε) ηλεκτροδίου. Προσδιορισμός του θερμικού συντελεστή ( Ε/ Τ) P. Προσδιορισμός του γινομένου διαλυτότητας του Agl. Αρχή μεθόδου:
Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Πανεπιστήμιο Δυτικής Αττικής - ΣΑΕΤ
 Γενική και Ανόργανη Χημεία Περιοδικές ιδιότητες των στοιχείων. Σχηματισμός ιόντων. Στ. Μπογιατζής 1 Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Π Δ Χειμερινό εξάμηνο 2018-2019 Π
Γενική και Ανόργανη Χημεία Περιοδικές ιδιότητες των στοιχείων. Σχηματισμός ιόντων. Στ. Μπογιατζής 1 Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Π Δ Χειμερινό εξάμηνο 2018-2019 Π
ITU-R P (2012/02) &' (
 ITU-R P.530-4 (0/0) $ % " "#! &' ( P ITU-R P. 530-4 ii.. (IPR) (ITU-T/ITU-R/ISO/IEC).ITU-R http://www.itu.int/itu-r/go/patents/en. ITU-T/ITU-R/ISO/IEC (http://www.itu.int/publ/r-rec/en ) () ( ) BO BR BS
ITU-R P.530-4 (0/0) $ % " "#! &' ( P ITU-R P. 530-4 ii.. (IPR) (ITU-T/ITU-R/ISO/IEC).ITU-R http://www.itu.int/itu-r/go/patents/en. ITU-T/ITU-R/ISO/IEC (http://www.itu.int/publ/r-rec/en ) () ( ) BO BR BS
Fusion de données multicapteurs pour la construction incrémentale du modèle tridimensionnel texturé d un environnement intérieur par un robot mobile
 Fusion de données multicapteurs pour la construction incrémentale du modèle tridimensionnel texturé d un environnement intérieur par un robot mobile Ayman Zureiki To cite this version: Ayman Zureiki. Fusion
Fusion de données multicapteurs pour la construction incrémentale du modèle tridimensionnel texturé d un environnement intérieur par un robot mobile Ayman Zureiki To cite this version: Ayman Zureiki. Fusion
Transformations d Arbres XML avec des Modèles Probabilistes pour l Annotation
 Transformations d Arbres XML avec des Modèles Probabilistes pour l Annotation Florent Jousse To cite this version: Florent Jousse. Transformations d Arbres XML avec des Modèles Probabilistes pour l Annotation.
Transformations d Arbres XML avec des Modèles Probabilistes pour l Annotation Florent Jousse To cite this version: Florent Jousse. Transformations d Arbres XML avec des Modèles Probabilistes pour l Annotation.
of the methanol-dimethylamine complex
 Electronic Supplementary Information for: Fundamental and overtone virational spectroscopy, enthalpy of hydrogen ond formation and equilirium constant determination of the methanol-dimethylamine complex
Electronic Supplementary Information for: Fundamental and overtone virational spectroscopy, enthalpy of hydrogen ond formation and equilirium constant determination of the methanol-dimethylamine complex
Χημική Θερμοδυναμική- Βιοενεργητική
 Χημική Θερμοδυναμική- Βιοενεργητική Χρήστος Κρούπης, MSc, PhD Επίκουρος Καθηγητής Κλινικής Βιοχημείας Αττικόν Πανεπιστημιακό Νοσοκομείο Ιατρική Σχολή Πανεπιστημίου Αθηνών 1 Ὺλη Θερμοδυναμικής -Βιοενεργητικής
Χημική Θερμοδυναμική- Βιοενεργητική Χρήστος Κρούπης, MSc, PhD Επίκουρος Καθηγητής Κλινικής Βιοχημείας Αττικόν Πανεπιστημιακό Νοσοκομείο Ιατρική Σχολή Πανεπιστημίου Αθηνών 1 Ὺλη Θερμοδυναμικής -Βιοενεργητικής
{3k + a : k N a = 1,2}.
 P P 1èt s t rð P Ôst ì t è t Ð Ð t èr è ❼ ❼s t t s s Ð s Ð sô t r s Ð t s Ô ❼r rì ì èq Ð ì r t t èr Ôt r t r trðt rìq r r❼2t r rqðs 1èt s t r t ì s s ❼ ì s èq Ð r❼2t st r t ì st Ôt r ì st trðt ì P t r
P P 1èt s t rð P Ôst ì t è t Ð Ð t èr è ❼ ❼s t t s s Ð s Ð sô t r s Ð t s Ô ❼r rì ì èq Ð ì r t t èr Ôt r t r trðt rìq r r❼2t r rqðs 1èt s t r t ì s s ❼ ì s èq Ð r❼2t st r t ì st Ôt r ì st trðt ì P t r
J! "#$ %"& ( ) ) ) " *+, -./0-, *- /! /!+12, ,. 6 /72-, 0,,3-8 / ',913-51:-*/;+ 5/<3/ +15;+ 5/<3=9 -!.1!-9 +17/> ) ) &
 J! "#$ %"& J ' ( ) ) ) " *+, -./0-, L *- /! /!+12,3-4 % +15,. 6 /72-, 0,,3-8 / ',913-51:-*/;+ 5/01 ',913-51:--
J! "#$ %"& J ' ( ) ) ) " *+, -./0-, L *- /! /!+12,3-4 % +15,. 6 /72-, 0,,3-8 / ',913-51:-*/;+ 5/01 ',913-51:--
Περιβαλλοντική Χημεία - Γεωχημεία. Διαφάνειες 4 ου Μαθήματος Γαλάνη Απ. Αγγελική, Χημικός Ph.D. Ε.ΔΙ.Π.
 Περιβαλλοντική Χημεία - Γεωχημεία Διαφάνειες 4 ου Μαθήματος Γαλάνη Απ. Αγγελική, Χημικός Ph.D. Ε.ΔΙ.Π. ΧΗΜΙΚΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ Η χημεία έχει αντικείμενο μελέτης της τους μετασχηματισμούς της ύλης που πραγματοποιούνται
Περιβαλλοντική Χημεία - Γεωχημεία Διαφάνειες 4 ου Μαθήματος Γαλάνη Απ. Αγγελική, Χημικός Ph.D. Ε.ΔΙ.Π. ΧΗΜΙΚΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ Η χημεία έχει αντικείμενο μελέτης της τους μετασχηματισμούς της ύλης που πραγματοποιούνται
Eliminacijski zadatak iz Matematike 1 za kemičare
 Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Modèles de représentation multi-résolution pour le rendu photo-réaliste de matériaux complexes
 Modèles de représentation multi-résolution pour le rendu photo-réaliste de matériaux complexes Jérôme Baril To cite this version: Jérôme Baril. Modèles de représentation multi-résolution pour le rendu
Modèles de représentation multi-résolution pour le rendu photo-réaliste de matériaux complexes Jérôme Baril To cite this version: Jérôme Baril. Modèles de représentation multi-résolution pour le rendu
 !"#!"!"# $ "# '()!* '+!*, -"*!" $ "#. /01 023 43 56789:3 4 ;8< = 7 >/? 44= 7 @ 90A 98BB8: ;4B0C BD :0 E D:84F3 B8: ;4BG H ;8
!"#!"!"# $ "# '()!* '+!*, -"*!" $ "#. /01 023 43 56789:3 4 ;8< = 7 >/? 44= 7 @ 90A 98BB8: ;4B0C BD :0 E D:84F3 B8: ;4BG H ;8

