2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass
|
|
|
- Ἀριστομάχη Βαμβακάς
- 7 χρόνια πριν
- Προβολές:
Transcript
1 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud metallide kindlakstegemiseks piisab, kui jälgida nende reageerimist (+) lahjendatud vesinikkloriidhappe, kontsentreeritud külma lämmastikhappe ja kontsentreeritud naatriumhüdroksiidi lahustega. Reaktiiv Metall I Metall II Metall III HCl + + HNO NaOH + + a) Millised keemilised elemendid on metallid I, II ja III? (3) b) Kirjutage tabelis toodud andmete põhjal vastavate reaktsioonide võrrandid (6 tk). (6) c) Põhjendage (kui võimalik, siis andke valemid), miks vaadeldavad metallid tavatingimustel ei korrodeeru. (2) 11 p 2. Saksamaal on püütud kasutada kütusena elementi A. Elemendi A abil energiaga saamisega ei kaasne keskkonda saastavate jääkainete moodustumist. Energia tootmisel ühineb element A katalüsaatori (CuO) juuresolekul C juures eksotermiliselt lihtainega B, mille tulemusena moodustub aine C. Aine C ei reosta keskkonda, sest reageerimisel liitainega E moodustuvad ammoniaak ja aine D. Ammoniaagist saab toota sooli, mida kasutatakse väetistena. Binaarne ühend D sisaldab 53% hapnikku ega reageeri veega. Tähelepanu! hapniku sisaldus on antud ainult kahe tüvenumbri täpsusega. a) i) Arvutage aine D valem ja kirjutage selle nimetus. ii) Kirjutage ainete A, B, C ja E valemid ja nimetused. (5) b) Kirjutage reaktsioonivõrrandid: i) A + B, ii) C + E ja iii) NH 3 väetis. (3) c) Kirjutage peamine põhjus, miks ülalkirjeldatud energiasaamise skeemi ei kasutata (1) 9p 3. NaOH täpse kaalutise järgi ei ole võimalik valmistada täpse molaarse kontsentratsiooniga lahust, sest NaOH on hügroskoopne ja võib teatud määral reageerida ka õhus sisalduva СО 2. 1 liitri ~0,1 M NaOH lahuse valmistamiseks mõõtis laborant 1 L mõõtekolbi 5,2 cm 3 küllastatud NaOH lahust ja täitis kolvi veega märgini. Saadud lahuse kontsentratsiooni määramiseks kasutas laborant varemvalmistatud täpse kontsentratsiooniga oblikhappe lahust. a) Kirjutage oblikhappe graafiline valem. (2) b) Kirjutage NaOH ja oblikhappe vahelise neutralisatsioonireaktsiooni võrrand. (1) c) Arvutage i) oblikhappedihüdraadi molaarmass ja ii) selle kristallhüdraadi mass, mis on vajalik täpselt 100 ml 0,05000 M lahuse valmistamiseks. (2) d) Arvutage valmistatud NaOH lahuse molaarne kontsentratsioon, kui laborandi poolt valmistatud täpselt 10 ml lahuse tiitrimiseks kulus 10,20 cm 3 NaOH lahust. (2) e) Arvutage küllastunud lahuses NaOH protsendiline sisaldus, kui selle lahuse tihedus on 1,54 g/cm 3. (2) 9 p aprillil 1912 läks Atlandi ookeani põhja kuulus Titanic. Katastroofil oli mitu põhjust, sealhulgas ka laevakonstruktsioonis kasutatud terase rabedus, mis on tingitud mittemetallide X ja Y liigsest sisaldusest. Neist esimene põhjustab terase rabedust kõrgel, teine madalal temperatuuril. Terase lähteaineks on malm, mille põhikomponendiks on lihtaine A ja mis sisaldab lisanditena mittemetalle Y, Q ja Z ning põhikomponendi ja mittemetalli X binaarset soola R. Soolas R on mittemetalli X sisaldus 36,5%. Elemendid Q ja Z paiknevad
2 perioodilisussüsteemi samas rühmas, elemendid X, Y ja Z aga samas perioodis. Terase tootmisel oksüdeerub mingi osa lihtainest A hapniku toimel madalaima oksüdatsiooniastmega ühendiks B. Seejärel toimuvad järgmised reaktsioonid: B + Y = A + D (oksiid D on suure molekulmassiga, elemendil Y on selles kõrgeim oksüdatsiooniaste ja D vesilahus on happeline). B + Q = A + E (oksiid E on mürgine gaas, kus element Q ei ole täielikult oksüdeerunud) B + Z = A + G (oksiidis G on elemendil Z kõrgeim o.a. ja selle lisamisel vette jääb keskkond neutraalseks). Et vabaneda soolast R, kasutatakse lubjakivi. Esmalt toimub lubjakivi lagunemine: lubjakivi = J + L (L on gaas, mis moodustub ka gaasilise E oksüdeerumisel). Seejärel toimub reaktsioon J + R = B + M (M on binaarne sool, milles mittemetalli X sisaldus on 44,4%). a) Kirjutage i) lihtaine A valem ja nimetus, ii) lubjakivi lagunemisreaktsiooni võrrand ning iii) ühendi B tekkereaktsiooni võrrand. (1,5) b) i) Milliste metallide ühendid on soolad R ja M? Arvutage elemendi X aatommass soolade ii) R ja iii) M protsendilise koostise järgi. (1,5) c) Identifitseerige (valem ja nimetus) ained Y, Q, Z, X, R, B, D, E, G, J, L, M. (3) d) Kirjutage reaktsioonivõrrandid: i) B + Y, ii) B + Q, iii) B + Z ; iv) J + R. (4)10p 5. Metalli X soola kristallhüdraat R esineb kolme isomeerina: A (sinkjas-violetne), B (tumeroheline) ja C (heleroheline). X koordinatsiooniarv on kuus; isomeerides A, B ja C on X oksüdatsiooniaste +III. Kristallhüdraadi R protsendiline koostis on järgmine: 19,5% elementi X, 40,0% mittemetalli Y, 4,5% vesinikku ja 36,0% hapnikku, kusjuures vesinik kuulub ainult veemolekulide koostisse. Isomeeride täpsed valemid (sise- ja väliskoordinatsioonisfäär) saab kindlaks teha, pannes vastava isomeeri värskelt valmistatud lahuse reageerima hõbenitraadiga (ühend Q). Reaktsiooni tulemusena tekib binaarne valge sade Z, mille hulga järgi saab määrata, milline hulk isomeerides sisalduvast elemendist Y on reaktsioonist osa võtnud. Q toimel aine A lahusele sadeneb (sademe Z koostises) kogu kristallhüdraadi R koostisse kuuluv element Y. Ühendi Q toimel aine B lahusele sadeneb 2/3 ja Q toimel aine C lahusele vaid 1/3 kristallhüdraadi R koostisesse kuuluvast elemendist Y. a) Kirjutage i) ioonide sümbolite ja ühendite valemite abil reaktsioonivõrrand: ioon Y + Q Z + ioon. ii) Kirjutage Y, Q ja Z valemid ja nimetused. (2,5) b) Leidke 100 g kristallhüdraadis elementide O ja H hulk (moolide arv). (2) c) Leidke kristallhüdraadi brutovalem ja arvutage elemendi X aatommass. Andke elemendi X sümbol ja nimetus. (3,5) d) Kirjutage kristallhüdraadi R isomeeride A, B ja C täpsed valemid. (3) 11 p 6. Anumas on 1, aine A molekuli. Kõikide orgaaniliste ühendite põlemisel moodustub lisaks ainele A ka aine B. Aine B koosneb sama perioodi elementidest. Mõningatel elusorganismidel on võime viia valguse toimel läbi reaktsiooni A + B Q + Z. Ühendi Q molekulmass on 180 ja selle koostises on 40,0% süsinikku, 6,7% vesinikku ja 53,3% hapnikku. Z on gaasiline lihtaine, mis kuulub nii ühendi A kui ka ühendi B koostisse. Aines A absorbeerus (neeldus) 1, gaasi C molekuli. Gaas C moodustub plahvatusega gaasidest D ja E välkvalguse toimel. Gaas D moodustub vee elektrolüüsil, gaas E on kollakas-roheline raske mürgine gaas. a) Kirjutage ainete A, B, Z, C, D ja E valemid ja nimetused. (3) b) Arvutage ühendi Q brutovalem ja kirjutage tema nimetus. (3) c) Kirjutage reaktsioonivõrrand A + B Q + Z. (1) d) Arvutage aine C lahustumisel moodustunud lahuse molaarne kontsentratsioon (mol/dm 3 ). Eeldage, et lahuse ruumala võrdub aine A ruumalaga ja ρ(a)=1,00 g/cm 3 (3)10p
3 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 11. klass 1. Majahoidja soovib teada, kui palju keedusoola kulub, et sulatada kogu majaesist teelõiku kattev jää (0,92 g/cm 3 ). Teelõigu pikkus on 55 m ja laius 1,5 m. Jää keskmiseks paksuseks hindas ta 5,0 cm. Välistemperatuur on -3,0 0 C. T = K kr m, kus K kr = 1,86 K kg/mol ja tähistab vee krüoskoopilist konstanti; m on osakeste (antud juhul ioonide) molaalne kontsentratsioon mol(ioone)/kg(lahusti). a) Arvutage, kui suur on teelõigu puhastamiseks vajalik keedusoola mass (kg). (4) b) Arvutage, millise temperatuurini on võimalik jää sulamistemperatuuri keedusoola abil alandada, kui keedusoola lahustuvus nendel tingimustel on 30,0 g. (2) Tähelepanu! a) ja b) lõppvastused andke õigete tüvenumbrite arvuga 6 p 2. Ained A, B, C ja D on lämmastiku binaarsed ühendid perioodilisustabeli ühe ja sama rühma elementidega. Ühend A on lenduv kahvatukollane õlijas vedelik, mille esimesena sünteesis aastal Dulong, juhtides Cl 2 läbi hapestatud NH 4 Cl lahuse. Ühend A on väga ebastabiilne ja laguneb pisimagi löögi toimel. Selle omaduse mittetundmise tõttu kaotas Dulong kolm sõrme ja ühe silma. Ühend A võib moodustuda (mitteohtlikul hulgal) basseinivee desinfitseerimisel klooriga. Uriinis ja higis sisalduv karbamiid [(NH 2 ) 2 CO] reageerib klooriveega, andes ühendi A, gaasi E ja tugeva binaarse mineraalhappe F. Hape F moodustus ka Dulongi katses. Ainet A saab sünteesida ka NH 4 Cl vesilahuse elektrolüüsil, kus kõrvalsaadustena moodustuvad vesinik ja gaas G. Gaasi G toimel värvub fenoolftaleiiniga immutatud filterpaber punaseks. Ühend B sünteesiti alles aastal ühenditest (Me 3 Si) 2 NBr ja ClBr temperatuuril 78 0 C. Sünteesi teiseks saadusaineks on trimetüülklorosilaan. Kristalse joodi reageerimisel ammoniaakhüdraadiga moodustuvad ammooniumjodiid ja vesi ning ühendi C kompleks, mille molekulis (446 g/mol) on ligandideks ammoniaagi molekulid. Puhtal kujul võib ühendit C saada boornitriidi reaktsioonil ühendiga IF, kus moodustub ka boorfluoriid. Ühendid B ja C lagunevad eksotermiliselt löögi toimel lihtaineteks. Suhteliselt püsiv on ühend D, mida sünteesitakse fluorist ja ammoniaagist vaskkatalüsaatoril. Reaktsioonisaaduseks on veel vesinikfluoriid. a) Kirjutage ühendite i) A G valemid ja nimetused, ii) ühendi trimetüülklorosilaani valem. iii) Arvutage ühendi C kompleksmolekuli valem. (4) b) Kirjutage reaktsioonivõrrandid: i) A, ii) (NH 2 ) 2 CO + Cl 2 + H 2 O; s elektrolüü iii) NH 4 Cl A, iv) B, v) I2 C kompleks, vi) IF C, vii) C det onatsioon, viii) D. (8) 12 p 3. 2-bromobutaani ja NaCN vahelisel reaktsioonil moodustub ühend A ja sool B. Redutseerides ühendit A vesiniku liiaga Ni pinnal võib saada ühendi C, mis kuulub hästituntud orgaaniliste ühendite klassi X. Ühendi A osalisel happelisel hüdrolüüsil moodustuvad ühendi D kristallid, mida võib LiAlH 4 abil vee juuresolekul redutseerida ühendiks C. Ühendi D üheks laboratoorse saamise viisiks on 2 metüülbutanoüülkloriidi reaktsioon ammoniaagiga. Benseeni töötlemisel lämmastikhappe ja väävelhappe seguga moodustub monoderivaat E. Selle derivaadi redutseerimisel Sn ja HCl seguga moodustub ühend F, mis kuulub samuti orgaaniliste ühendite aineklassi X. a) Kuidas nimetatakse orgaaniliste ühendite aineklassi X, kuhu kuuluvad ühendid C ja F? (0,5) b) Kirjutage ainete A, B, C, D, E ja F graafilised valemid ja nimetused. (5,5)
4 c) Kirjutage reaktsioonivõrrandid: i) 2 bromobutaan + NaCN, ii) 2 metüülbutanoüülkloriid + NH 3 ja iii) benseen E. (3) 9 p 4. Al on maakoores kõige levinum metall. Seda toodetakse mineraal boksiidist, mille koostis antakse valemiga: AlO x (OH) 3-2x, kus 0 < x < 1. Puhas Al 2 O 3 saadakse boksiidist (sisaldab lisanditena SiO 2 ja Fe 2 O 3 ), kasutades Al amfoteersust. Metallilist Al toodetakse sula (940 0 C) elektrolüüdi elektrolüüsil grafiitelektroodidega. Na 3 AlF 6, CaF 2 ja AlF 3 sulandis lahustatakse Al 2 O 3, mis dissotsieerub vastavalt võrrandile Al 2 O 3 Al AlO 3. Elektrolüüsi käigus anood põleb eraldunud hapnikus. Anioonist moodustub Al2O 3, mis dissotsieerub vastavateks ioonideks. a) Kirjutage reaktsioonivõrrandid: i) Al 2 O 3 +NaOH kompleksühend; ii) kompleksühend hüdroksiid; iii) hüdroksiid Al 2 O 3 (3) b) Kirjutage i) katoodprotsessi, ii) anoodprotsessi ja iii) summaarse elektrolüüsiprotsessi (reaktsioonide) võrrandid. (3) c) Arvutage elektrolüüseris kasutatud vool, kui täpselt ühe nädala jooksul toodeti 800 kg Al ja voolukaod olid 5,0%. (2) d) Arvutage täpselt ühe tonni Al tootmiseks kulunud elektrienergia maksumus, kui elektrolüüseris kasutatav pinge on 6,00 V ja 1 kwh hind on täpselt 1 kroon. (3) 11 p 5. KClO 4 lahustuvuse uurimiseks tehti kaks järgmist katset. I 50,0 ml destilleeritud vees püüti 4 0 C juures lahustada 1,30 g KClO 4, millest 0,59 g jäi lahustumatuks. Lahuse ruumala suurenes 0,3 cm 3 võrra. II 70,0 g perkloorhappe lahuses (1,00 g/cm 3 ; ph = 2,0) püüti lahustada 1,30 g KClO C juures. Saadud lahuse tihedus oli 1,01 g/cm 3. Molaarne lahustuvus (L M ) näitab antud temperatuuril lahustunud aine maksimaalset moolide arvu ühes liitris lahuses. a) Arvutage L M (KClO 4 ) destilleeritud vees 4 0 C juures. (3) b) Arvutage LK(KClO 4 ) (lahustuvuskorrutis) 4 0 C juures. (1) c) Arvutage katse II HClO 4 lahuses i) c( ClO 4 ) (molaarne kontsentratsioon) ja ii) L M ' (KClO 4 ) (4) d) Arvutage kaaliumperkloraadi lahustuvus [L(KClO 4 ] täpselt 100 g HClO 4 lahuses (katse II). (3) e) Arvutage katses II mittelahustunud soola mass. (1) 12 p 6. Metallid A, B ja C asuvad 4. perioodis. Metallid D ja E asuvad samas rühmas teineteise järel. Vesilahused, mis sisaldavad ioone D 3+ ja E 3+, on värvitud. Ioone A 2+ sisaldav vesilahus on taevasinine, ioone B 2+ sisaldav vesilahus on aga rohekas. NaOH ja A 2+ vahelisel reaktsioonil moodustuv sinine sade laguneb kuumutamisel veeks ja musta värvi oksiidiks. D 3+ ja NaOH reaktsioonil moodustunud valge sade kaotab kuumutamisel vee ja annab kollase oksiidi (465,96 g/mol). Metallide A ja B järjenumbrid erinevad 1 võrra, B ja C järjenumbrid aga 3 võrra. a) i) Kirjutage metalli D hüdroksiidist oksiidi saamise reaktsiooni võrrand. ii) Arvutage D aatommass ja iii) kirjutage selle sümbol ning nimetus. (3) b) Kirjutage metallide A, B, C ja E sümbolid ja nimetused. (4) c) Kirjutage ioonide A 2+, B 2+ ja C 2+ reaktsioonivõrrandid kloriidiooni ja vee molekulidega, kui on teada, et A 2+ moodustab tetraakvakompleksi ning B 2+ ja C 2+ moodustavad heksaakvakompleksid. (3) 10 p
5 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 12. klass 1. Väga aktiivne metall A avastati alles a. Bunseni poolt spektri kahe tumepunase joonena. Nendest spektrijoontest on tulnud ka metalli A nimetus. Metalli A põlemisel õhus moodustub kolmeaatomiline ühend B. Ühend B on võimeline reageerima metalliga A, moodustades kolmeaatomilise ühendi C. Ühendi C redutseerimisel vesinikuga moodustuvad hästidissotsieeruv ühend D ja ühend I. Ühendi I reageerimisel veega moodustuvad vesinik ja ühend D. Ühendi B reageerimisel nii vee kui väävelhappega moodustuvad lihtaine X ja ühend Q. Lihtaine X tekib ka ühendi Q lagunemisel. Reageerimisel veega saame ühendist B veel ühendi D, väävelhappega aga ühendi E. Ühendi E reageerimisel baariumhüdroksiidiga saame ühendi D. Ühendi D reageerimisel süsinikdioksiidiga moodustub happeline sool F, ammooniumkarbonaadiga aga happelisele soolale F vastav neutraalne sool G. Soola G reageerimisel vesinikjodiidiga tekib binaarne ühend H, milles metalli A sisaldus on 40,25%. a) Tõestage arvutustega metall A ja kirjutage selle sümbol ja nimetus. (1,5) b) Kirjutage ainete B, C, D, E, F, G, H, I, X ja Q valemid ja nimetused. (5) c) Kirjutage reaktsioonivõrrandid: i) B, ii) C, iii) C D, iv) I D, v) B + H 2 O, vi) B + H 2 SO 4, vii) Q X, viii) E D, ix) D F, x) D G, xi) G H (5,5) 12p 2. Radioaktiivsete ainete hoidlas oli ampull, milles oli 10,0 g valget samaariumoksiidi (Sm 2 O 3 ). Preperaadi aktiivsus oli 89,2 Bq/1 g (Bq bekrell; üks lagunemine sekundis). Radioaktiivsuse põhjustab samaariumis isotoop 147 Sm (τ ½ = 1, aastat). Samaariumoksiidi valmistamisest oli möödunud täpselt 5 aastat (aastas on 365,25 päeva) ja preparaadis ei olnud valmistamise momendil teiste elementide radioaktiivseid isotoope. a) Arvutage, mitme aasta möödudes on 10% esialgsetest radioaktiivsetest aatomitest lagunenud. (2) b) Arvutage, mitu protsenti esialgsest radioaktiivsest kogusest (100%) on alles 5 aasta möödudes. (1) c) Kasutades punkti b) tulemust, arvutage isotoobi 147 Sm ligikaudne protsendiline sisaldus samaariumis. (4) d) Arvutage täpselt 5 aasta jooksul isotoobi 147 Sm lagunenud tuumade ligikaudne arv 10,0 grammis samaariumoksiidis k t = ln (c 0 /c t ) (2) Märkus. Kui üks suurustest on teistega võrreldes kaduvväike, siis võib rakendada lähendust. 9 p 3. Optiliselt aktiivsel α-aminohappel X (C 4 H 8 NO 2 Cl) on kaks kiraalset tsentrit. Ühendi X reageerimisel NaOH lahusega moodustub ühend Y, mille koostises ei ole kloori ega ka naatriumi. Ühendi Y spekter viitab molekulis intramolekulaarse vesiniksideme olemasolule. Ühendi X reageerimisel NaOH liiaga moodustub ühend Z (C 4 H 8 NO 3 Na). Tähistame ühendi X S,S-isomeeri sümboliga SX. Ühendi SX redutseerimisel reagendiga NaBH 4 moodustub ühend M. Asendusreaktsioonis PCl 5 abil moodustub ühendist M ühend N. a) Joonistage ühendite X, Y ja Z Fischeri projektsioonid, kus tärniga ( * ) märkige kiraalsed tsentrid. (4) b) Joonistage intramolekulaarse vesiniksidemega molekuli Y graafiline valem. (1) c) Kasutades ruumilisi struktuurivalemeid (, ), kirjutage reaktsiooniskeem SX M N (3) 8 p
6 4. Terasdetailidelt rooste eemaldamise parimaks vahendiks on ortofosforhappe lahus. Oksiidi kihi eemaldamine toimub märgatavalt suurema kiirusega, kui metalli reageerimine ortofosforhappega. Raud(III)ioonid sadenevad nii raudhüdroksiidi kui raudfosfaadina. Ortofosforhappe dissotsiatsioonikonstandi väärtused on: K 1 = 7, M; K 2 = 6, M; K 3 = 1, M. 0,1000 M H 3 PO 4 dissotsiatsiooniaste α 3 = 3, LK(FePO 4 ) = 10-21,9, LK(Fe(OH) 3 = 10-37,4 a) Kirjutage ioonvõrrandid: i) Fe 2 O 3 + H + ; ii) Fe + H + ; iii) Fe PO 4 ; iv) Fe 3+ + OH - Märkus: H + saadakse ortofosforhappest. (2) b) Arvutage i) 0,100 M H 3 PO 4 lahuse ja ii) M H 3 PO 4 lahuse ph täpsusega, mis vastab kontsentratsiooni täpsusele. Põhjendage arvutust! (4) c) Arvutage [Fe 3+ ], kui FePO 4 sade on tasakaalus i) puhta veega ja ii) 0,100 M H 3 PO 4 lahusega. (4) 10 p 5. Elemendist A valmistatud preparaate kasutatakse meditsiinis aastatuhandeid. Üheks esimeseks ravimpreparaadiks oli erkpunase värvusega mineraal, mis on elemendi A binaarseks ühendiks elemendiga B. Elemendi B järjenumber on elemendi A järjenumbrist 5 korda erinev. Elementi A saadakse ühendi AB kuumutamisel õhuvoolus C juures. Eraldub värvitu, terava lõhnaga gaas C. Elemendi B redutseerimisel naatriumiga moodustub ühend D. Ühend D ja gaas C annavad ühendi E ja lisaks eraldub element B lihtainena. Ühend E kristalliseerub 5 veega ja seda kasutatakse nii jodomeetrias kui ka vastumürgina tsüaniidi mürgituse puhul. Elemendi A lahustuvate soolade reageerimisel leelisega saadakse oksiidid F ja G. Oksiidi F molaarmass moodustab 51,9% oksiidi G molaarmassist. a) Kirjutage ainete A, B, C, D, E, F ja G valemid (sümbolid) ja nimetused. (3,5) b) Kirjutage reaktsioonivõrrandid: i) AB A + C; ii) B + Na D ; iii) D + C E + +B; iv) E + I 2 NaI + ; v) KCN + E KSCN +.; vi) A nitraat + NaOH F; ' vii) A nitraat + NaOH G (7) c) Arvutage oksiidide F ja G molaarmassid. (0,5) 11 p 6. 4,5-dihüdroksü-1-fenüülheksaan-3-ooni (X) sünteesiskeem on järgmine: O EtCl AlCl 3 A i) ii) o B K 2 Cr 2 O 7 H 2 SO 4 Br iii) X OsO 4 ROH C AlCl 3 iv) D KMnO 4 H 2 O v) COOH E F CH 3 C CH O vi) AlCl 3 Ühendid C ja E sisaldavad kloori. Reaktsioonides kasutatavad reagendid on järgmised: Mg; OsO 4 /ROH; SOCl 2 ; H 2 /Pd(BaSO 4 ); Br 2 /hν; 1. B 2 H 6, 2. H 2 O 2 /NaOH. a) Kirjutage ainete A F graafilised struktuurvalemid. (6) b) Kirjutage reagendid i) vi). (3) c) Kirjutage ühendi X graafiline struktuurvalem. (1) 10 p
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
ETTEVALMISTUS KEEMIAOLÜMPIAADIKS II
 ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
Keemiliste elementide perioodilisustabel
 Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
IChO 2014, ülesanne 4
 IChO 2014, ülesanne 4 Zeise sool, K[PtCl3C2H4], oli üks esimesi metallorgaanilisi ühendeid. Kopenhaageni ülikooli professor W. C. Zeise valmistas selle ühendi lisades PtCl4-le keevas etanoolis kaaliumkloriidi
IChO 2014, ülesanne 4 Zeise sool, K[PtCl3C2H4], oli üks esimesi metallorgaanilisi ühendeid. Kopenhaageni ülikooli professor W. C. Zeise valmistas selle ühendi lisades PtCl4-le keevas etanoolis kaaliumkloriidi
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
=217 kj/mol (1) m Ühe mooli glükoosi sünteesil lihtainetest vabaneb footoneid: Δ H f, glükoos n (glükoos) =5,89 mol (1) E (footon)
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
( ) ( ) 2008/2009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
b) Täpne arvutus (aktiivsete kontsentratsioonide kaudu) ph arvutused I tugevad happed ja alused
 ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
32. Rahvusvaheline keemiaolümpiaad
 32. Rahvusvaheline keemiaolümpiaad Kopenhaagen Neljapäeval, 6. juulil 2000 TERIAVR TÄELEPANU! Kirjutage iga probleemi esimese lehe ülemisse nurka oma nimi ja kood. Sama probleemi järgnevatele lehtedele
32. Rahvusvaheline keemiaolümpiaad Kopenhaagen Neljapäeval, 6. juulil 2000 TERIAVR TÄELEPANU! Kirjutage iga probleemi esimese lehe ülemisse nurka oma nimi ja kood. Sama probleemi järgnevatele lehtedele
5. a) ρ (g/cm 3 ) = 0,119 = 11,9% 12% 2 p
 201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
1998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut
 Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Vektorid II. Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale
 Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
ORGAANILINE KEEMIA ANDRES TALVARI
 ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
HAPNIKUTARBE INHIBEERIMISE TEST
 HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ
 ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Sissejuhatus mehhatroonikasse MHK0120
 Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat
 Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
PLASTSED DEFORMATSIOONID
 PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
Leelismetallid, I A Li liitium, Na naatrium, K kaalium, Rb, Cs, Fr
 Leelismetallid, I A Li liitium, Na naatrium, K kaalium, Rb, Cs, Fr Li Na K Z 3 11 19 A r 6.941 22.990 39.098 El.neg. 1.0 0.97 0.8 st, C 180.5 97.8 63.2 kt, C 1317 890 753.8 ρ, g/cm 3 0.534 0.971 0.862
Leelismetallid, I A Li liitium, Na naatrium, K kaalium, Rb, Cs, Fr Li Na K Z 3 11 19 A r 6.941 22.990 39.098 El.neg. 1.0 0.97 0.8 st, C 180.5 97.8 63.2 kt, C 1317 890 753.8 ρ, g/cm 3 0.534 0.971 0.862
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
panagiotisathanasopoulos.gr
 . Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
. Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
KEEMIA ÜLESANNETE LAHENDAMINE II
 KEEMIA ÜLESANNETE LAHENDAMINE II ÜLESANDED JA LAHENDUSED Ülesanne 1 Ülesanne Ülesanne Vana münt diameetria, cm ja paksusea,0 mm on tehtud puhtast kullast (ρ = 1900 k m ). Kulla hind on 410$ ühe untsi eest
KEEMIA ÜLESANNETE LAHENDAMINE II ÜLESANDED JA LAHENDUSED Ülesanne 1 Ülesanne Ülesanne Vana münt diameetria, cm ja paksusea,0 mm on tehtud puhtast kullast (ρ = 1900 k m ). Kulla hind on 410$ ühe untsi eest
24. Balti keemiaolümpiaad. Teooriavoor. 9. aprill 2016 Tartu, Eesti
 24. Balti keemiaolümpiaad Teooriavoor 9. aprill 2016 Tartu, Eesti Juhised Kirjutage oma nimi ja kood igale lehele. Teil on ülesannete lahendamiseks 5 tundi. Alustage alles siis, kui on antud START märguanne.
24. Balti keemiaolümpiaad Teooriavoor 9. aprill 2016 Tartu, Eesti Juhised Kirjutage oma nimi ja kood igale lehele. Teil on ülesannete lahendamiseks 5 tundi. Alustage alles siis, kui on antud START märguanne.
Sissejuhatus. 44 th IChO Teoreetiline voor. Ametlikeesti keelne version.
 Sissejuhatus Kirjutage oma nimi ja kood igale vihiku leheküljele. Teoreeiline voor koosneb 8 ülesandest ja perioodilisustabelist, kokku 49 leheküljel. Teoreetilise vooru lahendamiseks on aega 5 tundi.
Sissejuhatus Kirjutage oma nimi ja kood igale vihiku leheküljele. Teoreeiline voor koosneb 8 ülesandest ja perioodilisustabelist, kokku 49 leheküljel. Teoreetilise vooru lahendamiseks on aega 5 tundi.
HULGATEOORIA ELEMENTE
 HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
Lokaalsed ekstreemumid
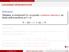 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Ca +2 K + Mg +2 H + Al +3 Na + Zn +2 S -2 NO 3. ΑΣΚΗΣΗ 1-Συμπληρώστε κατάλληλα, τα κενά του πίνακα με τα ονόματα και τους χημικούς τύπους των ενώσεων.
 Σελίδα: 1 Φ.Εργασίας Χημεία Α Λυκείου Κεφ. 2 ΤΟΛΟΓΙΑ / ΑΟ /ΧΗΜΙΚΟΙ ΤΥΠΟΙ / Mr - Επιμέλεια: Παναγιώτης Κουτσομπόγερας Όνομα & Επώνυμο : Τάξη: Ημερομηνία: ΤΥΠΟΣ Cl -1 CaCl 2 ΑΣΚΗΣΗ 1-Συμπληρώστε κατάλληλα,
Σελίδα: 1 Φ.Εργασίας Χημεία Α Λυκείου Κεφ. 2 ΤΟΛΟΓΙΑ / ΑΟ /ΧΗΜΙΚΟΙ ΤΥΠΟΙ / Mr - Επιμέλεια: Παναγιώτης Κουτσομπόγερας Όνομα & Επώνυμο : Τάξη: Ημερομηνία: ΤΥΠΟΣ Cl -1 CaCl 2 ΑΣΚΗΣΗ 1-Συμπληρώστε κατάλληλα,
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
2 η ΕΞΕΤΑΣΤΙΚΗ ΠΕΡΙΟΔΟΣ. Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Α1. Να βρεθεί η δομή των παρακάτω ατόμων: 23 11 Na, 40 20 Ca, 33 16 S, 127 53 I, 108
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Α1. Να βρεθεί η δομή των παρακάτω ατόμων: 23 11 Na, 40 20 Ca, 33 16 S, 127 53 I, 108
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
2005/2006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. = 52,5 g/mol
 005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
Kordamiseks Anorgaanilised ained täiendus loengule (2 loeng) Kaalium K Naatrium Na Leelismetallid - keemiliselt väga reaktsioonivõimelised.
 Kordamiseks Anorgaanilised ained täiendus loengule 13.09.05 (2 loeng) Kaalium K Naatrium Na Leelismetallid - keemiliselt väga reaktsioonivõimelised. Saadakse soolade elektrolüüsil (sulatatud ühendid) 2
Kordamiseks Anorgaanilised ained täiendus loengule 13.09.05 (2 loeng) Kaalium K Naatrium Na Leelismetallid - keemiliselt väga reaktsioonivõimelised. Saadakse soolade elektrolüüsil (sulatatud ühendid) 2
AΝΑΛΟΓΙΑ ΜΑΖΩΝ ΣΤΟΧΕΙΩΝ ΧΗΜΙΚΗΣ ΕΝΩΣΗΣ
 2 ο Γυμνάσιο Καματερού 1 ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΗΣ ΥΛΗΣ 1. Πόσα γραμμάρια είναι: ι) 0,2 kg, ii) 5,1 kg, iii) 150 mg, iv) 45 mg, v) 0,1 t, vi) 1,2 t; 2. Πόσα λίτρα είναι: i) 0,02 m 3, ii) 15 m 3, iii) 12cm
2 ο Γυμνάσιο Καματερού 1 ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΗΣ ΥΛΗΣ 1. Πόσα γραμμάρια είναι: ι) 0,2 kg, ii) 5,1 kg, iii) 150 mg, iv) 45 mg, v) 0,1 t, vi) 1,2 t; 2. Πόσα λίτρα είναι: i) 0,02 m 3, ii) 15 m 3, iii) 12cm
CaCO 3(s) --> CaO(s) + CO 2(g) H = kj. Näide
 3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
http://ekfe.chi.sch.gr ΦΕΒΡΟΥΑΡΙΟΣ 2010 Πειράματα Χημείας ΑΝΙΧΝΕΥΣΗ ΑΙΘΙΝΙΟΥ-ΑΝΟΡΘΩΣΗ ΤΡΙΠΛΟΥ ΔΕΣΜΟΥ ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΚΑΥΣΗ ΑΙΘΙΝΙΟΥ(ΑΚΕΤΥΛΕΝΙΟΥ)
 http://ekfe.chi.sch.gr 7 η - 8 η Συνάντηση ΦΕΒΡΟΥΑΡΙΟΣ 010 Πειράματα Χημείας ΑΝΙΧΝΕΥΣΗ ΑΙΘΙΝΙΟΥ-ΑΝΟΡΘΩΣΗ ΤΡΙΠΛΟΥ ΔΕΣΜΟΥ ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΚΑΥΣΗ ΑΙΘΙΝΙΟΥ(ΑΚΕΤΥΛΕΝΙΟΥ) ΑΝΙΧΝΕΥΣΗ ΑΛΔΕΥΔΩΝ ΚΑΙ ΑΠΛΩΝ ΣΑΚΧΑΡΩΝ ΟΞΕΙΔΩΣΗ
http://ekfe.chi.sch.gr 7 η - 8 η Συνάντηση ΦΕΒΡΟΥΑΡΙΟΣ 010 Πειράματα Χημείας ΑΝΙΧΝΕΥΣΗ ΑΙΘΙΝΙΟΥ-ΑΝΟΡΘΩΣΗ ΤΡΙΠΛΟΥ ΔΕΣΜΟΥ ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΚΑΥΣΗ ΑΙΘΙΝΙΟΥ(ΑΚΕΤΥΛΕΝΙΟΥ) ΑΝΙΧΝΕΥΣΗ ΑΛΔΕΥΔΩΝ ΚΑΙ ΑΠΛΩΝ ΣΑΚΧΑΡΩΝ ΟΞΕΙΔΩΣΗ
Θέμα Α. Ονοματεπώνυμο: Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Διαγώνισμα Χημείας Α Λυκείου
 1 Διαγώνισμα Χημείας Α Λυκείου 2 ο Κεφάλαιο... Θέμα 1 ο... 1.1. Να συμπληρωθούν τα κενά... Η εξωτερική στιβάδα ενός ατόμου δε μπορεί να περιέχει περισσότερα από... ηλεκτρόνια. Ειδικότερα αν αυτή είναι
1 Διαγώνισμα Χημείας Α Λυκείου 2 ο Κεφάλαιο... Θέμα 1 ο... 1.1. Να συμπληρωθούν τα κενά... Η εξωτερική στιβάδα ενός ατόμου δε μπορεί να περιέχει περισσότερα από... ηλεκτρόνια. Ειδικότερα αν αυτή είναι
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
προσθέτουµε 500ml ΗΝΟ ( ) ) . Επίσης, θ = 25 C
 Θέµ ο ( ) ( ) προσθέτουµε 500ml ΗΝΟ ( ) ) Α ιθέτουµε διάλυµ όγκου 500ml που περιέχει τις σθενείς βάσεις Β κι Γ µε συγκεντρώσεις 0,4Μ γι την κάθε µί Στο διάλυµ διλύµτος συγκέντρωσης 0,8Μ κι προκύπτει διάλυµ
Θέµ ο ( ) ( ) προσθέτουµε 500ml ΗΝΟ ( ) ) Α ιθέτουµε διάλυµ όγκου 500ml που περιέχει τις σθενείς βάσεις Β κι Γ µε συγκεντρώσεις 0,4Μ γι την κάθε µί Στο διάλυµ διλύµτος συγκέντρωσης 0,8Μ κι προκύπτει διάλυµ
ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΕΡΙΕΧΟΝΤΑΙ ΚΑΙ ΟΙ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ)
 ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΕΡΙΕΧΟΝΤΑΙ ΚΑΙ ΟΙ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ) ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 9 ΙΟΥΝΙΟΥ
ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΕΡΙΕΧΟΝΤΑΙ ΚΑΙ ΟΙ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ) ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 9 ΙΟΥΝΙΟΥ
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ A ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΥΡΙΑΚΗ 23/04/ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6)
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ A ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΥΡΙΑΚΗ 23/04/2017 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ A ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΥΡΙΑΚΗ 23/04/2017 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi
 Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2015 Β ΦΑΣΗ Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ ÅÍ-ÔÁÎÇ ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 15 Απριλίου 2015 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 15 Απριλίου 2015 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον
ΑΠΑΝΤΗΣΕΙΣ ΤΩΝ ΘΕΜΑΤΩΝ
 ΑΘΗΑ - ΕΞΕΤΑΖΟΕΝΗ ΥΛΗ ΧΗΕΙΑ Γ ΛΥΚΕΙΟΥ ΚΑΘΗΓΗΤΗΣ ΤΗΑ ΠΑΡΑΡΤΗΑ ΔΙΑΡΚΕΙΑ 3 ΩΡΕΣ ΘΕΑ Α ΑΠΑΝΤΗΣΕΙΣ ΤΩΝ ΘΕΑΤΩΝ Α1. 3, Α2. 3, Α3. 2, Α4. 3 Α5. 1. Λάθος, 2. Λάθος, 3. Σωστό, 4. Λάθος, 5. Σωστό. ΘΕΑ Β Β1. Ι) 1.
ΑΘΗΑ - ΕΞΕΤΑΖΟΕΝΗ ΥΛΗ ΧΗΕΙΑ Γ ΛΥΚΕΙΟΥ ΚΑΘΗΓΗΤΗΣ ΤΗΑ ΠΑΡΑΡΤΗΑ ΔΙΑΡΚΕΙΑ 3 ΩΡΕΣ ΘΕΑ Α ΑΠΑΝΤΗΣΕΙΣ ΤΩΝ ΘΕΑΤΩΝ Α1. 3, Α2. 3, Α3. 2, Α4. 3 Α5. 1. Λάθος, 2. Λάθος, 3. Σωστό, 4. Λάθος, 5. Σωστό. ΘΕΑ Β Β1. Ι) 1.
ΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΚΕΦ. 1-3
 ΘΕΜΑ 1 ΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΚΕΦ. 1-3 1. Ποια από τις παρακάτω τετράδες κβαντικών αριθµών n,, m, και ms περιγράφουν ένα από τα ηλεκτρόνια σθένους στη θεµελιώδη κατάσταση για το άτοµο του στροντίου
ΘΕΜΑ 1 ΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΚΕΦ. 1-3 1. Ποια από τις παρακάτω τετράδες κβαντικών αριθµών n,, m, και ms περιγράφουν ένα από τα ηλεκτρόνια σθένους στη θεµελιώδη κατάσταση για το άτοµο του στροντίου
Andmeanalüüs molekulaarbioloogias
 Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
1. Arrhenius. Ion equilibrium. ก - (Acid- Base) 2. Bronsted-Lowry *** ก - (conjugate acid-base pairs) HCl (aq) H + (aq) + Cl - (aq)
 Ion equilibrium ก ก 1. ก 2. ก - ก ก ก 3. ก ก 4. (ph) 5. 6. 7. ก 8. ก ก 9. ก 10. 1 2 สารล ลายอ เล กโทรไลต (Electrolyte solution) ก 1. strong electrolyte ก HCl HNO 3 HClO 4 NaOH KOH NH 4 Cl NaCl 2. weak
Ion equilibrium ก ก 1. ก 2. ก - ก ก ก 3. ก ก 4. (ph) 5. 6. 7. ก 8. ก ก 9. ก 10. 1 2 สารล ลายอ เล กโทรไลต (Electrolyte solution) ก 1. strong electrolyte ก HCl HNO 3 HClO 4 NaOH KOH NH 4 Cl NaCl 2. weak
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002
 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
Kehade soojendamisel või jahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks.
 KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ. Αριθμός νετρονίων (n) Ca 20 40 CL - 17 18 H + 1 1 Cu + 63 34 Ar 22 18. Μαζικός αριθμός (Α) Αριθμός πρωτονίων (p + )
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΘΕΜΑ Α α) Να συμπληρωθεί ο παρακάτω πίνακας : ΣΤΟΙΧΕΙΟ Ατομικός αριθμός (Ζ) Μαζικός αριθμός (Α) β) Ερωτήσεις πολλαπλής επιλογής. Να επιλέξετε την σωστή απάντηση a) Σε ένα άτομο μικρότερη
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΘΕΜΑ Α α) Να συμπληρωθεί ο παρακάτω πίνακας : ΣΤΟΙΧΕΙΟ Ατομικός αριθμός (Ζ) Μαζικός αριθμός (Α) β) Ερωτήσεις πολλαπλής επιλογής. Να επιλέξετε την σωστή απάντηση a) Σε ένα άτομο μικρότερη
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Θετικής Κατεύθυνσης Χημεία Γ Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ ΚΑΛΟΓΝΩΜΗΣ ΗΛΙΑΣΚΟΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Θετικής Κατεύθυνσης Χημεία Γ Λυκείου ΚΑΛΟΓΝΩΜΗΣ ΗΛΙΑΣΚΟΣ e-mail: info@iliaskosgr wwwiliaskosgr 0 2 7 1s 2s ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ 2p 3s 14 2 2 6
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Θετικής Κατεύθυνσης Χημεία Γ Λυκείου ΚΑΛΟΓΝΩΜΗΣ ΗΛΙΑΣΚΟΣ e-mail: info@iliaskosgr wwwiliaskosgr 0 2 7 1s 2s ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ 2p 3s 14 2 2 6
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014. ÄÉÁÍüÇÓÇ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ ΧΗΜΕΙΑΣ
 Θέμα Α Α1. δ Α. γ Α. α Α4. β Α5. δ ΑΓ.ΚΩΝΣΤΑΝΤΙΝΟΥ 11 -- ΠΕΙΡΑΙΑΣ -- 185 -- ΤΗΛ. -4475, 4687 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ ΧΗΜΕΙΑΣ Θέμα Β Β1. α. F: περίοδος, VIIA ομάδα Na: περίοδος, IA ομάδα Κ: 4 περίοδος, IA ομάδα
Θέμα Α Α1. δ Α. γ Α. α Α4. β Α5. δ ΑΓ.ΚΩΝΣΤΑΝΤΙΝΟΥ 11 -- ΠΕΙΡΑΙΑΣ -- 185 -- ΤΗΛ. -4475, 4687 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ ΧΗΜΕΙΑΣ Θέμα Β Β1. α. F: περίοδος, VIIA ομάδα Na: περίοδος, IA ομάδα Κ: 4 περίοδος, IA ομάδα
ΟΝΟΜΑΣΙΑ F - HF Υδροφθόριο S 2- H 2 S Υδρόθειο Cl - HCl Υδροχλώριο OH - H 2 O Οξείδιο του Υδρογόνου (Νερό) NO 3 HNO 3. Νιτρικό οξύ SO 3 H 2 SO 3
 1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
Funktsiooni diferentsiaal
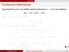 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Energiabilanss netoenergiavajadus
 Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) ( ) ΘΕΜΑ Α Α1.
 Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) (5 2 2017) ΘΕΜΑ Α Α1. Επιλέξτε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις : 1. Σε ποια από τις επόμενες ενώσεις το χλώριο έχει μεγαλύτερο αριθμό
Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) (5 2 2017) ΘΕΜΑ Α Α1. Επιλέξτε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις : 1. Σε ποια από τις επόμενες ενώσεις το χλώριο έχει μεγαλύτερο αριθμό
ΘΕΜΑΤΑ ΓΡΑΠΤΗΣ ΕΞΕΤΑΣΗΣ ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ. 1.2 H CH 3 OH (µεθυλική αλκοόλη) δεν αντιδρά µε το νερό γιατί έχει Κ α µικρότερη από:
 ΘΕΜΑΤΑ ΓΡΑΠΤΗΣ ΕΞΕΤΑΣΗΣ ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Εάν κάθε τροχιακό
ΘΕΜΑΤΑ ΓΡΑΠΤΗΣ ΕΞΕΤΑΣΗΣ ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Εάν κάθε τροχιακό
REAKTSIOONIKINEETIKA
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
AATOMI EHITUS KEEMILINE SIDE
 TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
Ημερομηνία: Τρίτη 18 Απριλίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ/Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 26/01/2014
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ/Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 26/01/2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.3 να γράψετε το γράμμα που αντιστοιχεί στη σωστή απάντηση δίπλα στον αριθμό
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ/Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 26/01/2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.3 να γράψετε το γράμμα που αντιστοιχεί στη σωστή απάντηση δίπλα στον αριθμό
XHMEIA ΚΑΤΕΥΘΥΝΣΗΣ. Απαντήσεις Θεμάτων Πανελληνίων Επαναληπτικών Εξετάσεων Γενικών Λυκείων. ΘΕΜΑ Α Α1. γ Α2. β Α3. δ Α4. γ Α5. α ΘΕΜΑ Β. Β1. α.
 27 Μαΐου 2015 XHMEIA ΚΑΤΕΥΘΥΝΣΗΣ Απαντήσεις Θεμάτων Πανελληνίων Επαναληπτικών Εξετάσεων Γενικών Λυκείων ΘΕΜΑ Α Α1. γ Α2. β Α3. δ Α4. γ Α5. α ΘΕΜΑ Β Β1. α. Σωστό Το γινόμενο της Κ a ασθενούς οξέος ΗA με
27 Μαΐου 2015 XHMEIA ΚΑΤΕΥΘΥΝΣΗΣ Απαντήσεις Θεμάτων Πανελληνίων Επαναληπτικών Εξετάσεων Γενικών Λυκείων ΘΕΜΑ Α Α1. γ Α2. β Α3. δ Α4. γ Α5. α ΘΕΜΑ Β Β1. α. Σωστό Το γινόμενο της Κ a ασθενούς οξέος ΗA με
Jätkusuutlikud isolatsioonilahendused. U-arvude koondtabel. VÄLISSEIN - COLUMBIA TÄISVALATUD ÕÕNESPLOKK 190 mm + SOOJUSTUS + KROHV
 U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
Ερωηήζεις Πολλαπλής Επιλογής
 Ερωηήζεις Θεωρίας 1. Ππθλφηεηα: α) δηαηχπσζε νξηζκνχ, β) ηχπνο, γ) είλαη ζεκειηψδεο ή παξάγσγν κέγεζνο;, δ) πνηα ε κνλάδα κέηξεζήο ηεο ζην Γηεζλέο Σχζηεκα (S.I.); ε) πνηα ε ρξεζηκφηεηά ηεο; 2. Γηαιπηφηεηα:
Ερωηήζεις Θεωρίας 1. Ππθλφηεηα: α) δηαηχπσζε νξηζκνχ, β) ηχπνο, γ) είλαη ζεκειηψδεο ή παξάγσγν κέγεζνο;, δ) πνηα ε κνλάδα κέηξεζήο ηεο ζην Γηεζλέο Σχζηεκα (S.I.); ε) πνηα ε ρξεζηκφηεηά ηεο; 2. Γηαιπηφηεηα:
Molekulid ei esine üksikuna vaid suurearvuliste kogumitena.
 2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
2.2.1 Geomeetriline interpretatsioon
 2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
ALGEBRA I. Kevad Lektor: Valdis Laan
 ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks
 4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΙΚΩΝ ΜΕ ΠΡΟΣΡΟΦΗΣΗ ΣΕ ΥΔΡΟΞΥ-ΟΞΕΙΔΙΑ ΣΙΔΗΡΟΥ ΑΠO ΤΗΝ ΕΚΡΟΗ ΒΙΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΛΥΜΑΤΩΝ. Κυριακή Καλαϊτζίδου MSc Χημικός Μηχανικός
 ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΙΚΩΝ ΜΕ ΠΡΟΣΡΟΦΗΣΗ ΣΕ ΥΔΡΟΞΥ-ΟΞΕΙΔΙΑ ΣΙΔΗΡΟΥ ΑΠO ΤΗΝ ΕΚΡΟΗ ΒΙΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΛΥΜΑΤΩΝ Κυριακή Καλαϊτζίδου MSc Χημικός Μηχανικός Φώσφορος Θεωρητικό Μέρος Παρουσιάζεται: Ορυκτά Ανθρώπινα
ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΙΚΩΝ ΜΕ ΠΡΟΣΡΟΦΗΣΗ ΣΕ ΥΔΡΟΞΥ-ΟΞΕΙΔΙΑ ΣΙΔΗΡΟΥ ΑΠO ΤΗΝ ΕΚΡΟΗ ΒΙΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΛΥΜΑΤΩΝ Κυριακή Καλαϊτζίδου MSc Χημικός Μηχανικός Φώσφορος Θεωρητικό Μέρος Παρουσιάζεται: Ορυκτά Ανθρώπινα
Χημεία Α ΓΕΛ 15 / 04 / 2018
 Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 7 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6)
 ΑΡΧΗ ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 7 ΙΟΥΝΙΟΥ 003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ ο Για τις ερωτήσεις. -.4 να γράψετε στο
ΑΡΧΗ ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 7 ΙΟΥΝΙΟΥ 003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ ο Για τις ερωτήσεις. -.4 να γράψετε στο
Βασικές γνώσεις Χημείας Λυκείου (Α, Β, Γ)
 Βασικές γνώσεις Χημείας Λυκείου (Α, Β, Γ) Διαλύματα Εκφράσεις περιεκτικότητας α λ% w/v: Σε 100 ml Διαλύματος περιέχονται λ g διαλυμένης ουσίας β λ% w/w: Σε 100 g Διαλύματος περιέχονται λ g διαλυμένης ουσίας
Βασικές γνώσεις Χημείας Λυκείου (Α, Β, Γ) Διαλύματα Εκφράσεις περιεκτικότητας α λ% w/v: Σε 100 ml Διαλύματος περιέχονται λ g διαλυμένης ουσίας β λ% w/w: Σε 100 g Διαλύματος περιέχονται λ g διαλυμένης ουσίας
ΙΑΓΩΝΙΣΜΑ 1 Ο ( 1 Ο ΚΕΦΑΛΑΙΟ)
 ΙΑΓΩΝΙΣΜΑ 1 Ο ( 1 Ο ΚΕΦΑΛΑΙΟ) ΘΕΜΑ 1 Ο Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές και να διορθώσετε τις λανθασµένες: 1. Τα άτοµα όλων των στοιχείων είναι διατοµικά.. Το 16 S έχει ατοµικότητα
ΙΑΓΩΝΙΣΜΑ 1 Ο ( 1 Ο ΚΕΦΑΛΑΙΟ) ΘΕΜΑ 1 Ο Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές και να διορθώσετε τις λανθασµένες: 1. Τα άτοµα όλων των στοιχείων είναι διατοµικά.. Το 16 S έχει ατοµικότητα
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 29 ΜΑΪΟΥ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 1 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 9 ΜΑΪΟΥ 01 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. γ Α. β Α. δ Α4. β Α5.α.i) Βάσεις κατά Arrhenius είναι
1 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 9 ΜΑΪΟΥ 01 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. γ Α. β Α. δ Α4. β Α5.α.i) Βάσεις κατά Arrhenius είναι
