Orgaanilise keemia õpiku küsimuste vastused
|
|
|
- Ἑνώχ Καψής
- 6 χρόνια πριν
- Προβολές:
Transcript
1 rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C C C C C C 7. a) b) C C C C C C C C 1
2 2. ALKAANID 2.1. Alkaanid ja nende nimetused (lk 29) 2. a) n-pentaan, b) 2-metüülheksaan, c) 2,3-dimetüülheksaan, d) 4-etüül-2,3,5,5-tetrametüülheptaan, e) 1,3-dimetüültsükloheksaan, f) 3-etüül-4-isopropüüloktaan ehk 3-etüül-4-(1-metüületüül)oktaan 3. a) b) c) d) C C C C C C C C C C C C C C C C C C C C C C C C C C C C C 4. a) isopropüül- = 1-metüületüülb) isobutüül- = 2-metüülpropüülc) tert-butüül- 1,1-dimetüületüül Isomeeria ja alkaanide esindajad (lk 34) 1. Ainete omadustest ja omaduste liigitamisest on juttu lk 32. Keedusool, suhkur ja vedelgaas on juhuslikud näited, võite neile lisada teisigi tuntud aineid. Küsimuste näiteid Kas vedelgaas on individuaalne ühend või ainete segu? Aga keedusool ja suhkur? Küsimusi füüsikaliste omaduste kohta 1. Milline on nende ainete agregaatolek toatemperatuuril? 2. Milline on nende ainete värvus? 3. Milline on nende ainete sulamistemperatuur? 4. Kas neid on võimalik sulatada ilma lagunemiseta? Küsimusi keemiliste omaduste kohta 1. Kui hästi või halvasti nad lahustuvad vees? 2. Kas nad reageerivad veega? Küsimusi füsioloogiliste omaduste kohta 1. Milline on nende ainete maitse ja lõhn? 2. Kas nad võivad olla inimese organismile kahjulikud või isegi mürgised? 2
3 2. eksaani isomeerid: a) n- heksaan, b) 2-metüülpentaan, c) 3-metüülpentaan, d) 2,2-dimetüülbutaan, e) 2,3-dimetüülbutaan. a) b) c) d) e) Märkus: tsükloheksaan ei ole heksaani isomeer! Miks? 4. Täielik põlemine: C C salisel põlemisel võib tekkida mitmesuguseid saadusi, mis erinevad süsiniku oksüdatsiooniastme poolest, nt 2C C + 4 2, aga ka 2C või C C + 2 jne. 5. Metaanis on süsinik redutseerunud kõige enam võimalikust, ta oksüdatsiooniaste on seal IV. Mistahes alkoholis on vähemalt üks süsiniku aatomitest osaliselt oksüdeerunud. Järelikult? Aga arvutame ka etanooli süsinike keskmise oksüdatsiooniastme (vt ka lk 21): Vesiniku o-a I apniku o-a [ 1 + ( 1) = 2], seega II 1. Süsiniku o-a [ 1 + ( 1) +1 = 1], seega I 2. Süsiniku o-a [ 1 + ( 1) + ( 1) = 3], seega III Süsiniku keskmine o-a [ ( 3) + ( 1) ] / 2 = 2, seega II C C 6. letame, et köögi põrandapind on 6 m 2, nii nagu see on paljudes vanemates korterelamutes. Ruumide standardkõrguse 2,5 m korral on köögi ruumala 15 m 3. Metaani plahvatusohtliku segu alumine piir on 5% (vt lk 23), seega siis võiks enam-vähem 3 (5% 15 m ) 3 3 ohutult lekkida kuni 0,75 m (750 dm ) gaasi. 100% oiatus! See arvutus on tehtud köögi koguruumala suhtes. Lekkiva kraani juures moodustub plahvatusohtlik gaasisegu varem, kui kogu köök gaasiseguga täitub Alkaanide omadused (lk 41) 1. Radikaali määratlus on toodud lk 37. Eristage reaktsioone, mis võivad toimuda radikaalide endaga (nt rekombinatsioon ehk omavahelineühinemine molekuliks) ja reaktsioone, mis kulgevad radikaalide tekkimise ja nende edasise reageerimise teel. Viimastest on juttu lk
4 2. Radikaalil on paardumata elektron ja seetõttu on ta kõrge energiaga ebastabiilne osake. Radikaal püüab selle elektroniga luua elektronipaari kas teise radikaali paardumata elektroniga või ühe elektroniga elektronipaarist, mis moodustab keemilist sidet mingis teises osakeses. Mõlemal juhul tekib madalama energiaga osake, millel pole paardumata elektroni. 3. Alkaani halogeenimine on summaarse võrrandi järgi asendusreaktsioon. Reaktsiooni mehhanismi, s.t protsessi kulgemise täpse kirjelduse alusel on see ahelreaktsioon. Arvutades süsiniku oksüdatsiooniastmed lähteainetes ja saadustes, leiame, et see on alkaani oksüdeerimise reaktsioon. 4. Esiteks peab halogeeni molekul lagunema radikaalideks. Siis peaks halogeeni radikaal ründama süsiniku aatomit, et tõrjuda välja (asendada) vesiniku radikaal, kuid halogeeni radikaal ei saa rünnata süsiniku aatomit kui reaktsioonitsentrit, sest see on varjatud vesiniku aatomite poolt. Seepärast on kõige kättesaadavamaks reaktsioonitsentriks hoopis vesiniku aatom, mille radikaal ära võtab. Nüüd on süsiniku aatomil radikaaltsenter (paardumata elektron) ja see reageerib lõpuks ühe halogeeni molekuliga (vt skeemi lk 39 40). 5. Vaatleme siin sidemete katkemisi ja moodustumisi ainult reaktsiooni summaarse võrrandi alusel, sest tegelikult on need protsessid üpris keerulised ja kulgevad hulga vaheastmete kaudu. a) on katkenud 4 süsinik vesinik-sidet ja moodustunud 2 vesiniku molekuli; b) on katkenud 2 süsinik vesinik-sidet, teine teise süsiniku juures, ja moodustus üks vesiniku molekul; c) on katkenud 2 süsinik vesinik-sidet pentaani ahela otsmiste süsinike juures ja need süsinikud on omavahel uue sideme moodustanud. Saaduseks on ka üks vesiniku molekul. d) C C 6. + C C + C 7. Metaani halogeenimisel (kloorimisel) on paratamatuks vaheühendiks metüülradikaal,mis peaks edasi reageerima kloori molekuliga (vt skeemi lk 39 40), kuid radikaalid võivad ka omavahel ühineda ja nii tekib kahest metüülradikaalist püsiv etaani molekul. Kui palju seda soovimatut kõrvalsaadust tekib, sõltub suurel määral reaktsioonitingimustest, nt kõrgemal rõhul moodustub etaani rohkem. 4
5 8. tsustamiseks arvutage süsiniku keskmised oksüdatsiooniastmed reaktsioonivõrrandite mõlemal poolel! Veel lihtsam on endale teadvustada, et vesiniku eraldumine molekulist on selle aine suhtes oksüdeerumine (pöördprotsess s.t vesiniku liitumine on ju redutseerumine!). 9. Vt täiendavat selgitust lk 38. Loomulikult reageerib kiiremini hargnenud süsinikahelaga 2-metüülpropaan. 10. C + 2 C + Arvestage, et see siin on põhimõtteline võrrand. Võimalike kõrvalsaadustega tegeleb nt järgmine ülesanne. 11. Põhiline reaktsioon oleks järgmine: + 2 C + Selle kõrval kulgeb üsnagi märgatavalt reaktsioon esimese süsiniku juures: Radikaalid, mis vahepeal moodustuvad, võivad anda selliseid reaktsioone (kõrvalsaadusi): C + C C C C + C + Peale selle võivad süsinikradikaalid disproportsioneeruda, nt C + C C + Kui võtta arvesse ka võimalikku dihalogeenimist (vt lk 40), on selge, et radikaalreaktsioonidega tootmisprotsessid ei ole kunagi väga hea saagisega, s.t oodatud sihtprodukti (selles näites 2-kloropropaani) ei teki 100% ulatuses lähteaine suhtes. Sellegipoolest kasutatakse radikaalreaktsioone tööstuslikus tootmises laialdaselt. 5
6 3. ALGEENIÜENDID (LK 66 67) 1. 1) jodotsüklopropaan; 2) 2-kloro-2-metüülpropaan; 3) 1-bromo-2-metüülpropaan; 4) 2-fluoropropaan 2. 1) 1,1-dibromobutaan; 2) 1,2-dibromobutaan; 3) 2,2-dibromobutaan; 5) 1,3-dibromobutaan; 6) 1,4-dibromobutaan; 7) 1,1-dibromo-2-metüülpropaan; 8) 1,2-dibromo-2-metüülpropaan; 9) 1,3-dibromo-2-metüülpropaan 3. δ+ δ δ+ δ δ+ δ δ+ δ I < Br < < F 4. Elektrofiil omastab elektrone Radikaal ühineb elektroniga Nukleofiil loovutab elektrone :N 3 B 3 g 2+ elektrofiil nukleofiil elektrofiil elektrofiil : N 2 : nukleofiil nukleofiil nukleofiil nukleofiil 6. δ+ δ δ+ δ δ+ δ δ+ δ+ δ a) Br b) c) d) δ+ δ+ δ δ+ δ+ δ C e) S f) N 2 δ 6
7 7. See on näidis kolme järgneva ülesande lahendamiseks. 8. Na + δ+ δ + I Ründav osake Lahkuv rühm δ+ δ + Na + I Lahkunud osake 9. K + CN δ+ δ + Br Ründav osake Lahkuv rühm δ+ δ CN + K + Br Lahkunud osake δ+ δ δ+ δ + P 2 + P2 Ründav osake Lahkuv rühm Lahkunud osake + + P2 P 2 Selgitus: kloriidioon ( ) on suhteliselt nõrk nukleofiil, aga anioon P 2 on veelgi nõrgem, kuna nukleofiilsus selles osakeses on hajutatud kahe tugevalt elektronegatiivse kloori aatomi vahel. 11. Sest tetraklorometaanis on süsinik kõrgeimas oksüdatsiooniastmes (IV) ehk rohkem oksüdeeruda pole enam võimalik. 7
8 4. ALKLID (LK 82 83) 2. C C C C C C 3. a) butaan-1-ool (n-butanool) b) butaan-2-ool (sec-butanool) C c) 2-metüülpropaan-1-ool (isobutanool) d) 2-metüülpropaan-2-ool (tert-butanool) C C 4. Rajage põhjendus alkoholide võimele moodustada omavahelisi vesiniksidemeid, mis puudub alküülhalogeniididel. 5. a) kt 78 C, kt 23 C b) ( ) 2 C kt 131 C, ( ) 2 C 32 C Kuna isomeeride molekulmassid on võrdsed, ei peaks nende keemistemperatuurid palju erinema, kuid alkoholide molekulid on omavahel seotud vesiniksidemetega, mistõttu nende keemis-temperatuurid on umbes sada kraadi (!) kõrgemad kui vastavatel eetritel
9 8. Mentool ja kolesterool on mõlemad küll alkoholid, kuid tuleb tähele panna nende süsivesinikosa erinevat suurust. Seepärast on nende sulamistemperatuurid vastavalt 43 Cja149 C. Mentool lahustub vees suhteliselt vähe, kuid lahustub hästi alkoholis. Kolesterool ei lahustu vees ega alkoholis. Küll aga lahustuvad mõlemad mittepolaarsetes lahustites nagu eeter, süsivesinikud jt. 9. Etüleenglükool ehk etaan-1,2-diool ja glütserool ehk propaan-1,2,3-triool on mitmehüdroksüülsed alkoholid, mis võimaldab neil moodustada arvukalt vesiniksidemeid vee molekulidega ja seetõttu seguneda veega (lahustuda) igas vahekorras. 10. Glütserool ja äädikhape segunevad veega igas vahekorras, seepärast kihti ei moodusta. Tsükloheksaan ning bensiin on süsivesinikud, seega veest kergemad ja asuvad ülemises kihis. Tetraklorometaan (ρ = 1,595 g/cm 3 ) on veest raskem. 11. Etanool lahustub vees. eksaan (ρ= 0,66 g/cm 3 ) moodustab pärast veega segamist ülemise kihi, aga dikloroetaan (ρ = 1,257g/cm 3 ) koguneb anuma põhja. 12. a) umbes 6 g eetrit ja b) umbes 8,5 g vett. 13. Kvalitatiivset hinnangut on kerge teha: mida väiksem on osaliselt oksüdeerunud süsiniku ( ) osakaal molekulis, seda suurem on alkoholi kütteväärtus kaaluühiku kohta. Selles võib veenduda keskmiste oksüdatsiooniastmete arvutamise abil. 14. Vein ja eriti õlu sisaldavad peale alkoholi vähesel määral ka muid toitaineid. Üksnes alkoholi alusel tehtud energeetilise väärtuse arvutus annab ligikaudselt: õlu 540 kj, kuiv vein 1180 kj, viski 4600 kj. Piima toiteväärtus (0,5 l 2,5 %-lise rasvasisaldusega piima) on vastavalt 1140 kj. 15. Lihtne hinnang annab 0,29 promilli. 16. Võrdleme elektronstruktuuri hapniku aatomi juures: 17. a) C I + K C + K b) Br + Na + NaBr c) + 2Na + 2Na 9
10 18. Vesi toimib alkoholaadile nii nagu hape soolale: Na Na 19. Vt ka eelmist ülesannet. Na Na Na C 2 + NaC madus Alkoholid Eetrid appelisus nõrk puudub Lahustuvus vees tänu vesiniksidemetele hea vähene Nukleofiilsus/aluselisus väike väike C -side väga püsiv, seepärast asendusreaktsioon süsiniku juures ( -rühma asendamine) toimub vaid erijuhtudel väga püsiv, seepärast asendusreaktsioon süsiniku juures ( -rühma asendamine) toimub vaid erijuhtudel. 21. Metüülalkoholi ja isobutüülalkoholi vahelisel reaktsioonil võivad tekkida järgmised eetrid: a) b) + C C c) C + C C2 C C2 C2 C + 2 Mittesümmeetrilise eetri valmistamiseks on parim lahendus alkoholaadi ja halogenoalkaani vaheline reaktsioon, näiteks: + Na, Na + C C3 C2 C Näites toodud ainete valik on põhjendatud sellega, et a) bromiidid ja jodiidid on palju kallimad b) metüülhalogeniidid (see oleks siis variant al + ( ) 2 C Na) on gaasilised või liiga lenduvad ja seepärast ei võimalda reaktsiooni soojendamise abil kiirendada. 10
11 23. 1kg N 2 ruumala on 878,73 cm 3. Sellise koguse nitrometaani põlemisel eraldub 12 MJ energiat. Järelikult 3500 cm 3 N 2 põlemisel eraldub 36,91 MJ energiat cm 3 N 2 mass on 3, 076 kg ning moolide arv 50,43 mol. 2 N 2 + 1,5 2 N 2 + 2C ,43 mol N 2 põletamiseks kulub 37,82 mol 2 ehk 847,17 dm 3 2 ehk 4236,12 dm 3 õhku sekundis. 1 kg C 8 18 ruumala on 1420,45 cm 3. Sellise koguse oktaani põlemisel eraldub 42 MJ energiat. Järelikult 36,91 MJ energia eraldumiseks on vaja põletada 1248,37 cm 3 ehk 878,85 g ehk 7,71 mol oktaani. C ,5 2 8C ,71 mol oktaani põletamiseks kulub 96,38 mol 2 ehk 2158,91 dm 3 2 ehk 10794,55 dm 3 õhku sekundis. Sama energiahulga saamiseks on alkaani kütuse kogus küll väiksem (1248 cm 3 ja 3500 cm 3 ), kuid õhu tarbimise erinevus suurem ( dm 3 ja 4236 dm 3 ). Tekib puhttehniline probleem: kuidas üldse nii suurt õhu hulka peaaegu momentaalselt põlemiskambrisse sisse suruda. Ja siis keemia natuke aitab! 11
12 5. AMIINID (LK 90) 1. a) + N 2 + C3 N 2 + b) N 2 + C N 3 C C3 + c) C N S 4 C N 3 S 4 2. N + 3. Br + N 3 N 3 + Br N 3+ Br + Na N NaBr 4. Nukleofiilid on a, b ja d, näiteks N + + Br N C2 C2C3 Br N + C N + 3 sakesed c ja e ei saa olla nukleofiilideks, sest kõik lämmastiku elektronipaarid on neis seotud. 5. N N 6. kt on 35 C, ( ) 2 N kt on 55 C ja on 118 C. Eetri molekulid ei moodusta omavahel vesiniksidemeid. Vesiniksidemed amiini molekulide vahel (vt eelmine ülesanne) ei ole väga tugevad (miks?), küll on aga vesiniksidemed tugevad alkoholis. 12
13 6. KÜLLASTUMATA ÜENDID (LK ) 1. σ-sideme kohta lugege lk 15 ning π-sidemest lk Pöörake tähelepanu nende sidemete geomeetriale, s.t nende ruumilisele ehitusele. Teoreetilises plaanis on ehk tähtsam, et neis sidemetes osalevad erineva energiaga elektronid. Kuna π-sideme elektronid on kõrgema energiaga, ei ole see side nii püsiv kui σ-side. 2. Küllastumatus on väga vana nimetus, mis tähistab alkaanide ja alküünide võimet liita vesinikku, halogeeni jt aineid sel viisil, et kaksik- või kolmiksideme asemele jääbsüsinike vahele tavaline (ja tugevam) σ-side. 3. Mittepolaarne kovalentne side. 5. trans-isomeer cis-isomeer 6. Arvutage süsinike oksüdatsiooniastmed mõlemal võrrandi poolel. Vajaduse korral vt eeskuju lk 21. Näeme, et süsiniku oksüdatsiooniaste kasvas ( II)-lt ( I)-le, seega on see oksüdeerimisreaktsioon Valime näiteks tsüklopentaani saamise n-pentaanist: + 2 Need kaks ainet ei saa olla isomeerid, kuna nende atomaarne koostis on erinev. Vesiniku eraldumine molekulist on alati oksüdeerumisprotsess. Selles võid veenduda kui arvutate kummagi ühendi keskmise oksüdatsiooniastme (need on vastavalt 2,4 ja 2). 8. A. Üldisem reaktsioonitüüp on liitumisreaktsioon. B. Alkeenide reaktsioonid algavad elektrofiilse osakese või tsentri rünnakuga ühele süsinikule. C. Küllastumata ühenditega reageerivad vesinik, halogeenid, vesinikhalogeniidid, vesi ja hapnik. 13
14 9. 1) 2) 3) 4) 5) C + 2 C + 2 C C + C C + 2 C C + 2 C + C 10. C C + 2Br 2 Br C C Br Br Br C C + 2Br Br C Br 11. II II III I 2 C + 2 Keskmine II Keskmine II Näeme, et hapniku sisestamine orgaanilise aine molekuli ei ole mitte alati oksüdeerimine. 12. C C [] C C [] C + C 13. C C + 1-kloro-2-metüülpropaan-2-ool C C + 2-metüülpropaan-2-ool 14
15 14. C C + I 2 C + I 3 I C I I C I Kaaliumjodiidi lisamisega tõuseb lahuses jodiidioonide kontsentratsioon, millega suureneb dijodoühendi moodustumisele viiva reaktsiooni osakaal (vee kontsentratsioon jääb ju samaks). 15. C C + I C ning I C I 16. Br C C + 2Br C ning Br Br C Br 18. A-vitamiin Limoneen Pineen Geraniool Mentool 15
16 7. AREENID (LK ) 1. a) 1,4-diklorobenseen; b) 2-nitrotolueen; c) trifenüülmetaan; d) 3-klorotolueen; e) fenüülmetanool; f) 4-nitropüridiin; g) aminobenseen (aniliin); h) 2,5-diklorofuraan 2. N 2 C N 2 C N 2 N N 2 3. A. rgaaniline aine, mille molekulis on üks või mitu aromaatset tuuma. B. Tasandiline suletud tsükkel ning ühtne π-elektronidest koosnev elektronpilv. C. Aromaatne tsükkel on nukleofiilne reaktsioonitsenter. Tema reageerimine algab elektrofiili ühinemisega. 4. VIGA! Vaata tabel lk 222, peab olema II osa lk 99 Fenüülalaniin, Trüptofaan, Türosiin, istidiin. 5. Ühe asendajaga naftaleenil on kaks isomeeri, asendajaga asendis 1 või 2(tähistatakse ka kui α-ja β-isomeeridena). Kahe ühesuguse asendajaga on näiteks 1,4-dimetüülnaftaleen 2,6-dimetüülnaftaleen 1,8-dimetüülnaftaleen 6. a) tsükloheksaan, b) bensoehape 7. eksaan ei reageeri broomiga tavatingimustes. ekseen liidab broomi kergesti, isegi vesilahusest (nn broomiveega reageerides). Benseen reageerib broomiga vaid soojendamisel katalüsaatori juuresolekul Br 2 kat Br + Br 9. N 2 + N 3 2 S
17 10. Klorometüülbenseenis on asendus külgahelas. Seda saab teostada nii nagu alkaanide halogeenimisel, s.t kõrgel temperatuuril ja soovitavalt ultraviolettkiirgust kasutades. t, h klorometüülbenseeni tuleb valmistada elektrofiilse asendusreaktsiooni teel, kasutades katalüsaatorit, nt alumiinium- või raud(iii)kloriidi. Temperatuur ei pea nii kõrge olema ja soovitavalt võiks reaktsiooninõud valguse eest varjata. kat a) b) C C või C C ja edasi reageerib katioon (elektrofiil): + C + C C Nikotiin on amiin. Kui muuta nikotiin ammooniumisoolaks, on ta vees lahustuv ning muust taimsest massist kergesti eraldatav. N N + N N + Niisiis tuleb tubakat happega töödelda ja segu filtreerida. Filtraadile leelise lisamise abil võib nikotiini soola muuta vees lahustumatuks amiiniks ja sel viisil nikotiin eraldada. N N + + Na N N + Na
18 13. Agent range oli preparaatide 2,4D ja 2,4,5T butüülestrite lahus. Viimast neist toodetakse väga lihtsa skeemi järgi: Na + Na + Na + CC 4 9 CC Na 2,4,5-triklorofenoksüetaanhappe butüülester Kahjuks kulgeb ka kõrvalreaktsioon, mille tulemusena tekib üks dioksiinidest: Na + Na + 2 Na Agent range sisaldas dioksiine 3,83 g/m 3. lgu märgitud, et kõik need reaktsioonid on nukleofiilsed asendused. Nukleofiilne asendus aromaatses tuumas ei ole väga tüüpiline aromaatsete ühendite reaktsioon, seepärast ei ole neid meie õpikus käsitletud, kuid nagu ülaltoodust näha, leiavad nad ka tööstuslikku kasutamist. 18
19 7.5. Fenoolid ja aromaatsed amiinid (lk ) 1. a) eeter b) fenool c) alkohol d) alkohol 2. Kresoolid: 2-metüülfenool 3-metüülfenool 4-metüülfenool Resortsiine: 1,3-dihüdroksübenseen 2-metüül- 4-metüül- 5-metüül- -1,3-dihüdroksü- -1,3-dihüdroksü- -1,3-dihüdroksübenseen benseen benseen 2,5-dimetüül- 4,5-dimetüül- 4,6-dimetüül- -1,3-dihüdroksübenseen -1,3-dihüdroksübenseen -1,3-dihüdroksübenseen 3. Fenooli kt on 182 C ja tolueenil 111 C. Tolueen on lihtsalt süsivesinik, aga fenooli molekulid on omavahel vesiniksidemetega seotud sarnaselt vee või alkoholidega. 4. Delokalisatsiooniks nimetatakse kas σ-ja π-sidemete omavahelist ühtlustumist või laengu (elektronipaari) jaotumist π-sidemete osavõtul. Delokalisatsioon stabiliseerib ühendit või osakest (iooni, radikaali), seetõttu on nt benseen küllalt raskesti oksüdeeritav, fenool palju tugevam hape kui alkohol ja aniliin omakorda nõrgem alus kui alküülamiinid. Meenutame siinkohal ka fenoolide ja aromaatsete amiinide lihtsat bromeerimist ja teisi asendusreaktsioone võrdluses asendamata benseeniga. 19
20 5. a) C Na + 3 Na Tasakaalulises segus on etoksiid- ja fenoksiidioon ning naatriumioon, kuid tasakaal on tugevasti nihutatud fenoksiidiooni suunas. b) Na + + Alkohol on sedavõrd nõrk hape, et alkoholaati praktiliselt ei teki. c) + + N 2 + N 3 N 3 + N 2 Tasakaalulises segus on fenüülammoonium- ja etüülammooniumioon ning kloriidioon, kuid tasakaal on tugevasti nihutatud etüülammooniumkloriidi suunas. 6. Br + 3Br 2 Br + 3Br Br Br N 2 + 3Br 2 Br N 2 + 3Br Br 7. + N N 2 + N 3 2 N See on türosiin. Kuna fenoolid nitreeruvad kergesti, siis türosiini fenoolne rühm nitreerub lämmastikhappe toimel ning värvib materjali kollaseks. 20
21 9. A. Kloori nukleofiilne asendamine aromaatses tuumas läheb väga raskesti, küll aga kergelt alifaatse süsiniku juures. + Na + Na B. Benseenituum oksüdeerub väga raskesti, küll aga alifaatsed külgahelad (alküülrühmad). C [] C C. Samal põhjusel, mis eelmises näites. [] C C + 2C 2 D. Alküülamiinid on palju tugevamad alused võrreldes aromaatsete amiinidega. N 2 N N 3 N Sest nad oksüdeeruvad õhuhapniku toimel. Seda näeme nende värvuse muutumisest õhu käes seismisel. Konkreetseid võrrandeid on raske anda, sest protsessid on keerulised. Igatahes moodustuvad muuhulgas ka kondensatsioonisaadused (tsüklite ühinemisega), mis on värvilised. 11. Aniliin on nõrk alus ja seetõttu on tema vesiniksidemed veega väga nõrgad, sellest siis ka vähene lahustuvus vees. Soolhappes moodustub aniliini sool (aniliiniumkloriid), mis lahustub vees hästi. 14. Antioksüdantide ülesanne on võtta endale õhuhapniku rünnak ning sel viisil hoida toiduainet või muud materjali oksüdeerumise eest (toiduainet rääsumise eest). Seega on nad eelkõige redutseerijad. Võiks eristada 1) väävliühendeid E220 E228, mis lihtsalt oksüdeeruvad kõrgema oksüdatsiooniastmega väävli ühenditeks; 2) kergesti oksüdeeruvaid askorbiinhappe (C-vitamiini) derivaate E300 E304, E315, E316; 3) küllastumata ühendeid, mis seovad hapniku oma kaksiksidemete abil E306 E309; 4) fenoolseid ühendeid, mis püüavad radikaale oma aromaatse tuumaga E320, E321, E310 E Koniin ei ole aromaatne ühend, vaid on tsükliline alküülamiin ja seepärast tugev alus. a) N + + N 2 C b) Na 2 + Br + NaBr + 2 N N 21
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
ORGAANILINE KEEMIA. Lühikonspekt gümnaasiumile. Koostaja: Kert Martma
 ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
ORGAANILINE KEEMIA. Lühikonspekt gümnaasiumile. Koostaja: Kert Martma
 ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Sisukord Sissejuhatus orgaanilisse keemiasse Alkaanid Halogeeniühendid Alkoholid Amiinid Küllastamata ühendid Areenid
ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Sisukord Sissejuhatus orgaanilisse keemiasse Alkaanid Halogeeniühendid Alkoholid Amiinid Küllastamata ühendid Areenid
ORGAANILINE KEEMIA I osa
 ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
SÜSIVESINIKUD. Kaido Viht
 SÜSIVSINIKUD Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2016 Süsivesinike struktuurid Käesolevas materjalis selgitame mõningaid süsivesinikele iseloomulikke reaktsioone. Süsivesinikud, nagu
SÜSIVSINIKUD Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2016 Süsivesinike struktuurid Käesolevas materjalis selgitame mõningaid süsivesinikele iseloomulikke reaktsioone. Süsivesinikud, nagu
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
FUNKTSIONAALSED RÜHMAD I osa. Kaido Viht
 FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
Keemiliste elementide perioodilisustabel
 Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
ORGAANILINE KEEMIA ANDRES TALVARI
 ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
( ) ( ) 2008/2009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
3. Solvendiefektide mõju ainete omadustele ja keemilistele protsessidele. 3.1 Solvendiefektid happe-aluse protsessidele. Tasakaal ja kiirus
 3. olvendiefektide mõju ainete omadustele ja keemilistele protsessidele Põhiallikas: Tasakaal ja kiirus Lahusti mõju tasakaalule ilmneb seeläbi, et erinevad lahustid solvateerivad erineva intensiivsusega
3. olvendiefektide mõju ainete omadustele ja keemilistele protsessidele Põhiallikas: Tasakaal ja kiirus Lahusti mõju tasakaalule ilmneb seeläbi, et erinevad lahustid solvateerivad erineva intensiivsusega
KARBOKSÜÜLHAPPED. Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COOH). Üldvalem R-COOH või HOOC-R
 KARBOKSÜÜLAPPED Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COO). Üldvalem R-COO või OOC-R Karboksüülhapete nimetused tuletatakse süsivesinike nimetustest ja
KARBOKSÜÜLAPPED Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COO). Üldvalem R-COO või OOC-R Karboksüülhapete nimetused tuletatakse süsivesinike nimetustest ja
Vektorid II. Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale
 Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass
 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
Lokaalsed ekstreemumid
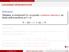 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Graafiteooria üldmõisteid. Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid
 Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
Kehade soojendamisel või jahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks.
 KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks
 4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
ORGAANILISE KEEMIA LABORIJUHEND ABISTAV MATERJAL
 TALLINNA ÜLIKL Matemaatika ja Loodusteaduste Instituut RGAANILISE KEEMIA LABRIJUEND ABISTAV MATERJAL Marju Robal ja Rando Tuvikene Tallinn 2008 SISUKRD 1. RGAANILISTE AINETE LAUSTUVUS JA LAUSTAMISVÕIME...3
TALLINNA ÜLIKL Matemaatika ja Loodusteaduste Instituut RGAANILISE KEEMIA LABRIJUEND ABISTAV MATERJAL Marju Robal ja Rando Tuvikene Tallinn 2008 SISUKRD 1. RGAANILISTE AINETE LAUSTUVUS JA LAUSTAMISVÕIME...3
=217 kj/mol (1) m Ühe mooli glükoosi sünteesil lihtainetest vabaneb footoneid: Δ H f, glükoos n (glükoos) =5,89 mol (1) E (footon)
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
5. a) ρ (g/cm 3 ) = 0,119 = 11,9% 12% 2 p
 201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
2.2.1 Geomeetriline interpretatsioon
 2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
Funktsiooni diferentsiaal
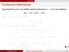 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
ETTEVALMISTUS KEEMIAOLÜMPIAADIKS II
 ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
TMR praktikum. Teooria: Aatomituuma varjestatus
 TMR praktikum Praktikum toimub 2-l praktikumipäeval ning koosneb kahest tööst. Tööde eesmärk on ühendite TMR spektrite interpreteerimine ning ainete identifitseerimine nii struktuurvalemi kui brutovalemi
TMR praktikum Praktikum toimub 2-l praktikumipäeval ning koosneb kahest tööst. Tööde eesmärk on ühendite TMR spektrite interpreteerimine ning ainete identifitseerimine nii struktuurvalemi kui brutovalemi
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
AATOMI EHITUS KEEMILINE SIDE
 TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
PLASTSED DEFORMATSIOONID
 PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
AROMAATSUS. Kaido Viht
 ARMAATSUS Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 018 Sisukord 1. Aromaatsus ja antiaromaatsus... 4. Aromaatsus annuleenide seerias... 6 3. Aromaatsus ioonilistes tsüklites... 8 4. Aromaatsus
ARMAATSUS Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 018 Sisukord 1. Aromaatsus ja antiaromaatsus... 4. Aromaatsus annuleenide seerias... 6 3. Aromaatsus ioonilistes tsüklites... 8 4. Aromaatsus
b) Täpne arvutus (aktiivsete kontsentratsioonide kaudu) ph arvutused I tugevad happed ja alused
 ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi
 Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Jätkusuutlikud isolatsioonilahendused. U-arvude koondtabel. VÄLISSEIN - COLUMBIA TÄISVALATUD ÕÕNESPLOKK 190 mm + SOOJUSTUS + KROHV
 U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
Fotosüntees. Peatükk 3.
 Fotosüntees. Peatükk 3. Fotosünteesiprotsess on keerulisem kui lihtne üldvõrrand, sest valguse energiat ei saa otse H 2 O seose-elektronidele anda ja neid otse CO 2 -le üle kanda. Seetõttu vaadeldakse
Fotosüntees. Peatükk 3. Fotosünteesiprotsess on keerulisem kui lihtne üldvõrrand, sest valguse energiat ei saa otse H 2 O seose-elektronidele anda ja neid otse CO 2 -le üle kanda. Seetõttu vaadeldakse
HSM TT 1578 EST 6720 611 954 EE (04.08) RBLV 4682-00.1/G
 HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
IChO 2014, ülesanne 4
 IChO 2014, ülesanne 4 Zeise sool, K[PtCl3C2H4], oli üks esimesi metallorgaanilisi ühendeid. Kopenhaageni ülikooli professor W. C. Zeise valmistas selle ühendi lisades PtCl4-le keevas etanoolis kaaliumkloriidi
IChO 2014, ülesanne 4 Zeise sool, K[PtCl3C2H4], oli üks esimesi metallorgaanilisi ühendeid. Kopenhaageni ülikooli professor W. C. Zeise valmistas selle ühendi lisades PtCl4-le keevas etanoolis kaaliumkloriidi
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 2016
 Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Lahused ja lahustumisprotsess konserveerimises
 Lahused ja lahustumisprotsess konserveerimises Lektor: Heige Peets Ennistuskoda Kanut, 6 44 25 63 esemed@kanut.ee Tallinn-Tartu 2004 Loengu eesmärgiks on anda ülevaade ja lühike selgitus kõige üldisematest
Lahused ja lahustumisprotsess konserveerimises Lektor: Heige Peets Ennistuskoda Kanut, 6 44 25 63 esemed@kanut.ee Tallinn-Tartu 2004 Loengu eesmärgiks on anda ülevaade ja lühike selgitus kõige üldisematest
Compress 6000 LW Bosch Compress LW C 35 C A ++ A + A B C D E F G. db kw kw /2013
 55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
Energiabilanss netoenergiavajadus
 Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
HULGATEOORIA ELEMENTE
 HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
Biomakromolekulid: struktuurist omadusteni. Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018
 Biomakromolekulid: struktuurist omadusteni Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018 Sissejuhatus 2 Biokeemia mõõtkava mm mm Inimese embrüo (6. nädal): 4 mm Suurem amööb: 0.8 mm Inimese punaverelible:
Biomakromolekulid: struktuurist omadusteni Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018 Sissejuhatus 2 Biokeemia mõõtkava mm mm Inimese embrüo (6. nädal): 4 mm Suurem amööb: 0.8 mm Inimese punaverelible:
p A...p D - gaasiliste ainete A...D osarõhud, atm K p ja K c vahel kehtib seos
 LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
TÄIENDAVAID TEEMASID KOOLIKEEMIALE III
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
Koduseid ülesandeid IMO 2017 Eesti võistkonna kandidaatidele vol 4 lahendused
 Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
,millest avaldub 21) 23)
 II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
7.7 Hii-ruut test 7.7. HII-RUUT TEST 85
 7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
20. SIRGE VÕRRANDID. Joonis 20.1
 κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
PÕLEVAINETE OMADUSED. Andres Talvari
 PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
3. LOENDAMISE JA KOMBINATOORIKA ELEMENTE
 3. LOENDAMISE JA KOMBINATOORIKA ELEMENTE 3.1. Loendamise põhireeglid Kombinatoorika on diskreetse matemaatika osa, mis uurib probleeme, kus on tegemist kas diskreetse hulga mingis mõttes eristatavate osahulkadega
3. LOENDAMISE JA KOMBINATOORIKA ELEMENTE 3.1. Loendamise põhireeglid Kombinatoorika on diskreetse matemaatika osa, mis uurib probleeme, kus on tegemist kas diskreetse hulga mingis mõttes eristatavate osahulkadega
STM A ++ A + A B C D E F G A B C D E F G. kw kw /2013
 Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika
 Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus
 Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus 1. Haljala valla metsa pindala Haljala valla üldpindala oli Maa-Ameti
Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus 1. Haljala valla metsa pindala Haljala valla üldpindala oli Maa-Ameti
CaCO 3(s) --> CaO(s) + CO 2(g) H = kj. Näide
 3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
Andmeanalüüs molekulaarbioloogias
 Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
Kontekstivabad keeled
 Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
28. Sirgvoolu, solenoidi ja toroidi magnetinduktsiooni arvutamine koguvooluseaduse abil.
 8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
KEEMIA ÜLESANNETE LAHENDAMINE II
 KEEMIA ÜLESANNETE LAHENDAMINE II ÜLESANDED JA LAHENDUSED Ülesanne 1 Ülesanne Ülesanne Vana münt diameetria, cm ja paksusea,0 mm on tehtud puhtast kullast (ρ = 1900 k m ). Kulla hind on 410$ ühe untsi eest
KEEMIA ÜLESANNETE LAHENDAMINE II ÜLESANDED JA LAHENDUSED Ülesanne 1 Ülesanne Ülesanne Vana münt diameetria, cm ja paksusea,0 mm on tehtud puhtast kullast (ρ = 1900 k m ). Kulla hind on 410$ ühe untsi eest
32. Rahvusvaheline keemiaolümpiaad
 32. Rahvusvaheline keemiaolümpiaad Kopenhaagen Neljapäeval, 6. juulil 2000 TERIAVR TÄELEPANU! Kirjutage iga probleemi esimese lehe ülemisse nurka oma nimi ja kood. Sama probleemi järgnevatele lehtedele
32. Rahvusvaheline keemiaolümpiaad Kopenhaagen Neljapäeval, 6. juulil 2000 TERIAVR TÄELEPANU! Kirjutage iga probleemi esimese lehe ülemisse nurka oma nimi ja kood. Sama probleemi järgnevatele lehtedele
Eesti koolinoorte XLIX täppisteaduste olümpiaad
 Eesti koolinoorte XLIX täppisteaduste olümpiaad MATEMAATIKA PIIRKONDLIK VOOR 26. jaanuaril 2002. a. Juhised lahenduste hindamiseks Lp. hindaja! 1. Juhime Teie tähelepanu sellele, et alljärgnevas on 7.
Eesti koolinoorte XLIX täppisteaduste olümpiaad MATEMAATIKA PIIRKONDLIK VOOR 26. jaanuaril 2002. a. Juhised lahenduste hindamiseks Lp. hindaja! 1. Juhime Teie tähelepanu sellele, et alljärgnevas on 7.
RF võimendite parameetrid
 RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
MATEMAATILISEST LOOGIKAST (Lausearvutus)
 TARTU ÜLIKOOL Teaduskool MATEMAATILISEST LOOGIKAST (Lausearvutus) Õppematerjal TÜ Teaduskooli õpilastele Koostanud E. Mitt TARTU 2003 1. LAUSE MÕISTE Matemaatilise loogika ühe osa - lausearvutuse - põhiliseks
TARTU ÜLIKOOL Teaduskool MATEMAATILISEST LOOGIKAST (Lausearvutus) Õppematerjal TÜ Teaduskooli õpilastele Koostanud E. Mitt TARTU 2003 1. LAUSE MÕISTE Matemaatilise loogika ühe osa - lausearvutuse - põhiliseks
ALGEBRA I. Kevad Lektor: Valdis Laan
 ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
REAKTSIOONIKINEETIKA
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
KRITON Platon. Siin ja edaspidi tõlkija märkused. Toim. Tõlkinud Jaan Unt
 KRITON Platon AKADEEMIA, 1/1994 lk 57 71 Tõlkinud Jaan Unt SOKRATES: Miks sa nii vara siin oled, Kriton? Või polegi enam vara? KRITON: On küll. SOKRATES: Ja kui vara siis? KRITON: Alles ahetab. SOKRATES:
KRITON Platon AKADEEMIA, 1/1994 lk 57 71 Tõlkinud Jaan Unt SOKRATES: Miks sa nii vara siin oled, Kriton? Või polegi enam vara? KRITON: On küll. SOKRATES: Ja kui vara siis? KRITON: Alles ahetab. SOKRATES:
F l 12. TRANSPORDINÄHTUSED JA BIOENERGEETIKA ALUSED
 1. TRANSPORDINÄHTUSED JA BIOENERGEETIKA ALUSED Eluks on vajalik pidev aine ja energia transport (e suunatud liikumine) läbi biosfääri ja konkreetselt bioloogilise aine. Biosfäär ehk elukeskkond on Maa
1. TRANSPORDINÄHTUSED JA BIOENERGEETIKA ALUSED Eluks on vajalik pidev aine ja energia transport (e suunatud liikumine) läbi biosfääri ja konkreetselt bioloogilise aine. Biosfäär ehk elukeskkond on Maa
Pesumasin Πλυντήριο ρούχων Mosógép Veļas mašīna
 ET Kasutusjuhend 2 EL Οδηγίες Χρήσης 17 HU Használati útmutató 34 LV Lietošanas instrukcija 50 Pesumasin Πλυντήριο ρούχων Mosógép Veļas mašīna ZWG 6120K Sisukord Ohutusinfo _ 2 Ohutusjuhised _ 3 Jäätmekäitlus
ET Kasutusjuhend 2 EL Οδηγίες Χρήσης 17 HU Használati útmutató 34 LV Lietošanas instrukcija 50 Pesumasin Πλυντήριο ρούχων Mosógép Veļas mašīna ZWG 6120K Sisukord Ohutusinfo _ 2 Ohutusjuhised _ 3 Jäätmekäitlus
ENERGEETIKA KÕIGE TÄHTSAM. Inimkond, üldisemalt kogu elusloodus,
 KÕIGE TÄHTSAM ENERGEETIKA ARVI FREIBERG Maailma asju liigutavat kaks jõudu sugutung ja surmahirm. Ehkki mitte täiesti alusetu väide, pole see kaugeltki kogu tõde. Nii üks kui teine muutuvad oluliseks alles
KÕIGE TÄHTSAM ENERGEETIKA ARVI FREIBERG Maailma asju liigutavat kaks jõudu sugutung ja surmahirm. Ehkki mitte täiesti alusetu väide, pole see kaugeltki kogu tõde. Nii üks kui teine muutuvad oluliseks alles
Vektoralgebra seisukohalt võib ka selle võrduse kirja panna skalaarkorrutise
 Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
Käesolevas peatükis tutvustatakse protsesside ahelat biomassist energiakandjani.
 Peatükk 04-00 lk 1 04-00: Biomass energia tootmiseks Energia muundamine Nagu selgitatud tekstiosas 01-00-02a, muundati päikese energia fotosünteesi käigus bioenergiaks ja see salvestus energiarikastes
Peatükk 04-00 lk 1 04-00: Biomass energia tootmiseks Energia muundamine Nagu selgitatud tekstiosas 01-00-02a, muundati päikese energia fotosünteesi käigus bioenergiaks ja see salvestus energiarikastes
EE - EP B1 KIRJELDUS
 EE - EP 2 270 010 B1 KIRJELDUS [0001] Käesolev leiutis käsitleb pürrolobensodiasepiine (PBD-sid) ja eriti C2-asendatud ühendite sünteesil kasulikke pürrolobensodiasepiine. Leiutise taust [0002] Mõnedel
EE - EP 2 270 010 B1 KIRJELDUS [0001] Käesolev leiutis käsitleb pürrolobensodiasepiine (PBD-sid) ja eriti C2-asendatud ühendite sünteesil kasulikke pürrolobensodiasepiine. Leiutise taust [0002] Mõnedel
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat
 Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
Molekulid ei esine üksikuna vaid suurearvuliste kogumitena.
 2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD
 KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
Algebraliste võrrandite lahenduvus radikaalides. Raido Paas Juhendaja: Mart Abel
 Algebraliste võrrandite lahenduvus radikaalides Magistritöö Raido Paas Juhendaja: Mart Abel Tartu 2013 Sisukord Sissejuhatus Ajalooline sissejuhatus iii v 1 Rühmateooria elemente 1 1.1 Substitutsioonide
Algebraliste võrrandite lahenduvus radikaalides Magistritöö Raido Paas Juhendaja: Mart Abel Tartu 2013 Sisukord Sissejuhatus Ajalooline sissejuhatus iii v 1 Rühmateooria elemente 1 1.1 Substitutsioonide
Eesti LIV matemaatikaolümpiaad
 Eesti LIV matemaatikaolümpiaad 31. märts 007 Lõppvoor 9. klass Lahendused 1. Vastus: 43. Ilmselt ei saa see arv sisaldada numbrit 0. Iga vähemalt kahekohaline nõutud omadusega arv sisaldab paarisnumbrit
Eesti LIV matemaatikaolümpiaad 31. märts 007 Lõppvoor 9. klass Lahendused 1. Vastus: 43. Ilmselt ei saa see arv sisaldada numbrit 0. Iga vähemalt kahekohaline nõutud omadusega arv sisaldab paarisnumbrit
Kas Androidi ostmiseks on õige aeg? Eesti esimene võrdlustest!
 Uus ipod Nano Nüüd kaamera ja raadioga Pentax K7 Mida arvata järjekordsest kaamerast? Odav ja hea ka Poola värk Poolakate telefoni käib kaks SIM-kaarti Säästuaeg Testis ilma jalata kuvar Kas Androidi ostmiseks
Uus ipod Nano Nüüd kaamera ja raadioga Pentax K7 Mida arvata järjekordsest kaamerast? Odav ja hea ka Poola värk Poolakate telefoni käib kaks SIM-kaarti Säästuaeg Testis ilma jalata kuvar Kas Androidi ostmiseks
