Rastvori i osobine rastvora
|
|
|
- Πρίσκιλλα Αντωνόπουλος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 Rastvori i osobine rastvora U srpskom jeziku reč rasvor predstavlja homogenu tečnu smešu. U engleskom reč solution predstavlja više od toga smešu dva gasa, legure (homogene smeše dva metala)... Na ovom predavanju ću uglavnom pričati o tečnim rastvorima
2 Rastvori i osobine rastvora Kod rastvora postoje dva bitna pojma: Rastvarač supstanca koja je u višku i koja je istog agregatnog stanja kao i smeša Rastvorena supstanca supstanca koje je u manjku Primer 1: Smeša dobijena mešanjem 25 g soli i 100 g vode -rastvarač je voda -rastvorena supstanca je so
3 Rastvori i osobine rastvora Primer 2: Smeša dobijena mešanjem 20 g alkohola i 80 g vode -rastvarač je voda -rastvorena supstanca je alkohol Primer 3: Smeša dobijena mešanjem 60 g alkohola i 40 g vode -rastvarač je alkohol -rastvorena supstanca je voda
4 Rastvori i osobine rastvora Primer 4: Smeša dobijena mešanjem 60 g vode i 100 g šećera -rastvarač je voda -rastvorena supstanca je šećer jer je smeša tečna
5 Proces rastvaranja Rastvori i osobine rastvora Rastvor nastaje kada se rastvorena supstanca ravnomerno rasporedi unutar rastvaraša. Međumolekulske interakcije su ključne prilikom proučavanja rastvora i ključne za rastvaranje Između molekula svih čistih supstanci (u kondenzovanoj fazi) posoje međumolekulske interakcije. Takođe i u rastvoru postoje međumolekulske interakcije između molekula rastvarača i rastvorene sustance.
6 Proces rastvaranja Rastvori i osobine rastvora Do rastvaranja jedne supstance u drugoj će doći onda kada je jačina međumolekulskih interakcija između rastvarača i rastvorene supstance slična jačini međumolekulskih interakcija između molekula čistog rastvarača i čiste rastvorene supstance. Na primer kuhinjska so (NaCl) će se rastvoriti u vodi jer su jon-dipol interakcije između jona (Na + i Cl - ) i molekula vode jače nego jon-jon interakcije (jonske veze) između samih jona u kristalnoj rešetci i vodoničnih veza i dipoldipol interakcija u samoj čistoj vodi.
7 Proces rastvaranja Rastvori i osobine rastvora Hidratisani Na + i Cl - jon
8 Rastvori i osobine rastvora Energetske promene prilikom rastvaranja Posmatramo samo entalpiju H i to u fazama. Šta imamo na početku tj. pre rastvaranja? NaCl u kristalnoj rešetci jonska veza Čistu vodu H veza i dipol-dipol interakcije
9 Rastvori i osobine rastvora Energetske promene prilikom rastvaranja Posmatramo samo entalpiju H i to u fazama. Prvo što treba da uradimo je da rasturimo jonsku vezu u NaCl i da dobijemo zasebne nevezane jone. To troši energiju H 1 > 0
10 Rastvori i osobine rastvora Energetske promene prilikom rastvaranja Posmatramo samo entalpiju H i to u fazama. Drugo što treba da uradimo je da rasturimo H-veze i dipoldipol interakcije između molekula vode i napravimo šupljine u koje će se smestiti joni To troši energiju H 2 > 0
11 Rastvori i osobine rastvora Energetske promene prilikom rastvaranja Posmatramo samo entalpiju H i to u fazama. Treće j ostalo samo da sad pomešamo te dve stvari (rastureni NaCl i vodu sa šupljinama) Ovde se oslobađa energija jer nastaju jon-dipol interakcije H 3 < 0
12 Rastvori i osobine rastvora Energetske promene prilikom rastvaranja Ukupna energetska promena prilikom rastvaranja će biti: H rastvaranja = H 1 + H 2 + H 3 Ukoliko je H rastvaranja negativno tada se so rastvara egzotermno uz zagrevanje rastvora. Primer je MgSO 4 Ukoliko je H rastvaranja pozitivno tada se so rastvara endotermno uz hlađenje rastvora. Primer je NH 4 NO 3
13 Rastvori i osobine rastvora Energetske promene prilikom rastvaranja
14 Rastvori i osobine rastvora Energetske promene prilikom rastvaranja Iz ovoga možemo zaključiti šta će se u čemu rastvarati. Jonska jedinjenja će se rastvarati spontano u vodi jer je voda polarna i nastale jon-dipol interakcije mogu da kompenzuju energiju koja se troši na kidanje jonske veze U nepolarnim organskim rastvaračima (koji nemaju ili imaju mali dipol) jonska jedinjenja se neće spontano rastvarati jer su jon-dipol interakcije isuviše male (ako ih uopšte ima) da bi kompenzovale za kidanje jonse veze
15 Rastvori i osobine rastvora Energetske promene prilikom rastvaranja Iz ovoga možemo zaključiti šta će se u čemu rastvarati. Jonska jedinjenja će se rastvarati spontano u vodi jer je voda polarna i nastale jon-dipol interakcije mogu da kompenzuju energiju koja se troši na kidanje jonske veze U nepolarnim organskim rastvaračima (koji nemaju ili imaju mali dipol) jonska jedinjenja se neće spontano rastvarati jer su jon-dipol interakcije isuviše male (ako ih uopšte ima) da bi kompenzovale za kidanje jonse veze
16 Rastvori i osobine rastvora Energetske promene prilikom rastvaranja Istom logikom nepolarna jedinjenja se neće rastvarati u vodi jer nastale diplo-dipol interakcije između nelarnog jedinjenja i vode ne mogu da kompenzuju energiju potrebnu da se raskinu vodonične veze i dipol-dipol interakcije u vodi i da se stvore šupljine.
17 Spontanost rastvaranja Rastvori i osobine rastvora Ne odlučuje samo entalpija da li će neki proces biti spontan već slobodna energija G = H T S Trebamo uzeti u obzir i promenu entropije
18 Rastvori i osobine rastvora Spontanost rastvaranja uloga entropije S Prilikom rastvaranja promena entropije sistema je uvek pozitivna Sve čestice će imati mnogo veću zapreminu za kretanje u rastvoru S > 0
19 Rastvori i osobine rastvora Spontanost rastvaranja slobodna energija G = H T S Ako je H negativno i S pozitivno rastvaranje će se dešavati spontano Ako je H pozitivno i S pozitivno rastvaranje će zavisiti od njihovog međusobonog odnosa tj. šta je veće Primer kod gasova: Kod gasova međumolekulske interakcije su veoma slabe tako da je H veoma malo (skoro 0) tako da se dva gasa uvek mešaju dajući homogenu smešu
20 Rastvori i osobine rastvora Spontanost rastvaranja slobodna energija Jedino što može da spreči mešanje dve supstance je da su međumolekulske interakcije u tim supstancama toliko jake da ne dozvoljavaju molekulima da se odvoje i pređu u rastvor.
21 Zasićenost rastvora Rastvori mogu biti: Nezasićeni Zasićeni Prezasićeni Rastvori i osobine rastvora Samo određena količina svake supstance se može rastvoriti u određenoj količini rastvarača pri nekoj temperaturi. Na 0 o C u 100 g vode će se rastvoriti 35,7 g NaCl Dolazi do uspostavljanja dinamičke ravnoteže između jona Na + i Cl - koji napuštaju kristal i onih koji se vraćaju.
22 Zasićenost rastvora Rastvori i osobine rastvora Dinamička ravnoteža isti broj jona u jedinici vremena pređe iz kristala u rastvor i vrati se iz rastvora u kristal
23 Zasićenost rastvora Rastvori i osobine rastvora Nezasićen rastvor onaj rastvor koji sadrži manje rastvorene supstance od maksimalne količine koju može da primi ta količina rastvarača Zasićen rastvor rastvor koji sadrži tačno maksimalnu količinu rastvorene supstance koju može da primi ta količina rastvarača. Zasićen rastvor se pravi tako što u rastvarač dodajemo supstancu sve dok se ona rastvara. Prvi višak supstance će se pojaviti kao talog na dnu čaše. Tada procedimo tu smešu da odvojimo rastvor od taloga i filtrat je zasićen rastvor.
24 Zasićenost rastvora Rastvori i osobine rastvora Prezasićen rastvor onaj rastvor koji sadrži više rastvorene supstance od maksimalne količine koju može da primi ta količina rastvarača. To je meta stabilno stanje i postiže se tako što zagrejemo rastvor, rastvorimo višak supstance i zatim ga naglo ohladimo tako da supstanca ne stigne da iskristališe.
25 Rastvorljivost i temperatura Rastvori i osobine rastvora Rastvorljivost većine čvrstih supstanci se povećava sa povećanjem temperature (setite se entropije)
26 Rastvorljivost i temperatura Rastvori i osobine rastvora Rastvorljivost svih gasova se smanjuje sa povećanjem temperature
27 Rastvorljivost i pritisak Rastvori i osobine rastvora Prilikom rastvaranja tečnosti ili čvrstih tela u tečnostima ne menja se bitno zapremina tako da pritisak ne utiče na rastvorljivost. Prilikom rastvaranja gasova u tečnostima zapremina se znatno menja i pritisak znatno utiće na rastvorljivost.
28 Rastvorljivost i pritisak Rastvori i osobine rastvora Što je pritisak gasa veći, veća količina gasa će moći da se rastvori. Henrijev zakon: S g = kp g S p je rastvorljivost gasa, P g parcijalni pritisak gasa, k Henrijeva konstanta (definisana za svaki gas-rastvarač sistem pri određenoj temperaturi)
29 Rastvori i osobine rastvora Načini za predstavljanje koncentarcije rastvora Mnogo raznih načina za predstavljanje koncentracije rastvora Procentna koncentracija Molski (molarni) udeo Molaritet (koncentracija) Molalitet
30 Rastvori i osobine rastvora Načini za predstavljanje koncentarcije rastvora Procentna koncentracija masa komponente % = 100 ukupna masa rastvora
31 Rastvori i osobine rastvora Načini za predstavljanje koncentarcije rastvora Molski (molarni) udeo X = broj molova komponente zbir broja molova svih komponenti rastvora
32 Rastvori i osobine rastvora Načini za predstavljanje koncentarcije rastvora Molaritet (koncentracija) M = broj molova komponente 3 zapremina rastvora u dm
33 Rastvori i osobine rastvora Načini za predstavljanje koncentarcije rastvora Molalitet m = broj molova komponente masa rastvaraca u kg
34 Koligativne osobine rastvora Neke fizičke osobine rastvora se znatno razlikuju od onih za čisti rastvarač. Na primer, čista voda mrzne na 0 o C ali zato vodeni rastvor etilen-glikola (antifriz) mrzne na znatno nižim temperaturama. Takođe ovaj rastvor ključa na višim temperaturama od 100 o C. One fizičke osobine rastvora (T T,T k ) koje ne zavise od toga koja je supstanca rastvorena već samo od njene koncentracije, tačnije broja rastvorenih čestica se zovu koligativne osobine rastvora
35 Koligativne osobine rastvora Koligativne osobine rastvora su: Smanjenje napona pare Povećanje tačke ključanja Sniženje tačke mržnjenja Povećanje osmotskog pritiska
36 Smanjenje napona pare Koligativne osobine rastvora Napon pare rastvora je niži od napona pare čistog rastvarača Raulov zakon P A = X A P A o P A napon pare rastvora X A molski udeo rastvarača u rastvoru P Ao napon pare čistog rastvarača
37 Koligativne osobine rastvora Povećanje tačke ključanja Sniženje tačke mržnjenja Izvode se iz faznog dijagrama (isti fazni dijagram sa prošlog časa)
38 Koligativne osobine rastvora Povećanje tačke ključanja, sniženje tačke mržnjenja Crna linija na dijagramu napon pare čistog rastvarača, plava linija napon pare rastvora
39 Povećanje tačke ključanja Koligativne osobine rastvora T k =K b m T k povećanje tačke ključanja K b ebulioskopska konstanta m - molalitet
40 sniženje tačke mržnjenja Koligativne osobine rastvora T t =K f m T k sniženje tačke mržnjenja K b krioskopska konstanta m - molalitet
41 Koligativne osobine rastvora Povećanje osmotskog pritiska Polupropusna membrana, može da propušta samo čestice rastvarača ali ne i rastvorene supstance
42 Koligativne osobine rastvora Povećanje osmotskog pritiska Ako se sa dve strane polupropusne membrane nađu rastvori različitih koncentracija (ili rastvor i čist rastvarač) doći će do prelaska molekula rastvarača kroz membranu iz razblaženijeg u koncentrovaniji rastvor. Ovaj prelazak možemo sprečiti jedino ako primenimo neki pritisak π na koncentrovaniji rastvor
43 Koligativne osobine rastvora Povećanje osmotskog pritiska Taj pritisak π se zove osmotski pritisak i jednak je : π = MRT π - omotski pritisak M molaritet R gasna konstanta T - temperatura
44 Koloidi koloidini rastvori Rastvore možemo podeliti prema veličini čestica rastvorene supstance na: Prave rastvore Koloidne rastvore Taloge Pravi rastvori čestice su manje od 10 Å (mali molekuli, joni) Talozi čestice su veće od 2000 Å padaju na dno posude, lako se cede Koloidni rastvori -čestice su između 10 Å i 2000 Å
45 Koloidi koloidini rastvori Koloidne čestice mogu biti sastavljenje od mnogo jona ili molekula il mogu biti čak jedan veliki molekul (protein) Tindalov efekat rasejavanje svetlosti na česticama koloidnog rastvora je osobina kako se oni mogu identifikovati
46 Koloidi koloidini rastvori Najzanimljiviji koloidi su oni koji nastaju u vodi. Koloidne čestice mogu biti hidrofilne (vole vodu) i hidrofobne (plaše se vode). Hidrofilni koloidi najčešći primer proteini i enzimi. Na površini imaju grupe koje sa vodom grede interakcije i upravo te interakcije ih drže u rastvoru. Veoma je teško istaložiti ih.
47 Koloidi koloidini rastvori Hidrofobne koloidne čestice nemaju afinitet za vodu i lako se talože ili formiraju sloj na površini vode. Mogu se stabilizovati adsorpcijom jona na svojoj površini čime površina postaje hidrofilna. U isto vreme zbog toga što su isto naelektrisane ove čestice se neće međusobno sudarati i uvećavati.
48 Koloidi koloidini rastvori Hidrofobne koloidne možemo stabilizovati i specijalnim stabilizatorima. Žučne kiseline imaju ulogu stabilizatora masti i ulja u našem digestivnom traktu.
49 Taloženje koloida Koloidi koloidini rastvori Isuviše male da bi se mogle cediti, prolaze kroz filter hartiju Moraju se uvećati koagulacija Koagulacija se može izazvati grejanjem rastvora povećava se brzina čestica i ućestalost sudara Dodavanjem elektrolita neutrališe se naelektrisanje na površine čestice i time se dozvoljava sudar između čestica i koagulacija Primer kada se reka uliva u more svi koloidi iz reke se talože čim pređu u slanu vodu i tako nastaje delta.
SEKUNDARNE VEZE međumolekulske veze
 PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
RASTVORI. više e komponenata. Šećer u vodi, O 2 u vodi, zubne plombe, vazduh, morska voda
 RASTVORI Rastvori su homogene smeše e 2 ili više e komponenata Šećer u vodi, O 2 u vodi, zubne plombe, vazduh, morska voda Fizička stanja rastvora Rastvori mogu da postoje u bilo kom od 3 agregatna stanja:
RASTVORI Rastvori su homogene smeše e 2 ili više e komponenata Šećer u vodi, O 2 u vodi, zubne plombe, vazduh, morska voda Fizička stanja rastvora Rastvori mogu da postoje u bilo kom od 3 agregatna stanja:
MEĐUMOLEKULSKE SILE JON-DIPOL DIPOL VODONIČNE NE VEZE DIPOL DIPOL-DIPOL DIPOL-INDUKOVANI INDUKOVANI JON-INDUKOVANI DISPERZNE SILE
 MEĐUMLEKULSKE SILE JN-DIPL VDNIČNE NE VEZE DIPL-DIPL JN-INDUKVANI DIPL DIPL-INDUKVANI INDUKVANI DIPL DISPERZNE SILE MEĐUMLEKULSKE SILE jake JNSKA VEZA (metal-nemetal) KVALENTNA VEZA (nemetal-nemetal) METALNA
MEĐUMLEKULSKE SILE JN-DIPL VDNIČNE NE VEZE DIPL-DIPL JN-INDUKVANI DIPL DIPL-INDUKVANI INDUKVANI DIPL DISPERZNE SILE MEĐUMLEKULSKE SILE jake JNSKA VEZA (metal-nemetal) KVALENTNA VEZA (nemetal-nemetal) METALNA
S t r a n a 1. 1.Povezati jonsku jačinu rastvora: a) MgCl 2 b) Al 2 (SO 4 ) 3 sa njihovim molalitetima, m. za so tipa: M p X q. pa je jonska jačina:
 S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
Rastvori rastvaračem rastvorenom supstancom
 Rastvori Rastvor je homogen sistem sastavljen od najmanje dvije supstance-jedne koja je po pravilu u velikom višku i naziva se rastvaračem i one druge, koja se naziva rastvorenom supstancom. Rastvorene
Rastvori Rastvor je homogen sistem sastavljen od najmanje dvije supstance-jedne koja je po pravilu u velikom višku i naziva se rastvaračem i one druge, koja se naziva rastvorenom supstancom. Rastvorene
II RASTVORI. Borko Matijević
 Borko Matijević II RASTVORI Rastvori predstavljaju složene disperzne sisteme u kojima su fino usitnjene čestice jedne supstance ravnomerno raspoređene između čestica druge supstance. Supstanca koja se
Borko Matijević II RASTVORI Rastvori predstavljaju složene disperzne sisteme u kojima su fino usitnjene čestice jedne supstance ravnomerno raspoređene između čestica druge supstance. Supstanca koja se
RASTVORI DISPERZNI SISTEMI OSOBINE PRAVIH RASTVORA ELEKTROLITI RAVNOTEŽE U RASTVORIMA ELEKTROLITA KOLOIDI
 RASTVORI DISPERZNI SISTEMI OSOBINE PRAVIH RASTVORA ELEKTROLITI RAVNOTEŽE U RASTVORIMA ELEKTROLITA KOLOIDI DISPERZNI SISTEMI Disperzija (lat.) raspršivanje, rasipanje Disperzni sistem je smeša u kojoj su
RASTVORI DISPERZNI SISTEMI OSOBINE PRAVIH RASTVORA ELEKTROLITI RAVNOTEŽE U RASTVORIMA ELEKTROLITA KOLOIDI DISPERZNI SISTEMI Disperzija (lat.) raspršivanje, rasipanje Disperzni sistem je smeša u kojoj su
3.1 Granična vrednost funkcije u tački
 3 Granična vrednost i neprekidnost funkcija 2 3 Granična vrednost i neprekidnost funkcija 3. Granična vrednost funkcije u tački Neka je funkcija f(x) definisana u tačkama x za koje je 0 < x x 0 < r, ili
3 Granična vrednost i neprekidnost funkcija 2 3 Granična vrednost i neprekidnost funkcija 3. Granična vrednost funkcije u tački Neka je funkcija f(x) definisana u tačkama x za koje je 0 < x x 0 < r, ili
SEMINAR IZ KOLEGIJA ANALITIČKA KEMIJA I. Studij Primijenjena kemija
 SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
Osnovni primer. (Z, +,,, 0, 1) je komutativan prsten sa jedinicom: množenje je distributivno prema sabiranju
 RAČUN OSTATAKA 1 1 Prsten celih brojeva Z := N + {} N + = {, 3, 2, 1,, 1, 2, 3,...} Osnovni primer. (Z, +,,,, 1) je komutativan prsten sa jedinicom: sabiranje (S1) asocijativnost x + (y + z) = (x + y)
RAČUN OSTATAKA 1 1 Prsten celih brojeva Z := N + {} N + = {, 3, 2, 1,, 1, 2, 3,...} Osnovni primer. (Z, +,,,, 1) je komutativan prsten sa jedinicom: sabiranje (S1) asocijativnost x + (y + z) = (x + y)
Apsolutno neprekidne raspodele Raspodele apsolutno neprekidnih sluqajnih promenljivih nazivaju se apsolutno neprekidnim raspodelama.
 Apsolutno neprekidne raspodele Raspodele apsolutno neprekidnih sluqajnih promenljivih nazivaju se apsolutno neprekidnim raspodelama. a b Verovatno a da sluqajna promenljiva X uzima vrednost iz intervala
Apsolutno neprekidne raspodele Raspodele apsolutno neprekidnih sluqajnih promenljivih nazivaju se apsolutno neprekidnim raspodelama. a b Verovatno a da sluqajna promenljiva X uzima vrednost iz intervala
Eliminacijski zadatak iz Matematike 1 za kemičare
 Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
PRAVA. Prava je u prostoru određena jednom svojom tačkom i vektorom paralelnim sa tom pravom ( vektor paralelnosti).
 PRAVA Prava je kao i ravan osnovni geometrijski ojam i ne definiše se. Prava je u rostoru određena jednom svojom tačkom i vektorom aralelnim sa tom ravom ( vektor aralelnosti). M ( x, y, z ) 3 Posmatrajmo
PRAVA Prava je kao i ravan osnovni geometrijski ojam i ne definiše se. Prava je u rostoru određena jednom svojom tačkom i vektorom aralelnim sa tom ravom ( vektor aralelnosti). M ( x, y, z ) 3 Posmatrajmo
UNIVERZITET U NIŠU ELEKTRONSKI FAKULTET SIGNALI I SISTEMI. Zbirka zadataka
 UNIVERZITET U NIŠU ELEKTRONSKI FAKULTET Goran Stančić SIGNALI I SISTEMI Zbirka zadataka NIŠ, 014. Sadržaj 1 Konvolucija Literatura 11 Indeks pojmova 11 3 4 Sadržaj 1 Konvolucija Zadatak 1. Odrediti konvoluciju
UNIVERZITET U NIŠU ELEKTRONSKI FAKULTET Goran Stančić SIGNALI I SISTEMI Zbirka zadataka NIŠ, 014. Sadržaj 1 Konvolucija Literatura 11 Indeks pojmova 11 3 4 Sadržaj 1 Konvolucija Zadatak 1. Odrediti konvoluciju
I.13. Koliki je napon između neke tačke A čiji je potencijal 5 V i referentne tačke u odnosu na koju se taj potencijal računa?
 TET I.1. Šta je Kulonova sila? elektrostatička sila magnetna sila c) gravitaciona sila I.. Šta je elektrostatička sila? sila kojom međusobno eluju naelektrisanja u mirovanju sila kojom eluju naelektrisanja
TET I.1. Šta je Kulonova sila? elektrostatička sila magnetna sila c) gravitaciona sila I.. Šta je elektrostatička sila? sila kojom međusobno eluju naelektrisanja u mirovanju sila kojom eluju naelektrisanja
OSOBINE RAZBLAŽENIH RASTVORA ili KOLIGATIVNE OSOBINE. KOLIGATIVNE OSOBINE zavise od broja čestica
 OSOBINE RAZBLAŽENIH RASTVORA ili KOLIGATIVNE OSOBINE KOLIGATIVNE OSOBINE zavise od broja čestica OSOBINE RAZBLAŽENIH RASTVORA ili KOLIGATIVNE OSOBINE Zašto koligativne? colligare (lat.) = povezati, udružiti
OSOBINE RAZBLAŽENIH RASTVORA ili KOLIGATIVNE OSOBINE KOLIGATIVNE OSOBINE zavise od broja čestica OSOBINE RAZBLAŽENIH RASTVORA ili KOLIGATIVNE OSOBINE Zašto koligativne? colligare (lat.) = povezati, udružiti
KOLOIDI. suspenzija. pravi rastvori. veće od. manje od < 1 nm. > 100 nm
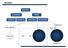 MATERIJA SUPSTANCE SMEŠE ELEMENTI JEDINJENJA HOMOGENE HETEROGENE pravi rastvori veće od suspenzija manje od < 1 nm od do > 100 nm Tomas Grem je dao ime rastvorima kod kojih je primetio da: Čestice dispergovane
MATERIJA SUPSTANCE SMEŠE ELEMENTI JEDINJENJA HOMOGENE HETEROGENE pravi rastvori veće od suspenzija manje od < 1 nm od do > 100 nm Tomas Grem je dao ime rastvorima kod kojih je primetio da: Čestice dispergovane
DISKRETNA MATEMATIKA - PREDAVANJE 7 - Jovanka Pantović
 DISKRETNA MATEMATIKA - PREDAVANJE 7 - Jovanka Pantović Novi Sad April 17, 2018 1 / 22 Teorija grafova April 17, 2018 2 / 22 Definicija Graf je ure dena trojka G = (V, G, ψ), gde je (i) V konačan skup čvorova,
DISKRETNA MATEMATIKA - PREDAVANJE 7 - Jovanka Pantović Novi Sad April 17, 2018 1 / 22 Teorija grafova April 17, 2018 2 / 22 Definicija Graf je ure dena trojka G = (V, G, ψ), gde je (i) V konačan skup čvorova,
IZVODI ZADACI ( IV deo) Rešenje: Najpre ćemo logaritmovati ovu jednakost sa ln ( to beše prirodni logaritam za osnovu e) a zatim ćemo
 IZVODI ZADACI ( IV deo) LOGARITAMSKI IZVOD Logariamskim izvodom funkcije f(), gde je >0 i, nazivamo izvod logarima e funkcije, o jes: (ln ) f ( ) f ( ) Primer. Nadji izvod funkcije Najpre ćemo logarimovai
IZVODI ZADACI ( IV deo) LOGARITAMSKI IZVOD Logariamskim izvodom funkcije f(), gde je >0 i, nazivamo izvod logarima e funkcije, o jes: (ln ) f ( ) f ( ) Primer. Nadji izvod funkcije Najpre ćemo logarimovai
Rastvor predstavlja homogenu smešu dve ili više komponenti. Uslovna podela komponenata na rastvorak i rastvarač:
 RASTVORI 1 Rastvor predstavlja homogenu smešu dve ili više komponenti. Uslovna podela komponenata na rastvorak i rastvarač: Rastvarač je komponenta koja ima isto agregatno stanje kao i dobijeni rastvor.
RASTVORI 1 Rastvor predstavlja homogenu smešu dve ili više komponenti. Uslovna podela komponenata na rastvorak i rastvarač: Rastvarač je komponenta koja ima isto agregatno stanje kao i dobijeni rastvor.
Kiselo bazni indikatori
 Kiselo bazni indikatori Slabe kiseline ili baze koje imaju različite boje nejonizovanog i jonizovanog oblika u rastvoru Primer: slaba kiselina HIn(aq) H + (aq) + In (aq) nejonizovani oblik jonizovani oblik
Kiselo bazni indikatori Slabe kiseline ili baze koje imaju različite boje nejonizovanog i jonizovanog oblika u rastvoru Primer: slaba kiselina HIn(aq) H + (aq) + In (aq) nejonizovani oblik jonizovani oblik
41. Jednačine koje se svode na kvadratne
 . Jednačine koje se svode na kvadrane Simerične recipročne) jednačine Jednačine oblika a n b n c n... c b a nazivamo simerične jednačine, zbog simeričnosi koeficijenaa koeficijeni uz jednaki). k i n k
. Jednačine koje se svode na kvadrane Simerične recipročne) jednačine Jednačine oblika a n b n c n... c b a nazivamo simerične jednačine, zbog simeričnosi koeficijenaa koeficijeni uz jednaki). k i n k
PARCIJALNI IZVODI I DIFERENCIJALI. Sama definicija parcijalnog izvoda i diferencijala je malo teža, mi se njome ovde nećemo baviti a vi ćete je,
 PARCIJALNI IZVODI I DIFERENCIJALI Sama definicija parcijalnog ivoda i diferencijala je malo teža, mi se njome ovde nećemo baviti a vi ćete je, naravno, naučiti onako kako vaš profesor ahteva. Mi ćemo probati
PARCIJALNI IZVODI I DIFERENCIJALI Sama definicija parcijalnog ivoda i diferencijala je malo teža, mi se njome ovde nećemo baviti a vi ćete je, naravno, naučiti onako kako vaš profesor ahteva. Mi ćemo probati
Kaskadna kompenzacija SAU
 Kaskadna kompenzacija SAU U inženjerskoj praksi, naročito u sistemima regulacije elektromotornih pogona i tehnoloških procesa, veoma često se primenjuje metoda kaskadne kompenzacije, u čijoj osnovi su
Kaskadna kompenzacija SAU U inženjerskoj praksi, naročito u sistemima regulacije elektromotornih pogona i tehnoloških procesa, veoma često se primenjuje metoda kaskadne kompenzacije, u čijoj osnovi su
VEŽBA 1 PRAVLJENJE RASTVORA. 1. Molarnost; količinska koncentracija Predstavlja količinu rastvorene supstance u n
 VEŽBA 1 PRAVLJENJE RASTVORA Unutrašnjost ćelije je ispunjena rastvorom različitih biopolimera, kao što su: proteini, nukleinske kiseline, polisaharidi, kao i malih organskih molekula i elektrolita. Kompleksni
VEŽBA 1 PRAVLJENJE RASTVORA Unutrašnjost ćelije je ispunjena rastvorom različitih biopolimera, kao što su: proteini, nukleinske kiseline, polisaharidi, kao i malih organskih molekula i elektrolita. Kompleksni
ISPITNA PITANJA Opšta i neorganska hemija I KOLOKVIJUM. 5. Navesti osobine amfoternih oksida i napisati 3 primera amfoternih oksida.
 Dr Sanja Podunavac-Kuzmanović, redovni profesor tel: (+381) 21 / 485-3693 fax: (+381) 21 / 450-413 e-mail: sanya@uns.ac.rs web page: hemijatf.weebly.com ISPITNA PITANJA Opšta i neorganska hemija I KOLOKVIJUM
Dr Sanja Podunavac-Kuzmanović, redovni profesor tel: (+381) 21 / 485-3693 fax: (+381) 21 / 450-413 e-mail: sanya@uns.ac.rs web page: hemijatf.weebly.com ISPITNA PITANJA Opšta i neorganska hemija I KOLOKVIJUM
Ispitna pitanja iz Osnova hemije
 I grupa pitanja Ispitna pitanja iz Osnova hemije 1. Hijerarhija materijala, smeše, metode razdvajanja smeša Materija: supstance i energija (polje). Supstance se dele na homogene i heterogene supstance.
I grupa pitanja Ispitna pitanja iz Osnova hemije 1. Hijerarhija materijala, smeše, metode razdvajanja smeša Materija: supstance i energija (polje). Supstance se dele na homogene i heterogene supstance.
Teorijske osnove informatike 1
 Teorijske osnove informatike 1 9. oktobar 2014. () Teorijske osnove informatike 1 9. oktobar 2014. 1 / 17 Funkcije Veze me du skupovima uspostavljamo skupovima koje nazivamo funkcijama. Neformalno, funkcija
Teorijske osnove informatike 1 9. oktobar 2014. () Teorijske osnove informatike 1 9. oktobar 2014. 1 / 17 Funkcije Veze me du skupovima uspostavljamo skupovima koje nazivamo funkcijama. Neformalno, funkcija
ELEKTROTEHNIČKI ODJEL
 MATEMATIKA. Neka je S skup svih živućih državljana Republike Hrvatske..04., a f preslikavanje koje svakom elementu skupa S pridružuje njegov horoskopski znak (bez podznaka). a) Pokažite da je f funkcija,
MATEMATIKA. Neka je S skup svih živućih državljana Republike Hrvatske..04., a f preslikavanje koje svakom elementu skupa S pridružuje njegov horoskopski znak (bez podznaka). a) Pokažite da je f funkcija,
SISTEMI NELINEARNIH JEDNAČINA
 SISTEMI NELINEARNIH JEDNAČINA April, 2013 Razni zapisi sistema Skalarni oblik: Vektorski oblik: F = f 1 f n f 1 (x 1,, x n ) = 0 f n (x 1,, x n ) = 0, x = (1) F(x) = 0, (2) x 1 0, 0 = x n 0 Definicije
SISTEMI NELINEARNIH JEDNAČINA April, 2013 Razni zapisi sistema Skalarni oblik: Vektorski oblik: F = f 1 f n f 1 (x 1,, x n ) = 0 f n (x 1,, x n ) = 0, x = (1) F(x) = 0, (2) x 1 0, 0 = x n 0 Definicije
U unutrašnja energija H entalpija S entropija G 298. G Gibsova energija TERMOHEMIJA I TERMODINAMIKA HEMIJSKA TERMODINAMIKA
 HEMIJSKA TERMODINAMIKA Bavi se energetskim promenama pri odigravanju hemijskih reakcija. TERMODINAMIČKE FUNKCIJE STANJA U unutrašnja energija H entalpija S entropija Ako su određene na standardnom pritisku
HEMIJSKA TERMODINAMIKA Bavi se energetskim promenama pri odigravanju hemijskih reakcija. TERMODINAMIČKE FUNKCIJE STANJA U unutrašnja energija H entalpija S entropija Ako su određene na standardnom pritisku
Riješeni zadaci: Nizovi realnih brojeva
 Riješei zadaci: Nizovi realih brojeva Nizovi, aritmetički iz, geometrijski iz Fukciju a : N R azivamo beskoači) iz realih brojeva i ozačavamo s a 1, a,..., a,... ili a ), pri čemu je a = a). Aritmetički
Riješei zadaci: Nizovi realih brojeva Nizovi, aritmetički iz, geometrijski iz Fukciju a : N R azivamo beskoači) iz realih brojeva i ozačavamo s a 1, a,..., a,... ili a ), pri čemu je a = a). Aritmetički
FTN Novi Sad Katedra za motore i vozila. Teorija kretanja drumskih vozila Vučno-dinamičke performanse vozila: MAKSIMALNA BRZINA
 : MAKSIMALNA BRZINA Maksimalna brzina kretanja F O (N) F OI i m =i I i m =i II F Oid Princip određivanja v MAX : Drugi Njutnov zakon Dokle god je: F O > ΣF otp vozilo ubrzava Kada postane: F O = ΣF otp
: MAKSIMALNA BRZINA Maksimalna brzina kretanja F O (N) F OI i m =i I i m =i II F Oid Princip određivanja v MAX : Drugi Njutnov zakon Dokle god je: F O > ΣF otp vozilo ubrzava Kada postane: F O = ΣF otp
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu
 Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Trigonometrijske jednačine i nejednačine. Zadaci koji se rade bez upotrebe trigonometrijskih formula. 00. FF cos x sin x
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Trigonometrijske jednačine i nejednačine. Zadaci koji se rade bez upotrebe trigonometrijskih formula. 00. FF cos x sin x
OM2 V3 Ime i prezime: Index br: I SAVIJANJE SILAMA TANKOZIDNIH ŠTAPOVA
 OM V me i preime: nde br: 1.0.01. 0.0.01. SAVJANJE SLAMA TANKOZDNH ŠTAPOVA A. TANKOZDN ŠTAPOV PROZVOLJNOG OTVORENOG POPREČNOG PRESEKA Preposavka: Smičući napon je konsanan po debljini ida (duž pravca upravnog
OM V me i preime: nde br: 1.0.01. 0.0.01. SAVJANJE SLAMA TANKOZDNH ŠTAPOVA A. TANKOZDN ŠTAPOV PROZVOLJNOG OTVORENOG POPREČNOG PRESEKA Preposavka: Smičući napon je konsanan po debljini ida (duž pravca upravnog
IZVODI ZADACI (I deo)
 IZVODI ZADACI (I deo) Najpre da se podsetimo tablice i osnovnih pravila:. C`=0. `=. ( )`= 4. ( n )`=n n-. (a )`=a lna 6. (e )`=e 7. (log a )`= 8. (ln)`= ` ln a (>0) 9. = ( 0) 0. `= (>0) (ovde je >0 i a
IZVODI ZADACI (I deo) Najpre da se podsetimo tablice i osnovnih pravila:. C`=0. `=. ( )`= 4. ( n )`=n n-. (a )`=a lna 6. (e )`=e 7. (log a )`= 8. (ln)`= ` ln a (>0) 9. = ( 0) 0. `= (>0) (ovde je >0 i a
Računarska grafika. Rasterizacija linije
 Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
100g maslaca: 751kcal = 20g : E maslac E maslac = (751 x 20)/100 E maslac = 150,2kcal 100g med: 320kcal = 30g : E med E med = (320 x 30)/100 E med =
 100g maslaca: 751kcal = 20g : E maslac E maslac = (751 x 20)/100 E maslac = 150,2kcal 100g med: 320kcal = 30g : E med E med = (320 x 30)/100 E med = 96kcal 100g mleko: 49kcal = 250g : E mleko E mleko =
100g maslaca: 751kcal = 20g : E maslac E maslac = (751 x 20)/100 E maslac = 150,2kcal 100g med: 320kcal = 30g : E med E med = (320 x 30)/100 E med = 96kcal 100g mleko: 49kcal = 250g : E mleko E mleko =
RAVNOTEŽA TEČNO-PARA
 RAVNOTEŽA TEČNO-PARA Smeša dve isparljive komponente (dve tečnosti) koje se mešaju u svim odnosima: f = c p + 2 = 2 2 + 2 = 2 tečna homogena smeša+para iznad tečnosti Ako su te dve nezavisno promenjive
RAVNOTEŽA TEČNO-PARA Smeša dve isparljive komponente (dve tečnosti) koje se mešaju u svim odnosima: f = c p + 2 = 2 2 + 2 = 2 tečna homogena smeša+para iznad tečnosti Ako su te dve nezavisno promenjive
Elementi spektralne teorije matrica
 Elementi spektralne teorije matrica Neka je X konačno dimenzionalan vektorski prostor nad poljem K i neka je A : X X linearni operator. Definicija. Skalar λ K i nenula vektor u X se nazivaju sopstvena
Elementi spektralne teorije matrica Neka je X konačno dimenzionalan vektorski prostor nad poljem K i neka je A : X X linearni operator. Definicija. Skalar λ K i nenula vektor u X se nazivaju sopstvena
2 tg x ctg x 1 = =, cos 2x Zbog četvrtog kvadranta rješenje je: 2 ctg x
 Zadatak (Darjan, medicinska škola) Izračunaj vrijednosti trigonometrijskih funkcija broja ako je 6 sin =,,. 6 Rješenje Ponovimo trigonometrijske funkcije dvostrukog kuta! Za argument vrijede sljedeće formule:
Zadatak (Darjan, medicinska škola) Izračunaj vrijednosti trigonometrijskih funkcija broja ako je 6 sin =,,. 6 Rješenje Ponovimo trigonometrijske funkcije dvostrukog kuta! Za argument vrijede sljedeće formule:
Reverzibilni procesi
 Reverzbln proces Reverzbln proces: proces pr koja sste nkada nje vše od beskonačno ale vrednost udaljen od ravnoteže, beskonačno ala proena spoljašnjh uslova ože vratt sste u blo koju tačku, proena ože
Reverzbln proces Reverzbln proces: proces pr koja sste nkada nje vše od beskonačno ale vrednost udaljen od ravnoteže, beskonačno ala proena spoljašnjh uslova ože vratt sste u blo koju tačku, proena ože
Kontrolni zadatak (Tačka, prava, ravan, diedar, poliedar, ortogonalna projekcija), grupa A
 Kontrolni zadatak (Tačka, prava, ravan, diedar, poliedar, ortogonalna projekcija), grupa A Ime i prezime: 1. Prikazane su tačke A, B i C i prave a,b i c. Upiši simbole Î, Ï, Ì ili Ë tako da dobijeni iskazi
Kontrolni zadatak (Tačka, prava, ravan, diedar, poliedar, ortogonalna projekcija), grupa A Ime i prezime: 1. Prikazane su tačke A, B i C i prave a,b i c. Upiši simbole Î, Ï, Ì ili Ë tako da dobijeni iskazi
Dvokomponentni sistemi: razblaženi rastvori
 Dvokomponentni sistemi: razblaženi rastvori Pod rastvorom se podrazumeva jednofazni sistem (bilo kog agregatnog stanja) od dve ili više komponenata u kome su hemijske vrste koje ga sačinjavaju dispergovane
Dvokomponentni sistemi: razblaženi rastvori Pod rastvorom se podrazumeva jednofazni sistem (bilo kog agregatnog stanja) od dve ili više komponenata u kome su hemijske vrste koje ga sačinjavaju dispergovane
M086 LA 1 M106 GRP. Tema: Baza vektorskog prostora. Koordinatni sustav. Norma. CSB nejednakost
 M086 LA 1 M106 GRP Tema: CSB nejednakost. 19. 10. 2017. predavač: Rudolf Scitovski, Darija Marković asistent: Darija Brajković, Katarina Vincetić P 1 www.fizika.unios.hr/grpua/ 1 Baza vektorskog prostora.
M086 LA 1 M106 GRP Tema: CSB nejednakost. 19. 10. 2017. predavač: Rudolf Scitovski, Darija Marković asistent: Darija Brajković, Katarina Vincetić P 1 www.fizika.unios.hr/grpua/ 1 Baza vektorskog prostora.
numeričkih deskriptivnih mera.
 DESKRIPTIVNA STATISTIKA Numeričku seriju podataka opisujemo pomoću Numeričku seriju podataka opisujemo pomoću numeričkih deskriptivnih mera. Pokazatelji centralne tendencije Aritmetička sredina, Medijana,
DESKRIPTIVNA STATISTIKA Numeričku seriju podataka opisujemo pomoću Numeričku seriju podataka opisujemo pomoću numeričkih deskriptivnih mera. Pokazatelji centralne tendencije Aritmetička sredina, Medijana,
Konstruisanje. Dobro došli na... SREDNJA MAŠINSKA ŠKOLA NOVI SAD DEPARTMAN ZA PROJEKTOVANJE I KONSTRUISANJE
 Dobro došli na... Konstruisanje GRANIČNI I KRITIČNI NAPON slajd 2 Kritični naponi Izazivaju kritične promene oblika Delovi ne mogu ispravno da vrše funkciju Izazivaju plastične deformacije Može doći i
Dobro došli na... Konstruisanje GRANIČNI I KRITIČNI NAPON slajd 2 Kritični naponi Izazivaju kritične promene oblika Delovi ne mogu ispravno da vrše funkciju Izazivaju plastične deformacije Može doći i
INTELIGENTNO UPRAVLJANJE
 INTELIGENTNO UPRAVLJANJE Fuzzy sistemi zaključivanja Vanr.prof. Dr. Lejla Banjanović-Mehmedović Mehmedović 1 Osnovni elementi fuzzy sistema zaključivanja Fazifikacija Baza znanja Baze podataka Baze pravila
INTELIGENTNO UPRAVLJANJE Fuzzy sistemi zaključivanja Vanr.prof. Dr. Lejla Banjanović-Mehmedović Mehmedović 1 Osnovni elementi fuzzy sistema zaključivanja Fazifikacija Baza znanja Baze podataka Baze pravila
Heterogene ravnoteže taloženje i otapanje. u vodi u prisustvu zajedničkog iona u prisustvu kompleksirajućegreagensa pri različitim ph vrijednostima
 Heterogene ravnoteže taloženje i otapanje u vodi u prisustvu zajedničkog iona u prisustvu kompleksirajućegreagensa pri različitim ph vrijednostima Ako je BA teško topljiva sol (npr. AgCl) dodatkom
Heterogene ravnoteže taloženje i otapanje u vodi u prisustvu zajedničkog iona u prisustvu kompleksirajućegreagensa pri različitim ph vrijednostima Ako je BA teško topljiva sol (npr. AgCl) dodatkom
Elektrotehnički fakultet univerziteta u Beogradu 17.maj Odsek za Softversko inžinjerstvo
 Elektrotehnički fakultet univerziteta u Beogradu 7.maj 009. Odsek za Softversko inžinjerstvo Performanse računarskih sistema Drugi kolokvijum Predmetni nastavnik: dr Jelica Protić (35) a) (0) Posmatra
Elektrotehnički fakultet univerziteta u Beogradu 7.maj 009. Odsek za Softversko inžinjerstvo Performanse računarskih sistema Drugi kolokvijum Predmetni nastavnik: dr Jelica Protić (35) a) (0) Posmatra
Idealno gasno stanje-čisti gasovi
 Idealno gasno stanje-čisti gasovi Parametri P, V, T i n nisu nezavisni. Odnos između njih eksperimentalno je utvrđeni izražava se kroz gasne zakone. Gasni zakoni: 1. ojl-maritov: PVconst. pri konstantnim
Idealno gasno stanje-čisti gasovi Parametri P, V, T i n nisu nezavisni. Odnos između njih eksperimentalno je utvrđeni izražava se kroz gasne zakone. Gasni zakoni: 1. ojl-maritov: PVconst. pri konstantnim
HEMIJSKE RAVNOTEŽE. a = f = f c.
 II RAČUNSKE VEŽBE HEMIJSKE RAVNOTEŽE TEORIJSKI DEO I POJAM AKTIVNOSTI JONA Razblaženi rastvori (do 0,1 mol/dm ) u kojima je interakcija između čestica rastvorene supstance zanemarljiva ponašaju se kao
II RAČUNSKE VEŽBE HEMIJSKE RAVNOTEŽE TEORIJSKI DEO I POJAM AKTIVNOSTI JONA Razblaženi rastvori (do 0,1 mol/dm ) u kojima je interakcija između čestica rastvorene supstance zanemarljiva ponašaju se kao
5. Karakteristične funkcije
 5. Karakteristične funkcije Profesor Milan Merkle emerkle@etf.rs milanmerkle.etf.rs Verovatnoća i Statistika-proleće 2018 Milan Merkle Karakteristične funkcije ETF Beograd 1 / 10 Definicija Karakteristična
5. Karakteristične funkcije Profesor Milan Merkle emerkle@etf.rs milanmerkle.etf.rs Verovatnoća i Statistika-proleće 2018 Milan Merkle Karakteristične funkcije ETF Beograd 1 / 10 Definicija Karakteristična
Iskazna logika 3. Matematička logika u računarstvu. novembar 2012
 Iskazna logika 3 Matematička logika u računarstvu Department of Mathematics and Informatics, Faculty of Science,, Serbia novembar 2012 Deduktivni sistemi 1 Definicija Deduktivni sistem (ili formalna teorija)
Iskazna logika 3 Matematička logika u računarstvu Department of Mathematics and Informatics, Faculty of Science,, Serbia novembar 2012 Deduktivni sistemi 1 Definicija Deduktivni sistem (ili formalna teorija)
GASNO STANJE.
 GASNO STANJE http://www.ffh.bg.ac.rs/geografi_fh_procesi.html AGREGATNA STANJA MATERIJE Četiri agregatna stanja materije na osnovu stepena uređenosti, tj. odnosa termalne energije čestica i energije međumolekulskih
GASNO STANJE http://www.ffh.bg.ac.rs/geografi_fh_procesi.html AGREGATNA STANJA MATERIJE Četiri agregatna stanja materije na osnovu stepena uređenosti, tj. odnosa termalne energije čestica i energije međumolekulskih
PREGLED OSNOVNIH VELIČINA ZA DEFINISANJE SASTAVA RASTVORA
 I RAČUNSKE EŽBE PREGLED OSNONIH ELIČINA ZA DEFINISANJE SASTAA RASTORA Za izražavanje kvantitativnog sastava rastvora u heiji koriste se različite fizičke veličine i odnosi. Koriste se i različite jedinice.
I RAČUNSKE EŽBE PREGLED OSNONIH ELIČINA ZA DEFINISANJE SASTAA RASTORA Za izražavanje kvantitativnog sastava rastvora u heiji koriste se različite fizičke veličine i odnosi. Koriste se i različite jedinice.
PARNA POSTROJENJA ZA KOMBINIRANU PROIZVODNJU ELEKTRIČNE I TOPLINSKE ENERGIJE (ENERGANE)
 (Enegane) List: PARNA POSTROJENJA ZA KOMBINIRANU PROIZVODNJU ELEKTRIČNE I TOPLINSKE ENERGIJE (ENERGANE) Na mjestima gdje se istovremeno troši električna i toplinska energija, ekonomičan način opskrbe energijom
(Enegane) List: PARNA POSTROJENJA ZA KOMBINIRANU PROIZVODNJU ELEKTRIČNE I TOPLINSKE ENERGIJE (ENERGANE) Na mjestima gdje se istovremeno troši električna i toplinska energija, ekonomičan način opskrbe energijom
RIJEŠENI ZADACI I TEORIJA IZ
 RIJEŠENI ZADACI I TEORIJA IZ LOGARITAMSKA FUNKCIJA SVOJSTVA LOGARITAMSKE FUNKCIJE OSNOVE TRIGONOMETRIJE PRAVOKUTNOG TROKUTA - DEFINICIJA TRIGONOMETRIJSKIH FUNKCIJA - VRIJEDNOSTI TRIGONOMETRIJSKIH FUNKCIJA
RIJEŠENI ZADACI I TEORIJA IZ LOGARITAMSKA FUNKCIJA SVOJSTVA LOGARITAMSKE FUNKCIJE OSNOVE TRIGONOMETRIJE PRAVOKUTNOG TROKUTA - DEFINICIJA TRIGONOMETRIJSKIH FUNKCIJA - VRIJEDNOSTI TRIGONOMETRIJSKIH FUNKCIJA
Pismeni ispit iz matematike Riješiti sistem jednačina i diskutovati rješenja sistema u zavisnosti od parametra: ( ) + 1.
 Pismeni ispit iz matematike 0 008 GRUPA A Riješiti sistem jednačina i diskutovati rješenja sistema u zavisnosti od parametra: λ + z = Ispitati funkciju i nacrtati njen grafik: + ( λ ) + z = e Izračunati
Pismeni ispit iz matematike 0 008 GRUPA A Riješiti sistem jednačina i diskutovati rješenja sistema u zavisnosti od parametra: λ + z = Ispitati funkciju i nacrtati njen grafik: + ( λ ) + z = e Izračunati
( ) ( ) 2 UNIVERZITET U ZENICI POLITEHNIČKI FAKULTET. Zadaci za pripremu polaganja kvalifikacionog ispita iz Matematike. 1. Riješiti jednačine: 4
 UNIVERZITET U ZENICI POLITEHNIČKI FAKULTET Riješiti jednačine: a) 5 = b) ( ) 3 = c) + 3+ = 7 log3 č) = 8 + 5 ć) sin cos = d) 5cos 6cos + 3 = dž) = đ) + = 3 e) 6 log + log + log = 7 f) ( ) ( ) g) ( ) log
UNIVERZITET U ZENICI POLITEHNIČKI FAKULTET Riješiti jednačine: a) 5 = b) ( ) 3 = c) + 3+ = 7 log3 č) = 8 + 5 ć) sin cos = d) 5cos 6cos + 3 = dž) = đ) + = 3 e) 6 log + log + log = 7 f) ( ) ( ) g) ( ) log
HEMIJSKA VEZA ŠTA DRŽI STVARI (ATOME) ZAJEDNO?
 HEMIJSKA VEZA ŠTA DRŽI STVARI (ATOME) ZAJEDNO? U OKVIRU OVOG POGLAVLJA ĆEMO RADITI Jonska i kovalentna veza. Metalna veza. Elektronska teorija hemijske veze. Struktura molekula. Međumolekulske interakcije.
HEMIJSKA VEZA ŠTA DRŽI STVARI (ATOME) ZAJEDNO? U OKVIRU OVOG POGLAVLJA ĆEMO RADITI Jonska i kovalentna veza. Metalna veza. Elektronska teorija hemijske veze. Struktura molekula. Međumolekulske interakcije.
3. razred gimnazije- opšti i prirodno-matematički smer ALKENI. Aciklični nezasićeni ugljovodonici koji imaju jednu dvostruku vezu.
 ALKENI Acikliči ezasićei ugljovodoici koji imaju jedu dvostruku vezu. 2 4 2 2 2 (etile) viil grupa 3 6 2 3 2 2 prope (propile) alil grupa 4 8 2 2 3 3 3 2 3 3 1-bute 2-bute 2-metilprope 5 10 2 2 2 2 3 2
ALKENI Acikliči ezasićei ugljovodoici koji imaju jedu dvostruku vezu. 2 4 2 2 2 (etile) viil grupa 3 6 2 3 2 2 prope (propile) alil grupa 4 8 2 2 3 3 3 2 3 3 1-bute 2-bute 2-metilprope 5 10 2 2 2 2 3 2
7 Algebarske jednadžbe
 7 Algebarske jednadžbe 7.1 Nultočke polinoma Skup svih polinoma nad skupom kompleksnih brojeva označavamo sa C[x]. Definicija. Nultočka polinoma f C[x] je svaki kompleksni broj α takav da je f(α) = 0.
7 Algebarske jednadžbe 7.1 Nultočke polinoma Skup svih polinoma nad skupom kompleksnih brojeva označavamo sa C[x]. Definicija. Nultočka polinoma f C[x] je svaki kompleksni broj α takav da je f(α) = 0.
Termohemija. C(s) + O 2 (g) CO 2 (g) H= -393,5 kj
 Termohemija Termodinamika proučava energiju i njene promene Termohemija grana termodinamike odnosi izmeñu hemijske reakcije i energetskih promena koje se pri tom dešavaju C(s) + O 2 (g) CO 2 (g) H= -393,5
Termohemija Termodinamika proučava energiju i njene promene Termohemija grana termodinamike odnosi izmeñu hemijske reakcije i energetskih promena koje se pri tom dešavaju C(s) + O 2 (g) CO 2 (g) H= -393,5
Matematika 1 - vježbe. 11. prosinca 2015.
 Matematika - vježbe. prosinca 5. Stupnjevi i radijani Ako je kut φ jednak i rad, tada je veza između i 6 = Zadatak.. Izrazite u stupnjevima: a) 5 b) 7 9 c). d) 7. a) 5 9 b) 7 6 6 = = 5 c). 6 8.5 d) 7.
Matematika - vježbe. prosinca 5. Stupnjevi i radijani Ako je kut φ jednak i rad, tada je veza između i 6 = Zadatak.. Izrazite u stupnjevima: a) 5 b) 7 9 c). d) 7. a) 5 9 b) 7 6 6 = = 5 c). 6 8.5 d) 7.
Kiselo-bazne ravnoteže
 Uvod u biohemiju (školska 2016/17.) Kiselo-bazne ravnoteže NB: Prerađena/adaptirana prezentacija američkih profesora! Primeri kiselina i baza iz svakodnevnog života Arrhenius-ova definicija kiselina i
Uvod u biohemiju (školska 2016/17.) Kiselo-bazne ravnoteže NB: Prerađena/adaptirana prezentacija američkih profesora! Primeri kiselina i baza iz svakodnevnog života Arrhenius-ova definicija kiselina i
radni nerecenzirani materijal za predavanja R(f) = {f(x) x D}
 Matematika 1 Funkcije radni nerecenzirani materijal za predavanja Definicija 1. Neka su D i K bilo koja dva neprazna skupa. Postupak f koji svakom elementu x D pridružuje točno jedan element y K zovemo funkcija
Matematika 1 Funkcije radni nerecenzirani materijal za predavanja Definicija 1. Neka su D i K bilo koja dva neprazna skupa. Postupak f koji svakom elementu x D pridružuje točno jedan element y K zovemo funkcija
18. listopada listopada / 13
 18. listopada 2016. 18. listopada 2016. 1 / 13 Neprekidne funkcije Važnu klasu funkcija tvore neprekidne funkcije. To su funkcije f kod kojih mala promjena u nezavisnoj varijabli x uzrokuje malu promjenu
18. listopada 2016. 18. listopada 2016. 1 / 13 Neprekidne funkcije Važnu klasu funkcija tvore neprekidne funkcije. To su funkcije f kod kojih mala promjena u nezavisnoj varijabli x uzrokuje malu promjenu
Operacije s matricama
 Linearna algebra I Operacije s matricama Korolar 3.1.5. Množenje matrica u vektorskom prostoru M n (F) ima sljedeća svojstva: (1) A(B + C) = AB + AC, A, B, C M n (F); (2) (A + B)C = AC + BC, A, B, C M
Linearna algebra I Operacije s matricama Korolar 3.1.5. Množenje matrica u vektorskom prostoru M n (F) ima sljedeća svojstva: (1) A(B + C) = AB + AC, A, B, C M n (F); (2) (A + B)C = AC + BC, A, B, C M
MEĐUMOLEKULSKE SILE Jon-jon Kulonove sile kj/mol, Šarl-Оgisten de Кulon (Charles-Augustin de Coulomb) , francuski fizičar
 MEĐUMOLEKULSKE SILE Jon-jon Kulonove sile 400-4000 kj/mol, Šarl-Оgisten de Кulon (Charles-Augustin de Coulomb) 1736-1806, francuski fizičar F = k Q 1 x Q 2 d 2 Privlačne i odbojne elektrostatičke sile
MEĐUMOLEKULSKE SILE Jon-jon Kulonove sile 400-4000 kj/mol, Šarl-Оgisten de Кulon (Charles-Augustin de Coulomb) 1736-1806, francuski fizičar F = k Q 1 x Q 2 d 2 Privlačne i odbojne elektrostatičke sile
NOMENKLATURA ORGANSKIH SPOJEVA. Imenovanje aromatskih ugljikovodika
 NOMENKLATURA ORGANSKIH SPOJEVA Imenovanje aromatskih ugljikovodika benzen metilbenzen (toluen) 1,2-dimetilbenzen (o-ksilen) 1,3-dimetilbenzen (m-ksilen) 1,4-dimetilbenzen (p-ksilen) fenilna grupa 2-fenilheptan
NOMENKLATURA ORGANSKIH SPOJEVA Imenovanje aromatskih ugljikovodika benzen metilbenzen (toluen) 1,2-dimetilbenzen (o-ksilen) 1,3-dimetilbenzen (m-ksilen) 1,4-dimetilbenzen (p-ksilen) fenilna grupa 2-fenilheptan
Zavrxni ispit iz Matematiqke analize 1
 Građevinski fakultet Univerziteta u Beogradu 3.2.2016. Zavrxni ispit iz Matematiqke analize 1 Prezime i ime: Broj indeksa: 1. Definisati Koxijev niz. Dati primer niza koji nije Koxijev. 2. Dat je red n=1
Građevinski fakultet Univerziteta u Beogradu 3.2.2016. Zavrxni ispit iz Matematiqke analize 1 Prezime i ime: Broj indeksa: 1. Definisati Koxijev niz. Dati primer niza koji nije Koxijev. 2. Dat je red n=1
Dvanaesti praktikum iz Analize 1
 Dvaaesti praktikum iz Aalize Zlatko Lazovi 20. decembar 206.. Dokazati da fukcija f = 5 l tg + 5 ima bar jedu realu ulu. Ree e. Oblast defiisaosti fukcije je D f = k Z da postoji ula fukcije a 0, π 2.
Dvaaesti praktikum iz Aalize Zlatko Lazovi 20. decembar 206.. Dokazati da fukcija f = 5 l tg + 5 ima bar jedu realu ulu. Ree e. Oblast defiisaosti fukcije je D f = k Z da postoji ula fukcije a 0, π 2.
MATEMATIKA 2. Grupa 1 Rexea zadataka. Prvi pismeni kolokvijum, Dragan ori
 MATEMATIKA 2 Prvi pismeni kolokvijum, 14.4.2016 Grupa 1 Rexea zadataka Dragan ori Zadaci i rexea 1. unkcija f : R 2 R definisana je sa xy 2 f(x, y) = x2 + y sin 3 2 x 2, (x, y) (0, 0) + y2 0, (x, y) =
MATEMATIKA 2 Prvi pismeni kolokvijum, 14.4.2016 Grupa 1 Rexea zadataka Dragan ori Zadaci i rexea 1. unkcija f : R 2 R definisana je sa xy 2 f(x, y) = x2 + y sin 3 2 x 2, (x, y) (0, 0) + y2 0, (x, y) =
OBRTNA TELA. Vladimir Marinkov OBRTNA TELA VALJAK
 OBRTNA TELA VALJAK P = 2B + M B = r 2 π M = 2rπH V = BH 1. Zapremina pravog valjka je 240π, a njegova visina 15. Izračunati površinu valjka. Rešenje: P = 152π 2. Površina valjka je 112π, a odnos poluprečnika
OBRTNA TELA VALJAK P = 2B + M B = r 2 π M = 2rπH V = BH 1. Zapremina pravog valjka je 240π, a njegova visina 15. Izračunati površinu valjka. Rešenje: P = 152π 2. Površina valjka je 112π, a odnos poluprečnika
HEMIJSKA VEZA TEORIJA VALENTNE VEZE
 TEORIJA VALENTNE VEZE Kovalentna veza nastaje preklapanjem atomskih orbitala valentnih elektrona, pri čemu je region preklapanja između dva jezgra okupiran parom elektrona. - Nastalu kovalentnu vezu opisuje
TEORIJA VALENTNE VEZE Kovalentna veza nastaje preklapanjem atomskih orbitala valentnih elektrona, pri čemu je region preklapanja između dva jezgra okupiran parom elektrona. - Nastalu kovalentnu vezu opisuje
Pošto pretvaramo iz veće u manju mjernu jedinicu broj 2.5 množimo s 1000,
 PRERAČUNAVANJE MJERNIH JEDINICA PRIMJERI, OSNOVNE PRETVORBE, POTENCIJE I ZNANSTVENI ZAPIS, PREFIKSKI, ZADACI S RJEŠENJIMA Primjeri: 1. 2.5 m = mm Pretvaramo iz veće u manju mjernu jedinicu. 1 m ima dm,
PRERAČUNAVANJE MJERNIH JEDINICA PRIMJERI, OSNOVNE PRETVORBE, POTENCIJE I ZNANSTVENI ZAPIS, PREFIKSKI, ZADACI S RJEŠENJIMA Primjeri: 1. 2.5 m = mm Pretvaramo iz veće u manju mjernu jedinicu. 1 m ima dm,
Novi Sad god Broj 1 / 06 Veljko Milković Bulevar cara Lazara 56 Novi Sad. Izveštaj o merenju
 Broj 1 / 06 Dana 2.06.2014. godine izmereno je vreme zaustavljanja elektromotora koji je radio u praznom hodu. Iz gradske mreže 230 V, 50 Hz napajan je monofazni asinhroni motor sa dva brusna kamena. Kada
Broj 1 / 06 Dana 2.06.2014. godine izmereno je vreme zaustavljanja elektromotora koji je radio u praznom hodu. Iz gradske mreže 230 V, 50 Hz napajan je monofazni asinhroni motor sa dva brusna kamena. Kada
TRIGONOMETRIJA TROKUTA
 TRIGONOMETRIJA TROKUTA Standardne oznake u trokutuu ABC: a, b, c stranice trokuta α, β, γ kutovi trokuta t,t,t v,v,v s α,s β,s γ R r s težišnice trokuta visine trokuta simetrale kutova polumjer opisane
TRIGONOMETRIJA TROKUTA Standardne oznake u trokutuu ABC: a, b, c stranice trokuta α, β, γ kutovi trokuta t,t,t v,v,v s α,s β,s γ R r s težišnice trokuta visine trokuta simetrale kutova polumjer opisane
IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f
 IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f 2. Nule i znak funkcije; presek sa y-osom IspitivaƬe
IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f 2. Nule i znak funkcije; presek sa y-osom IspitivaƬe
ANALITIČKA HEMIJA. Kvalitativna analiza Kvantitativna analiza
 ANALITIČKA HEMIJA Kvalitativna analiza Kvantitativna analiza RAZLIKE Kvalitativnom hemijskom analizom dolazi se do saznanja o sastavu uzorka, tj. dobija se odgovor na pitanje od kojih komponenti se uzorak
ANALITIČKA HEMIJA Kvalitativna analiza Kvantitativna analiza RAZLIKE Kvalitativnom hemijskom analizom dolazi se do saznanja o sastavu uzorka, tj. dobija se odgovor na pitanje od kojih komponenti se uzorak
1.4 Tangenta i normala
 28 1 DERIVACIJA 1.4 Tangenta i normala Ako funkcija f ima derivaciju u točki x 0, onda jednadžbe tangente i normale na graf funkcije f u točki (x 0 y 0 ) = (x 0 f(x 0 )) glase: t......... y y 0 = f (x
28 1 DERIVACIJA 1.4 Tangenta i normala Ako funkcija f ima derivaciju u točki x 0, onda jednadžbe tangente i normale na graf funkcije f u točki (x 0 y 0 ) = (x 0 f(x 0 )) glase: t......... y y 0 = f (x
MEHANIKA FLUIDA. Isticanje kroz otvore sa promenljivim nivoom tečnosti
 MEHANIKA FLUIDA Isticanje kroz otvore sa promenljivim nivoom tečnosti zadatak Prizmatična sud podeljen je vertikalnom pregradom, u kojoj je otvor prečnika d, na dve komore Leva komora je napunjena vodom
MEHANIKA FLUIDA Isticanje kroz otvore sa promenljivim nivoom tečnosti zadatak Prizmatična sud podeljen je vertikalnom pregradom, u kojoj je otvor prečnika d, na dve komore Leva komora je napunjena vodom
Trigonometrija 2. Adicijske formule. Formule dvostrukog kuta Formule polovičnog kuta Pretvaranje sume(razlike u produkt i obrnuto
 Trigonometrija Adicijske formule Formule dvostrukog kuta Formule polovičnog kuta Pretvaranje sume(razlike u produkt i obrnuto Razumijevanje postupka izrade složenijeg matematičkog problema iz osnova trigonometrije
Trigonometrija Adicijske formule Formule dvostrukog kuta Formule polovičnog kuta Pretvaranje sume(razlike u produkt i obrnuto Razumijevanje postupka izrade složenijeg matematičkog problema iz osnova trigonometrije
Računarska grafika. Rasterizacija linije
 Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
= T 2. AgBr (s) + ½ Cl 2(g) + ½ Br 2(g) = AgCl (s) O (l) O (g) +1/2O 2(g) H 2(g) =H 2. značaj navođenja agregatnog stanja
 TERMOEMIJA Termohemija proučava toplotne promene koje prate hemijske reakcije, fazne prelaze (topljenje, isparavanje, sublimacija, polimorfne promene), rastvaranje supstance, razblaživanje rastvora itd.
TERMOEMIJA Termohemija proučava toplotne promene koje prate hemijske reakcije, fazne prelaze (topljenje, isparavanje, sublimacija, polimorfne promene), rastvaranje supstance, razblaživanje rastvora itd.
Rastvori Osnovni pojmovi i izračunavanja
 Rastvori Osnovni pojmovi i izračunavanja Disperzni sistem je smeša u kojoj su jedna ili više supstanci raspršene u nekoj drugoj supstanci u obliku sitnih čestica. Disperzni sredstvo je supstanca u kojoj
Rastvori Osnovni pojmovi i izračunavanja Disperzni sistem je smeša u kojoj su jedna ili više supstanci raspršene u nekoj drugoj supstanci u obliku sitnih čestica. Disperzni sredstvo je supstanca u kojoj
Ĉetverokut - DOMAĆA ZADAĆA. Nakon odgledanih videa trebali biste biti u stanju samostalno riješiti sljedeće zadatke.
 Ĉetverokut - DOMAĆA ZADAĆA Nakon odgledanih videa trebali biste biti u stanju samostalno riješiti sljedeće zadatke. 1. Duljine dijagonala paralelograma jednake su 6,4 cm i 11 cm, a duljina jedne njegove
Ĉetverokut - DOMAĆA ZADAĆA Nakon odgledanih videa trebali biste biti u stanju samostalno riješiti sljedeće zadatke. 1. Duljine dijagonala paralelograma jednake su 6,4 cm i 11 cm, a duljina jedne njegove
DIMENZIONISANJE PRAVOUGAONIH POPREČNIH PRESEKA NAPREGNUTIH NA PRAVO SLOŽENO SAVIJANJE
 TEORIJA ETONSKIH KONSTRUKCIJA T- DIENZIONISANJE PRAVOUGAONIH POPREČNIH PRESEKA NAPREGNUTIH NA PRAVO SLOŽENO SAVIJANJE 3.5 f "2" η y 2 D G N z d y A "" 0 Z a a G - tačka presek koja određje položaj sistemne
TEORIJA ETONSKIH KONSTRUKCIJA T- DIENZIONISANJE PRAVOUGAONIH POPREČNIH PRESEKA NAPREGNUTIH NA PRAVO SLOŽENO SAVIJANJE 3.5 f "2" η y 2 D G N z d y A "" 0 Z a a G - tačka presek koja određje položaj sistemne
KVADRATNA FUNKCIJA. Kvadratna funkcija je oblika: Kriva u ravni koja predstavlja grafik funkcije y = ax + bx + c. je parabola.
 KVADRATNA FUNKCIJA Kvadratna funkcija je oblika: = a + b + c Gde je R, a 0 i a, b i c su realni brojevi. Kriva u ravni koja predstavlja grafik funkcije = a + b + c je parabola. Najpre ćemo naučiti kako
KVADRATNA FUNKCIJA Kvadratna funkcija je oblika: = a + b + c Gde je R, a 0 i a, b i c su realni brojevi. Kriva u ravni koja predstavlja grafik funkcije = a + b + c je parabola. Najpre ćemo naučiti kako
POVRŠINA TANGENCIJALNO-TETIVNOG ČETVEROKUTA
 POVRŠIN TNGENIJLNO-TETIVNOG ČETVEROKUT MLEN HLP, JELOVR U mnoštvu mnogokuta zanimljiva je formula za površinu četverokuta kojemu se istoobno može upisati i opisati kružnica: gje su a, b, c, uljine stranica
POVRŠIN TNGENIJLNO-TETIVNOG ČETVEROKUT MLEN HLP, JELOVR U mnoštvu mnogokuta zanimljiva je formula za površinu četverokuta kojemu se istoobno može upisati i opisati kružnica: gje su a, b, c, uljine stranica
Periodičke izmjenične veličine
 EHNČK FAKULE SVEUČLŠA U RJEC Zavod za elekroenergeiku Sudij: Preddiploski sručni sudij elekroehnike Kolegij: Osnove elekroehnike Nosielj kolegija: Branka Dobraš Periodičke izjenične veličine Osnove elekroehnike
EHNČK FAKULE SVEUČLŠA U RJEC Zavod za elekroenergeiku Sudij: Preddiploski sručni sudij elekroehnike Kolegij: Osnove elekroehnike Nosielj kolegija: Branka Dobraš Periodičke izjenične veličine Osnove elekroehnike
( , 2. kolokvij)
 A MATEMATIKA (0..20., 2. kolokvij). Zadana je funkcija y = cos 3 () 2e 2. (a) Odredite dy. (b) Koliki je nagib grafa te funkcije za = 0. (a) zadanu implicitno s 3 + 2 y = sin y, (b) zadanu parametarski
A MATEMATIKA (0..20., 2. kolokvij). Zadana je funkcija y = cos 3 () 2e 2. (a) Odredite dy. (b) Koliki je nagib grafa te funkcije za = 0. (a) zadanu implicitno s 3 + 2 y = sin y, (b) zadanu parametarski
Betonske konstrukcije 1 - vežbe 3 - Veliki ekscentricitet -Dodatni primeri
 Betonske konstrukcije 1 - vežbe 3 - Veliki ekscentricitet -Dodatni primeri 1 1 Zadatak 1b Čisto savijanje - vezano dimenzionisanje Odrediti potrebnu površinu armature za presek poznatih dimenzija, pravougaonog
Betonske konstrukcije 1 - vežbe 3 - Veliki ekscentricitet -Dodatni primeri 1 1 Zadatak 1b Čisto savijanje - vezano dimenzionisanje Odrediti potrebnu površinu armature za presek poznatih dimenzija, pravougaonog
10. STABILNOST KOSINA
 MEHANIKA TLA: Stabilnot koina 101 10. STABILNOST KOSINA 10.1 Metode proračuna koina Problem analize tabilnoti zemljanih maa vodi e na određivanje odnoa između rapoložive mičuće čvrtoće i proečnog mičućeg
MEHANIKA TLA: Stabilnot koina 101 10. STABILNOST KOSINA 10.1 Metode proračuna koina Problem analize tabilnoti zemljanih maa vodi e na određivanje odnoa između rapoložive mičuće čvrtoće i proečnog mičućeg
Osnovne teoreme diferencijalnog računa
 Osnovne teoreme diferencijalnog računa Teorema Rolova) Neka je funkcija f definisana na [a, b], pri čemu važi f je neprekidna na [a, b], f je diferencijabilna na a, b) i fa) fb). Tada postoji ξ a, b) tako
Osnovne teoreme diferencijalnog računa Teorema Rolova) Neka je funkcija f definisana na [a, b], pri čemu važi f je neprekidna na [a, b], f je diferencijabilna na a, b) i fa) fb). Tada postoji ξ a, b) tako
konst. Električni otpor
 Sveučilište J. J. Strossmayera u sijeku Elektrotehnički fakultet sijek Stručni studij Električni otpor hmov zakon Pri protjecanju struje kroz vodič pojavljuje se otpor. Georg Simon hm je ustanovio ovisnost
Sveučilište J. J. Strossmayera u sijeku Elektrotehnički fakultet sijek Stručni studij Električni otpor hmov zakon Pri protjecanju struje kroz vodič pojavljuje se otpor. Georg Simon hm je ustanovio ovisnost
Otpornost R u kolu naizmjenične struje
 Otpornost R u kolu naizmjenične struje Pretpostavimo da je otpornik R priključen na prostoperiodični napon: Po Omovom zakonu pad napona na otporniku je: ( ) = ( ω ) u t sin m t R ( ) = ( ) u t R i t Struja
Otpornost R u kolu naizmjenične struje Pretpostavimo da je otpornik R priključen na prostoperiodični napon: Po Omovom zakonu pad napona na otporniku je: ( ) = ( ω ) u t sin m t R ( ) = ( ) u t R i t Struja
UKUPAN BROJ OSVOJENIH BODOVA
 ŠIFRA DRŽAVNO TAKMIČENJE II razred UKUPAN BROJ OSVOJENIH BODOVA Test regledala/regledao...... Podgorica,... 008. godine 1. Izračunati steen disocijacije slabe kiseline, HA, ako je oznata analitička koncentracija
ŠIFRA DRŽAVNO TAKMIČENJE II razred UKUPAN BROJ OSVOJENIH BODOVA Test regledala/regledao...... Podgorica,... 008. godine 1. Izračunati steen disocijacije slabe kiseline, HA, ako je oznata analitička koncentracija
4.7. Zadaci Formalizam diferenciranja (teorija na stranama ) 343. Znajući izvod funkcije x arctg x, odrediti izvod funkcije x arcctg x.
 4.7. ZADACI 87 4.7. Zadaci 4.7.. Formalizam diferenciranja teorija na stranama 4-46) 340. Znajući izvod funkcije arcsin, odrediti izvod funkcije arccos. Rešenje. Polazeći od jednakosti arcsin + arccos
4.7. ZADACI 87 4.7. Zadaci 4.7.. Formalizam diferenciranja teorija na stranama 4-46) 340. Znajući izvod funkcije arcsin, odrediti izvod funkcije arccos. Rešenje. Polazeći od jednakosti arcsin + arccos
