KEMIJA ZA GIMNAZIJE 1
|
|
|
- φώλος Λαυρέντιος Ελευθερόπουλος
- 5 χρόνια πριν
- Προβολές:
Transcript
1 Nataša Bukovec KEMIJA ZA GIMNAZIJE 1 Zbirka nalog za 1. letnik gimnazij
2 VSEBINA Predgovor 1. VARN DEL V KEMIJSKEM LABRATRIJU 5 Laboratorijski inventar 5 Znaki za nevarnost opozorilne besede stavki o nevarnosti in previdnostni stavki 6 Izrazi ali definicije o strupenosti snovi 7 Zaščitna oprema odpadne kemikalije 7 Rešitve 8 2. ZGRADBA ATMV 9 snovni delci v atomu izotopi in relativna atomska masa 9 Zgradba elektronske ovojnice 11 Zgradba atomov in ionov ter periodni sistem 11 Atomski in ionski radiji 13 Prva ionizacijska energija 1 Rešitve KEMIJSKA VEZ IN ZGRADBA SNVI 17 Ionska vez in ionske spojine 17 Kovalentna vez polarna in nepolarna kovalentna vez dipoli molekul elektronegativnost elementov 19 blike molekul 20 Dolžina in jakost vezi 22 Kovinska vez 23 Molekulske vezi 2 Vodikova vez 26 Kristali 28 Rešitve 29. ML IN KEMIJSKA ENAČBA 33 Množina n(x) in masa snovi m(x) število delcev snovi N(X) ter molska masa snovi M(X) 33 Množina molska prostornina in molska masa plinov 35 Računanje množine in mase reaktantov in produktov iz urejene kemijske enačbe 37 Kemijsko enačbo predstavimo z delci reaktantov in produktov 39 Rešitve 2 5. KEMIJSKA REAKCIJA JE SNVNA IN ENERGIJSKA SPREMEMBA 3 Računanje energijskih sprememb pri kemijskih reakcijah z uporabo standardnih tvorbenih entalpij in standardnih reakcijskih entalpij 3 Računanje energijskih sprememb pri kemijskih reakcijah z uporabo energijskih diagramov 6 Rešitve 8 6. ALKALIJSKE KVINE IN HALGENI 9 Rešitve RAZTPINE 53 Masni delež topljenca w(x) 53 Masna koncentracija raztopin γ(x). Množinska koncentracija raztopin c(x) 55 Topnost snovi 60 Rešitve 63 Viri 6
3 Predgovor Zbirka nalog za 1. letnik gimnazij Kemija za gimnazije 1 je namenjena utrjevanju znanja kemije v prvem letniku gimnazije. Zajema sedem poglavij ki si sledijo v enakem vrstnem redu kot vsebine v učbeniku Kemija za gimnazije 1 in so usklajena s prenovljenim učnim načrtom. S to zbirko sem želela dopolniti in povečati nabor nalog za utrjevanje znanja ki so v učbeniku na koncu vsake učne enote in na koncu vsakega poglavja. Vsako poglavje v zbirki je zasnovano tako: da je v uvodu napisano katera znanja z nalogami utrjujemo nato sledijo naloge glede na učno vsebino in zahtevnost. Naloge označene z zvezdicami so zahtevnejše ali pa vključujejo posebna znanja iz prenovljenega učnega načrta. V nekaterih poglavjih najdemo zglede oziroma rešene primere. Večinoma so to računske naloge ali pa naloge pri katerih je potrebno napisati določeno razlago ali komentar ali odčitati diagram. Skupaj z učbenikom Kemija za gimnazije 1 ter elektronskimi vsebinami k učbeniku (slikovno gradivo in rešitve nalog iz Preveri znanje in Utrdimo) so dijaki in srednješolski učitelji s to zbirko nalog dobili zaokrožen nabor gradiv za učenje oziroma poučevanje kemije v prvem letniku gimnazije. Nataša Bukovec Spletna stran učnih gradiv za kemijo v gimnazijah in srednjih strokovnih šolah:
4 . ML IN KEMIJSKA ENAČBA Z nalogami bomo utrdili znanje o: množini n(x) in masi m(x) snovi številu delcev N(X) v snovi ter molski masi snovi M(X) plinih: množina molska prostornina in molska masa plinov pomenu in uporabi zapisa kemijske reakcije s kemijsko enačbo: računanje množine in mase reaktantov in produktov iz urejene kemijske enačbe (kako) kemijsko enačbo predstavimo z delci reaktantov in produktov Množina n(x) in masa snovi m(x) število delcev snovi N(X) ter molska masa snovi M(X) ZGLED 1. Koliko molov železa je v 279 g železa? m(fe) = 279 g M(Fe) = 5585 g mol 1 n(fe) =? n(fe) = m ( Fe) 27 9 g = 1 = 0500 mol M( Fe) gmol 2. Izračunaj množino snovi v: a) 150 g magnezijevega oksida Mg b) 172 g žveplove kisline H 2 S c) 852 g amoniaka NH 3 č) 150 g natrijevega hidroksida NaH. ZGLED 3. Koliko atomov kisika je v 60 g kisika? m() = 60 g M() = 160 g mol 1 N A = mol 1 N() =? n() = m ( ) M ( ) = 6 0 g gmol = 1 00 mol N() = n() N A = 00 mol mol 1 = Ali: N() = n() N A = m N 23 ( 2 ) A 6 0 g = = M( ) gmol 33
5 *15. Koliko atomov vodika je v: a) 220 g propana C 3 H 8 b) 323 g vodikovega sulfida H 2 S c) 29 g fosforjeve kisline H 3 P? *16. Koliko atomov kisika je v 220 g S 2? 17. Koliko atomov kisika je v: a) 018 mol žveplovega trioksida S 3 b) 015 mol nikljevega nitrata Ni(N 3 ) 2 c) 035 mol aluminijevega sulfata Al 2 (S ) 3? *18. Koliko gramov kisika je v 0700 mol bakrovega sulfata pentahidrata CuS 5H 2? 19. Kolikšna je molska masa spojine če je v 378 g te spojine 0571 mol spojine? Množina molska prostornina in molska masa plinov ZGLED 20. V dveh posodah z enako prostornino sta plina pri enaki temperaturi. a) V kateri posodi je večja množina plina? b) V kateri posodi je večji tlak plina? a) Večja množina je v posodi B kjer je večje število delcev. b) Večji tlak je v posodi B saj je v njej večje število delcev ki trčijo ob stene posode. Tlak plina pa je posledica trkov delcev na stene posode. 21. V posodah z enako prostornino so plini pri enaki temperaturi. a) Razvrsti posode s plini glede na tlak plinov v njih od najmanjšega do največjega tlaka. b) V kateri posodi je najmanjša množina plina? 22. V kateri posodi je večji tlak če je plin v obeh posodah pri enaki temperaturi? Pojasni odgovor. 35
6 *6. Uredi enačbo reakcije. C 3 H(l) + 2 (g) C 2 (g) + H 2 (l) Izračunaj maso propanola C 3 H ki mora zgoreti da nastane 918 L ogljikovega dioksida pri T = 100 C in P = 1013 kpa. Molska prostornina je pri teh pogojih (T P) 306 L mol 1. *7. Koliko gramov butana C H 10 mora zgoreti da nastane 810 g vode? Napiši in uredi enačbo reakcije za gorenje butana. Napiši agregatna stanja snovi. Kemijsko enačbo predstavimo z delci reaktantov in produktov 8. Shema ponazarja reakcijo med plinoma kisikom in dušikovim oksidom v zaprti posodi. a) Napiši formulo produkta ki nastane pri reakciji. b) Napiši in uredi enačbo reakcije. znači agregatna stanja reaktantov in produkta. 9. Plin didušikov oksid N 2 pri višjih temperaturah razpade v dušik in kisik. 2 N 2 (g) 2 N 2 (g) + 2 (g) V kateri shemi A B ali C je kemijska reakcija pravilno prikazana z delci? 39
7 Rešitve 2. a) n(mg) = 372 mol b) n(h 2 S ) = 175 mol c) n(nh 3 ) = 0500 mol č) n(nah) = 375 mol. a) N(Fe) = b) N(H 2 S ) = c) N(NH 3 ) = č) N(NaH) = a) m(100 atomov Ni) = g b) m(500 molekul HCl) = g 7. a) n(n) = 200 mol n(h) = 600 mol b) N(N) = N(H) = c) m(n) = 280 g m(h) = 605 g 8. n(c) = 050 mol n(h) = 15 mol 9. N(C) = N(H) = m(c) = 8 g m(h) = 10 g 11. m(c 2 ) = 11 g 12. m(nacl) = 19 g 13. a) n(p) = 0680 mol n() = 102 mol b) n(fe) = 108 mol n() = 1 mol c) n(h) = 022 mol n(s) = 011 mol 1. a) n(pb) = n(s) = 0209 mol b) n(c) = 0800 mol n(h) = 200 mol c) n(cu) = 072 mol n() = 0371 mol 15. a) N(H) = b) N(H) = c) N(H) = N() = a) N() = b) N() = c) N() = m() = 101 g 19. M(spojine) = 662 g mol a) P(A) < P(C) < P(B) < P(Č) b) V posodi A. 22. Večji tlak je v posodi B. Število molekul plina je v obeh posodah enako zato je število trkov v manjši posodi B večje in zato tudi večji tlak plina. 23. a) V posodah A in B. Ker je število molekul plina na enoto prostornine v posodah A in B enako. b) V posodi Č. Ker je število molekul v posodi Č najmanjše je tudi masa plina v tej posodi najmanjša. 2. a) A: N 2 B: N C: N 2 b) C c) B č) A 26. N(N 2 ) = m(ch ) = 802 g 28. V( 2 ) = 290 L; V(N 2 ) = 116 L; V(C 2 ) = 580 L Kisik ima najmanjšo prostornino. 29. V(H 2 ) = 12 L V(N 2 ) = 889 L V( 2 ) = 778 L V(H 2 S) = 731 L V(Cl 2 ) = 351 L L *31. V m = 253 L mol 1 *32. V(CH ) = 251 L 3. Cr Mg 2 Cr + 3 Mg m(cr) = 52 g 35. Cu 2 + H 2 2 Cu + H 2 m(cu) = 191 g 36. Ag Ag 2 n( 2 ) = 0125 mol 37. Na 2 S + 2 C Na 2 S + 2 C 2 m(c) = 566 g 38. CS Cl 2 CCl + S 2 Cl 2 m(ccl ) = 1282 g m(s 2 Cl 2 ) = 1125 g 39. PCl 5 + H 2 H 3 P + 5 HCl n(h 3 P ) = 0110 mol; m(h 3 P ) = 108 g 0. Pb + Pb H 2 S 2 PbS + 2 H 2 m(pbs ) = 603 g 1. 2 H 2 S(g) + S 2 (g) 3 S(s) + 2 H 2 (g) a) m(s) = 12 g; b) m(h 2 ) = 90 g 2. 2 Ca(N 3 ) 2 2 Ca + N m[ca(n 3 ) 2 ] = 821 g *3. 6 PCl Cl 2 + P PCl 3 m(pcl 3 ) = 27 g; m(cl 2 ) = 128 g; m(p 10 ) = 852 g *. CaC 2 (s) + 2 H 2 (l) Ca(H) 2 (aq) + C 2 H 2 (g) a) V(C 2 H 2 ) = 8713 L b) m(cac 2 ) = 205 g *5. 3 Mg(s) + N 2 (g) Mg 3 N 2 (s) a) m(n 2 ) = 215 g b) V(N 2 ) = 522 L *6. 2 C 3 H(l) (g) 6 C 2 (g) + 8 H 2 (l) m(c 3 H) = 601 g *7. 2 C H 10 (g) (g) 8 C 2 (g) + 10 H 2 (l) m(c H 10 ) = 523 g 8. a) N 2 b) 2 N(g) + 2 (g) 2 N 2 (g) 9. V shemi C. 50. a) X Y 2 XY b) C A 2 + C 2 2 A 2 C Nepravilna je trditev B. 52. a) S 3 b) 2 c) 2 S S CS Cl 2 CCl + S 2 Cl 2 5. CS C S 2 *55. a) A B 2 AB b) shema II 2
Simbolni zapis in množina snovi
 Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
Osnovne stehiometrijske veličine
 Osnovne stehiometrijske veličine Stehiometrija (grško: stoiheion snov, metron merilo) obravnava količinske odnose pri kemijskih reakcijah. Fizikalne veličine, s katerimi kemik najpogosteje izraža količino
Osnovne stehiometrijske veličine Stehiometrija (grško: stoiheion snov, metron merilo) obravnava količinske odnose pri kemijskih reakcijah. Fizikalne veličine, s katerimi kemik najpogosteje izraža količino
KOLI»INSKI ODNOSI. Kemik mora vedeti, koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane.
 KOLI»INSKI ODNOSI Kemik mora vedeti koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane 4 Mase atomov in molekul 42 tevilo delcev masa in mnoæina snovi 43 RaËunajmo maso mnoæino in πtevilo
KOLI»INSKI ODNOSI Kemik mora vedeti koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane 4 Mase atomov in molekul 42 tevilo delcev masa in mnoæina snovi 43 RaËunajmo maso mnoæino in πtevilo
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * NAVODILA ZA OCENJEVANJE. Sreda, 3. junij 2015 SPLOŠNA MATURA
 Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
Stehiometrija za študente veterine
 Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
Tretja vaja iz matematike 1
 Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Slika, vir: http://www.manataka.org
 KEMIJA Slika, vir: http://www.manataka.org RAZTOPINE SPLOŠNE INFORMACIJE O GRADIVU Učno gradivo je nastalo v okviru projekta Munus 2. Njegovo izdajo je omogočilo sofinanciranje Evropskega socialnega sklada
KEMIJA Slika, vir: http://www.manataka.org RAZTOPINE SPLOŠNE INFORMACIJE O GRADIVU Učno gradivo je nastalo v okviru projekta Munus 2. Njegovo izdajo je omogočilo sofinanciranje Evropskega socialnega sklada
MODERIRANA RAZLIČICA
 Dr`avni izpitni center *N07143132* REDNI ROK KEMIJA PREIZKUS ZNANJA Maj 2007 NAVODILA ZA VREDNOTENJE NACIONALNO PREVERJANJE ZNANJA b kncu 3. bdbja MODERIRANA RAZLIČICA RIC 2007 2 N071-431-3-2 NAVODILA
Dr`avni izpitni center *N07143132* REDNI ROK KEMIJA PREIZKUS ZNANJA Maj 2007 NAVODILA ZA VREDNOTENJE NACIONALNO PREVERJANJE ZNANJA b kncu 3. bdbja MODERIRANA RAZLIČICA RIC 2007 2 N071-431-3-2 NAVODILA
Diferencialna enačba, v kateri nastopata neznana funkcija in njen odvod v prvi potenci
 Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Energije in okolje 1. vaja. Entalpija pri kemijskih reakcijah
 Entalpija pri kemijskih reakcijah Pri obravnavi energijskih pretvorb pri kemijskih reakcijah uvedemo pojem entalpije, ki popisuje spreminjanje energije sistema pri konstantnem tlaku. Sistemu lahko povečamo
Entalpija pri kemijskih reakcijah Pri obravnavi energijskih pretvorb pri kemijskih reakcijah uvedemo pojem entalpije, ki popisuje spreminjanje energije sistema pri konstantnem tlaku. Sistemu lahko povečamo
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 21. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 22. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
IZPIT IZ ANALIZE II Maribor,
 Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Ponovi in utrdi svoje znanje Rešitve
 1. poglavje: Kakšne so lastnosti vode? 10. Ni dosežena, saj podgana zaužije 188,8 mg/kg. 11. LD 50 = 0,480 mg/kg 2. poglavje: Kaj je največje čudo na Zemlji? 5. Edini stabilni izotop natrija ima masno
1. poglavje: Kakšne so lastnosti vode? 10. Ni dosežena, saj podgana zaužije 188,8 mg/kg. 11. LD 50 = 0,480 mg/kg 2. poglavje: Kaj je največje čudo na Zemlji? 5. Edini stabilni izotop natrija ima masno
PONOVITEV SNOVI ZA 4. TEST
 PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ
 ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
VAJE IZ KEMIJE. Zbirka računskih nalog. za študente Fizikalne merilne tehnike
 VAJE IZ KEMIJE Zbirka računskih nalog za študente Fizikalne erilne tehnike Šolsko leto 008/009 MERSKE ENOTE Osnovne fizikalne veličine SI (International Syste of Units, ednarodni siste erskih enot) Ie
VAJE IZ KEMIJE Zbirka računskih nalog za študente Fizikalne erilne tehnike Šolsko leto 008/009 MERSKE ENOTE Osnovne fizikalne veličine SI (International Syste of Units, ednarodni siste erskih enot) Ie
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 5. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Gimnazija Krˇsko. vektorji - naloge
 Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK
 1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
panagiotisathanasopoulos.gr
 . Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
. Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
S t r a n a 1. 1.Povezati jonsku jačinu rastvora: a) MgCl 2 b) Al 2 (SO 4 ) 3 sa njihovim molalitetima, m. za so tipa: M p X q. pa je jonska jačina:
 S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
BRONASTE PREGLOVE PLAKETE
 ŠOLSKO TEKMOVNJE IZ ZNNJ KEMIJE Z RONSTE PREGLOVE PLKETE Tekmovalna pola za. letnik. marec 08 Pred vami je deset tekmovalnih nalog, ki so različnega tipa. Pri reševanju lahko uporabljajte le priložen periodni
ŠOLSKO TEKMOVNJE IZ ZNNJ KEMIJE Z RONSTE PREGLOVE PLKETE Tekmovalna pola za. letnik. marec 08 Pred vami je deset tekmovalnih nalog, ki so različnega tipa. Pri reševanju lahko uporabljajte le priložen periodni
Integralni račun. Nedoločeni integral in integracijske metrode. 1. Izračunaj naslednje nedoločene integrale: (a) dx. (b) x 3 +3+x 2 dx, (c) (d)
 Integralni račun Nedoločeni integral in integracijske metrode. Izračunaj naslednje nedoločene integrale: d 3 +3+ 2 d, (f) (g) (h) (i) (j) (k) (l) + 3 4d, 3 +e +3d, 2 +4+4 d, 3 2 2 + 4 d, d, 6 2 +4 d, 2
Integralni račun Nedoločeni integral in integracijske metrode. Izračunaj naslednje nedoločene integrale: d 3 +3+ 2 d, (f) (g) (h) (i) (j) (k) (l) + 3 4d, 3 +e +3d, 2 +4+4 d, 3 2 2 + 4 d, d, 6 2 +4 d, 2
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014. ÄÉÁÍüÇÓÇ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
VPLIV REAKCIJSKIH SPREMENLJIVK NA POTEK IN HITROST MODELNE REAKCIJE NATRIJEVEGA TIOSULFATA S KLOROVODIKOVO KISLINO
 OSNOVNA ŠOLA PRIMOŽA TRUBARJA LAŠKO VPLIV REAKCIJSKIH SPREMENLJIVK NA POTEK IN HITROST MODELNE REAKCIJE NATRIJEVEGA TIOSULFATA S KLOROVODIKOVO KISLINO (RAZISKOVALNO DELO) Avtorici: Lea Lešek Povšič in
OSNOVNA ŠOLA PRIMOŽA TRUBARJA LAŠKO VPLIV REAKCIJSKIH SPREMENLJIVK NA POTEK IN HITROST MODELNE REAKCIJE NATRIJEVEGA TIOSULFATA S KLOROVODIKOVO KISLINO (RAZISKOVALNO DELO) Avtorici: Lea Lešek Povšič in
Funkcijske vrste. Matematika 2. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 2. april Gregor Dolinar Matematika 2
 Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
a) Kateri tip hibridnih orbital na klorovem atomu uporabimo? a) Kateri tip hibridnih orbital na fosforjevem atomu uporabimo?
 76. Narišite strukturo karbonatnega iona. Upoštevajte dejstvo, da so vse vezi enako dolge. Kateri tip hibridizacije na ogljikovem atomu moramo uporabiti? Ogljik je element 4. skupine. a) sp 2 b) sp 3 c)
76. Narišite strukturo karbonatnega iona. Upoštevajte dejstvo, da so vse vezi enako dolge. Kateri tip hibridizacije na ogljikovem atomu moramo uporabiti? Ogljik je element 4. skupine. a) sp 2 b) sp 3 c)
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2019 Β ΦΑΣΗ
 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Δίνεται στοιχείο Χ το οποίο έχει οκτώ ηλεκτρόνια στην εξωτερική του στιβάδα.
ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Δίνεται στοιχείο Χ το οποίο έχει οκτώ ηλεκτρόνια στην εξωτερική του στιβάδα.
Κεφάλαιο 1. Έννοιες και παράγοντες αντιδράσεων
 Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
ΓΗ ΚΑΙ ΣΥΜΠΑΝ. Εικόνα 1. Φωτογραφία του γαλαξία μας (από αρχείο της NASA)
 ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
6. ΤΕΛΙΚΗ ΙΑΘΕΣΗ ΤΑΦΗ. 6.1. Γενικά
 6. ΤΕΛΙΚΗ ΙΑΘΕΣΗ ΤΑΦΗ 6.1. Γενικά Είναι γεγονός ότι ανέκαθεν ο τελικός αποδέκτης των υπολειµµάτων της κατανάλωσης και των καταλοίπων της παραγωγικής διαδικασίας υπήρξε το περιβάλλον. Στις παλιότερες κοινωνίες
6. ΤΕΛΙΚΗ ΙΑΘΕΣΗ ΤΑΦΗ 6.1. Γενικά Είναι γεγονός ότι ανέκαθεν ο τελικός αποδέκτης των υπολειµµάτων της κατανάλωσης και των καταλοίπων της παραγωγικής διαδικασίας υπήρξε το περιβάλλον. Στις παλιότερες κοινωνίες
fosfat fosfat H deoksiriboza H O KEMIJA Z BIOKEMIJO učbenik za študente visokošolskega strokovnega študija kmetijstva
 Cl Cl Na + Cl Na + Na + Cl Na + O H H Cl Cl O H H Na + O H H fosfat H deoksiriboza N C N fosfat H H N C C C N N C H H O H C C C N N C N deoksiriboza CH 3 C O C N O C C N fosfat H deoksiriboza H H N C H
Cl Cl Na + Cl Na + Na + Cl Na + O H H Cl Cl O H H Na + O H H fosfat H deoksiriboza N C N fosfat H H N C C C N N C H H O H C C C N N C N deoksiriboza CH 3 C O C N O C C N fosfat H deoksiriboza H H N C H
1. Definicijsko območje, zaloga vrednosti. 2. Naraščanje in padanje, ekstremi. 3. Ukrivljenost. 4. Trend na robu definicijskega območja
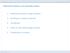 ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design
 Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2015 Β ΦΑΣΗ Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΑΣΚΗΣΗ
 ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΑΣΚΗΣΗ 1 η : A) 9,8g H 3 PO 4 αντιδρούν με την κατάλληλη ποσότητα NaCl σύμφωνα με την χημική εξίσωση: H 3 PO 4 + 3NaCl Na 3 PO 4 + 3HCl. Να υπολογίσετε πόσα λίτρα αέριου HCl παράγονται,
ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΑΣΚΗΣΗ 1 η : A) 9,8g H 3 PO 4 αντιδρούν με την κατάλληλη ποσότητα NaCl σύμφωνα με την χημική εξίσωση: H 3 PO 4 + 3NaCl Na 3 PO 4 + 3HCl. Να υπολογίσετε πόσα λίτρα αέριου HCl παράγονται,
Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih
 Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih različne Postopki ločevanja zmesi:iz zmesi je mogoče ločiti
Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih različne Postopki ločevanja zmesi:iz zmesi je mogoče ločiti
Delovna točka in napajalna vezja bipolarnih tranzistorjev
 KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
REŠITVE LABORATORIJSKE VAJE ZA KEMIJO V GIMNAZIJI. Marjeta Prašnikar
 REŠITVE LABORATORIJSKE VAJE ZA KEMIJO V GIMNAZIJI Andrej Nika Cebin Godec Manica Ivan Perdan Leban - Ocepek Marjeta Prašnikar 2 Rešitve VARNO EKSPERIMENTALNO DELO Kemija je eksperimentalna veda (str. 8)
REŠITVE LABORATORIJSKE VAJE ZA KEMIJO V GIMNAZIJI Andrej Nika Cebin Godec Manica Ivan Perdan Leban - Ocepek Marjeta Prašnikar 2 Rešitve VARNO EKSPERIMENTALNO DELO Kemija je eksperimentalna veda (str. 8)
Numerično reševanje. diferencialnih enačb II
 Numerčno reševanje dferencaln enačb I Dferencalne enačbe al ssteme dferencaln enačb rešujemo numerčno z več razlogov:. Ne znamo j rešt analtčno.. Posamezn del dferencalne enačbe podan tabelarčno. 3. Podatke
Numerčno reševanje dferencaln enačb I Dferencalne enačbe al ssteme dferencaln enačb rešujemo numerčno z več razlogov:. Ne znamo j rešt analtčno.. Posamezn del dferencalne enačbe podan tabelarčno. 3. Podatke
Booleova algebra. Izjave in Booleove spremenljivke
 Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
1A skupina alkalijske kovine
 1. NALOGA: KATERA IZMED SPOJIN JE NAJBOLJ TOPNA V VODI? NaCl, KBr, RbBr ALI NaF? ZAKAJ? 1. NALOGA: ODGOVOR Topnost je odvisna od mrežne entalpije ΔH mr (energija, potrebna za razgradnjo kristala na anione
1. NALOGA: KATERA IZMED SPOJIN JE NAJBOLJ TOPNA V VODI? NaCl, KBr, RbBr ALI NaF? ZAKAJ? 1. NALOGA: ODGOVOR Topnost je odvisna od mrežne entalpije ΔH mr (energija, potrebna za razgradnjo kristala na anione
γ) Βa(ΟΗ) 2 (aq) + ΗBr(aq)
 Θέμα 2 ο 2.1. Να συμπληρώσετε τις χημικές εξισώσεις (προϊόντα και συντελεστές) των παρακάτω αντιδράσεων που γίνονται όλες. α) CaI 2 (aq) + AgNO 3 (aq) β) Cl 2 (g) + H 2 S(aq) γ) Βa(ΟΗ) 2 (aq) + ΗBr(aq)
Θέμα 2 ο 2.1. Να συμπληρώσετε τις χημικές εξισώσεις (προϊόντα και συντελεστές) των παρακάτω αντιδράσεων που γίνονται όλες. α) CaI 2 (aq) + AgNO 3 (aq) β) Cl 2 (g) + H 2 S(aq) γ) Βa(ΟΗ) 2 (aq) + ΗBr(aq)
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ. δ. 39 φορές μεγαλύτερη από το της μάζας του ατόμου του 12 C 12 Μονάδες 5
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 25-02 - 2018 Μαρία Βασιλείου, Σπύρος Παπαμιχάλης, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 25-02 - 2018 Μαρία Βασιλείου, Σπύρος Παπαμιχάλης, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
u ê ê ê ê ê : ê ê ê } ê ê ê ê ê ê ê ê
 kemija 1_2.qxd 26.6.2009 7:56 Page 123 y u ê ê ê ê ê : ê ê ê } ê ê ê ê ê ê ê ê ê } ê ê ê ê ê ê ê ê w ê êr ê ê r ê ê ê 7. 1 Vodne raztopine so v nas in okoli nas Z raztopinami se sre~ujemo vsak dan. Pri
kemija 1_2.qxd 26.6.2009 7:56 Page 123 y u ê ê ê ê ê : ê ê ê } ê ê ê ê ê ê ê ê ê } ê ê ê ê ê ê ê ê w ê êr ê ê r ê ê ê 7. 1 Vodne raztopine so v nas in okoli nas Z raztopinami se sre~ujemo vsak dan. Pri
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ATOM, MOLEKULA, MOL. vsi atomi istega elementa imajo enako maso in enake lastnosti
 2. AO, OLEKULA, OL Iz Daltonove teorije sledi: eleenti so zgrajeni iz enakih atoov vsi atoi istega eleenta iajo enako aso in enake lastnosti atoi različnih eleentov iajo različne ase atoi različnih eleentov
2. AO, OLEKULA, OL Iz Daltonove teorije sledi: eleenti so zgrajeni iz enakih atoov vsi atoi istega eleenta iajo enako aso in enake lastnosti atoi različnih eleentov iajo različne ase atoi različnih eleentov
Talna kemija. Kaj je potrebno poznati:
 Talna kemija Kaj je potrebno poznati: splošno kemijo mol, molaren, normalnost, ekvivalent ionska jakost, aktivnost ravnotežne konstante funkcionalne skupine hidratacija, hidroliza redoks reakcije Redoks
Talna kemija Kaj je potrebno poznati: splošno kemijo mol, molaren, normalnost, ekvivalent ionska jakost, aktivnost ravnotežne konstante funkcionalne skupine hidratacija, hidroliza redoks reakcije Redoks
2. ATOM, MOLEKULA, MOL
 2. ATO, OLEKULA, OL ATO, OLEKULA, OL Iz Daltonove teorije sledi: eleenti so zgrajeni iz enakih atoov vsi atoi istega eleenta iajo enako aso in enake lastnosti atoi različnih eleentov iajo različne ase
2. ATO, OLEKULA, OL ATO, OLEKULA, OL Iz Daltonove teorije sledi: eleenti so zgrajeni iz enakih atoov vsi atoi istega eleenta iajo enako aso in enake lastnosti atoi različnih eleentov iajo različne ase
Državni izpitni center K E M I J A. Izpitna pola 1. Sreda, 28. avgust 2013 / 90 minut
 Š i f r a k a n d i d a t a : ržavni izpitni center *M13243111* JESENSKI IZPITNI RK K E M I J Izpitna pola 1 Sreda, 28. avgust 2013 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno pero
Š i f r a k a n d i d a t a : ržavni izpitni center *M13243111* JESENSKI IZPITNI RK K E M I J Izpitna pola 1 Sreda, 28. avgust 2013 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno pero
*M * Osnovna in višja raven MATEMATIKA NAVODILA ZA OCENJEVANJE. Sobota, 4. junij 2011 SPOMLADANSKI IZPITNI ROK. Državni izpitni center
 Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ
 Κεφάλαιο 1ο-ΟΞΕΙΔΩΑΝΑΓΩΓΗ 1 ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ Ορισμοί : -Αριθμός οξείδωσης: I)Σε μία ιοντική ένωση ο αριθμός οξείδωσης κάθε στοιχείου είναι ίσος με το ηλεκτρικό φορτίο που έχει το
Κεφάλαιο 1ο-ΟΞΕΙΔΩΑΝΑΓΩΓΗ 1 ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ Ορισμοί : -Αριθμός οξείδωσης: I)Σε μία ιοντική ένωση ο αριθμός οξείδωσης κάθε στοιχείου είναι ίσος με το ηλεκτρικό φορτίο που έχει το
*M * K E M I J A. Izpitna pola 1. Četrtek, 27. avgust 2009 / 90 minut JESENSKI IZPITNI ROK
 Š i f r a k a n d i d a t a : ržavni izpitni center *M09243111* JESENSKI IZPITNI ROK K E M I J Izpitna pola 1 Četrtek, 27. avgust 2009 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Š i f r a k a n d i d a t a : ržavni izpitni center *M09243111* JESENSKI IZPITNI ROK K E M I J Izpitna pola 1 Četrtek, 27. avgust 2009 / 90 minut ovoljeno gradivo in pripomočki: Kandidat prinese nalivno
Tabele termodinamskih lastnosti vode in vodne pare
 Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
αριθμός δοχείου #1# control (-)
 Μόνο απιονισμένο νερό #1# control (-) Μακροστοχεία: Ν, P, K, Ca, S, Εάν κάποια έλλειψη μετά 1 μήνα έχει σημαντικές επιπτώσεις προσθέτουμε σε δόσεις την έλλειψη έως ότου ανάπτυξη ΟΚ #2# control (+) Μακροστοχεία:
Μόνο απιονισμένο νερό #1# control (-) Μακροστοχεία: Ν, P, K, Ca, S, Εάν κάποια έλλειψη μετά 1 μήνα έχει σημαντικές επιπτώσεις προσθέτουμε σε δόσεις την έλλειψη έως ότου ανάπτυξη ΟΚ #2# control (+) Μακροστοχεία:
matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):
![matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij): matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):](/thumbs/87/96579490.jpg) 4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
Molekule. Za vodik dobimo gostoto 0,09 g/dm 3, za kisik 1,43 g/dm 3 in za ogljikov oksid 2,00 g/dm 3. Merilni balon
 23 Molekule Tehtanje plinov Reakcijska razmerja Molekule v plinih Molekule v gosti snovi Valenca atomov Velikost molekul Kilomol in kilomolska masa Splošna plinska konstanta Raztopine Osmozni tlak Reakcijske
23 Molekule Tehtanje plinov Reakcijska razmerja Molekule v plinih Molekule v gosti snovi Valenca atomov Velikost molekul Kilomol in kilomolska masa Splošna plinska konstanta Raztopine Osmozni tlak Reakcijske
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΔΙΕΠΙΣΤΗΜΟΝΙΚΟ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ (Δ.Π.Μ.Σ.) «ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ»
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΔΙΕΠΙΣΤΗΜΟΝΙΚΟ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ (Δ.Π.Μ.Σ.) «ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ» ΜΑΘΗΜΑ ΚΟΡΜΟΥ «ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ» ΥΔΑΤΙΚΑ ΟΙΚΟΣΥΣΤΗΜΑΤΑ Σημειώσεις
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΔΙΕΠΙΣΤΗΜΟΝΙΚΟ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ (Δ.Π.Μ.Σ.) «ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ» ΜΑΘΗΜΑ ΚΟΡΜΟΥ «ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΚΑΙ ΑΝΑΠΤΥΞΗ» ΥΔΑΤΙΚΑ ΟΙΚΟΣΥΣΤΗΜΑΤΑ Σημειώσεις
V tem poglavju bomo vpeljali pojem determinante matrike, spoznali bomo njene lastnosti in nekaj metod za računanje determinant.
 Poglavje IV Determinanta matrike V tem poglavju bomo vpeljali pojem determinante matrike, spoznali bomo njene lastnosti in nekaj metod za računanje determinant 1 Definicija Preden definiramo determinanto,
Poglavje IV Determinanta matrike V tem poglavju bomo vpeljali pojem determinante matrike, spoznali bomo njene lastnosti in nekaj metod za računanje determinant 1 Definicija Preden definiramo determinanto,
Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015)
 Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015) 1. Σε ποια απο τις παρακάτω ενώσεις το Ν έχει αριθμό οξέιδωσης +5 A. ΗΝΟ 2 C ΚΝΟ 3 B. ΝΗ 3 D Ν 2 Ο 3 2. Σε ποια απο τις παρακάτω
Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015) 1. Σε ποια απο τις παρακάτω ενώσεις το Ν έχει αριθμό οξέιδωσης +5 A. ΗΝΟ 2 C ΚΝΟ 3 B. ΝΗ 3 D Ν 2 Ο 3 2. Σε ποια απο τις παρακάτω
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ 1 ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ
 ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
*M * K E M I J A. Izpitna pola 2. Četrtek, 30. avgust 2007 / 90 minut JESENSKI ROK
 Š i f r a k a n d i d a t a : Državni izpitni center *M07243112* JESENSKI ROK K E M I J A Izpitna pola 2 Četrtek, 30. avgust 2007 / 90 minut Dovoljeno dodatno gradivo in pripomočki: Kandidat prinese s
Š i f r a k a n d i d a t a : Državni izpitni center *M07243112* JESENSKI ROK K E M I J A Izpitna pola 2 Četrtek, 30. avgust 2007 / 90 minut Dovoljeno dodatno gradivo in pripomočki: Kandidat prinese s
Χηµεία Α Γενικού Λυκείου
 Χηµεία Α Γενικού Λυκείου Απαντήσεις στα θέματα της Τράπεζας Θεμάτων Συγγραφή απαντήσεων: 'Αρης Ασλανίδης Χρησιμοποιήστε τους σελιδοδείκτες (bookmarks) στο αριστερό μέρος της οθόνης για την πλοήγηση μέσα
Χηµεία Α Γενικού Λυκείου Απαντήσεις στα θέματα της Τράπεζας Θεμάτων Συγγραφή απαντήσεων: 'Αρης Ασλανίδης Χρησιμοποιήστε τους σελιδοδείκτες (bookmarks) στο αριστερό μέρος της οθόνης για την πλοήγηση μέσα
KEMIJA PRVEGA LETNIKA
 KEMIJA naravoslovna znanost oz. veda, ki proučuje zakonitosti v naravi družboslovje proučuje zakonitosti v medčloveških odnosih matematika je veda, ki služi kot pripomoček k drugim naravoslovnim in družboslovnim
KEMIJA naravoslovna znanost oz. veda, ki proučuje zakonitosti v naravi družboslovje proučuje zakonitosti v medčloveških odnosih matematika je veda, ki služi kot pripomoček k drugim naravoslovnim in družboslovnim
Ονοματεπώνυμο: Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
2.1. Να χαρακτηρίσετε τις επόμενες προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ);
 Θέμα 2ο 2.1. Να χαρακτηρίσετε τις επόμενες προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ); α) Η διαφορά του ατομικού αριθμού από το μαζικό αριθμό ισούται με τον αριθμό νετρονίων του ατόμου. β) Το 19 Κ + έχει
Θέμα 2ο 2.1. Να χαρακτηρίσετε τις επόμενες προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ); α) Η διαφορά του ατομικού αριθμού από το μαζικό αριθμό ισούται με τον αριθμό νετρονίων του ατόμου. β) Το 19 Κ + έχει
Katedra za farmacevtsko kemijo. Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks. 25/11/2010 Vaje iz Farmacevtske kemije 3 1
 Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
Πορεία ανακρυστάλλωσης: Τα συνήθη βήματα μιας ανακρυστάλλωσης είναι τα ακόλουθα:
 Εργαστήριο Οργ. Χημείας 1 ου Εξαμήνου - Περιεχόμενα Μαθήματος Εισαγωγή στο Εργαστήριο Οργανικής Χημείας. Υάλινα σκεύη-θερμαντικά και ψυκτικά μέσα-γνωριμία με τις οργανικές ενώσεις Υγρά-στερεά; τήξη, βρασμός,
Εργαστήριο Οργ. Χημείας 1 ου Εξαμήνου - Περιεχόμενα Μαθήματος Εισαγωγή στο Εργαστήριο Οργανικής Χημείας. Υάλινα σκεύη-θερμαντικά και ψυκτικά μέσα-γνωριμία με τις οργανικές ενώσεις Υγρά-στερεά; τήξη, βρασμός,
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2015 Β ΦΑΣΗ ΕΚΦΩΝΗΣΕΙΣ ÏÅÖÅ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
Laboratorij za termoenergetiko. Vodikove tehnologije in PEM gorivne celice
 Laboratorij za termoenergetiko Vodikove tehnologije in PEM gorivne celice Pokrivanje svetovnih potreb po energiji premog 27% plin 22% biomasa 10% voda 2% sonce 0,4% veter 0,3% nafta 32% jedrska 6% geoterm.
Laboratorij za termoenergetiko Vodikove tehnologije in PEM gorivne celice Pokrivanje svetovnih potreb po energiji premog 27% plin 22% biomasa 10% voda 2% sonce 0,4% veter 0,3% nafta 32% jedrska 6% geoterm.
ZGRADBA ATOMA IN PERIODNI SISTEM
 ZGRADBA ATOMA IN PERIODNI SISTEM Kemijske lastnosti elementov se periodično spreminjajo z naraščajočo relativno atomsko maso oziroma kot vemo danes z naraščajočim vrstnim številom. Dmitrij I. Mendeljejev,
ZGRADBA ATOMA IN PERIODNI SISTEM Kemijske lastnosti elementov se periodično spreminjajo z naraščajočo relativno atomsko maso oziroma kot vemo danes z naraščajočim vrstnim številom. Dmitrij I. Mendeljejev,
SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK
 SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
Αλληλεπίδραση ακτίνων-χ με την ύλη
 Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
Άσκηση. Ισχυρό οξύ: Η 2 SeO 4 Ασθενές οξύ: (CH 3 ) 2 CHCOOH Ισχυρή βάση: KOH Ασθενής βάση: (CH 3 ) 2 CHNH 2
 Ασκήσεις κεφ. 1-3 Άσκηση Κατατάξτε τις παρακάτω ενώσεις ως ισχυρά και ασθενή οξέα ή ισχυρές και ασθενείς βάσεις α) Η 2 SeO 4, β) (CH 3 ) 2 CHCOOH γ) KOH, δ) (CH 3 ) 2 CHNH 2 Ισχυρό οξύ: Η 2 SeO 4 Ασθενές
Ασκήσεις κεφ. 1-3 Άσκηση Κατατάξτε τις παρακάτω ενώσεις ως ισχυρά και ασθενή οξέα ή ισχυρές και ασθενείς βάσεις α) Η 2 SeO 4, β) (CH 3 ) 2 CHCOOH γ) KOH, δ) (CH 3 ) 2 CHNH 2 Ισχυρό οξύ: Η 2 SeO 4 Ασθενές
Α ΤΑΞΗ ΛΥΚΕΙΟΥ ΑΠΑΝΤΗΣΕΙΣ
 ΑΡΧΗ 1 ΗΣ ΣΕΛΙΔΑΣ Α ΤΑΞΗ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 23/04/2014 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας το γράµµα που αντιστοιχεί
ΑΡΧΗ 1 ΗΣ ΣΕΛΙΔΑΣ Α ΤΑΞΗ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 23/04/2014 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας το γράµµα που αντιστοιχεί
ΦΡΟΝΤΙΣΤΗΡΙΟ Μ.Ε. ΣΥΜΒΟΛΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
Το άτομο του Υδρογόνου
 Το άτομο του Υδρογόνου Δυναμικό Coulomb Εξίσωση Schrödinger h e (, r, ) (, r, ) E (, r, ) m ψ θφ r ψ θφ = ψ θφ Συνθήκες ψ(, r θφ, ) = πεπερασμένη ψ( r ) = 0 ψ(, r θφ, ) =ψ(, r θφ+, ) π Επιτρεπτές ενέργειες
Το άτομο του Υδρογόνου Δυναμικό Coulomb Εξίσωση Schrödinger h e (, r, ) (, r, ) E (, r, ) m ψ θφ r ψ θφ = ψ θφ Συνθήκες ψ(, r θφ, ) = πεπερασμένη ψ( r ) = 0 ψ(, r θφ, ) =ψ(, r θφ+, ) π Επιτρεπτές ενέργειες
C M. V n: n =, (D): V 0,M : V M P = ρ ρ V V. = ρ
 »»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
»»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
Θέμα Α. Ονοματεπώνυμο: Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
2 η ΕΞΕΤΑΣΤΙΚΗ ΠΕΡΙΟΔΟΣ. Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Α1. Να βρεθεί η δομή των παρακάτω ατόμων: 23 11 Na, 40 20 Ca, 33 16 S, 127 53 I, 108
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Α1. Να βρεθεί η δομή των παρακάτω ατόμων: 23 11 Na, 40 20 Ca, 33 16 S, 127 53 I, 108
p 1 ENTROPIJSKI ZAKON
 ENROPIJSKI ZAKON REERZIBILNA srememba: moža je obrjea srememba reko eakih vmesih staj kot rvota srememba. Po obeh sremembah e sme biti obeih trajih srememb v bližji i dalji okolici. IREERZIBILNA srememba:
ENROPIJSKI ZAKON REERZIBILNA srememba: moža je obrjea srememba reko eakih vmesih staj kot rvota srememba. Po obeh sremembah e sme biti obeih trajih srememb v bližji i dalji okolici. IREERZIBILNA srememba:
Κεφάλαιο 1 Πραγματικοί Αριθμοί 1.1 Σύνολα
 x 2 + 1 = 0 N = {1, 2, 3....}, Z Q a, b a, b N c, d c, d N a + b = c, a b = d. a a N 1 a = a 1 = a. < > P n P (n) P (1) n = 1 P (n) P (n + 1) n n + 1 P (n) n P (n) n P n P (n) P (m) P (n) n m P (n + 1)
x 2 + 1 = 0 N = {1, 2, 3....}, Z Q a, b a, b N c, d c, d N a + b = c, a b = d. a a N 1 a = a 1 = a. < > P n P (n) P (1) n = 1 P (n) P (n + 1) n n + 1 P (n) n P (n) n P n P (n) P (m) P (n) n m P (n + 1)
1 η Σειρά προβλημάτων στο μάθημα Εισαγωγική Χημεία
 1 η Σειρά προβλημάτων στο μάθημα Εισαγωγική Χημεία Ημ. Παράδοσης: Δευτέρα 25/11/2013 11 πμ 1. Οι αντιδράσεις οξειδοαναγωγής σώζουν ζωές!!! Οι αερόσακοι στα αυτοκίνητα, όταν ανοίγουν γεμίζουν με άζωτο το
1 η Σειρά προβλημάτων στο μάθημα Εισαγωγική Χημεία Ημ. Παράδοσης: Δευτέρα 25/11/2013 11 πμ 1. Οι αντιδράσεις οξειδοαναγωγής σώζουν ζωές!!! Οι αερόσακοι στα αυτοκίνητα, όταν ανοίγουν γεμίζουν με άζωτο το
Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ. Παππάς Χρήστος Επίκουρος Καθηγητής
 ΗΛΕΚΤΡΟΝΙΚΗ ΟΜΗ ΚΑΙ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ Παππάς Χρήστος Επίκουρος Καθηγητής ΤΟ ΜΕΓΕΘΟΣ ΤΩΝ ΑΤΟΜΩΝ Ατομική ακτίνα (r) : ½ της απόστασης μεταξύ δύο ομοιοπυρηνικών ατόμων, ενωμένων με απλό ομοιοπολικό δεσμό.
ΗΛΕΚΤΡΟΝΙΚΗ ΟΜΗ ΚΑΙ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ Παππάς Χρήστος Επίκουρος Καθηγητής ΤΟ ΜΕΓΕΘΟΣ ΤΩΝ ΑΤΟΜΩΝ Ατομική ακτίνα (r) : ½ της απόστασης μεταξύ δύο ομοιοπυρηνικών ατόμων, ενωμένων με απλό ομοιοπολικό δεσμό.
3 o Μάθημα : Αντιδράσεις απλής αντικατάστασης
 3 o Μάθημα : Αντιδράσεις απλής αντικατάστασης 1. Στόχοι του μαθήματος Οι μαθητές να γνωρίσουν:i) πότε πραγματοποιείται μια αντίδραση απλής αντικατάστασης, με βάση τη σειρά δραστικότητας των μετάλλων και
3 o Μάθημα : Αντιδράσεις απλής αντικατάστασης 1. Στόχοι του μαθήματος Οι μαθητές να γνωρίσουν:i) πότε πραγματοποιείται μια αντίδραση απλής αντικατάστασης, με βάση τη σειρά δραστικότητας των μετάλλων και
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 15. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 15. oktober 2013 Oglejmo si, kako množimo dve kompleksni števili, dani v polarni obliki. Naj bo z 1 = r 1 (cosϕ 1 +isinϕ 1 )
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 15. oktober 2013 Oglejmo si, kako množimo dve kompleksni števili, dani v polarni obliki. Naj bo z 1 = r 1 (cosϕ 1 +isinϕ 1 )
ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ
 ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Σκοπός Εργαστηριακής Άσκησης Η παρατήρηση και η κατανόηση των μηχανισμών των οξειδοαναγωγικών δράσεων. Θεωρητικό Μέρος Οξείδωση ονομάζεται κάθε αντίδραση κατά την οποία συμβαίνει
ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Σκοπός Εργαστηριακής Άσκησης Η παρατήρηση και η κατανόηση των μηχανισμών των οξειδοαναγωγικών δράσεων. Θεωρητικό Μέρος Οξείδωση ονομάζεται κάθε αντίδραση κατά την οποία συμβαίνει
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ
 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
ΝΟΜΟΣ ΤΗΣ ΠΕΡΙΟ ΙΚΟΤΗΤΑΣ : Οι ιδιότητες των χηµικών στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ
 ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ Ορισμοί : -Αριθμός οξείδωσης: I)Σε μία ιοντική ένωση ο αριθμός οξείδωσης κάθε στοιχείου είναι ίσος με το ηλεκτρικό φορτίο που έχει το αντίστοιχο ιόν Παράδειγμα:
ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ Ορισμοί : -Αριθμός οξείδωσης: I)Σε μία ιοντική ένωση ο αριθμός οξείδωσης κάθε στοιχείου είναι ίσος με το ηλεκτρικό φορτίο που έχει το αντίστοιχο ιόν Παράδειγμα:
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (Επιλέγετε δέκα από τα δεκατρία θέματα) ΘΕΜΑΤΑ 1. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λάθος; Γιατί; (α) Από τα στοιχεία Mg, Al, Cl, Xe, C και Ρ, τον μεγαλύτερο
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (Επιλέγετε δέκα από τα δεκατρία θέματα) ΘΕΜΑΤΑ 1. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λάθος; Γιατί; (α) Από τα στοιχεία Mg, Al, Cl, Xe, C και Ρ, τον μεγαλύτερο
Χημεία Α ΓΕΛ 15 / 04 / 2018
 Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
ΑΠΑΝΤΗΣΕΙΣ ΤΩΝ ΘΕΜΑΤΩΝ
 ΑΘΗΑ - ΕΞΕΤΑΖΟΕΝΗ ΥΛΗ ΧΗΕΙΑ Γ ΛΥΚΕΙΟΥ ΚΑΘΗΓΗΤΗΣ ΤΗΑ ΠΑΡΑΡΤΗΑ ΔΙΑΡΚΕΙΑ 3 ΩΡΕΣ ΘΕΑ Α ΑΠΑΝΤΗΣΕΙΣ ΤΩΝ ΘΕΑΤΩΝ Α1. 3, Α2. 3, Α3. 2, Α4. 3 Α5. 1. Λάθος, 2. Λάθος, 3. Σωστό, 4. Λάθος, 5. Σωστό. ΘΕΑ Β Β1. Ι) 1.
ΑΘΗΑ - ΕΞΕΤΑΖΟΕΝΗ ΥΛΗ ΧΗΕΙΑ Γ ΛΥΚΕΙΟΥ ΚΑΘΗΓΗΤΗΣ ΤΗΑ ΠΑΡΑΡΤΗΑ ΔΙΑΡΚΕΙΑ 3 ΩΡΕΣ ΘΕΑ Α ΑΠΑΝΤΗΣΕΙΣ ΤΩΝ ΘΕΑΤΩΝ Α1. 3, Α2. 3, Α3. 2, Α4. 3 Α5. 1. Λάθος, 2. Λάθος, 3. Σωστό, 4. Λάθος, 5. Σωστό. ΘΕΑ Β Β1. Ι) 1.
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ
 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
Παραδοχές στις οποίες στις οποίες στηρίζεται ο αριθμός οξείδωσης
 Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
ΥΠΟΥΡΓΕΙΟ ΠΟΛΙΤΙΣΜΟΥ, ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ. Χημεία
 ΥΠΟΥΡΓΕΙΟ ΠΟΛΙΤΙΣΜΟΥ, ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ Χημεία Λύσεις Ασκήσεων Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Ομάδας Προσανατολισμού Θετικών Σπουδών ΙΝΣΤΙΤΟΥΤΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΠΟΛΟΓΙΣΤΩΝ ΚΑΙ
ΥΠΟΥΡΓΕΙΟ ΠΟΛΙΤΙΣΜΟΥ, ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ Χημεία Λύσεις Ασκήσεων Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Ομάδας Προσανατολισμού Θετικών Σπουδών ΙΝΣΤΙΤΟΥΤΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΠΟΛΟΓΙΣΤΩΝ ΚΑΙ
Raztopine. Raztopine. Elektroliti. Elektrolit je substanca, ki pri raztapljanju (v vodi) daje ione. A a B b aa b+ + bb a-
 Raztopine Mnoge analizne metode temeljijo na opazovanju ravnotežnih sistemov, ki se vzpostavijo v raztopinah. Najpogosteje uporabljeno topilo je voda! RAZTOPINE: topljenec topilo (voda) (Enote za koncentracije!)
Raztopine Mnoge analizne metode temeljijo na opazovanju ravnotežnih sistemov, ki se vzpostavijo v raztopinah. Najpogosteje uporabljeno topilo je voda! RAZTOPINE: topljenec topilo (voda) (Enote za koncentracije!)
Ερωηήζεις Πολλαπλής Επιλογής
 Ερωηήζεις Θεωρίας 1. Ππθλφηεηα: α) δηαηχπσζε νξηζκνχ, β) ηχπνο, γ) είλαη ζεκειηψδεο ή παξάγσγν κέγεζνο;, δ) πνηα ε κνλάδα κέηξεζήο ηεο ζην Γηεζλέο Σχζηεκα (S.I.); ε) πνηα ε ρξεζηκφηεηά ηεο; 2. Γηαιπηφηεηα:
Ερωηήζεις Θεωρίας 1. Ππθλφηεηα: α) δηαηχπσζε νξηζκνχ, β) ηχπνο, γ) είλαη ζεκειηψδεο ή παξάγσγν κέγεζνο;, δ) πνηα ε κνλάδα κέηξεζήο ηεο ζην Γηεζλέο Σχζηεκα (S.I.); ε) πνηα ε ρξεζηκφηεηά ηεο; 2. Γηαιπηφηεηα:
