Πρόρρηση Ισορροπίας Φάσεων. Χαμηλές Πιέσεις
|
|
|
- Ωρίων Διαμαντόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 Πρόρρηση Ισορροπίας Φάσεων Χαμηλές Πιέσεις
2 Ισορροπία Φάσεων Η βασική εξίσωση ια όλους τους υπολοισμούς ισορροπίας φάσεων ατμού-υρού είτε σε υψηλές είτε σε χαμηλές πιέσεις είναι η ισότητα των τάσεων διαφυής ια όλα τα συστατικά του μίματος: fˆ L fˆ V Η ποσοτική περιραφή της ισορροπίας ατμού-υρού εκφράζεται συνήθως με τους λόους ισορροπίας K : K y x Η σχετική πτητικότητα, α j, είναι η βασική ιδιότητα που προσδιορίζει την ευκολία ενός διαχωρισμού και χρησιμοποιείται στις απλοποιημένες μεθόδους σχεδιασμού a j K K j
3 3 Μη πολικά συστατικά Υψηλές πιέσεις: όπου οι συντελεστές τάσης διαφυής υπολοίζονται με κυβικές καταστατικές εξισώσεις (π.χ. PR ή SRK). Antone με Vral με ˆ, ˆ v P φ φ P x f P y f L L v v φ φ ˆ ˆ ˆ ˆ L v v Pe P x f P y f ) ( ˆ ˆ ˆ ˆ φ φ Πολικά συστατικά - Χαμηλές πιέσεις: όπου : UNIFAC Van Laar, Wlon, με ) ( exp ) ( l P P RT v Pe Υπολοισμοί Ισορροπίας Φάσεων Ιδανικά Διαλύματα Νόμος Raoult P P K / Ανάλοα με τη φύση των συστατικών του μίματος (ή της ολικής πίεσης του συστήματος) οι τάσεις διαφυής υπολοίζονται - ανάλοα και με τη φάση - ως: v L x y K φ φ ˆ / ˆ / j j P P a P Pe P K v φ φ ˆ / ) ( ˆ
4 Η Περίσσεια Ελεύθερης Ενέρειας Gbb και ο Συντελεστής Ενερότητας. ln E ( NG /RT ) N T, P, N j Σχόλια.Σε ένα ιδανικό μίμα η περίσσεια ελεύθερης ενέρειας Gbb είναι μηδέν, συνεπώς όλοι οι συντελεστές ενερότητας σε ένα τέτοιο μίμα είναι ίσοι με τη μονάδα.. Η ως άνω εξίσωση αποτελεί τη βάση ια την ανάπτυξη αναλυτικών εκφράσεων ια τους συντελεστές ενερότητας, όπως αυτές των van Laar, Margule, Wlon, κλπ. Για το σκοπό αυτό χρησιμοποιούνται ποιοτικές και ποσοτικές παραδοχές ια την ερμηνεία της απόκλισης ενός διαλύματος από την ιδανικότητα στις ίδιες συνθήκες, ώστε να αναπτυχθούν αναλυτικές εκφράσεις ια το G E ως συνάρτηση της θερμοκρασίας, της πίεσης και της συκέντρωσης. Με κατάλληλη παραώισή τους λαμβάνονται οι αναλυτικές εκφράσεις ια το συντελεστή ενερότητας κάθε συστατικού του μίματος.
5 Εκτίμηση του Συντελεστή Ενερότητας (Πειραματικά) Για ένα σύστημα Α-Υ που ισορροπεί μπορούν να μετρηθούν: * πίεση: Ρ * θερμοκρασία: Τ * σύσταση της υρής φάσης: (x, x ) * σύσταση της φάσης των ατμών: (y, y ) Από την εξίσωση των τάσεων διαφυής ια χαμηλές πιέσεις: fˆ L fˆ V x P y ˆ φ P φ (Pe ) ˆv, ˆ φ φ με Vral : B P φ ln φ ( y j Bj B) P RT RT ln ( Pe) l v exp ( P P ) RT P με Antone 5
6 Παράδειμα Για το σύστημα ακετόνης()-κυκλοεξανίου() στους 5 o C δίνονται τα δεδομένα του Πίνακα 3.Π. (Gmehlng et al, 979). Για διευκόλυνση των υπολοισμών και εξαιτίας των χαμηλών πιέσεων μπορεί να υποτεθεί ότι ο ατμός ακολουθεί ιδανική συμπεριφορά. Να υπολοιστούν οι συντελεστές ενερότητας yp x P, y P x P Από Antone P 9.9 mmhg και P 97.6 mmhg (πειραματικές τιμές και mmhg). Πίνακας 3.Π. Δεδομένα ισορροπίας ατμού-υρού ια το σύστημα ακετόνης()-κυκλοεξανίου() στους 5 o C. P (mm Hg) x y ln( / ) y P x P F ΣΧΟΛΙΟ F φ φ (Pe ) Για χαμηλές πιέσεις έως -3 bar, οι τιμές του F είναι πρακτικά στην περιοχή από 0.9 έως.. Αυτό δεν ισχύει σε συστήματα, που περιέχουν ορανικά οξέα, και συνεπώς, παρουσιάζουν μεάλες αποκλίσεις από την ιδανική συμπεριφορά, ακόμη και σε υποατμοσφαιρικές πιέσεις. 6
7 Έλεχος Θερμοδυναμικής Συνέπειας Πειραματικών Δεδομένων Η Gbb-Duhem όταν εφαρμόζεται ια την περίσσεια ελεύθερης ενέρειας Gbb δίνει: RT x d ln V όπου V Ε, S Ε είναι η περίσσεια του μολαρικού όκου και της εντροπίας του μίματος αντίστοιχα, σε δεδομένη θερμοκρασία, πίεση και σύσταση. Δηλαδή, οι συντελεστές ενερότητας των συστατικών ενός μίματος, που ισορροπεί, δεν μπορούν να μεταβάλλονται ανεξάρτητα: πρέπει να ικανοποιούν την ως άνω εξίσωση προκειμένου να είναι αποδεκτοί από θερμοδυναμική άποψη. Με ολοκλήρωση από x 0.0 σε x.0 ια ένα δυαδικό σύστημα προκύπτει: E dp S E dt ln 0 dx 0 H RT E dt dx dx (P : σταθερή) ln 0 dx 0 E V RT dp dx dx (T : σταθερή) 7
8 Έλεχος Θερμοδυναμικής Συνέπειας Πειραματικών Δεδομένων Area Tet Για ισοθερμοκρασιακά δεδομένα, ο δείκτης συνέπειας (C.I.: contency ndex) ορίζεται από την: CI A p A n A + A x00 p n ln 0 ln 0 dx 0 dx 0 (P : σταθερή) (T : σταθερή) όπου τα Α p, A n είναι εμβαδά επάνω και κάτω από το ln( / ) αντίστοιχα, και αποτελεί το μέτρο της ποιότητας των δεδομένων. Για ισοβαρή δεδομένα, μέτρο της ποιότητάς τους αποτελεί η ποσότητα (CI-J ), όπου το J δίνεται από τη σχέση: T J 50 T, T T max T mn mn Σχήμα 3.8 Έλεχος θερμοδυναμικής συνέπειας ια το σύστημα ακετόνης - κυκλοεξανίου στους 5 ο C. T max και T mn είναι τα ακρότατα της θερμοκρασίας ια το δυαδικό σύστημα, συμπεριλαμβανομένων των σημείων βρασμού των καθαρών συστατικών και του αζεοτρόπου, εάν υπάρχει, ενώ ο συντελεστής 50 είναι εμπειρικός και προτείνεται από τον Herngton με βάση τυπικά δεδομένα θερμοτήτων ανάμιξης (Prauntz). 3. Τιμές του CΙ μικρότερες του 5, ια ισοθερμοκρασιακά, και του (CI-J ) μικρότερες του 0, ια ισοβαρή, υποδεικνύουν καλά δεδομένα.
9 Έλεχος Θερμοδυναμικής Συνέπειας Πειραματικών Δεδομένων Area Tet CI A p A n A + A x00 p n T J 50 T, T T max T mn mn Τύπος Ισόθερμα (CI ) Ισοβαρή (CI-J ) Αριθμός % Καλά < 5 < Ικανοποιητικά Μικρής Ακρίβειας > 5 > Αναπόδεκτα: area tet αδύνατο 6 6 Σύνολο Πίνακας 3. Κατάταξη των τυπικών δεδομένων ΙΑΥ δυαδικών συστημάτων της βιβλιοραφίας σύμφωνα με το Area Thermodynamc Contency Tet (Slverman) Σχόλιο: Η ποιότητα των δεδομένων της βιβλιοραφίας απεικονίζεται στον Πίνακα 3. (Slverman, 984), που δείχνει ότι περίπου 40 % των δεδομένων από δυαδικά συστήματα που ελέχθηκαν, δεν ικανοποιεί τον παραπάνω έλεχο. 9
10 Συντελεστής Ενερότητας (Ποιοτικές παρατηρήσεις) Παράοντες που επηρεάζουν τους συντελεστές ενερότητας: * πίεση: Ρ * θερμοκρασία: Τ * φύση των συστατικών * σύσταση των φάσεων: (x, y ) 0
11 Επίδραση πίεσης και θερμοκρασίας V Πίεση Η επίδραση της πίεσης στο συντελεστή ενερότητας σε σταθερή θερμοκρασία και σύσταση δίνεται από τον τύπο: E ln P T,x E V RT είναι ο μερικός μολαρικός όκος περίσσειας του συστατικού στην υρή φάση. Σε χαμηλές πιέσεις είναι μία μικρή ποσότητα. Συνεπώς η επίδραση της πίεσης στο είναι πολύ μικρή. Θερμοκρασία Η επίδραση της θερμοκρασίας στο συντελεστή ενερότητας - σε σταθερή πίεση και συκέντρωση - δίνεται από τον τύπο: ln T P,x H RT E Παράδειμα: Διάλυμα νερού() και μεθανόλης() σε x 0.7, t 5 o E C, P atm, και V 0.3 cm 3 /mol. Υποθέτοντας ότι η τιμή τουv είναι ανεξάρτητη της πίεσης, τότε ο συντελεστής ενερότητας του νερού σε κάποια πίεση P, έστω 5 atm, σχετικά με την τιμή του στη atm, είναι: [5 atm] [ atm] που αποτελεί αμελητέα επίδραση (ίνεται όμως σημαντική σε υψηλές T και P ). E Σχήμα 3.7 Μεταβολή του συντελεστή ενερότητας άπειρης αραίωσης με τη θερμοκρασία (Perott et al, 959).
12 Επίδραση της φύσης και της συκέντρωσης των συστατικών P( deal ) x P + x P P + ( P P ) x P( real ) x P + x P Σχήμα 3.3 Θετικές (a) και αρνητικές (b) αποκλίσεις από τον νόμο του Raoult. Σχήμα 3. Πειραματικά προσδιορισμένοι συντελεστές ενερότητας (οι συνεχείς ραμμές προκύπτουν από την εξίσωση Margule με χρήση συντελεστών ενερότητας άπειρης αραίωσης). * Θετικές αποκλίσεις από το νόμο του Raoult: κ-επτάνιο()/π-διοξάνιο() στους 80 ο C. * Aρνητικές αποκλίσεις από το νόμο του Raoult: βουτυλαμίνη()/-προπανόλη() στους 45 ο C. Σχήμα 3.4 T-x-y (a) και y-x (b) διαράμματα ια το σύστημα -προπανόλης() και νερού() σε atm. L: Υρό, V: Ατμός.
13 Επίδραση της φύσης και της συκέντρωσης των συστατικών P( deal ) x P + x P P + ( P P ) x P( real ) x P + x P Σχήμα 3.5 Συντελεστές ενερότητας του κ-εννεανίου() σε μίμα με πολυβουταδιένιο () στους 00 ο C (Για διαλύματα πολυμερών χρησιμοποιείται συνήθως το κλάσμα όκου Φ αντί ια το ραμμομοριακό κλάσμα). Σχήμα 3.6 Επίδραση της ανομοιότητας των συστατικών ενός δυαδικού μίματος στο συντελεστή ενερότητας.
14 Συντελεστής Ενερότητας (Ποιοτικές παρατηρήσεις) Οι ποιοτικές παρατηρήσεις ια το συντελεστή ενερότητας συνοψίζονται στα ακόλουθα:. Ο συντελεστής ενερότητας είναι το μέτρο της απόκλισης από τη συμπεριφορά του ιδανικού διαλύματος, ο συντελεστής διόρθωσης στο νόμο του Raoult.. Όσο μειώνεται η συκέντρωση ενός δεδομένου συστατικού, τόσο αυξάνεται η απόκλιση του από τη μονάδα. 3. Όσο αυξάνεται η ανομοιότητα μεταξύ των συστατικών του μίματος, τόσο αυξάνεται η απόκλιση από την ιδανικότητα (και οι τιμές των από τη μονάδα). 4. Η ανομοιότητα μεταξύ των φυσικοχημικών δυνάμεων έχει τις πιο σημαντικές επιδράσεις στις τιμές των, ακολουθουμένη από την ανομοιότητα των μολαρικών όκων, η οποία κυριαρχεί στα συστήματα διαλύτη-πολυμερούς. 5. Τα περισσότερα συστήματα παρουσιάζουν θετικές αποκλίσεις από το νόμο του Raoult (εκτός από τα συστήματα διαλύτη-πολυμερούς). 6. Τυπικές τιμές των θετικών αποκλίσεων των : τελείως αναμίξιμα συστήματα:. - 0 μερικώς αναμίξιμα συστήματα: 0-00 μη αναμίξιμα συστήματα: 00 - πολύ υψηλές τιμές. (Ο συντελεστής ενερότητας άπειρης αραίωσης του βενζολίου στο νερό είναι της τάξης των 0000 με διαλυτότητα της τάξης των ppm). 7. Για αρνητικές αποκλίσεις, τα είναι τυπικά μεταξύ 0.5 και 0.9. Ακόμη μικρότερες τιμές εμφανίζονται ια το συντελεστή ενερότητας του διαλύτη σε συστήματα διαλύτη-πολυμερούς (Σχήμα 3.5). 4
15 Οι Εκφράσεις Τύπου Wohl H Γενική Έκφραση ια ένα Δυαδικό Σύστημα Ο Wohl (959) εξέφρασε την περίσσεια της ελεύθερης ενέρειας κατά Gbb σε ένα διάλυμα δύο συστατικών με μία δυναμοσειρά των "ενερών" κλασμάτων όκου των δύο συστατικών, z και z : E G RT( q x +q x ) a z z + 3a z z + 3a z z +... z x q xq + x q, z x q xq + x q q : μέτρο του μεέθους του μορίου ή της "σφαίρας επιρροής" του στο διάλυμα. a : παράμετρος αλληλεπίδρασης με φυσική σημασία παρόμοια με εκείνη των συντελεστών Vral.
16 Η εξίσωση van Laar Για ένα δυαδικό σύστημα, του οποίου τα συστατικά δεν είναι ιδιαίτερα ανόμοια χημικά, αλλά έχουν διαφορετικούς μολαρικούς όκους, μπορεί να υποτεθεί ότι οι συντελεστές αλληλεπίδρασης περισσοτέρων των δύο μορίων είναι αμελητέοι. Τότε η έκφραση του Wohl ίνεται: G E RT a Από την εξίσωση αυτή, προκύπτουν οι παρακάτω εκφράσεις ια τους συντελεστές ενερότητας: x όπου: A q a και B q a x x qq q + x q A ln [ ] +(Ax )/(Bx ) B ln [ ] +(Bx )/(Ax ) Σημείωση: Για την ακρίβεια ο van Laar - μαθητής και αρότερα συνεράτης του van der Waal - ανέπτυξε την έκφρασή του αρχίζοντας με την ΚΕ vdw.
17 Η Εξίσωση Margule Εάν τα μεέθη των μορίων των συστατικών ενός δυαδικού μίματος δεν είναι πολύ διαφορετικά, μπορεί να υποτεθεί ότι q q q και, αμελώντας τις αλληλεπιδράσεις μεταξύ περισσοτέρων των τριών μορίων, προκύπτουν οι παρακάτω εκφράσεις ια τους συντελεστές ενερότητας (διπαραμετρική εξίσωση Margule): 3 A x + B x ln A + B x -B x 3 3 ln όπου: A' q(a + 6a - 3a ) και B' q(6a - 6a ).
18 ΒΕΝΖΟΛΙΟ/,,4 ΤΡΙΜΕΘΥΛΟ ΠΕΝΤΑΝΙΟ ΣΤΟΥΣ 55 o C Ερώτηση: Πώς υπολοίζονται οι συντελεστές των εξισώσεων?
19 Εκτίμηση δυαδικών παραμέτρων,exp,exp,calc,exp,exp,calc + Q Καμπύλες σταθερής τιμής Q ια το σύστημα αιθανόλης-νερού στους 5 ο C με την εξίσωση Wlon.
20 Μοντέλα Τοπικής Σύστασης Το 964 ο Wlon πρότεινε ότι ια δεδομένο διάλυμα - δυαδικό έστω - σε μοριακό επίπεδο υπάρχουν δύο είδη "κυττάρων" : * ένα, που σχηματίζεται από τα μόρια, που περιβάλλουν ένα μόριο του συστατικού, και * ένα, που σχηματίζεται από τα μόρια, που περιβάλλουν ένα μόριο του συστατικού. Ακόμη περισσότερο, εξαιτίας των διαφορών στις δυνάμεις μεταξύ ομοίων και ανομοίων μορίων, οι παράμετροι της δυναμικής ενέρειας λ, λ και λ λ είναι διαφορετικές, οπότε οδηούν σε τοπικές συστάσεις, που δεν είναι όμοιες με την ολική σύσταση. Εάν, ια παράδειμα, οι - και - αλληλεπιδράσεις είναι ισχυρότερες από τις -, τα μόρια θα προτιμούν να περιβάλλονται από όμοιά τους. Έτσι, τα μολαρικά κλάσματα x j των "κυττάρων«, που αναφέρονται ως τοπικά (local) μολαρικά κλάσματα - με το να αντιπροσωπεύει το μόριο στο κέντρο του κυττάρου - διαφέρουν από τα ολικά. Δομή ρευστού σε τοπικό επίπεδο Στο ανωτέρω σχήμα είναι: x, x, x, x σε σύκριση με την ολική σύσταση: x x
21 Μοντέλα Τοπικής Σύστασης ln ln( Λ ) Η Εξίσωση Wlon x + x + x x + x x + x xj j x x x exp( λ /RT) j exp( λ /RT) Λ Λ ln ln( x + x Λ) + x x + x Λ x + x Λ Λ Λ Λ Λ Η Εξίσωση NRTL xj j x x x α j( g g j ) exp RT ln x τ G τ x + x G + G ( x + x G ) G τ G ln x τ + x+ xg ( x+ xg)
22 Tο μοντέλο UNIQUAC ια πολυσυστατικό μίμα ισχύει η σχέση: C ln ln + ln R όπου C είναι το συνδυαστικό τμήμα (διαφορές στο μέεθος και το σχήμα των μορίων) ln C Φ z Θ Φ ln + q ln + l Φ x j l j x x και R είναι το υπολειμματικό τμήμα (ενερειακές αλληλεπιδράσεις μεταξύ των μορίων) R ln q ln ( Θ τ j ) + q q Θ j Θ τ k j τ kj Θ και Φ κλάσματα επιφάνειας και όκου αντίστοιχα: Θ q x q j x j Φ r x r x z ο αριθμός σύνταξης ίσος με 0 q παράμετρος επιφάνειας r παράμετρος μεέθους Δu j ενερειακές παράμετροι Για τον υπολοισμό του απαιτούνται: l τ j j z exp ( r q ) ( r ) j j j u j R T α) x, T (ανεξάρτητες μεταβλητές) β) r, q, Δu j
23
24
25
26
27 Tο μοντέλο UNIFAC UNIquac Functonal group Actvty Coeffcent C ln ln + ln R ln C Φ z Θ Φ ln + q + ln l x j Φ l j x x Θ q x q j x j Φ r x r x l j z ( r q ) ( r ) j j j ν () () r k R k and q Q k k ν R [ ] Γ Γ () ln ln ln all group ν k k () k Θ m lnγ k Qk ln( Θm Ψmk) Q X m n m Q X n Θ Ψ m n km Θ Ψ nm U U a Ψmn exp ( ) exp RT T mn nn mn 7
28 Fg.. Current tatu of the UNIFAC group group nteracton parameter matrx (black, newly etmated parameter; lght grey, updated parameter; dark grey, orgnal parameter retaned wthout change). J.W. Kang, V. Dky, R.D. Chrco, J.W. Magee, C.D. Muzny, I. Abdulagatov, A.F. Kazakov, M. Frenkel A new method for evaluaton of UNIFAC nteracton parameter Flud Phae Equlbra, Vol 309(), 0, p
29
30
31 Τα Πλεονεκτήματα των Μοντέλων Τοπικής Σύστασης Τα μοντέλα τοπικής σύστασης υπερτερούν στην πρόρρηση των συντελεστών ενερότητας ως προς: την ποιότητα περιραφής των δυαδικών δεδομένων ΙΦΑΥ, την ευαισθησία των παραμέτρων στη θερμοκρασία, την πρόρρηση της πολυσυστατικής συμπεριφοράς μόνο από δυαδικά δεδομένα.
32 ΙΦΑΥ: Δύο προσείσεις φ φ- φ Πλεονεκτήματα Μειονεκτήματα Αξιόπιστη σε χαμηλές πιέσεις Δίνει καλά αποτελέσματα σε πολικά μίματα. Ιδιαίτερα τα μοντέλα NRTL και UNIQUAC Απλότητα Ευκολία στον προραμματισμό, ρήορα αποτελέσματα Η χρήση του μοντέλου UNIFAC οδηεί σε απευθείας πρόρρηση Εφαρμόζονται μόνο σε χαμηλές πιέσεις Απαιτούνται παράμετροι (πολλαπλά σετ), εκτός του μοντέλου UNIFAC Πλεονεκτήματα Μειονεκτήματα Εφαρμόζονται και σε υψηλές Τα και P Υπολοίζουν και PVT εκτός από ΙΦ Οι κυβικές ΚΕ έχουν ευκολία στον προραμματισμό, ρήορα αποτελέσματα Οι μη κυβικές ΚΕ είναι πολύπλοκες και απαιτούν μεάλους υπολοιστικούς χρόνους Οι κυβικές ΚΕ με κλασσικούς κανόνες ανάμειξης αποτυχάνουν στα πολικά μίματα
33 Συμπεράσματα. Η πιο σημαντική ποσότητα στην ΙΦΑΥ χαμηλών πιέσεων είναι ο συντελεστής ενερότητας, που αποτελεί το μέτρο της μη ιδανικότητας της υρής φάσης.. Ο συντελεστής ενερότητας είναι συνάρτηση της θερμοκρασίας και της σύστασης, ενώ η επίδραση της πίεσης είναι αμελητέα σε χαμηλές πιέσεις. 3. Οι πειραματικές μετρήσεις ΙΦΑΥ είναι δαπανηρές και χρονοβόρες, και συνεπώς, όποτε είναι δυνατό, χρησιμοποιούνται μέθοδοι πρόρρησης. 4. Τα μοντέλα τοπικής σύστασης: Wlon, NRTL/LEMF και UNIQUAC, παρέχουν εξαιρετικές συσχετίσεις των πειραματικών δεδομένων. 5. Τα ίδια μοντέλα παρέχουν αξιόπιστες προρρήσεις της πολυσυστατικής ΙΑΥ από δυαδικά δεδομένα. Η ακρίβεια ίνεται κάπως μικρότερη, όμως, ια ιδιαιτέρως μη ιδανικά διαλύματα. 6. Τα αποτελέσματα δεν είναι πολύ ευαίσθητα: o στην ποιότητα των δεδομένων των δυαδικών συστημάτων, που χρησιμοποιούνται o στη θερμοκρασία των δυαδικών δεδομένων σε σχέση με αυτή του εξεταζομένου o πολυσυστατικού συστήματος, και στη συνάρτηση ελαχιστοποίησης, που χρησιμοποιείται ια τον προσδιορισμό των τιμών των παραμέτρων από τα δεδομένα. 7. Για πλήρως αναμίξιμα συστήματα συνιστάται η εξίσωση Wlon, εξαιτίας της απλότητάς της. Σε περίπτωση συνδυασμού πλήρως και μερικώς αναμίξιμων συστημάτων, πρέπει να χρησιμοποιείται η εξίσωση UNIQUAC. 8. Στην περίπτωση ελλιπών δεδομένων, είναι συχνά δυνατόν να εκτιμηθεί η ΙΦΑΥ - κυρίως ια σκοπούς προκαταρκτικού σχεδιασμού- με το μοντέλο UNIFAC.
Πρόρρηση Ισορροπίας Φάσεων. Υψηλές Πιέσεις
 Πρόρρηση Ισορροπίας Φάσεων Υψηλές Πιέσεις 1 Ισορροπία Φάσεων Η βασική εξίσωση για όλους τους υπολογισμούς ισορροπίας φάσεων ατμού-υγρού είτε σε υψηλές είτε σε χαμηλές πιέσεις είναι η ισότητα των τάσεων
Πρόρρηση Ισορροπίας Φάσεων Υψηλές Πιέσεις 1 Ισορροπία Φάσεων Η βασική εξίσωση για όλους τους υπολογισμούς ισορροπίας φάσεων ατμού-υγρού είτε σε υψηλές είτε σε χαμηλές πιέσεις είναι η ισότητα των τάσεων
Πρόρρηση. Θερμοδυναμικών Ιδιοτήτων Μιγμάτων
 Πρόρρηση Θερμοδυναμικών Ιδιοτήτων Μιγμάτων 1 Χημικό Δυναμικό μ d = dg U = N V,S,N Για 1 mole καθαρής ουσίας: SdT +Vd j H = N S,,N j A = N V,T,N j G = N ( T, ) ( T,) = T T T,,N j SdT + όπου μ(t',') είναι
Πρόρρηση Θερμοδυναμικών Ιδιοτήτων Μιγμάτων 1 Χημικό Δυναμικό μ d = dg U = N V,S,N Για 1 mole καθαρής ουσίας: SdT +Vd j H = N S,,N j A = N V,T,N j G = N ( T, ) ( T,) = T T T,,N j SdT + όπου μ(t',') είναι
Ιδιότητες Μιγμάτων. Μερικές Μολαρικές Ιδιότητες
 Ιδιότητες Μιγμάτων Μερικές Μολαρικές Ιδιότητες ΙΔΑΝΙΚΟ ΔΙΑΛΥΜΑ = ή διαιρεμένη διά του = x όπου όλα τα προσδιορίζονται στην ίδια T και P. = Όπου ή διαιρεμένη διά του : = x ορίζεται η μερική μολαρική ιδιότητα
Ιδιότητες Μιγμάτων Μερικές Μολαρικές Ιδιότητες ΙΔΑΝΙΚΟ ΔΙΑΛΥΜΑ = ή διαιρεμένη διά του = x όπου όλα τα προσδιορίζονται στην ίδια T και P. = Όπου ή διαιρεμένη διά του : = x ορίζεται η μερική μολαρική ιδιότητα
Έκφραση της Ισορροπίας φάσεων ατμών υγρού με τη βοήθεια του Aspen plus
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Εργαστήριο Θερμοδυναμικής & Φαινομένων Μεταφοράς Έκφραση της Ισορροπίας φάσεων ατμών υγρού με τη βοήθεια του Aspen plus Η έννοια της ισορροπίας Εξ ορισμού
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Εργαστήριο Θερμοδυναμικής & Φαινομένων Μεταφοράς Έκφραση της Ισορροπίας φάσεων ατμών υγρού με τη βοήθεια του Aspen plus Η έννοια της ισορροπίας Εξ ορισμού
Ακρίβεια αποτελεσμάτων σχεδιασμού διεργασιών ΜΑΔ, 2013
 Ακρίβεια αποτελεσμάτων σχεδιασμού διεργασιών ΜΑΔ, 2013 1 ΣΚΟΠΟΣ και ΑΝΤΙΚΕΙΜΕΝΟ ΘΧΜ Σκοπός της θερμοδυναμικής χημικής μηχανικής είναι η παροχή των κατάλληλων θεωρητικών γνώσεων και των απαραίτητων υπολογιστικών-μεθοδολογικών
Ακρίβεια αποτελεσμάτων σχεδιασμού διεργασιών ΜΑΔ, 2013 1 ΣΚΟΠΟΣ και ΑΝΤΙΚΕΙΜΕΝΟ ΘΧΜ Σκοπός της θερμοδυναμικής χημικής μηχανικής είναι η παροχή των κατάλληλων θεωρητικών γνώσεων και των απαραίτητων υπολογιστικών-μεθοδολογικών
Πρόρρηση. Φυσικών Ιδιοτήτων Μιγμάτων
 Πρόρρηση Φυσικών Ιδιοτήτων Μιγμάτων Συντελεστής συμπιεστότητας, Ζ Αρχή Αντιστοίχων Καταστάσεων Τριών παραμέτρων Ptzer : z z (0) + ω z (1) Lee-Kesler: z (0), z (1) f(t r,p r ) Εξίσωση Ptzer Κανόνες Ανάμειξης
Πρόρρηση Φυσικών Ιδιοτήτων Μιγμάτων Συντελεστής συμπιεστότητας, Ζ Αρχή Αντιστοίχων Καταστάσεων Τριών παραμέτρων Ptzer : z z (0) + ω z (1) Lee-Kesler: z (0), z (1) f(t r,p r ) Εξίσωση Ptzer Κανόνες Ανάμειξης
ΑΝΑΛΥΣΗ ΚΑΙ ΣΧΕΔΙΑΣΜΟΣ ΔΙΕΡΓΑΣΙΩΝ ΔΙΑΧΩΡΙΣΜΟΥ ΜΑΔ, 2013
 ΑΝΑΛΥΣΗ ΚΑΙ ΣΧΕΔΙΑΣΜΟΣ ΔΙΕΡΓΑΣΙΩΝ ΔΙΑΧΩΡΙΣΜΟΥ ΜΑΔ, 2013 1 Ισορροπία Φάσεων Ανάλογα με τη φύση των συστατικών του μίγματος (ή της ολικής πίεσης του συστήματος) οι τάσεις διαφυγής υπολογίζονται - ανάλογα
ΑΝΑΛΥΣΗ ΚΑΙ ΣΧΕΔΙΑΣΜΟΣ ΔΙΕΡΓΑΣΙΩΝ ΔΙΑΧΩΡΙΣΜΟΥ ΜΑΔ, 2013 1 Ισορροπία Φάσεων Ανάλογα με τη φύση των συστατικών του μίγματος (ή της ολικής πίεσης του συστήματος) οι τάσεις διαφυγής υπολογίζονται - ανάλογα
5.3 Υπολογισμοί ισορροπίας φάσεων υγρού-υγρού
 5.3 Υπολογισμοί ισορροπίας φάσεων υγρού-υγρού Η αρχική εξίσωση που χρησιμοποιείται για τους υπολογισμούς της ΙΦΥΥ είναι η ικανοποίηση της βασικής θερμοδυναμικής απαίτησης της ισότητας των τάσεων διαφυγής
5.3 Υπολογισμοί ισορροπίας φάσεων υγρού-υγρού Η αρχική εξίσωση που χρησιμοποιείται για τους υπολογισμούς της ΙΦΥΥ είναι η ικανοποίηση της βασικής θερμοδυναμικής απαίτησης της ισότητας των τάσεων διαφυγής
Υπολογισμός & Πρόρρηση. Θερμοδυναμικών Ιδιοτήτων
 Υπολογισμός & Πρόρρηση Θερμοδυναμικών Ιδιοτήτων d du d Θερμοδυναμικές Ιδιότητες d dh d d d du d d dh U A H G d d da d d dg d du dq dq d / d du dq Θεμελιώδεις Συναρτήσεις περιέχουν όλες τις πληροφορίες
Υπολογισμός & Πρόρρηση Θερμοδυναμικών Ιδιοτήτων d du d Θερμοδυναμικές Ιδιότητες d dh d d d du d d dh U A H G d d da d d dg d du dq dq d / d du dq Θεμελιώδεις Συναρτήσεις περιέχουν όλες τις πληροφορίες
Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων
 Φυσικοχημεία II, Διαλύματα Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων o P = N P P = A A A N P o B B B PA + PB = P ολ Τ=const P = Ν ολ P + N P o o A A B B Ν Α + Ν =1 o o o P = P + A N ( ολ
Φυσικοχημεία II, Διαλύματα Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων o P = N P P = A A A N P o B B B PA + PB = P ολ Τ=const P = Ν ολ P + N P o o A A B B Ν Α + Ν =1 o o o P = P + A N ( ολ
Ισορροπία Υγρού-Υγρού ΠΡΟΧΩΡΗΜΕΝΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ
 Ισορροπία Υγρού-Υγρού ΠΡΟΧΩΡΗΜΕΝΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ Προχωρημένη Θερμοδυναμική Εαρινό εξάμηνο 08-09 Εισαγωγή Σε αντίθεση με τα αέρια τα οποία είναι αναμίξιμα σε όλες τις αναλογίες σε χαμηλές πιέσεις τα υγρά
Ισορροπία Υγρού-Υγρού ΠΡΟΧΩΡΗΜΕΝΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ Προχωρημένη Θερμοδυναμική Εαρινό εξάμηνο 08-09 Εισαγωγή Σε αντίθεση με τα αέρια τα οποία είναι αναμίξιμα σε όλες τις αναλογίες σε χαμηλές πιέσεις τα υγρά
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις. Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι
 Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ 9 ΣΤΡΟΒΙΛΟΚΙΝΗΤΗΡΩΝ
 ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΚΩΝ ΕΦΑΡΜΟΓΩΝ ΤΜΗΜΑ ΜΗΧΑΝΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΘΕΡΜΟΚΙΝΗΤΗΡΩΝ ΚΑΙ ΘΕΡΜΙΚΩΝ ΣΤΡΟΒΙΛΟΜΗΧΑΝΩΝ ΔΙΔΑΚΤΙΚΗ ΠΕΡΙΟΧΗ: ΕΡΓΑΣΤΗΡΙΟ ΣΤΡΟΒΙΛΟΚΙΝΗΤΗΡΩΝ Υπεύθυνος: Επικ. Καθηητής Δρ. Α. ΦΑΤΣΗΣ ΕΡΓΑΣΤΗΡΙΑΚΗ
ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΚΩΝ ΕΦΑΡΜΟΓΩΝ ΤΜΗΜΑ ΜΗΧΑΝΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΘΕΡΜΟΚΙΝΗΤΗΡΩΝ ΚΑΙ ΘΕΡΜΙΚΩΝ ΣΤΡΟΒΙΛΟΜΗΧΑΝΩΝ ΔΙΔΑΚΤΙΚΗ ΠΕΡΙΟΧΗ: ΕΡΓΑΣΤΗΡΙΟ ΣΤΡΟΒΙΛΟΚΙΝΗΤΗΡΩΝ Υπεύθυνος: Επικ. Καθηητής Δρ. Α. ΦΑΤΣΗΣ ΕΡΓΑΣΤΗΡΙΑΚΗ
Είδη ΙΦΥΥ δυαδικών μιγμάτων
 Είδη ΙΦΥΥ δυαδικών μιγμάτων T A X 1 X 1 ΙΦΥΥ τριαδικών μιγμάτων Τριγωνικά διαγράμματα C 0.1 0.2 0.3 0.4 0.5 P 0.9 0.8 0.7 0.6 0.5 0.4 0.3 0.2 0.1 0.6 0.7 0.8 0.9 κλάσμα βάρους του B κλάσμα βάρους του C
Είδη ΙΦΥΥ δυαδικών μιγμάτων T A X 1 X 1 ΙΦΥΥ τριαδικών μιγμάτων Τριγωνικά διαγράμματα C 0.1 0.2 0.3 0.4 0.5 P 0.9 0.8 0.7 0.6 0.5 0.4 0.3 0.2 0.1 0.6 0.7 0.8 0.9 κλάσμα βάρους του B κλάσμα βάρους του C
ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
 Ακαδημαϊκό έτος 34 ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ Επώνυμο: Όνομα: Προσωπικός Αριθμός: Ημερομηνία: Βαθμολογία θεμάτων 3 4 5 6 7 8 9 Γενικός Βαθμός η ΓΡΑΠΤΗ ΕΡΓΑΣΙΑ ΣΤΗ "ΦΥΣΙΚΟΧΗΜΕΙΑ" ΟΔΗΓΙΕΣ ΓΙΑ ΤΗΝ ΕΚΠΟΝΗΣΗ,
Ακαδημαϊκό έτος 34 ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ Επώνυμο: Όνομα: Προσωπικός Αριθμός: Ημερομηνία: Βαθμολογία θεμάτων 3 4 5 6 7 8 9 Γενικός Βαθμός η ΓΡΑΠΤΗ ΕΡΓΑΣΙΑ ΣΤΗ "ΦΥΣΙΚΟΧΗΜΕΙΑ" ΟΔΗΓΙΕΣ ΓΙΑ ΤΗΝ ΕΚΠΟΝΗΣΗ,
ΒΑΣΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ ΙΦ - ΣΧΕΔΙΑΣΜΟΣ ΑΠΟΣΤΑΚΤΙΚΩΝ ΣΤΗΛΩΝ ΜΑΔ, 2013
 ΒΑΣΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ ΙΦ - ΣΧΕΔΙΑΣΜΟΣ ΑΠΟΣΤΑΚΤΙΚΩΝ ΣΤΗΛΩΝ ΜΑΔ, 2013 1 Βασικοί Υπολογισμοί Ισορροπίας Φάσεων Ατμών Υγρού Οι βασικοί υπολογισμοί που ενδιαέρουν τον χημικό μηχανικό είναι οι ακόλουθοι : σημείο
ΒΑΣΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ ΙΦ - ΣΧΕΔΙΑΣΜΟΣ ΑΠΟΣΤΑΚΤΙΚΩΝ ΣΤΗΛΩΝ ΜΑΔ, 2013 1 Βασικοί Υπολογισμοί Ισορροπίας Φάσεων Ατμών Υγρού Οι βασικοί υπολογισμοί που ενδιαέρουν τον χημικό μηχανικό είναι οι ακόλουθοι : σημείο
διαιρούμε με το εμβαδό Α 2 του εμβόλου (1)
 1)Συνήθως οι πτήσεις των αεροσκαφών γίνονται στο ύψος των 15000 m, όπου η θερμοκρασία του αέρα είναι 210 Κ και η ατμοσφαιρική πίεση 10000 N / m 2. Σε αεροδρόμιο που βρίσκεται στο ίδιο ύψος με την επιφάνεια
1)Συνήθως οι πτήσεις των αεροσκαφών γίνονται στο ύψος των 15000 m, όπου η θερμοκρασία του αέρα είναι 210 Κ και η ατμοσφαιρική πίεση 10000 N / m 2. Σε αεροδρόμιο που βρίσκεται στο ίδιο ύψος με την επιφάνεια
Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου /3
 Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου 2014 1/3 Πρόβλημα 2. Καταστατική Εξίσωση Van der Waals (11 ) Σε ένα πολύ γνωστό μοντέλο του ιδανικού αερίου, του οποίου η καταστατική εξίσωση περιγράφεται από το νόμο
Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου 2014 1/3 Πρόβλημα 2. Καταστατική Εξίσωση Van der Waals (11 ) Σε ένα πολύ γνωστό μοντέλο του ιδανικού αερίου, του οποίου η καταστατική εξίσωση περιγράφεται από το νόμο
ΑΝΩΤΕΡΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΜΕΡΟΣ Β Η ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΤΩΝ ΑΠΛΩΝ ΥΛΙΚΩΝ
 ΑΝΩΤΕΡΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΜΕΡΟΣ Β Η ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΤΩΝ ΑΠΛΩΝ ΥΛΙΚΩΝ ΟΙ ΕΛΕΥΘΕΡΕΣ ΜΕΤΑΒΛΗΤΕΣ ΣΤΗΝ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΑΝΑΛΥΣΗ ΕΝ ΓΕΝΕΙ, ΟΛΕΣ ΟΙ ΠΑΡΑΜΕΤΡΟΙ ΕΝΟΣ ΑΠΛΟΥ, ΔΟΜΙΚΑ ΟΜΟΙΟΜΟΡΦΟΥ ΥΛΙΚΟΥ (ΔΗΛΑΔΗ ΟΤΑΝ ΟΛΗ
ΑΝΩΤΕΡΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΜΕΡΟΣ Β Η ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΤΩΝ ΑΠΛΩΝ ΥΛΙΚΩΝ ΟΙ ΕΛΕΥΘΕΡΕΣ ΜΕΤΑΒΛΗΤΕΣ ΣΤΗΝ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΑΝΑΛΥΣΗ ΕΝ ΓΕΝΕΙ, ΟΛΕΣ ΟΙ ΠΑΡΑΜΕΤΡΟΙ ΕΝΟΣ ΑΠΛΟΥ, ΔΟΜΙΚΑ ΟΜΟΙΟΜΟΡΦΟΥ ΥΛΙΚΟΥ (ΔΗΛΑΔΗ ΟΤΑΝ ΟΛΗ
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens. ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ ΥΓΡΟΥ Liquid Liquid Extraction
 Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ ΥΓΡΟΥ Liquid Liquid Extraction ΕΚΧΥΛΙΣΗ ΙΣΟΡΡΟΠΙΑΣ ΓΙΑ ΜΕΡΙΚΩΣ ΑΝΑΜΙΞΙΜΑ ΣΥΣΤΗΜΑΤΑ Περιοχές
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ ΥΓΡΟΥ Liquid Liquid Extraction ΕΚΧΥΛΙΣΗ ΙΣΟΡΡΟΠΙΑΣ ΓΙΑ ΜΕΡΙΚΩΣ ΑΝΑΜΙΞΙΜΑ ΣΥΣΤΗΜΑΤΑ Περιοχές
ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ Equilibrium or Flash Distillation
 Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ Equilibrium or Flash Distillation ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ 1. ΟΡΙΣΜΟΣ ΣΚΟΠΟΣ ΔΙΕΡΓΑΣΙΑΣ
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ Equilibrium or Flash Distillation ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ 1. ΟΡΙΣΜΟΣ ΣΚΟΠΟΣ ΔΙΕΡΓΑΣΙΑΣ
ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ N o 5 ΜΕΤΡΗΣΗ ΤΗΣ ΕΠΙΦΑΝΕΙΑΚΗΣ ΤΑΣΗΣ ΥΓΡΩΝ
 ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ N o 5 ΜΕΤΡΗΣΗ ΤΗΣ ΕΠΙΦΑΝΕΙΑΚΗΣ ΤΑΣΗΣ ΥΓΡΩΝ ΣΚΟΠΟΣ Στην άσκηση αυτή θα μετρηθεί ο συντελεστής επιφανειακής τάσης υρών και συκεκριμένα του νερού, της αιθανόλης καθώς και διαφόρων διαλυμάτων
ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ N o 5 ΜΕΤΡΗΣΗ ΤΗΣ ΕΠΙΦΑΝΕΙΑΚΗΣ ΤΑΣΗΣ ΥΓΡΩΝ ΣΚΟΠΟΣ Στην άσκηση αυτή θα μετρηθεί ο συντελεστής επιφανειακής τάσης υρών και συκεκριμένα του νερού, της αιθανόλης καθώς και διαφόρων διαλυμάτων
1 IΔΑΝΙΚΑ ΑΕΡΙΑ 1.1 ΓΕΝΙΚΑ
 1 1 IΔΑΝΙΚΑ ΑΕΡΙΑ 1.1 ΓΕΝΙΚΑ Θα αρχίσουμε τη σειρά των μαθημάτων της Φυσικοχημείας με τη μελέτη της αέριας κατάστασης της ύλης. Η μελέτη της φύσης των αερίων αποτελεί ένα ιδανικό μέσο για την εισαγωγή
1 1 IΔΑΝΙΚΑ ΑΕΡΙΑ 1.1 ΓΕΝΙΚΑ Θα αρχίσουμε τη σειρά των μαθημάτων της Φυσικοχημείας με τη μελέτη της αέριας κατάστασης της ύλης. Η μελέτη της φύσης των αερίων αποτελεί ένα ιδανικό μέσο για την εισαγωγή
Σκοπός του Μαθήµατος
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓΑΣΤΗΡΙΟ ΘΕΡΜΟ ΥΝΑΜΙΚΗΣ & ΦΑΙΝΟΜΕΝΩΝ ΜΕΤΑΦΟΡΑΣ Ισορροπία Φάσεων: Από πού Ξεκινήσαµε, που Φθάσαµε, Εφαρµογές ηµήτρης Τασιός, Οµότιµος Καθηγητής, ΕΜΠ
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓΑΣΤΗΡΙΟ ΘΕΡΜΟ ΥΝΑΜΙΚΗΣ & ΦΑΙΝΟΜΕΝΩΝ ΜΕΤΑΦΟΡΑΣ Ισορροπία Φάσεων: Από πού Ξεκινήσαµε, που Φθάσαµε, Εφαρµογές ηµήτρης Τασιός, Οµότιµος Καθηγητής, ΕΜΠ
Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη
 Διαλύματα 1 Διαδικασία διάλυσης Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται
Διαλύματα 1 Διαδικασία διάλυσης Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται
ΤΥΠΟΛΟΓΙΟ-ΒΑΣΙΚΟΙ ΟΡΙΣΜΟΙ ΚΕΦΑΛΑΙΟΥ 2 ΕΡΓΟ ΑΕΡΙΟΥ
 ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΤΥΠΟΛΟΓΙΟ-ΒΑΣΙΚΟΙ ΟΡΙΣΜΟΙ ΚΕΦΑΛΑΙΟΥ ΕΡΓΟ ΑΕΡΙΟΥ Κατά την εκτόνωση ενός αερίου, το έρο του είναι θετικό ( δηλαδή παραόμενο). Κατά την συμπίεση ενός
ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΤΥΠΟΛΟΓΙΟ-ΒΑΣΙΚΟΙ ΟΡΙΣΜΟΙ ΚΕΦΑΛΑΙΟΥ ΕΡΓΟ ΑΕΡΙΟΥ Κατά την εκτόνωση ενός αερίου, το έρο του είναι θετικό ( δηλαδή παραόμενο). Κατά την συμπίεση ενός
ΠΟΛΥΦΑΣΙΚΑ ΣΥΣΤΗΜΑΤΑ
 . ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΟΛΥΦΑΣΙΚΑ ΣΥΣΤΗΜΑΤΑ ΣΩΤΗΡΗΣ ΤΣΙΒΙΛΗΣ, Καθ. ΕΜΠ 135 ΔΙΑΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ 1 2 3 4 1 στερεό (solid) 2 υγρό (liquid) 3 ατμός (vapor) 4 αέριο (gas) A 1+2+3
. ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΟΛΥΦΑΣΙΚΑ ΣΥΣΤΗΜΑΤΑ ΣΩΤΗΡΗΣ ΤΣΙΒΙΛΗΣ, Καθ. ΕΜΠ 135 ΔΙΑΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ 1 2 3 4 1 στερεό (solid) 2 υγρό (liquid) 3 ατμός (vapor) 4 αέριο (gas) A 1+2+3
Ι Α Γ Ω Ν Ι Σ Μ Α ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ & ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ. Θέµα 1 ο. α. Το σύστηµα των ηλεκτρικών φορτίων έχει δυναµική ενέργεια
 Ι Α Γ Ω Ν Ι Σ Μ Α ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΘΕΙΚΗΣ & ΕΧΝΟΛΟΓΙΚΗΣ ΚΑΕΥΘΥΝΣΗΣ Θέµα ο Στις παρακάτω ερωτήσεις να ράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το ράµµα που αντιστοιχεί στη σωστή απάντηση..
Ι Α Γ Ω Ν Ι Σ Μ Α ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΘΕΙΚΗΣ & ΕΧΝΟΛΟΓΙΚΗΣ ΚΑΕΥΘΥΝΣΗΣ Θέµα ο Στις παρακάτω ερωτήσεις να ράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το ράµµα που αντιστοιχεί στη σωστή απάντηση..
ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι. Ενότητα 8: Θερμοχωρητικότητα Χημικό δυναμικό και ισορροπία. Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών
 ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι Ενότητα 8: Θερμοχωρητικότητα Χημικό δυναμικό και ισορροπία Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοποί ενότητας Σκοπός της ενότητας αυτής είναι η ανάπτυξη μαθηματικών
ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι Ενότητα 8: Θερμοχωρητικότητα Χημικό δυναμικό και ισορροπία Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοποί ενότητας Σκοπός της ενότητας αυτής είναι η ανάπτυξη μαθηματικών
Enrico Fermi, Thermodynamics, 1937
 I. Θερµοδυναµικά συστήµατα Enrico Feri, herodynaics, 97. Ένα σώµα διαστέλλεται από αρχικό όγκο. L σε τελικό όγκο 4. L υπό πίεση.4 at. Να υπολογισθεί το έργο που παράγεται. W - -.4 at 5 a at - (4..) - -
I. Θερµοδυναµικά συστήµατα Enrico Feri, herodynaics, 97. Ένα σώµα διαστέλλεται από αρχικό όγκο. L σε τελικό όγκο 4. L υπό πίεση.4 at. Να υπολογισθεί το έργο που παράγεται. W - -.4 at 5 a at - (4..) - -
Τμήμα Χημείας Μάθημα: Φυσικοχημεία Ι Εξέταση: Περίοδος Ιουνίου (21/6/2017)
 Τμήμα Χημείας Μάθημα: Φυσικοχημεία Ι Εξέταση: Περίοδος Ιουνίου -7 (//7). Δίνεται η θεμελιώδης εξίσωση για την εσωτερική ενέργεια ενός συστήματος ενός συστατικού όπου κατάλληλη σταθερά. Να προσδιορίσετε
Τμήμα Χημείας Μάθημα: Φυσικοχημεία Ι Εξέταση: Περίοδος Ιουνίου -7 (//7). Δίνεται η θεμελιώδης εξίσωση για την εσωτερική ενέργεια ενός συστήματος ενός συστατικού όπου κατάλληλη σταθερά. Να προσδιορίσετε
ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ
 ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ Έννοιες που πρέπει να γνωρίζετε Ισορροπία φάσεων, εξίσωση Clauiu-Clapeyron Θέμα ασκήσεως Προσρόφηση ουσίας από αραιά διαλύματα. Προσδιορισμός ισόθερμων
ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ Έννοιες που πρέπει να γνωρίζετε Ισορροπία φάσεων, εξίσωση Clauiu-Clapeyron Θέμα ασκήσεως Προσρόφηση ουσίας από αραιά διαλύματα. Προσδιορισμός ισόθερμων
& τεχνολογική. Συνοπτική θεωρία των παραγράφων 2.1 μέχρι 2.13
 èåôéêþ êáôåýèõíóç & τεχνολοική ΔΕΥΤΕΡΟ ΚΕΦΑΛΑΙΟ Συνοπτική θεωρία των παραράφων. μέχρι.3 Θερμοδυναμικό σύστημα λέεται το σύστημα ια την περιραφή του οποίου χρησιμοποιούνται εκτός από νωστά μεέθη της μηχανικής
èåôéêþ êáôåýèõíóç & τεχνολοική ΔΕΥΤΕΡΟ ΚΕΦΑΛΑΙΟ Συνοπτική θεωρία των παραράφων. μέχρι.3 Θερμοδυναμικό σύστημα λέεται το σύστημα ια την περιραφή του οποίου χρησιμοποιούνται εκτός από νωστά μεέθη της μηχανικής
Παράγοντες που εξηγούν τη διαλυτότητα. Είδη διαλυμάτων
 Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΛΥΜΕΝΑ ΘΕΜΑΤΑ
 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΛΥΜΕΝΑ ΘΕΜΑΤΑ 1 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 Θέμα 1 Επιλέγοντας το κατάλληλο διάγραμμα φάσεων για ένα πραγματικό
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΛΥΜΕΝΑ ΘΕΜΑΤΑ 1 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 Θέμα 1 Επιλέγοντας το κατάλληλο διάγραμμα φάσεων για ένα πραγματικό
1 ΦΥΣΙΚΟ ΦΥΣΙΚ ΧΗΜΕΙΑ Ο ΣΥΣΤΗΜΑΤΩΝ
 1 ΦΥΣΙΚΟΧΗΜΕΙΑ ΣΥΣΤΗΜΑΤΩΝ Φυσικοχημεία συστημάτων 2 «Όμοιος Ό αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη είναι δύο ουσίες τόσο μεγαλύτερη είναι η αμοιβαία διαλυτότητά τους. Οι ανόργανες ενώσεις διαλύονται
1 ΦΥΣΙΚΟΧΗΜΕΙΑ ΣΥΣΤΗΜΑΤΩΝ Φυσικοχημεία συστημάτων 2 «Όμοιος Ό αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη είναι δύο ουσίες τόσο μεγαλύτερη είναι η αμοιβαία διαλυτότητά τους. Οι ανόργανες ενώσεις διαλύονται
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα. Θερμοδυναμική
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Θερμοδυναμική Ενότητα 3 : Ιδανικά Αέρια Δρ Γεώργιος Αλέξης Τμήμα Μηχανολόγων Μηχανικών Τ.Ε. Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Θερμοδυναμική Ενότητα 3 : Ιδανικά Αέρια Δρ Γεώργιος Αλέξης Τμήμα Μηχανολόγων Μηχανικών Τ.Ε. Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΝΤΙΚΕΙΜΕΝΟ ΘΕΜΑ 1 Ο
 ΑΝΤΙΚΕΙΜΕΝΟ 1 ο κεφάλαιο: «Κινητική Θεωρία των Αερίων» ο κεφάλαιο: «O 1 ος θερµοδυναµικός νόµος» ΘΕΜΑ 1 Ο 1Α Ερωτήσεις πολλαπλής επιλογής. Σηµειώστε τη σωστή από τις προτάσεις που ακολουθούν. 1) Κατά την
ΑΝΤΙΚΕΙΜΕΝΟ 1 ο κεφάλαιο: «Κινητική Θεωρία των Αερίων» ο κεφάλαιο: «O 1 ος θερµοδυναµικός νόµος» ΘΕΜΑ 1 Ο 1Α Ερωτήσεις πολλαπλής επιλογής. Σηµειώστε τη σωστή από τις προτάσεις που ακολουθούν. 1) Κατά την
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Ιωάννης Πούλιος ΔΥΑΔΙΚΑ ΣΥΣΤΗΜΑΤΑ ΜΕΛΕΤΗ ΤΩΝ ΔΙΑΓΡΑΜΜΑΤΩΝ ΤΟΥ ΣΗΜΕΙΟΥ ΖΕΣΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Ιωάννης Πούλιος ΔΥΑΔΙΚΑ ΣΥΣΤΗΜΑΤΑ ΜΕΛΕΤΗ ΤΩΝ ΔΙΑΓΡΑΜΜΑΤΩΝ ΤΟΥ ΣΗΜΕΙΟΥ ΖΕΣΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ
Ισορροπία (γενικά) Ισορροπίες σε διαλύματα. Εισαγωγική Χημεία
 Ισορροπία (γενικά) Ισορροπίες σε διαλύματα Εισαγωγική Χημεία 2013-14 1 Χημική Ισορροπία Εισαγωγική Χημεία 2013-14 2 Ισορροπία: Βαθμός συμπλήρωσης αντίδρασης Ν 2 (g) + 3H 2(g) 2NH 3 (g) Όταν αναφερόμαστε
Ισορροπία (γενικά) Ισορροπίες σε διαλύματα Εισαγωγική Χημεία 2013-14 1 Χημική Ισορροπία Εισαγωγική Χημεία 2013-14 2 Ισορροπία: Βαθμός συμπλήρωσης αντίδρασης Ν 2 (g) + 3H 2(g) 2NH 3 (g) Όταν αναφερόμαστε
ΚΛΑΣΙΚΗ ΘΕΡΜΟ ΥΝΑΜΙΚΗ ΜΑΘΗΜΑ-V ΑΣΚΗΣΗ Α2 - JOULE-THOMSON
 ΚΛΑΣΙΚΗ ΘΕΡΜΟ ΥΝΑΜΙΚΗ ΜΑΘΗΜΑ-V ΑΣΚΗΣΗ Α2 - JOULE-THOMSON Τµήµα Χηµείας, Πανεπιστήµιο Κρήτης, και Ινστιτούτο Ηλεκτρονικής οµής και Λέιζερ, Ιδρυµα Τεχνολογίας και Ερευνας, Ηράκλειο, Κρήτη http://tccc.iesl.forth.gr/education/local.html
ΚΛΑΣΙΚΗ ΘΕΡΜΟ ΥΝΑΜΙΚΗ ΜΑΘΗΜΑ-V ΑΣΚΗΣΗ Α2 - JOULE-THOMSON Τµήµα Χηµείας, Πανεπιστήµιο Κρήτης, και Ινστιτούτο Ηλεκτρονικής οµής και Λέιζερ, Ιδρυµα Τεχνολογίας και Ερευνας, Ηράκλειο, Κρήτη http://tccc.iesl.forth.gr/education/local.html
ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΙΙ. Μ. Κροκίδα
 ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΙΙ Μ. Κροκίδα ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓ. ΣΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Βασικές αρχές Η διεργασία της απόσταξης στηρίζεται
ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΙΙ Μ. Κροκίδα ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓ. ΣΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Βασικές αρχές Η διεργασία της απόσταξης στηρίζεται
ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΣΤΗ ΣΤΑΤΙΣΤΙΚΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΦΥΣΙΚΟΧΗΜΕΙΑ ΦΥΕ22
 Λυμένες ασκήσεις Στατιστική Θερμοδυναμική Οκτώβριος ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΣΤΗ ΣΤΑΤΙΣΤΙΚΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΦΥΣΙΚΟΧΗΜΕΙΑ ΦΥΕ Άσκηση.: Το άθροισμα καταστάσεων της δονητικής κίνησης των μορίων του Ι αποτελείται από
Λυμένες ασκήσεις Στατιστική Θερμοδυναμική Οκτώβριος ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΣΤΗ ΣΤΑΤΙΣΤΙΚΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΦΥΣΙΚΟΧΗΜΕΙΑ ΦΥΕ Άσκηση.: Το άθροισμα καταστάσεων της δονητικής κίνησης των μορίων του Ι αποτελείται από
Για αραιά διαλύματα : x 1 0 : μ i = μ i 0 RTlnx i χ. όπου μ i φ =μ i 0 χ
 Για ιδανικά διαλύματα : μ i = μ i lnx i x= γ=1 Για αραιά διαλύματα : x 1 : μ i = μ i lnx i χ μ i = μ i φ lnx i όπου μ i φ =μ i χ Χημική Ισορροπία λ Από σελ. 7 Χημική Ισορροπία όταν ν i μ i = (T,P σταθερό)
Για ιδανικά διαλύματα : μ i = μ i lnx i x= γ=1 Για αραιά διαλύματα : x 1 : μ i = μ i lnx i χ μ i = μ i φ lnx i όπου μ i φ =μ i χ Χημική Ισορροπία λ Από σελ. 7 Χημική Ισορροπία όταν ν i μ i = (T,P σταθερό)
Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ
 Φυσικοχημεία II, Διαλύματα Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 pulis@chem.auth.gr phtcatalysisgrup.web.auth.gr Διαλύματα και Συστήματα υγρών Διαμόρφωση μαθήματος Θεωρία/Ασκήσεις
Φυσικοχημεία II, Διαλύματα Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 pulis@chem.auth.gr phtcatalysisgrup.web.auth.gr Διαλύματα και Συστήματα υγρών Διαμόρφωση μαθήματος Θεωρία/Ασκήσεις
Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη
 Διαλύματα 1 Διαδικασία διάλυσης Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται
Διαλύματα 1 Διαδικασία διάλυσης Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ. Τράπεζα θεμάτων. Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ
 ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ 16111 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ 16111 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση
Τ, Κ Η 2 Ο(g) CΟ(g) CO 2 (g) Λύση Για τη συγκεκριμένη αντίδραση στους 1300 Κ έχουμε:
 ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ - ΑΣΚΗΣΕΙΣ 5-6 (Α. Χημική Θερμοδυναμική) η Άσκηση Η αντίδραση CO(g) + H O(g) CO (g) + H (g) γίνεται σε θερμοκρασία 3 Κ. Να υπολογιστεί το κλάσμα των ατμών του
ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ - ΑΣΚΗΣΕΙΣ 5-6 (Α. Χημική Θερμοδυναμική) η Άσκηση Η αντίδραση CO(g) + H O(g) CO (g) + H (g) γίνεται σε θερμοκρασία 3 Κ. Να υπολογιστεί το κλάσμα των ατμών του
[6] Να επαληθευθεί η εξίσωση του Euler για (i) ιδανικό αέριο, (ii) πραγματικό αέριο
![[6] Να επαληθευθεί η εξίσωση του Euler για (i) ιδανικό αέριο, (ii) πραγματικό αέριο [6] Να επαληθευθεί η εξίσωση του Euler για (i) ιδανικό αέριο, (ii) πραγματικό αέριο](/thumbs/53/32819377.jpg) [1] Να βρεθεί ο αριθμός των ατόμων του αέρα σε ένα κυβικό μικρόμετρο (κανονικές συνθήκες και ιδανική συμπεριφορά) (Τ=300 Κ και P= 1 atm) (1atm=1.01x10 5 Ν/m =1.01x10 5 Pa). [] Να υπολογισθεί η απόσταση
[1] Να βρεθεί ο αριθμός των ατόμων του αέρα σε ένα κυβικό μικρόμετρο (κανονικές συνθήκες και ιδανική συμπεριφορά) (Τ=300 Κ και P= 1 atm) (1atm=1.01x10 5 Ν/m =1.01x10 5 Pa). [] Να υπολογισθεί η απόσταση
ΑΝΩΤΕΡΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΣΧΕΣΕΙΣ
 ΑΝΩΤΕΡΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΣΧΕΣΕΙΣ Η ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΣΤΟ ΠΡΟΗΓΟΥΜΕΝΟ ΜΑΘΗΜΑ ΑΝΑΦΕΡΘΗΚΑΜΕ ΣΤΙΣ ΚΑΤΑΣΤΑΤΙΚΕΣ ΕΞΙΣΩΣΕΙΣ ΤΗΣ ΜΟΡΦΗΣ f(p,v,t)=0 ΠΟΥ ΧΡΗΣΙΜΟΠΟΙΟΥΝΤΑΙ ΓΙΑ ΝΑ ΣΥΝΔΕΟΥΝ ΤΗΝ ΠΙΕΣΗ,
ΑΝΩΤΕΡΗ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΣΧΕΣΕΙΣ Η ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΣΤΟ ΠΡΟΗΓΟΥΜΕΝΟ ΜΑΘΗΜΑ ΑΝΑΦΕΡΘΗΚΑΜΕ ΣΤΙΣ ΚΑΤΑΣΤΑΤΙΚΕΣ ΕΞΙΣΩΣΕΙΣ ΤΗΣ ΜΟΡΦΗΣ f(p,v,t)=0 ΠΟΥ ΧΡΗΣΙΜΟΠΟΙΟΥΝΤΑΙ ΓΙΑ ΝΑ ΣΥΝΔΕΟΥΝ ΤΗΝ ΠΙΕΣΗ,
M V n. nm V. M v. M v T P P S V P = = + = σταθερή σε παραγώγιση, τον ορισµό του συντελεστή διαστολής α = 1, κυκλική εναλλαγή 3
 Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξέταση: Περίοδος εκεµβρίου 04- (//04. ίνονται οι ακόλουθες πληροφορίες για τον διθειάνθρακα (CS. Γραµµοµοριακή µάζα 76.4 g/mol, κανονικό σηµείο ζέσεως 46 C, κανονικό
Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξέταση: Περίοδος εκεµβρίου 04- (//04. ίνονται οι ακόλουθες πληροφορίες για τον διθειάνθρακα (CS. Γραµµοµοριακή µάζα 76.4 g/mol, κανονικό σηµείο ζέσεως 46 C, κανονικό
Επανάληψη των Κεφαλαίων 1 και 2 Φυσικής Γ Έσπερινού Κατεύθυνσης
 Επανάληψη των Κεφαλαίων 1 και Φυσικής Γ Έσπερινού Κατεύθυνσης Φυσικά µεγέθη, µονάδες µετρήσεως (S.I) και µετατροπές P: Η πίεση ενός αερίου σε N/m (1atm=1,013 10 5 N/m ). : Ο όγκος τουαερίου σε m 3 (1m
Επανάληψη των Κεφαλαίων 1 και Φυσικής Γ Έσπερινού Κατεύθυνσης Φυσικά µεγέθη, µονάδες µετρήσεως (S.I) και µετατροπές P: Η πίεση ενός αερίου σε N/m (1atm=1,013 10 5 N/m ). : Ο όγκος τουαερίου σε m 3 (1m
Σφαιρικές συντεταγμένες (r, θ, φ).
 T T r e r 1 T e r Σφαιρικές συντεταγμένες (r, θ, φ). 1 T e. (2.57) r sin u u e u e u e, (2.58) r r οπότε το εσωτερικό γινόμενο u.t γίνεται: T u T u T u. T ur. (2.59) r r r sin 2.5 Η ΑΡΧΗ ΔΙΑΤΗΡΗΣΗΣ ΤΗΣ
T T r e r 1 T e r Σφαιρικές συντεταγμένες (r, θ, φ). 1 T e. (2.57) r sin u u e u e u e, (2.58) r r οπότε το εσωτερικό γινόμενο u.t γίνεται: T u T u T u. T ur. (2.59) r r r sin 2.5 Η ΑΡΧΗ ΔΙΑΤΗΡΗΣΗΣ ΤΗΣ
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C.
 4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens. ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ- ΥΓΡΟΥ Liquid- Liquid Extraction
 Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ- ΥΓΡΟΥ Liquid- Liquid Extraction ΕΚΧΥΛΙΣΗ ΙΣΟΡΡΟΠΙΑΣ ΓΙΑ ΜΕΡΙΚΩΣ ΑΝΑΜΙΞΙΜΑ ΣΥΣΤΗΜΑΤΑ Τριγωνικές
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ- ΥΓΡΟΥ Liquid- Liquid Extraction ΕΚΧΥΛΙΣΗ ΙΣΟΡΡΟΠΙΑΣ ΓΙΑ ΜΕΡΙΚΩΣ ΑΝΑΜΙΞΙΜΑ ΣΥΣΤΗΜΑΤΑ Τριγωνικές
Θερμοδυναμική. Ενότητα 3: Ασκήσεις στη Θερμοδυναμική. Κυρατζής Νικόλαος Τμήμα Μηχανικών Περιβάλλοντος και Μηχανικών Αντιρρύπανσης ΤΕ
 Θερμοδυναμική Ενότητα 3: Ασκήσεις στη Θερμοδυναμική Κυρατζής Νικόλαος Τμήμα Μηχανικών Περιβάλλοντος και Μηχανικών Αντιρρύπανσης ΤΕ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Θερμοδυναμική Ενότητα 3: Ασκήσεις στη Θερμοδυναμική Κυρατζής Νικόλαος Τμήμα Μηχανικών Περιβάλλοντος και Μηχανικών Αντιρρύπανσης ΤΕ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Ζήτημα 1 0. Επώνυμο... Όνομα... Αγρίνιο 1/3/2015. Επιλέξτε τη σωστή απάντηση
 1 Επώνυμο... Όνομα... Αγρίνιο 1/3/2015 Ζήτημα 1 0 Επιλέξτε τη σωστή απάντηση 1) Η θερμότητα που ανταλλάσει ένα αέριο με το περιβάλλον θεωρείται θετική : α) όταν προσφέρεται από το αέριο στο περιβάλλον,
1 Επώνυμο... Όνομα... Αγρίνιο 1/3/2015 Ζήτημα 1 0 Επιλέξτε τη σωστή απάντηση 1) Η θερμότητα που ανταλλάσει ένα αέριο με το περιβάλλον θεωρείται θετική : α) όταν προσφέρεται από το αέριο στο περιβάλλον,
Σύνοψη ΜΗΧΑΝΙΚΗΣ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Χημική αντίδραση : a 1. + α 2 Α (-a 1 ) A 1. +(-a 2
 ΠΑ- Σύνοψη ΜΗΧΑΝΙΚΗΣ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Χημική αντίδραση : a A + α Α +... ------------>...+a A ή σε μορφή γραμμικής εξίσωσης a A +...+(-a ) A +(-a ) A +... 0 a Στοιχειομετρικοί συντελεστές ως προς Α (
ΠΑ- Σύνοψη ΜΗΧΑΝΙΚΗΣ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Χημική αντίδραση : a A + α Α +... ------------>...+a A ή σε μορφή γραμμικής εξίσωσης a A +...+(-a ) A +(-a ) A +... 0 a Στοιχειομετρικοί συντελεστές ως προς Α (
Ανάλυση Τροφίμων. Ενότητα 6: Διαλύματα & οι ιδιότητές τους Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ. Τμήμα Τεχνολογίας Τροφίμων. Ακαδημαϊκό Έτος
 Ανάλυση Τροφίμων Ενότητα 6: Διαλύματα & οι ιδιότητές τους Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Διαλύματα Τα ομοιογενή μίγματα
Ανάλυση Τροφίμων Ενότητα 6: Διαλύματα & οι ιδιότητές τους Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Διαλύματα Τα ομοιογενή μίγματα
Θερμοδυναμική Ενότητα 4:
 Θερμοδυναμική Ενότητα 4: Ισοζύγια Ενέργειας και Μάζας σε ανοικτά συστήματα Κυρατζής Νικόλαος Τμήμα Μηχανικών Περιβάλλοντος και Μηχανικών Αντιρρύπανσης ΤΕ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται
Θερμοδυναμική Ενότητα 4: Ισοζύγια Ενέργειας και Μάζας σε ανοικτά συστήματα Κυρατζής Νικόλαος Τμήμα Μηχανικών Περιβάλλοντος και Μηχανικών Αντιρρύπανσης ΤΕ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται
ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΘΕΩΡΙΑ
 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΘΕΩΡΙΑ Περιεχόμενα 1. Όρια καταστατικής εξίσωσης ιδανικού αερίου 2. Αποκλίσεις των Ιδιοτήτων των πραγματικών αερίων από τους Νόμους
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΘΕΩΡΙΑ Περιεχόμενα 1. Όρια καταστατικής εξίσωσης ιδανικού αερίου 2. Αποκλίσεις των Ιδιοτήτων των πραγματικών αερίων από τους Νόμους
ΕΞΙΣΩΣΗ CLAUSIUS-CLAPEYRON ΘΕΩΡΙΑ
 ΕΞΙΣΩΣΗ CLAUSIUS-CLAEYRON ΘΕΩΡΙΑ Περιεχόμενα 1. 3D Διάγραμμα Φάσης 2. Λανθάνουσα θερμότητα 3. Εξίσωση Clausius Clapeyron 4. Συμπιεστότητα 5. Θερμική διαστολή 6. Θερμοχωρητικότητα 1 στερεό στερεό+υγρό υγρό
ΕΞΙΣΩΣΗ CLAUSIUS-CLAEYRON ΘΕΩΡΙΑ Περιεχόμενα 1. 3D Διάγραμμα Φάσης 2. Λανθάνουσα θερμότητα 3. Εξίσωση Clausius Clapeyron 4. Συμπιεστότητα 5. Θερμική διαστολή 6. Θερμοχωρητικότητα 1 στερεό στερεό+υγρό υγρό
ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι. Ενότητα 9: Θερμοδυναμική αερίων. Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών
 ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι Ενότητα 9: Θερμοδυναμική αερίων Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοποί ενότητας Σκοπός της ενότητας αυτής είναι ο ορισμός του ιδανικού αερίου με βάση το χημικό
ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι Ενότητα 9: Θερμοδυναμική αερίων Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοποί ενότητας Σκοπός της ενότητας αυτής είναι ο ορισμός του ιδανικού αερίου με βάση το χημικό
Σε ένα διάλυμα η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη
 Διαλύματα 1 Διαδικασία διάλυσης Σε ένα διάλυμα η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται από
Διαλύματα 1 Διαδικασία διάλυσης Σε ένα διάλυμα η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται από
Μεταβολή Q, W, ΔU Παρατηρήσεις (3) ) Q = nrt ln V 1. W = Q = nrt ln U = 0 (5). Q = nc V T (8) W = 0 (9) U = nc V T (10)
 Θερμοδυναμική 1 1 Θερμοδυναμική 11 Τυπολόγιο Θερμοδυναμικής Πίνακας 1: Οι Μεταβολές Συνοπτικά Μεταβολή Q, W, ΔU Παρατηρήσεις Ισόθερμη Μεταβολή Νόμος oyle = σταθερό (1) 1 1 = 2 2 (2) Q = nrt ln ( 2 W =
Θερμοδυναμική 1 1 Θερμοδυναμική 11 Τυπολόγιο Θερμοδυναμικής Πίνακας 1: Οι Μεταβολές Συνοπτικά Μεταβολή Q, W, ΔU Παρατηρήσεις Ισόθερμη Μεταβολή Νόμος oyle = σταθερό (1) 1 1 = 2 2 (2) Q = nrt ln ( 2 W =
IΣΟΡΡΟΠΙΑ ΣΥΣΤΗΜΑΤΩΝ ΠΟΛΛΩΝ ΣΥΣΤΑΤΙΚΩΝ ΜΗ ΗΛΕΚΤΡΟΛΥΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΥΓΡΩΝ
 Ιωάννης Πούλιος Εργαστήριο Φυσικής Χημείας, Τμήμα Χημείας, ΑΠΘ IΣΟΡΡΟΠΙΑ ΣΥΣΤΗΜΑΤΩΝ ΠΟΛΛΩΝ ΣΥΣΤΑΤΙΚΩΝ ΜΗ ΗΛΕΚΤΡΟΛΥΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΥΓΡΩΝ ΘΕΣΣΑΛΟΝΙΚΗ 2018 ς Πούλιος Εργαστήριο Φυσικής Χημείας, Τμήμα Χημείας,
Ιωάννης Πούλιος Εργαστήριο Φυσικής Χημείας, Τμήμα Χημείας, ΑΠΘ IΣΟΡΡΟΠΙΑ ΣΥΣΤΗΜΑΤΩΝ ΠΟΛΛΩΝ ΣΥΣΤΑΤΙΚΩΝ ΜΗ ΗΛΕΚΤΡΟΛΥΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΥΓΡΩΝ ΘΕΣΣΑΛΟΝΙΚΗ 2018 ς Πούλιος Εργαστήριο Φυσικής Χημείας, Τμήμα Χημείας,
Ενεργότητα και συντελεστές ενεργότητας- Οξέα- Οι σταθερές ισορροπίας. Εισαγωγική Χημεία
 Ενεργότητα και συντελεστές ενεργότητας- Οξέα- Οι σταθερές ισορροπίας 1 Εισαγωγική Χημεία 2013-14 Από τον ορισμό της Ιοντικής Ισχύος (Ι) τα χημικά είδη ψηλού φορτίου συνεισφέρουν περισσότερο στην ιοντική
Ενεργότητα και συντελεστές ενεργότητας- Οξέα- Οι σταθερές ισορροπίας 1 Εισαγωγική Χημεία 2013-14 Από τον ορισμό της Ιοντικής Ισχύος (Ι) τα χημικά είδη ψηλού φορτίου συνεισφέρουν περισσότερο στην ιοντική
ΚΛΑΣΙΚΗ (ΧΗΜΙΚΗ) ΘΕΡΜΟ ΥΝΑΜΙΚΗ ΕΙΣΑΓΩΓΗ
 ΚΛΑΣΙΚΗ (ΧΗΜΙΚΗ) ΘΕΡΜΟ ΥΝΑΜΙΚΗ ΕΙΣΑΓΩΓΗ Σταύρος Κ. Φαράντος Τµήµα Χηµείας, Πανεπιστήµιο Κρήτης, και Ινστιτούτο Ηλεκτρονικής οµής και Λέιζερ, Ιδρυµα Τεχνολογίας και Ερευνας, Ηράκλειο, Κρήτη http://tccc.iesl.forth.gr/education/local.html
ΚΛΑΣΙΚΗ (ΧΗΜΙΚΗ) ΘΕΡΜΟ ΥΝΑΜΙΚΗ ΕΙΣΑΓΩΓΗ Σταύρος Κ. Φαράντος Τµήµα Χηµείας, Πανεπιστήµιο Κρήτης, και Ινστιτούτο Ηλεκτρονικής οµής και Λέιζερ, Ιδρυµα Τεχνολογίας και Ερευνας, Ηράκλειο, Κρήτη http://tccc.iesl.forth.gr/education/local.html
ΚΕΦΑΛΑΙΟ 3 Ο ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ
 Σχολικό Έτος 016-017 67 ΚΕΦΑΛΑΙΟ Ο ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ Α. ΕΙΣΑΓΩΓΗ ΣΤΑ ΑΕΡΙΑ 1. Σχετικές Ατομικές και Μοριακές Μάζες Σχετική Ατομική Μάζα (Α r) του ατόμου ενός στοιχείου, ονομάζεται ο αριθμός
Σχολικό Έτος 016-017 67 ΚΕΦΑΛΑΙΟ Ο ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ Α. ΕΙΣΑΓΩΓΗ ΣΤΑ ΑΕΡΙΑ 1. Σχετικές Ατομικές και Μοριακές Μάζες Σχετική Ατομική Μάζα (Α r) του ατόμου ενός στοιχείου, ονομάζεται ο αριθμός
Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ
 Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ Η υγρή εκχύλιση βρίσκει εφαρμογή όταν. Η σχετική πτητικότητα των συστατικών του αρχικού διαλύματος είναι κοντά στη
Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ Η υγρή εκχύλιση βρίσκει εφαρμογή όταν. Η σχετική πτητικότητα των συστατικών του αρχικού διαλύματος είναι κοντά στη
ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ
 ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ ο αριθμός Avogadro, N A, L = 6,022 10 23 mol -1 η σταθερά Faraday, F = 96 487 C mol -1 σταθερά αερίων R = 8,314 510 (70) J K -1 mol -1 = 0,082 L atm mol -1 K -1 μοριακός
ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ ο αριθμός Avogadro, N A, L = 6,022 10 23 mol -1 η σταθερά Faraday, F = 96 487 C mol -1 σταθερά αερίων R = 8,314 510 (70) J K -1 mol -1 = 0,082 L atm mol -1 K -1 μοριακός
Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας
 Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας ΙΣΟΡΡΟΠΙΑΙ ΙΔΑΝΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΜΕΘ ΕΤΕΡΑΣ ΦΑΣΕΩΣ ΕΚ ΚΑΘΑΡΟΥ ΔΙΑΛΥΤΟΥ Προσδιορισμός μοριακού βάρους κρυοσκοπικώς Γραμμομοριακή
Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας ΙΣΟΡΡΟΠΙΑΙ ΙΔΑΝΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΜΕΘ ΕΤΕΡΑΣ ΦΑΣΕΩΣ ΕΚ ΚΑΘΑΡΟΥ ΔΙΑΛΥΤΟΥ Προσδιορισμός μοριακού βάρους κρυοσκοπικώς Γραμμομοριακή
ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΕΠΑΝΑΛΗΠΤΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ (Α. Χημική Θερμοδυναμική) H 298
 ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΕΠΑΝΑΛΗΠΤΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ 4-5 (Α. Χημική Θερμοδυναμική) η Άσκηση Από τα δεδομένα του πίνακα που ακολουθεί και δεχόμενοι ότι όλα τα αέρια είναι ιδανικά, να υπολογίσετε: α)
ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΕΠΑΝΑΛΗΠΤΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ 4-5 (Α. Χημική Θερμοδυναμική) η Άσκηση Από τα δεδομένα του πίνακα που ακολουθεί και δεχόμενοι ότι όλα τα αέρια είναι ιδανικά, να υπολογίσετε: α)
R T ενώ σε ολοκληρωµένη, αν θεωρήσουµε ότι οι ενθαλπίες αλλαγής φάσεως είναι σταθερές στο διάστηµα θερµοκρασιών που εξετάζουµε, είναι
 Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξετάσεις: Περίοδος Σεπτεµβρίου 007-0 (.9.00) Θέµα. Η τάση ατµών του στερεού µονοξειδίου του άνθρακα σε 60 K είναι.6 kpa και σε 65 K είναι. kpa. Η τάση ατµών του υγρού
Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξετάσεις: Περίοδος Σεπτεµβρίου 007-0 (.9.00) Θέµα. Η τάση ατµών του στερεού µονοξειδίου του άνθρακα σε 60 K είναι.6 kpa και σε 65 K είναι. kpa. Η τάση ατµών του υγρού
β) διπλασιάζεται. γ) υποδιπλασιάζεται. δ) υποτετραπλασιάζεται. Μονάδες 4
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΕΝΔΟΦΡΟΝΤΙΣΤΗΡΙΑΚΗΣ ΠΡΟΣΟΜΟΙΩΣΗΣ B ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 5 ΙΑΝΟΥΑΡΙΟΥ 009 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΦΥΣΙΚΗ ΘΕΤΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΕΝΔΟΦΡΟΝΤΙΣΤΗΡΙΑΚΗΣ ΠΡΟΣΟΜΟΙΩΣΗΣ B ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 5 ΙΑΝΟΥΑΡΙΟΥ 009 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΦΥΣΙΚΗ ΘΕΤΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ
Κινητική θεωρία ιδανικών αερίων
 Κινητική θεωρία ιδανικών αερίων (γέφυρα μακροσκοπικών και μικροσκοπικών ποσοτήτων) Εμπειρικές σχέσεις Boyle, Gay-Lussac, Charles, υπόθεση Avogadro «όταν δυο ή περισσότερα αέρια έχουν τα ίδια V, P και Τ
Κινητική θεωρία ιδανικών αερίων (γέφυρα μακροσκοπικών και μικροσκοπικών ποσοτήτων) Εμπειρικές σχέσεις Boyle, Gay-Lussac, Charles, υπόθεση Avogadro «όταν δυο ή περισσότερα αέρια έχουν τα ίδια V, P και Τ
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΤΕΛΟΣ 1ΗΣ ΣΕΛΙΔΑΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΕΝΔΟΦΡΟΝΤΙΣΤΗΡΙΑΚΗΣ ΠΡΟΣΟΜΟΙΩΣΗΣ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΥΡΙΑΚΗ 23 ΝΟΕΜΒΡΙΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΦΥΣΙΚΗ ΘΕΤΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΕΝΔΟΦΡΟΝΤΙΣΤΗΡΙΑΚΗΣ ΠΡΟΣΟΜΟΙΩΣΗΣ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΥΡΙΑΚΗ 23 ΝΟΕΜΒΡΙΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΦΥΣΙΚΗ ΘΕΤΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ
ΠΑΡΑΡΤΗΜΑ 3 ΥΠΟΛΟΓΙΣΜΟΣ ΔΙΑΓΡΑΜΜΑΤΩΝ ΦΑΣΕΩΝ ΑΠΟ ΘΕΡΜΟΔΥΝΑΜΙΚΑ ΔΕΔΟΜΕΝΑ
 ΠΑΡΑΡΤΗΜΑ 3-ΥΠΟΛΟΓΙΣΜΟΣ ΔΙΑΓΡΑΜΜΑΤΩΝ ΦΑΣΕΩΝ ΠΑΡΑΡΤΗΜΑ 3 ΥΠΟΛΟΓΙΣΜΟΣ ΔΙΑΓΡΑΜΜΑΤΩΝ ΦΑΣΕΩΝ ΑΠΟ ΘΕΡΜΟΔΥΝΑΜΙΚΑ ΔΕΔΟΜΕΝΑ 1 Εισαγωγή Τα διαγράμματα φάσεων δεν είναι εμπειρικά σχήματα αλλά είναι ουσιαστικής σημασίας
ΠΑΡΑΡΤΗΜΑ 3-ΥΠΟΛΟΓΙΣΜΟΣ ΔΙΑΓΡΑΜΜΑΤΩΝ ΦΑΣΕΩΝ ΠΑΡΑΡΤΗΜΑ 3 ΥΠΟΛΟΓΙΣΜΟΣ ΔΙΑΓΡΑΜΜΑΤΩΝ ΦΑΣΕΩΝ ΑΠΟ ΘΕΡΜΟΔΥΝΑΜΙΚΑ ΔΕΔΟΜΕΝΑ 1 Εισαγωγή Τα διαγράμματα φάσεων δεν είναι εμπειρικά σχήματα αλλά είναι ουσιαστικής σημασίας
Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ. Ενότητα 4: Θερμοδυναμική και Κινητική της Δομής. Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών
 Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ Ενότητα 4: Θερμοδυναμική και Κινητική της Δομής Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ Ενότητα 4: Θερμοδυναμική και Κινητική της Δομής Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 18 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΦΥΣΙΚΗ
 ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 18 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΦΥΣΙΚΗ ΘΕΜΑ 1ο Στις ερωτήσεις 1-4 να γράψετε στο τετράδιό σας τον αριθμό
ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 18 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΦΥΣΙΚΗ ΘΕΜΑ 1ο Στις ερωτήσεις 1-4 να γράψετε στο τετράδιό σας τον αριθμό
Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις
 Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση α: Συντελεστής Joule Thomson (Τζουλ Τόμσον ) Αθανάσιος Τσεκούρας Τμήμα Χημείας Θεωρία 3 Μετρήσεις 6 3 Επεξεργασία Μετρήσεων 6 Σελίδα Θεωρία Η καταστατική εξίσωση
Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση α: Συντελεστής Joule Thomson (Τζουλ Τόμσον ) Αθανάσιος Τσεκούρας Τμήμα Χημείας Θεωρία 3 Μετρήσεις 6 3 Επεξεργασία Μετρήσεων 6 Σελίδα Θεωρία Η καταστατική εξίσωση
Ισορροπία φάσεων σε υδατικά διαλύματα που περιέχουν ελαφρείς υδρογονάνθρακες και παρεμποδιστές υδριτών. Πετροπούλου Ειρήνη
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ II Ισορροπία φάσεων σε υδατικά διαλύματα που περιέχουν ελαφρείς υδρογονάνθρακες και παρεμποδιστές υδριτών. Πετροπούλου Ειρήνη Τυπικά στοιχεία
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ II Ισορροπία φάσεων σε υδατικά διαλύματα που περιέχουν ελαφρείς υδρογονάνθρακες και παρεμποδιστές υδριτών. Πετροπούλου Ειρήνη Τυπικά στοιχεία
ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι. Ενότητα 11: Μεταπτώσεις πρώτης και δεύτερης τάξης. Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών
 ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι Ενότητα 11: Μεταπτώσεις πρώτης και δεύτερης τάξης Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοποί ενότητας Σκοπός της ενότητας αυτής είναι η εισαγωγή του παράγοντα της
ΘΕΡΜΟΔΥΝΑΜΙΚΗ Ι Ενότητα 11: Μεταπτώσεις πρώτης και δεύτερης τάξης Σογομών Μπογοσιάν Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοποί ενότητας Σκοπός της ενότητας αυτής είναι η εισαγωγή του παράγοντα της
ΠΥΚΝΟΤΗΤΑ ΠΟΛΥΜΕΡΙΚΗΣ ΑΛΥΣΙΔΑΣ
 ΠΥΚΝΟΤΗΤΑ ΠΟΛΥΜΕΡΙΚΗΣ ΑΛΥΣΙΔΑΣ Ποιά είναι η πυκνότητα μίας πολυμερικής αλυσίδας με μοριακό βάρος Μ και Ν μονομέρη; (η συγκέντρωση δηλαδή των μονομερών μέσα στον όγκο που καταλαμβάνει η αλυσίδα). Μέγεθος
ΠΥΚΝΟΤΗΤΑ ΠΟΛΥΜΕΡΙΚΗΣ ΑΛΥΣΙΔΑΣ Ποιά είναι η πυκνότητα μίας πολυμερικής αλυσίδας με μοριακό βάρος Μ και Ν μονομέρη; (η συγκέντρωση δηλαδή των μονομερών μέσα στον όγκο που καταλαμβάνει η αλυσίδα). Μέγεθος
ΦΥΣΙΚΟΧΗΜΕΙΑ. Δημήτριος Τσιπλακίδης e-mail: dtsiplak@chem.auth.gr url: users.auth.gr/~dtsiplak. Φυσικοχημεία συστημάτων
 1 ΦΥΣΙΚΟΧΗΜΕΙΑ Δημήτριος Τσιπλακίδης e-mail: dtsiplak@chem.auth.gr url: users.auth.gr/~dtsiplak Φυσικοχημεία συστημάτων Φυσικοχημεία συστημάτων 2 «Όμοιος αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη
1 ΦΥΣΙΚΟΧΗΜΕΙΑ Δημήτριος Τσιπλακίδης e-mail: dtsiplak@chem.auth.gr url: users.auth.gr/~dtsiplak Φυσικοχημεία συστημάτων Φυσικοχημεία συστημάτων 2 «Όμοιος αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη
ΔΙΑΓΩΝΙΣΜΑ Α. Θέµα 1 ο Να επιλέξετε τη σωστή απάντηση σε κάθε µία από τις παρακάτω ερωτήσεις:
 ΔΙΑΓΩΝΙΣΜΑ Α Θέµα ο Να επιλέξετε τη σωστή απάντηση σε κάθε µία από τις παρακάτω ερωτήσεις: Σύµφωνα µε την κινητική θεωρία των ιδανικών αερίων η σχέση που συνδέει την πίεση του αερίου µε τις ταχύτητες των
ΔΙΑΓΩΝΙΣΜΑ Α Θέµα ο Να επιλέξετε τη σωστή απάντηση σε κάθε µία από τις παρακάτω ερωτήσεις: Σύµφωνα µε την κινητική θεωρία των ιδανικών αερίων η σχέση που συνδέει την πίεση του αερίου µε τις ταχύτητες των
Θεωρία και Μεθοδολογία
 Θεωρία και Μεθοδολογία Εισαγωγή/Προαπαιτούμενες γνώσεις (κάθετη δύναμη) Πίεση p: p = F A (εμβαδόν επιφάνειας) Μονάδα μέτρησης πίεσης στο S.I. είναι το 1 Ν m2, που ονομάζεται και Pascal (Pa). Συνήθως χρησιμοποιείται
Θεωρία και Μεθοδολογία Εισαγωγή/Προαπαιτούμενες γνώσεις (κάθετη δύναμη) Πίεση p: p = F A (εμβαδόν επιφάνειας) Μονάδα μέτρησης πίεσης στο S.I. είναι το 1 Ν m2, που ονομάζεται και Pascal (Pa). Συνήθως χρησιμοποιείται
ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ ΘΕΩΡΙΑ
 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 693 946778 ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ ΘΕΩΡΙΑ Περιεχόμενα 1. Κινητική Θεωρία των Αεριών. Πίεση 3. Κινητική Ερμηνεία της Πίεσης 4. Καταστατική εξίσωση των Ιδανικών
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 693 946778 ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ ΘΕΩΡΙΑ Περιεχόμενα 1. Κινητική Θεωρία των Αεριών. Πίεση 3. Κινητική Ερμηνεία της Πίεσης 4. Καταστατική εξίσωση των Ιδανικών
Physics by Chris Simopoulos
 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΑΕΡΙΩΝ Η εξίσωση που συνδέει την πίεση τον όγκο και την θερμοκρασία ενός ιδανικού αερίου που βρίσκεται σε κατάσταση ισορροπίας ονομάζεται καταστατική εξίσωση αερίου και δίνεται όπως
ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΑΕΡΙΩΝ Η εξίσωση που συνδέει την πίεση τον όγκο και την θερμοκρασία ενός ιδανικού αερίου που βρίσκεται σε κατάσταση ισορροπίας ονομάζεται καταστατική εξίσωση αερίου και δίνεται όπως
Βασικές Διεργασίες Μηχανικής Τροφίμων
 Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 8: Εκχύλιση, 1ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Τύποι εκχύλισης
Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 8: Εκχύλιση, 1ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Τύποι εκχύλισης
ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΚΑΙ ΤΑΣΗ ΑΤΜΩΝ
 ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΚΑΙ ΤΑΣΗ ΑΤΜΩΝ 2 Διεργασίες Πολυφασικών συστημάτων Πολλές διεργασίες στη Χημική Μηχανική στηρίζονται στη μεταφορά μάζας μεταξύ διαφορετικών φάσεων (αέρια, υγρή, στερεή) Εξάτμιση-Εξάχνωση
ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΚΑΙ ΤΑΣΗ ΑΤΜΩΝ 2 Διεργασίες Πολυφασικών συστημάτων Πολλές διεργασίες στη Χημική Μηχανική στηρίζονται στη μεταφορά μάζας μεταξύ διαφορετικών φάσεων (αέρια, υγρή, στερεή) Εξάτμιση-Εξάχνωση
ΤΥΠΟΛΟΓΙΟ ΚΙΝΗΤΙΚΗΣ ΘΕΩΡΙΑΣ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ T 1 <T 2 A
 ΤΥΠΟΛΟΓΙΟ ΚΙΝΗΤΙΚΗΣ ΘΕΩΡΙΑΣ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ 1. ΝΟΜΟΣ OYLE-MRIOTTE = σταθ. (όταν Τ = σταθ.) (1) Ο νόμος των oyle Mariotte εφαρμόζεται σε ισόθερμη μεταβολή (Τ = σταθ.) π.χ. στην μεταβολή Α T 1
ΤΥΠΟΛΟΓΙΟ ΚΙΝΗΤΙΚΗΣ ΘΕΩΡΙΑΣ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ 1. ΝΟΜΟΣ OYLE-MRIOTTE = σταθ. (όταν Τ = σταθ.) (1) Ο νόμος των oyle Mariotte εφαρμόζεται σε ισόθερμη μεταβολή (Τ = σταθ.) π.χ. στην μεταβολή Α T 1
ΝΟΜΟΙ ΑΕΡΙΩΝ ΘΕΡΜΟΔΥΝΑΜΙΚΗ
 ΝΟΜΟΙ ΑΕΡΙΩΝ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΑΣΚΗΣΗ 1 Μία θερμική μηχανή λειτουργεί μεταξύ των θερμοκρασιών T h 400 Κ και T c με T c < T h Η μηχανή έχει απόδοση e 0,2 και αποβάλλει στη δεξαμενή χαμηλής θερμοκρασίας θερμότητα
ΝΟΜΟΙ ΑΕΡΙΩΝ ΘΕΡΜΟΔΥΝΑΜΙΚΗ ΑΣΚΗΣΗ 1 Μία θερμική μηχανή λειτουργεί μεταξύ των θερμοκρασιών T h 400 Κ και T c με T c < T h Η μηχανή έχει απόδοση e 0,2 και αποβάλλει στη δεξαμενή χαμηλής θερμοκρασίας θερμότητα
Οδηγίες χρήσης Aspen Plus 7.1
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Εργαστήριο Θερμοδυναμικής & Φαινομένων Μεταφοράς Οδηγίες χρήσης Aspen Plus 7.1 Έναρξη προσομοίωσης (1/2) Έναρξη προσομοίωσης (2/2) Εμφανίζεται το ακόλουθο
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Εργαστήριο Θερμοδυναμικής & Φαινομένων Μεταφοράς Οδηγίες χρήσης Aspen Plus 7.1 Έναρξη προσομοίωσης (1/2) Έναρξη προσομοίωσης (2/2) Εμφανίζεται το ακόλουθο
Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ. Χημεία ΒΑΣΙΚΕΣ ΓΝΩΣΕΙΣ ΑΣΠΡΟΠΥΡΓΟΣ
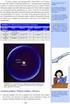 ΑΕΝ / ΑΣΠΡΟΠΥΡΓΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ Χημεία ΒΑΣΙΚΕΣ ΓΝΩΣΕΙΣ ΑΣΠΡΟΠΥΡΓΟΣ 2 Ογκομέτρηση προχοϊδα διάλυμα HCl ΕΔΩ ακριβώς μετράμε τον όγκο ( στην εφαπτομένη της καμπύλης
ΑΕΝ / ΑΣΠΡΟΠΥΡΓΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ Χημεία ΒΑΣΙΚΕΣ ΓΝΩΣΕΙΣ ΑΣΠΡΟΠΥΡΓΟΣ 2 Ογκομέτρηση προχοϊδα διάλυμα HCl ΕΔΩ ακριβώς μετράμε τον όγκο ( στην εφαπτομένη της καμπύλης
Αλληλεπίδραση δίπόλο-δίπολο
 Αλληλεπίδραση δίπόλο-δίπολο δίπολο Εκτός από την αλληλεπίδραση µέσω των δεσµικών ηλεκτρονίων, τα πυρηνικά σπίν αλληλεπιδρούν και µέσω του χώρου. Αυτή η αλληλεπίδραση ονοµάζεται αλληλεπίδραση δίπολο-δίπολο.
Αλληλεπίδραση δίπόλο-δίπολο δίπολο Εκτός από την αλληλεπίδραση µέσω των δεσµικών ηλεκτρονίων, τα πυρηνικά σπίν αλληλεπιδρούν και µέσω του χώρου. Αυτή η αλληλεπίδραση ονοµάζεται αλληλεπίδραση δίπολο-δίπολο.
ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ Ενότητα : Ισορροπίες φάσεων, διαλυτότητα
 ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ Ενότητα : Ισορροπίες φάσεων, διαλυτότητα Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών IΣΟΡΡΟΠΙΕΣ ΦΑΣΕΩΝ. ΔΙΑΛΥΤΟΤΗΤΑ Τα διαλύματα των μακρομορίων
ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ Ενότητα : Ισορροπίες φάσεων, διαλυτότητα Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών IΣΟΡΡΟΠΙΕΣ ΦΑΣΕΩΝ. ΔΙΑΛΥΤΟΤΗΤΑ Τα διαλύματα των μακρομορίων
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Θερμοδυναμική. Μη Αντιστρεπτότητα και ο 2ος Θ.ν. Διδάσκων : Καθηγητής Γ.
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Θερμοδυναμική Μη Αντιστρεπτότητα και ο 2ος Θ.ν. Διδάσκων : Καθηγητής Γ. Φλούδας Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Θερμοδυναμική Μη Αντιστρεπτότητα και ο 2ος Θ.ν. Διδάσκων : Καθηγητής Γ. Φλούδας Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
V P P. [3] (α) Να δειχθεί ότι για ένα υδροστατικό σύστημα ισχύει: P V
![V P P. [3] (α) Να δειχθεί ότι για ένα υδροστατικό σύστημα ισχύει: P V V P P. [3] (α) Να δειχθεί ότι για ένα υδροστατικό σύστημα ισχύει: P V](/thumbs/64/51699713.jpg) ΘΕΡΜΟΔΥΝΑΜΙΚΗ (ΦΥΣΙΚΗ I) 1 [1] Θεωρώντας την εσωτερική ενέργεια ενός υδροστατικού συστήματος σα συνάρτηση των Τ και, αποδείξτε τις παρακάτω εξισώσεις: d d dq (1) β () β κ ) ( κ () [] Θεωρώντας την εσωτερική
ΘΕΡΜΟΔΥΝΑΜΙΚΗ (ΦΥΣΙΚΗ I) 1 [1] Θεωρώντας την εσωτερική ενέργεια ενός υδροστατικού συστήματος σα συνάρτηση των Τ και, αποδείξτε τις παρακάτω εξισώσεις: d d dq (1) β () β κ ) ( κ () [] Θεωρώντας την εσωτερική
