H τέλεια κρυσταλλική δομή των καθαρών μετάλλων
|
|
|
- Ζένα Αντωνόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 Κεφάλαιο 3 H τέλεια κρυσταλλική δομή των καθαρών μετάλλων Μετά από κάποια εισαγωγικά στοιχεία συζητιέται ο τρόπος δημιουργίας βασικών κρυσταλλικών δομών (SC, BCC, FCC, HCP), ως τρισδιάστατες στοιβάδες δισδιάστατων διατάξεων. Στη συνέχεια αναφέρονται όλα τα κρυσταλλικά συστήματα και οι τύποι κυψελίδων που διαθέτει το καθένα. Εισάγονται βασικοί υπολογισμοί στην κρυσταλλική δομή των καθαρών μετάλλων. Σ το προηγούμενο κεφάλαιο έγινε αναφορά στην «ενδοατομική» δομή των ατόμων των στοιχείων, στον τρόπο δημιουργίας των ηλεκτρονίων σθένους καθώς και στους μηχανισμούς που τα στοιχεία ενώνονται μεταξύ τους για τη δημιουργία μεγαλύτερων (μονο-, δι- ή πολυστοιχειακών) μορίων. Σε αυτό το κεφάλαιο θα συζητηθούν οι τρόποι με τους οποίους τα άτομα των στοιχείων διατάσσονται στο χώρο ώστε να δημιουργήσουν τις κρυσταλλικές δομές των υλικών. Σε πρώτη φάση η συζήτηση θα αφορά κρυσταλλικές δομές στις οποίες όλα τα άτομα είναι ίδια, δηλαδή του ίδιου στοιχείου. Τέτοιες είναι οι δομές των καθαρών μετάλλων. Κρυσταλλική δομή 3.1 Εισαγωγικά στοιχεία Επίπεδες διατάξεις Όταν λέμε ότι η δομή κάποιου υλικού είναι κρυσταλλική (και γίνεται λόγος για κρυσταλλικό υλικό (crystalline material))εννοούμε ότι η διάταξη των ατόμων στο χώρο είναι περιοδική. Δηλαδή, η δομή μπορεί αυτούσια (με όλα τα στοιχεία συμμετρίας της) να αναπαραχθεί με την επανάληψη μιας κατάλληλης βασικής μονάδας. Στην αντίθετη περίπτωση η δομή ονομάζεται άμορφη και το υλικό άμορφο υλικό (amorphous ή noncrystalline material). Στη φύση υπάρχουν τόσο κρυσταλλικά (π.χ. σίδηρος) όσο και άμορφα υλικά (π.χ. κοινό γυαλί) υψηλού τεχνολογικού ενδιαφέροντος. Γενικά, τα μέταλλα, τα περισσότερα κεραμικά αλλά και αρκετά πολυμερή έχουν κρυσταλλική δομή. Η άμορφη κατάσταση ευνοείται όταν υπάρχουν πολύπλοκα μόρια και δομές αλλά και όταν από υψηλές θερμοκρασίες (π.χ. ένα τήγμα) μέσω αρκετά γρήγορης ψύξης δεν δοθεί χρόνος στα άτομα να αναδιαταχθούν και να αποκτήσουν κρυσταλλική δομή, η οποία πλέον σε θερμοκρασίες περιβάλλοντος λόγω ιδιαίτερα αργής κινητικής πρακτικά δεν αποκτάται ποτέ. 3.1
2 Ένα ενδιαφέρον ερώτημα σχετίζεται το γιατί τα άτομα τείνουν να αποκτήσουν κρυσταλλικές δομές. Μια απλουστευμένη αλλά κατανοητή απάντηση δίνεται μέσω του σχήματος της Εικόνας 3.1. Στην άμορφη κατάσταση η μέση απόσταση ισορροπίας των δεσμών μεταξύ των ατόμων είναι μεγαλύτερη από αυτήν που αντιστοιχεί στην ελάχιστη ενέργεια του συστήματος, σε αντίθεση με την κρυσταλλική κατάσταση. Κατά συνέπεια τα άτομα τείνουν να καταλάβουν κρυσταλλικές δομές ώστε να ελαχιστοποιηθεί η ενέργεια του συστήματος. Εικόνα 3.1: Σχηματική παράσταση της ελαχιστοποίησης της ενέργειας δεσμού μέσω περιοδικής (κρυσταλλικής) διάταξης ατόμων Ατομικό μοντέλο Π Α Ρ Α Δ Ε Ι Γ Μ Α Στη συζήτηση που θα ακολουθήσει περί κρυσταλλικής δομής ενδιαφέρει η διάταξη των ατόμων στο χώρο και όχι η ίδια η δομή τους ούτε αυτή καθ αυτή η φύση του μεταξύ τους δεσμού. Κατά συνέπεια το άτομο κάποιου στοιχείου θα παρίσταται ως τέλεια σφαίρα ακτίνας R (και διαμέτρου D=2R) με όλες τις γνωστές ιδιότητες. Ο όγκος του ατόμου θα είναι V at. = 4 3 πr3 και η προβολή του (το «αποτύπωμά» του) σε μια επιφάνεια θα είναι κύκλος ακτίνας R και εμβαδού S at. = πr 2. Από τα δεδομένα του Πίνακα 2.1 της σελίδας 30 διαπιστώνουμε ότι ο Σίδηρος (Fe) έχει ατομική ακτίνα R Fe =0.124 nm ενώ το Μολυβδαίνιο (Μο) R Μο =0.175 nm. Μπορούμε λοιπόν να θεωρήσουμε ότι ο όγκος του ατόμου του Μολυβδαινίου (V at. Mo ) είναι V at.mo V at.fe = R 3 Mo R3 = Fe (0.175 nm)3 (0.124 nm) 3 = φορές μεγαλύτερος από τον όγκο του ατόμου του σιδήρου. Επίσης, για μια γραμμική διάταξη μήκους ενός μέτρου απαιτούνται: 1 m m άτομα Μολυβδαινίου και ~4.03x10 9 άτομα Σιδήρου, το ένα δίπλα στο άλλο και χωρίς ενδιάμεσα κενά. 3.2
3 Επίπεδες ατομικές διατάξεις Απλή επίπεδη διάταξη Πριν γίνει αναφορά στον τρόπο δημιουργίας τρισδιάστατων μεταλλικών δομών κρίνεται σκόπιμο να γίνει αναφορά σε επίπεδες (δισδιάστατες διατάξεις ατόμων) διότι αφενός αυτές αποτελούν τη βάση ανάπτυξης τρισδιάστατων δομών, αφετέρου βοηθούν στην απλούστερη εισαγωγή ορισμένων βασικών εννοιών. Η πιο απλή επίπεδη διάταξη σφαιρικών ατόμων ακτίνας R που μπορεί να φανταστεί κανείς είναι αυτή που παρουσιάζεται στην Εικόνα 3.2 και ονομάζεται απλή διάταξη (simple packing, SP). Τα άτομα τοποθετούνται στοιχισμένα το ένα δίπλα στο άλλο. Εικόνα 3.2: Σχηματική παράσταση απλής επίπεδης διάταξης ατόμων ακτίνας R. Ορίζουμε ως αριθμό ένταξης (coordination number, CN) επίπεδης διάταξης ίδιων ατόμων, τον αριθμό των ατόμων με τα οποία ένα οποιοδήποτε άτομο της διάταξης εφάπτεται (δηλαδή συνάπτει χημικό δεσμό). Από την Εικόνα 3.2 εύκολα διαπιστώνεται ότι ο αριθμός της απλής επίπεδης διάταξης είναι CN SP = 4. Κάθε άτομο της διάταξης εφάπτεται με τέσσερα άτομα. Σημείωση: Οι διατάξεις σε αυτές τις σημειώσεις αλλά και σε όλα τα σχετικά βιβλία απεικονίζονται για πρακτικούς λόγους ως πεπερασμένες. Αυτό δεν πρέπει να παρερμηνεύεται και θα πρέπει να θεωρούνται ότι εκτείνονται στο άπειρο προς όλες τις κατευθύνσεις. Η επίπεδη διάταξη της Εικόνας 3.2 εκτείνεται στο άπειρο τόσο προς την κατεύθυνση x όσο και προς την κατεύθυνση y. Σε μια επίπεδη διάταξη μπορούμε επίσης να ορίσουμε και έναν συντελεστή επιφανειακής κάλυψης (ΣΕΚ), ως το κλάσμα της επιφάνειας που καλύπτεται από άτομα: ΣΕΚ = επιφάνεια που καλύπτεται από άτομα συνολική επιφάνεια (3.1) 3.3
4 Το ερώτημα που γεννάται είναι πως θα προσδιοριστεί ο συγκεκριμένος συντελεστής εφόσον η διάταξη εκτείνεται στο άπειρο και οι ακριβείς της διαστάσεις δεν είναι γνωστές. Η απάντηση είναι απλή. Εφόσον η διάταξη είναι περιοδική, αρκεί να εντοπίσουμε μια βασική μονάδα, επανάληψη της οποίας αναπαραγάγει πλήρως τη διάταξη, και να υπολογίσουμε τον ΣΕΚ της βασικής μονάδας. Στη συγκεκριμένη απλή επίπεδη διάταξη μπορούμε να ορίσουμε πολλές βασικές μονάδες, τρία παραδείγματα δίνονται στην Εικόνα 3.3. Η σχέση (3.1) μπορεί να εφαρμοσθεί είτε στη βασική μονάδα Α, είτε στη βασική μονάδα Β, είτε στη βασική μονάδα Γ (είτε σε κάποια άλλη κατάλληλα ορισμένη βασική μονάδα): ΣΕΚ Α = n at.s at. S tot. ΣΕΚ Β = n at.s at. S tot. = 1 πr2 (2R) 2 = π 4 = 4 πr2 (4R) 2 = π 4 ΣΕΚ Γ = n at.s at. (4 1 = 4 ) πr2 S tot. (2R) 2 = π 4 Είναι προφανές ότι ο ΣΕΚ θα πρέπει να είναι ανεξάρτητος της βασικής μονάδας εφόσον πρόκειται για την ίδια διάταξη. Για την απλή επίπεδη διάταξη ισχύει: Εικόνα 3.3: Σχηματική αναπαραγωγή απλής επίπεδης διάταξης από διάφορες βασικές μονάδες. ΣΕΚ SP = π % 4 Δηλαδή, σε μια απλή επίπεδη διάταξη το 78.5% της επιφάνειας καταλαμβάνεται από άτομα ενώ το υπόλοιπο =21.5% είναι ακάλυπτη επιφάνεια. Επίπεδη διάταξη ψηλής πυκνότητας O δεύτερος τρόπος βάσει του οποίου μπορούν να διαταχθούν σφαιρικά άτομα στο επίπεδο, είναι αυτός που παρουσιάζεται στην Εικόνα 3.4. Η διάταξη αυτή ονομάζεται επίπεδη διάταξη ψηλής πυκνότητας (closed packing, CP). Όπως φαίνεται και στην εικόνα ο αριθμός ένταξης της επίπεδης διάταξης υψηλής πυκνότητας είναι
5 Εικόνα 3.4: Σχηματική παράσταση επίπεδης διάταξης ψηλής πυκνότητας Ο ΣΕΚ προσδιορίζεται με τρόπο ανάλογο με αυτόν που χρησιμοποιήθηκε για τον προσδιορισμό του ΣΕΚ της απλής επίπεδης διάταξης. Στην Εικόνα 3.5 δίνονται δύο βασικές μονάδες που θα μπορούσαν να αναπαραγάγουν πλήρως μια επίπεδη διάταξη ψηλής πυκνότητας ατόμων ακτίνας R. Εικόνα 3.5: Σχηματική αναπαραγωγή επίπεδης διάταξης ψηλής πυκνότητας από δύο διαφορετικές βασικές μονάδες. Εφαρμογή της σχέσης (3.1) στις βασικές μονάδες Α και Β δίνει: ΣΕΚ Α = n at.s at. ΣΕΚ Α = n at.s at. = ( ) πr2 S tot. 2R 2R 3 = ( ) πr2 S tot. 6R 2 3 = π 3 6 = π 3 6 Σημείωση: Στην παραπάνω σχέση ο παρονομαστής 6R 2 3 εκφράζει το εμβαδόν του κανονικού εξαγώνου πλευράς 2R. 3.5
6 Συμπερασματικά, για επίπεδη διάταξη ψηλής πυκνότητας ατόμων ακτίνας R ισχύει: ΣΕΚ CP = π % Συγκρίνοντας τους συντελεστές επιφανειακής κάλυψης της απλής και της ψηλής πυκνότητας διάταξης είναι φανερό ότι η ψηλής πυκνότητας διάταξη κάνει μεγαλύτερη και αποτελεσματικότερη χρήση της επιφάνειας. Σημείωση: Αξίζει να προσεχθεί ο τρόπος καταμέτρησης του αριθμού των ατόμων που περιέχει η κάθε βασική μονάδα. Π.χ. η βασική μονάδα Γ της εικόνας 3.3 περιέχει έναν συνολικό αριθμό ενός ατόμου ο οποίος απαρτίζεται από τέσσερα τμήματα κάθε ένα εκ των οποίων είναι ίσο με το 1/4 ενός ατόμου. Αντίστοιχα η βασική μονάδα Β της Εικόνας 3.5 περιέχει έναν συνολικό αριθμό τριών ατόμων ο οποίος απαρτίζεται από ένα ολόκληρο άτομο στο εσωτερικό και από 6 τμήματα κάθε ένα εκ των οποίων είναι ίσο με το 1/3 ενός ατόμου. Εάν διατάξουμε τις βασικές μονάδες στο επίπεδο διαπιστώνουμε ότι κάποια άτομα μοιράζονται εξ ίσου σε περισσότερες από μία βασικές μονάδες (π.χ. σε δύο, τρεις, τέσσερεις κλπ.). Σε αυτές τις περιπτώσεις σε κάθε βασική μονάδα απόδίδεται μόνο το τμήμα του ατόμου που της ανήκει (π.χ. το 1/2, 1/3, 1/4 κλπ.). Σημείωση: Επίσης αξίζει να σημειωθεί ότι ο ΣΕΚ είναι ανεξάρτητος της ακτίνας R των ατόμων της διάταξης. A Σ Κ Η Σ Η 3. 1 Ποια θα είναι η ποσοστιαία μεταβολή συνολικής επιφάνειας αν ο ίδιος αριθμός ατόμων αναδιαταχθεί από απλή επίπεδη διάταξη σε επίπεδη διάταξη ψηλής πυκνότητας. Για την κάθε διάταξη ισχύει: ΣΕΚ SP = π = n at.s at. n 4 S at. S at. = π S tot.sp tot.sp 4 ΣΕΚ CP = π 3 = n at.s at. n 6 S at. S at. = π 3S tot.cp tot.cp 6 (3.2) (3.3) Εφόσον πρόκειται για τον ίδιο αριθμό ατόμων (ίδιας ακτίνας) τα αριστερά μέλη των εξισώσεων (3.2) και (3.3) είναι ίδια, οπότε: π S tot.sp 4 = π 3S tot.cp 6 S tot.cp S tot.sp = = Δηλαδή, με την αναδιάταξη η συνολική επιφάνεια θα μειωθεί κατά 13.4% Απεικονίσεις Σε όλες τις μέχρι τώρα απεικονίσεις ατομικών διατάξεων χρησιμοποιήθηκε το μοντέλο των εφαπτόμενων σφαιρών, δηλαδή το κάθε άτομο παρίσταται ως σφαίρα. Αυτός ο τρόπος απεικόνισης έχει το πλεονέκτημα ότι αναπαριστά αρκετά πιστά την πραγματικότητα αλλά και το μειονέκτημα ότι δεν είναι πρακτικός και, σε πιο περίπλοκες περιπτώσεις, δεν παρέχει εποπτική αντίληψη της δομής. Γι αυτό το λόγο στην «Επιστήμη και Τεχνολογία των Υλικών» υιοθετήθηκε ένα άλλο μοντέλο απεικόνισης και διατάξεων, το λεγόμενο μοντέλο των διευρυμένων διατομικών αποστάσεων. Σύμφωνα με αυτό το μοντέλο, τα άτομα θεωρούνται σημεία που βρίσκονται στο κέντρο των σφαιρών και συγκεντρώνουν όλη τη μάζα, οι δε διατάξεις και δομές παριστάνονται κυρίως με τις ευθείες που ενώνουν τα κέντρα των σφαιρών. Οι επίπεδες διατάξεις που απεικονίζονται, σύμφωνα με το μοντέλο των 3.6
7 εφαπτόμενων σφαιρών, στις Εικόνες 3.2 και 3.4, παριστάνονται σύμφωνα με το μοντέλο των διευρυμένων διατομικών αποστάσεων στην Εικόνα 3.6 Εικόνα 3.6: Παράσταση επίπεδων διατάξεων σύμφωνα με το μοντέλο των διευρυμένων διατομικών αποστάσεων Αξίζει να σημειωθεί ότι στην παράσταση με διευρυμένες διατομικές αποστάσεις παρουσιάζονται ορισμένα φαινομενικά παράδοξα (π.χ. η διάμετρος του κάθε ατόμου είναι 2R ενώ 2R είναι και η απόσταση μεταξύ των κέντρων παρακείμενων ατόμων) τα οποία απλά οφείλονται στο γεγονός πως ο συγκεκριμένος τρόπος απεικόνισης αποτελεί συμβατική αναπαράσταση του μοντέλου των εφαπτόμενων σφαιρών που εκφράζει πιο πιστά την πραγματικότητα. Στις παραγράφους που ακολουθούν θα γίνει αρχικά παράλληλη χρήση και των δύο μοντέλων για παιδαγωγικούς λόγους, σταδιακά δε, θα υιοθετηθεί μόνο το μοντέλο των διευρυμένων διατομικών αποστάσεων. 3.2 Βασικές τρισδιάστατες διατάξεις - δομές Oι τρισδιάστατες κρυσταλλικές δομές των μετάλλων ουσιαστικά προκύπτουν από την ανάπτυξη επίπεδων διατάξεων στην τρίτη διάσταση (z). Eιδικά δε ένας μεγάλος αριθμός τεχνολογικά σημαντικών μετάλλων προκύπτει από ανάπτυξη στην τρίτη διάσταση επίπεδων στοιβάδων απλής και υψηλής πυκνότητας. Στις επόμενες παραγράφους θα συζητηθεί με μεγαλύτερη λεπτομέρεια ο τρόπος δημιουργίας αυτών των σημαντικών δομών και τα κύρια χαρακτηριστικά τους. Η απλή κυβική δομή Εάν θεωρήσουμε απλές επίπεδες στοιβάδες ατόμων ακτίνας R οι οποίες τοποθετούνται, κατά τον άξονα των z, ακριβώς η μια πάνω στην άλλη τότε προκύπτει η τρισδιάστατη δομή που φαίνεται στην Εικόνα 3.7 σύμφωνα με τους δύο τρόπους απεικόνισης που προαναφέρθηκαν. Η δομή που προκύπτει με αυτόν τον τρόπο ονομάζεται απλή κυβική (simple cubic, SC). Λέμε ότι τα άτομα βρίσκονται σε απλή κυβική διάταξη. Επειδή η δομή προκύπτει από διαδοχικές επίπεδες στοιβάδες τοποθετημένες η μια πάνω στην άλλη με τον ίδιο τρόπο λέμε ότι είναι δομή τύπου ΑΑΑ. Με αυτόν τον τρόπο δημιουργείται ένα τρισδιάστατο πλέγμα (lattice). Τα σημεία στα οποία βρίσκονται τα άτομα ονομάζονται πλεγματικά σημεία (lattice sites). Στην εικόνα 3.7 παρουσιάζεται το πλέγμα της απλής κυβικής δομής. 3.7
8 Αριθμός ένταξης Εικόνα 3.7: Το πλέγμα της απλής κυβικής δομής σε απεικόνιση εφαπτόμενων σφαιρών και διευρυμένων διατομικών αποστάσεων Ο αριθμός ένταξης ατόμων σε τρισδιάστατη διάταξη ορίζεται ακριβώς με τον ίδιο τρόπο που ορίστηκε και σε επίπεδες διατάξεις, μόνο που τώρα πρέπει να ληφθούν υπόψη τα εφαπτόμενα άτομα και στις τρεις διαστάσεις. Από την εικόνα 3.8 εύκολα διαπιστώνεται πως ο αριθμός ένταξης των ατόμων στην απλή κυβική διάταξη είναι 6 (τέσσερα εφαπτόμενα άτομα στο ίδιο επίπεδο, ένα στο αμέσως πάνω και ένα στο αμέσως κάτω). Η βασική μονάδα Όπως και στην επίπεδη περίπτωση οι τρισδιάστατες δομές εκτείνονται στο άπειρο προς όλες τις διαστάσεις άσχετα αν οι απεικονίσεις τους, για πρακτικούς λόγους είναι πεπερασμένες. Κατά συνέπεια για την ποσοτική περιγραφή χαρακτηριστικών τους αρκεί ο εντοπισμός μιας κατάλληλης (προφανώς τρισδιάστατης) βασικής μονάδας η οποία περιέχει όλα τα στοιχεία συμμετρίας της δομής και την αναπαραγάγει με απλή επανάληψη στο χώρο. Και στις δομές μπορούν να ορισθούν διάφορες βασικές Εικόνα 3.8: H ένταξη ατόμου σε απλή κυβική διάταξη μονάδες. Η μικρότερη βασική μονάδα με επανάληψη της οποίας μπορεί να αναπαραχθεί η δομή ονομάζεται μοναδιαία κυψελίδα (unit cell). Όπως προκύπτει από την συμβατική αναπαράσταση του πλέγματος της απλής κυβικής διάταξης η μοναδιαία κυψελίδα είναι κύβος με ακμή 2R ο οποίος περιέχει πλεγματικά σημεία στις κορυφές του. Η συνήθης αναπαράσταση της μοναδιαίας κυψελίδες είναι αυτή που παρουσιάζεται στην Εικόνα 3.9. Για την καλύτερη κατανόησή κρίνεται σκόπιμο στο 3.8
9 σημείο αυτό να αναφερθούν κάποια σχόλια. H συμβατική αναπαράσταση του πλέγματος με διευρυμένες διατομικές αποστάσεις προκύπτει από την αναπαράσταση των εφαπτόμενων σφαιρών θεωρώντας τα σφαιρικά άτομα ως σημεία που βρίσκονται στο κέντρο των σφαιρών. Κατά συνέπεια η σωστή αναπαράσταση της μοναδιαίας κυψελίδας Εικόνα 3.9: Η συνήθης αναπαράσταση της μοναδιαίας κυψελίδας της απλής κυβικής διάταξης όπως προκύπτει από το πλέγμα. σύμφωνα με το μοντέλο εφαπτόμενων σφαιρών είναι αυτή που απεικονίζεται στην Εικόνα 3.10γ. Δηλαδή, σε κάθε κυψελίδα ουσιαστικά περιέχεται το 1/8 της σφαίρας (εφόσον κάθε άτομο στην τρισδιάστατη δομή επιμερίζεται εξ ισου σε οκτώ κυψελίδες). (α) (β) (γ) (δ) (ε) 3.9
10 Εικόνα 3.10: Η συμβατική αναπαράσταση της μοναδιαίας κυψελίδας της απλής κυβικής διάταξης και η ακριβής αναπαράσταση σύμφωνα με το μοντέλο των εφαπτόμενων σφαιρών. Σύμφωνα με τα παραπάνω ο αριθμός των ατόμων που περιέχει η μοναδιαία κυψελίδα της απλής κυβικής διάταξης είναι 1 (δηλ. 8x1/8). Αυτό δεν είναι προφανές χωρίς τις πληροφορίες που αναφέρονται παραπάνω και πολύ συχνά η απλή κυβική διάταξη σε βιβλία Επιστήμης και Τεχνολογίας Υλικών παριστάνεται ενδεικτικά με τα σχήματα των Εικόνων 3.10β και 3.10ε. Θα πρέπει να θεωρείται γνωστό ότι κάθε άτομο συμμετέχει κατά το 1/8 σε αυτήν. Η δε ακμή του κύβου της κυψελίδας είναι α SC = 2R. Σημείωση: Το σχήμα της εικόνας 3.10(β) θα μπορούσε επίσης να θεωρηθεί ότι αποτελεί βασική μονάδα της απλής κυβικής διάταξης. Πρόκειται για κύβο με ακμή 4R ο οποίος περιέχει 8 άτομα, διότι όλα βρίσκονται στο εσωτερικό του και δεν επιμερίζονται σε άλλες κυψελίδες. Δεν αποτελεί όμως τη μικρότερη βασική μονάδα ή μοναδιαία κυψελίδα όπως το σχήμα της εικόνας 3.10(γ). Συντελεστής Ατομικής Πλήρωσης Σε τρισδιάστατες διατάξεις δεν έχει νόημα ο ορισμός συντελεστή επιφανειακής κάλυψης. Ορίζεται ο συντελεστής ατομικής πλήρωσης (Atomic Packing Factor, APF) ως το κλάσμα του όγκου της διάταξης που καταλαμβάνεται από άτομα: APF = όγκος που καταλαμβάνεται από άτομα συνολικός όγκος (3.4) Για την απλή κυβική διάταξη στη βάση μιας μοναδιαίας κυψελίδας υπολογίζουμε: APF SC = n at. V at. = (8 1 8 ) 4 3 πr3 = πr3 = π V tot. (2R) 3 (2R) (3.5) To 52.36% του όγκου καταλαμβάνεται από άτομα ενώ το υπόλοιπο 47.64% είναι κενός χώρος μεταξύ των ατόμων. Υλικά Α Σ Κ Η Σ Η 3. 2 H απλή κυβική διάταξη είναι σπάνια στα μέταλλα κυρίως εξαιτίας του χαμηλού APF (ο μεταλλικός δεσμός είναι ισότροπος και τα άτομα τείνουν να δημιουργήσουν πιο πυκνές δομές για να ελαττωθεί η απόσταση ισορροπίας του δεσμού και κατά συνέπεια η ενέργεια του συστήματος). Μόνο το Πολώνιο (Po) από τα μέταλλα κρυσταλλώνεται σε αυτή τη δομή. Όπως όμως θα διαπιστωθεί σε επόμενα κεφάλαια στην απλή κυβική διάταξη κρυσταλλώνονται συχνά ανιόντα και κατιόντα σε ενώσεις. Εάν 1 mol ατόμων Πολωνίου (Po), ατομικής ακτίνας R, κρυσταλλωθεί στην απλή κυβική διάταξη ποιος θα είναι o ο συνολικός όγκος του υλικού; Το 1 mole ατόμων είναι προφανές ότι περιέχει Ν ΑV άτομα ακτίνας R, με όγκο Ν ΑV 4 3 πr3 Εάν αυτά τοποθετηθούν σε απλή κυβική διάταξη, θα καταλάβουν μόνο 52.36% του συνολικού όγκου της διάταξης, ο οποίος κατά συνέπεια θα είναι: V tot = Ν ΑV 4 3 πr3 APF SC = Ν 4 ΑV 3 πr3 π 6 = 8Ν ΑV R
11 Μια άλλη προσέγγιση είναι να θεωρηθεί ότι 1 mol (Ν ΑV άτομα) σε διάταξη SC δημιουργεί Ν ΑV κυψελίδες ( 1 άτομο ανά κυψελίδα) με όγκο (2R) 3 η κάθε μια και συνολικό όγκο: V tot = N AV (2R) 3 = 8Ν ΑV R 3 Η χωροκεντρωμένη κυβική δομή As θεωρήσουμε τώρα επίσης μια απλή επίπεδη διάταξη σαν κι αυτή της Εικόνας 3.2 με τη διαφορά ότι τα άτομα δεν εφάπτονται αλλά η απόσταση των κέντρων δύο διαδοχικών ατόμων είναι α>2r (Εικόνα 3.11). Ας θεωρήσουμε τώρα μια δεύτερη ίδια επίπεδη διάταξη η οποία τοποθετείται με τέτοιο τρόπο πάνω στην πρώτη ώστε το κάθε άτομο να βρίσκεται στο διάκενο που σχηματίζεται από τα τέσσερα άτομα της πρώτης στοιβάδας. Εν συνεχεία τοποθετούμε μια τρίτη ίδια στοιβάδα ακριβώς όπως η πρώτη, μια τέταρτη ακριβώς όπως η δεύτερη κ.ο.κ.. Η τρισδιάστατη δομή που προκύπτει με αυτόν τον τρόπο είναι του τύπου ΑΒΑΒΑΒ και ονομάζεται χωροκεντρωμένη κυβική (body centered cubic, ΒCC). Εικόνα 3.11: Ανάπτυξη της κυβικής χωροκεντρωμένης δομής από απλές επίπεδες στοιβάδες. Αριθμός ένταξης Ο αριθμός ένταξης ενός οποιουδήποτε ατόμου στη χωροκεντρωμένη κυβική διάταξη είναι 8 (κάθε άτομο εφάπτεται με τα τέσσερα άτομα της αμέσως υπερκείμενης στοιβάδας και με τα τέσσερα άτομα της στοιβάδας που βρίσκεται ακριβώς από κάτω. Στο ίδιο επίπεδο, επειδή α>2r δεν υπάρχουν εφαπτόμενα άτομα). 3.11
12 Εικόνα 3.12: Το πλέγμα της χωροκεντρωμένης κυβικής διάταξης και ο αριθμός ένταξης ενός τυχαίου ατόμου Η μοναδιαία κυψελίδα (α) (β) (γ) (δ) (ε) Εικόνα 3.13: Η συμβατική αναπαράσταση της μοναδιαίας κυψελίδας της χωροκεντρωμένης κυβικής διάταξης και η ακριβής αναπαράσταση σύμφωνα με το μοντέλο των εφαπτόμενων σφαιρών. Η συμβατική αναπαράσταση της μοναδιαίας κυψελίδας είναι αυτή που παρουσιάζεται στην Εικόνα 3.13(ε). Από την ακριβή αναπαράσταση όμως του μοντέλου των εφαπτόμενων σφαιρών (Εικόνα 3.13(γ)) προκύπτει ότι η κυψελίδα περιέχει ένα άτομο στο κέντρο της που ανήκει εξολοκλήρου σε αυτήν και δεν επιμερίζεται με καμιά παρακείμενη κυψελίδα, και 8 άτομα στις κορυφές της τα οποία (όπως και στην περίπτωση της απλής κυβικής δομής) ανήκουν μόνο κατά το 1/8 στην υπό θεώρηση κυψελίδα, δεδομένου ότι επιμερίζονται εξίσου σε οκτώ κυψελίδες με κοινή κορυφή. Κατά συνέπεια ο συνολικός αριθμός των ατόμων στη BCC κυψελίδα είναι 2 (δηλαδή 1+8x1/8 =2). 3.12
13 Η σχέση μεταξύ μήκους ακμής κυψελίδας (α) και ατομικής ακτίνας R διεξάγεται εύκολα αν ληφθεί υπόψη ότι τα άτομα εφάπτονται κατά μήκος της διαγωνίου του κύβου (Εικόνα 3.14). Βάσει αυτής της παρατήρησης μπορούμε να γράψουμε: Εικόνα 3.14: Στη χωροκεντρωμένη κυβική διάταξη τα άτομα εφάπτονται κατά μήκος της διαγωνίου της μοναδιαίας κυψελίδας a 3 = 4R a = 4 R > 2R (3.6) 3 Συντελεστής ατομικής πλήρωσης Ο APF της διάταξης μπορεί με τα υπάρχοντα δεδομένα να υπολογιστεί πολύ εύκολα: APF ΒCC = n at. V at. = (1+(8 1 8 )) 4 3 πr3 = π 3 V tot. ( 4 3 R) (3.7) Συγκρίνοντας με την απλή κυβική διάταξη παρατηρούμε πως η «πυκνότητα» της χωροκεντρωμένης κυβικής δομής είναι μεγαλύτερη από την «πυκνότητα» της απλής κυβικής. Αυτό σημαίνει ότι στη χωροκεντρωμένη κυβική δομή γίνεται πιο αποτελεσματική χρήση του χώρου. Υλικά Α Σ Κ Η Σ Η 3. 3 Στη δομή ΒCC κρυσταλλώνονται πολλά μέταλλα όπως το Βολφράμιο (W), το Χρώμιο (Cr), το Ταντάλιο (Ta) και το Μολυβδαίνιο (Μο). Ίσως το πιο γνωστό μέταλλο της δομής BCC είναι ο α-σίδηρος (α-fe), που είναι η κρυσταλλογραφική ονομασία του μαλακού Σιδήρου. Η ατομική ακτίνα του Σιδήρου είναι R Fe =0.124 nm (Πίνακας 2.1, σελ.30). Πόσες μοναδιαίες κυψελίδες και πόσα άτομα Σιδήρου υπάρχουν σε ένα κυβικό εκατοστό καθαρού κρυσταλλικού υλικού H σταθερά της μοναδιαίας κυψελίδας δίνεται από τη σχέση (3.6): α α Fe = 4 R 3 Fe = nm = nm 3 Ο αριθμός των κυψελίδων (Ν cell ) που υπάρχουν σε όγκο V=1cm 3 καθαρού κρυσταλλικού υλικού είναι: Ν cell = V V cell = V = 1 cm 3 a 3 = cells a Fe ( ) 3cm3 cell 3.13
14 Εφόσον κάθε κυψελίδα περιέχει δύο άτομα Σιδήρου ο συνολικός αριθμός των ατόμων Σιδήρου θα είναι: Ν at = 2 at. cell cells = atoms Δηλαδή κάτι ~7 φορές λιγότερα άτομα από αυτά που περιέχονται σε 1 mole Σιδήρου Οι προηγούμενες δύο δομές που μελετήθηκαν (SC και ΒCC) αναπτύχθηκαν από απλές (ή σχεδόν απλές) επίπεδες διατάξεις. Στις επόμενες παραγράφους θα συζητηθούν δύο ιδιαίτερα ενδιαφέρουσες δομές που προκύπτουν από επίπεδες διατάξεις υψηλής πυκνότητας. H κυβική δομή υψηλής πυκνότητας Ας θεωρήσουμε μια επίπεδη διάταξη υψηλής πυκνότητας παρόμοια με αυτήν που παρουσιάστηκε στην Εικόνα 3.4 (Εικόνα 3.15α). Εικόνα 3.15: Ανάπτυξη της κυβικής δομής υψηλής πυκνότητας από επίπεδες στοιβάδες υψηλής πυκνότητας. Μεταξύ των ατόμων μπορούμε να διακρίνουμε δύο ομάδες διάκενων (χρωματισμένα στην εικόνα μπλέ και κόκκινα αντίστοιχα). Δεν υπάρχει καμιά ουσιαστική διαφορά μεταξύ των δύο αυτών ομάδων και ο διαχωρισμός γίνεται καθαρά για χωροταξικούς λόγους. Τοποθετούμε τώρα πάνω σε αυτήν μια ίδια επίπεδη διάταξη ατόμων (δηλαδή υψηλής πυκνότητας), όχι όμως ακριβώς πάνω στην πρώτη, αλλά πάνω από μια ομάδα διάκενων (π.χ. έστω πάνω από αυτήν που είναι χρωματισμένη κόκκινη) (Εικόνα 3.15β). Παρατηρούμε ότι η δεύτερη ομάδα διάκενων (μπλε) συνεχίζει να είναι ακάλυπτη. Τοποθετούμε τώρα μια τρίτη ίδια επίπεδη στοιβάδα υψηλής πυκνότητας ακριβώς πάνω από τη δεύτερη (μπλε) ομάδα διάκενων (Εικόνα 3.15γ), και η διαδικασία αυτής της τριπλής αλληλουχίας επίπεδων στοιβάδων υψηλής πυκνότητας επαναλαμβάνεται. Η δομή ή η τρισδιάστατη διάταξη που προκύπτει με αυτόν τον τρόπο είναι του τύπου ABCABC (επαναλαμβανόμενη τριπλή αλληλουχία επίπεδων στοιβάδων) και ονομάζεται κυβική δομή υψηλής πυκνότητας (cubic closed packed, CCP). Αριθμός Ένταξης 3.14
15 Ο αριθμός ένταξης ενός οποιουδήποτε ατόμου κυβικής διάταξης υψηλής πυκνότητας είναι 12. Κάθε άτομο εφάπτεται με έξι άτομα του επιπέδου του (επίπεδη στοιβάδα υψηλής πυκνότητας), με τρία άτομα της στοιβάδας που βρίσκεται ακριβώς από επάνω του και με τρία άτομα της στοιβάδας που βρίσκεται ακριβώς από κάτω του (Εικόνα 3.16). Εικόνα 3.16: O αριθμός ένταξης στην κυβική διάταξη υψηλής πυκνότητας Μοναδιαία κυψελίδα Ο ορισμός και ο σχηματισμός της μοναδιαίας κυψελίδας στην διάταξη CCP παρουσιάζεται στην Εικόνα Εικόνα 3.17: O σχηματισμός της μοναδιαίας κυψελίδας στην δομή CCP (αριστερά: μοντέλο εφαπτόμενων σφαιρών, δεξιά: μοντέλο διευρυμένων διατομικών αποστάσεων Αποδεικνύεται ότι η δομή μπορεί να περιγραφεί πλήρως από την εδροκεντρωμένη κυβική κυψελίδα (face centered cubic, FCC), δηλαδή από έναν κύβο με άτομα στις κορυφές και στα μέσα των εδρών του κύβου. Αξίζει να σημειωθεί ότι στη δομή CCP η μοναδιαία κυψελίδα δεν έχει τον ίδιο (x,y,z) προσανατολισμό με τη διάταξη των επίπεδων στοιβάδων (όπως συμβαίνει στις άλλες δομές που μελετήθηκαν). Έτσι η συμβατική αναπαράσταση της μοναδιαίας κυψελίδας είναι συνήθως αυτή της Εικόνας 3.18β. Θα πρέπει να είναι γνωστό ότι αυτή ουσιαστικά προκύπτει με περιστροφή της διάταξης των στοιβάδων κατά 45 ο C (Εικόνα 3.18α) καθώς και ότι αν επιθυμείται η διάκριση στοιβάδων στη μοναδιαία κυψελίδα αυτή θα πρέπει να γίνει διαγώνια (Εικόνα 3.18γ) και όχι όπως ακριβώς παριστάνεται η κυψελίδα. 3.15
16 Εικόνα 3.18: Η σχέση μεταξύ διάταξης επίπεδων στοιβάδων ψηλής πυκνότητας και μοναδιαίας κυψελίδας στην κυβική δομή ψηλής πυκνότητας Στην Εικόνα 3.19 παρουσιάζεται εποπτικά ο σχηματισμός της συμβατικής FCC κυψελίδας στη CCP διάταξη. (α) (β) (γ) 3.16
17 (δ) (ε) Εικόνα 3.19: Η συμβατική αναπαράσταση της μοναδιαίας κυψελίδας της κυβικής διάταξης υψηλής πυκνότητας και η ακριβής αναπαράσταση σύμφωνα με το μοντέλο των εφαπτόμενων σφαιρών. Από την Εικόνα 3.19(γ) προκύπτει ότι η μοναδιαία κυψελίδα της δομής CCP περιέχει (κατά τα γνωστά) οκτώ άτομα στις κορυφές του κύβου τα οποία επιμερίζονται εξίσου σε οκτώ παρακείμενες κυψελίδες και κατά συνέπεια ανήκουν κατά το 1/8 σε αυτήν, και επιπρόσθετα έξι άτομα στα κέντρα των εδρών του κύβου τα οποία επιμερίζονται εξίσου σε δύο κυψελίδες και κατά συνέπεια ανήκουν κατά το ½ σε αυτήν. Συνολικά η FCC κυψελίδα περιέχει (8 1 8 ) + (6 1 2 ) = 4 άτομα. Η σχέση μεταξύ της ακμής (α) της FCC κυψελίδας και της ακτίνας R των ατόμων της Εικόνα 3.20: Στην κυβική διάταξη υψηλής τα άτομα εφάπτονται κατά μήκος των διαγωνίων των εδρών της μοναδιαίας FCC κυψελίδας CCP διάταξης προκύπτει αν λάβουμε υπόψη τον τρόπο δημιουργίας της δομής (π.χ. Εικόνα 3.17) και παρατηρήσουμε ότι τα άτομα εφάπτονται κατά μήκους των διαγωνίων των εδρών του κύβου (Εικόνα 3.20). Με βάση αυτήν την παρατήρηση έχουμε: a 2 = 4R a = 4 R (3.8) 2 Συντελεστής ατομικής πλήρωσης Με γνωστές όλες τις απαραίτητες πληροφορίες μπορούμε πλέον να προβούμε στον υπολογισμό του APF της CCP διάταξης: APF CCP = n at. V at. = [(8 1 8 )+(6 1 2 )] 4 3 πr3 = π V tot. ( 4 2 R) (3.9) 3.17
18 Δηλαδή η CCP είναι η πιο πυκνή διάταξη από όσες μελετήθηκαν έως τώρα και εκμεταλλεύεται το 74% του συνολικού όγκου το οποίο καταλαμβάνεται από άτομα (το υπόλοιπο 26% παραμένει κενό). Υλικά Α Σ Κ Η Σ Η 3. 4 Ο Χρυσός (Au), o Λευκόχρυσος (Pt) και ο Άργυρος (Ag) κρυσταλλώνονται στη δομή CCP. Επίσης πολλά ευρέως χρησιμοποιούμενα μέταλλα όπως ο Χαλκός (Cu), το Νικέλιο (Ni), το Αργίλιο (Al) και ο Μόλυβδος (Pb) κρυσταλλώνονται σε αυτή τη δομή και περιγράφονται από την FCC κυψελίδα. O a-σίδηρος (α-fe) της ΒCC δομής σε θερμοκρασίες μεγαλύτερες των 912 ο C μετασχηματίζεται στον γ-σίδηρο (γ-fe) της CCP δομής. Σημείωση: Γενικότερα το φαινόμενο κατά το οποίο ένα υλικό εμφανίζεται σε περισσότερες από μια διακριτές κρυσταλλικές καταστάσεις ονομάζεται αλλοτροπία (εάν πρόκειται για μονοστοιχειακό υλικό) ή πολυμορφισμός (εάν πρόκειται για ένωση) (allotropy, polymorphism). Μια άλλη γνωστή περίπτωση αλλοτροπίας είναι οι κρυσταλλικές δομές του άνθρακα στο διαμάντι και στο γραφίτη που θα συζητηθούν σε επόμενο κεφάλαιο. Να υπολογιστεί εάν αυτός ο μετασχηματισμός του Σιδήρου συνοδεύεται από μεταβολή όγκου και πόση. Για την περίπτωση του ΒCC υλικού έχουμε: ΑPF BCC = n at. V at. V tot.βcc (3.10) ενώ για την περίπτωση του CCP υλικού με την FCC κυψελίδα έχουμε: APF CCP = n at. V at. V tot.ccp (3.11) Εφόσον πρόκειται για τον ίδιο αριθμό ατόμων Σιδήρου με τον ίδιο (στερεό) όγκο τότε στις σχέσεις (3.10) και (3.11) το n at. V at. είναι το ίδιο. Διαιρώντας κατά μέλη έχουμε: V tot.ccp V tot.βcc = ΑPF BCC APF CCP = V tot.fcc = 0.92V tot.βcc Δηλαδή κατά τον BCC CCP μετασχηματισμό θα επέλθει μείωση όγκου κατά 8%. Μια άλλη (πιο επίπονη) προσέγγιση θα ήταν να θεωρήσουμε έναν αριθμό ατόμων Σιδήρου Ν Fe τα οποία αν κρυσταλλωθούν στη BCC δομή θα δημιουργήσουν Ν Fe 2 κυψελίδες με συνολικό όγκο: V tot.bcc = N Fe 2 ( 4 3 R Fe) 3. Στη συνέχεια τα ίδια άτομα αναδιατάσσονται στην CCP δομή με συνολικό όγκο V tot.ccp = N Fe 4 ( 4 2 R Fe) 3. Συνεπώς 3.18
19 V tot.ccp V tot.bcc = N Fe 4 ( R Fe) N Fe 2 ( 4 3 R Fe) 3 = 1 2 ( 3 2 ) 3 = 0.92 Η εξαγωνική δομή υψηλής πυκνότητας Θεωρούμε μια επίπεδη διάταξη υψηλής πυκνότητας και στη συνέχεια μια δεύτερη επίπεδη διάταξη υψηλής πυκνότητας η οποία τοποθετείται σε μία ομάδα διάκενων, όπως ακριβώς και κατά τη δημιουργία της δομής CCP (Εικόνα 3.21). Εικόνα 3.21: Ανάπτυξη της εξαγωνικής δομής υψηλής πυκνότητας από επίπεδες στοιβάδες υψηλής πυκνότητας. Στη συνέχεια, η τρίτη επίπεδη στοιβάδα τοποθετείται ακριβώς όπως και η πρώτη στοιβάδα. Η δομή ή η τρισδιάστατη διάταξη είναι του τύπου ΑΒΑΒΑΒ και ονομάζεται εξαγωνική δομή υψηλής πυκνότητας (hexagonal closed packed, HCP), (Εικόνα 3.22). Αριθμός ένταξης Μοναδιαία κυψελίδα Είναι προφανές ότι όπως και στην περίπτωση της δομής CCP έτσι και στη δομή HCP ο αριθμός ένταξης Εικόνα 3.22: Η δομή HCP ως τρισδιάστατη διάταξη επίπεδων στοιβάδων είναι 12. Κάθε άτομο της διάταξης εφάπτεται με έξι άτομα στο επίπεδό του, με τρία άτομα που βρίσκονται στο επίπεδο ακριβώς από πάνω και με τρία στο επίπεδο που βρίσκεται ακριβώς από κάτω (π.χ. Εικόνα 3.16). Ο σχηματισμός της μοναδιαίας κυψελίδας στη διάταξη HCP παρουσιάζεται στην Εικόνα
20 Εικόνα 3.23: O σχηματισμός της μοναδιαίας κυψελίδας στην δομή HCP (αριστερά: μοντέλο εφαπτόμενων σφαιρών, δεξιά: μοντέλο διευρυμένων διατομικών αποστάσεων Πρόκειται για μια εξαγωνική μοναδιαία κυψελίδα οι βάσεις της οποίας είναι κανονικά εξάγωνα πλευράς α=2r και ύψους c. (α) (β) (γ) (δ) (ε) Εικόνα 3.24: Η συμβατική αναπαράσταση της μοναδιαίας κυψελίδας της εξαγωνικής διάταξης υψηλής πυκνότητας και η ακριβής αναπαράσταση σύμφωνα με το μοντέλο των εφαπτόμενων σφαιρών. Η συμβατική και συνήθης αναπαράσταση της μοναδιαίας κυψελίδας της HCP διάταξης είναι αυτή που παρουσιάζεται στην Εικόνα 3.24(ε). Όπως όμως και στις προηγούμενες περιπτώσεις έτσι και εδώ θα πρέπει να είναι γνωστό ότι αυτή προκύπτει από τη συμβατική (δηλαδή με διευρυμένες διατομικές αποστάσεις μεταξύ των κέντρων των σφαιρών) 3.20
21 παράσταση του πλέγματος (Εικόνα 3.24(β)). Κατά συνέπεια η ακριβής αναπαράσταση της μοναδιαίας κυψελίδας είναι αυτή που παρουσιάζεται στην Εικόνα 3.24(γ). Ο αριθμός των ατόμων ανά μοναδιαία εξαγωνική κυψελίδα μπορεί να υπολογιστεί από την Εικόνα 3.24(γ). Κάθε άτομο στις κορυφές των εξαγώνων επιμερίζεται σε έξι κυψελίδες (τρείς στο επίπεδό του και τρείς στο αμέσως υπερκείμενο επίπεδο) και κατά συνέπεια ανήκει κατά το 1/6 στην υπό θεώρηση κυψελίδα (Εικόνα 3.25(α) ). Συνολικά υπάρχουν 12 άτομα ανά έξι στις κορυφές των εξαγώνων των δύο βάσεων της κυψελίδας. Επιπρόσθετα υπάρχουν τρία άτομα (της ενδιάμεσης στοιβάδας) τα οποία ανήκουν εξ ολοκλήρου στην υπό θεώρηση κυψελίδα και δεν επιμερίζονται. Τέλος, υπάρχουν και 2 άτομα που βρίσκονται στα κέντρα των βάσεων και τα οποία, κατά τα γνωστά, επιμερίζονται μεταξύ δύο κυψελίδων. Συνολικά ο αριθμός των ατόμων ανά μοναδιαία εξαγωνική κυψελίδα είναι: Εικόνα 3.25: Σχηματική παράσταση διάταξης κυψελίδων για την πλήρωση του χώρου ( ) (2 1 2 ) = 6 άτομα. Σημείωση: Όπως θα αναφερθεί και στη συνέχεια αυτού του Κεφαλαίου όλες οι μοναδιαίες κυψελίδες ουσιαστικά είναι παραλληλεπίπεδα (όπως άλλωστε και αυτές των διατάξεων SC, BCC και CCP). Τα άτομα στις κορυφές παραλληλεπιπέδων επιμερίζονται στην υπό θεώρηση κυψελίδα κατά το 1/8 διότι η επαναλαμβανόμενη διάταξη παραλληλεπιπέδων για την πλήρωση του χώρου είναι τέσσερα με κοινή κορυφή ανά επίπεδο (Εικόνα 3.25(β)), δηλαδή στο χώρο οκτώ με κοινή κορυφή. Η εξαγωνική κυψελίδα είναι η μοναδική περίπτωση κυψελίδας όπου για την πλήρωση του χώρου απαιτείται επαναλαμβανόμενη διάταξη τριών με κοινή κορυφή ανά επίπεδο (Εικόνα 3.25(α)), δηλαδή στο χώρο έξι με κοινή κορυφή. Κατά συνέπεια αποτελεί και τη μοναδική περίπτωση κυψελίδας όπου τα άτομα κορυφής επιμερίζονται σ αυτήν κατά το 1/6. Όσον αφορά άτομα που ανήκουν εξ ολοκλήρου σε μια κυψελίδα επειδή βρίσκονται στο εσωτερικό της ή άτομα που βρίσκονται σε κέντρα εδρών οι επιμερισμοί όγκου για όλες τις περιπτώσεις και χωρίς καμιά εξαίρεση είναι 1 και 1/2 αντίστοιχα. Η μοναδιαία κυψελίδα της δομής HCP για την οποία έγινε λόγος στα προηγούμενα δεν είναι η μοναδική. Συνήθως αυτή αποκαλείται και εκτεταμένη εξαγωνική κυψελίδα. Αυτό για να γίνει διάκριση από την επίσης πολύ συχνά χρησιμοποιούμενη βασική εξαγωνική κυψελίδα (Εικόνα 3.26). Ουσιαστικά η βασική κυψελίδα είναι το 1/3 της εκτεταμένης. Αποδεικνύεται ότι απλή επανάληψη και αυτής της κυψελίδας στο χώρο δίνει επίσης τη δομή HCP. H μόνη διαφορά είναι ότι ο αριθμός των ατόμων που περιέχει είναι κατά τα γνωστά 8x1/8 + 1=2 και όχι 6 (προφανώς θα πρέπει να περιέχει το 1/3 των ατόμων και του όγκου της εκτεταμένης). Το πλεονέκτημα είναι ότι θεωρώντας τη βασική κυψελίδα η οποία είναι παραλληλεπίπεδο η δομή HCP δεν διαφοροποιείται από τις άλλες δομές των υλικών των οποίων οι μοναδιαίες κυψελίδες είναι επίσης παραλληλεπίπεδα. 3.21
22 Εικόνα 3.26: H βασική μοναδιαία κυψελίδα της δομής HCP Σε αντίθεση με τις προηγούμενες περιπτώσεις κυβικών κυψελίδων για την περιγραφή των οποίων ήταν απαραίτητη η γνώση μόνο μίας διάστασης (εφόσον ήταν κυβικές), για την ποσοτική περιγραφή της εξαγωνικής κυψελίδας απαιτούνται δύο παράμετροι α και c. H σχέση μεταξύ της παραμέτρου α και της ακτίνας των ατόμων της διάταξης (α=2r) διεξάγεται εύκολα από τον τρόπο ανάπτυξης της δομής. Στην περίπτωση της ιδανικής εξαγωνικής δομής αποδεικνύεται πως c a = 8 3 c = 2R 8 3 Συντελεστής ατομικής πλήρωσης Με γνωστές τις διαστάσεις της ιδανικής κυψελίδας και τον αριθμό των ατόμων ακτίνας R που περιέχει, ο APF μπορεί σχετικά εύκολα να υπολογιστεί είτε από την εκτεταμένη είτε από τη βασική κυψελίδα. Το εμβαδόν Ε της βάσης της εκτεταμένης εξαγωνικής κυψελίδας το οποίο απαρτίζεται από έξι ισόπλευρα τρίγωνα πλευράς 2R θα είναι: Ε = 6 1 2R R 3 = 6 3R2 2 O όγκος V tot. της εκτεταμένης ιδανικής εξαγωνικής κυψελίδας είναι: V tot. = 6 3R 2 2R 8 3 = 24 2R2 και ο συντελεστής ατομικής πλήρωσης: APF HCP = n at. V at. = πr2 V tot.ηcp 24 2R 2 = π Παρατηρούμε ότι οι δομές CCP και ΗCP έχουν τον ίδιο APF, δηλαδή την ίδια αποτελεσματικότητα εκμετάλλευσης του χώρου. Αυτό είναι αναμενόμενο γιατί και στις δύο περιπτώσεις πρόκειται για διατάξεις αποτελούμενες από επίπεδες στοιβάδες υψηλής 3.22
23 πυκνότητας και διαφέρουν μόνο ως προς την ομάδα των «διάκενων» στην οποία τοποθετούνται. Με ελαφρά μετακίνηση π.χ. της τρίτης στοιβάδας της FCC δομής από τη μία ομάδα διάκενων στην άλλη, λαμβάνουμε την HCP δομή χωρίς μεταβολή όγκου. Υλικά Αντιπροσωπευτικά παραδείγματα γνωστών μετάλλων που κρυσταλλώνονται στη δομή HCP είναι το Κάδμιο (Cd), το Μαγνήσιο (Mg), το Τιτάνιο (Ti) και ο Ψευδάργυρος (Zn). Σημείωση: Στο σημείο αυτό κρίνεται σκόπιμο να γίνει αναφορά στην ακριβή χρήση των όρων. Η απλή κυβική διάταξη ή δομή (SC διάταξη) περιγράφεται από την απλή κυβική κυψελίδα (SC κυψελίδα). Η χωροκεντρωμένη κυβική διάταξη (BCC διάταξη) περιγράφεται από την χωροκεντρωμένη κυβική κυψελίδα (BCC κυψελίδα). Η εξαγωνική διάταξη υψηλής πυκνότητας (HCP διάταξη) περιγράφεται από την εξαγωνική κυψελίδα. Η κυβική διάταξη υψηλής πυκνότητας (CCP διάταξη) περιγράφεται από την εδροκεντρωμένη κυβική κυψελίδα (FCC κυψελίδα). Πολύ συχνά σε βιβλία υλικών γίνεται, καταχρηστικά, λόγος για FCC δομή ή για CCP κυψελίδα. Ο όρος FCC αποδίδεται κυρίως στον τύπο της κυψελίδας ενώ η διάταξη ονομάζεται κυβική υψηλής πυκνότητας (CCP). Στον Πίνακα 3.1 παρουσιάζονται συνοπτικά τα κύρια χαρακτηριστικά των βασικών δομών που μελετήθηκαν στις προηγούμενες παραγράφους. 3.23
24 Ονομασία και τύπος Διάταξης Μοναδιαία κυψελίδα ΑPF CN Νat. α=f(r) Απλή κυβική (SC) (AAAA) π a = 2R Po Χωροκεντρωμένη κυβική (ΒCC) (ABABAB) π α = 4 3 R α-fe, W, Cr, Ta, Mo Κυβική υψηλής πυκνότητας (CCP) (ABCABC) π a = 4 2 R γ-fe, Cu, Ni, Al, Pb, Au, Pt, Ag
25 Εξαγωνική υψηλής πυκνότητας (HCP) (ABABAB) Πίνακας 3.1: Συνοπτικά στοιχεία βασικών μεταλλικών δομών π (2) a = 2R c = 2R 8 3 Cd, Mg, Ti, Zn 3.25
26 3.3 Τα κρυσταλλικά συστήματα Οι δομές που μελετήθηκαν κάπως διεξοδικά στις προηγούμενες παραγράφους είναι δομές πολλών υλικών υψηλού τεχνολογικού ενδιαφέροντος. Επιπρόσθετα οι ίδιες διατάξεις απαντώνται σε ανιόντα ή κατιόντα για τη διαμόρφωση της δομής των κρυσταλλικών ενώσεων. Δεν είναι όμως οι μόνες, υπάρχουν πολύ περισσότερες. Σε αυτή την παράγραφο θα γίνει μια γενική αναφορά στα βασικά χαρακτηριστικά όλων των μορφών και σε αυτό το πλαίσιο θα ενταχθούν και οι δομές για τις οποίες έγινε συζήτηση. Οι τρισδιάστατες περιοδικές διατάξεις σημείων (ατόμων) στο χώρο π.χ. σαν κι αυτές που απεικονίζονται στις Εικόνες 3.7, 3.12, 3.17 και 3.23 ονομάζονται πλέγματα (lattices). Κάθε κρυσταλλικό υλικό χαρακτηρίζεται από το δικό του πλέγμα. Τα σημεία του πλέγματος στα οποία υπάρχουν άτομα, ονομάζονται πλεγματικά σημεία (lattice sites). Για την περιγραφή κάθε τέτοιας περιοδικής διάταξης ατόμων στο χώρο αρκεί (όπως είδαμε) ο ορισμός της μοναδιαίας κυψελίδας, ενός δηλαδή, εν γένει, παραλληλεπιπέδου επανάληψη του οποίου να γεμίζει το χώρο. Κατά συνέπεια για τον βασικό ορισμό του πλέγματος απαιτείται ο ορισμός του παραλληλεπιπέδου ο οποίος επιτυγχάνεται πλήρως με τον ορισμό των τριών διαστάσεών του στους και τον ορισμό των γωνιών μεταξύ των αξόνων. Το σύστημα των αξόνων δεν είναι εξ ορισμού ορθοκανονικό αλλά ταυτίζεται με τις κατευθύνσεις των τριών διαστάσεων της μοναδιαίας κυψελίδας (Εικόνα 3.27). Kατά κανόνα a,b,c είναι οι διαστάσεις της μοναδιαίας κυψελίδας στους άξονες x, y και z, αντίστοιχα, ενώ α,β,γ είναι οι γωνίες μεταξύ των αξόνων που δεν περιλαμβάνουν τον x, y, και z, αντίστοιχα. Ο τύπος του παραλληλεπιπέδου (της μοναδιαίας κυψελίδας) που περιγράφει το πλέγμα και εκφράζει τη συμμετρία του, ορίζει το κρυσταλλικό σύστημα του υλικού. Έχει βρεθεί ότι οι συμμετρίες των Εικόνα 3.27: Ο ορισμός της μοναδιαίας πλεγμάτων των μετάλλων κυψελίδας ενός πλέγματος εκφράζονται από επτά τύπους παραλληλεπιπέδων οι οποίοι ορίζουν και τα επτά κρυσταλλικά συστήματα. Στην Εικόνα 3.28 που ακολουθεί παρουσιάζονται αυτοί οι επτά τύποι συμμετρίας (τα επτά κρυσταλλικά συστήματα) με την ονομασία του καθενός και τις χαρακτηριστικές σχέσεις μεταξύ των διαστάσεων της κυψελίδας και των γωνιών της. Είναι προφανές ότι οι διατάξεις SC, BCC και CCP έχουν όλες κυβική συμμετρία και ανήκουν στο κυβικό κρυσταλλικό σύστημα ενώ η διάταξη HCP έχει εξαγωνική συμμετρία και ανήκει στο εξαγωνικό κρυσταλλικό σύστημα.
27 Εικόνα 3.28: Οι επτά τύποι συμμετρίας ή αλλιώς τα επτά κρυσταλλικά συστήματα των μεταλλικών δομών (το εξαγωνικό σύστημα αναφέρεται με την βασική κυψελίδα)
28 Πέρα από τη συμμετρία (το κρυσταλλικό σύστημα) υπάρχουν και τα σημεία του πλέγματος τα οποία και για πλέγματα της ίδιας συμμετρίας μπορεί να διαφέρουν. Για παράδειγμα τόσο η SC, η BCC και η CCP διάταξη είναι κυβικής συμμετρίας αλλά περιγράφονται από διαφορετικές μοναδιαίες κυψελίδες δηλαδή με διαφορετική «χωροθέτηση» ατόμων η κάθε μια. Το θέμα είναι γενικότερο και σε κάθε κρυσταλλικό σύστημα θα μπορούσαν να εμφανισθούν κυψελίδες απλές (δηλαδή με άτομα μόνο στις κορυφές), χωροκεντρωμένες (δηλαδή με άτομα στις κορυφές και στο κέντρο), εδροκεντρωμένες (δηλαδή με άτομα στις κορυφές και στα κέντρα των εδρών) καθώς και μερικά εδροκεντρωμένες (δηλαδή με άτομα στις κορυφές και στα κέντρα δύο αντικείμενων εδρών). Σημείωση: Οι προαναφερόμενοι τύποι κυψελίδων έχουν και διεθνείς συμβολισμούς. Η απλή κυψελίδα συμβολίζεται με P, η χωροκεντρωμένη με Ι και η πλήρως εδροκεντρωμένη με F. Oι μερικά εδροκεντρωμένες κυψελίδες μπορεί γενικά να είναι τριών ειδών και συμβολίζονται με Α,Β,C ανάλογα με το αν οι αντικείμενες δύο έδρες που περιέχουν άτομα στα κέντρα τους είναι κατά μήκος του άξονα x,y και z, αντίστοιχα. Όσον αφορά τον αριθμό των ατόμων ισχύουν όσα αναφέρθηκαν σε προηγούμενες παραγράφους και σύμφωνα με τα οποία η απλή κυψελίδα περιέχει ένα άτομο, η χωροκεντρωμένη δύο, η εδροκεντρωμένη 4 και η μερικά εδροκεντρωμένη 2. Θα περίμενε λοιπόν κανείς για κάθε ένα από τα επτά κρυσταλλικά συστήματα 6 διαφορετικούς τύπους κυψελίδων, δηλαδή συνολικά 42 διαφορετικούς τύπους κυψελίδων. Λόγοι συμμετρίας όμως (που ξεφεύγουν αρκετά από το σκοπό του μαθήματος και στους οποίους δεν θα γίνει αναφορά) απαγορεύουν την εμφάνιση κάποιων τύπων σε πολλά κρυσταλλικά συστήματα έτσι ώστε τελικά να έχουμε τους γνωστούς 14 τύπους πλεγμάτων του Bravais, οι οποίοι παρουσιάζονται στον Πίνακα 3.2 και στην Εικόνα Πίνακας 3.2: Οι 14 τύποι πλεγμάτων Bravais Κρυσταλλικό σύστημα Τρικλινές (1) Μονοκλινές (2) Επιτρεπόμενες κυψελίδες Απλή (P) Απλή (P), Μερικά Εδροκεντρωμένη (C) Ορθορομβικό (4) Απλή (P), Χωροκεντρωμένη (Ι), Εδροκεντρωμένη (F), Μερικά Εδροκεντρωμένη (C) Ρομβοεδρικό (1) Εξαγωνικό (1) Τετραγωνικό (2) Απλή (P) Χωροκεντρωμένη (Ι) Απλή (P), Χωροκεντρωμένη (Ι) Κυβικό (3) Απλή (P), Xωροκεντρωμένη (I), Εδροκεντρωμένη (F)
29 Τρικλινές Τριγωνικό Εξαγωνικό Κυβικό Ορθορομβικό Μονοκλινές Τετραγωνικό Εικόνα 3.29: Οι μοναδιαίες κυψελίδες των 14 τύπων πλεγμάτων Bravais 3.4 Η θεωρητική πυκνότητα των τέλειων και καθαρών μετάλλων Η θεωρητική πυκνότητα των μετάλλων (ρ th ) είναι αυτή που υπολογίζουμε με βάση τα δεδομένα της τέλειας κρυσταλλικής δομής όπως αυτή έχει περιγραφεί στις προηγούμενες παραγράφους. Στη βάση μιας μοναδιαίας κυψελίδας με όγκο V cell και συνολική μάζα m cell η οποία συνίσταται από τη μάζα αριθμού ατόμων n at. μάζας m at. το κάθε ένα: ρ th = m cell V cell = n at.m at. V cell (3.12) Στο κεφάλαιο 2 (σχέση (2.3), σελ.18) αναφέρθηκε πως η μάζα ενός ατόμου Χ ισούται με το λόγο της ατομικής μάζας του στοιχείου Α Χ προς τη σταθερά του Αvogadro. Kατά συνέπεια η σχέση (3.12) μπορεί να γραφεί:
30 ρ th.χ = n at. Α Χ Ν ΑV = n ata x V cell Ν ΑV V cell (3.13) Ο όγκος της σταθεράς της κυψελίδας υπολογίζεται από τις διαστάσεις της (a,b,c) oι οποίες είτε υπολογίζονται από την (γνωστή) ατομική ακτίνα του στοιχείου είτε είναι γνωστές επειδή έχουν προσδιοριστεί πειραματικά (π.χ. με τη μέθοδο της περίθλασης ακτίνων x, που θα αναφερθεί στο επόμενο Κεφάλαιο). Η θεωρητική πυκνότητα δεν είναι η μέγιστη πυκνότητα ενός υλικού, εν προκειμένω, μετάλλου. Είναι η πυκνότητα που αντιστοιχεί στην τέλεια και ιδανική κρυσταλλική δομή. Όπως θα δούμε σε επόμενα Κεφάλαια οι πραγματικές δομές των υλικών παρουσιάζουν διάφορες ατέλειες και αποκλίσεις από την ιδανική δομή, μια εκ των οποίων συνίσταται στην παρουσία ξένων ατόμων άλλων στοιχείων (ιχνοστοιχείων) τα οποία ενδεχομένως να έχουν μεγαλύτερη (ή μικρότερη) μάζα από τα άτομα του υπό θεώρηση υλικού. Σε αυτήν την περίπτωση και αν οι μεταβολές που προκαλεί η πρόσμιξη στον όγκο της μοναδιαίας κυψελίδας δεν είναι σημαντικές, η πυκνότητα του υλικού μπορεί να είναι μεγαλύτερη (ή μικρότερη) από την θεωρητική. Α Σ Κ Η Σ Η 3. 5 Ο α-σίδηρος κρυσταλλώνεται στην κυβική χωροκεντρωμένη δομή και η ατομική του ακτίνα είναι R Fe = nm. Να υπολογιστεί η θεωρητική του πυκνότητα και ο αριθμός των ατόμων Σιδήρου σε 1 m 3 κρυσταλλικού υλικού (Α Fe =55.85 g mol -1 ) Η διάσταση α της μοναδιαίας κυψελίδας της BCC διάταξης είναι: α = 4 R 3 Fe = nm = nm 3 Εφαρμόζοντας τώρα κατάλληλα την σχέση (3.13) έχουμε: ρ th,fe = 2 atoms g cell mol atoms mol ( ) 3cm3 cell = 7.88 g cm 3 O αριθμός των ατόμων σε ένα κυβικό μέτρο μπορεί να υπολογιστεί ακριβώς όπως στην Άσκηση 3.3. Με γνωστή όμως τη θεωρητική πυκνότητα μπορεί επίσης να υπολογιστεί και από τη σχέση: Ν Fe = 7.88 g cm 3 atoms g cm3 mol m 3 = 8.5 atoms 1028 m 3 mol στην οποία τα gr ανά cm 3 (ή m 3 ) που εκφράζονται από την πυκνότητα μετατράπηκαν σε mole (διαιρώντας με την ατομική μάζα) και στη συνέχεια σε άτομα (πολλαπλασιάζοντας με τη σταθερά του Avogadro). 3.28
31 ΑΣΚ Η Σ Η 3. 6 Το Νικέλιο (Ni) κρυσταλλώνεται στο εδροκεντρωμένο κυβικό σύστημα. Εάν η θεωρητική του πυκνότητα είναι g cm -3 να υπολογιστούν οι διαστάσεις της μοναδιαίας κυψελίδας και η ατομική ακτίνα του Νικελίου (Α Νi =58.71 g mol -1 ) Mε τα γνωστά δεδομένα της κρυσταλλικής δομής του Νικελίου και κατάλληλη εφαρμογή της σχέσης (3.13) έχουμε: ρ th.ni = n ata Ni V Ν ΑV V cell = n ata Ni 4 at. = cell g mol cell Ν ΑV ρ th.ni at. mol g cm 3 V cell = cm 3 Πρόκειται για κυψελίδα κυβικής συμμετρίας οπότε θα ισχύει: V cell = a 3 3 a = V cell 3 = cm 3 = cm = pm Από τη σχέση που συνδέει τη σταθερά κυψελίδας με την ατομική ακτίνα στην FCC δομή έχουμε: α = 4 a 2 R R = 2 4 = 352.4pm 2 R = pm = nm 4 Θα πρέπει να είναι σαφής η διαφορά μεταξύ της θεωρητικής πυκνότητας του υλικού που είναι μέγεθος διαστατοποιημένο και εκφράζεται σε g cm -3 και της πυκνότητας διάταξης (APF) που εκφράζει την αποτελεσματικότητα της διάταξης των ατόμων για την πλήρωση του χώρου, είναι μέγεθος αδιάστατο και η μεγαλύτερη τιμή που μπορεί να πάρει είναι 1. Υψηλό ΑPF δεν συνεπάγεται και ψηλή πυκνότητα όπως και ψηλή πυκνότητα δεν συνεπάγεται ψηλό ΑPF. H μάζα των ατόμων της μοναδιαίας κυψελίδας είναι καθοριστικής σημασίας στον προσδιορισμό της ποιότητας ενώ ο αριθμός τους είναι καθοριστικής σημασίας στον προσδιορισμό του APF. Στο σημείο αυτό αξίζουν κάποια σχόλια σχετικά με την Εικόνα 1.5 (Κεφ.1, σελ.4). Τα μέταλλα έχουν κατά κανόνα μεγαλύτερες πυκνότητες από τα άλλα υλικά επειδή είναι σε θέση τα άτομά τους να στοιβάζονται στο χώρο σε πυκνές διατάξεις. Σε αυτό βοηθάει πολύ και ο ανισότροπος χαρακτήρας του μεταλλικού δεσμού ο οποίος δεν θέτει χωροταξικούς περιορισμούς και η έντασή του δεν εξαρτάται από την κατεύθυνση. Στα κεραμικά υλικά από την άλλη μεριά (π.χ. οξείδια) τα σχετικά μεγάλης ατομικής μάζας κεραμικά κατιόντα «διαλύονται» στην κρυσταλλική δομή από το σχετικά μικρής ατομικής μάζας οξυγόνο. Αυτό οδηγεί σε χαμηλής πυκνότητας κατιοντικές διατάξεις και κατά συνέπεια κατά κανόνα σε πυκνότητες μικρότερες από ότι τα μέταλλα (ο ιοντικός δεσμός των περισσοτέρων κεραμικών είναι επίσης ανισότροπος). Τέλος, τα πολυμερή υλικά έχουν τις μικρότερες πυκνότητες διότι αφενός αποτελούνται από σχετικά ελαφρά στοιχεία (π.χ. C, H, O) αφετέρου πολλά από αυτά είναι άμορφα και όχι κρυσταλλικά με αποτέλεσμα τη χαμηλή εκμετάλλευση του χώρου στη διάταξη. Τα σύνθετα υλικά εμφανίζουν ενδιάμεσες πυκνότητες 3.29
32 δεδομένου ότι αυτές μπορούν να θεωρηθούν ως σταθμισμένοι μέσοι όροι των υλικών των κύριων κατηγοριών από τις οποίες αποτελούνται. 3.5 Η έννοια του μορίου και του χημικού τύπου στα τέλεια και καθαρά μέταλλα Ας θεωρήσουμε ένα αέριο π.χ. το οξυγόνο με χημικό τύπο (Ο 2 ). Ως γνωστόν η μικρότερη μονάδα (η οποία έχει τις ιδιότητες του αερίου) επανάληψη της οποίας (χωρίς κανόνες) αναπαραγάγει τη δομή του αερίου είναι το διατομικό μόριο του οξυγόνου (Εικόνα 3.30).Ο χημικός τύπος Ο 2 μας πληροφορεί ότι η βασική μονάδα αποτελείται από δύο άτομα οξυγόνου. Η βασική μονάδα δεν θα μπορούσε να είναι το ένα άτομο οξυγόνου διότι επανάληψή του στο χώρο δεν δίνει κατ αρχήν αέριο με τις ίδιες φυσικές και χημικές ιδιότητες. Επίσης δεν θα μπορούσε, για τον ίδιο λόγο, να είναι το Ο 3. Ίδια είναι η κατάσταση και με άλλα αέρια όπως π.χ. CH 4 ή υγρά π.χ. Η 2Ο. Ο χημικός τύπος δίνει την αναλογία των στοιχείων στο μόριο εκφραζόμενη με τους μικρότερους δυνατούς ακεραίους. Στα κρυσταλλικά μονοστοιχειακά στερεά π.χ. στα καθαρά μέταλλα ο χημικός τύπος του υλικού (π.χ. Fe, Ni, Cu) έχει λίγο διαφορετική σημασία από ότι στα μοριακά υλικά. Η βασική μονάδα η οποία επαναλαμβανόμενη αναπαραγάγει το στερεό δεν είναι απλά το άτομο Fe αλλά το σύνολο των δύο ατόμων Σιδήρου διατεταγμένα στο χώρο σύμφωνα με τους κανόνες της BCC συμμετρίας, η μοναδιαία κυψελίδα. Θα μπορούσαμε να ορίσουμε τον χημικό τύπο της μοναδιαίας κυψελίδας ως Fe 2 η για τον FCC Χαλκό Cu 4. O χημικός τύπος όμως εκφράζει την αναλογία ανά άτομο οπότε διαιρώντας με το 2 ή με το 4 αντίστοιχα έχουμε τελικά τον συμβολισμό Fe ή Cu. Αυτό θα μπορούσε να ερμηνευθεί πως στο υλικό Fe (ή Cu) ανά άτομο υλικού έχουμε ένα άτομο Σιδήρου (ή Χαλκού). Θα μπορούσαμε να πούμε ότι ο χημικός τύπος υπεισέρχεται στην κυψελίδα 2 φορές (για τον BCC Σίδηρο) ή 4 φορές (για τον FCC χαλκό). Ορισμένα πλεονεκτήματα αυτής της ερμηνείας θα διαφανούν όταν γίνει συζήτηση για κράματα μετάλλων και για ενώσεις. Αν θεωρήσουμε π.χ. ένα κράμα (αντικατάστασης) Cu-Ni της δομής FCC στο οποίο τα μισά άτομα είναι Cu και τα άλλα μισά Ni, τότε ο μέσος χημικός τύπος της κυψελίδας θα είναι Cu 2 Ni 2 (η FCC κυψελίδα εξακολουθεί να απαρτίζεται από τέσσερα άτομα) και ανάγοντας ανά άτομο διαιρώντας με το 4 έχουμε τον χημικό τύπο του υλικού, του κράματος Cu 0.5 Ni 0.5 ο οποίος εξακολουθεί να υπεισέρχεται στην κυψελίδα 4 φορές. Ανά «άτομο υλικού» έχουμε 0.5 άτομα Χαλκού και 0.5 Νικελίου. Οι δεκαδικοί αριθμοί δεν θα πρέπει να ξενίζουν γιατί έχουν λογιστική και όχι φυσική σημασία (τα άτομα στα πλαίσια αυτού του μαθήματος δεν τεμαχίζονται). Συμβολισμοί Κεφαλαίου APF: Συντελεστής ατομικής πλήρωσης (Atomic Packing Factor) 3.30
33 Α Χ : Ατομική μάζα στοιχείου Χ b: Διάσταση μοναδιαίας κυψελίδας (στον y-άξονα) ΒCC: Χωροκεντρωμένη κυβική διάταξη (Body Centered Cubic) c: Διάσταση μοναδιαίας κυψελίδας (στον z-άξονα) CCP: Κυβική διάταξη υψηλής πυκνότητας CN: Αριθμός ένταξης (Coordination Number) CP: Επίπεδης διάταξης ψηλής πυκνότητας (Closed Packing) D: Διάμετρος ατόμου Ε: Εμβαδόν FCC: Εδροκεντρώμενη κυβική κυψελίδα (Face Centered Cubic) HCP: Eξαγωνική διάταξη υψηλής πυκνότητας (Hexagonal Closed Packed) m cell : Μάζα μοναδιαίας κυψελίδας N AV : Σταθερά Avogadro = x mol -1 Ν cell : Αριθμός μοναδιαίων κυψελίδων Ν, N at, n at. : Αριθμός ατόμων R: Ακτίνα ατόμου SC: Απλή κυβική διάταξη (Simple Cubic) r: Διατομική απόσταση r 0 : Aπόσταση ισορροπίας δεσμού δύο ατόμων S at. : Αποτύπωμα προβολής ατόμου σε επιφάνεια S tot. : Συνολική επιφάνεια SP: Απλής επίπεδης διάταξης ατόμων (Simple Packing) V: Ογκος V at. : Όγκος ατόμου V cell : Όγκος μοναδιαίας κυψελίδας V tot : Συνολικός όγκος V cell : Όγκος μοναδιαίας κυψελίδας W: Συνολική ενέργεια συστήματος δύο ατόμων α,a: Διάσταση μοναδιαίας κυψελίδας (στον x-άξονα) π: Σταθερά ~3.14 ρ th : Θεωρητική πυκνότητα ΣΕΚ: Συντελεστής επιφανειακής κάλυψης Ερωτήσεις Κατανόησης 1. Ποια σχέση θα συνδέει τους συντελεστές επιφανειακής κάλυψης (ΣΕΚ) απλών επίπεδων διατάξεων ατόμων ακτίνας R/2, R και 2R ; 2. Ποια σχέση συνδέει τους συντελεστές επιφανειακής κάλυψης (ΣΕΚ) επίπεδων διατάξεων ψηλής πυκνότητας ατόμων ακτίνας R/2, R και 2R ; 3. Ένα mole Πολωνίου (Po) κρυσταλλώνεται ιδανικά στην απλή κυβική δομή. Ο αριθμός των μοναδιαίων κυψελίδων που θα σχηματιστούν θα είναι: 3.31
34 Α: Ν ΑV B: Ν ΑV 2 Γ: Ν ΑV 4 Δ: Ν ΑV 8 4. Ένα μέταλλο Χ με ατομική μάζα Α Χ (g mol -1 ) κρυσταλλώνεται στην απλή κυβική δομή. Ποια θα είναι η μάζα του μετάλλου σε μία μοναδιαία κυψελίδα; 5. Υποθέστε έναν αριθμό ατόμων κάποιου μετάλλου που κρυσταλλώνεται στην απλή κυβική δομή και στη συνέχεια μέσω κάποιου μετασχηματισμού ο ίδιος αριθμός κρυσταλλώνεται στη χωροκεντρωμένη κυβική δομή. Ο αριθμός των κυψελίδων: Α: θα υποδιπλασιαστεί Γ: θα διπλασιαστεί Β: θα παραμείνει ο ίδιος Δ: θα τετραπλασιαστεί 6. Υποθέστε έναν αριθμό ατόμων κάποιου μετάλλου που κρυσταλλώνεται στη χωροκεντρωμένη κυβική δομή και στη συνέχεια μέσω κάποιου μετασχηματισμού ο ίδιος αριθμός κρυσταλλώνεται στην εδροκεντρωμένη κυβική δομή. Ο αριθμός των κυψελίδων: Α: θα υποδιπλασιαστεί Γ: θα διπλασιαστεί Β: θα παραμείνει ο ίδιος Δ: θα τετραπλασιαστεί 7. Για συγκεκριμένη ατομική ακτίνα R ποια μοναδιαία κυψελίδα θα έχει τη μεγαλύτερη σταθερά α; Α: η απλή Β: η χωροκεντρωμένη Γ: η εδροκεντρωμένη 8. Ο Χαλκός βρίσκεται στην τέταρτη περίοδο και στην ΙΒ ομάδα του περιοδικού πίνακα. Ο Χρυσός βρίσκεται στην έκτη περίοδο της ίδιας ομάδας. Και τα δύο μέταλλα κρυσταλλώνονται στη δομή CCP. Ποιο από τα δύο θα περιμένατε να έχει τη μεγαλύτερη σταθερά μοναδιαίας κυψελίδας; Α: Ο Χαλκός Β: Ο Χρυσός Γ: ίδια 9. Ο Σίδηρος βρίσκεται στην VΙΙΙ ομάδα και στην 4 η περίοδο στον περιοδικό πίνακα. Το Βανάδιο βρίσκεται στην VB ομάδα της ίδιας περιόδου. Και τα δύο μέταλλα κρυσταλλώνονται στη χωροκεντρωμένη κυβική δομή. Ποιο από τα δύο θα περιμένατε να έχει τη μεγαλύτερη σταθερά μοναδιαίας κυψελίδας; Α: Ο Σίδηρος Β: Το Βανάδιο Γ: ίδια 10. Η εκτεταμένη εξαγωνική κυψελίδα περιέχει: Α: 2 Β: 3 Γ: 4 Δ: 6 βασικές εξαγωνικές κυψελίδες 3.32
35 11. Ο συντελεστής ατομικής πλήρωσης (APF) της εκτεταμένης εξαγωνικής κυψελίδας σε σχέση με αυτόν της βασικής εξαγωνικής κυψελίδας είναι: Α: τριπλάσιος Β: ίσος με το 1/3 του Γ: ίσος 12. Από τα επτά κρυσταλλικά συστήματα αυτά που έχουν και τις τρεις γωνίες ορθές είναι: Α: 1 Β: 2 Γ: 3 Δ: Το μοναδικό κρυσταλλικό σύστημα που εμφανίζει P, I, F και C τύπου κυψελίδες είναι το: Α: κυβικό Β: τετραγωνικό Γ: ορθορομβικό Δ: εξαγωνικό 14. Σε ποιο κρυσταλλικό σύστημα ανήκει το υλικό η μοναδιαία κυψελίδα του οποίου παρουσιάζεται στην Εικόνα, και τι είδους κυψελίδα είναι; 15. Ένα μέταλλο που κρυσταλλώνεται στην απλή κυβική δομή με ΑPF=0.52 θα έχει πάντα μικρότερη πυκνότητα από ένα μέταλλο που κρυσταλλώνεται στην κυβική δομή υψηλής πυκνότητας με APF=0.74 Α: Σωστό Β: Λάθος 16. Εάν ένα μέταλλο ατομικής μάζας Α, κρυσταλλώνεται σε κυψελίδα με σταθερές α,b,c (α=β=γ=90 ο ) εντός της οποίας υπάρχουν n άτομα μετάλλου, τότε η θεωρητική πυκνότητα θα δίνεται από τη σχέση: Α: ρ th = n A N AV a b c B: ρ th = n N AV (a b c) A Γ: ρ th = n A Ν ΑV (a b c) 17. Εάν ρ th (g cm -3 ) είναι η θεωρητική πυκνότητα ενός καθαρού κρυσταλλικού μετάλλου ατομικής A (g mol -1 ) και Ν ΑV είναι η σταθερά του Avogadro (mol -1 ), τότε ο αριθμός των ατόμων Ν σε 1 m 3 κρυσταλλικού υλικού θα είναι: Α: Ν = ρ th A N AV B: Ν = ρ th N AV A 10 6 Γ: Ν = ρ th A N AV 10 6 Δ: Ν = ρ th N AV A
36 18. Φανταστείτε μια εκτεταμένη εξαγωνική μοναδιαία κυψελίδα ενός μετάλλου Α στην οποία τα τρία άτομα της μεσαίας στοιβάδας έχουν αντικατασταθεί από άτομα κάποιου άλλου μετάλλου Β. Ουσιαστικά έχει αντικατασταθεί: Α: το 25% Β: το 50% Γ: το 75% των ατόμων 19. Κατ αναλογία με τα ιδανικά αέρια ο γραμμομοριακός όγκος (ο όγκος ενός mole υλικού) των καθαρών κρυσταλλικών μετάλλων είναι σταθερός. Α: Σωστό Β: Λάθος 20. Κατά την στερεοποίηση με ψύξη κάποιου τήγματος σε ποια περίπτωση οι πιθανότητες είναι περισσότερες να σχηματισθεί κρυσταλλικό και όχι άμορφο στερεό; όταν οι δεσμοί μεταξύ των ατόμων του σχηματιζόμενου στερεού είναι ιοντικοί ή ομοιοπολικοί; 21. Ζωγραφίστε μια FCC κυψελίδα. Στη συνέχεια επιλέξτε ένα άτομο μιας κορυφής και προσδιορίστε ποια από τα υπάρχοντα άτομα της εν λόγω κυψελίδας είναι πλησιέστεροι γείτονές του (δηλαδή εφάπτονται). Προβλήματα για εξάσκηση 1. Θεωρείστε άτομα Σιδήρου με ακτίνα R Fe =124 pm διατεταγμένα σε επίπεδη διάταξη α) απλή και β) υψηλής πυκνότητας. Για συνολική επιφάνεια διάταξης 5 mm 2 να υπολογιστεί και για τις δύο περιπτώσεις α) και β). 3.34
37 Ι) Η επιφάνεια που είναι ακάλυπτη από άτομα Σιδήρου ΙΙ) Ο αριθμός των ατόμων Σιδήρου Απάντηση: α) mm 2, β) mm 2 Απάντηση: α) Fe atoms, β) Fe atoms ΙΙΙ) Στην περίπτωση της επίπεδης διάταξης υψηλής πυκνότητας από πόσες βασικές μονάδες Β (Εικόνα 3.5) απαρτίζεται η διάταξη; Απάντηση: βασικές μονάδες Β ΙV) Tα άτομα ενός mole Fe διατάσσονται σε επίπεδη διάταξη ψηλής πυκνότητας. Πόση θα είναι η συνολική επιφάνεια της διάταξης; Απάντηση: ~32081 m 2 2. Διαθέτουμε 1 mol ατόμων κάποιου στοιχείου με ατομική ακτίνα 0.14 nm. α)πόσες κυψελίδες θα δημιουργηθούν εάν το υλικό αυτό κρυσταλλωθεί στην απλή κυβική δομή; β) Πόσες κυψελίδες θα δημιουργηθούν εάν το υλικό κρυσταλλωθεί στην χωροκεντρωμένη κυβική δομή; γ) Ποιος θα είναι ο όγκος του στερεού κρυσταλλικού υλικού σε κάθε περίπτωση; Απάντηση: α) 6.023x10 23 cells, β) x10 23 cells γ) SC: cm 3, BCC: 10.18cm 3 3. Να αποδειχθεί ότι στην ιδανική εξαγωνική δομή όπου α=2r, ισχύει η σχέση c a = 8 3 Βοηθητική Υπόδειξη: Να θεωρήσετε το κανονικό τετράπλευρο ΑΒΓΔ της βασικής εξαγωνικής κυψελίδας, πλευράς α και ύψους ΑΗ=c/2 4. Θεωρώντας τη βασική εξαγωνική κυψελίδα να αποδειχθεί ότι ο συντελεστής ατομικής πλήρωσης είναι APF HCP = π To Νιόβιο (Nb, A Nb = g mol -1 ) κρυσταλλώνεται στη χωροκεντρωμένη κυβική δομή. Εάν η θεωρητική του πυκνότητα είναι g cm -3 να υπολογιστούν οι διαστάσεις της μοναδιαίας κυψελίδας του Νιοβίου. Απάντηση: α=330 pm 3.35
38 6. Να υπολογιστεί η σταθερά της χωροκεντρωμένης κυβικής κυψελίδας του Μολυβδαινίου γνωρίζοντας ότι η ιοντική ακτίνα του Μολυβδαινίου είναι 1.36 Å. Απάντηση: α=3.14 Å 7. To κρυσταλλικό σύστημα του ασβεστίου (Ca, A Ca =40.08 g mol -1 ) είναι το εδροκεντρωμένο κυβικό (CCP). Η σταθερά της κυβικής κυψελίδας είναι 557 pm. Nα υπολογιστεί η ατομική ακτίνα του ασβεστίου και η θεωρητική του πυκνότητα. Απάντηση: a=197 pm, ρ th, Ca =1.54 g cm To τιτάνιο (Ti, A Ti =47.88 g mol-1) κρυσταλλώνεται στην εξαγωνική δομή υψηλής πυκνότητας (ΗCP). Η μοναδιαία κυψελίδα του τιτανίου δεν είναι ιδανική αλλά έχει λόγο c/a = Εάν η ατομική ακτίνα του τιτανίου είναι nm, να υπολογιστούν ο όγκος της μοναδιαίας εκτεταμένης κυψελίδας και η θεωρητική του πυκνότητα. Απάντηση: V cell =9.91x10-23 cm 3, ρ th, Ti =4.81 g cm Η κρυσταλλική δομή του ψευδαργύρου (Ζn, A Zn =65.39 g mol -1 ) είναι η εξαγωνική υψηλής πυκνότητας (HCP) με λόγο διαστάσεων κυψελίδας c/a = H θεωρητική πυκνότητα του ψευδαργύρου είναι 7.13 g cm -3. Nα υπολογιστεί η ατομική ακτίνα του ψευδαργύρου. Απάντηση: R Zn =0.133 nm 10. Στον παρακάτω πίνακα δίνονται κάποια μέταλλα, η ατομική τους μάζα, η θεωρητική πυκνότητα και η ατομική ακτίνα. Να προσδιοριστεί σε ποια από τις δομές SC, BCC και FCC κρυσταλλώνονται. Mέταλλο Ατομική μάζα (g mol -1 ) Θεωρητική πυκνότητα (g cm -3 ) Aτομική Ακτίνα (nm) Χαλκός (Cu) Μολυβδαίνιο (Mo) Χρώμιο (Cr) Νικέλιο (Ni) Απάντηση: Χαλκός (FCC), Μολυβδαίνιο (ΒCC), Χρώμιο (ΒCC), Νικέλιο (FCC) 11. Να υπολογιστεί ο αριθμός των ατόμων αλουμινίου (Αl, Α Αl =26.98 g mol -1 ) που βρίσκονται σε ένα cm 3 καθαρού κρυσταλλικού αλουμινίου δομής FCC και ατομικής ακτίνας nm Απάντηση: ~9.88 x 10 7 άτομα 3.36
39 12. Tο Πρωτακτίνιο (Pa, A Pa = g mol -1 ), στοιχείο της σειράς των Ακτινιδίων, κρυσταλλώνεται σε χωροκεντρωμένη τετραγωνική κυψελίδα με διαστάσεις α= nm και c= nm. Nα υπολογιστεί η μάζα (m cell ) της μοναδιαίας κυψελίδας σε γραμμάρια, ο όγκος (V cell ) της μοναδιαίας κυψελίδας σε κυβικά εκατοστά και η θεωρητική πυκνότητα του υλικού σε g cm -3. Απάντηση: m cell = 7.67 x g, V cell =4.99x10-23 cm 3, ρ th = g cm Ένα υποθετικό μεταλλικό υλικό κρυσταλλώνεται στην απλή κυβική δομή. Κάτω από συγκεκριμένες συνθήκες λαμβάνει χώρα κρυσταλλογραφικός μετασχηματισμός και η ίδια μάζα μετάλλου κρυσταλλώνεται στη χωροκεντρωμένη κυβική δομή. Εν συνεχεία και κάτω από άλλες συνθήκες λαμβάνει πάλι χώρα κρυσταλλογραφικός μετασχηματισμός και η ίδια μάζα μετάλλου κρυσταλλώνεται στην εδροκεντρωμένη κυβική δομή. Να υπολογιστούν α) η ποσοστιαία μεταβολή όγκου κατά τον πρώτο μετασχηματισμό β) η ποσοστιαία μεταβολή όγκου κατά τον δεύτερο μετασχηματισμό γ) η ποσοστιαία ολική μεταβολή όγκου (υποτίθεται ότι η ατομική ακτίνα παραμένει σταθερή και είναι ανεξάρτητη της κρυσταλλικής δομής). Βοηθητική υπόδειξη: Α τρόπος: Σε κάθε κρυσταλλική δομή μπορεί να υπολογιστεί ο θεωρητικός αριθμός κυψελίδων που θα προέκυπτε. Ο όγκος της κάθε κυψελίδας μπορεί να συνεχεία να υπολογιστεί συναρτήσει της ατομικής ακτίνας. Β τρόπος: Για κάθε κρυσταλλικό σύστημα, ο ολικός όγκος πολλαπλασιαζόμενος με τον αριθμό ατομικής πλήρωσης προφανώς θα ισούται με τον όγκο της σταθερής και αμετάβλητης μάζας του υλικού. Απάντηση: α) ελάττωση ~23%, β) ~ελάττωση 8.1% γ)~ ελάττωση 29.3% 14. To Ίνδιο (In, A In =114.8 g mol -1 ) κρυσταλλώνεται στο τετραγωνικό σύστημα με διαστάσεις κυψελίδας α = και c= pm. Εάν η θεωρητική του πυκνότητα είναι 7.29 g cm -3 να προσδιοριστεί ο τύπος της κυψελίδας. Απάντηση: n=2, τετραγωνική χωροκεντρωμένη 15. Ο κασσίτερος (Sn) έχει μοναδιαία κυψελίδα τετραγωνικής συμμετρίας με διαστάσεις α = και c = nm, αντίστοιχα. Εάν η πυκνότητά του είναι 7.30 g cm -3, η ατομική του ακτίνα nm και η ατομική του μάζα A Sn = g mol -1 να υπολογιστεί ο αριθμός των ατόμων ανά κυψελίδα και συντελεστής ατομικής πλήρωσης, ΑPF. Απάντηση: n = 4 άτομα/κυψελίδα, APF Sn = To θείο (S) έχει μοναδιαία κυψελίδα ορθορομβικής συμμετρίας με διαστάσεις α= pm, b = pm και c = pm. H θεωρητική πυκνότητα του θείου είναι 2.09 g cm -3 και η ατομική του ακτίνα 100 pm. Εάν η ατομική μάζα του θείου είναι Α S =32.06 g cm -3 να υπολογιστεί ο συντελεστής ατομικής πλήρωσης APF. Απάντηση: APF S =
40 17. Το ιώδιο (Ι) έχει ορθορομβική μοναδιαία κυψελίδα με σταθερές α = nm, b = nm και c = nm. Εάν ο συντελεστής ατομικής πλήρωσης APF είναι και η ατομική του ακτίνα nm να υπολογιστεί ο αριθμός των ατόμων ανά μοναδιαία κυψελίδα. Εάν η ατομική μάζα του ιωδίου είναι Α Ι = g mol -1 να υπολογιστεί η θεωρητική πυκνότητα του ιωδίου. Απάντηση: n = 8 άτομα/κυψελίδα, ρ th =4.96 g cm Το Ζιρκόνιο (Zr) κρυσταλλώνεται στην εξαγωνική δομή υψηλής πυκνότητας και έχει θεωρητική πυκνότητα 6.51 g cm -3. α) Να υπολογιστεί ο όγκος της μοναδιαίας κυψελίδας σε m 3 β) Εάν ο λόγος c/α είναι να υπολογιστούν οι τιμές του c και του α. Απάντηση: V cell = m 3 /unit cell, α=0.323nm, c=0.515 nm 19. Ένα διστοιβαδικό μεταλλικό έλασμα αποτελείται από δύο καθαρά μέταλλα Α και Β όπως δείχνει το διπλανό σχήμα. Το μέταλλο Α έχει ατομική μάζα ΜΒ Α δομή bcc και ατομική ακτίνα nm. To μέταλλο Β έχει ατομική μάζα ΜΒ Β δομή ιδανική hcp και ατομική ακτίνα nm. Nα δοθεί η σχέση για τον υπολογισμό της ολικής πυκνότητας ρ th, oλ του ελάσματος (σε g cm -3 ) σαν συνάρτηση της ατομικής μάζας των μετάλλων (σε g mol -1 ). (Θεωρείται ότι δεν υπάρχει ασυνέχεια στη διεπιφάνεια που να έχει σοβαρή επίδραση στην πυκνότητα). Απάντηση: 0.046MB MB th, o A B 20. Στη διπλανή εικόνα Α παρουσιάζεται η μοναδιαία Α κυψελίδα κάποιου υλικού. α) Σε ποιο κρυσταλλικό σύστημα ανήκει το υλικό; β) Πως ονομάζεται η συγκεκριμένη μοναδιαία κρυσταλλική κυψελίδα γ) Εάν το συγκεκριμένο υλικό έχει ατομική μάζα 141 g mol -1 να υπολογιστεί η μάζα της μοναδιαίας κυψελίδας (m cell ) και η θεωρητική του πυκνότητα δ) Εάν η τυπική μοναδιαία κυψελίδα του υλικού δεν είναι αυτή του σχήματος Α αλλά αυτή του σχήματος Β, όπου το άτομο του κέντρου της κυψελίδας έχει αντικατασταθεί από το άτομο κάποιου άλλου στοιχείου με ατομική μάζα 80 g mol -1 ποια θα είναι τώρα η μάζα της μοναδιαίας κυψελίδας και η θεωρητική πυκνότητα του υλικού; 3.38
Καταστάσεις της ύλης. Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο.
 Καταστάσεις της ύλης Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο. Υγρά: Τάξη πολύ µικρού βαθµού και κλίµακας-ελκτικές δυνάµεις-ολίσθηση. Τα µόρια βρίσκονται
Καταστάσεις της ύλης Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο. Υγρά: Τάξη πολύ µικρού βαθµού και κλίµακας-ελκτικές δυνάµεις-ολίσθηση. Τα µόρια βρίσκονται
ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ
 ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ 1. ΓΕΝΙΚΑ Από τις καταστάσεις της ύλης τα αέρια και τα υγρά δεν παρουσιάζουν κάποια τυπική διάταξη ατόμων, ενώ από τα στερεά ορισμένα παρουσιάζουν συγκεκριμένη διάταξη ατόμων
ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ 1. ΓΕΝΙΚΑ Από τις καταστάσεις της ύλης τα αέρια και τα υγρά δεν παρουσιάζουν κάποια τυπική διάταξη ατόμων, ενώ από τα στερεά ορισμένα παρουσιάζουν συγκεκριμένη διάταξη ατόμων
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 4 η σειρά διαφανειών Δημήτριος Λαμπάκης Ορισμός και ιδιότητες των μετάλλων Τα χημικά στοιχεία διακρίνονται σε μέταλλα (περίπου 70 τον αριθμό)
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 4 η σειρά διαφανειών Δημήτριος Λαμπάκης Ορισμός και ιδιότητες των μετάλλων Τα χημικά στοιχεία διακρίνονται σε μέταλλα (περίπου 70 τον αριθμό)
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 3 η σειρά διαφανειών Δημήτριος Λαμπάκης Τύποι Στερεών Βασική Ερώτηση: Πως τα άτομα διατάσσονται στο χώρο ώστε να σχηματίσουν στερεά? Τύποι Στερεών
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 3 η σειρά διαφανειών Δημήτριος Λαμπάκης Τύποι Στερεών Βασική Ερώτηση: Πως τα άτομα διατάσσονται στο χώρο ώστε να σχηματίσουν στερεά? Τύποι Στερεών
Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ. Ενότητα 2: Κρυσταλλική Δομή των Μετάλλων. Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών
 Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ Ενότητα 2: Κρυσταλλική Δομή των Μετάλλων Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ Ενότητα 2: Κρυσταλλική Δομή των Μετάλλων Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Γραπτή εξέταση προόδου «Επιστήμη και Τεχνολογία Υλικών Ι»-Νοέμβριος 2015
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) ΘΕΜΑ 1 ο (15 Μονάδες) Πόσα γραμμάρια καθαρού κρυσταλλικού
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) ΘΕΜΑ 1 ο (15 Μονάδες) Πόσα γραμμάρια καθαρού κρυσταλλικού
Γραπτή εξέταση προόδου «Επιστήμη και Τεχνολογία Υλικών Ι»-Νοέμβριος 2016
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Θέμα 1: Ερωτήσεις (10 Μονάδες) (Σύντομη αιτιολόγηση.
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Θέμα 1: Ερωτήσεις (10 Μονάδες) (Σύντομη αιτιολόγηση.
Επιστήμη των Υλικών. Πανεπιστήμιο Ιωαννίνων. Τμήμα Φυσικής
 Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Κρυσταλλικά Συστήματα Κυβικό Εξαγωνικό Τετραγωνικό Ρομβοεδρικό ή Τριγωνικό Ορθορομβικό Μονοκλινές Τρικλινές Κρυσταλλική δομή των
Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Κρυσταλλικά Συστήματα Κυβικό Εξαγωνικό Τετραγωνικό Ρομβοεδρικό ή Τριγωνικό Ορθορομβικό Μονοκλινές Τρικλινές Κρυσταλλική δομή των
ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ
 Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 6 η Ενότητα ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Δημήτριος Λαμπάκης Τύποι Στερεών Βασική Ερώτηση: Πως τα άτομα
Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 6 η Ενότητα ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Δημήτριος Λαμπάκης Τύποι Στερεών Βασική Ερώτηση: Πως τα άτομα
Γραπτή εξέταση «Επιστήμη και Τεχνολογία Υλικών Ι»-Σεπτέμβριος 2016
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) ΘΕΜΑ 1 ο (30 Μονάδες) Στην εικόνα δίνονται οι επίπεδες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) ΘΕΜΑ 1 ο (30 Μονάδες) Στην εικόνα δίνονται οι επίπεδες
Η Δομή των Μετάλλων. Γ.Ν. Χαϊδεμενόπουλος, Καθηγητής
 Η Δομή των Μετάλλων Γ.Ν. Χαϊδεμενόπουλος, Καθηγητής Τρισδιάστατο Πλέγμα Οι κυψελίδες των 14 πλεγμάτων Bravais (1) απλό τρικλινές, (2) απλό μονοκλινές, (3) κεντροβασικό μονοκλινές, (4) απλό ορθορομβικό,
Η Δομή των Μετάλλων Γ.Ν. Χαϊδεμενόπουλος, Καθηγητής Τρισδιάστατο Πλέγμα Οι κυψελίδες των 14 πλεγμάτων Bravais (1) απλό τρικλινές, (2) απλό μονοκλινές, (3) κεντροβασικό μονοκλινές, (4) απλό ορθορομβικό,
Γραπτή εξέταση προόδου στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Νοέμβριος 2017
 Γραπτή εξέταση προόδου στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Νοέμβριος 017 Ερώτηση 1 (5 μονάδες ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ
Γραπτή εξέταση προόδου στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Νοέμβριος 017 Ερώτηση 1 (5 μονάδες ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις
 Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Γραπτή εξέταση προόδου στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Ιανουάριος 2018
 Γραπτή εξέταση προόδου στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Ιανουάριος 018 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ
Γραπτή εξέταση προόδου στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Ιανουάριος 018 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ
 ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 5 Δομή ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Κρυσταλλικά υλικά Άμορφα υλικά Κρύσταλλος είναι ένα υλικό που παρουσιάζει τρισδιάστατη περιοδική τάξη ατόμων,
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 5 Δομή ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Κρυσταλλικά υλικά Άμορφα υλικά Κρύσταλλος είναι ένα υλικό που παρουσιάζει τρισδιάστατη περιοδική τάξη ατόμων,
Τελική γραπτή εξέταση «Επιστήμη και Τεχνολογία Υλικών Ι»-Ιανουάριος 2017
 Τελική γραπτή εξέταση «Επιστήμη και Τεχνολογία Υλικών Ι»-Ιανουάριος 017 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ
Τελική γραπτή εξέταση «Επιστήμη και Τεχνολογία Υλικών Ι»-Ιανουάριος 017 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ
Θεωρία Μοριακών Τροχιακών (ΜΟ)
 Θεωρία Μοριακών Τροχιακών (ΜΟ) Ετεροπυρηνικά διατομικά μόρια ή ιόντα (πολικοί δεσμοί) Το πιο ηλεκτραρνητικό στοιχείο (με ατομικά τροχιακά χαμηλότερης ενεργειακής στάθμης) συνεισφέρει περισσότερο στο δεσμικό
Θεωρία Μοριακών Τροχιακών (ΜΟ) Ετεροπυρηνικά διατομικά μόρια ή ιόντα (πολικοί δεσμοί) Το πιο ηλεκτραρνητικό στοιχείο (με ατομικά τροχιακά χαμηλότερης ενεργειακής στάθμης) συνεισφέρει περισσότερο στο δεσμικό
Θεµατικό Περιεχόµενο Μαθήµατος
 Θεµατικό Περιεχόµενο Μαθήµατος 1. Κρυσταλικές δοµές Ιονική ακτίνα Ενέργεια πλέγµατος Πυκνές διατάξεις 4εδρικές 8εδρικές οπές Μέταλλα ιοντικά στερεά Πώς περιγράφεται η δοµή τους Πως προσδιορίζεται η δοµή
Θεµατικό Περιεχόµενο Μαθήµατος 1. Κρυσταλικές δοµές Ιονική ακτίνα Ενέργεια πλέγµατος Πυκνές διατάξεις 4εδρικές 8εδρικές οπές Μέταλλα ιοντικά στερεά Πώς περιγράφεται η δοµή τους Πως προσδιορίζεται η δοµή
Γραπτή «επί πτυχίω» εξέταση στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Ιούνιος 2017
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Στην παραπάνω Εικόνα δίνονται οι κρυσταλλικές δομές δύο
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Στην παραπάνω Εικόνα δίνονται οι κρυσταλλικές δομές δύο
7.14 Προβλήματα για εξάσκηση
 7.14 Προβλήματα για εξάσκηση 7.1 Το ορυκτό οξείδιο του αλουμινίου (Corundum, Al 2 O 3 ) έχει κρυσταλλική δομή η οποία μπορεί να περιγραφεί ως HCP πλέγμα ιόντων οξυγόνου με τα ιόντα αλουμινίου να καταλαμβάνουν
7.14 Προβλήματα για εξάσκηση 7.1 Το ορυκτό οξείδιο του αλουμινίου (Corundum, Al 2 O 3 ) έχει κρυσταλλική δομή η οποία μπορεί να περιγραφεί ως HCP πλέγμα ιόντων οξυγόνου με τα ιόντα αλουμινίου να καταλαμβάνουν
Γραπτή «επί πτυχίω» εξέταση «Επιστήμη και Τεχνολογία Υλικών Ι»-Ιούνιος 2016
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 ο (25 Μονάδες) (Καθ. Β.Ζασπάλης) Ι) Να προσδιοριστούν οι δείκτες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 ο (25 Μονάδες) (Καθ. Β.Ζασπάλης) Ι) Να προσδιοριστούν οι δείκτες
Εργαστηριακή Άσκηση Β3: Πειράματα περίθλασης από κρύσταλλο λυσοζύμης
 Βιοφυσική & Νανοτεχνολογία Εργαστηριακή Άσκηση Β3: Πειράματα περίθλασης από κρύσταλλο λυσοζύμης Ημερομηνία εκτέλεσης άσκησης... Ονοματεπώνυμα... Περίληψη Σκοπός της άσκησης είναι η εξοικείωση με την χρήση
Βιοφυσική & Νανοτεχνολογία Εργαστηριακή Άσκηση Β3: Πειράματα περίθλασης από κρύσταλλο λυσοζύμης Ημερομηνία εκτέλεσης άσκησης... Ονοματεπώνυμα... Περίληψη Σκοπός της άσκησης είναι η εξοικείωση με την χρήση
ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ. Ενότητα 2: ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 2: ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 2: ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Σχολή Εφαρμοσμένων Μαθηματικών και Φυσικών Επιστημών Εθνικό Μετσόβιο Πολυτεχνείο. Φυσική Συμπυκνωμένης Ύλης. Ενότητα 2. Βασίλειος Γιαννόπαπας
 Σχολή Εφαρμοσμένων Μαθηματικών και Φυσικών Επιστημών Εθνικό Μετσόβιο Πολυτεχνείο Φυσική Συμπυκνωμένης Ύλης Ενότητα 2 Βασίλειος Γιαννόπαπας Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
Σχολή Εφαρμοσμένων Μαθηματικών και Φυσικών Επιστημών Εθνικό Μετσόβιο Πολυτεχνείο Φυσική Συμπυκνωμένης Ύλης Ενότητα 2 Βασίλειος Γιαννόπαπας Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
ΕΝΟΤΗΤΑ 2η:Ταξινόμηση των στοιχείων-στοιχεία με ιδιαίτερο ενδιαφέρον
 ΕΝΟΤΗΤΑ 2η:Ταξινόμηση των στοιχείων-στοιχεία με ιδιαίτερο ενδιαφέρον 1. ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Η ανάγκη της ταξινόμησης των στοιχείων Ενώ στην αρχαιότητα ήταν γνωστά γύρω στα 13 περίπου στοιχεία, τον 18o αιώνα
ΕΝΟΤΗΤΑ 2η:Ταξινόμηση των στοιχείων-στοιχεία με ιδιαίτερο ενδιαφέρον 1. ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Η ανάγκη της ταξινόμησης των στοιχείων Ενώ στην αρχαιότητα ήταν γνωστά γύρω στα 13 περίπου στοιχεία, τον 18o αιώνα
Κρυσταλλογραφία: επιστήμη που ασχολείται με τη περιγραφή της γεωμετρίας των κρυστάλλων και της διάταξης στο εσωτερικό τους.
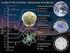 I. Κρυσταλλική Δομή Κρυσταλλογραφία Κρυσταλλογραφία: επιστήμη που ασχολείται με τη περιγραφή της γεωμετρίας των κρυστάλλων και της διάταξης στο εσωτερικό τους. Η συμμετρία του κρυστάλλου επηρεάζει τις
I. Κρυσταλλική Δομή Κρυσταλλογραφία Κρυσταλλογραφία: επιστήμη που ασχολείται με τη περιγραφή της γεωμετρίας των κρυστάλλων και της διάταξης στο εσωτερικό τους. Η συμμετρία του κρυστάλλου επηρεάζει τις
Επιστήμη των Υλικών. Πανεπιστήμιο Ιωαννίνων. Τμήμα Φυσικής
 Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Σημειακές ατέλειες Στοιχειακά στερεά Ατέλειες των στερεών Αυτοπαρεμβολή σε ενδοπλεγματική θέση Κενή θέση Αριθμός κενών θέσεων Q
Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Σημειακές ατέλειες Στοιχειακά στερεά Ατέλειες των στερεών Αυτοπαρεμβολή σε ενδοπλεγματική θέση Κενή θέση Αριθμός κενών θέσεων Q
Βασικά σωματίδια της ύλης
 1 Βασικά σωματίδια της ύλης Τα βασικά σωματίδια της ύλης είναι τα άτομα, τα μόρια και τα ιόντα. «Άτομο ονομάζουμε το μικρότερο σωματίδιο της ύλης που μπορεί να πάρει μέρος στο σχηματισμό χημικών ενώσεων».
1 Βασικά σωματίδια της ύλης Τα βασικά σωματίδια της ύλης είναι τα άτομα, τα μόρια και τα ιόντα. «Άτομο ονομάζουμε το μικρότερο σωματίδιο της ύλης που μπορεί να πάρει μέρος στο σχηματισμό χημικών ενώσεων».
ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα. Θεωρητικη αναλυση
 ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα Θεωρητικη αναλυση ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ στα στερεα Ομοιοπολικός δεσμός Ιοντικός δεσμός Μεταλλικός δεσμός Δεσμός του υδρογόνου Δεσμός van der Waals ΔΟΜΗ ΑΤΟΜΟΥ Στοιβάδες Χώρος κίνησης των
ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα Θεωρητικη αναλυση ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ στα στερεα Ομοιοπολικός δεσμός Ιοντικός δεσμός Μεταλλικός δεσμός Δεσμός του υδρογόνου Δεσμός van der Waals ΔΟΜΗ ΑΤΟΜΟΥ Στοιβάδες Χώρος κίνησης των
Γραπτή «επί πτυχίω» εξέταση «Επιστήμη και Τεχνολογία Υλικών ΙΙ»-Ιανουάριος 2017
 Ερώτηση 1 (10 μονάδες) - ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Σε μια διεργασία ενανθράκωσης
Ερώτηση 1 (10 μονάδες) - ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Σε μια διεργασία ενανθράκωσης
ΑΣΚΗΣΗ 1. Περίληψη. Θεωρητική εισαγωγή. Πειραματικό μέρος
 ΑΣΚΗΣΗ 1 Περίληψη Σκοπός της πρώτης άσκησης ήταν η εξοικείωση μας με τα όργανα παραγωγής και ανίχνευσης των ακτίνων Χ και την εφαρμογή των κανόνων της κρυσταλλοδομής σε μετρήσεις μεγεθών στο οεργαστήριο.
ΑΣΚΗΣΗ 1 Περίληψη Σκοπός της πρώτης άσκησης ήταν η εξοικείωση μας με τα όργανα παραγωγής και ανίχνευσης των ακτίνων Χ και την εφαρμογή των κανόνων της κρυσταλλοδομής σε μετρήσεις μεγεθών στο οεργαστήριο.
οµή των στερεών ιάλεξη 4 η
 οµή των στερεών ιάλεξη 4 η Ύλη τέταρτου µαθήµατος Οι καταστάσεις της ύλης, Γιατί τις µελετάµε; Περιοδική τοποθέτηση των ατόµων, Κρυσταλλική και άµορφη δοµή, Κρυσταλλικό πλέγµα κρυσταλλική κυψελίδα, Πλέγµατα
οµή των στερεών ιάλεξη 4 η Ύλη τέταρτου µαθήµατος Οι καταστάσεις της ύλης, Γιατί τις µελετάµε; Περιοδική τοποθέτηση των ατόµων, Κρυσταλλική και άµορφη δοµή, Κρυσταλλικό πλέγµα κρυσταλλική κυψελίδα, Πλέγµατα
(α ) Αποδείξτε ότι λ / σ = φ αλλά και χ / λ = φ όπου χ = σ + ψ + σ. Η χρυσή τομή φ = 1+ 5
 Ασκήσεις Κεφαλαίου 1. Άσκηση 1.1 Χωρίζουμε ένα ευθύγραμμο τμήμα σε τέσσερα ίσα μέρη, μετά εξαιρούμε το δεύτερο και το τέταρτο, ενώ συνεχίζουμε αυτή τη διαδικασία επ' άπειρον στα ευθύγραμμα τμήματα που
Ασκήσεις Κεφαλαίου 1. Άσκηση 1.1 Χωρίζουμε ένα ευθύγραμμο τμήμα σε τέσσερα ίσα μέρη, μετά εξαιρούμε το δεύτερο και το τέταρτο, ενώ συνεχίζουμε αυτή τη διαδικασία επ' άπειρον στα ευθύγραμμα τμήματα που
Ασκήσεις ακαδ. έτους
 Τμήμα Επιστήμης και Τεχνολογίας Υλικών Πανεπιστήμιο Κρήτης Επιστήμη Επιφανειών - Νανοϋλικών (ETY/METY 346) Μεταπτυχιακό: Νανοτεχνολογία για Ενεργειακές Εφαρμογές ¹ Nanomaterials for Energy (Νανοϋλικά για
Τμήμα Επιστήμης και Τεχνολογίας Υλικών Πανεπιστήμιο Κρήτης Επιστήμη Επιφανειών - Νανοϋλικών (ETY/METY 346) Μεταπτυχιακό: Νανοτεχνολογία για Ενεργειακές Εφαρμογές ¹ Nanomaterials for Energy (Νανοϋλικά για
, όπου Α, Γ, l είναι σταθερές με l > 2.
 Φυσική Στερεάς Κατάστασης: Εισαγωγή Θέμα 1 Η ηλεκτρική χωρητικότητα ισούται με C=Q/V όπου Q το φορτίο και V η τάση. (α) Εκφράστε τις διαστάσεις του C στις βασικές διαστάσεις L,M,T,I. (β) Σφαίρα είναι φορτισμένη
Φυσική Στερεάς Κατάστασης: Εισαγωγή Θέμα 1 Η ηλεκτρική χωρητικότητα ισούται με C=Q/V όπου Q το φορτίο και V η τάση. (α) Εκφράστε τις διαστάσεις του C στις βασικές διαστάσεις L,M,T,I. (β) Σφαίρα είναι φορτισμένη
Κεφάλαιο 2 Χημικοί Δεσμοί
 Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Γραπτή εξέταση προόδου «Επιστήμη και Τεχνολογία Υλικών ΙΙ»-Απρίλιος 2016
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 ο (25 Μονάδες) (Καθ. Β.Ζασπάλης) Σε μια διεργασία ενανθράκωσης κάποιου
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 ο (25 Μονάδες) (Καθ. Β.Ζασπάλης) Σε μια διεργασία ενανθράκωσης κάποιου
1 η ΕΝΟΤΗΤΑ ΔΟΜΙΚΑ ΥΛΙΚΑ (ΕΙΣΑΓΩΓΗ)
 ΣΧΟΛΗ ΠΟΛΙΤΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΜΠ ΤΕΧΝΙΚΑ ΥΛΙΚΑ 1 η ΕΝΟΤΗΤΑ ΔΟΜΙΚΑ ΥΛΙΚΑ (ΕΙΣΑΓΩΓΗ) Ε. Βιντζηλαίου (Συντονιστής), Ε. Βουγιούκας, Ε. Μπαδογιάννης Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΣΧΟΛΗ ΠΟΛΙΤΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΜΠ ΤΕΧΝΙΚΑ ΥΛΙΚΑ 1 η ΕΝΟΤΗΤΑ ΔΟΜΙΚΑ ΥΛΙΚΑ (ΕΙΣΑΓΩΓΗ) Ε. Βιντζηλαίου (Συντονιστής), Ε. Βουγιούκας, Ε. Μπαδογιάννης Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ
 ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 3. ΟΙ 32 ΚΡΥΣΤΑΛΛΙΚΕΣ ΤΑΞΕΙΣ Ταξινόμηση των κρυστάλλων σαν στερεά σχήματα και οι συμμετρίες Ηλίας Χατζηθεοδωρίδης,
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 3. ΟΙ 32 ΚΡΥΣΤΑΛΛΙΚΕΣ ΤΑΞΕΙΣ Ταξινόμηση των κρυστάλλων σαν στερεά σχήματα και οι συμμετρίες Ηλίας Χατζηθεοδωρίδης,
Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ. Ενότητα 3: Στερεά διαλύματα και ενδομεταλλικές ενώσεις. Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών
 Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ Ενότητα 3: Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό
Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ Ενότητα 3: Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό
Θέμα 1 ο (30 μονάδες)
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Θέμα 1 ο (30 μονάδες) (Καθ. Β.Ζασπάλης) Θεωρείστε ένα δοκίμιο καθαρού Νικελίου
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Θέμα 1 ο (30 μονάδες) (Καθ. Β.Ζασπάλης) Θεωρείστε ένα δοκίμιο καθαρού Νικελίου
ΔΙΑΤΑΡΑΧΕΣ (DISLOCATIONS )
 ΔΙΑΤΑΡΑΧΕΣ (DISLOCATIONS ) 1. ΕΙΣΑΓΩΓΉ Η αντοχή και η σκληρότητα είναι μέτρα της αντίστασης ενός υλικού σε πλαστική παραμόρφωση Σε μικροσκοπική κλίμακα, πλαστική παραμόρφωση : - συνολική κίνηση μεγάλου
ΔΙΑΤΑΡΑΧΕΣ (DISLOCATIONS ) 1. ΕΙΣΑΓΩΓΉ Η αντοχή και η σκληρότητα είναι μέτρα της αντίστασης ενός υλικού σε πλαστική παραμόρφωση Σε μικροσκοπική κλίμακα, πλαστική παραμόρφωση : - συνολική κίνηση μεγάλου
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ Ενότητα:
 ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΧΑΡΑΛΑΜΠΟΣ ΔΡΙΒΑΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 1 η ΣΕΙΡΑ ΑΣΚΗΣΕΩΝ 1. Τι τάξη μεγέθους είναι οι ενδοατομικές αποστάσεις και ποιες υποδιαιρέσεις του
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΧΑΡΑΛΑΜΠΟΣ ΔΡΙΒΑΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 1 η ΣΕΙΡΑ ΑΣΚΗΣΕΩΝ 1. Τι τάξη μεγέθους είναι οι ενδοατομικές αποστάσεις και ποιες υποδιαιρέσεις του
2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος
 2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος Όπως είναι γνωστό από την καθημερινή εμπειρία τα περισσότερα σώματα που χρησιμοποιούνται στις ηλεκτρικές ηλεκτρονικές
2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος Όπως είναι γνωστό από την καθημερινή εμπειρία τα περισσότερα σώματα που χρησιμοποιούνται στις ηλεκτρικές ηλεκτρονικές
Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών Χτίζοντας τους κρυστάλλους από άτομα Είδη δεσμών Διδάσκων : Επίκουρη Καθηγήτρια
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών Χτίζοντας τους κρυστάλλους από άτομα Είδη δεσμών Διδάσκων : Επίκουρη Καθηγήτρια
Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Πανεπιστήμιο Δυτικής Αττικής - ΣΑΕΤ
 Γενική και Ανόργανη Χημεία Περιοδικές ιδιότητες των στοιχείων. Σχηματισμός ιόντων. Στ. Μπογιατζής 1 Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Π Δ Χειμερινό εξάμηνο 2018-2019 Π
Γενική και Ανόργανη Χημεία Περιοδικές ιδιότητες των στοιχείων. Σχηματισμός ιόντων. Στ. Μπογιατζής 1 Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Π Δ Χειμερινό εξάμηνο 2018-2019 Π
Χημεία Α ΓΕΛ 15 / 04 / 2018
 Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Εισαγωγή στην Επιστήμη των Υλικών Διαγράμματα Φάσεων Callister Κεφάλαιο 11, Ashby Οδηγός μάθησης Ενότητα 2
 Εισαγωγή στην Επιστήμη των Υλικών Διαγράμματα Φάσεων Callister Κεφάλαιο 11, Ashby Οδηγός μάθησης Ενότητα 2 Έννοιες που θα συζητηθούν Ορισμός Φάσης Ορολογία που συνοδεύει τα διαγράμματα και τους μετασχηματισμούς
Εισαγωγή στην Επιστήμη των Υλικών Διαγράμματα Φάσεων Callister Κεφάλαιο 11, Ashby Οδηγός μάθησης Ενότητα 2 Έννοιες που θα συζητηθούν Ορισμός Φάσης Ορολογία που συνοδεύει τα διαγράμματα και τους μετασχηματισμούς
ΑΞΟΝΟΜΕΤΡΙΑ. Εισαγωγή
 ΑΞΟΝΟΜΕΤΡΙΑ Εισαγωγή Η προβολή τρισδιάστατου αντικειμένου πάνω σε δισδιάστατη επιφάνεια αποτέλεσε μια από τις βασικές αναζητήσεις μεθόδων απεικόνισης και απασχόλησε από πολύ παλιά τους ανθρώπους. Με την
ΑΞΟΝΟΜΕΤΡΙΑ Εισαγωγή Η προβολή τρισδιάστατου αντικειμένου πάνω σε δισδιάστατη επιφάνεια αποτέλεσε μια από τις βασικές αναζητήσεις μεθόδων απεικόνισης και απασχόλησε από πολύ παλιά τους ανθρώπους. Με την
Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Σχολή Θετικών Επιστημών - Τμήμα Φυσικής Εργαστήριο Ακτίνων-Χ, Οπτικού Χαρακτηρισμού και Θερμικής Ανάλυσης
 Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Σχολή Θετικών Επιστημών - Τμήμα Φυσικής Εργαστήριο Ακτίνων-Χ, Οπτικού Χαρακτηρισμού και Θερμικής Ανάλυσης ΑΣΚΗΣΗ Σκοπός της άσκησης είναι ο υπολογισμός των μηκών
Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Σχολή Θετικών Επιστημών - Τμήμα Φυσικής Εργαστήριο Ακτίνων-Χ, Οπτικού Χαρακτηρισμού και Θερμικής Ανάλυσης ΑΣΚΗΣΗ Σκοπός της άσκησης είναι ο υπολογισμός των μηκών
ΜΑΘΗΜΑΤΑ ΜΑΘΗΜΑΤΙΚΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Β ΛΥΚΕΙΟΥ
 ΜΑΘΗΜΑΤΑ ΜΑΘΗΜΑΤΙΚΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Β ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 1 ο : ΔΙΑΝΥΣΜΑΤΑ 1 ΜΑΘΗΜΑ 1 ο +2 ο ΕΝΝΟΙΑ ΔΙΑΝΥΣΜΑΤΟΣ Διάνυσμα ορίζεται ένα προσανατολισμένο ευθύγραμμο τμήμα, δηλαδή ένα ευθύγραμμο τμήμα
ΜΑΘΗΜΑΤΑ ΜΑΘΗΜΑΤΙΚΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Β ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 1 ο : ΔΙΑΝΥΣΜΑΤΑ 1 ΜΑΘΗΜΑ 1 ο +2 ο ΕΝΝΟΙΑ ΔΙΑΝΥΣΜΑΤΟΣ Διάνυσμα ορίζεται ένα προσανατολισμένο ευθύγραμμο τμήμα, δηλαδή ένα ευθύγραμμο τμήμα
κρυστάλλου απείρου μεγέθους.
 Κρυστάλλωση Πολυμερών Θερμοδυναμική της κρυστάλλωσης πολυμερών Θερμοκρασία ρασία τήξης πολυμερών Μεταβολή ειδικού όγκου ως προς τη θερμοκρασία σε γραμμικό πολυαιθυλένιο:., ακλασματοποίητο πολυμερές, ο,
Κρυστάλλωση Πολυμερών Θερμοδυναμική της κρυστάλλωσης πολυμερών Θερμοκρασία ρασία τήξης πολυμερών Μεταβολή ειδικού όγκου ως προς τη θερμοκρασία σε γραμμικό πολυαιθυλένιο:., ακλασματοποίητο πολυμερές, ο,
11. Υγρά και Στερεά ΣΚΟΠΟΣ
 11. Υγρά και Στερεά ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε τις άλλεςδύοκαταστάσειςτηςύλης, την υγρή και τη στερεά, να μελετήσουμε και να ερμηνεύσουμε τις ιδιότητες των υγρών, να δούμε τους
11. Υγρά και Στερεά ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε τις άλλεςδύοκαταστάσειςτηςύλης, την υγρή και τη στερεά, να μελετήσουμε και να ερμηνεύσουμε τις ιδιότητες των υγρών, να δούμε τους
ΘΕΩΡΙΑ Β ΓΥΜΝΑΣΙΟΥ. Μια παράσταση που περιέχει πράξεις με μεταβλητές (γράμματα) και αριθμούς καλείται αλγεβρική, όπως για παράδειγμα η : 2x+3y-8
 ΘΕΩΡΙΑ Β ΓΥΜΝΑΣΙΟΥ Άλγεβρα 1 ο Κεφάλαιο 1. Τι ονομάζουμε αριθμητική και τι αλγεβρική παράσταση; Να δώσετε από ένα παράδειγμα. Μια παράσταση που περιέχει πράξεις με αριθμούς, καλείται αριθμητική παράσταση,
ΘΕΩΡΙΑ Β ΓΥΜΝΑΣΙΟΥ Άλγεβρα 1 ο Κεφάλαιο 1. Τι ονομάζουμε αριθμητική και τι αλγεβρική παράσταση; Να δώσετε από ένα παράδειγμα. Μια παράσταση που περιέχει πράξεις με αριθμούς, καλείται αριθμητική παράσταση,
Κρυσταλλικές ατέλειες στερεών
 Κρυσταλλικές ατέλειες στερεών Χαράλαμπος Στεργίου Dr.Eng. chstergiou@uowm.gr Ατέλειες Τεχνολογία Υλικών Ι Ατέλειες Ατέλειες στερεών Ο τέλειος κρύσταλλος δεν υπάρχει στην φύση. Η διάταξη των ατόμων σε δομές
Κρυσταλλικές ατέλειες στερεών Χαράλαμπος Στεργίου Dr.Eng. chstergiou@uowm.gr Ατέλειες Τεχνολογία Υλικών Ι Ατέλειες Ατέλειες στερεών Ο τέλειος κρύσταλλος δεν υπάρχει στην φύση. Η διάταξη των ατόμων σε δομές
Μαθηματικά Α' Γυμ. - Ερωτήσεις Θεωρίας 1 ΕΡΩΤΗΣΕΙΣ. (1) Ποιοι είναι οι φυσικοί αριθμοί; Γράψε τέσσερα παραδείγματα.
 Μαθηματικά Α' Γυμ. - Ερωτήσεις Θεωρίας 1 ΕΡΩΤΗΣΕΙΣ (1) Ποιοι είναι οι φυσικοί αριθμοί; Γράψε τέσσερα παραδείγματα. (2) Ποιοι είναι οι άρτιοι και ποιοι οι περιττοί αριθμοί; Γράψε από τρία παραδείγματα.
Μαθηματικά Α' Γυμ. - Ερωτήσεις Θεωρίας 1 ΕΡΩΤΗΣΕΙΣ (1) Ποιοι είναι οι φυσικοί αριθμοί; Γράψε τέσσερα παραδείγματα. (2) Ποιοι είναι οι άρτιοι και ποιοι οι περιττοί αριθμοί; Γράψε από τρία παραδείγματα.
«Επί πτυχίω» εξέταση στο μάθημα «Επιστήμη και Τεχνολογία Υλικών ΙΙ»-Ιανουάριος 2018
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 (25 μονάδες) (Καθ. Β.Ζασπάλης) Σε μια φυσική διεργασία αέριο υδρογόνο
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 (25 μονάδες) (Καθ. Β.Ζασπάλης) Σε μια φυσική διεργασία αέριο υδρογόνο
2.1 ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ
 2.1 ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ ΕΙΣΑΓΩΓΗ Ένας κρύσταλλος ή ακριβέστερα ένας µονοκρύσταλλος, µπορεί να οριστεί µακροσκοπικά ως ένα στερεό αντικείµενο µε οµοιόµορφη χηµική σύσταση που, όπως απαντάται στη φύση
2.1 ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ ΕΙΣΑΓΩΓΗ Ένας κρύσταλλος ή ακριβέστερα ένας µονοκρύσταλλος, µπορεί να οριστεί µακροσκοπικά ως ένα στερεό αντικείµενο µε οµοιόµορφη χηµική σύσταση που, όπως απαντάται στη φύση
Τελική γραπτή εξέταση «Επιστήμη και Τεχνολογία Υλικών Ι»-Ιανουάριος 2016
 ΘΕΜΑ 1 ο (0 Μονάδες) ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Το Τιτάνιο (ατομική ακτίνα RTi=0.1
ΘΕΜΑ 1 ο (0 Μονάδες) ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Το Τιτάνιο (ατομική ακτίνα RTi=0.1
Κεφάλαιο 2 ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ
 Κεφάλαιο ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ Προαπαιτούμενη γνώση Πλέγμα Brvis, θεμελιώδης και μοναδιαία κυψελίδα, πλεγματικά επίπεδα, δείκτες Miller, ανάστροφο πλέγμα, ζώνη Brillouin, σημειακές ομάδες χώρου. Πρόβλημα Το
Κεφάλαιο ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ Προαπαιτούμενη γνώση Πλέγμα Brvis, θεμελιώδης και μοναδιαία κυψελίδα, πλεγματικά επίπεδα, δείκτες Miller, ανάστροφο πλέγμα, ζώνη Brillouin, σημειακές ομάδες χώρου. Πρόβλημα Το
2.3 ΜΕΡΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΜΕΤΑΛΛΩΝ. Επιμέλεια παρουσίασης Παναγιώτης Αθανασόπουλος Δρ - Χημικός
 2.3 ΜΕΡΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΜΕΤΑΛΛΩΝ Επιμέλεια παρουσίασης Παναγιώτης Αθανασόπουλος Δρ - Χημικός Σκοπός του μαθήματος: Να επισημαίνουμε τη θέση των μετάλλων στον περιοδικό πίνακα των στοιχείων. Να αναφέρουμε
2.3 ΜΕΡΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΜΕΤΑΛΛΩΝ Επιμέλεια παρουσίασης Παναγιώτης Αθανασόπουλος Δρ - Χημικός Σκοπός του μαθήματος: Να επισημαίνουμε τη θέση των μετάλλων στον περιοδικό πίνακα των στοιχείων. Να αναφέρουμε
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 26 04 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Στον επόμενο πίνακα δίνονται τα σημεία τήξης και τα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 26 04 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Στον επόμενο πίνακα δίνονται τα σημεία τήξης και τα
Χημεία Α ΓΕΛ 15 / 04 / 2018
 Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
ΕΤΥ-349 ΜΗΧΑΝΙΚΕΣ ΚΑΙ ΘΕΡΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ
 ΕΤΥ-349 ΜΗΧΑΝΙΚΕΣ ΚΑΙ ΘΕΡΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ Χειμερινό εξάμηνο ακαδημαϊκού έτους 2017-2018 Τμήμα Επιστήμης και Τεχνολογία Υλικών, Πανεπιστήμιο Κρήτης Διδάσκων: Βασίλης Παλτόγλου email: vaspal@physics.uoc.gr
ΕΤΥ-349 ΜΗΧΑΝΙΚΕΣ ΚΑΙ ΘΕΡΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ Χειμερινό εξάμηνο ακαδημαϊκού έτους 2017-2018 Τμήμα Επιστήμης και Τεχνολογία Υλικών, Πανεπιστήμιο Κρήτης Διδάσκων: Βασίλης Παλτόγλου email: vaspal@physics.uoc.gr
Επιστήμη των Υλικών. Πανεπιστήμιο Ιωαννίνων. Τμήμα Φυσικής
 Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Διαγράμματα Φάσεων Δημιουργία κραμάτων: διάχυση στοιχείων που έρχονται σε άμεση επαφή Πως συμπεριφέρονται τα επιμέρους άτομα των
Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Διαγράμματα Φάσεων Δημιουργία κραμάτων: διάχυση στοιχείων που έρχονται σε άμεση επαφή Πως συμπεριφέρονται τα επιμέρους άτομα των
Εργαστηριακή άσκηση 01. Τα επτά συστήματα κρυστάλλωσης και κρυσταλλικές μορφές
 Εργαστηριακή άσκηση 01 Τα επτά συστήματα κρυστάλλωσης και κρυσταλλικές μορφές Ηλίας Χατζηθεοδωρίδης Οκτώβριος / Νοέμβριος 2004 Τι περιλαμβάνει η άσκηση Θα μάθετε τα 7 κρυσταλλογραφικά συστήματα και πως
Εργαστηριακή άσκηση 01 Τα επτά συστήματα κρυστάλλωσης και κρυσταλλικές μορφές Ηλίας Χατζηθεοδωρίδης Οκτώβριος / Νοέμβριος 2004 Τι περιλαμβάνει η άσκηση Θα μάθετε τα 7 κρυσταλλογραφικά συστήματα και πως
W el = q k φ (1) W el = z k e 0 N A φn k = z k F φn k (2)
 Το ηλεκτρολυτικό διάλυμα στην ισορροπία Αντώνης Καραντώνης 19 Απριλίου 211 Σταθερές 1. Σταθερά των αερίων, R = 8.314 J mol 1 K 1 2. Στοιχειώδες φορτίο, e = 1.62 1 19 C 3. Αριθμός Avogadro, N A = 6.23 1
Το ηλεκτρολυτικό διάλυμα στην ισορροπία Αντώνης Καραντώνης 19 Απριλίου 211 Σταθερές 1. Σταθερά των αερίων, R = 8.314 J mol 1 K 1 2. Στοιχειώδες φορτίο, e = 1.62 1 19 C 3. Αριθμός Avogadro, N A = 6.23 1
Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C.
 4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
2. ΜΕΤΑΛΛΑ - ΚΡΑΜΑΤΑ. 2.2 Κύριοι χημικοί δεσμοί
 1 2. ΜΕΤΑΛΛΑ - ΚΡΑΜΑΤΑ 2.1 Γενικά Τα μικρότερα σωματίδια της ύλης, που μπορούν να βρεθούν ελεύθερα και να διατηρούν τις ιδιότητες του σώματος στο οποίο ανήκουν, λέγονται μόρια. Τα ελάχιστα σωματίδια της
1 2. ΜΕΤΑΛΛΑ - ΚΡΑΜΑΤΑ 2.1 Γενικά Τα μικρότερα σωματίδια της ύλης, που μπορούν να βρεθούν ελεύθερα και να διατηρούν τις ιδιότητες του σώματος στο οποίο ανήκουν, λέγονται μόρια. Τα ελάχιστα σωματίδια της
ΕΠΑΝΑΛΗΨΗ Α ΓΥΜΝΑΣΙΟΥ
 ΕΠΑΝΑΛΗΨΗ Α ΓΥΜΝΑΣΙΟΥ ΘΕΩΡΙΑ ΑΛΓΕΒΡΑ ΚΕΦΑΛΑΙΟ Α.1. 1) Ποιοι φυσικοί αριθμοί λέγονται άρτιοι και ποιοι περιττοί; ( σ. 11 ) 2) Από τι καθορίζεται η αξία ενός ψηφίου σ έναν φυσικό αριθμό; ( σ. 11 ) 3) Τι
ΕΠΑΝΑΛΗΨΗ Α ΓΥΜΝΑΣΙΟΥ ΘΕΩΡΙΑ ΑΛΓΕΒΡΑ ΚΕΦΑΛΑΙΟ Α.1. 1) Ποιοι φυσικοί αριθμοί λέγονται άρτιοι και ποιοι περιττοί; ( σ. 11 ) 2) Από τι καθορίζεται η αξία ενός ψηφίου σ έναν φυσικό αριθμό; ( σ. 11 ) 3) Τι
ΑΡΧΕΣ ΚΡΥΣΤΑΛΛΟΧΗΜΕΙΑΣ. Γεωχημεία (Υ4203) Χ. Στουραϊτη
 ΑΡΧΕΣ ΚΡΥΣΤΑΛΛΟΧΗΜΕΙΑΣ Γεωχημεία (Υ4203) Χ. Στουραϊτη Κρύσταλλοι Τα ορυκτά σχηματίζουν κρυστάλλους: διατάξεις ατόμων που συνδέονται στο χώρο (3 διαστάσεις) και που έχουν μια συγκεκριμένη διάταξη (order)
ΑΡΧΕΣ ΚΡΥΣΤΑΛΛΟΧΗΜΕΙΑΣ Γεωχημεία (Υ4203) Χ. Στουραϊτη Κρύσταλλοι Τα ορυκτά σχηματίζουν κρυστάλλους: διατάξεις ατόμων που συνδέονται στο χώρο (3 διαστάσεις) και που έχουν μια συγκεκριμένη διάταξη (order)
Τελική γραπτή εξέταση «Επιστήμη και Τεχνολογία Υλικών ΙΙ»-Ιούνιος 2016
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 ο (25 Μονάδες) (Καθ. Β.Ζασπάλης) Δοκίμιο από PMMA (Poly Methyl MethAcrylate)
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 ο (25 Μονάδες) (Καθ. Β.Ζασπάλης) Δοκίμιο από PMMA (Poly Methyl MethAcrylate)
ΑΣΚΗΣΕΙΣ ΥΠΟΛΟΓΙΣΜΟΥ ΜΑΖΑΣ ΘΕΣΗΣ ΚΕΝΤΡΟΥ ΜΑΖΑΣ ΡΟΠΗΣ ΑΔΡΑΝΕΙΑΣ ΣΩΜΑΤΩΝ
 ΑΣΚΗΣΕΙΣ ΥΠΟΛΟΓΙΣΜΟΥ ΜΑΖΑΣ ΘΕΣΗΣ ΚΕΝΤΡΟΥ ΜΑΖΑΣ ΡΟΠΗΣ ΑΔΡΑΝΕΙΑΣ ΣΩΜΑΤΩΝ ΓΕΝΙΚΕΣ ΠΑΡΑΤΗΡΗΣΕΙΣ Α. Υπολογισμός της θέσης του κέντρου μάζας συστημάτων που αποτελούνται από απλά διακριτά μέρη. Τα απλά διακριτά
ΑΣΚΗΣΕΙΣ ΥΠΟΛΟΓΙΣΜΟΥ ΜΑΖΑΣ ΘΕΣΗΣ ΚΕΝΤΡΟΥ ΜΑΖΑΣ ΡΟΠΗΣ ΑΔΡΑΝΕΙΑΣ ΣΩΜΑΤΩΝ ΓΕΝΙΚΕΣ ΠΑΡΑΤΗΡΗΣΕΙΣ Α. Υπολογισμός της θέσης του κέντρου μάζας συστημάτων που αποτελούνται από απλά διακριτά μέρη. Τα απλά διακριτά
1. ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ. 19. Βλέπε θεωρία σελ. 9 και 10.
 19. Βλέπε θεωρία σελ. 9 και 10. 7 1. ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 20. Βλέπε θεωρία α) σελ. 8, β) σελ. 8, γ) σελ. 9. 21. α) ζυγού, β) I. προχοΐδας Π. ογκομετρικού κυλίνδρου. 22. Με το ζυγό υπολογίζουμε τη μάζα. O όγκος
19. Βλέπε θεωρία σελ. 9 και 10. 7 1. ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 20. Βλέπε θεωρία α) σελ. 8, β) σελ. 8, γ) σελ. 9. 21. α) ζυγού, β) I. προχοΐδας Π. ογκομετρικού κυλίνδρου. 22. Με το ζυγό υπολογίζουμε τη μάζα. O όγκος
ΙΙΙ. Αρχές Κρυσταλλοχημείας. Γεωχημεία (Υ4203) Χ. Στουραϊτη
 ΙΙΙ. Αρχές Κρυσταλλοχημείας Γεωχημεία (Υ4203) Χ. Στουραϊτη Κρύσταλλοι Τα ορυκτά σχηματίζουν κρυστάλλους: διατάξεις ατόμων που συνδέονται στο χώρο (3 διαστάσεις) και που έχουν μια συγκεκριμένη διάταξη (order)
ΙΙΙ. Αρχές Κρυσταλλοχημείας Γεωχημεία (Υ4203) Χ. Στουραϊτη Κρύσταλλοι Τα ορυκτά σχηματίζουν κρυστάλλους: διατάξεις ατόμων που συνδέονται στο χώρο (3 διαστάσεις) και που έχουν μια συγκεκριμένη διάταξη (order)
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Γραπτό τεστ (συν-)αξιολόγησης στο μάθημα: «ΔΙΑΓΝΩΣΤΙΚΕΣ ΜΕΘΟΔΟΙ ΣΤΗ ΜΕΛΕΤΗ
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Γραπτό τεστ (συν-)αξιολόγησης στο μάθημα: «ΔΙΑΓΝΩΣΤΙΚΕΣ ΜΕΘΟΔΟΙ ΣΤΗ ΜΕΛΕΤΗ
Θερμοκρασία - Θερμότητα. (Θερμοκρασία / Θερμική διαστολή / Ποσότητα θερμότητας / Θερμοχωρητικότητα / Θερμιδομετρία / Αλλαγή φάσης)
 Θερμοκρασία - Θερμότητα (Θερμοκρασία / Θερμική διαστολή / Ποσότητα θερμότητας / Θερμοχωρητικότητα / Θερμιδομετρία / Αλλαγή φάσης) Θερμοκρασία Ποσοτικοποιεί την αντίληψή μας για το πόσο ζεστό ή κρύο είναι
Θερμοκρασία - Θερμότητα (Θερμοκρασία / Θερμική διαστολή / Ποσότητα θερμότητας / Θερμοχωρητικότητα / Θερμιδομετρία / Αλλαγή φάσης) Θερμοκρασία Ποσοτικοποιεί την αντίληψή μας για το πόσο ζεστό ή κρύο είναι
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ. Τράπεζα θεμάτων. Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ
 ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ 16111 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ 16111 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΜΕΤΡΩΝΤΑΣ ΤΟΝ ΠΛΑΝΗΤΗ ΓΗ
 του Υποπυραγού Αλέξανδρου Μαλούνη* Μέρος 2 ο - Χαρτογραφικοί μετασχηματισμοί Εισαγωγή Είδαμε λοιπόν ως τώρα, ότι η γη θα μπορούσε να χαρακτηρισθεί και σφαιρική και αυτό μπορεί να γίνει εμφανές όταν την
του Υποπυραγού Αλέξανδρου Μαλούνη* Μέρος 2 ο - Χαρτογραφικοί μετασχηματισμοί Εισαγωγή Είδαμε λοιπόν ως τώρα, ότι η γη θα μπορούσε να χαρακτηρισθεί και σφαιρική και αυτό μπορεί να γίνει εμφανές όταν την
1 ο Γυμνάσιο Αργυρούπολης. Χημεία Γ Γυμνασίου. 1. Γενικά να γνωρίζεις Α. τα σύμβολα των παρακάτω στοιχείων
 1 ο Γυμνάσιο Αργυρούπολης Π. Γκίνης 1. Γενικά να γνωρίζεις Α. τα σύμβολα των παρακάτω στοιχείων Β. τις παρακάτω ρίζες Χημεία Γ Γυμνασίου Οξυγόνο O Βρώμιο Br Χαλκός Cu Υδρογόνο H Ιώδιο I Αργίλιο Al Άζωτο
1 ο Γυμνάσιο Αργυρούπολης Π. Γκίνης 1. Γενικά να γνωρίζεις Α. τα σύμβολα των παρακάτω στοιχείων Β. τις παρακάτω ρίζες Χημεία Γ Γυμνασίου Οξυγόνο O Βρώμιο Br Χαλκός Cu Υδρογόνο H Ιώδιο I Αργίλιο Al Άζωτο
Γενική Φυσική V (Σύγχρονη Φυσική) Φυσική Ακτίνων-Χ και Αλληλεπίδραση Ακτίνων-Χ και Ηλεκτρονίων με την Ύλη
 Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Τμήμα Φυσικής Εργαστήριο Εφαρμοσμένης Φυσικής Γενική Φυσική V (Σύγχρονη Φυσική) Φυσική Ακτίνων-Χ και Αλληλεπίδραση Ακτίνων-Χ και Ηλεκτρονίων με την Ύλη Περιεχόμενα
Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Τμήμα Φυσικής Εργαστήριο Εφαρμοσμένης Φυσικής Γενική Φυσική V (Σύγχρονη Φυσική) Φυσική Ακτίνων-Χ και Αλληλεπίδραση Ακτίνων-Χ και Ηλεκτρονίων με την Ύλη Περιεχόμενα
Διαγράμματα φάσεων-phase Diagrams
 Διαγράμματα φάσεων-phase Diagrams Φωτογραφία ηλεκτρονικού μικροσκοπίου που δείχνει την μικροκρυασταλλική δομή ανθρακούχου χάλυβα με περιεκτικότητα 0,44%C Περλίτης Φερρίτης (φερρίτης+σεμεντίτης) Φάσεις
Διαγράμματα φάσεων-phase Diagrams Φωτογραφία ηλεκτρονικού μικροσκοπίου που δείχνει την μικροκρυασταλλική δομή ανθρακούχου χάλυβα με περιεκτικότητα 0,44%C Περλίτης Φερρίτης (φερρίτης+σεμεντίτης) Φάσεις
Αγωγιμότητα στα μέταλλα
 Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Στ Τάξη. Α/Α Μαθηματικό περιεχόμενο Δείκτες Επιτυχίας Ώρες Διδ. 1 ENOTHTA 1
 Ενδεικτική Οργάνωση Ενοτήτων Στ Τάξη Α/Α Μαθηματικό περιεχόμενο Δείκτες Επιτυχίας Ώρες Διδ. 1 ENOTHTA 1 15 Αρ3.1 Απαγγέλουν, διαβάζουν, γράφουν και αναγνωρίζουν ποσότητες αριθμών Επανάληψη μέχρι το 1 000
Ενδεικτική Οργάνωση Ενοτήτων Στ Τάξη Α/Α Μαθηματικό περιεχόμενο Δείκτες Επιτυχίας Ώρες Διδ. 1 ENOTHTA 1 15 Αρ3.1 Απαγγέλουν, διαβάζουν, γράφουν και αναγνωρίζουν ποσότητες αριθμών Επανάληψη μέχρι το 1 000
Ενδεικτικό Φύλλο Εργασίας 1. Επίπεδα και Ευθείες Ονοματεπώνυμο:... Τάξη Τμήμα:... Ημερομηνία:...
 Διδακτική των Μαθηματικών με Τ.Π.Ε Σελίδα 1 από 13 Ενδεικτικό Φύλλο Εργασίας 1. Επίπεδα και Ευθείες Ονοματεπώνυμο:... Τάξη Τμήμα:... Ημερομηνία:... Όλες οι εφαρμογές που καλείσθε να χρησιμοποιήσετε είναι
Διδακτική των Μαθηματικών με Τ.Π.Ε Σελίδα 1 από 13 Ενδεικτικό Φύλλο Εργασίας 1. Επίπεδα και Ευθείες Ονοματεπώνυμο:... Τάξη Τμήμα:... Ημερομηνία:... Όλες οι εφαρμογές που καλείσθε να χρησιμοποιήσετε είναι
Αγωγιμότητα στα μέταλλα
 Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ
 Φυσικοχημεία II, Διαλύματα Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 poulios@chem.auth.gr photocatalysisgroup.web.auth.gr ΚΡΑΜΑΤΑ Χρώμα κραμάτων αποτελούμενα από Χρυσό (Au),
Φυσικοχημεία II, Διαλύματα Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 poulios@chem.auth.gr photocatalysisgroup.web.auth.gr ΚΡΑΜΑΤΑ Χρώμα κραμάτων αποτελούμενα από Χρυσό (Au),
Μαθηματική Εισαγωγή Συναρτήσεις
 Φυσικός Ραδιοηλεκτρολόγος (MSc) ο Γενικό Λύκειο Καστοριάς A. Μαθηματική Εισαγωγή Πράξεις με αριθμούς σε εκθετική μορφή Επίλυση βασικών μορφών εξισώσεων Συναρτήσεις Στοιχεία τριγωνομετρίας Διανύσματα Καστοριά,
Φυσικός Ραδιοηλεκτρολόγος (MSc) ο Γενικό Λύκειο Καστοριάς A. Μαθηματική Εισαγωγή Πράξεις με αριθμούς σε εκθετική μορφή Επίλυση βασικών μορφών εξισώσεων Συναρτήσεις Στοιχεία τριγωνομετρίας Διανύσματα Καστοριά,
Κεφάλαιο 3 Κρυσταλλογραφία
 Κεφάλαιο 3 Κρυσταλλογραφία Σύνοψη Μελετάται ο σχηματισμός των κρυστάλλων με τα αντίστοιχα στάδια ανάπτυξης αυτών, τα κρυσταλλικά συστήματα, τα κρυσταλλικά πλέγματα, η μελέτη των κρυσταλλικών δομών μεγίστης
Κεφάλαιο 3 Κρυσταλλογραφία Σύνοψη Μελετάται ο σχηματισμός των κρυστάλλων με τα αντίστοιχα στάδια ανάπτυξης αυτών, τα κρυσταλλικά συστήματα, τα κρυσταλλικά πλέγματα, η μελέτη των κρυσταλλικών δομών μεγίστης
Μαθηματική Εισαγωγή Συναρτήσεις
 Φυσικός Ραδιοηλεκτρολόγος (MSc) ο Γενικό Λύκειο Καστοριάς Καστοριά, Ιούλιος 14 A. Μαθηματική Εισαγωγή Πράξεις με αριθμούς σε εκθετική μορφή Επίλυση βασικών μορφών εξισώσεων Συναρτήσεις Στοιχεία τριγωνομετρίας
Φυσικός Ραδιοηλεκτρολόγος (MSc) ο Γενικό Λύκειο Καστοριάς Καστοριά, Ιούλιος 14 A. Μαθηματική Εισαγωγή Πράξεις με αριθμούς σε εκθετική μορφή Επίλυση βασικών μορφών εξισώσεων Συναρτήσεις Στοιχεία τριγωνομετρίας
Στοιχειομετρία. Το mol (ή και mole)
 Στοιχειομετρία. Το mol (ή και mole) Μια παρουσίαση για την Α Λυκείου ΕΠΑΛ από τον Π.ΑΡΦΑΝΗ, 2011 Μια χημική αντίδραση Κάντε κλικ στην εικόνα Μια χημική αντίδραση Ωραίες οι αντιδράσεις ιδίως αν γίνεται
Στοιχειομετρία. Το mol (ή και mole) Μια παρουσίαση για την Α Λυκείου ΕΠΑΛ από τον Π.ΑΡΦΑΝΗ, 2011 Μια χημική αντίδραση Κάντε κλικ στην εικόνα Μια χημική αντίδραση Ωραίες οι αντιδράσεις ιδίως αν γίνεται
3, ( 4), ( 3),( 2), 2017
 ΕΡΩΤΗΣΕΙΣ ΘΕΜΑΤΑ ΘΕΩΡΙΑΣ ΣΤΑ ΜΑΘΗΜΑΤΙΚΑ ΤΗΣ Α ΓΥΜΝΑΣΙΟΥ ΑΛΓΕΒΡΑ 1 ο ΚΕΦΑΛΑΙΟ 1. α. Τι γνωρίζετε για την Ευκλείδεια διαίρεση; Πότε λέγεται τέλεια; β. Αν σε μια διαίρεση είναι Δ=δ, πόσο είναι το πηλίκο και
ΕΡΩΤΗΣΕΙΣ ΘΕΜΑΤΑ ΘΕΩΡΙΑΣ ΣΤΑ ΜΑΘΗΜΑΤΙΚΑ ΤΗΣ Α ΓΥΜΝΑΣΙΟΥ ΑΛΓΕΒΡΑ 1 ο ΚΕΦΑΛΑΙΟ 1. α. Τι γνωρίζετε για την Ευκλείδεια διαίρεση; Πότε λέγεται τέλεια; β. Αν σε μια διαίρεση είναι Δ=δ, πόσο είναι το πηλίκο και
ΘΕΩΡΗΤΙΚΗ ΑΣΚΗΣΗ. Διάθλαση μέσω πρίσματος - Φασματοσκοπικά χαρακτηριστικά πρίσματος.
 Ο1 ΘΕΩΡΗΤΙΚΗ ΑΣΚΗΣΗ. Διάθλαση μέσω πρίσματος - Φασματοσκοπικά χαρακτηριστικά πρίσματος. 1. Σκοπός Όταν δέσμη λευκού φωτός προσπέσει σε ένα πρίσμα τότε κάθε μήκος κύματος διαθλάται σύμφωνα με τον αντίστοιχο
Ο1 ΘΕΩΡΗΤΙΚΗ ΑΣΚΗΣΗ. Διάθλαση μέσω πρίσματος - Φασματοσκοπικά χαρακτηριστικά πρίσματος. 1. Σκοπός Όταν δέσμη λευκού φωτός προσπέσει σε ένα πρίσμα τότε κάθε μήκος κύματος διαθλάται σύμφωνα με τον αντίστοιχο
ΕΡΩΤΗΣΕΙΣ ΘΕΩΡΙΑΣ ΜΑΘΗΜΑΤΙΚΑ Β ΓΥΜΝΑΣΙΟΥ. ΜΕΡΟΣ 1ο ΑΛΓΕΒΡΑ
 1. Τι καλείται μεταβλητή; ΕΡΩΤΗΣΕΙΣ ΘΕΩΡΙΑΣ ΜΑΘΗΜΑΤΙΑ Β ΓΥΜΝΑΣΙΟΥ ΜΕΡΟΣ 1ο ΑΛΓΕΒΡΑ Μεταβλητή είναι ένα γράμμα (π.χ., y, t, ) που το χρησιμοποιούμε για να παραστήσουμε ένα οποιοδήποτε στοιχείο ενός συνόλου..
1. Τι καλείται μεταβλητή; ΕΡΩΤΗΣΕΙΣ ΘΕΩΡΙΑΣ ΜΑΘΗΜΑΤΙΑ Β ΓΥΜΝΑΣΙΟΥ ΜΕΡΟΣ 1ο ΑΛΓΕΒΡΑ Μεταβλητή είναι ένα γράμμα (π.χ., y, t, ) που το χρησιμοποιούμε για να παραστήσουμε ένα οποιοδήποτε στοιχείο ενός συνόλου..
ΘΕΩΡΙΑ Α ΓΥΜΝΑΣΙΟΥ. Η διαίρεση καλείται Ευκλείδεια και είναι τέλεια όταν το υπόλοιπο είναι μηδέν.
 ΑΛΓΕΒΡΑ 1 ο ΚΕΦΑΛΑΙΟ ΘΕΩΡΙΑ Α ΓΥΜΝΑΣΙΟΥ 1. Τι είναι αριθμητική παράσταση; Με ποια σειρά εκτελούμε τις πράξεις σε μια αριθμητική παράσταση ώστε να βρούμε την τιμή της; Αριθμητική παράσταση λέγεται κάθε
ΑΛΓΕΒΡΑ 1 ο ΚΕΦΑΛΑΙΟ ΘΕΩΡΙΑ Α ΓΥΜΝΑΣΙΟΥ 1. Τι είναι αριθμητική παράσταση; Με ποια σειρά εκτελούμε τις πράξεις σε μια αριθμητική παράσταση ώστε να βρούμε την τιμή της; Αριθμητική παράσταση λέγεται κάθε
Στοιχειομετρικοί Υπολογισμοί στη Χημεία
 Στοιχειομετρικοί Υπολογισμοί στη Χημεία Δομικές μονάδες της ύλης ΑΤΟΜΑ ΜΟΡΙΑ ΣΤΟΙΧΕΙΑ ΕΝΩΣΕΙΣ Αριθμός Avogadro N A = 6,02 10 23 mol -1 Δηλαδή αυτός ο αριθμός παριστάνει την ποσότητα μιας ουσίας που περιέχει
Στοιχειομετρικοί Υπολογισμοί στη Χημεία Δομικές μονάδες της ύλης ΑΤΟΜΑ ΜΟΡΙΑ ΣΤΟΙΧΕΙΑ ΕΝΩΣΕΙΣ Αριθμός Avogadro N A = 6,02 10 23 mol -1 Δηλαδή αυτός ο αριθμός παριστάνει την ποσότητα μιας ουσίας που περιέχει
ΚΕΦΑΛΑΙΟ 8 IAΣTOΛH KAI ΣYΣTOΛH
 ΚΕΦΑΛΑΙΟ 8 IAΣTOΛH KAI ΣYΣTOΛH 8.1 Γραµµική διαστολή των στερεών Ένα στερεό σώµα θεωρείται µονοδιάστατο, όταν οι δύο διαστάσεις του είναι αµελητέες σε σχέση µε την τρίτη, το µήκος, όπως συµβαίνει στην
ΚΕΦΑΛΑΙΟ 8 IAΣTOΛH KAI ΣYΣTOΛH 8.1 Γραµµική διαστολή των στερεών Ένα στερεό σώµα θεωρείται µονοδιάστατο, όταν οι δύο διαστάσεις του είναι αµελητέες σε σχέση µε την τρίτη, το µήκος, όπως συµβαίνει στην
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ
 ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ Μαρία Περράκη, Επίκουρη Καθηγήτρια ΑΔΕΙΑ ΧΡΗΣΗΣ Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ Μαρία Περράκη, Επίκουρη Καθηγήτρια ΑΔΕΙΑ ΧΡΗΣΗΣ Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Εργαστήριο Τεχνολογίας Υλικών
 Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 02 Μεταλλογραφική Παρατήρηση Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ ΘεόδωροςΛούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών Πάτρα 2011
Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 02 Μεταλλογραφική Παρατήρηση Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ ΘεόδωροςΛούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών Πάτρα 2011
