Antibakterijski lijekovi
|
|
|
- Ἀντιόπη Γιαννόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 POGLAVLJE 15 Antibakterijski lijekovi Branka Bedenić Lijekovi se koriste za liječenje infektivnih bolesti još od 17. stoljeća (kinin za liječenje malarije, emetin za amebijazu). Međutim, kemoterapija kao znanost, s razumijevanjem principa selektivne toksičnosti, specifične kemijske veze između mikrobnog patogena i lijeka, razvoja bakterijske rezistencije na antibiotike i uloge kombinirane terapije, započinje se razvijati u prvom desetljeću XX stoljeća. Prvi planirani kemoterapijski postupak je doveo do upotrebe arsena za liječenje luesa. Diferencijalno bojenje tkiva i bakterija je bilo temelj istraživanja kemoterapije jer se pokazalo da se kemijski spojevi drukčije odnose prema domaćinu nego prema infeckcioznom agensu, što se pokazalo kao osnova selektivne toksičnosti. Tako je Paul Ehrlich godine ukazao na potrebu pronalaska tvari koje će imati veću moć uništavanja mikroorganizma nego oštećenja tkiva domaćina, čime bi se omogućilo razaranje mikroorganizma bez veće štete za makroorganizam. Era antimikrobne kemoterapije je počela godine otkrićem sulfonamida. Penicilin je otkriven godine, kada je A. Fleming primijetio da je plijesan, koja je kontaminirala kulturu stafilokoka, razorila okolne porasle kolonije bakterija. Taj filtrat bujonske kulture plijesni je nazvao penicilin i utvrdio je da on ima antibakterijski učinak. Chain i Florey su godine pročistili penicilin i utvrdili njegovu djelotvornost i izrazito malu toksičnost u eksperimentalnim infekcijama. Godine penicilin je prvi puta korišten kao terapijski agens kod bolesnika koji je imao brojne apscese na koži i u plućima, što je dovelo do pada temperature i povlačenja apscesa. Prije primjene na bolesniku, penicilin je testiran na osobi oboljeloj od karcinoma dojke u terminalnom stadiju i utvrđeno je da nema značajnih nuspojava osim laganog povišenja temperature. Tokom narednih 25 godina istraživanja kemoterapijskih agenasa su se fokusirala na supstance mikrobnog porijekla koje se nazvane antibiotici. Na- Sažetak Terminologija koja se koristi kod opisivanja antimikrobne aktivnosti lijekova Spektar antibakterijskog djelovanja: opseg aktivnosti antimikrobijalnog agensa protiv bakterija; antibakterijski agensi širokog spektra inhibiraju razli~ite gram-pozitivne i gram-negativne bakterije; antibakterijski agensi uskog spektra su aktivni samo protiv ograni~enog broja bakterija Bakteriostatska aktivnost: razina antimikrobijalne aktivnosti koja inhibira rast bakterije; odre uje se in vitro testiranjem aktivnosti standardizirane koncentracije bakterija u serijskim razrje enjima antibiotika; najniža koncentracija antibiotika koja inhibira rast bakterija naziva se minimalna inhibitorna koncentracija (MIK) Baktericidna aktivnost: razina antimikrobijalne aktivnosti koja ubija testiranu bakteriju; odre uje se in vitro testiranjem aktivnosti standardizirane koncentracije bakterija u serijskim razrje enjima antibiotika; najniža koncentracija antibiotika koja ubija 99,9% bakterija se naziva minimalna baktericidna koncentracija (MBK) Kombinirana terapija koristi se: da bi se proširio antibakterijski spektar kod empirijske terapije ili kod terapije polimikrobijalnih infekcija; da bi se prevenirao nastanak rezistentnih bakterija tokom terapije ili da se postigne sinergisti~ko djelovanje u cilju uništenja uzro~nika Sinergizam: kombinacija dva antibiotika koji, kada se testiraju skupa, imaju poja~anu baktericidnu aktivnost u odnosu na aktivnost svakog pojedina~nog antibiotika Antagonizam: kombinacija antibiotika, u kojoj jedan interferira s djelovanjem drugoga (zbir ukupne aktivnosti je manji nego najaktivniji pojedina~ni lijek) β-laktamaze: enzim koji hidrolizira β-laktamski prsten β-laktamske grupe antibiotika i inaktiviraju antibiotik; enzimi specifi~ni za peniciline, cefalosporine i karbapeneme su penicilinaze, cefalosporinaze i karbapenemaze (metaloβ-laktamaze) 221
2 Antibakterijski lijekovi Poglavlje 15 kon izolacije, koncentracije, purifikacije i masovne proizvodnje penicilina došlo je do otkrića cefalosporina i kasnije streptomicina, tetraciklina, kloramfenikola i mnogih drugih lijekova. Ove supstancije su izolirane iz filtrata kultura plijesni. Sintetska modifikacija tih originalnih supstanci dovela je do razvoja novih antimikrobnih lijekova (Sažetak 15.1). Mehanizmi djelovanja antimikrobnih lijekova Nekoliko je mehanizama djelovanja antimikrobnih lijekova: selektivna toksičnost, inhibicija sinteze staničnog zida bakterije, inhibicija sinteze proteina i inhibicija sinteze nukleinskih kiselina (Slika 15.1). SELEKTIVNA TOKSIČNOST Idealni antimikrobni agens iskazuje selektivnu toksičnost, što znači da je lijek štetan za patogena, ali ne i za domaćina. Selektivna toksičnost je obično relativna, a ne apsolutna, što znači da lijek u koncentracijama koje domaćin tolerira može uništititi infekciozni agens. Selektivna toksičnost je funkcija specifičnih receptora potrebnih za vezanje lijeka koji se nalaze na stanici mikroorganizma, ali ne i domaćina, ili može ovisiti o inhibiciji biokemijskih reakcija neophodnih za patogena, ali ne i za čovjeka. INHIBICIJA SINTEZE STANIČNOG ZIDA Bakterije imaju čvrsti stanični zid koji održava njihov oblik i veličinu, te ih ujedno štiti od mehaničkih i osmotskih oštećenja. Osmotski tlak unutar bakterijske stanice je veći nego izvan nje, tako da ozljede staničnog zida (npr. uslijed djelovanja lizozima ili inhibicije sinteze staničnog zida zbog učinka antibiotika) mogu dovesti do lize stanice. U hipertoničnoj otopini (npr. 20% saharoza), oštećeno oblikovanje staničnog zida dovodi do stvaranja protoplasta u gram-pozitivnih bakterija (oblici bakterije bez staničnog zida), ili sferoplasta u gram-negativnih bakterija, te su ovi oblici omeđeni jedino krhkom citoplazmatskom membranom. Ako protoplaste ili sferoplaste stavimo u normotoničan medij oni upijaju tekućinu, bubre i prsnu. Uzorci bolesnika koji su bili tretirani antibioticima inhibitorima sinteze staničnog zida često sadržavaju oštećene ili deformirane bakterije. Stanični zid bakterija sadržava polimer koji se naziva peptidoglikan (Poglavlje 9 Građa i struktura bak- Slika Mjesta djelovanja antibiotika u bakterijskoj stanici 222
3 B. Bedeni} terija). Čvrstoća peptidoglikana postiže se poprečnim umrežavanjem polipeptidnih lanaca (kroz pentaglicinske veze) kao rezultat traspeptidacijske reakcije koju kataliziraju različiti enzimi. U gram-pozitivnih bakterija je sloj peptidoglikana mnogo deblji nego u gram-negativnih bakterija. Svi β-laktamski antibiotici su selektivni inhibitori sinteze bakterijskog staničnog zida i zbog toga su aktivni samo prema bakterijama koje su u stadiju razmnožavanja. Prvi korak u djelovanju β-laktamskih antibiotika je vezanje na receptore koji vežu penicilin (penicilin binding protein, PBP), a koji se nalaze na citoplazmatskoj membrani bakterija i imaju funkciju transpeptidaza. Pojedini receptori imaju različit afinitet vezanja na određene β-laktamske antibiotike i imaju različite učinke. Vezanje na neke PBP molekule uzrokuje elongaciju bakterijskih stanica, dok neki drugi PBP receptori uzrokuju lizu bakterijskih stanica. Mutacije PBP molekula mogu dovesti do smanjenog afiniteta vezanja pojedinih β-laktamskih antibiotika, a to može dovesti do pojave rezistencije. Nakon što se β-laktamski antibiotik vezao na receptor dolazi do inhibicije transpeptidacijske reakcije i do prestanka sinteze peptidoglikana. Sljedeći korak uključuje odstranjenje ili inaktivaciju inhibitora autolitičkih enzima u stijenci bakterije. To aktivira litičke enzime i dolazi do lize bakterija u izotoničnom mediju. U hipertoničnom mediju bakterije prelaze u protoplaste i sferoplaste koji su prekriveni samo s tankom citoplazmatskom membranom. U takvim stanicama se još neko vrijeme odvija sinteza proteina i nukleinskih kiselina. Innhibicija transpeptidaza nastaje zbog strukturne sličnosti penicilina i cefalosporina s acil- D-alanil-Dalaninom koji je strukturna komponenta peptidoglikana. Transpeptidacijska reakcija uzrokuje gubitak D-alanina iz pentapeptida. Nedostatak toksičnosti β-laktamskih antibiotika za sisavce tumači se činjenicom da u stanicama sisavaca ne postoji peptidoglikan. Razlike u osjetljivosti prema pojedinim penicilinima i cefalosporinima između gram-pozitivnih i gram-negativnih bakterija ovise o strukturnim različitostima (količina peptidoglikana, prisutnost receptora, prirodno poprečno umrežavanje, aktivnost autolitičkih enzima), koje određuju penetraciju, vezanje i aktivnost ovih lijekova. INHIBICIJA FUNKCIJE CITOPLAZMATSKE MEMBRANE Citoplazma bakterija je okružena citoplazmatskom membranom koja služi kao selektivna permeabilna barijera, vrši aktivni transport i kontrolira unutarnji sastav bakterijske stanice (vidi Poglavlje 8 Morfologija bakterija, struktura i sinteza staničnog zida). Ukoliko se poremeti funkcionalni integritet citoplazmatske membrane, makromolekule i ioni će izlaziti iz bakterijske stanice i uslijedit će oštećenje ili smrt bakterije. Citoplazmatska membrana bakterija i gljiva se razlikuje po svom sastavu od stanične citoplazmatske membrane animalnih stanica i može se lakše oštetiti djelovanjem određenih agenasa, što predstavlja temelj selektivne toksičnosti. Primjer takvog mehanizma je djelovanje polimiksina na gram-negativne bakterije i poliena na gljive. Za djelovanje poliene je potrebno da se oni vežu na sterol koji je prisutan u stanicama gljiva, ali ga nema u bakterijskoj citoplazmatskoj membrani. Iz toga proizlazi da polieni nisu djelotvorni prema prema bakterijama, a polimiksini nisu djelotvorni prema prema gljivama. INHIBICIJA SINTEZE PROTEINA Makrolidi, tetraciklini, aminoglikozidi i kloramfenikol inhibiraju sintezu proteina u bakterijskoj stanici. Aminoglikozidi djeluju tako što se vežu na receptore na 30S podjedinici ribosoma i sprječavaju vezanje glasničke RNK (mrnk) na ribosom i stvaranje inicijacijskog kompleksa. Drugi mehanizam djelovanja antibiotika je pogrešno očitavanje genetskog koda što dovodi do ugrađivanja krivih aminokiselina u polipeptidni lanac i sinteze nefunkcionalnih bjelančevina koje ne mogu vršiti svoju ulogu kao enzimi ili strukturni elementi bakterijske stanice. Treće, vezanje aminoglikozida dovodi do pucanja polisoma i nastanka monosoma koji ne mogu vršiti sintezu bjelančevina. Kromosomska rezistencija na aminoglikozide nastaje zbog nedostatka specifičnog proteinskog receptora na 30S podjedinici ribosoma. Plazmidna rezistencija na aminoglikozide ovisi o produkciji enzima koji modificiraju molekulu aminoglikozida adenilacijom, fosforilacijom ili acetilacijom. Tako modificirana molekula nema antibakterijsko djelovanje. Treći mehanizam rezistencije je smanjena permeabilnost zbog gubitka porina vanjske membrane tako da je reduciran aktivni trasport molekule aminoglikozida u citoplazmu bakterijske stanice. Treba naglasiti da kod anaerobnih bakterija postoji intrinzična (svojstvena, urođena) rezistencija na aminoglikozide zbog nedostatka aktivnog transportnog sistema koji unosi molekulu aminoglikozida u bakterijsku stanicu. 223
4 Antibakterijski lijekovi Poglavlje 15 Makrolidi i azalidi inhibiraju sintezu proteina vezanjem na 50S podjedinicu ribosoma, a mjesto vezanja je 23S rrnk (ribosmske RNK). Oni interferiraju sa stvaranjem inicijacijskog kompleksa ili s aminoacil translokacijskom reakcijom. Rezistencija na makrolide nastaje zbog nedostatka receptora na ribosomu kroz metilaciju rrnk. Rezistencija može biti pod kromosomskom ili plazmidnom kontrolom. Klindamicin se veže na 50S podjedinicu ribosoma. Rezistencija na klindamicin nastaje zbog promijenjenog receptora na 50S podjedinici ribosoma uslijed mutacije kromosomskih gena. Tetraciklini se vežu na 30S podjedinicu ribosoma i inhibiraju sintezu bjelančevina blokiranjem vezanja aminoacil-trnk (transportna RNK) na ribosom. Na taj način oni sprječavaju ugradnju nove aminokiseline u rastući polipeptidni lanac. Djelovanje je inhibitorno i reverzibilno nakon što se lijek ukloni. Rezistencija na tetracikline nastaje zbog efluksa ili impermeabilnosti za lijek. Tetraciklini se unose u bakterijsku stanicu pomoću aktivnog transporta, tako da su koncentracije lijeka puno veće u stanici nego izvan nje. Stanice sisavaca nemaju ovakav aktivni transportni sistem, tako da tetraciklini nemaju značajan učinak na sintezu bjelančevina u humanim stanicama. INHIBICIJA SINTEZE NUKLEINSKIH KISELINA Antibiotici koji djeluju na sintezu nukleinskih kiselina u bakterija su kinoloni, pirimetamin, rifampicin, sulfonamidi i trimetoprim. Rifampicin inhibira rast bakterija vezanjem na DNK- ovisnu RNK-polimerazu bakterija. Na taj način inhibira sintezu bakterijske RNK. Kinoloni inhibiraju sintezu bakterijske DNK blokiranjem enzima DNK-giraze. Sulfonamidi i trimetoprim ometaju metabolizam folne kiseline, pa djeluju kao antifolati. P-aminobenzojeva kiselina (PABA) je esencijalni metabolit za sintezu purinskih baza u mnogih mikroorganizama. Način djelovanja PABA je kondenzacija pteridina u dihidropteronsku kiselinu i ovisna je o adenozin-trifosfatu (ATP). Dihidropteronska kiselina se pretvara u folnu kiselinu koja je prekursor nukleinskih kiselina. Sulfonamidi koji su strukturno slični PABA inhibiraju sintetazu dihidropteroata. Sulfonamidi ulaze u reakciju umjesto PABA i natječu se za aktivni centar enzima. Kao rezultat nastaje nefunkcionalni analog folne kiseline, što sprječava razmnožavanje bakterija. Učinak sulfonamida može se poništiti u prisustvu velike količine PABA mehanizmom kompetitivne inhibicije. Animalne stanice ne sintetiziraju vlastitu folnu kiselinu nego ju dobivaju iz vanjskih izvora, te usljed toga nisu ugrožene antimetaboličkim učinkom sulfonamida. Također, neke bakterije koje ne sintetiziraju vlastitu folnu kiselinu nisu inhibirane sulfonamidima. Trimetoprim inhibira dihidrofolat reduktazu, puta jače u bakterija nego u stanica sisavaca. Enzim dihidrofolat-reduktaza pretvara (konvertira) dihidrofolnu kiselinu u tetrahidrofolnu kiselinu, što je slijedeći korak u sintezi purina i bakterijske DNK. Sulfonamidi i trimetoprim mogu se koristiti pojedinačno za inhibiciju rasta bakterija, ali ako se primjenjuju zajedno postiže se sinergistički učinak blokadom dviju uzastopnih reakcija u sintezi nukleinskih kiselina. Takva kombinacija sulfonamida i trimetoprima (omjer 5:1) koristi se za liječenje pneumocistis-pneumonije, malarije, bacilarne dizenterije, sistemskih salmoneloza, te infekcija urinarnog i respiratornog trakta. Pirimetamin inhibira dihidrofolat reduktazu, ali jače od trimetoprima djeluje i na enzim u animalnim stanicama, tako da je toksičniji od trimetoprima. Pirimetamin u kombinaciji sa sulfonamidom primjenjuje se za terapiju toksoplazmoze i drugih protozoarnih infekcija. Rezistencija na antimikrobne lijekove MEHANIZMI BAKTERIJSKE REZISTENCIJE NA ANTIBIOTIKE Postoje različiti mehanizmi pomoću kojih bakterije postaju otporne na antibiotike. Proizvodnja enzima pomoću kojih se mijenja struktura antibiotika Stafilokoki rezistentni na penicilin G proizvode enzim β-laktamazu koji razara β-laktamski prsten u penicilinu, te nastaje peniciloična kiselina koja nema antibakterijski učinak. Gram-negativne bakterije proizvode različite β-laktamaze koje se po svom supstratnom profilu dijele na penicilinaze, cefalosporinaze i β-laktamaze širokog spektra. Β-laktamaze proširenog spektra su odgovorne za rezistenciju na oksimino-cefalosporine i monobaktame, proširene su najviše među hospitalnim izolatima K. pneumoniae i E. coli, a javljaju se, 224
5 B. Bedeni} premda rjeđe, i kod ostalih enterobakterija i nefermentativnih bakterija. Većina β-laktamaza proširenog spektra spada u TEM i SHV porodicu, a u novije vrijeme sve više izolata posjeduje i CTX-M β-laktamaze, koje se tipično javljaju u izvanbolničkoj populaciji. Osjetljive su na inhibiciju klavulanskom kiselinom i ostalim suicidnim (samoubilačkim, molekula inhibitora biva uništenja nakon vezanja na beta-laktamazu) inhibitorima, kao što su sulbaktam i tazobaktam. Karbapenemaze su bakterijski enzimi koji hidroliziraju karbapeneme, a dijele se na: karbapenemaze grupe A, koje su inhibirane klavulanskom kiselinom, karbapenemaze grupe B ( metalo-β-laktamaze), koje sadržavaju cink kao kofaktor i osjetljive su na inhibiciju kelatorima metalnih iona, kao što su EDTA i merkaptopropionska kiselina, te karbapenemaze grupe D (oksacilinaze). Najviši stupanj rezistencije na karbapeneme izazivaju metalo β-laktamaze koje se najčešće javljaju u izolatima P. aeruginosa, a kodirane su prenosivim genetskim elementima, kao što su integroni koji obično sadržavaju i gene rezistencije na ne-β-laktamske antibiotike, kao što su aminoglikozidi. Oksacilinaze i karbapenemaze grupe A uzrokuju klinički manifestnu rezistenciju na karbapeneme jedino u kombinaciji s ostalim mehanizmima rezistencije kao što su gubitak porina vanjske membrane ili efluks. Budući da se geni koji kodiraju te enzime obično nalaze na kromosomu, taj tip rezistencije nije prenosiv i ne predstavlja opasnost epidemijskog širenja, kao što je slučaj kod metalo β-laktamaza ili β-laktamaza proširenog spektra. Gram-negativne bakterije stječu rezistenciju na aminoglikozide proizvodnjom enzima koji mijenjaju strukturu aminoglikozida tako što vrše adenilaciju, fosforilaciju ili acetilaciju molekule, a modificirani produkt nema antibakterijsko djelovanje. Promjena permeabilnosti za lijekove Promjene u strukturi porina vanjske membrane mogu dovesti do smanjene propusnost za β-laktamske antibiotike. Tetraciklini se akumuliraju u osjetljivim bakterijama, ali ne u rezistentnim. Rezistencija na polimiksine je također posljedica impermeabilnosti za te lijekove. Anaerobne bakerije imaju intrinzičnu rezistenciju na aminoglikozide jer im nedostaje aktivni transportni sistem koji je ovisan o citokromu. Modificiranje receptorske molekule za antibiotike Promjene PBP molekula onemogućuju vezanje β-laktamskih antibiotika ili se oni vežu sa smanjenim afinitetom, tako da ne može doći do inhibicije transpeptidaza koje su važne za poprečno umrežavanje molekule peptidoglikana. Rezistencija na peniciline u S. pneumoniae i enterokoka nastaje zbog promjene ili gubitka PBP molekula. Eritromicin-rezistentni organizmi imaju promjenjeni receptor na 50S podjedinici ribosoma zbog metilacije 23S ribosomske RNA. Prelazak na metabolički put koji zaobilazi reakciju inhibiranu lijekom Bakterije rezistentne na sulfonamide ne trebaju ekstracelularnu PABA, nego poput stanica sisavaca koriste preformiranu folnu kiselinu iz okoliša. Proizvodnja drugih enzima Proizvodnja drugih enzima koji su daleko manje osjetljivi na lijek, ali koji mogu izvršiti svoju metaboličku funkciju. U bakterija rezistentnih na trimetoprim enzim dihidrofolat-reduktaza je mnogo slabije osjetljiva na inhibiciju trimetoprimom nego u trimetoprim-osjetljivih bakterija. PORIJEKLO REZISTENCIJE NA ANTIMIKROBNE LIJEKOVE Većina antibiotika djeluje na bakterije u fazi njihovog aktivnog razmnožavanja. Kao posljedica toga, mikroorganizmi koji su metabolički inaktivni i nisu u fazi razmnožavanja postaju otporni na učinak lijekova. Primjer: mikobakterije u tkivu mogu ostati žive mnogo godina nakon infekcije, ali se uslijed obrambenih mehanizama domaćina ne umnožavaju. Takvi perzistirajući sojevi su rezistentni na antituberkulotike i ne mogu biti eradicirani lijekovima. Međutim, ako se oni u jednom trenutku započnu razmnožavati (npr. zbog smanjenja staničnog imuniteta), tada postaju potpuno osjetljivi na terapiju. Slično, β-laktamski antibiotici djeluju samo na bakterije koje se nalaze u eksponencijalnoj fazi razmnožavanja, kada dolazi do aktivne sinteze staničnog zida. Mikroorganizmi mogu izgubiti ciljnu strukturu za antibiotik i na taj način postati rezistentni. Na primjer, na penicilin osjetljivi mikroorganizmi, tokom terapije penicilinom, mogu preći u L-oblike. Budući da L-oblici nemaju staničnog zida, oni postaju otporni na inhibitore sinteze peptidoglikana, kao što su penicilini i cefalosporini, te ostaju otporni kroz nekoliko generacija. Kada takvi oblici ponovno uspostave sintezu peptidoglikana i pređu u svoje parentalne oblike, ponovno se uspostavi i osjetljivost na penicilin. 225
6 Antibakterijski lijekovi Poglavlje 15 Mikroorganizmi mogu izazvati infekciju na mjestima gdje se antimikrobni lijekovi izlučuju, ali se nalaze u inaktivnom obliku. Na primjer, aminoglikozidi, kao što su gentamicin ili tobramicin, nisu učinkoviti u liječenju salmonela groznica, budući da su salmonele smještene intracelularno, a aminoglikozidi ne ulaze u stanicu. Slično tome, samo antibiotici koji postižu visoke intracelularne koncentracije, kao što su tetraciklini, djeluje na intracelularno smještene bakterije kao što su brucele, listerije ili legionele. Većina mikroorganizama rezistentnih na antibiotike nastaje kao rezultat genetskih promjena i posljedične selekcije rezistentih mutanata pod utjecajem antimikrobnih lijekova. Kromosomska rezistencija Nastaje kao rezultat spontanih mutacija u kromosomskom lokusu koji kontrolira osjetljivost na određeni antimikrobni lijek. Prisutnost antimikrobnog lijeka djeluje kao selekcijski mehanizam koji suprimira rast osjetljivih organizama i daje prednost rezistentnom mutantu. Spontane mutacije se događaju rijetko, s frekvencijom od do 10-7, i zbog toga nisu često uzrok pojave antimikrobne rezistencije. Međutim, kromosomske mutacije koje dovode do rezistencije na rifampicin događaju se s visokom frekvencijom, od 10-7 do 10-5 (vidi Poglavlje 10 Genetika bakterija). Kao posljedica toga, terapija samim rifampicinom često ne uspjeva. Kromosomske mutacije najčešće dovode do promjene strukture receptora za određeni antibiotik. Na primjer, protein P12 na 30S podjedinici ribosoma služi kao receptor za streptomicin. Mutacije gena koji kodira taj strukturni protein rezultiraju u nemogućnosti vezanja streptomicina na receptor. Mutacije mogu uzrokovati gubitak PBP molekula ili nemogućnost vezanja β-laktamskih antibiotika na ove molekule što dovodi do rezistencije na β-laktamske antibiotike. Ekstrakromosomska rezistencija Bakterije često sadržavaju ekstrakromosomske genetske elemente koji se nazivaju plazmidi. Neki plazmidi nose gene rezistencije na jedan ili više antimikrobnih lijekova. Plazmidni geni za antimikrobnu rezistenciju obično kodiraju sintezu enzima koji mijenjaju strukturu antimikrobnih lijekova. Tako npr. β-laktamaze razgrađuju β-laktamski prsten, a enzimi koji modificiraju strukturu aminoglikozida čine to fosforilacijom, nukleotidilacijom ili adenilacijom molekule. Produkt enzimske razgradnje obično nema antimikrobnu aktivnost. Plazmidi se mogu prenijeti iz jedne bakterijske stanice u drugu konjugacijom ili transdukcijom. Osim na plazmidima, geni rezistencije mogu bili locirani i na integronima koji često sadržavaju gene koji kodiraju produkciju metalo-β-laktamaza (bakterijskih enzima koji razgrađuju karbapeneme). Integroni često sadržavaju osim gena za metalo β-laktamaze i gene rezistencije za aminoglikozide (vidi Poglavlje 10 Genetika bakterija). Unakrsna rezistencija Mikroorganizmi rezistentni na određeni antibiotik također mogu biti otporni i na ostale antibiotike iz iste skupine koji djeluju istim mehanizmom. Takva veza postoji među agensima koji su kemijski srodni, npr. različiti aminoglikozidi, ili kod onih koji imaju isti mehanizam djelovanja, npr. makrolidi i linkomicini. U nekih skupina antibiotika je aktivna jezgra toliko slična među različitim predstavnicima, da postoji vrlo izražena unakrsna rezistencija, kao što je slučaj u tetraciklina. MJERE ZA OGRANIČENJE ANTIMIKROBNE REZISTENCIJE Pojava rezistencije na antimikrobne lijekove može se smanjiti: održavanjem dovoljno visokih koncentracija antibiotika u tjelesnim tekućinama i tkivima za inhibiciju izvorne populacije bakterija i mutanata prvog stupnja; istovremenom primjenom dva ili više lijekova koji nemaju unakrsnu rezistenciju (npr. rifampicin i izonijazid za liječenje tuberkuloze); smanjenjem izlaganja mikroorganizama anti bioticima koji se koriste kao rezervni antibiotici u bolnicama i čiju djelotvornost treba zaštititi ograničenjem upotrebe. KLINIČKE IMPLIKACIJE REZISTENCIJE NA ANTIBIOTIKE Neisseria gonorrhoeae. Kada su sulfonamidi prvi puta uvedeni u terapiju gonoreje u kasnim tridesetim godinama prošlog stoljeća, praktički svi izolati gonokoka bili su osjetljivi na ove lijekove i većina infekcija je bila izlječena. Nekoliko godina kasnije većina izolata je postala otporna i gonoreja se rijetko mogla liječiti sulfonamidima. Većina gonokoka u to vrijeme bila je još uvijek vrlo osjetljiva na penicilin. Tokom slijedećih decenija postepeno se povećavala rezistencija i na penicilin, ali su visoke doze još uvijek bile djelotvorne. U 70-im godina prošlog stoljeća 226
7 B. Bedeni} pojavili su se β-laktamaza producirajući izolati gonokoka, prvo na Filipinima i u Zapadnoj Africi, a kasnije su se proširili diljem svijeta. Gonoreja se nakon toga prestala liječiti penicilinom, te je u terapiju uveden spektinomicin na kojeg je većina izolata bila osjetljiva. Nakon što se pojavila rezistencija i na spektinomicin, u terapiju gonoreje uvedeni su cefalosporini treće generacije i fluorokinoloni, koji i danas predstavljaju antibiotike izbora za tu infekciju. Neisseria meningitidis. Do godine meningokoki su bili uniformno osjetljivi na sulfonamide tako da su ovi lijekovi bili pogodni i za liječenje, i za profilaksu bolesti. Nakon pojave izolata rezistentnih na sulfonamide, oni su izgubili svoju djelotvornost u liječenju i prevenciji meningokoknih infekcija. Penicilin je nakon toga uveden kao antibiotik za liječenje meningokoknog meningitisa i sepse, ali je došlo do pojave rezistencije i na taj antibiotik tako da je danas ceftriakson lijek izbora, budući nije zabilježena rezistencije na ovaj antibiotik i zbog toga što dobro prodire u likvor. Rifampicin se koristi za profilaksu, ali se rezistencija na njega pojavljuje u oko 1% izolata meningokoka ako je osoba dobivala profilaksu. Staphylococcus spp. Kada je godine započela klinička primjena penicilina, većina izolata stafilokoka bila je osjetljiva na ovaj antibiotik godine, nakon početka masovne upotrebe penicilina, 85% hospitalnih izolata je pokazivalo rezistenciju zbog produkcije β-laktamaze. Uvođenje β-laktamaza stabilnih penicilina, kao što su meticilin, nafcilin, kloksacilin itd., pokazalo se kao privremeno rješenje dok se nisu pojavili meticilin rezistentni stafilokoki (MRSA). MRSA izolati su rezistentni na sve β-laktamske antibiotike tako da se u terapiji obično koriste glikopeptidi (vankomicin ili teikoplanin). Rezistencija na vankomicin je još uvijek rijetka u stafilokoka, ali postoji sve više izvještaja o takvim sojevima, tako da je za očekivati da će to biti terapijski problem u budućnosti (vidi Poglavlje 17 Staphylococcus, Micrococcus i drugi katalaza-pozitivni koki). Streptococcus pneumoniae. Ova bakterija bila je potpuno osjetljiva na penicilin do godine kada su pronađeni penicilin-rezistentni pneumokoki otkriveni na Novoj Gvineji, a nakon toga i u Južnoj Africi, Japanu, Španjolskoj, te kasnije diljem svijeta. U SAD-u je 5 do 10% pneumokoka otporno na penicilin G (MIK >2 mg/l), a 20% sojeva je umjereno otporno (MIK 0.1 do 1 mg/l). Rezistencija na penicilin nastaje zbog promijenjenih PBP molekula, koje ne mogu vezati penicilin. Pneumokoki su, također, često otporni na kotrimoksazol (sulfometoksazol/trimetoprim), eritromicin i tetracikline. Enterococcus. Enterokoki imaju intrinzičnu rezistenciju na veliki broj antibiotika: cefalosporine, klindamicin, sulfonamide i trimetoprim. Oni, također, imaju stečenu rezistenciju na veliki broj antimikrobnih lijekova: na β-laktamske antibiotike zbog gubitka PBP molekula, visoki stupanj rezistencije na aminoglikozide, fluorokinolone, makrolide, azalide i tetracikline. Neki sojevi enterokoka su stekli plazmide koji kodiraju sintezu β-laktamaza, pa su potpuno rezistentni na ampicilin i penicilin G. Najveće značenje ima razvoj rezistencije na vankomicin kod enterokoka koja se sve više širi po Europi i sjevernoj Americi, premda postoje geografske varijacije u prevalenciji vankomicin-rezistentnih enterokoka. Enterococcus faecium je vrsta koja najčešće stječe rezistenciju na vankomicin. U novije vrijeme među enterokokima se pojavila i rezistencija na streptogramine (quinupristin-dalfopristin). Gram-negativne crijevne bakterije. Rezistencija na lijekove u enterobakterija je većinom posljedica masovne transmisije plazmida koji nose gene rezistencije na antibiotike. Oko 50% izolata šigela u nekim geografskim područjima danas je multiplo rezistentno na nekoliko antibiotika. Animalni izolati salmonela su često otporni na tetracikline koji se dodaju u hranu za životinje. Dodatak antibiotika u animalnu hranu povećava fekalno kliconoštvo multiplo-rezistentnih enterobakterija. Masovna primjena antibiotika u bolnicama je dovela do supresije osjetljivih mikroorganizama u crijevima i proliferacije rezistentnih mikroorganizama koji sadržavaju R plazmide, kao što su npr. izolati K. pneumoniae i E. coli koji proizvode β-laktamaze proširenog spektra. Mikobakterije. Primarna rezistencija se događa u M. tuberculosis u 10% izolata i to najčešće na izonijazid i streptomicin, a rjeđe na rifampicin i etambutol. Izonijazid i rifampicin su najčešće korišteni antituberkulotici u terapiji, ostali lijekovi prvog izbora su pirazinamid, etambutol i streptomicin. Da bi se spriječila pojava rezistencije važno je primjenjivati trojnu terapiju. Najviše stope rezitencije na antituberkulotike zabilježene su u Aziji. Neredovito uzimanje lijekova je najčešći uzrok pojave rezistencije tokom terapije. 227
8 Antibakterijski lijekovi Poglavlje 15 Određivanje antimikrobne aktivnosti in vitro Antimikrobna aktivnost se određuje in vitro da bi se odredila: djelotvornost antibiotika u otopini, koncentracija u tjelesnim tekućinama i tkivima, i osjetljivost testiranog mikroorganizma in vitro. FAKTORI KOJI UTJEČU NA ANTIMIKROBNU AKTIVNOST IN VITRO Stupanje kiselosti (ph) medija utječe na antimikrobnu aktivnost in vitro, npr. nitrofurantoin je djelotvorniji u kiselom ph, dok su aminoglikozidi i sulfonamidi aktivniji uz alkalni ph. Sastav medija. Neki spojevi, kao što su natrijev poliensulfat, koji se dodaje u podloge za hemokulture, i ostali anionski detergenti inhibiraju aktivnost aminoglikozida. PABA antagonozira učinak sulfonamida. Serumski proteini vežu peniciline u rasponu od 40% (za meticilin) do 95% (za dikloksacilin). Dodatak natrijevog klorida u podlogu olakšava detekciju meticilin rezistentnog stafilokoka. Stabilnost lijeka. Na sobnoj temperaturi mnogi antimikrobni lijekovi gube svoju aktivnost: penicilini se polagano inaktiviraju, dok aminoglikozidi i ciprofloksacin ostaju stabilni kroz duže vrijeme. Karbapenemi i kombinacije β-laktama i inhibitora β-laktamaza pokazuju izrazitu nestabilnost u otopini. Veličina inokuluma. Testiranje osjetljivosti antibiotika se vrši uz standardnu veličinu inokuluma od 5x10 5 CFU/mL (engl. Colony Forming Units). Porast veličine inokuluma utječe na smanjenje osjetljivosti prema testiranom antibiotiku. Izolati koji proizvode β-laktamazu imaju izražen inokulum efekt kod testiranja njihova osjetljivost na β-laktamske antibiotike, što se tumači činjenicom da veći broj bakterija proizvodi i veću količinu tog enzima koji onda hidrolizira β-laktamske antibiotike podložne hidrolizi tim enzimom. Inokulum efekt je naročito izražen kod penicilina i cefalosporina, dok kod aztreonama i karbapenema ima neznatan učinak. Pored toga, rezistentni mutanti će se pojavljivati mnogo češće ukoliko je populacija bakterija veća. Dužina inkubacije. Kod kratke inkubacije su mnogi mikroorganizmi samo inhibirani, ali ne dolazi do baktericidnog učinka. S druge strane, kod duge inkubacije postoji veća mogućnost da se razviju i razmnože rezistentni mutanti. Metabolička aktivnost mikroorganizma. Bakterije koje su u fazi intenzivnog razmnožavanja su u pravilu osjetljivije na antimikrobne lijekove nego one koje su u fazi mirovanja. Metabolički neaktivni mikroorganizmi mogu preživjeti dugotrajno izlaganje antibioticima. Primjer su metabolički neaktivne mikobakterije u kavernama tuberkuloznih bolesnika koje je gotovo nemoguće uništiti antituberkuloticima ANTIMIKROBNA AKTIVNOST IN VIVO Analiza antimikrobne aktivnosti in vivo je mnogo kompleksnija nego one in vitro. Aktivnost ne ovisi samo o odnosu između antibiotika i bakterije, nego postoji i treći faktor domaćin. Odnos lijeka i bakterije Različiti faktori iz okoliša utječu na mikroorganizam u tijelu koji može biti lociran u različitim tkivima i tjelesnim tekućinama, a koji se razlikuje od uvjeta u umjetnom hranilištu. Odgovor mikrobne populacije na antibiotike u organizmu čovjeka nije tako uniformiran kao kod testiranja u epruveti. Stanje metaboličke aktivnosti. U makroorganizmu je stanje metaboličke aktivnosti bakterija različito; mnoge bakterije egzistiraju na niskom nivou biosintetičke aktivnosti i zbog toga su relativno neosjetljive na učinak antibiotika. Ovi spavajući mikroorganizmi mogu preživjeti visoke koncentracije antibiotika, te mogu uzrokovati klinički recidiv infekcije. Distribucija lijeka. U tijelu čovjeka antimikrobni lijek se nejednoliko distribuira u tkiva i tjelesne tekućine. Mnogi antibiotici ne mogu postići dovoljno visoke koncentracije u središnjem živčanom sistemu. Koncentracije antibiotika u urinu su obično znatno više nego u krvi i ostalim tjelesnim tekućinama. Tkivni odgovor induciran mikroorganizmom može ga zaštititi od djelovanja antibiotika. Nekrotično tkivo ili gnoj mogu adsorbirati antibiotik i spriječiti njegov kontakt s bakterijama. Lokacija mikroorganizma. U ljudskom organizmu bakterije mogu biti locirane unutar stanica. Antibiotici obično slabo prodiru u stanice i zbog toga intracelularne bakterije lako izmaknu djelovanju antibiotika. Tetraciklini postižu podjednake koncentracije unutar stanice kao i u ekstracelularnoj tekućini, dok aminoglikozidi ne prodiru u stanice. Po tome se in vivo uvjeti razlikuju od in vitro djelovanja u epruveti gdje mikroorganizmi dolaze direktno u kontakt s antimikrobnim lijekom. Interferirajuće tvari. Biokemijski okoliš bakterija u živom organizmu je vrlo kompleksan i rezultira u 228
9 B. Bedeni} značajnim interferencijama između tvari koje se nalaze u tkivima i tjelesnim tekućinama i lijekova. Antibiotik se može vezati na krvne stanice, serumske bjelančevine i fosfolipide u tkivu; također može reagirati s nukleinskim kiselinama u gnoju i može biti fizički adsorbiran na eksudate, stanice i nekrotični debris. U nekrotičnom tkivu ph može biti izrazito alkalan i nepovoljan za mnoge antibiotike (npr. za aminoglikozide). Koncentracija antibiotika In vitro je mikroorganizam izložen konstantnim koncentracijama antibiotika, dok u tijelu koncentracija varira ovisno o farmakokinetskim svojstima lijeka i metaboličkim svojstima domaćina. Apsorpcija lijeka iz gastrointestinalnog trakta kod peroralne primjene ili iz tkiva kod parenteralne primjene je varijabilna. Istovremeno s apsorpcijom odvija se i ekskrecija i inaktivacija lijeka. Kao rezultat, koncentracije lijeka fluktuiraju, a mikroorganizmi su izloženi varijabilnim koncentracijama antimikrobnog lijeka. Za razliku od toga, u in vitro testiranjima bakterije su izložene konstantnim koncentracijama antibiotika. Distribucija lijekova varira u različitim tkivima i tjelesnim tekućinama. Neki antibiotici slabo prodiru o određena tkiva (npr. središnji živčani sistem, kosti, prostata) uslijed čega koncentracije lijeka koje se postižu nakon parenteralne primjene mogu biti nedostatne za djelotvornost terapije. S druge strane, na površini kože ili sluznice (zvukovod ili konjuktiva) lokalna (topijska) primjena antibiotika koji se inače slabo resorbiraju omogućuje djelotvorne koncentracije bez štetnih sistemskih nuspojava. Koncentracije antibiotika u urinu su obično mnogo više nego u krvi. Varijabilnost koncentracija. Ključni problem je održavanje terapijske koncentracije lijeka na mjestu gdje se infektivni mikroorganizam umnožava. Koncentracija se mora održavati kroz dovoljno dugo vrijeme da se eradicira mikroorganizam. Zbog intermitentne primjene lijeka i varijabilne apsorpcije i eksrecije koncentracije lijeka na mjestu infekcije fluktuiraju. Da bi se održale dovoljne koncentracije antibiotika kroz dovoljno dugi period treba uzeti u obzir farmakokinetska svojstva antibiotika, individualne varijacije u farmakokinetici kod pojedinih bolesnika, kao i in vitro osjetljivost bakterije i lokaciju infekcije. Ovi faktori su važni da bi se odredilo adekvatno doziranje antibiotika. Ako se daje veća doza antibiotika može se produžiti interval doziranja, a ako se daje manja doza potrebno je davati više doza dnevno da bi se održale adekvatne koncentracije antibiotika. Postantibiotski učinak je odgoda ponovnog razmnožavanja bakterija nakon kratkotrajnog izlaganja antibiotiku. Mnogi antimikrobni lijekovi pokazuju postantibiotski učinak, ali je on najviše izražen kod karbapenema i fluorokinolona. β-laktamski antibiotici, osim karbapenema, ne pokazuju postantibiotski učinak prema gram-negativnim bacilima. Odnos domaćin-patogen Odnos domaćin-patogen se može promjeniti pod utjecajem antimikrobnih lijekova na različite načine. Promjena tkivnog odgovora. Upalni odgovor tkiva na infekciju se može promjeniti ako lijek suprimira umnožavanje mikroorganizma, ali ga ne eliminira iz tijela. Na taj način akutni proces može preći u kronični. Za razliku od toga, supresija upalnog odgovora tkiva oštećenjem stanične imunosti u transplantiranih ili imunokompromitiranih bolesnika uzrokuje povećanu osjetljivost na infekciju i smanjeni odgovor na antimikrobne lijekove. Promjena imunog odgovora. Na imuni odgovor domaćina također može utjecati modificiran tok infekcije nastao primjenom antimikrobnog lijeka. Na primjer, tonzilofaringitis uzrokovan β-hemolitičkim streptokokom grupe A često je popraćen stvaranjem antistreptokoknih protutijela koja mogu reagirati sa sarkolemom mišićnih vlakana srca ili glomerulanom bazalnom membranom i uzrokovati reumatsku groznicu ili poststreptokni glomerulonefritis. Ako se infektivni proces pravovremeno prekine primjenom antimikrobnog lijeka može se prevenirati stvaranje protutijela i pojava reumatske groznice. Primjena lijekova koji eradiciraju bakteriju (penicilin) je djelotvornija nego primjena lijekova koji djeluju bakteriostatski (tetraciklini). Promjena mikrobne flore. Antimikrobni lijekovi ne utječu samo na patogene bakterije nego i na one koje čine normalnu floru makroorganizma. Antibiotici širokog spektra koji se primjenjuju oralno uništavaju fiziološku floru crijeva i predisponirajući su faktor za nastanak crijevne infekcije. U najtežim slučajevima može doći do pseudomembranskog enterokolitisa kojeg uzrokuje C. difficile. Nadalje, u hospitaliziranih bolesnika koji primaju antimikrobnu terapiju dolazi do supresije normalne flore i dolazi do kolonizacije bakterijama iz okoliša koje su često multirezistentne i mogu uzrokovati teške infekcije 229
10 Antibakterijski lijekovi Poglavlje 15 (meticilin-rezistentni stafilokoki ili bakterije iz roda Pseudomonas). U žena koje dobivaju oralno antibiotike dolazi do uništenja normalne vaginalne flore što omogućuje kolonizaciju i namnožavanje gljiva vrste Candida koje dolaze iz debelog crijeva, i kao posljedica nastaje vaginitis. Kod postojanja opstrukcije u urinarnom traktu raste tendencija nastanka infekcije urinarnog trakta. Ako je organizam osjetljiv (E. coli), a terapija provedena adekvatnim antibiotikom, dolazi do eradikacije bakterije. U nekim slučajevima dolazi do reinfekcije drugom gram-negativnom bakterijom otpornom na primjenjivani antibiotik i ona zauzima mjesto one bakterije koja je eradicirana primjenom antimikrobnog lijeka. Klinička primjena antibiotika ODABIR ANTIBIOTIKA Racionalni odabir antibiotika ovisi o nekoliko faktora. Dijagnoza. Da bi se izabrao najbolji antibiotik za terapiju potrebno je postaviti specifičnu etiološku dijagnozu bolesti. To se često može učiniti na temelju kliničkih pokazatelja. Na primjer, kod lobarne pneumonije ili akutne urinarne infekcije odnos između kliničke slike i uzročnog agensa je dovoljno konstantan da omogući odabir antibiotika samo na temelju kliničkog pregleda. Međutim, iz predostrožnosti je ipak bolje da se i u ovim slučajevima uzme uzorak za bakteriološku pretragu prije propisivanja antimikrobnog lijeka. U većini infekcija odnos između uzročnog agensa i kliničke slike nije konstantan. Zbog toga je neophodno uzeti uzorak za bakteriološku pretragu i identifikaciju uzročnog agensa. Nakon što je uzet uzorak može se započeti s empirijskom kemoterapijom. Kada se identificira uzročni agens i odredi njegova osjetljivost na antimikrobne lijekove, može se modificirati inicijalna terapija. Procjena uzročnog agensa temelji se na slijedećim kriterijima: mjesto infekcije (npr. pneumonija, infekcija urinarnog trakta itd.), dob bolesnika (npr. kod meningitisa: novorođenče, malo dijete, odrasli), mjesto gdje je stečena infekcija (bolnica ili izvanbolnička sredina), mehanički predisponirajući činitelji (intravaskularni kateteri, urinarni kateteri, respirator, izlaganje vektoru), predisponirajući faktori od strane domaćina (imunodeficijencija, terapija kortikosteroidima ili citotoksičnim lijekovima, stanja nakon transplantacije organa). Kada je poznat uzročni agens antibiotik se određuje na temelju postojećeg kliničkog iskustva. U ostalim slučajevima potrebno je testiranje osjetljivosti da bi se odredio najbolji mogući antibiotik (Tabela 15.1). TESTIRANJE OSJETLJIVOSTI NA ANTIBIOTIKE Laboratorijsko testiranje osjetljivosti bakterijskog izolata na antibiotike je indicirano u slijedećim slučajevima: kada izolirani mikroorganizam pripada vrsti koja je često rezistentna na antibiotike (npr. gram-negativne crijevne bakterije ili nefermentativne bakterije), kada je infektivni proces takav da može završiti fatalno ukoliko se ne primjeni specifična terapija (npr. sepsa ili meningitis), kod infekcija kod kojih eradikacija uzročnika zahtijeva primjenu antibiotika koji su baktericidni, a ne samo bakteriostatski (npr. endokarditis). NEPRIMJERENA UPOTREBA ANTIBIOTIKA Kod primjene antibiotika valja voditi računa o slijedećim aspektima. Antibiotici mogu dovesti do alergijske senzibilizacije koja se može manifestirati kao osip, svrbež, eozinofilija, povišena temperatura, a u najtežim slučajevima kao anafilaktički šok. Neki antibiotici, također, uzrokuju smanjenje broja krvnih stanica (anemiju, granulocitopeniju ili trombocitopeniju), kolestatski hepatitis, a dovode se u vezu i sa nastankom kolagenoza. Promjene normalne flore na koži, sluznicama i debelom crijevu mogu dovesti do kolonizacije multirezistentnih sojeva bakterija ili kandida, te superinfekcije ovim mikroorganizmima. Antibiotici mogu prikriti simptome infekcije, a da pri tome ne eradiciraju infekciju. (Na primjer, simptomi apscesa mogu biti suprimirani, a da se istovremeno infektivni proces nastavlja). Neki antibiotici pokazuju direktnu toksičnost (pojava granulocitopenije ili trombocitopenije kod primjene cefalosporina; oštećenja bubrega i slušnog živca kod primjene aminoglikozida). Razvoj antimikrobne rezistencije u populaciji bakterija posljedica je eliminacije osjetljive populacije mikroorganizama djelovanjem antibiotika i njihova nadomještanja rezistentnim sojevima što se često događa u bolničkom ambijentu koji je saturiran (u kojem se mnogo primjenjuju antibiotici) antibioticima. 230
11 B. Bedeni} KOMBINIRANA PRIMJENA ANTIBIOTIKA Nekoliko je razloga za istovremenu primjenu dva ili više antibiotika. U teško bolesnog pacijenta, za kojeg se sumnja da ima ozbiljnu polimikrobnu infekciju, istovremena primjena dva ili više antibiotika omogućuje dobru pokrivenost različitih uzročnika. Prije početka terapije važno je uzeti uzorke za identifikaciju etiološkog agensa i za testiranje njegove osjetljivosti na antibiotike. Primjeri primjene kombinirane terapije su: sumnja na sepsu uzrokovanu stafilokokom ili gram-negativnim bakterijama u imunokompromitiranog domaćina; bakterijski meningitis u djece. Kombinirana terapija antibioticima ujedno sprječava pojavu rezistentnih mutanata u kroničnim infekcijama koje zahtjevaju dugotrajnu terapiju; na primjer, terapija tuberkuloze provodi se istovremeno s tri antituberkulotika. Terapija s nekoliko antibiotika istovremeno provodi se i za liječenje miješanih infekcija, naročito onih koje nastaju nakon masivne traume ili ako su zahvaćene vaskularne strukture. Svaki lijek u kombinaciji djeluje ciljano na jednog uzročnika. Kombiniranom terapijom se postiže sinergizam ili se osigurava baktericidni učinak. Na primjer, u terapiji bakterijskog endokarditisa, uzrokovanog enterokokima ili stafilokokima, primjenjuju se β-laktamski antibiotici u kombinaciji s aminoglikozidima, jer se na taj način ostvaruje sinergističko djelovanje: β-laktamski antibiotik inhibira sintezu staničnog zida tako da nastaju oblici bakterija bez stijenke i to omogućuje aminoglikozidima lakši prodor u citoplazmu do njihovih ciljnih molekula na ribosomima; sulfonamidi, kao i trimetoprim, kada se primjenjuju pojedinačno imaju bakteriostatsko djelovanje, ali kada se ova dva lijeka primjene u kombinaciji učinak je baktericidan, što znači da udruženim djelovanjem dva bakteriostatska lijeka prelaze u baktericidnu kombinaciju. Glavni nedostatak primjene kombinirane terapije jeste mogućnost otežanog postavljanja etiološke dijagnoze infekcije. Veći broj lijekova, također, povećava učestalost pojave nuspojava, a povećavaju se i troškovi liječenja. Kombinacije antimikrobnih lijekova obično ne postižu bolji učinak nego svaki lijek pojedinačno, a u rijetkim slučajevima jedan antibiotik može antagonizirati učinak drugog (npr. cefalosporin i karbapenem). MEHANIZAM SINERGISTIČKOG DJELOVANJA Krajnji rezultat kombinirane primjene dva antibiotika može biti indiferentan, aditivan, sinergistički ili antagonistički. Indiferentan učinak je onaj koji ne daje bolji rezultat nakon kombinirane primjene u odnosu na primjenu svakog pojedinačnog antibiotika. Aditivan je učinak jednak zbroju učinaka svakog pojedinačnog antibiotika. Sinergizam predstavlja značajno veći učinak kombinirane primjene nego što je to zbroj učinaka pojedinačnih antibiotika Antagonizam je uzajamno smanjenje djelovanja dva ili više antibiotika koji se primjenjuju u kombinaciji. Ovi efekti se mogu istraživati in vitro i in vivo. Djelovanje antibiotika u kombinaciji ovisi o vrsti bakterije i o bakterijskom soju, tako da ne možemo govoriti o univerzalnom sinergističkom djelovanju. Antimikrobni sinergizam se može događati različitim mehanizmima. Primjer 1: Dva antimikrobna lijeka sekvencijalno blokiraju određeni metabolički put u bakteriji. Sulfonamidi inhibiraju sintezu para-amino-benzojeve kiseline koja je prethodnik folne kiseline. Trimetoprim koči slijedeću fazu, a to je pretvaranje folne kiseline u foliničnu (tetrahidrofolnu kiselinu). Simultana primjena sulfonamida i trimetoprima je učinkovita u bakterijskih (šigeloza, salmoneloza) i protozoarnih (pneumocistoza, malarija) infekcija. Pirimetamin ima sinergističko djelovanje sa sulfonamidima u liječenju toksoplazmoze. Primjer 2: Antibiotici koji inhibiraju sintezu staničnog zida djeluju sinergistički s aminoglikozidima koji im olakšavaju ulazak u bakterijsku stanicu. Penicilin povećava prihvat streptomicina ili gentamicina u enterokoka. Zbog toga se ampicilin koristi u kombinaciji sa gentamicinom za liječenje endokarditisa uzrokovanog enterokokima. Piperacilin ima sinergistički učinak sa tobramicinom kod infekcija uzrokovanih s P. aeruginosa. Primjer 3: Jedan lijek može djelovati na citoplazmatsku membranu i olakšati ulazak drugog antimikrobnoj lijeka. Amfotericin djeluje sinergistički s flucitozinom prema nekim gljivama (kandida, kriptokok). Primjer 4: Jedan antimikrobni lijek može spriječiti inaktivaciju drugog. Inhibitori β-laktamaza, kao što su klavulanska kiselina, sulbaktam i tazobaktam, zaštićuju molekulu partnerskog β-laktamskog antibiotika od enzimske destrukcije. Klavulanska kiselina se kombinira s amoksicilinom i tikarcilinom, a sulbaktam s ampicilinom, da bi se ostvarilo sinergističko djelovanje prema izolatima koji produciraju 231
12 Antibakterijski lijekovi Poglavlje 15 Tabela Antibiotici izbora za pojedine bakterijske patogene Etiološki agens Antibiotici prvog izbora Alternativni antibiotici Gram-negativni koki Moraxella catarrhalis Neisseria gonorrhoeae sulfametoksazol/trimetoprim, fluorokinolon ceftriakson, ciprofloksacin, ofloksacin cefuroksim, ceftibuten, eritromicin, tetraciklin, azitromicin spektinomicin, cefpodoksim proksetil Neisseria meningitidis ceftriakson penicilin, cefotaksim, ampicilin, kloramfenikol Gram-pozitivni koki Streptococcus pneumoniae penicilin eritromicin, cefalosporin, vankomicin, kotrimoksazol, kloramfenikol, klindamicin, azitromicin, tetraciklin, fluorokinolon, linezolid Streptococcus β-haemoliticus (grupe A, B, C, G) penicilin eritromicin, cefalosporin, vankomicin, klindamicin, azitromicin, klaritromicin Viridans streptokoki penicilin+gentamicin cefalosporin, vankomicin Staphylococcus spp.(penicilinaza- negativan) Staphylococcus spp.(penicilinaza-pozitivan) Staphylococcus spp.(meticilin-rezistentni, MRSA) penicilin meticilin, kloksacilin, flukloksacilin vankomicin+gentamicin, rifampicin cefalosporin, vankomicin, imipenem, fluorokinolon, klindamicin vankomicin, cefalosporin, klindamicin, flurokinolon, imipenem, meropenem, amoksilin/klavulanat, piperacilin/tazobaktam kotrimoksazol, minociklin, fluorokinolon, linezolid, klindamicin Enterococcus faecalis ampicilin+gentamicin vankomicin+gentamicin Enterococcus faecium vankomicin+gentamicin linezolid, quinupristin/dalfopristin Gram-negativni štapi}i Escherichia coli (sepsa) Escherichia coli (nekomplicirane infekcije urinarnog trakta) ceftazidim+gentamicin, cefotaksim+gentamicin, ceftriakson+gentamicin, cefepim+gentamicin fluorokinoloni, nitrofurantoin imipenem, meropenem, fluorokinoloni kotrimoksazol, oralni cefalosporini (cefuroksim, cefaleksin, ceftibuten) Klebsiella pneumoniae cefalosporin+gentamicin imipenem, meropenem, fluorokinoloni, piperacilin/tazobaktam, aztreonam Proteus spp., Providentia spp., Morganella spp. ceftazidim, cefotaksim, ceftriakson, cefepim aminoglikozid, kotrimoksazol, imipenem, meropenem, fluorokinolon P. mirabilis ampicilin aminoglikozid, kotrimoksazol, fluorokinolon, cefalosporin Serratia spp. Enterobacter spp. ceftazidim, cefotaksim, ceftriakson, cefepim kotrimoksazol, imipenem, meropenem imipenem, meropenem, aminoglikozid, fluorokinolon, aminoglikozid, fluorokinolon, cefepim 232
13 B. Bedeni} Tabela Antibiotici izbora za pojedine bakterijske patogene (nastavak) Etiološki agens Antibiotici prvog izbora Alternativni antibiotici Salmonella spp. (bakterijemija) ceftriakson, fluorokinolon kotrimoksazol, ampicilin, kloramfenikol Shigella spp. fluorokinolon ampicilin, kotrimoksazol, ceftriakson Yersinia pestis (kuga) streptomicin+tetraciklin kloramfenikol, kotrimoksazol Vibrio spp. (kolera, sepsa) tetraciklin kotrimoksazol, fluorokinolon Campylobacter spp. eritromicin ili azitromicin tetraciklin, fluorokinolon, gentamicin Helicobacter pylori Pseudomonas aeruginosa amoksicilin+klaritromicin+omeprazol tetraciklin+metronidazol+ bizmut subsalicilat antipseudomonas penicilin (tikarcilin, karbenicilin, piperacilin) +aminoglikozid klaritromicin+bizmut subsalicilat+tetraciklin, amoksicilin+metronidazol+bizmut subsalicilat ceftazidim+aminoglikozid; imipenem, meropenem+aminoglikozid, ciprofloksacin+piperacilin, ciprofloksacin+ceftazidim Acinetobacter spp. imipenem ili meropenem, minociklin, kotrimoksazol, doksiciklin, aminoglikozid, piperacilin, fluorokinolon Haemophilus spp. (meningitis i druge teške infekcije) Haemophilus spp. (respiratorne infekcije, otitis media) ceftriakson, cefotaksim, ceftazidim kotrimoksazol kloramfenikol, meropenem ampicilin, amoksicilin, doksicilin, azitromicin, klaritromicin, cefotaksim, ceftriakson, amoksicilin/klavulanat Brucella spp. tetraciklin+rifampicin kotrimoksazol+ gentamicin, kloramfenikol+gentamicin, doksiciklin+gentamicin Legionella spp Anaerobni gram-negativni štapi}i eritromicin, klaritromicin ili azitromicin ili fluorokinolon+rifampicin kotrimoksazol, doksiciklin+rifampicin Prevotella spp. (orofarinks) klindamicin penicilin, metronidazol, cefloksitin, cefotetan Bacteroides spp. (GI trakt) metronidazol cefoksitin, kloramfenikol, klindamicin, cefotetan, imipenem, meropenem, piperacilin/sulbaktam, ampicilin/sulbaktam Gram-pozitivni štapi}i Actinomyces spp. penicilin tetraciklin, klindamicin Bacillus spp.(uklju~uju}i antraks) Clostridium spp. (plinska gangrena, tetanus) penicilin (ciprofloksacin ili doksiciklin za antraks) penicilin eritromicin, tetraciklin ili fluorokinolon metronidazol, kloramfenikol, klindamicin, imipenem ili meropenem Corynebacterium diphteriae eritromicin penicilin Corynebacterium jeikium vankomicin ciprofloksacin, penicilin+gentamicin Listeria monocytogenes ampicilin+aminoglikozid kotrimoksazol 233
14 Antibakterijski lijekovi Poglavlje 15 Tabela Antibiotici izbora za pojedine bakterijske patogene (nastavak) Etiološki agens Antibiotici prvog izbora Alternativni antibiotici Acidorezistentni štapi}i Mycobacterium tuberculosis izonijazid+rifampicin+pirazinamid+ etambutol ili streptomicin ostali antituberkulotici Mycobacterium leprae dapson+rifampicin+etambutol minociklin, ofloksacin, klaritromicin Mycobacterium kansasii izonijazid+rifampicin+etambutol etionamid, cikloserin Mycobacterium avium klaritromicin ili azitromicin, etambutol, rifampicin, ciprofloksacin amikacin Mycobacterium fortuitum-cheilonei amikacin+klaritromicin cefoksitin, sulfonamid, doksiciklin, rifampicin Nocardia spp. kotrimoksazol minociklin, imipenem ili meropenem, sulfizoksazol, linezolid Spirohete Borrelia recurrentis (povratna groznica) Borrelia burgdorferi (Lymska bolest) doksiciklin doksiciklin, amoksicilin, cefuroksim aksetil penicilin ceftriakson, cefotaksim, penicilin, azitromicin, klaritromicin Leptospira spp. penicilin doksiciklin Treponema pallidum (lues) penicilin doksiciklin, ceftriakson Treponema pertenue (frambezija) penicilin doksiciklin Mycoplasma spp. eritromicin ili doksiciklin klaritromicin, azitromicin, fluorokinolon Chlamydia spp. C. psitaci doksiciklin kloramfenikol C. trachomatis doksiciklin ili azitromicin ofloksacilin C. pneumoniae doksiciklin eritromicin, klaritromicin, azitromicin, fluorokinolon Rickettsia spp. doksiciklin kloramfenikol, fluorokinolon β-laktamazu. Inhibitor se veže s visokim afinitetom na molekulu β-laktamaze tako da se ona ne može vezati na β-laktamski antibiotik. Antagonizam antibiotika in vivo rijedak je fenomen u medicini. Primjer 1: U slučajevima bakterijskog meningitisa kada je istovremeno primijenjen bakteriostatski (npr. kloramfenikol ili tetraciklin) i baktericidni antibiotik (npr. penicilin). U slučaju da bakteriostatski lijek dospije na mjesto infekcije prije baktericidnog lijeka, dolazi do antagonizma jer je za djelovanje baktericidnog antibiotika, kao što je penicilin, potrebno da se bakterije aktivno umnožavaju. Primjer 2: Istovremena primjena imipenema i piperacilina za liječenje infekcija koje uzrokuje P. aeruginosa. Imipenem je snažan induktor β-laktamaze, koja zatim razgrađuje molekulu piperacilina i čini ju nedjelotvornom. ANTIMIKROBNA KEMOPROFILAKSA Antiinfektivna kemoprofilaksa označava upotrebu antimikrobnih lijekova u cilju sprječavanja infekcije. U širem smislu, to znači i primjenu antibiotika neposredno nakon kontakta s patogenim mikroorganizmima (npr. komplicirani prijelom kostiju ili kontakt s oboljelim od meningokoknog meningitisa), ali prije nego se infekcija razvije. 234
15 B. Bedeni} Korisna kemoprofilaksa treba biti usmjerena na ciljani mikroorganizam djelotvornim antibiotikom. Nastojanja da se prevenira kolonizacija svih mikroorganizama iz okoliša rezultira u selekciji najrezistentnijih organizama kao uzročnika buduće infekcije. Pri odabiru lijeka za profilaksu infekcije treba uzeti u obzir rizik razvoja infekcije u odnosu na moguće nuspojave, troškove, i opasnost razvoja superinfekcije rezistentnim mikroorganizmima. Profilaksa u osoba s normalnom osjetljivošću Kod osoba s normalnom osjetljivošću primjenjuje se specifični lijek za prevenciju određene infekcije. Navešćemo nekoliko primjera: injekcija benzilpenicilina daje se intramuskularno, svake 3 do 4 sedmice, osobama koje imaju reumatsku groznicu da bi se spriječio recidiv infekcije piogenim streptokokom; prevencija meningokoknog meningitisa u osoba koje su bile u kontaktu s oboljelim; prevencija luesa davanjem benzilpenicilina; prevencija plućne kuge oralnim davanjem tetraciklina osobama koje su bile u kapljičnom kontaktu s oboljelim; prevencija rikecioza oralnim davanjem tetraciklina za vrijeme ekspozicije; prevencija leptospiroza oralnim davanjem doksiciklina u hiperendemskim područjima. Profilaksa u osoba s povećanom osjetljivošću U osoba s povećanom osjetljivošću neke anatomske i funkcionalne abnormalnosti su predisponirajuće za pojavu teških infekcija. U ovim slučajevima je moguće spriječiti infekciju davanjem specifičnih antibiotika kroz kraći vremenski period. Bolesti srca. Osobe s oštećenim srčanim zaliscima ili umjetnim zaliscima sklone su naseljavanju mikroorganizama koji cirkuliraju krvlju. Infektivni endokarditis se može spriječiti ako se adekvatni lijek primjeni tokom perioda bakterijemije. Veliki broj viridans streptokoka ulazi u cirkulaciju tokom zahvata na zubima ili operacija u usnoj šupljini ili ždrijelu. U takvim slučajevima je indicirana profilaktička primjena antibiotika protiv viridans streptokoka. Najčešće se daje amoksicilin, oralno prije zahvata, te 2 sata nakon zahvata. Bolesnicima alergičnim na penicilin, može se dati eritromicin. Enterokoki uzrokuju 5-15% slučajeva infektivnog endokarditisa. Oni ulaze u krvotok iz probavnog, urinarnog ili genitalnog trakta. Tokom zahvata na ovim sistemima može doći do bakterijemije i naseljavanja enterokoka na oštećenim ili umjetnim srčanih zaliscima. Za prevenciju je potrebno dati ampicilin u kombinaciji s gentamicinom ili nekim drugim aminoglikozidom, intravenski ili intramuskularno, pola sata prije zahvata. Bakterijemija se može pojaviti i prilikom kateterizacije srca, u 10 do 20% bolesnika, ali samo mali broj pacijenata dobije endokarditis, tako da profilaktička primjena antibiotika nije indicirana kod ovih zahvata. Bolesti respiratornog sistema. Bolesnici koji imaju funkcionalne ili anatomske abnormalnosti respiratornog trakta, kao što su kronična opstruktivna plućna bolest ili bronhiektazije, skloni su napadajima akutnog bronhitisa. To je recidivirajuća bakterijska infekcija često izazvana akutnom virusnom infekcijom, a može dovesti do respiratorne dekompenzacije. Najčešći uzročnici akutnih egzacerbacija bronhitisa su H. influenzae i pneumokoki. Antibiotici se daju kod kronične opstruktivne plućne bolesti u slijedećim slučajevima: kao profilaksu u bolesnika s čestim recidivima kroničnog bronhitisa, za terapiju akutnih epizoda bronhitisa ili za terapiju teških egzacerbacija kronične opstruktivne plućne bolesti. Nema dokaza da antibiotska profilaksa pomaže bolesnicima s kroničnom opstruktivnom bolešću, ali bolesnici s akutnim egzacerbacijama kroničnog bronhitisa s promjenama u količini i svojstvima sputuma dobro reagiraju na terapiju antibioticima. Antibiotska profilaksa se primjenjuje i kod djece s cističnom fibrozom koja nisu hospitalizirana. Usprkos tome, ovi bolesnici često dobiju teške infekcije uzrokovane stafilokokima ili pseudomonasom. Za profilaksu pneumocistis-pneumonije u imunokompromitiranih bolesnika koristi se kotromoksazol oralno i pentamidin u obliku spreja. Recidivirajuće urinarne infekcije. Ženama koje imaju recidivirajuće infekcije urinarnog trakta, oralno uzimanje nitrofurantoina ili kotrimoksazola svakodnevno ili tri puta tjedno može značajno smanjiti učestalost simptomatskih recidiva kroz duži vremenski period. Oportunističke infekcije u bolesnika s teškom granulocitopenijom. Bolesnici koji su na terapiji citotoksičnim lijekovima ili transplantirani bolesnici koji dobivaju imunosupresivnu terapiju mogu razviti tešku leukopeniju. Kada broj neutrofila padne ispod 1000/µl, pacijent postaje veoma osjetljiv na oportunističke infekcije, najčešće uzrokovane gram-negativnim bakterijama. Ovim osobama se obično daju profilaktički fluorokinoloni ili cefalosporin, ili kombinacija antibiotika (npr. vankomicin+ gentamicin+cefalosporin), usmjerena na najčešće 235
16 Antibakterijski lijekovi uzročnike oportunističkih infekcija. Ova terapija se nastavlja i nekoliko dana nakon porasta broja granulocita. Profilaksa u kirurgiji Kod odabira antibiotika u kirurškoj profilaksi važno je uzeti u obzir određene specifične okolnosti. Kod čistih selektivnih kirurških zahvata, kod kojih ne dolazi do oštećenja tkiva koje sadržava normalnu floru, nije idicirana primjena antibiotika. U ovim slučajevima opasnost od mogućih nuspojava nastalih primjenom antibiotika veća je nego eventualna korist od profilakse. Izuzetak su jedino zahvati kod kojih se ugrađuju koštani ili zglobni implantati. Profilaktička primjena antibiotika je indicirana ako je očekivana učestalost infekcija 3-5%. Izuzetak je insercija implantata (koštanih ili kardiovaskularnih), budući bi nastanak infekcije u ovim slučajevima imao fatalne posljedice. Inicijalna doza profilaktičkog antibiotika trebala bi se davati za vrijeme indukcije anestezije. Izuzetak su operativni zahvati na debelom crijevu kod kojih bi se antibiotik trebalo davati nekoliko sati prije zahvata. Produžena primjena antimikrobnih lijekova mijenja normalnu floru, potiskuje osjetljive mikroorganizme i favorizira kolonizaciju rezistentnim sojevima. Iz tih razloga antimikrobnu profilaksu ne bi trebalo provoditi duže od jedan dan nakon zahvata i po mogućnosti samo preoperativno. Koncentracije antibiotika, nakon njegove sistemske primjene, obično ne sprječavaju nastanak infekcija rana, pneumoniju ili urinarne infekcije, ako su prisutne anatomske ili fiziološke abnormalnosti, ili strano tijelo. Lokalna primjena antibiotika za profilaksu kod bolesnika s intravenskim kateterom, zatvorenim urinarnim drenom, u kiruršku ranu ili u koštani cement, ima samo ograničeni uspjeh. Kemijska klasifikacija antibiotika (Tabela 15.2) BETA (β) - LAKTAMSKI ANTIBIOTICI Penicilini Penicilin se dobiva rastom gljivica roda Penicillium, dubokom fermentacijom u tankovima. Ovisno o soju gljivica i o sastavu hranilišta, dobivanju se benzilpenicilin (penicilin G) ili fenoksimetilpeniclin (penicilin V) godine uspjela se fermentacijom dobiti penicilinska jezgra (6 - aminopenicilanska kiselina), što je omogućilo dodavanje različitih postraničnih lanaca i stvaranje polusintetskih peniclina različitih svojstava. Važno je imati na umu da svi penicilini ne pokazuju jednaku antibakterijsku aktivnost, te da je među postojećim penicilinima potrebno obaviti ciljani izbor, kao da se radi o pripadnicima različitih skupina antimikrobnih lijekova. Mehanizam djelovanja. β-laktamski antibiotici ometaju sintezu peptidoglikana koji je sastavni dio stijenke bakterijske stanice i štiti ju od nepovoljnih utjecaja iz okolice. β-laktamski prsten u antibiotiku po strukturi je analogan alanil-alaninu, sastojku N- acetil muraminske kiseline, koja stvara poprečne veze između peptidnih lanaca i peptidoglikanskog sloja (Slika 8.15). Poremećena sinteza stijenke onemogućava bakteriji da održava osmotski gradijent između stanice i njene okolice, pa stanica bubri i puca. Penicilini imaju baktericidni učinak i stoga su djelotvorni samo na mikroorganizme koji su u fazi dijeljenja, budući organizmi u fazi mirovanja ne stvaraju novu stijenku. Znatna neškodljivost penicilina za čovjeka temelji se na činjenici da u humanim stanicama ne postoji peptidoglikan, koji je ciljno mjesto djelovanja penicilina. Budući da u stanicama sisavaca ne postoji peptidoglikan, koji je osnova selektivne toksičnosti β-laktama, ovi antibiotici uništavaju bakterije, a pri tome ne djeluju na ljudske stanice. Mehanizmi rezistencije su: produkcija β-laktamaza, promjene u porinima i mutacije ciljnih molekula proteina koji vežu penicilin (engl. penicillin binding protein, PBP) (Slika 8.15., Slika 15.1). Farmakokinetika. Neke peniciline razlaže želučana kiselina, te su nepogodni za peroralnu primjenu (benzilpenicilin). Oni koji su otporni na djelovanje želučane kiseline (fenoksimetilpenicilin) se apsorbiraju u gornjim djelovima tankog crijeva i postižu vršne (maksimalne) koncentracije u plazmi sat vremena nakon primjene. Poluvrijeme eliminacije u plazmi je kratko (oko 30 minuta), raspoređuju se uglavnom u ekstracelularnoj tekućini, slabo prodiru u tkiva (volumen distribucije 18 litara). Penicilini su uglavnom organske kiseline i izlučuju se tubularnom sekrecijom u bubrezima. Brzina izlučivanja penicilina može se znatno usporiti istodobnom primjenom probenecida, koji se uspješno s njim natječe na razini transportnog mehanizma u tubulima. Kod bolesnika s oštećenjem funkcije bubrega potrebna je korekcija doze penicilina. Nuspojave. U najvažnije nuspojave ubrajamo alergijske reakcije (svrbež, osip, povišena temperatura, angio- 236
17 B. Bedeni} Tabela Kemijska klasifikacija antibiotika i spektar djelovanja Grupa antibiotika Antibiotik Mehanizam djelovanja Spektar djelovanja BETA (β)- LAKTAMSKI ANTIBIOTICI Penicilini prirodni penicilini: benzilpenicilin (penicilin G), fenoksimetilpenicilin (penicilin V) inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana djeluje na streptokoke grupe A, S. pneumoniae (ako nisu otporni ili smanjeno osjetljivi na penicilin), N. meningitidis (opisana rezistencija zbog gubitka porina), N. gonorrhoeae (rezistencija nastaje zbog produkcije penicilinaze), klostridije, B. anhtracis, B. fragilis, T. pallidum, borelije, leptospire, Pasteurella multocida semisintetski penicilini penicilini otporni na penicilazu: meticilin, nafcilin, oksacilin, kloksacilin, dikloksacilin inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana pokazuju aktivnost prema stafilokima (S. aureus i S. epidermidis) koji produciraju β-laktamazu, ukoliko se ne radi o meticilin rezistentnim sojevima, djeluju i na S. pneumoniae i S. pyogenes, ali slabije nego penicilin G penicilini proširenog spektra: aminopenicilini (ampicilin, amoksicilin, karbenicilin, tikarcilin); ureidopeniclini (piperacilin) Inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana ampicilin i amoksicilin imaju sli~an spektar kao penicilin G, ali pokazuju bolji u~inak prema Listeria monocytogenes i enterokokima, djeluju i na H. influenzae, ali je 25% sojeva rezistentno od enterobakterija djeluju na salmonele i šigele; neki sojevi E. coli i P. mirabilis su osjetljivi na ampicilin i amoksicilin karboksipenicilini i ureidopenicilini djeluju na enterobakterije koje su rezistentne na ampicilin ali nemaju u~inka na Klebsiella spp.; imaju snažno djelovanje na P. aeruginosa; imaju baktericidno djelovanje na Heamophilus spp., najserije i anaerobne bakterije. Kombinacija β-laktama (penicilin) i inhibitora β-laktamaza: ampicilin + sulbaktam, amoksicilin + klavulanska kiselina, tikarcilin + klavulanska kiselina, piperacilin + tazobaktam Inhibiraju sintezu stani~nog zida; vežu β-laktamaze i sprje~avaju enzimatsku inaktivaciju β-laktama koriste se za lije~enje infekcija uzrokovanih bakterijama koje proizvode plazmidne β-laktamaze: E. coli, K. pneumoniae, P. mirabilis, M. catarrhalis, H. influenzae, B. fragilis. Cefalosporini prva generacija (uskog spektra): cefazolin, cefaloridin, cefaleksin, cefradin, cefapirin Inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana dobra aktivnost prema gram-pozitivnim bakterijama (stafilokoki, pneumokoki, β-hemoliti~ki streptokoki); slabiji u~inak prema gram-negativnim bakterijama, izražena rezistencija me u enterobakterijama druga generacija (proširen spektar): cefaklor, cefuroksim inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana dobra aktivnost prema gram-pozitivnim bakterijama (stafilokoki); bolji u~inak prema-gram-negativnim bakterijama u odnosu na prvu generaciju; cefoksitin ima snažnu inhibitornu aktivnost protiv anaerobnih bakterija 237
18 Antibakterijski lijekovi Poglavlje 15 Grupa antibiotika Antibiotik Mehanizam djelovanja Spektar djelovanja tre}a generacija (prošireni spektar): ceftazidim, cefotaksim, ceftriakson, cefoperazon, ceftibuten, cefiksim, cefetamet ~etvrta generacija (široki spektar): cefpirom, cefepime, cefaciklidin cefamicini proširenog spektra: cefoksitin, cefotetan, moksalaktam inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana slabiji u~inak na gram-pozitivne bakterije a bolji prema gram-negativnim bakterijama; stabilni su prema β-laktamazama osim β-laktamaza proširenog spektra i metalo-βlaktamaza; ceftazidim i cefoperazon djeluju snažno protiv Pseudomonas aeruginosa, a ceftriakson djelotvorno inhibira penicilinaza pozitivne gonokoke i meningokoke slabiji u~inak na gram-pozitivne bakterije a bolji prema gram-negativnim bakterijama; stabilni su prema β-laktamazama; kvarterni amonijev ion koji se nalazi u strukturi cefalosporina ~etvrte generacije daje izrazitu stabilnost prema β-laktamazama (osim β-laktamaza proširenog spektra i metalo-β-laktamaza), pokazuju dobru penetraciju kroz vanjsku membranu gram-negativnih bakterija i visok afinitet vezanja za PBP molekule Dobar u~inak prema anaerobnim bakterijama Monobaktami aztreonam inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana djeluje na gram-negativne crijevne bakterije (E. coli, Klebsiella spp., Enterobacter spp.), P. aeruginosa, Haemophilus spp. i Neisseria spp. Acinetobacter spp., Burgholderia cepacia i Stenotrophomonas maltophilia su u visokom postotku rezistentni; stabilan je prema ve}ini kromosomalnih i plazmidnih β-laktamaza i ne inducira njihovu produkciju Karbapenemi imipenem, meropenem, ertapenem inhibicija sinteze peptidoglikaza vezanjem na PBP molekule i inhibiranjem aktivnosti transpeptidaza koje vrše završnu fazu umrežavanja peptidoglikana najširi spektar djelovanja do sada: djeluju na ve}inu aerobnih i anaerobnih gram-pozitivnih i gram-negativnih bakterija (osim oksacilin-rezistentnih stafilokoka), Enterococcus faecium, i na gram-negativne štapi} aste bakterije rezistentne na beta-laktamske antibiotike i aminoglikozide (Acinetobacter spp., Enterobacter. spp, Citrobacter spp., i Serratia spp) AMINOGLIKO- ZIDI streptomicin, kanamicin, gentamicin, tobramicin, klaritromicin, netilmicin inhibicija sinteze proteina vezanjem na 30S podjedinicu ribosoma, spre~avaju vezanje glasni~ke RNA na ribosom, dovode do krivog ~itanja genetskog kod i do sinteze neupotrebljivih bjelan~evina stafilokoki, enterobakterije, nefermentativne bakterije, streptomicin: mikobakterije, F. tularensis, brucele, Y. pestis AMINOCIKLI- TOLI spektinomicin (strukturno sli~ni aminoglikozidima) inhibicija sinteze proteina vezanjem na 30S podjedinicu ribosoma, spre~avanju vezanje mrnk na ribosom Neisseria gonorrhoeae SULFONAMIDI sulfonamid, trimetoprim, sulfonamid + trimetoprim inhibiraju sintezu folne kiseline, ugra uju se umjesto PABA kojoj su strukturno sli~ni, djeluju po principu kompetitivne inhibicije gram-pozitivne bakterije: stafilokoki, streptokoki (osim enterokoka), B. anthracis; gram-negativne bakterije: najserije, H. influenzae, enterobakterije (E. coli, Shigella spp., Salmonellae spp., Yersiniae spp., neki sojevi Proteus spp.); klamidije i nokardije, P. carinii 238
19 B. Bedeni} Grupa antibiotika Antibiotik Mehanizam djelovanja Spektar djelovanja TETRACIKLINI tetraciklin doksiciklin minociklin klortetraciklin demeklocilin metaciklin oksitetraciklin inhibicija sinteze bjelan~e vi na vezanjem za ribozome i sprje~avanje pristupa aminokiselina vezanih na transfer (t)rnk molekulu na ribozomu na kojega je vezana mrnk; ovaj mehanizam djelovanja se ostvaruje u humanim i u bakterijskim stanicama, ali su bakterijske stanice osjetljivije jer imaju aktivni transportni sistem, koji prenosi tetracikline protiv koncentracijskog gradijenta ~ime se postižu visoke koncentracije unutar bakterijske stanice; na taj na~in dobiva se selektivnost jer stanice ljudskog organizma ne posjeduju sli~ni mehanizam za koncentraciju tetraciklina. gram-pozitivni i gram-negativnih koki, neke vrste enterobakterija, Heamophilus spp., Vibrio cholerae, klostridije, aktinomicete, spirohete, rikecije i klamidije, P. falciparum MAKROLIDI AZALIDI eritromicin klaritromicin azitromicin vežu se na ribosome i sprje~avaju kontakt trnk na koju je vezana aminokiselina s mrnk, te na taj na~in ometaju sintezu bjelan~evina stafilokoki, streptokoki, korinebakterije, legionele, bordetele, klamidije, spirohete, Campylobacter spp. KLORAMFENI- KOLI kloramfenikol inhibira sintezu bjelan~evina, na taj na~in što onemogu}ava pri~vrš} ivanje rastu}eg polipeptidnog lanca na 50S jedinicu ribosoma. H. influenzae, S. pneumoniae, neke vrste enterobakterija, najserije, anaerobne bakterije gram-pozitivni koki, mikoplazme, klamidije i rikecije. LINKOZAMINI klindamicin linkomicin veže se na 50S podjednicu ribosoma i inhibira sintezu bjelan~evina gram-pozitivni koki i štapi}i, anaerobne bakterije KINOLONI kinoloni uskog spektra: nalidiksi~na kiselina kinoloni širokog spektra: ciprofloksacin, levofloksacin, ofloksacin kinoloni proširenog spektra: gatifloksacin, grepafloksacin, moksifloksacin inhibiraju DNA girazu (bakterijski enzim koji je neophodan za replikaciju DNK) aktivni prema gram-negativnim štapi}ima; ne djeluju na gram-pozitivne bakterije široki spektar aktivnosti koji uklju~uje i gramnegativne i gram-pozitivne bakterije široki spektar s naglašenom aktivnoš}u prema gram-pozitivnim bakterijama (osobito prema streptokokima i enterokokima), aktivnost prema gram-negativnim bakterijama je komparabilna s ciprofloksacinom GLIKOPEPTIDI vankomicin teikoplanin inhibiraju sintezu peptidoglikana u stani~noj stijenci bakterije stvaranjem kompleksa s D-alanil-D alaninom, koji je prekursor stani~nog zida aerobne i anaerobne gram-pozitivne bakterije: stafilokoki (uklju~uju}i i MRSA), streptokoki, enterokoki, Corynebacterium spp., Bacillus spp, Lactobacillus spp., L. monocytogenes, Clostridium spp., Actinomyces spp METRONIDA- ZOL metronidazol nitro grupa u kemijskoj strukturi metronidazola reducira se pod djelovanjem nitroreduktaze i nastaje visoko toski~ni intermedijarni produkt, koji se razlaže u slobodne radikale i ošte}uje DNK anaerobne bakterije: B. fragilis, Fusobacterius spp, Clostridium spp; Trichomonas vaginalis, Giardia lamblia, Enthamoeba histolytica 239
20 Antibakterijski lijekovi Poglavlje 15 Grupa antibiotika Antibiotik Mehanizam djelovanja Spektar djelovanja OKSAZOLIDINI linezolid veže se na 50S podjedinicu ribosoma i inhibira sintezu bjelan~evina gram-pozitivni koki (stafilokoki, streptokoki, enterokoki); umjereno aktivni prema M. catarrhlis i Bacteroides spp. STREPTOGRA- MINI kuinupristin/dalfopristin gram pozitivni koki: S. aureus (uklju~uju} i i MRSA), S. pneumoniae, enterokoki, (uklju~uju}i i VRE), najserije, H. influenzae LIPOPEPTIDI daptomicin ugra uju se u citoplazmatsku membranu gram-pozitivnih bakterija i dovode do stvaranja pora, što dovodi do efluksa važnih komponenti bakterijske stanice, posebno kalijevih iona, što rezultira u depolarizaciji citoplazmatske membrane i smrti stanice. Daptomicin ostvaruje baktericidni u~inak bez lize stanica, što zna~i da se smanjuje rizik osloba anja egzotoksina u cirkulaciju POLIMIKSINI bacitracin djeluju kao detergenti ili surfaktanti, reagiraju s fosfolipidima u citoplazmatskoj membrani, pove} avaju permeabilnost stanice i narušavaju osmotski integritet, dolazi do gubitka intracelularnih sastojaka i do propadanja bakterijske stanice gram pozitivni koki: S. aureus (uklju~uju} i i MRSA), S. pneumoniae, enterokoki, (uklju~uju}i i VRE), uklju~uju}i i multirezistentne sojeve koagulaza negativnih stafilokoka gram negativne bakterije, naro~ito P. aeruginosa; Proteus spp., Providencia sp., Serrratia spp. i Neisseria spp. su obi~no rezistentni. neurotski edem, anafilaktički šok), proljev (promjena normalne crijevne flore i oportunističke infekcije uzrokovane bakterijama iz rodova Pseudomonas i Klebsiella, ili kandidama). U rijeđe nuspojave spadaju krvne diskrazije (neutropenija, hemolitička anemija) i konvulzije kod primjene velikih doza. Benzilpenicilin se primjenjuje kada je potrebno postići visoke koncentracije u plazmi i akutno upaljenim tkivima. Veoma je djelotvoran protiv pneumokoka i grupe A β-hemolitičkih streptokoka. Viridans streptokoki su također uobičajeno osjetljivi, osim ako bolesnik nije nedavno primao penicilin. Enterokok je slabije osjetljiv, a kod teških infekcija kao što je endokarditis treba ga davati u kombinaciji s aminoglikozidima (najčešće s gentamicinom). Zbog sve većeg širenja rezistencije, osobito među stafilokokima i gram-negativnim bakterijama, primjena benzilpenicilina danas je vrlo ograničena. Indikacije za primjenu benzilpenicilina su: infekcije izazvane pneumokokom (pneumonija, sinusitis, otitis media), infekcije izazvane piogenim streptokokom (faringitis, angina, skarlatina, babinja groznica, erizipel), endokarditis uzrokovan enterokokom u kombinaciji s gentamici- nom, meningokokni meningitis (danas ga je zamjenio ceftriakson), gonoreja (danas zamjenjen ceftriaksonom), antraks, plinska gangrena, tetanus, lues, leptospiroze, povratna groznica, Lyme-borelioza (teži oblici). Prokain i benzatin penicilin. To su depo-preparati za intramuskularnu primjenu, koji polako oslobađaju penicilin i postižu male, ali dugotrajne koncentracije u krvi (do 4 sedmice). Ne primjenjuju se u akutnim infekcija zbog neadekvatnih koncentracija u krvi. Indicirani su u liječenju kongenitalnog luesa i u kemoprofilaksi. Injekcije su bolne i postoji rizik od produženih nuspojava. Fenoksimetilpenicilin (penicilin V) je otporan na želučanu kiselinu i nepromijenjen ulazi u tanko crijevo odakle se pouzdano resorbira. Manje je djelotvoran od benzilpenicilina na N. gonorrhoeae i N. meningitidis, te stoga nije pogodan za liječenje gonoreje i meningokoknog meningitisa. Prikladna je zamjena za benzilpenicilin i liječenje infekcija uzrokovanih pneumokokom, piogenim sreptokokom i stafilokokima osjetljivima na penicilin, nakon što se akutna infekcija smirila primjenom benzilpenicilina. 240
21 B. Bedeni} Beta-laktamaza stabilni penicilini su djelotvorni i na druge bakterije koje podliježu djelovanju i ostalih penicilina, no važno je znati da je benzilpenicilin čak do 20 puta djelotvorniji ako se radi o osjetljivim uzročnicima, kao što su pneumokoki, β-hemolitički streptokoki i najserije. Penicilini proširenog spektra. Djelotvornost ovih polusintetskih penicilina je šira od učinka benzilpenicilina na gram-pozitivne i gram-negativne koke, a obuhvaća i mnoge gram-negativne bacile. Ovi penicilini nisu otporni na β-laktamaze i stoga ne djeluju na mikroorganizme koji produciraju ove enzime. Aminopenicilini su slabije aktivni od benzilpenicilina na većinu gram-pozitivnih koka. Važna je njihova djelotvornost protiv enterokoka i Haemophilus influenzae, no zabrinjava pojava sojeva hemofilusa koji produciraju β-laktamazu. E. coli i P. mirabilis su različito osjetljivi, te je potrebno uvijek ispitati njihovu osjetljivost antibiogramom. Pseudomonas spp. i Proteus vulgaris obično nisu osjetljivi na aminopeniciline. Kombinacija amoksicilina s klavulanskom kiselinom (augmentin, klavocin) koristi se za liječenje infekcija uzrokovanih mikroorganizmima koji stvaraju β-laktamazu. Klavulanska kiselina je inhibitor β-laktamaza, koji se veže na taj enzim i kompetitivno zaštićuje molekulu antibiotika. Na taj način pojačava učinak penicilina protiv onih bakterija koje bi, inače, bile rezistentne jer produciraju β-laktamazu. Aminopenicilini se koriste se za liječenje infekcija gram-negativnim bakterijama uključujući E. coli, salmonele i šigele. Najčešća primjena je liječenje crijevnih infekcija uzrokovanih navedenim mikroorganizmima i liječenje infekcija urinarnog trakta, ako su uzročnici otporni na ostale antibiotike. Osjetljivi su na β-laktamaze. Karboksipenicilini imaju sličan spektar djelovanja, kao i ampicilin, uz dodatnu djelotvornost na P. aeruginosa. Ureidopenicilini imaju prošireni spektar djelovanja, koji uključuje i djelotvornost na Pseudomonas aeruginosa. Cefalosporini Cefalosporini su prvi put dobiveni iz kulture plijesni Cephalosporium spp. Njihova molekularna struktura slična je kao kod penicilina. U ovoj grupi se nalazi čitav niz antimikrobnih lijekova koji imaju širok spektar aktivnosti i malu toksičnost. Mehanizam djelovanja je sličan djelovanju penicilina, budući da obje skupine lijekova posjeduju β-laktamski prsten i onemogućuju sintezu bakterijske stijenke vezanjem na PBP molekule, koje imaju važnu funkciju u završnoj etapi sinteze peptidoglikana. Dodatak različitih postraničnih lanaca na molekulu cefalosporina nosi različita farmakokinetska i antibakterijska svojstva pojedinih članova. Cefalosporini su osjetljivi na djelovanje β-laktamaza, premda β-laktamski prsten može biti zaštićen promjenama u strukturi molekule, a što je dovelo do pojave novih generacija cefalosporina s povećanom aktivnošću prema gram-negativnim bakterijama. Najčešće nuspojave su alergijske reakcije (osip, svrbež, vrućica, anafilaktički šok), te proljev ili opstipacija kod oralnih cefalosporina. Ostali beta-laktamski antibiotici Monobaktami imaju monocikličku jezgru s različitim postraničnim lancima. Aztreonam (jedini monobaktam u kliničkoj upotrebi) se veže na PBP 3 molekulu na citoplazmatskoj membrani i inhibira sintezu peptidoglikana. Primjenjuje se parenteralno. Nuspojave su slične kao i kod ostalih β-laktama (mučnina, osip, eozinofilija, blagi porast serumskih transaminaza). Aztreonam se može koristiti kod bolesnika alergičnih na penicilin. Karbapenemi. Imipenem je prvi karbapenem u kliničkoj primjeni. Danas se, uz imipenem, koristi i meropenem, a u nekim zemljama je uveden i ertapenem. To su semisintetski derivati tienamicina koje proizvodi Streptomyces spp. Tienamicini se razlikuju od ostalih β-laktama po tome što imaju transkonfiguraciju hidroksietil postraničnog lanca na poziciji 6, a i po tome što nemaju atom sumpora ili kisika u bicikličkoj jezgri. Takva stereokemija postraničnog lanca osigurava stabilnost prema β-laktamazama. Karbapenemi se vežu na PBP 1 i PBP 2 molekule gram-negativnih i gram-pozitivnih bakterija, te uzrokuju elongaciju i lizu stanica. Stabilni su prema većini plazmidnih i kromosomalnih β-laktamaza, osim onih koje proizvode Stenotrophomonas maltophilia, P. aeruginosa i neki sojevi Bacteroides fragilis. Karbapenemi imaju najširi spektar djelovanja od dosada poznatih antibiotika, djeluju snažno antibakterijski na gram-pozitivne koke, većinu enterobakterija (uključujući i one rezistentne na ostale β-laktame i aminoglikozide), Acinetobacter spp., Enterobacter. spp, Citrobacter spp. i Serratia spp. Rezistencija je zapažena kod nekih sojeva P. aeruginosa i kod Stenotrophomonas maltophilia koji ima intrinzičnu rezistenciju na karbapeneme. Rezistencija kod P. aeruginosa često se razvija u toku terapije. Zbog 241
22 Antibakterijski lijekovi Poglavlje 15 indukcije β-laktamaze zapažen je antagonistički učinak, kada se primjenjuje skupa s cefalosporinima treće generacije ili penicilinima širokog spektra. Nuspojave karbapenema su slične kao i kod ostalih β-laktama (gastrointestinalni poremećaji, alergijske reakcije). Inhibitori beta-laktamaza. Klavulanska kiselina se dobiva iz kulture Strepotmyces clavuligerus i ima slabo prirodno antimikrobno djelovanje, ali inhibira β-laktamaze mnogih gram-pozitivnih i gramnegativnih bakterija. Djeluje kao suicidni (samoubilački, što znači da molekula inhibitora biva uništena nakon vezanja na beta-laktamazu) inhibitor, formirajući ireverzibilni acilni kompleks s β-laktamazom, što dovodi do gubitka aktivnosti tog enzima. Na taj način ima sinergistički efekt s penicilinima i cefalosporinima protiv β-laktamaza-producirajućih sojeva Staphylococcus spp., Klebsiella spp., H. influenzae, M. catarrhalis, N. gonorrhoeae, E. coli, Proteus spp. i Bacteroides spp. Snažno inhibira plazmidne TEM i SHV β-laktamaze, koje su često prisutne kod izolata K. pneumoniae i E. coli. Inducibilne β-laktamaze koje proizvode vrste Enterobacter, Citrobacter, Serratia, Acinetobacter i Pseudomonas, nisu inhibirane klavulanatom i u njih klavulanska kiselina ima antagonistički učinak, tj. inducira produkciju betalaktamaze. Klavulanska kiselina se koristi u kombinaciji s amoksicilinom i tikarcilinom, kojima pojačava učinak protiv onih sojeva koji proizvode β-laktamaze. Sulbaktam je semisintetski 6-desaminopenicilin sulfon sa slabo izraženom antibakterijskom aktivnošću, ali efektivno inhibira plazmidne β-laktamaze koje luče sojevi S. aureus, entrobakterije, H. influenzae, M. catarrhalis, Neisseria spp. i Bacteroides spp. Posebno snažno inhibira plazmidne TEM i SHV β-laktamaze, koje se često nalaze u izolatima K. pneumoniae i E. coli. Jednako kao i klavulanska kiselina, ne djeluje na inducibilne β-laktamaze koje proizvode vrste Enterobacter, Citrobacter, Proteus, Stenotrophomnas maltophilia i Pseudomonas. Često se kombinira s ampicilinom zbog sličnih farmakokinetskih svojstava. Tazobaktam je novi sulfonski derivat, strukturno sličan sulbaktamu, sa slabom intrinzičnom antibakterijskom aktivnošću (primjenjuje se u kombinaciji s piperacilinom). On snažno inhibira β-laktamaze koje proizvode S. aureus, K. pneumoniae i E. coli, Enterobacter, Citrobacter, H. influenzae, M. catarrhalis, Neisseria spp i Bacteroides spp. Veže se na PBP 1 i PBP 2 molekule na citoplazmatskoj membrani bakterija, kao i sulbaktam i klavulanski kiselina, snizuje MIK β-laktamskog antibiotika i do 20 puta u onih sojeva koji proizvode β-laktamaze. AMINOGLIKOZIDI Mehanizam djelovanja. Aminoglikozidi su baktericidni antibiotici koji inhibiraju sintezu bjelančevina ireverzibilnim vezanjem na 30 S podjedinicu ribosoma. Ribosom, na koji se vezao aminoglikozid, ne može vršiti translaciju mrnk tokom sinteze proteina, što dovodi do uginuća bakterijske stanice. Drugi mehanizam je pogrešno čitanje genetskog koda, što rezultira sintezom neupotrebljivih bjelančevina koje ne vrše svoju funkciju kao enzimi ili strukturni djelovi bakterijske stanice. Prodiranje aminoglikozida do ciljnog mjesta na ribosomu odvija se aerobno uz utrošak ATP. Djelovanje aminoglikozida je potencirano u prisustvu inhibitora sinteze staničnog zida, kao što su β-laktamski antibiotici ili vankomicin, te usljed toga kombinacija β-laktama i aminoglikozida ima sinergističko djelovanje na bakterije. Najvažniji mehanizmi rezistencije na aminoglikozide su: enzimska modifikacija (fosforilacija, acetilacija), promjene na ribosomskim proteinima koje rezultiraju u smanjenom vezanju lijeka na ribosome (opisano kod enterokoka, stafilokoka, gonokoka), Intrinzična rezistencija na aminoglikozide, kod anaerobnih bakterija, uzrokovana je nedostatkom citokromskog elektronskog transportnog sistema, koji je potreban za ulazak tih antibiotika u citoplazmu bakterijske stanice. Farmakologija. Svi aminoglikozidi imaju slična farmakološka svojstva. Slabo se resorbiraju iz gastrointestinalnog trakta, pa se primjenjuju parenteralno. Zbog visoke toksičnosti kod sistemske primjene, neomicin je dostupan samo za oralnu i lokalnu primjenu. Nakon intravenozne (i.v.) primjene, aminoglikozidi se distribuiraju u ekstravaskularnom prostoru, ali slabo prodiru u likvor, oko, bilijarni trakt, prostatu i traheobronhalne sekrete, čak i u prisustvu upale. U odraslih, s normalnom bubrežnom funkcijom, poluvrijeme eliminacije iz plazme iznosi 2 do 3 sata. Aminoglikozidi se pretežno izlučuju nepromijenjeni preko bubrega, glomerularnom filtracijom i tubularnom sekrecijom. Kod bolesnika s renalnom insuficijencijom, ovi lijekovi se akumuliraju u organizmu, pa je potrebno smanjenje doze i praćenje serumske koncentracije lijeka, da bi se osigurala adekvatna terapija i smanjila toksičnost. 242
23 B. Bedeni} Spektar djelovanja. Aminoglikozidi, kao grupa lijekova, posebno su djelotvorni protiv enterobakterija, P. aeruginosa, Acinetobacter spp., i Providencia spp., a od gram-pozitivnih bakterija djeluju dobro na stafilokoke, a znatno slabije na streptokoke. Postoje razlike u spektru djelovanja između pojedinih aminoglikozida. Streptomicin je uveden kao prvi aminoglikozid za terapiju teških infekcija uzrokovanih gramnegativnim bakterijama. Međutim, danas ima ograničeni spektar zbog proširene pojave rezistencije među gram-negativnim bacilima. Streptomicin se primjenjuje kao monoterapija za liječenje tularemije (uzročnik F. tularensis) i kuge (Yerisinia pestis), a u kombinaciji s tetraciklinima koristi se za liječnje bruceloze. Među aminoglikozidima, streptomicin ima najsnažnije djelovanje na M. tuberculosis, a može se koristiti, u kombinaciji s penicilinom ili vankomicinom, za terapiju infektivnog endokarditisa uzrokovanog viridans streptokokima ili enterokokima, ukoliko uzročnici nemaju ribosomsku ili enzimatsku rezistenciju visokog stupnja na streptomicin. Kanamicin ima ograničeni spektar djelovanja zbog uobičajene rezistencije sojeva P. aeruginosa i česte pojave rezistencije zbog sinteze inaktivirajućih enzima kodiranih plazmidima među enterobakterijama, pa se danas koristi jedino u kombinaciji s ostalim antibioticima u terapiji tuberkuloze. Gentamicin i tobramicin imaju sličan antimikrobni profil, ali je gentamicin djelotvorniji protiv Serratia spp., dok tobramicin ima jače djelovanje na P. aeruginosa. Koriste se za liječenje teških infekcija respiratornog, urinarnog trakta i opekotina. Gentamicin i tobramicin su osjetljivi na iste modificirajuće enzime koje proizvode rezistentne bakterije (6-acetiltransferaza, 4-adeniltransferaza). Netilmicin ima sličan spektar djelovanja kao gentamicin, ali je efikasniji od njega prema koagulaza pozitivnim i koagulaza negativnim stafilokokima. Aminociklitoli su strukturno slični aminoglikozidima, a u tu skupinu ubrajamo spektinomicin, koji se koristi za liječenje gonoreje. Sistemska primjena aminoglikozida kod infekcija uzrokovanih gram-negativnim bacilima (sepsa, abdominalna sepsa ili sepsa uzrokovana infekcijom u zdjelici), podrazumijeva primjenu gentamicina zbog dokazane djelotvornosti kod teških infekcija, dok tobramicin i netilmicin pokazuju manju ototoksičnost i nefrotoksičnost. Tobramicin ima prednost kod infekcija uzrokovanih s P. aeruginosa. Amikacin ima najširi antibakterijski spektar djelovanja, ali ga treba čuvati za liječenje infekcija uzrokovanih sojevima koji su rezistentni na gentamicin. Aminoglikozidi se uključuju, u kombinaciji s β-laktamima, za terapiju sepse prije nego se identificira uzročnik. Za liječenje bakterijskog endokarditisa uzrokovanog streptokokima, enterokokima ili stafilokokima, aminoglikozidi se koriste u kombinaciji s β-laktamskim antibioticima za liječenje endokarditisa. Aminoglikozidi se također koriste za liječenje tuberkuloze, tularemije, kuge i bruceloze. Lokalna primjena gentamicina se ne preporučuje, jer se brzo selekcioniraju rezistentni sojevi pseudomonasa, enterobakterija i stafilokoka. Neomicin je suviše toksičan za sistemsku primjenu, ali je djelotvoran ako se primjeni lokalno u liječenju infekcije spojnice oka ili vanjskog uha. Također, primjenjuje se i za preoperativnu sterilizaciju crijeva bolesnika. Nuspojave. Oštećenja sluha (ototoksičnost) se češće javljaju tokom primjene amikacina, neomicina i kanamicina, a oštećenja vestibularnog aparata su češća kod primjene streptomicina, gentamicina i tobramicina. Prvi simptom oštećenja slušnog živca može biti zujanje u ušima, dok rani znakovi oštećenja vestibularne funkcije uključuju glavobolju, koja se pojavljuje pri promjeni položaja tijela, vrtoglavicu ili mučninu. Ovi su simptomi razlog da se obustavi primjena lijeka ili da se promjeni doza lijeka. Ototoksičnost se može pojačati ako se istovremeno uz aminoglikozide, primjenjuju i drugi ototoksični lijekovi, kao što su diuretici Henleove petlje. Aminoglikozidi mogu dovesti do oštećenja stanica bubrežnih tubula (nefrotoksičnost) u kojima se gomilaju, a toksični učinak ovisi o primijenjenoj dozi. Predisponirajući činioci su nizak krvni tlak, prethodna terapija nefrotoksičnim lijekovima, kao što su diuretici Henleove petlje i poodmakla životna dob. Nefrotoksičnost je izrazitija kod neomicina i gentamicina. Velike količine streptomicina mogu izazvati respiratornu paralizu zbog kompetitivnog neuromuskularnog bloka (neurotoksičnost), posebno kod bolesnika koji su dobili mišićne relaksanse ili boluju od mijastenije gravis. U ostale nuspojave ubrajamo osip, povišenu temperaturu i hematološke poremećaje zbog depresije koštane srži. 243
24 Antibakterijski lijekovi Poglavlje 15 SULFONAMIDI Mehanizam djelovanja. Sulfonamidi djeluju na principu kompetitivne inhibicije, ometanjem metabolizma folne kiseline. Folna kiselina je faktor rasta mnogih bakterija i prekursor je purina koji su važan sastavni dio DNK i RNK. Folna kiselina ima svog metaboličkog prethodnika, paraamino-benzojeva kiselina (PABA), kojoj su sulfonamidi kemijski slični. Neke bakterije moraju sintetizirati vlastitu folnu kiselinu iz PABA. Pretpostavlja se da se u tim bakterijama sulfonamidi natječu s PABA i njihova neznatno različita struktura onemogućuje bakterijama sintezu folne kiseline. Bakterije lišene neophodnog metabolita se prestaju dijeliti, tako da su sulfonamidi u prvom redu bakteriostatski antibiotici. Organizam čovjeka nije sposoban sintetizirati folnu kiselinu, nego se koristi već formiranim folatima iz lisnatog povrća i stoga njegove stanice ne mogu biti oštećene metaboličkim učincima sulfonamida. Sulfonamidi se često koriste u kombinaciji s trimetoprimom zbog sinergističkog učinka. Sulfonamidi ometaju pretvaranje PABA u dihidrofolnu kiselinu, dok trimetoprim zaustavlja sljedeću fazu, a to je konverzija folne u foliničnu (tetrahidrofolnu) kiselinu. Ova inhibicija dviju sukcesivnih reakcija u sintezi DNK i RNK, pretvara dva bakteriostatska antibiotika u baktericidnu kombinaciju. To je primjer farmakološkog potenciranja; mikroorganizmi koji su slabije osjetljivi na pojedinačne komponente mogu biti uništeni primjenom kombinacije komponenata. Prva faza koju inhibiraju sulfonamidi ne odvija se u ljudskom organizmu, dok se druga faza koju inhibira trimetoprim odvija, ali je osjetljivost inhibiranog enzima (dihidrofolat reduktaza) u bakterijama puta veća nego u čovjeku, tako da je taj lijek za čovjeka relativno neškodljiv. Međutim, dugotrajna primjena lijeka može ometati hematopoezu. Mehanizmi rezistencije nastaju usljed promjena ciljnog metaboličkog puta, pri čemu se koristi alternativni metabolički put za sintezu nukleinskih kiselina, ili zbog smanjenja permeabilnosti. Farmakokinetika. Sulfonamidi se dobro resorbiraju u crijevima, tako da su pogodni za oralnu primjenu. Vezanje za bjelančevine plazme iznosi između 20% i 90%, ovisno o vrsti, a koncentracije u likvoru iznose 40% do 80% onih u plazmi. Metaboliziraju se konjugacijom s acetilnom skupinom, a izlučuju se glomerularnom filtracijom ili tubularnom sekrecijom. U alkalnoj mokraći su djelotvorniji i postižu veće koncentracije. Spektar djelovanja. Sulfonamidi djeluju bakteriostatski na gram-pozitivne bakterije: stafilokoke, streptokoke, osim enterokoka, B. anthracis; i na gram-negativne bakterije: najserije, enterobakterije (E. coli, Shigella spp., Salmonellae spp., Yersiniae spp., neki sojevi Proteusa), klamidije i nokardije. Indikacije za primjenu sulfonamida u kombinaciji s trimetoprimom su: pneumonije uzrokovane Pneumocystis carinii, infekcije uzrokovane Nocardiom asteroides, crijevna groznica uzrokovana S. Typhi i S. Paratyphi, ako je uzročnik rezistentan na kloramfenikol, bacilarna dizenterija, ako je uzročnik rezistentan na amoksicilin. Indikacije za primjenu trimetoprima (bez sulfonamida) su: infekcije urinarnog trakta uzrokovane osjetljivim mikroorganizmima (E. coli, Proteus), infekcije respiratornog traka uzrokovane S. pneumoniae i H. influenzae. Indikacije za primjenu sulfonamida (bez trimetoprima) su: meningokokni meningitis, infekcije urinarnog trakta uzrokovane osjetljivim mikroorganizmima, u rijetkim slučajevima infekcije respiratornog trakta. U najčešće nuspojave spadaju slabost, glavobolja, mučnina, povraćanje, proljev, a u rijetkim slučajevima cijanoza zbog methemoglobinemije. Kristalurija može nastati u toku primjene sulfonamida koji se brzo izlučuju, može proći bez simptoma ili izazvati kolike, hematuriju, oliguriju, pa čak i anuriju; važno je uzimati što više tekućine i alkalizirati mokraću kalijevim ili natrijevim bikarbonatom. Alergijske reakcije uključuju osip, temperaturu, hepatitis, agranulocitozu, purpuru, aplastičnu anemiju, periferni neuritis, sindrom nalik na serumsku bolest, nodozni poliarteritis i Stevens-Johnsonov sindrom. Kombinacija trimetoprima i sulfametoksazola (kotrimoksazol) se obično dobro podnosi. TETRACIKLINI Mehanizam djelovanja. Tetraciklini su bakteriostatski antibiotici, koji inhibiraju sintezu proteina vežući se na 30S podjedinicu ribosoma, sprječavaju pristup aminokiseline vezane na molekulu transportne (prijenosne) (t)rnk na ribosom, na koji je vezana glasnička (m)rnk. Ovaj mehanizam djelovanja se ostvaruje u stanicama čovjeka i u bakterijskoj stanici, s tim da su bakterijske stanice osjetljivije, jer imaju aktivni transportni sistem koji prenosi tetracikline nasuprot koncentracijskog gradijenta, čime se postižu visoke koncentracije unutar bakterijske sta- 244
25 B. Bedeni} nice. Na taj način se postiže selektivnost, budući stanice ljudskog organizma ne posjeduju slični mehanizam za koncentraciju tetraciklina. Farmakokinetika. Djelomično se apsorbiraju iz probavnog trakta, te u crijevnom sadržaju ostaje dovoljna količina da uništi crijevnu floru i izazove nuspojave, kao što je pseudomembranski enterokolitis. Mliječni proizvodi smanjuju apsorpciju ovih antibiotika, budući kalcij stvara kelate s tetraciklinima. Slično djeluju i antacidi, i preparati željeza. Dobro se raspoređuju po čitavom organizmu, ali slabo prodiru u cerebrospinalni likvor (CSL). Koncentracije u žuči su 5-10 puta veće nego u plazmi, izlučuju se nepromijenjeni urinom. Biološko poluvrijeme se kreće u rasponu od 6 do 12 sati, ali se produžuje kod oštećene bubrežne funkcije. Antianabolni učinak tetraciklina očituje se porastom ureje i kreatinina u krvi. Doksiciklin i minociklin, u određenim slučajevima, mogu se primjeniti kod oštećenja bubrega jer se djelomično izlučuju ekstrarenalnim putovima. Spektar djelovanja tetraciklina je bakteriostatski na većinu gram-pozitivnih i gram-negativnih koka, na enterobakterije, vrste iz roda Heamophilus spp., na Vibrio cholerae, klostridije, aktinomicete, spirohete, rikecije i klamidije. Terapijska primjena tetraciklina Tetraciklini su terapija izbora za brucelozu (u kombinaciji sa streptomicinom), koleru, pneumoniju uzrokovanu mikoplazmom, infekcije uzrokovane rikecijama (kloramfenikol je također djelotvoran), povratnu groznicu, tularemiju, psitakozu, venerični limfogranulom, trahom, salpingitis uzrokovan klamidijama, nespecifični uretritis, granuloma inguinale, melidiozu, tropsku spru. Kao alternativna terapija tetraciklini se koriste za liječenje: akutnog ili kroničnog bronhitisa, infekcija bilijarnog sistema, sinusitisa, bubonske kuge (streptomicin je bolji), gonoreje, luesa, stomatitis angularis (žvale), aktinomikoze, antraksa, leptospiroze, meningitisa uzrokovanog s H. influenzae, bacilarne dizenterije, infekcije uzrokovane s Y. enterocolitica, bolesti štakorskog ugriza, Whippleove bolesti i falciparum malarije (u kombinaciji s kininom), te za eradikaciju kliconoštva meningokoka (samo minociklin). Najvažnije nuspojave su: od strane GI trakta (mučnina, povraćanje, proljev usljed poremećaja crijevne flore), oportunističke infekcije (Candida albicans, Proteus spp., Pseudomonas spp., stafilokoki) kod čije je pojave potrebno prekinuti terapiju, poremećaj apsorpcije B vitamina (stomatitis), glositis, disfagija, oštećenje kosti i zubi kod fetusa i djece (posljedica stvaranja kelata s kalcijevim fosfatom, što uzrokuje hipoplaziju cakline, malformaciju krune, žutu ili smeđu pigmentaciju zubi, te povećanu sklonost karijesu). Usljed toga, tetraciklini su kontraindicirani nakon 14 sedmica trudnoće, te kod djece do 8. godine života. Antianabolički učinak uzrokuje porast ureje u krvi što može imati značaj kod oštećenja bubrega. Tetraciklini, također, mogu uzrokovati fotosenzibilizaciju i pojavu osipa na koži, te porast jetrenih transaminaza. MAKROLIDI Mehanizam djelovanja. Makrolidi su bakteriostatski antibiotici, koji se vežu na 50S podjedinicu ribosoma i sprječavaju kontakt trnk na koju je vezana aminokiselina s mrnk, te na taj način ometaju sintezu bjelančevina. Farmakokinetika. Makrolidi su pogodni za oralnu primjenu. Eritromicin-estolat hidrolizira se u tijelu i pretvara se u aktivni eritromicin i dobro prodire u tkiva. Poluvrijeme eliminacije u plazmi je 1.5 h, a gotovo potpuno se izlučuje preko žuči i stolice. Spektar djelovanja obuhvaća gram-pozitivne bakterije, spirohete, brucele i legionele. Terapijska primjena eritromicina obuhvaća: pneumoniju uzrokovanu mikoplazmom u djece, (kod odraslih treba dati prednost tetraciklinu), legionarsku bolest (L. pneumophila) kod koje se daje sâm ili u kombinaciji s rifampicinom, infekcije uzrokovane klamidijama, difteriju, pertussis, gastroenteritis uzrokovan C. jejuni (odstranjuje mikroorganizam iz stolice, ali pritom ne mora doći do skraćivanja trajanje simptoma). Koristi se i kao alternativna terapija za liječenje bolesnika preosjetljivih na penicilin, koji boluju od infekcije uzrokovane stafilokokima, streptokokima ili T. palidum. Eritromicin nije toksičan, ali može uzrokovati kolestatski hepatitis, praćen abdominalnim bolovima i povišenom temperaturom. Nakon prestanka uzimanja lijeka, obično dolazi do potpunog oporavka. U rijeđim slučajevima mogu se javiti alergijske reakcije, gastrointestinalni poremećaji i oportunističke infekcije. KLORAMFENIKOL Mehanizam djelovanja je bakteriostatski, na taj način što se onemogućava pričvrščivanje rastućeg polipeptidnog lanca na 50S jedinicu ribosoma. Farmakokinetika. Pogodan je za oralnu primjenu, a primjenjuje se u obliku estera: palmitata koji je ne- 245
26 Antibakterijski lijekovi Poglavlje 15 topiv i koristi se za pripremanje suspenzije, te sukcinata koji je topiv i daje se parenteralno. Raspodjeljuje se ravnomjerno u tjelesnim tekućinama, ali je koncentracija u likvoru i pleuralnoj tekućini upola manja nego u plazmi. Inaktivira se konjugacijom s glukuronidom u jetri. Poluvrijeme eliminacije je otprilike 2 sata u odraslih, a u novorođenčadi su procesi hidroksilacije i glukuronidacije polagani, pa su koncentracije u plazmi vrlo varijabilne. Spektar djelovanja je baktericidan prema većini sojeva H. influenzae i pneumokoka, a djeluje bakteriostatski na enterobakterije, najserije, anaerobne bakterije i gram-pozitivne koke, djeluje također na mikoplazme, klamidije i rikecije, dok je P. aeruginosa rezistentan. Terapijska primjena kloramfenikola obuhvaća: bakterijski meningitis (u kombinaciji s penicilinom) dok se ne utvrdi uzročnik (nastavak terapije s kloramfenikolom, ako se radi o H. influenzae), liječenje moždanog apscesa u kombinaciji s penicilinom, teške infekcije (npr. infekcije CNS-a ili respiratornog sistema) uzrokovane s H. influenzae kod bolesnika preosjetljivih na β-laktame, sistemske infekcije uzrokovane salmonelama (tifusna groznica, sepsa uzrokovana salmonelama) pri čemu se može zamijeniti s amoksicilinom ili kombinacijom sulfametoksazola i trimetoprima koji imaju manje nuspojava, infekcije oka uzrokovane osjetljivim uzročnicima (dobro prodire u očnu vodicu i staklovinu nakon lokalne ili sistemske primjene). Koristi se kao alternativna terapija za liječenje infekcija uzrokovanih klamidijama i rikecijama, ako se zbog bilo kojeg razloga ne mogu primjeniti lijekovi izbora (tetraciklini ili eritromicin) Nuspojave kloramfenikola su: poremećaji u probavnom traktu zbog promjene bakterijske flore, osip na koži, oštećenje vidnog živca, hematološki poremećaji (najteži oblik je aplastična anemija, ali se mogu pojaviti i trombocitopenija ili agranulocitoza, pa su potrebne redovite kontrole krvne slike), cirkulacijski kolaps novorođenčadi (grey sindrom) koji nastaje zbog nezrelosti sistema za glukuronidaciju i izlučivanje kloramfenikola. LINKOZAMINI Mehanizam djelovanja. Klindamicin je klorirani derivat linkomicina, koji ga je uglavnom zamijenio zbog bolje antibakterijske aktivnosti i bolje apsorpcije iz crijeva.veže se na ribosome bakterija i inhibira sintezu bjelančevina, a također pojačava opsonizaciju i fagocitozu bakterija, te aktivira komplement. Klindamicin, kao i kloramfenikol, inhibira elongaciju rastućeg polipeptidnog lanca vezanjem na 50S podjedinicu ribosoma. Rezistencija na klindamicin može nastati zbog metilacije 23S ribosomske (r)rnk. Ovu rezistenciju mogu inducirati i klindamicin i eritromicin, tako da može nastati unakrsna rezistencija na oba antibiotika. Spektar djelovanja klindamicina obuhvaća grampozitivne koke i štapiće, dok mu je učinak na gramnegativne bakterije znatno slabiji (izuzetak su anaerobne bakterije iz roda Bacteroides). Enterobakterije i Pseudomonas spp su rezistentni. Indikacije za primjenu klindamicina su: anaerobne infekcije (orodentalne infekcije, aspiracijska pneumonija, plućni apsces) ako je uzročnik rezistentan na penicilin (kod infekcija središnjeg živčanog sistema se ne preporučuje), intraabdominalna sepsa i upalna bolest zdjelice kod žena (klindamicin se kombinira s aminoglikozidima), infekcije kosti i zglobova s obzirom da lijek dobro prodire u ova tkiva. Najznačajnija nuspojava je pseudomembranski enterokolitis koji nastaje kao posljedica oportunističke infekcije s C. difficile, koji proizvodi enterotoksin, tako da odmah nakon pojave proljeva treba prestati uzimanje klindamicina. Kod i.v. primjene može doći do pojave tromboflebitisa. KINOLONI Mehanizam djelovanja kinolona usmjeren je na DNA-girazu, bakterijski enzim neophodan za replikaciju DNK. Djeluju i baktericidno inhibicijom sinteze DNK. Antibakterijsko djelovanje je smanjeno u prisustvu niskog ph, urina i dvovalentnih kationa (Mg 2+ i Ca 2+ ). Farmakologija. Kinoloni se dobro resorbiraju iz GI trakta. Antacidi koji sadrže aluminij ili magnezij smanjuju apsorpciju kinolona iz GI trakta i njihovu koncentraciju u serumu. Najviše koncentracije u plazmi postižu za 1 do 2 sata nakon primjene, a stupanj vezanja za proteine plazme je nizak. Imaju dug poluživot u plazmi, što omogućuje doziranje dva puta dnevno. Dobro prodiru u pluća, bubrege, mišiće, kosti, stijenku crijeva i ekstravaskularnu tekućinu. Koncentracije u urinu su 25 do 100 puta veće nego u plazmi, te su pogodni za liječenje urinarnih infekcija. Koncentracije u likvoru su niske, tako da nisu pogodni za liječenje meningitisa. Dobro prodiru u fagocite, te su koncentracije u neutrofilima 14 puta veće nego u serumu, i to svojstvo pridonosi njihovoj izvrsnoj aktivnosti protiv intracelularnih patogena 246
27 B. Bedeni} kao što su Brucella spp., Listeria spp., Salmonella spp. i Mycobacterium spp. Kinoloni se eliminiraju preko bubrega aktivnom tubularnom sekrecijom i glomelurarnom filtracijom. Njihova renalna eliminacija je blokirana probenecidom. Izlučivanje ovih lijekova je usporeno kod insuficijencije bubrega. Spektar djelovanja kinolona je snažno antibakterijsko protiv enterobakterija, P. aeruginosa, Acinetobacter spp., H. influenzae i gram-negativnih koka, kao što su N. gonorrhoeae, N. meningitidis i Moraxella catarrhalis. Također su aktivni i prema stafilokokima, uključujući i MRSA, ali su slabije aktivni prema streptokokima i enterokokima. Nisu djelotvorni protiv anaerobnih bakterija, kao što su B. fragilis i C. difficile. Enteropatogeni gram-negativni bacili, kao što su salmonele, šigele, Yersinia enterocolitica, Vibrio spp, Aeromonas spp, Plesiomonas spp, Campylobacter jejuni i Campylobacter coli, i enterotoksični sojevi E. coli, osjetljivi su prema kinolonima. Klinička istraživanja su pokazala da su kinoloni djelotvorni u liječenju i prevenciji infektivne dijareje. Legionella spp. je osjetljiva na ovu skupinu antibiotika, a minimalne inhibitorne koncentracije (MIK) za većinu sojeva su veoma niske. Ciprofloksacin je najaktivniji od svih kinolona prema P. aeruginosa, dok su B. cepacia i S. maltophilia rezistentni na kinolone. In vitro su aktivni prema M. tuberculosis, M. fortuitum, M. cheloneae, M. kansasii i M. xenopi, dok prema M. avium i M. intracellulare pokazuju samo neznatnu aktivnost. Djeluju snažno baktericidno na izolate Chlamydia trachomatis i Mycoplasma hominis, a slabije na Ureaplasma urealyticum. Ciprofloksacin i pefloksacin inhibiraju izolate Rickettsia conori, Rickettsia rickettsii i Coxiella burneti, a utvrđeno je da djeluju i na protozoon Plasmodium falciparum. Nocardia spp. je rezistentna na ovu skupinu antibiotika. Pri testiranju osjetljivosti na antibiotike, ne pokazuju značajan inokulum efekt, što znači da velika gustoća bakterija ne utječe na rezultat testiranja. Kombinacija ovih antibiotika s β-laktamima ili aminoglikozidima ima aditivno ili sinergističko djelovanje. Baktericidni učinak kinolona se poništava u prisustvu rifampicina ili kloramfenikola. Najvažniji predstavnici su nalidiksična kiselina, oksolinična kiselina, norfloksacin, ciprofloksacin, pefloksacin, enoksacin, ofloksacin i lomefloksacin. Nalidiksična kiselina je prvi kinolon u kliničkoj upotrebi, koji se koristio za liječenje urinarnih infekcija, ali je danas zbog proširene rezistencije zamijenjena novijim lijekovima. Najčešće nuspojave su simptomi od strane gastrointestinalnog (GI) trakta, kao što su mučnina, povraćanje i proljev, koji se pojavljuju u oko 5% bolesnika, a među teške nuspojave spada enterokolitis uzrokovan s C. difficile. Ostale nuspojave uključuju glavobolje, vrtoglavicu, umor, nesanicu i osjećaj nemira. Alergijske reakcije su rijetke i manifestiraju se kao osip, urtikarija, svrbež i eozinofilija. Kinoloni su kontraindicirani kod trudnica, dojilja i djece do 14 godina starosti zbog mogućnosti izazivanja koštanih malformacija. GLIKOPEPTIDI U glikopeptide ubrajamo vankomicin i teikoplanin. Mehanizam djelovanja glikopeptida je inhibicija sinteze peptidoglikana u staničnoj stijenci bakterije stvaranjem kompleksa s D-alanil-D-alaninom, koji je prekursor u sintezi staničnog zida. Na stafilokoke djeluju baktericidno, a na enterokoke bakteriostatski. Farmakologija. Vankomicin je dostupan u oralnom ili parenteralnom obliku. Njegova resorpcija iz GI trakta je slaba, usljed čega postiže visoke koncentracije u stolici, pa je pogodan za liječenje pseudomembranskog enterokolitisa. Terapijske koncentracije postiže u sinovijalnoj, perikardijalnoj i pleuralnoj tekućini i ascitesu, ali slabo prodire u likvor. Poluvrijeme u plazmi iznosti 6 do 8 sati, a izlučuje se glomerularnom filtracijom. Spektar djelovanja glikopeptida obuhvaća aerobne i anaerobne gram-pozitivne bakterije (stafilokoki uključujuči i MRSA, meticilin rezistentni S. aureus), streptokoki, enterokoki, Corynebacterium spp., Bacillus spp, Lactobacillus spp., L. monocytogenes, Clostridium spp., Actinomyces spp.). Sve češće dolazi do pojave rezistencije među enterokokima i koagulaza negativnim stafilkokima. Gliko peptidi ne djeluju na gram-negativne bakterije i mikobakterije. Imaju sinergistički učinak s aminoglikozidima i rifampicinom protiv stafilokoka, enterokoka, streptokoka i listerija. Terapijske indikacije za primjenu glikopeptida su: infekcije čiji je uzročnik MRSA ili pneumokok rezistentan na penicilin, endokarditis uzrokovan grampozitivnim bakterijama u bolesnika alergičnih na penicilin, infekcije uzrokovane korinebakterijama JK grupe, meningitis uzrokovan s Flavobacterium meningosepticum, enterokolitis nakon antibiotske terapije (C. difficile). 247
28 Antibakterijski lijekovi Poglavlje 15 METRONIDAZOL Mehanizam djelovanja. Za baktericidni učinak metronidazola važna je nitro grupa u kemijskoj strukturi. Metronidazol u citoplazmi reducira se pod djelovanjem nitroreduktaze, pa nastaje visokotoksični interrmedijarni produkt, koji se razlaže u slobodne radikale što rezultira oštećenjem DNK. Spektar djelovanja metronidazola obuhvaća anaerobne bakterije (B. fragilis, Fusobacterium spp., Clostridium spp.), Trichomonas vaginalis, Giardia lamblia i Enthamoeba histolytica, dok su Actinomyces, Arachnia i Propionibacterium spp. rezistentni. Terapijske indikacije za primjenu metronidazola su: sepsa uzrokovana anaerobnim bakterijama (poslije kirurškog zahvata u abdomenu), intraabdominalne infekcije, infekcije u maloj zdjelici, osteomijelitis, apsces mozga, prevencija kirurške infekcije nakon zahvata na debelom crijevu, trihomonijaza urogenitalnog trakta i amebijaza (intestinalna i ekstraintestinalna. OKSAZOLIDINONI Mehanizam djelovanja linezolida je inhibicija inicijacije sinteze proteina vezanjem na 50S podjedinicu ribosoma i time baktericidno djelovanje. Mehanizmi rezistencije su efluks u gram-negativnih bakterija i mutacija 23S rrnk. Spektar djelovanja obuhvaća: gram-pozitivne koke (stafilokoki, streptokoki, enterokoki), a umjerena aktivnost prema M. catarrhalis i Bacteroides spp. Haemophilus influenzae je obično rezistentan. Terapijske indikacije su teške infekcije uzrokovane gram-pozitivnim kokima, MRSA, VRSA (vankomicin rezistentan S. aureus), VRE (vankomicin-rezistentan enterokok). STREPTOGRAMINI Quinupristin-dalfopristin je parenteralni streptogramin, koji sadržava mješavinu (30:70) dva semisintetska derivata pristinamicina (grupa B streptogramina) i dalfopristina (grupa A streptogramina). Dvije komponente djeluju sinergistički, u smislu inhibicije gram-pozitivnih bakterija, uključujući i MRSA, VRE i penicilin rezistentne pneumokoke. Quinupristindalfopristin je aktivan prema nekim anaerobima i nekim gram-negativnim bakterijama (npr. Neisseria gonorrhoeae i Haemophilus influenzae). Streptogramini nisu djelotvorni prema enterobakterijama i nefermentativnim bakterijama. Opisani su vankomicin-rezistentni enterokoki, koji su također otporni na streptogramine, ali su rijetki. GLIKOLIPIDI Glikolipidi su najnoviji antibiotici, čiji je glavni predstavnik daptomicin. Djeluju na gram-pozitivne koke, uključujući MRSA, VRE i multirezistentne sojeve koagulaza negativnih stafilokoka. Ugrađuju se u citoplazmatsku membranu gram-pozitivnih bakterija i dovode do stvaranja pora, što dovodi do efluksa važnih komponenti bakterijske stanice, posebno kalijevih iona, a to rezultira u depolarizaciji citoplazmatske membrane i smrti stanice. Daptomicin ostvaruje baktericidni učinak bez lize stanica, što znači da se smanjuje rizik oslobađanja egzotoksina u cirkulaciju. BACITRACIN Bacitracin je polipeptid koji se dobiva od bakterije Bacillus subtilis. Slabo se resorbira iz intestinalnog trakta, tako da se koristi za lokalnu primjenu na kožu, sluznicu i rane. POLIMIKSINI Polimiksini su kationski polipeptidi koji su nefrotoksični i neurotoksični. Polimiksini su baktericidni za gram-negativni aerobne bakterije. Mehanizam njihova djelovanja je vezanje na citoplazmatsku membranu bogatu fosfolipidima, te razaranje membranskih funkcija aktivnog transporta i permeabilne barijere. Zbog toksičnosti uglavnom se koriste lokalno, a vrlo rijetko kod sistemskih infekcija. Metode testiranja osjetljivosti bakterija na antimikrobne lijekove DILUCIJSKE METODE Dilucijskim metodama određuje se minimalna inhibitorna koncentracija, a to je najniža koncentracija antibiotika koja sprječava rast bakterija.može se izvoditi na tekućoj ili čvrstoj podlozi, tako da se antibiotik serijski razrijeđuje, inkorporira u bakteriološku podlogu i zatim se u nju, ili na nju, inokulira ispitivani soj bakterije. Nakon inkubacije od 18 do 24 sata na 35 C - 37 C gleda se prisutnost zamućenja (bujona) ili porast kolonija (na čvrstoj) podlozi. Koncentracija antibiotika, koja se nalazi u prvoj podlozi (u nizu), u kojoj nema porasta bakterija, naziva se minimalna inhibitorna koncentracija (MIK) i izražava se mg/l ili µg/ml (Slika 15.2). Dilucijska metoda se može izvoditi kao mikrodilucija, 248
29 B. Bedeni} Slika Mikrodilucijski test u bujonu: bunarčići u kojima je bujon ostao bistar, sadržavaju dovoljno visoku koncentraciju antibiotika potrebnu za inhibiciju rasta, a oni u kojima se bujon zamutio, sadržavaju antibiotik u koncentraciji nižoj od MIK-a tako da su se bakterije umnožile (Izvor: iz vlastite zbirke, B. Bedenić, 2005.) ako se izvodi u mikrotitar pločicama, ili kao makrodilucija, ako se izvodi u nizu epruveta. Danas se uglavnom primjenjuje mikrodilucijska metoda, jer je jednostavnija za izvođenje i jeftinija (manji je utrošak podloga). Ako se u dilucijskoj metodi u bujonu, nakon inkubacije od 18 do 24 sata, podloge bez vidljivog porasta bakterija subkultiviraju na čvrstu podlogu bez antibiotika, može se odrediti i minimalna baktericidna koncentracija (MBK), tj. ona najniža koncentracija antibiotika koja ubija određenu bakteriju, a izražava se također u mg/l. MBK je u pravilu veća od MIK vrijednosti do 32 puta (ako je omjer MIK/MBK veći od 32, govori se o toleranciji bakterije na antibiotik). MIK se određuje samo ukoliko postoje posebne indikacije, kao što su: testiranje osjetljivosti bakterija koje rastu sporo, kod anaerobnih bakterija, ako postoji potreba preciznog određivanja osjetljivosti bakterije koja je u antibiogramu slabije osjetljiva na određeni antibiotik (kako bi se mogao primjenjivati u visokoj dozi), te kod bakterija kod kojih disk-difuzijski test daje nepouzdane rezultate (kao što je npr. penicilin rezistentni pneumokok izoliran iz likvora ili hemokulture). DIFUZIJSKA METODA Antibiogram je kvalitativni test, vrlo dobro standardiziran za gotovo sve brzorastuće aerobne i fakultativno anaerobne bakterije, i u općoj je primjeni u većini kliničkih mikrobioloških laboratorija. Najčešće se izvodi kao disk-difuzija: papirnati disk, natopljen standardiziranom količinom antibiotika, postavlja se na površinu čvrste podloge (Mueller-Hinton agar, M-H) na koju se prethodno inokulira čista kultura ispitivane bakterije, te se inkubira na temperaturi od 35 C - 37 C kroz sata (Slika 15.3). Antibiotik iz diska difundira u podlogu, te ako je djelotvoran, sprječava bakterijski rast, tako da bakterija poraste tek na određenoj udaljenosti od diska na kojoj je koncentracija difundiranog antibiotika premala i stoga nedjelotvorna (Slika 15.4). Ovaj izostanak rasta se naziva zona inhibicije (prečnik zone mjeri se u mm). Osjetljivost soja se interpretira ovisno o promjeru inhibicijske zone kao: osjetljiv (3), umjereno osjetljiv (2) i rezistentan (0). Kod izvođenja antibiograma veličinu inokuluma, s kojom se izvodi test, treba podesiti prema standardnoj McFarland suspenziji 0,5 tako da se dobije semi-konfluentni rast na podlozi. Kod prevelikog inokuluma inhibicijske zone biće (lažno) manje, a kod premalog inokuluma (lažno) prevelike. Također, treba paziti da se inokulum nanese ravnomjerno po površini ploče i da diskovi budu dovoljno udaljeni, kako jedan od drugoga, tako i od ruba ploče. E-test predstavlja kombinaciju dilucijske i difuzijske metode. Ispitivani soj inokulira se na Mueller-Hinton agar kao za disk difuzijske test, zatim se nanose E- test trake s predefiniranim gradijentom koncentracija antibiotika, koji se prenosi s trake na krutu podlogu. Nakon inkubacije od 18 h do 24 h očitava se MIK na temelju veličine inhibicijske zone (Slika 15.5). TESTOVI ZA DOKAZ PRODUKCIJE β-laktamaza PROŠIRENOG SPEKTRA (ESBL) Detekcija β-laktamaza proširenog spektra (engl. extended-spectrum β-lactamase, ESBL) uglavnom se vrši za izolate K. pnemoniae i E.coli, iako se Slika Izvođenje disk-difuzijskog testa: suspenzija testiranog soja (čija se gustoća podesi prema Mc Farlandu 0,5) nanese se pomoću brisa na površinu Mueller-Hinton agara, te nakon toga, diskovi se nanose na površinu ploče pomoću dispenzera ili pincete (Izvor: iz vlastite zbirke, B. Bedenić, 2005.) 249
30 Antibakterijski lijekovi Poglavlje 15 Slika Očitavanje disk-difuzijskog testa: ravnalom se mjeri promjer inhibicijske zone, te na temelju toga, određuje se da li je soj osjetljiv, umjereno osjetljiv ili rezistentan (testirani soj na slici je osjetljiv na ceftazidim, cefoperazon i ciprofloksacin, a rezistentan je na gentamicin) (Izvor: iz vlastite zbirke, B. Bedenić, 2005.) one ponekad mogu pojaviti i kod ostalih enterobakterija, pa čak i kod nefermentativnih bakterija. Svi fenotipski testovi za detekciju ESBL temelje se na sinergizmu između cefalosporina proširenog spektra ili aztreonama i klavulanske kiseline, te zbog toga ovi testovi ne otkrivaju AmpC β-laktamaze proširenog spektra, koje najčešće nisu inhibirane klavulanatom. Dvostruki disk-sinergistički test Test koji se najčešće provodi u rutinskim laboratorijima je dvostruki disk-sinergistički test. Testirani soj suspendiramo u fiziološkoj otopini, na jednaki način kao za izvođenje antibiograma, i sterilnim brisom ga nanesemo na površinu Mueller- Hinton agara. U sredinu se stavlja disk koji sadržava amoksicilin, kombiniran s klavulanskom kiselinom, a na udaljenost od 2 do 3 cm se stavljaju diskovi ceftazidima, cefotaksima, ceftriaskona i aztreonama. Optimalna udaljenost između cefalosporinskog i centralnog diska ovisi o soju, stupnju njegove rezistencije i količini β-laktamaze koju proizvodi. Ploče se zatim inkubiraju h na 37 ºC i zatim se očitava rezultat: ako dođe do širenja inhibicijske zone oko diska cefalosporina ili aztreonama u smjeru prema centralnom disku, onda se to smatra pozitivnim rezultatom testa (Slika 15.6). Prednost testa je u njegovom jednostavnom izvođenju, a nedostatak je subjektivnost u čitanju rezultata. Neki autori preporučuju upotrebu diska cefpodoksima umjesto gore navedenih diskova, jer on uspješno detektira ESBL iz sve tri porodice: TEM, SHV i CTX- M. Disk na disk test Soj se nanosi na Mueller-Hinton agar na jednaki način kao za dvostruki disk-sinergistički test i na povr- A B Slika Očitavanje E-testa. A) za penicilin kod S. pneumoniae: MIK penicilina je 0,25 mg/l, što znači da se radi o soju osjetljivom na penicilin; B) za vankomicin kod enterokoka: MIK je veći od 256 mg/l, što znači da se radi vankomicin-rezistentnom enterokoku (VRE) (Izvor: iz vlastite zbirke, B. Bedenić, 2005.) 250
31 B. Bedeni} šinu agara se nanose diskovi ceftazidima, cefotaksima, ceftriaksona i aztreonama. Na navedene diskove stavlja se disk ko-amoksiklava, kao izvor klavulanske kiseline. Povećanje promjera zone inhibicije za najmanje 5 mm u odnosu na kontrolnu ploču, koja sadržava samo cefalosporinske diskove bez koamoksiklava, dokaz je produkcije ESBL. Inhibitorom potencirani disk-difuzijski test Za ovaj test je potrebno pripremiti Mueller-Hinton agar s inkorporiranom klavulanskom kiselinom. Klavulansku kiselinu dodajemo u koncentraciji od 4 mg/l u podlogu, koja mora biti prethodno ohlađena na 55 ºC. Kontrolna ploča ne sadržava klavulanat. Testirani soj se inokulira na ploču s klavulanskom kiselinom i na ploču bez inkorporirane klavulanske kiseline. Na ploče se postavljaju diskovi cefalosporina (ceftazidim, cefotaksim, ceftriakson) i aztreonama, i mjere se zone inhibicije na ploči s klavulanatom, i na ploči bez klavulanata. Dokaz produkcije ESBL je povećanje zone inhibicije rasta oko cefalosporinskog diska za najmanje 10 mm na ploči s klavulanskom kiselinom u odnosu na kontrolnu ploču. Određivanje minimalnih inhibitornih koncentracija ceftazidima sa i bez klavulanske kiseline Da bi se dokazala produkcija ESBL, potrebno je odrediti MIK samog ceftazidima i MIK uz dodatak fiksne koncentracije klavulanske kiseline (4 mg/l). Pozitivan rezultat je smanjenje MIK-a ceftazidima za najmanje četiri razrijeđenja u prisustvu klavulanske kiseline. Slika Dvostruki disk-sinergistički test: soj je pozitivan na produkciju β-laktamaza proširenog spektra. Vidljivo je proširenje inhibicijske zone oko diska ceftriaksona, cefoperazona i cefotaksima prema centralnom disku koji sadrži klavulansku kiselinu (Izvor: iz vlastite zbirke, B. Bedenić, 2005.) E-test za određivanje ESBL Testirani soj suspendira se u fiziološkoj otopini, kao što je opisano za izradu antibiograma, te se nanosi sterilnim brisom na M-H agar. Na ploču se zatim postavlja E-test traka, koja s jedne strane ima gradijent koncentracija za ceftazidim, a s druge strane ceftazidim u kombinaciji s klavulanskom kiselinom. Interpretacija rezultata se vrši prema uputama proizvođača. Literatura Božinović D: Antimikrobni lijekovi. U: Kalenić S, Mlinarić- Missoni E. Medicinska bakteriologija i mikologija. Zagreb: Prehrambeno-tehnološki inženjering, 1995: Brooks GF, Butel JS, Morse SA. Jawetz, Melnick, and Adelberg s Medical Microbiology. (23. izd.) New York, Chicaco, San Francisco, London, Lisbon: Lange Medical Books/McGraw- Hill, 2004: Murray PR, Rosenthal KS, Pfaller KS. Medical microbiology. (5. izd.) Philadelphia (Pe), USA: Elsevier Mosby, 2005: Francetić I. Antibakterijski lijekovi. U: Laurence D, Bennet PN. Klinička farmakologija. Zagreb: JUMENA, 1988: Francetić I. Kemoterapija bakterijskih infekcija. U: Laurence D, Bennet PN. Klinička farmakologija. Zagreb: JUMENA, 1988: Thornsberry C. Antimicrobial susceptibility Testing: General consideration. U: Balows A, Hausler WJ, Herrmann KL, Isenberg HD, Shadomy HJ. Manual of clinical microbiology. (5. izd.) Washington D. C.: American Society for Microbiology, 1991: Yao JD, Moellering RC. Antibacterial Agents. U: Balows A, Hausler WJ, Herrmann KL, Isenberg HD, Shadomy HJ. Manual of clinical microbiology. (5. izd.) Washington D. C.: American Society for Microbiology, 1991:
3.1 Granična vrednost funkcije u tački
 3 Granična vrednost i neprekidnost funkcija 2 3 Granična vrednost i neprekidnost funkcija 3. Granična vrednost funkcije u tački Neka je funkcija f(x) definisana u tačkama x za koje je 0 < x x 0 < r, ili
3 Granična vrednost i neprekidnost funkcija 2 3 Granična vrednost i neprekidnost funkcija 3. Granična vrednost funkcije u tački Neka je funkcija f(x) definisana u tačkama x za koje je 0 < x x 0 < r, ili
UNIVERZITET U NIŠU ELEKTRONSKI FAKULTET SIGNALI I SISTEMI. Zbirka zadataka
 UNIVERZITET U NIŠU ELEKTRONSKI FAKULTET Goran Stančić SIGNALI I SISTEMI Zbirka zadataka NIŠ, 014. Sadržaj 1 Konvolucija Literatura 11 Indeks pojmova 11 3 4 Sadržaj 1 Konvolucija Zadatak 1. Odrediti konvoluciju
UNIVERZITET U NIŠU ELEKTRONSKI FAKULTET Goran Stančić SIGNALI I SISTEMI Zbirka zadataka NIŠ, 014. Sadržaj 1 Konvolucija Literatura 11 Indeks pojmova 11 3 4 Sadržaj 1 Konvolucija Zadatak 1. Odrediti konvoluciju
18. listopada listopada / 13
 18. listopada 2016. 18. listopada 2016. 1 / 13 Neprekidne funkcije Važnu klasu funkcija tvore neprekidne funkcije. To su funkcije f kod kojih mala promjena u nezavisnoj varijabli x uzrokuje malu promjenu
18. listopada 2016. 18. listopada 2016. 1 / 13 Neprekidne funkcije Važnu klasu funkcija tvore neprekidne funkcije. To su funkcije f kod kojih mala promjena u nezavisnoj varijabli x uzrokuje malu promjenu
numeričkih deskriptivnih mera.
 DESKRIPTIVNA STATISTIKA Numeričku seriju podataka opisujemo pomoću Numeričku seriju podataka opisujemo pomoću numeričkih deskriptivnih mera. Pokazatelji centralne tendencije Aritmetička sredina, Medijana,
DESKRIPTIVNA STATISTIKA Numeričku seriju podataka opisujemo pomoću Numeričku seriju podataka opisujemo pomoću numeričkih deskriptivnih mera. Pokazatelji centralne tendencije Aritmetička sredina, Medijana,
Trigonometrija 2. Adicijske formule. Formule dvostrukog kuta Formule polovičnog kuta Pretvaranje sume(razlike u produkt i obrnuto
 Trigonometrija Adicijske formule Formule dvostrukog kuta Formule polovičnog kuta Pretvaranje sume(razlike u produkt i obrnuto Razumijevanje postupka izrade složenijeg matematičkog problema iz osnova trigonometrije
Trigonometrija Adicijske formule Formule dvostrukog kuta Formule polovičnog kuta Pretvaranje sume(razlike u produkt i obrnuto Razumijevanje postupka izrade složenijeg matematičkog problema iz osnova trigonometrije
Osnovni primer. (Z, +,,, 0, 1) je komutativan prsten sa jedinicom: množenje je distributivno prema sabiranju
 RAČUN OSTATAKA 1 1 Prsten celih brojeva Z := N + {} N + = {, 3, 2, 1,, 1, 2, 3,...} Osnovni primer. (Z, +,,,, 1) je komutativan prsten sa jedinicom: sabiranje (S1) asocijativnost x + (y + z) = (x + y)
RAČUN OSTATAKA 1 1 Prsten celih brojeva Z := N + {} N + = {, 3, 2, 1,, 1, 2, 3,...} Osnovni primer. (Z, +,,,, 1) je komutativan prsten sa jedinicom: sabiranje (S1) asocijativnost x + (y + z) = (x + y)
2 tg x ctg x 1 = =, cos 2x Zbog četvrtog kvadranta rješenje je: 2 ctg x
 Zadatak (Darjan, medicinska škola) Izračunaj vrijednosti trigonometrijskih funkcija broja ako je 6 sin =,,. 6 Rješenje Ponovimo trigonometrijske funkcije dvostrukog kuta! Za argument vrijede sljedeće formule:
Zadatak (Darjan, medicinska škola) Izračunaj vrijednosti trigonometrijskih funkcija broja ako je 6 sin =,,. 6 Rješenje Ponovimo trigonometrijske funkcije dvostrukog kuta! Za argument vrijede sljedeće formule:
SEMINAR IZ KOLEGIJA ANALITIČKA KEMIJA I. Studij Primijenjena kemija
 SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
beta-laktamski antibiotici (i) Penicilini
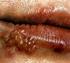 1 e-nastavni članak beta-laktamski antibiotici (i) Penicilini MEHANIZAM DJELOVANJA Beta-laktamski antibiotici djeluju baktericidno, a načelno se smatra da je osnovni mehanizam njihovog baktericidnog učinka
1 e-nastavni članak beta-laktamski antibiotici (i) Penicilini MEHANIZAM DJELOVANJA Beta-laktamski antibiotici djeluju baktericidno, a načelno se smatra da je osnovni mehanizam njihovog baktericidnog učinka
ELEKTROTEHNIČKI ODJEL
 MATEMATIKA. Neka je S skup svih živućih državljana Republike Hrvatske..04., a f preslikavanje koje svakom elementu skupa S pridružuje njegov horoskopski znak (bez podznaka). a) Pokažite da je f funkcija,
MATEMATIKA. Neka je S skup svih živućih državljana Republike Hrvatske..04., a f preslikavanje koje svakom elementu skupa S pridružuje njegov horoskopski znak (bez podznaka). a) Pokažite da je f funkcija,
Kaskadna kompenzacija SAU
 Kaskadna kompenzacija SAU U inženjerskoj praksi, naročito u sistemima regulacije elektromotornih pogona i tehnoloških procesa, veoma često se primenjuje metoda kaskadne kompenzacije, u čijoj osnovi su
Kaskadna kompenzacija SAU U inženjerskoj praksi, naročito u sistemima regulacije elektromotornih pogona i tehnoloških procesa, veoma često se primenjuje metoda kaskadne kompenzacije, u čijoj osnovi su
Teorijske osnove informatike 1
 Teorijske osnove informatike 1 9. oktobar 2014. () Teorijske osnove informatike 1 9. oktobar 2014. 1 / 17 Funkcije Veze me du skupovima uspostavljamo skupovima koje nazivamo funkcijama. Neformalno, funkcija
Teorijske osnove informatike 1 9. oktobar 2014. () Teorijske osnove informatike 1 9. oktobar 2014. 1 / 17 Funkcije Veze me du skupovima uspostavljamo skupovima koje nazivamo funkcijama. Neformalno, funkcija
M086 LA 1 M106 GRP. Tema: Baza vektorskog prostora. Koordinatni sustav. Norma. CSB nejednakost
 M086 LA 1 M106 GRP Tema: CSB nejednakost. 19. 10. 2017. predavač: Rudolf Scitovski, Darija Marković asistent: Darija Brajković, Katarina Vincetić P 1 www.fizika.unios.hr/grpua/ 1 Baza vektorskog prostora.
M086 LA 1 M106 GRP Tema: CSB nejednakost. 19. 10. 2017. predavač: Rudolf Scitovski, Darija Marković asistent: Darija Brajković, Katarina Vincetić P 1 www.fizika.unios.hr/grpua/ 1 Baza vektorskog prostora.
SEKUNDARNE VEZE međumolekulske veze
 PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
Eliminacijski zadatak iz Matematike 1 za kemičare
 Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Matematička analiza 1 dodatni zadaci
 Matematička analiza 1 dodatni zadaci 1. Ispitajte je li funkcija f() := 4 4 5 injekcija na intervalu I, te ako jest odredite joj sliku i inverz, ako je (a) I = [, 3), (b) I = [1, ], (c) I = ( 1, 0].. Neka
Matematička analiza 1 dodatni zadaci 1. Ispitajte je li funkcija f() := 4 4 5 injekcija na intervalu I, te ako jest odredite joj sliku i inverz, ako je (a) I = [, 3), (b) I = [1, ], (c) I = ( 1, 0].. Neka
IZRADA ANTIBIOGRAMA. 1. Reagensi za disk-difuzioni test
 PREPORUKE ZA ISPITIVANJE OSETLJIVOSTI BAKTERIJA NA ANTIMIKROBNE LEKOVE PREMA CLSI 2009 Novi Sad, 2009 IZRADA ANTIBIOGRAMA 1. Reagensi za disk-difuzioni test 1. Podloga - preporučuje se upotreba Mueller
PREPORUKE ZA ISPITIVANJE OSETLJIVOSTI BAKTERIJA NA ANTIMIKROBNE LEKOVE PREMA CLSI 2009 Novi Sad, 2009 IZRADA ANTIBIOGRAMA 1. Reagensi za disk-difuzioni test 1. Podloga - preporučuje se upotreba Mueller
PRAVA. Prava je u prostoru određena jednom svojom tačkom i vektorom paralelnim sa tom pravom ( vektor paralelnosti).
 PRAVA Prava je kao i ravan osnovni geometrijski ojam i ne definiše se. Prava je u rostoru određena jednom svojom tačkom i vektorom aralelnim sa tom ravom ( vektor aralelnosti). M ( x, y, z ) 3 Posmatrajmo
PRAVA Prava je kao i ravan osnovni geometrijski ojam i ne definiše se. Prava je u rostoru određena jednom svojom tačkom i vektorom aralelnim sa tom ravom ( vektor aralelnosti). M ( x, y, z ) 3 Posmatrajmo
ODPORNOST BAKTERIJ PROTI ANTIBIOTIKOM V SLOVENIJI IN PO SVETU
 ODPORNOST BAKTERIJ PROTI ANTIBIOTIKOM V SLOVENIJI IN PO SVETU Manica Müller Premru, dr. med., spec. klin. mikrobiol. Inštitut za mikrobiologijo in imunologijo Medicinska fakulteta Univerza v Ljubljani
ODPORNOST BAKTERIJ PROTI ANTIBIOTIKOM V SLOVENIJI IN PO SVETU Manica Müller Premru, dr. med., spec. klin. mikrobiol. Inštitut za mikrobiologijo in imunologijo Medicinska fakulteta Univerza v Ljubljani
a M a A. Može se pokazati da je supremum (ako postoji) jedinstven pa uvodimo oznaku sup A.
 3 Infimum i supremum Definicija. Neka je A R. Kažemo da je M R supremum skupa A ako je (i) M gornja meda skupa A, tj. a M a A. (ii) M najmanja gornja meda skupa A, tj. ( ε > 0)( a A) takav da je a > M
3 Infimum i supremum Definicija. Neka je A R. Kažemo da je M R supremum skupa A ako je (i) M gornja meda skupa A, tj. a M a A. (ii) M najmanja gornja meda skupa A, tj. ( ε > 0)( a A) takav da je a > M
konst. Električni otpor
 Sveučilište J. J. Strossmayera u sijeku Elektrotehnički fakultet sijek Stručni studij Električni otpor hmov zakon Pri protjecanju struje kroz vodič pojavljuje se otpor. Georg Simon hm je ustanovio ovisnost
Sveučilište J. J. Strossmayera u sijeku Elektrotehnički fakultet sijek Stručni studij Električni otpor hmov zakon Pri protjecanju struje kroz vodič pojavljuje se otpor. Georg Simon hm je ustanovio ovisnost
DISKRETNA MATEMATIKA - PREDAVANJE 7 - Jovanka Pantović
 DISKRETNA MATEMATIKA - PREDAVANJE 7 - Jovanka Pantović Novi Sad April 17, 2018 1 / 22 Teorija grafova April 17, 2018 2 / 22 Definicija Graf je ure dena trojka G = (V, G, ψ), gde je (i) V konačan skup čvorova,
DISKRETNA MATEMATIKA - PREDAVANJE 7 - Jovanka Pantović Novi Sad April 17, 2018 1 / 22 Teorija grafova April 17, 2018 2 / 22 Definicija Graf je ure dena trojka G = (V, G, ψ), gde je (i) V konačan skup čvorova,
Iskazna logika 3. Matematička logika u računarstvu. novembar 2012
 Iskazna logika 3 Matematička logika u računarstvu Department of Mathematics and Informatics, Faculty of Science,, Serbia novembar 2012 Deduktivni sistemi 1 Definicija Deduktivni sistem (ili formalna teorija)
Iskazna logika 3 Matematička logika u računarstvu Department of Mathematics and Informatics, Faculty of Science,, Serbia novembar 2012 Deduktivni sistemi 1 Definicija Deduktivni sistem (ili formalna teorija)
Zavod za javno zdravlje Leskovac Leskovac, Maksima Kovačevića 11 Tel.: 016/ ; ; Faks: 016/
 Strana: 1 od 6 Strana: 2 od 6 Mehanizmi rezistencije bakterija Bakterijske infekcije spadaju u retka oboljenja gde postoji mogućnost odgovarajuće etiološke terapije antibioticima.terapija infekcija antibioticima
Strana: 1 od 6 Strana: 2 od 6 Mehanizmi rezistencije bakterija Bakterijske infekcije spadaju u retka oboljenja gde postoji mogućnost odgovarajuće etiološke terapije antibioticima.terapija infekcija antibioticima
Bakteriološka dijagnostika infekcija i oboljenja izazvanih. Streptococcus i Enterococcus
 Bakteriološka dijagnostika infekcija i oboljenja izazvanih bakterijama rodova Streptococcus i Enterococcus Rod Streptococcus Gram pozitivne koke raspoređene u lancima nepokretne asporogene nutritivni izbirači
Bakteriološka dijagnostika infekcija i oboljenja izazvanih bakterijama rodova Streptococcus i Enterococcus Rod Streptococcus Gram pozitivne koke raspoređene u lancima nepokretne asporogene nutritivni izbirači
INTEGRALNI RAČUN. Teorije, metodike i povijest infinitezimalnih računa. Lucija Mijić 17. veljače 2011.
 INTEGRALNI RAČUN Teorije, metodike i povijest infinitezimalnih računa Lucija Mijić lucija@ktf-split.hr 17. veljače 2011. Pogledajmo Predstavimo gornju sumu sa Dodamo još jedan Dobivamo pravokutnik sa Odnosno
INTEGRALNI RAČUN Teorije, metodike i povijest infinitezimalnih računa Lucija Mijić lucija@ktf-split.hr 17. veljače 2011. Pogledajmo Predstavimo gornju sumu sa Dodamo još jedan Dobivamo pravokutnik sa Odnosno
RIJEŠENI ZADACI I TEORIJA IZ
 RIJEŠENI ZADACI I TEORIJA IZ LOGARITAMSKA FUNKCIJA SVOJSTVA LOGARITAMSKE FUNKCIJE OSNOVE TRIGONOMETRIJE PRAVOKUTNOG TROKUTA - DEFINICIJA TRIGONOMETRIJSKIH FUNKCIJA - VRIJEDNOSTI TRIGONOMETRIJSKIH FUNKCIJA
RIJEŠENI ZADACI I TEORIJA IZ LOGARITAMSKA FUNKCIJA SVOJSTVA LOGARITAMSKE FUNKCIJE OSNOVE TRIGONOMETRIJE PRAVOKUTNOG TROKUTA - DEFINICIJA TRIGONOMETRIJSKIH FUNKCIJA - VRIJEDNOSTI TRIGONOMETRIJSKIH FUNKCIJA
Kontrolni zadatak (Tačka, prava, ravan, diedar, poliedar, ortogonalna projekcija), grupa A
 Kontrolni zadatak (Tačka, prava, ravan, diedar, poliedar, ortogonalna projekcija), grupa A Ime i prezime: 1. Prikazane su tačke A, B i C i prave a,b i c. Upiši simbole Î, Ï, Ì ili Ë tako da dobijeni iskazi
Kontrolni zadatak (Tačka, prava, ravan, diedar, poliedar, ortogonalna projekcija), grupa A Ime i prezime: 1. Prikazane su tačke A, B i C i prave a,b i c. Upiši simbole Î, Ï, Ì ili Ë tako da dobijeni iskazi
Cefalosporini ostali β-laktami
 Cefalosporini ostali β-laktami doc.dr. Marko Anderluh 12. januar 2012 Vir cefalosporinov Cephalosporium acremonium Cefalosporin C Enaka tarča kot pri penicilinih Podoben mehanizem delovanja Cefalosporini
Cefalosporini ostali β-laktami doc.dr. Marko Anderluh 12. januar 2012 Vir cefalosporinov Cephalosporium acremonium Cefalosporin C Enaka tarča kot pri penicilinih Podoben mehanizem delovanja Cefalosporini
Apsolutno neprekidne raspodele Raspodele apsolutno neprekidnih sluqajnih promenljivih nazivaju se apsolutno neprekidnim raspodelama.
 Apsolutno neprekidne raspodele Raspodele apsolutno neprekidnih sluqajnih promenljivih nazivaju se apsolutno neprekidnim raspodelama. a b Verovatno a da sluqajna promenljiva X uzima vrednost iz intervala
Apsolutno neprekidne raspodele Raspodele apsolutno neprekidnih sluqajnih promenljivih nazivaju se apsolutno neprekidnim raspodelama. a b Verovatno a da sluqajna promenljiva X uzima vrednost iz intervala
1 Promjena baze vektora
 Promjena baze vektora Neka su dane dvije različite uredene baze u R n, označimo ih s A = (a, a,, a n i B = (b, b,, b n Svaki vektor v R n ima medusobno različite koordinatne zapise u bazama A i B Zapis
Promjena baze vektora Neka su dane dvije različite uredene baze u R n, označimo ih s A = (a, a,, a n i B = (b, b,, b n Svaki vektor v R n ima medusobno različite koordinatne zapise u bazama A i B Zapis
Linearna algebra 2 prvi kolokvij,
 1 2 3 4 5 Σ jmbag smjer studija Linearna algebra 2 prvi kolokvij, 7. 11. 2012. 1. (10 bodova) Neka je dano preslikavanje s : R 2 R 2 R, s (x, y) = (Ax y), pri čemu je A: R 2 R 2 linearan operator oblika
1 2 3 4 5 Σ jmbag smjer studija Linearna algebra 2 prvi kolokvij, 7. 11. 2012. 1. (10 bodova) Neka je dano preslikavanje s : R 2 R 2 R, s (x, y) = (Ax y), pri čemu je A: R 2 R 2 linearan operator oblika
Operacije s matricama
 Linearna algebra I Operacije s matricama Korolar 3.1.5. Množenje matrica u vektorskom prostoru M n (F) ima sljedeća svojstva: (1) A(B + C) = AB + AC, A, B, C M n (F); (2) (A + B)C = AC + BC, A, B, C M
Linearna algebra I Operacije s matricama Korolar 3.1.5. Množenje matrica u vektorskom prostoru M n (F) ima sljedeća svojstva: (1) A(B + C) = AB + AC, A, B, C M n (F); (2) (A + B)C = AC + BC, A, B, C M
NOMENKLATURA ORGANSKIH SPOJEVA. Imenovanje aromatskih ugljikovodika
 NOMENKLATURA ORGANSKIH SPOJEVA Imenovanje aromatskih ugljikovodika benzen metilbenzen (toluen) 1,2-dimetilbenzen (o-ksilen) 1,3-dimetilbenzen (m-ksilen) 1,4-dimetilbenzen (p-ksilen) fenilna grupa 2-fenilheptan
NOMENKLATURA ORGANSKIH SPOJEVA Imenovanje aromatskih ugljikovodika benzen metilbenzen (toluen) 1,2-dimetilbenzen (o-ksilen) 1,3-dimetilbenzen (m-ksilen) 1,4-dimetilbenzen (p-ksilen) fenilna grupa 2-fenilheptan
radni nerecenzirani materijal za predavanja
 Matematika 1 Funkcije radni nerecenzirani materijal za predavanja Definicija 1. Kažemo da je funkcija f : a, b R u točki x 0 a, b postiže lokalni minimum ako postoji okolina O(x 0 ) broja x 0 takva da je
Matematika 1 Funkcije radni nerecenzirani materijal za predavanja Definicija 1. Kažemo da je funkcija f : a, b R u točki x 0 a, b postiže lokalni minimum ako postoji okolina O(x 0 ) broja x 0 takva da je
PT ISPITIVANJE PENETRANTIMA
 FSB Sveučilišta u Zagrebu Zavod za kvalitetu Katedra za nerazorna ispitivanja PT ISPITIVANJE PENETRANTIMA Josip Stepanić SADRŽAJ kapilarni učinak metoda ispitivanja penetrantima uvjeti promatranja SADRŽAJ
FSB Sveučilišta u Zagrebu Zavod za kvalitetu Katedra za nerazorna ispitivanja PT ISPITIVANJE PENETRANTIMA Josip Stepanić SADRŽAJ kapilarni učinak metoda ispitivanja penetrantima uvjeti promatranja SADRŽAJ
21. ŠKOLSKO/OPĆINSKO/GRADSKO NATJECANJE IZ GEOGRAFIJE GODINE 8. RAZRED TOČNI ODGOVORI
 21. ŠKOLSKO/OPĆINSKO/GRADSKO NATJECANJE IZ GEOGRAFIJE 2014. GODINE 8. RAZRED TOČNI ODGOVORI Bodovanje za sve zadatke: - boduju se samo točni odgovori - dodatne upute navedene su za pojedine skupine zadataka
21. ŠKOLSKO/OPĆINSKO/GRADSKO NATJECANJE IZ GEOGRAFIJE 2014. GODINE 8. RAZRED TOČNI ODGOVORI Bodovanje za sve zadatke: - boduju se samo točni odgovori - dodatne upute navedene su za pojedine skupine zadataka
Imunofluorescencija. vizualizacija molekula protutijela obilježenih fluorokromom vezanih za antigene na stanicama ili tkivnim preparatima
 Imunofluorescencija 1944. - Robert Coons protutijela se mogu označiti molekulama koje imaju sposobnost fluorescencije fluorokromi - apsorbiraju svjetlost jedna valne duljine (ekscitacija), a emitiraju
Imunofluorescencija 1944. - Robert Coons protutijela se mogu označiti molekulama koje imaju sposobnost fluorescencije fluorokromi - apsorbiraju svjetlost jedna valne duljine (ekscitacija), a emitiraju
radni nerecenzirani materijal za predavanja R(f) = {f(x) x D}
 Matematika 1 Funkcije radni nerecenzirani materijal za predavanja Definicija 1. Neka su D i K bilo koja dva neprazna skupa. Postupak f koji svakom elementu x D pridružuje točno jedan element y K zovemo funkcija
Matematika 1 Funkcije radni nerecenzirani materijal za predavanja Definicija 1. Neka su D i K bilo koja dva neprazna skupa. Postupak f koji svakom elementu x D pridružuje točno jedan element y K zovemo funkcija
Strukture podataka i algoritmi 1. kolokvij 16. studenog Zadatak 1
 Strukture podataka i algoritmi 1. kolokvij Na kolokviju je dozvoljeno koristiti samo pribor za pisanje i službeni šalabahter. Predajete samo papire koje ste dobili. Rezultati i uvid u kolokvije: ponedjeljak,
Strukture podataka i algoritmi 1. kolokvij Na kolokviju je dozvoljeno koristiti samo pribor za pisanje i službeni šalabahter. Predajete samo papire koje ste dobili. Rezultati i uvid u kolokvije: ponedjeljak,
SAŽETAK OPISA SVOJSTAVA LIJEKA
 SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Klavocin bid 1 g tablete 2. KVALITATIVNI I KVANTITATIVNI SASTAV Jedna filmom obložena tableta sadrži 875 mg amoksicilina u obliku amoksicilin trihidrata
SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Klavocin bid 1 g tablete 2. KVALITATIVNI I KVANTITATIVNI SASTAV Jedna filmom obložena tableta sadrži 875 mg amoksicilina u obliku amoksicilin trihidrata
Pismeni ispit iz matematike Riješiti sistem jednačina i diskutovati rješenja sistema u zavisnosti od parametra: ( ) + 1.
 Pismeni ispit iz matematike 0 008 GRUPA A Riješiti sistem jednačina i diskutovati rješenja sistema u zavisnosti od parametra: λ + z = Ispitati funkciju i nacrtati njen grafik: + ( λ ) + z = e Izračunati
Pismeni ispit iz matematike 0 008 GRUPA A Riješiti sistem jednačina i diskutovati rješenja sistema u zavisnosti od parametra: λ + z = Ispitati funkciju i nacrtati njen grafik: + ( λ ) + z = e Izračunati
Dijagonalizacija operatora
 Dijagonalizacija operatora Problem: Može li se odrediti baza u kojoj zadani operator ima dijagonalnu matricu? Ova problem je povezan sa sljedećim pojmovima: 1 Karakteristični polinom operatora f 2 Vlastite
Dijagonalizacija operatora Problem: Može li se odrediti baza u kojoj zadani operator ima dijagonalnu matricu? Ova problem je povezan sa sljedećim pojmovima: 1 Karakteristični polinom operatora f 2 Vlastite
7 Algebarske jednadžbe
 7 Algebarske jednadžbe 7.1 Nultočke polinoma Skup svih polinoma nad skupom kompleksnih brojeva označavamo sa C[x]. Definicija. Nultočka polinoma f C[x] je svaki kompleksni broj α takav da je f(α) = 0.
7 Algebarske jednadžbe 7.1 Nultočke polinoma Skup svih polinoma nad skupom kompleksnih brojeva označavamo sa C[x]. Definicija. Nultočka polinoma f C[x] je svaki kompleksni broj α takav da je f(α) = 0.
PARCIJALNI IZVODI I DIFERENCIJALI. Sama definicija parcijalnog izvoda i diferencijala je malo teža, mi se njome ovde nećemo baviti a vi ćete je,
 PARCIJALNI IZVODI I DIFERENCIJALI Sama definicija parcijalnog ivoda i diferencijala je malo teža, mi se njome ovde nećemo baviti a vi ćete je, naravno, naučiti onako kako vaš profesor ahteva. Mi ćemo probati
PARCIJALNI IZVODI I DIFERENCIJALI Sama definicija parcijalnog ivoda i diferencijala je malo teža, mi se njome ovde nećemo baviti a vi ćete je, naravno, naučiti onako kako vaš profesor ahteva. Mi ćemo probati
Riješeni zadaci: Nizovi realnih brojeva
 Riješei zadaci: Nizovi realih brojeva Nizovi, aritmetički iz, geometrijski iz Fukciju a : N R azivamo beskoači) iz realih brojeva i ozačavamo s a 1, a,..., a,... ili a ), pri čemu je a = a). Aritmetički
Riješei zadaci: Nizovi realih brojeva Nizovi, aritmetički iz, geometrijski iz Fukciju a : N R azivamo beskoači) iz realih brojeva i ozačavamo s a 1, a,..., a,... ili a ), pri čemu je a = a). Aritmetički
IZVODI ZADACI (I deo)
 IZVODI ZADACI (I deo) Najpre da se podsetimo tablice i osnovnih pravila:. C`=0. `=. ( )`= 4. ( n )`=n n-. (a )`=a lna 6. (e )`=e 7. (log a )`= 8. (ln)`= ` ln a (>0) 9. = ( 0) 0. `= (>0) (ovde je >0 i a
IZVODI ZADACI (I deo) Najpre da se podsetimo tablice i osnovnih pravila:. C`=0. `=. ( )`= 4. ( n )`=n n-. (a )`=a lna 6. (e )`=e 7. (log a )`= 8. (ln)`= ` ln a (>0) 9. = ( 0) 0. `= (>0) (ovde je >0 i a
Linearna algebra 2 prvi kolokvij,
 Linearna algebra 2 prvi kolokvij, 27.. 20.. Za koji cijeli broj t je funkcija f : R 4 R 4 R definirana s f(x, y) = x y (t + )x 2 y 2 + x y (t 2 + t)x 4 y 4, x = (x, x 2, x, x 4 ), y = (y, y 2, y, y 4 )
Linearna algebra 2 prvi kolokvij, 27.. 20.. Za koji cijeli broj t je funkcija f : R 4 R 4 R definirana s f(x, y) = x y (t + )x 2 y 2 + x y (t 2 + t)x 4 y 4, x = (x, x 2, x, x 4 ), y = (y, y 2, y, y 4 )
SAŽETAK OPISA SVOJSTAVA LIJEKA. Piperacillin/Tazobactam Aurobindo 4 g/0,5 g prašak za otopinu za infuziju
 SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Piperacillin/Tazobactam Aurobindo 4 g/0,5 g prašak za otopinu za infuziju 2. KVALITATIVNI I KVANTITATIVNI SASTAV 1 bočica sadrži piperacilin (u obliku
SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Piperacillin/Tazobactam Aurobindo 4 g/0,5 g prašak za otopinu za infuziju 2. KVALITATIVNI I KVANTITATIVNI SASTAV 1 bočica sadrži piperacilin (u obliku
IZVODI ZADACI ( IV deo) Rešenje: Najpre ćemo logaritmovati ovu jednakost sa ln ( to beše prirodni logaritam za osnovu e) a zatim ćemo
 IZVODI ZADACI ( IV deo) LOGARITAMSKI IZVOD Logariamskim izvodom funkcije f(), gde je >0 i, nazivamo izvod logarima e funkcije, o jes: (ln ) f ( ) f ( ) Primer. Nadji izvod funkcije Najpre ćemo logarimovai
IZVODI ZADACI ( IV deo) LOGARITAMSKI IZVOD Logariamskim izvodom funkcije f(), gde je >0 i, nazivamo izvod logarima e funkcije, o jes: (ln ) f ( ) f ( ) Primer. Nadji izvod funkcije Najpre ćemo logarimovai
Zavrxni ispit iz Matematiqke analize 1
 Građevinski fakultet Univerziteta u Beogradu 3.2.2016. Zavrxni ispit iz Matematiqke analize 1 Prezime i ime: Broj indeksa: 1. Definisati Koxijev niz. Dati primer niza koji nije Koxijev. 2. Dat je red n=1
Građevinski fakultet Univerziteta u Beogradu 3.2.2016. Zavrxni ispit iz Matematiqke analize 1 Prezime i ime: Broj indeksa: 1. Definisati Koxijev niz. Dati primer niza koji nije Koxijev. 2. Dat je red n=1
TRIGONOMETRIJSKE FUNKCIJE I I.1.
 TRIGONOMETRIJSKE FUNKCIJE I I Odredi na brojevnoj trigonometrijskoj kružnici točku Et, za koju je sin t =,cost < 0 Za koje realne brojeve a postoji realan broj takav da je sin = a? Izračunaj: sin π tg
TRIGONOMETRIJSKE FUNKCIJE I I Odredi na brojevnoj trigonometrijskoj kružnici točku Et, za koju je sin t =,cost < 0 Za koje realne brojeve a postoji realan broj takav da je sin = a? Izračunaj: sin π tg
FTN Novi Sad Katedra za motore i vozila. Teorija kretanja drumskih vozila Vučno-dinamičke performanse vozila: MAKSIMALNA BRZINA
 : MAKSIMALNA BRZINA Maksimalna brzina kretanja F O (N) F OI i m =i I i m =i II F Oid Princip određivanja v MAX : Drugi Njutnov zakon Dokle god je: F O > ΣF otp vozilo ubrzava Kada postane: F O = ΣF otp
: MAKSIMALNA BRZINA Maksimalna brzina kretanja F O (N) F OI i m =i I i m =i II F Oid Princip određivanja v MAX : Drugi Njutnov zakon Dokle god je: F O > ΣF otp vozilo ubrzava Kada postane: F O = ΣF otp
POTPUNO RIJEŠENIH ZADATAKA PRIRUČNIK ZA SAMOSTALNO UČENJE
 **** MLADEN SRAGA **** 011. UNIVERZALNA ZBIRKA POTPUNO RIJEŠENIH ZADATAKA PRIRUČNIK ZA SAMOSTALNO UČENJE SKUP REALNIH BROJEVA α Autor: MLADEN SRAGA Grafički urednik: BESPLATNA - WEB-VARIJANTA Tisak: M.I.M.-SRAGA
**** MLADEN SRAGA **** 011. UNIVERZALNA ZBIRKA POTPUNO RIJEŠENIH ZADATAKA PRIRUČNIK ZA SAMOSTALNO UČENJE SKUP REALNIH BROJEVA α Autor: MLADEN SRAGA Grafički urednik: BESPLATNA - WEB-VARIJANTA Tisak: M.I.M.-SRAGA
SISTEMI NELINEARNIH JEDNAČINA
 SISTEMI NELINEARNIH JEDNAČINA April, 2013 Razni zapisi sistema Skalarni oblik: Vektorski oblik: F = f 1 f n f 1 (x 1,, x n ) = 0 f n (x 1,, x n ) = 0, x = (1) F(x) = 0, (2) x 1 0, 0 = x n 0 Definicije
SISTEMI NELINEARNIH JEDNAČINA April, 2013 Razni zapisi sistema Skalarni oblik: Vektorski oblik: F = f 1 f n f 1 (x 1,, x n ) = 0 f n (x 1,, x n ) = 0, x = (1) F(x) = 0, (2) x 1 0, 0 = x n 0 Definicije
Grafičko prikazivanje atributivnih i geografskih nizova
 Grafičko prikazivanje atributivnih i geografskih nizova Biserka Draščić Ban Pomorski fakultet u Rijeci 17. veljače 2011. Grafičko prikazivanje atributivnih nizova Atributivni nizovi prikazuju se grafički
Grafičko prikazivanje atributivnih i geografskih nizova Biserka Draščić Ban Pomorski fakultet u Rijeci 17. veljače 2011. Grafičko prikazivanje atributivnih nizova Atributivni nizovi prikazuju se grafički
PARNA POSTROJENJA ZA KOMBINIRANU PROIZVODNJU ELEKTRIČNE I TOPLINSKE ENERGIJE (ENERGANE)
 (Enegane) List: PARNA POSTROJENJA ZA KOMBINIRANU PROIZVODNJU ELEKTRIČNE I TOPLINSKE ENERGIJE (ENERGANE) Na mjestima gdje se istovremeno troši električna i toplinska energija, ekonomičan način opskrbe energijom
(Enegane) List: PARNA POSTROJENJA ZA KOMBINIRANU PROIZVODNJU ELEKTRIČNE I TOPLINSKE ENERGIJE (ENERGANE) Na mjestima gdje se istovremeno troši električna i toplinska energija, ekonomičan način opskrbe energijom
Računarska grafika. Rasterizacija linije
 Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
III VEŽBA: FURIJEOVI REDOVI
 III VEŽBA: URIJEOVI REDOVI 3.1. eorijska osnova Posmatrajmo neki vremenski kontinualan signal x(t) na intervalu definisati: t + t t. ada se može X [ k ] = 1 t + t x ( t ) e j 2 π kf t dt, gde je f = 1/.
III VEŽBA: URIJEOVI REDOVI 3.1. eorijska osnova Posmatrajmo neki vremenski kontinualan signal x(t) na intervalu definisati: t + t t. ada se može X [ k ] = 1 t + t x ( t ) e j 2 π kf t dt, gde je f = 1/.
ISPITIVANJE OSETLJIVOSTI BAKTERIJA NA ANTIBIOTIKE I
 ISPITIVANJE OSETLJIVOSTI BAKTERIJA NA ANTIBIOTIKE I HEMIOTERAPEUTIKE Šta je antibiogram? Postupak za ispitivanje osetljivosti bakterija na antibiotike i hemioterapeutike Metode antibiograma Fenotipske
ISPITIVANJE OSETLJIVOSTI BAKTERIJA NA ANTIBIOTIKE I HEMIOTERAPEUTIKE Šta je antibiogram? Postupak za ispitivanje osetljivosti bakterija na antibiotike i hemioterapeutike Metode antibiograma Fenotipske
Sume kvadrata. mn = (ax + by) 2 + (ay bx) 2.
 Sume kvadrata Koji se prirodni brojevi mogu prikazati kao zbroj kvadrata dva cijela broja? Propozicija 1. Ako su brojevi m i n sume dva kvadrata, onda je i njihov produkt m n takoder suma dva kvadrata.
Sume kvadrata Koji se prirodni brojevi mogu prikazati kao zbroj kvadrata dva cijela broja? Propozicija 1. Ako su brojevi m i n sume dva kvadrata, onda je i njihov produkt m n takoder suma dva kvadrata.
Sortiranje prebrajanjem (Counting sort) i Radix Sort
 Sortiranje prebrajanjem (Counting sort) i Radix Sort 15. siječnja 2016. Ante Mijoč Uvod Teorem Ako je f(n) broj usporedbi u algoritmu za sortiranje temeljenom na usporedbama (eng. comparison-based sorting
Sortiranje prebrajanjem (Counting sort) i Radix Sort 15. siječnja 2016. Ante Mijoč Uvod Teorem Ako je f(n) broj usporedbi u algoritmu za sortiranje temeljenom na usporedbama (eng. comparison-based sorting
SAŽETAK OPISA SVOJSTAVA LIJEKA
 SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Trefpod 100 mg filmom obložene tablete Trefpod 200 mg filmom obložene tablete 2. KVALITATIVNI I KVANTITATIVNI SASTAV 100 mg: Jedna filmom obložena
SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Trefpod 100 mg filmom obložene tablete Trefpod 200 mg filmom obložene tablete 2. KVALITATIVNI I KVANTITATIVNI SASTAV 100 mg: Jedna filmom obložena
(P.I.) PRETPOSTAVKA INDUKCIJE - pretpostavimo da tvrdnja vrijedi za n = k.
 1 3 Skupovi brojeva 3.1 Skup prirodnih brojeva - N N = {1, 2, 3,...} Aksiom matematičke indukcije Neka je N skup prirodnih brojeva i M podskup od N. Ako za M vrijede svojstva: 1) 1 M 2) n M (n + 1) M,
1 3 Skupovi brojeva 3.1 Skup prirodnih brojeva - N N = {1, 2, 3,...} Aksiom matematičke indukcije Neka je N skup prirodnih brojeva i M podskup od N. Ako za M vrijede svojstva: 1) 1 M 2) n M (n + 1) M,
5. Karakteristične funkcije
 5. Karakteristične funkcije Profesor Milan Merkle emerkle@etf.rs milanmerkle.etf.rs Verovatnoća i Statistika-proleće 2018 Milan Merkle Karakteristične funkcije ETF Beograd 1 / 10 Definicija Karakteristična
5. Karakteristične funkcije Profesor Milan Merkle emerkle@etf.rs milanmerkle.etf.rs Verovatnoća i Statistika-proleće 2018 Milan Merkle Karakteristične funkcije ETF Beograd 1 / 10 Definicija Karakteristična
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu
 Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Trigonometrijske jednačine i nejednačine. Zadaci koji se rade bez upotrebe trigonometrijskih formula. 00. FF cos x sin x
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Trigonometrijske jednačine i nejednačine. Zadaci koji se rade bez upotrebe trigonometrijskih formula. 00. FF cos x sin x
Periodičke izmjenične veličine
 EHNČK FAKULE SVEUČLŠA U RJEC Zavod za elekroenergeiku Sudij: Preddiploski sručni sudij elekroehnike Kolegij: Osnove elekroehnike Nosielj kolegija: Branka Dobraš Periodičke izjenične veličine Osnove elekroehnike
EHNČK FAKULE SVEUČLŠA U RJEC Zavod za elekroenergeiku Sudij: Preddiploski sručni sudij elekroehnike Kolegij: Osnove elekroehnike Nosielj kolegija: Branka Dobraš Periodičke izjenične veličine Osnove elekroehnike
41. Jednačine koje se svode na kvadratne
 . Jednačine koje se svode na kvadrane Simerične recipročne) jednačine Jednačine oblika a n b n c n... c b a nazivamo simerične jednačine, zbog simeričnosi koeficijenaa koeficijeni uz jednaki). k i n k
. Jednačine koje se svode na kvadrane Simerične recipročne) jednačine Jednačine oblika a n b n c n... c b a nazivamo simerične jednačine, zbog simeričnosi koeficijenaa koeficijeni uz jednaki). k i n k
Verovatnoća i Statistika I deo Teorija verovatnoće (zadaci) Beleške dr Bobana Marinkovića
 Verovatnoća i Statistika I deo Teorija verovatnoće zadaci Beleške dr Bobana Marinkovića Iz skupa, 2,, 00} bira se na slučajan način 5 brojeva Odrediti skup elementarnih dogadjaja ako se brojevi biraju
Verovatnoća i Statistika I deo Teorija verovatnoće zadaci Beleške dr Bobana Marinkovića Iz skupa, 2,, 00} bira se na slučajan način 5 brojeva Odrediti skup elementarnih dogadjaja ako se brojevi biraju
SAŽETAK OPISA SVOJSTAVA LIJEKA
 SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Ketocef 750 mg prašak za otopinu za injekciju Ketocef 1,5 g prašak za otopinu za injekciju 2. KVALITATIVNI I KVANTITATIVNI SASTAV 1 bočica Ketocef
SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Ketocef 750 mg prašak za otopinu za injekciju Ketocef 1,5 g prašak za otopinu za injekciju 2. KVALITATIVNI I KVANTITATIVNI SASTAV 1 bočica Ketocef
- pravac n je zadan s točkom T(2,0) i koeficijentom smjera k=2. (30 bodova)
 MEHANIKA 1 1. KOLOKVIJ 04/2008. grupa I 1. Zadane su dvije sile F i. Sila F = 4i + 6j [ N]. Sila je zadana s veličinom = i leži na pravcu koji s koordinatnom osi x zatvara kut od 30 (sve komponente sile
MEHANIKA 1 1. KOLOKVIJ 04/2008. grupa I 1. Zadane su dvije sile F i. Sila F = 4i + 6j [ N]. Sila je zadana s veličinom = i leži na pravcu koji s koordinatnom osi x zatvara kut od 30 (sve komponente sile
( ) ( ) 2 UNIVERZITET U ZENICI POLITEHNIČKI FAKULTET. Zadaci za pripremu polaganja kvalifikacionog ispita iz Matematike. 1. Riješiti jednačine: 4
 UNIVERZITET U ZENICI POLITEHNIČKI FAKULTET Riješiti jednačine: a) 5 = b) ( ) 3 = c) + 3+ = 7 log3 č) = 8 + 5 ć) sin cos = d) 5cos 6cos + 3 = dž) = đ) + = 3 e) 6 log + log + log = 7 f) ( ) ( ) g) ( ) log
UNIVERZITET U ZENICI POLITEHNIČKI FAKULTET Riješiti jednačine: a) 5 = b) ( ) 3 = c) + 3+ = 7 log3 č) = 8 + 5 ć) sin cos = d) 5cos 6cos + 3 = dž) = đ) + = 3 e) 6 log + log + log = 7 f) ( ) ( ) g) ( ) log
Cauchyjev teorem. Postoji više dokaza ovog teorema, a najjednostvniji je uz pomoć Greenove formule: dxdy. int C i Cauchy Riemannovih uvjeta.
 auchyjev teorem Neka je f-ja f (z) analitička u jednostruko (prosto) povezanoj oblasti G, i neka je zatvorena kontura koja čitava leži u toj oblasti. Tada je f (z)dz = 0. Postoji više dokaza ovog teorema,
auchyjev teorem Neka je f-ja f (z) analitička u jednostruko (prosto) povezanoj oblasti G, i neka je zatvorena kontura koja čitava leži u toj oblasti. Tada je f (z)dz = 0. Postoji više dokaza ovog teorema,
OBRTNA TELA. Vladimir Marinkov OBRTNA TELA VALJAK
 OBRTNA TELA VALJAK P = 2B + M B = r 2 π M = 2rπH V = BH 1. Zapremina pravog valjka je 240π, a njegova visina 15. Izračunati površinu valjka. Rešenje: P = 152π 2. Površina valjka je 112π, a odnos poluprečnika
OBRTNA TELA VALJAK P = 2B + M B = r 2 π M = 2rπH V = BH 1. Zapremina pravog valjka je 240π, a njegova visina 15. Izračunati površinu valjka. Rešenje: P = 152π 2. Površina valjka je 112π, a odnos poluprečnika
2log. se zove numerus (logaritmand), je osnova (baza) log. log. log =
 ( > 0, 0)!" # > 0 je najčešći uslov koji postavljamo a još je,, > 0 se zove numerus (aritmand), je osnova (baza). 0.. ( ) +... 7.. 8. Za prelazak na neku novu bazu c: 9. Ako je baza (osnova) 0 takvi se
( > 0, 0)!" # > 0 je najčešći uslov koji postavljamo a još je,, > 0 se zove numerus (aritmand), je osnova (baza). 0.. ( ) +... 7.. 8. Za prelazak na neku novu bazu c: 9. Ako je baza (osnova) 0 takvi se
VJEŽBE 3 BIPOLARNI TRANZISTORI. Slika 1. Postoje npn i pnp bipolarni tranziostori i njihovi simboli su dati na slici 2 i to npn lijevo i pnp desno.
 JŽ 3 POLAN TANZSTO ipolarni tranzistor se sastoji od dva pn spoja kod kojih je jedna oblast zajednička za oba i naziva se baza, slika 1 Slika 1 ipolarni tranzistor ima 3 izvoda: emitor (), kolektor (K)
JŽ 3 POLAN TANZSTO ipolarni tranzistor se sastoji od dva pn spoja kod kojih je jedna oblast zajednička za oba i naziva se baza, slika 1 Slika 1 ipolarni tranzistor ima 3 izvoda: emitor (), kolektor (K)
Elementi spektralne teorije matrica
 Elementi spektralne teorije matrica Neka je X konačno dimenzionalan vektorski prostor nad poljem K i neka je A : X X linearni operator. Definicija. Skalar λ K i nenula vektor u X se nazivaju sopstvena
Elementi spektralne teorije matrica Neka je X konačno dimenzionalan vektorski prostor nad poljem K i neka je A : X X linearni operator. Definicija. Skalar λ K i nenula vektor u X se nazivaju sopstvena
Počela biostatistike, Poslijediplomski interdisciplinarni doktorski studij Molekularne bioznanosti. Molekularne bioznanosti. Molekularne bioznanosti
 Analiza brojčanih podataka Nora Nikolac Klinički zavod za kemiju KB Sestre milosrdnice Kolegij: Počela biostatistike Statistička hipoteza postupak testiranja 1. postavljanje hipoteze: H 0, H 1 2. odabir
Analiza brojčanih podataka Nora Nikolac Klinički zavod za kemiju KB Sestre milosrdnice Kolegij: Počela biostatistike Statistička hipoteza postupak testiranja 1. postavljanje hipoteze: H 0, H 1 2. odabir
Ispitivanje toka i skiciranje grafika funkcija
 Ispitivanje toka i skiciranje grafika funkcija Za skiciranje grafika funkcije potrebno je ispitati svako od sledećih svojstava: Oblast definisanosti: D f = { R f R}. Parnost, neparnost, periodičnost. 3
Ispitivanje toka i skiciranje grafika funkcija Za skiciranje grafika funkcije potrebno je ispitati svako od sledećih svojstava: Oblast definisanosti: D f = { R f R}. Parnost, neparnost, periodičnost. 3
S t r a n a 1. 1.Povezati jonsku jačinu rastvora: a) MgCl 2 b) Al 2 (SO 4 ) 3 sa njihovim molalitetima, m. za so tipa: M p X q. pa je jonska jačina:
 S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
POVRŠINA TANGENCIJALNO-TETIVNOG ČETVEROKUTA
 POVRŠIN TNGENIJLNO-TETIVNOG ČETVEROKUT MLEN HLP, JELOVR U mnoštvu mnogokuta zanimljiva je formula za površinu četverokuta kojemu se istoobno može upisati i opisati kružnica: gje su a, b, c, uljine stranica
POVRŠIN TNGENIJLNO-TETIVNOG ČETVEROKUT MLEN HLP, JELOVR U mnoštvu mnogokuta zanimljiva je formula za površinu četverokuta kojemu se istoobno može upisati i opisati kružnica: gje su a, b, c, uljine stranica
KVADRATNA FUNKCIJA. Kvadratna funkcija je oblika: Kriva u ravni koja predstavlja grafik funkcije y = ax + bx + c. je parabola.
 KVADRATNA FUNKCIJA Kvadratna funkcija je oblika: = a + b + c Gde je R, a 0 i a, b i c su realni brojevi. Kriva u ravni koja predstavlja grafik funkcije = a + b + c je parabola. Najpre ćemo naučiti kako
KVADRATNA FUNKCIJA Kvadratna funkcija je oblika: = a + b + c Gde je R, a 0 i a, b i c su realni brojevi. Kriva u ravni koja predstavlja grafik funkcije = a + b + c je parabola. Najpre ćemo naučiti kako
MATRICE I DETERMINANTE - formule i zadaci - (Matrice i determinante) 1 / 15
 MATRICE I DETERMINANTE - formule i zadaci - (Matrice i determinante) 1 / 15 Matrice - osnovni pojmovi (Matrice i determinante) 2 / 15 (Matrice i determinante) 2 / 15 Matrice - osnovni pojmovi Matrica reda
MATRICE I DETERMINANTE - formule i zadaci - (Matrice i determinante) 1 / 15 Matrice - osnovni pojmovi (Matrice i determinante) 2 / 15 (Matrice i determinante) 2 / 15 Matrice - osnovni pojmovi Matrica reda
IZRAČUNAVANJE POKAZATELJA NAČINA RADA NAČINA RADA (ISKORIŠĆENOSTI KAPACITETA, STEPENA OTVORENOSTI RADNIH MESTA I NIVOA ORGANIZOVANOSTI)
 IZRAČUNAVANJE POKAZATELJA NAČINA RADA NAČINA RADA (ISKORIŠĆENOSTI KAPACITETA, STEPENA OTVORENOSTI RADNIH MESTA I NIVOA ORGANIZOVANOSTI) Izračunavanje pokazatelja načina rada OTVORENOG RM RASPOLOŽIVO RADNO
IZRAČUNAVANJE POKAZATELJA NAČINA RADA NAČINA RADA (ISKORIŠĆENOSTI KAPACITETA, STEPENA OTVORENOSTI RADNIH MESTA I NIVOA ORGANIZOVANOSTI) Izračunavanje pokazatelja načina rada OTVORENOG RM RASPOLOŽIVO RADNO
IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f
 IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f 2. Nule i znak funkcije; presek sa y-osom IspitivaƬe
IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f IspitivaƬe funkcija: 1. Oblast definisanosti funkcije (ili domen funkcije) D f 2. Nule i znak funkcije; presek sa y-osom IspitivaƬe
Izbor statističkih testova Ana-Maria Šimundić
 Izbor statističkih testova Ana-Maria Šimundić Klinički zavod za kemiju Klinička jedinica za medicinsku biokemiju s analitičkom toksikologijom KBC Sestre milosrdnice Izbor statističkog testa Tajna dobrog
Izbor statističkih testova Ana-Maria Šimundić Klinički zavod za kemiju Klinička jedinica za medicinsku biokemiju s analitičkom toksikologijom KBC Sestre milosrdnice Izbor statističkog testa Tajna dobrog
Matematika 1 - vježbe. 11. prosinca 2015.
 Matematika - vježbe. prosinca 5. Stupnjevi i radijani Ako je kut φ jednak i rad, tada je veza između i 6 = Zadatak.. Izrazite u stupnjevima: a) 5 b) 7 9 c). d) 7. a) 5 9 b) 7 6 6 = = 5 c). 6 8.5 d) 7.
Matematika - vježbe. prosinca 5. Stupnjevi i radijani Ako je kut φ jednak i rad, tada je veza između i 6 = Zadatak.. Izrazite u stupnjevima: a) 5 b) 7 9 c). d) 7. a) 5 9 b) 7 6 6 = = 5 c). 6 8.5 d) 7.
Veleučilište u Rijeci Stručni studij sigurnosti na radu Akad. god. 2011/2012. Matematika. Monotonost i ekstremi. Katica Jurasić. Rijeka, 2011.
 Veleučilište u Rijeci Stručni studij sigurnosti na radu Akad. god. 2011/2012. Matematika Monotonost i ekstremi Katica Jurasić Rijeka, 2011. Ishodi učenja - predavanja Na kraju ovog predavanja moći ćete:,
Veleučilište u Rijeci Stručni studij sigurnosti na radu Akad. god. 2011/2012. Matematika Monotonost i ekstremi Katica Jurasić Rijeka, 2011. Ishodi učenja - predavanja Na kraju ovog predavanja moći ćete:,
SAŢETAK OPISA SVOJSTAVA LIJEKA. 5 ml oralne suspenzije sadrži 250 mg amoksicilina u obliku amoksicilin trihidrata.
 SAŢETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV LIJEKA AMOKSICILIN Belupo 250 mg/5 ml prašak za oralnu suspenziju 2. KVALITATIVNI I KVANTITATIVNI SASTAV 5 ml oralne suspenzije sadrži 250 mg amoksicilina u obliku
SAŢETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV LIJEKA AMOKSICILIN Belupo 250 mg/5 ml prašak za oralnu suspenziju 2. KVALITATIVNI I KVANTITATIVNI SASTAV 5 ml oralne suspenzije sadrži 250 mg amoksicilina u obliku
Heterogene ravnoteže taloženje i otapanje. u vodi u prisustvu zajedničkog iona u prisustvu kompleksirajućegreagensa pri različitim ph vrijednostima
 Heterogene ravnoteže taloženje i otapanje u vodi u prisustvu zajedničkog iona u prisustvu kompleksirajućegreagensa pri različitim ph vrijednostima Ako je BA teško topljiva sol (npr. AgCl) dodatkom
Heterogene ravnoteže taloženje i otapanje u vodi u prisustvu zajedničkog iona u prisustvu kompleksirajućegreagensa pri različitim ph vrijednostima Ako je BA teško topljiva sol (npr. AgCl) dodatkom
Ĉetverokut - DOMAĆA ZADAĆA. Nakon odgledanih videa trebali biste biti u stanju samostalno riješiti sljedeće zadatke.
 Ĉetverokut - DOMAĆA ZADAĆA Nakon odgledanih videa trebali biste biti u stanju samostalno riješiti sljedeće zadatke. 1. Duljine dijagonala paralelograma jednake su 6,4 cm i 11 cm, a duljina jedne njegove
Ĉetverokut - DOMAĆA ZADAĆA Nakon odgledanih videa trebali biste biti u stanju samostalno riješiti sljedeće zadatke. 1. Duljine dijagonala paralelograma jednake su 6,4 cm i 11 cm, a duljina jedne njegove
SAŽETAK OPISA SVOJSTAVA LIJEKA
 SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Sinersul 400 mg + 80 mg tablete Sinersul forte 800 mg + 160 mg tablete 2. KVALITATIVNI I KVANTITATIVNI SASTAV Sinersul 400 mg + 80 mg tablete Jedna
SAŽETAK OPISA SVOJSTAVA LIJEKA 1. NAZIV GOTOVOG LIJEKA Sinersul 400 mg + 80 mg tablete Sinersul forte 800 mg + 160 mg tablete 2. KVALITATIVNI I KVANTITATIVNI SASTAV Sinersul 400 mg + 80 mg tablete Jedna
Implementacija HE4 i ROMA indeksa u Klinici za tumore Centru za maligne bolesti KBCSM
 Implementacija HE4 i ROMA indeksa u Klinici za tumore Centru za maligne bolesti KBCSM Dr.sc. Ljiljana Mayer, spec.med.biokemije Zagreb, 18. ožujka 2017. Klinika za tumore Centar za maligne bolesti, KBCSM
Implementacija HE4 i ROMA indeksa u Klinici za tumore Centru za maligne bolesti KBCSM Dr.sc. Ljiljana Mayer, spec.med.biokemije Zagreb, 18. ožujka 2017. Klinika za tumore Centar za maligne bolesti, KBCSM
INTELIGENTNO UPRAVLJANJE
 INTELIGENTNO UPRAVLJANJE Fuzzy sistemi zaključivanja Vanr.prof. Dr. Lejla Banjanović-Mehmedović Mehmedović 1 Osnovni elementi fuzzy sistema zaključivanja Fazifikacija Baza znanja Baze podataka Baze pravila
INTELIGENTNO UPRAVLJANJE Fuzzy sistemi zaključivanja Vanr.prof. Dr. Lejla Banjanović-Mehmedović Mehmedović 1 Osnovni elementi fuzzy sistema zaključivanja Fazifikacija Baza znanja Baze podataka Baze pravila
Prof. dr Ljubiša TOPISIROVIĆ. G(+) G(-) Antimikrobnatolerancija: svojstvo bakterija da prežive tretman baktericidnih
 Istorijat antimikrobne terapije Sumeri (500 p.n.e) su davali pacijentima supu od piva u koju su stavljali kožu zmije i nastrugan oklop kornjače. Vavilonci su koristili mast napravljenu od žuči žabe i kiselog
Istorijat antimikrobne terapije Sumeri (500 p.n.e) su davali pacijentima supu od piva u koju su stavljali kožu zmije i nastrugan oklop kornjače. Vavilonci su koristili mast napravljenu od žuči žabe i kiselog
DINAMIČKA MEHANIČKA ANALIZA (DMA)
 Karakterizacija materijala DINAMIČKA MEHANIČKA ANALIZA (DMA) Dr.sc.Emi Govorčin Bajsić,izv.prof. Zavod za polimerno inženjerstvo i organsku kemijsku tehnologiju Da li je DMA toplinska analiza ili reologija?
Karakterizacija materijala DINAMIČKA MEHANIČKA ANALIZA (DMA) Dr.sc.Emi Govorčin Bajsić,izv.prof. Zavod za polimerno inženjerstvo i organsku kemijsku tehnologiju Da li je DMA toplinska analiza ili reologija?
Uvod u neparametrijske testove. Usporedba. Neparametrijske inačice t-testa za dva nezavisna uzorka. dr. sc. Goran Kardum
 Uvod u neparametrijske testove dr. sc. Goran Kardum 1 Usporedba NACRT ISTRAŽIVANJA PARAMETRIJSKA PROCEDURA NEPARAMETRIJSKA PROCEDURA Dva nezavisna uzorka T-test Mann-Whitney U-test Dva zavisna uzorka T-test
Uvod u neparametrijske testove dr. sc. Goran Kardum 1 Usporedba NACRT ISTRAŽIVANJA PARAMETRIJSKA PROCEDURA NEPARAMETRIJSKA PROCEDURA Dva nezavisna uzorka T-test Mann-Whitney U-test Dva zavisna uzorka T-test
Više dokaza jedne poznate trigonometrijske nejednakosti u trokutu
 Osječki matematički list 000), 5 9 5 Više dokaza jedne poznate trigonometrijske nejednakosti u trokutu Šefket Arslanagić Alija Muminagić Sažetak. U radu se navodi nekoliko različitih dokaza jedne poznate
Osječki matematički list 000), 5 9 5 Više dokaza jedne poznate trigonometrijske nejednakosti u trokutu Šefket Arslanagić Alija Muminagić Sažetak. U radu se navodi nekoliko različitih dokaza jedne poznate
HEMIJSKA VEZA TEORIJA VALENTNE VEZE
 TEORIJA VALENTNE VEZE Kovalentna veza nastaje preklapanjem atomskih orbitala valentnih elektrona, pri čemu je region preklapanja između dva jezgra okupiran parom elektrona. - Nastalu kovalentnu vezu opisuje
TEORIJA VALENTNE VEZE Kovalentna veza nastaje preklapanjem atomskih orbitala valentnih elektrona, pri čemu je region preklapanja između dva jezgra okupiran parom elektrona. - Nastalu kovalentnu vezu opisuje
Funkcije dviju varjabli (zadaci za vježbu)
 Funkcije dviju varjabli (zadaci za vježbu) Vidosava Šimić 22. prosinca 2009. Domena funkcije dvije varijable Ako je zadano pridruživanje (x, y) z = f(x, y), onda se skup D = {(x, y) ; f(x, y) R} R 2 naziva
Funkcije dviju varjabli (zadaci za vježbu) Vidosava Šimić 22. prosinca 2009. Domena funkcije dvije varijable Ako je zadano pridruživanje (x, y) z = f(x, y), onda se skup D = {(x, y) ; f(x, y) R} R 2 naziva
