5. a) ρ (g/cm 3 ) = 0,119 = 11,9% 12% 2 p
|
|
|
- Ê Ζάνος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine, osaliselt ka päevitumine. 1 p Keemilised nähtused: raudnaela roostetamine; butaani põlemine; päevitumine. 1 p d) i) Tiigel; ii) jahuti; iii) uhmer; iv) bürett. 2 p e) i) K; ii) Cl; iii) Na; iv) Br -. 2 p f) Toimus neutralisatsioonireaktsioon, mille käigus tekkisid NaCl (söögisool) ja 2. Söövitavat hapet ega leelist alles ei jäänud. 2 p (10) 2. a) 2 Na Na + 2 b) Al() + Cl AlCl + 2 c) BaCl2 + Al2(S4) BaS4 + 2 AlCl d) 2 + N2 2 N e) Ba(N)2 + (N4)2C BaC + 2 N4N f) K2C + 2 Cl 2 KCl C2 g) 2 S S h) 2 Na Na + 2 (iga õigesti tasakaalustatud võrrand 1 p; eksitud ühe koefitsiendiga 0,5 p; eksitud rohkem kui ühe koefitsiendiga 0 p) (8). a) Element X on vesinik (). Elemendi Y aatommass on 1 12=12, seega Y on süsinik (C). Element Z aatomis on 2 prootonit rohkem, kui süsiniku aatomis, seega 6+2=8 prootonit ja element Z on hapnik (). p b) Vesiniku ( 1 ) aatomis on 1 prooton, 0 neutronit ja 1 elektron, süsinikul ( 12 C) 6 prootonit, 6 neutronit ja 6 elektroni, hapniku ( 16 ) aatomis 8 prootonit, 8 neutronit ja 8 elektroni. p c) YZ = C, vingugaas, süsinikmonooksiid YZ2 = C2, süsihappegaas, süsinikdioksiid YX4 = C4, soogaas / maagaas, metaan X2Z = 2, vesi, divesinikmonooksiid 4 p (10) lahustuvate ainete lisamisel. Näiteks tuntud eksperiment Coca-Cola ja Mentosega vallandab vägagi tormilise ja kleepuva purskkaevu. 2 p d) Küllastunud gaasilahuseid tuleb ettevaatlikult soojendada 1 p, tahkete ja vedelate ainete küllastunud lahuseid ettevaatlikult jahutada 1 p. (11) 5. a) ρ (g/cm ) Suhkru protsendiline koostis (%) p b) Suhkru protsendilise sisalduse tõustes lahuse tihedus suureneb. 1 p c) ρ(10%-line lahus) = 1,05 g/cm m(lahus) = ρv= 1,05 g/cm * 120 cm = 124,2 g m(suhkur) = 124,2 g 0,10 = 12,4g 12 g p d) i) %lahus= 100g 0,04+65g 0,24 = 19,6g = 0,119 = 11,9% 12% 2 p 100g+65g 165g ii) ρ(11,9%-line lahus) 1,04 g/cm 1 p iii) V = m/ρ = 165 g / 1,04 g/cm = 158 cm 1 p (11), 4. a) msuhkur = = 00 g; VCoca-Cola = = 2,8 l Mihkel saab päevase süsivesikute koguse 2,8 liitri Coca-Cola joomisel. p b) C(suhkurPepsi) = =,, = 120 g/l 2 p c) Gaseeritud joogid on süsihappegaasi küllastunud lahused. Pudeli avamisel rõhk joogi kohal alaneb ning C2 hakkab lahusest kihinal eralduma. 2 p Gaas eraldub veel lahuse segamisel/raputamisel, soojendamisel ja teiste
2 6. Lisaküsimuse vastus: Naatriumhüdroksiid. Iga õige sõna annab 1 punkti. (10) P S R A Ü D L U S E E N L I L S L T K G M U N A T A R S E E B I K I V I E R J K M L I N A U L Õ T I K S E B I D I P E E U V A R M I B I E M R I N E Л А У К Г Г Т М И А Л С Д Р У З Л Е Т И И Б С В О Р У С Т Р О Е Г О П Т И О В С Е Д К И Й Н А Т Р Н А Л З Я Н Т Ы Л А Б Я У Я У К Т Ц М Ь И А Я Г А
3 201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesannete lahendused 9. klass 1. a) iga kõigi õigete oküdatsiooniastmeetga aine 1 punkt, õige aineklass 0,5 punkti. i) I Cl VII -II 4, hape ii) K I 4[Fe II (C II N -III )6], sool iii) N -III I I 2 -II, alus iv) Na I Co III (N III -II 2)6, sool ( = 6) b) iga õige keskkond 0,5 punkti i) S, happeline ii) N, neutraalne iii) Na2S4, neutraalne iv) K, aluseline v) Cl, happeline vi) K2S, aluseline (6 0.5 = ) c) iga õige klassifikatsioon 0,5 punkti i) 2S ii) S iii) S, 2S (4 0.5= 2) (kokku 11) 2. a) n(2s4) = 0,00224 l 1, M = 2, mol b) Basseinis on vett 2, l / 0,0100 l = 2, korda rohkem, mistõttu ka väävelhapet kulub 200 miljonit korda rohkem. n(2s4) = 2, mol 2, = 44,8 mol () c) V(6% 2S4) = 44,8 mol 98,1 g/mol / 0,60 / 1270 g/l = 9,61 l () (kokku 8). a) Zn+2Cl ZnCl2+2 Cu ei reageeri soolhappega. b) Ideaalgaasi molaarne ruumala 1 atm juures: 24,5 dm /mol (25 C). 4,9 dm vastab 4,9 dm /24,5 dm /mol= 0,20 mol gaasi. Kõik tekkinud gaasi oli 2, järelikult tsinki reageeris sama palju, kuna reaktsioonis on Zn:2 <-> 1:1. M(Zn)=65,4 g/mol; m(zn)=65,4 g/mol*0,20 mol= 1,08 g; m(cu)= 2,7-1,08= 19,62 g; %(Cu)=19,62g/2,7g*100%= 60%. c) Muidu ei oleks kogu tsink sulamis saanud soolhappega reageerida, kuna vask kaitseb sulami sisemuses asuvat tsinki soolhappe eest. (kokku 8) 4. a) Messing ehk valgevask b) A = Zn, tsink B = Cu, vask c) Zn + 2Cl ZnCl2 + 2 Cu + Cl reaktsiooni ei toimu d) C = Al, aluminium e) 2Al + Cl2 2AlCl f) m(sn) = 5,74 g * 1%= 0,0574g n = m/m = 0,0574g/ 118,7 g/mol = 0,00048 mol = 0,48 mmol (kokku 9) 5. a) X hapnik ( ) A 2 hapnik ehk dihapnik ( ) B osoon ( ) C I2 iood ( ) D - I vesinikjodiid ( ) b) a. 2KI K + I2 + 2 b. 2 + I2 2I c. 2KMn4 K2Mn4 + Mn2 + 2 d. 2I I2 + 2 e. 6I + 2S4 I2 + S + 42 c) VI oksüdeerija, I redutseerija ( ) V 2S4 oksüdeerija, I redutseerija ( ) (kokku 11) 6. a) Definitsioonid (iga õige definitsioon 0,5 punkti): Amorfne tahkis tahkes olekus aine, mille osakesed ei ole paigutunud ruumis üksteise suhtes korrapäraselt. (0,5) Segu mitmest erineva keemilise koostisega ainest koosnev süsteem. (0,5) Polümeer suur molekul, mis koosneb korduvatest väiksematest sarnase keemilise struktuuriga struktuurühikutest (struktuurühiku all mõeldakse omavahel keemilise sideme kaudu ühendatud aatomeid). (0,5) b) Aineklassid (iga õige aineklass 0.5 punkti): Aine A on karboksüülhape (osaliselt õige vastus on ka (küllastumata, tsüklit sisaldav) süsivesinik). (0,5) Aine B on alkohol (osaliselt õige vastus on ka (küllastumata, tsüklit sisaldav) süsivesinik). (0,5) Aine C on (küllastumata, tsüklit sisaldav) süsivesinik. (0,5) c) Brutovalemid (iga brutovalem 0,5 punkti) Aine A on C2002 (0,5) Aine B on C202 (0,5) Aine C on C202 (0,5) Molekulmassid (iga õige molekulmass 0,5 punkti) M(aine A) = 20 12,01+0 1, ,00=02,5 amü (0,5)
4 M(aine B) = 20 12,01+2 1,00+16,00=288,5 amü (0,5) M(aine A) = 20 12,01+0 1,00=272,5 amü (0,5) d) Kuna merevaigu põhikomponentideks on raskeid aatomeid (nt Cl, Br jms) mitte-sisaldavad süsivesinikud, siis võiks merevaigu tihedus olla vee omaga praktiliselt võrdne. Tõepoolest, merevaigu keskmine tihedus on 1,1 g/cm (tihedust vähendavad ka merevaigu koostises esinevad õhumullid). Seega saaks ehtsat merevaiku eristada klaasist n-ö ujutamistestiga küllastunud soolalahuses (tihedus 1,2 g/cm ): merevaigu tükk peaks jääma lahuse pinnale, klaas vajuma põhja. e) i) Kergel kuumutamisel ( C) muutub merevaik pehmeks (temperatuuril 50 C hakkab sulama ja samaaegselt lagunema; vastust sulab loetakse samuti õigeks, vastust põleb mitte). ii) Merevaigu panemisel puhtasse vette ei juhtu midagi, merevaik jääb anuma põhja. iii) Merevaigu panemisel vähepolaarsetesse orgaanilistesse lahustitesse toimub merevaigu osaline lahustumine (vastust lahustub loetakse õigeks, vastust laguneb osaliselt õigeks). f) Suktsiinhappe struktuur: C C 2 C 2 C Molekulmass on amü. (kokku 1)
5 1. 201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesannete lahendused. 10. klass a) Täieliku põlemise saadusteks on C2 ja 2. C = C b) Tärklis tekib glükoosi (C6126) polümerisatsioonil. c) C2 ja C4. d) Põleb minimaalse o.-a.-ga ühend. (0,5) e) i) Na22 (+I ja I) ii) F2 (+II ja I) iii) Mg2 (+II ja I) (1,5) f) => B, Be, Na, Sr g) Õige järjekord on: iii, ii, i, iv. b) (1x0,5) C C C C Si 2 c) 2. a) Tasakaalustatud reaktsioonivõrrandid: I. C CaC Ca(C)2 / C C; CaC (t) Ca + (l) + C 2- (l); 2C+C 2- (l) C - II. Ca(C)2 CaC + C2 + 2 III. Ca(C)2 + Na2C CaC + 2NaC IV. CaC Ca + C2 V. Ca + 2 Ca()2 (5x1,2) b) C - - alus ja hape; 2 alus ja hape; C 2- - alus; (2C hape); - - alus; (6x0,5). a) 2x y 2 1 C x y ( ) 2 xc 2 y x 5, 6 C x y C y a) A g, elavhõbe; B Br2, broom; C gbr2, elavhõbe(ii)bromiid; D NaC, naatriumvesinikkarbonaat; E Na2C, naatriumkarbonaat; F C2, süsinikdioksiid; G 2, vesi; Br, vesinikbromiid; I NaBr, naatriumbromiid; J Na, naatriumhüdroksiid. (10x0,5) b) i) Na + Cl = NaCl + 2 (näiteks); ii) g + Br2 = gbr2; iii) Na2C + 2Br = 2NaBr C2 ; iv) C2 + 2Na = Na2C + 2 (4x1) c) Näiteks: N + Cl = N4Cl 5. a) tahked: KN, C, S ja K2S (6x0,25) gaasilised: N2 ja C2
6 6. b) KN kaaliumnitraat e salpeeter (1,5) c) oksüdeerub: C (x0,5) redutseeruvad: S ja N d) Reaktsioonivõrrandi järgi peab KN-e olema 2n mooli, süsinikku n mooli ja väävlit n mooli. Saame võrrandi 2n M(KN) + n M(C) + n M(S) = 100 g 202n + 6n + 2n = 100 n=0,704 mol m(kn)= 2n M(KN) = 74,8 g m(c) = n M(C) = 1, g m(s) = n M(S) = 11,9 g (x0,5) e) 1 mooli väävli kohta tekib +1=4 mooli gaasilist ainet 100 g püssirohu kohta tekib gaasilist ainet n(gaas)= 4 n=1,48 mol a) i) ii) iii) iv) (4x1) b) A äädikhape (etaanhape) B etanool 7. I oktüülatsetaat (oktüületanaat) J bensüülalkohol K bensüülatsetaat (bensüületanaat) (11x0,5) a) X Si A C B C Cl D Na G SiC, ränikarbiid Si2, ränidioksiid I 2, dihapnik/hapnik J, osoon K Cl2, kloor L SiCl4, ränitetrakloriid M Cl, vesinikkloriidhape N Na, naatriumhüdroksiid (5x0,5) (8x0,5) b) i) Si + 2 Si2 ii) C + 2 C2 iii) 2 2 iv) SiCl Si2 + 4 Cl v) Na + Cl NaCl + 2 (5x1) c) Si + 4 Na [Si4] Na C etüülatsetaat (etüületanaat) D propaan-1-ool või n-propanool E butaan-1-ool või n-butanool F oktaan-1-ool või n-oktanool G propüülatsetaat (propüületanaat) butüülatsetaat (butüületanaat)
7 8. a,b) c) + FeBr A -Benseen B -Bromobenseen Br + Na + Na + Br - t C - Fenool Na + C 2 t, P D - 2-hüdroksübensoehape + 2 S 4 Br Br + Br + (nimetused 4x1, reaktsioonivõrrandid 4x1,5) + Keemistemperatuur on kõrgem kui N2-l, sest vesi moodustab molekulide vahel vesiniksidemeid, mis on täiendavaks molekule kooshoidvaks jõuks. c) Madalam keemistemperatuur on kõige madalama molekulmassiga kloriidil ehk Cl-l, sest erinevalt 2-st (kõige madalama molekulmassiga oksiid) ei moodusta see vesiniksidemeid. d) S + 2 2S4 või Mg + 2 Mg()2 9. d) + C (salitsüülhape) 2 S 4 a) Kõige madalama sulamistemperatuuriga: S. S on kõige madalama sulamistemperatuuriga, sest selle kristallvõre on molekulaarne (kristalli hoiavad koos molekulide vahelised jõud). Si2 on kõrgema sulamistemperatuuriga, sest kristallvõre on atomaarne (kristalli hoiavad koos kovalentsed sidemed). Mg on kõrgema sulamistemperatuuriga, sest kristallvõre on iooniline (kristalli hoiavad koos ioonilised sidemed). (Molekulide vahelised jõud on üldjuhul nõrgemad kui kovalentsed või ioonilised sidemed) b) Divesinikoksiid ehk vesi. Molekulvalem
8 201/14 õ.a. keemiaolümpiaadi piirkonnavooru ülesannete lahendused 11.klass 1. a) Metaan (-IV), metanool (-II), metanaal (0), metaanhape (II), süsihape (IV) b) Br, 2S4, Cl4 (1,5) osakest 181,9g mol -1 c) m(v25) = = 5 6, osakest mol -1 6, g d) benseen; propaan; but-2-een; N,N-dimetüületaanamiid e) 16Cl + 2KMn KCl + 2MnCl2 + 5Cl g mol-1 0,62 58 g mol -1 0,28 a) N(C) = = ~ N() = = ~1 12 g mol g mol -1 N() = = 6 (1,5) A - atsetoon ehk propaan-2-oon, summaarne valem: C6, struktuurvalem: CCC (iga õige valem ja nimetus 0,5p) (1,5) b) B - aminorühm, R-N2 C - karboksüülrühm, R-C (või vastupidi) D - amiid- ehk peptiidside, R-CN-R (iga õige nimetus ja valem 0,5p) () E - hüdrolüüs: R-CN-R + 2 R-C + 2N-R. a) 222 = Nii redutseerijaks kui ka oksüdeerijaks on hapnik. (2 0,5) b) ntekkis = l/(22,4 l mol -1 ) = 1, mol n(22)reageeris = 2 1, mol = 2, mol ühes sekundis reageerinud peroksiidi hulk: v = 2, mol/(60 s) = mol/s (0,5) ühes milliliitris olev ensüümi hulk: n(katalaas) = 10 - l 10-9 mol l -1 = mol (0,5) kkat = mols -1 /(10-12 mol) = s -1 c) 1/( s -1 ) = 2, s = 25 ns d) i) 2KI S4 = I2 + K2S ii) 2KMn S4 = MnS4 + K2S Na2S4 reaktsiooni produkti kaalutise järgi ei saa arvutada, sest CaS4 on vähelahustuv ja ei sadene täielikult. Kuna kaltsium- ja kaaliumnitraat annavad värvitu lahuse, aga vask värvib lahuse siniseks, on võimalik spektroskoopiliselt leida just tema kontsentratsioon teise 10 ml proovi analüüsist. xproov(g/ml) = (y-0,06)/8 = (0,6-0,06)/8 = 0,015 g/ml (1,5) m(cu(n)2)proov = 0,015 g ml ml = 1,5 g m(cu) = m(cun ) 2 M(Cu) 1,5 g 6,5 g mol-1 = = 0,51 g M(CuN ) 2 187,5 g mol -1 Na2C toimel sadenevad CuC ja CaC lahusest välja. Nende ühine mass oli 9,404 g järgi jäänud 80 ml lahuses. m(karbonaadid)100ml = 9,404 g 100/80 = 11,755 g m(cuc) = mcu M(CuC ) M(Cu) m(ca) = mcac M(Ca) M(CaC ) = = 0,508 g 12,5 g mol-1 6,5 g mol -1 = 0,988 g 11,755 g-0,988 g 40 g mol g mol -1 = 4,068 g ~ 4, g (1,5) Kõikide metallide kontsentratsioonid: c(cu) = 0,508 g/50 ml = 0,0102 g/ml ~0,010 g/ml c(ca) = 4,1 g/50 ml = 0,0862 g/ml ~0,086 g/ml c(k) = [m nitraatide segu - m(cun ) 2 - mca(n ) 2 ] M(K) = M(KN ) 50 ml [26,56 g - 1,5 g - 17,7 g] 9 g mol-1 = 101 g mol = 0,0571 g/ml ~0,057 g/ml ml m(me(n)2) = mme M(Me(N ) 2 ) M(Me) 5. a) d = 2a + b/2 b) i) 16 d 2a b 2 100% 12a + b + 14c + 16d ii) % c) C6N66 = 2 + N2 + C 1 mol nrdx = 1 dm 24 dm 9 (1,5) mrdx = 0,0046 mol 222 g = 1,0 g 1 mol (1,5) 6. a) X N, lämmastik (0,5p ka siis kui on kirjutatud ainult valem või nimetus) A N2, lämmastik B 2, vesinik C N, ammoniaak D NaCl, naatriumhüpoklorit E N24, hüdrasiin F N, lämmastikmonooksiid G N2, lämmastikdioksiid N, lämmastikhape I MgN2, magneesiumnitriid (iga õige nimetuse ja valemi eest 0,25p) (4,5) b) i) N N (0,75)
9 ii) 2N + NaCl N24 + NaCl + 2 iii) N N iv) 4N N + 62 v) 2N + 2 2N2 (0,75) vi) N N + N vii) Mg + N2 MgN2 viii) MgN N + Mg()2 (sellest tasakaalustamise eest kõigil juhtudel 0,25 p; 1 vale ühend lähteainetes või saadustes langetab punkte 0,25p võrra) (kokku 7,5)
10 201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesannete lahendused. 12. klass 1. a) Propaan > etüülatsetaat > äädikhape b) Vesinikside > dipool-dipool dipool-indutseeritud dipool dispersioonijõud c) Lisades süsteemi inertgaasi, vähendades süsteemi ruumala, lisades lähteaineid, eemaldades saaduseid. d) i) appelised: CC, C2, (N4)2S4 ii) Neutraalsed: Mn2, KI, Fe2, NaCl iii) Aluselised: NaS, Ca, Ba()2 (0,5x10=5) 2. a) CaC Ca+C2 MgC Mg+C2 N4N N2+22 b) Ca()2+C2 CaC+2 2(g) 2(v) (Piisab ka, kui on kirjutatud, et vesi kondenseerub või et ta on sellel temperatuuril vedelik) N2 on neutraalne oksiid ning ei reageeri ei vee ega ka kaltsiumhüdroksiidiga ning läbib lahuse gaasina c) Ülesande tekstist lähtuvalt saame koostada võrrandid: 1) Kõigi ainete mass kokku on nmgc M MgC ncac M CaC nn N M 4 N 4N 40, 20g 2) Vastavalt reaktsioonivõrranditele on peale lagunemist gaasisegu koostis ( nmgc ncac n N N ) RT K V6,44L p ) Peale Ca()2 vesilahusest läbijuhtimist ning 298 K jahutamist on alles nn RT 2 298K ainult N2 V,740L p Alustades võrrandist ) saame teada N2 hulga kaudu N4N moolid: nn n 2 N 4N 1bar,740L bar L 0, K molk 0, 151mol Seejärel arvutame kuumas gaasisegus olnud gaaside koguhulga: nmgc ncac 6,44L 1bar nn N 4 bar L 0, K molk 0, 76mol Siit saab avaldada metallide soolade hulga: nmgc n CaC 0,76mol 0,151mol 0, 10mol Avaldades näiteks MgC moolide arvu: nmgc ( 0,10 ncac ) mol Nüüd saame saadud väärtused asetada võrrandisse 1): g g g (0,10 ncac ) mol 84, ncac mol 100,1 0,151mol 80 40,20g mol mol mol 26,1g 84,nCaC 100,1n CaC 12,08g 40,20g n CaC 0,126mol Seega MgC hulk on: n MgC 0,10mol 0,126mol 0, 184mol Ainete massid algses segus: mmgc 15,5g mcac 12,6g mn 4N 12,1g. a) CaC Ca()2 + C22 b) Reaktsiooni entalpia tekkeentalpiate kaudu: ( Ca( ) ) ( C ) CaC r f 2 f 2 2 f 2 2 f 2 kj kj kj kj kj r 986,1 226,7 59,8 2( 285,8 ) 128 mol mol mol mol mol Reageerinud CaC2 moolide arv: m 15,0g n 0, 24mol M 64,0g / mol Toimunud reaktsiooni soojusefekt: r 0,24mol ( 128kJ / mol) 0, 0kJ c) Reaktsioon on eksotermiline (sest <0). d) 15,0 g kaltsiumkarbiidi moolide arv on 0,24 mol (vt b) ), vastavalt reaktsiooni stöhhiomeetriale (vt a) ) tekkis järelikult 0,24 mol etüüni. Tekkinud etüüni põlemise soojusefekt on seega: 1256kJ / mol 0,24mol 294kJ e) Põlemine muudaks (tõstaks) temperatuuri rohkem, kuna põlemise soojusefekt on suurem. 4. a) Eeldame, et meil on 100 g ainet. Siis on meil 55,1 g hapnikku, 41,4 g süsinikku ja,5 g vesinikku. Kui me arvutame need moolihulkadeks ümber, saame teada, et :C: suhtuvad üksteisesse moolide järgi kui 1:1:1. Kuna tegemist on dikarboksüülhappega, siis hapnikke on kokku 4, seega brutovalemiks peab olema C444. b) Kuna maleiinhappel on kaksikside, siis peab ta olema cis kujul, kuna trans isomeer on üldjuhul stabiilsem cis isomeerist. Nimetus: (Z) buteendihape
11 c) a) Cl (0,5) Cl + () d) Reaktsioon toimub kiiremini happelises keskkonnas, kuna karbonüülrühma protoneerimine aktiveerib karbonüülrühma ja -rühm muutub paremini lahkuvaks rühmaks. 5. a) i) katood Pb2 (0,5) anood Pb (0,5) elektrolüüt 2S4(aq) (0,5) ii) katood S8 õige ka lihtsalt S (0,5) anood Na (0,5) elektrolüüt naatriumaluminaat xna2 yal2 (0,5) iii) katood Br2 (0,5) anood Zn (0,5) elektrolüüt ZnBr2(aq) (0,5) b) i) katood: Pb2 + 2S e = PbS anood: Pb + 2S4 = PbS4 + 2e ii) katood: S8 + 16e = 8S 2 või 2S + 2e - = S2 2- anood: Na = Na + + e iii) katood: Br2 + 2e = 2Br anood: Zn = Zn e c) M(NaS)= 55 g/mol; M(Pb-2S4)= 05 g/mol; M(ZnBr2)= 225 g/mol. Kui eeldada, et kõik akud annavad ühe mooli kohta ligikaudu võrdse koguse energiat, siis on väikseim ekvivalentmass Na-S akul. Selle energiamahtuvus on umbes 150 Wh/kg. Plii- ja ZnBr2 energiamahtuvused on 0 50 Wh/kg. + Cl b) Kuna seos kontsentratsiooni ja neelduvuse vahel on lineaarne, siis: M 5 c 1 0,82AU 9,5 10 M 876AU m 461mg c) n TCP 2, mmol M 197,45mg / mmol Leiame TCP moolide hulga oktanoolis: TCP TCP TCP 5 nok tan oolis n nvees 2,mmol 9,52 10 M 5ml 2, mmol (1, koos põhjendusega lugeda õigeks ka lahendus, kus eeldatakse, et TCP on praktiliselt täielikult okatnoolis) ning nüüd kontsentratsiooni oktanoolis: n 2,mmol c TCP ok tan oolis 0, 47M V 5ml 0,47M d) log( P ) log 5 9,52 10 M, 7 log P 1,19 e) P Et ruumalad on võrdsed, siis cok tan oolis nok tan oolis P cvees nvees siit nok tan oolis P nvees n vees n vees P n vees n vees n vees ( P 1) P ,5 1
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
1998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
( ) ( ) 2008/2009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2005/2006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. = 52,5 g/mol
 005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
=217 kj/mol (1) m Ühe mooli glükoosi sünteesil lihtainetest vabaneb footoneid: Δ H f, glükoos n (glükoos) =5,89 mol (1) E (footon)
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
Keemiliste elementide perioodilisustabel
 Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass
 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
b) Täpne arvutus (aktiivsete kontsentratsioonide kaudu) ph arvutused I tugevad happed ja alused
 ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
Lokaalsed ekstreemumid
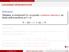 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Vektorid II. Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale
 Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
ETTEVALMISTUS KEEMIAOLÜMPIAADIKS II
 ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi
 Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Koduseid ülesandeid IMO 2017 Eesti võistkonna kandidaatidele vol 4 lahendused
 Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Funktsiooni diferentsiaal
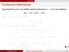 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
ΦΡΟΝΤΙΣΤΗΡΙΟ Μ.Ε. ΣΥΜΒΟΛΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
Kehade soojendamisel või jahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks.
 KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design
 Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
panagiotisathanasopoulos.gr
 . Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
. Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
Minion Pro Condensed A B C D E F G H I J K L M N O P Q R S T U
 Minion Pro Condensed Latin capitals A B C D E F G H I J K L M N O P Q R S T U V W X Y Z & Æ Ł Ø Œ Þ Ð Á Â Ä À Å Ã Ç É Ê Ë È Í Î Ï Ì İ Ñ Ó Ô Ö Ò Õ Š Ú Û Ü Ù Ý Ÿ Ž Ă Ā Ą Ć Č Ď Đ Ě Ė Ē Ę Ğ Ģ Ī Į Ķ Ĺ Ľ Ļ Ń
Minion Pro Condensed Latin capitals A B C D E F G H I J K L M N O P Q R S T U V W X Y Z & Æ Ł Ø Œ Þ Ð Á Â Ä À Å Ã Ç É Ê Ë È Í Î Ï Ì İ Ñ Ó Ô Ö Ò Õ Š Ú Û Ü Ù Ý Ÿ Ž Ă Ā Ą Ć Č Ď Đ Ě Ė Ē Ę Ğ Ģ Ī Į Ķ Ĺ Ľ Ļ Ń
ORGAANILINE KEEMIA I osa
 ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
TÄIENDAVAID TEEMASID KOOLIKEEMIALE III
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
5. TUGEVUSARVUTUSED PAINDELE
 TTÜ EHHTROONKNSTTUUT HE00 - SNTEHNK.5P/ETS 5 - -0-- E, S 5. TUGEVUSRVUTUSE PNELE Staatika üesandes (Toereaktsioonide eidmine) vaadatud näidete ause koostada taade sisejõuepüürid (põikjõud ja paindemoment)
TTÜ EHHTROONKNSTTUUT HE00 - SNTEHNK.5P/ETS 5 - -0-- E, S 5. TUGEVUSRVUTUSE PNELE Staatika üesandes (Toereaktsioonide eidmine) vaadatud näidete ause koostada taade sisejõuepüürid (põikjõud ja paindemoment)
ΓΗ ΚΑΙ ΣΥΜΠΑΝ. Εικόνα 1. Φωτογραφία του γαλαξία μας (από αρχείο της NASA)
 ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014. ÄÉÁÍüÇÓÇ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ
 23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
Graafiteooria üldmõisteid. Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid
 Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Ασκήσεις Προβλήματα. Μετρήσεις Μονάδες Γνωρίσματα της Ύλης
 Ασκήσεις Προβλήματα Μετρήσεις Μονάδες Γνωρίσματα της Ύλης 19. Ποιες μονάδες χρησιμοποιούν συνήθως οι χημικοί για την πυκνότητα των: α) στερεού, β) υγρού και γ) αερίου σώματος; Να εξηγήσετε τη διαφορά.
Ασκήσεις Προβλήματα Μετρήσεις Μονάδες Γνωρίσματα της Ύλης 19. Ποιες μονάδες χρησιμοποιούν συνήθως οι χημικοί για την πυκνότητα των: α) στερεού, β) υγρού και γ) αερίου σώματος; Να εξηγήσετε τη διαφορά.
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (Επιλέγετε δέκα από τα δεκατρία θέματα) ΘΕΜΑΤΑ 1. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λάθος; Γιατί; (α) Από τα στοιχεία Mg, Al, Cl, Xe, C και Ρ, τον μεγαλύτερο
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (Επιλέγετε δέκα από τα δεκατρία θέματα) ΘΕΜΑΤΑ 1. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λάθος; Γιατί; (α) Από τα στοιχεία Mg, Al, Cl, Xe, C και Ρ, τον μεγαλύτερο
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2019 Β ΦΑΣΗ
 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Δίνεται στοιχείο Χ το οποίο έχει οκτώ ηλεκτρόνια στην εξωτερική του στιβάδα.
ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Δίνεται στοιχείο Χ το οποίο έχει οκτώ ηλεκτρόνια στην εξωτερική του στιβάδα.
Αλληλεπίδραση ακτίνων-χ με την ύλη
 Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
αριθμός δοχείου #1# control (-)
 Μόνο απιονισμένο νερό #1# control (-) Μακροστοχεία: Ν, P, K, Ca, S, Εάν κάποια έλλειψη μετά 1 μήνα έχει σημαντικές επιπτώσεις προσθέτουμε σε δόσεις την έλλειψη έως ότου ανάπτυξη ΟΚ #2# control (+) Μακροστοχεία:
Μόνο απιονισμένο νερό #1# control (-) Μακροστοχεία: Ν, P, K, Ca, S, Εάν κάποια έλλειψη μετά 1 μήνα έχει σημαντικές επιπτώσεις προσθέτουμε σε δόσεις την έλλειψη έως ότου ανάπτυξη ΟΚ #2# control (+) Μακροστοχεία:
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Sissejuhatus mehhatroonikasse MHK0120
 Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
ΚΕΦΑΛΑΙΟ 5: ΟΞΕΙΟΑΑΝ ΑΓΩΓΗ - ΗΑΕΚΤΡΟΛΥΣΗ
 45 ΚΕΦΑΛΑΙΟ 5: ΟΞΕΙΟΑΑΝ ΑΓΩΓΗ - ΗΑΕΚΤΡΟΛΥΣΗ 1-12. Οι απαντήσεις προκύπτουν εύκολα από τη θεωρία. Ερωτήσεις - ασκήσεις - προβλήματα 13. Η3ΡΟ4: 3 + χ + (-8) = 0 ή χ = +5 Ρ 4 : ο Α.Ο. στα ελεύθερα στοιχεία
45 ΚΕΦΑΛΑΙΟ 5: ΟΞΕΙΟΑΑΝ ΑΓΩΓΗ - ΗΑΕΚΤΡΟΛΥΣΗ 1-12. Οι απαντήσεις προκύπτουν εύκολα από τη θεωρία. Ερωτήσεις - ασκήσεις - προβλήματα 13. Η3ΡΟ4: 3 + χ + (-8) = 0 ή χ = +5 Ρ 4 : ο Α.Ο. στα ελεύθερα στοιχεία
Ηράκλειο Κρήτης, 22 Ιουνίου 2018 (Παρασκευή)
 Ηράκλειο Κρήτης, 22 Ιουνίου 2018 (Παρασκευή) Επίπεδα А1, А2, В1, В2 (όλες οι ενότητες) Τόπος διεξαγωγής: Πανεπιστήμιο Κρήτης, Πανεπιστημιούπολη Βουτών, ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΥΠΟΛΟΓΙΣΤΩΝ, ΑΜΦΙΘΕΑΤΡΟ Β, 2ο όροφο
Ηράκλειο Κρήτης, 22 Ιουνίου 2018 (Παρασκευή) Επίπεδα А1, А2, В1, В2 (όλες οι ενότητες) Τόπος διεξαγωγής: Πανεπιστήμιο Κρήτης, Πανεπιστημιούπολη Βουτών, ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΥΠΟΛΟΓΙΣΤΩΝ, ΑΜΦΙΘΕΑΤΡΟ Β, 2ο όροφο
Lisa 1 Tabel 1. Veeproovide analüüside ja mõõtmiste tulemused Kroodi
 Lisa 1 Tabel 1. Veeproovide analüüside ja mõõtmiste tulemused Kroodi Proovi nr EE14002252 EE14001020 EE14002253 EE140022980 EE14001021 9 2-6 EE14002255 2-7 EE1 4002254 10 2-8 EE140022981 Kraav voolamise
Lisa 1 Tabel 1. Veeproovide analüüside ja mõõtmiste tulemused Kroodi Proovi nr EE14002252 EE14001020 EE14002253 EE140022980 EE14001021 9 2-6 EE14002255 2-7 EE1 4002254 10 2-8 EE140022981 Kraav voolamise
Θέμα Α. Ονοματεπώνυμο: Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
,millest avaldub 21) 23)
 II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2012. Ηµεροµηνία: Τετάρτη 18 Απριλίου 2012 ΕΚΦΩΝΗΣΕΙΣ
 ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 0 Ε_.ΧλΘ(ε) ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 8 Απριλίου
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 0 Ε_.ΧλΘ(ε) ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 8 Απριλίου
Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) ( ) ΘΕΜΑ Α Α1.
 Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) (5 2 2017) ΘΕΜΑ Α Α1. Επιλέξτε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις : 1. Σε ποια από τις επόμενες ενώσεις το χλώριο έχει μεγαλύτερο αριθμό
Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) (5 2 2017) ΘΕΜΑ Α Α1. Επιλέξτε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις : 1. Σε ποια από τις επόμενες ενώσεις το χλώριο έχει μεγαλύτερο αριθμό
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ
 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
Διαγώνισμα Χημείας Α Λυκείου Οξέα Βάσεις Αλατα, και Χημικές αντιδράσεις. Θέμα 1 ο...
 Διαγώνισμα Χημείας Α Λυκείου Οξέα Βάσεις Αλατα, και Χημικές αντιδράσεις. Θέμα 1 ο.... Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις, 1.1. Από τις ενώσεις: HCl, H 2 O, NH 3, H 2 SO
Διαγώνισμα Χημείας Α Λυκείου Οξέα Βάσεις Αλατα, και Χημικές αντιδράσεις. Θέμα 1 ο.... Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις, 1.1. Από τις ενώσεις: HCl, H 2 O, NH 3, H 2 SO
Molekulid ei esine üksikuna vaid suurearvuliste kogumitena.
 2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
PÕLEVAINETE OMADUSED. Andres Talvari
 PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
KORDAMINE RIIGIEKSAMIKS V teema Vektor. Joone võrrandid.
 KORDMINE RIIGIEKSMIKS V teema Vektor Joone võrrandid Vektoriaalseid suuruseid iseloomustavad a) siht b) suund c) pikkus Vektoriks nimetatakse suunatud sirglõiku Vektori alguspunktiks on ja lõpp-punktiks
KORDMINE RIIGIEKSMIKS V teema Vektor Joone võrrandid Vektoriaalseid suuruseid iseloomustavad a) siht b) suund c) pikkus Vektoriks nimetatakse suunatud sirglõiku Vektori alguspunktiks on ja lõpp-punktiks
p A...p D - gaasiliste ainete A...D osarõhud, atm K p ja K c vahel kehtib seos
 LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
SUPPLEMENTAL INFORMATION. Fully Automated Total Metals and Chromium Speciation Single Platform Introduction System for ICP-MS
 Electronic Supplementary Material (ESI) for Journal of Analytical Atomic Spectrometry. This journal is The Royal Society of Chemistry 2018 SUPPLEMENTAL INFORMATION Fully Automated Total Metals and Chromium
Electronic Supplementary Material (ESI) for Journal of Analytical Atomic Spectrometry. This journal is The Royal Society of Chemistry 2018 SUPPLEMENTAL INFORMATION Fully Automated Total Metals and Chromium
20. SIRGE VÕRRANDID. Joonis 20.1
 κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
CaCO 3(s) --> CaO(s) + CO 2(g) H = kj. Näide
 3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 4
 ΚΕΦΑΛΑΙΟ 4 ΣΤΟΙΧΕΙΟΜΕΤΡΙΑ ΕΡΩΤΗΣΕΙΣ ΜΕ ΤΙΣ ΑΠΑΝΤΗΣΕΙΣ: 1. Τι είναι ατομικό και τί μοριακό βάρος; Ατομικό βάρος είναι ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη η μάζα του ατόμου από το 1/12 της
ΚΕΦΑΛΑΙΟ 4 ΣΤΟΙΧΕΙΟΜΕΤΡΙΑ ΕΡΩΤΗΣΕΙΣ ΜΕ ΤΙΣ ΑΠΑΝΤΗΣΕΙΣ: 1. Τι είναι ατομικό και τί μοριακό βάρος; Ατομικό βάρος είναι ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη η μάζα του ατόμου από το 1/12 της
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ. δ. 39 φορές μεγαλύτερη από το της μάζας του ατόμου του 12 C 12 Μονάδες 5
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 25-02 - 2018 Μαρία Βασιλείου, Σπύρος Παπαμιχάλης, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 25-02 - 2018 Μαρία Βασιλείου, Σπύρος Παπαμιχάλης, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD
 KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
Eesti LIV matemaatikaolümpiaad
 Eesti LIV matemaatikaolümpiaad 31. märts 007 Lõppvoor 9. klass Lahendused 1. Vastus: 43. Ilmselt ei saa see arv sisaldada numbrit 0. Iga vähemalt kahekohaline nõutud omadusega arv sisaldab paarisnumbrit
Eesti LIV matemaatikaolümpiaad 31. märts 007 Lõppvoor 9. klass Lahendused 1. Vastus: 43. Ilmselt ei saa see arv sisaldada numbrit 0. Iga vähemalt kahekohaline nõutud omadusega arv sisaldab paarisnumbrit
ORGAANILINE KEEMIA. Lühikonspekt gümnaasiumile. Koostaja: Kert Martma
 ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
AΝΑΛΟΓΙΑ ΜΑΖΩΝ ΣΤΟΧΕΙΩΝ ΧΗΜΙΚΗΣ ΕΝΩΣΗΣ
 2 ο Γυμνάσιο Καματερού 1 ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΗΣ ΥΛΗΣ 1. Πόσα γραμμάρια είναι: ι) 0,2 kg, ii) 5,1 kg, iii) 150 mg, iv) 45 mg, v) 0,1 t, vi) 1,2 t; 2. Πόσα λίτρα είναι: i) 0,02 m 3, ii) 15 m 3, iii) 12cm
2 ο Γυμνάσιο Καματερού 1 ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΗΣ ΥΛΗΣ 1. Πόσα γραμμάρια είναι: ι) 0,2 kg, ii) 5,1 kg, iii) 150 mg, iv) 45 mg, v) 0,1 t, vi) 1,2 t; 2. Πόσα λίτρα είναι: i) 0,02 m 3, ii) 15 m 3, iii) 12cm
ORGAANILINE KEEMIA. Lühikonspekt gümnaasiumile. Koostaja: Kert Martma
 ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Sisukord Sissejuhatus orgaanilisse keemiasse Alkaanid Halogeeniühendid Alkoholid Amiinid Küllastamata ühendid Areenid
ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Sisukord Sissejuhatus orgaanilisse keemiasse Alkaanid Halogeeniühendid Alkoholid Amiinid Küllastamata ühendid Areenid
Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika
 Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
ΝΟΜΟΣ ΤΗΣ ΠΕΡΙΟ ΙΚΟΤΗΤΑΣ : Οι ιδιότητες των χηµικών στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
KORDAMINE RIIGIEKSAMIKS VII teema Vektor. Joone võrrandid.
 KORDMINE RIIGIEKSMIKS VII teema Vektor Joone võrrandid Vektoriaalseid suuruseid iseloomustavad a) siht b) suund c) pikkus Vektoriks nimetatakse suunatud sirglõiku Vektori alguspunktiks on ja lõpp-punktiks
KORDMINE RIIGIEKSMIKS VII teema Vektor Joone võrrandid Vektoriaalseid suuruseid iseloomustavad a) siht b) suund c) pikkus Vektoriks nimetatakse suunatud sirglõiku Vektori alguspunktiks on ja lõpp-punktiks
ΥΠΟΥΡΓΕΙΟ ΠΟΛΙΤΙΣΜΟΥ, ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ. Χημεία
 ΥΠΟΥΡΓΕΙΟ ΠΟΛΙΤΙΣΜΟΥ, ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ Χημεία Λύσεις Ασκήσεων Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Ομάδας Προσανατολισμού Θετικών Σπουδών ΙΝΣΤΙΤΟΥΤΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΠΟΛΟΓΙΣΤΩΝ ΚΑΙ
ΥΠΟΥΡΓΕΙΟ ΠΟΛΙΤΙΣΜΟΥ, ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ Χημεία Λύσεις Ασκήσεων Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Ομάδας Προσανατολισμού Θετικών Σπουδών ΙΝΣΤΙΤΟΥΤΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΠΟΛΟΓΙΣΤΩΝ ΚΑΙ
3. Να συμπληρωθούν οι παρακάτω αντιδράσεις:
 1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
3 o Μάθημα : Αντιδράσεις απλής αντικατάστασης
 3 o Μάθημα : Αντιδράσεις απλής αντικατάστασης 1. Στόχοι του μαθήματος Οι μαθητές να γνωρίσουν:i) πότε πραγματοποιείται μια αντίδραση απλής αντικατάστασης, με βάση τη σειρά δραστικότητας των μετάλλων και
3 o Μάθημα : Αντιδράσεις απλής αντικατάστασης 1. Στόχοι του μαθήματος Οι μαθητές να γνωρίσουν:i) πότε πραγματοποιείται μια αντίδραση απλής αντικατάστασης, με βάση τη σειρά δραστικότητας των μετάλλων και
C M. V n: n =, (D): V 0,M : V M P = ρ ρ V V. = ρ
 »»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
»»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 2016
 Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Ονοματεπώνυμο: Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
Χημεία Α ΓΕΛ 15 / 04 / 2018
 Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ
 ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΠΡΕΣΒΕΙΑ ΤΗΣ ΕΛΛΑΔΟΣ ΣΤO ΚΙEBO
 ΠΡΕΣΒΕΙΑ ΤΗΣ ΕΛΛΑΔΟΣ ΣΤO ΚΙEBO ΓΡΑΦΕΙΟ ΟΙΚΟΝΟΜΙΚΩΝ ΚΑΙ ΕΜΠΟΡΙΚΩΝ ΥΠΟΘΕΣΕΩΝ Κίεβο, 18 Δεκεμβρίου 2017 Α.Π.: Φ. 2700/341 Σας αποστέλλουμε συνημμένα, για ενημέρωση, Investor Survey και 2018 Economic Forecast
ΠΡΕΣΒΕΙΑ ΤΗΣ ΕΛΛΑΔΟΣ ΣΤO ΚΙEBO ΓΡΑΦΕΙΟ ΟΙΚΟΝΟΜΙΚΩΝ ΚΑΙ ΕΜΠΟΡΙΚΩΝ ΥΠΟΘΕΣΕΩΝ Κίεβο, 18 Δεκεμβρίου 2017 Α.Π.: Φ. 2700/341 Σας αποστέλλουμε συνημμένα, για ενημέρωση, Investor Survey και 2018 Economic Forecast
ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ
 Κεφάλαιο 1ο-ΟΞΕΙΔΩΑΝΑΓΩΓΗ 1 ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ Ορισμοί : -Αριθμός οξείδωσης: I)Σε μία ιοντική ένωση ο αριθμός οξείδωσης κάθε στοιχείου είναι ίσος με το ηλεκτρικό φορτίο που έχει το
Κεφάλαιο 1ο-ΟΞΕΙΔΩΑΝΑΓΩΓΗ 1 ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ Ορισμοί : -Αριθμός οξείδωσης: I)Σε μία ιοντική ένωση ο αριθμός οξείδωσης κάθε στοιχείου είναι ίσος με το ηλεκτρικό φορτίο που έχει το
Χημεία Α ΓΕΛ 15 / 04 / 2018
 Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Κεφάλαιο 1. Έννοιες και παράγοντες αντιδράσεων
 Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
