2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
|
|
|
- Δωρίς Κουβέλης
- 7 χρόνια πριν
- Προβολές:
Transcript
1 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma Alaniin -H 3 Seriin -H (-H) ja teise aminorühma (-NH 2 ) ühinemisel 2 -H Glutamiinhape -H 2 -H 2 -H tekib 2-st aminohappest koosnev peptiid ja eraldub vesi. Kõigil aminohapetel on olemas karboksüül- ja aminorühm ning erinevus on teise süsiniku kõlvalrühmas R. a) Joonistage peptiid glütsiin-alaniin-seriin-glutamiinhape. Aminohappeid on võimalik dekarboksüülida reaktsiooni käigus asendub H rühm vesinikuga ning eraldub 2. Seriinist saab selle reaktsiooni käigus etanoolamiin (rakumembraanide koostisosa) ning glutamiinhappest signaalmolekul γ-aminobutaanhape. b) Joonistage etanoolamiini ning γ-aminobutaanhappe struktuurvalemid. (10) 2. Faraday 1. seaduse kohaselt on elektrolüüsi ajal elektroodidel toimuvates keemilistes reaktsioonides tekkiva aine hulk võrdeline elektroodidele kantud laenguhulgaga. Faraday konstant näitab ühe mooli elektronide laengut (F= /mol). Na 2 S 4 vesilahuse elektrolüüsil juhiti lahusest läbi laenguhulk 2316 (kulonit). Tekkivad gaasid koguti eraldi tagurpidistesse veega täidetud katseklaasidesse. Ühes katseklaasis tõrjus eraldunud gaas välja kaks korda enam vett kui teises katseklaasis. a) Kirjutada anoodil ja katoodil toimuvate poolreaktsioonide võrrandid ning summaarne reaktsioonivõrrand. b) Arvutage: i) Elektrolüüsil tekkinud ainete massid, ii) Elektrolüüsi tulemusel tekkinud ainete reageerimise tulemusel tekkiva(te) aine(te) hulk. c) Mis ained tekiksid (valem ja nimetus), kui samadel tingimustel kasutatakse Na 2 S 4 asemel us 4 vesilahust? (10) 3. Laborant pidi valmistama 500 ml lahust, mis sisaldab 0,25 M sulfaatioone (S4 2- ). Selleks oli tal kasutada 37,4 g Al2(S4)3 18H2. Veevaba alumiiniumsulfaadi lahustuvus on 5 o juures on 31,7 g/100 ml vees ja 20 o juures 36,4 g/100 ml vees. a) Mis on Al 2 (S 4 ) 3 18H 2 süstemaatiline nimetus? Millisesse soolade alamklassi see kuulub? b) Mitu grammi Al 2 (S 4 ) 3 18H 2 peab laborant võtma, et valmistada soovitud kontsentratsiooniga sulfaatioonide lahus? Mitu grammi soola jääb alles? c) Mitu mooli alumiiniumsulfaati peab lahustama 0,25 dm 3 vees, et saada küllastunud Al 2 (S 4 ) 3 lahust (20 o juures)? Mitu grammi soola sadeneb välja saadud lahuse jahutamisel 5 kraadini? (10) 4. Lõhkeaine X molekulid sisaldavad elemente A (37,8%), B (16,2%), (43,2%) ja D. A on lihtaine koostises õhu peamine komponent. Elementi B leidub kõigis orgaanilistes ühendites. on levinuim element maakoores. X molaarmass on 222,1 g/mol. Aine X molekul sisaldab ainult A-A, A-B, B-D ja A- vahelisi sidemeid, kusjuures iga A aatomiga on seotud kolm teist aatomit ning molekulis on ka üks kuuest aatomist moodustunud tsükkel. Aine X lagunemist saab kirjeldada lihtsustatud reaktsioonivõrrandiga, milles on ainult kolm saadust. Kaks neist on kaheaatomilised gaasid, millest üks koosneb elemendist A ja teine elementidest B ning, ent kolmas saadus on kolmeaatomiline vedelik (n.t.). a) Leidke elementide A, B, ja D sümbolid ja nimetused. b) Leidke arvutustega i) aine X empiiriline valem ja ii) aine X molekulivalem. c) Kirjutage aine X lagunemisreaktsiooni tasakaalustatud võrrand. d) Joonistage aine X struktuurivalem. (10) 5. Täpselt pool liitrit gaasisegu (n.t.) koosnes kahest ainest: A ja B. Aine A on mittetsükliline alkaan ja seda on segus 8,93 millimooli. Aine B ei sisalda vesinikku. Gaasisegule lisati 1,857 g hapnikku, seejärel süüdati. Pärast reaktsiooni toimumist oli järele jäänud vaid kaks ainet: 0,804 g vett ja 2,16 g süsinikdioksiidi. a) Leidke arvutustega aine A brutovalem. b) Joonistage A brutovalemile vastavad võimalikud struktuurivalemid. c) Mis on aine B? d) Arvutage esialgse gaasisegu (A+B) tihedus heeliumi suhtes. (10) 6. Ninhüdriin on värvitu orgaaniline aine (struktuur toodud H joonisel), mis reageerib kergesti primaarsete amiinidega, H tekitades tumesinise värvusega produkti. Seepärast on H ninhüdriini lahused kasutusel kriminaaluuringutes H sõrmejälgede ilmutamiseks pindadel. a) Millistes inimorganismi biomakromolekulides (biopolümeerides) leidub primaarseid aminorühmi? b) Nimetage kaks põhjust, miks eelistatakse kasutada ninhüdriini lahust etanoolis või atsetoonis, mitte vees. c) Ekspert Mari kasutab sõrmejälgede ilmutamiseks lahust, mida ta saab 0,50 grammi ninhüdriini lahustamisel täpselt 100 ml etanoolis (etanooli tihedus on 0,789 g/cm 3 ). Arvutage selles lahuses ninhüdriini jaoks: i) massiprotsent, ii) molaarne kontsentratsioon, iii) moolimurd Lahuse ja lahusti tihedused on võrdsed. d) Milliseid kaitsevahendeid peab ekspert Mari kindlasti kasutama ninhüdriini lahuse pihustamisel uuritavale pinnale? (10) H H
2 2012/2013 õ.a. keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. a) Joonistage ühendi 3 H 2 Brl kõik võimalikud isomeerid. b) Süsivesiniku X molekulmass on 104. Leidke tema brutovalem ning ruumiline struktuur, kui süsivesinikus ei esine ühtegi kaksiksidet ja teda läbib kolm sümmeetriatasandit. (10) 2. Alkoholide struktuurid saadakse süsivesinikes ühe või mitme vesiniku aatomi asendamisel hüdroksüülrühmadega. Alkoholide klassi kõige lihtsamaks esindajaks on metanool, mida toodetakse süsinikmonooksiidi redutseerimisel vesinikuga katalüsaatorite juuresolekul (reaktsioon 1). Teiseks levinud alkoholide esindajaks on etanool. Etanooli peamisteks saamismeetoditeks on eteeni hüdraatimine (reaktsioon 2) ja sahhariidide kääritamine. Alkoholide hüdroksüülrühm on nõrgalt happeline ja reageerib aktiivsete metallidega (reaktsioon 3). Karboksüülhapete reaktsioonil alkoholidega tekivad estrid. a) Kirjutage metanooli ja etanooli täieliku põlemise võrrandid. b) Kirjutage ja tasakaalustage reaktsioonid 1-3. Reaktsiooni 3 korral valige alkohol ja sobiv metall ise. c) Kirjutage lõpuni ja tasakaalustage glükoosi käärimise võrrand. d) Kirjutage 3,3-dimetüülpentaanhappe ja 2-metüülpropaan-2-ooli vahelise reaktsiooni võrrand struktuurvalemitega. Andke saadusele nimetus. (8) 3. Element X on looduses üks levinumaid keemilisi elemente ning see on ühendite A-G koostises. ksiid A on värvitu gaas, mis hapnikuga ühinemisel (i) moodustab oksiidi B. Samas võib oksiid B reageerida osooniga (ii) ning moodustada oksiidi. ksiidi D lahustamisel vees (iii) tekib nõrk hape E. ksiid A happeid ei moodusta, kuid see-eest oksiid B annab veega reageerides (iv) kahe happe E ja F segu. ksiidid A ja B võivad lisaks reageerida omavahel (v) ning anda ühe eelpoolnimetatud oksiididest. Hapet F on võimalik toota ühest eelminetatud oksiidist (vi) vee ja hapniku abil. Lõpetuseks, viiendat elemendi X oksiidi G kasutatakse närvisüsteemi ergutamiseks. a) Kirjuta kõikide nimetatud ainete (A-G) valemid ja nimetused. b) Kirjuta kõik kirjeldatud reaktsioonide tasakaalustatud võrrandid (i-vi) (9,5) 4. A on pehme hall metall, mille leekreaktsioon annab tumepunase värvuse. Metalli A oksiid B on valge tahkis, mida leidub tsemendis. ksiid B tekib ka lubjakivi peamise koostisosa kuumutamisel üle 825 ( reaktsioon 1). Veega reageerides tekib B-st alus D (reaktsioon 2). D reaktsioonil gaasilise lihtainega E 2 tekib 2 metalli A soola F (E oksüdatsiooniaste on I) ja G (E o.a on I) ning vesi (reaktsioon 3). E 2 on õhust 2,45 korda raskem gaas. F on kasutusel valgendi ja desinfektandina. Lisades F-le tugevat hapet H (sisaldab E-d), tekib taas sool G, vesi ning eraldub gaas E 2 (reaktsioon 4). a) Kirjutage i) ainete A-H valemid ja nimetused; ii) B, D ja H triviaalsed nimetused b) Kirjutage ja tasakaalustage reaktsioonid 1-4 (9,5) 5. Metanogeenid on mikroorganismid, mis saavad elutegevuseks vajaliku energia ensüümkatalüütilistest reaktsioonidest, mille saaduseks on metaan: 2 + 4H 2 = H 4 + 2H 2 H 3 H = H Metanogeene leidub mäletsejate soolestikus, näiteks lehm võib ööpäevas emiteerida 200 liitrit metaani. Metanogeenid elavad arvatavasti ka tuldpurskavate lohede seedesüsteemis. Lohe organismis on spetsiaalne metaanipõieke, kuhu kogunenud gaasi väljapaiskamine ja süütamine põhjustabki tulepurske. a) Märkida, millised elemendid metaani tekkereaktsioonides on redutseerijad ja millised oksüdeerijad. b) Arvutada metaani tekkereaktsioonide entalpiamuudud, kui vee tekkeentalpia on -286 kj/mol, metaani põlemisentalpia -890 kj/mol ja etaanhappe põlemisentalpia -875 kj/mol. c) Kirjutada metaani põlemisreaktsiooni võrrand ja arvutada 200 l metaani (25, R = 8,314 J mol -1 K -1 ) põlemisel eralduv soojushulk. d) Kas sama hulga (moolide) metanooli põlemisel eraldub suurem või väiksem energiahulk võrreldes metaaniga? (12) 6. Fenool ( 6 H 5 H) on vesilahustes nõrk hape ning püridiin ( 5 H 5 N) on nõrk alus. Fenooli dissotsiatsioonireaktsiooni jaoks on tasakaalukonstant K a = 1, (reaktsioon 1) ning püridiini ja vesinikiooni vahelise reaktsiooni jaoks on tasakaalukonstant K b = 1, (reaktsioon 2). a) Kirjutage reaktsioonide 1 ja 2 avaldised ning neile vastavate tasakaalukonstantide avaldised. b) Kirjutage püridiini ja fenooli vahelise reaktsiooni võrrand ning seda reaktsiooni kirjeldava tasakaalukonstandi avaldis. c) Leidke püridiini ja fenooli vahelise reaktsiooni tasakaalukonstandi väärtus. d) 9,4 g fenooli lahustamisel 1 liitris vees saadakse nõrgalt happeline lahus. Leidke lahuse ph väärtus! e) See lahus segatakse 1 liitri 0,1 M püridiini lahusega. Leidke saadud lahuses püridiiniumiooni ( 5 H 5 NH + ) ja fenolaatiooni ( 6 H 5 - ) sisaldus. Eeldada, et lahuste segamise ruumalaefekti ei esine. (11)
3 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 11. klass 1. a) Milline element moodustab iseendaga ja oma vasaku ning parema naabriga perioodilisustabelis ühendeid, kus esineb kümnes erinevas oksüdatsiooniastmes? b) Kirjutage vastavate ainete struktuurvalemid ja nimed. Ainetes võivad olla esindatud kõigi kolme elemendi aatomid. (9) 2. Haloperidool on tuntud ravim psüühikahäirete ravis. Seda kasutatakse ka narkootikumide võõrutusravis. Selle aine sünteesi ühte lähteainet saadakse järgmise skeemi alusel: D 2 l 2, All 3 A KMn 4 MgBr E + 2 HBr + H 3 H - Hl, - S 2 D B + Sl 2 - Hl benzoüül peroksiid F NH 3-2 HBr G Selle skeemi lahendamiseks on antud alljärgnealt rida vihjeid: 1 H-NMR andmed aine A jaoks: s(3h) δ = 2.35 ppm, d(2h) 6.95 ppm, d(2h) 7.2 ppm. B brutovalem on 7 H 5 l 2. D elemendiline koostis on: M = 170,5; 56,3%, 4,11% H, 20,8% l, ülejäänud on. etapp D E: Grignardi reaktsioon 2 mol etenüülmagneesiumbromiidiga etapp E F: 2 mooli HBr liitumine anti-markovnikov i järgi F brutovalem: 11 H 13 Br 2 l etapp F G: tsüklisatsioon NH 3 -ga, mis annab piperidiini derivaadi. a) Kirjutage A-G struktuurvalemid. b) Miks kasutatakse etapis E-F bensoüülperoksiidi? c) Joonistage produkti struktuurvalem, mis oleks tekkinud etapis E-F ilma bensoüülperoksiidita. d) Milliste omadustega peab olema etapis D E kasutatav lahusti? (8) aastatel võeti insener Thomas Midgely eestvedamisel bensiini oktaaniarvu tõstmiseks kasutusele ühend A (M = 323,4 g/mol, sisaldab 64,1% elementi X, 29,7% elementi Y ja 6,2% elementi Z). Ühendi A mürgisus põhjustas arvukalt haigestumis- ja surmajuhtumeid sellega kokku puutunud tööliste seas, ent aine ohtlikkust üritati varjata. Kuna aine A kasutamine viis ülemaailmse neurotoksilise elemendi X reostuseni ning ühtlasi mürgitas ka autode katalüütilisi konvertereid, on A kasutamine kütustes alates 20. sajandi lõpust keelatud. Aine A tööstuslikuks sünteesiks kasutatakse kolme elementi sisaldavat ainet B (37,2% Y ja 7,8% Z) ning metalli X sulamit naatriumiga, kusjuures kõrvalproduktidena eralduvad metalliline X ning Na-sool. Laboratoorselt on ühendit A võimalik valmistada ühendi B reaktsioonil Mg ja metalliga X dietüüleetris. Kõrge temperatuuri mõjul aine A laguneb. Esimese lagunemise etapi järel tekivad radikaalid ja D. Edasistel reaktsioonidel laguneb ja annab mitmete etappide järel metalli X. Arvatakse, et metalli oksüdeerumisel moodustunud oksiid E põhjustab kütuse plahvatuskindluse kasvu, reageerides mõnede põlemises osalevate radikaalidega. E reageerib radikaaliga F (3,1% Z), andes ühendi G ja radikaali H (5,9% Z). H liitumisel oksiidiga E tekib ühend I, mis omakorda H radikaaliga reageerides moodustab G ja vesi. G redutseerimisel tekib uuesti ühend E. a) Kirjutage elementide X, Y ja Z sümbolid ning ainete A I valemid. b) Kirjutage järgnevate reaktsioonide tasakaalustatud võrrandid: i) NaX + B A + X +...; ii) B + X + Mg A +...; iii) A + D; iv) E + F G + H; v) H + E I; vi) I + H H 2 + G c) Kaks D molekuli võivad omavahel reageerides anda kahe erineva reaktsiooni kaudu stabiilseid produkte. Kirjutage nende võimalike reaktsioonide võrrandid. d) Thomas Midgley teine oluline avastus, mis seisnes uut tüüpi ühendite kasutuselevõtus külmutusseadmetes, põhjustas samuti ulatusliku keskkonnaprobleemi atmosfääris. Milliste ühenditega oli tegu? (10) 4. Paaris ja paaritu -aatomite arvuga karboksüülhapete looduslik kättesaadavus ei ole võrdne. Näiteks kaprüülhapet (8) saab kookoseõlist, aga ühe süsiniku võrra lühema ahelaga hapet nii palju looduses ei leidu. Selle sünteesiks saab kasutada Barbier-Wieland i alifaatsete hapete degradatsiooni meetodit, mis on näidatud skeemil. Hargnemata ahelaga hape F sisaldab 24,6%. r 3 põhjustab kordse sideme oksüdatiivse lõhestumise (mõlemas ühendis F ja G süsiniku oksüdatsiooniaste kasvab maksimaalselt, ühendis G on 8,8% ). a) Leidke ühendi F struktuur. b) Kirjutage i) ühendite A-G struktuurivalemid ja ii) ühendite A, D, F ja G süstemaatilised nimetused. (12) 5. Ühed tähtsamad metallorgaanilised ühendid on Grignardi reagendid, mille üldvalem on R-Mg-X (tegelik struktuur on keerulisem). Nimetus tuleneb
4 reagendi avastaja nimest. Victor Grignard ( ) oli prantsuse keemik, kes sai selliste magneesiumorgaaniliste reagentide avastamise eest aastal Nobeli preemia. Grignardi reagentide tegemisel peab olema väga tähelepanelik, kuna reagent ise on päris tugev alus ja seetõttu valmistatakse see vahetult enne tema kasutamist ning sageli viiakse järgnev reaktsioon läbi samas kolvis, kus ta sünteesiti. a) i) Kirjutage reaktsioonivõrrand H 3 H 2 MgBr saamiseks. ii) Kas reaktsiooni peaks läbi viima inertses keskkonnas? Põhjendage. b) Grignardi reagendid reageerivad hästi karbonüülsete süsinikega. Kirjutage välja atsetooni karbonüülsele süsinikule liitumise reaktsiooni mehhanism H 3 H 2 MgBr näitel. c) Mida on vaja reaktsioonisegule lisada, et saada kätte stabiilne lõppsaadus? Mis juhtuks siis, kui viimane samm teha kohe pärast Grignardi reagendi tekkimist? (Kirjutage reaktsioonivõrrand) d) Milline produkt tekiks, kui kuivale jääle lisada antud Grignardi reagendi lahust? (10) 6. a) 0,247 grammi puhta alkaani põlemisel tekkinud gaasid juhiti 100 ml 5%- lisse Ba(H) 2 lahusesse. Tekkinud valge sade filtreeriti ja kuivatati ning selle massiks mõõdeti 3,356 grammi. b) Kolme järjestikuse süsinike arvuga gaasilise alkeeni (s.t. süsinike arv erineb ühe võrra) ekvimolaarse segu põlemisel tekkinud 2 ruumala oli kolm korda suurem esialgsest gaaside segu ruumalast. i) Millised alkeenid olid segus? ii) Leia segu massiprotsendiline koostis. (11)
5 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 12. klass 1. Massispektromeetrias mõõdetakse uuritavate ioonide massi ja laengu suhet. Hea spektrilahutuse korral on võimalik eristada erineva isotoopkoostisega ioone. Elektronionisatsioonil tekkib bromobenseenist elektroni väljalöömisel 6 H 5 Br +. Looduslikud broomi, süsiniku ja vesiniku isotoopkoostised on järgmised: Br: 50,7% 79 Br ja 49,3% 81 Br; : 98,9% 12 ja 1,1% 13 ; H: 99,99% 1 H ja 0,01% 2 H. a) Kui paljude erinevate isotoopkoostistega ioone võib ionisatsioonil bromobenseenist tekkida (erinevaid geomeetrilisi asendeid mitte arvesse võtta)? b) Millised neli isotoopkoostisega iooni on kõige suuremas hulgas, kui analüüsiks võetud bromobenseenis vastab kõikide elementide isotoopkoostis looduslikule? (10) 2. Fiibrilistest polümeeridest on kõige levinumad nailonid: NH nailon-6,6 Nailon-6,6 sünteesi skeem on järgmine: A + 2 H H ul/nh 4 l B H 2 /Ni 1. Ph 3 PBr 2 2. KN taandamine G NH F n 0,3% H 3 P H 2 hüdrolüüs H D E nailon-6 Na 3 P H 2 NH n Ühendite G ja H polükondensatsioonil moodustub nailon-6,6. Ühendist on võimalik saada tsükliline eeter D, mida sageli kasutatakse lahustina. Ühend E on sünteetilise kautšuki lähteaineks. n veel teada, et ühendi A trimerisatsioonil moodustub benseen. 2,00 g ühendi lahus 100 grammis vees külmub 0,413 juures [K kr (H 2 ) = 1,86 K kg/mol]. Ühendis on 53,3% süsinikku ja 11,2% vesinikku. Ühendis F on süsinikku 66,7%. Ph 3 PBr 2 on bromeeriv reagent. a) Arvutage ühendi brutovalem. b) Joonistage ühendite A - H graafilised valemid. Nailon-6 võib saada ühendi J polümerisatsioonil. Ühend J saadakse tsükloheksanooni töötlemisel hüdroksüülamiiniga, mille tulemusena tekib ühend I ( 6 H 11 N). Ühendi I töötlemisel ooleumis moodustub laktaam J ( 6 H 11 N). c) Joonistage ühendite I ja J graafilised valemid. d) Joonistage graafilised valemid saadustest, mis tekivad aine E reageerimisel Br 2 -ga tetraklorometaanis. (10) 3. Lähenevale suusamaratonile mõeldes otsustas Juku välja arvutada, millisel kujul on kõige otstarbekam 63 kilomeetri läbimiseks energiavarusid kaasas kanda. a) i) Arvutage süsivesikute (glükoos), ii) rasvade (heksadekaanhape) ja iii) valkude (alaniin) põlemisentalpia (MJ/kg). Heksadekaanhape: H 0 f = -848 kj/mol ja S 0 = 452 J/(mol K); Glükoos: H 0 f = kj/mol ja S 0 = 209 J/(mol K); Alaniin ( 3 H 7 N 2 ) H 0 f= -560 kj/mol ja S 0 = 119 J/(mol K); 2 : H 0 f( 2 ) = -394 kj/mol ja S 0 = 214 J/(mol K); H 2 : H 0 f = -286 kj/mol ja S 0 = 189 J/(mol K). b) i) Kui palju kulus energiat, kui 5,5 h jooksul arendas Juku võimsust 200 W (kasutegur 24 %)? Kui palju tuleks kaasa võtta ii) saiapätse (320 g, 60% süsivesikuid), iii) seapekki või iv) tailiha? Eeldada, et süsivesikud on ainult glükoosi, rasv heksadekaanhappe ja tailiha alaniini kujul. lla või mitte olla, mõtles Juku (pärast suusamaratoni) ja arvutas enda täieliku oksüdeerumise standardne entroopia muut S 0 ning tasakaalukonstandi K. c) Arvutage reaktsiooni Juku H 2 i) S 0, ii) H 0, iii) G 0 ja iv) K kui 75 kg kaaluv Juku sisaldab ligikaudu 12% rasva, 20% valku ja 0,4 % süsivesikuid. v) Miks ei põle Juku iseeneslikult ära? (10) G 0 = H 0 T S 0 = -RTlnK 4. Linalool on looduslik terpeen, mida leidub näiteks sidrunis, viinamarjas ja apelsiniõlis. Linalooli kasutatakse laialdaselt parfümeeriatoodete valmistamisel. Ainet saab sünteesida järgmise skeemi järgi: H Et HBr (48%) EtNa/EtH A B NaH/H 2 Hl/H 2, t - 2 D linalool Mg Br E F H+ /H 2 a) Kirjutage ühendite А-F stuktuurvalemid. b) Kirjutage ühendi A tekkereaktsiooni mehhanism. с) Millise kuulsa keemiku nimega on nimetatud ühendite klass, kuhu kuulub Е? (10) 5. Lahendage toodud reaktsioonide ahelad. n teada, et aine Z 1.00 mol lagunemisel tekib 35,5 l (n.t.) gaasilist ainet Y. Ained A ja E on nõrgad alused; ained X ja Y on lihtained. Na N 2 Hl E A B D Z E + Y + A p, t H 2 2 Nal X + Y A E (NH 2 ) 2 Fe 3 4 NaH H
6 a) Kirjutage ainete A-E, X, Y ja Z valemid ja nimetused. b) Kirjutage kõikide reaktsioonide võrrandid. (10) 6. Üks tudeng uuris Saksamaal siirdemetallide poolt katalüüsitavaid reaktsioone. Siirdemetallide ühendite kõrge hinna tõttu tuli tal neid ise valmistada. Selleks võttis ta kollase värvusega metalli X, mis ei lahustu tavapärastes hapetes. Seega lahustas ta selle Hl ja HN 3 segus, tekkis ühend A ning eraldus diatomaarne gaas B. X reageerib gaasiga (tihedus õhu suhtes 2,45), Hl vesilahuses, andes taas ühendi A. A reaktsioonil 2 molekuli dimetüülsulfiidiga vee juuresolekul (ühe väävliaatomi oksüdatsiooniaste muutub 2 võrra suuremaks), tekib ühend D, mille komplekskatioon sisaldab nii väävlit kui ka 76,06% metalli X. Lisaks tekib 1 mol aine A kohta 1 mol orgaanilises keemias tuntud lahustit ning 3 mol ühte levinud anorgaanilist hapet. Ühend D on metalli X kompleksühendite sünteesi levinuim lähteaine, kuna ligandasendusreaktsioonid toimuvad väga kiiresti. Selleks, et saada vajalikku kompleksühendit E, oli tudengil tarvis sooritada veel reaktsioon trifenüülfosfaaniga ( 6 H 5 ) 3 P. Kuna tudeng oli väsinud, otsustas ta selle reaktsiooni järgmisel päeval sooritada ning jättis aine D lahusesse ööseks seisma. Hommikul aga avastas ta, et aine D lahuses oli kollane sade ning kõik reaktsioonid tuli uuesti teha. a) Arvutage molaarmass ning kirjutage valem ja nimetus. b) Kirjutage metalli X ja gaasi B nimetused. c) Kirjutage mainitud reaktsioonide võrrandid. (10)
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass
 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
( ) ( ) 2008/2009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
Keemiliste elementide perioodilisustabel
 Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
=217 kj/mol (1) m Ühe mooli glükoosi sünteesil lihtainetest vabaneb footoneid: Δ H f, glükoos n (glükoos) =5,89 mol (1) E (footon)
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
Vektorid II. Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale
 Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
b) Täpne arvutus (aktiivsete kontsentratsioonide kaudu) ph arvutused I tugevad happed ja alused
 ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
IChO 2014, ülesanne 4
 IChO 2014, ülesanne 4 Zeise sool, K[PtCl3C2H4], oli üks esimesi metallorgaanilisi ühendeid. Kopenhaageni ülikooli professor W. C. Zeise valmistas selle ühendi lisades PtCl4-le keevas etanoolis kaaliumkloriidi
IChO 2014, ülesanne 4 Zeise sool, K[PtCl3C2H4], oli üks esimesi metallorgaanilisi ühendeid. Kopenhaageni ülikooli professor W. C. Zeise valmistas selle ühendi lisades PtCl4-le keevas etanoolis kaaliumkloriidi
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
ETTEVALMISTUS KEEMIAOLÜMPIAADIKS II
 ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
32. Rahvusvaheline keemiaolümpiaad
 32. Rahvusvaheline keemiaolümpiaad Kopenhaagen Neljapäeval, 6. juulil 2000 TERIAVR TÄELEPANU! Kirjutage iga probleemi esimese lehe ülemisse nurka oma nimi ja kood. Sama probleemi järgnevatele lehtedele
32. Rahvusvaheline keemiaolümpiaad Kopenhaagen Neljapäeval, 6. juulil 2000 TERIAVR TÄELEPANU! Kirjutage iga probleemi esimese lehe ülemisse nurka oma nimi ja kood. Sama probleemi järgnevatele lehtedele
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
ORGAANILINE KEEMIA. Lühikonspekt gümnaasiumile. Koostaja: Kert Martma
 ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Funktsiooni diferentsiaal
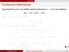 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
5. a) ρ (g/cm 3 ) = 0,119 = 11,9% 12% 2 p
 201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
ORGAANILINE KEEMIA I osa
 ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
ORGAANILINE KEEMIA. Lühikonspekt gümnaasiumile. Koostaja: Kert Martma
 ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Sisukord Sissejuhatus orgaanilisse keemiasse Alkaanid Halogeeniühendid Alkoholid Amiinid Küllastamata ühendid Areenid
ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Sisukord Sissejuhatus orgaanilisse keemiasse Alkaanid Halogeeniühendid Alkoholid Amiinid Küllastamata ühendid Areenid
Sissejuhatus. 44 th IChO Teoreetiline voor. Ametlikeesti keelne version.
 Sissejuhatus Kirjutage oma nimi ja kood igale vihiku leheküljele. Teoreeiline voor koosneb 8 ülesandest ja perioodilisustabelist, kokku 49 leheküljel. Teoreetilise vooru lahendamiseks on aega 5 tundi.
Sissejuhatus Kirjutage oma nimi ja kood igale vihiku leheküljele. Teoreeiline voor koosneb 8 ülesandest ja perioodilisustabelist, kokku 49 leheküljel. Teoreetilise vooru lahendamiseks on aega 5 tundi.
Graafiteooria üldmõisteid. Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid
 Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Lokaalsed ekstreemumid
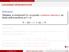 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
KEEMIA ÜLESANNETE LAHENDAMINE II
 KEEMIA ÜLESANNETE LAHENDAMINE II ÜLESANDED JA LAHENDUSED Ülesanne 1 Ülesanne Ülesanne Vana münt diameetria, cm ja paksusea,0 mm on tehtud puhtast kullast (ρ = 1900 k m ). Kulla hind on 410$ ühe untsi eest
KEEMIA ÜLESANNETE LAHENDAMINE II ÜLESANDED JA LAHENDUSED Ülesanne 1 Ülesanne Ülesanne Vana münt diameetria, cm ja paksusea,0 mm on tehtud puhtast kullast (ρ = 1900 k m ). Kulla hind on 410$ ühe untsi eest
Kontekstivabad keeled
 Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
ORGAANILINE KEEMIA ANDRES TALVARI
 ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
p A...p D - gaasiliste ainete A...D osarõhud, atm K p ja K c vahel kehtib seos
 LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
24. Balti keemiaolümpiaad. Teooriavoor. 9. aprill 2016 Tartu, Eesti
 24. Balti keemiaolümpiaad Teooriavoor 9. aprill 2016 Tartu, Eesti Juhised Kirjutage oma nimi ja kood igale lehele. Teil on ülesannete lahendamiseks 5 tundi. Alustage alles siis, kui on antud START märguanne.
24. Balti keemiaolümpiaad Teooriavoor 9. aprill 2016 Tartu, Eesti Juhised Kirjutage oma nimi ja kood igale lehele. Teil on ülesannete lahendamiseks 5 tundi. Alustage alles siis, kui on antud START märguanne.
ELUKS OLULISED SÜSINIKÜHENDID
 Koostanud: Martin Saar 2012 Ülesanne nr 1 A. Katt, Saar Keemia töövihik 9. klassile Sahhariide nimetatakse ka süsivesikuteks (vene keeles углево ды, saksa keeles Kohlenhydrate, inglise keeles carbohydrate).
Koostanud: Martin Saar 2012 Ülesanne nr 1 A. Katt, Saar Keemia töövihik 9. klassile Sahhariide nimetatakse ka süsivesikuteks (vene keeles углево ды, saksa keeles Kohlenhydrate, inglise keeles carbohydrate).
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat
 Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
CaCO 3(s) --> CaO(s) + CO 2(g) H = kj. Näide
 3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks
 4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
HSM TT 1578 EST 6720 611 954 EE (04.08) RBLV 4682-00.1/G
 HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
HULGATEOORIA ELEMENTE
 HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
Kehade soojendamisel või jahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks.
 KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika
 Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut
 Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
HAPNIKUTARBE INHIBEERIMISE TEST
 HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
Andmeanalüüs molekulaarbioloogias
 Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
Eesti koolinoorte XLIX täppisteaduste olümpiaad
 Eesti koolinoorte XLIX täppisteaduste olümpiaad MATEMAATIKA PIIRKONDLIK VOOR 26. jaanuaril 2002. a. Juhised lahenduste hindamiseks Lp. hindaja! 1. Juhime Teie tähelepanu sellele, et alljärgnevas on 7.
Eesti koolinoorte XLIX täppisteaduste olümpiaad MATEMAATIKA PIIRKONDLIK VOOR 26. jaanuaril 2002. a. Juhised lahenduste hindamiseks Lp. hindaja! 1. Juhime Teie tähelepanu sellele, et alljärgnevas on 7.
Biomakromolekulid: struktuurist omadusteni. Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018
 Biomakromolekulid: struktuurist omadusteni Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018 Sissejuhatus 2 Biokeemia mõõtkava mm mm Inimese embrüo (6. nädal): 4 mm Suurem amööb: 0.8 mm Inimese punaverelible:
Biomakromolekulid: struktuurist omadusteni Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018 Sissejuhatus 2 Biokeemia mõõtkava mm mm Inimese embrüo (6. nädal): 4 mm Suurem amööb: 0.8 mm Inimese punaverelible:
RF võimendite parameetrid
 RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
3. Solvendiefektide mõju ainete omadustele ja keemilistele protsessidele. 3.1 Solvendiefektid happe-aluse protsessidele. Tasakaal ja kiirus
 3. olvendiefektide mõju ainete omadustele ja keemilistele protsessidele Põhiallikas: Tasakaal ja kiirus Lahusti mõju tasakaalule ilmneb seeläbi, et erinevad lahustid solvateerivad erineva intensiivsusega
3. olvendiefektide mõju ainete omadustele ja keemilistele protsessidele Põhiallikas: Tasakaal ja kiirus Lahusti mõju tasakaalule ilmneb seeläbi, et erinevad lahustid solvateerivad erineva intensiivsusega
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi
 Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
SÜSIVESINIKUD. Kaido Viht
 SÜSIVSINIKUD Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2016 Süsivesinike struktuurid Käesolevas materjalis selgitame mõningaid süsivesinikele iseloomulikke reaktsioone. Süsivesinikud, nagu
SÜSIVSINIKUD Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2016 Süsivesinike struktuurid Käesolevas materjalis selgitame mõningaid süsivesinikele iseloomulikke reaktsioone. Süsivesinikud, nagu
FUNKTSIONAALSED RÜHMAD I osa. Kaido Viht
 FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
1998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
FUNKTSIONAALSED RÜHMAD. II OSA
 TATU ÜLIKL TEADUSKL TÄIENDAVAID TEEMASID KLIKEEMIALE III FUNKTSINAALSED ÜHMAD. II SA Heiki Timotheus Õppevahend TK õpilastele Tartu 2007 Funktsionaalsed rühmad. II osa Karboksüülhappeid ja nende derivaate
TATU ÜLIKL TEADUSKL TÄIENDAVAID TEEMASID KLIKEEMIALE III FUNKTSINAALSED ÜHMAD. II SA Heiki Timotheus Õppevahend TK õpilastele Tartu 2007 Funktsionaalsed rühmad. II osa Karboksüülhappeid ja nende derivaate
Teaduskool. Alalisvooluringid. Koostanud Kaljo Schults
 TARTU ÜLIKOOL Teaduskool Alalisvooluringid Koostanud Kaljo Schults Tartu 2008 Eessõna Käesoleva õppevahendi kasutajana on mõeldud eelkõige täppisteaduste vastu huvi tundvaid gümnaasiumi õpilasi, kes on
TARTU ÜLIKOOL Teaduskool Alalisvooluringid Koostanud Kaljo Schults Tartu 2008 Eessõna Käesoleva õppevahendi kasutajana on mõeldud eelkõige täppisteaduste vastu huvi tundvaid gümnaasiumi õpilasi, kes on
ORGAANILISE KEEMIA LABORIJUHEND ABISTAV MATERJAL
 TALLINNA ÜLIKL Matemaatika ja Loodusteaduste Instituut RGAANILISE KEEMIA LABRIJUEND ABISTAV MATERJAL Marju Robal ja Rando Tuvikene Tallinn 2008 SISUKRD 1. RGAANILISTE AINETE LAUSTUVUS JA LAUSTAMISVÕIME...3
TALLINNA ÜLIKL Matemaatika ja Loodusteaduste Instituut RGAANILISE KEEMIA LABRIJUEND ABISTAV MATERJAL Marju Robal ja Rando Tuvikene Tallinn 2008 SISUKRD 1. RGAANILISTE AINETE LAUSTUVUS JA LAUSTAMISVÕIME...3
Sissejuhatus mehhatroonikasse MHK0120
 Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
STM A ++ A + A B C D E F G A B C D E F G. kw kw /2013
 Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
AATOMI EHITUS KEEMILINE SIDE
 TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
2005/2006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. = 52,5 g/mol
 005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
KARBOKSÜÜLHAPPED. Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COOH). Üldvalem R-COOH või HOOC-R
 KARBOKSÜÜLAPPED Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COO). Üldvalem R-COO või OOC-R Karboksüülhapete nimetused tuletatakse süsivesinike nimetustest ja
KARBOKSÜÜLAPPED Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COO). Üldvalem R-COO või OOC-R Karboksüülhapete nimetused tuletatakse süsivesinike nimetustest ja
2.2.1 Geomeetriline interpretatsioon
 2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
Compress 6000 LW Bosch Compress LW C 35 C A ++ A + A B C D E F G. db kw kw /2013
 55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
TÄIENDAVAID TEEMASID KOOLIKEEMIALE III
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
,millest avaldub 21) 23)
 II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
Ecophon Line LED. Süsteemi info. Mõõdud, mm 1200x x x600 T24 Paksus (t) M329, M330, M331. Paigaldusjoonis M397 M397
 Ecophon Line LED Ecophon Line on täisintegreeritud süvistatud valgusti. Kokkusobiv erinevate Focus-laesüsteemidega. Valgusti, mida sobib kasutada erinevates ruumides: avatud planeeringuga kontorites; vahekäigus
Ecophon Line LED Ecophon Line on täisintegreeritud süvistatud valgusti. Kokkusobiv erinevate Focus-laesüsteemidega. Valgusti, mida sobib kasutada erinevates ruumides: avatud planeeringuga kontorites; vahekäigus
DEF. Kolmnurgaks nim hulknurka, millel on 3 tippu. / Kolmnurgaks nim tasandi osa, mida piiravad kolme erinevat punkti ühendavad lõigud.
 Kolmnurk 1 KOLMNURK DEF. Kolmnurgaks nim hulknurka, millel on 3 tippu. / Kolmnurgaks nim tasandi osa, mida piiravad kolme erinevat punkti ühendavad lõigud. Kolmnurga tippe tähistatakse nagu punkte ikka
Kolmnurk 1 KOLMNURK DEF. Kolmnurgaks nim hulknurka, millel on 3 tippu. / Kolmnurgaks nim tasandi osa, mida piiravad kolme erinevat punkti ühendavad lõigud. Kolmnurga tippe tähistatakse nagu punkte ikka
Molekulid ei esine üksikuna vaid suurearvuliste kogumitena.
 2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
Koduseid ülesandeid IMO 2017 Eesti võistkonna kandidaatidele vol 4 lahendused
 Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Jätkusuutlikud isolatsioonilahendused. U-arvude koondtabel. VÄLISSEIN - COLUMBIA TÄISVALATUD ÕÕNESPLOKK 190 mm + SOOJUSTUS + KROHV
 U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
Energiabilanss netoenergiavajadus
 Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD
 KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 2016
 Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Ecophon Square 43 LED
 Ecophon Square 43 LED Ecophon Square 43 on täisintegreeritud süvistatud valgusti, saadaval Dg, Ds, E ja Ez servaga toodetele. Loodud kokkusobima Akutex FT pinnakattega Ecophoni laeplaatidega. Valgusti,
Ecophon Square 43 LED Ecophon Square 43 on täisintegreeritud süvistatud valgusti, saadaval Dg, Ds, E ja Ez servaga toodetele. Loodud kokkusobima Akutex FT pinnakattega Ecophoni laeplaatidega. Valgusti,
Aritmeetilised ja loogilised operaatorid. Vektor- ja maatriksoperaatorid
 Marek Kolk, Tartu Ülikool Viimati muudetud : 6.. Aritmeetilised ja loogilised operaatorid. Vektor- ja maatriksoperaatorid Aritmeetilised operaatorid Need leiab paletilt "Calculator" ja ei vaja eraldi kommenteerimist.
Marek Kolk, Tartu Ülikool Viimati muudetud : 6.. Aritmeetilised ja loogilised operaatorid. Vektor- ja maatriksoperaatorid Aritmeetilised operaatorid Need leiab paletilt "Calculator" ja ei vaja eraldi kommenteerimist.
[0001] Käesoleva patenditaotlusega taotletakse prioriteetsust USA eeltaotluse nr 60/ suhtes, mis esitati 11. detsembril 2002.
![[0001] Käesoleva patenditaotlusega taotletakse prioriteetsust USA eeltaotluse nr 60/ suhtes, mis esitati 11. detsembril 2002. [0001] Käesoleva patenditaotlusega taotletakse prioriteetsust USA eeltaotluse nr 60/ suhtes, mis esitati 11. detsembril 2002.](/thumbs/63/48683882.jpg) SEOTUD PATENDITAOTLUSED [0001] Käesoleva patenditaotlusega taotletakse prioriteetsust USA eeltaotluse nr 60/432 49 suhtes, mis esitati 11. detsembril 02. LEIUTISE TAUST [0002] Entekaviir, [1S-(1α, 3α,
SEOTUD PATENDITAOTLUSED [0001] Käesoleva patenditaotlusega taotletakse prioriteetsust USA eeltaotluse nr 60/432 49 suhtes, mis esitati 11. detsembril 02. LEIUTISE TAUST [0002] Entekaviir, [1S-(1α, 3α,
3. LOENDAMISE JA KOMBINATOORIKA ELEMENTE
 3. LOENDAMISE JA KOMBINATOORIKA ELEMENTE 3.1. Loendamise põhireeglid Kombinatoorika on diskreetse matemaatika osa, mis uurib probleeme, kus on tegemist kas diskreetse hulga mingis mõttes eristatavate osahulkadega
3. LOENDAMISE JA KOMBINATOORIKA ELEMENTE 3.1. Loendamise põhireeglid Kombinatoorika on diskreetse matemaatika osa, mis uurib probleeme, kus on tegemist kas diskreetse hulga mingis mõttes eristatavate osahulkadega
REAKTSIOONIKINEETIKA
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
ALGEBRA I. Kevad Lektor: Valdis Laan
 ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
MATEMAATIKA AJALUGU MTMM MTMM
 Õppejõud: vanemteadur Mart Abel Õppejõud: vanemteadur Mart Abel Loenguid: 14 Õppejõud: vanemteadur Mart Abel Loenguid: 14 Seminare: 2 Õppejõud: vanemteadur Mart Abel Loenguid: 14 Seminare: 2 Hindamine:
Õppejõud: vanemteadur Mart Abel Õppejõud: vanemteadur Mart Abel Loenguid: 14 Õppejõud: vanemteadur Mart Abel Loenguid: 14 Seminare: 2 Õppejõud: vanemteadur Mart Abel Loenguid: 14 Seminare: 2 Hindamine:
PÕLEVAINETE OMADUSED. Andres Talvari
 PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
PLASTSED DEFORMATSIOONID
 PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
1.1. NATURAAL-, TÄIS- JA RATSIONAALARVUD
 1. Reaalarvud 1.1. NATURAAL-, TÄIS- JA RATSIONAALARVUD Arvu mõiste hakkas kujunema aastatuhandeid tagasi, täiustudes ja üldistudes koos inimkonna arenguga. Juba ürgühiskonnas tekkis vajadus teatavaid hulki
1. Reaalarvud 1.1. NATURAAL-, TÄIS- JA RATSIONAALARVUD Arvu mõiste hakkas kujunema aastatuhandeid tagasi, täiustudes ja üldistudes koos inimkonna arenguga. Juba ürgühiskonnas tekkis vajadus teatavaid hulki
sin 2 α + cos 2 sin cos cos 2α = cos² - sin² tan 2α =
 KORDAMINE RIIGIEKSAMIKS III TRIGONOMEETRIA ) põhiseosed sin α + cos sin cos α =, tanα =, cotα =, cos sin + tan =, tanα cotα = cos ) trigonomeetriliste funktsioonide täpsed väärtused α 5 6 9 sin α cos α
KORDAMINE RIIGIEKSAMIKS III TRIGONOMEETRIA ) põhiseosed sin α + cos sin cos α =, tanα =, cotα =, cos sin + tan =, tanα cotα = cos ) trigonomeetriliste funktsioonide täpsed väärtused α 5 6 9 sin α cos α
