p A...p D - gaasiliste ainete A...D osarõhud, atm K p ja K c vahel kehtib seos
|
|
|
- Γιάννης Δαγκλής
- 7 χρόνια πριν
- Προβολές:
Transcript
1 LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside näiteks on reaktsioonid, mille käigus üks reaktsioonisaadustest (gaas või sade) eraldub süsteemist 2KClO 3(s) 2KCl(s) + 3O 2(g) Vastuidises suunas see reaktsioon ei kulge. Paljud reaktsioonid on aga öörduvad, sõltuvalt tingimustest (temeratuur, ainete kontsentratsioonid, rõhk) võivad nad kulgeda nii ühes kui teises suunas. Madalamal temeratuuril kulgeb näiteks reaktsioon H 2(g) + I 2(g) 2 HI(g) kõrgemal temeratuuril aga laguneb vesinikjodiid uuesti vesinikuks ja joodiks. Seeärast märgistatakse öörduvaid reaktsioone sageli kahe vastassuunalise noolega * H 2(g) + I 2(g) 2HI(g) Kui tingimused ei muutu, saabub selliste reaktsioonide uhul mingil hetkel olukord, kus vastassuunaliste reaktsioonide kiirused saavad võrdseks, ühegi aine kontsentratsioon enam ajas ei muutu ja tekkinud segus on sõltuvalt tingimustest rohkem või vähem kõiki reaktsioonis osalevaid aineid nii lähteaineid kui saadusi. Sellist olukorda nimetatakse keemiliseks tasakaaluks. Keemiline tasakaal on nn dünaamiline tasakaal, sest rotsessid ei ole lõenud, vaid nad kulgevad vastassuundades ühesuguse kiirusega. Kirjutame ühe reaktsioonivõrrandi üldkujul K d [ C] [ D] [ A] [ ] a B b = () [A]...[D] - ainete A...D kontsentratsioonid tasakaaluolekus, mol/dm 3 a, b,, ja d - koefitsiendid reaktsioonivõrrandist Tasakaalukonstant sõltub temeratuurist, kuid ei sõltu reageerivate ainete kontsentratsioonist. Tasakaalukonstanti (K ), mis on avaldatud molaarsete kontsentratsioonide kaudu kasutatakse sageli reaktsioonide korral, kus kõik ained on vesilahustes või vedelikud. Gaasiliste ainete osavõtul kulgevate reaktsioonide korral avaldatakse tasakaalukonstant tavaliselt osarõhkude kaudu (tähis K ) K C a A d D b B = (2) A... D - gaasiliste ainete A...D osarõhud, atm Kui reaktsioonis osaleb lisaks gaasidele ka tahkeid või vedelas olekus aineid, siis neid tasakaalukonstandi avaldisse ei anda, kuna tahke aine ning vedelikuiisk reageerivad vaid innalt ja ei moodusta gaasiga homogeenset segu. Nii sisaldab järgmise reaktsiooni tasakaalukonstandi avaldis vaid CO 2 osarõhku CaO(s) + CO 2(g) CaCO 3(s) K = CO2 a A + b B V V 2 C + d D K ja K vahel kehtib seos ning tähistame ärisuunalise reaktsiooni kiiruse v ning vastassuunalise reaktsiooni kiiruse v 2. Tasakaaluolekus v = v 2 Tasakaaluoleku matemaatiliseks kirjeldamiseks kasutatakse tasakaalukonstanti (K ), kusjuures molaarseid kontsentratsioone tasakaaluolekus tähistatakse sageli nurksulgudega. Meeles idada, et ikka on saaduste kontsentratsioonid (vastavates astmetes) murrujoone eal ja lähteained all K ( R T ) n = K (3) R - universaalne gaasikonstant, J/mol K T - absoluutne temeratuur, K n - gaasiliste ühendite moolide arvu muutus reaktsioonis 2CO(g) + O 2(g) 2CO 2(g) siin n = 2-3 = - Mida suurem on K või K, seda enam on tasakaalusegus saadusi, st reaktsiooni tasakaal on nihutatud aremale - saaduste tekke suunas. * Tegelikult uudub standardkirjatüüide hulgas äris õige märk, siin on kasutatud graafilist kujutist. MS Offie'i kirjatüü Wingdings 3 sisaldab märki Tasakaaluolekute arvutamisega sõltuvalt tingimustest tegeleb keemiline termodünaamika. Vastavat tarkvara kasutades (HSC, ThermoCal) saab reaktsioonist osavõtvate ainete kontsentratsioone keerulistes tasakaalusegudes üsna täselt välja arvutada. 2
2 Le Chatelier' rintsii Keemilise reaktsiooni kiirus Kuna tasakaalusegus võib olla nii lähteaineid kui saadusi, siis kuidas saavutada just saaduste võimalikult kõrge sisaldus ehk kuidas nihutada tasakaalu aremale, saaduste tekke suunas. Hinnangu võimaldab Le Chatelier' (Henry Le Chatelier, ) rintsii. Tingimuste muutmine tasakaalusüsteemis kutsub esile tasakaalu nihkumise suunas, mis aneb süsteemi avaldama vastuanu tekitatud muutustele. Tingimused, mida saab mõjutada, on eelkõige lähteainete kontsentratsioon, temeratuur ja rõhk. Vaatame ammoniaagi sünteesireaktsiooni näitel nende tingimuste muutumisest tulenevat tasakaalu nihkumist N 2(g) + 3H 2(g) 2NH 3(g) H = kj Lähteainete kontsentratsiooni suurendamine nihutab reaktsiooni tasakaalu aremale. Lähteainete kontsentratsioonide suurendamisele avaldab süsteem vastuanu sellega, et kulutab neid rohkem ära, seega tekib rohkem ammoniaaki. Temeratuuri tõstmine nihutab endotermilise (soojuse neeldumisega kulgeva) reaktsiooni tasakaalu aremale, eksotermilise reaktsiooni tasakaalu aga vasakule (lähteainete tekke suunas). Ammoniaagi süntees on eksotermiline rotsess, sest reaktsiooni käigus eraldub soojust ( H = kj). Temeratuuri tõstmisele avaldab see süsteem vastuanu sellega, et kulutab rohkem soojust. Seega hakkab kulgema vastassuunaline reaktsioon: ammoniaagi lagunemine lähteaineteks, milles soojus neeldub. Rõhu tõstmine gaasiliste ainete osavõtul kulgevates tasakaalureaktsioonides nihutab tasakaalu suunas, kus gaasiliste ainete molekulide arv väheneb. Selles rotsessis on kõik ained gaasilises olekus. Vasakul ool on kokku 4, aremal 2 mooli gaasi. Seega nihkub tasakaal aremale. Järelikult on ammoniaagi sünteesil arimateks tingimusteks lähteainete võimalikult kõrge kontsentratsioon või ka tekkiva ammoniaagi idev väljaviimine süsteemist, suhteliselt madal temeratuur ja võimalikult kõrge rõhk. Olles kindlaks teinud kõik võimalused tasakaalu mõjutamiseks, on vajalik ka, et tasakaaluolekuni jõutaks suhteliselt lühikese ajaga, st et reaktsioonikiirus oleks maksimaalne. Reaktsioonikiirus homogeenses süsteemis näitab reageerivate ainete kontsentratsioonide muutust ajaühikus (mol / dm 3 s). Eristatakse (vt joonist) keskmist kiirust ajavahemikus τ C v = τ ja kiirust mingil ajahetkel τ v τ = - tan α mis leitakse funktsiooni C = f (τ) uutuja tõusunurga tangensi õhjal. Põhitegurid, mis mõjutavad reaktsioonikiirust, oleksid järgmised: Reageerivate ainete eriära. Ained käituvad sarnastes tingimustes vägagi erinevalt. Nii näiteks reageerib väike vasetükk kontsentreeritud lämmastikhaega sekundite jooksul, nikkel aga kestval keetmisel. Reageerivate ainete kokkuuuteinna suurus. Tahkete ainete reageerimise kiirust saab oluliselt tõsta neid eenestades, vedelikke võib aga ihustada. Reageerivate ainete kontsentratsioon. Reaktsioonid on seotud osakeste kokkuõrgetega. Mida rohkem on ruumalaühikus osakesi, seda sagedamini nad kokku õrkavad. Seega suurendab lähteainete kontsentratsiooni tõstmine reaktsioonikiirust. Pärisuunalise reaktsiooni v aa + bb saadused kiirus v sõltub lähteainete kontsentratsioonist järgmiselt (nn massitoimeseadus): 3 4
3 kus = q B v k C C A (4) k q + q reaktsiooni kiiruskonstant reaktsiooni järk aine A suhtes reaktsiooni järk aine B suhtes reaktsiooni summaarne järk Mõlema lähteaine suhtes esimest järku (NB! summaarselt teist järku) reaktsiooni korral v = k C C A B ja seega sõltub sellise reaktsiooni kiirus lineaarselt (vt joonis lk. 0) ühe lähteaine kontsentratsioonist. Kiiruskonstant k ning reaktsiooni järgud olenevad reageerivate ainete eriärast ja reaktsiooni tingimustest ning määratakse ekserimentaalselt. Vaid üksikute reaktsioonide korral on järgud ja q võrdsed tasakaalustatud reaktsioonivõrrandi koefitsientidega a ja b. Temeratuur. Mida kõrgem on temeratuur, seda intensiivsem on molekulide soojusliikumine ja suurem nende kineetiline energia. See suurendab molekulide efektiivsete kokkuõrgete tõenäosust ning koos sellega reaktsioonikiirust. Temeratuuri mõju võimaldab ligikaudu hinnata van't Hoffi (Jaobus Hendrius van't Hoff, 852 9) reegel Temeratuuri tõstmine 0 C võrra suurendab reaktsioonikiirust kaks kuni neli korda. Matemaatiliselt võiks selle kirja anna järgmiselt: v t v t 2 t2 t 0 = γ (5) v t reaktsioonikiirus temeratuuril t v t2 reaktsioonikiirus temeratuuril t 2 γ reaktsiooni temeratuuritegur (γ 2 4) Kiiruse sõltuvus temeratuurist ole seega lineaarne, vaid sellist temeratuursõltuvust kirjeldab astmefunktsiooni graafik. Kui tulla tagasi ammoniaagi sünteesi näite juurde, siis mõjutab lähteainete kontsentratsiooni suurendamine soodsalt nii saagist kui reaktsioonikiirust. Temeratuuri tõstmine suurendab reaktsioonikiirust, aga vähendab saagist. Siin tuleb otimaalne temeratuur leida katseliselt. Tavaliselt viiakse ammoniaagi süntees läbi temeratuuril 500 C. Rõhu tõstmine suurendab saagist, seeärast viiakse rotsess läbi rõhul kuni 000 atm. Kiirust aitab oluliselt tõsta ka raudkatalüsaator. Katse Ainete kontsentratsiooni muutuse mõju tasakaalule Kirjutada välja tasakaalukonstandi avaldis raud(iii)kloriidi ja ammooniumtiotsüanaadi lahuste vahelisele reaktsioonile FeCl 3(aq) + 3NH 4SCN(aq) Fe(SCN) 3(aq) + 3NH 4Cl(aq) unane Hinnata, millises suunas nihkub tasakaal kui suurendada a) FeCl 3 kontsentratsiooni? b) NH 4SCN kontsentratsiooni? ) NH 4Cl kontsentratsiooni? Hinnata tasakaalukonstandi avaldise õhjal kumma aine, kas NH 4Cl või FeCl 3 kontsentratsiooni suurendamine mõjutab tasakaalu enam. Kontrollida tasakaalu nihkumist katseliselt. Selleks võtta keeduklaasi 20 ml destilleeritud vett ja lisada tilk küllastatud FeCl 3 lahust ning tilk NH 4SCN lahust. Segada hoolikalt ning jagada tekkinud unane lahus võrdsete osadena nelja katseklaasi. Lahuse unane värvus on tingitud reaktsioonil tekkivast raud(iii)tiotsüanaadist *, kus värvi intensiivsus oleneb tema kontsentratsioonist. Reaktsiooni tasakaalu nihkumist on lihtne jälgida lahuse värvuse muutumise järgi. Esimene katseklaas jätta võrdluseks Teise katseklaasi lisada kaks tilka FeCl 3 lahust. Mida võib tähele anna? Kummas suunas nihkub tasakaal? Kolmandasse katseklaasi lisada 2 tilka NH 4SCN lahust. Kummas suunas nihkub tasakaal? Kas muutus on suurem või väiksem võrreldes FeCl 3 lisamisega? Neljandasse katseklaasi lisada tahket NH 4Cl ja loksutada tugevasti Kuidas muutub lahuse värvus. Anda selgitus. Van't Hoffi reegel kehtib siiski vaid toatemeratuurile lähedastel temeratuuridel ning täsemate sõltuvuste saamiseks tuleb kasutada Arrheniuse võrrandit. Katalüsaatorite toime. Katalüsaatorid on ained, mis muudavad reaktsioonikiirust. Osaledes mingis reaktsiooni järgus, taastuvad nad reaktsiooni lõuks keemiliselt ja endises hulgas. Katalüsaatorite mõju on selektiivne: katalüsaator kiirendab ainult kindlat reaktsiooni ja sellise katalüsaatori leidmine eeldab sageli mahukaid ekserimente. * Paralleelselt tekib ka unase värvusega [FeSCN] 2+ komleks 5 6
4 Katse 2 Reaktsioonikiiruse sõltuvus lähteainete kontsentratsioonist ja temeratuurist Reaktsioonikiiruse sõltuvus Na 2S 2O 3 kontsentratsioonist Tabel Reaktiivid: %-ne Na 2S 2O 3 lahus, %-ne H 2SO 4 lahus. Töövahendid: Büretid, katseklaaside komlekt (8 tk), kummikork, esuudelid, keeduklaas, termomeeter, elektriliit. Töö käik Reaktsioonikiiruse sõltuvust reageerivate ainete kontsentratsioonist ning temeratuurist on hea vaadelda väävelhae ning naatriumtiosulfaadi vahelise reaktsiooni abil Na 2S 2O 3 + H 2SO 4 Na 2SO 4 + H 2O + SO 2 + S Selles reaktsioonis tekkiv hägune väävlisade on hõlsasti jälgitav ning suhteliselt lahjade (~ %) lahuste korral on ajavahemik lahuste kokkuvalamise hetkest kuni hägu tekkimiseni mõni minut. Töö õnnestumise eelduseks on uhtus. Katseklaasid tuleb enne töö algust esta hoolikalt kraanivee ja harjaga ning loutada 2-3 korda destilleeritud veega. Samuti toimitakse kahe katse vahel ning töö lõul. Eksida ei tohi bürettide täitmisel - õige lahus õigesse büretti. Kui mõnes büretis on hakanud tekkima hägu, tuleb bürett uhtaks esta, loutada mõned korrad lahusega, millega bürett täidetakse, ning alustada tööd otsast eale.. Reaktsioonikiiruse sõltuvus lähteainete kontsentratsioonist Kaheksa katseklaasi jagada neljaks aariks. Ühes katseklaasis igast aarist on väävelhaelahus, teises naatriumtiosulfaadilahus, mille kontsentratsioon aariti erineb. Algul täita neli katseklaasi H 2SO 4 lahusega - igasse katseklaasi 6 m 3 (6 ml). Erineva kontsentratsiooniga Na 2S 2O 3 lahused valmistada järgmiselt: ühte katseklaasi mõõta 6 m 3 Na 2S 2O 3 lahust, teise 4 m 3 Na 2S 2O 3 lahust ja 2 m 3 destilleeritud vett, kolmandasse 3 m 3 Na 2S 2O 3 lahust ja 3 m 3 vett, neljandasse 2 m 3 Na 2S 2O 3 lahust ning 4 m 3 vett. Katseklaaside aar Na 2S 2O 3 maht m 3 H 2O maht m 3 Na 2S 2O 3 suhteline kontsentratsioon Reaktsioonikiiruse sõltuvus temeratuurist Aeg τ min Reaktsioonikiirus v = /τ min - Kui katseklaasid on hoolikalt estud, võib alustada järgmist katset. Jällegi võtta neli aari katseklaase. Et neid hiljem mitte segi ajada, märgistada katseklaasid, mis sisaldavad Na 2S 2O 3 ühtmoodi, ja katseklaasid väävelhaelahusega teistmoodi. Üks katseklaas igast aarist täita 4 m 3 väävelhaelahusega, teine 4 m 3 Na 2S 2O 3 lahusega. Edasi täita oolenisti veega üks suurem keeduklaas ning asetada sinna kõik katseklaasid ning termomeeter. Siis tõsta keeduklaas koos katseklaasidega elektriliidile ning hakata jälgima temeratuuri tõusu. Katsed sooritada temeratuuridel 30 C, 40 C, 50 C ja 60 C järgnevalt: Kui temeratuur on jõudnud ~32 C-ni, tõsta keeduklaas koos katseklaasidega liidilt maha, võtta kätte esimese aari katseklaasid, valada lahused kokku, segada kiiresti ning asetada siis katseklaas koheselt sooja vette tagasi. Mõõta aeg lahuste kokkuvalamise momendist kuni hägu tekkimiseni. Seejärel võib keeduklaasi uuesti liidile asetada ning tõsta temeratuuri ~42 C-ni. Siis võtta keeduklaas taas liidilt ning korrata katset järgmise lahuste aariga. Oluline on, et hägu teket jälgitaks sooja vee sees. Vastasel juhul jahtub katseklaas kiiresti maha ning saadakse vale sõltuvus. Analoogiliselt tehakse kõik neli katset. Katsetulemused fikseerida nagu tabelis 2. Töö lõenud, esta hoolikalt katseklaasid ning korrastada töökoht. Katses mõõta aega lahuste kokkuvalamise momendist kuni hetkeni, mil lahus on muutunud häguseks. Selleks võtta esimene aar, valada lahused ühte katseklaasi kokku, sulgeda katseklaas korgiga ning segada katseklaasi kiiresti aar korda ümber öörates. Samal momendil fikseerida kella või stoeriga katse algus ning, kui tekib hägu, katse lõ. Samamoodi toimida teise, kolmanda ja neljanda aariga. Et aega kokku hoida, võib ülejäänud aarid omavahel kokku valada enam-vähem korraga, kiiresti kõik läbi segada, käivitada kell ning oodata hägu tekkimist algul teises, siis kolmandas ja lõuks neljandas aaris, milles on Na 2S 2O 3 kontsentratsioon kõige väiksem. Mõõdetud ajavahemikud fikseerida nii, nagu näidatud tabelis. 7 8
5 Reaktsioonikiiruse sõltuvus temeratuurist Tabel 2 Reaktsioonikiiruse sõltuvus Na 2S 2O 3 kontsentratsioonist Tabel 3 Katseklaaside aar Katse temeratuur t C Protokolli vormistamine Aeg τ min Reaktsioonikiirus v = /τ min -. Protokoll eab sisaldama uuritava reaktsiooni võrrandi ning korrektselt vormistatud tabelid. 2. Katsetulemuste alusel joonistada kaks graafikut, mis kirjeldavad a) reaktsioonikiiruse v sõltuvust reageerivate ainete kontsentratsioonist v = f (C) b) reaktsioonikiiruse v sõltuvust katse temeratuurist v = f (t) 3. Arvutada reaktsiooni keskmine temeratuuritegur γ k. Selleks leida van't Hoffi reegli õhjal temeratuuritegurid (γ, γ 2 ja γ 3) algul kolmele temeratuurivahemikule eraldi (vahemikud C; C ja C) ning võtta seejärel nendest keskmine. 4. Kirjutada järeldused, mis näitavad a) kuidas sõltub reaktsioonikiirus ühe lähteaine Na 2S 2O 3 kontsentratsioonist ning milline on selle reaktsiooni järk Na 2S 2O 3 suhtes b) mitu korda tõuseb antud reaktsiooni kiirus temeratuuri tõstmisel 0 C võrra Graafikute vormistamisest Alustades tabelist 3 tuleks toimida nii: Esmalt hinnata suurimad väärtused x (kontsentratsioon) ja y (kiirus) telgedel: 6,0 ja 0,66. Seejärel mõelda välja samm mõlema telje tarvis. Samm eab olema ühtlane ja ilusate numbriliste väärtustega (sõltuvalt arvude suurusest 0, 0,2 0,25 0,5 või siis 2 ja 5 või 0,0 0,02 0,025 0,05 mitte aga 0,33 0,7 vms, ei soovitata ka murdarve /2 /3 ). Mitte anna telgedele otse tabelist võetud väärtusi 0,9 0,28 0,45 jne, ealegi veel ebaühtlaste vahedega. Antud tabeli uhul sobiks x telje sammuks 2 (nullist kaheksani) ja y telje sammuks 0,2 (nullist 0,8-ni). Siiski ole alati vajalik just nullist alustada. Na 2 S 2 O 3 suhteline konts. Aeg τ min : s Aeg τ min Kiirus v min - 2,0 5:8 5,30 0,9 3,0 3:36 3,60 0,28 4,0 2:2 2,20 0,45 6,0 :30,50 0,66 Joonistada teljed, kanda telgedele ühtlaste vahedega jaotused, kirjutada jaotuste juurde numbrid. Võib kirjutamata jätta näiteks iga teise numbri, aga vähemalt kolm-neli numbrit eaks telgede juures ikkagi olema. Märkida telgede juurde ka suurus, mis antud teljel esitatud Na 2S 2O 3 suhteline konts. x teljele ja v, min y teljele (vt. joonis). Märkida graafikule unktid (markeriks ei tohi olla lihtsalt liiatsitä, eelistada tuleks ristikest kolmnurka, seest tühja ringikest vms ). Kõige sellega saab näiteks Exel suureäraselt ise hakkama, kui valida õige graafikutüü (Satter) ja alamtüü (markerid ilma neid ühendava sirgeta). Tõmmata unktidest joonlauaga või lekaaliga läbi sirge või kõver, mis teie arvates sõltuvust kõige aremini iseloomustab. (Exelis: Add Trendline). Matemaatiliselt vastab sellele nn "vähemruutude meetod" sirge tõmmatakse nii, et katseunktide kõrvalekalded sirgest oleksid minimaalsed. v, min - v, min A B Na 2 S 2 O 3 suhteline kontsentratsioon t, o C v = f (C) v = f (t) Joonis. Reaktsioonikiiruse sõltuvus ühe lähteaine kontsentratsioonist (A) ja katse temeratuurist (B). 9 0
6 Kordamisküsimused Mõisted o Keemiline tasakaal o La Chatelier' rintsii o Keemilise reaktsiooni kiirus (ühikud) o Massitoimeseadus (valem) o Reaktsiooni kiirust mõjutavad tegurid o Reaktsiooni tasakaalu nihkumist õhjustavad tegurid o Katalüüs, katalüsaatorid 9. Visandada graafik, mis kirjeldab reaktsioonikiiruse sõltuvust temeratuurist. 0. Visandada graafik, mis kirjeldab ühe lähteaine suhtes a) esimest järku b) teist järku reaktsiooni kiiruse sõltuvust selle aine kontsentratsioonist.. Mitu korda kasvab järgmise reaktsiooni kiirus, kui suurendada a) CO kontsentratsiooni 2 korda b) O 2 kontsentratsiooni 2 korda 2CO(g) + O 2(g) 2CO 2(g) arvestades, et reaktsiooni järgud vastavate ainete suhtes võib lugeda võrdseks koefitsientidega reaktsioonivõrrandis? Küsimused ja ülesanded. Millised reaktsioonid on öörduvad, millised öördumatud tuua näiteid. 2. Millises suunas nihkub reaktsiooni CO 2(g) + H 2(g) CO(g) + H 2O(g) tasakaal, kui a) reaktsiooni keskkonda lisada veeauru, b) reaktsiooni keskkonda juhtida süsinikdioksiidi, ) reaktsiooni keskkonnast juhtida välja vesinikku, d) reaktsiooni keskkonnast juhtida välja süsinikmonooksiidi, e) reaktsiooni keskkonnast juhtida välja veeauru. 3. Kuidas nihkub reaktsiooni N 2(g) + 3H 2(g) 2NH 3(g) ( H = -92,4 kj) tasakaal a) rõhu muutmisel, b) temeratuuri muutmisel, ) lämmastiku, vesiniku ja ammoniaagi kontsentratsioonide muutmisel? 4. Mitu korda kasvab reaktsioonikiirus, kui temeratuuritegur γ = 3 ja temeratuuri tõsta 20 C võrra? [ 9 korda] 5. Milline on reaktsiooni temeratuuriteguri väärtus, kui temeratuuri tõstmisel 20 C juurest 40 C-ni kasvas reaktsioonikiirus 6 korda? [γ = 4] 6. Arvutada reaktsiooni temeratuuritegur, kui 30 C juures kulus reaktsiooni toimumiseks 5 minutit, 50 C juures aga 80 sekundit. [γ =.9] 7. Kui alju aega kulub reaktsiooni toimumiseks 5 C juures, kui 25 C juures kulus selleks 40 sekundit ja reaktsiooni temeratuuritegur on 2,0? [3 min ja 9 s] 8. Kirjutada järgmiste reaktsioonide tasakaalukonstandi (K ) avaldised: N 2(g) + 3H 2(g) 2NH 3(g) 2 NO(g) + O 2(g) 2 NO 2(g) 2C(s) + O 2(g) 2CO(g) 2
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
CaCO 3(s) --> CaO(s) + CO 2(g) H = kj. Näide
 3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
TÄIENDAVAID TEEMASID KOOLIKEEMIALE III
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Vektorid II. Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale
 Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
Funktsiooni diferentsiaal
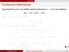 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Lokaalsed ekstreemumid
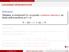 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
Graafiteooria üldmõisteid. Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid
 Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Sissejuhatus mehhatroonikasse MHK0120
 Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
PLASTSED DEFORMATSIOONID
 PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
2.2.1 Geomeetriline interpretatsioon
 2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
PÕLEVAINETE OMADUSED. Andres Talvari
 PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
HAPNIKUTARBE INHIBEERIMISE TEST
 HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
Tuletis ja diferentsiaal
 Peatükk 3 Tuletis ja diferentsiaal 3.1 Tuletise ja diferentseeruva funktsiooni mõisted. Olgu antud funktsioon f ja kuulugu punkt a selle funktsiooni määramispiirkonda. Tuletis ja diferentseeruv funktsioon.
Peatükk 3 Tuletis ja diferentsiaal 3.1 Tuletise ja diferentseeruva funktsiooni mõisted. Olgu antud funktsioon f ja kuulugu punkt a selle funktsiooni määramispiirkonda. Tuletis ja diferentseeruv funktsioon.
b) Täpne arvutus (aktiivsete kontsentratsioonide kaudu) ph arvutused I tugevad happed ja alused
 ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
=217 kj/mol (1) m Ühe mooli glükoosi sünteesil lihtainetest vabaneb footoneid: Δ H f, glükoos n (glükoos) =5,89 mol (1) E (footon)
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
Kontekstivabad keeled
 Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi
 Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks
 4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
Vektoralgebra seisukohalt võib ka selle võrduse kirja panna skalaarkorrutise
 Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
Jätkusuutlikud isolatsioonilahendused. U-arvude koondtabel. VÄLISSEIN - COLUMBIA TÄISVALATUD ÕÕNESPLOKK 190 mm + SOOJUSTUS + KROHV
 U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
28. Sirgvoolu, solenoidi ja toroidi magnetinduktsiooni arvutamine koguvooluseaduse abil.
 8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
REAKTSIOONIKINEETIKA
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika
 Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
ORGAANILINE KEEMIA ANDRES TALVARI
 ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
4.1 Funktsiooni lähendamine. Taylori polünoom.
 Peatükk 4 Tuletise rakendusi 4.1 Funktsiooni lähendamine. Talori polünoom. Mitmetes matemaatika rakendustes on vaja leida keerulistele funktsioonidele lihtsaid lähendeid. Enamasti konstrueeritakse taolised
Peatükk 4 Tuletise rakendusi 4.1 Funktsiooni lähendamine. Talori polünoom. Mitmetes matemaatika rakendustes on vaja leida keerulistele funktsioonidele lihtsaid lähendeid. Enamasti konstrueeritakse taolised
20. SIRGE VÕRRANDID. Joonis 20.1
 κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
Koduseid ülesandeid IMO 2017 Eesti võistkonna kandidaatidele vol 4 lahendused
 Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Funktsioonide õpetamisest põhikooli matemaatikakursuses
 Funktsioonide õpetamisest põhikooli matemaatikakursuses Allar Veelmaa, Loo Keskkool Funktsioon on üldtähenduses eesmärgipärane omadus, ülesanne, otstarve. Mõiste funktsioon ei ole kasutusel ainult matemaatikas,
Funktsioonide õpetamisest põhikooli matemaatikakursuses Allar Veelmaa, Loo Keskkool Funktsioon on üldtähenduses eesmärgipärane omadus, ülesanne, otstarve. Mõiste funktsioon ei ole kasutusel ainult matemaatikas,
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
MATEMAATILISEST LOOGIKAST (Lausearvutus)
 TARTU ÜLIKOOL Teaduskool MATEMAATILISEST LOOGIKAST (Lausearvutus) Õppematerjal TÜ Teaduskooli õpilastele Koostanud E. Mitt TARTU 2003 1. LAUSE MÕISTE Matemaatilise loogika ühe osa - lausearvutuse - põhiliseks
TARTU ÜLIKOOL Teaduskool MATEMAATILISEST LOOGIKAST (Lausearvutus) Õppematerjal TÜ Teaduskooli õpilastele Koostanud E. Mitt TARTU 2003 1. LAUSE MÕISTE Matemaatilise loogika ühe osa - lausearvutuse - põhiliseks
,millest avaldub 21) 23)
 II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
HSM TT 1578 EST 6720 611 954 EE (04.08) RBLV 4682-00.1/G
 HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
Energiabilanss netoenergiavajadus
 Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
RF võimendite parameetrid
 RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
Mitmest lülist koosneva mehhanismi punktide kiiruste ja kiirenduste leidmine
 TALLINNA TEHNIKAÜLIKOOL MEHAANIKAINSTITUUT Dünaamika kodutöö nr. 1 Mitmest lülist koosnea mehhanismi punktide kiiruste ja kiirenduste leidmine ariant ZZ Lahendusnäide Üliõpilane: Xxx Yyy Üliõpilase kood:
TALLINNA TEHNIKAÜLIKOOL MEHAANIKAINSTITUUT Dünaamika kodutöö nr. 1 Mitmest lülist koosnea mehhanismi punktide kiiruste ja kiirenduste leidmine ariant ZZ Lahendusnäide Üliõpilane: Xxx Yyy Üliõpilase kood:
Kui ühtlase liikumise kiirus on teada, saab aja t jooksul läbitud teepikkuse arvutada valemist
 KOOLIFÜÜSIKA: MEHAANIKA (kaugõppele). KINEMAATIKA. Ühtlane liikumine Punktmass Punktmassiks me nimetame keha, mille mõõtmeid me antud liikumise juures ei pruugi arestada. Sel juhul loemegi keha tema asukoha
KOOLIFÜÜSIKA: MEHAANIKA (kaugõppele). KINEMAATIKA. Ühtlane liikumine Punktmass Punktmassiks me nimetame keha, mille mõõtmeid me antud liikumise juures ei pruugi arestada. Sel juhul loemegi keha tema asukoha
6.6 Ühtlaselt koormatud plaatide lihtsamad
 6.6. Ühtlaselt koormatud plaatide lihtsamad paindeülesanded 263 6.6 Ühtlaselt koormatud plaatide lihtsamad paindeülesanded 6.6.1 Silindriline paine Kui ristkülikuline plaat on pika ristküliku kujuline
6.6. Ühtlaselt koormatud plaatide lihtsamad paindeülesanded 263 6.6 Ühtlaselt koormatud plaatide lihtsamad paindeülesanded 6.6.1 Silindriline paine Kui ristkülikuline plaat on pika ristküliku kujuline
HULGATEOORIA ELEMENTE
 HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
1. Soojuskiirguse uurimine infrapunakiirguse sensori abil. 2. Stefan-Boltzmanni seaduse katseline kontroll hõõglambi abil.
 LABORATOORNE TÖÖ NR. 1 STEFAN-BOLTZMANNI SEADUS I TÖÖ EESMÄRGID 1. Soojuskiirguse uurimine infrapunakiirguse sensori abil. 2. Stefan-Boltzmanni seaduse katseline kontroll hõõglambi abil. TÖÖVAHENDID Infrapunase
LABORATOORNE TÖÖ NR. 1 STEFAN-BOLTZMANNI SEADUS I TÖÖ EESMÄRGID 1. Soojuskiirguse uurimine infrapunakiirguse sensori abil. 2. Stefan-Boltzmanni seaduse katseline kontroll hõõglambi abil. TÖÖVAHENDID Infrapunase
NÄIDE KODUTÖÖ TALLINNA TEHNIKAÜLIKOOL. Elektriajamite ja jõuelektroonika instituut. AAR0030 Sissejuhatus robotitehnikasse
 TALLINNA TEHNIKAÜLIKOOL Elektriajamite ja jõuelektroonika instituut AAR000 Sissejuhatus robotitehnikasse KODUTÖÖ Teemal: Tööstusroboti Mitsubishi RV-6SD kinemaatika ja juhtimine Tudeng: Aleksei Tepljakov
TALLINNA TEHNIKAÜLIKOOL Elektriajamite ja jõuelektroonika instituut AAR000 Sissejuhatus robotitehnikasse KODUTÖÖ Teemal: Tööstusroboti Mitsubishi RV-6SD kinemaatika ja juhtimine Tudeng: Aleksei Tepljakov
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass
 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
1. Õppida tundma kalorimeetriliste mõõtmiste põhimõtteid ja kalorimeetri ehitust.
 Kaorimeetriised mõõtmised LABORATOORNE TÖÖ NR. 3 KALORIMEETRILISED MÕÕTMISED TÖÖ EESMÄRGID 1. Õppida tundma aorimeetriiste mõõtmiste põhimõtteid ja aorimeetri ehitust. 2. Määrata jää suamissoojus aorimeetriise
Kaorimeetriised mõõtmised LABORATOORNE TÖÖ NR. 3 KALORIMEETRILISED MÕÕTMISED TÖÖ EESMÄRGID 1. Õppida tundma aorimeetriiste mõõtmiste põhimõtteid ja aorimeetri ehitust. 2. Määrata jää suamissoojus aorimeetriise
Smith i diagramm. Peegeldustegur
 Smith i diagramm Smith i diagrammiks nimetatakse graafilist abivahendit/meetodit põhiliselt sobitusküsimuste lahendamiseks. Selle võttis 1939. aastal kasutusele Philip H. Smith, kes töötas tol ajal ettevõttes
Smith i diagramm Smith i diagrammiks nimetatakse graafilist abivahendit/meetodit põhiliselt sobitusküsimuste lahendamiseks. Selle võttis 1939. aastal kasutusele Philip H. Smith, kes töötas tol ajal ettevõttes
Compress 6000 LW Bosch Compress LW C 35 C A ++ A + A B C D E F G. db kw kw /2013
 55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
Kehade soojendamisel või jahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks.
 KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
Eesti koolinoorte XLIX täppisteaduste olümpiaad
 Eesti koolinoorte XLIX täppisteaduste olümpiaad MATEMAATIKA PIIRKONDLIK VOOR 26. jaanuaril 2002. a. Juhised lahenduste hindamiseks Lp. hindaja! 1. Juhime Teie tähelepanu sellele, et alljärgnevas on 7.
Eesti koolinoorte XLIX täppisteaduste olümpiaad MATEMAATIKA PIIRKONDLIK VOOR 26. jaanuaril 2002. a. Juhised lahenduste hindamiseks Lp. hindaja! 1. Juhime Teie tähelepanu sellele, et alljärgnevas on 7.
Ülesanne 4.1. Õhukese raudbetoonist gravitatsioontugiseina arvutus
 Ülesanne 4.1. Õhukese raudbetoonist gravitatsioontugiseina arvutus Antud: Õhuke raudbetoonist gravitatsioontugisein maapinna kõrguste vahega h = 4,5 m ja taldmiku sügavusega d = 1,5 m. Maapinnal tugiseina
Ülesanne 4.1. Õhukese raudbetoonist gravitatsioontugiseina arvutus Antud: Õhuke raudbetoonist gravitatsioontugisein maapinna kõrguste vahega h = 4,5 m ja taldmiku sügavusega d = 1,5 m. Maapinnal tugiseina
TEOREETILINE OSA. Joonis 5.1. Valguse levimissuuna ning vektori E r ja magnetvälja vektori H r perioodiline muutumine.
 LABORATOORNE TÖÖ NR. 5 VALGUSE POLARISATSIOON TEOREETILINE OSA Valgusel on lainelised ja korpuskulaarsed omadused. Laineoptika põhinähtused on interferents, difraktsioon, dispersioon ja polarisatsioon.
LABORATOORNE TÖÖ NR. 5 VALGUSE POLARISATSIOON TEOREETILINE OSA Valgusel on lainelised ja korpuskulaarsed omadused. Laineoptika põhinähtused on interferents, difraktsioon, dispersioon ja polarisatsioon.
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
Arvuteooria. Diskreetse matemaatika elemendid. Sügis 2008
 Sügis 2008 Jaguvus Olgu a ja b täisarvud. Kui leidub selline täisarv m, et b = am, siis ütleme, et arv a jagab arvu b ehk arv b jagub arvuga a. Tähistused: a b b. a Näiteks arv a jagab arvu b arv b jagub
Sügis 2008 Jaguvus Olgu a ja b täisarvud. Kui leidub selline täisarv m, et b = am, siis ütleme, et arv a jagab arvu b ehk arv b jagub arvuga a. Tähistused: a b b. a Näiteks arv a jagab arvu b arv b jagub
Andmeanalüüs molekulaarbioloogias
 Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
1 Funktsioon, piirväärtus, pidevus
 Funktsioon, piirväärtus, pidevus. Funktsioon.. Tähistused Arvuhulki tähistatakse üldlevinud viisil: N - naturaalarvude hulk, Z - täisarvude hulk, Q - ratsionaalarvude hulk, R - reaalarvude hulk. Piirkonnaks
Funktsioon, piirväärtus, pidevus. Funktsioon.. Tähistused Arvuhulki tähistatakse üldlevinud viisil: N - naturaalarvude hulk, Z - täisarvude hulk, Q - ratsionaalarvude hulk, R - reaalarvude hulk. Piirkonnaks
7.7 Hii-ruut test 7.7. HII-RUUT TEST 85
 7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
KORDAMINE RIIGIEKSAMIKS VII teema Vektor. Joone võrrandid.
 KORDMINE RIIGIEKSMIKS VII teema Vektor Joone võrrandid Vektoriaalseid suuruseid iseloomustavad a) siht b) suund c) pikkus Vektoriks nimetatakse suunatud sirglõiku Vektori alguspunktiks on ja lõpp-punktiks
KORDMINE RIIGIEKSMIKS VII teema Vektor Joone võrrandid Vektoriaalseid suuruseid iseloomustavad a) siht b) suund c) pikkus Vektoriks nimetatakse suunatud sirglõiku Vektori alguspunktiks on ja lõpp-punktiks
ALGEBRA I. Kevad Lektor: Valdis Laan
 ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 2016
 Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Joonis 1. Teist järku aperioodilise lüli ülekandefunktsiooni saab teisendada võnkelüli ülekandefunktsiooni kujul, kui
 Ülesnded j lhendused utomtjuhtimisest Ülesnne. Süsteem oosneb hest jdmisi ühendtud erioodilisest lülist, mille jonstndid on 0,08 j 0,5 ning õimendustegurid stlt 0 j 50. Leid süsteemi summrne ülendefuntsioon.
Ülesnded j lhendused utomtjuhtimisest Ülesnne. Süsteem oosneb hest jdmisi ühendtud erioodilisest lülist, mille jonstndid on 0,08 j 0,5 ning õimendustegurid stlt 0 j 50. Leid süsteemi summrne ülendefuntsioon.
F l 12. TRANSPORDINÄHTUSED JA BIOENERGEETIKA ALUSED
 1. TRANSPORDINÄHTUSED JA BIOENERGEETIKA ALUSED Eluks on vajalik pidev aine ja energia transport (e suunatud liikumine) läbi biosfääri ja konkreetselt bioloogilise aine. Biosfäär ehk elukeskkond on Maa
1. TRANSPORDINÄHTUSED JA BIOENERGEETIKA ALUSED Eluks on vajalik pidev aine ja energia transport (e suunatud liikumine) läbi biosfääri ja konkreetselt bioloogilise aine. Biosfäär ehk elukeskkond on Maa
STM A ++ A + A B C D E F G A B C D E F G. kw kw /2013
 Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
sin 2 α + cos 2 sin cos cos 2α = cos² - sin² tan 2α =
 KORDAMINE RIIGIEKSAMIKS III TRIGONOMEETRIA ) põhiseosed sin α + cos sin cos α =, tanα =, cotα =, cos sin + tan =, tanα cotα = cos ) trigonomeetriliste funktsioonide täpsed väärtused α 5 6 9 sin α cos α
KORDAMINE RIIGIEKSAMIKS III TRIGONOMEETRIA ) põhiseosed sin α + cos sin cos α =, tanα =, cotα =, cos sin + tan =, tanα cotα = cos ) trigonomeetriliste funktsioonide täpsed väärtused α 5 6 9 sin α cos α
DEF. Kolmnurgaks nim hulknurka, millel on 3 tippu. / Kolmnurgaks nim tasandi osa, mida piiravad kolme erinevat punkti ühendavad lõigud.
 Kolmnurk 1 KOLMNURK DEF. Kolmnurgaks nim hulknurka, millel on 3 tippu. / Kolmnurgaks nim tasandi osa, mida piiravad kolme erinevat punkti ühendavad lõigud. Kolmnurga tippe tähistatakse nagu punkte ikka
Kolmnurk 1 KOLMNURK DEF. Kolmnurgaks nim hulknurka, millel on 3 tippu. / Kolmnurgaks nim tasandi osa, mida piiravad kolme erinevat punkti ühendavad lõigud. Kolmnurga tippe tähistatakse nagu punkte ikka
( ) ( ) 2008/2009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
KORDAMINE RIIGIEKSAMIKS V teema Vektor. Joone võrrandid.
 KORDMINE RIIGIEKSMIKS V teema Vektor Joone võrrandid Vektoriaalseid suuruseid iseloomustavad a) siht b) suund c) pikkus Vektoriks nimetatakse suunatud sirglõiku Vektori alguspunktiks on ja lõpp-punktiks
KORDMINE RIIGIEKSMIKS V teema Vektor Joone võrrandid Vektoriaalseid suuruseid iseloomustavad a) siht b) suund c) pikkus Vektoriks nimetatakse suunatud sirglõiku Vektori alguspunktiks on ja lõpp-punktiks
1. Paisksalvestuse meetod (hash)
 1. Paisksalvestuse meetod (hash) Kas on otsimiseks võimalik leida paremat ajalist keerukust kui O(log n)? Parem saaks olla konstantne keerukus O(1), mis tähendaks seda, et on kohe teada, kust õige kirje
1. Paisksalvestuse meetod (hash) Kas on otsimiseks võimalik leida paremat ajalist keerukust kui O(log n)? Parem saaks olla konstantne keerukus O(1), mis tähendaks seda, et on kohe teada, kust õige kirje
Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus
 Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus 1. Haljala valla metsa pindala Haljala valla üldpindala oli Maa-Ameti
Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus 1. Haljala valla metsa pindala Haljala valla üldpindala oli Maa-Ameti
Veaarvutus ja määramatus
 TARTU ÜLIKOOL Tartu Ülikooli Teaduskool Veaarvutus ja määramatus Urmo Visk Tartu 2005 Sisukord 1 Tähistused 2 2 Sissejuhatus 3 3 Viga 4 3.1 Mõõteriistade vead................................... 4 3.2 Tehted
TARTU ÜLIKOOL Tartu Ülikooli Teaduskool Veaarvutus ja määramatus Urmo Visk Tartu 2005 Sisukord 1 Tähistused 2 2 Sissejuhatus 3 3 Viga 4 3.1 Mõõteriistade vead................................... 4 3.2 Tehted
Ecophon Line LED. Süsteemi info. Mõõdud, mm 1200x x x600 T24 Paksus (t) M329, M330, M331. Paigaldusjoonis M397 M397
 Ecophon Line LED Ecophon Line on täisintegreeritud süvistatud valgusti. Kokkusobiv erinevate Focus-laesüsteemidega. Valgusti, mida sobib kasutada erinevates ruumides: avatud planeeringuga kontorites; vahekäigus
Ecophon Line LED Ecophon Line on täisintegreeritud süvistatud valgusti. Kokkusobiv erinevate Focus-laesüsteemidega. Valgusti, mida sobib kasutada erinevates ruumides: avatud planeeringuga kontorites; vahekäigus
Staatika ja kinemaatika
 Staatika ja kinemaatika MHD0071 I. Staatika Leo eder Mehhatroonikainstituut Mehaanikateaduskond allinna ehnikaülikool 2016 Sisukord I Staatika 1. Sissejuhatus. 2. Newtoni seadused. 3. Jõud. 4. ehted vektoritega.
Staatika ja kinemaatika MHD0071 I. Staatika Leo eder Mehhatroonikainstituut Mehaanikateaduskond allinna ehnikaülikool 2016 Sisukord I Staatika 1. Sissejuhatus. 2. Newtoni seadused. 3. Jõud. 4. ehted vektoritega.
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD
 KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
Sirgete varraste vääne
 1 Peatükk 8 Sirgete varraste vääne 8.1. Sissejuhatus ja lahendusmeetod 8-8.1 Sissejuhatus ja lahendusmeetod Käesoleva loengukonspekti alajaotuses.10. käsitleti väändepingete leidmist ümarvarrastes ja alajaotuses.10.3
1 Peatükk 8 Sirgete varraste vääne 8.1. Sissejuhatus ja lahendusmeetod 8-8.1 Sissejuhatus ja lahendusmeetod Käesoleva loengukonspekti alajaotuses.10. käsitleti väändepingete leidmist ümarvarrastes ja alajaotuses.10.3
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
LOFY Füüsika looduslikus ja tehiskeskkonnas I (3 EAP)
 LOFY.01.087 Füüsika looduslikus ja tehiskeskkonnas I (3 EAP) Sissejuhatus... 1 1. Füüsika kui loodusteadus... 2 1.1. Loodus... 2 1.2. Füüsika... 3 1.3. Teaduse meetod... 4 2. Universumiõpetus... 7 3. Liikumine
LOFY.01.087 Füüsika looduslikus ja tehiskeskkonnas I (3 EAP) Sissejuhatus... 1 1. Füüsika kui loodusteadus... 2 1.1. Loodus... 2 1.2. Füüsika... 3 1.3. Teaduse meetod... 4 2. Universumiõpetus... 7 3. Liikumine
T~oestatavalt korrektne transleerimine
 T~oestatavalt korrektne transleerimine Transleerimisel koostatakse lähtekeelsele programmile vastav sihtkeelne programm. Transleerimine on korrektne, kui transleerimisel programmi tähendus säilib. Formaalsemalt:
T~oestatavalt korrektne transleerimine Transleerimisel koostatakse lähtekeelsele programmile vastav sihtkeelne programm. Transleerimine on korrektne, kui transleerimisel programmi tähendus säilib. Formaalsemalt:
Deformeeruva keskkonna dünaamika
 Peatükk 4 Deformeeruva keskkonna dünaamika 1 Dünaamika on mehaanika osa, mis uurib materiaalsete keskkondade liikumist välismõjude (välisjõudude) toimel. Uuritavaks materiaalseks keskkonnaks võib olla
Peatükk 4 Deformeeruva keskkonna dünaamika 1 Dünaamika on mehaanika osa, mis uurib materiaalsete keskkondade liikumist välismõjude (välisjõudude) toimel. Uuritavaks materiaalseks keskkonnaks võib olla
4. KEHADE VASTASTIKMÕJUD. JÕUD
 4. KEHADE VASTASTIKMÕJUD. JÕUD Arvatavasti oled sa oma elus kogenud, et kõik mõjud on vastastikused. Teiste sõnadega: igale mõjule on olemas vastumõju. Ega füüsikaski teisiti ole. Füüsikas on kehade vastastikuse
4. KEHADE VASTASTIKMÕJUD. JÕUD Arvatavasti oled sa oma elus kogenud, et kõik mõjud on vastastikused. Teiste sõnadega: igale mõjule on olemas vastumõju. Ega füüsikaski teisiti ole. Füüsikas on kehade vastastikuse
AEGLASE SÕIDUKI LIIKLUSOHUTUSEST
 133 AEGLASE SÕIDUKI LIIKLUSOHUTUSEST Eesti Maaülikool Sissejuhatus Liiklusohutuse teooriast on teada, et liiklusvoolu kiirusest erineva kiirusega sõitvad sõidukid (juhid) satuvad liiklusõnnetustesse sagedamini
133 AEGLASE SÕIDUKI LIIKLUSOHUTUSEST Eesti Maaülikool Sissejuhatus Liiklusohutuse teooriast on teada, et liiklusvoolu kiirusest erineva kiirusega sõitvad sõidukid (juhid) satuvad liiklusõnnetustesse sagedamini
Termodünaamika I seadus. Termodünaamika. Süsteemid
 Termodünaamika I seadus Süsteemid ja olekud. Töö ja energia. Soojus Kalorimeetria Entalpia ja soojusmahtuvus Faasiülemineku entalpiad Aurustumine ja kondenseerumine Sulamine ja tahkumine Reaktsioonientalpia
Termodünaamika I seadus Süsteemid ja olekud. Töö ja energia. Soojus Kalorimeetria Entalpia ja soojusmahtuvus Faasiülemineku entalpiad Aurustumine ja kondenseerumine Sulamine ja tahkumine Reaktsioonientalpia
