BORON - ΒΟΡΙΟ SBS001. Boron has a vacant p-orbital - Το βόριο έχει ένα άδειο π-τροχιακό. H B. H empty p orbital H H άδειο π-τροχιακό diborane
|
|
|
- ŌÁĒ Βλαχόπουλος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 oron has a vacant p-orbital - Το βόριο έχει ένα άδειο π-τροχιακό. N - ΒΟΡΙΟ SS001 empty p orbital άδειο π-τροχιακό diborane borane διβοράνιο βοράνιο (a) Vacant p-orbital lone pair of e - s (Lewis base) neutral species or (b) vacant p-orbital nucleophile negatively charged tetrahedral anion. (α) Άδειο π-τροχιακό μονήρες ζεύγος e - (Βάση Lewis) ουδέτερα είδη ή (β) άδειο π-τροχιακό πυρηνόφιλο αρνητικά φορτισμένο τετραεδρικό ανιόν (a) S real rxn πραγματική αντίδραση S (b) imaginary rxn φανταστική αντίδραση planar επίπεδο tetrahedral τετραεδρικό planar επίπεδο tetrahedral τετραεδρικό
2 ydroboration-the addition of boron hydrides to alkenes and alkynes. SS002 Υδροβορίωση - η προσθήκη βορονικών υδριδίων σε αλκένια και αλκύνια (1) orane (electrophile) alkene (nucleophile) borane in which one of the hydrogen atoms has been replaced by an alkane. (1) Βοράνιο(ηλεκτρονιόφιλο) αλκένιο(πυρηνόφιλο) βοράνιο στο οποίο ένα από τα άτομα υδρογόνου αντικαταστάθηκε από ένα αλκάνιο. (1) hydroboration υδροβορίωση Monoalkyl borane ( 2 ) Μονοάλκυλ βοράνιο ( 2 ) (2) hydroboration υδροβορίωση Dialkyl borane ( 2 ) Διάλκυλ βοράνιο ( 2 ) (3) hydroboration υδροβορίωση Trialkyl borane ( 3 ) Τριάλκυλ βοράνιο ( 3 )
3 ydroboration is regioselective-boron always adds to the end of alkene. SS003 Η υδροβορίωση είναι τοποεκλεκτική - το βόριο πάντα προστίθεται στο τέλος του αλκενίου warning: this is NT the complete mechanism ΠΡΟΣΟΧΗ: αυτός δεν είναι ο ολοκληρωμένος μηχανισμός What really happens: Αυτό που πραγματικά συμβαίνει είναι:
4 Monoalkyl borane ( 2 ) 2 2 Μονοάλκυλ βοράνιο alcohol αλκοόλη SS004 hydrogenation υδρογόνωση [] 2 2, Na The - attacks the neutral cleaves - alkyl bond releases the alcohol Το ΟΗ - χτυπά το ουδέτερο Β ανοίγει τον Β-Ο αλκυλ δεσμό ελευθερώνει την αλκοόλη 2 [] 2 2, Na 2 goes backwards & forwards between planar neutral structures anionic Td structures Το Β μπορεί να πάρει τόσο επίπεδες ουδέτερες όσο και ανιονικές τετραεδρικές δομές alcohol αλκοόλη Na Βορίου. stable ( 3 ) neutral, 3 atoms donating e - s into the empty p orbital on. σταθερό ( 3 ) ουδέτερο, 3 άτομα Ο προσφέρουν e- στο άδειο π-τροχιακό του stable boric acid σταθερό βορικό οξύ
5 2 water (cis addition) alcohol ( - going to the less substituted end of the alkene). 2 νερό (cis προσθήκη) αλκοόλη ( το ΟΗ - πηγαίνει στο λιγότερο υποκατεστημένο άκρο του αλκενίου) SS005 3.TF 2 Na 2 C 3, o C 100% earrangement-migration of the carbon to oxygen (cf. aeyer-villiger rearrangement). Αναδιάταξη-μετακίνηση από τον άνθρακα στο οξυγόνο (βλ.αναδιάταξη aeyer-villiger) C 3 Na Same alcohol can be made by aeyer-villiger rearrangement (stereochem. is set up before V step). Με τον ίδιο τρόπο μπορεί να γίνει και η αλκοόλη με αναδιάταξη V(η στερεοχημεία καθορίζεται στο προηγούμενο στάδιο) 2 2 2
6 xymercuration-gives the anti product (whereas hydroboration adds syn to the alkene). SS006 Οξυυδραργύρωση-δίνει το anti προϊόν (ενώ η υδροβορίωση προστίθεται συν στο αλκένιο) gac gac g(ac) 2 2 Na 4 gac ydroboration-oxidation is normally done via the trialkyl borane the stability of compounds. Υδροβορίωση-οξείδωση γίνεται κανονικά μέσω του τριάλκυλ βορανίου η σταθερότητα των ενώσεων 3 molecules 3 μόρια rearrangement x 2 αναδιάταξη 2 hydrolysis υδρόλυση 3 molecules 3 μόρια () 3
7 If we have a mixed trialkyl borane, all the alkyl groups migrate: xidation ydrolysis Alcohols SS007 Αν έχουμε ασύμμετρο τριάλκυλ βοράνιο, όλες οι αλκυλ ομάδες μετακινούνται: Οξείδωση Υδρόλυση Αλκοόλες 2 Na Na, TF, rt 96% 99% ulky substituents the selectivity of hydroboration. Ογκώδεις υποκαταστάτες την εκλεκτικότητα της υδροβορίωσης 3 very slow πολύ αργά "Thexyl borane" Thexyl borane often written as Th 2 and drawn as: 2 Το thexyl βοράνιο συχνά γράφεται ως Th 2 και σχεδιάζεται ως:
8 2 nd hydroboration is fast intramolecular (regioselectivity is under thermodynamic control). Η 2η υδροβορίωση είναι γρήγορη ενδομοριακή(τοποεκλεκτικότητα ελέγχεται θερμοδυναμικά) 3 rd hydroboration is very slow. Η 3η υδροβορίωση είναι πολύ αργή SS fast γρήγορα = cycloocta-1,5-diene κυκλοοκτα-1,5-διένιο 9-N often drawn as: 9-N συχνά σχεδιάζεται ως: 9-N Simple trialkyl alkene borane disiamylborane (very regioselective, hindered structure). Απλό τριάλκυλ αλκένιο βοράνιο δισιαμυλβοράνιο(πολύ τοποεκλεκτικό, παρεμποδισμένη δομή). 3 fast γρήγορα 2 3 fast γρήγορα disiamylborane or Sia 2 δισιαμυλβοράνιο ή Sia 2 very slow πολύ αργά 3
9 ulkier boranes Πιο ογκώδη βοράνια G enhance regioselectivity of hydroboration of trisubstituted alkenes. αυξημένη τοποεκλεκτικότητα της υδροβορίωσης των τριυποκατεστημένων αλκενίων high diastereoselectivity if there is a stereogenic centre next to the alkene. ψηλή διαστερεοεκλεκτικότητα αν υπάρχει στερεογονικό κέντρο δίπλα από το αλκένιο SS009 n-u n-u 1. Th 2, TF n-u n-u n-u n-u /Na 72% 8 : 1 Attack occurs syn to the group and anti to the larger butyl group. Η προσβολή γίνεται συν στην ΟΗ ομάδα και αντι στη μεγαλύτερη βουτυλ ομάδα. n-u n-u 2 TF n-u 2 n-u 2 2 Na n-u n-u
10 Alkynes Vinyl boranes [] nol Αλκύνια Βινυλο βοράνια [] Ενόλη Tautomerization Ταυτομερισμός Aldehyde Αλδεϋδη SS010 Sia 2 Sia 2 -vinyl borane Ε- βινυλο βοράνιο Na Na, TF, rt 79% C- bonds can be transformed stereospecifically into C-X, where X =, N or C. Y is a L.G. Οι δεσμοί C- μπορούν να μετατραπούν στερεοειδικά σε C-X, όπου Χ=Ο,Ν ή C. Y αποχωρούσα ομάδα X Y X Y rearrangement αναδιάταξη X 2 X
11 ydroboration-amination of pipene regioselective syn addition of ammonia across the alkene (from the less hindered side). SS011 Υδροβορίωση-κίνηση του πιπενίου τοποεκλεκτική συν προσθήκη της αμμωνίας κατά μήκος του αλκενίου (από τη λιγότερο παρεμποδισμένη πλευρά) NS 3 N 2 42% hydroboration from underneath υδροβορίωση από την κάτω πλευρά 3 2 N S 3 3 N S3
12 The order in which groups migrate from boron to carbon is: n-alkyl > s-alkyl > t-alkyl. Η σειρά με την οποία οι ομάδες μετακινούνται από το βόριο στον άνθρακα είναι: SS012 C- bond G. C-C bond. r t-uk 42% t-u t-uk r C 2 r C 2
13 Difference between aeyer-villiger rearrangement and boron chemistry Διαφορά μεταξύ αναδιάταξης aeyer-villiger και χημείας του Βορίου SS013 The aeyer-villiger rearrangement- the transition state has a positive charge. Αναδιάταξη aeyer-villiger-η μεταβατική κατάσταση έχει θετικό φορτίο 1 2 δ C C 2 δ- In boron rearrangements the whole transition state has a negative charge. Στις αναδιατάξεις του βορίου η μεταβατική κατάσταση έχει αρνητικό φορτίο δ- δ
14 ridged bicyclic ketones peroxy-acids more migration of the 1 o alkyl group than 2 o. SS014 Γεφυρωμένες δικυκλικές κετόνες υπεροξέα μεγαλύτερη μετακίνηση της πρωτοταγούς αλκυλικής ομάδας παρά της δευτεροταγούς 2 o 3 o major product κύριο προϊόν minor product δευτερεύον προϊόν
15 Alkyl and crotyl boranes react using the double bond. SS015 Αλκυλικά και κροτυλικά βοράνια αντιδρούν χρησιμοποιώντας το διπλό δεσμό L L L L L L 2 2 Na ther allylic organometallic reagents frequently react with 1,3-rearrangement. Άλλα αλλυλικά οργανομεταλλικά αντιδραστήρια συχνά αντιδρούν με 1,3-αναδιάταξη M direct addition απευθείας προσθήκη M M rearrangement αναδιάταξη
16 Allylic rearrangement-even Grignard reagents react with aldehydes via a cyclic 6-membered TS. SS016 Αλλυλική αναδιάταξη-ακόμα και τα αντιδραστήρια Grignard αντιδρούν με αλδεϋδες μέσω μιας κυκλικής 6-μελούς μεταβατικής κατάστασης Mgr r Mg rmg 3 nantioselective allylation is possible with optically pure ligands on boron. Εναντιοεκλεκτική αλλυλίωση είναι πιθανή με οπτικά ενεργούς υποκαταστάτες στο βόριο t o C instantaneous αμέσως almost enantiomerically pure σχεδόν εναντιομερικώς καθαρό carene καρένιο
17 (a) -Crotyl boranes (or boronates) aldehyde anti homoallylic alcohols via chair TS in which the aldehyde group adopts a pseudoequatorial position to minimize steric repulsion. SS017 (α) Ε-κροτυλικά βοράνια(ή βορονικά) αλδεϋδη αντι ομοαλλυλικές αλκοόλες μέσω ΜΚ ανακλίντρου στην οποία η αλδεϋδική ομάδα υιοθετά μια ψευδοϊσημερινή θέση για να ελαχιστοποιήσει στερική παρεμπόδιση. -crotyl boronate Ε-κροτυλo βορονικό L favoured equatorial in transition state στη μεταβατική κατάσταση το ισημερινό προτιμάται L L L -78 o C [] anti αντι staggered conformation διαβαθμισμένη διαμόρφωση L L disfavoured axial το αξονικό δεν προτιμάται
18 (b) Z-Crotyl boranes (or boronates) aldehyde syn homoallylic alcohols. SS018 (β) Ζ-κροτυλο βοράνια (ή βορονικά) αλδεϋδη συν ομοαλλυλική αλκοόλη Z-Crotyl boronate Ζ-κροτυλο βορονικό -78 o C syn συν L L L L [] staggered conformation διαβαθμισμένη διαμόρφωση favoured equatorial in transition state στη μεταβατική κατάσταση το ισημερινό προτιμάται L L disfavoured axial το αξονικό δεν προτιμάται
19 Chiral ligand on boron allows the production of a single enantiomer of a single diastereoisomer. Χειρικός υποκαταστάτης στο βόριο επιτρέπει την παραγωγή απλού εναντιομερούς?ενός? απλού διαστερεοϊσομερούς SS019 absolute stereochemistry of the ligand is the same η απόλυτη στερεοχημεία του υποκαταστάτη είναι ίδια 2 geometry of the crotyl group is different η γεωμετρία της κροτυλο ομάδας είναι διαφορετική t 2-78 o C 99% one diastereoisomer 94-98% ee t 2 2 Z -78 o C 99% one diastereoisomer 94-98% ee
20 -valency = 4 - σθένος = 4 -forms tetrahedral compounds - σχηματίζει τετραεδρικές ενώσεις SILICN - ΠΥΡΙΤΙΟ SS020 g. Si 3 Si Si Si a useful electrophile χρήσιμο ηλεκτρονιόφιλο a protected alcohol προστατευμένη αλκοόλη an allyl silane αλλυλo σιλάνιο a silyl benzene σιλυλο-βενζόλιο Si electronegativity < C, Si ηλεκτροαρνητικότητα < C C-Si bonds are polarized towards the C makes Si susceptible to attack by Nuc. Οι δεσμοί C-Si πολώνονται προς τον C το Si γίνεται ευάλωτο να προσβληθεί από Nuc. δ- C Si δ Si has an affinity for electronegative atoms. Si έχει προτίμηση για ηλεκτροαρνητικά άτομα t-u F Si u 4 NF t-u Si F t-u Si F a protected alcohol pentacovalent Si alcohol προστατευμένη αλκοόλη πεντασθενές Si αλκοόλη
21 S N 2 process at silicon. SS021 S N 2 μηχανισμός στο πυρίτιο 2 hydroboration υδροβορίωση Na 2 [] Na hydrolysis υδρόλυση tetrahedral τετραεδρικό Β 2 hydrolysis υδρόλυση The silicon aeyer-villiger rearrangement Η αναδιάταξη aeyer-villiger στο πυρίτιο X Si 2 2 X Si X Si Na [] pentacovalent Si πεντασθενές Si rearrangement αναδιάταξη also via pentacovalent silicon επίσης μέσω πεντασθενούς πυριτίου hydrolysis
22 Differences between the 'S N 2' reaction at silicon and the S N 2 reaction at carbon. Διαφορές μεταξύ του 'S N 2' μηχανισμού στο πυρίτιο και του 'S N 2' μηχανισμού στον άνθρακα SS022 S N 2 unfavourable δεν ευνοείται X C S N 1 C stable t-butyl cation σταθερό t-βουτυλo κατιόν X C X Si S N 1 does not occur δε συμβαίνει X Si "S N 2" very favourable πολύ ευνοϊκό X Si stable silicon anion σταθερό ανιόν πυριτίου X Si The best nucleophiles for silicon are charged and based on highly electronegative atoms e.g. F, and. Τα καλύτερα πυρηνόφιλα για το πυρίτιο είναι φορτισμένα και βασισμένα σε πολύ ηλεκτροαρνητικά άτομα π.χ F,, 3 Si X Si 3 X "S N 2" S N 2
23 When the 3 Si group is removed with -, the product is the silyl ether 'hexamethyldisiloxane'. Όταν η 3 Si ομάδα φεύγει με το ΟΗ -, το προϊόν είναι ο σιλυλο-αιθέρας 'εξαμεθυλοδισιλοξάνιο' SS023 3 Si X 3 Si 3 Si 3 Si X 3 Si Si 3 Acetal formation-silylation occurs 2x at the carbonyl and the final L.G. is hexamethyldisiloxane. Ακεταλική διαμόρφωση-πυριτίωση γίνεται 2 φορές στο καρβονυλικό Ο και η τελική Α.Ο είναι το εξαμεθυλοδισιλοξάνιο. 3 Si Tf Si 3 Si 3 Si 3 3 Si Tf Si 3 Si 3 94%
24 Silyl enol ether formation- silylation of carbonyl addition of a weak base (to remove the SS024 after silylation). Σχηματισμός σιλυλο-ενολικού αιθέρα-πυριτίωση του καρβονυλικού Ο προσθήκη ασθενούς βάσης(για να απομακρύνει το μετά την πυριτίωση) 3 Si 3 Si Tf 3 Si Nt 3 Acetal silyl enol ether aldol style condensation. 85% Ακετάλη σιλυλο-ενολικός αιθέρας αλδολική συμπύκνωση 3 Si Tf Si 3 Si 3 Si 3 Tf 89% Silyl ethers are versatile protecting groups for alcohols. Σιλυλο-αιθέρες είναι πολύ καλές προστατευτικές ομάδες για αλκοόλες
25 SS025 Si Si Si Si 3 Si t-u 2 Si t-u 2 Si i-pr 3 Si TMS TDMS TDPS TIPS The large steric bulk of the TDPS group helps to selectively protect unhindered primary alcohols. Ο μεγάλος στερικός όγκος της ομάδας TDPS βοηθά στο να προστατεύει εκλεκτικά, ανεμπόδιστες πρωτοταγείς αλκοόλες t-u Si N N DMF t-u Si TDPS diol διόλη imidazole ιμιδαζόλη TDPS ether αιθέρας TDPS
26 Acidic proton on terminal alkynes can be removed by very strong bases such as organometallic reagents e.g. Grignards, Li. Το όξινο πρωτόνιο σε τελικό αλκύνιο μπορεί να φύγει με πολύ δυνατές βάσεις όπως οργανομεταλλικά αντιδραστήρια π.χ Grignards, Li SS026 protection προστασία uli or tmgr or M 3 Si Si 3 terminal alkyne τελικό αλκύνιο LDA or NaN 2 organometallic οργανομεταλλικό protected alkyne προστατευμένο αλκύνιο Si 3 group protects the terminus of the alkyne and can be removed with F - or Na. Η ομάδα Si 3 προστατεύει το τελικό άκρο του αλκυνίου και μπορεί να φύγει με F - ή Na. reaction αντίδραση deprotection αποπροστασία uli Li Si 3 Si 3 u 4 NF or Na organometallic οργανομεταλλικό protected product προστατευμένο προϊόν product προϊόν
27 emoval of the Si 3 with K 2 C 3 in allows further reaction on the other end of the alkyne. Μετακίνηση της ομάδας Si 3 με K 2 C 3 σε επιτρέπει περαιτέρω αντίδραση στο άλλο άκρο του αλκυνίου. SS027 Si 3 uli TF Li Si 3 TF DNPU u 4 NI Si 3 K 2 C 3 78% Silicon stabilizes a positive charge on the β carbon. Το πυρίτιο σταθεροποιεί το θετικό φορτίο στο β άνθρακα. Nu Si 3 Si 3
28 -Carbocation stability tertiary > secondary > primary -Stabilization by σ donation SS028 -Σταθερότητα καρβοκατιόντος τριτοταγές> δευτεροταγές> πρωτοταγές -Σταθεροποίηση με σ προσφορά Si 3 Si 3 no stabilization όχι σταθεροποίηση Nucleophilic attack removes Si. Πυρηνόφιλη προσβολή μετακινεί το πυρίτιο or Si 3 stabilized by β-silicon σταθεροποιείται με β πυρίτιο vacant p-orbital άδειο π-τροχιακό Si 3 filled C-Si σ orbital κατειλημμένο σ-τροχιακό Si 3 Si 3 X stabilized by β-silicon σταθεροποιείται με β πυρίτιο 3 SiX product προϊόν Alkynyl silanes acid chlorides (in the presence of L.A) ketone Αλκυνυλο σιλάνια χλωρίδιο οξέως (στην παρουσία οξέωςlewis) κετόνη u Si 3 Al 3 u Si 3 u Si 3 u stabilized by β-silicon σταθεροποιείται με β-πυρίτιο alkynyl ketone αλκυνιλική κετόνη
29 Aryl silanes undergo ipso substitution with electrophiles. Αρυλο σιλάνια δέχονται ipso υποκατάσταση με ηλεκτρονιόφιλα SS029 Nu Si 3 Si 3 Si 3 filled C-Si σ orbital κατειλημμένο σ τροχιακό stabilized by β-silicon σταθεροποιείται με β-πυρίτιο vacant p-orbital άδειο π-τροχιακό orbital perfectly aligned τροχιακό τέλεια ευθυγραμμισμένο Alternative site of attack-not very stable cation, the vacant p orbital is orthogonal to C-Si bond cannot interact with it. Εναλλακτική πλευρά προσβολής-όχι πολύ σταθερό κατιόν, το άδειο π τροχιακό είναι ορθογωνικό στο δεσμό C-Si δεν μπορεί να αντιδράσει με αυτό Si 3 Si 3 C-Si bond is orthogonal to empty p orbital ο δεσμός C-Si είναι ορθογωνικός στο άδειο π τροχιακό Si 3 vacant p-orbital άδειο π-τροχιακό
30 Stable phenyl dimethylsilyl group Σταθερή φαινυλική διμεθυλσιλυλική ομάδα "silyl aeyer- Villiger" rxn alcohol. αλκοόλη SS030 Si 2 1. r Na enyl silane bromine bromobenzene silyl bromide. Φαινυλο σιλάνιο βρώμιο βρωμοβενζόλιο σιλυλοβρωμίδιο Si r r r Si r r Si r stabilized by β-silicon σταθεροποιείται με β-πυρίτιο
31 Displacement of r - by - addition of - rearrangement hydrolysis. Μετακίνηση r - από - προσθήκη ΟΗ - αναδιάταξη υδρόλυση SS031 Si r Na 2 2 Si Si Na rearrangement αναδιάταξη hydrolysis υδρόλυση Lindlar hydrogenation hydrogen is added across the alkyne in a cis fashion (Z-isomer). Υδρογόνωση Lindlar το υδρογόνο προστίθεται κατά μήκος του αλκυνίου σε cis διαμόρφωση (Ζ-ισομερές) 3 Si n-u 2 Lindlar catalyst καταλύτης Lindlar 3 Si Z n-u Propargylic alcohol ed Al reduction -isomer Προπαργυλική αλκοόλη αναγωγή ed Al Ε-ισομερές 3 Si 1. ed Al Si Al 2 ed Al Na
32 egioselectivity of hydroalumination is determined by Si: the electrophile attacks the alkyne on the C bearing the silyl group. Η τοποεκλεκτικότητα της υδροαργιλίωσης καθορίζεται από το Si: το ηλεκτρονιόφιλο προσβάλλει το αλκύνιο στον άνθρακα που έχει τη σιλυλο ομάδα SS032 3 Si 3 Si 1. ed Al ligand exchange αλλαγή υποκαταστάτη Al Al hydroalumination υδροαργιλίωση 3 Si Al 2. 3 hydrolysis υδρόλυση 3 Si Cis addition of and Si 3 to an alkyne by hydrosilylation. Cis προσθήκη of and Si 3 σε αλκύνιο με υδροπυριτίωση Si 3 3 Si 2 Pt 6 cat. Si 3 hv -vinyl silane Ε-βινυλo σιλάνιο Z-vinyl silane Ζ-βινυλo σιλάνιο
33 metal-halogen Vinyl halides vinyl silanes. exchange SS033 ανταλλαγή Βινυλo-αλογονίδια βινυλo σιλάνια μετάλλου-αλογόνου r 2 x t-uli -120 o C Li 3 Si Si 3 Na, t 2 3 Si Na Si 3
34 Vinyl silanes can be prepared directly from ketones using the Shapiro reaction. Βινυλo σιλάνια μπορούν να γίνουν κατευθείαν από κετόνες χρησιμοποιώντας την αντίδραση Shapiro SS034 Ar S Ar S N N 2 N N 1) 2 x uli 2) 3 Si Si 3 Ar 2 x uli S LiN N αργό στάδιο slow step ArS 2 Li N N N 2 Li 3 Si vinyl silane S N N 2 Li Li Si a bulky sulfonyl hydrazine for the Shapiro reaction ογκώδης σουλφονυλική υδραζίνη για την αντίδραση Shapiro
35 Si is replaced by the electrophile D, at the ipso C atom (retention of geometry). Το πυρίτιο αντικαθίσταται από το ηλεκτρονιόφιλο D στο ipso άτομο C(διατήρηση γεωμετρίας) SS035 Si 3 D Si 3 D D D attacks the π bond, 3 Si group moves upwards. As it rotates, the angle between the C-Si bond and the remaining p orbital from 90. προσβάλλει τον π δεσμό, η ομάδα κινείται προς τα πάνω. Όπως περιστρέφεται, η γωνία μεταξύ του δεσμού C-Si και του εναπομείναντος π τροχιακού από 90. As the angle the interaction between the C-Si bond and the empty p orbital of the cation. Όσο η γωνία η αλληλεπίδραση μεταξύ του δεσμού C-Si και του άδειου π τροχιακού του κατιόντος. silicon starts to rotate upwards το πυρίτιο αρχίζει να περιστρέφεται προς τα πάνω D Si 3 silicon continues to rotate upwards το πυρίτιο συνεχίζει να περιστρέφεται προς τα πάνω D Si 3 Si 3 D C-Si bond is parallel to p orbital of cation ο δεσμός C-Si είναι παράλληλος στο π τροχιακό του κατιόντος deuteration from underneath δευτερίωση από κάτω
36 Intermediate cation has only a single bond, rotation might be expected to give a mixture of geometrical isomers. Instead we get only one product, either the or the Z-isomer. SS036 Το ενδιάμεσο κατιόν έχει μόνο ένα απλό δεσμό, Η περιστροφή ενδεχομένως να δίνει μίγμα γεωμετρικών ισομερών Αντιθέτως παίρνουμε μόνο ένα προϊόν, το Ε ή το Ζ-ισομερές -vinyl silane Ε-βινυλο σιλάνιο Si 3 Si 3 deuteration from underneath δευτερίωση από κάτω Z-vinyl silane Ζ-βινυλο σιλάνιο D Si 3 D rotation continues D η περιστροφή συνεχίζεται correctly aligned stabilized by β-silicon σωστά ευθυγραμμισμένο σταθεροποιείται από το β-πυρίτιο D 3 Si Si 3 D Si 3 deuteration from underneath δευτερίωση από κάτω D D rotation continues η περιστροφή συνεχίζεται correctly aligned stabilized by β-silicon σωστά ευθυγραμμισμένο σταθεροποιείται από το β-πυρίτιο D
37 nergy diagram for the two alternative rotations Ενεργειακό διάγραμμα για τις δύο εναλλακτικές περιστροφές SS037 energy ενέργεια large energy barrier μεγάλο ενεργειακό φράγμα D Si 3 least stable conformation C-Si σ orthogonal to p orbital ελάχιστα σταθερή διαμόρφωση C-Si σ ορθογωνικό στο π τροχιακό small energy barrier μικρό ενεργειακό φράγμα favoured rotation ευνοϊκή περιστροφή Si 3 Si 3 D D starting conformation αρχική διαμόρφωση disfavoured rotation μη ευνοϊκή περιστροφή D Si 3 stable conformation C-Si σ parallel to p orbital σταθερή διαμόρφωση C-Si σ παράλληλος με το π τροχιακό conformation of the cation διαμόρφωση του κατιόντος stable conformation C-Si σ parallel to p orbital σταθερή διαμόρφωση C-Si σ παράλληλος με το π τροχιακό
38 alogens are useful electrophiles. rganic halides (e.g. acid chlorides in the presence of L.A.) vinyl halides unsaturated ketones (of defined geometry) SS038 Τα αλογόνα είναι χρήσιμα ηλεκτρονιόφιλα. Οργανικά αλογονίδια(π.χ χλωρίδια οξέως στην παρουσία L.A) βινυλικά αλογονίδια ακόρεστες κετόνες(ορισμένης γεωμετρίας) Z-vinyl silane Ζ-βινυλο σιλάνιο -vinyl silane Ε-βινυλο σιλάνιο Si 3 I I 2 C 2 2, 0 o C Si 3 I 2 C 2 2, 0 o C 1 I Z-vinyl silane Ζ-βινυλο σιλάνιο -vinyl silane Ε-βινυλο σιλάνιο Si Si Al 3 Al 3 C 2 2, 0 o C C 2 2, 0 o C
39 Peterson Grignard reagent Ce 3 ester tertiary alcohol allyl silane. elimination SS039 απόσπαση Αντιδραστήριο Grignard Ce 3 εστέρας τριτοταγής αλκοόλη αλλυλο σιλάνιο Peterson 3 Si I Mg t 2 3 Si MgI Ce 3 MgI Si 3 Peterson Si 3 3 Si Wittig reagent cyclohexanone Ylid yild (anion fomation next to P) allyl silane. alkylation αντιδραστήριο Wittig cyclohexanone Υλίδιο Υλίδιο (σχηματισμός ανιόντος δίπλα στο Ρ) αλλυλo σιλάνιο αλκυλίωση P 3 Υlid Υλίδιο 3 Si alkylation (S N 2) αλκυλίωση I 3 Si P 3 uli 3 Si New ylid Νέο υλίδιο P 3 Wittig Si 3 allyl silane αλλυλo σιλάνιο
40 3 Si group is large, but C-Si bond is long, steric effect of 3 Si group < steric effect of 3 C group. SS040 Η ομάδα 3 Si είναι μεγάλη, αλλά ο δεσμός C-Si είναι μακρύς, στερική επίδραση της ομάδας 3 Si < στερική επίδραση της ομάδας 3 C. X Si I longer bond μακρύτερος δεσμός fast reaction γρήγορη αντίδραση Si approach of nucleophile hindered παρεμποδισμένη προσέγγιση πυρηνόφιλου X X neopentyl iodide νεοπεντυλικό ιωδίδίο I very slow πολύ αργά X Allyl silanes are more reactive than vinyl silanes but also reαct through β-silyl cations. Αλλυλικά σιλάνια πιο αντιδραστικά από τα βινυλικά σιλάνια αλλά επίσης αντιδρούν μέσω β-σιλυλo κατιόντων Si 3 Si 3 Si 3 Si 3 a vinyl silane βινυλο σιλάνιο no interaction between orthogonal orbitals καμία αλληλεπίδραση μεταξύ ορθογωνικών τροχιακών an allyl silane αλλυλο σιλάνιο interaction between parallel orbitals αλληλεπίδραση μεταξύ παράλληλων τροχιακών
41 allyl silanes αλλυλo σιλάνια Thermodynamic stability Θερμοδυναμική σταθερότητα vinyl silanes βινυλo σιλάνια SS041 A compound having both vinyl silane and allyl silane functional groups, reacts exclusively as an allyl silane. Vinylic Si is not involved as the C- Si bond is orthogonal to the π system. Μια ένωση που έχει και βινυλικό σιλάνιο και αλλυλικό σιλάνιο για λειτουργικές ομάδες, αντιδρά αποκλειστικά σαν ένα αλλυλικό σιλάνιο. Βινυλικό Si δε συμμετέχει καθώς ο δεσμός C-Si είναι ορθογωνικός στο π σύστημα. Si 3 Si 3 Al 3, C 2 2 cis Si 3 trans Si 3 Allyl silanes react with even greater regioselectivity than that of vinyl silanes. Αλλυλικά σιλάνια αντιδρούν με ακόμη μεγαλύτερη τοποεκλεκτικότητα από τα βινυλικά σιλάνια. Similarities: Differences: (1) A cation β to the silyl group is formed. (1) lectrophile attacks at the other end of theallylic system. (2) No rotation is necessary. Ομοιότητες: Διαφορές: (1) Δημιουργείται κατιόν β στη σιλυλική ομάδα (1) Ηλεκτρονιόφιλο προσβάλλει στο άλλο άκρο του αλλυλικού συστήματος (2) Η περιστροφή δεν είναι απαραίτητη Si 3 Si 3 β-silyl cation β-σιλυλο κατιόν
42 lectophilic substitution with allylic rearrangement- oth the side of attachment of the electrophile and the position of the new double bond are dictated by Si. Ηλεκτρονιόφιλη υποκατάσταση με αλλυλική αναδιάταξη- Τόσο η πλευρά παγίδευσης του ηλεκτρονιόφιλου όσο και η θέση του νέου διπλού δεσμού υπαγορεύονται από το Si. SS042 filled π orbital κατειλημμένο π τροχιακό Si 3 vacant orbital άδειο τροχιακό filled σ orbital κατειλημμένο σ τροχιακό filled σ orbital κατειλημμένο σ τροχιακό Si 3 vacant p orbital άδειο τροχιακό filled σ orbital κατειλημμένο σ τροχιακό filled σ orbital κατειλημμένο σ τροχιακό filled π orbital κατειλημμένο π τροχιακό Si 3
43 A: General reaction of allyl silanes with electrophiles. SS043 Γενική αντίδραση αλλυλικών σιλανίων με ηλεκτρονιόφιλα : ven reaction with a occurs at the other end of the allyl system with movement of the double bond. Ακόμα και αντίδραση με Η γίνεται στο άλλο τελικό άκρο του αλλυλικού συστήματος με μετακίνηση του διπλού δεσμού. A Si 3 F 3 Ac ther : acylium ions (from acid chlorides), carbocations, activated enones and epoxides all in the presence of L.A. Αλλα Ε :??? ιόντα(από χλωρίδια οξέως), καρβοκατιόντα, ενεργοποιημένες ενόνες και εποξείδια όλα στην παρουσία L.A 99% X Ti 4 Ac Ti 4 Si 3 82% Ti 4 Ti 4 55%
44 - and Z-isomers both react stereoselectively enantiomeric products. Ε- και Ζ-ισομερή αντιδρούν στερεοεκλεκτικά εναντιομερικά προϊόντα SS044 The reactions are completely stereospecific. Οι αντιδράσεις είναι τελείως στερεοειδικές Si 3 t-u Ti 4, -78 o C t-u Si 3 Z t-u t-u Ti 4, -78 o C Allyl silanes attack C= when activated by coordination of the carbonyl atom to a L.A. Αλλυλo σιλάνια προσβάλλουν C= όταν ενεργοποιηθεί με μετατροπή του καρβονυλικού οξυγόνου σε L.A M aldehyde αλδεϋδη MX n M oxonium ion ιόν οξωνίου Si 3 M X Si 3 homoallylic alcohol ομοαλλυλική αλκοόλη
45 L.A.-catalysed breakdown of acetal oxonium ion. L.A.- καταλυτικό σπάσιμο ακετάλης ιόν οξωνίου. SS045 If we have a silyl acatal, the same oxonium ion can be produced in situ using more Si in the form of TMSTf as the L.A. catalyst. Αν έχουμε σιλυλική ακετάλη, το ίδιο ιόν οξωνίιου μπορεί να παραχθεί χρησιμοποιώντας περισσότερο Si στη μορφή TMSTf ως τον καταλύτη L.A M MX n 1 Si 3 1 aldehyde αλδεϋδη acetal ακετάλη oxonium ion ιόν οξωνίου homoallylic ether ομοαλλυλικός αιθέρας 3 Si Tf 3 Si 1 3 SiTf 1 Si 3 (3 Si) 2
46 Intramolecular reaction on to an acetal promoted by Sn 4 (regiocontrol). Ενδομοριακή αντίδραση πάνω σε μια ακετάλη προωθημένη από Sn 4 (regiocontrol) SS046 Sn 4 Si 3 Sn 4 Si 3 Si 3 Si 3
47 Crotyl silanes are powerful reagents in stereoselective synthesis. Κροτυλικά σιλάνια ισχυρά αντιδραστήρια στη στερεοεκλεκτική σύνθεση. SS047 n Ar TMSTf C 2 2, -78 o C Ar Si 2 a crotyl silane κροτυλο σιλάνιο C 2 n Ar C 2 > 30:1 diastereoselectivity διαστερεοεκλεκτικότητα Ar n Si 2 C 2 S 2' rxn Ar n C 2 Ar n C 2 Favoured ευνοείται otate περιστροφή
48 2 atom removes a hydrogen atom from one of the C 3 groups primary radical next to Si, which reacts in turn with a 2 the radical chain continues. SS048 Άτομο 2 απομακρύνει ένα υδρογόνο μιας από τις ομάδες C 3 πρωτοταγής ρίζα δίπλα από το Si, η οποία αντιδρά με το 2 η αλυσίδα συνεχίζεται 2 Si hv Si. Si. C 2. Si Chloride reacts by the S N 2 mechanism. It also forms organometallic reagents such as Grignard reagents and lithium derivatives. Χλωρίδιο αντιδρά με S N 2 μηχανισμό. Επίσης, σχηματίζει οργανομεταλλικά αντιδραστήρια όπως αντιδραστήρια Grignard και παράγωγα λιθίου. Si Si Nu Si Mg t 2 Si Mg Si Nu poxidation - Εποξείδωση Si 3 m-cpa Si 3 Z Si m-cpa 3 Si 3 poxides react stereospecifically with nucleophiles single diastereoisomers. Εποξείδια αντιδρούν στερεοειδικά με πυρηνόφιλα απλά διαστερεοισομερή 1 Si 3 ( 2 ) 2 CuLi ( 2 ) 2 CuLi 1 Si 3 Si Si 3 2
49 limination in base is a Wittig-style syn process but an anti elimination occurs in acid. Απόσπαση σε βάση είναι συν, Wittig-στυλ, αλλά σε οξύ συμβαίνει αντι απόσπαση. Si 3 base 1 2 syn 1 1 Si F 3 elimination 3 or Si 2 X anti elimination SS Conversion of epoxide to the carbonyl compound. Stereochemistry does not matter in this rxn. Μετατροπή εποξειδίου στην καρβονυλική ένωση. Στερεοχημεία δεν παίζει ρόλο σε αυτή την αντίδραση. Si 3 2 Si 3 2 Silyl groups stabilize carbanions. - Σιλυλο ομάδες σταθεροποιούν τα καρβανιόντα. 1. uli 3 P Si 3 3 P 2. C 3 Si Si 3 1. uli 2. C 3 Si The first reagent prefers to do the Peterson rxn rather than the Wittig, nucleophilic attack at Si is faster than nucleophilic attack at P. Το πρώτο αντιδραστήριο προτιμά να κάνει την αντίδραση Petterson παρά την Wittig, πυρηνόφιλη προσβολή στο Si πιο γρήγορη παρά στο Ρ. 1. uli 2. C 3 P Si 3 3 P 3 P Si 3 3 P Si 3 Si 3 3 P 3 Si
50 - must attack one of the 3 Si groups and the Peterson rxn must occur. - πρέπει να προσβάλει μια από τις ομάδες 3 Si και η αντίδραση Peterson πρέπει να γίνει. 1. uli 2. C 3 Si Si 3 3 Si Si 3 Si Si 3 3 Si 3 Si 3 The stabilization of anions is weak, weaker than from P or S. Η σταθεροποίηση ανιόντων είναι αδύνατη, πιο αδύνατη από το Ρ ή το S. SS050 3 Si 3 Si 3 Si P 3 Si-stabilized carbanion Si-σταθεροποιεί το καρβανιόν 3 Si P 3 uli 3 Si P 3 phosphorus ylid υλίδιο φωσφόρου Allyl silanes can give a Li derivative that reacts with ketones (electrophiles) in the γ-position relative to the 3 Si group. Αλλυλο σιλάνια μπορούν να δώσουν παράγωγο Li το οποίο αντιδρά με κετόνες(ηλεκτρονιόφιλα) στη γ-θέση σε σχέση με την ομάδα 3 Si. 3 Si s-uli 3 Si 3 Si 88% If is used as the electrophile with F 3 as the L.A cyclic acetals. Αν η χρησιμοποιείται ως το ηλεκτρονιόφιλο με F 3 ως L.A κυκλικές ακετάλες 3 Si m-cpa 3 Si 78% F 3
51 Nucleophilic attack occurs next to Si. Peterson elimination gives an enol ether. Πυρηνόφιλη προσβολή συμβαίνει δίπλα στο Si. Απόσπαση Peterson δίνει ενολικό αιθέρα. 3 Si F 3 3 Si F 3 xidation under acidic conditions spirocyclic lactone lactone. Οξείδωση κάτω από όξινες συνθήκες σπιροκυκλική λακτόνη λακτόνη SS051 enol ether ενολικός αιθέρας Allyl silane behaves as a d 3 synthon or homoenolate. Αλλυλο σιλάνιο συμπεριφέρεται σαν d 3 σινθόνη ή ομοενολικό. Cr 3 2 S 4 76% acetone C C 3 4 1,4-di C
52 rook rearrangement- the silyl group migrates from C to. Nucleophilic substitution at Si. Αναδιάταξη rook-η σιλυλο ομάδα μετακινείται από τον C στο Ο. Πυρηνόφιλη υποκατάσταση στο Si. SS052 Si 3 Na Si 3 Si Si 3 Si 3 Si 3 Central rxn should be shown as an equilibrium going to the right with catalytic base and to the left with a full equivalent of base. Κεντρική αντίδραση μπορεί να δειχθεί σαν μια ισορροπία προς τα δεξιά με καταλυτική βάση και προς τα αριστερά με ολόκληρα ισοδύναμα βάσης. Si 3 Dihydroxylation: Διυδροξυλίωση catalytic base Si 3 καταλυτική βάση Si 3 cat. s 4 3 N vinyl silane βινυλο σιλάνιο product when stoichiometric base is used προϊόν όταν στοιχειομετρική βάση χρησιμοποιείται Si 3 Si 3 Na t 2 verall rxn: insertion of an atom between the Si and the alkene. Συνολική αντίδραση: εισαγωγή ενός ατόμου Ο μεταξύ του Si και του αλκενίου Si 3 Na t 2 Si 3 rook stoichiometric base στοιχειομετρική βάση Si 3 Si3 Si 3 product when catalytic base is used προϊόν όταν καταλυτική βάση χρησιμοποιείται silyl enol ether σιλυλο ενολικός αιθέρας Si3
53 Sila-Pummerer rearrangement: a silyl group migrates to. Αναδιάταξη Sila-Pummerer: μια σιλυλο ομάδα μετακινείται στο Ο. SS053 S Si o C S Si 3 Si 3 S S Si 3 S Si 3 chanism similar to Sila-Pummerer rearrangement except that the Nuc that attacks the Si atom is carbonyl rather than sulfoxide. Μηχανισμός παρόμοιος με την αναδιάταξη Sila-Pummerer εκτός από το ότι το Nuc το οποίο προσβάλλει το άτομο Si είναι το καρβονυλικό Ο αντί το σουλφοξιδικό Ο. Si 3 Si 3 Si 3 P 3 P 3
54 GANTIN CMPUNDS ΟΡΓΑΝΟΚΑΣΣΙΤΕΡΙΚΕΣ ΕΝΩΣΕΙΣ SS054 Tetramethyltin acid chlorides methyl ketones. Τετραμεθυλκασσίτερος χλωρίδια οξέως μεθυλ κετόνες Sn Sn S N 2 reaction at Sn. S N 2 αντίδραση στον Sn r Mg u 3 Sn Snu 3 Mgr Snu 3 Snu 3 Snu3 S N 2 reaction at C. S N 2 αντίδραση στον Sn Li Sn 3 Ts Sn 3
55 Direct hydrostannylation of an alkyne with tin hydride Z-isomer. Άμεσος υδροκασσιτερισμός ενός αλκυνίου με υδρίδιο κασσιτέρου Ζ-ισομερές SS055 xcess tin hydride or enough radicals present isomerization into more stable -isomer. Περίσσεια υδριδίου του κασσιτέρου ή παρουσία αρκετής ρίζας ισομερείωση στο πιο σταθερό Ε-ισομερές u 3 Sn Snu 3. Snu3 Snu 3 Addition of from another molecule of u 3 Sn occurs from the less hindered side Z-vinyl stannane. Προσθήκη υδρογόνου από άλλο μόριο u 3 Sn συμβαίνει από τη λιγότερο παρεμποδισμένη πλευρά Ζ-βινυλο κασσιτερικό If there is more u 3 Sn more stable -isomer. Αν υπάρχει περισσότερο u 3 Sn πιο σταθερό Ε-ισομερές u 3 Sn.. Snu3. Snu3 maintains radical chain συντηρά αλυσίδα ριζών Z Snu 3
56 utyl Li (very reactive nucleophile) reacts at the Sn and expels an organolithium species. Βουτυλο Li (πολύ δραστικό πυρηνόφιλο) αντιδρά στον Sn και αποβάλλει οργανολιθικά είδη SS056 u u u Sn u Li n-u Li u u u Sn u 5-valent Sn anion 5-σθενές ανιόν Sn Li u u Sn u u Li Sn-Li exchange. Ανταλλαγή Sn-Li u 3 Sn t t uli Li t t t t
57 Crotyl stannanes reαct with good stereochemical control, for example: Κροτυλο κασσιτερικά αντιδρούν με καλό στερεοχημικό έλεγχο, για παράδειγμα: SS057 Sn 3 heat 3 Sn 1 1 Z Sn 3 1 heat 3 Sn 1 1 Tin chemistry allows the formation of organolithium compounds that cannot be made by direct lithiation. Η χημεία κασσιτέρου επιτρέπει τη δημιουργία οργανολιθικών ενώσεων τα οποία δεν μπορούν να γίνουν με άμεση λιθίωση. 2 uli 2 uli Li 1 r This problem can be solved by the addition of a tributyltin Li reagent to the aldehyde. Το πρόβλημα αυτό μπορεί να λυθεί με την προσθήκη τριβουτυλκασσιτερικού αντιδραστηρίου Li στην αλδεϋδη. 1 Li Snu 3? 2 r 1 Snu 3? 2 uli 1 Snu 3? 1 2 Li
58 LDA is much less nucleophilic than uli, it removes a proton from tributyltin hydride. LDA είναι λιγότερο πυρηνόφιλο από το uli, διώχνει ένα πρωτόνιο από το τριβουτυλκασσιτερικό υδρίδιο. SS058 Snu 3 LDA TF Li Snu 3 u 4 Sn uli TF u 3 Sn Snu 3 TF solutions of u3sn-li are stable only at low temperatures so the aldehyde must be added immediately. Διαλύματα TF u3sn-li είναι σταθερά μόνο σε χαμηλές θερμοκρασίες έτσι η αλδεϋδη πρέπει να προστεθεί αμέσως. u 3 Sn Snu 3 1. uli, TF 2. C Li N 4 Snu 3 Snu 3 t N 2 t Snu 3
59 SS059 Sn-Li exchange is rapid even at low temperatures. No products from the addition of uli to the carbonyl group are seen. Ανταλλαγή Sn-Li είναι γρήγορη ακόμη και σε χαμηλές θερμοκρασίες. Δε φαίνονται προϊόντα από την προσθήκη uli στην καρβονυλική ομάδα. t Snu 3 Li t t u Li u 3 SnLi adducts with one enantiomer of an acid chloride and resolved by separating the diastereoisomers. u 3 SnLi ενώνεται με ένα εναντιομερές χλωριδίου οξέως και αναλύεται με διαχωρισμό των διαστερεοϊσομερών. (u 3 Sn) 2 1. uli, TF 2. C 3. N 4 Snu 3 CF 3 CF 3 CF 3 Snu 3 Snu 3 eavage of the ester by reduction with DIAL (i-u 2 Al). Μετακίνηση εστέρα με αναγωγή με DIAL. CF 3 Snu 3 DIAL Snu 3 i-pr 2 Nt n n Snu 3 1. uli 2. n
BORON - ΒΟΡΙΟ SBS001. Boron has a vacant p-orbital - Το βόριο έχει ένα άδειο π-τροχιακό. H B. H empty p orbital H H άδειο π-τροχιακό diborane
 oron has a vacant p-orbital - Το βόριο έχει ένα άδειο π-τροχιακό. N - ΒΟΡΙΟ SS001 empty p orbital άδειο π-τροχιακό diborane borane διβοράνιο βοράνιο (a) Vacant p-orbital + lone pair of e - s (ewis base)
oron has a vacant p-orbital - Το βόριο έχει ένα άδειο π-τροχιακό. N - ΒΟΡΙΟ SS001 empty p orbital άδειο π-τροχιακό diborane borane διβοράνιο βοράνιο (a) Vacant p-orbital + lone pair of e - s (ewis base)
SILICON - ΠΥΡΙΤΙΟ. Cl Me. an allyl silane αλλυλo σιλάνιο. a protected alcohol pentacovalent Si alcohol προστατευμένη αλκοόλη πεντασθενές Si αλκοόλη
 -valency = 4 - σθένος = 4 -forms tetrahedral compounds - σχηματίζει τετραεδρικές ενώσεις SILICN - ΠΥΡΙΤΙΟ SBS020 g. a useful electrophile χρήσιμο ηλεκτρονιόφιλο a protected alcohol προστατευμένη αλκοόλη
-valency = 4 - σθένος = 4 -forms tetrahedral compounds - σχηματίζει τετραεδρικές ενώσεις SILICN - ΠΥΡΙΤΙΟ SBS020 g. a useful electrophile χρήσιμο ηλεκτρονιόφιλο a protected alcohol προστατευμένη αλκοόλη
Πυρηνόφιλα του Άνθρακα: ΥΛΙΔΙΑ ΦΩΣΦΟΡΟΥ Αντίδραση WITTIG
 Georg Wittig Νόµπελ Χηµείας 1979 Πυρηνόφιλα του Άνθρακα: ΥΛΙΔΙΑ ΦΩΣΦΟΡΟΥ Αντίδραση WITTIG Υλίδιο: Ουδέτερη ένωση µε αρνητικά φορτισµένο άτοµο (C-) ενωµένο µε θετικά φορτισµένο ετεροάτοµο (P+) Υβρίδιο Δοµών
Georg Wittig Νόµπελ Χηµείας 1979 Πυρηνόφιλα του Άνθρακα: ΥΛΙΔΙΑ ΦΩΣΦΟΡΟΥ Αντίδραση WITTIG Υλίδιο: Ουδέτερη ένωση µε αρνητικά φορτισµένο άτοµο (C-) ενωµένο µε θετικά φορτισµένο ετεροάτοµο (P+) Υβρίδιο Δοµών
Οργανική Χημεία. Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια
 Οργανική Χημεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν ομάδες υδροξυλίου συνδεδεμένες με κορεσμένα άτομα άνθρακα υβριδισμού sp 3 Βάσει παραπάνω ορισμού,
Οργανική Χημεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν ομάδες υδροξυλίου συνδεδεμένες με κορεσμένα άτομα άνθρακα υβριδισμού sp 3 Βάσει παραπάνω ορισμού,
Solutions to the Schrodinger equation atomic orbitals. Ψ 1 s Ψ 2 s Ψ 2 px Ψ 2 py Ψ 2 pz
 Solutions to the Schrodinger equation atomic orbitals Ψ 1 s Ψ 2 s Ψ 2 px Ψ 2 py Ψ 2 pz ybridization Valence Bond Approach to bonding sp 3 (Ψ 2 s + Ψ 2 px + Ψ 2 py + Ψ 2 pz) sp 2 (Ψ 2 s + Ψ 2 px + Ψ 2 py)
Solutions to the Schrodinger equation atomic orbitals Ψ 1 s Ψ 2 s Ψ 2 px Ψ 2 py Ψ 2 pz ybridization Valence Bond Approach to bonding sp 3 (Ψ 2 s + Ψ 2 px + Ψ 2 py + Ψ 2 pz) sp 2 (Ψ 2 s + Ψ 2 px + Ψ 2 py)
Οργανική Χηµεία. Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια
 Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
nitronium ion - ιόν νιτρονίου
 Common Electrophilic eactions Κοινές Ηλεκτροφιλικές Αντιδράσεις A005 ITATI ΝΙΤΡΙΩΣΗ E = 2 nitronium ion ιόν νιτρονίου 3 2 2 S 4 2 3 2S 4 Must use stronger acid than 3 Πρέπει να χρησηµοποιηθεί ισχυρότερο
Common Electrophilic eactions Κοινές Ηλεκτροφιλικές Αντιδράσεις A005 ITATI ΝΙΤΡΙΩΣΗ E = 2 nitronium ion ιόν νιτρονίου 3 2 2 S 4 2 3 2S 4 Must use stronger acid than 3 Πρέπει να χρησηµοποιηθεί ισχυρότερο
Aντιδράσεις Καρβονυλίου C=O (1)
 Aντιδράσεις Καρβονυλίου = (1) Πυρηνόφιλη προσθήκη (αλδεΰδες, κετόνες) Πυρηνόφιλη ακυλο-υποκατάσταση (καρβοξυλικά οξέα και παράγωγα) α-υποκατάσταση (καρβονυλοενώσεις: αλδεΰδες, κετόνες, καρβοξυλικά οξέα
Aντιδράσεις Καρβονυλίου = (1) Πυρηνόφιλη προσθήκη (αλδεΰδες, κετόνες) Πυρηνόφιλη ακυλο-υποκατάσταση (καρβοξυλικά οξέα και παράγωγα) α-υποκατάσταση (καρβονυλοενώσεις: αλδεΰδες, κετόνες, καρβοξυλικά οξέα
Ηλεκτρονιόφιλα Πυρηνόφιλα αντιδραστήρια. Επίκουρος καθηγητής Χρήστος Παππάς
 Ηλεκτρονιόφιλα Πυρηνόφιλα αντιδραστήρια Επίκουρος καθηγητής Χρήστος Παππάς 1 Ηλεκτρονιόφιλα - πυρηνόφιλα αντιδραστήρια Ηλεκτρονιόφιλα λέγονται τα αντιδραστήρια τα οποία δέχονται ένα ή δύο ηλεκτρόνια σε
Ηλεκτρονιόφιλα Πυρηνόφιλα αντιδραστήρια Επίκουρος καθηγητής Χρήστος Παππάς 1 Ηλεκτρονιόφιλα - πυρηνόφιλα αντιδραστήρια Ηλεκτρονιόφιλα λέγονται τα αντιδραστήρια τα οποία δέχονται ένα ή δύο ηλεκτρόνια σε
ΕΝΟΤΗΤΑ
 Παρασκευές Αλδεϋδών - Κετονών 17.9 ΕΝΟΤΗΤΑ 17.9 7.8 7.8 8.5 8.5 16.4 Μηχανισµός Ενυδάτωσης Αλκυνίων µε άλατα υδραργύρου ΕΝΟΤΗΤΑ 8.5 Υδροβορίωση τελικών Αλκυνίων και οξείδωση δίνει αλδεΰδες Παρασκευές Αλδεϋδών
Παρασκευές Αλδεϋδών - Κετονών 17.9 ΕΝΟΤΗΤΑ 17.9 7.8 7.8 8.5 8.5 16.4 Μηχανισµός Ενυδάτωσης Αλκυνίων µε άλατα υδραργύρου ΕΝΟΤΗΤΑ 8.5 Υδροβορίωση τελικών Αλκυνίων και οξείδωση δίνει αλδεΰδες Παρασκευές Αλδεϋδών
Αλκάνια. κορεσμένοι υδρογονάνθρακες. αποτελούνται μόνο από C και H συνδεδεμένα με απλούς δεσμούς. έχουν το γενικό τύπο: C n H 2n+2 (γραμμικά αλκάνια)
 Υδρογονάνθρακες Αλκάνια Alkanes Αλκάνια κορεσμένοι υδρογονάνθρακες αποτελούνται μόνο από C και H συνδεδεμένα με απλούς δεσμούς έχουν το γενικό τύπο: C n H 2n+2 (γραμμικά αλκάνια) Αλκάνια Φυσικές ιδιότητες
Υδρογονάνθρακες Αλκάνια Alkanes Αλκάνια κορεσμένοι υδρογονάνθρακες αποτελούνται μόνο από C και H συνδεδεμένα με απλούς δεσμούς έχουν το γενικό τύπο: C n H 2n+2 (γραμμικά αλκάνια) Αλκάνια Φυσικές ιδιότητες
Κεφάλαιο 2. Οι μεταβλητές των οργανικών αντιδράσεων
 Κεφάλαιο 2 Οι μεταβλητές των οργανικών αντιδράσεων Σύνοψη Στο κεφάλαιο αυτό αναφέρονται οι αντιδράσεις χωρίς τους μηχανισμούς τους, με στόχο να δοθεί έμφαση στις συνέπειες από τις μεταβολές ορισμένων χαρακτηριστικών
Κεφάλαιο 2 Οι μεταβλητές των οργανικών αντιδράσεων Σύνοψη Στο κεφάλαιο αυτό αναφέρονται οι αντιδράσεις χωρίς τους μηχανισμούς τους, με στόχο να δοθεί έμφαση στις συνέπειες από τις μεταβολές ορισμένων χαρακτηριστικών
aldo B 1 Σχήµα 15. Παρουσία κετόνης (πηγή πρωτονίων) προκαλείται σταδιακή µετατροπή του κινητικού µίγµατος ενολικών σε θερµοδυναµικό.
 aldo B 1 ογκώδεις υποκαταστάτες του αζώτου αλλά δηµιουργώντας έτσι αλλυλική τάση Α 1, 2 µε το µεθύλιο της θέσης 1 (τοποθέτηση cis των µεθυλοµάδων στο trans ενολικό). Η ΜΚ του cis-ενολικού µε αξονική µεθυλοµάδα
aldo B 1 ογκώδεις υποκαταστάτες του αζώτου αλλά δηµιουργώντας έτσι αλλυλική τάση Α 1, 2 µε το µεθύλιο της θέσης 1 (τοποθέτηση cis των µεθυλοµάδων στο trans ενολικό). Η ΜΚ του cis-ενολικού µε αξονική µεθυλοµάδα
Αρωματικοί Υδρογονάνθρακες Aromatic Hydrocarbons- Αρένια (Arenes)
 Αρωματικοί Υδρογονάνθρακες Aromatic Hydrocarbons- Αρένια (Arenes) Αρένια- Βενζόλιο C-C (στο βενζόλιο): 1,39Å C-C : 1,54Å Σημείο ζέσης: 80 C C=C: 1,34 Å Οι αρωματικοί υδρογονάνθρακες ή αρένια είναι αδιάλυτα
Αρωματικοί Υδρογονάνθρακες Aromatic Hydrocarbons- Αρένια (Arenes) Αρένια- Βενζόλιο C-C (στο βενζόλιο): 1,39Å C-C : 1,54Å Σημείο ζέσης: 80 C C=C: 1,34 Å Οι αρωματικοί υδρογονάνθρακες ή αρένια είναι αδιάλυτα
O O. i) HOCH 2 CH 2 OH/H + ii) LiAlH 4 iii) H 3 O +
 ACETALS & KETALS Protecting Group Chemistry Χηµεία προστασίας οµάδων CA019 i) ii) Et Et ii) iii) i) C 2 C 2 / ii) LiAl 4 iii) 3 iii) XS F 2 C= 1 o 2 2 Imine Ιµίνη 2 o 2 2 ucleophilicity 1 o = 2 o Πυρηνοφιλικότητα
ACETALS & KETALS Protecting Group Chemistry Χηµεία προστασίας οµάδων CA019 i) ii) Et Et ii) iii) i) C 2 C 2 / ii) LiAl 4 iii) 3 iii) XS F 2 C= 1 o 2 2 Imine Ιµίνη 2 o 2 2 ucleophilicity 1 o = 2 o Πυρηνοφιλικότητα
Πυρηνόφιλη Προσθήκη Αµινών: Ιµίνες και Εναµίνες
 Πυρηνόφιλη Προσθήκη Αµινών: Ιµίνες και Εναµίνες Πυρηνόφιλα Αζώτου - Πρωτοταγείς Αµίνες: ΜΗΧΑΝΙΣΜΟΣ Σχηµατισµός Ιµινών ΣΗΜΑΝΤΙΚΕΣ ΛΕΠΤΟΜΕΡΕΙΕΣ Η ταχύτητα σχηµατισµού ιµίνης εξαρτάται από το ph: Σε υψηλό
Πυρηνόφιλη Προσθήκη Αµινών: Ιµίνες και Εναµίνες Πυρηνόφιλα Αζώτου - Πρωτοταγείς Αµίνες: ΜΗΧΑΝΙΣΜΟΣ Σχηµατισµός Ιµινών ΣΗΜΑΝΤΙΚΕΣ ΛΕΠΤΟΜΕΡΕΙΕΣ Η ταχύτητα σχηµατισµού ιµίνης εξαρτάται από το ph: Σε υψηλό
5.8 Παρασκευές Αλκενίων: Αντιδράσεις απόσπασης. Äρ. ΧÜρηò Ε. ΣεìιδαλÜò Επßκουροò ΚαθηγητÞò ΑΤΕΙ ΑθÞναò
 5.8 Παρασκευές Αλκενίων: Αντιδράσεις απόσπασης Äρ. ΧÜρηò Ε. ΣεìιδαλÜò Επßκουροò ΚαθηγητÞò ΑΤΕΙ ΑθÞναò Σύνοψη των αντιδράσεων της β-απόσπασης Αφυδρογόνωση των αλκανίων: X = Y = Αφυδάτωση των αλκοολών: X
5.8 Παρασκευές Αλκενίων: Αντιδράσεις απόσπασης Äρ. ΧÜρηò Ε. ΣεìιδαλÜò Επßκουροò ΚαθηγητÞò ΑΤΕΙ ΑθÞναò Σύνοψη των αντιδράσεων της β-απόσπασης Αφυδρογόνωση των αλκανίων: X = Y = Αφυδάτωση των αλκοολών: X
Αλκυλαλογονίδια. Επίκουρος καθηγητής Χρήστος Παππάς
 Αλκυλαλογονίδια Επίκουρος καθηγητής Χρήστος Παππάς 1 Αλκυλαλογονίδια Αλκυλαλογονίδια ονομάζονται οι οργανικές ενώσεις οι οποίες, ως λειτουργική ομάδα, διαθέτουν την ομάδα C-X: -X= -F, -Cl, -Br, -I. Η ισχύς
Αλκυλαλογονίδια Επίκουρος καθηγητής Χρήστος Παππάς 1 Αλκυλαλογονίδια Αλκυλαλογονίδια ονομάζονται οι οργανικές ενώσεις οι οποίες, ως λειτουργική ομάδα, διαθέτουν την ομάδα C-X: -X= -F, -Cl, -Br, -I. Η ισχύς
Ε. Μαλαμίδου-Ξενικάκη
 Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 ΑΛΚΥΝΙΑ: C ν H 2ν-2 Ο τριπλός δεσμός άνθρακα άνθρακα Τριπλός δεσμός αλκυνίου ΑΛΚΥΝΙΑ Μόρια πρότυπα για «μοριακούς διακόπτες» Μικροσκοπία σάρωσης σήραγγας (Scanning
Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 ΑΛΚΥΝΙΑ: C ν H 2ν-2 Ο τριπλός δεσμός άνθρακα άνθρακα Τριπλός δεσμός αλκυνίου ΑΛΚΥΝΙΑ Μόρια πρότυπα για «μοριακούς διακόπτες» Μικροσκοπία σάρωσης σήραγγας (Scanning
Οργανική Χημεία ΕΝΟΤΗΤΑ 11: Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών ΑΛΚΕΝΙΑ ΚΑΙ ΑΛΚΙΝΙΑ ΙΔΙΟΤΗΤΕΣ ΚΑΙ ΣΥΝΘΕΣΗ
 Οργανική Χημεία ΕΝΟΤΗΤΑ 11: ΑΛΚΕΝΙΑ ΚΑΙ ΑΛΚΙΝΙΑ ΙΔΙΟΤΗΤΕΣ ΚΑΙ ΣΥΝΘΕΣΗ Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περίληψη ΙΔΙΟΤΗΤΕΣ ΑΛΚΕΝΙΩΝ ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΚΑΙ ΟΝΟΜΑΤΟΛΟΓΙΑ ΣΤΑΘΕΡΟΤΗΤΑ
Οργανική Χημεία ΕΝΟΤΗΤΑ 11: ΑΛΚΕΝΙΑ ΚΑΙ ΑΛΚΙΝΙΑ ΙΔΙΟΤΗΤΕΣ ΚΑΙ ΣΥΝΘΕΣΗ Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περίληψη ΙΔΙΟΤΗΤΕΣ ΑΛΚΕΝΙΩΝ ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΚΑΙ ΟΝΟΜΑΤΟΛΟΓΙΑ ΣΤΑΘΕΡΟΤΗΤΑ
10 o Μάθημα. Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους
 Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους 2017-2018 10 o Μάθημα Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό Προσωπικό,
Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους 2017-2018 10 o Μάθημα Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό Προσωπικό,
4.8 Παρασκευή αλκυλαλογονιδίων από αλκοόλες και υδραλογόνα
 4.8 Παρασκευή αλκυλαλογονιδίων από αλκοόλες και υδραλογόνα RO X RX 2 O ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Αντίδραση αλκοολών με υδραλογόνα RO X RX O δραστικότητα υδραλογόνων I Br Cl
4.8 Παρασκευή αλκυλαλογονιδίων από αλκοόλες και υδραλογόνα RO X RX 2 O ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Αντίδραση αλκοολών με υδραλογόνα RO X RX O δραστικότητα υδραλογόνων I Br Cl
HOMEWORK 4 = G. In order to plot the stress versus the stretch we define a normalized stretch:
 HOMEWORK 4 Problem a For the fast loading case, we want to derive the relationship between P zz and λ z. We know that the nominal stress is expressed as: P zz = ψ λ z where λ z = λ λ z. Therefore, applying
HOMEWORK 4 Problem a For the fast loading case, we want to derive the relationship between P zz and λ z. We know that the nominal stress is expressed as: P zz = ψ λ z where λ z = λ λ z. Therefore, applying
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ
 ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr ΠΥΡΗΝΟΦΙΛΗ ΠΡΟΣΒΟΛΗ ΣΕ ΚΑΡΒΟΝΥΛΙΚΕΣ
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr ΠΥΡΗΝΟΦΙΛΗ ΠΡΟΣΒΟΛΗ ΣΕ ΚΑΡΒΟΝΥΛΙΚΕΣ
2
 1 2 3 4 5 6 7 8 9 Η μικρότερη σταθερότητα της βινυλικής ρίζας (για παράδειγμα σε σχέση με τη μεθυλική) θα μπορούσε να εξηγηθεί στη βάση του πόσο ισχυρά έλκονται τα ηλεκτρόνια από το κάθε άτομο άνθρακα.
1 2 3 4 5 6 7 8 9 Η μικρότερη σταθερότητα της βινυλικής ρίζας (για παράδειγμα σε σχέση με τη μεθυλική) θα μπορούσε να εξηγηθεί στη βάση του πόσο ισχυρά έλκονται τα ηλεκτρόνια από το κάθε άτομο άνθρακα.
Οργανική Χημεία. Κεφάλαιο 5: Επισκόπηση οργανικών αντιδράσεων
 Οργανική Χημεία Κεφάλαιο 5: Επισκόπηση οργανικών αντιδράσεων 1. Κατηγορίες οργανικών αντιδράσεων Γενικά, εξετάζουμε το είδος της αντίδρασης και τον τρόπο που αυτές συντελούνται Γενικοί τύποι αντιδράσεων
Οργανική Χημεία Κεφάλαιο 5: Επισκόπηση οργανικών αντιδράσεων 1. Κατηγορίες οργανικών αντιδράσεων Γενικά, εξετάζουμε το είδος της αντίδρασης και τον τρόπο που αυτές συντελούνται Γενικοί τύποι αντιδράσεων
5.3 Κατηγορίες οργανικών αντιδράσεων και μερικοί μηχανισμοί οργανικών αντιδράσεων
 5. Κατηγορίες οργανικών αντιδράσεων και μερικοί μηχανισμοί οργανικών αντιδράσεων Κατηγορίες οργανικών αντιδράσεων Η ταξινόμηση των οργανικών αντιδράσεων μπορεί να γίνει με δύο διαφορετικούς τρόπους : α.
5. Κατηγορίες οργανικών αντιδράσεων και μερικοί μηχανισμοί οργανικών αντιδράσεων Κατηγορίες οργανικών αντιδράσεων Η ταξινόμηση των οργανικών αντιδράσεων μπορεί να γίνει με δύο διαφορετικούς τρόπους : α.
Περίληψη Κεφαλαίου 5
 Περίληψη Κεφαλαίου 5 Είδη αντιδράσεων: προσθήκης, απόσπασης, υποκατάστασης & αναδιάταξης Μηχανισµός αντίδρασης: πλήρης περιγραφή τρόπου πραγµατοποίησης Μηχανισµοί µέσω ριζών ή πολικοί Πολική αντίδράση
Περίληψη Κεφαλαίου 5 Είδη αντιδράσεων: προσθήκης, απόσπασης, υποκατάστασης & αναδιάταξης Μηχανισµός αντίδρασης: πλήρης περιγραφή τρόπου πραγµατοποίησης Μηχανισµοί µέσω ριζών ή πολικοί Πολική αντίδράση
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ
 ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr Η ΦΥΣΗ ΕΙΝΑΙ ΑΣΥΜΜΕΤΡΗ!!!!!!!!!!!!!!
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr Η ΦΥΣΗ ΕΙΝΑΙ ΑΣΥΜΜΕΤΡΗ!!!!!!!!!!!!!!
Οργανική Χηµεία. Κεφάλαια 10 &11: Αλκυλαλογονίδια, ιδιότητες και αντιδράσεις
 Οργανική Χηµεία Κεφάλαια 10 &11: Αλκυλαλογονίδια, ιδιότητες και αντιδράσεις 1. Αλκυλαλογονίδια Βιοµηχανικοί διαλύτες, εισπνεόµενα αναισθητικά στην ιατρική, ψυκτικά µέσα, εντοµοκτόνα και απολυµαντικά Ευρέως
Οργανική Χηµεία Κεφάλαια 10 &11: Αλκυλαλογονίδια, ιδιότητες και αντιδράσεις 1. Αλκυλαλογονίδια Βιοµηχανικοί διαλύτες, εισπνεόµενα αναισθητικά στην ιατρική, ψυκτικά µέσα, εντοµοκτόνα και απολυµαντικά Ευρέως
ΚΕΦΑΛΑΙΟ 9. Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων
 ΚΕΦΑΛΑΙΟ 9 Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων 1 Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων Το αιθοξυαιθάνιο (διαιθυλαιθέρας ή απλώς «αιθέρας») ανακαλύφθηκε ως αναισθητικό
ΚΕΦΑΛΑΙΟ 9 Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων 1 Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων Το αιθοξυαιθάνιο (διαιθυλαιθέρας ή απλώς «αιθέρας») ανακαλύφθηκε ως αναισθητικό
Α.Π.Α.Υ. ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ
 Α.Π.Α.Υ. ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ Όλα τα παράγωγα καρβοξυλικών οξέων µπορούν να συντεθούν από καρβοξυλικά οξέα, µέσω αντίδρασης πυρηνόφιλης άκυλο υποκατάστασης (ΑΠΥΑ). ΠΑΡΑΣΚΕΥΗ ΧΛΩΡΙΔΙΩΝ ΟΞΕΩΝ ΜΕ SCl 2 ΑΝΤΙΔΡΑΣΗ:
Α.Π.Α.Υ. ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ Όλα τα παράγωγα καρβοξυλικών οξέων µπορούν να συντεθούν από καρβοξυλικά οξέα, µέσω αντίδρασης πυρηνόφιλης άκυλο υποκατάστασης (ΑΠΥΑ). ΠΑΡΑΣΚΕΥΗ ΧΛΩΡΙΔΙΩΝ ΟΞΕΩΝ ΜΕ SCl 2 ΑΝΤΙΔΡΑΣΗ:
ΚΥΠΡΙΑΚΗ ΕΤΑΙΡΕΙΑ ΠΛΗΡΟΦΟΡΙΚΗΣ CYPRUS COMPUTER SOCIETY ΠΑΓΚΥΠΡΙΟΣ ΜΑΘΗΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΠΛΗΡΟΦΟΡΙΚΗΣ 19/5/2007
 Οδηγίες: Να απαντηθούν όλες οι ερωτήσεις. Αν κάπου κάνετε κάποιες υποθέσεις να αναφερθούν στη σχετική ερώτηση. Όλα τα αρχεία που αναφέρονται στα προβλήματα βρίσκονται στον ίδιο φάκελο με το εκτελέσιμο
Οδηγίες: Να απαντηθούν όλες οι ερωτήσεις. Αν κάπου κάνετε κάποιες υποθέσεις να αναφερθούν στη σχετική ερώτηση. Όλα τα αρχεία που αναφέρονται στα προβλήματα βρίσκονται στον ίδιο φάκελο με το εκτελέσιμο
Οργανική Χημεία. Κεφάλαια 20 & 21: Καρβοξυλικά οξέα, παράγωγα τους και αντιδράσεις ακυλο υποκατάστασης
 Οργανική Χημεία Κεφάλαια 20 & 21: Καρβοξυλικά οξέα, παράγωγα τους και αντιδράσεις ακυλο υποκατάστασης 1. Καρβοξυλικά οξέα Σημαντικά ακυλο (-COR) παράγωγα Πλήθος καρβοξυλικών ενώσεων στη φύση, π.χ. οξικό
Οργανική Χημεία Κεφάλαια 20 & 21: Καρβοξυλικά οξέα, παράγωγα τους και αντιδράσεις ακυλο υποκατάστασης 1. Καρβοξυλικά οξέα Σημαντικά ακυλο (-COR) παράγωγα Πλήθος καρβοξυλικών ενώσεων στη φύση, π.χ. οξικό
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Αλκένια. Τα άτομα άνθρακα του διπλού δεσμού έχουν sp 2 υβριδίωση, με
 Αλκένια Ως αλκένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχεται τουλάχιστον ένας διπλός δεσμός =. Είναι δυνατόν να υπάρξουν ως άκυκλα ή κυκλικά αλκένια. Τα άτομα άνθρακα του
Αλκένια Ως αλκένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχεται τουλάχιστον ένας διπλός δεσμός =. Είναι δυνατόν να υπάρξουν ως άκυκλα ή κυκλικά αλκένια. Τα άτομα άνθρακα του
Supporting Information
 Supporting Information rigin of the Regio- and Stereoselectivity of Allylic Substitution of rganocopper Reagents Naohiko Yoshikai, Song-Lin Zhang, and Eiichi Nakamura* Department of Chemistry, The University
Supporting Information rigin of the Regio- and Stereoselectivity of Allylic Substitution of rganocopper Reagents Naohiko Yoshikai, Song-Lin Zhang, and Eiichi Nakamura* Department of Chemistry, The University
Chemistry 506: Allied Health Chemistry 2. Chapter 14: Carboxylic Acids and Esters. Functional Groups with Single & Double Bonds to Oxygen
 Chemistry 506 Dr. Hunter s Class Chapter 14. Chemistry 506: Allied Health Chemistry 2 1 Chapter 14: Carboxylic Acids and Esters Functional Groups with Single & Double Bonds to Oxygen Introduction to General,
Chemistry 506 Dr. Hunter s Class Chapter 14. Chemistry 506: Allied Health Chemistry 2 1 Chapter 14: Carboxylic Acids and Esters Functional Groups with Single & Double Bonds to Oxygen Introduction to General,
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 7 η θεματική ενότητα: Οι αντιδράσεις του διπλού δεσμού
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 7 η θεματική ενότητα: Οι αντιδράσεις του διπλού δεσμού Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 7 η θεματική ενότητα: Οι αντιδράσεις του διπλού δεσμού Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ Α ΕΞΑΜΗΝΟ
 ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ Α ΕΞΑΜΗΝΟ Σύμπλοκες Ενώσεις και η καθοριστική σημασία τους στη γεωργία και τη ζωή. Διδάσκων : ΦΙΛΙΠΠΟΣ ΒΕΡΒΕΡΙΔΗΣ Διάλεξη 9η Κεφ. 9 ΠΕΡΙΕΧΟΜΕΝΑ ΠΩΣ ΔΗΜΙΟΥΡΓΟΥΝΤΑΙ ΤΑ ΣΥΜΠΛΟΚΑ ΑΛΑΤΑ ΟΡΟΛΟΓΙΑ
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ Α ΕΞΑΜΗΝΟ Σύμπλοκες Ενώσεις και η καθοριστική σημασία τους στη γεωργία και τη ζωή. Διδάσκων : ΦΙΛΙΠΠΟΣ ΒΕΡΒΕΡΙΔΗΣ Διάλεξη 9η Κεφ. 9 ΠΕΡΙΕΧΟΜΕΝΑ ΠΩΣ ΔΗΜΙΟΥΡΓΟΥΝΤΑΙ ΤΑ ΣΥΜΠΛΟΚΑ ΑΛΑΤΑ ΟΡΟΛΟΓΙΑ
Κεφάλαιο 4: Ηλεκτρονιόφιλη αλειφατική υποκατάσταση
 Κεφάλαιο 4: Ηλεκτρονιόφιλη αλειφατική υποκατάσταση Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων ηλεκτρονιόφιλης αλειφατικής υποκατάστασης [μηχανισμοί S E 1, S E 2 (εμπρόσθιος και οπίσθιος)
Κεφάλαιο 4: Ηλεκτρονιόφιλη αλειφατική υποκατάσταση Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων ηλεκτρονιόφιλης αλειφατικής υποκατάστασης [μηχανισμοί S E 1, S E 2 (εμπρόσθιος και οπίσθιος)
The Simply Typed Lambda Calculus
 Type Inference Instead of writing type annotations, can we use an algorithm to infer what the type annotations should be? That depends on the type system. For simple type systems the answer is yes, and
Type Inference Instead of writing type annotations, can we use an algorithm to infer what the type annotations should be? That depends on the type system. For simple type systems the answer is yes, and
derivation of the Laplacian from rectangular to spherical coordinates
 derivation of the Laplacian from rectangular to spherical coordinates swapnizzle 03-03- :5:43 We begin by recognizing the familiar conversion from rectangular to spherical coordinates (note that φ is used
derivation of the Laplacian from rectangular to spherical coordinates swapnizzle 03-03- :5:43 We begin by recognizing the familiar conversion from rectangular to spherical coordinates (note that φ is used
Περίληψη Κεφαλαίου 2
 Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
Κεφάλαιο 2: Πυρηνόφιλη αλειφατική υποκατάσταση
 Κεφάλαιο 2: Πυρηνόφιλη αλειφατική υποκατάσταση Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων πυρηνόφιλης αλειφατικής υποκατάστασης (μηχανισμοί S N 1 και S N 2) και τις παραμέτρους που
Κεφάλαιο 2: Πυρηνόφιλη αλειφατική υποκατάσταση Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων πυρηνόφιλης αλειφατικής υποκατάστασης (μηχανισμοί S N 1 και S N 2) και τις παραμέτρους που
EE512: Error Control Coding
 EE512: Error Control Coding Solution for Assignment on Finite Fields February 16, 2007 1. (a) Addition and Multiplication tables for GF (5) and GF (7) are shown in Tables 1 and 2. + 0 1 2 3 4 0 0 1 2 3
EE512: Error Control Coding Solution for Assignment on Finite Fields February 16, 2007 1. (a) Addition and Multiplication tables for GF (5) and GF (7) are shown in Tables 1 and 2. + 0 1 2 3 4 0 0 1 2 3
Δομή. Ως συζυγιακά διένια ορίζουμε τους υδρογονάνθρακες που στην. κύριο χαρακτηριστικό την εναλλαγή των δεσμών (απλών και διπλών) στο μόριο.
 ΣΥΖΥΓΙΑΚA ΔΙΕΝΙA Δομή Ως συζυγιακά διένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχουν δυο διπλούς δεσμούς με κύριο χαρακτηριστικό την εναλλαγή των δεσμών (απλών και διπλών)
ΣΥΖΥΓΙΑΚA ΔΙΕΝΙA Δομή Ως συζυγιακά διένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχουν δυο διπλούς δεσμούς με κύριο χαρακτηριστικό την εναλλαγή των δεσμών (απλών και διπλών)
Οργανική Χημεία ΕΝΟΤΗΤΑ 12: Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών ΑΝΤΙΔΡΑΣΕΙΣ ΠΡΟΣΘΗΚΗΣ ΣΕ ΑΛΚΕΝΙΑ
 Οργανική Χημεία ΕΝΟΤΗΤΑ 12: ΑΝΤΙΔΡΑΣΕΙΣ ΠΡΟΣΘΗΚΗΣ ΣΕ ΑΛΚΕΝΙΑ Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περίληψη ΑΝΤΙΔΡΑΣΕΙΣ ΠΡΟΣΘΗΚΗΣ ΣΕ ΑΛΚΕΝΙΑ ΓΕΝΙΚΟΣ ΜΗΧΑΝΙΣΜΟΣ ΗΛΕΚΤΡΟΝΙΟΦΙΛΗΣ ΠΡΟΣΘΗΚΗΣ
Οργανική Χημεία ΕΝΟΤΗΤΑ 12: ΑΝΤΙΔΡΑΣΕΙΣ ΠΡΟΣΘΗΚΗΣ ΣΕ ΑΛΚΕΝΙΑ Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περίληψη ΑΝΤΙΔΡΑΣΕΙΣ ΠΡΟΣΘΗΚΗΣ ΣΕ ΑΛΚΕΝΙΑ ΓΕΝΙΚΟΣ ΜΗΧΑΝΙΣΜΟΣ ΗΛΕΚΤΡΟΝΙΟΦΙΛΗΣ ΠΡΟΣΘΗΚΗΣ
ΑΝΑΓΩΓΗ ΚΑΡΒΟΝΥΛΙΟΥ. O Me 3 SiCl. Μόνο σε κυκλοεξανικά παράγωγα R 2 C R 3. R 1 H p-tosyl = p-ts + H 2 NHN SO 2 CH 3. 2RLi. - Ts.
 ΑΝΑΓΩΓΗ ΚΑΡΒΟΝΥΛΙΟΥ Me 3 Sil Zn Μόνο σε κυκλοεξανικά παράγωγα R 2 R 3 + 2 S 2 3 R 1 p-tosyl = p-ts R 2 R 3 2RLi R 2 R 3 - Ts R 1 Ts R 1 Ts R 2 R 3 R 2 R 3 R 2-2 2 R 3 R 1 Li R 1 Li R 1 Κ. Τσολερίδης Τμ.
ΑΝΑΓΩΓΗ ΚΑΡΒΟΝΥΛΙΟΥ Me 3 Sil Zn Μόνο σε κυκλοεξανικά παράγωγα R 2 R 3 + 2 S 2 3 R 1 p-tosyl = p-ts R 2 R 3 2RLi R 2 R 3 - Ts R 1 Ts R 1 Ts R 2 R 3 R 2 R 3 R 2-2 2 R 3 R 1 Li R 1 Li R 1 Κ. Τσολερίδης Τμ.
60
 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 Η (συνήθης) αύξηση του πυρηνόφιλου χαρακτήρα όσο κατερχόμαστε σε μία ομάδα του περιοδικού πίνακα οφείλεται στην αντίστοιχη μείωση της ηλεκτραρνητικότητας
59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 Η (συνήθης) αύξηση του πυρηνόφιλου χαρακτήρα όσο κατερχόμαστε σε μία ομάδα του περιοδικού πίνακα οφείλεται στην αντίστοιχη μείωση της ηλεκτραρνητικότητας
ιαστερεοεκλεκτικότητα σε κυκλικά δικυκλικά µόρια. Πενταµελείς και εξαµελείς συµπυκνωµένοι δακτύλιοι.
 diabicy1 1 ιαστερεοεκλεκτικότητα σε κυκλικά δικυκλικά µόρια. Πενταµελείς και εξαµελείς συµπυκνωµένοι δακτύλιοι. Cis-συµπυκνωµένοι πενταµελείς δακτύλιοι. Ένα δικυκλικό σύστηµα µε δυο συµπυκνωµένους πενταµελείς
diabicy1 1 ιαστερεοεκλεκτικότητα σε κυκλικά δικυκλικά µόρια. Πενταµελείς και εξαµελείς συµπυκνωµένοι δακτύλιοι. Cis-συµπυκνωµένοι πενταµελείς δακτύλιοι. Ένα δικυκλικό σύστηµα µε δυο συµπυκνωµένους πενταµελείς
Κεφάλαιο 6: Αντιδράσεις ενολών και ενολικών ανιόντων
 Κεφάλαιο 6: Αντιδράσεις ενολών και ενολικών ανιόντων Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων των ενολών και των ενολικών ανιόντων εστιάζοντας κυρίως σε εκείνα που προέρχονται από
Κεφάλαιο 6: Αντιδράσεις ενολών και ενολικών ανιόντων Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων των ενολών και των ενολικών ανιόντων εστιάζοντας κυρίως σε εκείνα που προέρχονται από
[1] P Q. Fig. 3.1
![[1] P Q. Fig. 3.1 [1] P Q. Fig. 3.1](/thumbs/79/80362156.jpg) 1 (a) Define resistance....... [1] (b) The smallest conductor within a computer processing chip can be represented as a rectangular block that is one atom high, four atoms wide and twenty atoms long. One
1 (a) Define resistance....... [1] (b) The smallest conductor within a computer processing chip can be represented as a rectangular block that is one atom high, four atoms wide and twenty atoms long. One
Phys460.nb Solution for the t-dependent Schrodinger s equation How did we find the solution? (not required)
 Phys460.nb 81 ψ n (t) is still the (same) eigenstate of H But for tdependent H. The answer is NO. 5.5.5. Solution for the tdependent Schrodinger s equation If we assume that at time t 0, the electron starts
Phys460.nb 81 ψ n (t) is still the (same) eigenstate of H But for tdependent H. The answer is NO. 5.5.5. Solution for the tdependent Schrodinger s equation If we assume that at time t 0, the electron starts
Οργανική Χημεία. Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες
 Οργανική Χημεία Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες 1. Καρβονυλικές ενώσεις Καρβονυλική ομάδα C=O σημαντικότερη λειτουργική ομάδα οργανικής χημείας Καρβονυλικές ομάδες βρίσκονται
Οργανική Χημεία Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες 1. Καρβονυλικές ενώσεις Καρβονυλική ομάδα C=O σημαντικότερη λειτουργική ομάδα οργανικής χημείας Καρβονυλικές ομάδες βρίσκονται
Ηλεκτρονιόφιλη αρωµατική υποκατάσταση
 Ηλεκτρονιόφιλη αρωµατική υποκατάσταση Νικόλαος Αργυρόπουλος Θεσσαλονίκη 2007 Τυπικές αντιδράσεις ηλεκτρονιόφιλης αρωµατικής υποκατάστασης Ηλεκτρονιόφιλη προσθήκη στα αλκένια Μηχανισµός C C C C C C Το ηλεκτρονικό
Ηλεκτρονιόφιλη αρωµατική υποκατάσταση Νικόλαος Αργυρόπουλος Θεσσαλονίκη 2007 Τυπικές αντιδράσεις ηλεκτρονιόφιλης αρωµατικής υποκατάστασης Ηλεκτρονιόφιλη προσθήκη στα αλκένια Μηχανισµός C C C C C C Το ηλεκτρονικό
Κεφάλαιο 3. Στοιχειώδεις αντιδράσεις στην Οργανική Χημεία
 Κεφάλαιο 3 Στοιχειώδεις αντιδράσεις στην Οργανική Χημεία Σύνοψη Στο κεφάλαιο αυτό παρουσιάζονται οι στοιχειώδεις αντιδράσεις στην Οργανική Χημεία, οι οποίες μπορούν να διαχωριστούν στις εξής κατηγορίες:
Κεφάλαιο 3 Στοιχειώδεις αντιδράσεις στην Οργανική Χημεία Σύνοψη Στο κεφάλαιο αυτό παρουσιάζονται οι στοιχειώδεις αντιδράσεις στην Οργανική Χημεία, οι οποίες μπορούν να διαχωριστούν στις εξής κατηγορίες:
Capacitors - Capacitance, Charge and Potential Difference
 Capacitors - Capacitance, Charge and Potential Difference Capacitors store electric charge. This ability to store electric charge is known as capacitance. A simple capacitor consists of 2 parallel metal
Capacitors - Capacitance, Charge and Potential Difference Capacitors store electric charge. This ability to store electric charge is known as capacitance. A simple capacitor consists of 2 parallel metal
ΣΤΕΡΕΟΗΛΕΚΤΡΟΝΙΚΑ ΕΛΕΓΧΟΜΕΝΕΙΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΕ ΚΥΚΛΟΕΞΑΝΙΑ ΜΕ ΟΜΗ ΗΜΙΑΝΑΚΛΙΝΤΡΟΥ α. διάνοιξη του οξιρανικού δακτυλίου σε κυκλοεξενοξείδια.
 bstelc ΣΤΕΡΕΟΗΛΕΚΤΡΟΝΙΚΑ ΕΛΕΓΧΟΜΕΝΕΙΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΕ ΚΥΚΛΟΕΞΑΝΙΑ ΜΕ ΟΜΗ ΗΜΙΑΝΑΚΛΙΝΤΡΟΥ α. διάνοιξη του οξιρανικού δακτυλίου σε κυκλοεξενοξείδια. Όπως έχει αναφερθεί κατά τη συζήτηση των διαµορφώσεων των
bstelc ΣΤΕΡΕΟΗΛΕΚΤΡΟΝΙΚΑ ΕΛΕΓΧΟΜΕΝΕΙΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΕ ΚΥΚΛΟΕΞΑΝΙΑ ΜΕ ΟΜΗ ΗΜΙΑΝΑΚΛΙΝΤΡΟΥ α. διάνοιξη του οξιρανικού δακτυλίου σε κυκλοεξενοξείδια. Όπως έχει αναφερθεί κατά τη συζήτηση των διαµορφώσεων των
Mean bond enthalpy Standard enthalpy of formation Bond N H N N N N H O O O
 Q1. (a) Explain the meaning of the terms mean bond enthalpy and standard enthalpy of formation. Mean bond enthalpy... Standard enthalpy of formation... (5) (b) Some mean bond enthalpies are given below.
Q1. (a) Explain the meaning of the terms mean bond enthalpy and standard enthalpy of formation. Mean bond enthalpy... Standard enthalpy of formation... (5) (b) Some mean bond enthalpies are given below.
ΕΣΤΕΡΕΣ. Ένα αντιβιοτικό προφάρµακο. Υδρόλυση του εστέρα απελευθερώνει την ενεργή χλωραµφαινικόλη
 ΕΣΤΕΡΕΣ Ένα αντιβιοτικό προφάρµακο. Υδρόλυση του εστέρα απελευθερώνει την ενεργή χλωραµφαινικόλη Πολυµερή «σταδιακής ανάπτυξης» Σύγκρινε µε τα «αλυσιδωτής αντίδρασης» (Ενότητα 7.11) PET (Dacron, Mylar):
ΕΣΤΕΡΕΣ Ένα αντιβιοτικό προφάρµακο. Υδρόλυση του εστέρα απελευθερώνει την ενεργή χλωραµφαινικόλη Πολυµερή «σταδιακής ανάπτυξης» Σύγκρινε µε τα «αλυσιδωτής αντίδρασης» (Ενότητα 7.11) PET (Dacron, Mylar):
Αντιδράσεις Πολυμερών
 Αντιδράσεις Πολυμερών Αντιδράσεις Μετατροπής Πολυμερών Αντιδράσεις που αφορούν την κυρία αλυσίδα Αντιδράσεις που αφορούν πλευρικές ομάδες R Αντιδράσεις τελικής ομάδας X R X Y Αντιδράσεις Κύριας Αλυσίδας
Αντιδράσεις Πολυμερών Αντιδράσεις Μετατροπής Πολυμερών Αντιδράσεις που αφορούν την κυρία αλυσίδα Αντιδράσεις που αφορούν πλευρικές ομάδες R Αντιδράσεις τελικής ομάδας X R X Y Αντιδράσεις Κύριας Αλυσίδας
Non Aromatic Heterocyclic Chemistry & Natural Products Μη αρωματική ετεροκυκλική Χημεία και Φυσικά Προϊόντα
 on Aromatic eterocyclic Chemistry & atural Products Μη αρωματική ετεροκυκλική Χημεία και Φυσικά Προϊόντα A001 ubjects: 1. mall ring (3 & 4); steroids & β-lactones (lactams). 2. 5 & 6 medium rings; carbohydrate
on Aromatic eterocyclic Chemistry & atural Products Μη αρωματική ετεροκυκλική Χημεία και Φυσικά Προϊόντα A001 ubjects: 1. mall ring (3 & 4); steroids & β-lactones (lactams). 2. 5 & 6 medium rings; carbohydrate
ΑΝΟΡΓΑΝΗ ΙΙΙ. Prof. Dr. Maria Louloudi. Laboratory of Biomimetic Catalysis & Biomimetic Materials. Chemistry Department. University of Ioannina
 Prof. Dr. Maria Louloudi Laboratory of Biomimetic Catalysis & Biomimetic Materials Chemistry Department University of Ioannina ΑΝΟΡΓΑΝΗ ΙΙΙ Μηχανισµοί Ανόργανων Αντιδράσεων (στοιχειοµετρικές αντιδράσεις)
Prof. Dr. Maria Louloudi Laboratory of Biomimetic Catalysis & Biomimetic Materials Chemistry Department University of Ioannina ΑΝΟΡΓΑΝΗ ΙΙΙ Μηχανισµοί Ανόργανων Αντιδράσεων (στοιχειοµετρικές αντιδράσεις)
HET 020. δ 6.87. σ-effect not so strong. δ 6.99 ΘΕΙΟΦΑΝΙΟ THIOPHENE PHYSICAL AND SPECTROSCOPIC PROPOERTIES ΦΥΣΙΚΕΣ ΚΑΙ ΦΑΣΜΑΤΟΣΚΟΠΙΚΕΣ ΙΔΙΟΤΗΤΕΣ
 TIPEE ΘΕΙΟΦΑΝΙΟ ET 020 PYICAL AD PECTCPIC PPETIE ΦΥΣΙΚΕΣ ΚΑΙ ΦΑΣΜΑΤΟΣΚΟΠΙΚΕΣ ΙΔΙΟΤΗΤΕΣ LIQUID, BP 84 o C PLAA VEY IMILA T BEZEE ΚΑΚΟΣ ΔΟΤΗΣ e - ΚΑΚΟ π ΤΡΟΧΙΑΚΟ ΑΛΛΗΛΟΕΠΙΚΑΛΥΨΗ: ΕΠΟΜΕΝΩΣ ΜΕΓΑΛΥΤΕΡΑ δ poor
TIPEE ΘΕΙΟΦΑΝΙΟ ET 020 PYICAL AD PECTCPIC PPETIE ΦΥΣΙΚΕΣ ΚΑΙ ΦΑΣΜΑΤΟΣΚΟΠΙΚΕΣ ΙΔΙΟΤΗΤΕΣ LIQUID, BP 84 o C PLAA VEY IMILA T BEZEE ΚΑΚΟΣ ΔΟΤΗΣ e - ΚΑΚΟ π ΤΡΟΧΙΑΚΟ ΑΛΛΗΛΟΕΠΙΚΑΛΥΨΗ: ΕΠΟΜΕΝΩΣ ΜΕΓΑΛΥΤΕΡΑ δ poor
Περίληψη Κεφαλαίου 4
 Περίληψη Κεφαλαίου 4 Αλκάνια: διαθέτουν διαµορφώσεις που αλληλοµετατρέπονται Προβολές κατά Newman: απεικόνιση αλλαγών λόγω περιστροφής απλού δεσµού Διαβαθµισµένη διαµόρφωση αιθανίου σταθερότερη κατά 12
Περίληψη Κεφαλαίου 4 Αλκάνια: διαθέτουν διαµορφώσεις που αλληλοµετατρέπονται Προβολές κατά Newman: απεικόνιση αλλαγών λόγω περιστροφής απλού δεσµού Διαβαθµισµένη διαµόρφωση αιθανίου σταθερότερη κατά 12
Οργανική Χημεία. Κεφάλαιο 16: Χημεία του βενζολίου: ηλεκτρονιόφιλη αρωματική υποκατάσταση
 Οργανική Χημεία Κεφάλαιο 16: Χημεία του βενζολίου: ηλεκτρονιόφιλη αρωματική υποκατάσταση 1. Αντιδράσεις αρωματικών ενώσεων Σημαντικότερη αντίδραση αρωματικών ενώσεων: ηλεκτρονιόφιλη αρωματική υποκατάσταση
Οργανική Χημεία Κεφάλαιο 16: Χημεία του βενζολίου: ηλεκτρονιόφιλη αρωματική υποκατάσταση 1. Αντιδράσεις αρωματικών ενώσεων Σημαντικότερη αντίδραση αρωματικών ενώσεων: ηλεκτρονιόφιλη αρωματική υποκατάσταση
ΑΝΤΩΝΗΣ ΚΟΛΟΚΟΥΡΗΣ ANAΠΛΗΡΩΤΗΣ ΚΑΘΗΓΗΤΗΣ ΦΑΡΜΑΚΟΧΗΜΕΙΑΣ. PDF created with pdffactory trial version www.pdffactory.com
 ΑΝΤΩΝΗΣ ΚΟΛΟΚΟΥΡΗΣ ANAΠΛΗΡΩΤΗΣ ΚΑΘΗΓΗΤΗΣ ΦΑΡΜΑΚΟΧΗΜΕΙΑΣ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΙΙ Γιατί χρειάζεται ηοργανική χημεία στη Φαρμακευτική; Θεραπευτική και Φαρμακευτική Επιστήμη γνώσεις ιατρικής επιστήμης (φυσιολογία,
ΑΝΤΩΝΗΣ ΚΟΛΟΚΟΥΡΗΣ ANAΠΛΗΡΩΤΗΣ ΚΑΘΗΓΗΤΗΣ ΦΑΡΜΑΚΟΧΗΜΕΙΑΣ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΙΙ Γιατί χρειάζεται ηοργανική χημεία στη Φαρμακευτική; Θεραπευτική και Φαρμακευτική Επιστήμη γνώσεις ιατρικής επιστήμης (φυσιολογία,
Μέθοδοι παρασκευής κλασικών συμπλόκων ενώσεων
 ΣΚΟΠΟΣ Ο σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε τις σημαντικότερες παραμέτρους που παίζουν ρόλο στη σύνθεση συμπλόκων ενώσεων, καθώς και τον τρόπο με τον οποίον γίνεται η ταξινόμηση των αντιδράσεων
ΣΚΟΠΟΣ Ο σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε τις σημαντικότερες παραμέτρους που παίζουν ρόλο στη σύνθεση συμπλόκων ενώσεων, καθώς και τον τρόπο με τον οποίον γίνεται η ταξινόμηση των αντιδράσεων
Καρβοξυλικά οξέα R-COOH (1)
 Καρβοξυλικά οξέα - (1) Δομή, φυσικές ιδιότητες Οξύτητα Σύνθεση καρβοξυλικών οξέων Aντιδράσεις καρβοξυλικών οξέων Καρβοξυλικά οξέα - (2) Ονοματολογία -ιο fi -οϊκό 3 2 προπανοϊκό οξύ 3 1 3 2 2 5 4 3 2 4-μεθυλοπεντανοϊκό
Καρβοξυλικά οξέα - (1) Δομή, φυσικές ιδιότητες Οξύτητα Σύνθεση καρβοξυλικών οξέων Aντιδράσεις καρβοξυλικών οξέων Καρβοξυλικά οξέα - (2) Ονοματολογία -ιο fi -οϊκό 3 2 προπανοϊκό οξύ 3 1 3 2 2 5 4 3 2 4-μεθυλοπεντανοϊκό
Οργανική Χημεία ΕΝΟΤΗΤΑ 10: Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών ΑΝΤΙΔΡΑΣΕΙΣ ΑΠΟΣΠΑΣΗΣ ΥΠΟΚΑΤΑΣΤΑΣΗ VS ΑΠΟΣΠΑΣΗ
 Οργανική Χημεία ΕΝΟΤΗΤΑ 10: ΑΝΤΙΔΡΑΣΕΙΣ ΑΠΟΣΠΑΣΗΣ ΥΠΟΚΑΤΑΣΤΑΣΗ VS ΑΠΟΣΠΑΣΗ Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περίληψη ΑΝΤΙΔΡΑΣΕΙΣ ΑΠΟΣΠΑΣΗΣ ΑΝΤΙΔΡΑΣΕΙΣ ΑΠΟΣΠΑΣΗΣ ΑΛΚΥΛΑΛΟΓΟΝΙΔΙΩΝ
Οργανική Χημεία ΕΝΟΤΗΤΑ 10: ΑΝΤΙΔΡΑΣΕΙΣ ΑΠΟΣΠΑΣΗΣ ΥΠΟΚΑΤΑΣΤΑΣΗ VS ΑΠΟΣΠΑΣΗ Ε. Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περίληψη ΑΝΤΙΔΡΑΣΕΙΣ ΑΠΟΣΠΑΣΗΣ ΑΝΤΙΔΡΑΣΕΙΣ ΑΠΟΣΠΑΣΗΣ ΑΛΚΥΛΑΛΟΓΟΝΙΔΙΩΝ
ΚΕΦΑΛΑΙΟ ΕΝΝΕΑ. Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων
 ΚΕΦΑΛΑΙΟ ΕΝΝΕΑ Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων Το αιθοξυαιθάνιο (διαιθυλαιθέρας ή απλώς «αιθέρας») ανακαλύφθηκε ως
ΚΕΦΑΛΑΙΟ ΕΝΝΕΑ Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων Το αιθοξυαιθάνιο (διαιθυλαιθέρας ή απλώς «αιθέρας») ανακαλύφθηκε ως
1.6 Other Intramolecular Decarboxylative Coupling Reactions Decarboxylative Coupling Reaction of Allyl Carboxylates
 Contents Part I New Carbon Carbon Coupling Reactions Based on Decarboxylation 1 Transition Metal-Catalyzed Decarboxylation and Decarboxylative Cross-Couplings... 3 1.1 Introduction... 3 1.2 Metal-Catalyzed
Contents Part I New Carbon Carbon Coupling Reactions Based on Decarboxylation 1 Transition Metal-Catalyzed Decarboxylation and Decarboxylative Cross-Couplings... 3 1.1 Introduction... 3 1.2 Metal-Catalyzed
Assalamu `alaikum wr. wb.
 LUMP SUM Assalamu `alaikum wr. wb. LUMP SUM Wassalamu alaikum wr. wb. Assalamu `alaikum wr. wb. LUMP SUM Wassalamu alaikum wr. wb. LUMP SUM Lump sum lump sum lump sum. lump sum fixed price lump sum lump
LUMP SUM Assalamu `alaikum wr. wb. LUMP SUM Wassalamu alaikum wr. wb. Assalamu `alaikum wr. wb. LUMP SUM Wassalamu alaikum wr. wb. LUMP SUM Lump sum lump sum lump sum. lump sum fixed price lump sum lump
ΚΑΡΒΟΝΥΛΙΚΕΣ ΕΝΩΣΕΙΣ
 ΚΑΡΒΟΝΥΛΙΚΕΣ ΕΝΩΣΕΙΣ Ονοματολογία κατά IUPAC Αλδεϋδες Ονομασία μητρικής ένωσης :. 1. Η μακρύτερη ανθρακική αλυσίδα που περιέχει την καρβονυλομάδα λαμβάνεται ως η βασική δομή 2. Ονομάζεται ο αντίστοιχος
ΚΑΡΒΟΝΥΛΙΚΕΣ ΕΝΩΣΕΙΣ Ονοματολογία κατά IUPAC Αλδεϋδες Ονομασία μητρικής ένωσης :. 1. Η μακρύτερη ανθρακική αλυσίδα που περιέχει την καρβονυλομάδα λαμβάνεται ως η βασική δομή 2. Ονομάζεται ο αντίστοιχος
Καρβονυλικές ενώσεις. Επίκουρος καθηγητής Χρήστος Παππάς
 Επίκουρος καθηγητής Χρήστος Παππάς 1 Καρβονυλικές λειτουργική ομάδα το C=O. ονομάζονται οι ενώσεις οι οποίες περιέχουν ως αλδεΰδες κετόνες οξέα C O Χλωρίδια οξέων εστέρες αμίδια 2 Δομή καρβονυλίου - Δραστικότητα
Επίκουρος καθηγητής Χρήστος Παππάς 1 Καρβονυλικές λειτουργική ομάδα το C=O. ονομάζονται οι ενώσεις οι οποίες περιέχουν ως αλδεΰδες κετόνες οξέα C O Χλωρίδια οξέων εστέρες αμίδια 2 Δομή καρβονυλίου - Δραστικότητα
Ηλεκτρονικά Φαινόμενα
 Ηλεκτρονικά Φαινόμενα Το επαγωγικό όμως φαινόμενο οδηγεί στη διάχυση της πόλωσης και στο υπόλοιπο μόριο. Έτσι πολώνονται, με φθίνουσα όμως ένταση, και οι επόμενοι άνθρακες που είναι συνδεδεμένοι μέσω σ
Ηλεκτρονικά Φαινόμενα Το επαγωγικό όμως φαινόμενο οδηγεί στη διάχυση της πόλωσης και στο υπόλοιπο μόριο. Έτσι πολώνονται, με φθίνουσα όμως ένταση, και οι επόμενοι άνθρακες που είναι συνδεδεμένοι μέσω σ
3.4 SUM AND DIFFERENCE FORMULAS. NOTE: cos(α+β) cos α + cos β cos(α-β) cos α -cos β
 3.4 SUM AND DIFFERENCE FORMULAS Page Theorem cos(αβ cos α cos β -sin α cos(α-β cos α cos β sin α NOTE: cos(αβ cos α cos β cos(α-β cos α -cos β Proof of cos(α-β cos α cos β sin α Let s use a unit circle
3.4 SUM AND DIFFERENCE FORMULAS Page Theorem cos(αβ cos α cos β -sin α cos(α-β cos α cos β sin α NOTE: cos(αβ cos α cos β cos(α-β cos α -cos β Proof of cos(α-β cos α cos β sin α Let s use a unit circle
Χημεία Γ Λυκείου Διαγώνισμα 1 ο 1 ο Κεφ. :μέχρι και περιοδικός πίνακας. 5 ο Κεφ. : μέχρι και απόσπαση. Θέμα 1 ο
 Χημεία Γ Λυκείου Διαγώνισμα 1 ο 1 ο Κεφ. :μέχρι και περιοδικός πίνακας. 5 ο Κεφ. : μέχρι και απόσπαση. Θέμα 1 ο Σημειώστε πάνω στα θέματα την σωστή απάντηση στις ερωτήσεις 1.1 έως 1.5 1.1. Κατά τις μεταπτώσεις:
Χημεία Γ Λυκείου Διαγώνισμα 1 ο 1 ο Κεφ. :μέχρι και περιοδικός πίνακας. 5 ο Κεφ. : μέχρι και απόσπαση. Θέμα 1 ο Σημειώστε πάνω στα θέματα την σωστή απάντηση στις ερωτήσεις 1.1 έως 1.5 1.1. Κατά τις μεταπτώσεις:
Κεφάλαιο 5: Προσθήκες σε πολλαπλούς δεσμούς
 Κεφάλαιο 5: Προσθήκες σε πολλαπλούς δεσμούς Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων προσθήκης σε μεμονωμένους και συζυγιακούς δεσμούς C=C (ηλεκτρονιόφιλες και πυρηνόφιλες), σε δεσμούς
Κεφάλαιο 5: Προσθήκες σε πολλαπλούς δεσμούς Σύνοψη Το κεφάλαιο αυτό ασχολείται με τη μελέτη των αντιδράσεων προσθήκης σε μεμονωμένους και συζυγιακούς δεσμούς C=C (ηλεκτρονιόφιλες και πυρηνόφιλες), σε δεσμούς
Homework 3 Solutions
 Homework 3 Solutions Igor Yanovsky (Math 151A TA) Problem 1: Compute the absolute error and relative error in approximations of p by p. (Use calculator!) a) p π, p 22/7; b) p π, p 3.141. Solution: For
Homework 3 Solutions Igor Yanovsky (Math 151A TA) Problem 1: Compute the absolute error and relative error in approximations of p by p. (Use calculator!) a) p π, p 22/7; b) p π, p 3.141. Solution: For
ΚΑΡΒΟΞΥΛΙΚΑ ΟΞΕΑ ΚΑΙ ΠΑΡΑΓΩΓΑ
 ΚΑΡΒΟΞΥΛΙΚΑ ΟΞΕΑ ΚΑΙ ΠΑΡΑΓΩΓΑ Εισαγωγή στα Καρβοξυλικά Οξέα Ονοματολογία των Καρβοξυλικών Οξέων Δομή και Ιδιότητες των Καρβοξυλικών Οξέων Παρασκευή των Καρβοξυλικών Οξέων Αντιδράσεις των Καρβοξυλικών Οξέων
ΚΑΡΒΟΞΥΛΙΚΑ ΟΞΕΑ ΚΑΙ ΠΑΡΑΓΩΓΑ Εισαγωγή στα Καρβοξυλικά Οξέα Ονοματολογία των Καρβοξυλικών Οξέων Δομή και Ιδιότητες των Καρβοξυλικών Οξέων Παρασκευή των Καρβοξυλικών Οξέων Αντιδράσεις των Καρβοξυλικών Οξέων
7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή
 7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή Στερεοχημεία της προσθήκης στα αλκένια C C + E Y E C C Y Για να μάθετε να κατανοείτε τη στερεοχημεία του προϊόντος, χρειάζεται να γνωρίζετε δυο πράγματα:
7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή Στερεοχημεία της προσθήκης στα αλκένια C C + E Y E C C Y Για να μάθετε να κατανοείτε τη στερεοχημεία του προϊόντος, χρειάζεται να γνωρίζετε δυο πράγματα:
Approximation of distance between locations on earth given by latitude and longitude
 Approximation of distance between locations on earth given by latitude and longitude Jan Behrens 2012-12-31 In this paper we shall provide a method to approximate distances between two points on earth
Approximation of distance between locations on earth given by latitude and longitude Jan Behrens 2012-12-31 In this paper we shall provide a method to approximate distances between two points on earth
(1) Describe the process by which mercury atoms become excited in a fluorescent tube (3)
 Q1. (a) A fluorescent tube is filled with mercury vapour at low pressure. In order to emit electromagnetic radiation the mercury atoms must first be excited. (i) What is meant by an excited atom? (1) (ii)
Q1. (a) A fluorescent tube is filled with mercury vapour at low pressure. In order to emit electromagnetic radiation the mercury atoms must first be excited. (i) What is meant by an excited atom? (1) (ii)
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ
 ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr Εναντιομερή λέγονται τα στερεοισομερή
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr Εναντιομερή λέγονται τα στερεοισομερή
Εισαγωγή στις βασικές έννοιες που αφορούν τις οργανομεταλλικές ενώσεις, την κατάλυση και τις βασικές αρχές της, καθώς και τη χρησιμότητα των
 124 Εισαγωγή στις βασικές έννοιες που αφορούν τις οργανομεταλλικές ενώσεις, την κατάλυση και τις βασικές αρχές της, καθώς και τη χρησιμότητα των καταλυτών των μετάλλων μεταπτώσεως στην οργανική σύνθεση.
124 Εισαγωγή στις βασικές έννοιες που αφορούν τις οργανομεταλλικές ενώσεις, την κατάλυση και τις βασικές αρχές της, καθώς και τη χρησιμότητα των καταλυτών των μετάλλων μεταπτώσεως στην οργανική σύνθεση.
the total number of electrons passing through the lamp.
 1. A 12 V 36 W lamp is lit to normal brightness using a 12 V car battery of negligible internal resistance. The lamp is switched on for one hour (3600 s). For the time of 1 hour, calculate (i) the energy
1. A 12 V 36 W lamp is lit to normal brightness using a 12 V car battery of negligible internal resistance. The lamp is switched on for one hour (3600 s). For the time of 1 hour, calculate (i) the energy
4.15 Αλογόνωση των αλκανίων RH + X 2 RX + HX
 4.15 Αλογόνωση των αλκανίων R + X 2 RX + X Ενεργειακό περιεχόμενο R + X 2 RX + X εκρηκτική για το F 2 εξώθερμη για το Cl 2 και το Br 2 ενδόθερμη για το I 2 4.16 Χλωρίωση του Μεθανίου Χλωρίωση του Μεθανίου
4.15 Αλογόνωση των αλκανίων R + X 2 RX + X Ενεργειακό περιεχόμενο R + X 2 RX + X εκρηκτική για το F 2 εξώθερμη για το Cl 2 και το Br 2 ενδόθερμη για το I 2 4.16 Χλωρίωση του Μεθανίου Χλωρίωση του Μεθανίου
Πολυμερισμός Προσθήκης
 Είδη Πολυμερισμού 1 Πολυμερισμός Προσθήκης Ελευθέρων Ριζών: Ενεργό Κέντρο ελεύθερη Ρίζα. Ανιοντικός Ενεργό Κέντρο Ανιόν - X + Κατιοντικός Ενεργό κέντρο κατιόν + Y - 2 Ιοντικοί Πολυμερισμοί Ανιοντικός Πολυμερισμός
Είδη Πολυμερισμού 1 Πολυμερισμός Προσθήκης Ελευθέρων Ριζών: Ενεργό Κέντρο ελεύθερη Ρίζα. Ανιοντικός Ενεργό Κέντρο Ανιόν - X + Κατιοντικός Ενεργό κέντρο κατιόν + Y - 2 Ιοντικοί Πολυμερισμοί Ανιοντικός Πολυμερισμός
6.1. Dirac Equation. Hamiltonian. Dirac Eq.
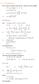 6.1. Dirac Equation Ref: M.Kaku, Quantum Field Theory, Oxford Univ Press (1993) η μν = η μν = diag(1, -1, -1, -1) p 0 = p 0 p = p i = -p i p μ p μ = p 0 p 0 + p i p i = E c 2 - p 2 = (m c) 2 H = c p 2
6.1. Dirac Equation Ref: M.Kaku, Quantum Field Theory, Oxford Univ Press (1993) η μν = η μν = diag(1, -1, -1, -1) p 0 = p 0 p = p i = -p i p μ p μ = p 0 p 0 + p i p i = E c 2 - p 2 = (m c) 2 H = c p 2
CHAPTER 25 SOLVING EQUATIONS BY ITERATIVE METHODS
 CHAPTER 5 SOLVING EQUATIONS BY ITERATIVE METHODS EXERCISE 104 Page 8 1. Find the positive root of the equation x + 3x 5 = 0, correct to 3 significant figures, using the method of bisection. Let f(x) =
CHAPTER 5 SOLVING EQUATIONS BY ITERATIVE METHODS EXERCISE 104 Page 8 1. Find the positive root of the equation x + 3x 5 = 0, correct to 3 significant figures, using the method of bisection. Let f(x) =
2 Composition. Invertible Mappings
 Arkansas Tech University MATH 4033: Elementary Modern Algebra Dr. Marcel B. Finan Composition. Invertible Mappings In this section we discuss two procedures for creating new mappings from old ones, namely,
Arkansas Tech University MATH 4033: Elementary Modern Algebra Dr. Marcel B. Finan Composition. Invertible Mappings In this section we discuss two procedures for creating new mappings from old ones, namely,
C.S. 430 Assignment 6, Sample Solutions
 C.S. 430 Assignment 6, Sample Solutions Paul Liu November 15, 2007 Note that these are sample solutions only; in many cases there were many acceptable answers. 1 Reynolds Problem 10.1 1.1 Normal-order
C.S. 430 Assignment 6, Sample Solutions Paul Liu November 15, 2007 Note that these are sample solutions only; in many cases there were many acceptable answers. 1 Reynolds Problem 10.1 1.1 Normal-order
Κεφάλαιο 4. Κατάταξη οργανικών αντιδράσεων
 Κεφάλαιο 4 Κατάταξη οργανικών αντιδράσεων Σύνοψη Στο κεφάλαιο αυτό εξετάζεται ο τρόπος πραγματοποίησης των αντιδράσεων και προσδιορίζονται οι παράγοντες που επηρεάζουν την πορεία τους, δηλαδή ο μηχανισμός
Κεφάλαιο 4 Κατάταξη οργανικών αντιδράσεων Σύνοψη Στο κεφάλαιο αυτό εξετάζεται ο τρόπος πραγματοποίησης των αντιδράσεων και προσδιορίζονται οι παράγοντες που επηρεάζουν την πορεία τους, δηλαδή ο μηχανισμός
Χημεία Γ ΓΕΛ 15 / 04 / 2018
 Γ ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α5 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Στην αντίδραση με χημική εξίσωση
Γ ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α5 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Στην αντίδραση με χημική εξίσωση
Finite Field Problems: Solutions
 Finite Field Problems: Solutions 1. Let f = x 2 +1 Z 11 [x] and let F = Z 11 [x]/(f), a field. Let Solution: F =11 2 = 121, so F = 121 1 = 120. The possible orders are the divisors of 120. Solution: The
Finite Field Problems: Solutions 1. Let f = x 2 +1 Z 11 [x] and let F = Z 11 [x]/(f), a field. Let Solution: F =11 2 = 121, so F = 121 1 = 120. The possible orders are the divisors of 120. Solution: The
Περαιτέρω αντιδράσεις των αλογονοαλκανίων
 Περαιτέρω αντιδράσεις των αλογονοαλκανίων Μονομοριακή υποκατάσταση και πορείες απόσπασης ΚΕΦΑΛΑΙΟ 7 1 Οι κλινικοί χημικοί χρησιμοποιούν πολλές αντιδράσεις για να διερευνήσουν τις σχέσεις δομής-δραστικότητας
Περαιτέρω αντιδράσεις των αλογονοαλκανίων Μονομοριακή υποκατάσταση και πορείες απόσπασης ΚΕΦΑΛΑΙΟ 7 1 Οι κλινικοί χημικοί χρησιμοποιούν πολλές αντιδράσεις για να διερευνήσουν τις σχέσεις δομής-δραστικότητας
CRASH COURSE IN PRECALCULUS
 CRASH COURSE IN PRECALCULUS Shiah-Sen Wang The graphs are prepared by Chien-Lun Lai Based on : Precalculus: Mathematics for Calculus by J. Stuwart, L. Redin & S. Watson, 6th edition, 01, Brooks/Cole Chapter
CRASH COURSE IN PRECALCULUS Shiah-Sen Wang The graphs are prepared by Chien-Lun Lai Based on : Precalculus: Mathematics for Calculus by J. Stuwart, L. Redin & S. Watson, 6th edition, 01, Brooks/Cole Chapter
Example Sheet 3 Solutions
 Example Sheet 3 Solutions. i Regular Sturm-Liouville. ii Singular Sturm-Liouville mixed boundary conditions. iii Not Sturm-Liouville ODE is not in Sturm-Liouville form. iv Regular Sturm-Liouville note
Example Sheet 3 Solutions. i Regular Sturm-Liouville. ii Singular Sturm-Liouville mixed boundary conditions. iii Not Sturm-Liouville ODE is not in Sturm-Liouville form. iv Regular Sturm-Liouville note
