CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC EDIŢIA a III-a
|
|
|
- Τέρις Διαμαντόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC EDIŢIA a III-a SUBIECTE PROPUSE Adrian Chiriac, Delia Isac, Otilia Bizerea, Horia Popovici, Daniela Dascălu, Titus Vlase, Dana Vlascici, Vlad Chiriac, Gabriela Vlase, Beatrice Vlad-Oros Universitatea de Vest din Timişoara, Facultatea de Chimie, Biologie, Geografie CLASA A VII-A 1. La ce operaţie de laborator se foloseşte instalaţia? Indicaţi denumirea tuturor componentelor sale. 2. Reprezentaţi structura nucleelor celor trei izotopi 12 6 C, 6 C, 6 C. Precizaţi importanţa deosebită a unuia dintre ei. 3. Să se coreleze coloanele privind amestecuri şi metode fizice de separare a substanţelor din acestea: 1. apă + alcool a. decantarea 2. apă + pulbere de sulf b. filtrarea 3. apă + sare de bucătărie c. distilarea 4. apă + nisip d. cristalizarea 4. I. Descrieţi modul de lucru, substanţele şi ustensilele folosite, observaţiile experimentale la realizarea a 200 grame de soluţie sare de bucătărie de concentraţie 10%. II. Cum puteţi dilua această soluţie la 5%? III. Calculaţi cantitatea de apă care trebuie îndepărtată prin încălzire din soluţia iniţială pentru ca să devină de concentraţie 15%. 5. Răspundeţi cu Adevărat /Fals şi justificaţi afirmaţiile: a. 140 grame Fier conţin 2,5 N A atomi b. 10 moli sulf conţin 6, atomi c. 120 grame Ca corespund la 2,5 moli Ca
2 6. Puneţi semnul F (Fizic) sau Ch (chimic) la cifra, care desemnează fenomenul: 1. arderea cărbunilor 6. topirea zăpezii 2. spargerea sticlei 7. fermentarea mustului 3. acrirea laptelui 8. râncezirea grăsimilor 4. ridicarea mercurului în termometru 9. fierberea apei 5. ruginirea fierului 10. coclirea aramei 7. Pe masa de laborator aveţi următorul amestec apă + zahăr +ulei + nisip şi ustensilele de lucru necesare. Care sunt mijloacele şi modalităţile de separare a componentelor sale pe baza proprietăţilor fizice? 8. Completaţi spaţiile libere: a. Soluţia este formată din...şi din... b. Dizolvarea substanţelor solide în lichide este influenţată de...şi de... c. Soluţia diluată conţine o cantitate mică de d. Oţetul este un amestec... e. Trecerea unei substanţe din starea..în starea...se numeşte topire. 9. Un aliaj conţine 75% nichel şi 25% Crom. Calculaţi numărul de moli de Ni care revin la un mol de Cr. (Mase atomice: Ni = 59, Cr = 52, Fe = 56, Ca = 40, S = 32). CLASA A VIII-A 1. Pentru a verifica proprietăţile unor substanţe anorganice se propun ecuaţiile reacţiilor chimice: (1) Cl 2 + H 2 O a + b (4) Cl 2 + e NaClO + NaCl + H 2 O (2) b a + c (5) N 2 + d f (3) Cl 2 + d a (6) O 3 O 2 + c Să se identifice substanţele a, b, c, d, e şi f aplicând legea conservării atomilor. 2. Praful de copt este: a) clorură de amoniu; d) sulfat de amoniu b) carbonat de amoniu e) sulfură de amoniu c) azotat de amoniu Cum explicaţi utilizarea lui în produsele alimentare? 3. Ecuaţia chimică NaOH + HCl NaCl + H 2 O, corespunde unei reacţii : a) de schimb d) exotermă b) endotermă e) rapidă c) lentă 4. În 200 grame soluţie NaOH 4,6% (procente de masă) se introduc 2,3 grame de sodiu. a) Ce masă de apă conţine soluţia rezultată după reacţie? b) Care este concentraţia procentuală a soluţiei? Mase atomice Na: 23, O: 16, H: Ecuaţia termochimică asociată procesului de fotosinteză este.. 6. Pornind de la malachit, prin reacţii succesive, prezentaţi două modalităţi de obţinere a cuprului.
3 7. Dintr-o marcă de oţel ce conţine 12% crom s-au confecţionat linguriţe cântărind 100 g. Câţi moli de crom sunt conţinuţi într-un set de 12 linguriţe din acest material? (masa atomică Cr: 52) 8. Propuneţi un experiment poluant din cauza reactanţilor, sau a produşilor de reacţie, urmând în prezentare etapele: mod de lucru, substanţe şi ustensile folosite, observaţii experimentale, ecuaţiile reacţiilor chimice, concluzii. 9. Se prepară 840 g soluţie AgNO 3 cu concentraţia 8,5% pentru a fi folosită astfel: în 40 g soluţie azotat de argint se introduce o plǎcuţǎ de cupru de 100 g şi se lasǎ timp îndelungat; restul soluţiei se trateazǎ cu 25 g amestec NaCl + KI. Sǎ se calculeze: a) masa plǎcuţei la sfârşitul reacţiei; b) compoziţia procentualǎ (% de masǎ) a amestecului de halogenuri. Mase atomice Ag: 108, N: 14, O: 16, K: 39, Na: 23, I: 127, Cl: 35,5, Cu: 64. CLASA A IX-A 1. Indicaţi A (adevărat) sau F (fals) pentru fiecare afirmaţie: a) Elementul chimic este un amestec de izotopi, în diferite proporţii; b) Un atom din grupa VII A, perioada a 2-a poate ceda un electron; c) În grupele secundare ale sistemului periodic sunt cuprinse atât metale cât şi nemetale; d) Configuraţia electronicǎ a Fe 3+ este [Ar]3d 5 ; e) Repartizarea electronilor în N 3 este [Ne]3s 2 3p Suflând printr-un tub de cauciuc într-o soluţie de Ca(OH) 2, se observă formarea unui precipitat. Dacă se suflă în continuare, după un timp se observă că precipitatul se dizolvă. a) Ce reacţii chimice au loc însoţite fiind de aceste observaţii experimentale? b) Stabiliţi tipul lor. c) Care este importanţa lor practică? 3. Propuneţi metode de obţinere a următoarelor combinaţii complexe: [Cu(NH 3 ) 4 ](OH) 2, Na[Al(OH) 4 ] şi Na 2 [Zn(OH) 4 ] ca activităţi experimentale urmând calea: mod de lucru, substanţe şi ustensile folosite, observaţii experimentale, ecuaţiile reacţiilor chimice, concluzii. 4. Un aliaj de cupru şi aluminiu conţine 87,7% cupru şi 12,3% aluminiu. Să se stabilească formula chimică a compusului intermetalic format. Se dau: A Cu = 63,5; A Al = Fie A, B, C, D elementele chimice cu numerele atomice Z A = 17; Z B = 18; Z C = 19; Z D = 20. a) Să se aşeze aceste elemente în ordinea creşterii energiilor (potenţialelor) de ionizare. b) Să se scrie formulele compuşilor acestor elemente cu hidrogenul respectiv oxigenul (la valenţă maximă) precizând tipurile de legătură chimică şi reţea cristalină ale acestora în stare solidǎ. 6. Ecuaţia chimică: H 2 SO 4 + 2KOH K 2 SO 4 + 2H 2 O Corespunde unei reacţii: a) de schimb; d) exotermă b) endotermă; e) rapidă
4 c) lentă; 7. Se dizolvă în apă 3,855 g amestec de KBr, NaCl şi BaCl 2. Soluţia obţinută se tratează cu soluţie proaspǎtǎ de AgNO 3, iar precipitatul format se separă şi se cântăreşte, găsindu-se că el are masa 6,185 g. Soluţia rămasă după separarea precipitatului este tratată cu soluţie de H 2 SO 4 în exces, obţinându-se un precipitat cu masa de 2,33 g. Să se calculeze compoziţia procentuală (% masă) a amestecului solid de KBr, NaCl şi BaCl 2 analizat.se dau: A Ag = 108; A K = 39; A Na = 23; A Ba = 137; A Cl = 35,5; A Br = 80; A S = 32; A O = 16; A N = Explicaţi, pe baza structurii substanţelor, următoarele proprietăţi fizicochimice constatate experimental: a) Solubilitatea: 1) Br 2 în CCl 4 ; 3) NaCl în apă 2) S 8 în CS 2 ; 4) HCl în apă b) Conductibilitatea electrică în topitură sau soluţie a substanţelor ionice; c) Punctul de topire mai mare al Al 2 O 3 (2000 o C) decât al NaCl (801 o C) g soluţie apoasă de clorură a unui metal divalent s-au împărţit în două părţi egale. În prima parte s-a introdus o lamelă de fier, în a doua una de cadmiu. Reacţiile care au loc sunt totale. Masa lamelei de fier a crescut cu 0,1 g, iar a celei de cadmiu a scăzut cu 0,6 g. a) Determinaţi formula chimicǎ a clorurii metalice; b) Stabiliţi concentraţia procentuală a soluţiei utilizate. = Se dau: A Fe 56; A Cd = 112; A Cl = 35,5. CLASA A XII-A I. Completează spaţiile libere astfel încât propoziţiile să aibă sens 1. Reacţiile chimice sunt.transformări ale substanţelor ce duc la substanţe.cu proprietăţi..de ale substanţelor iniţiale. 2. Reacţiile endoenergetice decurg cu..de căldură. 3. Căldura cedată sau primită într-o reacţie chimică este şi este determinată numai de starea şi cea..a sistemului, indiferent de calea urmată de reacţie. 4. Reacţiile în care entalpia reactanţilor este mai mare decât cea a produşilor sunt reacţii. II. Apreciază cu A (adevărat) şi cu F (fals) afirmaţiile următoare. Corectează afirmaţiile false 1. Într-o reacţie de forma aa + bb cc + dd căldura de reacţie se calculează astfel: H = (ah o A + bh o B) - (ch o C + dh o D) 2. O substanţă este cu atât mai instabilă cu cât căldura de formare a acelei substanţe este mai negativă. 3. Reacţia C (s) + O 2 (g) CO 2 (g) + 393,2 KJ este o reacţie endotermă. 4. Entalpiile de formare standard pentru Cl 2 (g), Br 2 (l), I 2 (s) sunt egale. III. Alege răspunsul corect: Căldura de formare din elemente a H 2 SO 4 (l) dacă se cunosc: S (s) + O 2 (g) SO 2 (g) H 1 SO 2 (g) + 1/2 O 2 (g) SO 3 (g) H 2 SO 3 (g) + H 2 O (l) H 2 SO 4 (l) H 3 H 2 (g) + 1/2 O 2 (g) H 2 O (l) H 4 se calculează conform relaţiei:
5 I. H = H 1 + H 2 + H 3 + H 4 II. H = H 1 - H 2 + H 3 - H 4 III. H = H 1 + H 2 - H 3 - H 4 IV. Care dintre următoarele afirmaţii este falsă: a) entalpia de reacţie nu depinde de drumul urmat de sistem între starea iniţială şi cea finală; b) entalpia de reacţie este aceeaşi, indiferent dacă reacţia se petrece într-o etapă sau în mai multe; c) entalpia unei reacţii globale rezultată prin însumarea algebrică a mai multor reacţii se obţine ca sumă algebrică a entalpiilor acestora; d) entalpia unui proces nu depinde de sensul procesului; e) entalpia unei reacţii chimice este egală cu suma algebrică a entalpiilor reactanţilor şi produşilor de reacţie amplificate cu numărul de moli din specia respectivă. V. Să se calculeze entalpia standard de formare a SO 3 (g) cunoscând entalpiile standard pentru următoarele procese: PbO (s) + S (s) + 1,5 O 2 (g) PbSO 4 (s) ΔH 0 1 = -693 kj/mol PbO (s) + H 2 SO 4 5H 2 O (l) PbSO 4 (s) + 6 H 2 O (l) ΔH 0 2 = -98 kj/mol SO 3 (g) + 6 H 2 O (l) H 2 SO 4 5H 2 O (l) ΔH 0 3 = -172 kj/mol VI. Într-o reacţie de ordinul unu, concentraţia reactantului se reduce la 50% după 10 minute. La cât se reduce concentraţia reactantului, în raport cu cea iniţială, după 20, respectiv 30 min. a) 33% şi 25%; b) 25% şi 10%; c) 2,5% şi 1,25%; d) 25% şi 12,5%; e) 25% şi 16,6%. VII. Stabiliţi coeficienţii stoechiometrici ai reacţiei redox şi calculaţi echivalentul gram al acidului azotic (μ - masa moleculară a acidului azotic): Cu + HNO 3 Cu(NO 3 ) 2 + NO + H 2 O VIII. Ce cantitate de CaO, de puritate 90%, se obţine prin calcinarea a 83,33 kg CaCO 3 de puritate 80% dacă randamentul procesului este de 75% ( se dau masele atomice A Ca = 40, A C = 12, A O = 16)? SOLUŢII ŞI BAREM DE CORECTARE CLASA A VII-A Se acordă 10 puncte pentru fiecare subiect 1. denumirea operaţiei denumirea corecta a tuturor componentelor 2. reprezentarea nucleelor precizarea importantei izotopului 6 C 3. R: 1c, 2b, 3d, 4a 4. I. Modul de lucru: Se cântăresc 20 g sare de bucătărie si se măsoară 180 ml = 180 g apă ( ρ = 1 g/ml). Acestea se introduc într-un pahar Erlenmayer şi se amestecă cu o baghetă de sticlă până la omogenizare. Substanţe: sare de bucătărie, apă. Ustensile balanţă, spatulă, cilindru gradat de cel puţin 200 ml, pahar Erlenmayer de 250 ml, baghetă de sticlă. II. Se calculează, se măsoară şi se adaugă la soluţia iniţială a g (ml) apă (200+a) g soluţie...20 g sare de bucătărie
6 100 g soluţie...5 g sare de bucătărie a = 200g = 200 ml apă III. Se calculează a g (ml) apă ce trebuie îndepărtată prin încălzire, din soluţia iniţială (200-a) g soluţie...20 g sare de bucătărie 100 g soluţie...15 g sare de bucătărie a = 66,66 g (ml) apă 5. a-a, b- F, c- F 6. 1-Ch, 2- F, 3- Ch, 4-F, 5 Ch, 6 F, 7 Ch, 8 Ch, 9 F, 10 Ch. 7. decantare, filtrare, separare, cristalizare 8. Completaţi spaţiile libere: a) Soluţia este formata din...dizolvant...şi din...dizolvat... b) Dizolvarea substanţelor solide în lichide este influenţată de: temperatură, agitarea componentelor şi de (suprafaţa de contact) grad de fărâmiţare. c) Soluţia diluată conţine o cantitate mică de dizolvat d) Oţetul este un amestec..omogen... e) Trecerea unei substanţe din starea solidă..în starea lichidă...se numeşte topire. /afirmaţie corectă 9. nr moli Ni = 75/59 = 1,27 moli nr moli Cr = 25/52 = 0,48 moli 1,27 moli Ni...0,48 moli Cr x...1 x = 2,65 moli CLASA A VIII-A 1. (1) Cl 2 + H 2 O HCl + HClO 2, (2) HClO HCl + [O] 1, (3) Cl 2 + H 2 2HCl 1, (4) Cl 2 + 2NaOH NaClO + NaCl + H 2 O 1, (5) N 2 + 3H 2 2NH 3 1, (6) O 3 O 2 + [O] 1, a = HCl, b = HClO, c = [O], d = H 2, e = NaOH, f = NH 3, [O] simbolistica oxigenului atomic. 2. b) 4 p t (NH 4 ) 2 CO 3 2NH 3 + CO 2 + H 2 O (v) 6 p La coacerea aluatului, în care s-a introdus praf de copt, se degajă un amestec gazos care-l creşte (afânează). 3. a), d), e) ; 4 p; 4 p g 2 18 g 2 40 g 2 g 2Na + 2HOH 2NaOH + H 2 2,3 g 1,8 g cons. 4 g 0,1 g a) soluţia iniţială: 9,2 g NaOH, 200 9,2 = 190,8 g H 2 O, mh 2 O sol finală = 190,8 1,8 = 189 g 3 p b) m sol finală = ,3 0,1 = 202,2 g
7 13,2 c % = 100 = 6,52% 202, p 6CO 2 + 6H 2 O clorofilă C 6 H 12 O 6 + 6O 2 - Q p 1 12 g Cr/linguriţă 12 linguriţe g/mol = 2,77 moli Cr Arderea sulfului SO 2 (poluant) Mod de lucru: O mică cantitate de sulf se arde într-o lingură de ars. Se introduce lingura într-un pahar Erlenmeyer, în care se găseşte puţină apă cu turnesol. 1, Substanţe: sulf, apă, turnesol şi ustensile: lingura de ars, bec de gaz sau spirtieră, pahar Erlenmeyer, spatulă. 1, Observaţii experimentale: Sulful (pucioasă) este solid, galben cu miros neplăcut. Arde cu flacără albastră iar, gazul obţinut are miros înecăcios. Apa cu turnesol se înroşeşte. Ecuaţiile reacţiilor chimice: S + O 2 SO 2 (1) (a) (b) SO 2 + H 2 O H 2 SO 3 (2) t o H 2 / C / CO CuO CuCO. Cu(OH)2 3 malachit H 2 SO 4 Fe CuSO 4 Concluzii: (1) Reacţie de combinare, metodă de obţinere a unui oxid de nemetal. (2) Reacţie reversibilă: (a) reacţie de combinare. (b) reacţie de descompunere. H 2 SO 3 cu caracter acid înroşeşte turnesolul. 9. a) 100 g soluţie... 8,5 g AgNO g soluţie. x = 71,40 g AgNO g soluţie... 8,5 g AgNO g soluţie... y = 3,4 g AgNO 3 Cu + 2AgNO 3 2Ag + Cu(NO 3 ) 2 x = 0,64 3,4 y = 2,16 m plǎcuţǎ la sfârşitul reacţiei = 100 0,64 + 2,16 = 101,52 g b) 100 g sol 8,5 g AgNO g. z = 68 g AgNO 3 a a NaCl + AgNO 3 AgCl + NaNO 3 b b KI + AgNO 3 AgI + KNO 3 t o Cu
8 a, b = moli 58,5 a b = a b = 68 moli NaI 2,49 g KI 22,51 %NaCl = % 25 2, 49 %KI = % 25 a = 0,385 moli NaCl 22,51 g NaCl, b = 0,015 CLASA A IX-A 1. a) A, b) F, c) F, d) A, e) F 5 x 2. a) Ca(OH) 2 + CO 2 CaCO 3 + H 2 O (1) 4 p CaCO 3 + CO 2 + H 2 O a b Ca(HCO 3 ) 2 (2) b) (1)- reacţie de schimb; (2a) - reacţie de combinare; (2b) - reacţie de descompunere 3 p c) Importanţa practică: (1) uscarea zugrăvelilor, întărirea mortarului; (2)formarea fenomenelor carstice. 3 p 3. Mod de lucru: În 3 eprubete (1), (2), (3) ce conţin soluţii de CuSO 4, AlCl 3 respectiv ZnCl 2 se adaugă în picături soluţie diluată de NaOH (sau NH 3 ), apoi exces soluţie NH 3 în (1) şi exces soluţie NaOH în (2) şi (3) Substanţe: soluţiile sărurilor de Cu, Al, Zn, soluţie NaOH, soluţie NH 3. Ustensile: eprubete în stativ, pipete. Observaţii experimentale: (1) iniţial precipitat albastru gelatinos, final soluţie albastru intens; (2) iniţial precipitat alb gelatinos, final soluţie incoloră; (3) iniţial precipitat alb gelatinos, final soluţie incoloră. Ecuaţiile reacţiilor chimice: (1) CuSO 4 + 2NaOH = Cu(OH) 2 + Na 2 SO 4 Sau: CuSO 4 + 2NH 3 + 2H 2 O = Cu(OH) 2 + (NH 4 ) 2 SO 4 Cu(OH) 2 + 4NH 3 = [Cu(NH 3 ) 4 ](OH) 2 (2) AlCl 3 + 3NaOH = Al(OH) 3 +3 NaCl Sau: AlCl 3 + 3NH 3 + 3H 2 O = Al(OH) 3 + 3NH 4 Cl Al(OH) 3 + NaOH = Na[Al(OH) 4 ] ZnCl 2 + 2NaOH = Zn(OH) 2 + 2NaCl Sau: ZnCl 2 + 2NH 3 + 2H 2 O = Zn(OH) 2 + 2NH 4 Cl Zn(OH) 2 + 2NaOH = Na 2 [Zn(OH) 4 ] Concluzii: În (1), (2) şi (3) au loc reacţii de precipitare şi reacţii de complexare, toate cu importanţă analitică ,7 = 1,38 atomi-gram Cu 63,5 12,3 = 0,455 atomi-gram Al 27 Formula chimică este Cu 3 Al
9 1,38 0,455 = 3 atomi Cu 0,455 = 1 atom Al 0, a) Cl, Ar, K, Ca C < D < A < B b) HCl legătură covalentă polară; reţea moleculară Ar nu formează compuşi cu hidrogenul sau oxigenul K + H - legătură ionică; reţea ionică Ca 2+ 2H - legătură ionică; reţea ionică Cl 2 O 7 legături covalente; reţea moleculară K 2 O legătură ionică; reţea ionică CaO legătură ionică; reţea ionică 6. a), d), e) ; 4 p; 4 p KBr + AgNO 3 = AgBr + KNO 3 0, x 4 reacţii = a x 58,5 143,5 NaCl + AgNO 3 = AgCl + NaNO 3 b y ,5 BaCl 2 + 2AgNO 3 = 2AgCl + Ba(NO 3 ) 2 c z 3,855 g amestec conţin: a g KBr + b g NaCl + c g BaCl 2 6,185 g precipitat conţin: x g AgBr + y g AgCl + z g AgCl a + b + c = 3,855 x + y + z = 6, Ba(NO 3 ) 2 + H 2 SO 4 = BaSO 4 + 2HNO 3 2,33 c = 2,08 g BaCl 2 în amestec z = 2,87 g AgCl rezultat în reacţia cu BaCl 2 a + b = 3,855 2,08 = 1,775 x + y = 6,185 2,87 = 3, a x = ,5b y = 58,5 Rezultă: b = 0,585 g NaCl; a = 1,19 g KBr 30,87% KBr; 15,17% NaCl; 53,96 % BaCl 2 Determinarea cantităţii de: BaCl 2 (inclusiv %) NaCl (%) 3 p KBr (%) 3 p
10 8. a) Solubilitatea substanţelor este favorizată sau defavorizată de structurile lor chimice şi ale solvenţilor cu care se pot confrunta. Cu cât structurile solvatului şi solventului sunt mai asemănătoare, substanţele se solubilizează mai uşor. Cl Br 2 şi S 8 cu legături covalente nepolare se solubilizează în Cl C Clşi S=C=S care sunt Cl solvenţi nepolari, întrucât simetria moleculelor a anulat polaritatea lor. Na + Cl - solvat ionic; H 2 O solvent puternic polar. Fizic: se rup legăturile ionice din sare. Chimic: solvatare (hidratare); legături ion-dipol. HCl moleculă polară. Fizic: apa deformează (gâtuie) molecula de HCl. Chimic: reacţia de ionizare: HCl + H 2 O H 3 O + + Cl - b) Cristalele ionice nu conduc curentul electric, deoarece ionii ocupă poziţii fixe în reţeaua cristalină, iar legătura ionică este puternică. În topitură sau soluţie, ionii devin mobili şi, sub acţiunea unei diferenţe de potenţial, se pot deplasa spre electrozi făcând posibilă trecerea curentului electric. 3 p c) Considerând formule brute energia necesară distrugerii atracţiei electrostatice dintre 2 ioni Al 3+ şi 3 ioni O 2- este mai mare decât cea necesară ruperii legăturilor între 1 ion Na + şi 1 ion Cl -. (Legea Coulomb: forţa de atracţie este proporţională cu produsul sarcinilor). 3 p 9. În fiecare porţiune de 100 g soluţie sunt m grame ioni de metal (Me 2+ ), care reacţionează cu x grame Fe, respectiv y grame Cd. A Me 56 Me 2+ + Fe = Me + Fe 2+ m x A Me 112 Me 2+ + Cd = Me + Cd 2+ m y m - x = 0,1 56m 112m A Me = = y = 2x y - m = 0,6 x y m - x = 0,1 2x - m = 0,6 x = 0,7 g Fe; m = 0,8 g Me A Me = 64, Me = Cu Formula este CuCl 2 masa CuCl 2 = 135 0, 8 = 1,6875 g 64 CuCl2 în 100 grame soluţie C % = 1,6875% 1,69% 6 p CLASA A XII-A I. 1. Reacţiile chimice sunt acele transformări ale substanţelor ce duc la substanţe noi cu proprietăţi diferite de ale substanţelor iniţiale. 2, 2. Reacţiile endoenergetice decurg cu absorbţie de căldură. 2,
11 3. Căldura cedată sau primită într-o reacţie chimică este entalpia de reacţie şi este determinată numai de starea iniţială şi cea finală a sistemului, indiferent de calea urmată de reacţie. 2, 4. Reacţiile în care entalpia reactanţilor este mai mare decât cea a produşilor sunt reacţii exoterme. 2, II. 1. F 2, 2. F 2, 3. F 2, 4. A (prin convenţie 0) 2, III. Corect I H = H 1 + H 2 + H 3 + H 4 IV. Corect d) 10 p V. H = H 1 H 2 H 3 = 693 ( 98) ( 172) = 423 kj/mol 10 p VI. Corect d) 7, C0 C0 C0 t1/ 2 = 10' ; t' 1/ 2 = 20' ; t'' 1/ 2 = 30' = 12,5% 8 7, VII. Corect c) 3Cu + 8HNO 3 3Cu(NO 3 ) 2 + 2NO + 4H 2 O VIII. CaCO 3 CaO + CO ,33 0,8 m ( CaO) t = p 83,33 0,8 m ( CaO) p = 56 0, p ,33 0,8 m( CaO) r = 56 0,75 = 31, 11 g BIBLIOGRAFIE SELECTIVĂ: 1. C. D. Neniţescu, Chimie Generală, Ed. Didactică şi Pedagogică Bucureşti 2. M.Iuşut, Probleme de chimie generală şi anorganică, Ed. Tehnică, Bucureşti, Veronica Chiriac, A. Chiriac, V. Chiriac, Teste de chimie generală şi anorganică, Ed. Mirton, Timişoara, F. Borcan, L. Pitulice, D. Dascălu, V. Chiriac, C. Bolcu, D. Isac, Algoritmizare, modelare, experiment chimic chimie anorganică, Ed. Eurostampa, Manuale şcolare în vigoare EVALUAREA CONCURSULUI Au participat elevi din judeţele Arad, Caraş Severin, Maramureş, Mehedinţi, Timiş cu următoarele rezultate: Clasa Concurenţi % elevi peste 70 puncte % elevi (50 70) puncte VII 66 37,88 43,94 VIII 23 26,08 17,39 IX 44 18,18 11,36 XII 7 28,57 71,43
12 LISTA PREMIANŢILOR Nr. Numele şi prenumele Premiul Clasa Şcoala Profesor crt. elevului obţinut 1. Cherciu V. Andrada Violeta C.N. Iulia Hasdeu Lugoj Ana Nichita I 2. Cerbu V. Gabriela C.N. Iulia Hasdeu Lugoj Ana Nichita II a VII a 3. Ciuban D. Ancuţa Corina C.N. Iulia Hasdeu Lugoj Ana Nichita III 4. Velcsov G. Maria C. N. C. Brediceanu Lugoj Vîlcu-Micu Maria Menţiune 5. Ţîrc Sorin Lic. Teor. "W. Shakespeare" Timişoara Petrean Diana I 6. Bran Diana C. N. "Moise Nicoară" Arad Avram Adela II a VIII a 7. Vasit Andrei Şcoala Generală Nr. 1 Arad Ienciu Monica III 8. Fer D. Bianca Şc cu clasele I-VIII Nr. 30 Timişoara Feidi Anuţa Menţiune 9. Cristescu G. Bianca Sporea-Iacob Lic. "Grigore Moisil" Timişoara Cristina Florina I 10. Soare Razvan Lic. Teor. "Traian Lalescu" Orşova Stoinel Mirela II Avram a IX a 11. Ţociu Laura C. N. "Moise Nicoară" Arad Adela/Crişan II Cristina 12. De Sabata Carla Sporea-Iacob Lic. "Grigore Moisil" Timişoara Antoanela Florina Menţiune 13. Sfârcoci Emanuel C. N. Bănăţean Timişoara Vert Silvia I 14. Szasz Francisc C. N. Bănăţean Timişoara Luchian Oltea I a XII a 15. Moza Bogdan C. N. Bănăţean Timişoara Luchian Oltea III 16. Laţcu Silviu C. N. Bănăţean Timişoara Vert Silvia Menţiune
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
5.1. Noţiuni introductive
 ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
II. 5. Probleme. 20 c 100 c = 10,52 % Câte grame sodă caustică se găsesc în 300 g soluţie de concentraţie 10%? Rezolvare m g.
 II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
a. 11 % b. 12 % c. 13 % d. 14 %
 1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare.
 Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
a. 0,1; 0,1; 0,1; b. 1, ; 5, ; 8, ; c. 4,87; 6,15; 8,04; d. 7; 7; 7; e. 9,74; 12,30;1 6,08.
 1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
Aplicaţii ale principiului I al termodinamicii la gazul ideal
 Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
ΦΡΟΝΤΙΣΤΗΡΙΟ Μ.Ε. ΣΥΜΒΟΛΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Capitolul 1-INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme
 Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu
 Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu Ediția a-5-a, 18 noiembrie 2017, Iași Clasa a XII-a, secțiunea a-2-a: Chimie Aplicată în Protecția Mediului Alegeţi răspunsul corect
Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu Ediția a-5-a, 18 noiembrie 2017, Iași Clasa a XII-a, secțiunea a-2-a: Chimie Aplicată în Protecția Mediului Alegeţi răspunsul corect
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate.
 Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Subiecte Clasa a VII-a
 lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
Metode iterative pentru probleme neliniare - contractii
 Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Planul determinat de normală şi un punct Ecuaţia generală Plane paralele Unghi diedru Planul determinat de 3 puncte necoliniare
 1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
(a) se numeşte derivata parţială a funcţiei f în raport cu variabila x i în punctul a.
 Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM 1 electronica.geniu.ro
 Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Probleme clasa a VII-a
 Probleme clasa a VII-a 1.Un cui de fier este supus unor transformări chimice prin; a) îndoire b) magnetizare c) rupere d) ruginire 2.Substanţele obţinute în urma vaporizăriii: a) îşi modifică compoziţia
Probleme clasa a VII-a 1.Un cui de fier este supus unor transformări chimice prin; a) îndoire b) magnetizare c) rupere d) ruginire 2.Substanţele obţinute în urma vaporizăriii: a) îşi modifică compoziţia
7.Separarea clorurii de sodiu (sare de bucătărie) dintr-un amestec se realizează prin: a. decantarea; b. filtrare;
 MINISTERUL EDUCAŢIEI, CERCETĂRII, TINERETULUI SI SPORTULUI INSPECTORATUL ŞCOLAR AL JUDEŢULUI SUCEAVA COLEGIUL NAŢIONAL EUDOXIU HURMUZACHI RĂDĂUŢI, Calea Bucovinei 5, Cod: 725400, Tel: 0230/561522, Fax:0230/
MINISTERUL EDUCAŢIEI, CERCETĂRII, TINERETULUI SI SPORTULUI INSPECTORATUL ŞCOLAR AL JUDEŢULUI SUCEAVA COLEGIUL NAŢIONAL EUDOXIU HURMUZACHI RĂDĂUŢI, Calea Bucovinei 5, Cod: 725400, Tel: 0230/561522, Fax:0230/
Unitatea atomică de masă (u.a.m.) = a 12-a parte din masa izotopului de carbon
 ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
Sisteme diferenţiale liniare de ordinul 1
 1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
ANALIZE FIZICO-CHIMICE MATRICE APA. Tip analiza Tip proba Metoda de analiza/document de referinta/acreditare
 ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
III. Serii absolut convergente. Serii semiconvergente. ii) semiconvergentă dacă este convergentă iar seria modulelor divergentă.
 III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
Curs 14 Funcţii implicite. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi"
 Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
Subiecte Clasa a VIII-a
 Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
R R, f ( x) = x 7x+ 6. Determinați distanța dintre punctele de. B=, unde x și y sunt numere reale.
 5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile
 Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Curs 1 Şiruri de numere reale
 Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
COLEGIUL NATIONAL CONSTANTIN CARABELLA TARGOVISTE. CONCURSUL JUDETEAN DE MATEMATICA CEZAR IVANESCU Editia a VI-a 26 februarie 2005.
 SUBIECTUL Editia a VI-a 6 februarie 005 CLASA a V-a Fie A = x N 005 x 007 si B = y N y 003 005 3 3 a) Specificati cel mai mic element al multimii A si cel mai mare element al multimii B. b)stabiliti care
SUBIECTUL Editia a VI-a 6 februarie 005 CLASA a V-a Fie A = x N 005 x 007 si B = y N y 003 005 3 3 a) Specificati cel mai mic element al multimii A si cel mai mare element al multimii B. b)stabiliti care
Asupra unei inegalităţi date la barajul OBMJ 2006
 Asupra unei inegalităţi date la barajul OBMJ 006 Mircea Lascu şi Cezar Lupu La cel de-al cincilea baraj de Juniori din data de 0 mai 006 a fost dată următoarea inegalitate: Fie x, y, z trei numere reale
Asupra unei inegalităţi date la barajul OBMJ 006 Mircea Lascu şi Cezar Lupu La cel de-al cincilea baraj de Juniori din data de 0 mai 006 a fost dată următoarea inegalitate: Fie x, y, z trei numere reale
Capitolul 4-COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ-
 Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Capitolul 2-HIDROCARBURI-2.3.-ALCHINE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
5. FUNCŢII IMPLICITE. EXTREME CONDIŢIONATE.
 5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE
 DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
5.5. REZOLVAREA CIRCUITELOR CU TRANZISTOARE BIPOLARE
 5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
Curs 4 Serii de numere reale
 Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Integrala nedefinită (primitive)
 nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
ŞTIINŢA ŞI INGINERIA. conf.dr.ing. Liana Balteş curs 7
 ŞTIINŢA ŞI INGINERIA MATERIALELOR conf.dr.ing. Liana Balteş baltes@unitbv.ro curs 7 DIAGRAMA Fe-Fe 3 C Utilizarea oţelului în rândul majorităţii aplicaţiilor a determinat studiul intens al sistemului metalic
ŞTIINŢA ŞI INGINERIA MATERIALELOR conf.dr.ing. Liana Balteş baltes@unitbv.ro curs 7 DIAGRAMA Fe-Fe 3 C Utilizarea oţelului în rândul majorităţii aplicaţiilor a determinat studiul intens al sistemului metalic
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC Clasa a VII-a
 FACULTATEA DE CHIMIE, BIOLOGIE, GEOGRAFIE Departamentul de Chimie Str. Petalozzi 6, Timişoara 3005, Tel/Fax: 056/5960 CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC 7.0.007 Claa a VII-a. Proprietăţi
FACULTATEA DE CHIMIE, BIOLOGIE, GEOGRAFIE Departamentul de Chimie Str. Petalozzi 6, Timişoara 3005, Tel/Fax: 056/5960 CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC 7.0.007 Claa a VII-a. Proprietăţi
MARCAREA REZISTOARELOR
 1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
CURSUL 3 ECHILIBRE DE DIZOLVARE
 CURSUL 3 ECHILIBRE DE DIZOLVARE Soluţii: ţ definiţie, ţ compoziţie, ţ exemple Soluţia mediu dispersant (solvent) fază dispersată (solut, solvit) Importanţa soluţiilor: olocul de desfăşurare a majorităţii
CURSUL 3 ECHILIBRE DE DIZOLVARE Soluţii: ţ definiţie, ţ compoziţie, ţ exemple Soluţia mediu dispersant (solvent) fază dispersată (solut, solvit) Importanţa soluţiilor: olocul de desfăşurare a majorităţii
OLIMPIADA NAȚIONALĂ DE CHIMIE
 MINISTERUL EDUCAȚIEI ȘI CERCETĂRII ȘTIINȚIFICE INSPECTORATUL ȘCOLAR JUDEȚEAN GALAȚI OLIMPIADA NAȚIONALĂ DE CHIMIE EDIȚIA a XLIX-a GALAȚI 5-10 APRILIE 2015 Proba teoretică Clasa a VIII-a Subiectul I (20
MINISTERUL EDUCAȚIEI ȘI CERCETĂRII ȘTIINȚIFICE INSPECTORATUL ȘCOLAR JUDEȚEAN GALAȚI OLIMPIADA NAȚIONALĂ DE CHIMIE EDIȚIA a XLIX-a GALAȚI 5-10 APRILIE 2015 Proba teoretică Clasa a VIII-a Subiectul I (20
Seminar 5 Analiza stabilității sistemelor liniare
 Seminar 5 Analiza stabilității sistemelor liniare Noțiuni teoretice Criteriul Hurwitz de analiză a stabilității sistemelor liniare În cazul sistemelor liniare, stabilitatea este o condiție de localizare
Seminar 5 Analiza stabilității sistemelor liniare Noțiuni teoretice Criteriul Hurwitz de analiză a stabilității sistemelor liniare În cazul sistemelor liniare, stabilitatea este o condiție de localizare
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014. ÄÉÁÍüÇÓÇ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
Metode de interpolare bazate pe diferenţe divizate
 Metode de interpolare bazate pe diferenţe divizate Radu Trîmbiţaş 4 octombrie 2005 1 Forma Newton a polinomului de interpolare Lagrange Algoritmul nostru se bazează pe forma Newton a polinomului de interpolare
Metode de interpolare bazate pe diferenţe divizate Radu Trîmbiţaş 4 octombrie 2005 1 Forma Newton a polinomului de interpolare Lagrange Algoritmul nostru se bazează pe forma Newton a polinomului de interpolare
REACŢII DE ADIŢIE NUCLEOFILĂ (AN-REACŢII) (ALDEHIDE ŞI CETONE)
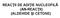 EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor X) functia f 1
 Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor
 Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
Laborator 11. Mulţimi Julia. Temă
 Laborator 11 Mulţimi Julia. Temă 1. Clasa JuliaGreen. Să considerăm clasa JuliaGreen dată de exemplu la curs pentru metoda locului final şi să schimbăm numărul de iteraţii nriter = 100 în nriter = 101.
Laborator 11 Mulţimi Julia. Temă 1. Clasa JuliaGreen. Să considerăm clasa JuliaGreen dată de exemplu la curs pentru metoda locului final şi să schimbăm numărul de iteraţii nriter = 100 în nriter = 101.
1. PROPRIETĂȚILE FLUIDELOR
 1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
Esalonul Redus pe Linii (ERL). Subspatii.
 Seminarul 1 Esalonul Redus pe Linii (ERL). Subspatii. 1.1 Breviar teoretic 1.1.1 Esalonul Redus pe Linii (ERL) Definitia 1. O matrice A L R mxn este in forma de Esalon Redus pe Linii (ERL), daca indeplineste
Seminarul 1 Esalonul Redus pe Linii (ERL). Subspatii. 1.1 Breviar teoretic 1.1.1 Esalonul Redus pe Linii (ERL) Definitia 1. O matrice A L R mxn este in forma de Esalon Redus pe Linii (ERL), daca indeplineste
Olimpiada Naţională de Matematică Etapa locală Clasa a IX-a M 1
 Calea 13 Septembrie, r 09, Sector 5, 0507, București Tel: +40 (0)1 317 36 50 Fax: +40 (0)1 317 36 54 Olimpiada Naţioală de Matematică Etapa locală -00016 Clasa a IX-a M 1 Fie 1 abc,,, 6 şi ab c 1 Să se
Calea 13 Septembrie, r 09, Sector 5, 0507, București Tel: +40 (0)1 317 36 50 Fax: +40 (0)1 317 36 54 Olimpiada Naţioală de Matematică Etapa locală -00016 Clasa a IX-a M 1 Fie 1 abc,,, 6 şi ab c 1 Să se
XHMEIA Α ΛΥΚΕΙΟΥ GI_A_CHIM_0_3499 ΜΑΡΑΓΚΟΥ ΝΙΚΗ
 ΜΑΘΗΜΑ: ΘΕΜΑΤΑ: XHMEIA Α ΛΥΚΕΙΟΥ GI_A_CHIM_0_3499 ΗΜΕΡΟΜΗΝΙΑ: 26/05/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΡΑΓΚΟΥ ΝΙΚΗ ΕΚΦΩΝΗΣΕΙΣ Θέµα 2ο 2.1 Α) Να υπολογιστεί ο αριθµός οξείδωσης του αζώτου στις παρακάτω χηµικές ενώσεις:
ΜΑΘΗΜΑ: ΘΕΜΑΤΑ: XHMEIA Α ΛΥΚΕΙΟΥ GI_A_CHIM_0_3499 ΗΜΕΡΟΜΗΝΙΑ: 26/05/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΡΑΓΚΟΥ ΝΙΚΗ ΕΚΦΩΝΗΣΕΙΣ Θέµα 2ο 2.1 Α) Να υπολογιστεί ο αριθµός οξείδωσης του αζώτου στις παρακάτω χηµικές ενώσεις:
Electronegativitatea = capacitatea unui atom legat de a atrage electronii comuni = concept introdus de Pauling.
 Cursul 8 3.5.4. Electronegativitatea Electronegativitatea = capacitatea unui atom legat de a atrage electronii comuni = concept introdus de Pauling. Cantitativ, ea se exprimă prin coeficienţii de electronegativitate
Cursul 8 3.5.4. Electronegativitatea Electronegativitatea = capacitatea unui atom legat de a atrage electronii comuni = concept introdus de Pauling. Cantitativ, ea se exprimă prin coeficienţii de electronegativitate
CLASIFICAREA REACŢIILOR CHIMICE
 CLASIFICAREA REACŢIILOR CHIMICE 1. Reacţii de combinare Reacţia de combinare este reacţia chimică ce are loc între două sau mai multe substanţe chimice, simple sau compuse, cu obţinerea unei singure substanţe
CLASIFICAREA REACŢIILOR CHIMICE 1. Reacţii de combinare Reacţia de combinare este reacţia chimică ce are loc între două sau mai multe substanţe chimice, simple sau compuse, cu obţinerea unei singure substanţe
Θέμα Α. Ονοματεπώνυμο: Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Componente şi Circuite Electronice Pasive. Laborator 3. Divizorul de tensiune. Divizorul de curent
 Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Ecuaţia generală Probleme de tangenţă Sfera prin 4 puncte necoplanare. Elipsoidul Hiperboloizi Paraboloizi Conul Cilindrul. 1 Sfera.
 pe ecuaţii generale 1 Sfera Ecuaţia generală Probleme de tangenţă 2 pe ecuaţii generale Sfera pe ecuaţii generale Ecuaţia generală Probleme de tangenţă Numim sferă locul geometric al punctelor din spaţiu
pe ecuaţii generale 1 Sfera Ecuaţia generală Probleme de tangenţă 2 pe ecuaţii generale Sfera pe ecuaţii generale Ecuaţia generală Probleme de tangenţă Numim sferă locul geometric al punctelor din spaţiu
Problema a II - a (10 puncte) Diferite circuite electrice
 Olimpiada de Fizică - Etapa pe judeţ 15 ianuarie 211 XI Problema a II - a (1 puncte) Diferite circuite electrice A. Un elev utilizează o sursă de tensiune (1), o cutie cu rezistenţe (2), un întrerupător
Olimpiada de Fizică - Etapa pe judeţ 15 ianuarie 211 XI Problema a II - a (1 puncte) Diferite circuite electrice A. Un elev utilizează o sursă de tensiune (1), o cutie cu rezistenţe (2), un întrerupător
3. Momentul forţei în raport cu un punct...1 Cuprins...1 Introducere Aspecte teoretice Aplicaţii rezolvate...4
 SEMINAR 3 MMENTUL FRŢEI ÎN RAPRT CU UN PUNCT CUPRINS 3. Momentul forţei în raport cu un punct...1 Cuprins...1 Introducere...1 3.1. Aspecte teoretice...2 3.2. Aplicaţii rezolvate...4 3. Momentul forţei
SEMINAR 3 MMENTUL FRŢEI ÎN RAPRT CU UN PUNCT CUPRINS 3. Momentul forţei în raport cu un punct...1 Cuprins...1 Introducere...1 3.1. Aspecte teoretice...2 3.2. Aplicaţii rezolvate...4 3. Momentul forţei
Reactia de amfoterizare a aluminiului
 Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ
 23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
2. Sisteme de forţe concurente...1 Cuprins...1 Introducere Aspecte teoretice Aplicaţii rezolvate...3
 SEMINAR 2 SISTEME DE FRŢE CNCURENTE CUPRINS 2. Sisteme de forţe concurente...1 Cuprins...1 Introducere...1 2.1. Aspecte teoretice...2 2.2. Aplicaţii rezolvate...3 2. Sisteme de forţe concurente În acest
SEMINAR 2 SISTEME DE FRŢE CNCURENTE CUPRINS 2. Sisteme de forţe concurente...1 Cuprins...1 Introducere...1 2.1. Aspecte teoretice...2 2.2. Aplicaţii rezolvate...3 2. Sisteme de forţe concurente În acest
3. Να συμπληρωθούν οι παρακάτω αντιδράσεις:
 1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
In cazul sistemelor G-L pentru care nu se aplica legile amintite ale echilibrului de faza, relatia y e = f(x) se determina numai experimental.
 ECHILIBRUL FAZELOR Este descris de: Legea repartitiei masice Legea fazelor Legea distributiei masice La echilibru, la temperatura constanta, raportul concentratiilor substantei dizolvate in doua faze aflate
ECHILIBRUL FAZELOR Este descris de: Legea repartitiei masice Legea fazelor Legea distributiei masice La echilibru, la temperatura constanta, raportul concentratiilor substantei dizolvate in doua faze aflate
1.7. AMPLIFICATOARE DE PUTERE ÎN CLASA A ŞI AB
 1.7. AMLFCATOARE DE UTERE ÎN CLASA A Ş AB 1.7.1 Amplificatoare în clasa A La amplificatoarele din clasa A, forma de undă a tensiunii de ieşire este aceeaşi ca a tensiunii de intrare, deci întreg semnalul
1.7. AMLFCATOARE DE UTERE ÎN CLASA A Ş AB 1.7.1 Amplificatoare în clasa A La amplificatoarele din clasa A, forma de undă a tensiunii de ieşire este aceeaşi ca a tensiunii de intrare, deci întreg semnalul
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ
 ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2015 Β ΦΑΣΗ Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
Seminariile Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reziduurilor
 Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
a n (ζ z 0 ) n. n=1 se numeste partea principala iar seria a n (z z 0 ) n se numeste partea
 Serii Laurent Definitie. Se numeste serie Laurent o serie de forma Seria n= (z z 0 ) n regulata (tayloriana) = (z z n= 0 ) + n se numeste partea principala iar seria se numeste partea Sa presupunem ca,
Serii Laurent Definitie. Se numeste serie Laurent o serie de forma Seria n= (z z 0 ) n regulata (tayloriana) = (z z n= 0 ) + n se numeste partea principala iar seria se numeste partea Sa presupunem ca,
Curs 2 DIODE. CIRCUITE DR
 Curs 2 OE. CRCUTE R E CUPRN tructură. imbol Relația curent-tensiune Regimuri de funcționare Punct static de funcționare Parametrii diodei Modelul cu cădere de tensiune constantă Analiza circuitelor cu
Curs 2 OE. CRCUTE R E CUPRN tructură. imbol Relația curent-tensiune Regimuri de funcționare Punct static de funcționare Parametrii diodei Modelul cu cădere de tensiune constantă Analiza circuitelor cu
CONCURSUL DE MATEMATICĂ APLICATĂ ADOLF HAIMOVICI, 2017 ETAPA LOCALĂ, HUNEDOARA Clasa a IX-a profil științe ale naturii, tehnologic, servicii
 Clasa a IX-a 1 x 1 a) Demonstrați inegalitatea 1, x (0, 1) x x b) Demonstrați că, dacă a 1, a,, a n (0, 1) astfel încât a 1 +a + +a n = 1, atunci: a +a 3 + +a n a1 +a 3 + +a n a1 +a + +a n 1 + + + < 1
Clasa a IX-a 1 x 1 a) Demonstrați inegalitatea 1, x (0, 1) x x b) Demonstrați că, dacă a 1, a,, a n (0, 1) astfel încât a 1 +a + +a n = 1, atunci: a +a 3 + +a n a1 +a 3 + +a n a1 +a + +a n 1 + + + < 1
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2019 Β ΦΑΣΗ
 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Δίνεται στοιχείο Χ το οποίο έχει οκτώ ηλεκτρόνια στην εξωτερική του στιβάδα.
ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Δίνεται στοιχείο Χ το οποίο έχει οκτώ ηλεκτρόνια στην εξωτερική του στιβάδα.
Profesor Blaga Mirela-Gabriela DREAPTA
 DREAPTA Fie punctele A ( xa, ya ), B ( xb, yb ), C ( xc, yc ) şi D ( xd, yd ) în planul xoy. 1)Distanţa AB = (x x ) + (y y ) Ex. Fie punctele A( 1, -3) şi B( -2, 5). Calculaţi distanţa AB. AB = ( 2 1)
DREAPTA Fie punctele A ( xa, ya ), B ( xb, yb ), C ( xc, yc ) şi D ( xd, yd ) în planul xoy. 1)Distanţa AB = (x x ) + (y y ) Ex. Fie punctele A( 1, -3) şi B( -2, 5). Calculaţi distanţa AB. AB = ( 2 1)
Toate subiectele sunt obligatorii. Timpul de lucru efectiv este de 3 ore. Se acordă din oficiu 10 puncte. SUBIECTUL I.
 Modelul 4 Se acordă din oficiu puncte.. Fie numărul complex z = i. Calculaţi (z ) 25. 2. Dacă x şi x 2 sunt rădăcinile ecuaţiei x 2 9x+8 =, atunci să se calculeze x2 +x2 2 x x 2. 3. Rezolvaţi în mulţimea
Modelul 4 Se acordă din oficiu puncte.. Fie numărul complex z = i. Calculaţi (z ) 25. 2. Dacă x şi x 2 sunt rădăcinile ecuaţiei x 2 9x+8 =, atunci să se calculeze x2 +x2 2 x x 2. 3. Rezolvaţi în mulţimea
Rezolvarea problemelor la chimie prin metoda algebrică
 Ministerul Educaţiei şi Tineretului al Republicii Moldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă Rezolvarea problemelor la chimie prin metoda algebrică Autor: Postolache Ion,
Ministerul Educaţiei şi Tineretului al Republicii Moldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă Rezolvarea problemelor la chimie prin metoda algebrică Autor: Postolache Ion,
Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II)
 Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II) Varianta 9 Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL
Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II) Varianta 9 Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL
Capitolul 2-HIDROCARBURI-2.5.-ARENE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.5.ARENE Exerciţii şi probleme E.P.2.5. 1. Denumeşte conform IUPAC următoarele hidrocarburi aromatice mononucleare: Determină formula generală a hidrocarburilor aromatice mononucleare
Capitolul 2 - HIDROCARBURI 2.5.ARENE Exerciţii şi probleme E.P.2.5. 1. Denumeşte conform IUPAC următoarele hidrocarburi aromatice mononucleare: Determină formula generală a hidrocarburilor aromatice mononucleare
LUCRĂRI PRACTICE DE CHIMIE GENERALĂ ŞI ANORGANICĂ LUCRĂRI PRACTICE DE CHIMIE GENERALĂ ŞI ANORGANICĂ ISBN
 Raluca Pop Mihaiela Andoni LUCRĂRI PRACTICE DE CHIMIE GENERALĂ ŞI ANORGANICĂ ISBN 978-606-8456-56-0 1 Editura Victor Babeş Piaţa Eftimie Murgu 2, cam. 316, 300041 Timişoara Tel./ Fax 0256 495 210 e-mail:
Raluca Pop Mihaiela Andoni LUCRĂRI PRACTICE DE CHIMIE GENERALĂ ŞI ANORGANICĂ ISBN 978-606-8456-56-0 1 Editura Victor Babeş Piaţa Eftimie Murgu 2, cam. 316, 300041 Timişoara Tel./ Fax 0256 495 210 e-mail:
riptografie şi Securitate
 riptografie şi Securitate - Prelegerea 12 - Scheme de criptare CCA sigure Adela Georgescu, Ruxandra F. Olimid Facultatea de Matematică şi Informatică Universitatea din Bucureşti Cuprins 1. Schemă de criptare
riptografie şi Securitate - Prelegerea 12 - Scheme de criptare CCA sigure Adela Georgescu, Ruxandra F. Olimid Facultatea de Matematică şi Informatică Universitatea din Bucureşti Cuprins 1. Schemă de criptare
ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ. β) Να βρεθεί σε ποια οµάδα και σε ποια περίοδο του Περιοδικού Πίνακα ανήκουν.
 ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ: 03490 ΗΜΕΡΟΜΗΝΙΑ: 27/5/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ ΕΚΦΩΝΗΣΕΙΣ Θέμα 2ο Α) Για τα στοιχεία: 12 Μg και 8 Ο α) Να κατανεµηθούν τα ηλεκτρόνιά τους σε στιβάδες. (µονάδες 2) β)
ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ: 03490 ΗΜΕΡΟΜΗΝΙΑ: 27/5/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ ΕΚΦΩΝΗΣΕΙΣ Θέμα 2ο Α) Για τα στοιχεία: 12 Μg και 8 Ο α) Να κατανεµηθούν τα ηλεκτρόνιά τους σε στιβάδες. (µονάδες 2) β)
Ονοματολογία ανόργανων χημικών ενώσεων Γραφή ανόργανων χημικών ενώσεων Οξέα, βάσεις, άλατα
 Ονοματολογία ανόργανων χημικών ενώσεων Γραφή ανόργανων χημικών ενώσεων Οξέα, βάσεις, άλατα Βοηθητικές Σημειώσεις Αγγελική Απ. Γαλάνη, Χημικός Ph.D. Εργαστηριακό Διδακτικό Προσωπικό, (Ε.ΔΙ.Π.) Χημείας Γραφή
Ονοματολογία ανόργανων χημικών ενώσεων Γραφή ανόργανων χημικών ενώσεων Οξέα, βάσεις, άλατα Βοηθητικές Σημειώσεις Αγγελική Απ. Γαλάνη, Χημικός Ph.D. Εργαστηριακό Διδακτικό Προσωπικό, (Ε.ΔΙ.Π.) Χημείας Γραφή
ΙΑΦΑ Φ ΝΕΙ Ε ΕΣ Ε ΧΗΜΕ Μ Ι Ε ΑΣ ΓΥΜΝ Μ ΑΣΙΟΥ H
 Hταξινόµηση των στοιχείων τάξη Γ γυµνασίου Αναγκαιότητα ταξινόµησης των στοιχείων Μέχρι το 1700 µ.χ. ο άνθρωπος είχε ανακαλύψει µόνο 15 στοιχείακαι το 1860 µ.χ. περίπου 60στοιχεία. Σηµαντικοί Χηµικοί της
Hταξινόµηση των στοιχείων τάξη Γ γυµνασίου Αναγκαιότητα ταξινόµησης των στοιχείων Μέχρι το 1700 µ.χ. ο άνθρωπος είχε ανακαλύψει µόνο 15 στοιχείακαι το 1860 µ.χ. περίπου 60στοιχεία. Σηµαντικοί Χηµικοί της
Valori limită privind SO2, NOx şi emisiile de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili
 Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
OLIMPIADA DE CHIMIE etapa judeţeană
 Clasa a VIII-a OLIMPIADA DE CHIMIE etapa judeţeană Str. General Berthelot nr. 28-30, Sector 1, Cod 010168, Bucureşti Tel: +40 (0)21 405 62 21 Fax: +40 (0)21 313 55 47 www.edu.ro DIRECȚIA GENERALĂ EDUCAȚIE
Clasa a VIII-a OLIMPIADA DE CHIMIE etapa judeţeană Str. General Berthelot nr. 28-30, Sector 1, Cod 010168, Bucureşti Tel: +40 (0)21 405 62 21 Fax: +40 (0)21 313 55 47 www.edu.ro DIRECȚIA GENERALĂ EDUCAȚIE
SERII NUMERICE. Definiţia 3.1. Fie (a n ) n n0 (n 0 IN) un şir de numere reale şi (s n ) n n0
 SERII NUMERICE Definiţia 3.1. Fie ( ) n n0 (n 0 IN) un şir de numere reale şi (s n ) n n0 şirul definit prin: s n0 = 0, s n0 +1 = 0 + 0 +1, s n0 +2 = 0 + 0 +1 + 0 +2,.......................................
SERII NUMERICE Definiţia 3.1. Fie ( ) n n0 (n 0 IN) un şir de numere reale şi (s n ) n n0 şirul definit prin: s n0 = 0, s n0 +1 = 0 + 0 +1, s n0 +2 = 0 + 0 +1 + 0 +2,.......................................
T R A I A N ( ) Trigonometrie. \ kπ; k. este periodică (perioada principală T * =π ), impară, nemărginită.
 Trignmetrie Funcţia sinus sin : [, ] este peridică (periada principală T * = ), impară, mărginită. Funcţia arcsinus arcsin : [, ], este impară, mărginită, bijectivă. Funcţia csinus cs : [, ] este peridică
Trignmetrie Funcţia sinus sin : [, ] este peridică (periada principală T * = ), impară, mărginită. Funcţia arcsinus arcsin : [, ], este impară, mărginită, bijectivă. Funcţia csinus cs : [, ] este peridică
VII.2. PROBLEME REZOLVATE
 Teoria Circuitelor Electrice Aplicaţii V PROBEME REOVATE R7 În circuitul din fiura 7R se cunosc: R e t 0 sint [V] C C t 0 sint [A] Se cer: a rezolvarea circuitului cu metoda teoremelor Kirchhoff; rezolvarea
Teoria Circuitelor Electrice Aplicaţii V PROBEME REOVATE R7 În circuitul din fiura 7R se cunosc: R e t 0 sint [V] C C t 0 sint [A] Se cer: a rezolvarea circuitului cu metoda teoremelor Kirchhoff; rezolvarea
Conice. Lect. dr. Constantin-Cosmin Todea. U.T. Cluj-Napoca
 Conice Lect. dr. Constantin-Cosmin Todea U.T. Cluj-Napoca Definiţie: Se numeşte curbă algebrică plană mulţimea punctelor din plan de ecuaţie implicită de forma (C) : F (x, y) = 0 în care funcţia F este
Conice Lect. dr. Constantin-Cosmin Todea U.T. Cluj-Napoca Definiţie: Se numeşte curbă algebrică plană mulţimea punctelor din plan de ecuaţie implicită de forma (C) : F (x, y) = 0 în care funcţia F este
Activitatea A5. Introducerea unor module specifice de pregătire a studenţilor în vederea asigurării de şanse egale
 POSDRU/156/1.2/G/138821 Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educaţiaşiformareaprofesionalăînsprijinulcreşteriieconomiceşidezvoltăriisocietăţiibazatepecunoaştere
POSDRU/156/1.2/G/138821 Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educaţiaşiformareaprofesionalăînsprijinulcreşteriieconomiceşidezvoltăriisocietăţiibazatepecunoaştere
Să se arate că n este număr par. Dan Nedeianu
 Primul test de selecție pentru juniori I. Să se determine numerele prime p, q, r cu proprietatea că 1 p + 1 q + 1 r 1. Fie ABCD un patrulater convex cu m( BCD) = 10, m( CBA) = 45, m( CBD) = 15 și m( CAB)
Primul test de selecție pentru juniori I. Să se determine numerele prime p, q, r cu proprietatea că 1 p + 1 q + 1 r 1. Fie ABCD un patrulater convex cu m( BCD) = 10, m( CBA) = 45, m( CBD) = 15 și m( CAB)
Liceul de Ştiinţe ale Naturii Grigore Antipa Botoşani
 Fişă de lucru RANDAMENT. CONVERSIE UTILĂ. CONVERSIE TOTALĂ 1. Randament A. Hidrocarburile alifatice pot fi utilizate drept combustibili, sau pot fi transformate în compuşi cu aplicaţii practice. 1. Scrieţi
Fişă de lucru RANDAMENT. CONVERSIE UTILĂ. CONVERSIE TOTALĂ 1. Randament A. Hidrocarburile alifatice pot fi utilizate drept combustibili, sau pot fi transformate în compuşi cu aplicaţii practice. 1. Scrieţi
ΟΝΟΜΑΣΙΑ F - HF Υδροφθόριο S 2- H 2 S Υδρόθειο Cl - HCl Υδροχλώριο OH - H 2 O Οξείδιο του Υδρογόνου (Νερό) NO 3 HNO 3. Νιτρικό οξύ SO 3 H 2 SO 3
 1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
Structura sistemului periodic... 9
 Cuprins Structura atomului Atomul. Particula. Molecula... 1 Modele atomice... 4 A.) Modelul lui J.J. Thomson... 4 B.) Modelul lui Rutherford sau modelul planetar al atomului... 4 C.) Modelul lui Bohr...
Cuprins Structura atomului Atomul. Particula. Molecula... 1 Modele atomice... 4 A.) Modelul lui J.J. Thomson... 4 B.) Modelul lui Rutherford sau modelul planetar al atomului... 4 C.) Modelul lui Bohr...
Ημερομηνία: Τρίτη 18 Απριλίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
Παραδοχές στις οποίες στις οποίες στηρίζεται ο αριθμός οξείδωσης
 Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
