Laboratorijske vaje iz fizikalne kemije. Navodila in predloge za pisanje poročil iz vaj. Interno gradivo
|
|
|
- Βαρθολομαίος Σπυρόπουλος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 Laboratorijske vaje iz fizikalne kemije Navodila in predloge za pisanje poročil iz vaj Interno gradivo
2 Navodila za izdelavo grafov s programom Excel 1. Označite stolpca (označeni stolpec na levi strani so vrednosti na osi x) in v orodni vrstici izberite primeren graf (največkrat razstreseni oz. ang. scatter) 2. Na delovnem listu se prikaže graf v surovi obliki, katerega je potrebno oblikovati do primerne končne oblike. Večina oblikovalskih zahtev je označenih na spodnjem primeru grafa. 1,20 1,18 1,16 Λ / S dm 2 mol -1 1,14 1,12 1,10 1,08 Točke in premica zavzemajo celotno površino na grafu. Razmerje dolžin osi je približno 1. Simboli za točke so primerne velikosti. Točkam je prilegana ustrezna regresijska krivulja (premica, eksponentna ali polinomska krivulja). 1,06 0,05 0,10 0,15 0,20 0,25 0,30 Obe osi sta označeni s primernima oznakama za količini, poleg sta dopisani pripadajoči enoti. c / mol 1/2 dm -3/2 Vse številke na posameznih oseh so podane na isto število decimalnih mest 3. Graf naj bo primerne velikosti (približno polovica strani A4) katerega natisnite in prilepite v poročilo s celotno hrbtno stranjo. 4. Če je graf neustrezen, ga popravite v programu in ponovno natisnite in prilepite.
3 Uporaba funkcije LINEST v programu EXCEL 1. V Excelovi mapi, ki vsebuje podatke, s pomočjo miške označite štiri celice (2 x 2). 2. Vtipkajte sledeči niz: =linest( 3. Pri tem se vam pod celico, v katero vpisujete tekst, samodejno prikaže celica s pomočjo, v kateri vidite, kakšna naj bi bila ustrezna oblika ukaza, ki ga vpisujete. Takoj za oklepajem je najprej potrebno podati vrednosti y. To naredite tako, da z miško označite celice s temi vrednostmi (lahko v stolpcu ali v vrstici). 4. Nato je potrebno vpisati ločilo, ki ločuje posamezne parametre ukazne vrstice (vejica ali podpičje, odvisno od različice programa). 5. Nato s pomočjo miške označite celice z vrednostmi x in zopet vtipkate ustrezno ločilo. 6. V nadaljevanju je potrebno v ukazno vrstico vpisati parameter [const], za katerega se vam v celici s pomočjo ponudita v izbiro logični vrednosti, in sicer TRUE (1) ali FALSE (0). Če napišete prvo, je modelna funkcija, ki jo prilegate točkam, enaka y = kx + n, v primeru FALSE pa y = kx. Največkrat boste imeli opravka s prvim primerom, zato vpišite TRUE ali številko 1. Vpišite še ustrezno ločilo. 7. Podati je potrebno še parameter [stats], za katerega imate zopet na izbiro vrednosti TRUE (1) ali FALSE (0). V prvem primeru vam funkcija LINEST vrne regresijsko statistiko (standardni odmik naklona in odseka premice), v nasprotnem pa ne. Ker leto za oceno napake potrebujete, vpišite TRUE oziroma številko Ko ste vpisali v polje vse potrebne parametre, vtipkajte zaklepaj in pritisnite kombinacijo tipk CTRL+SHIFT+ENTER. S to kombinacijo tipk se bo ukaz izvedel in v prvotno označenih 4 celicah se bodo pokazali rezultati: v zgornji vrstici se v prvi celici izpiše vrednost naklona (k) v drugi celici pa vrednost odseka (n), v spodnji vrstici pa pripadajoča standardna odmika (σ k in σ n ). Podrobnejša navodila za uporabo funkcije LINEST najdete na povezavi:
4 Kalorimetrija Ime in priimek: Turnus in skupina: Datum: 1. Naloga Z uporabo kalorimetra določi topilno entalpijo soli v vodi in ionizacijsko entalpijo za reakcijo med kislino in bazo. 2. Osnove Pri procesih, ki potekajo pri stalnem tlaku, je izmerjena reakcijska toplota Q enaka spremembi entalpije sistema H. Za določitev reakcijske toplote oz. entalpije največkrat uporabljamo kalorimeter. Reakcijske toplote ne merimo neposredno, ampak jo določimo posredno z merjenjem spremembe temperature, ki jo povzroči reakcija v toplotno dobro izoliranem kalorimetru. Toploto (- dq), ki se npr. sprosti pri reakciji, zapišemo kot dq =-Cd T = dh p S pri čemer smo z C S označili celotno toplotno kapaciteto kalorimetra z vsebino vred. Z integracijo zgornje enačbe dobimo H = Q =-C T p S Toplotno kapaciteto sistema določamo z električnim gretjem; v sistemu izmerimo dovedeno električno energijo in povišanje temperature. Množino električne energije Q e izračunamo iz enačbe Q = UIt= C T e S e Iz razmerja zadnjih dveh enačb dobimo spremembo entalpije H=-UIt T T e Integralna topilna entalpija t H pri molalni koncentraciji b je reakcijska toplota, ki jo izmerimo, če en mol soli raztopimo v toliko topila, da dobimo raztopino s koncentracijo b. Ker pri vaji ne poznamo molske mase soli, bomo topilno entalpijo izračunali na gram raztopljene soli Q t = p UIt T H =- m m T s s e Ionizacijska toplota vode ( i H) je količina toplote, ki se porabi pri razpadu enega mola molekul vode v vodikove (oksonijeve) in hidroksilne ione. V praksi določimo i H posredno tako, da v kalorimetru zmešamo raztopino močne kisline z raztopino močne baze ter izmerimo povišanje temperature. Nevtralizacijska entalpija ( n H), ki jo na tak način določimo, je enaka ionizacijski entalpiji vode z nasprotnim predznakom. = - UIt T nh ih= n Te kjer je n množina zreagirane kisline oz. baze.
5 3. Skica aparature 4. Meritve a) Pogoji v laboratoriju: p zun. = T = φ = b) topilna entalpija t / min t / s T / C t / min t / s T / C 0:00 0 6:00 (2) 360 0: : : : : : : : : : : : : : : : : : : : : : :00 (1) 180 9:00 (3) 540 3: : : : : : : : : : : : : : : : : : : : : : : opombe: (1) reakcija, (2) začetek gretja, (3) konec gretja U = t = I = m s =
6 c) ionizacijska entalpija t / min t / s T / C t / min t / s T / C 0:00 0 6:00 (2) 360 0: : : : : : : : : : : : : : : : : : : : : : :00 (1) 180 9:00 (3) 540 3: : : : : : : : : : : : : : : : : : : : : : : opombe: (1) reakcija, (2) začetek gretja, (3) konec gretja U = t = I = m s =
7 5. Računi in grafi - graf 1 : Odvisnost temperature v kalorimetru od časa (topilna entalpija) T = T e = - graf 2: Odvisnost temperature v kalorimetru od časa (ionizacijska entalpija) T = T e =
8 - Izračun topilne entalpije in koncentracije raztopine: th =- UIt T = m T s e γ m s r = = Vr - Izračun ionizacijske entalpije: nh= - UIt T = n T e H= H= i n 6. Ocena napake - topilna entalpija ( th) U I t ms ( T) ( Te) relativna napaka: = = H U I t m T T t s e absolutna napaka: ( th)= rn.. th= - ionizacijska entalpija ( ih) U I t ms ( T) ( Te) relativna napaka: = = H U I t m T T i s e absolutna napaka: ( ih)= rn.. ih= 7. Rezultati -topilna entalpija t H= ( ± ) kj g -1 = kj g -1 (1 ± ) -ionizacijska entalpija H =( ± ) kj i mol-1 = kj mol -1 (1 ± )
9 Parni tlak tekočin in izparilna entalpija Ime in priimek: Turnus in skupina: Datum: 1. Naloga Določi parni tlak tekočine pri različnih temperaturah in izračunaj molsko izparilno entalpijo. 2. Osnove Ravnotežni parni tlak je tlak pare tekočine v parni fazi, ko sta plinska faza in tekoča faza v termodinamskem ravnotežju. Pri segrevanju tekočine narašča tudi njen parni tlak, dokler ta ne postane enak zunanjemu tlaku. Tedaj tekočina zavre; temperatura vrelišča je tako odvisna od zunanjega tlaka. Če to odvisnost eksperimentalno določimo, dobimo odvisnost parnega tlaka od temperature. Zvezo med ravnotežnim parnim tlakom (p) in temperaturo (T) podaja zveza: d p = izph dt T V izp m m kjer je izp H m molska izparilna entalpije tekočine in izp V m. molski volumen pare. Ta je veliko večji od molskega volumna tekočine ( V g m >> V ), pri čemer lahko predpostavimo, da se para obnaša kot l m idealni plin. Obe predpostavki nas pripeljeta do Clausius-Clapeyronove enačbe: d ln p H = dt RT izp m 2 ki ima v integrirani obliki obliko (ob predpostavki, da je entalpija neodvisna od temperature): H 1 1 izp m lnp2 - ln p1= - - R T2 T1 S pomočjo te zveze bomo pri vaji določili izparilno entalpijo. Če narišemo diagram lnp v odvisnosti od 1/T, je naklon premice enak - izp H m /R. Parni tlak tekočine pri različnih temperaturah bomo določali s statično metodo pri kateri bomo uporabili izoteniskop. 3. Skica aparature
10 4. Meritve a) Pogoji v laboratoriju: p zun. = T = φ = b) T nastavljena / C T / C h levi / mm h desni / mm h / mm Računi in grafi T / K p parni / torr 1/T / 10-3 K -1 lnp parni
11 - graf 1 : Odvisnost parnega tlaka tekočine od temperature - graf 2: Odvisnost logaritma parnega tlaka od recipročne vrednosti temperature - Podatki pridobljeni s pomočjo funkcije LINEST v Excelu: k n σ k σ n
12 - Izračun izparilne entalpije: H = k R= izp m 6. Ocena napake absolutna napaka: ( izphm) = σ k R= relativna napaka: ( izphm) = H izp m 7. Rezultat izp H m = ( ± ) kj mol -1 = kj mol -1 (1 ± )
13 Določanje molske mase s krioskopsko metodo Ime in priimek: Turnus in skupina: Datum: 1. Naloga Iz znižanja zmrzišča raztopine določi molsko maso preiskovane snovi. 2. Osnove Če topilu dodamo topljenec, se pri dani temperaturi in tlaku zniža zmrzišče raztopine. Znižanje zmrzišča raztopine je povezano z njeno sestavo takole *2 z T = RT H tal 1 x 2 * kjer je T z zmrzišče čistega topila, talh1 talilna entalpija topila in x 2 molski delež topljenca v raztopini. Slednjega lahko pri nizkih koncentracijah izrazimo z molalnostjo b, kot x 2 = bm 1 in dobimo *2 RTz M1 T = b = Kk b H tal 1 kjer količino K k imenujemo krioskopska konstanta; njena vrednost je odvisna le od lastnosti topila. Iz zadnje enačbe in izraza b = m 2 /m 1 M 2, izpeljemo enačbo za izračun molske mase topljenca M 2 2 k M2 m 1 T = mk 3. Skica aparature
14 4. Meritve a) Pogoji v laboratoriju: p zun. = T = φ = b) m 2 = topilo raztopina T / C t / min t / s T / C t / min t / s 0,3 0,3 0,2 0,2 0,1 0,1 0,0 0,0-0,1-0,1-0,2-0,2-0,3-0,3-0,4-0,4-0,5-0,5-0,6-0,6-0,7-0,7-0,8-0,8-0,9-0,9-1,0-1,0
15 T / C t / min t / s T / C t / min t / s
16 5. Računi in grafi - graf: Ohlajevalna krivulja za topilo in raztopino - Izračun molske mase topljenca: T * z z = T = T = T T = * z z M mk mk m T V T 2 k 2 k 2= = = 1 ρ Ocena napake M2 m2 V1 ( T) relativna napaka: = + + = M m V T absolutna napaka: M2 = rn.. M2= 7. Rezultat M 2 = ( ± ) g mol -1 = g mol -1 (1 ± )
17 Galvanski členi - Napetost in notranja upornost galvanskega člena Ime in priimek: Turnus in skupina: Datum: - Merjenje ph 1. Naloga - Sestavi preprost galvanski člen in s kompenzacijsko metodo določi njegovo napetost in notranjo upornost - Danim vzorcem izmeri vrednosti ph s pomočjo kombinirane steklene elektrode 2. Osnove Galvanski člen je elektrokemijska celica, v kateri spontano poteka kemijska reakcija. Galvanski člen je sestavljen iz dveh elektrod, ki sta potopljeni v raztopini pripadajočih ionov in med seboj povezani z vodnikom. Raztopini povezuje elektrolitski ključ. V galvanskem členu poteka reakcija, za katero lahko pri danem tlaku in temperaturi izračunamo prosto entalpijo iz zveze G r G= zfe X. Napetost galvanskega člena lahko določimo s kompenzacijsko metodo, pri kateri uporabimo električno vezje, ki jo boste narisali v točki skica aparature (a). Bistvo metode je v tem, da damo merjeni napetosti nasproti znano in enako veliko nasprotno napetost. Tako lahko izračunamo napetost galvanskega člena E X kot E X = l X ES l S kjer so E S napetost standarda (etalon napetosti), l X in l S pa dolžini žice, potrebni za kompenzacijo napetosti galvanskega člena in standarda. Če vežemo k prvotnemu električnemu vezju še zunanji upor R Z in stikalo, potem lahko določimo še notranjo upornost galvanskega člena po zvezi R l X N = RZ lx ' 1 kjer je l X ' dolžina žice pri sklenjenem stikalu. Vrednost ph je definirana kot negativni desetiški logaritem aktivnosti ionov H + ( a + ), ki jo izrazimo H a = ( c / c ) γ, kjer sta c + in γ + koncentracija in koeficient aktivnosti ionov H +. V raztopinah o kot H H H H H vrednosti ph najpogosteje določamo z merjenjem napetosti galvanskega člena (E), v katerem smo kot indikatorsko elektroda uporabili stekleno elektrodo. Pri vaji bomo uporabljali kombinirano stekleno elektrodo, ki jo boste narisali v točki skica aparature (b). Pred meritvami instrument za merjenje ph (ph-meter) praviloma umerimo z ustreznimi standardnimi raztopinami (pufri), katerih vrednosti ph so znane. Enačba za izračun vrednosti ph ima obliko RT E = E' ln(10) ph F kjer je E' potencial, ki ustreza pravilni vrednosti ph.
18 3. Skica aparature a) b) 4. Meritve a) Pogoji v laboratoriju: p zun. = T = φ = b) Napetost in notranja upornost galvanskega člena 1. člen: I / ma l X / cm l ' X l S / cm E S = R Z = 2. člen: I / ma l X / cm l ' X l S / cm E S = R Z = c) Merjenje ph ph (vzorec 1) = ph (vzorec 2) =
19 5. Računi a) Napetost in notranja upornost galvanskega člena - Izračun napetosti galvanskega člena: lx 1. EX = ES = l lx 2. EX = ES = l S S - Izračun notranje upornosti galvanskega člena: l X 1. RN = RZ 1 = l X ' l X 2. RN = RZ 1 = l X ' - Tabela izračunov: 1. člen: I / ma E X / V R N / Ω E X R N - Izračun proste entalpije za reakcijo v členu: SKUPNA REAKCIJA V ČLENU: G G= zfe = r X 2. člen: I / ma E X / V R N / Ω E X R N
20 - Izračun proste entalpije za reakcijo v členu: SKUPNA REAKCIJA V ČLENU: G G= zfe = r X 6. Ocena napake a) Napetost in notranja upornost galvanskega člena -absolutna napaka 1. člen: 2. člen: GE X / V GR N / Ω GE X / V GR N / Ω G E = max E E = i X X X G E = max E E = i X X X G R = max R R = i N N N G R = max R R = i N N N GG ( G) = zfg E = r X GG ( G) = zfg E = r X -relativna napaka EX = E X R R N N r = GG ( rg) = G G EX = E X R R N N r = GG ( rg) = G G b) Merjenje ph GpH = 0,05
21 7. Rezultati a) Napetost in notranja upornost galvanskega člena E X = ( ± ) V = V (1 ± ) R N = ( ± ) Ω = Ω (1 ± ) G r G = ( ± ) kj mol -1 = kj mol -1 (1 ± ) b) Merjenje ph vzorec 1: ph = ± = (1 ± ) vzorec 2: ph = ± = (1 ± )
22 Viskoznost in površinska napetost tekočin Ime in priimek: Turnus in skupina: Datum: 1. Naloga a) S pomočjo Cannon-Fenskejevega viskozimetra določi viskoznost tekočin. b) Z manometrično in tenziometrično metodo določi površinsko napetost tekočin. 2. Osnove a) Viskoznost je merilo za medsebojno zaviranje gibajočih se plasti tekočine ali plinov. Če si predstavljamo tekočino med dvema vodoravnima ploščama z medsebojno razdaljo y, potem je sila F potrebna za premik zgornje plošče na tekočini, definirana kot v x F = η S y kjer je S površina plošče in v x hitrost premikanja plošče. Konstanta η je dinamična viskoznost tekočine, ki jo izražamo v Pa s oz. v stari enoti poise P ( P = 1 cp = 1 mpa s). Viskoznost s temperaturo pada, zato mora biti pri merjenju ta stalna. Metod za merjenje viskoznosti je precej, vendar jih je le nekaj pogosteje v rabi. Na vajah bomo spoznali pretok skozi kapilaro, kjer merimo pretočni čas tekočine (t) skozi kapilaro v izbranem viskozimetru. Zveza za izračun viskoznosti ima obliko π η= 8Vl 4 r gh ρt kjer je r polmer kapilare, g težnostni pospešek, h časovno povprečje višinske razlike med površino tekočine v zgornji in spodnji bučki, ρ gostota tekočine, V pa njen pretočen volumen. Da se izognemo težavam, povezanim z natančnim določevanjem količin v enačbi, viskozimeter običajno umerimo s tekočino z znano viskoznostjo η 0 in gostoto ρ 0. Tako dobimo ρ t η= η0 ρ 0t0 kjer sta t 0 in t pretočna časa za obe tekočini. Pogoj za veljavnost zadnje zveze je enak volumen tekočin. b) V tekočini delujejo med molekulami privlačne in odbojne sile. Globoko v notranjosti homogene tekočine delujejo na vsako molekulo sile v vseh smereh enako močno. Drugače pa je na površini tekočine, kjer rezultanta sil na molekule kaže v notranjost tekočine. Navzven se to kaže kot sila na površino tekočine, ki jo imenujemo tudi površinska napetost in jo označujemo z γ. Zaradi te je tlak tik pod površino tekočine različen od tlaka nad površino tekočine. Če ima površina kroglasto obliko je razlika tlakov enaka
23 2γ p= r kjer je r polmer krivinski polmer površine. Metod za določanje površinske napetosti je več, pri čemer bomo na vajah uporabljali manometrično in tenziometrično metodo. Pri manometrični metodi skozi stekleno kapilaro, ki je s spodnjim koncem potopljena v tekočino, sesamo v tekočino zrak in merimo podtlak, ki je potreben za nastanek zračnega mehurčka. Površinsko napetost tekočine, v katero je pomočena kapilara do globine l, izračunamo iz enačbe γ = 1 ( ρ ρ ) 0 2 gr h l kjer je g težnostni pospešek, r polmer kapilare, ρ 0 in ρ gostoti vode in tekočine in h razlika višin vodnih stolpcev na U-manometru, s katerim merimo podtlak. Pri tenziometričnem načinu merimo silo, ki je potrebna, da se kovinski obroček odtrga od površine tekočine, ki ji določamo površinsko napetost. Na tenziometru, s katerim bomo merili površinske napetosti, direktno odčitamo povšinsko napetost v enotah mn m -1. Točnost tenziometra preverimo z vodo, katere povšinsko napetost pri temperaturi merjenja izračunano po zvezi iz skript na strani Skica aparature a) Viskoznost tekočin b) Površinska napetost
24 4. Meritve a) Pogoji v laboratoriju: p zun. = T = φ = b) Viskoznost tekočin viskozimeter 1 viskozimeter 2 voda tekočina 1 voda tekočina 2 ρ 1 = ρ 2 = t t 0 / s t 1 / s t 0 / s t 2 / s ρ (20 C)= HO 2 c) Površinska napetost - manometrični način 1. meritev 2. meritev 3. meritev voda (ρ 0 = ) tekočina 1 (ρ = ) tekočina 2 (ρ = ) l 0 / cm h 0 / cm l / cm h / cm l / cm h / cm - tenziometrični način 1. meritev 2. meritev 3. meritev povprečje voda tekočina 1 tekočina 2 γ / mn m -1
25 5. Računi a) Viskoznost tekočin η ρ t = η0 = ρ 0 t0 η ρ t = η0 = ρ 0 t0 b) Površinska napetost - manometrični način γ 0(H20) = r 2γ gρ ( h l ) 0 = = γ = 1 ( ρ ρ ) = 0 2 gr h l - tabela izračunov Tekočina 1 Tekočina 2 r / mm γ / mn m -1 γ / mn m meritev 2. meritev 3. meritev povprečje r = γ = γ = 6. Ocena napake a) Viskoznost tekočin relativna napaka: η1 t0 t1 max t0 t0 max t1 t1 = + = + = η t t t t η2 t0 t2 max t0 t0 max t2 t2 = + = + = η t t t t absolutna napaka: η1 = rn..xη1 =
26 η = rn..xη = 2 2 b) Površinska napetost - manometrični način absolutna napaka: γ1= max γi γ = γ 1 relativna napaka: = γ γ = max γ γ = 1 2 i γ 2 = γ 2 - tenziometrični način absolutna napaka: γ1= max γi γ = γ 1 relativna napaka: = γ γ = max γ γ = 1 2 i γ 2 = γ 2 7. Rezultati a) Viskoznost tekočin η 1 = ( ± ) cp = cp (1 ± ) η 2 = ( ± ) cp = cp (1 ± ) b) Površinska napetost γ 1 = ( ± ) mn m -1 = mn m -1 (1 ± ) γ 2 = ( ± ) mn m -1 = mn m -1 (1 ± )
27 Adsorpcija Ime in priimek: Turnus in skupina: Datum: 1. Naloga Pri tej vaji bomo raziskali adsorpcijo ocetne kisline na aktivno oglje. 2. Osnove Če pride plin v stik s trdno snovjo, je v ravnotežju koncentracija plinskih molekul tik ob površini vedno večja kot v samem plinu. Ta pojav imenujemo adsorpcija. Snov, ki se adsorbira, imenujemo adsorbat, snov, na kateri se adsorbat se adsorbat adsorbira, pa adsorbent. Adsorpcija plina je spontan proces, zato se prosta entalpija sistema pri tem zmanjša (G ads G < 0). Ker se pri prehodu plina v adsorbirano plast zmanjša število njegovih prostostnih stopenj, pride tudi do znižanja entropije sistema (G ads S < 0). Iz enačbe G adsh=g adsg+ TG adss torej sledi, da mora biti adsorpcija vedno eksotermen pojav (G ads H < 0). Odvisnost množine adsorbiranega plina od tlaka pri konstantni temperaturi predstavimo z adsorpcijsko izotermo, ki jo pogosto zapišemo s Freundlichovo empirično zvezo x ap m = b kjer x/m pomeni množino adsorbiranega plina na enoto mase adsorbenta, a in b sta empirični konstanti, p pa je ravnotežni tlak plina. Za adsorpcijo komponent iz raztopin na površine trdnih adsorbentov veljajo enake splošne zakonitosti kot za adsorpcijo plinov. Zgornjo izotermo lahko tako zapišemo x ac m = b kjer je c ravnotežna koncentracija raztopine v mol/dm 3. Če enačbo logaritmiramo dobimo x/ m a c log log b log 3 mol/g = + mol/g mol/dm Če narišemo odvisnost log(x/m) od logc, dobimo premico z naklonom b, odsek na ordinatni osi pa je enak loga. 3. Skica aparature
28 4. Meritve a) Pogoji v laboratoriju: p zun. = T = φ = b) titracija razt. ocetne kisline (K) z NaOH približna c K / M m oglja / g V K / ml c NaOH / M 1. 0, , , , , ,4 5 0,01 0,1 PRED STRESANJEM 0 V NaOH / ml PO STRESANJU 1 V NaOH / ml 5. Računi in grafi c = ( c V )/ V = 0 0 NaOH NaOH K c= ( c V )/ V = 1 NaOH NaOH K x= ( c c) V = 0 V = 100 ml c 0 / M c / M x / mol x/m /mol g -1 log c log(x/m)
29 graf 1: Adsorpcijska izoterma: odvisnost x/m od c graf 2: Odvisnost log(x/m) od logc - Podatki pridobljeni s pomočjo funkcije LINEST v Excelu: k n k = b = n = loga a = 10 n = σ k σ n
30 6. Ocena napake absolutna napaka: a= ln(10) a σ = b= σ k = relativna napaka: a = a b = b n 7. Rezultat a = ( ± ) mol 1-b L b g -1 = mol 1-b L b g -1 (1 ± ) b = ± = (1 ± )
31 Kemijska kinetika Ime in priimek: Turnus in skupina: Datum: 1. Naloga Proučevali bomo hitrost hidrolize saharoze v glukozo in fruktozo. 2. Osnove Vsaka kemijska reakcija poteka z določeno, od narave snovi in razmer odvisno hitrostjo. Nanjo vplivajo koncentracija, tlak, temperatura, prisotnost katalizatorja in drugo. Reakcijska hitrost (v) je v splošnem odvisna od koncentracije reaktantov in produktov, za enosmerno reakcijo, pri kateri reagira ena sama snov, pa velja sledeča zveza dc v= = kc dt n kjer je c koncentracija reaktanta in k konstanta reakcijske hitrosti. n je red reakcije in je lahko celo število ali ulomek, redko pa je večje od 2. Če je red reakcije enak ena, pravimo, da je reakcija prvega reda, itd. Za reakcijo prvega reda dobimo po preureditvi zgornje enačbe in integraciji ln c 0 c = kt Hidroliza saharoze poteka po enačbi: H + C H O +HO CH O +CH O saharoza glukoza fruktoza Reakcijo katalizirajo ioni H+, zato jo lahko pospešimo z dodatkom kisline. Reakcijo lahko opišemo s hitrostnim zakonom za reakcije prvega reda. Saharoza, glukoza in fruktoza so optične aktivne snovi, kar pomeni da sukajo ravnino polarizacije linearno polarizirane svetlobe. V začetku, ko je v raztopini le saharoza, je raztopina desnosučna, raztopina zmesi glukoze in fruktoze, ki jo dobimo ob zaključku reakcije, pa je levosučna. Potek reakcije lahko zasledujemo tako, da s polarimetrom merimo kot zasuka ravnine linearno polarizirane svetlobe. Enačbo s pomočjo katere bomo določili navidezno konstanto reakcijske hitrosti ima obliko αz αk ln = k' t α α t k kjer sta α z in α k začetni in končni kot zasuka in α t kot zasuka ob času t. 3. Skica aparature
32 4. Meritve a) Pogoji v laboratoriju: p zun. = T = φ = b) 0,5 M HCl 1,0 M HCl c S / M t / min α t / t / min α t / 0,5 M HCl 1. 1,0 M HCl S...saharoza 5. Računi in grafi začetni kot zasuka: α [ αs] z = l cs= T končni kot zasuka: αk l [ αg] [ αf] T λ T ( λ λ) = + c = - tabela izračunov 0,5 M HCl 1,0 M HCl α k = α k = t / min α t -α k / ln(α t -α k ) t / min α t -α k / ln(α t -α k ) S
33 - graf 1: Odvisnost ln(α t - α k ) od časa t - Podatki pridobljeni s pomočjo funkcije LINEST v Excelu: 0,5 M HCl 1,0 M HCl k = k' k = k' σ k σ k
34 6. Ocena napake - absolutna napaka: 0,5 M HCl: k' = σ k = 1,0 M HCl: k' = σ k = - relativna napaka: 0,5 M HCl: 1,0 M HCl: k' = k' k' = k' 7. Rezultati 0,5 M HCl: k' = ( ± ) min -1 = min -1 (1 ± ) 1,0 M HCl: k' = ( ± ) min -1 = min -1 (1 ± )
35 Električna prevodnost raztopin elektrolitov Ime in priimek: Turnus in skupina: Datum: 1. Naloga Izmeri prevodnost močnega in šibkega elektrolita pri več koncentracijah ter obema določi molsko prevodnost pri neskončnem razredčenju Λ ter konstanti A za močen elektrolit in K c za šibek elektrolit. 2. Osnove Elektroliti so snovi, ki so v talini in/ali raztopini prisotni v obliki ionov in prevajajo električni tok. V grobem jih delimo na močne in šibke elektrolite. Močni elektroliti so v vodni raztopini praktično popolnoma disociirani, medtem ko pri šibkih disociacija ni popolna. Električno upornost raztopine R lahko izrazimo kot l R = ρ S kjer je ρ specifična prevodnost raztopine, razmerje l/s pa razmerje, ki ga določa geometrija celice s katero merimo prevodnost raztopine. To razmerje definiramo kot konstanto celice K cel z enoto cm -1. Le-to določamo z raztopino z znano specifično prevodnostjo, ki je običajno vodna raztopina KCl. Zgornjo zvezo lahko zapišemo tudi v recipročni obliki, v kateri definiramo specifično prevodnost κ (=1/ρ). Da lažje primerjamo prispevke različnih elektrolitov k prevodnosti, izražamo κ na enoto koncentracije. Tako definiramo molsko prevodnost Λ κ Λ= c Molska prevodnost močnih elektrolitov pri nizkih koncentracijah pada linearno s korenom koncentracije. To odvisnost imenujemo Kohlrauchev zakon in ima obliko Λ=Λ A c kjer je Λ molska prevodnost pri neskončnem razredčenju in A konstanta, značilna za izbrani elektrolit, topilo in temperaturo. Disociacijo enostavnega 1:1-elektrolita KA v raztopini zapišemo z ravnotežjem KA K + A K c + - (aq) (aq) (aq) za katero lahko zapišemo konstanto ravnotežja K c α c/ c = 1 α 2 O kjer je α stopnja disociacije šibkega elektrolita. Molsko prevodnost šibkega elektrolita lahko zapišemo kot Λ = α Λ. Iz zadnjih dveh enačb izpeljemo izraz za določitev Λ in K c c c 1 Λ 2 Λ = K ( ) O c Λ KcΛ
36 3. Skica aparature 4. Meritve a) Pogoji v laboratoriju: p zun. = T = φ = b) močni elektroliti šibki elektroliti K cel = K cel = c / mol L -1 κ r / ms cm -1 c / mol L -1 κ r / µs cm -1 0,08 0,002 0,04 0,001 0,02 0,0005 0,01 0, ,005 voda 5. Računi in grafi - Izračun molske prevodnosti elektrolita: κr κho 2 Λ= = c - Tabela izračunov za močne elektrolite: c / mol 1/2 dm -3/2 Λ / S dm 2 mol -1
37 - graf 1: Odvisnost molske prevodnosti močnega elektrolita od korena koncentracije raztopine - Podatki pridobljeni s pomočjo funkcije LINEST v Excelu: k n σ k σ n
38 - Tabela izračunov za šibke elektrolite: c / mol L -1 κr κho 2 Λ ( = )/ S dm 2 mol -1 1 c Λ / S-1 dm -2 mol 0,002 0,001 0,0005 0,00025 c Λ / S dm 2 mol -1 O c c - graf 2: Odvisnost Λ od 1 O c Λ za šibke elektrolite - Podatki pridobljeni s pomočjo funkcije LINEST v Excelu: k n σ k k Λ = = n 2 n Kc = = k σ n
39 6. Ocena napake močni elektroliti - absolutna napaka: Λ = σ = σ = A = σ = σ = A Λ k n - relativna napaka: Λ = Λ A = A šibki elektroliti - relativna napaka: σ n σ k Λ n k = + = Λ Kc σn σ = k 2 + = K n k c - absolutna napaka: Λ = r.n. x K c = r.n. x K c = Λ = 7. Rezultati - močni elektroliti Λ = ( ± ) S dm 2 mol -1 = S dm 2 mol -1 (1 ± ) A = ( ± ) S dm 7/2 mol -3/2 = S dm 7/2 mol -3/2 (1 ± ) - šibki elektroliti Λ = ( ± ) S dm 2 mol -1 = S dm 2 mol -1 (1 ± ) K c = ( ± ) = (1 ± )
Diferencialna enačba, v kateri nastopata neznana funkcija in njen odvod v prvi potenci
 Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 5. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 14. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
Tretja vaja iz matematike 1
 Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Funkcijske vrste. Matematika 2. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 2. april Gregor Dolinar Matematika 2
 Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 21. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):
![matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij): matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):](/thumbs/87/96579490.jpg) 4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 22. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
Mojca Slemnik POSKUSI V FIZIKALNI KEMIJI. zbrano gradivo, zbirka vaj
 Mojca Slemnik POSKUSI V FIZIKALNI KEMIJI zbrano gradivo, zbirka vaj Maribor, februar 2014 Mojca Slemnik, Poskusi v fizikalni kemiji Avtor: Vrsta publikacije: Založnik: Naklada: Dostopno: Doc. dr. Mojca
Mojca Slemnik POSKUSI V FIZIKALNI KEMIJI zbrano gradivo, zbirka vaj Maribor, februar 2014 Mojca Slemnik, Poskusi v fizikalni kemiji Avtor: Vrsta publikacije: Založnik: Naklada: Dostopno: Doc. dr. Mojca
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 10. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
Osnove elektrotehnike uvod
 Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
PONOVITEV SNOVI ZA 4. TEST
 PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 12. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 12. november 2013 Graf funkcije f : D R, D R, je množica Γ(f) = {(x,f(x)) : x D} R R, torej podmnožica ravnine R 2. Grafi funkcij,
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 12. november 2013 Graf funkcije f : D R, D R, je množica Γ(f) = {(x,f(x)) : x D} R R, torej podmnožica ravnine R 2. Grafi funkcij,
Simbolni zapis in množina snovi
 Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
Delovna točka in napajalna vezja bipolarnih tranzistorjev
 KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
Tabele termodinamskih lastnosti vode in vodne pare
 Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
Kontrolne karte uporabljamo za sprotno spremljanje kakovosti izdelka, ki ga izdelujemo v proizvodnem procesu.
 Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * FIZIKA NAVODILA ZA OCENJEVANJE. Petek, 10. junij 2016 SPLOŠNA MATURA
 Državni izpitni center *M16141113* SPOMLADANSKI IZPITNI ROK FIZIKA NAVODILA ZA OCENJEVANJE Petek, 1. junij 16 SPLOŠNA MATURA RIC 16 M161-411-3 M161-411-3 3 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor
Državni izpitni center *M16141113* SPOMLADANSKI IZPITNI ROK FIZIKA NAVODILA ZA OCENJEVANJE Petek, 1. junij 16 SPLOŠNA MATURA RIC 16 M161-411-3 M161-411-3 3 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor
1. Trikotniki hitrosti
 . Trikotniki hitrosti. Z radialno črpalko želimo črpati vodo pri pogojih okolice z nazivnim pretokom 0 m 3 /h. Notranji premer rotorja je 4 cm, zunanji premer 8 cm, širina rotorja pa je,5 cm. Frekvenca
. Trikotniki hitrosti. Z radialno črpalko želimo črpati vodo pri pogojih okolice z nazivnim pretokom 0 m 3 /h. Notranji premer rotorja je 4 cm, zunanji premer 8 cm, širina rotorja pa je,5 cm. Frekvenca
1. Definicijsko območje, zaloga vrednosti. 2. Naraščanje in padanje, ekstremi. 3. Ukrivljenost. 4. Trend na robu definicijskega območja
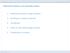 ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
Energije in okolje 1. vaja. Entalpija pri kemijskih reakcijah
 Entalpija pri kemijskih reakcijah Pri obravnavi energijskih pretvorb pri kemijskih reakcijah uvedemo pojem entalpije, ki popisuje spreminjanje energije sistema pri konstantnem tlaku. Sistemu lahko povečamo
Entalpija pri kemijskih reakcijah Pri obravnavi energijskih pretvorb pri kemijskih reakcijah uvedemo pojem entalpije, ki popisuje spreminjanje energije sistema pri konstantnem tlaku. Sistemu lahko povečamo
Termodinamika vlažnega zraka. stanja in spremembe
 Termodinamika vlažnega zraka stanja in spremembe Termodinamika vlažnega zraka Najpogostejši medij v sušilnih procesih konvektivnega sušenja je VLAŽEN ZRAK Obravnavamo ga kot dvokomponentno zmes Suhi zrak
Termodinamika vlažnega zraka stanja in spremembe Termodinamika vlažnega zraka Najpogostejši medij v sušilnih procesih konvektivnega sušenja je VLAŽEN ZRAK Obravnavamo ga kot dvokomponentno zmes Suhi zrak
Numerično reševanje. diferencialnih enačb II
 Numerčno reševanje dferencaln enačb I Dferencalne enačbe al ssteme dferencaln enačb rešujemo numerčno z več razlogov:. Ne znamo j rešt analtčno.. Posamezn del dferencalne enačbe podan tabelarčno. 3. Podatke
Numerčno reševanje dferencaln enačb I Dferencalne enačbe al ssteme dferencaln enačb rešujemo numerčno z več razlogov:. Ne znamo j rešt analtčno.. Posamezn del dferencalne enačbe podan tabelarčno. 3. Podatke
KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK
 1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
diferencialne enačbe - nadaljevanje
 12. vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 diferencialne enačbe - nadaljevanje Ortogonalne trajektorije Dana je 1-parametrična družina krivulj F(x, y, C) = 0. Ortogonalne
12. vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 diferencialne enačbe - nadaljevanje Ortogonalne trajektorije Dana je 1-parametrična družina krivulj F(x, y, C) = 0. Ortogonalne
Kotne in krožne funkcije
 Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
IZPIT IZ ANALIZE II Maribor,
 Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Splošno o interpolaciji
 Splošno o interpolaciji J.Kozak Numerične metode II (FM) 2011-2012 1 / 18 O funkciji f poznamo ali hočemo uporabiti le posamezne podatke, na primer vrednosti r i = f (x i ) v danih točkah x i Izberemo
Splošno o interpolaciji J.Kozak Numerične metode II (FM) 2011-2012 1 / 18 O funkciji f poznamo ali hočemo uporabiti le posamezne podatke, na primer vrednosti r i = f (x i ) v danih točkah x i Izberemo
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * NAVODILA ZA OCENJEVANJE. Petek, 12. junij 2015 SPLOŠNA MATURA
 Državni izpitni center *M543* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Petek,. junij 05 SPLOŠNA MATURA RIC 05 M543 M543 3 IZPITNA POLA Naloga Odgovor Naloga Odgovor Naloga Odgovor Naloga Odgovor
Državni izpitni center *M543* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Petek,. junij 05 SPLOŠNA MATURA RIC 05 M543 M543 3 IZPITNA POLA Naloga Odgovor Naloga Odgovor Naloga Odgovor Naloga Odgovor
Kotni funkciji sinus in kosinus
 Kotni funkciji sinus in kosinus Oznake: sinus kota x označujemo z oznako sin x, kosinus kota x označujemo z oznako cos x, DEFINICIJA V PRAVOKOTNEM TRIKOTNIKU: Kotna funkcija sinus je definirana kot razmerje
Kotni funkciji sinus in kosinus Oznake: sinus kota x označujemo z oznako sin x, kosinus kota x označujemo z oznako cos x, DEFINICIJA V PRAVOKOTNEM TRIKOTNIKU: Kotna funkcija sinus je definirana kot razmerje
Fazni diagram binarne tekočine
 Fazni diagram binarne tekočine Žiga Kos 5. junij 203 Binarno tekočino predstavljajo delci A in B. Ti se med seboj lahko mešajo v različnih razmerjih. V nalogi želimo izračunati fazni diagram take tekočine,
Fazni diagram binarne tekočine Žiga Kos 5. junij 203 Binarno tekočino predstavljajo delci A in B. Ti se med seboj lahko mešajo v različnih razmerjih. V nalogi želimo izračunati fazni diagram take tekočine,
*M * Osnovna in višja raven MATEMATIKA NAVODILA ZA OCENJEVANJE. Sobota, 4. junij 2011 SPOMLADANSKI IZPITNI ROK. Državni izpitni center
 Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
Vaje: Električni tokovi
 Barbara Rovšek, Bojan Golli, Ana Gostinčar Blagotinšek Vaje: Električni tokovi 1 Merjenje toka in napetosti Naloga: Izmerite tok, ki teče skozi žarnico, ter napetost na žarnici Za izvedbo vaje potrebujete
Barbara Rovšek, Bojan Golli, Ana Gostinčar Blagotinšek Vaje: Električni tokovi 1 Merjenje toka in napetosti Naloga: Izmerite tok, ki teče skozi žarnico, ter napetost na žarnici Za izvedbo vaje potrebujete
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 15. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 15. oktober 2013 Oglejmo si, kako množimo dve kompleksni števili, dani v polarni obliki. Naj bo z 1 = r 1 (cosϕ 1 +isinϕ 1 )
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 15. oktober 2013 Oglejmo si, kako množimo dve kompleksni števili, dani v polarni obliki. Naj bo z 1 = r 1 (cosϕ 1 +isinϕ 1 )
CO2 + H2O sladkor + O2
 VAJA 5 FOTOSINTEZA CO2 + H2O sladkor + O2 Meritve fotosinteze CO 2 + H 2 O sladkor + O 2 Fiziologija rastlin laboratorijske vaje SVETLOBNE REAKCIJE (tilakoidna membrana) TEMOTNE REAKCIJE (stroma kloroplasta)
VAJA 5 FOTOSINTEZA CO2 + H2O sladkor + O2 Meritve fotosinteze CO 2 + H 2 O sladkor + O 2 Fiziologija rastlin laboratorijske vaje SVETLOBNE REAKCIJE (tilakoidna membrana) TEMOTNE REAKCIJE (stroma kloroplasta)
SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK
 SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
NEPARAMETRIČNI TESTI. pregledovanje tabel hi-kvadrat test. as. dr. Nino RODE
 NEPARAMETRIČNI TESTI pregledovanje tabel hi-kvadrat test as. dr. Nino RODE Parametrični in neparametrični testi S pomočjo z-testa in t-testa preizkušamo domneve o parametrih na vzorcih izračunamo statistike,
NEPARAMETRIČNI TESTI pregledovanje tabel hi-kvadrat test as. dr. Nino RODE Parametrični in neparametrični testi S pomočjo z-testa in t-testa preizkušamo domneve o parametrih na vzorcih izračunamo statistike,
Enačba, v kateri poleg neznane funkcije neodvisnih spremenljivk ter konstant nastopajo tudi njeni odvodi, se imenuje diferencialna enačba.
 1. Osnovni pojmi Enačba, v kateri poleg neznane funkcije neodvisnih spremenljivk ter konstant nastopajo tudi njeni odvodi, se imenuje diferencialna enačba. Primer 1.1: Diferencialne enačbe so izrazi: y
1. Osnovni pojmi Enačba, v kateri poleg neznane funkcije neodvisnih spremenljivk ter konstant nastopajo tudi njeni odvodi, se imenuje diferencialna enačba. Primer 1.1: Diferencialne enačbe so izrazi: y
Integralni račun. Nedoločeni integral in integracijske metrode. 1. Izračunaj naslednje nedoločene integrale: (a) dx. (b) x 3 +3+x 2 dx, (c) (d)
 Integralni račun Nedoločeni integral in integracijske metrode. Izračunaj naslednje nedoločene integrale: d 3 +3+ 2 d, (f) (g) (h) (i) (j) (k) (l) + 3 4d, 3 +e +3d, 2 +4+4 d, 3 2 2 + 4 d, d, 6 2 +4 d, 2
Integralni račun Nedoločeni integral in integracijske metrode. Izračunaj naslednje nedoločene integrale: d 3 +3+ 2 d, (f) (g) (h) (i) (j) (k) (l) + 3 4d, 3 +e +3d, 2 +4+4 d, 3 2 2 + 4 d, d, 6 2 +4 d, 2
13. Jacobijeva metoda za računanje singularnega razcepa
 13. Jacobijeva metoda za računanje singularnega razcepa Bor Plestenjak NLA 25. maj 2010 Bor Plestenjak (NLA) 13. Jacobijeva metoda za računanje singularnega razcepa 25. maj 2010 1 / 12 Enostranska Jacobijeva
13. Jacobijeva metoda za računanje singularnega razcepa Bor Plestenjak NLA 25. maj 2010 Bor Plestenjak (NLA) 13. Jacobijeva metoda za računanje singularnega razcepa 25. maj 2010 1 / 12 Enostranska Jacobijeva
Booleova algebra. Izjave in Booleove spremenljivke
 Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
Matematika 2. Diferencialne enačbe drugega reda
 Matematika 2 Diferencialne enačbe drugega reda (1) Reši homogene diferencialne enačbe drugega reda s konstantnimi koeficienti: (a) y 6y + 8y = 0, (b) y 2y + y = 0, (c) y + y = 0, (d) y + 2y + 2y = 0. Rešitev:
Matematika 2 Diferencialne enačbe drugega reda (1) Reši homogene diferencialne enačbe drugega reda s konstantnimi koeficienti: (a) y 6y + 8y = 0, (b) y 2y + y = 0, (c) y + y = 0, (d) y + 2y + 2y = 0. Rešitev:
Na pregledni skici napišite/označite ustrezne točke in paraboli. A) 12 B) 8 C) 4 D) 4 E) 8 F) 12
 Predizpit, Proseminar A, 15.10.2015 1. Točki A(1, 2) in B(2, b) ležita na paraboli y = ax 2. Točka H leži na y osi in BH je pravokotna na y os. Točka C H leži na nosilki BH tako, da je HB = BC. Parabola
Predizpit, Proseminar A, 15.10.2015 1. Točki A(1, 2) in B(2, b) ležita na paraboli y = ax 2. Točka H leži na y osi in BH je pravokotna na y os. Točka C H leži na nosilki BH tako, da je HB = BC. Parabola
Tema 1 Osnove navadnih diferencialnih enačb (NDE)
 Matematične metode v fiziki II 2013/14 Tema 1 Osnove navadnih diferencialnih enačb (NDE Diferencialne enačbe v fiziki Večina osnovnih enačb v fiziki je zapisana v obliki diferencialne enačbe. Za primer
Matematične metode v fiziki II 2013/14 Tema 1 Osnove navadnih diferencialnih enačb (NDE Diferencialne enačbe v fiziki Večina osnovnih enačb v fiziki je zapisana v obliki diferencialne enačbe. Za primer
vezani ekstremi funkcij
 11. vaja iz Matematike 2 (UNI) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 ekstremi funkcij več spremenljivk nadaljevanje vezani ekstremi funkcij Dana je funkcija f(x, y). Zanimajo nas ekstremi nad
11. vaja iz Matematike 2 (UNI) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 ekstremi funkcij več spremenljivk nadaljevanje vezani ekstremi funkcij Dana je funkcija f(x, y). Zanimajo nas ekstremi nad
Funkcije več spremenljivk
 DODATEK C Funkcije več spremenljivk C.1. Osnovni pojmi Funkcija n spremenljivk je predpis: f : D f R, (x 1, x 2,..., x n ) u = f (x 1, x 2,..., x n ) kjer D f R n imenujemo definicijsko območje funkcije
DODATEK C Funkcije več spremenljivk C.1. Osnovni pojmi Funkcija n spremenljivk je predpis: f : D f R, (x 1, x 2,..., x n ) u = f (x 1, x 2,..., x n ) kjer D f R n imenujemo definicijsko območje funkcije
Ravnotežja v raztopini
 Ravnotežja v raztopini TOPILO: komponenta, ki jo je več v raztopini.v analizni kemiji uporabljamo organska in anorganska topila. Topila z veliko dielektrično konstanto (ε > 10) so polarna in ionizirajo
Ravnotežja v raztopini TOPILO: komponenta, ki jo je več v raztopini.v analizni kemiji uporabljamo organska in anorganska topila. Topila z veliko dielektrično konstanto (ε > 10) so polarna in ionizirajo
Dinamika kapilarnega pomika
 UNIVERZA V LJUBLJANI FAKULTETA ZA MATEMATIKO IN FIZIKO ODDELEK ZA FIZIKO Goran Bezjak SEMINARSKA NALOGA Dinamika kapilarnega pomika Mentor: izr. prof. dr. Gorazd Planinšič Ljubljana, december 2007 1 Povzetek
UNIVERZA V LJUBLJANI FAKULTETA ZA MATEMATIKO IN FIZIKO ODDELEK ZA FIZIKO Goran Bezjak SEMINARSKA NALOGA Dinamika kapilarnega pomika Mentor: izr. prof. dr. Gorazd Planinšič Ljubljana, december 2007 1 Povzetek
2.1. MOLEKULARNA ABSORPCIJSKA SPEKTROMETRIJA
 2.1. MOLEKULARNA ABSORPCJSKA SPEKTROMETRJA Molekularna absorpcijska spektrometrija (kolorimetrija, fotometrija, spektrofotometrija) temelji na merjenju absorpcije svetlobe, ki prehaja skozi preiskovano
2.1. MOLEKULARNA ABSORPCJSKA SPEKTROMETRJA Molekularna absorpcijska spektrometrija (kolorimetrija, fotometrija, spektrofotometrija) temelji na merjenju absorpcije svetlobe, ki prehaja skozi preiskovano
Gimnazija Krˇsko. vektorji - naloge
 Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
Univerza v Novi Gorici Fakulteta za znanosti o okolju Okolje (I. stopnja) Meteorologija 2013/2014. Energijska bilanca pregled
 Univerza v Novi Gorici Fakulteta za znanosti o okolu Okole (I. stopna) Meteorologia 013/014 Energiska bilanca pregled 1 Osnovni pomi energiski tok: P [W = J/s] gostota energiskega toka: [W/m ] toplota:q
Univerza v Novi Gorici Fakulteta za znanosti o okolu Okole (I. stopna) Meteorologia 013/014 Energiska bilanca pregled 1 Osnovni pomi energiski tok: P [W = J/s] gostota energiskega toka: [W/m ] toplota:q
KISLINE IN BAZE ARRHENIUSOVA DEFINICIJA KISLIN IN BAZ
 6. KISLINE IN BAZE KISLINE IN BAZE ARRHENIUSOVA DEFINICIJA KISLIN IN BAZ kisline so snovi, ki v vodni raztopini disocirajo vodikove ione (H + ), baze pa snovi, ki v vodni raztopini disocirajo hidroksidne
6. KISLINE IN BAZE KISLINE IN BAZE ARRHENIUSOVA DEFINICIJA KISLIN IN BAZ kisline so snovi, ki v vodni raztopini disocirajo vodikove ione (H + ), baze pa snovi, ki v vodni raztopini disocirajo hidroksidne
Podobnost matrik. Matematika II (FKKT Kemijsko inženirstvo) Diagonalizacija matrik
 Podobnost matrik Matematika II (FKKT Kemijsko inženirstvo) Matjaž Željko FKKT Kemijsko inženirstvo 14 teden (Zadnja sprememba: 23 maj 213) Matrika A R n n je podobna matriki B R n n, če obstaja obrnljiva
Podobnost matrik Matematika II (FKKT Kemijsko inženirstvo) Matjaž Željko FKKT Kemijsko inženirstvo 14 teden (Zadnja sprememba: 23 maj 213) Matrika A R n n je podobna matriki B R n n, če obstaja obrnljiva
V tem poglavju bomo vpeljali pojem determinante matrike, spoznali bomo njene lastnosti in nekaj metod za računanje determinant.
 Poglavje IV Determinanta matrike V tem poglavju bomo vpeljali pojem determinante matrike, spoznali bomo njene lastnosti in nekaj metod za računanje determinant 1 Definicija Preden definiramo determinanto,
Poglavje IV Determinanta matrike V tem poglavju bomo vpeljali pojem determinante matrike, spoznali bomo njene lastnosti in nekaj metod za računanje determinant 1 Definicija Preden definiramo determinanto,
Iterativno reševanje sistemov linearnih enačb. Numerične metode, sistemi linearnih enačb. Numerične metode FE, 2. december 2013
 Numerične metode, sistemi linearnih enačb B. Jurčič Zlobec Numerične metode FE, 2. december 2013 1 Vsebina 1 z n neznankami. a i1 x 1 + a i2 x 2 + + a in = b i i = 1,..., n V matrični obliki zapišemo:
Numerične metode, sistemi linearnih enačb B. Jurčič Zlobec Numerične metode FE, 2. december 2013 1 Vsebina 1 z n neznankami. a i1 x 1 + a i2 x 2 + + a in = b i i = 1,..., n V matrični obliki zapišemo:
Eliminacijski zadatak iz Matematike 1 za kemičare
 Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Matematika. Funkcije in enačbe
 Matematika Funkcije in enačbe (1) Nariši grafe naslednjih funkcij: (a) f() = 1, (b) f() = 3, (c) f() = 3. Rešitev: (a) Linearna funkcija f() = 1 ima začetno vrednost f(0) = 1 in ničlo = 1/. Definirana
Matematika Funkcije in enačbe (1) Nariši grafe naslednjih funkcij: (a) f() = 1, (b) f() = 3, (c) f() = 3. Rešitev: (a) Linearna funkcija f() = 1 ima začetno vrednost f(0) = 1 in ničlo = 1/. Definirana
Poglavje 7. Poglavje 7. Poglavje 7. Regulacijski sistemi. Regulacijski sistemi. Slika 7. 1: Normirana blokovna shema regulacije EM
 Slika 7. 1: Normirana blokovna shema regulacije EM Fakulteta za elektrotehniko 1 Slika 7. 2: Principielna shema regulacije AM v KSP Fakulteta za elektrotehniko 2 Slika 7. 3: Merjenje komponent fluksa s
Slika 7. 1: Normirana blokovna shema regulacije EM Fakulteta za elektrotehniko 1 Slika 7. 2: Principielna shema regulacije AM v KSP Fakulteta za elektrotehniko 2 Slika 7. 3: Merjenje komponent fluksa s
SEMINAR IZ KOLEGIJA ANALITIČKA KEMIJA I. Studij Primijenjena kemija
 SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
13. poglavje: Energija
 13. poglavje: Energija 1. (Naloga 3) Koliko kilovatna je peč za hišno centralno kurjavo, ki daje 126 MJ toplote na uro? Podatki: Q = 126 MJ, t = 3600 s; P =? Če peč z močjo P enakomerno oddaja toploto,
13. poglavje: Energija 1. (Naloga 3) Koliko kilovatna je peč za hišno centralno kurjavo, ki daje 126 MJ toplote na uro? Podatki: Q = 126 MJ, t = 3600 s; P =? Če peč z močjo P enakomerno oddaja toploto,
Raztopine. Raztopine. Elektroliti. Elektrolit je substanca, ki pri raztapljanju (v vodi) daje ione. A a B b aa b+ + bb a-
 Raztopine Mnoge analizne metode temeljijo na opazovanju ravnotežnih sistemov, ki se vzpostavijo v raztopinah. Najpogosteje uporabljeno topilo je voda! RAZTOPINE: topljenec topilo (voda) (Enote za koncentracije!)
Raztopine Mnoge analizne metode temeljijo na opazovanju ravnotežnih sistemov, ki se vzpostavijo v raztopinah. Najpogosteje uporabljeno topilo je voda! RAZTOPINE: topljenec topilo (voda) (Enote za koncentracije!)
MATEMATIČNI IZRAZI V MAFIRA WIKIJU
 I FAKULTETA ZA MATEMATIKO IN FIZIKO Jadranska cesta 19 1000 Ljubljan Ljubljana, 25. marec 2011 MATEMATIČNI IZRAZI V MAFIRA WIKIJU KOMUNICIRANJE V MATEMATIKI Darja Celcer II KAZALO: 1 VSTAVLJANJE MATEMATIČNIH
I FAKULTETA ZA MATEMATIKO IN FIZIKO Jadranska cesta 19 1000 Ljubljan Ljubljana, 25. marec 2011 MATEMATIČNI IZRAZI V MAFIRA WIKIJU KOMUNICIRANJE V MATEMATIKI Darja Celcer II KAZALO: 1 VSTAVLJANJE MATEMATIČNIH
Kovinske indikatorske elektrode. Inertne elektrode. Membranske indikatorske elektrode
 Indikatorske elektrode Indikatorske elektrode Kovinske indikatorske elektrode Inertne elektrode Membranske indikatorske elektrode Elektroda 1. reda je kovinska elektroda (Ag, Cu, Hg, Cd, Pb), ki je v stiku
Indikatorske elektrode Indikatorske elektrode Kovinske indikatorske elektrode Inertne elektrode Membranske indikatorske elektrode Elektroda 1. reda je kovinska elektroda (Ag, Cu, Hg, Cd, Pb), ki je v stiku
Stehiometrija za študente veterine
 Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
[ ]... je oznaka za koncentracijo
![[ ]... je oznaka za koncentracijo [ ]... je oznaka za koncentracijo](/thumbs/62/48148191.jpg) 9. Vaja: Elektrolitska disociacija a) Osnove: Elektroliti so snovi, ki prevajajo električni tok; to so raztopine kislin, baz in soli. Elektrolitska disociacija je razpad elektrolita na ione. Stopnja elektrolitske
9. Vaja: Elektrolitska disociacija a) Osnove: Elektroliti so snovi, ki prevajajo električni tok; to so raztopine kislin, baz in soli. Elektrolitska disociacija je razpad elektrolita na ione. Stopnja elektrolitske
Tokovi v naravoslovju za 6. razred
 Tokovi v naravoslovju za 6. razred Bojan Golli in Nada Razpet PeF Ljubljana 7. december 2007 Kazalo 1 Fizikalne osnove 2 1.1 Energija in informacija............................... 3 2 Projekti iz fizike
Tokovi v naravoslovju za 6. razred Bojan Golli in Nada Razpet PeF Ljubljana 7. december 2007 Kazalo 1 Fizikalne osnove 2 1.1 Energija in informacija............................... 3 2 Projekti iz fizike
II. gimnazija Maribor PROJEKTNA NALOGA. Mentor oblike: Mirko Pešec, prof. Predmet: kemija - informatika
 II. gimnazija Maribor PROJEKTNA NALOGA Mentor vsebine: Irena Ilc, prof. Avtor: Andreja Urlaub Mentor oblike: Mirko Pešec, prof. Predmet: kemija - informatika Selnica ob Dravi, januar 2005 KAZALO VSEBINE
II. gimnazija Maribor PROJEKTNA NALOGA Mentor vsebine: Irena Ilc, prof. Avtor: Andreja Urlaub Mentor oblike: Mirko Pešec, prof. Predmet: kemija - informatika Selnica ob Dravi, januar 2005 KAZALO VSEBINE
Najprej zapišemo 2. Newtonov zakon za cel sistem v vektorski obliki:
 NALOGA: Po cesi vozi ovornjak z hirosjo 8 km/h. Tovornjak je dolg 8 m, širok 2 m in visok 4 m in ima maso 4 on. S srani začne pihai veer z hirosjo 5 km/h. Ob nekem času voznik zaspi in ne upravlja več
NALOGA: Po cesi vozi ovornjak z hirosjo 8 km/h. Tovornjak je dolg 8 m, širok 2 m in visok 4 m in ima maso 4 on. S srani začne pihai veer z hirosjo 5 km/h. Ob nekem času voznik zaspi in ne upravlja več
8. Diskretni LTI sistemi
 8. Diskreti LI sistemi. Naloga Določite odziv diskretega LI sistema s podaim odzivom a eoti impulz, a podai vhodi sigal. h[] x[] - - 5 6 7 - - 5 6 7 LI sistem se a vsak eoti impulz δ[] a vhodu odzove z
8. Diskreti LI sistemi. Naloga Določite odziv diskretega LI sistema s podaim odzivom a eoti impulz, a podai vhodi sigal. h[] x[] - - 5 6 7 - - 5 6 7 LI sistem se a vsak eoti impulz δ[] a vhodu odzove z
S t r a n a 1. 1.Povezati jonsku jačinu rastvora: a) MgCl 2 b) Al 2 (SO 4 ) 3 sa njihovim molalitetima, m. za so tipa: M p X q. pa je jonska jačina:
 S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
POROČILO 3.VAJA DOLOČANJE REZULTANTE SIL
 POROČILO 3.VAJA DOLOČANJE REZULTANTE SIL Izdba aje: Ljubjana, 11. 1. 007, 10.00 Jan OMAHNE, 1.M Namen: 1.Preeri paraeogramsko praio za doočanje rezutante nezporedni si s skupnim prijemaiščem (grafično)..dooči
POROČILO 3.VAJA DOLOČANJE REZULTANTE SIL Izdba aje: Ljubjana, 11. 1. 007, 10.00 Jan OMAHNE, 1.M Namen: 1.Preeri paraeogramsko praio za doočanje rezutante nezporedni si s skupnim prijemaiščem (grafično)..dooči
Galvanski členi. Mentor: Gregor Skačej. 24. september 2009
 Galvanski členi Blaž Šterbenc Mentor: Gregor Skačej 24. september 2009 Povzetek V seminarju bom na kratko opisal zgodovinski razvoj galvanskih členov, obravnaval nernstovo enačbo uporaba za izračun električnih
Galvanski členi Blaž Šterbenc Mentor: Gregor Skačej 24. september 2009 Povzetek V seminarju bom na kratko opisal zgodovinski razvoj galvanskih členov, obravnaval nernstovo enačbo uporaba za izračun električnih
Transformator. Delovanje transformatorja I. Delovanje transformatorja II
 Transformator Transformator je naprava, ki v osnovi pretvarja napetost iz enega nivoja v drugega. Poznamo vrsto različnih izvedb transformatorjev, glede na njihovo specifičnost uporabe:. Energetski transformator.
Transformator Transformator je naprava, ki v osnovi pretvarja napetost iz enega nivoja v drugega. Poznamo vrsto različnih izvedb transformatorjev, glede na njihovo specifičnost uporabe:. Energetski transformator.
Prenos toplote prenos energije katerega pogojuje razlika temperatur temperatura je krajevno od točke do točke različna
 PRENOS OPOE Def. Prenos toplote prenos energije katerega pogojuje razlika temperatur temperatura je krajevno od točke do točke različna Načini prenosa toplote: PREVAJANJE (kondukcija, PRESOP (konvekcija
PRENOS OPOE Def. Prenos toplote prenos energije katerega pogojuje razlika temperatur temperatura je krajevno od točke do točke različna Načini prenosa toplote: PREVAJANJE (kondukcija, PRESOP (konvekcija
cot x ni def. 3 1 KOTNE FUNKCIJE POLJUBNO VELIKEGA KOTA (A) Merske enote stopinja [ ] radian [rad] 1. Izrazi kot v radianih.
![cot x ni def. 3 1 KOTNE FUNKCIJE POLJUBNO VELIKEGA KOTA (A) Merske enote stopinja [ ] radian [rad] 1. Izrazi kot v radianih. cot x ni def. 3 1 KOTNE FUNKCIJE POLJUBNO VELIKEGA KOTA (A) Merske enote stopinja [ ] radian [rad] 1. Izrazi kot v radianih.](/thumbs/72/66438140.jpg) TRIGONOMETRIJA (A) Merske enote KOTNE FUNKCIJE POLJUBNO VELIKEGA KOTA stopinja [ ] radian [rad] 80 80 0. Izrazi kot v radianih. 0 90 5 0 0 70. Izrazi kot v stopinjah. 5 8 5 (B) Definicija kotnih funkcij
TRIGONOMETRIJA (A) Merske enote KOTNE FUNKCIJE POLJUBNO VELIKEGA KOTA stopinja [ ] radian [rad] 80 80 0. Izrazi kot v radianih. 0 90 5 0 0 70. Izrazi kot v stopinjah. 5 8 5 (B) Definicija kotnih funkcij
Reševanje sistema linearnih
 Poglavje III Reševanje sistema linearnih enačb V tem kratkem poglavju bomo obravnavali zelo uporabno in zato pomembno temo linearne algebre eševanje sistemov linearnih enačb. Spoznali bomo Gaussovo (natančneje
Poglavje III Reševanje sistema linearnih enačb V tem kratkem poglavju bomo obravnavali zelo uporabno in zato pomembno temo linearne algebre eševanje sistemov linearnih enačb. Spoznali bomo Gaussovo (natančneje
Matematika I (VS) Univerza v Ljubljani, FE. Melita Hajdinjak 2013/14. Pregled elementarnih funkcij. Potenčna funkcija. Korenska funkcija.
 1 / 46 Univerza v Ljubljani, FE Potenčna Korenska Melita Hajdinjak Matematika I (VS) Kotne 013/14 / 46 Potenčna Potenčna Funkcijo oblike f() = n, kjer je n Z, imenujemo potenčna. Število n imenujemo eksponent.
1 / 46 Univerza v Ljubljani, FE Potenčna Korenska Melita Hajdinjak Matematika I (VS) Kotne 013/14 / 46 Potenčna Potenčna Funkcijo oblike f() = n, kjer je n Z, imenujemo potenčna. Število n imenujemo eksponent.
Logatherm WPL 14 AR T A ++ A + A B C D E F G A B C D E F G. kw kw /2013
 WP 14 R T d 9 10 11 53 d 2015 811/2013 WP 14 R T 2015 811/2013 WP 14 R T Naslednji podatki o izdelku izpolnjujejo zahteve uredb U 811/2013, 812/2013, 813/2013 in 814/2013 o dopolnitvi smernice 2010/30/U.
WP 14 R T d 9 10 11 53 d 2015 811/2013 WP 14 R T 2015 811/2013 WP 14 R T Naslednji podatki o izdelku izpolnjujejo zahteve uredb U 811/2013, 812/2013, 813/2013 in 814/2013 o dopolnitvi smernice 2010/30/U.
p 1 ENTROPIJSKI ZAKON
 ENROPIJSKI ZAKON REERZIBILNA srememba: moža je obrjea srememba reko eakih vmesih staj kot rvota srememba. Po obeh sremembah e sme biti obeih trajih srememb v bližji i dalji okolici. IREERZIBILNA srememba:
ENROPIJSKI ZAKON REERZIBILNA srememba: moža je obrjea srememba reko eakih vmesih staj kot rvota srememba. Po obeh sremembah e sme biti obeih trajih srememb v bližji i dalji okolici. IREERZIBILNA srememba:
vaja Kvan*ta*vno določanje proteinov. 6. vaja Kvan*ta*vno določanje proteinov. 6. vaja Kvan*ta*vno določanje proteinov
 28. 3. 11 UV- spektrofotometrija Biuretska metoda Absorbanca pri λ=28 nm (A28) UV- spektrofotometrija Biuretska metoda vstopni žarek intenziteta I Lowrijeva metoda Bradfordova metoda Bradfordova metoda
28. 3. 11 UV- spektrofotometrija Biuretska metoda Absorbanca pri λ=28 nm (A28) UV- spektrofotometrija Biuretska metoda vstopni žarek intenziteta I Lowrijeva metoda Bradfordova metoda Bradfordova metoda
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * NAVODILA ZA OCENJEVANJE. Sreda, 3. junij 2015 SPLOŠNA MATURA
 Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
UPOR NA PADANJE SONDE V ZRAKU
 UPOR NA PADANJE SONDE V ZRAKU 1. Hitrost in opravljena pot sonde pri padanju v zraku Za padanje v zraku je odgovorna sila teže. Poleg sile teže na padajoče telo deluje tudi sila vzgona, ki je enaka teži
UPOR NA PADANJE SONDE V ZRAKU 1. Hitrost in opravljena pot sonde pri padanju v zraku Za padanje v zraku je odgovorna sila teže. Poleg sile teže na padajoče telo deluje tudi sila vzgona, ki je enaka teži
Osnove sklepne statistike
 Univerza v Ljubljani Fakulteta za farmacijo Osnove sklepne statistike doc. dr. Mitja Kos, mag. farm. Katedra za socialno farmacijo e-pošta: mitja.kos@ffa.uni-lj.si Intervalna ocena oz. interval zaupanja
Univerza v Ljubljani Fakulteta za farmacijo Osnove sklepne statistike doc. dr. Mitja Kos, mag. farm. Katedra za socialno farmacijo e-pošta: mitja.kos@ffa.uni-lj.si Intervalna ocena oz. interval zaupanja
2 VAJA: POVRŠINSKO AKTIVNE SNOVI IN KRITIČNA MICELSKA KONCENTRACIJA
 MEDFAZNA NAPETOST IN MOČENJE 2 VAJA: POVRŠINSKO AKTIVNE SNOVI IN KRITIČNA MICELSKA KONCENTRACIJA 2.1 Površinska in medfazna napetost Vsako molekulo v tekočini privlačijo sosednje molekule in rezultante
MEDFAZNA NAPETOST IN MOČENJE 2 VAJA: POVRŠINSKO AKTIVNE SNOVI IN KRITIČNA MICELSKA KONCENTRACIJA 2.1 Površinska in medfazna napetost Vsako molekulo v tekočini privlačijo sosednje molekule in rezultante
MERITVE LABORATORIJSKE VAJE. Študij. leto: 2011/2012 UNIVERZA V MARIBORU. Skupina: 9
 .cwww.grgor nik ol i c NVERZA V MARBOR FAKTETA ZA EEKTROTEHNKO, RAČNANŠTVO N NFORMATKO 2000 Maribor, Smtanova ul. 17 Študij. lto: 2011/2012 Skupina: 9 MERTVE ABORATORJSKE VAJE Vaja št.: 4.1 Določanj induktivnosti
.cwww.grgor nik ol i c NVERZA V MARBOR FAKTETA ZA EEKTROTEHNKO, RAČNANŠTVO N NFORMATKO 2000 Maribor, Smtanova ul. 17 Študij. lto: 2011/2012 Skupina: 9 MERTVE ABORATORJSKE VAJE Vaja št.: 4.1 Določanj induktivnosti
Zaporedna in vzporedna feroresonanca
 Visokonapetostna tehnika Zaporedna in vzporedna feroresonanca delovanje regulacijskega stikala T3 174 kv Vaja 9 1 Osnovni pogoji za nastanek feroresonance L C U U L () U C () U L = U L () U C = ωc V vezju
Visokonapetostna tehnika Zaporedna in vzporedna feroresonanca delovanje regulacijskega stikala T3 174 kv Vaja 9 1 Osnovni pogoji za nastanek feroresonance L C U U L () U C () U L = U L () U C = ωc V vezju
PROCESIRANJE SIGNALOV
 Rešive pisega izpia PROCESIRANJE SIGNALOV Daum: 7... aloga Kolikša je ampliuda reje harmoske kompoee arisaega periodičega sigala? f() - -3 - - 3 Rešiev: Časova fukcija a iervalu ( /,/) je lieara fukcija:
Rešive pisega izpia PROCESIRANJE SIGNALOV Daum: 7... aloga Kolikša je ampliuda reje harmoske kompoee arisaega periodičega sigala? f() - -3 - - 3 Rešiev: Časova fukcija a iervalu ( /,/) je lieara fukcija:
LABORATORIJSKE VAJE IZ KEMIJE
 UNIVERZA V LJUBLJANI Biotehniška fakulteta Oddelek za živilstvo LABORATORIJSKE VAJE IZ KEMIJE Dodatek za študente bolonjskega študija 1. stopnje Živilstva in prehrane Nataša Šegatin Ljubljana, 2015 Naslov:
UNIVERZA V LJUBLJANI Biotehniška fakulteta Oddelek za živilstvo LABORATORIJSKE VAJE IZ KEMIJE Dodatek za študente bolonjskega študija 1. stopnje Živilstva in prehrane Nataša Šegatin Ljubljana, 2015 Naslov:
Slika, vir: http://www.manataka.org
 KEMIJA Slika, vir: http://www.manataka.org RAZTOPINE SPLOŠNE INFORMACIJE O GRADIVU Učno gradivo je nastalo v okviru projekta Munus 2. Njegovo izdajo je omogočilo sofinanciranje Evropskega socialnega sklada
KEMIJA Slika, vir: http://www.manataka.org RAZTOPINE SPLOŠNE INFORMACIJE O GRADIVU Učno gradivo je nastalo v okviru projekta Munus 2. Njegovo izdajo je omogočilo sofinanciranje Evropskega socialnega sklada
Frekvenčna analiza neperiodičnih signalov. Analiza signalov prof. France Mihelič
 Frekvenčna analiza neperiodičnih signalov Analiza signalov prof. France Mihelič Vpliv postopka daljšanja periode na spekter periodičnega signala Opazujmo družino sodih periodičnih pravokotnih impulzov
Frekvenčna analiza neperiodičnih signalov Analiza signalov prof. France Mihelič Vpliv postopka daljšanja periode na spekter periodičnega signala Opazujmo družino sodih periodičnih pravokotnih impulzov
Osnove matematične analize 2016/17
 Osnove matematične analize 216/17 Neža Mramor Kosta Fakulteta za računalništvo in informatiko Univerza v Ljubljani Kaj je funkcija? Funkcija je predpis, ki vsakemu elementu x iz definicijskega območja
Osnove matematične analize 216/17 Neža Mramor Kosta Fakulteta za računalništvo in informatiko Univerza v Ljubljani Kaj je funkcija? Funkcija je predpis, ki vsakemu elementu x iz definicijskega območja
Vaja: Odbojnostni senzor z optičnimi vlakni. Namen vaje
 Namen vaje Spoznavanje osnovnih fiber-optičnih in optomehanskih komponent Spoznavanje načela delovanja in praktične uporabe odbojnostnega senzorja z optičnimi vlakni, Delo z merilnimi instrumenti (signal-generator,
Namen vaje Spoznavanje osnovnih fiber-optičnih in optomehanskih komponent Spoznavanje načela delovanja in praktične uporabe odbojnostnega senzorja z optičnimi vlakni, Delo z merilnimi instrumenti (signal-generator,
3.1 Površinska napetost
 3 Tekočine Lastnosti tekočin so za fiziologijo pomembne, saj kar približno 70 % človeškega telesa sestavlja najpomembnejša tekočina voda. Osnovna lastnost tekočin je, da ohranjajo prostornino, ne pa tudi
3 Tekočine Lastnosti tekočin so za fiziologijo pomembne, saj kar približno 70 % človeškega telesa sestavlja najpomembnejša tekočina voda. Osnovna lastnost tekočin je, da ohranjajo prostornino, ne pa tudi
Bojan Božič, Jure Derganc, Gregor Gomišček, Vera Kralj-Iglič, Janja Majhenc, Mojca Mally, Praktikum iz biofizike Študijsko leto 2017/2018
 Bojan Božič, Jure Derganc, Gregor Gomišček, Vera Kralj-Iglič, Janja Majhenc, Mojca Mally, Primož Peterlin, Saša Svetina in Boštjan Žekš Praktikum iz biofizike Študijsko leto 2017/2018 Ljubljana, oktober
Bojan Božič, Jure Derganc, Gregor Gomišček, Vera Kralj-Iglič, Janja Majhenc, Mojca Mally, Primož Peterlin, Saša Svetina in Boštjan Žekš Praktikum iz biofizike Študijsko leto 2017/2018 Ljubljana, oktober
TRDNOST (VSŠ) - 1. KOLOKVIJ ( )
 TRDNOST (VSŠ) - 1. KOLOKVIJ (17. 12. 03) Pazljivo preberite besedilo vsake naloge! Naloge so točkovane enakovredno (vsaka 25%)! Pišite čitljivo! Uspešno reševanje! 1. Deformiranje telesa je podano s poljem
TRDNOST (VSŠ) - 1. KOLOKVIJ (17. 12. 03) Pazljivo preberite besedilo vsake naloge! Naloge so točkovane enakovredno (vsaka 25%)! Pišite čitljivo! Uspešno reševanje! 1. Deformiranje telesa je podano s poljem
Analiza 2 Rešitve 14. sklopa nalog
 Analiza Rešitve 1 sklopa nalog Navadne diferencialne enačbe višjih redov in sistemi diferencialnih enačb (1) Reši homogene diferencialne enačbe drugega reda s konstantnimi koeficienti: (a) 6 + 8 0, (b)
Analiza Rešitve 1 sklopa nalog Navadne diferencialne enačbe višjih redov in sistemi diferencialnih enačb (1) Reši homogene diferencialne enačbe drugega reda s konstantnimi koeficienti: (a) 6 + 8 0, (b)
1. Έντυπα αιτήσεων αποζημίωσης... 2 1.1. Αξίωση αποζημίωσης... 2 1.1.1. Έντυπο... 2 1.1.2. Πίνακας μεταφράσεων των όρων του εντύπου...
 ΑΠΟΖΗΜΙΩΣΗ ΘΥΜΑΤΩΝ ΕΓΚΛΗΜΑΤΙΚΩΝ ΠΡΑΞΕΩΝ ΣΛΟΒΕΝΙΑ 1. Έντυπα αιτήσεων αποζημίωσης... 2 1.1. Αξίωση αποζημίωσης... 2 1.1.1. Έντυπο... 2 1.1.2. Πίνακας μεταφράσεων των όρων του εντύπου... 3 1 1. Έντυπα αιτήσεων
ΑΠΟΖΗΜΙΩΣΗ ΘΥΜΑΤΩΝ ΕΓΚΛΗΜΑΤΙΚΩΝ ΠΡΑΞΕΩΝ ΣΛΟΒΕΝΙΑ 1. Έντυπα αιτήσεων αποζημίωσης... 2 1.1. Αξίωση αποζημίωσης... 2 1.1.1. Έντυπο... 2 1.1.2. Πίνακας μεταφράσεων των όρων του εντύπου... 3 1 1. Έντυπα αιτήσεων
3. VAJA IZ TRDNOSTI. Rešitev: Pomik v referenčnem opisu: u = e y 2 e Pomik v prostorskem opisu: u = ey e. e y,e z = e z.
 3. VAJA IZ TRDNOSTI (tenzor deformacij) (pomiki togega telesa, Lagrangev in Eulerjev opis, tenzor velikih deformacij, tenzor majhnih deformacij in rotacij, kompatibilitetni pogoji) NALOGA 1: Gumijasti
3. VAJA IZ TRDNOSTI (tenzor deformacij) (pomiki togega telesa, Lagrangev in Eulerjev opis, tenzor velikih deformacij, tenzor majhnih deformacij in rotacij, kompatibilitetni pogoji) NALOGA 1: Gumijasti
0,00275 cm3 = = 0,35 cm = 3,5 mm.
 1. Za koliko se bo dvignil alkohol v cevki termometra s premerom 1 mm, če se segreje za 5 stopinj? Prostorninski temperaturni razteznostni koeficient alkohola je 11 10 4 K 1. Volumen alkohola v termometru
1. Za koliko se bo dvignil alkohol v cevki termometra s premerom 1 mm, če se segreje za 5 stopinj? Prostorninski temperaturni razteznostni koeficient alkohola je 11 10 4 K 1. Volumen alkohola v termometru
Kvadratne forme. Poglavje XI. 1 Definicija in osnovne lastnosti
 Poglavje XI Kvadratne forme V zadnjem poglavju si bomo ogledali še eno vrsto preslikav, ki jih tudi lahko podamo z matrikami. To so tako imenovane kvadratne forme, ki niso več linearne preslikave. Kvadratne
Poglavje XI Kvadratne forme V zadnjem poglavju si bomo ogledali še eno vrsto preslikav, ki jih tudi lahko podamo z matrikami. To so tako imenovane kvadratne forme, ki niso več linearne preslikave. Kvadratne
