Στερεοηλεκτρονικά ελεγχόμενοι μετασχηματισμοί.
|
|
|
- Βαυκις Ζάχος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 Σελίδα 1 /24 1. ΑΣΚΗΣΗ Η 5-κετοεννεανο-1,9-διόλη, με θέρμανση παρουσία καταλυτικής ποσότητας οξέος, κυκλοποιείται με αφυδάτωση προς την σπειροκετάλη,όπως φαίνεται στο σχήμα που ακολουθεί. Προτείνετε ένα μηχανισμό για την κυκλοποίηση συμπεριλαμβάνοντας και τα ενδιάμεσα που σχηματίζονται. Σχεδιάστε τα δύο εναντιομερή της σπειροκετάλης χρησιμοποιώντας τύπους ανάκλιντρου για τους εξαμελείς δακτυλίους. Σχεδιάστε τα διαμορφομερή της δομής της σπειροκετάλης Ποιο από τα διαμορφομερή θεωρείτε ότι είναι το επικρατέστερο εξηγώντας με ποια κριτήρια καταλήξατε στο συμπέρασμα. Παρατήρηση α) Στις κετάλες και ημιακετάλες λειτουργούν ανωμερικά φαινόμενα. Παρατήρηση β) Για την σχεδίαση των ανακλίντρων των σπειροενώσεων είναι πολύ σημαντικό να ακολουθείται ο τρόπος σχεδίασης που υποδεικνύεται παρακάτω,προκειμένου να προκύπτουν ευκρινείς και κατανοητοί τύποι. Τυπική λύση-απάντηση και σχετικά σχόλια. Η αντίδραση κυκλοποίησης παράγει την χειρόμορφη σπειροκετάλη ως το μοναδικό προϊόν,ρακεμικό μείγμα των δύο εναντιομερών μορφών της.
2 Σελίδα 2 /24 Η χειρομορφία εμφανίζεται κατά την δημιουργία της ενδιάμεσης ημιακετάλης, η οποία προκύπτει ως ρακεμικό μείγμα από την προσθήκη της ακραίας υδροξυλομάδας στην μια ή την άλλη από τις δύο εναντιοτοπικές πλευρές του καρβονυλίου. Οι δύο υδροξυλομάδες είναι ισοδύναμες (ομοτοπικές) λόγω του άξονα συμμετρίας C2 κατά μήκος του καρβονυλίου. Η κάθε μία από τις εναντιομερείς ημιακετάλες με το κλείσιμο του δεύτερου δακτυλίου μετατρέπεται αποκλειστικά στο αντίστοιχο εναντιομερές της σπειροένωσης. Τα δύο εναντιομερή βρίσκονται σε δυναμική ισορροπία όχι με απευθείας αλληλομετατροπή τους αλλά μέσω της αρχικής κετόνης.
3 Σελίδα 3 /24 Εάν δεχτούμε ότι οι δυο σπειροδακτύλιοι βρίσκονται σε διαμορφώσεις ανακλίντρων,τότε με τις αναστροφές των δακτυλίων θα πρέπει να προκαλείται διαμορφωτική ισομερίωση και τα ισομερή αυτά θα βρίσκονται όπως συμβαίνει πολύ συχνά, σε δυναμική ισορροπία. Τα διαμορφομερή της σπειροκετάλης. Εάν σχεδιασθεί η σπειροκετάλη όπως υποδεικνύεται στην παρατήρηση 2,με τα άτομα οξυγόνου σε αξονική τοποθέτηση όσον αφορά και τα δύο ανάκλιντρα, λαμβάνεται το πρώτο διαμορφομερές του σχήματος που ακολουθεί. Η αμοιβαίες αξονικές θέσεις των οξυγόνων σημειώνονται με έντονους κόκκινους δεσμούς. Τυχαία επιλέχτηκε να σχεδιασθεί η (S) εναντιομερής μορφή αλλά προφανώς τα ίδια ισχύουν και για την ( R). Με προσεκτική παρατήρηση της δομής της σπειροκετάλης διαπιστώνεται η ύπαρξη ενός άξονα συμμετρίας C2 στην διχοτόμο της γωνίας των οξυγόνων,όπως δείχνεται στο προηγούμενο σχήμα. Η ύπαρξη αυτού του στοιχείου συμμετρίας καθιστά τα δύο ανάκλιντρα ομοτοπικά και συνεπώς αρκεί να
4 Σελίδα 4 /24 ελεγχθούν οι συνδυασμοί : A) αναστροφή ενός μόνο δακτυλίου (οποιουδήποτε!). B) αναστροφή ταυτόχρονα και των δύο δακτυλίων. Αναστροφή του οριζόντιου ανάκλιντρου,που σημειώνεται με έντονους δεσμούς, οδηγεί από την δις αξονική δομή στην αξονική-ισημερινή δομή,όπου ο ισημερινός δεσμός οξυγόνου σημειώνεται με έντονο πράσινο. Αναστροφή αμφότερων των ανακλίντρων οδηγεί στο διαμορφομερές με αμφότερα τα οξυγόνα σε ισημερινές θέσεις και για τους δύο δακτυλίους, που σημειώνονται με έντονο πράσινο. Συνολικά λοιπόν εντοπίζονται τρία διαμορφομερή σε δυναμική ισορροπία: δις αξονικό- αξονικό-ισημερινό- δις ισημερινό
5 Σελίδα 5 /24 Οσον αφορά τις σχετικές τους θερμοδυναμικές σταθερότητες ένα προφανές δομικό χαρακτηριστικό είναι οι σχετικές θέσεις των οξυγόνων που έχει σαν αποτέλεσμα την εμφάνιση η μη της ανωμερικής αλληλεπίδρασης (που είναι πάντα σταθεροποιητικός παράγοντας): Διπλό ανωμερικό >> απλό ανωμερικό >> καθόλου ανωμερικό. Συμπληρωματικά για το ζήτημα 1. Τρόποι σχεδίασης. Καλοί και κακοί τύποι. Αλλαγές της προοπτικής σχεδίασης προκειμένου να προκύψει ένας στερεοχημικά ακριβής αλλά και εύκολα αντιληπτός τύπος.
6 Σελίδα 6 /24 2. ΑΣΚΗΣΗ Όταν το δις-διυδροπυράνιο (ένωση 1) θερμανθεί με αιθυλενογλυκόλη σε διάλυμα τολουολίου παρουσία καταλυτικής ποσότητας 4-τολουολοσουλφονικού οξέος μετατρέπεται κατά 75% σε ένα μείγμα δισπειροκεταλών (2,3,4) το οποίο βρίσκεται σε δυναμική ισορροπία με την αρχική ουσία. Μια από τις δισπειροκετάλες υπερέχει κατά πολύ των άλλων δύο και αποτελεί το κύριο συστατικό του μίγματος. Ποιό είναι το κύριο προϊόν της αντίδρασης? Που οφείλεται αυτή η στερεοεκλεκτικότητα της αντίδρασης? Μπορούν οι σπειροκετάλες 2,3 και 4 να αλληλομετατραπούν χωρίς διάνοιξη ενός τουλάχιστον από τους δακτυλίους? (Είναι δηλαδή διαστερεομερείς δομές εκ διαμορφώσεως η όχι?) Τυπική απάντηση: Εφόσον το μίγμα αρχικής ουσίας και διαστερεομερών προϊόντων βρίσκεται σε θερμοδυναμική ισορροπία το επικρατέστερο προϊόν θα είναι το θερμοδυναμικά σταθερότερο. Οι εναλλακτικές δομές που δίδονται,ως κετάλες που είναι,εμφανίζουν τη δυνατότητα ανωμερικής σταθεροποίησης εφόσον βέβαια οι δεσμοί των οξυγόνων έχουν τις απαιτούμενες αξονικές τοποθετήσεις στους υφιστάμενους εξαμελείς δακτυλίους. Με προσεκτική παρατήρηση των δομών προκύπτει ότι η δομή Ι εμφανίζει τετραπλή ανωμερική αλληλεπίδραση σε αντίθεση με τις ΙΙ και ΙΙΙ που εμφανίζουν μόνο τριπλή και διπλή αντίστοιχα.
7 Σελίδα 7 /24 Στο σχήμα εμφανίζονται χρωματισμένοι οι δεσμοί και τα ασύζευκτα ηλεκτρόνια των οξυγόνων που πληρούν την απαραίτητη αντιπαραλληλία που μεγιστοποιεί την ανωμερική σταθεροποίηση. Με διαμορφωτικές αλλαγές στους εξαμελείς δακτυλίους των εικονιζόμενων δομών δεν είναι εφικτή η αλληλομετατροπή τους η οποία μπορεί να επιτευχθεί μόνο με διάνοιξη δεσμών, δηλαδή μόνο μέσω της αρχικής δομής ( η και των ενδιαμέσων) της συνολικής ισορροπίας. Συκγεκριμένα: Η δομή 3 της ερώτησης είναι το εναντιομερές της ανεστραμμένης 1 και αν και ισοενεργειακή με αυτήν δεν μπορεί να προκύψει από την 1 με απλή διαμορφωτική αλλαγή. Όσον αφορά την δομή 2 της ερώτησης προφανώς δεν υπάρχει διαμορφωτική συσχέτιση με τις 1 και2. Συμπληρωματικά για την άσκηση. Συνολικός αριθμός στερεοϊσομερών ν. Οι δύο σπειροάνθρακες συνιστούν δύο στερεογονικά κέντρα στο τελικό προϊόν. Με βάση το διοξανικό δακτύλιο (μεσαίος)οι κατευθύνσεις των οξυγόνων μπορεί να είναι trans είτε cis μεταξύ τους (δομές 2 είτε 3 και 1 είτε 4,αντίστοιχα).
8 Σελίδα 8 /24 Σχήμα 1. Προσθήκη των υδροξυλίων της διόλης στο δδ του βυνυλαιθέρα. Σχήμα 2. cis-trans ισομερή στον διοξανικό δακτύλιο. 1: R,S 2: R,R 3: S,S 4: S,R Οι δομές 2 και 3 δεν είναι κατ ανάγκη εναντιόμορφα όπως φαίνεται στις επίπεδες (προβολικές ) απεικονίσεις. Ομοίως και οι δομές 1,4 δεν είναι η ίδια μεσομορφή και αυτό γιατί οι δακτύλιοι δεν είναι επίπεδοι αλλά ανάκλιντρα στο χώρο και επί πλέον με δυνατότητα αναστροφών. Σχήμα 3. Δομή 1: cis -ισομερές. Δομή 2: trans -ισομερές.
9 Σελίδα 9 /24 Οι διαμορφώσεις των πλευρικών δακτυλίων δεν επηρεάζουν την σχετική στερεοχημεία του διοξανικού δακτυλίου και μπορούν προς στιγμήν να αγνοηθούν προκειμένου να διευκολυνθεί η σχεδίαση τύπων η οποία είναι ούτως η άλλως δύσκολη για τα δισπειροσυστήματα. Σχήμα 4 To cis διοξάνιο με αναστροφή του δακτυλίου εναντιομεριώνεται διατηρώντας το συνολικό αριθμό αξονικών οξυγόνων. Το trans ισομερές μπορει να βρίσκεται ασφαλώς είτε στην trans διαξονική είτε την trans διισημερινή διαμόρφωση Η δομή 2 εμφανίζει τη μέγιστη σταθεροποίηση επειδή επιτρέπει την λειτουργία ενός τετραπλού ανωμερικού φαινομένου μεταξύ των οξυγόνων που όλα τους κατέχουν αξονικές θέσεις. Με αναστροφή του διοξανικού ανάκλιντρου το trans διαξονικό ισομερές 2 μετατρέπεται στο trans διισημερινό το οποίο έχει χάσει την σταθεροποίηση που συνεισέφεραν τα δυο αξονικά οξυγόνα και μένει μόνο με το διπλό ανωμερικό στους πλευρικούς δακτυλίους.
10 Σελίδα 10 /24 Σχήμα 5. Αναστροφή του trans υποκατεστημένου διοξανικού δακτυλίου προς το διισημερινό διαμορφομερές (μέσα στην παρένθεση).αλλαγή της προοπτικής με περιστροφή περί κατακόρυφο άξονα προκειμένου να βελτιωθεί το σχέδιο της δομής. Εάν αναστραφούν και οι πλευρικοί δακτύλιοι η διαμορφομερής δομή που προκύπτει έχει όλα τα οξυγόνα σε ισημερινές θέσεις και δεν επωφελείται από κανένα ανωμερικό φαινόμενο.θεωρείται λοιπόν η λιγότερο σταθερή υπο την προϋπόθεση ότι το μοναδικό κριτήριο σταθεροποίσης είναι το ανωμερικό φαινόμενο και ότι δεν υπάρχουν άλλοι στερεοχημικοί παράγοντες που παίζουν ρόλο. Εικόνα 6. Το σταθερότερο διαστερεοισομερές 2 στο οποίο ο διοξανικός δακτύλιος φέρει τους υποκαταστάτες οξυγόνα σε trans σχετική στερεοχημεία και όλοι οι δεσμοί C-O είναι αξονικοί για όλα τα ανάκλιντρα. Για να δείτε και να περιεργασθείτε ένα τρισδιάστατο διαδραστικό μοντέλο της δομής αυτής μεταβείτε σε αυτή τη θέση.
11 Σελίδα 11 /24 Εικόνα 7. To trans διισημερινό διαμορφομερές το οποίο δεν διαθέτει ανωμερική σταθεροποίηση στον διοξανικό δακτύλιο. Οι πλευρικοί δακτύλιοι είναι ανάκλιντρα με αξονικούς δεσμούς στα οξυγόνα και διαθέτουν ανωμερική σταθεροποίηση. Για να δείτε και να περιεργασθείτε ένα τρισδιάστατο διαδραστικό μοντέλο της δομής αυτής μεταβείτε σε αυτή τη θέση. 3. ΑΣΚΗΣΗ Η αντίδραση που περιγράφεται στο ακόλουθο σχήμα είναι μια αντίδραση θραυσμάτωσης του σκελετού δεκαλίνης του παραγώγου που προκαλείται από την ισχυρή βάση. Προτείνετε ένα μηχανισμό γι αυτή την αντίδραση χρησιμοποιώντας στερεοχημικούς τύπους ανάκλιντρου και κυρτά βέλη για να δείξετε τις μετακινήσεις ηλεκτρονικής πυκνότητας. Εξηγήστε γιατί η στερεοχημεία της αρχικής ουσίας είναι καθοριστική για την πραγματοποίηση της μετατροπής και σημειώσετε τους δεσμούς που διανοίγονται. Τυπική απάντηση: Η μετακίνηση της ηλεκτρονικής πυκνότητας γίνεται κατά μήκος των αντιπαράλληλων δεσμών του σκελετού της δεκαλίνης
12 Σελίδα 12 /24 Ο δότης είναι το άτομο βορίου το οποίο είναι αρνητικά φορτισμένο λόγω της προσθήκης υδροξειδίου ανιόντος από το βασικό περιβάλλον. Ο δέκτης της ηλεκτρονικής πυκνότητας είναι η τοσυλοξυ ομάδα η οποία και αποσπάται ως ανιόν ενώ ταυτόχρονα σχηματίζεται ο δδ του οποίου η trans γεωμετρία επιβάλλεται από την αντιπαραλληλία των δεσμών. 4. ΑΣΚΗΣΗ. Η αντίδραση του ακόλουθου σχήματος περιγράφηκε από τον R.B.Woodward και είναι ενα κρίσιμο στάδιο της σύνθεσης προσταγλανδίνης που πραγματοποίησε ο ίδιος. Πρόκειται για μια μεταθετική αντίδραση που καταλήγει σε σμίκρυνση δακτυλίου (τύπου Tiffeneau-Demjanov ).Η αντίδραση, λόγω της αποβολής αερίου αζώτου από την διάσπαση του διαζωνιακού άλατος, είναι μη αντιστρεπτή και κατά συνέπεια θεωρείται ότι λειτουργεί αποκλειστικά υπό κινητικό έλεγχο. Προτείνετε ένα μηχανισμό γι αυτό το μετασχηματισμό. Προβλέψατε την στερεοχημεία στα χειρικά κέντρα του προϊόντος που είναι σημειωμένα με αστερίσκους.
13 Σελίδα 13 /24 Δείξτε τους δεσμούς που εμπλέκονται στην διεργασία και προσδιορίστε με κυρτά βέλη την μετακίνηση ηλεκτρονικής πυκνότητας. Τυπική απάντηση: Η αντίδραση Tiffeneau-Demjanov είναι μια μετάθεση παρόμοια με την πινακολινική μετάθεση αλλά με αποχωρούσα ομάδα το διαζόνιο κατιόν (ως στοιχειακό άζωτο).επειδή τα αλειφατικά διαζωνιακά άλατα δεν είναι απομονώσιμα αλλά διασπώνται αμέσως μόλις σχηματισθούν,παρασκευάζονται in situ από την κατάλληλη πρωτοταγή αμίνη με μια τυπική αντίδραση διαζώτωσης, πχ με επίδραση όξινου διαλύματος NaNO 2. Ο μηχανισμός της διαζώτωσης είναι όπως φαίνεται παρακάτω. Μόλις σχηματισθεί το διαζωνιακό (κόκκινο πλαίσιο) αποβάλει αέριο άζωτο προκαλώντας την διάσπαση και μετακίνηση του αντιπαράλληλου δεσμού C-C του εξαμελούς δακτυλίου ο οποίος έτσι μετατρέπεται σε πενταμελή. Ο άλλος αντιπαράλληλος δεσμός του ανάκλιντρου δεν διασπάται ασφαλώς επειδή δεν διαθέτει την υδροξυλομάδα που θ; σταθεροποιήσει το αναπτυσσόμενο θετικό φορτίο (σχηματίζοντας την σταθερή καρβονυλομάδα). Σχηματισμός in situ του διαζωνιακού κατιόντος Διάσπαση του διαζωνιακού και μετακίνηση του αντιπαράλληλου σ-δεσμού.
14 Σελίδα 14 /24 Οι έντονα χρωματισμένοι δεσμοί είναι αντιπαράλληλοι. Ηλεκτρονική πυκνότητα μετατοπίζεται από το μη δεσμικό τροχιακό του Οξυγόνου προς το θετικά φορτισμένο διαζώνιο. Η μεταθετικός μηχανισμός εξηγεί πλήρως την παρατηρούμενη αντίδραση και ιδιαίτερα την στερεοχημεία του προϊόντος αφού η αλδεϋδομάδα οδηγείται από το μηχανισμό να σχηματισθεί σε θέση cis προς τον προϋπάρχοντα πενταμελή δακτύλιο. Εναλλακτικός μηχανισμός; Προσεκτικότερη παρατήρηση του διαζωνιακού αποκαλύπτει ότι η ύπαρξη της αξονικής β- υδροξυλομάδας δίνει την δυνατότητα να διατυπωθεί και μια δεύτερη πρόταση ως προς τον τρόπο με τον οποίο γίνεται η αντίδραση: 1 ο στάδιο: Θραυσμάτωση τύπου Grob,όπου και πάλι διανοίγεται ο ίδιος όπως και προηγούμενα αντιπαράλληλος δεσμός αλλά με την συμμετοχή μονήρους ζεύγους από το οξυγόνο της β-υδροξυλομάδας.μια τέτοια μετακίνηση ηλεκτρονίων οδηγεί στο σχηματισμό μιας διαλδεϋδης (η α-αλδεϋδη ως ενόλη) 2 ο στάδιο: Αλδολική συμπύκνωση που οδηγεί στο σχηματισμό της αλδεϋδομάδας και του πενταμελούς δακτυλίου του προϊόντος, όπως δείχνεται στο σχήμα που ακολουθεί. Ένας τέτοιος μηχανισμός όμως δεν φαίνεται να είναι στερεοχημικά ελεγχόμενος και συνεπώς ενδέχεται το προϊόν να σχηματισθεί ως μείγμα διαστερεομερών σε μη προβλέψιμες αναλογίες. Αυτό βεβαίως δεν αποκλείει λογικά την λειτουργία ενός τέτοιου μηχανισμού,τον κάνει όμως λιγότερο πιθανό.
15 Σελίδα 15 /24 5. ΑΣΚΗΣΗ Α) Σχεδιάστε το σταθερότερο διαμορφομερές για κάθε μια από τις ενώσεις 1-7 εξηγώντας τις επιλογές που κάνατε. Απάντηση. Β) Όταν κάθε μία από τις διαστερεομερείς βρωμοϋδρίνες 1 4 υποστεί κατεργασία με οξείδιο του Αργύρου(Ι), (Ag 2 O) μετατρέπεται σε μία ( κυρίως ) από τις ενώσεις 5-7. Προσδιορίστε ποιο προϊόν προκύπτει από κάθε βρωμοϋδρίνη και δικαιολογήστε σχετικά.
16 Σελίδα 16 /24 Η τριτοταγής βουτυλομάδα είναι τόσο ογκώδης που προτιμά κατά πολύ να βρίσκεται σε ισημερινή θέση προκειμένου να αποφύγει τις δυσμενείς 1,3-διαξονικές παρεμποδίσεις. Αυτό έχει ως συνέπεια την διαμορφωτική «ακινητοποίηση» πρακτικά του μορίου στην μία μόνο από τις δύο εναλλακτικές διαμορφώσεις ανακλίντρου ώστε οι σχετικές θέσεις των διάφορων υποκαταστατών να είναι σαφώς καθορισμένες (αξονικές είτε ισημερινές). Το άτομο αργύρου(ι) είναι οξύ Lewis και μάλιστα με αυξημένη προτίμηση στα μονήρη ζεύγη των αλογόνων με τα οποία τελικά σχηματίζει τα σταθερά αλογονίδια του αργύρου AgX.H σύμπλεξή του στην προκειμένη περίπτωση με το ισημερινό βρώμιο της ένωσης 1,αποσταθεροποιεί τον δεσμό C-Br ο οποίος έλκει ηλεκτρόνια από τον αντιπαράλληλο δεσμό του δακτυλίου και προκαλεί την μετάθεση 1,2 που δημιουργεί τον πενταμελή δακτύλιο. Η ίδια γεωμετρία ισχύει και για το ισομερές 2 το οποίο και αυτό δίνει το ίδιο προϊόν αλδεΰδη. Σχήμα: 8 Σμίκρυνση δακτυλίου μέσω της 1,2 μετάθεσης αλκυλίου (ημιπινακολινική μετάθεση) που προκαλείται απο την απόσπαση του ισημερινού βρωμίου. Στην ένωση 3 το βρώμιο έχει αξονική θέση και συνεπώς ο γειτονικός αντιπαράλληλος δεσμός (αξονικός) είναι αυτός που έχει την βέλτιστη γεωμετρία για να προσφέρει ηλεκτρόνια.παρατηρείται λοιπόν (κατά κύριο λόγο) μετάθεση ανιόντος υδρογόνου και ταυτόχρονος σχηματισμός του σταθερού καρβονυλικού δεσμού στην ίδια θέση,ώστε το προϊόν να είναι το παράγωγο της κυκλοεξανόνης 6. Για την ένωση 3 θα μπορούσε να προταθεί εναλλακτικά ένας μηχανισμός β-απόσπασης πρωτονίου (αφυδραλογόνωση) και σχηματισμού δδ ενόλης ο οποίος θα οδηγούσε με ταυτομερίωση στην αντίστοιχη κετομορφή ( προϊόν 6.) Το μειονέκτημα αυτής της πρότασης είναι ότι οι αποσπάσεις πρωτονίου χρειάζονται γενικά την παρουσία μιας βάσης και το οξείδιο του αργύρου μολονότι είναι ένα μεταλλοξείδιο, δεν θεωρείται αρκετά βασικό γι αυτό το ρόλο. Πέραν αυτού,η αφυδροβρωμίωση είναι ένας λογικός μηχανισμός γι αυτή την αντίδραση.
17 Σελίδα 17 /24 Σχήμα 9: Μετακίνηση υδριδίου απο την αντιπαράλληλη θέση στο απομακρυνόμενο βρώμιο. Όσον αφορά την ένωση 4 το αξονικό βρώμιο έχει σε αντιπαράλληλη αξονική τοποθέτηση την υδροξυλομάδα και συνεπώς η προσφορότερη πηγή ηλεκτρονίων είναι τα μονήρη ζεύγη του οξυγόνου το οποίο έτσι σχηματίζει δεσμό με τον ηλεκτροθετικό άνθρακα που φέρει το βρώμιο παράγοντας το εποξείδιο 7. Σχήμα 10. Σχηματισμός εποξειδίου (τριμελής δακτύλιος οξιρανίου) από την αντιπαράλληλη υδροξυλομάδα. 6. ΑΣΚΗΣΗ Τα στερεοηλεκτρονικά φαινόμενα προκύπτουν από την επικάλυψη μοριακών τροχιακών σε γειτονικά άτομα ενός μορίου. Σταθεροποιητικές αλληλεπιδράσεις προκύπτουν πχ από ένα μη δεσμικό ζεύγος και ένα παρακείμενο αντιδεσμικό τροχιακό κλπ. Α)Δείξτε σε ένα ενεργειακό διάγραμμα πως η αλληλοεπικάλυψη κατειλημμένων και κενών τροχιακών σε γειτονικές θέσεις μειώνει την ενέργεια του συστήματος. Β)Εξηγήστε πως εξαρτάται η σταθεροποίηση από τις ενεργειακές στάθμες και τον προσανατολισμό των τροχιακών που αλληλεπιδρούν.
18 Σελίδα 18 /24 ΕΝΔΕΙΚΤΙΚΗ ΑΠΑΝΤΗΣΗ. Το κατειλημμένο τροχιακό (πχ ένα n μη δεσμικό τροχιακό) πρέπει να να βρίσκεται σε χαμηλώτερη ενεργειακή στάθμη από το κενό τροχιακό (πχ ένα σ* αντιδεσμικό τροχιακό).η αλληλεπίδραση ανάμεσα σ αυτά τα δύο τροχιακά δημιουργεί δύο νέα μοριακά τροχιακά: Ένα σε ενεργειακή στάθμη χαμηλότερη από αυτήν και των δύο αρχικών τροχιακών και ένα σε υψηλότερη. Δύο ηλεκτρόνια καταλαμβάνουν το τροχιακό χαμηλότερης ενέργειας και συνεπώς επέρχεται σταθεροποίηση κατά: Εσταθ Σχήμα 11. Ενεργειακό Διάγραμμα υβριδοποίησης μοριακών τροχιακών. Η ενέργεια σταθεροποίησης (ΔΕ) είναι αντιστρόφως ανάλογη της ενεργειακής διαφοράς των αρχικών τροχιακών που αλληλεπιδρούν. Όσο πλησιέστερες είναι οι στάθμες των τροχιακών τόσο μεγαλύτερο είναι το ενεργειακό όφελος. Η ενέργεια σταθεροποίησης είναι ευθέως ανάλογη προς το τετράγωνο του ολοκληρώματος επικάλυψης.το ολοκλήρωμα επικάλυψης είναι ένα μέτρο της αποτελεσματικότητας της αμοιβαίας γεωμετρικής επικάλυψης των τροχιακών. Η αποτελεσματικότητα της επικάλυψης εξαρτάται άμεσα από το σχετικό προσανατολισμό των τροχιακών όπως και από το σχετικό μέγεθός τους. Σε γενικές γραμμές ισχύει η ακόλουθη διαπίστωση: Αντι-περιεπίπεδη σχέση (anti) είναι η βέλτιστη Συν-περιεπίπεδη σχέση (syn) είναι μέτρια έως καλή Όλες οι άλλες τοποθετήσεις είναι αναποτελεσματικές.
19 Σελίδα 19 /24 Σχήμα 12. Η γεωμετρία της καλύτερης επικάλυψης είναι η anti (αντι-περιεπίπεδη). 7. ΑΣΚΗΣΗ. Τα γεωμετρικά ισομερή του διφθοροδιιμίδιου (i) βρίσκονται σε συνήθεις συνθήκες σε θερμοδυναμική ισορροπία η οποία όμως είναι μετατοπισμένη υπέρ του ενός εκ των δύο. Τα διαμορφομερή της υδραζίνης (ii) επίσης δείχνουν διαφορετική σταθερότητα. Προσδιορίστε προς ποιά πλευρά είναι μετατοπισμένες οι ισορροπίες και εξηγήστε χρησιμοποιώντας στερεοηλεκτρονικά επιχειρήματα. ΑΠΑΝΤΗΣΗ.
20 Σελίδα 20 /24 (i). Το cis-ισομερές είναι το προτιμώμενο, δηλ αυτό με την χαμηλότερη ενέργεια. Παρ όλον ότι το trans-ισομερές είναι και λιγότερο παρεμποδισμένο στερεοχημικά και έχει καλύτερη διπολική σταθεροποίηση (με αντιπαράλληλα τα δίπολα Ν-F), εν τούτοις δεν είναι το κυρίαρχο μέλος της ισορροπίας. Ο καθοριστικός παράγοντας εδώ είναι η ανωμερική σταθεροποίηση μεταξύ μονήρων ζευγών του οξυγόνου και του γειτονικού δεσμού N-F.Αυτή η σταθεροποίηση είναι βέλτιστη για το cis ισομερές όπου κάθε φθόριο έχει σε αντιπαράλληλη θέση το μονήρες ζεύγος του γειτονικού αζώτου. Σχήμα 13. Το φαινόμενο gauche για το διφθοροδιιμίδιο. (i).το συνκλινές (gauche) διαμορφομερές είναι το προτιμώμενο (χαμηλότερης ενέργειας).και τα δύο διαμορφομερή είναι διαβαθμισμένα και έτσι ελαχιστοποιούν την διεδρική τάση (στροφική τάση η τάση Pfizzer).To anti διαμορφομερές ευνοείται από διπολικά φαινόμενα αλλά και πάλι ο καθοριστικός παράγοντας είναι η λειτουργία δυο ανωμερικών φαινομένων μεταξύ των μονήρων ζευγών του αζώτου και των αντιπαράλληλων με αυτά σ* Ν-Η τροχιακών. Σχήμα 14. Το φαινόμενο gauche στο μόριο της υδραζίνης. 8. ΑΣΚΗΣΗ.
21 Σελίδα 21 /24 Προτείνετε μία εξήγηση για την ασυνήθιστα μεγάλη διαφορά στη συχνότητα δόνησης του καρβονυλίου που παρατηρείται ανάμεσα στα δύο αμίδια που εικονίζονται παρακάτω. ΑΠΑΝΤΗΣΗ. Η δόνηση τάσης του καρβονυλικού δεσμού είναι ένα μέτρο της ισχύος αυτού του δεσμού.η ισχύς του δεσμού συσχετίζεται με την τάξη του δεσμού δηλ το ποσοστό δδ το οποίο με τη σειρά του συσχετίζεται με την αποτελεσματικότητα του συντονισμού n Np ->π* c=o.όσο καλύτερος είναι αυτός ο συντονισμός τόσο λιγότερο χαρακτήρα δδ έχει το καρβονύλιο και συνεπώς τόσο μικρότερη τάξη δεσμού δηλ τόσο ασθενέστερος θα είναι ο καρβονυλικός δεσμός, δηλ τόσο χαμηλότερη θα είναι η συχνότητα απορρόφησης στο IR. Για την λακτάμη στα δεξιά, το άζωτο βρίσκεται σε κεφαλή γέφυρας μικρού δικυκλικού σκελετού και συνεπώς είναι αναγκαστικά πυραμιδικής γεωμετρίας η οποία επιβάλει στον λοβό που περιέχει το μονήρες ζεύγος κατεύθυνση σχεδόν ορθογωνική προς το τροχιακό του καρβονυλίου. Έτσι η επικάλυψη είναι κακή και ο καρβονυλικός δεσμός ισχυρός δηλαδή υψηλότερης συχνότητας. Σχήμα 15. Έλλειψη αμιδικού χαρακτήρα στο παράγωγο της κινουκλιδόνης
22 Σελίδα 22 /24 9. ΑΣΚΗΣΗ. Το διχλωρίδιο που εικονίζεται παρακάτω είναι ένα εύτηκτο κρυσταλλικό στερεό η κρυσταλλογραφική ανάλυση του οποίου έδωσε τα μήκη δεσμών που αναγράφονται στο σχήμα. Εξηγήστε γιατί το αξονικό άτομο χλωρίου έχει μακρύτερο δεσμό από το ισημερινό. ΑΠΑΝΤΗΣΗ. Ο αξονικός δεσμός είναι πιο επιμηκυμένος επειδή το αντιδεσμικό τροχιακό σ* αυτού του δεσμού συμμετέχει σε ένα ανωμερικό φαινόμενο με το αντιπαράλληλο μονήρες ζεύγος (n osp3 ).του γειτονικού οξυγόνου του δακτυλίου. Ο ισημερινός δεσμός C-Cl δεν μπορεί να κάνει κάτι ανάλογο επειδή σε αντιπαράλληλη θέση βρίσκεται ένας δεσμός C-O ο οποίος είναι κακός δότης. Αξίζει να αναφερθεί επίσης ότι το ανάκλιντρο αναστρέφεται ταχύτατα στο ισοενεγειακό εναντιομερές (διαμορφωτική εναντιομερίωση) στο οποίο τα χλώρια έχουν ανταλλάξει θέσεις. Προφανώς στο κρυσταλλικό πλέγμα τα χλώρια διατηρούν τον διαφορετικό τους χαρακτήρα.
23 Σελίδα 23 / ΑΣΚΗΣΗ. Προτείνετε ένα μηχανισμό για τις ακόλουθες δύο αντιδράσεις αναφέροντας επίσης εάν υπάρχει στερεοηλεκτρονικός έλεγχος. Λάβετε υπ όψιν σας ότι το διαζωμεθάνιο είναι ένα καλό πυρηνόφιλο το οποίο αντιδρά με ηλεκτρονιόφιλους άνθρακες. ΑΠΑΝΤΗΣΗ. Για την πρώτη αντίδραση: Πρωτονίωση του υδροξυλίου δημιουργεί την καλή αποχωρούσα ομάδα Η 2 Ο.Η απόσπαση νερού ξεκινά μια πινακολινική μετάθεση η οποία καταλήγει σε διεύρυνση δακτυλίου.οι γεωμετρικές απαιτήσεις του μηχανισμού είναι η αντιπαραλληλία όλων των εμπλεκόμενων τροχιακών. Για την δεύτερη αντίδραση:
24 Σελίδα 24 /24 Πυρηνόφιλη προσθήκη του διαζωμεθανίου στο καρβονύλιο έχει σαν αποτέλεσμα την δημιουργία ενός διαζώνιου κατιόντος το οποίο διασπώμενο δίνει το έναυσμα για το ξεκίνημα μια ημιπινακολινικής αντίδρασης μετάθεσης η οποία καταλήγει όπως και προηγουμένως σε διεύρυνση δακτυλίου. Σημείωση: Από το σχετικό σχήμα είναι φανερό ότι το θετικό φορτίο που δημιουργεί στον πρωτοταγή άνθρακα το διαζώνιο κατιόν, μπορεί να εξουδετερωθεί και απ ευθείας από το μονήρες ζεύγος του οξυγόνου με δημιουργία ενός οξιρανικού δακτυλίου. Είναι γνωστό άλλωστε ότι τα προϊόντα μετάθεσης αυτών των αντιδράσεων συνοδεύονται σχεδόν πάντα από παραπροϊόντα εποξείδια. Σχήμα 16. Σχηματισμός εποξειδίου ανταγωνιστικά προς την μεταθετική αντίδραση.
ΣΤΕΡΕΟΗΛΕΚΤΡΟΝΙΚΑ ΕΛΕΓΧΟΜΕΝΕΙΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΕ ΚΥΚΛΟΕΞΑΝΙΑ ΜΕ ΟΜΗ ΗΜΙΑΝΑΚΛΙΝΤΡΟΥ α. διάνοιξη του οξιρανικού δακτυλίου σε κυκλοεξενοξείδια.
 bstelc ΣΤΕΡΕΟΗΛΕΚΤΡΟΝΙΚΑ ΕΛΕΓΧΟΜΕΝΕΙΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΕ ΚΥΚΛΟΕΞΑΝΙΑ ΜΕ ΟΜΗ ΗΜΙΑΝΑΚΛΙΝΤΡΟΥ α. διάνοιξη του οξιρανικού δακτυλίου σε κυκλοεξενοξείδια. Όπως έχει αναφερθεί κατά τη συζήτηση των διαµορφώσεων των
bstelc ΣΤΕΡΕΟΗΛΕΚΤΡΟΝΙΚΑ ΕΛΕΓΧΟΜΕΝΕΙΣ ΑΝΤΙ ΡΑΣΕΙΣ ΣΕ ΚΥΚΛΟΕΞΑΝΙΑ ΜΕ ΟΜΗ ΗΜΙΑΝΑΚΛΙΝΤΡΟΥ α. διάνοιξη του οξιρανικού δακτυλίου σε κυκλοεξενοξείδια. Όπως έχει αναφερθεί κατά τη συζήτηση των διαµορφώσεων των
ιαστερεοεκλεκτικότητα σε κυκλικά δικυκλικά µόρια. Πενταµελείς και εξαµελείς συµπυκνωµένοι δακτύλιοι.
 diabicy1 1 ιαστερεοεκλεκτικότητα σε κυκλικά δικυκλικά µόρια. Πενταµελείς και εξαµελείς συµπυκνωµένοι δακτύλιοι. Cis-συµπυκνωµένοι πενταµελείς δακτύλιοι. Ένα δικυκλικό σύστηµα µε δυο συµπυκνωµένους πενταµελείς
diabicy1 1 ιαστερεοεκλεκτικότητα σε κυκλικά δικυκλικά µόρια. Πενταµελείς και εξαµελείς συµπυκνωµένοι δακτύλιοι. Cis-συµπυκνωµένοι πενταµελείς δακτύλιοι. Ένα δικυκλικό σύστηµα µε δυο συµπυκνωµένους πενταµελείς
O H ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση. Στερεοχημεία-Μηχανισμοί (Μάθημα 629, Επιλεγόμενο) Διδάσκων :Κ.Χ.Φρούσιος Τμηματικές Εξετάσεις 08 ΣΕΠ 2010 Διάρκεια εξέτασης
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση. Στερεοχημεία-Μηχανισμοί (Μάθημα 629, Επιλεγόμενο) Διδάσκων :Κ.Χ.Φρούσιος Τμηματικές Εξετάσεις 08 ΣΕΠ 2010 Διάρκεια εξέτασης
aldo B 1 Σχήµα 15. Παρουσία κετόνης (πηγή πρωτονίων) προκαλείται σταδιακή µετατροπή του κινητικού µίγµατος ενολικών σε θερµοδυναµικό.
 aldo B 1 ογκώδεις υποκαταστάτες του αζώτου αλλά δηµιουργώντας έτσι αλλυλική τάση Α 1, 2 µε το µεθύλιο της θέσης 1 (τοποθέτηση cis των µεθυλοµάδων στο trans ενολικό). Η ΜΚ του cis-ενολικού µε αξονική µεθυλοµάδα
aldo B 1 ογκώδεις υποκαταστάτες του αζώτου αλλά δηµιουργώντας έτσι αλλυλική τάση Α 1, 2 µε το µεθύλιο της θέσης 1 (τοποθέτηση cis των µεθυλοµάδων στο trans ενολικό). Η ΜΚ του cis-ενολικού µε αξονική µεθυλοµάδα
EtOH. OEt. µοναδικό ισοµερές, cis ή trans ;
 ΠΡΟΒΛΗΜΑ 2.1 2 / i + 3 C Et 3 C ακόρεστη ακετάλη A Et Et ισοµερίωση B µοναδικό ισοµερές, cis ή trans ; Το φάσµα 1 MR της υδρογονωµένης ακετάλης δείχνει σήµατα σε δ 3,95 ( 1 Η, πολύπλοκη, J 0.5, 3.9, 9.5
ΠΡΟΒΛΗΜΑ 2.1 2 / i + 3 C Et 3 C ακόρεστη ακετάλη A Et Et ισοµερίωση B µοναδικό ισοµερές, cis ή trans ; Το φάσµα 1 MR της υδρογονωµένης ακετάλης δείχνει σήµατα σε δ 3,95 ( 1 Η, πολύπλοκη, J 0.5, 3.9, 9.5
ΘΕΜΑ 1. ΘΕΜΑ 2. NH 2 H 2. Σχηματίζεται γρήγορα. Σταθερότερο
 ΘΕΜΑ 1. Πείραμα Α. Ενα μείγμα ισομοριακών ποσοτήτων κυκλοεξανόνης,φουρφουράλης και σεμικαρβαζιδίου βράζεται με αναρροή σε διαλύτη αιθανόλη επι εξι ώρες,ψύχεται και η σεμικαρβαζόνη που αποβάλεται απομονώνεται
ΘΕΜΑ 1. Πείραμα Α. Ενα μείγμα ισομοριακών ποσοτήτων κυκλοεξανόνης,φουρφουράλης και σεμικαρβαζιδίου βράζεται με αναρροή σε διαλύτη αιθανόλη επι εξι ώρες,ψύχεται και η σεμικαρβαζόνη που αποβάλεται απομονώνεται
ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΗΣ ΣΧΕΤΙΚΗΣ ΣΤΕΡΕΟΧΗΜΕΙΑΣ ΥΠΟΚΑΤΕΣΤΗΜΕΝΩΝ ΚΥΚΛΙΚΩΝ ΕΝΩΣΕΩΝ (cis trans ισοµέρεια)
 relst1 1 ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΗΣ ΣΧΕΤΙΚΗΣ ΣΤΕΡΕΟΧΗΜΕΙΑΣ ΥΠΟΚΑΤΕΣΤΗΜΕΝΩΝ ΚΥΚΛΙΚΩΝ ΕΝΩΣΕΩΝ (cis trans ισοµέρεια) Οι θέσεις των διάφορων υποκαταστατών ενός κυκλικού µορίου µε αναφορά στο επίπεδο του δακτυλίου,
relst1 1 ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΗΣ ΣΧΕΤΙΚΗΣ ΣΤΕΡΕΟΧΗΜΕΙΑΣ ΥΠΟΚΑΤΕΣΤΗΜΕΝΩΝ ΚΥΚΛΙΚΩΝ ΕΝΩΣΕΩΝ (cis trans ισοµέρεια) Οι θέσεις των διάφορων υποκαταστατών ενός κυκλικού µορίου µε αναφορά στο επίπεδο του δακτυλίου,
Σχεδιάστε τύπους ανακλίντρων για τις ενώσεις Α και Β και εξηγήστε σχετικά. Yπόδειξη : Η αντίδραση Μichael θεωρείται γενικά αντιστρεπτή αντίδραση.
 1 1 H 3 C H 3 C αναγωγή H 3 C H 3 C H H ± A B Η διφαινυλική κετόνη Α εµφανίζει ατροποϊσοµέρεια και σε συνήθη θερµοκρασία µπορεί να αναλυθεί σε δυο σταθερές έναντιοµερικές µορφές. 1. Χαρακτηρίστε τις πλευρές
1 1 H 3 C H 3 C αναγωγή H 3 C H 3 C H H ± A B Η διφαινυλική κετόνη Α εµφανίζει ατροποϊσοµέρεια και σε συνήθη θερµοκρασία µπορεί να αναλυθεί σε δυο σταθερές έναντιοµερικές µορφές. 1. Χαρακτηρίστε τις πλευρές
Tα λογικά βήματα της λύσης μπορεί να είναι αναλυτικά τα ακόλουθα:
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση-Στερεοχημεία και Μηχανισμοί. Μάθημα 629,Επιλεγόμενο Διδάσκων: Κ. Χ. Φρούσιος Εξεταστική Περίοδος Ιουνίου 2013 Διάρκεια εξέτασης
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση-Στερεοχημεία και Μηχανισμοί. Μάθημα 629,Επιλεγόμενο Διδάσκων: Κ. Χ. Φρούσιος Εξεταστική Περίοδος Ιουνίου 2013 Διάρκεια εξέτασης
Me O N H C 2. S D 2 χειρική δοµή. R εναντιοµερές
 ΠΡΟΒΛΗΜΑ 1.1 Απάντηση/ ανάλυση Για την επεξεργασία του συγκεκριµένου προβλήµατος είναι κατάλληλες οι απεικονίσεις κατά Newmman κάθετα στο διφαινυλικό δεσµό. Εάν επιπλέον δεχθούµε ότι το αµιδικό σύστηµα
ΠΡΟΒΛΗΜΑ 1.1 Απάντηση/ ανάλυση Για την επεξεργασία του συγκεκριµένου προβλήµατος είναι κατάλληλες οι απεικονίσεις κατά Newmman κάθετα στο διφαινυλικό δεσµό. Εάν επιπλέον δεχθούµε ότι το αµιδικό σύστηµα
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ
 ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr ΠΥΡΗΝΟΦΙΛΗ ΠΡΟΣΒΟΛΗ ΣΕ ΚΑΡΒΟΝΥΛΙΚΕΣ
ΣΥΓΧΡΟΝΕΣ ΜΕΘΟΔΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΣΥΝΘΕΣΗ ΓΙΑ ΤΟΥΣ ΦΟΙΤΗΤΕΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Δρ. ΧΡΙΣΤΟΦΟΡΟΣ ΚΟΚΟΤΟΣ Email: ckokotos@chem.uoa.gr ΠΥΡΗΝΟΦΙΛΗ ΠΡΟΣΒΟΛΗ ΣΕ ΚΑΡΒΟΝΥΛΙΚΕΣ
Οργανική Χημεία. Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια
 Οργανική Χημεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν ομάδες υδροξυλίου συνδεδεμένες με κορεσμένα άτομα άνθρακα υβριδισμού sp 3 Βάσει παραπάνω ορισμού,
Οργανική Χημεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν ομάδες υδροξυλίου συνδεδεμένες με κορεσμένα άτομα άνθρακα υβριδισμού sp 3 Βάσει παραπάνω ορισμού,
Οργανική Χημεία. Κεφάλαια 20 & 21: Καρβοξυλικά οξέα, παράγωγα τους και αντιδράσεις ακυλο υποκατάστασης
 Οργανική Χημεία Κεφάλαια 20 & 21: Καρβοξυλικά οξέα, παράγωγα τους και αντιδράσεις ακυλο υποκατάστασης 1. Καρβοξυλικά οξέα Σημαντικά ακυλο (-COR) παράγωγα Πλήθος καρβοξυλικών ενώσεων στη φύση, π.χ. οξικό
Οργανική Χημεία Κεφάλαια 20 & 21: Καρβοξυλικά οξέα, παράγωγα τους και αντιδράσεις ακυλο υποκατάστασης 1. Καρβοξυλικά οξέα Σημαντικά ακυλο (-COR) παράγωγα Πλήθος καρβοξυλικών ενώσεων στη φύση, π.χ. οξικό
7.9 Αντιδράσεις που δηµιουργούν ένα στερεογονικό κέντρο
 7.9 Αντιδράσεις που δηµιουργούν ένα στερεογονικό κέντρο Πολλές αντιδράσεις µετατρέπουν µη χειρόµορφα αντιδρώντα σε χειρόµορφα προϊόντα. Εν τούτοις, είναι σηµαντικό να αναγνωρίσουµε, οτι εάν όλα τα συστατικά
7.9 Αντιδράσεις που δηµιουργούν ένα στερεογονικό κέντρο Πολλές αντιδράσεις µετατρέπουν µη χειρόµορφα αντιδρώντα σε χειρόµορφα προϊόντα. Εν τούτοις, είναι σηµαντικό να αναγνωρίσουµε, οτι εάν όλα τα συστατικά
ΕΝΟΤΗΤΑ
 Παρασκευές Αλδεϋδών - Κετονών 17.9 ΕΝΟΤΗΤΑ 17.9 7.8 7.8 8.5 8.5 16.4 Μηχανισµός Ενυδάτωσης Αλκυνίων µε άλατα υδραργύρου ΕΝΟΤΗΤΑ 8.5 Υδροβορίωση τελικών Αλκυνίων και οξείδωση δίνει αλδεΰδες Παρασκευές Αλδεϋδών
Παρασκευές Αλδεϋδών - Κετονών 17.9 ΕΝΟΤΗΤΑ 17.9 7.8 7.8 8.5 8.5 16.4 Μηχανισµός Ενυδάτωσης Αλκυνίων µε άλατα υδραργύρου ΕΝΟΤΗΤΑ 8.5 Υδροβορίωση τελικών Αλκυνίων και οξείδωση δίνει αλδεΰδες Παρασκευές Αλδεϋδών
Οργανική Χημεία. Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες
 Οργανική Χημεία Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες 1. Καρβονυλικές ενώσεις Καρβονυλική ομάδα C=O σημαντικότερη λειτουργική ομάδα οργανικής χημείας Καρβονυλικές ομάδες βρίσκονται
Οργανική Χημεία Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες 1. Καρβονυλικές ενώσεις Καρβονυλική ομάδα C=O σημαντικότερη λειτουργική ομάδα οργανικής χημείας Καρβονυλικές ομάδες βρίσκονται
ΣΤΕΡΕΟΧΗΜΕΙΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΑΝΤΙ ΡΑΣΕΩΝ ΤΟΥ ΚΥΚΛΟΥ KREBS.
 krb1 1 ΣΤΕΡΕΟΧΗΜΕΙΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΑΝΤΙ ΡΑΣΕΩΝ ΤΟΥ ΚΥΚΛΟΥ KREBS. Η προσθήκη νερού στο φουµαρικό οξύ. si si re φουìαρüση anti-προσθþκη 2 re φουìαρικü οξý S-ìηλικü οξý anti- προσθήκη νερού στο δ.δ. του φουµαρικού
krb1 1 ΣΤΕΡΕΟΧΗΜΕΙΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΑΝΤΙ ΡΑΣΕΩΝ ΤΟΥ ΚΥΚΛΟΥ KREBS. Η προσθήκη νερού στο φουµαρικό οξύ. si si re φουìαρüση anti-προσθþκη 2 re φουìαρικü οξý S-ìηλικü οξý anti- προσθήκη νερού στο δ.δ. του φουµαρικού
Καρβονυλοενώσεις 1α) 1α 1β, Σχήμα χχχ)) Σχήμα χχχχ)
 Καρβονυλοενώσεις Καρβονυλοενώσεις (1α) είναι η σημαντικότερη κατηγορία χημικών ενώσεων και χαρακτηρίζεται από ένα διπλό δεσμό μεταξύ ενός ατόμου άνθρακα και ενός οξυγόνου (το καρβονύλιο). Περιλαμβάνει
Καρβονυλοενώσεις Καρβονυλοενώσεις (1α) είναι η σημαντικότερη κατηγορία χημικών ενώσεων και χαρακτηρίζεται από ένα διπλό δεσμό μεταξύ ενός ατόμου άνθρακα και ενός οξυγόνου (το καρβονύλιο). Περιλαμβάνει
Οργανική Χηµεία. Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια
 Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
N Ph + J. Σχήµα 1. Ισορροπία εναντιοµερίωσης ενός ασταθούς χειρικού αµµωνιακού άλατος.
 asrac1 1 Ασύµµετροι µετασχηµατισµοί ρακεµικών µιγµάτων Η απόδοση µιας ανάλυσης ρακεµικού µίγµατος περιορίζεται κατά µέγιστο στο 50% της ποσότητας του ρακεµικού, δηλαδή στο 100% της ποσότητας του ενός εκ
asrac1 1 Ασύµµετροι µετασχηµατισµοί ρακεµικών µιγµάτων Η απόδοση µιας ανάλυσης ρακεµικού µίγµατος περιορίζεται κατά µέγιστο στο 50% της ποσότητας του ρακεµικού, δηλαδή στο 100% της ποσότητας του ενός εκ
Ηλεκτρονικά Φαινόμενα
 Ηλεκτρονικά Φαινόμενα Το επαγωγικό όμως φαινόμενο οδηγεί στη διάχυση της πόλωσης και στο υπόλοιπο μόριο. Έτσι πολώνονται, με φθίνουσα όμως ένταση, και οι επόμενοι άνθρακες που είναι συνδεδεμένοι μέσω σ
Ηλεκτρονικά Φαινόμενα Το επαγωγικό όμως φαινόμενο οδηγεί στη διάχυση της πόλωσης και στο υπόλοιπο μόριο. Έτσι πολώνονται, με φθίνουσα όμως ένταση, και οι επόμενοι άνθρακες που είναι συνδεδεμένοι μέσω σ
Οργανική Χημεία. Κεφάλαιο 26: Βιομόρια: υδατάνθρακες
 Οργανική Χημεία Κεφάλαιο 26: Βιομόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισμό Άμυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαμβάκι είναι καθαροί υδατάνθρακες
Οργανική Χημεία Κεφάλαιο 26: Βιομόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισμό Άμυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαμβάκι είναι καθαροί υδατάνθρακες
Περίληψη Κεφαλαίων 6 & 7
 Περίληψη Κεφαλαίων 6 & 7 Αλκένια: υδρογονάνθρακες µε 1 ή περισσότερους διπλούς δεσµούς Παρεµπόδιση περιστροφής γύρω από δ.δ. cis-trans ισοµέρεια (Ε ή Ζ) Αλκένια δίνουν αντιδράσεις ηλεκτρονιόφιλης προσθήκης
Περίληψη Κεφαλαίων 6 & 7 Αλκένια: υδρογονάνθρακες µε 1 ή περισσότερους διπλούς δεσµούς Παρεµπόδιση περιστροφής γύρω από δ.δ. cis-trans ισοµέρεια (Ε ή Ζ) Αλκένια δίνουν αντιδράσεις ηλεκτρονιόφιλης προσθήκης
2
 1 2 3 4 5 6 7 8 9 Η μικρότερη σταθερότητα της βινυλικής ρίζας (για παράδειγμα σε σχέση με τη μεθυλική) θα μπορούσε να εξηγηθεί στη βάση του πόσο ισχυρά έλκονται τα ηλεκτρόνια από το κάθε άτομο άνθρακα.
1 2 3 4 5 6 7 8 9 Η μικρότερη σταθερότητα της βινυλικής ρίζας (για παράδειγμα σε σχέση με τη μεθυλική) θα μπορούσε να εξηγηθεί στη βάση του πόσο ισχυρά έλκονται τα ηλεκτρόνια από το κάθε άτομο άνθρακα.
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
Αλκυλαλογονίδια. Επίκουρος καθηγητής Χρήστος Παππάς
 Αλκυλαλογονίδια Επίκουρος καθηγητής Χρήστος Παππάς 1 Αλκυλαλογονίδια Αλκυλαλογονίδια ονομάζονται οι οργανικές ενώσεις οι οποίες, ως λειτουργική ομάδα, διαθέτουν την ομάδα C-X: -X= -F, -Cl, -Br, -I. Η ισχύς
Αλκυλαλογονίδια Επίκουρος καθηγητής Χρήστος Παππάς 1 Αλκυλαλογονίδια Αλκυλαλογονίδια ονομάζονται οι οργανικές ενώσεις οι οποίες, ως λειτουργική ομάδα, διαθέτουν την ομάδα C-X: -X= -F, -Cl, -Br, -I. Η ισχύς
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
ΕΝΟΤΗΤΑ 1: ΙΣΟΜΕΡΕΙΑ
 ΕΝΟΤΗΤΑ 1: ΙΣΟΜΕΡΕΙΑ 1 Ισομέρεια, ή ισομερισμός (ως αποτέλεσμα επιδράσεων), λέγεται το φαινόμενο κατά το οποίο δύο ή περισσότερες χημικές ενώσεις αν και αποτελούνται από τα ίδια χημικά στοιχεία, του αυτού
ΕΝΟΤΗΤΑ 1: ΙΣΟΜΕΡΕΙΑ 1 Ισομέρεια, ή ισομερισμός (ως αποτέλεσμα επιδράσεων), λέγεται το φαινόμενο κατά το οποίο δύο ή περισσότερες χημικές ενώσεις αν και αποτελούνται από τα ίδια χημικά στοιχεία, του αυτού
7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή
 7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή Στερεοχημεία της προσθήκης στα αλκένια C C + E Y E C C Y Για να μάθετε να κατανοείτε τη στερεοχημεία του προϊόντος, χρειάζεται να γνωρίζετε δυο πράγματα:
7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή Στερεοχημεία της προσθήκης στα αλκένια C C + E Y E C C Y Για να μάθετε να κατανοείτε τη στερεοχημεία του προϊόντος, χρειάζεται να γνωρίζετε δυο πράγματα:
Πυρηνόφιλα του Άνθρακα: ΥΛΙΔΙΑ ΦΩΣΦΟΡΟΥ Αντίδραση WITTIG
 Georg Wittig Νόµπελ Χηµείας 1979 Πυρηνόφιλα του Άνθρακα: ΥΛΙΔΙΑ ΦΩΣΦΟΡΟΥ Αντίδραση WITTIG Υλίδιο: Ουδέτερη ένωση µε αρνητικά φορτισµένο άτοµο (C-) ενωµένο µε θετικά φορτισµένο ετεροάτοµο (P+) Υβρίδιο Δοµών
Georg Wittig Νόµπελ Χηµείας 1979 Πυρηνόφιλα του Άνθρακα: ΥΛΙΔΙΑ ΦΩΣΦΟΡΟΥ Αντίδραση WITTIG Υλίδιο: Ουδέτερη ένωση µε αρνητικά φορτισµένο άτοµο (C-) ενωµένο µε θετικά φορτισµένο ετεροάτοµο (P+) Υβρίδιο Δοµών
Μηχανισµός και στερεοχηµεία των ενζυµατικών οξειδοαναγωγών µε συνένζυµα νουκλεοτίδια της πυριδίνης. Εφαρµογή σε οργανικές συνθέσεις.
 nad 1 Μηχανισµός και στερεοχηµεία των ενζυµατικών οξειδοαναγωγών µε συνένζυµα νουκλεοτίδια της πυριδίνης. Εφαρµογή σε οργανικές συνθέσεις. Οι αφυδρογονάσες που καταλύουν την αντιστρεπτή µετατροπή διάφορων
nad 1 Μηχανισµός και στερεοχηµεία των ενζυµατικών οξειδοαναγωγών µε συνένζυµα νουκλεοτίδια της πυριδίνης. Εφαρµογή σε οργανικές συνθέσεις. Οι αφυδρογονάσες που καταλύουν την αντιστρεπτή µετατροπή διάφορων
Οργανική Χηµεία. Κεφάλαιο 26: Βιοµόρια: υδατάνθρακες
 Οργανική Χηµεία Κεφάλαιο 26: Βιοµόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισµό Άµυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαµβάκι είναι καθαροί υδατάνθρακες
Οργανική Χηµεία Κεφάλαιο 26: Βιοµόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισµό Άµυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαµβάκι είναι καθαροί υδατάνθρακες
ΚΑΡΒΟΞΥΛΙΚΑ ΟΞΕΑ ΚΑΙ ΠΑΡΑΓΩΓΑ
 ΚΑΡΒΟΞΥΛΙΚΑ ΟΞΕΑ ΚΑΙ ΠΑΡΑΓΩΓΑ Εισαγωγή στα Καρβοξυλικά Οξέα Ονοματολογία των Καρβοξυλικών Οξέων Δομή και Ιδιότητες των Καρβοξυλικών Οξέων Παρασκευή των Καρβοξυλικών Οξέων Αντιδράσεις των Καρβοξυλικών Οξέων
ΚΑΡΒΟΞΥΛΙΚΑ ΟΞΕΑ ΚΑΙ ΠΑΡΑΓΩΓΑ Εισαγωγή στα Καρβοξυλικά Οξέα Ονοματολογία των Καρβοξυλικών Οξέων Δομή και Ιδιότητες των Καρβοξυλικών Οξέων Παρασκευή των Καρβοξυλικών Οξέων Αντιδράσεις των Καρβοξυλικών Οξέων
Ηλεκτρονιόφιλα Πυρηνόφιλα αντιδραστήρια. Επίκουρος καθηγητής Χρήστος Παππάς
 Ηλεκτρονιόφιλα Πυρηνόφιλα αντιδραστήρια Επίκουρος καθηγητής Χρήστος Παππάς 1 Ηλεκτρονιόφιλα - πυρηνόφιλα αντιδραστήρια Ηλεκτρονιόφιλα λέγονται τα αντιδραστήρια τα οποία δέχονται ένα ή δύο ηλεκτρόνια σε
Ηλεκτρονιόφιλα Πυρηνόφιλα αντιδραστήρια Επίκουρος καθηγητής Χρήστος Παππάς 1 Ηλεκτρονιόφιλα - πυρηνόφιλα αντιδραστήρια Ηλεκτρονιόφιλα λέγονται τα αντιδραστήρια τα οποία δέχονται ένα ή δύο ηλεκτρόνια σε
Οργανική Χηµεία. Κεφάλαια 10 &11: Αλκυλαλογονίδια, ιδιότητες και αντιδράσεις
 Οργανική Χηµεία Κεφάλαια 10 &11: Αλκυλαλογονίδια, ιδιότητες και αντιδράσεις 1. Αλκυλαλογονίδια Βιοµηχανικοί διαλύτες, εισπνεόµενα αναισθητικά στην ιατρική, ψυκτικά µέσα, εντοµοκτόνα και απολυµαντικά Ευρέως
Οργανική Χηµεία Κεφάλαια 10 &11: Αλκυλαλογονίδια, ιδιότητες και αντιδράσεις 1. Αλκυλαλογονίδια Βιοµηχανικοί διαλύτες, εισπνεόµενα αναισθητικά στην ιατρική, ψυκτικά µέσα, εντοµοκτόνα και απολυµαντικά Ευρέως
Υποδειγματικά Λυμένα Προβλήματα Κεφαλαίου 4
 ΔΟΜΗ, ΔΡΑΣΤΙΚΟΤΗΤΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ STRUTURE, REATIVITY AND MEANISM IN ORGANI EMISTRY Διονύσης Α. Παπαϊωάννου Καθηγητής Οργανικής Χημείας Dionysios A. Papaioannou Professor of Organic
ΔΟΜΗ, ΔΡΑΣΤΙΚΟΤΗΤΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ STRUTURE, REATIVITY AND MEANISM IN ORGANI EMISTRY Διονύσης Α. Παπαϊωάννου Καθηγητής Οργανικής Χημείας Dionysios A. Papaioannou Professor of Organic
Ε. Μαλαμίδου-Ξενικάκη
 Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 Ηλεκτρονιόφιλη προσβολή σε παράγωγα του βενζολίου Ασπιρίνη Η ασπιρίνη παρασκευάζεται βιομηχανικά με εκλεκτική ηλεκτρονιόφιλη αρωματική υποκατάσταση της φαινόλης.
Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 Ηλεκτρονιόφιλη προσβολή σε παράγωγα του βενζολίου Ασπιρίνη Η ασπιρίνη παρασκευάζεται βιομηχανικά με εκλεκτική ηλεκτρονιόφιλη αρωματική υποκατάσταση της φαινόλης.
Πυρηνόφιλη Προσθήκη Αµινών: Ιµίνες και Εναµίνες
 Πυρηνόφιλη Προσθήκη Αµινών: Ιµίνες και Εναµίνες Πυρηνόφιλα Αζώτου - Πρωτοταγείς Αµίνες: ΜΗΧΑΝΙΣΜΟΣ Σχηµατισµός Ιµινών ΣΗΜΑΝΤΙΚΕΣ ΛΕΠΤΟΜΕΡΕΙΕΣ Η ταχύτητα σχηµατισµού ιµίνης εξαρτάται από το ph: Σε υψηλό
Πυρηνόφιλη Προσθήκη Αµινών: Ιµίνες και Εναµίνες Πυρηνόφιλα Αζώτου - Πρωτοταγείς Αµίνες: ΜΗΧΑΝΙΣΜΟΣ Σχηµατισµός Ιµινών ΣΗΜΑΝΤΙΚΕΣ ΛΕΠΤΟΜΕΡΕΙΕΣ Η ταχύτητα σχηµατισµού ιµίνης εξαρτάται από το ph: Σε υψηλό
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C;
 Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Διαμόρφωση-διαμορφωμερή
 Οργανική Χημεία Πέτρος Ταραντίλης Αναπληρωτής Καθηγητής Εργαστήριο Χημείας, Τμήμα Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax:
Οργανική Χημεία Πέτρος Ταραντίλης Αναπληρωτής Καθηγητής Εργαστήριο Χημείας, Τμήμα Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax:
Οργανική Χημεία. Κεφάλαιο 16: Χημεία του βενζολίου: ηλεκτρονιόφιλη αρωματική υποκατάσταση
 Οργανική Χημεία Κεφάλαιο 16: Χημεία του βενζολίου: ηλεκτρονιόφιλη αρωματική υποκατάσταση 1. Αντιδράσεις αρωματικών ενώσεων Σημαντικότερη αντίδραση αρωματικών ενώσεων: ηλεκτρονιόφιλη αρωματική υποκατάσταση
Οργανική Χημεία Κεφάλαιο 16: Χημεία του βενζολίου: ηλεκτρονιόφιλη αρωματική υποκατάσταση 1. Αντιδράσεις αρωματικών ενώσεων Σημαντικότερη αντίδραση αρωματικών ενώσεων: ηλεκτρονιόφιλη αρωματική υποκατάσταση
Περίληψη Κεφαλαίου 5
 Περίληψη Κεφαλαίου 5 Είδη αντιδράσεων: προσθήκης, απόσπασης, υποκατάστασης & αναδιάταξης Μηχανισµός αντίδρασης: πλήρης περιγραφή τρόπου πραγµατοποίησης Μηχανισµοί µέσω ριζών ή πολικοί Πολική αντίδράση
Περίληψη Κεφαλαίου 5 Είδη αντιδράσεων: προσθήκης, απόσπασης, υποκατάστασης & αναδιάταξης Μηχανισµός αντίδρασης: πλήρης περιγραφή τρόπου πραγµατοποίησης Μηχανισµοί µέσω ριζών ή πολικοί Πολική αντίδράση
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
C n (H 2 O) ν 22/11/2016 2
 22/11/2016 1 1 C n (H 2 O) ν 22/11/2016 2 Εκτιμάται πως ετησίως παράγονται 100 δισεκατομμύρια τόνοι υδατανθράκων με τη διαδικασία της φωτοσύνθεσης 22/11/2016 3 δεν μπορούν να υδρολυθούν σε άλλα μικρότερα
22/11/2016 1 1 C n (H 2 O) ν 22/11/2016 2 Εκτιμάται πως ετησίως παράγονται 100 δισεκατομμύρια τόνοι υδατανθράκων με τη διαδικασία της φωτοσύνθεσης 22/11/2016 3 δεν μπορούν να υδρολυθούν σε άλλα μικρότερα
MAΘΗΜΑ 3 ο Υ ΑΤΑΝΘΡΑΚΕΣ
 MAΘΗΜΑ ο Υ ΑΤΑΝΘΡΑΚΕΣ Γλυκόζη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr Απλοί υδατάνθρακες ή Μονοσακχαρίτες Σύνθετοι υδατάνθρακες γλυκόζη σακχαρόζη φρουκτόζη
MAΘΗΜΑ ο Υ ΑΤΑΝΘΡΑΚΕΣ Γλυκόζη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr Απλοί υδατάνθρακες ή Μονοσακχαρίτες Σύνθετοι υδατάνθρακες γλυκόζη σακχαρόζη φρουκτόζη
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
- H 2 O O - Σχήµα 1. Σχηµατισµός β-υδροξυκαρβονυλικής και α-ακόρεστης καρβονυλικής ένωσης και ο ρόλος της κατάλυσης (όξινης ή βασικής).
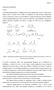 Aldo A 1 ΑΛ ΟΛΙΚΗ ΑΝΤΙ ΡΑΣΗ Γενικά. Ως αλδολική χαρακτηρίζεται η αντίδραση µεταξύ µιας καρβονυλικής ένωσης η οποία υπό τη µορφή ενόλης ή ενολικού ιόντος επιδρά ως πυρηνόφιλο επί µιας δεύτερης καρβονυλικής
Aldo A 1 ΑΛ ΟΛΙΚΗ ΑΝΤΙ ΡΑΣΗ Γενικά. Ως αλδολική χαρακτηρίζεται η αντίδραση µεταξύ µιας καρβονυλικής ένωσης η οποία υπό τη µορφή ενόλης ή ενολικού ιόντος επιδρά ως πυρηνόφιλο επί µιας δεύτερης καρβονυλικής
Μάθημα 21 ο. Το σχήμα των μορίων. Θεωρία VSEPR. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
Δομή. Ως συζυγιακά διένια ορίζουμε τους υδρογονάνθρακες που στην. κύριο χαρακτηριστικό την εναλλαγή των δεσμών (απλών και διπλών) στο μόριο.
 ΣΥΖΥΓΙΑΚA ΔΙΕΝΙA Δομή Ως συζυγιακά διένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχουν δυο διπλούς δεσμούς με κύριο χαρακτηριστικό την εναλλαγή των δεσμών (απλών και διπλών)
ΣΥΖΥΓΙΑΚA ΔΙΕΝΙA Δομή Ως συζυγιακά διένια ορίζουμε τους υδρογονάνθρακες που στην ανθρακική τους αλυσίδα περιέχουν δυο διπλούς δεσμούς με κύριο χαρακτηριστικό την εναλλαγή των δεσμών (απλών και διπλών)
H 2 N CH 2 CH 3 O S. Σχήµα 1. Τα τέσσερα στερεοϊσοµερή µιας ένωσης µε 2 χειρικά κέντρα.
 corlst1 1 Στερεοχηµικοί συσχετισµοί. Απόλυτη και σχετική στερεοχηµεία. Σύγκριση δυο χειρικών κέντρων στο ίδιο µόριο. Έστω για παράδειγµα η διαπίστωση της στερεοχηµείας ενός απλού µορίου µε δυο χειρικά
corlst1 1 Στερεοχηµικοί συσχετισµοί. Απόλυτη και σχετική στερεοχηµεία. Σύγκριση δυο χειρικών κέντρων στο ίδιο µόριο. Έστω για παράδειγµα η διαπίστωση της στερεοχηµείας ενός απλού µορίου µε δυο χειρικά
Κυκλικοί υδρογονάνθρακες
 Κυκλικοί υδρογονάνθρακες C 2 Y C 2 Y C 2 C 2 C n 2n+2 C n 2n : Κορεσμένοι = Ισομερή των αλκενίων C n 2n C n 2n-2 : Μονοακόρεστοι = ισομερή των αλκινίων 1 1. Καύση Αντιδράσεις Αλκανίων C 3 -C 2 -C 3 + 5
Κυκλικοί υδρογονάνθρακες C 2 Y C 2 Y C 2 C 2 C n 2n+2 C n 2n : Κορεσμένοι = Ισομερή των αλκενίων C n 2n C n 2n-2 : Μονοακόρεστοι = ισομερή των αλκινίων 1 1. Καύση Αντιδράσεις Αλκανίων C 3 -C 2 -C 3 + 5
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
Περίληψη Κεφαλαίου 3
 Περίληψη Κεφαλαίου 3 Λειτουργική οµάδα: άτοµο ή σύνολο ατόµων ενός µορίου που προσδίδει χαρακτηριστική χηµική συµπεριφορά στο µόριο Αλκάνια: κατηγορία υδρογονανθράκων µε γενικό µοριακό τύπο C v H 2v+2
Περίληψη Κεφαλαίου 3 Λειτουργική οµάδα: άτοµο ή σύνολο ατόµων ενός µορίου που προσδίδει χαρακτηριστική χηµική συµπεριφορά στο µόριο Αλκάνια: κατηγορία υδρογονανθράκων µε γενικό µοριακό τύπο C v H 2v+2
ΚΕΦΑΛΑΙΟ 9. Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων
 ΚΕΦΑΛΑΙΟ 9 Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων 1 Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων Το αιθοξυαιθάνιο (διαιθυλαιθέρας ή απλώς «αιθέρας») ανακαλύφθηκε ως αναισθητικό
ΚΕΦΑΛΑΙΟ 9 Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων 1 Περισσότερες αντιδράσεις αλκοολών και η χημεία των αιθέρων Το αιθοξυαιθάνιο (διαιθυλαιθέρας ή απλώς «αιθέρας») ανακαλύφθηκε ως αναισθητικό
5.8 Παρασκευές Αλκενίων: Αντιδράσεις απόσπασης. Äρ. ΧÜρηò Ε. ΣεìιδαλÜò Επßκουροò ΚαθηγητÞò ΑΤΕΙ ΑθÞναò
 5.8 Παρασκευές Αλκενίων: Αντιδράσεις απόσπασης Äρ. ΧÜρηò Ε. ΣεìιδαλÜò Επßκουροò ΚαθηγητÞò ΑΤΕΙ ΑθÞναò Σύνοψη των αντιδράσεων της β-απόσπασης Αφυδρογόνωση των αλκανίων: X = Y = Αφυδάτωση των αλκοολών: X
5.8 Παρασκευές Αλκενίων: Αντιδράσεις απόσπασης Äρ. ΧÜρηò Ε. ΣεìιδαλÜò Επßκουροò ΚαθηγητÞò ΑΤΕΙ ΑθÞναò Σύνοψη των αντιδράσεων της β-απόσπασης Αφυδρογόνωση των αλκανίων: X = Y = Αφυδάτωση των αλκοολών: X
Ανάλυση Τροφίμων. Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ. Τμήμα Τεχνολογίας Τροφίμων. Ακαδημαϊκό Έτος
 Ανάλυση Τροφίμων Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση:
Ανάλυση Τροφίμων Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση:
Οργανική Χημεία. Κεφάλαιο 15: Βενζόλιο και αρωματικότητα
 Οργανική Χημεία Κεφάλαιο 15: Βενζόλιο και αρωματικότητα 1. Αρωματικές ενώσεις Αρωματικές ενώσεις: ενώσεις με ευχάριστη οσμή Αρωματικές ενώσεις αναφέρονται συνήθως στο βενζόλιο και σε ενώσεις με συγγενική
Οργανική Χημεία Κεφάλαιο 15: Βενζόλιο και αρωματικότητα 1. Αρωματικές ενώσεις Αρωματικές ενώσεις: ενώσεις με ευχάριστη οσμή Αρωματικές ενώσεις αναφέρονται συνήθως στο βενζόλιο και σε ενώσεις με συγγενική
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ένωση Χ 3 το κεντρικό άτομο Χ φέρει δύο μονήρη ζεύγη ηλεκτρονίων σθένους, ενώ στην ένωση Υ 2 το κεντρικό άτομο Υ φέρει τρία μονήρη ζεύγη ηλεκτρονίων σθένους.
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ένωση Χ 3 το κεντρικό άτομο Χ φέρει δύο μονήρη ζεύγη ηλεκτρονίων σθένους, ενώ στην ένωση Υ 2 το κεντρικό άτομο Υ φέρει τρία μονήρη ζεύγη ηλεκτρονίων σθένους.
ΠΑΡΑΓΩΓΑ ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ. Η κυρίαρχη αντίδραση που καθορίζει τη χηµεία αυτών των παραγώγων είναι οι ΑΝΤΙΔΡΑΣΕΙΣ ΠΥΡΗΝΟΦΙΛΗΣ ΑΚΥΛΟ ΥΠΟΚΑΤΆΣΤΑΣΗΣ:
 ΠΑΡΑΓΩΓΑ ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ Η κυρίαρχη αντίδραση που καθορίζει τη χηµεία αυτών των παραγώγων είναι οι ΑΝΤΙΔΡΑΣΕΙΣ ΠΥΡΗΝΟΦΙΛΗΣ ΑΚΥΛΟ ΥΠΟΚΑΤΆΣΤΑΣΗΣ: ΠΑΡΑΓΩΓΑ ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ ΣΤΗ ΦΥΣΗ Ρυθµίζει τον κύκλο
ΠΑΡΑΓΩΓΑ ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ Η κυρίαρχη αντίδραση που καθορίζει τη χηµεία αυτών των παραγώγων είναι οι ΑΝΤΙΔΡΑΣΕΙΣ ΠΥΡΗΝΟΦΙΛΗΣ ΑΚΥΛΟ ΥΠΟΚΑΤΆΣΤΑΣΗΣ: ΠΑΡΑΓΩΓΑ ΚΑΡΒΟΞΥΛΙΚΩΝ ΟΞΕΩΝ ΣΤΗ ΦΥΣΗ Ρυθµίζει τον κύκλο
Περίληψη Κεφαλαίου 2
 Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 7 η θεματική ενότητα: Οι αντιδράσεις του διπλού δεσμού
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 7 η θεματική ενότητα: Οι αντιδράσεις του διπλού δεσμού Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 7 η θεματική ενότητα: Οι αντιδράσεις του διπλού δεσμού Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
Περίληψη 1 ου Κεφαλαίου
 Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Ε. Μαλαμίδου-Ξενικάκη
 Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 ΑΛΚΥΝΙΑ: C ν H 2ν-2 Ο τριπλός δεσμός άνθρακα άνθρακα Τριπλός δεσμός αλκυνίου ΑΛΚΥΝΙΑ Μόρια πρότυπα για «μοριακούς διακόπτες» Μικροσκοπία σάρωσης σήραγγας (Scanning
Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 ΑΛΚΥΝΙΑ: C ν H 2ν-2 Ο τριπλός δεσμός άνθρακα άνθρακα Τριπλός δεσμός αλκυνίου ΑΛΚΥΝΙΑ Μόρια πρότυπα για «μοριακούς διακόπτες» Μικροσκοπία σάρωσης σήραγγας (Scanning
Ασκήσεις. Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3
 Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής
 ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
Κεφάλαιο 2. Οι μεταβλητές των οργανικών αντιδράσεων
 Κεφάλαιο 2 Οι μεταβλητές των οργανικών αντιδράσεων Σύνοψη Στο κεφάλαιο αυτό αναφέρονται οι αντιδράσεις χωρίς τους μηχανισμούς τους, με στόχο να δοθεί έμφαση στις συνέπειες από τις μεταβολές ορισμένων χαρακτηριστικών
Κεφάλαιο 2 Οι μεταβλητές των οργανικών αντιδράσεων Σύνοψη Στο κεφάλαιο αυτό αναφέρονται οι αντιδράσεις χωρίς τους μηχανισμούς τους, με στόχο να δοθεί έμφαση στις συνέπειες από τις μεταβολές ορισμένων χαρακτηριστικών
Α Ε Τ. ΤΕΙ Αθήνας. Στ. Μπογιατζής, επίκουρος καθηγητής ΤΕΙ Αθήνας. ΤΕΙ Αθήνας / ΣΑΕΤ / Στ. Μπογιατζής
 Στ. Μπογιατζής, επίκουρος καθηγητής Ομοιοπολικές χημικές ενώσεις Ενώσεις του άνθρακα Χαρακτηριστικές ομάδες Τετραεδρική μοριακή δομή Επίπεδη τριγωνική μοριακή δομή Ευθύγραμμη μοριακή δομή Τα οργανικά μόρια
Στ. Μπογιατζής, επίκουρος καθηγητής Ομοιοπολικές χημικές ενώσεις Ενώσεις του άνθρακα Χαρακτηριστικές ομάδες Τετραεδρική μοριακή δομή Επίπεδη τριγωνική μοριακή δομή Ευθύγραμμη μοριακή δομή Τα οργανικά μόρια
Επιφανειακή οξεοβασική κατάλυση
 Επιφανειακή οξεοβασική κατάλυση Μια μεγάλη κατηγορία στερεών καταλυτών εκδηλώνουν επιφανειακή οξεοβασική συμπεριφορά γ-αl 2 O 3, SiO 2, TiO 2, MgO, SiO 2 -Al 2 O 3, ζεόλιθοι Στην επιφάνεια τέτοιων οξειδίων
Επιφανειακή οξεοβασική κατάλυση Μια μεγάλη κατηγορία στερεών καταλυτών εκδηλώνουν επιφανειακή οξεοβασική συμπεριφορά γ-αl 2 O 3, SiO 2, TiO 2, MgO, SiO 2 -Al 2 O 3, ζεόλιθοι Στην επιφάνεια τέτοιων οξειδίων
Οργανική Χημεία. Κεφάλαιο 4: Στερεοχημεία αλκανίων και κυκλοαλκανίων
 Οργανική Χημεία Κεφάλαιο 4: Στερεοχημεία αλκανίων και κυκλοαλκανίων 1. Διατάξεις μορίων στο χώρο Η μορφή των μορίων στο χώρο εξαρτάται από πολλές δυνάμεις Μόριο μπορεί να λάβει διαφορετικές μορφές στο
Οργανική Χημεία Κεφάλαιο 4: Στερεοχημεία αλκανίων και κυκλοαλκανίων 1. Διατάξεις μορίων στο χώρο Η μορφή των μορίων στο χώρο εξαρτάται από πολλές δυνάμεις Μόριο μπορεί να λάβει διαφορετικές μορφές στο
Aντιδράσεις Καρβονυλίου C=O (1)
 Aντιδράσεις Καρβονυλίου = (1) Πυρηνόφιλη προσθήκη (αλδεΰδες, κετόνες) Πυρηνόφιλη ακυλο-υποκατάσταση (καρβοξυλικά οξέα και παράγωγα) α-υποκατάσταση (καρβονυλοενώσεις: αλδεΰδες, κετόνες, καρβοξυλικά οξέα
Aντιδράσεις Καρβονυλίου = (1) Πυρηνόφιλη προσθήκη (αλδεΰδες, κετόνες) Πυρηνόφιλη ακυλο-υποκατάσταση (καρβοξυλικά οξέα και παράγωγα) α-υποκατάσταση (καρβονυλοενώσεις: αλδεΰδες, κετόνες, καρβοξυλικά οξέα
5.14 Αφυδραλογόνωση των αλκυλαλογονιδίων. Δρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας
 5.14 Αφυδραλογόνωση των αλκυλαλογονιδίων Δρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Περίληψη αντιδράσεων β-απόσπασης Αφυδρογόνωση των αλκανίων: X = Y = H Αφυδάτωση των αλκοολών: X = H Y = OH
5.14 Αφυδραλογόνωση των αλκυλαλογονιδίων Δρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Περίληψη αντιδράσεων β-απόσπασης Αφυδρογόνωση των αλκανίων: X = Y = H Αφυδάτωση των αλκοολών: X = H Y = OH
Bιομόρια : Υδατάνθρακες (1)
 Bιομόρια : Υδατάνθρακες () C δομή, ταξινόμηση C απεικονίσεις, διαμορφώσεις C αντιδράσεις Bιομόρια : Υδατάνθρακες (2) C ταξινόμηση - δομή C η γλυκόζη ήταν ο πρώτος απλός υδατάνθρακας που απομονώθηκε σε
Bιομόρια : Υδατάνθρακες () C δομή, ταξινόμηση C απεικονίσεις, διαμορφώσεις C αντιδράσεις Bιομόρια : Υδατάνθρακες (2) C ταξινόμηση - δομή C η γλυκόζη ήταν ο πρώτος απλός υδατάνθρακας που απομονώθηκε σε
4.8 Παρασκευή αλκυλαλογονιδίων από αλκοόλες και υδραλογόνα
 4.8 Παρασκευή αλκυλαλογονιδίων από αλκοόλες και υδραλογόνα RO X RX 2 O ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Αντίδραση αλκοολών με υδραλογόνα RO X RX O δραστικότητα υδραλογόνων I Br Cl
4.8 Παρασκευή αλκυλαλογονιδίων από αλκοόλες και υδραλογόνα RO X RX 2 O ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Αντίδραση αλκοολών με υδραλογόνα RO X RX O δραστικότητα υδραλογόνων I Br Cl
O 3,44 S 2,58 N 3,04 P 2,19
 Περιοδικός Πίνακας (Σύστημα) των Ατόμων Περιοδικό σύστημα είναι ο πίνακας στον οποίο κατατάσσονται όλα τα άτομα με βάση τον αριθμό των πρωτονίων (θετικά φορτισμένα σωματίδια) που ευρίσκονται στον πυρήνα
Περιοδικός Πίνακας (Σύστημα) των Ατόμων Περιοδικό σύστημα είναι ο πίνακας στον οποίο κατατάσσονται όλα τα άτομα με βάση τον αριθμό των πρωτονίων (θετικά φορτισμένα σωματίδια) που ευρίσκονται στον πυρήνα
Γεωμετρία Μορίων Θεωρία VSEPR
 Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια.
 ΑΡΧΕΣ ΧΗΜΕΙΑΣ Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια. Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές
ΑΡΧΕΣ ΧΗΜΕΙΑΣ Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια. Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές
Σύζευξη σπιν-σπιν J = 0 J 0
 Σύζευξη σπιν-σπιν Ας υποθέσουµε ότι έχουµε δύο πυρήνες Α και Χ, οι οποίοι είτε συνδέονται απ ευθείας µε έναν δεσµό είτε η σύνδεσή γίνεται µε περισσότερους δεσµούς. A X J = 0 J 0 Α Χ Α Χ Το σπάσιµο των
Σύζευξη σπιν-σπιν Ας υποθέσουµε ότι έχουµε δύο πυρήνες Α και Χ, οι οποίοι είτε συνδέονται απ ευθείας µε έναν δεσµό είτε η σύνδεσή γίνεται µε περισσότερους δεσµούς. A X J = 0 J 0 Α Χ Α Χ Το σπάσιµο των
Εναντιοεκλεκτικότητα κατά την αντίδραση χειρικών ενολικών µε αχειρικά ηλεκτρονιόφιλα. Ενολικά ιόντα εστέρων και αµιδίων.
 enalkb 1 Εναντιοεκλεκτικότητα κατά την αντίδραση χειρικών ενολικών µε αχειρικά ηλεκτρονιόφιλα. Ενολικά ιόντα εστέρων και αµιδίων. Ένα ενολικό µε ένα τυπικό χειρικό κέντρο στο µόριο του εµφανίζει ασφαλώς
enalkb 1 Εναντιοεκλεκτικότητα κατά την αντίδραση χειρικών ενολικών µε αχειρικά ηλεκτρονιόφιλα. Ενολικά ιόντα εστέρων και αµιδίων. Ένα ενολικό µε ένα τυπικό χειρικό κέντρο στο µόριο του εµφανίζει ασφαλώς
ΑΝΟΡΓΑΝΗ ΙΙΙ. Prof. Dr. Maria Louloudi. Laboratory of Biomimetic Catalysis & Biomimetic Materials. Chemistry Department. University of Ioannina
 Prof. Dr. Maria Louloudi Laboratory of Biomimetic Catalysis & Biomimetic Materials Chemistry Department University of Ioannina ΑΝΟΡΓΑΝΗ ΙΙΙ Μηχανισµοί Ανόργανων Αντιδράσεων (στοιχειοµετρικές αντιδράσεις)
Prof. Dr. Maria Louloudi Laboratory of Biomimetic Catalysis & Biomimetic Materials Chemistry Department University of Ioannina ΑΝΟΡΓΑΝΗ ΙΙΙ Μηχανισµοί Ανόργανων Αντιδράσεων (στοιχειοµετρικές αντιδράσεις)
ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ (Α. Χημική Θερμοδυναμική) 1 η Άσκηση
 ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ 004-05 (Α. Χημική Θερμοδυναμική) η Άσκηση Στερεό CO, βάρους 6 g, εισάγεται μέσα σε κενό δοχείο όγκου 00 cm 3 που βρίσκεται συνεχώς σε θερμοκρασία δωματίου (300
ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ 004-05 (Α. Χημική Θερμοδυναμική) η Άσκηση Στερεό CO, βάρους 6 g, εισάγεται μέσα σε κενό δοχείο όγκου 00 cm 3 που βρίσκεται συνεχώς σε θερμοκρασία δωματίου (300
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ταξινομήστε τις παρακάτω ενώσεις κατά σειρά αυξανόμενου όξινου χαρακτήρα: (α) HBr, H Se, H S (β) HBr, HCl, HBr.. Ποιες από τις ακόλουθες προτάσεις είναι σωστές και
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ταξινομήστε τις παρακάτω ενώσεις κατά σειρά αυξανόμενου όξινου χαρακτήρα: (α) HBr, H Se, H S (β) HBr, HCl, HBr.. Ποιες από τις ακόλουθες προτάσεις είναι σωστές και
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
60
 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 Η (συνήθης) αύξηση του πυρηνόφιλου χαρακτήρα όσο κατερχόμαστε σε μία ομάδα του περιοδικού πίνακα οφείλεται στην αντίστοιχη μείωση της ηλεκτραρνητικότητας
59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 Η (συνήθης) αύξηση του πυρηνόφιλου χαρακτήρα όσο κατερχόμαστε σε μία ομάδα του περιοδικού πίνακα οφείλεται στην αντίστοιχη μείωση της ηλεκτραρνητικότητας
ΕΣΤΕΡΕΣ. Ένα αντιβιοτικό προφάρµακο. Υδρόλυση του εστέρα απελευθερώνει την ενεργή χλωραµφαινικόλη
 ΕΣΤΕΡΕΣ Ένα αντιβιοτικό προφάρµακο. Υδρόλυση του εστέρα απελευθερώνει την ενεργή χλωραµφαινικόλη Πολυµερή «σταδιακής ανάπτυξης» Σύγκρινε µε τα «αλυσιδωτής αντίδρασης» (Ενότητα 7.11) PET (Dacron, Mylar):
ΕΣΤΕΡΕΣ Ένα αντιβιοτικό προφάρµακο. Υδρόλυση του εστέρα απελευθερώνει την ενεργή χλωραµφαινικόλη Πολυµερή «σταδιακής ανάπτυξης» Σύγκρινε µε τα «αλυσιδωτής αντίδρασης» (Ενότητα 7.11) PET (Dacron, Mylar):
Οι δομές, οι οποίες δεν περιέχουν τυπικά φορτία υψηλά (δηλαδή είναι 2) είναι:
 Answers to Homework Set 3 12162016 1. Πριν από μερικά χρόνια δημοσιεύθηκε η σύνθεση του ιόντος 5 +. Ποια είναι η πλέον πιθανή α) γεωμετρία ηλεκτρονικών ζευγών, και β) μοριακή γεωμετρική δομή του ιόντος
Answers to Homework Set 3 12162016 1. Πριν από μερικά χρόνια δημοσιεύθηκε η σύνθεση του ιόντος 5 +. Ποια είναι η πλέον πιθανή α) γεωμετρία ηλεκτρονικών ζευγών, και β) μοριακή γεωμετρική δομή του ιόντος
Οργανική Χημεία. Κεφάλαιο 5: Επισκόπηση οργανικών αντιδράσεων
 Οργανική Χημεία Κεφάλαιο 5: Επισκόπηση οργανικών αντιδράσεων 1. Κατηγορίες οργανικών αντιδράσεων Γενικά, εξετάζουμε το είδος της αντίδρασης και τον τρόπο που αυτές συντελούνται Γενικοί τύποι αντιδράσεων
Οργανική Χημεία Κεφάλαιο 5: Επισκόπηση οργανικών αντιδράσεων 1. Κατηγορίες οργανικών αντιδράσεων Γενικά, εξετάζουμε το είδος της αντίδρασης και τον τρόπο που αυτές συντελούνται Γενικοί τύποι αντιδράσεων
επßπεδο ανüκλασηò κüθετο στη σελßδα η σελßδα Απεικονίσεις της αχειρικής ένωσης 1,1- διχλωροαιθάνιο.
 rflsym1 1 Κατοπτρική συµµετρία και χειρικότητα. Κατοπτρική συµµετρία έχει µια δοµή όταν µια δεύτερη δοµή που δηµιουργείται (κατοπτρική δοµή, είδωλο) µε αντιστοίχηση όλων των σηµείων της πρώτης σε ισαπέχουσες
rflsym1 1 Κατοπτρική συµµετρία και χειρικότητα. Κατοπτρική συµµετρία έχει µια δοµή όταν µια δεύτερη δοµή που δηµιουργείται (κατοπτρική δοµή, είδωλο) µε αντιστοίχηση όλων των σηµείων της πρώτης σε ισαπέχουσες
1. Να δείξετε πως τα παρακάτω μόρια μπορούν να παρασκευαστούν με αντίδρασεις Mannich
 1. Να δείξετε πως τα παρακάτω μόρια μπορούν να παρασκευαστούν με αντίδρασεις Mannich (!) (") (C 3 ) 2 (#) ($) 2. αντίδραση της τριτοταγούς αμίνης τροπινόνη με βρωμομεθυλο βενζόλιο (βενζυλο βρωμίδιο) δίνει
1. Να δείξετε πως τα παρακάτω μόρια μπορούν να παρασκευαστούν με αντίδρασεις Mannich (!) (") (C 3 ) 2 (#) ($) 2. αντίδραση της τριτοταγούς αμίνης τροπινόνη με βρωμομεθυλο βενζόλιο (βενζυλο βρωμίδιο) δίνει
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΙΟΝΤΙΚΟΣ Ή ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ
 ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
Κεφάλαιο 1 Χημικός δεσμός
 Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2006 2007 Ημερομηνία εξετάσεων: 17 Ιουνίου 2007
 ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2006 2007 Ημερομηνία εξετάσεων: 17 Ιουνίου 2007 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή το
ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2006 2007 Ημερομηνία εξετάσεων: 17 Ιουνίου 2007 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή το
5. Συμμετρία, Πολικότητα και Οπτική Ενεργότητα των μορίων
 5. Συμμετρία, Πολικότητα και Οπτική Ενεργότητα των μορίων ιδακτικοί στόχοι Μετά την ολοκλήρωση της μελέτης του κεφαλαίου αυτού θα μπορείτε να... o προβλέπετε με βάση τη συμμετρία αν ένα μόριο έχει μόνιμη
5. Συμμετρία, Πολικότητα και Οπτική Ενεργότητα των μορίων ιδακτικοί στόχοι Μετά την ολοκλήρωση της μελέτης του κεφαλαίου αυτού θα μπορείτε να... o προβλέπετε με βάση τη συμμετρία αν ένα μόριο έχει μόνιμη
διακλαδισμένο αλκάνιο γραμμικό αλκάνιο ΑΛΚΑΝΙΑ
 ΑΛΚΑΝΙΑ Ως αλκάνια ορίζουμε τις κορεσμένες οργανικές ενώσεις που αποτελούνται αποκλειστικά από άτομα άνθρακα και υδρογόνου και περιέχουν μόνο απλούς δεσμούς τύπου C C και C. Διακρίνονται δε σε άκυκλα αλκάνια
ΑΛΚΑΝΙΑ Ως αλκάνια ορίζουμε τις κορεσμένες οργανικές ενώσεις που αποτελούνται αποκλειστικά από άτομα άνθρακα και υδρογόνου και περιέχουν μόνο απλούς δεσμούς τύπου C C και C. Διακρίνονται δε σε άκυκλα αλκάνια
10 o Μάθημα. Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους
 Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους 2017-2018 10 o Μάθημα Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό Προσωπικό,
Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους 2017-2018 10 o Μάθημα Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό Προσωπικό,
ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας.
![ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας. ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας.](/thumbs/102/153828250.jpg) ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ 1 ο Εξάμηνο Χημικων Μηχανικών Εξεταστική Περίοδος Σεπτέμβριος 2019 Διδάσκοντες: Γ. Κακάλη, Κ. Κορδάτος 5/9/20199 ΘΕΜΑ 1 i) Να υπολογιστεί η ενέργεια ιοντισμού 1 mol υδρογόνου με βάση τη
ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ 1 ο Εξάμηνο Χημικων Μηχανικών Εξεταστική Περίοδος Σεπτέμβριος 2019 Διδάσκοντες: Γ. Κακάλη, Κ. Κορδάτος 5/9/20199 ΘΕΜΑ 1 i) Να υπολογιστεί η ενέργεια ιοντισμού 1 mol υδρογόνου με βάση τη
Μοριακή Γεωμετρία Πολικότητα των Μορίων. Εισαγωγική Χημεία
 Μοριακή Γεωμετρία Πολικότητα των Μορίων Εισαγωγική Χημεία 2013-14 1 Τα σχήματα των μορίων Οι δομές Lewis δίνουν πληροφορίες για την σύνδεση μεταξύ των ατόμων : Μας πληροφορούν για το ποια άτομα συνδέονται
Μοριακή Γεωμετρία Πολικότητα των Μορίων Εισαγωγική Χημεία 2013-14 1 Τα σχήματα των μορίων Οι δομές Lewis δίνουν πληροφορίες για την σύνδεση μεταξύ των ατόμων : Μας πληροφορούν για το ποια άτομα συνδέονται
Κεφάλαιο 9. Ιοντικός και Ομοιοπολικός Δεσμός
 Κεφάλαιο 9 Ιοντικός και Ομοιοπολικός Δεσμός Ηλεκτρόνια σθένους είναι τα ηλεκτρόνια της εξώτατης στοιβάδας ενός ατόμου. Είναι τα ηλεκτρόνια τα οποία συμμετέχουν στους χημικούς δεσμούς. Ομάδα Δομή e - #
Κεφάλαιο 9 Ιοντικός και Ομοιοπολικός Δεσμός Ηλεκτρόνια σθένους είναι τα ηλεκτρόνια της εξώτατης στοιβάδας ενός ατόμου. Είναι τα ηλεκτρόνια τα οποία συμμετέχουν στους χημικούς δεσμούς. Ομάδα Δομή e - #
ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Γενικό Τμήμα Εργαστήριο Χημείας, Καθηγητής Μόσχος Πολυσίου ΣΑΚΧΑΡΑ
 ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Γενικό Τμήμα Εργαστήριο Χημείας, Καθηγητής Μόσχος Πολυσίου ΣΑΚΧΑΡΑ ΣΑΚΧΑΡΑ Σάκχαρα ή υδατάνθρακες Τι είναι; Πολυυδροξυαλδεΰδες ή πολυυδροξυκετόνες ή ουσίες που όταν υδρολύονται
ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Γενικό Τμήμα Εργαστήριο Χημείας, Καθηγητής Μόσχος Πολυσίου ΣΑΚΧΑΡΑ ΣΑΚΧΑΡΑ Σάκχαρα ή υδατάνθρακες Τι είναι; Πολυυδροξυαλδεΰδες ή πολυυδροξυκετόνες ή ουσίες που όταν υδρολύονται
