ATMOSFÄÄRI- JA MEREFÜÜSIKA ALUSED. Loengukonspekt. I osa
|
|
|
- Δημοσθένης Παπάγος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ARU ÜLIKOOL KESKKONNAFÜÜSIKA INSIUU AMOSFÄÄRI- JA MEREFÜÜSIKA ALUSED Loengukonspekt I osa Koostanud H. Ohvril Aprill 2005 artu
2 Konspekt on koostatud toetamaks Füüsika õppekava magistriõppe loengukursust Atmosfääri- ja merefüüsika alused, FKKF , 2 AP. Et kergendada konspekti kasutamist loengukursuse demo-versiooni jälgimisel, on tähtsamad tekstiosad (valemid, konstandid, sümbolid jne) esitatud suuremas tähesuuruses ja bold-kirjas. H. Ohvril, 2005
3 SISUKORD SISSEJUHAUS... 3 I osa MERD JA AMOSFÄÄRI ISELOOMUSAVAE HÜDRODÜNAAMILISE JA ERMODÜNAAMILISE OMADUSE SARNASUS JA ERINEVUS MERI JA AMOSFÄÄR KUI ERMODÜNAAMILSED SÜSEEMID Mere ja atmosfääri termodünaamiline üldiseloomustus Niiske õhu olekuvõrrand integraalkujus Virtuaalse temperatuuri mõiste molekulaarkineetiline selgitus Õhuniiskuse karakteristikud Merevee olekuvõrrand integraalkujus VESI KUI ERANDLIK AINE JA ERANDLIK VEDELIK Vee omadused on erandlikud Keemilised sidemed Vee mikrostruktuur Iooonide hüdraadid merevees Vee erandlikke füüsikalisi omadusi Osmoos, adapteerumine soolsusega, Läänemere elustik ÕHU JA VEE ERISOOJUSED ermodünaamika põhivõrrand Isokoorne protsess Isobaarne protsess Isobaarse ja isokoorse erisoojuse vahe Õhu erisoojuste erinevus Vee erisoojuste erinevus ADIABAAILINE PROSESS emperatuuri adiabaatiline gradient Adiabaatilise temperatuurigadiendi arvulised väärtusd POENSIAALNE EMPERAUUR Potentsiaalse temperatuuri mõiste Õhu potentsiaalne temperatuur Merevee potentsiaalne temperatuur AMOSFÄÄRI JA MERE VERIKAALNE ASAKAAL Atmosfääri vertikaalne tasakaal Väisälä-Brunti sagedus Kirjandusviited
4 2
5 SISSEJUHAUS Käesolevas kursuses püüame vaadelda merd ja atmosfääri ühtse 2-komponendilise süsteemina. Selline geofüüsikaline käsitlusviis on õigustatud kahel põhjusel: 1) suur osa hüdro-termodünaamika võrrandeid on identsed nii atmosfääri kui mere jaoks, erinedes vaid konstantide väärtuste poolest, 2) atmosfäär ja meri on tihedas vastasmõjus. Näiteid atmosfääri mõjust merele 1. Suur osa meres toimuvatest liikumistest on tuule poolt genereeritud: 1) tuulelained, 2) turbulentne liikumine mere ülakihtides, 3) triivhoovused (kõik tähtsamad statsionaarsed pinnahoovused on vähemalt osaliselt triivhoovused). 2. Atmosfäär tagastab sademete näol osa (ca 90%) Maailmamerest aurunud veevarusid. äpsemalt aastas aurub merepinnalt ca 1 m paksune veekiht. Sellest tagastatakse 10 cm jõgede vooluga ja 90 cm sademetega mere kohal [Физика океана, 1978, 14]. oodud arvud on Maailmamere keskmised. Subtroopilistes piirkondades võib aastane aurumine ulatuda 2.5 meetrini, aastane sademete hulk aga Vaikse ookeani ekvatoriaalses osas kuni 5 meetrini. Kõrgematel laiustel (üle 65 ) langeb aastane aurumine alla 0.2 m/aastas [Хотон 1987, ]. 3. Atmosfäär on ookeanile mitmete gaaside (N 2, O 2, Ar, CO 2 jne) allikaks. 4. Atmosfäär annab ookeanile õhus aerosoolina hõljuvaid tahkeid ja vedelaid lisandeid (meenutame et aerosool tolmud, suitsud, udud). Neist üha suurem osa on antropogeense päritoluga. Näiteid mere mõjust atmosfäärile 1. Maailmameri on gigantne soojamahuti. Meri akumuleerib teda soojendavat kiirgusenergiat (Päikese lühilaineline kiirgus ja atmosfääri pikalaineline vastukiirgus) hoopis ratsionaalsemalt maismaast. Nimetatud nähtusel on 2 põhjust. Esiteks on merepinna albeedo (peegeldusvõime) ligi 2 korda väiksem maismaa omast, merepind on maismaast tumedam. Näiteks Päikese seniidis olles (h 90 ) on sileda 3
6 veepinna albeedo otsekiirguse jaoks ainult 2.1%, Päikese kõrgusel h 60 ainult 2.2%, kõrgusel h 50, ainult 2.5% jne., tabel 0.1 [Кондратьев, 1969, 187]. Kuigi horisondilähedase Päikese korral ulatuvad merepinna albeedo väärtused arvutuste järgi 100%-ni, on siis merepinnani jõudva Päikese kiirguse väärtused nii tühised, et ei jõuaks vett oluliselt soojendada ka väiksema albeedo puhul. Summaarse kiirguse albeedo hakkab Päikese loojudes alates 10 (ja allapoole) langema, sest siis kasvab hajusa kiirguse osatähtsus summaarses kiirguses. Maismaa albeedo langeb 5%-ni ainult tumedal taimestikuta pinnasel [Климатология, 1989, 206]. abel 0.1. Rahuliku merepinna albeedo Päikese otsekiirguse jaoks selge taeva korral (teoreetilised arvutused [Кондратьев, 1969, ] h A, % Mere ratsionaalse soojenemise teiseks põhjuseks on soojuse ühtlane ja kiire jaotumine ligi 100 m ülemises veekihis nii lühilainelise kiirguse tungimise tõttu paarikümnemeetrise sügavuseni (selges vees) kui vee vertikaalse tsirkulatsiooni tõttu. Viimasel põhjusel akumuleerub sügavamatesse kihtidesse ka atmosfääri pikalaineline vastukiirgus, mis neeldub juba mõnemillimeetrises veekihis. Süsteemi Maailmameri atmosfäär maismaa termiline tasakaal on aga selline, et Maailmamere pinnakihi keskmine temperatuur on 17.8 C [Каменкович и др, 1987, 16], õhu keskmine temperatuur maismaa kohal, taandatuna merepinna nivoole ainult 14.2 C [Климатология, 1989, 252], seega 3.6 C vähem. Kui keskmistada Maailmamere temperatuur sügavuseni 4000 m (ilma Põhja-Jäämereta), saaksime tulemuseks 3.8 C. Atmosfääri kogu massi keskmine temperatuur on vaid 17 C, seega tervelt 20.8 C vähem [Каменкович и др, 1987, 17]. Mere ja atmosfääri temperatuurikontrastid võimenduvad ka seetõttu, et vee erisoojus (4.19 kj/kg deg) on 4 korda suurem õhu omast (1.006 kj/kg deg) [Справочник 1974, 74, 77]. Seega on ookean planeedi tõeline soojamahuti, mis atmosfääri vahendusel kütab maismaad. Soojuse loovutamine atmosfäärile toimub: 80% ulatuses pikalainelise kiirgusena (soojuskiirgusena), 4
7 16% ulatuses varjatud e. aurustumissoojusena (ookean loovutab niiskust veeauruna, kui veeaur kondenseerub (tavaliselt pilvedes), saab atmosfäär soojuse lõpuks kätte), 4% ulatuses mittevarjatud soojusega ehk molekulaarse soojusjuhtivusega ehk kontaktse soojusjuhtivusega. Kõige suurem on ookeanist ülessuunatud soojusvoog talvel, kui vee kohal on kuiv külm õhk mandritelt, mis on suuteline soojust ja niiskust vastu võtma. 2. Maailmameri pehmendab ajalis-ruumilisi temperatuurikontraste. Atmosfääri vahendusel pehmenevad lokaalsed temperatuurierinevused maismaal: 1) rannikualadel öö ja päeva vahel, 2) merelise kliimaga aladel suve ja talve vahel. Atmosfääritsirkulatsiooni kui merehoovuste mõjul vähendatakse ka globaalseid temperatuurierinevusi: 3) ekvaatori ja polaarpiirkondade vahel. 3. Ookean on atmosfäärile niiskuse allikaks. Nagu öeldud, aurab Maailmamere pinnalt keskmiselt 1 meetri paksune veekiht [Физика океана, 1978, 14], mõnedel andmetel [Хотон, 1987, 312] koguni 1.2 meetrine. Lugedes Maailmamere keskmiseks sügavuseks 3800 m, saame ajavahemikuks, mille jooksul kihtide kaupa auraks ära kogu Maailmameri (iga aastaga 1.2 meetrit), üle 3000 a. Sellise ajavahemiku jooksul oleks nagu kogu Maailmameri atmosfäärist läbi käinud. Seepärast loetaksegi Maailmamere uuenemise ajaks umbes 3000 aastat. Võrdluseks pinnasevesi maismaal uueneb umbes aastaga, atmosfääris olev niiskus 10 päevaga. 4. Ookean pehmendab (demfereerib) O 2 ja CO 2 kontsentratsioonimuutusi atmosfääris. On üldtunnustatud CO 2 kontsentratsiooni jätkuv kiire kasv atmosfääris (võimalik kahekordistumine XXI sajandil). Ookeani gaasivahetus atmosfääriga on keeruline füüsikaliste, keemiliste ja bioloogiliste protsesside kogum, mille detailne olemus pole veel päris selge. Hinnanguliselt neelab ookean poole antropogeensest CO 2 -st [Хотон 1987, 350]. Osa sellest fotosünteesitakse veetaimede, põhiliselt fütoplanktoni, poolt glükoosiks ja hapnikuks 6 CO H 2 O + valgus C 6 H 12 2O O Meri on maismaa kohale kanduva merelise aerosooli (aerosool suitsud, tolmud, udud) allikaks. Laias laastus domineerivad kaks erinevat protsessi: 1) merevee pritsmed (tilgad) ongi juba valmis aerosooliosakesteks, mis sisaldavad meresooli; õhus toimub pritsmete osaline või täielik aurustumine, mille käigus meresoolade (NaCl, KCl jne) kontsentratsioon tilgas kasvab; 2) merevees on lahustunud väävlit sisaldavad gaasid (näiteks (CH 3 ) 2 S dimetüülsulfiid, H 2 S väävelvesinik, CS 2 süsiniksulfiid, COS karbonüülsulfiid), mis satuvad õhku kas lahustununa tilkades või otse gaasilisena; õhus hapnikuga (O 2 ) või veeauruga (H 2 O) reageerides annavad need väävlit sisaldavad gaasid tulemuseks vääveldioksiidi (SO 2 ), mis võib levida suuremate vahemaade taha ja millest seejärel tekib väävelhape (H 2 SO 4 ), mis siirdub põhiliselt aerosooliosakestesse (väga vähesel määral esineb H 2 SO 4 ka gaasina); kaks vääveldioksiidi (SO 2 ) tekkimise reaktsiooni on järgmised: 5
8 (CH 3 ) 2 S + O 2 SO 2 + CO 2 + H 2 0, dimetüülsulfiid H 2 S + O 2 SO 2 + H 2 O. Edasi tekib vääveldioksiidist väävelhape: SO 2 + O SO 3, SO 3 + H 2 O H 2 SO 4. Keemilisi termineid dimetüülsulfiid, keemilise valemina esitatakse kujul (CH 3 ) 2 S või (CH 3 )S(CH 3 ), orgaaniliste ainete laguprodukt; ka maismaa pinnaühiku kohta eraldub umbes samasugune kogus dimetüülsulfiidi, kuid tervikuna eraldub merest rohkem, kuna mere pindala on suurem; metüülrühm, metüülradikaal (kr methy vein) CH 3, esipunkt märgib paardumata elektroni, seega keemilist aktiivsust; näiteks OH CH 3 ehk CH 3 OH (ei kirjutata CH 4 O) metüülpiiritus ehk metüülalkohol, ehk metanool ehk puupiiritus (väga mürgine, põhjustab nägemise kaotust ja surma), näiteks H CH 3 ehk CH 4 metaan; radikaal (ld. radicalis tüveline) aatomite rühm, mis läheb ühest keemilisest ühendist muutumatult üle teise, sageli keemiliselt aktiivne; paardumata elektroniga molekul. 6
9 I osa MERD JA AMOSFÄÄRI ISELOOMUSAVAE HÜDRODÜNAAMILISE JA ERMODÜNAAMILISE OMADUSE SARNASUS JA ERINEVUS 1. MERI JA AMOSFÄÄR KUI ERMODÜNAAMILISED SÜSEEMID 1.1. Mere ja atmosfääri termodünaamiline üldiseloomustus Nii meres kui atmosfääris toimuvate protsesside ühiseks algseks energiaallikaks on Päike, mille kiirgusenergia muundub teisteks energialiikideks. Energia muundumise seaduspärasused ja energia seosed aine olekutega on termodünaamika uurimisobjektiks. ermodünaamika uurib lõplike mõõtmetega süsteeme, ainekoguseid, mis pole ei lõpmatult suured (st mittehõlmatavad) ega lõpmatult väikesed (st ei piirdu mõne molekuliga). Atmosfäär ja ookean nii ühtse tervikuna kui eraldi, aga ka väiksemate osade kaupa rahuldavad seda tingimust. Seepärast käsitletaksegi nii atmosfääri kui ookeani (merd, Maailmamerd) termodünaamiliste süsteemidena. Soojuse, liikumishulga ja aine ülekannet atmosfääri ja ookeani vahel, agregaatolekute muutumist, vaadeldakse kui protsesse, mis viivad termodünaamilise süsteemi ühest olekust teise. ermodünaamilise süsteemi olek see on seisund, mis on iseloomustatav selliste (makro)- karakteristikutega nagu: tihedus ρ, temperatuur, rõhk P, soolsus (niiskus) S jne. ermodünaamika seisukohalt on atmosfääril ja ookeanil rida ühiseid jooni: mõlemad on pidevad keskkonnad (kui mitte laskuda molekulaarse struktuurini), mõlemad on kokkusurutavad keskkonnad (tõsi, vee molekulid paiknevad üksteisele väga lähedal, mistõttu kokkusurumine õnnestub ainult väga suurtel rõhkudel, kuid vee tiheduste erinevus tingituna temperatuurierinevustest on ometi märgatav vees toimuvate vertikaalsete liikumiste kaudu), mõlemates, nii meres kui atmosfääris on vähesel hulgal lisandeid, viimaste hulk on aga nii väike, et nii merevett kui atmosfääriõhku võib käsitleda kui puhtaid aineid, nii merevee kui atmosfääriõhu jaoks on rakendatav nn olekuvõrrand, mis seob tiheduse ρ või eriruumala υ (eriruumala υ on massiühiku ruumala st tiheduse pöördväärtus 1/ρ): 7
10 temperatuuriga, rõhuga P, kontsentratsiooni S omavate lisanditega (soolsus või niiskus). Olekuvõrrand diferentsiaalkujus omab kuju [Доронин 1981, 18]: υ υ υ dυ d + dp + ds. (1.1.1) PS P S S P Et saada eriruumala muutust ruumiühiku kohta, jagame olekuvõrrandi kõiki liikmeid eriruumalaga υ. emperatuuri, rõhu ja lisandite kontsentratsiooni diferentsiaalide ette tekivad nüüd konstandid, millised tähistame järgnevalt: k 1 υ υ PS termilise (soojusliku) paisumise koefitsient, tavaliselt k > 0, sest temperatuuri kasvades harilikult aine massiühiku ruumala paisumise tõttu suureneb, vee puhul on erandiks jäätumistemperatuurist pisut kõrgem temperatuur (magedal veel 0 4 C), k P 1 υ υ P S υ kokkusurutavus, tuletis < 0, sest rõhu kasvades P S ruumala alati väheneb, k S υ 1 υ S P lisanditest tingitud ruumilise deformatsiooni koefitsient, merevee korral soolsusliku kokkusurumise koefitsient, υ < 0, sest sama massiga soolane vesi võtab alati P S vähem ruumi kui mage vesi (põhjuseks elektrostaatiline tõmbumine soola molekuli moodustavate ioonide (näit Na + ja Cl ) ja dipoolsete veemolekulide vahel; samas on kuiv õhk raskem kui samal temperatuuril ja rõhul olev niiske õhk, põhjus on veeauru kerges molekulkaalus lämmastiku ja hapnikuga võrreldes. Seega, ka soolsuse kasvu korral eriruumala väheneb (nagu ka rõhu kasvu korral). Nimetatud kolme koefitsienti kasutades saab nii merevett kui atmosfääriõhku kirjeldav olekuvõrrand diferentsiaalsena järgmise kuju: dυ υ k d kp dp ks ds. (1.1.2) Sellises lihtsas kujus on olekuvõrrand kasutatav siiski vaid termodünaamilistes teoreetilistes arvutustes. Ebamugavuseks on koefitsientide k, k P ja k S mittekonstantsus, nende sõltuvus muutujatest, P, S. Seepärast, kui on vaja arvutada õhu või merevee tihedust kindlatel temperatuuri, rõhu, niiskuse (soolsuse) väärtustel, kasutatakse olekuvõrrandeid integraalses kujus, lubades teatavaid lihtsustusi (ideaalse gaasi eeldus õhu korral) ja empiirikat (merevee korral). 8
11 1.2. Niiske õhu olekuvõrrand integraalkujus Õhk on vaadeldav järgmise 2-komponendilise ideaalsete gaaside seguna (ideaalse gaasi molekulid ei oma ruumala ega pole omavahelises interaktsioonis, põrked absoluutselt elastsed): 1. komponent kuiv õhk, kilomoolimass µ kõ kg, 2. komponent veeaur, kilomoolimass µ va kg. Ideaalse gaasi olekuvõrrandiks on Clapeyron-Mendelejevi võrrand m PV R, (1.2.1) µ kus: Benoit Clapeyron ( ) m gaasikoguse mass kilogrammides, Dmitri Mendelejev ( ) µ antud gaasi ühe kilomooli mass, seega murd µ m kujutab endast kilomoolide arvu gaasikoguses, universaalne gaasikonstant omab väärtust J 8313 kmol R. Jagame olekuvõrrandit (1.2.1) ruumalaga V : m PV R : V. (1.2.2) µ Arvestades, et m/v ρ, saame K ρ P R. (1.2.3) µ Rakendame viimast võrrandit nii kuiva õhu kui veeauru osarõhkudele, summeerides tulemused saame niiske õhu kogurõhu P: ρ P kõ kõ R µ kõ ρ + P va va R µ va P + P 142 kõ 43 va ρ kõ R µ kõ + ρ va R µ va P, niiske õhu kogurõhk, Daltoni seaduse järgi. (1.2.4) 9
12 Defineerime gaasikonstandid vastavalt kuiva õhu ja veeauru massiühikule 8313 J kmol J R kõ R 287 µ kmol K kg, K kg kõ 8313 J kmol J R va R 461 µ kmol K kg. K kg va Niiske õhu kogurõhu valem (1.2.4) saab nüüd kuju P ( ρkõ Rkõ+ ρva Rva ). (1.2.5) Võtame kuiva õhu gaasikonstandi R kõ sulgude ette R ρ P R R ρ + va va kõ kõ. (1.2.6) kõ ähistame gaasisegu (niiske õhu) kogu tiheduse ρ-ga: ρ ρkõ + ρ va, millest kuiva õhu tihedus ρkõ ρ ρva. Rvaρ P R va kõ va, R (1.2.7) ρ ρ + kõ võtame ρ sulgude ette 1 va R P R ρ va ρ va kõ ρ +, (1.2.8) ρ { R kõ { ρ q q q eriniiskus R 1 va P Rkõ ρ + q 1 R. (1.2.9) kõ virtuaalne Arvestades R va ja R kõ ülaltoodud väärtusi, saab virtuaalse temperatuuri avaldada ligikaudse valemiga: virtuaalne ( q). (1.2.10) 10
13 Valemi (1.2.9) järgi on niiske õhu olekuvõrrand integraalkujus P R kõ ρ virtuaalne, (1.2.11) millest järeldub, et samasuguse tihedusega ρ, aga temperatuuriga virtuaalne kuiv õhk avaldab samuti rõhku P nagu niiske õhk. Virtuaalse temperatuuri definitsioon: temperatuuri, rõhku P ja tihedust ρ omavale niiskele õhule vastav virtuaalne temperatuur virtuaalne on selline temperatuur, mille omandaks kuiv õhk rõhuga P ja tihedusega ρ. Seega on virtuaalne temperatuur niiskele õhule vastava tiheduse ja rõhuga kuiva õhu temperatuur (joon ). Nagu näeme valemist (1.2.10), on virtuaalne temperatuur alati kõrgem tavalisest ehk niiske õhu temperatuurist: virtuaalne >. Niiske õhk P ρ Kuiv õhk P ρ virtuaalne Joonis Rõhk liikuvale vaheseinale on mõlemalt poolt võrdne. Jagades valemi (1.2.11) mõlemat poolt tihedusega ρ, 1 P ρ R kõ virtuaalne, ja avaldades tiheduse pöördväärtuse eriruumala kaudu, υ 1 : ρ P υ R kõ virtuaalne, (1.2.12) saame valemi, mis on üsna sarnane Mendelejev-Clapeyroni võrrandile. Virtuaalse temperatuuri kasutamine võimaldab säilitada niiske õhu olekuvõrrandis kuiva õhu gaasikonstanti. Rõhutame veelkord, et virtuaalne temperatuur on alati kõrgem tavalisest temperatuurist, sõltudes õhu niiskusest (maksimaalne erinevus on siis, kui suhteline niiskus on maksimaalne, RH 100%). Virtuaalset temperatuuri võib korrutatava (multiplikatiivse) paranduskoefitsiendi ( q) asemel esitada ka liidetava (aditiivse) temperatuuriparandina virtuaalne : 11
14 virtuaalne ( q ) + virtuaalne, (1.2.13) virtuaalne q. (1.2.14) abel Maksimaalsed virtuaalsed temperatuuriparandid, RH 100% (Тверской 1962, с. 33). Õhu temperatuur, C p, mb abelist näeme, et maapinnal suviste temperatuuride juures ulatuks virtuaalne temperatuuriparand RH 100% korral maksimaalselt mõne kraadini, madalatel talvistel temperatuuridel piirdub mõne kraadikümnendikuga. egelikkuses pole aga suviste päevaste temperatuuride korral suhteline niiskus harilikult 100%, seega on virtuaalsed temperatuuriparandid väiksemad kui tabelis toodud. Ligikaudsete arvutuste juures lugeda virtuaalse temperatuuri võrdseks tavalisega, mis sisuliselt tähendab õhurõhu arvutustes veeaururõhu mittearvestamist Virtuaalse temperatuuri mõiste molekulaarkineetiline selgitus Miks ikkagi virtuaalne temperatuur on kõrgem tavalisest ehk niiske õhu temperatuurist? Vastame tuginedes ideaalse gaasi molekulaarkineetilisele teooriale. Selle teooria põhivõrrand: 1 2 P m n v, (1.3.1) 3 vasemal pool on makroparameeter rõhk P, paremal pool mikroparameetrid: m molekuli mass, n molekulide kontsentratsioon (arv ruumiühikus), 2 v molekulide kiiruse ruudu keskväärtus. Et molekuli massi m ja molekulide kontsentratsiooni n korrutis annab tiheduse ρ: ρ m n, siis molekulaarkineetilise teooria põhivõrrand teiseneb: 1 P ρ v 2. (1.3.2) 3 Rakendame võrrandit (1.3.2) mingile gaasile, näiteks veeaurule, mille tihedus on ρ ja mille molekule tähistame indeksiga "1": 12
15 1 P ρ v 2 1. (1.3.3) 3 Vahetame nüüd anumas oleva gaasi mingi teise gaasiga (indeks "2"), mille molekulide mass on teistsugune, konkreetsuse mõttes eeldame, et uued molekulid on raskemad m 2 > m 1. Kuid teise gaasi molekulide arvu vähendame, et tihedus oleks sama nagu esimesel gaasil, ρ. Seame tingimuse, et rõhk anumas säilib. Seega molekulaarkineetilise teooria põhivõrrand teise gaasi jaoks saab kuju 1 P ρ v 2 2. (1.3.4) 3 Ühendades valemid (1.3.3) ja (1.3.4): P ρ v1 ρ v2, 3 3 millest järeldub, et võrdse tiheduse korral peab võrdse rõhu saavutamiseks teise gaasi molekulide kiiruse ruudu keskväärtus olema võrdne esimese gaasi molekulide omaga v 2 v1 v. Hindame nüüd mõlema gaasi temperatuuri. emperatuur on molekulaarkineetilise teooria järgi seotud molekulide keskmise kineetilise energiaga järgmiselt: 2 m esimene gaas 1 v 3 E 1 k 1 (k Boltmanni konstant), (1.3.5) m teine gaas 2 v 3 E 2 k 2. (1.3.6) 2 2 Kuna teise gaasi molekulid olid raskemad (m 2 > m 1 ), kiirused aga samad, siis ka teise gaasi molekulide keskmine kineetiline energia on suurem E 2 > E 1, järelikult ka teise gaasi temperatuur on kõrgem 2 > 1. Jagame võrrandi (1.3.6) võrrandiga (1.3.5): E 2 2 2, E1 m1 1 millest teise gaasi temperatuur esimese oma kaudu m 13
16 m (1.3.7) m1 Seega, kui niiskes õhus olevad veeauru molekulid asendada kuiva õhu koostisse kuuluvate raskemate molekulidega (hapnik, lämmastik), siis sama tiheduse korral tuleb rõhu säilitamiseks tõsta temperatuuri. Ülesanne 1.1 Kasutades ideaalse gaasi olekuvõrrandit ehk Clapeyron-Mendelejevi võrrandit, m PV R, µ kus: m gaasikoguse mass kg, µ antud gaasi ühe kilomooli mass, kg/kmol, 3 J R , kmol K näidata, et igasuguse gaasi gramm-molekul (mool) täidab normaaltingimustel ruumala 22.4 liitrit. Ülesanne 1.2 Arvutada kuiva õhu tihedus normaaltingimustel. Kuiva õhu kilomoolimass on kg/kmol. 14
17 1.4. Õhuniiskuse karakteristikud Küllastava veeauru rõhk E, e küllast, mbar. Mida kõrgem on õhutemperatuur, seda rohkem võib õhk sisaldada veeauru. Kuid igal temperatuuril on õhus olevatele veemolekulidele teatav kontsentratsiooniline piir, mida iseloomustatakse nn küllastava veeauru rõhuga. Kui see piir on saavutatud, siis täiendavate veemolekulide õhku lisamisel kondenseerub osa veemolekule välja. Saksa teadlane Heinrich Gustav Magnus ( ) koostas eksponentsiaalse valemi küllastava veeauru rõhu arvutamiseks. Selle valemi konstante on aastate jooksul pisut muudetud, kuid üldkuju on jäänud samaks. eatmiku Atmosfera (1991, lk 76) järgi sõltub küllastava veeauru rõhk E, mbar, temperatuurist t ( C) järgmiselt E 7.665t t , Magnuse (tüüpi) valem. (1.4.1) abel Küllastava veeauru rõhk temperatuuri funktsioonina. t, C E, mbar E, mbar Joon Magnuse valemi (1.4.1) järgi arvutatud küllastava veeauru rõhk E. sõltuvana temperatuurist t, C. 15
18 Õhus oleva veeauru rõhk e, mbar. Harilikult on õhus vähem niiskust kui oleks vaja küllastamiseks. Õhus kui gaaside segus parajasti oleva veeauru rõhk (täpsemalt osarõhk ehk partsiaalne rõhk) on üks meteojaamades mõõdetavatest õhuniiskuse parameetritest. Eestis on veeauru rõhu kuukeskmised väärtused: e 3 4 mbar talvekuudel, e mbar suvekuudel. Psühromeeter. Kahest ühesugusugusest termomeetrist koosnev seade, milles ühe termomeetri reservuaari niisutatakse (märja marliga). Auramise tõttu langeb märja termomeetri näit. Kuiva ja märja termomeetri näitude vahet nimetatakse psühromeetriliseks diferentsiks. Veeauru rõhk e arvutatakse psühromeetrilisest diferentsist psühromeetrilise valemi abil (esitus hiljem). Vt psühromeetri joonist, M. Jürissaar Meteoroloogia, lk 22. Veeauru rõhk e on tähtsaim õhuniiskuse karakteristik, selle teadmine võimaldab arvutada mitmeid teisi õhuniiskuse karakteristikuid. Suhteline e. relatiivne niiskus r, RH, %. Õhus tegelikult oleva veeauru rõhu suhe samal temperatuuril õhku küllastava veeauru rõhusse, harilikult väljendatakse protsentides: e RH 100% (RH Relative Humidity). (1.4.2) E Mitmed looduses toimuvad füüsikalised protsessid (näit materjalide pikenemine ja lühenemine jne) sõltuvad suhtelisest niiskusest, see võimaldab suhtelist niiskust mõõta otseselt, ilma veeauru osarõhu ja küllastava auru rõhuta. Meteoroloogilises praktikas mõõdetakse suhtelist niiskust juushügromeetriga, tundlikuks elemendiks on kimp inimese juukseid, mis on tehtud rasvavabaks. Vt juushügromeetri joonist, M. Jürissaar Meteoroloogia, lk 23. Absoluutne niiskus a, ρ, g/m 3. Veeauru kogus grammides 1 m 3 niiske õhu kohta ehk veeauru tihedus ühikutes g/m 3. Kui veeauru osarõhk on määratud, saab veeauru olekuvõrrandist leida ka veeauru tiheduse ehk eriruumala pöördväärtuse: e υ veeaur Rveeaur : υ veeaur (1.4.3) e 1 R veeaur, υveeaur e ρ veeaur Rveeaur, ρ e veeaur R. (1.4.4) veeaur 16
19 Paigutades siia valemisse veeauru gaasikonstandi J R veeaur 461.5, kg K saame veeauru tiheduse SI-süsteemi ühikutes kg/m 3 : e ρ veeaur Kasutades veeauru tiheduse ühikutena g/m 3, on veeauru tihedus numbriliselt 1000 korda suurem, seega tuleb vastavalt suurendada võrrandi paremat poolt: 1000e ρ veeaur. Edasi arvestame, et veeauru rõhku mõõdetakse millibaarides, mis on 100 korda tugevam ühik kui paskal: 1 mbar 100 Pa 1 hpa, tulemust tuleb veel 100x suurendada: e e e g ρ veeaur m kus e mõõtühikuks on mbar. Harilikult tähistatakse veeauru tihedust ehk absoluutset niiskust tähega a: e a 217. (1.4.5) Viimases valemis on temperatuur absoluutses skaalas. Seos Celsiuse skaalaga: kus t (1 + t) (1+ αt), (1.4.6) α Absoluutse niiskuse arvutusvalem teiseneb: a e e 0.793e 0.8e α t 1+ α t 1+ α t Seega absoluutse niiskuse kaks arvutusvalemit, kus e millibaarides ehk hektopaskalites:, e 0.8e 1+ α t g m a (1.4.7) 17
20 NB! Nii meteoroloogilisi tabeleid kui teatmike valemeid kasutades tuleb alati veenduda, kas veeauru rõhu ühikuna on kasutusel olnud mbar või mmhg. äiendavalt aetakse meteroloogilises praktikas segamini ka veeauru rõhk ja absoluutne niiskus. Eriniiskus s, q. Veeauru suhteline mass, algebralisel kujul sobiv kui ühikuta ja konstandiga läbi korrutamata suurus. Praktikas suurendatakse aga eriniiskust 1000 korda, st esitatakse suhteline mass tuhandikes. Selliselt saadakse veeauru mass grammides 1 kg niiske õhu kohta, ühik vastavalt g/kg ehk ehk ppt (parts per thousand, analoogselt merevee soolsusega). ähistame: ρ kuiv niiskes õhus oleva kuiva õhu (osa)tihedus, ρ veeaur niiskes õhus oleva veeauru (osa)tihedus. Eriniiskus nende tiheduste kaudu (lihtsalt suhtelise suurusena): ρ s veeaur. (1.4.8) ρveeaur + ρkuiv Eriniiskuse valemi teisendmiseks esitame niiskes õhus oleva kuiva õhu ja veeauru osarõhud vastavate olekuvõrrandite kaudu: p p e R, kuiv ρ kuiv kuiv kuiva õhu gaasikonstant veeauru oma kaudu (vt valemite ja vahel olevaid R väärtusi): seega R kuiv R veeaur, p e ρ 0. R, kuiv 622 veeaur millest kuiva õhu tihedus (täpsemalt õhu koostises oleva kuiva õhu tihedus): p e ρ kuiv. (1.4.9) Rveeaur Analoogselt veeauru osarõhk ja tihedus olekuvõrrandi abil e ρ veeaur Rveeaur, ρ e veeaur Rveeaur. (1.4.10) Paigutame koostisgaaside tiheduste valemid eriniiskuse valemisse (1.4.8): e ρ R s veeaur veeaur, ρveeaur + ρkuiv e p e + R R veeaur 18 veeaur saadud keerukas murd lihtsustub, kui korrutame lugejat ja nimetajat suurusega R veeaur :
21 e e e s p e e e + p e p 0.378e, seega saime tulemuseks 0.622e s. (1.4.11) p 0.378e Praktikas kasutatakse seda valemit lihtsustatud kujul. Nimelt p >> e, (p 1000 mbar, e mbar 5.7 mbar, erinevus 175 korda, seega eriniiskuse valem ümardatult 0.622e s. (1.4.12) p Kastepunkt t d, τ, dew point, punto rocío, точка росы. emperatuur, mille juures õhus olemasolev niiskus muutub küllastavaks. eisiti öeldes, kui jahutada õhku, siis teatud temperatuuri juures hakkab niiskus sadestuma õhus olevatele esemetele. Vastav temperatuur ongi kastepunkt ehk kastepunkti temperatuur. Õhuniiskuse kondenseerumine on sagedane nähtus õhtuti soojal aastaajal. Antud veeaururõhule ja temperatuurile vastava kastepunkti kiireks ligikaudseks leidmiseks paigutatakse veeauru osarõhk e(t) Magnuse valemisse, valemist leitakse tagurpidi kastepunkt t d : e( t) e ( td ) td td avaldades siit t d, saamegi kastepunkti valemi t d [ log e( t) ] log[ e( t) ], (Magnuse valem) (1.4.13) Kastepunkti defitsiit. Vahe tegeliku õhutemperatuuri ja kastepunkti vahel. Kasutatakse harva. Küllastusvajak d. Antud temperatuuril õhku küllastava veeauru rõhu ja õhus tegelikult oleva veeauru osarõhu vahel d E e, kasutatakse harva. (1.4.14) Niiskusvajak ehk niiskuse defitsiit g/cm 3. Vahe küllastava absoluutse niiskuse ja tegeliku absoluutse niiskuse vahel. Kasutatakse harva. Psühromeetriline valem. See on valem veeauru rõhu arvutamiseks kuiva ja märja termomeetri näitude järgi e E märg K (t kuiv t märg ) p, 19
22 Psühromeetriline koefitsient K sõltub psühromeetri konstruktsioonist, eriti märja termomeetri ventilatsioonitingimustest. Levinuima, nn Assmanni psühromeetri korral K , seega psühromeetriline valem Assmanni psühromeetri jaoks e E märg (t kuiv t märg ) p. (1.4.15) Arvutusnäide (vt tabel M. Jürissaare õpikust, lk 22), algandmed: t kuiv 25.5 C, t märg 20.1 C. Arvutame Magnuse valemi järgi märja termomeetri näidule 20.1 C vastava küllastava veeauru rõhu E märg (NB! loeme õhurõhuks p mbar): E t t märg märg märg (mbar), otsitav veeauru osarõhk e psühromeetrilise valemi järgi e ( ) (mbar). Arvutame kastepunkti, sisestame kastepunkti valemisse (1.4.13) veeauru rõhu mbar, saame t d C (ei lange kokku M.J. õpiku väärtusega 16.8 C). Arvutame absoluutse niiskuse valemi (1.4.7) järgi a 217 e g ( m arvutatud absoluutne niiskus ei lange kokku M.J. õpiku väärtusega 19.1 g/m 3. Arvutame Magnuse valemi abil kuiva termomeetri näidule 25.5 C vastava maksimaalse võimaliku veeauru rõhu E: E kuiv mbar. Arvutame suhtelise niiskuse RH 100% % 61% (ei lange kokku M.J. õpiku 59% -ga) ), 20
23 Ülesanne 1.3 Kontrollida iseseisvalt M. Jürissaare õpiku (1998, lk 22) tabelit. abel Õhuniiskuse parameetrid, kui t kuiv 25.5 C, t märg 20.1 C (M. Jürissaar (1998), lk 22). M. Jürissaar, lk 22 Kontrolltulemus Kuiva termomeetri lugem 25.5 C Märja termomeetri lugem 20.1 C Absoluutne niiskus 19.1 g/m 3 Relatiivne niiskus 59% Niiskuse defitsiit 13.5 g/m 3 Kastepunkt 16.8 C Kastepunkti defitsiit Soovitused ülesande lahendamiseks: ( C) 1) kasutades M. Jürissaare õpiku lõpus (lk 170) või konspekti järgmisel lehel olevat suhtelise niiskuse nomogrammi, kontrollida antud ülesande suhtelise niiskuse RH arvutust, 2) arvutada Magnuse valemi järgi (või leida ülejärgmise lehekülje psühromeetrilisest tabelist) maksimaalselt võimalik veeauru rõhk E, kui t 25.5 C, 3) arvutada suhtelise niiskuse RH ja küllastava veeauru rõhu E järgi veeauru osarõhk e, 4) arvutada absoluutne niiskus a, 5) leida lisatud (ülejärgmisel leheküljel) psühromeetrilise tabeli järgi kastepunkt t d. Ülesanne 1.4. eisendada absoluutse niiskuse arvutamise valem on antud vanades rõhuühikutes, mmhg. e a 217 kujule, kus veeauru rõhk e 21
24 Joon Nomogramm suhtelise niiskuse määramiseks kuiva ja märja termomeetri lugemite järgi (M. Jürissaare õpik, lk 170). Näiteks järgmistest algandmetest: kuiva termomeetri lugem 30 C, märja termomeetri lugem 20 C, järeldub, et RH 40%. 22
25 abel Küllastava veeauru rõhk. äiskraadid Kraadi kümnendikosad Maksimaalne veeauru rõhk vee kohal, mbar 0 6,1 6,2 6,2 6,2 6,3 6,3 6,4 6,4 6,5 6,5 1 6,6 6,6 6,7 6,7 6,8 6,8 6,9 6,9 7,0 7,0 2 7,0 7,1 7,2 7,2 7,3 7,3 7,4 7,4 7,5 7,5 3 7,6 7,6 7,7 7,7 7,8 7,8 7,9 8,0 8,0 8,1 4 8,1 8,2 8,2 8,3 8,4 8,4 8,5 8,5 8,6 8,7 5 8,7 8,8 8,8 8,9 9,0 9,0 9,1 9,2 9,2 9,3 6 9,4 9,4 9,5 9,5 9,6 9,7 9,7 9,8 9,9 10,0 7 10,0 10,1 10,2 10,2 10,3 10,4 10,4 10,5 10,6 10,6 8 10,7 10,8 10,9 11,0 11,0 11,1 11,2 11,2 11,3 11,4 9 11,5 11,6 11,6 11,7 11,8 11,9 12,0 12,0 12,1 12, ,3 12,4 12,4 12,5 12,6 12,7 12,8 12,9 13,0 13, ,1 13,2 13,3 13,4 13,5 13,6 13,7 13,8 13,8 13, ,0 14,1 14,2 14,3 14,4 14,5 14,6 14,7 14,8 14, ,0 15,1 15,2 15,3 15,4 15,5 15,6 15,7 15,8 15, ,0 16,1 16,2 16,3 16,4 16,5 16,6 16,7 16,8 17, ,1 17,2 17,3 17,4 17,5 17,6 17,7 17,8 18,0 18, ,2 18,3 18,4 18,5 18,7 18,8 18,9 19,0 19,1 19, ,4 19,5 19,6 19,8 19,9 20,0 20,1 20,3 20,4 20, ,6 20,8 20,9 21,0 21,2 21,3 21,4 21,6 21,7 21, ,0 22,1 22,3 22,4 22,5 22,7 22,8 23,0 23,1 23, ,4 23,5 23,7 23,8 24,0 24,1 24,3 24,4 24,6 24, ,9 25,0 25,2 25,4 25,5 25,7 25,8 26,0 26,1 26, ,5 26,6 26,8 26,9 27,1 27,3 27,4 27,6 27,8 27, ,1 28,3 28,5 28,6 28,8 29,0 29,2 29,3 29,5 29, ,9 30,0 30,2 30,4 30,6 30,8 31,0 31,1 31,3 31, ,7 31,9 32,1 32,3 32,5 32,7 32,9 33,0 33,2 33, ,6 33,8 34,0 34,2 34,4 34,6 34,9 35,1 35,3 35, ,7 35,9 ˇ36,1 36,3 36,5 365,8 37,0 37,2 37,4 37, ,8 38,1 38,3 38,5 38,7 39,0 39,2 39,4 39,6 39, ,1 40,3 40,6 40,8 41,0 41,3 41,5 41,8 42,0 42, ,5 42,7 43,0 43,2 43,5 43,7 44,0 44,2 44,5 44, ,0 45,2 45,5 45,8 46,0 46,3 46,5 46,8 47,1 47, ,6 47,9 48,1 48,4 48,7 49,0 49,2 49,5 49,8 50, ,4 50,6 50,9 51,2 51,5 51,8 52,1 52,4 52,7 53, ,3 53,6 53,8 54,2 54,5 54,8 55,1 55,4 55,7 56, ,3 56,6 56,9 57,2 57,6 57,9 58,2 58,5 58,8 59, ,5 59,8 60,1 60,5 60,8 61,1 61,5 61,8 62,2 62, ,8 63,2 63,5 63,9 64,2 64,6 64,9 65,3 65,6 66, ,3 66,7 67,0 67,4 67,8 68,2 68,5 68,9 69,3 69, ,0 70,4 70,8 71,1 71,5 71,9 72,3 72,7 73,1 73, ,8 74,2 74,6 75,0 75,4 75,8 76,2 76,6 77,1 77, ,9 78,3 78,7 79,1 79,5 80,0 80,4 80,8 81,2 81, ,1 82,5 83,0 83,4 83,8 84,3 84,7 85,2 85,6 86, ,5 87,0 87,4 87,9 88,3 88,8 89,2 89,7 90,2 90, ,1 91,6 92,1 92,6 93,0 93,5 94,0 94,5 95,0 95, ,0 96,4 96,9 97,4 97,9 98,4 98,9 99,4 100,0 100, ,0 101,5 102,0 102,6 103,1 103,6 104,4 104,6 105,2 105, ,3 106,8 107,3 107,9 108,4 109,0 109,5 110,1 110,6 111,2 23
26 1.5. Merevee olekuvõrrand integraalkujus Vedelikus on molekulid üksteisele nii lähedal, et nendevahelisi tõmbejõude arvestamata jätta ei saa. Ideaalsele gaasile analoogset ideaalse vedeliku termodünaamilist mudelit pole õnnestunud luua (ideaalse vedeliku all mõeldakse hüdrodünaamikas vedelikku, mis: 1) on kokkusurumatu, 2) ei oma sisehõõret (on mitteviskoosne). Merevee olekuvõrrandid, mis kirjeldavad tiheduse sõltuvust temperatuurist, rõhust ja soolsusest, ρ ρ (, P, S), on empiirilised. Esitame näitena suhteliselt lihtsa P. Lineikini valemi [Доронин, 1981, 20; Доронин, 1978, 27]: kus ρ(, P, S) ρ 0 g ρ 0 1, 3 cm 5 ε C -1, ε C -2, ε C -1 ( ) -1, ε 4 82 ( ) -1, ε Pa -1. ( ε ε ε S + ε S + ε UNESCO soovitab alates aastast kasutada keerukamat, 2-etapilist merevee tiheduse arvutamist: 1) arvutatakse merevee tihedus standardsel atmosfäärirõhul mb, mis vastab merevee tihedusele merepinnal antud temperatuuri ja soolsuse korral, 2) arvutatakse tihedus sügavamates veekihtides P), Vastavad valemid võib asjasthuvitatu leida O.I. Mamajevi raamatust [1987]. 24
27 2. VESI KUI ERANDLIK AINE JA ERANDLIK VEDELIK Looduses olev vesi, sh merevesi, kujutab endast lahust, kus lahustiks on puhas vesi, mis põhiliselt määrab vaadeldava looduslikku vee tähtsamad füüsikalised omadused tiheduse, sulamis- ja keemistemperatuuri, kokkusurutavuse, sisehõõrdeteguri jne. Lahustunud ained (soolad, orgaanilised ühendid) suurendavad oluliselt vee elektrijuhtivust, muudavad vee pindpinevust ja värvust. Kuid lisandid ei pruugi mõjustada kõiki vee omadusi, näiteks soola- ja suhkrulahused jätavad vee värvituks ja läbipaistvaks. eisalt kujutab looduslik vesi endast suspensiooni vees on hõljuvas olekus mikromõõtmetes mineraalseid ja orgaanilisi aineid ning elusorganisme (planktonit). Lahustumata hõljum vähendab vee läbipaistvust ning suurendab valguse hajumist ja neeldumist Vee omadused on erandlikud Planeedi levinumaid ja tähtsamaid aineid, vesi (H 2 O), on erandlike omadustega. Kõigepealt on üllatav, et tavatingimustel on vesi vedelas olekus, mitte aga gaasilises. Kirjutame näiteks välja vesiniku ja perioodilisuse süsteemi VI rühma elementide ühendite sulamis- ja keemistemperatuurid. abel. Vesinikuühendite külmumis- ja keemistemperatuurid. VI rühma element nr. 8, O 2 (hapnik) Ühend vesinikuga H 2 O (hapnikvesinik ehk vesi) 25 Külmumis temperatuur, C Keemistemperatuur, C nr. 16, S (väävel) H 2 S (väävelvesinik) nr. 34, Se (seleen) H 2 Se (seleenvesinik) nr. 52, e (telluur) H 2 e (telluurvesinik) 53 5 Analoogia põhjal peaks vee külmumistemperatuur olema madalam kui 83 C ja keemistemperatuur madalam kui 63 C. Seega, kui tabeli alumise kolme rea loogika kehtiks, peaks vesi meie planeedil esinema põhiliselt gaasilisena, veeauru kujul, välja arvatud polaaralad talvel, kui harukordadel (temperatuur alla 63 C) esineks vett vedelas olekus. Anomaalselt suured on vee erisoojus, võime lahustada teisi aineid jne Keemilised sidemed Suvalise aine üksik aatom on reageerimisvõimeline teiste aatomitega (erandiks on väärisgaaside aatomid), et moodustada liitosakesi molekule, ioone, kristalle. Moodustuv liitosake on küll koostiselt keerukam, kuid tema moodustumisel vabaneb energiat. Seega on liitosake energeetiliselt püsivam kui üksikud aatomid. Aatomite liitumine ja liitosakese püsimine toimub keemiliste sidemete abil. Viimaseid on terve rida iooniline, mittepolaarne kovalentne, polaarne kovalentne jne. Valentselektronid. Keemiline side moodustub aatomite vahele sel teel, et omavahel reageerivad aatomid loovutavad või liidavad (võtavad endale juurde) elektrone. Neid elektrone, mis osalevad keemilise sideme moodustamisel, nimetatakse valentselektronideks.
28 Oktetiprintsiip. Keemilise sideme moodustamisel püüavad aatomid elektronide loovutamise või endaga liitmise teel saavutada olukorda, kus aatomi väliselektronkihil on kaheksa (või kaks) elektroni. Elektronegatiivsus. USA teadlase L. Paulingi (Linus Carl Pauling, , Nobeli keemiapreemia 1954, Nobeli rahupreemia 1962), ettepanekul hakati a. elementide reageerimisvõime iseloomustamiseks kasutama elektronegatiivsuse mõistet. Elektronegatiivsuse all mõistetakse elemendi võimet siduda endaga elektrone. Kui kaks aatomit reageerivad, siis suurema elektronegatiivsusega aatom haarab elektrone juurde, väiksema elektronegatiivsusega aatom aga loovutab elektrone. Elektronegatiivsuse ühikuks on liitiumi elektronegatiivsus, X Li 1. Liitium on 1. rühma element, järjekorra üldnumber 3 (perioodilisuse tabeli esimesed kolm elementi on H, He, Li). Element Elektronegatiivsus, X K 0.8 Na 0.9 Li 1.0 H 2.1 Cl 3.0 O 3.5 F 4.0 Mida suurem on elemendi elektronegatiivsus, seda mittemetallilisem ta on. Mida väiksem on elemendi elektronegatiivsus, seda metallilisem ta on. Piiriks metallide ja mittemetallide elektronegatiivsuste vahel on väärtus X 1.8. Iooniline side. Aatomid, mille väliskihis on 1 kuni 3 elektroni, loovutavad neid kergesti ja muutuvad positiivselt laetud ioonideks, mille väliskihis on 8 elektroni, näit.: Na e Na + (tekkinud naatriumiooni elektronstruktuur on analoogne väärisgaas neoonile). Aatomid, mille väliskihis on 6 kuni 7 elektroni, haaravad neid kergesti ja muutuvad negatiivselt laetud ioonideks, mille väliskihis on 8 elektroni, näiteks: Cl + e Cl (analoogne väärisgaas argoonile). ekkinud erinimeliselt laetud ioonid (näit. Na + ja Cl ) tõmbuvad elektrostaatiliselt, tekib iooniline side. Kõrgel temperatuuril, gaasi või auru faasis, moodustub NaCl iseseisev molekul. Madalamal temperatuuril moodustub ioonvõrega kristall. Viimase puhul ei saa rääkida NaCl molekulist, sest iga Na + ioon on võres ümbritsetud kuue Cl -ga ja vastupidi. Polaarne kovalentne side. Kumbki aatom loovutab ühe elektroni ühisesse elektronpaari. Ühine elektronpaar nihkub suurema elektronegatiivsusega (mittemetalsema) elemendi aatomi poole. Näiteks vesinikkloriidis (soolhape) on ühine elektronpaar tõmmatud rohkem kloori aatomi tuuma poole, sest kloori elektronegatiivsus on suurem (kloori molekul on ka raskem): H :Cl. 26
29 Elektronpaari negatiivse laengu tulemusena omandab elektronegatiivsem element väikese negatiivse osalaengu ( δ). Elektropositiivsem element omandab väikese positiivse osalaengu (+δ). ekkinud keemilist molekuli skitseeritakse järgmiselt + δ δ H Cl. Elektriliselt kujutab selline molekul endast dipooli. Polaarne kovalentne side esineb üksteisest mitte järsult erinevate omadustega aatomite vahel, näit HCl, H 2 S, H 2 O, CH Vee mikrostruktuur Hapniku aatom ja vesiniku aatom on ühendatud polaarse kovalentse sidememega O H on elektronpaar tõmmatud suurema elektronegatiivsusega elemendi, hapniku aatomi, poole. Ka vee molekulis H O H on mõlemad elektronpaarid nihkunud raskema hapniku aatomi poole, mistõttu 3 aatomit ei paikne ühes reas, nagu üleskirjutuses H O H, vaid moodustavad kolmnurga (joon. 2.1), mis on ka dipool. 2δ O 105 H H + δ + δ Joon Vee molekul kujutab endast dipooli. Dipoolse struktuuri tõttu tekitab vee molekul elektrivälja, millega mõjustatakse vee naabermolekule ja vees olevate lisandite aatomeid ja molekule, ning ollakse ise mõjustatav. Piltlikult öeldes on vee molekul suhtlemisaldis. Üsna populaarne on hüpotees, et elektrostaatilise tõmbe tõttu moodustavad vee molekulid ca 10 molekulist koosnevaid kogumeid, nn klastreid. Kui liituvad kaks vee molekuli, nimetatakse tekkinud ühendit dimeeriks, (H 2 O) 2. H H O O H H Joon Kaks vee molekuli moodustavad liitudes dimeeri. 27
30 Edasi järgnevad trimeer (H 2 O) 3, tetrameer (H 2 O) 4, pentameer (H 2 O) 5 jne. Mida madalam on temperatuur, seda rohkem molekule on koondunud klastritesse, milles igaühes võib olla mitukümmend veemolekuli. Esmapilgul tundub, et temperatuuri alanedes soodustavad klastrid kristallvõre tekkimist ning jäätumist. Samas võib vett ettevaatlikult ja aeglaselt jahutades säilitada vedela oleku isegi temperatuurini kuni 40 C. Seda fakti on kasutatud klastrite teooria kritiseerimiseks. Joon Veemolekulide koondumine klastriteks. Joon Jää, vee ja veeauru mikrostruktuur, iga punkt kujutab üht veemolekuli, W H on veemolekulide summarne seoseenergia ja W kineetiline energia. 28
31 Klastriteooria pooldajad väidavad, et erinevate klastrite servad on erineva struktuuriga ja võivad küll haakuda, kuid tekkinud struktuur on erinev kristallvõre omast. Et klastrite struktuur kohanduks kristallvõre struktuuriks, on allajahutatud vett vaja raputada Ioonide hüdraadid merevees hüdraat vee molekulidega ümbritsetud osake Ühes kilogrammis merevees on keskmiselt 35 g soolasid. See tähendab, et 100 veemolekuli kohta on ainult 3-4 soolamolekuli. Kui paigutada soolakristall puhtasse vette, siis oma polaarsuse tõttu tungivad vee molekulid soola kristallvõresse ja ümbritsevad üksikud soolamolekulid arvukate veemolekulidega. Seejärel soolamolekulid dissotsieeruvad (lahutuvad, lagunevad) veemolekulide toimel ioonideks. Joon Veekeskkonnas dissotsieerub soola molekul ioonideks. Veemolekulide poolt ümbritsetud iooni nimetatakse ioonhüdraadiks. Soola koostisosade tekkinud ioonid ümbritsetakse veemolekulide poolt, tekivad nn. ioonhüdraadid. Viimased, omades iooni laengut, pole enam elektriliselt neutraalsed. Seega on vette ilmunud laetud osakesed (laengukandjad), mis oluliselt suurendavad vee elektrijuhtivust) Puhta vee elektrijuhtivuse suurusjärk on Ω cm
32 1 1 1 Merevee elektrijuhtivuse suurusjärk on üle miljoni korra suurem, 10 Ω cm. Üldistavalt võib nimetada kolm tähtsat muutust, mida soola lisamine põhjustab vee mikrostruktuuris: 1) suur osa puhta vee klastreid hävib, loovutades oma molekulid ioonhüdraatidele; 2) uued tekkinud klastrid ioonhüdraadid on stabiilsemad puhta vee klastritest, sest seos ioon veemolekul on tugevam kui seos veemolekul veemolekul; 3) elektrostaatilise tõmbe tõttu paigutuvad molekulid soolvees tihedamalt kui puhtas vees, seepärast vee tihedus kasvab (eriruumala väheneb), nn. vee soolsuslik kokkusurumine. Klastrit, mis koosneb ioonist ja seda ümbritsevatest vee molekulidest, nimetatakse ioonhüdraadiks või ioonagregaadiks. Arvatakse, et see koosneb kolmest erinevast tsoonist iooni ümber (järgmine joonis). Vahetult iooni ümbritsevad veemolekulid moodustavad tsooni A. ugeva elektrostaatilise tõmbe tõttu on selles tsoonis kõige suurem aine tihedus ja kõige väiksem kokkusurutavus. Järgmises, B tsoonis, on iooni elektriväli nõrgem ning vee molekulid moodustavad ka omavahelisi seoseid. ihedus on väiksem kui tsoonis A. Joon Veemolekulide tsoonid Na + iooni ümber. 30
33 soonis C on iooni mõju vaevumärgatav, kuid osa vee molekule on siiski orienteeritud vastavalt iooni elektriväljale. Molekulide arv tsoonides sõltub temperatuurist, kõrgematel temperatuuridel on vee molekulide kineetiline energia suurem ning nad on raskemini hõivatavad tsoonidesse. Hinnanguliselt on tabelis toodud molekulide üldarv tsoonides A ja B: emperatuur Molekulide arv tsoonides A ja B kokku 5 C C C 21 Kas merevees toimub ka soolaioonide rekombinatsioon (taasühinemine) näiteks valemi + Na + Cl NaCl järgi ning soolamolekulide taasmoodustumine? Kuna merevesi kujutab endast lahjat lahust, siis on iga soola koostisosa ioon (Na +, Cl -, K + jne) ümbritsetud paljudest vee molekulidest ning rekombinatsioonide osa on tühine Vee erandlikke füüsikalisi omadusi abel Vee erandlikke füüsikalisi omadusi. Omadus Võrdlus teiste ainetega ähtsus Soojusmahtuvus (Specific heat, heat capacity) Varjatud sulamissoojus (Latent heat of fusion) Varjatud aurustumisssoojus (Latent heat of evaporation) Soojuspaisumine (hermal expansion) Pindpinevus (Surface tension) Suurim kõigist tahkistest ja vedelikest, välja arvatud ammoniaak (NH 3 terava lõhnaga, mürgine, õhust kergem gaas) Suurim kõigist ainetest, välja arvatud NH 3 Suurim kõigist ainetest Magevee maksimaalne tihedus on kõrgemal temperatuuril kui külmumispunkt Suurim looduslikest vedelikest (vrdl sula klaas) Väldib ekstreemseid temperatuure veekeskkonnas Väldib ekstreemseid temperatuure kehades Soojuse ülekanne veemasside liikumisel Sulamise ja jäätumise termostaatiline efekt Suur soojuse ülekanne atmosfääris aurustumisel ja veeldumisel Jääkate ei vaju veekogu põhja Koevedelike liikumine kapillaarides 31
34 2.6. Osmoos, adapteerumine soolsusega, Läänemere elustik osmos (kr.k) tõuge, lahustimolekulide eelistatud liikumine (imbumine) läbi poolläbilaskva vaheseina osmoos on difusiooni üks eriliikidest Osmootne rõhk Osmootne rõhk on osmoosi tagajärjel tekkiv täiendav rõhk. Vaatleme NaCl lahuseid U- torus, mis on jaotatud poolläbilaskva membraaniga kaheks osaks. Vasakul vaheseinast on kange NaCl lahus, paremal pool lahja lahus. Katse alguses on katseklaasi vasemas ja paremas harus vedelikunivoode kõrgused võrdsed. Mõne aja pärast ühes harus nivoo tõuseb, teises langeb. ekivad osmootne rõhk ja osmootne rõhulangus. Millises katseklaasi harus vedelikunivoo tõuseb, vasakus või paremas? NaCl kange lahus NaCl lahja lahus poolläbilaskev membraan (avad ca 1 nm) Joon Osmoos NaCl lahustega. Vesilahuste korral annab osmootse rõhu tekkimisele vastuse veemolekuli erandlik ehitus. Nagu eespool öeldud, ei paikne H 2 O molekulis aatomid reas, vaid 105 nurga all, molekul kujutab endast elektrilist dipooli. Kui vette lisada soola, siis H 2 O dipoolid lõhuvad soolamolekulid ioonideks ja ümbritsevad igat tekitatud iooni mitmekihilise kobarana (solvaatmantliga). ekkinud klaster, mille tsentris on soolaioon, ei mahu difundeeruma läbi membraani. Ka solvaatmantlis olevad veemolekulid on hõivatud ega pääse difundeeruma, kuid soolalahuses on vabu veemolekule, mis difundeeruvad sinnapoole membraani, kus vett vähem on, st sinna, kus soolade kontsentratsioon on suurem. Seega tõuseb nivoo vasakpoolses harus. urgor turgor lad. k. turgēre turgestsents, turdus, kudede pingus Loomsetes kudedes reguleeritakse osmootset rõhku rakkudevahelise vedeliku e. ekstratsellulaarse vedeliku kontsetratsiooni abil. Rakuvälise vedeliku soolade kontsentratsioon on pisut madalam kui raku sees. Seega tungib vesi rakku, hoides seda täispuhutuna, nagu kilekotti. Vedeliku kontsentratsiooni kahel pool rakuseina reguleerib organism sellisena, et rakk liigselt ei paisuks. 32
35 aimsete rakkude erinevuseks on nende tugev tselluloosist ja pektiinidest koosnev rakusein, mis ei luba rakul osmootse rõhu tõttu suureks venida. Rakkudes oleva rõhu tõttu on varred ja lehed püsti. Rakusisest rõhku nimetatakse turgoriks. Osmootne šokk choc pr k, järsu ning tugeva vapustuse halvav, vahel ka surmav toime organismi; organismi regulatsiooni pidurdumisest tingitud vereringe ja ainevahetuse häired Looduslikes veekogudes (jõed, järved, mered, ookeanid) on põhiliselt kahesuguse soolsusega vett: 1) praktiliselt null-soolsusega vesi ehk magevesi (S 0), mis on enamikes siseveekogudes (välja arvatud soolajärved), 2) ookeanivesi soolsusega S 35; soolsuse ühikut (, g/kg, ppt, psu) UNESCO soovituse järgi pole vaja lisada, viimastel aastate teaduskirjanduses lisatakse siiski psu (practical salinity unit), märkimaks soolsuse kaudset mõõtmist elektrijuhtivuse kaudu. Pidevalt veekeskkonnas elavad loomsed ja taimsed organismid on kohastunud soolsustele kas 35 või 0. Läänemeri oma vähese soolsusega (pinnakihtides 5 12), on erandlik. Vähese soolsusega vett kutsutakse riimveeks. Elusorganismide rakuvedelike ja ektratsellulaarsete (rakkude vahel olevate) vedelike soolsus on magevee ja ookeanivee vahepealne. Kui magevee loom või taim satub ookeanivette, või vastupidi, ookeanis kohastunud organism satub magevette, siis muudab suunda läbi naha toimuv osmootne difusioon. Näiteks ookeanivette sattunud magevee konn kaotab kaalus, sest tema sisemusest hakkab vesi välja imbuma, üritades ookeanivee soolsust alandada. Magevette sattunud ookeanikala soolasesse sisemusse hakkab aga tungima magevesi, kala massi suurendades. Luustikku omavate kalade koevedelike soolsus on 7 8. Järgnevas tabelis on loetletud magevee- ja ookeanikalade veevahetuse tähtsamad iseärasused. abel Luustikku omavate magevee- ja ookeanikalade veevahetus. Mageveekalad Hüpertoonilised, organismi soolsus suurem kui mageveel. Magevesi siseneb kala organismi naha kaudu. Mageveekalad ei joo vett. Rakuseinad hoiavad sooli kinni, säilitades organismi soolavarusid. Ookeanikalad Hüpotoonilised, organismi soolsus väiksem kui ookeaniveel. Organismis olev vesi difundeerub naha kaudu ookeani. Vedelikukao kompenseerimiseks joovad ookeanikalad suures koguses vett, mis imendub sooltoru kaudu. Eritavad soolalahust eriliste rakkude kaudu, mis paiknevad lõpustes. Nii eritatakse ühevalentseid ioone (Na +, K +, Cl ). 33
36 Üleliigse vee väljutamiseks eritavad neerude kaudu suures koguses lahjat uriini. Ookeanivees kui sobimatus keskkonnas hakkab mageveekalast vesi naha kaudu organismist välja difundeeruma. Selle tagajärjel väheneb uriini eritumine ja laguproduktide väljaviimine organismist on takistatud. Laguproduktide kuhjumine põhjustab mürgituse. Sellele lisandub suurenenud soolasisalduse mürgine toime. Organism tõenäoliselt hukkub. Üleliigsete soolade väljutamiseks eritavad neerude kaudu väheses koguses kontsentreeritud uriini. Nii eritatakse kahevalentseid ioone (Mg ++, Ca ++ ). Soolade eritumine toimub ka väljaheidetega. Sattudes magedasse vette hakkab magevesi läbi ookeanikala naha organismi tungima. Kehamass suureneb, organismi vedelike kontsentratsioon väheneb (lahjeneb). Organism tõenäoliselt hukkub kehavedelike kontsentratsiooni liigse alanemise tõttu. Inimorganism vees Inimorganismi koevedelike soolsus on ca 9. Osmoosi suhtes kõige tundlikumad osad on silmad ja lõikehaavad. Nii magevette kui ookeanivette ujuma minnes hakkavad silmad kipitama. Kui vee soolsus on samuti ca 9, siis on ebameldiv tunne silmades minimaalne, lõikehaavad (klaasikild jalas) kipitavad sellises vees vähem. Läänemere kui riimveelise veekogu soolsus on 5 12, osmoosi silmas pidades on Läänemeri sobivam ujumiseks kui magevesi või ookeanivesi. Füsioloogiline lahus meditsiinis Soolsus ca (meditsiinilises praktikas kasutatakse protsente, %). Odavaimate füsioloogilise lahuste koostises on sooladest ainult NaCl. Kallimates on ka teisi sooli, glükoosi jm. Manustatakse veeni organismis ringleva vedelikuhulga taastamiseks suure vere- või vedelikukaotuse puhul. Organismide adapteerumine soolsusega Veeorganismid, nii taimsed kui loomsed, kohanduvad halvasti teistsuguse soolsusega. Ellujäänutel asendub osmootne šokk osmootse stressiga. Erineva soolsusega vees elavad kalad (lõhe, lest, tursk jt) suudavad reguleerida vee omastamist (joomist) ja uriini eritumist. Suuri soolsuse muutusi talub angerjas. Angerja kehapinda kattev limakiht piirab vee- ja soolavahetust naha kaudu. Luukaladest erinev veevahetus on avaookeani kõhrkaladel (hai, rai). Viimastel on koevedelike soolsus ligilähedane ookeanivee soolsusele, mistõttu osmoos läbi kattenaha puudub. Kõhrkalade toiduks tarvitamisel tuleb soolad kulinaarselt (leotamise, keetmisega) kalalihast eemaldada. 34
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PLASTSED DEFORMATSIOONID
 PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Vektorid II. Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale
 Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
2.2.1 Geomeetriline interpretatsioon
 2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
Funktsiooni diferentsiaal
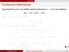 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Lokaalsed ekstreemumid
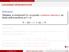 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Kehade soojendamisel või jahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks.
 KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
Sissejuhatus mehhatroonikasse MHK0120
 Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks
 4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
Töö nr. 2. Õhurõhu, temperatuuri ja õhuniiskuse määramine.(2013)
 Töö nr. 2. Õhurõhu, temperatuuri ja õhuniiskuse määramine.(2013) Maakera ümbritseb õhukiht, mille paksus on umbes 1000 km (poolustel õhem, ekvaatoril paksem). 99% õhust asub 25-km paksuses kihis. Õhk on
Töö nr. 2. Õhurõhu, temperatuuri ja õhuniiskuse määramine.(2013) Maakera ümbritseb õhukiht, mille paksus on umbes 1000 km (poolustel õhem, ekvaatoril paksem). 99% õhust asub 25-km paksuses kihis. Õhk on
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
Keemiliste elementide perioodilisustabel
 Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Graafiteooria üldmõisteid. Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid
 Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi
 Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
Compress 6000 LW Bosch Compress LW C 35 C A ++ A + A B C D E F G. db kw kw /2013
 55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
20. SIRGE VÕRRANDID. Joonis 20.1
 κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus
 Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus 1. Haljala valla metsa pindala Haljala valla üldpindala oli Maa-Ameti
Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus 1. Haljala valla metsa pindala Haljala valla üldpindala oli Maa-Ameti
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
Molekulid ei esine üksikuna vaid suurearvuliste kogumitena.
 2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
Energiabilanss netoenergiavajadus
 Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
AATOMI EHITUS KEEMILINE SIDE
 TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 2016
 Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
HULGATEOORIA ELEMENTE
 HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
SOOJUSFÜÜSIKA ALUSED. Tehniline termodünaamika Soojusläbikanne ANDRES TALVARI
 SOOJUSFÜÜSIKA ALUSED Tehniline termodünaamika Soojusläbikanne ANDRES TALVARI Õppevahend on mõeldud kasutamiseks Sisekaitseakadeemia päästekolledži üliõpilastele õppeaine Soojusfüüsika omandamisel, kuid
SOOJUSFÜÜSIKA ALUSED Tehniline termodünaamika Soojusläbikanne ANDRES TALVARI Õppevahend on mõeldud kasutamiseks Sisekaitseakadeemia päästekolledži üliõpilastele õppeaine Soojusfüüsika omandamisel, kuid
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
Sirgete varraste vääne
 1 Peatükk 8 Sirgete varraste vääne 8.1. Sissejuhatus ja lahendusmeetod 8-8.1 Sissejuhatus ja lahendusmeetod Käesoleva loengukonspekti alajaotuses.10. käsitleti väändepingete leidmist ümarvarrastes ja alajaotuses.10.3
1 Peatükk 8 Sirgete varraste vääne 8.1. Sissejuhatus ja lahendusmeetod 8-8.1 Sissejuhatus ja lahendusmeetod Käesoleva loengukonspekti alajaotuses.10. käsitleti väändepingete leidmist ümarvarrastes ja alajaotuses.10.3
HSM TT 1578 EST 6720 611 954 EE (04.08) RBLV 4682-00.1/G
 HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
Jätkusuutlikud isolatsioonilahendused. U-arvude koondtabel. VÄLISSEIN - COLUMBIA TÄISVALATUD ÕÕNESPLOKK 190 mm + SOOJUSTUS + KROHV
 U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
Arvuteooria. Diskreetse matemaatika elemendid. Sügis 2008
 Sügis 2008 Jaguvus Olgu a ja b täisarvud. Kui leidub selline täisarv m, et b = am, siis ütleme, et arv a jagab arvu b ehk arv b jagub arvuga a. Tähistused: a b b. a Näiteks arv a jagab arvu b arv b jagub
Sügis 2008 Jaguvus Olgu a ja b täisarvud. Kui leidub selline täisarv m, et b = am, siis ütleme, et arv a jagab arvu b ehk arv b jagub arvuga a. Tähistused: a b b. a Näiteks arv a jagab arvu b arv b jagub
Deformatsioon ja olekuvõrrandid
 Peatükk 3 Deformatsioon ja olekuvõrrandid 3.. Siire ja deformatsioon 3-2 3. Siire ja deformatsioon 3.. Cauchy seosed Vaatleme deformeeruva keha meelevaldset punkti A. Algolekusontemakoor- dinaadid x, y,
Peatükk 3 Deformatsioon ja olekuvõrrandid 3.. Siire ja deformatsioon 3-2 3. Siire ja deformatsioon 3.. Cauchy seosed Vaatleme deformeeruva keha meelevaldset punkti A. Algolekusontemakoor- dinaadid x, y,
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Kontekstivabad keeled
 Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
8. Faasid ja agregaatolekud.
 Soojusõpetus 8a 1 8. Faasid ja agregaatolekud. 8.1. Faasi ja agregaatoleku mõisted. Faas = süsteemi homogeenne ja mehaaniliselt eraldatav osa. Keemiliselt heterogeense süsteemi näide: õli + vesi. Keemiliselt
Soojusõpetus 8a 1 8. Faasid ja agregaatolekud. 8.1. Faasi ja agregaatoleku mõisted. Faas = süsteemi homogeenne ja mehaaniliselt eraldatav osa. Keemiliselt heterogeense süsteemi näide: õli + vesi. Keemiliselt
6. ATMOSFÄÄRI JA MERE VERTIKAALNE TASAKAAL 6.1. Atmosfääri vertikaalne tasakaal
 9-03-04, 2:6, \\Cumulus\NEDAA\Meri-atm_NEDAA\A-mf-6_Vert_tasak.doc 6. AMOSFÄÄRI JA MERE VERIKAALNE ASAKAAL 6.. Atmosfääri vertikaalne tasakaal Mingi objekt või süsteem võib olla kolmes erinevas tasakaaluolekus:
9-03-04, 2:6, \\Cumulus\NEDAA\Meri-atm_NEDAA\A-mf-6_Vert_tasak.doc 6. AMOSFÄÄRI JA MERE VERIKAALNE ASAKAAL 6.. Atmosfääri vertikaalne tasakaal Mingi objekt või süsteem võib olla kolmes erinevas tasakaaluolekus:
Vektoralgebra seisukohalt võib ka selle võrduse kirja panna skalaarkorrutise
 Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika
 Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
STM A ++ A + A B C D E F G A B C D E F G. kw kw /2013
 Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
Teaduskool. Alalisvooluringid. Koostanud Kaljo Schults
 TARTU ÜLIKOOL Teaduskool Alalisvooluringid Koostanud Kaljo Schults Tartu 2008 Eessõna Käesoleva õppevahendi kasutajana on mõeldud eelkõige täppisteaduste vastu huvi tundvaid gümnaasiumi õpilasi, kes on
TARTU ÜLIKOOL Teaduskool Alalisvooluringid Koostanud Kaljo Schults Tartu 2008 Eessõna Käesoleva õppevahendi kasutajana on mõeldud eelkõige täppisteaduste vastu huvi tundvaid gümnaasiumi õpilasi, kes on
Ülesanne 4.1. Õhukese raudbetoonist gravitatsioontugiseina arvutus
 Ülesanne 4.1. Õhukese raudbetoonist gravitatsioontugiseina arvutus Antud: Õhuke raudbetoonist gravitatsioontugisein maapinna kõrguste vahega h = 4,5 m ja taldmiku sügavusega d = 1,5 m. Maapinnal tugiseina
Ülesanne 4.1. Õhukese raudbetoonist gravitatsioontugiseina arvutus Antud: Õhuke raudbetoonist gravitatsioontugisein maapinna kõrguste vahega h = 4,5 m ja taldmiku sügavusega d = 1,5 m. Maapinnal tugiseina
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
6.6 Ühtlaselt koormatud plaatide lihtsamad
 6.6. Ühtlaselt koormatud plaatide lihtsamad paindeülesanded 263 6.6 Ühtlaselt koormatud plaatide lihtsamad paindeülesanded 6.6.1 Silindriline paine Kui ristkülikuline plaat on pika ristküliku kujuline
6.6. Ühtlaselt koormatud plaatide lihtsamad paindeülesanded 263 6.6 Ühtlaselt koormatud plaatide lihtsamad paindeülesanded 6.6.1 Silindriline paine Kui ristkülikuline plaat on pika ristküliku kujuline
Tuletis ja diferentsiaal
 Peatükk 3 Tuletis ja diferentsiaal 3.1 Tuletise ja diferentseeruva funktsiooni mõisted. Olgu antud funktsioon f ja kuulugu punkt a selle funktsiooni määramispiirkonda. Tuletis ja diferentseeruv funktsioon.
Peatükk 3 Tuletis ja diferentsiaal 3.1 Tuletise ja diferentseeruva funktsiooni mõisted. Olgu antud funktsioon f ja kuulugu punkt a selle funktsiooni määramispiirkonda. Tuletis ja diferentseeruv funktsioon.
Molekulaarfüüsika - ja termodünaamika alused
 Molekulaarfüüsika - ja termodünaamika alused Ettevalmistus kontrolltööks 1. Missugustel väidetel põhineb molekulaarkineetiline teooria? Aine koosneb molekulidest Osakesed on pidevas liikumises Osakestele
Molekulaarfüüsika - ja termodünaamika alused Ettevalmistus kontrolltööks 1. Missugustel väidetel põhineb molekulaarkineetiline teooria? Aine koosneb molekulidest Osakesed on pidevas liikumises Osakestele
(Raud)betoonkonstruktsioonide üldkursus 33
 (Raud)betoonkonstruktsioonide üldkursus 33 Normaallõike tugevusarvutuse alused. Arvutuslikud pinge-deormatsioonidiagrammid Elemendi normaallõige (ristlõige) on elemendi pikiteljega risti olev lõige (s.o.
(Raud)betoonkonstruktsioonide üldkursus 33 Normaallõike tugevusarvutuse alused. Arvutuslikud pinge-deormatsioonidiagrammid Elemendi normaallõige (ristlõige) on elemendi pikiteljega risti olev lõige (s.o.
=217 kj/mol (1) m Ühe mooli glükoosi sünteesil lihtainetest vabaneb footoneid: Δ H f, glükoos n (glükoos) =5,89 mol (1) E (footon)
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
ORGAANILINE KEEMIA I osa
 ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
TÄIENDAVAID TEEMASID KOOLIKEEMIALE III
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
4.1 Funktsiooni lähendamine. Taylori polünoom.
 Peatükk 4 Tuletise rakendusi 4.1 Funktsiooni lähendamine. Talori polünoom. Mitmetes matemaatika rakendustes on vaja leida keerulistele funktsioonidele lihtsaid lähendeid. Enamasti konstrueeritakse taolised
Peatükk 4 Tuletise rakendusi 4.1 Funktsiooni lähendamine. Talori polünoom. Mitmetes matemaatika rakendustes on vaja leida keerulistele funktsioonidele lihtsaid lähendeid. Enamasti konstrueeritakse taolised
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Eesti koolinoorte 51. täppisteaduste olümpiaad
 Eesti koolinoorte 5 täppisteaduste olümpiaad Füüsika lõppvoor 7 märts 2004 a Põhikooli ülesannete lahendused ülesanne (KLAASTORU) Plaat eraldub torust siis, kui petrooleumisamba rõhk saab võrdseks veesamba
Eesti koolinoorte 5 täppisteaduste olümpiaad Füüsika lõppvoor 7 märts 2004 a Põhikooli ülesannete lahendused ülesanne (KLAASTORU) Plaat eraldub torust siis, kui petrooleumisamba rõhk saab võrdseks veesamba
8. KEEVISLIITED. Sele 8.1. Kattekeevisliide. Arvutada kahepoolne otsõmblus terasplaatide (S235J2G3) ühendamiseks. F = 40 kn; δ = 5 mm.
 TTÜ EHHATROONIKAINSTITUUT HE00 - ASINATEHNIKA -, 5AP/ECTS 5 - -0-- E, S 8. KEEVISLIITED NÄIDE δ > 4δ δ b k See 8.. Kattekeevisiide Arvutada kahepoone otsõmbus teraspaatide (S5JG) ühendamiseks. 40 kn; δ
TTÜ EHHATROONIKAINSTITUUT HE00 - ASINATEHNIKA -, 5AP/ECTS 5 - -0-- E, S 8. KEEVISLIITED NÄIDE δ > 4δ δ b k See 8.. Kattekeevisiide Arvutada kahepoone otsõmbus teraspaatide (S5JG) ühendamiseks. 40 kn; δ
28. Sirgvoolu, solenoidi ja toroidi magnetinduktsiooni arvutamine koguvooluseaduse abil.
 8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
Koduseid ülesandeid IMO 2017 Eesti võistkonna kandidaatidele vol 4 lahendused
 Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
F l 12. TRANSPORDINÄHTUSED JA BIOENERGEETIKA ALUSED
 1. TRANSPORDINÄHTUSED JA BIOENERGEETIKA ALUSED Eluks on vajalik pidev aine ja energia transport (e suunatud liikumine) läbi biosfääri ja konkreetselt bioloogilise aine. Biosfäär ehk elukeskkond on Maa
1. TRANSPORDINÄHTUSED JA BIOENERGEETIKA ALUSED Eluks on vajalik pidev aine ja energia transport (e suunatud liikumine) läbi biosfääri ja konkreetselt bioloogilise aine. Biosfäär ehk elukeskkond on Maa
ORGAANILINE KEEMIA ANDRES TALVARI
 ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
ETTEVALMISTUS KEEMIAOLÜMPIAADIKS II
 ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
REAKTSIOONIKINEETIKA
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
,millest avaldub 21) 23)
 II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
p A...p D - gaasiliste ainete A...D osarõhud, atm K p ja K c vahel kehtib seos
 LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
PÕLEVAINETE OMADUSED. Andres Talvari
 PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
Eessõna 7 Maa atmosfäär 11 Pilvede olemus, tekkimine ja tähtsus 16 Pilvede klassifitseerimine, süstemaatika ja omavahelised seosed 26
 SISUKORD Eessõna 7 Maa atmosfäär 11 Pilvede olemus, tekkimine ja tähtsus 16 Pilvede klassifitseerimine, süstemaatika ja omavahelised seosed 26 Pilvede süstemaatika ajalugu 27 Pilvede nimetamine ja pilvede
SISUKORD Eessõna 7 Maa atmosfäär 11 Pilvede olemus, tekkimine ja tähtsus 16 Pilvede klassifitseerimine, süstemaatika ja omavahelised seosed 26 Pilvede süstemaatika ajalugu 27 Pilvede nimetamine ja pilvede
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
ALGEBRA I. Kevad Lektor: Valdis Laan
 ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
ALGEBRA I Kevad 2013 Lektor: Valdis Laan Sisukord 1 Maatriksid 5 1.1 Sissejuhatus....................................... 5 1.2 Maatriksi mõiste.................................... 6 1.3 Reaalarvudest ja
2 Hüdraulika teoreetilised alused 2.1 Füüsikalised suurused
 2 2.1 Füüsikalised suurused Mass m Inertsi ja gravitatsiooni iseloomustaja ning mõõt. Keha mass on SI-süsteemi põhiühik. Massi mõõtühikuks SIsüsteemis on kilogramm. Jõud F Kehade vastastikuse mehaanilise
2 2.1 Füüsikalised suurused Mass m Inertsi ja gravitatsiooni iseloomustaja ning mõõt. Keha mass on SI-süsteemi põhiühik. Massi mõõtühikuks SIsüsteemis on kilogramm. Jõud F Kehade vastastikuse mehaanilise
4. KEHADE VASTASTIKMÕJUD. JÕUD
 4. KEHADE VASTASTIKMÕJUD. JÕUD Arvatavasti oled sa oma elus kogenud, et kõik mõjud on vastastikused. Teiste sõnadega: igale mõjule on olemas vastumõju. Ega füüsikaski teisiti ole. Füüsikas on kehade vastastikuse
4. KEHADE VASTASTIKMÕJUD. JÕUD Arvatavasti oled sa oma elus kogenud, et kõik mõjud on vastastikused. Teiste sõnadega: igale mõjule on olemas vastumõju. Ega füüsikaski teisiti ole. Füüsikas on kehade vastastikuse
CaCO 3(s) --> CaO(s) + CO 2(g) H = kj. Näide
 3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
Deformeeruva keskkonna dünaamika
 Peatükk 4 Deformeeruva keskkonna dünaamika 1 Dünaamika on mehaanika osa, mis uurib materiaalsete keskkondade liikumist välismõjude (välisjõudude) toimel. Uuritavaks materiaalseks keskkonnaks võib olla
Peatükk 4 Deformeeruva keskkonna dünaamika 1 Dünaamika on mehaanika osa, mis uurib materiaalsete keskkondade liikumist välismõjude (välisjõudude) toimel. Uuritavaks materiaalseks keskkonnaks võib olla
Joonis 1. Teist järku aperioodilise lüli ülekandefunktsiooni saab teisendada võnkelüli ülekandefunktsiooni kujul, kui
 Ülesnded j lhendused utomtjuhtimisest Ülesnne. Süsteem oosneb hest jdmisi ühendtud erioodilisest lülist, mille jonstndid on 0,08 j 0,5 ning õimendustegurid stlt 0 j 50. Leid süsteemi summrne ülendefuntsioon.
Ülesnded j lhendused utomtjuhtimisest Ülesnne. Süsteem oosneb hest jdmisi ühendtud erioodilisest lülist, mille jonstndid on 0,08 j 0,5 ning õimendustegurid stlt 0 j 50. Leid süsteemi summrne ülendefuntsioon.
( ) ( ) 2008/2009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
KATEGOORIATEOORIA. Kevad 2010
 KTEGOORITEOORI Kevad 2010 Loengukonspekt Lektor: Valdis Laan 1 1. Kategooriad 1.1. Hulgateoreetilistest alustest On hästi teada, et kõigi hulkade hulka ei ole olemas. Samas kategooriateoorias sooviks me
KTEGOORITEOORI Kevad 2010 Loengukonspekt Lektor: Valdis Laan 1 1. Kategooriad 1.1. Hulgateoreetilistest alustest On hästi teada, et kõigi hulkade hulka ei ole olemas. Samas kategooriateoorias sooviks me
1. Soojuskiirguse uurimine infrapunakiirguse sensori abil. 2. Stefan-Boltzmanni seaduse katseline kontroll hõõglambi abil.
 LABORATOORNE TÖÖ NR. 1 STEFAN-BOLTZMANNI SEADUS I TÖÖ EESMÄRGID 1. Soojuskiirguse uurimine infrapunakiirguse sensori abil. 2. Stefan-Boltzmanni seaduse katseline kontroll hõõglambi abil. TÖÖVAHENDID Infrapunase
LABORATOORNE TÖÖ NR. 1 STEFAN-BOLTZMANNI SEADUS I TÖÖ EESMÄRGID 1. Soojuskiirguse uurimine infrapunakiirguse sensori abil. 2. Stefan-Boltzmanni seaduse katseline kontroll hõõglambi abil. TÖÖVAHENDID Infrapunase
KATEGOORIATEOORIA. Kevad 2016
 KTEGOORITEOORI Kevad 2016 Loengukonspekt Lektor: Valdis Laan 1 1. Kategooriad 1.1. Hulgateoreetilistest alustest On hästi teada, et kõigi hulkade hulka ei ole olemas. Samas kategooriateoorias sooviks me
KTEGOORITEOORI Kevad 2016 Loengukonspekt Lektor: Valdis Laan 1 1. Kategooriad 1.1. Hulgateoreetilistest alustest On hästi teada, et kõigi hulkade hulka ei ole olemas. Samas kategooriateoorias sooviks me
Algebraliste võrrandite lahenduvus radikaalides. Raido Paas Juhendaja: Mart Abel
 Algebraliste võrrandite lahenduvus radikaalides Magistritöö Raido Paas Juhendaja: Mart Abel Tartu 2013 Sisukord Sissejuhatus Ajalooline sissejuhatus iii v 1 Rühmateooria elemente 1 1.1 Substitutsioonide
Algebraliste võrrandite lahenduvus radikaalides Magistritöö Raido Paas Juhendaja: Mart Abel Tartu 2013 Sisukord Sissejuhatus Ajalooline sissejuhatus iii v 1 Rühmateooria elemente 1 1.1 Substitutsioonide
1 Funktsioon, piirväärtus, pidevus
 Funktsioon, piirväärtus, pidevus. Funktsioon.. Tähistused Arvuhulki tähistatakse üldlevinud viisil: N - naturaalarvude hulk, Z - täisarvude hulk, Q - ratsionaalarvude hulk, R - reaalarvude hulk. Piirkonnaks
Funktsioon, piirväärtus, pidevus. Funktsioon.. Tähistused Arvuhulki tähistatakse üldlevinud viisil: N - naturaalarvude hulk, Z - täisarvude hulk, Q - ratsionaalarvude hulk, R - reaalarvude hulk. Piirkonnaks
Fotosüntees. Peatükk 3.
 Fotosüntees. Peatükk 3. Fotosünteesiprotsess on keerulisem kui lihtne üldvõrrand, sest valguse energiat ei saa otse H 2 O seose-elektronidele anda ja neid otse CO 2 -le üle kanda. Seetõttu vaadeldakse
Fotosüntees. Peatükk 3. Fotosünteesiprotsess on keerulisem kui lihtne üldvõrrand, sest valguse energiat ei saa otse H 2 O seose-elektronidele anda ja neid otse CO 2 -le üle kanda. Seetõttu vaadeldakse
RF võimendite parameetrid
 RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
TMR praktikum. Teooria: Aatomituuma varjestatus
 TMR praktikum Praktikum toimub 2-l praktikumipäeval ning koosneb kahest tööst. Tööde eesmärk on ühendite TMR spektrite interpreteerimine ning ainete identifitseerimine nii struktuurvalemi kui brutovalemi
TMR praktikum Praktikum toimub 2-l praktikumipäeval ning koosneb kahest tööst. Tööde eesmärk on ühendite TMR spektrite interpreteerimine ning ainete identifitseerimine nii struktuurvalemi kui brutovalemi
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
Biomakromolekulid: struktuurist omadusteni. Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018
 Biomakromolekulid: struktuurist omadusteni Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018 Sissejuhatus 2 Biokeemia mõõtkava mm mm Inimese embrüo (6. nädal): 4 mm Suurem amööb: 0.8 mm Inimese punaverelible:
Biomakromolekulid: struktuurist omadusteni Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018 Sissejuhatus 2 Biokeemia mõõtkava mm mm Inimese embrüo (6. nädal): 4 mm Suurem amööb: 0.8 mm Inimese punaverelible:
HAPNIKUTARBE INHIBEERIMISE TEST
 HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD
 KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
KOMBINATSIOONID, PERMUTATSIOOND JA BINOOMKORDAJAD Teema 3.1 (Õpiku peatükid 1 ja 3) Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Kombinatoorika 1 / 31 Loengu kava 1 Tähistusi 2 Kombinatoorsed
MATEMAATILISEST LOOGIKAST (Lausearvutus)
 TARTU ÜLIKOOL Teaduskool MATEMAATILISEST LOOGIKAST (Lausearvutus) Õppematerjal TÜ Teaduskooli õpilastele Koostanud E. Mitt TARTU 2003 1. LAUSE MÕISTE Matemaatilise loogika ühe osa - lausearvutuse - põhiliseks
TARTU ÜLIKOOL Teaduskool MATEMAATILISEST LOOGIKAST (Lausearvutus) Õppematerjal TÜ Teaduskooli õpilastele Koostanud E. Mitt TARTU 2003 1. LAUSE MÕISTE Matemaatilise loogika ühe osa - lausearvutuse - põhiliseks
7.7 Hii-ruut test 7.7. HII-RUUT TEST 85
 7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
