ORGAANILISE KEEMIA LABORIJUHEND ABISTAV MATERJAL
|
|
|
- Ευστοργιος Φλέσσας
- 6 χρόνια πριν
- Προβολές:
Transcript
1 TALLINNA ÜLIKL Matemaatika ja Loodusteaduste Instituut RGAANILISE KEEMIA LABRIJUEND ABISTAV MATERJAL Marju Robal ja Rando Tuvikene Tallinn 2008
2 SISUKRD 1. RGAANILISTE AINETE LAUSTUVUS JA LAUSTAMISVÕIME VAN DER WAALSI JÕUD* VESINIKSIDEMED RGAANILISTE AINETE PÕLEMINE ALKAANID JA ALKEENID ETEENI SAAMINE ETEENI REAKTSIN BRMIGA ETEENI REAKTSIN KAALIUMPERMANGANAADIGA (BAEYERI TEST) BRMILAUSE TIME ALKAANIDESSE KAALIUMPERMANGANAADI LAUSE TIME ALKAANIDESSE AREENID AREENIDE BRMIGA REAGEERIMISE KIIRUSE VÕRDLEMINE KAALIUMPERMANGANAADI TIME BENSEENISSE JA TLUEENISSE NITRFENLIDE SAAMINE FENLIDE TÕESTAMINE LÄMMASTIKUSAPPEGA (LIEBERMANNI REAKTSIN) FENLIDE VÄRVUSREAKTSINID RAUD(III)KLRIIDIGA ALGEENIÜENDID ALGEENIÜENDITE JA ALKAANIDE TIEDUSE VÕRDLEMINE ALKLID SCIFFI REAKTIIVI VALMISTAMINE VASKGLÜTSERAADI SAAMINE ALKLIDE KSÜDEERIMINE ALDEÜÜDIDEKS JA KARBKSÜÜLAPETEKS ALKLAADI MDUSTUMINE METANLI JA ETANLI ERISTAMINE KSÜDEERIMISE TEEL BRAKSI TEST KSÜENDID (ALDEÜÜDID JA KETNID) ALDEÜÜDIDE REAKTSIN VASK(II) ÜDRKSIIDIGA ÕBEPEEGLIREAKTSIN (TLLENSI REAKTSIN) KARBKSÜÜLÜENDID KARBKSÜÜLAPETE TUGEVUSE VÕRDLEMINE MAVAEL JA TEISTE APETEGA KARBKSÜÜLAPETE SLADE SAAMINE JA LAGUNDAMINE ESTRI TEKKIMINE ESTRI ÜDRLÜÜS FENLFTALEIINI SAAMINE FLURESTSEIINI SAAMINE DESTILLATSIN SEGUDE ERALDAMINE, KEEMISTEMPERATUURI MÄÄRAMINE JA AINETE PUASTAMINE LITDESTILLAT-SINI ABIL LUMINESTSENTS KEMLUMINESTSENTS LUMINLI KSÜDEERUMINE KRISTALSE RGAANILISE AINE SÜNTEES, PUASTAMINE JA UURIMINE DIBENSALATSETNI SÜNTEES ALDLKNDENSATSIN (CLAISEN-SCMIDT I KNDENSAT-SIN) AINETE PUASTAMINE ÜMBERKRISTALLIMISE ABIL AINETE SULAMISTEMPERATUURIDE MÄÄRAMINE AINETE SPEKTRFTMEETRILINE UURIMINE
3 1. RGAANILISTE AINETE LAUSTUVUS JA LAUSTAMISVÕIME Aine lahustumise protsessi võib kujutada järgmise skeemi alusel: lahusti lahustuv aine lahus lahusti molekulid lahustuva aine molekulid Aine lahustub siis, kui lahusti molekulide vahel mõjuvad tõmbejõud (F 1 ) ja lahustuva aine molekulide vahel mõjuvad tõmbejõud (F 2 ) on mõlemad väiksemad kui lahusti ja lahustuva aine molekulide vahel mõjuvad tõmbejõud (F 3 ): F 1 F 2 F 3 Lahustuvuse tingimus: F 1 F 3 ja F 2 F 3 Lahustumine toimub ka siis, kui tõmbejõud F 1 ja F 2 on ligikaudu võrdsed tõmbejõuga F 3. Lahustumine leiab aset, kui tekkiv süsteem (lahus) on stabiilsem (molekulid tugevamalt seotud) võrreldes algsete puhaste komponentidega (lahusti, lahustunud aine). Süsteemi stabiliseerimise juures on olulised van der Waalsi tõmbejõud ning vesiniksidemed. Erinevate molekulivaheliste jõudude (van der Waalsi jõud) tugevuse võrdlemisel (vt tabel 1) võib teha lihtsa üldistuse sarnane lahustab sarnast: Polaarsed ained lahustuvad polaarsetes lahustites. Mittepolaarsed ained lahustuvad mittepolaarsetes lahustites. Väga polaarsed ained (näiteks ioonidena esinevad soolad) lahustuvad väga polaarsetes lahustites (näiteks vees), kuid ei lahustu mittepolaarsetes või nõrgalt polaarsetes lahustites (näiteks heksaanis, eetris või diklorometaanis). Süsivesinikud ja teised mittepolaarsed ühendid lahustuvad mittepolaarsetes lahustites, kuid mitte vees. Tabel 1. Erinevate vastastoimete tugevuste võrdlus. Vastastoime tüüp Energia (kj/mol) Mõju avaldumise tingimus Keemiline side ~ Vesinikside ~20-40 Vesiniksidet moodustavad molekulid rientatsioonitoime ~1-5 Polaarne molekul - polaarne molekul Induktsioonitoime ~0,05-2 Polaarne molekul - mittepolaarne molekul Dispersioonitoime ~0,05-2 Kõik molekulid 3
4 1.1 VAN DER WAALSI JÕUD* Molekulidevahelisi jõudusid nimetatakse van der Waalsi jõududeks. Dispersioonijõud (Londoni jõud) elektronide liikumisel tekkivate hetkeliste dipoolide nõrk vastastikune mõju. Mittepolaarsetes molekulides ei esine laengu ebaühtlast jaotumist. See on õige aga ainult keskmiselt (mingi ajaühiku jooksul on molekuli iga piirkonna keskmine laeng 0). Elektronide tiirlemise tõttu võib ühel hetkel paikneda aatomi (seega ka molekuli) teatud piirkonnas suurem arv elektrone, mistõttu omandab see piirkond negatiivsema laengu (δ-). Elektronide defitsiidis olev molekuli piirkond omandab seevastu positiivsema laengu (δ). Järgmisel ajahetkel on elektronide asukohad muutunud ning negatiivse laengu omandab teine molekuli piirkond. Elektronide pideva liikumise tõttu tekivad seega hetkelised dipoolid, milles erinimelised laengud pidevalt asukohta vahetavad: δ δ- δ- δ etkeliste dipoolide vastastikuse mõju tulemusena tekivad molekulide vahel nõrgad dispersioonijõud. See on seletatav järgmise näite abil: Elektronide ebaühtlase paiknemise tõttu hetkeliseks dipooliks muutunud molekul läheneb teisele molekulile, milles just sellel hetkel on laengud täiesti võrdselt jaotunud. (Väga ebatõenäoline olukord, kuid teeb protsessi kirjeldamise lihtsamaks. Tegelikkuses on ühel molekulil suurem hetkeline polaarsus kui teisel). δ- δ Antud hetkel mittepolaarne molekul (parempoolne) muutub hetkelisele dipoolile (vasakpoolne) lähenedes samuti hetkeliseks dipooliks (indutseeritud dipooliks). δ- δ δ- δ indutseeritud dipool Järgmisel hetkel võib vasakpoolses molekulis elektronide defitsiit tekkida teises piirkonnas, selle tulemusena muutuvad ka indutseeritud dipooli erinimeliselt laetud pooluste asukohad. δ δ- δ δ- Seni kuni molekulid on teineteisele piisavalt lähedal, muutuvad nende erinimeliselt laetud pooluste asukohad sünkroonselt ning molekulide vahel mõjub alati väike tõmbejõud. 4
5 Selline erinimeliste pooluste tõmbumine ja nende asukoha sünkroonne muutumine hoiavad koos suurt hulka molekule. δ- δ δ- δ δ- δ δ- δ δ- δ δ δ- δ δ- δ δ- δ δ- δ δ- δ- δ δ- δ δ- δ δ- δ δ- δ Dispersioonijõudude tugevus sõltub olulisel määral molekulide suurusest ja kujust. Mida suurem on elektronide arv aatomis ja mida kaugemal elektronid tuumast paiknevad, seda suurema hetkelise polaarsuse võivad aatomid saavutada ning seda suuremad on dispersioonijõud. Dispersioonijõud on omased kõikidele molekulidele nii polaarsetele kui ka mittepolaarsetele. Ühesuguse elektronide arvuga molekulide puhul on dispersioonijõud tugevamad piklikuma kujuga molekulide puhul. Ka võivad pikliku kujuga molekulid paikneda üksteisele lähemale (tihedamalt üksteise kõrvale), see teeb dispersioonijõud efektiivsemaks (jõud vähenevad tunduvalt kauguse suurenedes). Kui võrrelda 2-metüülpropaani ja butaani molekule (mõlemal molekulvalem C 4 10 ), selgub, et dispersioonijõud on eelmainitud omaduste tõttu suuremad butaani puhul. C 3 C 2 C 2 C 3 C 3 C C 3 C 3 butaan 2-metüülpropaan rientatsioonijõud (Keesomi jõud) jõud polaarsete (püsiva dipoolmomendiga) molekulide vahel või ioon-dipool vastastoime. Polaarsed molekulid orienteeruvad lähenemisel üksteise suhtes korrapäraselt: samanimeliselt laetud piirkonnad tõukuvad, erinimelised poolused tõmbuvad. Mida polaarsemad on molekulid, seda tugevamini tõmbuvad nende erinimeliselt laetud poolused teineteise poole. Molekulide soojusliikumine vähendab tunduvalt kindla orientatsiooni võimalust. Seetõttu on vastastikune orientatsioon seda nõrgem, mida kõrgem on temperatuur. Induktsioonijõud (Debye jõud) jõud polaarsete ja mittepolaarsete molekulide vahel (polaarne molekul tekitab teises samuti dipoolmomendi). Samaaegselt orientatsiooniga toimub molekulide deformatsioon kõrvalekaldumine normaalsest sisemisest ehitusest. Deformatsioon põhjustab molekulide polarisatsiooni, s.o dipooli pikkuse suurenemist ja molekulidevahelise mõju suurenemist. 5
6 Polaarse ja mittepolaarse molekuli teineteisele lähenemisel tekitab polaarse molekuli püsiv dipool mittepolaarses molekulis ajutise dipooli, mille tõttu molekulid vastastikku tõmbuvad. Niisugust molekulide vastastikust toimet nimetatakse induktsiooniks; seda põhjustavad induktsioonijõud. Erinevalt orientatsioonist ei sõltu induktsioon temperatuurist. Induktsiooni efekt ei ole suur, kuid ta etendab tunduvat osa juhul, kui tugevasti polaarne molekul mõjutab molekuli, millel puudub dipoolmoment, kuid mis on kergesti polariseeritav. Reeglina mida suurem on elektronide arv, seda kaugemal nad tuumast paiknevad, seda suurem on polariseeritavus. Molekulidevahelise toime energia on tunduvalt väiksem tüüpilise keemilise sideme energiast, kuid ta on küllaldane molekulide liitmiseks (agregaatide moodustamiseks). Missugusel määral ühed või teised jõud võtavad osa molekulidevahelistest reaktsioonidest (vt tabel 2), see oleneb molekulide eneste omadustest: dipoolmomendist ja polariseeritavusest. Kui molekulil on suur dipoolmoment (vesi), on ülekaalus orientatsioonijõud, kui molekulil on suur polariseeritavus (I), ilmnevad peamiselt dispersioonijõud. Tabel 2. Van der Waalsi jõudude protsentuaalne jaotus erinevates molekulides. Van der Waalsi jõudude protsentuaalne jaotus erinevates molekulides Ühend rientatsioonijõud (Keesom) Induktsioonijõud (Debye) Dispersioonijõud (London) CCl Etanool 42,6 9,7 47,6 Etüüleeter 10,2 7,1 82,7 Benseen Klorobenseen 13,3 8,6 78,1 Fluorobenseen 10,6 7,5 81,9 Fenool 14,5 8,6 76,9 Aniliin 13,6 8,5 77,9 Tolueen 0,1 0,9 99,0 t-butanool 23,1 9,7 67,2 Vesi 84,8 4,5 10,5 6
7 1.2 VESINIKSIDEMED Vesiniksidemeid moodustavad molekulid, milles vesinikuaatom on seotud elektronegatiivse, N või F aatomiga. Vesiniksidet moodustavad tsentrid (hüdrofiilsed piirkonnad) määravad ära ainete lahustuvuse vees. Kui hüdrofiilne osa on molekuli suurusega võrreldes väike (seega on suur hüdrofoobne osa), ei lahustu aine vees. Enamasti on orgaanilistes molekulides hüdrofiilseteks osadeks -, -N 2 ja -C rühmad. Näide. Miks lahustuvad etanool, glütserool ja isoamüülalkohol vees erinevalt? C 2 C C 3 C C 2 C 2 C 3 C 3 C 2 glütserool isoamüülalkohol etanool Etanooli molekuli hüdrofiilne osa (hüdroksüülrühm) on molekuli suurusega võrreldes suhteliselt suur, hüdrofoobne osa (etüülrühm) aga suhteliselt väike. Seetõttu seguneb etanool veega igasuguses vahekorras. Glütseroolil on samuti suhteliselt suur hüdrofiilne osa (kolm -rühma), seetõttu seguneb ta samuti veega igas vahekorras. Isoamüülalkoholi molekuli hüdrofoobne osa (isopentüülrühm) on palju suurem (eelmainitud alkoholidega võrreldes), seetõttu lahustub isoamüülalkohol vees halvasti. 7
8 2. RGAANILISTE AINETE PÕLEMINE Molekuli mõõtmete suurenedes muutuvad süsivesinikud raskemini süttivaks. Suuremaid molekule hoiavad koos tugevamad molekulisisesed jõud, see teeb nende lõhkumise raskemaks. Võrreldes kergesti lenduvate ainetega põlevad vähelenduvad vedelikud halvemini, sest ainult vedeliku pinnakihi molekulid reageerivad hapnikuga. Süsivesinikud, mille molekulis on süsinikku protsentuaalselt rohkem, põlevad õhus kollase tahmava leegiga. Kogu süsinik ei oksüdeeru maksimaalse oksüdatsiooniastmeni ja eraldub osaliselt tahmana (süsinik). Piisaval hapniku juurdevoolul põleb kogu tahm leegi sees ja ei eraldu keskkonda. Tahma põlemine annab leegile oranžikaskollase värvuse, tahmaosakesed kuumenevad hõõgumiseni ja emiteerivad palju infrapunakiirgust. Kõigi süsivesinike ja alkoholide (välja arvatud metanool) põlemisel tekib tahmaosakesi. Leegi võib välimuse järgi jaotada järgmiselt: Vaevumärgatav sinakas leek nt. metanool elendav kollakas leek nt. heksaan Tahmav kollakas leek nt. aromaatsed ühendid. Kergesti süttiv Väiksed molekulid Vähe süsinikuaatomeid Kergesti lagunevad molekulid Lenduvad Põlevad vaevumärgatava sinaka leegiga Raskesti süttiv Suured molekulid Palju süsinikuaatomeid Raskesti lagunevad molekulid Vähelenduvad Põlevad helendava kollaka leegiga Beilsteini test alogeeni aatomid reageerivad kuuma vasktraadiga ja moodustavad lenduvaid vaseühendeid, mis muudavad leegi värvuse iseloomulikult rohekaks. Selline halogeeniühendite tuvastamise moodus kannab Beilsteini testi nimetust ja võimaldab määrata kloori, broomi ja joodi sisaldumist uuritavas aines. Mõnikord (kuid mitte alati) on võimalik eristada, millise halogeeniga tegemist on. Kloor muudab leegi rohekaks, broom rohekassiniseks, jood siniseks. Fluor leegi värvust ei muuda, kuna vaskfluoriid (CuF) ei ole lenduv. 8
9 3. ALKAANID JA ALKEENID 3.1 Eteeni saamine Kõrgemal temperatuuril toimub vee eraldumine etanoolist ja tekib eteen: k. 2 S 4 C 3 C 2 C 2 C S 4 seob tekkiva vee. 3.2 Eteeni reaktsioon broomiga alogeeni liitumisel alkeeniga moodustub dihalogenoalkaan eteen liidab kiiresti Br 2, andes 1,2- dibromoetaani: C 2 =C 2 Br 2 C 2 Br-C 2 Br (Vesinikhalogeniidi liitumisel alkeeniga moodustuks halogenoalkaan.) Broomivee puhul moodustub 2-bromoetanool (eteen valastab broomivett): C 2 =C 2 Br 2 2 C 2 Br-C 2 Br Broomivee valastumine võimaldab selgitada, kas tegemist on küllastumata süsivesinikuga. 3.3 Eteeni reaktsioon kaaliumpermanganaadiga (Baeyeri test) Alkeenid oksüdeeruvad kaaliumpermanganaadi toimel kiiresti erinevateks glükoolideks (kahe hüdroksüülrühmaga alkoholid). Eteen oksüdeerub etüleenglükooliks (1,2-etaandiooliks): 3 C 2 =C 2 2 KMn Mn 2 2 K 3 C 2 -C 2 Reaktsiooni käigus kaob kaaliumpermanganaadi lahuse lilla värvus, mistõttu on võimalik määrata, kas ühend on küllastumata Baeyeri test. KMn 4 redutseerumisel tekib pruunikas Mn 2 sade. 3.4 Broomilahuse toime alkaanidesse Alkaanid külmalt Br 2 -ga ei reageeri, kuna ei sisalda kordseid sidemeid ega kergesti asendatavaid vesinikuaatomeid. 3.5 Kaaliumpermanganaadi lahuse toime alkaanidesse KMn 4 on leeliselises keskkonnas küllalt tugev oksüdeerija. Alkaanid ei sisalda aga toatemperatuuril kergesti oksüdeeruvaid rühmi. Seetõttu värvuse kiiret kadumist ei toimu (1 minuti jooksul). 9
10 4. AREENID 4.1 Areenide broomiga reageerimise kiiruse võrdlemine Benseen reageerib broomiga külmalt ning ilma katalüsaatori juuresolekuta väga aeglaselt. Raualaastude lisamisel tekib FeBr 3, mis katalüüsib areenide broomimisreaktsiooni. Samuti kiirendab seda temperatuuri tõstmine. Katalüsaatori (FeBr 3, AlBr 3 ) juuresolekul toimub benseeni broomimisreaktsioon kiiresti, andes esmalt bromobenseeni ning seejärel peamiselt p-dibromobenseeni: Br Br FeBr 3 2 Br Br Br Br FeBr 3 2 Br Br Reaktsiooni tulemusena tekivad kõik 3 võimalikku isomeeri (kõige rohkem p-dibromobenseeni): Br Br Br Br o-dibromobenseen m-dibromobenseen p-dibromobenseen Br Br FeBr 3 katalüsaator polariseerib Br 2 molekuli ja moodustub halogeeni kandev Br [FeBr 4 ] - kompleks. C 6 6 Br [FeBr 3 ] C 6 5 Br Br FeBr 3 Raud ise reaktsioonis katalüsaatoriks ei ole, raua reageerimisel broomiga tekib raud(iii)bromiid: 2 Fe 3 Br 2 2 FeBr 3 Päikesevalguse toimel liitub broom benseenituumaga (eriti soojas), andes heksabromobenseeni. 10
11 4.2 Kaaliumpermanganaadi toime benseenisse ja tolueenisse Benseen KMn 4 -ga ei reageeri. Tolueen oksüdeerub KMn 4 toimel, andes bensoehappe soola: KMn 4 C 3 CK 2 KMn 4 2 Mn 2 K Nitrofenoolide saamine Mõned asendusrühmad (-, -N 2 ) muudavad benseenituuma oluliselt reaktiivsemaks ja mõjutavad oluliselt produktide jaotust orto- ja para- asendatud derivaatide kasuks. Teised (-N 2, -C) vähendavad reaktiivsust ja produktid on eelistatult meta- asendatud. Fenool reageerib lahjendatud lämmastikhappega toatemperatuuril, andes 2-nitrofenooli ja 4-nitrofenooli segu (orto- ja para- asendused): N 3 N 2 N 2 Kontsentreeritud lämmastikhappe toimel fenoolisse tekib peamiselt 2,4,6-trinitrofenool (pikriinhape): 2 N N 2 k. N 3 N Fenoolide tõestamine lämmastikushappega (Liebermanni reaktsioon) Seda reaktsiooni ei anna kõik fenoolid, kõige paremini kulgeb reaktsioon üheaatomiliste fenoolidega, mille paraasend on vaba (orto- ja metaasendis võib olla mingi asendusrühm, välja arvatud nitrorühm). Mitmeaatomilistest fenoolidest kulgeb reaktsioon resortsiiniga. 11
12 NaN 2 2 S 4 2 N 2 S 4 N S 4 N sinine 2 N punane Na N Na sinine 4.5 Fenoolide värvusreaktsioonid raud(iii)kloriidiga Fenoolid moodustavad raud(iii)kloriidiga värvilisi (punaseid, siniseid, rohelisi või violetseid) kompleksühendeid: 3 C 6 5 FeCl 3 Fe(C 6 5 ) 3 3 Cl 3 Fe 3 Fe kollane 3 sinakasvioletne Tekkiv värvus oleneb hüdroksüülrühmade arvust ning ka teistest asendajatest, samuti lahustist. Näiteks annavad fenool, resortsiin, floroglutsiin värvuse sinisest violetseni, hüdrokinoon kollase, pürogallool punase, pürokatehhool rohelise värvuse. 12
13 5. ALGEENIÜENDID 5.1 alogeeniühendite ja alkaanide tiheduse võrdlemine alogeeniühendid on suurema tihedusega kui vesi ning vajuvad vees põhja. Alkaanid on väiksema tihedusega kui vesi ja tõusevad pinnale. Et erinevad vedelikukihid oleksid paremini nähtavad, peab veekiht olema värviline (kuid mitte liialt tume). rgaaniliste ühendite suhteline tihedus Süsivesinikud on madala tihedusega, tihti jääb see näitaja 0,8 g/ml lähedale. Väheste orgaaniliste ühendite tihedus on üle 1,2 g/ml (enamasti mitut halogeeniaatomit sisaldavad ühendid). rgaaniliste vedelike suhtelisi tihedusi on võimalik küllaltki lihtsalt ette ennustada. Tahkete ainete puhul on see keerulisem. rgaaniliste vedelike tiheduse määravad kolm peamist faktorit: molekulmass; raskete aatomite (nt. halogeenid) ja süsinikuaatomite vahekord molekulis; molekulidevahelised kaugused aines. Molekulmass. Sarnase suurusega molekulide puhul on tihedamaks suurema molekulmassiga ühend. Näiteks on tsükloheksaani ja tsükloheksaan-d 12 (kõik vesinikuaatomid on asendatud deuteeriumi aatomitega) tihedused vastavalt 0,78 ja 0,89 g/ml. Tihedus (g/ml) Molekulmass Tsükloheksaan C ,78 84 Tsükloheksaan-d 12 C ,89 96 Raskete aatomite ja süsinikuaatomite vahekord molekulis. Molekulis esinevad rasked aatomid, mis võtavad enda alla suhteliselt väikse ruumala (halogeenid), suurendavad märgatavalt aine tihedust. Näiteks on van der Waalsi raadius metüülrühmal (C 3 ) 200 pm, broomi aatomil 195 pm. Metüülrühma molekulmass on 15, broomi aatommass 80. Seega on broomi aatom metüülrühmast enam kui viis korda suurema massiga, võttes samas enda alla väiksema ruumala. Seetõttu on broomi aatom metüülrühmast märgatavalt suurema tihedusega. Peaaegu ühesuguse molekulruumalaga pentaani ja 1-bromobutaani tihedused on vastavalt 0,62 ja 1,27 g/ml. Tihedus (g/ml) Molekulmass Pentaan C 3 -C 2 -C 2 -C 2 -C 3 0, bromobutaan C 3 -C 2 -C 2 -C 2 -Br 1, rgaaniliste vedelike suhtelist tihedust vee suhtes saab ennustada lihtsa reegli abil: iga molekul, mis sisaldab vähemalt ühte broomi, joodi või vähemalt kahte kloori aatomit (näiteks CCl 3 ), on 13
14 veest (1 g/ml) suurema tihedusega. Teiste orgaaniliste vedelike tihedus on enamasti vee omast väiksem. See reegel on vähemefektiivne suurte molekulide puhul, sest nende puhul ei mängi funktsionaalsed rühmad nii suurt rolli. Molekulidevahelised kaugused aines. Mida lähemal naabermolekulid üksteisele paiknevad, seda suurem on aine tihedus. Siin on oluline osa molekulide kujul. Näiteks on tsükloheksaanil (0,78 g/ml) suurem tihedus kui heksaanil (0,66 g/ml), sest sümmeetrilised tsükloheksaani molekulid paigutuvad tihedamalt üksteise kõrvale. eksaani isomeerid: heksaan 2-metüülpentaan 3-metüülpentaan 2,3-dimetüülbutaan 2,2-dimetüülbutaan Molekulide üksteisele lähenemise ulatuse ja suuremate agregaatide moodustumise võimalikkuse määravad molekulidevahelised jõud (van der Waalsi jõud, vesiniksidemed). Molekulidevahelised tõmbejõud (eriti aga vesiniksidemed) suurendavad vedelike tihedust (ning ka viskoossust). Näiteks on vesiniksidemeid moodustaval 1-butanoolil suurem tihedus (0,81 g/ml) kui tema vesiniksidemeid mittemoodustaval isomeeril dietüüleetril (0,71 g/ml). C 3 C 2 C 2 C 3 C 3 C 2 C 2 C 2 dietüüleeter 1-butanool 0,71 g/ml 0,81 g/ml 14
15 6. ALKLID 6.1 Schiffi reaktiivi valmistamine Schiffi reaktiiv (heksametüül-p-rosaniliin hüdrokloriid; happepõhine indikaator, mis muudab oma värvi rohelisest siniseks kui p on üle 1) kujutab endast fuksiini ja väävlishappe (või Na 2 S 3 ) vesilahust, mida kasutatakse aldehüüdide olemasolu määramiseks. Aldehüüdide juuresolekul lahuses värvub Schiffi reaktiiv roosaks, punaseks (fuksia) või purpurseks. Nime on Schiffi reaktiiv saanud oma leiutaja ugo Schiff`i järgi. Fuksiin ehk p-rosaniliin hüdrokloriid on tumeroheline kristalne (värv)aine, mis vees lahustumisel muutub punaseks. n kinoonse struktuuriga (kinoon tsüklilised diketoonid, milles karbonüülse süsiniku suhtes 2-asendis on kaksiksidemed). Kasutatakse tektiili ja bakterite värvimisel, vahel ka desinfektsioonivahendina. Väävlishappe (või Na 2 S 3 ja Cl) lisamisel fuskiini vesilahusesse, muutub fuksiin värvituks S 3 -ioon kinnitub trifenüülmetaani keskmesse, mille tulemusena häirub harunenud konjugeeritud molekuli soodne resonatsolek. Väävlishappe külluses reageerib S 3 -ioon vabade amiinirühmadega, mille tulemusena tekivad nn. sulfiinhapperühmad. 2 N 2 S N N 2 Cl 3 2 S 3 N 3 Cl S 3 2 N 2 S N fuksiin Schiffi reaktiiv (roosa) (värvitu) 6.2 Vaskglütseraadi saamine Etanool sisaldab molekulis ainult ühte -rühma ning ei moodusta Cu() 2 -ga värvilist lahustuvat komplekssoola. Glütserool (1,2,3-propaantriool) sisaldab molekulis aga kolme kõrvuti asuvat -rühma ning moodustab Cu() 2 -ga tumesinise lahustuva komplekssoola. 2 C 2 C C 2 Cu() Cu 2 2 C C C 2 2 C 2 C C 2 15
16 6.3 Alkoholide oksüdeerimine aldehüüdideks ja karboksüülhapeteks Primaarsed alkoholid oksüdeeruvad astmeliselt esmalt aldehüüdideks, seejärel karboksüülhapeteks: [] R-C 2 - R-C R-C [] ksüdeerijaks on tavaliselt kaaliumdikromaadi (või kaaliumpermanganaadi) ja väävelhappe segu, mille reageerimisel tekivad hapniku aatomid: K 2 Cr S 4 K 2 S 4 Cr 2 (S 4 ) [] (oranž) (roheline) 2 KMn S 4 K 2 S 4 2 MnS [] (violetne) (värvitu) Kaaliumdikromaadi oranži värvuse vahetumine kroom(iii)sulfaadi rohelise vastu on alkomeetrite funktsioneerimise põhialuseks. Sekundaarsed alkoholid oksüdeeruvad ketoonideks, tertsiaarsed alkoholid ülaltoodud tingimustel ei oksüdeeru. 6.4 Alkoholaadi moodustumine Naatrium reageerib etanooliga energiliselt, andes naatriumetanolaadi: 2 C 3 C 2 2 Na 2 C 3 C 2 Na Metanooli ja etanooli eristamine oksüdeerimise teel KMn 4 toimel toimub happelises keskkonnas metanooli ja etanooli oksüdeerumine vastavalt metanaaliks ja etanaaliks: [] C 2 - C [] C 3 -C 2 - C 3 -C Schiffi reaktiiv annab erinevate aldehüüdidega mitmesuguse intensiivsuse ja erineva püsivusega roosa või violetse värvusega ühendeid. Selle rakstiooni abil on võimalik eristada metanooli etanoolist, aga ka tõestada metanooli lisandit etanoolis. Püsiv lillakas- või sinakaspunane värvus tõestab metanooli olemasolu, punane värvus, mis kaob 15 min jooksul tõestab etanooli olemasolu. 16
17 2 S N C 3 R S N S 3 N 3 Cl R aldehüüd N 2 Cl 2 S N Schiffi reaktiiv R S N (värvitu) (violetne/punane) 6.6 Booraksi test Naatriumtetraboraatdekahüdraat (Na 2 B 4 7 *10 2 ehk Na 2 [B 4 5 () 4 ]*8 2 ), igapäevase nimetusega booraks on valge kristalne aine. Boorhappest ja booraksist valmistatakse mürksööta prussakate ja sipelgate hävitamiseks. Booraksi ja metanooli vaheline reaktsioon toimub järgmiselt: B() 3C 3 B(C 3 ) Metanooli mõlemisel annab leegile rohelise värvuse reaktsiooni käigus tekkinud trimetüülboraat. Metanool (C 3 ), rahvapärase nimetusega puupiiritus on värvuseta tüüpilise alkoholi lõhnaga veest kergem madala keemistemperatuuriga (~65 o C) vedelik. Metanool on väga mürgine põhjustades silmade, neeru-, südame ja maksakahjustusi. 10 grammi manustamine põhjustab pimedaks jäämist, 20 grammi manustamisele järgneb suure tõenäosusega surm. Erinevalt teistest alkoholidest võib metanooli mürgistuse saada juba aurude sissehingamisel või naha kaudu organismi sattumisel. Metanooli kasutatakse keemiatööstuses toormena ja kütusena. Etanool (C 3 C 2 ) ehk piiritus on värvuseta iseloomuliku alkoholi lõhnaga põletava maitsega madala keemistemperatuuriga (~78 o C) veest kergem vedelik. Sõna piiritus tuleneb ladinakeelesest väljendist spiritus vini`st, mis tõlkes tähendab veini vaimu. Füüsikalistelt omadustelt on etanool äravahetamiseni sarnane metanooliga. Väikestes kogustes mõjub etanool joovet tekitava narkootilise ainena, suurtemates kogustes on mürgine, surmav. Kõige enam kahjustab etanool inimese närvisüsteemi, eriti peaaju, samuti ka suu-, mao- ja soolte limaskesti, maksa ning neerusid. Nahale ja silma sattumisel tekitab sügelust ja punetust, hingamisteedes mõjub ärritavalt. Inimese kehas oksüdeeritakse etanool lõppsaadusena C 2 -ks ja 2 -ks. Kui puuduks kaitsemehhanism mao alkoholi-dehüdrogenaasi (ensüüm) näol, oleks etanool inimesele üliohtlik mürk. 17
18 7. KSÜENDID (ALDEÜÜDID JA KETNID) 7.1 Aldehüüdide reaktsioon vask(ii) hüdroksiidiga Aldehüüdid on tugevad redutseerijad, nad oksüdeeruvad kergesti, kuumutamisel toimub reaktsioon: RC 2 Cu() 2 RC 2 Cu 2 Tekkiv vask(i)hüdroksiidi sade on kollane, edasisel kuumutamisel muutub ta punakaspruuniks vask(i) oksiidiks: 2 Cu Cu 2 2 Cu 2 võib edasi redutseeruda ja tekib metalliline vask: RC Cu 2 RC 2 Cu 7.2 õbepeeglireaktsioon (Tollensi reaktsioon) Algul sadestub AgN 3 lahusest leelise (Na) toimel must Ag 2 : 2 AgN 3 2 Na Ag 2 2 NaN 3 2 Ag 2 sade lahustub N 3 toimel: Ag 2 N [Ag(N 3 ) 2 ] Aldehüüd kui tugev redutseerija sadestab lahusest metallilise hõbeda: R 2 [Ag(N 3 ) 2 ] 2 Ag R N N 3 õbepeeglireaktsioon on oluline ka redutseerivate sahhariidide (nt glükoos) määramisel. Ka fruktoos (ketoos) tekitab katseklaasi seintele hõbepeegli, sest aluselistes tingimustes muundub ta glükoosiks. õbepeegli tekkimiseks peab katseklaas olema puhas, rasvad ja mustus takistavad hõbedakihi tekkimsit klaasile. 18
19 8. KARBKSÜÜLÜENDID 8.1 Karboksüülhapete tugevuse võrdlemine omavahel ja teiste hapetega Etanool ja fenool on nii nõrgad happed, et nende kontsentreeritud lahused indikaatorpaberi värvi esialgselt ei muuda. Erinevalt etanoolist, mis reageerib ainult metallilise naatriumiga, reageerib fenool ka Na lahusega. Etaanhape (äädikhape) muudab indikaatorpaberi värvust vähe, etaandihape (oblikhape) rohkem ja vesinikkloriidhape annab tugevalt happelise keskkonna. 8.2 Karboksüülhapete soolade saamine ja lagundamine Karboksüülhapped on nõrgad happed, kuid Na-ga reageerides annavad nad siiski vastavad Na-soolad. RC Na RCNa 2 Need soolad lahustuvad vees hästi, sest on ioonse sidemega ühendid. Lisades mineraalhapet ( 2 S 4 ), tõrjub viimane karboksüülhapped nende sooladest välja: 2 RCNa 2 S 4 2 RC Na 2 S Estri tekkimine rgaanilised happed reageerivad etanooliga, moodustades estreid. Reaktsiooni katalüüsivad tugevad mineraalhapped (Cl, 2 S 4 ): C 3 C C 2 5 C 3 CC Lenduvad (väikese molekulmassiga) estrid on meeldiva puuviljalõhnaga. 8.4 Estri hüdrolüüs Leelise toimel ester hüdrolüüsub, andes karboksüülhappe soola ja alkoholi: R1 R2 Na R1 Na R2 C 3 CC 2 5 Na C 3 CNa C 3 C 2 etüületanaat naatriumetanaat 19
20 Tekkinud alkohol oksüdeerub kroomsegu toimel vastavaks karboksüülhappeks, kusjuures Cr(VI) oranž värvus muutub Cr(III) roheliseks värvuseks: 3 C 3 C 2 4 Cr S 4 3 C 3 C 2 Cr 2 (S 4 ) Fenoolftaleiini saamine Ftaalhappe anhüdriid astub kondensatsioonireaktsiooni fenoolidega, moodustades trifenüülmetaani derivaate. Sellise kondensatsiooniga kaasneb vee molekuli moodustumine anhüdriidi ühe karbonüülse hapniku ja kahe fenooli molekuli benseenituuma liikuva vesiniku arvel. See veemolekul seotakse konts. 2 S 4 poolt. Fenoolist moodustub fenoolftaleiin järgmiselt: 2 k. 2 S 4-2 Fenoolftaleiin hüdrolüüsub aluselises keskkonnas kergelt, moodustuv anioon annab lahusele intensiivse vaarikapunase värvuse. Leelise liig viib värvitu kolmelaengulise aniooni moodustumiseni: kiire p ~ 8 aeglane p > 11 fenoolftaleiin (värvitu) fenoolftaleiin (punane) fenoolftaleiin (värvitu) 8.6 Fluorestseiini saamine Resortsiini puhul toimub fenooliga analoogne kondensatsioon (vt 8.5). Eraldub aga veel teine molekul vett resortsiini hüdroksüülrühmade arvelt ning moodustub fluorestseiin (ehk resortsiinftaleiin): 2 k. 2 S
21 Fluorestseiin annab leelise lahuses intensiivse fluorestsentsi, mis on märgatav isegi suurel lahjendusel (1 : ). 9. DESTILLATSIN Destillatsiooni puhul kuumutatakse eraldatav segu keemiseni, tekkivad aurud juhitakse jahutisse, kondenseeritakse ja kogutakse destillaadina. 9.1 Segude eraldamine, keemistemperatuuri määramine ja ainete puhastamine lihtdestillatsiooni abil rgaaniliste ainete eraldamine destillatsioonil põhineb üksikühendite keemistemperatuuride erinevusel. Kui segu komponentide keemistemperatuurid erinevad vähe (vähem kui 50 C), ei ole neid lihtdestillatsioonil võimalik täielikult eraldada, kuigi ka sel juhul on destillaat rikastunud kergemini keeva komponendiga. Destillatsiooni käigus väheneb madalamal temperatuuril keeva komponendi kogus eraldatavas segus pidevalt. Termomeeter oluline on termomeetri asend aparatuuris (elavhõbeda- reservuaar peab paiknema mm madalamal destillatsioonikolvi külgtorust), mis tagab täpsema keemistemperatuuri registreerimise. Liebigi jahuti eraldatav segu jahutusvesi välja jahutusvesi sisse Joonis 1. Lihtdestillatsiooni aparatuur destillaat 21
22 Lihtdestillatsioon viiakse tavaliselt läbi järgnevalt: Destillatsioonikolb täidetakse eraldatava seguga, täitmisaste ei tohi ületada 2/3 kolvi mahust. Segusse lisatakse poorne tellisetükike (või kapillaari) tagamaks segu ühtlast keemist (see aitab ära hoida vedeliku ülekuumenemist ja vähendab vedeliku jahutisse paiskumise ohtu). Segu kuumutatakse aeglaselt keemiseni elektrilise kolvisoojendajaga ja reguleeritakse nii, et destillatsiooni kiirus oleks umbes 20 tilka minutis (destillatsioon peab toimuma piisavalt aeglaselt, et kõik aurud jõuaks jahutis kondenseeruda paljud orgaanilised ained on tuleohtlikud ning nende aurud võivad aparatuurist välja sattudes süttida). Mitmekomponentse segu eraldamine koosneb erinevatest etappidest, mida illustreerib joonis 2. Joonisel on kujutatud kolmekomponentse (ained A, B ja C) segu eraldamise kuus etappi: 1. Segu soojeneb kolvis, temperatuur (termomeetri näit) tõuseb pidevalt. Destillaat hakkab jahutist vastuvõtjasse (nt. kolbi) tilkuma. Üles märgitakse esimese tilga ilmumise aeg (võimaldab hinnata, kas destilleeritav segu sisaldab kergesti lenduvaid komponente). Termomeetri näitu tuleb pidevalt jälgida, et registreerida hetk, mil temperatuur enam ei tõuse. 2. Temperatuur stabiliseerub, vastuvõtja tuleb asendada uuega (vahetada kolb) ja koguda kõik tilgad, mis antud temperatuuril kondenseeruvad (temperatuur võib selles etapis kõikuda pikema aja jooksul vaid 2..3 kraadi). Selles etapis kogutud destillaat on peamiselt komponent A segus madalaima keemistemperatuuriga aine. Temperatuur (või temperatuuride vahemik tihti pole võimalik täpselt piiritleda), mille juures destillaat koguti, on aine A keemistemperatuur. 3. Temperatuur hakkab uuesti tõusma, vastuvõtja tuleb asendada uuega, sest selles etapis ei kondenseeru enam puhas aine. 4. Temperatuur stabiliseerub, vastuvõtja tuleb asendada uuega ja koguda kõik tilgad, mis antud temperatuuril kondenseeruvad. Selles etapis kogutud destillaat on peamiselt komponent B allesjäänud segus madalaima keemistemperatuuriga aine. 5. Temperatuur hakkab uuesti tõusma, vastuvõtja tuleb asendada uuega, sest selles etapis ei kondenseeru enam puhas aine. 6. Temperatuur stabiliseerub, vastuvõtja tuleb asendada uuega ja koguda kõik tilgad, mis antud temperatuuril kondenseeruvad. Selles etapis kogutud destillaat on peamiselt komponent C algses segus kõrgeima keemistemperatuuriga aine (siin ei arvestata lisandeid, mis võivad olla veelgi kõrgema keemistemperatuuriga). 22
23 t C A B C aeg Joonis 2. Kolmekomponentse (ained A, B ja C) segu eraldamisel esinevad etapid (1..6) Seega saadakse antud olukorras puhtad (või enam-vähem puhtad sõltub keemistemperatuuride erinevusest) fraktsioonid etappidel 2, 4, 6 ja ebapuhtad fraktsioonid etappidel 3, 5. Esimesel etapil kogutud fraktsioon on puhas (aine A) juhul, kui eraldatav segu ei sisalda ainest A kergemini lenduvaid (madalamal temperatuuril keevaid) lisandeid. Kõik kogutud fraktsioonid (1..6) tuleks säilitada seni, kuni on kindel, et soovitud komponent on destillatsiooni käigus korralikult eraldatud (vastasel juhul ei ole pärast, halva eralduse korral, enam võimalik kogu vajalikku ainet kätte saada). Kolbi ei tohi täiesti kuivaks aurutada (kolvisoojendada tuleb eemaldada, kui kolvis on veel väike kogus destilleeritavat ainet), sest aurutusjäägis võivad sisalduda plahvatusohtlikud peroksiidid. Ka tõuseb tühja kolvi kuumutamisel temperatuur kiiresti, mistõttu võivad süttida kolvis olevad tuleohtlike ainete aurud. Destillatsiooniaparatuuri kokkupanemisel tuleb jälgida, et kõik lihvid ja ühenduskohad oleks õhukindlad. Aparatuurist välja pääsevad aurud võivad süttida või olla mürgised. Ka ei tohi kunagi kuumutada suletud süsteemi jälgida, et destillatsiooniaparatuur on õigesti konstrueeritud (vt. joonis 1). Keemistemperatuuri määramine lihtdestillatsiooni abil Lihtdestillatsiooni abil saab hästi määrata vedelike keemistemperatuure, see lihtsustab ainete identifitseerimist. Tavaliselt määratakse keemistemperatuurid termomeetriga destillatsiooni käigus nii, nagu kirjeldatud punktis 1.1. Mõõdetakse aine aurude temperatuuri aurude temperatuur ühtib destillatsiooniseadmes keeva vedeliku temperatuuriga. Termomeetri asetamisel keevasse vedelikku võib saada mõnevõrra suurema näidu, sest vedelik võib olla ülekuumenenud või sisaldada lisandeid. 23
24 Ainete puhastamine destillatsiooni abil Destilleerimist kasutatakse vedelike puhastamiseks mittelenduvatest või vähelenduvatest lisandites, näiteks destilleeritud vee saamine looduslikust veest. Ainete puhastamist destilleerimise abil on otstarbekas rakendada järgmistel juhtudel: Puhastatav aine on toatemperatuuril vedelas olekus. Vedelik on suhteliselt puhas (mitte üle 10% lisandeid). Vedelikus sisalduvad lisandid on mittelenduvad (näiteks tahked osakesed) või vähelenduvad. Lisandina esineva aine (või ainete) keemistemperatuur erineb puhastatava vedeliku keemistemperatuurist vähemalt 50 C võrra. 10. LUMINESTSENTS Paljude põlemisreaktsioonidga kaasneb valguskiirguse eraldumine soojuslik valguskiirgus. Mõnede reaktsioonide puhul eraldub valgust aga ka toatemperatuuril mittesoojuslik valguskiirgus ehk luminestsents. Kemoluminestsents keemilises reaktsioonis tekkiv mittesoojuslik valguskiirgus. Näiteks luminooli oksüdeerumine. o Bioluminestsents elusorganismides toimuv kemoluminestsents. Näiteks jaanimardika (Lampyris noctiluca) poolt toodetav rohekas valgus (tekib orgaanilise aine lutsiferiini reageerimisel ensüüm lutsiferaasi juuresolekul hapnikuga). Fotoluminestsents valguse või ultraviolettkiirguse toimel tekkiv luminestsents. o Fluorestsents aine võime valgustamisel lühikest aega helenduda. Näiteks klorofülli või fluorestseiini helendumine valguse käes. o Fosforestsents aine pikaajaline helendumine pärast kiiritust või ergastust. Triboluminestsents aine helendumine hõõrdumisel või purunemisel (mehhaaniline energia kandub üle molekulidele). Näiteks kahe kvartsitüki teineteise vastu hõõrumisel tekkivad valgussähvatused Kemoluminestsents luminooli oksüdeerumine Luminool muundub aluselises keskkonnas resonants-stabiliseeritud aniooniks (1), mis oksüdeerub vesinikperoksiidi toimel ergastatud dikarboksülaatiooniks (2). Dikarboksülaatioon läheb kõrgema energiaga olekust üle madalama energiaga olekusse (3) ja kiirgab selle lisaenergia arvel valgust (hν). 24
25 Vesilahustes katalüüsivad luminooli oksüdatsioonireaktsiooni mitmed metalliioonid (näiteks raud(ii)ioonid ja vask(ii)ioonid). Seetõttu kasutatakse luminooli kriminalistikas kuriteopaigalt verejälgede avastamiseks hemoglobiinis sisalduv raud katalüüsib luminooli oksüdeerumisreaktsiooni (päevavalguses nähtamatud verejäljed muutuvad vastava lahuse pealepealepihustamisel pimedas helendavaks). N 2 N 2 N 2 N N - N N 2 2 N N luminool 1 N 2 * N N 2 - hv
26 11. KRISTALSE RGAANILISE AINE SÜNTEES, PUASTAMINE JA UURIMINE 11.1 Dibensalatsetooni süntees aldoolkondensatsioon (Claisen-Schmidt i kondensatsioon) 2 Na C C 3 bensaldehüüd atsetoon dibensalatsetoon 1,5-difenüül-1,4-pentadieen-3-oon Dibensalatsetoon (C ) ei ole mürgine (väikestes kogustes) ja kasutatakse laialdaselt päikesekreemide koostisainena. Kondensatsioonireaktsioon kujutab endast niisugust liitumist oksoühendiga, kus polaarseks reagendiks on tavaliselt oksoühend ise ja ühe karbonüülse kaksiksideme katkemisel vabanenud valentsid küllastatakse teise samasuguse molekuli fragmentidega. Tavaline liitumisreaktsioon. Aldoolkondensatsiooniks nimetatakse kondensatsiooni, kui reaktsioon lõpeb hüdroküaldehüüdi või -ketooni moodustumisega. R5 R4 R3 R2 R1 - R5 R4 R3 R2 R1 R4 R5 R2 R Aldoolkondensatsiooni katalüüsivad tavaliselt alused, mõnedel juhtudel on aga võimalik katalüsaatorina kasutada ka happeid. Klassikaline aldoolkondensatsioon toimub tavaliselt kahe ühesuguse aldehüüdi molekuli vahel, kahe ühesuguse ketooni molekuli vahel või ühe aldehüüdi ja ühe ketooni molekuli vahel. Kokku on viis erinevat võimalust: Kaks ühesugust aldehüüdi molekuli reaktsiooni tasakaal on nihkunud paremale. Kaks ühesugust ketooni molekuli reaktsiooni tasakaal on tavaliselt nihkunud vasakule. Kaks erinevat aldehüüdi molekuli Claisen-Schmidt i kondensatsioon. Kaks erinevat ketooni molekuli Claisen-Schmidt i kondensatsioon. Üks aldehüüdi ja üks ketooni molekul Claisen-Schmidt i kondensatsioon. 26
27 Kahe erineva molekuli vahel toimuvat aldoolkondensatsiooni nimetatakse ka Claisen-Schmidt i kondensatsiooniks. Sõltuvalt olukorrast võib reaktsiooni tasakaal olla nihkunud paremale või vasakule. Ülaltoodud skeemi järgi võib lahti kirjutada ka dibensalatsetooni sünteesireaktsiooni: C 3 C 3 C Ainete puhastamine ümberkristallimise abil Tihti on laboris sünteesitud (või eraldatud) ained ebapuhtad ja sisaldavad suuremal või vähemal määral lisaneid. Kristalsete orgaaniliste aine puhastamiseks kasutatakse tihti ümberkristallimist. See meetod põhineb ainete erineval lahustuvusel ja lahustuvuse temperatuurist sõltuvusel (vt joonis 3). Ümberkristallimine on efektiivne, kui puhastatava aine lahustuvus kasvab temperatuuri tõstmisel oluliselt ja lisandeid on vähe. Ümberkristallimise puhul läheb alati teatud osa puhastatavast ainest kaduma. Et võimalikult palju puhastatavat ainet säiluks, tuleb leida sobivate omadustega lahusti: puhastatav aine lahustub kuumas lahustis, puhastatav aine on lahustumatu või nõrgalt lahustuv külmas lahustis, lisandid on kas täielikult lahustuvad külmas lahustis või täielikult mittelahustuvad kuumas lahustis. 27
28 filtraat lisandid jahtumine filtrimine 2 Puhastatav aine ja lisandid lahustuvad kuumas lahustis. 3 Puhastatav aine kristallub külmas lahustis, lisandid lahustuvad külmas lahustis. 4 Puhastatud (ümberkristallitud) aine kristallid. 1 Lisandeid sisaldav (puhastatav) kristalne aine ei lahustu külmas lahustis. sade (lisandid) filtrimine filtraat jahtumine filtrimine 2a Puhastatav aine lahustub kuumas lahustis, lisandid ei lahustu. 3a Puhastatav aine lahustub kuumas lahustis. 4a Puhastatav aine kristallub külmas lahustis. Joonis 3. Ümberkristallimise kaks stsenaariumit: lisandid lahustuvad nii kuumas kui ka külmas lahustis (1, 2, 3, 4); lisandid ei lahustu kuumas ega külmas lahustis (1, 2a, 3a, 4a, 4). Kui puhastatav aine sisaldab mitut sorti lisandeid: ühed lahustuvad külmas lahustis ja teised ei lahustu külmas ega kuumas lahustis, siis tuleb ümberkristallimiseks kasutada joonis 3 põhjal kolmandat stsenaariumit 1, 2, 2a, 3a, 3, 4. Puhastatav aine paigutatakse Erlenmeyeri kolbi, lisatakse väike kogus lahustit ja kuumutatakse segu keemiseni. Kui kogu aine mõneminutilise keetmise jooksul ei lahustu, lisatakse aeglaselt lahustit (hoides segu nõrgal keemisel) aine täieliku lahustumiseni. Lahustumatute lisandite esinemisel (nt rooste, paberitükid jne) eemaldatakse need segu kuumalt kurdfiltriga filtrides. Lahusel lastakse jahtuda ja kogutakse kristallid Büchneri filtri abil (lahustuvad lisandid jäävad filtraati). Kristallidele jäänud lahusel lastakse ära aurata. 28
29 Sobiva lahusti valimine Ümberkristallimiseks sobiva lahusti valimine võib teatud juhtudel olla üsna keeruline. Kõige lihtsam on lahusti valimisel juhinduda vastavatest käsiraamatutest. Mõnede lahustite omadused on toodud tabelis 3. Lahustil peavad olema kolm eespool mainitud omadust. Lahusti ei tohi puhastatava ainega reageerida. Lahusti ei tohiks olla väikese lenduvusega (jääb peale ümberkristallimist puhastatava aine külge). Seetõttu kasutatakse harva lahusteid, mille keemistemperatuur ületab 100 C. Lahusti keemistemperatuur ei tohiks olla alla 50 C, kuna lahustuvus keemistemperatuuril peab olema märgatavalt kõrgem lahustuvusest toatemperatuuril (paarikümnekraadine muutus ei mõjuta lahustuvust tavaliselt väga tugevalt). ästi ei saa kasutada lahustit, mille keemistemperatuur on kõrgem puhastatava aine sulamistemperatuurist, sest see viib tõenäoliselt õli (mitte kristallide) tekkeni. Seega tuleks puhastatava aine lahustuvust kontrollida lenduvates inertsetes lahustites, mille keemistemperatuurid jäävad vahemikku C. Lahustuvuse testimiseks asetatakse 0,10 g puhastatavat ainet katseklaasi, lisatakse 3 ml lahustit ja loksutatakse tugevalt. Kui aine lahustub, on lahusti ümberkristallimiseks halb (tuleb proovida uue lahustiga). Kui aine on lahustumatu või nõrgalt lahustuv, kuumutatakse segu ettevaatlikult keemiseni. Kui aine ikka ei lahustu (või lahustub halvasti), tuleb proovida teist lahustit. Kui märgatav osa ainest lahustub, jahutatakse kasteklaas külmal vesivannil ja jälgitakse kristallide teket. Kristallide mitteilmumise korral hõõrutakse katseklaasi põhja seestpoolt klaaspulgaga. Kristallide tekkimine näitab, et tegemist on sobiva lahustiga (vastasel juhul tuleb proovida uue lahustiga). Kui sobivat lahustit leida ei õnnestu, võib proovida ümberkristallimist lahustite segus. Sellisel juhul kasutatakse kahe lahusti segu, millest ühes peab puhastatav aine olema üsna lahustuv ja teises praktiliselt lahustumatu. Tabel 3. Mõnede lahustite omadused. Lahusti Keemistemp. ( C) Kirjeldus Vesi 100 Sobiv polaarsete ühendite puhul, raske kristallidelt eemaldada Etanool 78 Väga tavaline, polaarne, kerge kristallidelt eemaldada, võib reageerida hapete ja estritega 2-butanoon 80 Keskmise polaarsusega, kerge kristallidelt eemaldada Tolueen 110 Vähepolaarne, raske kristallidelt eemaldada, suhteliselt inertne Ligroiin/ petrooleeter 60-90/30-60 Mittepolaarne, inertne 29
30 11.3 Ainete sulamistemperatuuride määramine Aine sulamistemperatuur on temperatuur, mille juures aine tahke ja vedel faas on normaalrõhul tasakaalus. Sulamistemperatuurist madalamatel temperatuuridel on aine tahkes olekus, sellest kõrgematel temperatuuridel aga vedelas olekus. Sulamistemperatuur iseloomustab hästi ainet ja tema puhtusastet. Üleminek tahke ja vedela faasi vahel on järsk, mistõttu võib sulamistemperatuure määrata 0,1 C täpsusega. Nii täpne määramine eeldab aga keeruka aparatuuri olemasolu. Lihtsate vahenditega saab sulamistemperatuuri määrata kapillaaris. Sellisel juhul saadakse temperatuuride (mõnekraadine) vahemik temperatuur mille juures aine sulama hakkab ning temperatuur, mille juures kogu aine on sulanud. Lisandid suurendavad tavaliselt sulamistemperatuuri vahemikku ja nihutavad seda madalamate temperatuuride suunas (puhtal ainel on võrreldes lisandeid sisaldavaga väiksem sulamistemperatuuri vahemik ja selle arvulised väärtused on kõrgemad). Tundmatu aine puhul määratakse sulamistemperatuur kaks korda: 1. kiirelt, et teada saada aine ligikaudne sulamistemperatuur; 2. oodatava sulamistemperatuuri piirkonnas aeglaselt (1-2 C minutis), et sulamistemperatuur täpsemalt fikseerida. Saadud andmeid võrreldakse käsiraamatus esitatutega. Dibensalatsetooni sulamistemperatuur on C Ainete spektrofotomeetriline uurimine Spektrofotomeetri abil on võimalik uurida, kuidas neelab uuritav aine elektromagnetkiirgust erinevatel lainepikkustel (aine neeldumisspekter; vt joonis 4). Neeldumisspekter võimaldab aineid identifitseerida ja hinnata nende puhtusastet (erinevatel ainetel on erinev neeldumisspekter). Lisaks ainete identifitseerimisele võimaldab neeldumisspekter määrata ka ainete kontsentratsioone. Seose aine kontsentratsiooni ja absorptsiooni (kindlal lainepikkusel) vahel annab Lambert-Beeri seadus: A λ = c ε λ b ε λ [l mol -1 cm -1 ] analüüdi molaarne neeldumistegur (ehk ekstinktsioonitegur) mingil kindlal lainepikkusel λ. Ainete molaarsed ekstinktsioonitegurid on esitatud käsiraamatutes. A λ absorptsioon (ehk neelduvus ehk optiline tihedus) mingil kindlal lainepikkusel λ. c [mol l -1 ] analüüdi molaarne kontsentratsioon. b [cm] lahusekihi paksus. 30
31 Absorptsioon Lainepikkus (nm) Joonis 4. Dibensalatsetooni (lahustatud etanoolis) neeldumisspekter (max 330 nm). Tabel 4. Ultraviolett kiirguste lainepikkusi Lühend Lainepikkus (nm) UVA UVB UVC Tabel 5. Nähtava valguse komponenentide lainepikkused Värv Lainepikkus (nm) violetne indigo sinine Sinine/roheline roheline kollane oraanž punane
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
Vektorid II. Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale
 Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
3. Solvendiefektide mõju ainete omadustele ja keemilistele protsessidele. 3.1 Solvendiefektid happe-aluse protsessidele. Tasakaal ja kiirus
 3. olvendiefektide mõju ainete omadustele ja keemilistele protsessidele Põhiallikas: Tasakaal ja kiirus Lahusti mõju tasakaalule ilmneb seeläbi, et erinevad lahustid solvateerivad erineva intensiivsusega
3. olvendiefektide mõju ainete omadustele ja keemilistele protsessidele Põhiallikas: Tasakaal ja kiirus Lahusti mõju tasakaalule ilmneb seeläbi, et erinevad lahustid solvateerivad erineva intensiivsusega
Lahused ja lahustumisprotsess konserveerimises
 Lahused ja lahustumisprotsess konserveerimises Lektor: Heige Peets Ennistuskoda Kanut, 6 44 25 63 esemed@kanut.ee Tallinn-Tartu 2004 Loengu eesmärgiks on anda ülevaade ja lühike selgitus kõige üldisematest
Lahused ja lahustumisprotsess konserveerimises Lektor: Heige Peets Ennistuskoda Kanut, 6 44 25 63 esemed@kanut.ee Tallinn-Tartu 2004 Loengu eesmärgiks on anda ülevaade ja lühike selgitus kõige üldisematest
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
ETTEVALMISTUS KEEMIAOLÜMPIAADIKS II
 ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
ORGAANILINE KEEMIA. Lühikonspekt gümnaasiumile. Koostaja: Kert Martma
 ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
Graafiteooria üldmõisteid. Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid
 Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat
 Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
ORGAANILINE KEEMIA. Lühikonspekt gümnaasiumile. Koostaja: Kert Martma
 ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Sisukord Sissejuhatus orgaanilisse keemiasse Alkaanid Halogeeniühendid Alkoholid Amiinid Küllastamata ühendid Areenid
ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Sisukord Sissejuhatus orgaanilisse keemiasse Alkaanid Halogeeniühendid Alkoholid Amiinid Küllastamata ühendid Areenid
2.2.1 Geomeetriline interpretatsioon
 2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
( ) ( ) 2008/2009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
Funktsiooni diferentsiaal
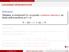
 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
SÜSIVESINIKUD. Kaido Viht
 SÜSIVSINIKUD Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2016 Süsivesinike struktuurid Käesolevas materjalis selgitame mõningaid süsivesinikele iseloomulikke reaktsioone. Süsivesinikud, nagu
SÜSIVSINIKUD Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2016 Süsivesinike struktuurid Käesolevas materjalis selgitame mõningaid süsivesinikele iseloomulikke reaktsioone. Süsivesinikud, nagu
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
Keemiliste elementide perioodilisustabel
 Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Molekulid ei esine üksikuna vaid suurearvuliste kogumitena.
 2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised
KARBOKSÜÜLHAPPED. Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COOH). Üldvalem R-COOH või HOOC-R
 KARBOKSÜÜLAPPED Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COO). Üldvalem R-COO või OOC-R Karboksüülhapete nimetused tuletatakse süsivesinike nimetustest ja
KARBOKSÜÜLAPPED Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COO). Üldvalem R-COO või OOC-R Karboksüülhapete nimetused tuletatakse süsivesinike nimetustest ja
p A...p D - gaasiliste ainete A...D osarõhud, atm K p ja K c vahel kehtib seos
 LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
HAPNIKUTARBE INHIBEERIMISE TEST
 HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks
 4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
ORGAANILINE KEEMIA I osa
 ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
Lokaalsed ekstreemumid
 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
ORGAANILINE KEEMIA ANDRES TALVARI
 ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
28. Sirgvoolu, solenoidi ja toroidi magnetinduktsiooni arvutamine koguvooluseaduse abil.
 8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
Kehade soojendamisel või jahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks.
 KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
HSM TT 1578 EST 6720 611 954 EE (04.08) RBLV 4682-00.1/G
 HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
HSM TT 1578 EST 682-00.1/G 6720 611 95 EE (0.08) RBLV Sisukord Sisukord Ohutustehnika alased nõuanded 3 Sümbolite selgitused 3 1. Seadme andmed 1. 1. Tarnekomplekt 1. 2. Tehnilised andmed 1. 3. Tarvikud
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
Vektoralgebra seisukohalt võib ka selle võrduse kirja panna skalaarkorrutise
 Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass
 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
5. a) ρ (g/cm 3 ) = 0,119 = 11,9% 12% 2 p
 201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 2016
 Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Keskkonnaefektidest superhapete ja superalusteni
 Keskkonnaefektidest superhapete ja superalusteni Ilmar Koppel Tartu Ülikool Lihtne S 1 tüüpi solvolüüs K n (CH 3 ) 3 C-Cl: + (HOR) n (CH 3 ) 3 C-Cl: (HOR) n k 0 k 1 produktid produktid J.B. Conant,. Semjonov
Keskkonnaefektidest superhapete ja superalusteni Ilmar Koppel Tartu Ülikool Lihtne S 1 tüüpi solvolüüs K n (CH 3 ) 3 C-Cl: + (HOR) n (CH 3 ) 3 C-Cl: (HOR) n k 0 k 1 produktid produktid J.B. Conant,. Semjonov
Andmeanalüüs molekulaarbioloogias
 Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
Sissejuhatus mehhatroonikasse MHK0120
 Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
Sissejuhatus mehhatroonikasse MHK0120 2. nädala loeng Raavo Josepson raavo.josepson@ttu.ee Loenguslaidid Materjalid D. Halliday,R. Resnick, J. Walker. Füüsika põhikursus : õpik kõrgkoolile I köide. Eesti
TMR praktikum. Teooria: Aatomituuma varjestatus
 TMR praktikum Praktikum toimub 2-l praktikumipäeval ning koosneb kahest tööst. Tööde eesmärk on ühendite TMR spektrite interpreteerimine ning ainete identifitseerimine nii struktuurvalemi kui brutovalemi
TMR praktikum Praktikum toimub 2-l praktikumipäeval ning koosneb kahest tööst. Tööde eesmärk on ühendite TMR spektrite interpreteerimine ning ainete identifitseerimine nii struktuurvalemi kui brutovalemi
CaCO 3(s) --> CaO(s) + CO 2(g) H = kj. Näide
 3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
AATOMI EHITUS KEEMILINE SIDE
 TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut
 Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
TÄIENDAVAID TEEMASID KOOLIKEEMIALE III
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika
 Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
PLASTSED DEFORMATSIOONID
 PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
Fotosüntees. Peatükk 3.
 Fotosüntees. Peatükk 3. Fotosünteesiprotsess on keerulisem kui lihtne üldvõrrand, sest valguse energiat ei saa otse H 2 O seose-elektronidele anda ja neid otse CO 2 -le üle kanda. Seetõttu vaadeldakse
Fotosüntees. Peatükk 3. Fotosünteesiprotsess on keerulisem kui lihtne üldvõrrand, sest valguse energiat ei saa otse H 2 O seose-elektronidele anda ja neid otse CO 2 -le üle kanda. Seetõttu vaadeldakse
1998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus
 Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus 1. Haljala valla metsa pindala Haljala valla üldpindala oli Maa-Ameti
Lisa 2 ÜLEVAADE HALJALA VALLA METSADEST Koostanud veebruar 2008 Margarete Merenäkk ja Mati Valgepea, Metsakaitse- ja Metsauuenduskeskus 1. Haljala valla metsa pindala Haljala valla üldpindala oli Maa-Ameti
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
b) Täpne arvutus (aktiivsete kontsentratsioonide kaudu) ph arvutused I tugevad happed ja alused
 ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
Jätkusuutlikud isolatsioonilahendused. U-arvude koondtabel. VÄLISSEIN - COLUMBIA TÄISVALATUD ÕÕNESPLOKK 190 mm + SOOJUSTUS + KROHV
 U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
4. KEHADE VASTASTIKMÕJUD. JÕUD
 4. KEHADE VASTASTIKMÕJUD. JÕUD Arvatavasti oled sa oma elus kogenud, et kõik mõjud on vastastikused. Teiste sõnadega: igale mõjule on olemas vastumõju. Ega füüsikaski teisiti ole. Füüsikas on kehade vastastikuse
4. KEHADE VASTASTIKMÕJUD. JÕUD Arvatavasti oled sa oma elus kogenud, et kõik mõjud on vastastikused. Teiste sõnadega: igale mõjule on olemas vastumõju. Ega füüsikaski teisiti ole. Füüsikas on kehade vastastikuse
PÕLEVAINETE OMADUSED. Andres Talvari
 PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
Ülesanne 4.1. Õhukese raudbetoonist gravitatsioontugiseina arvutus
 Ülesanne 4.1. Õhukese raudbetoonist gravitatsioontugiseina arvutus Antud: Õhuke raudbetoonist gravitatsioontugisein maapinna kõrguste vahega h = 4,5 m ja taldmiku sügavusega d = 1,5 m. Maapinnal tugiseina
Ülesanne 4.1. Õhukese raudbetoonist gravitatsioontugiseina arvutus Antud: Õhuke raudbetoonist gravitatsioontugisein maapinna kõrguste vahega h = 4,5 m ja taldmiku sügavusega d = 1,5 m. Maapinnal tugiseina
Kontekstivabad keeled
 Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
Ecophon Line LED. Süsteemi info. Mõõdud, mm 1200x x x600 T24 Paksus (t) M329, M330, M331. Paigaldusjoonis M397 M397
 Ecophon Line LED Ecophon Line on täisintegreeritud süvistatud valgusti. Kokkusobiv erinevate Focus-laesüsteemidega. Valgusti, mida sobib kasutada erinevates ruumides: avatud planeeringuga kontorites; vahekäigus
Ecophon Line LED Ecophon Line on täisintegreeritud süvistatud valgusti. Kokkusobiv erinevate Focus-laesüsteemidega. Valgusti, mida sobib kasutada erinevates ruumides: avatud planeeringuga kontorites; vahekäigus
HULGATEOORIA ELEMENTE
 HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
Joonis 1. Teist järku aperioodilise lüli ülekandefunktsiooni saab teisendada võnkelüli ülekandefunktsiooni kujul, kui
 Ülesnded j lhendused utomtjuhtimisest Ülesnne. Süsteem oosneb hest jdmisi ühendtud erioodilisest lülist, mille jonstndid on 0,08 j 0,5 ning õimendustegurid stlt 0 j 50. Leid süsteemi summrne ülendefuntsioon.
Ülesnded j lhendused utomtjuhtimisest Ülesnne. Süsteem oosneb hest jdmisi ühendtud erioodilisest lülist, mille jonstndid on 0,08 j 0,5 ning õimendustegurid stlt 0 j 50. Leid süsteemi summrne ülendefuntsioon.
RF võimendite parameetrid
 RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
RF võimendite parameetrid Raadiosageduslike võimendite võimendavaks elemendiks kasutatakse põhiliselt bipolaarvõi väljatransistori. Paraku on transistori võimendus sagedusest sõltuv, transistor on mittelineaarne
Biomakromolekulid: struktuurist omadusteni. Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018
 Biomakromolekulid: struktuurist omadusteni Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018 Sissejuhatus 2 Biokeemia mõõtkava mm mm Inimese embrüo (6. nädal): 4 mm Suurem amööb: 0.8 mm Inimese punaverelible:
Biomakromolekulid: struktuurist omadusteni Darja Lavõgina Keemia õppesessioon 15. jaanuar 2018 Sissejuhatus 2 Biokeemia mõõtkava mm mm Inimese embrüo (6. nädal): 4 mm Suurem amööb: 0.8 mm Inimese punaverelible:
FUNKTSIONAALSED RÜHMAD I osa. Kaido Viht
 FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
Vedelikud ja tahkised. Aine olekud. Molekulidevahelised jõud E P
 Molekulidevahelised jõud Vedelike struktuur ja omadused Viskoossus ja pindpinevus Vedelike vastasmõju tahkisega Tahkised Kristalli struktuur Metallid Sulamid Ioonilised tahkised Molekulaarsed tahkised
Molekulidevahelised jõud Vedelike struktuur ja omadused Viskoossus ja pindpinevus Vedelike vastasmõju tahkisega Tahkised Kristalli struktuur Metallid Sulamid Ioonilised tahkised Molekulaarsed tahkised
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi
 Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Fotomeetria. Laineoptika
 Fotomeetria 1. Päikese ja Maa vaheline kaugus on 1,5 10 8 km. Kui kaua tuleb valgus Päikeselt Maale? (Vastus: 500 s) 2. Fizeau ajaloolises katses valguse kiiruse määramiseks oli 720 hambaga hammasratta
Fotomeetria 1. Päikese ja Maa vaheline kaugus on 1,5 10 8 km. Kui kaua tuleb valgus Päikeselt Maale? (Vastus: 500 s) 2. Fizeau ajaloolises katses valguse kiiruse määramiseks oli 720 hambaga hammasratta
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Smith i diagramm. Peegeldustegur
 Smith i diagramm Smith i diagrammiks nimetatakse graafilist abivahendit/meetodit põhiliselt sobitusküsimuste lahendamiseks. Selle võttis 1939. aastal kasutusele Philip H. Smith, kes töötas tol ajal ettevõttes
Smith i diagramm Smith i diagrammiks nimetatakse graafilist abivahendit/meetodit põhiliselt sobitusküsimuste lahendamiseks. Selle võttis 1939. aastal kasutusele Philip H. Smith, kes töötas tol ajal ettevõttes
Teaduskool. Alalisvooluringid. Koostanud Kaljo Schults
 TARTU ÜLIKOOL Teaduskool Alalisvooluringid Koostanud Kaljo Schults Tartu 2008 Eessõna Käesoleva õppevahendi kasutajana on mõeldud eelkõige täppisteaduste vastu huvi tundvaid gümnaasiumi õpilasi, kes on
TARTU ÜLIKOOL Teaduskool Alalisvooluringid Koostanud Kaljo Schults Tartu 2008 Eessõna Käesoleva õppevahendi kasutajana on mõeldud eelkõige täppisteaduste vastu huvi tundvaid gümnaasiumi õpilasi, kes on
AROMAATSUS. Kaido Viht
 ARMAATSUS Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 018 Sisukord 1. Aromaatsus ja antiaromaatsus... 4. Aromaatsus annuleenide seerias... 6 3. Aromaatsus ioonilistes tsüklites... 8 4. Aromaatsus
ARMAATSUS Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 018 Sisukord 1. Aromaatsus ja antiaromaatsus... 4. Aromaatsus annuleenide seerias... 6 3. Aromaatsus ioonilistes tsüklites... 8 4. Aromaatsus
IChO 2014, ülesanne 4
 IChO 2014, ülesanne 4 Zeise sool, K[PtCl3C2H4], oli üks esimesi metallorgaanilisi ühendeid. Kopenhaageni ülikooli professor W. C. Zeise valmistas selle ühendi lisades PtCl4-le keevas etanoolis kaaliumkloriidi
IChO 2014, ülesanne 4 Zeise sool, K[PtCl3C2H4], oli üks esimesi metallorgaanilisi ühendeid. Kopenhaageni ülikooli professor W. C. Zeise valmistas selle ühendi lisades PtCl4-le keevas etanoolis kaaliumkloriidi
LABORATOORIUMIS KASUTATAVAD VAHENDID
 Ettevalmistus keemiaolümpiaadiks I LABORATOORIUMIS KASUTATAVAD VAHENDID Õppematerjal Autor: Aksel Koorits Täiendatud: Katrin Kestav TARTU 2016 Käesolev TÜ teaduskooli õppematerjal on kaasajastatud (terminid,
Ettevalmistus keemiaolümpiaadiks I LABORATOORIUMIS KASUTATAVAD VAHENDID Õppematerjal Autor: Aksel Koorits Täiendatud: Katrin Kestav TARTU 2016 Käesolev TÜ teaduskooli õppematerjal on kaasajastatud (terminid,
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Elekter ja magnetism. Elektrostaatika käsitleb paigalasuvate laengute vastastikmõju ja asetumist
 Elekter ja magnetism Elektrilaeng, elektriväli ja elektrivälja tugevus Elektriline potentsiaalne energia, potentsiaal ja pinge Elektrivälja töö ja võimsus Magnetväli Elektromagnetiline induktsioon Elektromagnetlained,
Elekter ja magnetism Elektrilaeng, elektriväli ja elektrivälja tugevus Elektriline potentsiaalne energia, potentsiaal ja pinge Elektrivälja töö ja võimsus Magnetväli Elektromagnetiline induktsioon Elektromagnetlained,
Hübridisatsioonitehnikad ja polümeraasi ahelreaktsioon (PCR)
 Hübridisatsioonitehnikad ja polümeraasi ahelreaktsioon (PCR) Kahe erineva päritoluga komplementaarse nukleiinhappe üksikahela kokkusegamisel toimub nendevaheline hübridisatsioon, mille käigus nende nukleiinhapete
Hübridisatsioonitehnikad ja polümeraasi ahelreaktsioon (PCR) Kahe erineva päritoluga komplementaarse nukleiinhappe üksikahela kokkusegamisel toimub nendevaheline hübridisatsioon, mille käigus nende nukleiinhapete
FUNKTSIONAALSED RÜHMAD. II OSA
 TATU ÜLIKL TEADUSKL TÄIENDAVAID TEEMASID KLIKEEMIALE III FUNKTSINAALSED ÜHMAD. II SA Heiki Timotheus Õppevahend TK õpilastele Tartu 2007 Funktsionaalsed rühmad. II osa Karboksüülhappeid ja nende derivaate
TATU ÜLIKL TEADUSKL TÄIENDAVAID TEEMASID KLIKEEMIALE III FUNKTSINAALSED ÜHMAD. II SA Heiki Timotheus Õppevahend TK õpilastele Tartu 2007 Funktsionaalsed rühmad. II osa Karboksüülhappeid ja nende derivaate
Sissejuhatus. 44 th IChO Teoreetiline voor. Ametlikeesti keelne version.
 Sissejuhatus Kirjutage oma nimi ja kood igale vihiku leheküljele. Teoreeiline voor koosneb 8 ülesandest ja perioodilisustabelist, kokku 49 leheküljel. Teoreetilise vooru lahendamiseks on aega 5 tundi.
Sissejuhatus Kirjutage oma nimi ja kood igale vihiku leheküljele. Teoreeiline voor koosneb 8 ülesandest ja perioodilisustabelist, kokku 49 leheküljel. Teoreetilise vooru lahendamiseks on aega 5 tundi.
Koduseid ülesandeid IMO 2017 Eesti võistkonna kandidaatidele vol 4 lahendused
 Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
7.7 Hii-ruut test 7.7. HII-RUUT TEST 85
 7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
9 kl füüsika. Q= cm(t 2 t 1 ) või Q= cmδt Q=λ m Q=Lm. J džaul 1J= 1Nm
 9 kl füüsika Füüsikaline nähtus või suurus ja tähis Valem Ühikud Soojusõpetus Aineosake on aine kõige väiksem osake - kas aatom või molekul Potentsiaalne energia on kehadel või aineosakestel, mis teineteist
9 kl füüsika Füüsikaline nähtus või suurus ja tähis Valem Ühikud Soojusõpetus Aineosake on aine kõige väiksem osake - kas aatom või molekul Potentsiaalne energia on kehadel või aineosakestel, mis teineteist
Eessõna 7 Maa atmosfäär 11 Pilvede olemus, tekkimine ja tähtsus 16 Pilvede klassifitseerimine, süstemaatika ja omavahelised seosed 26
 SISUKORD Eessõna 7 Maa atmosfäär 11 Pilvede olemus, tekkimine ja tähtsus 16 Pilvede klassifitseerimine, süstemaatika ja omavahelised seosed 26 Pilvede süstemaatika ajalugu 27 Pilvede nimetamine ja pilvede
SISUKORD Eessõna 7 Maa atmosfäär 11 Pilvede olemus, tekkimine ja tähtsus 16 Pilvede klassifitseerimine, süstemaatika ja omavahelised seosed 26 Pilvede süstemaatika ajalugu 27 Pilvede nimetamine ja pilvede
Molekulaarfüüsika - ja termodünaamika alused
 Molekulaarfüüsika - ja termodünaamika alused Ettevalmistus kontrolltööks 1. Missugustel väidetel põhineb molekulaarkineetiline teooria? Aine koosneb molekulidest Osakesed on pidevas liikumises Osakestele
Molekulaarfüüsika - ja termodünaamika alused Ettevalmistus kontrolltööks 1. Missugustel väidetel põhineb molekulaarkineetiline teooria? Aine koosneb molekulidest Osakesed on pidevas liikumises Osakestele
8. Faasid ja agregaatolekud.
 Soojusõpetus 8a 1 8. Faasid ja agregaatolekud. 8.1. Faasi ja agregaatoleku mõisted. Faas = süsteemi homogeenne ja mehaaniliselt eraldatav osa. Keemiliselt heterogeense süsteemi näide: õli + vesi. Keemiliselt
Soojusõpetus 8a 1 8. Faasid ja agregaatolekud. 8.1. Faasi ja agregaatoleku mõisted. Faas = süsteemi homogeenne ja mehaaniliselt eraldatav osa. Keemiliselt heterogeense süsteemi näide: õli + vesi. Keemiliselt
