Čvrsto stanje osobine
|
|
|
- Ήλιόδωρος Ζαφειρόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 Fizička hemija II Doc. dr Gordana Ćirić-Marjanović Čvrsto stanje može biti kristalno ili amorfno. Čvrsto stanje osobine Kristalne čvrste supstancije generalno pokazuju oštru tačku topljenja; ispitivanja golim okom ili pomoću mikroskopa pokazuju kristale koji imaju dobro razvijene površine i karakterističan oblik. Difrakcija X-zraka pokazuje da kristalna čvrsta supstancija ima regularnu, uređenu strukturu, sastavljenu od identičnih ponavljajućih jedinica koje imaju istu orjentaciju kroz ceo kristal. Ove ponavljajuće jedinice su grupe atoma, molekula ili jona. Amorfno čvrsto stanje nema karakterističan kristalni oblik. Pri zagrevanju omekšava i topi se u širem temperaturskom opsegu. Difrakcija X-zraka pokazuje neuređenu strukturu. Staklo je amorfna čvrsta supstancija dobivena hlađenjem tečnog stanja. Najčešće se staklo dobija iz rastopljenog SiO koji sadrži različite količine metalnih oksida. Ono sadrži lance i prstenove sa Si-O vezama, a struktura je neuređena i iregularna. Polimeri (makromolekuli), supstancije čiji se molekuli sastoje od velikog broja ponavljajućih jedinica (monomera) koje su vezane kovalentnom vezom, su često amorfne čvrste supstancije, mada mogu biti i kristalni, ili delimično kristalni-delimično amorfni. U čvrstom stanju, strukturne jedinice (atomi, molekuli, joni) stoje praktično nepokretno na svojim mestima. Za razliku od njih, u tečnostima strukturne jedinice mogu da se pomeraju tako da je stepen uređenosti u tečnostima mnogo manji nego u kristalnom čvrstom stanju. Tečnosti imaju uređenost kratkog ranga, na taj način da molekuli u najbližem okruženju datog molekula teže da postignu pogodnu orjentaciju i međumolekulsko rastojanje, ali tečnosti nemaju uređenost dugog ranga, što znači da nema korelacije između orjentacija dva udaljena molekula i nema ograničenja njihovog međusobnog rastojanja. Amorfno čvrsto stanje liči na tečno stanje po tome što nema uređenost dugog ranga. Hemijske veze u čvrstom stanju Kristali se dele na jonske, kovalentne, metalne i molekulske, prema prirodi hemijske veze i međumolekulskih sila u kristalu. Jonski kristali se sastoje od pozitivnih i negativnih jona koji se drže zajedno Kulonovom privlačnom silom između suprotno naelektrisanih jona. Primeri su NaCl, MgO, CaCl, KNO 3. Metalni kristali su sastavljeni od vezanih atoma metala. Neki od valentnih elektrona su delokalizovani kroz ceo metal. Primeri su Na, Cu, Fe i različite legure. Kovalentni kristali se sastoje od beskonačne mreže atoma koji se drže zajedno kovalentnim (polarnim ili nepolarnim) vezama. Individualni molekuli nisu prisutni. Primeri su ugljenik u formi dijamanta (Slika 1) ili grafita, Si, SiO, SiC. 1
2 Slika 1. Jedinična ćelija dijamanta, kovalentnog kristala. Osenčeni atomi nalaze se unutar jedinične ćelije, a tačkasti atomi leže na površinama jedinične ćelije U dijamantu, svaki C atom vezan je sa četiri druga C atoma koja ga okružuju tetraedarski. Tako se dobija trodimenzionalna mreža koja se širi kroz ceo kristal. Silicijum ima istu strukturu. SiO ima trodimenzionalnu mrežu u kojoj je svaki Si vezan sa četiri O u tetraedarskim uglovima, a svaki O je vezan sa dva Si atoma. Kod mnogih kovalentnih kristala mreža je dvodimenzionalna. Primer je grafit. On se sastoji od slojeva heksagonalnih prstenova, u okviru sloja veze predstavljaju sredinu između jednostruke i dvostruke veze (kao kod benzena), a susedni slojevi drže se zajedno van der Waals-ovim silama. Jednodimenzione mreže formiraju kovalentni kristali BeCl (Slika ) i BeH. Be Cl Cl Be Cl Cl Be Cl Cl Be Cl Cl Be Slika. Struktura čvrstog BeCl kovalentni kristal, jednodimenzionalna mreža. Četiri Cl atoma oko svakog Be su približno tetraedarski raspoređena Primer kovalentnog kristala koji formira trodimenzionalnu mrežu su neki sintetički polimeri, npr. guma. Kovalentne veze između pojedinih lanaca povezuju ceo materijal u jedan ogromni molekul; to su umreženi polimeri; npr. pri vulkanizaciji sirovog kaučuka dodaje se sumpor, koji otvara dvostruke veze u polimernim lancima i umrežava susedne molekule (lance) vezama preko jednog ili više S atoma, ovo umrežavanje znatno povećava jačinu guma. Kod jonskih, metalnih i kovalentnih kristala ceo kristal je jedan džinovski molekul - ne možemo razlikovati pojedinačne molekule. Koordinacioni broj nekog atoma ili jona u čvrstoj supstanciji je broj najbližih suseda toga atoma ili jona. U NaCl na primer, (Slika 3.) svaki Na + okružen je sa 6 najbližih Cl - jona tako da je koordinacioni broj Na + jona 6. Kod metala koordinacioni broj je obično 8 ili 1.
3 Slika 3. a) Jedinična ćelija NaCl označena je debljim linijama b) pakovanje jona u NaCl Molekulski kristali su sastavljeni od individualnih molekula, a atomi unutar svakog molekula drže se zajedno kovalentnim vezama. Relativno slabe van der Waals-ove sile ili vodoničnr veze drže molekule zajedno u kristalu. Molekulski kristali dele se na van der Waals-ove kristale, u kojima su međumolekulska privlačenja dipol-dipol, dipol-indukovani dipol ili disperzione sile i na vodonično-vezane kristale, kod kojih su glavna međumolekulska privlačenja vodonične veze. Primeri van der Waals-ovih kristala su: Ar, CO, HgCl, SnCl 4, C 6 H 5 NO Primeri vodonično- vezanih kristala su: H O, HF, NH 3, amino kiseline. Struktura kristala Kristal je izgrađen od pravilno ponavljajuće strukturne jedinice, koja se zove strukturni motiv (ili bazis). Strukturni motiv se ponavlja u tri dimenzije dajući strukturu kristala. Strukturni motiv može biti jedan atom ili molekul, ili grupa atoma, molekula ili jona. Svaki ponavljajući motiv ima istu strukturu i istu prostornu orjentaciju kao i bilo koji drugi uočeni motiv u kristalu. Takođe, on mora imati isti stehiometrijski sastav kao i kristal. Kod NaCl, motiv se sastoji od jednog Na + jona i jednog Cl - jona. Kod Cu, motiv je samo jedan Cu atom. Kod Zn, motiv čine dva Zn atoma. U dijamantu, motiv čine dva C atoma. Prostorna rešetka Prostorna rešetka je trodimenzionalan, beskonačni niz tačaka; svaka tačka je na identičan način okružena svojim susedima. Svakoj tački prostorne rešetke pridružen je po jedan identičan strukturni motiv (Slika 4 ) i na taj način se gradi struktura kristala. Nije obavezno da se bilo koji od atoma motiva poklapa sa tačkom rešetke. Kod I na primer, tačka rešetke nalazi se u centru molekula I, a strukturni motiv sačinjavaju dva molekula I, Slika 5. 3
4 Slika 4. Struktura kristala dobija se pridruživanjem strukturnog motiva svakoj tački rešetke (kao primer dat je motiv A-B izgrađen od atoma A i B). Na slici je prikazana dvodimenzionalna rešetka i hipotetična dvodimenziona struktura kristala. Slika 5. Kristal I,; strukturni motiv čine dva molekula I pridružena svakoj tački rešetke, ali tačka rešetke leži u centru jenog od ta dva molekula I Jedinična ćelija Prostorna rešetka kristala može se (imaginarno) podeliti na identične paralelepipede spajanjem tačaka rešetke pravim linijama. (Paralelepiped je geometrijsko telo koje ima 6 strana koje su sve paralelogrami). Svaki takav paralelepiped je jedinična ćelija. Ceo kristal se može (misleno) izgraditi čisto translatornim premeštanjem jedinične ćelije. Postoji bezbroj različitih jediničnih ćelija kojima se može opisati ista rešetka, (dve jedinične ćelije kod dvodimenzionalne rešetke prikazane su na Slici 6 a i b) ali se u kristalografiji jedinična ćelija bira tako da njene ivice imaju najkraće dužine (tj. da ona ima najmanju moguću zapreminu) i da ima maksimalan broj normalnih ivica (što znači maksimalnu simetriju), odnosno da su uglovi između ivica što bliži pravom uglu. Slika 6. Dva načina formiranja jediničnih ćelija u dvodimenzionalnoj rešetki sa Slike 4. 4
5 U dve dimenzije jedinična ćelija je paralelogram sa stranama dužina a i b i uglom γ između ovih strana. U tri dimenzije jedinična ćelija je paralelepiped sa ivicama dužine a, b i c i uglovima α, β i γ, gde je α ugao između ivica b i c, γ je ugao između ivica a i b, i β je ugao između ivica a i c. Jedinične ćelije klasifikuju se u sedam kristalnih sistema, prema rotacionim elementima simetrije koje poseduje jedinična ćelija, Tabela 1. Tabela 1. Sedam kristalnih sistema SISTEM Suštinske simetrije Primeri Triklinični Nema Kalijum dihromat Monoklinični Jedna C osa Monoklinični sumpor Ortorombični 3 normalne C ose Rombični sumpor Romboedarski (trigonalan) Jedna C 3 osa Kalcit Tetragonalan Jedna C 4 osa Beli kalaj Heksagonalan Jedna C 6 osa Grafit Kubični 4 C 3 ose u tetraedarskom uređenju NaCl Kubična jedinična ćelija, na primer, ima četiri C 3 ose u tetraedarskom uređenju. Triklinična ćelija nema rotacionu simetriju, tipično za nju je da su sve tri strane i sva tri ugla različita. Suštinske simetrije (Tabela 1) znače elemente koji moraju biti prisutni u jediničnoj ćeliji da bi ona pripadala određenom kristalnom sistemu Bravais je pokazao da postoji 14 različitih kristalnih rešetki u tri dimenzije. Slika 7. ilustruje jedinične ćelije 14 Bravais-ovih rešetaka. Jedinična ćelija koja ima tačke rešetke samo u uglovima naziva se primitivna (P). Sedam Braveovih rešetaka ima primitivne jedinične ćelije. Zapreminski centrirana (I, od nemačkog innenzentrierte) jedinična ćelija ima tačku rešetke unutar ćelije, u njenom centru, osim tačaka na vrhovima. Tri Braveove rešetke su sa zapreminski centriranom jediničnom ćelijom Površinski centrirana (F, face) jedinična ćelija ima tačke rešetke na centrima strana (6), osim tačaka rešetke na vrhovima. Dve Braveove rešetke su površinski centrirane. Centrirana na krajevima, C- kada se tačke rešetke nalaze u centrima dveju suprotnih strana (čije su ivice a i b), slično je značenje za jedinične ćelije A i B. 5
6 kubični tetragonalan ortorombičan heksagonalan romboedarski monokliničan trikličan Slika 7. Jedinične ćelije 14 Bravais-ovih rešetki 6
7 Svaka tačka u uglu jedinične ćelije podeljena je između 8 susednih jediničnih ćelija u rešetki, četiri u posmatranom nivou, a 4 odmah iznad ili ispod (Slika 8). Slika 8. Prikazana tačka rešetke podeljena je između 4 jedinične ćelije prikazanog nivoa i 4 jedinične ćelije u nivou odmah iznad. Otuda, primitivna jedinična ćelija ima 8/8 =1 tačku rešetke po jediničnoj ćeliji i jedan strukturni motiv po jediničnoj ćeliji. Površinski centrirana (F) ima dodatno još 6 tačaka na centrima strana, svaku od njih dele po dve jedinične ćelije, tako da je broj tačaka rešetke po jednoj jediničnoj ćeliji jednak 8/8 +6/ =4, a takođe ima 4 strukturna motiva po jediničnoj ćeliji. Zapreminski centrirana jedinična ćelija imaće 8/8 +1 =, dakle tačke rešetke po jediničnoj ćeliji. Primitivna jedinična ćelija se može koristiti za opis bilo koje kristalne strukture, ali pošto u mnogim slučajevima ova ćelija ima manju simetriju od ćelije centrirane rešetke, to je pogodnije koristiti centriranu rešetku, Slika 9. Slika 9 a) Dvodimenziona rešetka podeljena u centrirane jedinične ćelije b) ista rešetka podeljena u manje simetrične primitivne jedinične ćelije Obeležavanje tačaka i ravni. Milerovi indeksi Da bi označili položaj neke tačke u jediničnoj ćeliji, biramo koordinatni sistem sa početkom u uglu jedinične ćelije i ose koje se podudaraju sa a,b i c ivicama ćelije. Ove ose ne moraju da budu uzajamno normalne. Položaj neke tačke u ćeliji se označava dajući njene koordinate kao frakcije dužina a, b i c jedinične ćelije. Na primer, tačka u koordinatnom početku je 000; tačka u centru jedinične zapreminski centrirane ćelije ima koordinate 1/ 1/ 1/; tačka u centru površine čije su ivice b i c je 0 1/ 1/. Rastojanje tačaka rešetke u kristalu je važan kvantitativan aspekt njegove strukture i ispitivanja kristala metodama difrakcije. Međutim, ima mnogo različitih setova ravni (Slika 10) i potrebno je označiti ih. 7
8 P 1 Slika 10. Setovi ravni p 1 i p (samo dva od velikog broja mogućih) koje prolaze kroz tačke rešetke Orjentacija kristalnih ravni opisuje se Milerovim indeksima (hkl). Oni predstavljaju recipročne vrednosti odsečaka koje data ravan odseca na na kristalografskim osama, izražene malim celim brojevima (h k l) Postupak određivanja Milerovih indeksa je 1. nalaze se preseci (odsečci) ravni na a,b i c osama kao umnošci dužina jedinične ćelije a, b, c. pišu se recipročne vrednosti ovih brojeva 3. ako se ne dobiju celi brojevi u koraku, tada se tri dobivena broja množe odgovarajućim faktorom kako bi se dobili celi brojevi. Ovo će biti jasnije na sledećim primerima. Razmatramo ravni prikazane na Slici 11. Slika 11. Odredjivanje Milerovih indeksa pojedinih ravni kristala Primer 1. Osenčena ravan r seče a osu u a/ i b osu u b/, a leži paralelno c osi tako da je odsečak jednak. Korak 1 daje ½, ½,. Korak daje,,0. Tako, Milerovi indeksi ove ravni su (0). Primer. Ravan označena sa s ima Milerove indekse (110) Primer 3. Ravan t ima odsečke 3 a, 3 b,, korak. daje 3, 3,0 Milerovi indeksi su (0) Primer 4. Ravan u ima odsečke a, b,, korak daje 1/, 1/, 0, a korak 3 daje Milerove indekse (110) Zapažamo da veća vrednost Milerovog indeksa h date ravni znači da je odsečak na osi a bliže koordinatnom početku. Ravni s i u, kao i beskonačan broj njima paralelnih ravni (od kojih su svake dve susedne na podjednakom rastojanju kao i ravni s i u) obrazuju set ravni (110). Za set ravni (0) smatra se da uključuje (110) ravni plus ravni koje se nalaze po sredini (110) ravni. Ravni r,s,t,u,... obrazuju set (0). Na slici 11. a) prikazan je set (0) ravni. Pri određivanju Milerovih indeksa seta paralelnih ekvidistantnih ravni posmatraju se odsečci ravni najbližih koordinatnom početku, ali koje ne sadrže koordinatni početak. 8
9 Fizička hemija II Doc. dr Gordana Ćirić-Marjanović Čvrsto stanje nastavak Jonski kristali Veza Avogadrovog broja i gustine kristala Sa Z ćemo označiti broj formulskih jedinica po jediničnoj ćeliji. (Formulska jedinica natrijum hlorida je NaCl). Slika 1. Jedinična ćelija NaCl označena je debljom linijom Kako odrediti broj Z za kristal NaCl? Natrijum hlorid pripada grupi jonskih kristala i ima površinski centriranu kubnu rešetku (PCK), vidi Sliku 1, gde je jedinična ćelija označena podebljanom linijom. Mnoga jedinjenja imaju strukturu NaCl tipa npr. LiCl, KCN, KF, NaCN, NaBr, MgO, CaO, CeN, AgBr, PbS Strukturni motiv (bazis) sačinjavaju jedan Na + jon i jedan Cl - jon, koji se pridružuju svakoj tački rešetke. U prethodnoj lekciji smo za PCK (ili ranija oznaka F) odredili da je broj strukturnih motiva po jediničnoj ćeliji jednak 4 (8/8 + 6/ = 4), a na svaki strukturni motiv dolazi po jedan Na + i jedan Cl -, odnosno po jedna jedinična formula NaCl, zaključujemo da je broj Z formulskih jedinica po jediničnoj ćeliji NaCl jednak 4, kod kristala tipa natrijum hlorida. Broj Z kod NaCl možemo odrediti i na drugi način. Kao što vidimo na Slici 1. ima 8 Cl - jona u uglovima i 6 Cl - jona na središtima strana kocke, tako da jedinična ćelija ima 8/8 + 6/ = 4 Cl - jona. Dalje, ima 1 Na + jona na ivicama jedinične ćelije, svakog od njih deli po 4 jedinične ćelije i ima još jedan Na + u centru jedinične ćelije. Otuda ima 1/4 + 1/1 = 4 Na + jona po jediničnoj ćeliji. Znači, ima 4 Cl - jona i 4 jona Na + po jediničnoj ćeliji, a to znači 4 formulske jedinice NaCl po jediničnoj ćeliji, tj. Z = 4. Jedan mol kristala ima N A formulskih jedinica. Pošto jedna jedinična ćelija ima Z formulskih jedinica sledi da je N A /Z broj jediničnih ćelija u jednom molu kristala. Zapremina pravougaone jedinične ćelije V data je proizvodom abc dužina njenih ivica. Molarna zapremina V M je otuda 1
10 V M = N A abc Z Gustina kristala ρ je data izrazom gde je M molarna masa. Otuda je ρ = M V M M Z ρ = za α = β = γ = 90 o (1) a b c N A Na osnovu poslednje formule, pomoću difrakcije X zraka određuju se a, b, c i Z, i uz poznavanje gustine kristala (na datoj temperaturi) može se odrediti Avogadrova konstanta N A. Ovaj metod određivanja N A je jedan od najtačnijih. Obrnuto, znajući N A može se odrediti na primer dužina ivice jedinične ćelije a kod kubne rešetke (a = b = c): ρ = a M Z 3 N A a M Z = 3 () ρ N A Metalni kristali U metalima elektroni su delokalizovani preko niza identičnih katjona i vezuju ih zajedno u čvrstu celinu. Kristalna struktura metala u mnogim slučajevima može se rastumačiti modelom u kome se sferični metalni katjoni pakuju zajedno na uređeni način. a) b) Slika a) prvi sloj A gusto (zbijeno) pakovanih sfera b) drugi sloj B gusto pakovanih sfera koje zaokupljuju šupljine prvog sloja, dva sloja su AB komponente strukture najgušćeg pakovanja
11 a) b) Slika 3. a) treći sloj najgušće pakovanih sfera može da zaposeda ulegnuća (šupljine) koja su direktno iznad sfera prvog sloja, što daje ABA strukturu, koja odgovara heksagonalnom najgušćem pakovanju b) treći sloj leži u ulegnućima koja nisu iznad sfera u prvom sloju, rezultat je ABC struktura, koja odgovara kubičnom najgušćem pakovanju a) b) Slika 4. a) ABA najgušće pakovanje (heksagonalno) i b) ABC najgušće pakovanje (kubično). Najgušće pakovanje sfera, odnosno pakovanje koje daje minimalnu nezauzetu zapreminu, tako da prazan prostor zauzima 6% ukupnog prostora, a popunjeno je 74 % ukupne zapremine, postiže se na dva različita načina. To su kubno najgušće pakovanje, koje se odnosi na površinski centriranu kubnu jediničnu ćeliju (PCK) i heksagonalno najgušće pakovanje. Neka je prvi sloj označen kao sloj A, kao na Slici.a) Umesto da se drugi sloj B dodaje direktno iznad prvog, on se može pridodati tako da se sfera drugog sloja smesti u šupljinu koju formiraju sfere prvog sloja (Slika b). Treći sloj može se formirati na dva načina. Kod jednog, sfere su smeštene tako da reprodukuju prvi sloj (Slika 3. a i 4. a)) dajući ABA pakovanje (prvi i treći sloj se podudaraju). Kod drugog načina, sfere trećeg sloja nalaze se iznad šupljina u prvom sloju (Slika 3 b i 4b), odnosno sfere trećeg sloja nisu tačno iznad sfera prvog sloja, dajući ABC raspored slojeva.. Ponavljanje rasporeda ABA daje niz slojeva ABABAB..., i to je heksagonalno najgušće pakovanje Slika 3a. Ako se šema ABC ponavlja, dobija se sekvenca ABCABC..., tada je to kubno najgušće pakovanje, Slika 3b. Kubno najgušće pakovanje odgovara površinski centriranoj kubičnoj kubičnoj jediničnoj ćeliji (PCK), Slika 3b. 3
12 Strukturni motiv (bazis) kod kubnog najgušćeg pakovanja (PCK) je sačinjen od jednog atoma (u svakoj tački rešetke), a kod heksagonalnog bazis čine dva atoma koja se pridružuju svakoj tački rešetke (Slika 5). Koordinacioni broj je 1 i kod heksagonalnog i kod kubičnog najgušćeg pakovanja. Slika 5. Heksagonalno pakovanje, jedinična ćelija obeležena je debljim linijama. PCK struktura je veoma česta kod metala. Primeri su: Al, Cu, Au, Ag, Pb, Pt, Pd, Ni, Ca. Heksagonalno najgušće pakovanje imaju metali Be, Mg, Cd, Co, Zn, Ti, Tl. Mnogi metali imaju strukture koje nisu najgušće pakovanje. Takva je zapreminski centrirana kubična rešetka (ZCK), sa jednom sferom u centru kocke koju formira 8 drugih sfera. Koordinacioni broj ZCK strukture je 8, pošto svaki atom dodiruje 4 atoma u sloju iznad njega i 4 u sloju ispod njega, i nijednog u njegovom sloju. Ova struktura ima 68 % popunjenog prostora. Bazis predstavlja jedan atom (u svakoj tački rešetke). Na Slici 6. prikazano je pakovanje sfera kod ZCK rešetke. U prvom sloju sfere su uređene tako da su im centri razdvojeni rastojanjem koje iznosi / 3 puta prečnik sfere = 1,15 x prečnik sfere. Sfere drugog sloja (osenčene sfere) nalaze se u šupljinama prvog sloja, dok su sfere trećeg sloja direktno iznad sfera prvog sloja. Primeri metala sa ZCK strukturom su Ba, Cs, Cr, Fe, K, Li, Mo, Mn, Rb, Na, Ta, W. Slika 6. Formiranje ZCK rešetke 4
13 Kod strukture sa prostom (primitivnom) kubičnom rešetkom samo 5 % ukupne zapremine je zauzeto sferama. U ovom slučaju formira se prvi sloj sfera, gde se svaka uočena sfera dodiruje sa još četiri susednih (Slika 7). Slika 7. Prvi sloj kod formiranja proste kubične rešetke Sledeći (drugi) sloj iznad prvog uočenog sloja dodaje se tako što je svaka sfera u tom drugom (gornjem) sloju tačno iznad jedne sfere u donjem sloju; tako se formira struktura koja ima prostu kubičnu prostornu rešetku. Strukturni motiv (bazis) kod proste kubične rešetke čini jedan atom u svakoj tački rešetke. Prosta kubična rešetka je veoma retka za metale, jedini poznati primer je polonijum, Po. Koordinacioni broj je u ovom slučaju 6, jer se svaka uočena sfera dodiruje sa 4 sfere u jednom istom sloju, i sa još jednom sferom u sloju iznad tog sloja i još jednom sferom u sloju ispod. Neki metali menjaju strukturu sa promenom temperature i pritiska. Na primer, Fe je PCK strukture kada je temperatura između 906 i 1401 o C, a iznad i ispod ovog ranga je ZCK, na pritisku od 1 atm. Kod metalnih kristala takođe možemo pomoću formule () izračunati a, ukoliko znamo broj Z. Kod površinski centrirane kubične rešetke (PCK) strukturni motiv se sastoji od jednog atoma, (dakle, po jedan atom se nalazi u svakoj tački rešetke) a broj strukturnih motiva po jediničnoj ćeliji PCK smo odredili u prethodnoj lekciji da iznosi 4, tako da je broj Z jednak 4. Sada je broj Z ujedno jednak i broju atoma po elementarnoj ćeliji (formulska jedinica je sam atom metala). Primer 1. Gustina srebra je ρ = 10,5 g cm -3, molska masa M=107,87 g mol -1, a kristalna rešetka je površinski centrirana kubična. Odrediti dužinu ivice jedinične (elementarne) ćelije a. Rešenje Z =4 a M Z = 3 = 3 ρ N A 107,87 g mol 10,5 g cm 3 1 x 4 6,0 x10 3 = 4,086 x 10-8 cm = 0,41 nm Rastojanje ravni rešetke Milerovi indeksi se koriste za izračunavanje rastojanja između ravni rešetke. Za kvadratnu rešeku (dve dimenzije) prikazanu na slici 8. može se pokazati da je rastojanje između (hk0) ravni dato izrazom (3): 5
14 1 d hk 0 h + k = a (3) Slika 8. Izračunavanje rastojanja ravni kvadratne rešetke d hk Izvođenje izraza (3) Pitagorina teorema za trougao ABD daje m = ( k a ) + ( h a ) Površina trougla ABC je d ( m n) P ABC = a površina trougla ACD je d n P ACD = Površina trougla ABD je jednaka trougla, odnosno (4) (5) (6) 1 a a ( ) a takođe je jednaka i zbiru površina prethodna dva h k d ( m n) + d n = a hk (7) a posle sređivanja izraz (7) postaje a dm = (8) h k Kvadriranjm izraza (8) i izražavanjem m preko izraza (4) dobija se 6
15 4 a [( ) a + ( ) ] d a = k h h k odakle sledi 1 h + k = d hk 0 a Proširenjem na tri dimenzije, međusobno rastojanje ravni (hkl) kubične rešetke dato je izrazom: 1 d hkl = h + k + l a (9) a odgovarajući izraz za ortorombičnu rešetku je generalizacija izraza (9): 1 d hkl h k l + + a b c = (10) Bitno je primetiti da ako se sva tri Milerova indeksa pomnože brojem n (uvećaju n puta), rastojanje ravni se smanjuje za faktor n, odnosno d d nh, nk, nl = hkl (11) n što se može lako dokazati na sledeći način 1 d nh, nk, nl ( nh) = a ( nk) + b ( nl) + c h = n ( a k + b l n + ) = c d hkl Sledi d nh, nk, nl = d hkl n Na slici 9. ilustrovano je značenje izraza (11)- vidi se da je međusobno rastojanje ravni (0) dva puta manje od međusobnog rastojanja ravni (110). Slika 9. Međusobno rastojanje ravni (0) dva puta manje od međusobnog rastojanja ravni (110). 7
16 Primer. Izračunati međusobno rastojanje (13) i (46) ravni u ortorombičnoj ćeliji sa dužinama ivica elementarne ćelije a= 0,8 nm, b = 0,94 nm i c = 0,75 nm. Rešenje Zadatak se rešava primenom izraza (10) = + + = nm - d13 0,8 0,94 0,75 d 13 =0, nm Odmah se, na osnovu izraza (11) može izračunati d 46 d13 d 46 = =0,11 nm Određivanje strukture kristala Difrakcija X-zraka Međuatomska rastojanja u kristalima su reda veličine 1 Å = 1 x m. Elektromagnetno zračenje talasnih dužina od 1 Å pripada regionu X-zraka. Otuda, kristali deluju kao difrakcione rešetke za X-zrake. Prvi put je takav eksperiment realizovan 191. (Max von Laue je sugerisao da ako λ zračenja postane mala koliko i rastojanje atoma u kristalu, trebalo bi da se pojavi difrakciona slika, to su eksperimentalno proverili Walter Friedrich i Paul Knipping). Stvorena je osnova za određivanje struktura kristala (a istovremeno potvrđena i talasna priroda X-zraka). Podsetimo se da X-zraci nastaju bombardovanjem metala visokoenergijskim elektronima (jedan od načina). Sudarom upadnog elektrona sa elektronom iz unutrašnje ljuske atoma izbija se elektron unutrašnje ljuske atoma, a na njegovo upražnjeno mesto dolazi neki elektron (više energije) iz viših ljuski pri čemu se višak energije emituje kao foton X-zračenja. Ako je izbijeni elektron iz K ljuske X-zračenje se zove K-zračenje, a linije obeležavaju K α, K β... Slika 10. Difrakciona slika dobivena propuštanjem X-zraka kroz kristal bakarsulfata, von Laue. 8
17 Bragg-ov metod Bragg-ova metoda koristi monohromatski snop X-zraka (tj. određene talasne dužine). Fizičari Henri i Lorens Bragg protumačili su pojavu rasejavanja X- zračenja na kristalnoj rešetki kao refleksiju sa ravni kristala- kao da ove ravni predstavljaju ogledala. Tako kristal predstavlja mnoštvo reflektujućih ravni rešetke, koje su na međusobnom rastojanju d hkl. Oni su u skladu sa ovim modelom postavili odgovarajući uslov neophodan za pojačavanje (konstruktivnu interferenciju) reflektovanog zračenja. Slika 11. Izvođenje Bragg-ovog zakona prema modelu koji tretira svaku ravan rešetke kao reflektujuću za upadno zračenje. Projekcije međusobno paralelnih ravni na ravan crteža su prave, Slika 11. Putna razlika dva zraka koja su prikazana na Slici 11. je AB + BC = d sinθ (1) gde je θ ugao pod kojim zračenje pada u odnosu na posmatranu ravan (odnosno skup paralelnih ravni), tj. ugao između upadnog snopa i ravni kristala. Pri refleksiji, odbojni ugao jednak je upadnom.čestice koje čine kristal (atomi, joni, molekuli) rasejavaju zračenje u svim pravcima. Interesuje nas pod kojim uglovima dolazi do konstruktivne interferencije reflektovanog zračenja. Za mnoge uglove θ putna razlika nije celobrojni umnožak talasnih dužina i talasi interferiraju destruktivno. Međutim, kada je putna razlika dva jednaka celobrojnom umnošku talasnih dužina, tj. AB + BC = n λ (13) 9
18 reflektovani talasi su u fazi i interferiraju konstruktivno. Tako se svetle (pojačane) refleksije dobijaju kada ugao θ zadovoljava Bragg-ov zakon nλ = d hkl sinθ n =1,,3,... (14) refleksije sa n =,3, zovu se drugog reda, trećeg reda itd. One odgovaraju putnim razlikama od, 3, talasne dužine. U savremenom radu uobičajeno je da se Bragg-ov zakon piše kao λ = d nh,nk,nl sinθ (15) pri čemu se smatra da refleksija n-tog reda potiče od (nh, nk, nl) ravni prema relaciji d nh, nk, nl = d hkl n Termin refleksija se koristi da se označi intenzivan rasejani snop koji potiče od konstruktivne interferencije. Aparatura koja koristi Bragg ov metod Prvi kristali koji su proučavani Bragg ovom metodom bili su NaCl i KCl. Jedan kristal se postavlja u spektrometar, Slika 1. tako da monohromatski snop X zraka pada na jednu od značajnih ravni (100), (110) ili (111). (tj. na pljosan kristala koja je paralelna seriji ravni sa kojih želimo da dobijemo refleksiju). Reflektovani snop pada na detektor (jonizacionu komoru ili fotoploču). U eksperimentu, pri obrtanju kristala za ugao θ, detektor mora da se okrene za ugao θ. Obrtanjem kristala, traže se uglovi θ koji, za određeno λ zadovoljavaju Bragovu jednačinu. Pri uglovima između pravca upadnog snopa i pljosni kristala θ koji zadovoljavaju Bragovu jednačinu dobija se porast struje u jonizacionoj komori ili zacrnjenje na filmu. Slika 13 prikazuje Bragg ove spektrometrijske podatke. Slika 1. Šema Bragovog eksperimentalnog uređaja 10
19 Slika 13. Bragovi spektrometrijski podaci. Primer 3. Refleksija sa ravni (111) kubičnog kristala dobivena je za upadni ugao (ugao između upadnog snopa i ravni kristala) od 11, o. Korišćena je K α linija X zračenja bakra, talasne dužine 154 pm. Kolika je dužina ivice jedinične ćelije? Rešenje Koristimo relaciju (15) λ = d nh,nk,nl sinθ d 111 = λ sinθ 1 h + k + i relaciju (9) = d hkl a iz koje dobijamo za zadate uslove l a d 111 = 3 Otuda je a = 3 d 111 = 3 λ sinθ = 687 pm Postoji druga varijanta metode u kojoj je kristal učvršćen, a koristi se kontinualno X-zračenje. Tada će ravni kristala da odaberu onu komponentu zračenja čija talasna dušina, za određeno rastojanje ravni d i dati ugao θ između snopa i ravni, zadovoljava uslov za konstruktivnu interferenciju. To je Laueova metoda. 11
20 Metod kristalnog praha Ovu metodu prvi su upotrebili Peter Debye i Paul Scherrer. Umesto jednog kristala koji ima određenu orjentaciju prema snopu X-zraka, upotrebljavaju se fino isitnjeni, sprašeni kristali u kojima kristalići imaju haotičnu orjentaciju. Koristi se monohromatsko X zračenje. Za svaku seriju ravni mogu da se nađu kristalići koji su u odnosu na upadni snop usmereni tako da zadovoljavaju Bragov uslov, pri određenoj talasnoj dužini λ. Slika 14. Metoda kristalnog praha Slika 15. Metoda kristalnog praha. Za detekciju se koristi film, koji je cilindrično omotan oko uzorka, Slika 14. Ako je za odgovarajući tip ravni i za talasnu dužinu λ Bragov ugao θ, tada difraktovani zrak gradi sa upadnim zrakom ugao θ, Slika 14 i 15. Ugao θ može imati različite orjentacije oko pravca upadnog snopa, što odgovara različitim oorjentacijama pojedinih kristalića. Stoga, za svaki niz mrežnih ravni, 1
21 reflektovani snopovi grade konus. Ovaj konus preseca cilindrični film oko uzorka i na njemu stvara tamne linije-lukove, koji su delovi koncentričnih krugova (čiji je centar u tački koju daje upadni nedifraktovani zrak, slike 14 i 15). Svaka linija (luk) odgovara određenom tipu ravni. Ako je R poluprečnik cilindrične komore, a r poluprečnik kruga r = tgθ ~ sinθ ~ sinθ R zamenom u Bragovoj jednačini (14) sinθ sa R r dobija se nλ = d hkl r R odakle se može odrediti rastojanje između ravni d hkl ako je poznato λ. Podaci za rastojanja d hkl često se bez daljeg izračunavanja koriste za identifikaciju čvrstih supstancija ili analizu čvrstih smeša. Postoje opširne tablice koje omogućavaju brzu identifikaciju. Difrakciona tehnika praha koristi se za identifikaciju uzoraka čvrstih supstancija putem poređenja položaja difrakcionih linija i njihovih intenziteta sa velikom»bankom«podataka. Tehnika se koristi i za početno određivanje dimenzija i simetrije jedinične ćelije, kako je objašnjeno u sledećem odeljku. Indeksiranje refleksija Neki tipovi jediničnih ćelija daju karakterističan i lako prepoznatljiv raspored linija. Na primer, za kubičnu rešetku sa jediničnom ćelijom ivice a rastojanje ravni d dato je izrazom 1 d hkl h + k + l = a tako da su uglovi pri kojima (hkl) ravni daju konstruktivnu interferenciju (refleksiju), primenom Bragovog uslova dati izrazom sinθ = (h + k + l ) 1/ λ a Nađene vrednosti za sinθ se na ovaj način označavaju indeksima, tj. indeksiranje znači pripisivanje vrednosti (hkl) refleksijama, tj vrednostima sinθ. Refleksije se mogu predvideti zamenom vrednosti za h, k i l: (hkl) (100) (110) (111) (00) (10) (11) (0) (300) (1) (310) h + k + l Zapažamo da zbir h + k + l = 7 ( i 15, ) nedostaje jer suma kvadrata tri cela broja ne može dati 7 (ili 15, ). Difrakciona slika sa ovakvim odsustvom vrednosti 7, 15,.. zbira h + k + l karakteristika je proste (primitivne) kubične rešetke. 13
22 Dalje, može se pokazati da se zapreminski centrirana kubična rešetka prepoznaje po tome što su u njenoj difrakcionoj slici odsutne sve refleksije sa neparnim vrednostima zbira h + k + l. Kod površinski centrirane kubične rešetke prisutne su samo refleksije kod kojih su indeksi h, k, l svi parni ili svi neparni, Slika 16. Slika 16. Difrakcione slike dobivene metodom kristalnog praha za tri varijante kubične rešetke. 14
23 Metalna veza Kristalna rešetka metala je veoma stabilna što znači da je i veza između atoma veoma jaka. Metalna veza može da se posmatra kao posebna vrsta kovalentne veze, a kristal metala kao veliki «molekul». Metalna veza može postojati samo u većim agregatima atoma (kakvi su kristali) dok obična kovalentna veza postoji u molekulima. Metalna veza nije prostorno usmerena, za razliku od kovalentne. Prema Polingu, metalna veza je u suštini kovalentna veza, sa tom razlikom što kod metala, zbog nedovoljnog broja valentnih elektrona, na jednu vezu dolazi manje od jednog elektronskog para. Za stvaranje veze na raspolaganju stoji više orbitala nego što ima elektrona da ih popune. Zbog toga se ova veza može posmatrati kao delokalizovana jednostruka veza koja se stalno premešta između različitih parova atoma metala.. Fizička i hemijska svojstva metala vode zaključku da u njima postoje pokretljivi elektroni. Male energije jonizacije atoma metala i pojava fotoefekta su na primer dokaz da metali lako otpuštaju elektrone, dok su dobra provodljivosti toplote i elektriciteta dokazi za veliku pokretljivost elektrona kroz kristalnu rešetku metala. Ova svojstva se mogu objasniti pomoću dva modela, prvi je model elektronskog gasa a drugi model elektronskih traka. Model elektronskog gasa Metalna veza uspostavlja se između jona M n+ i «slobodnih elektrona», koji čine tzv. «elektronski gas» koji se kreće između pozitivnih jona, Slika 16. Negativno naelektrisanje svih elektrona raspodeljenih po celoj rešetki drši pozitivne jone na ravnotežnom rastojanju.. Ovaj model je dosta uprošćen i nije uvek u saglasnosti sa eksperimentalnim podacima. Slika 1. Metalna veza po modelu elektronskog gasa za jednovalentan i dvovalentan metal Model elektronskih traka Metal se posmatra kao beskonačno veliki molekul u kome su atomi toliko blizu jedan drugom da se njihove atomske orbitale preklapaju. One postaju zajedničke svim atomima, pa ih elektroni u parovima zauzimaju kao molekulske orbitale. Energije elektrona u pojedinim molekulskim 15
24 orbitalama u metalu se malo razlikuju, tako da one čine traku energijskih nivoa-elektronsku traku. Molekulske» orbitale nastale preklapanjem atomskih orbitala istog tipa (1s, s...) izgrađuju odgovarajuću elektronsku traku. Preklapanje s-orbitala daje s-traku, preklapanje p-orbitala daje p-traku itd., vidi Sliku. Elektronske trake mogu biti potpuno popunjene, delimično popunjene ili nepopunjene. Elektronske trake međusobno su odvojene zabranjenim zonama, koje ne sadrže dozvoljene energijske nivoe, pa se u njima ne mogu nalaziti elektroni. Elektronska traka koja je delimično popunjena zove se valentna traka. Najviši energijski nivo popunjen elektronima na apsolutnoj nuli (T= 0 K) zove se Fermijev nivo. Pri dovođenju energije (T>0) elektroni mogu prelaziti na slobodne nivoe u okviru valentne trake, čime se omogućuje kretanje elektrona kroz kristal. Iznad valentne elektronske trake nalazi se nepopunjena traka, koja se zove provodna traka. Ukoliko metal sadrži veći broj elektrona, trake su šire i može doći do preklapanja valentne trake (potpuno popunjene) i provodne trake, Slika 3 b). Ovo omogućuje kretanje elektrona kroz provodnu traku pod uticajem električnog polja. Što je redni broj metala veći ovo preklapanje je izraženije, zbog manje razlike u energijama s i p elektrona. Najbolji provodnici elektriciteta, među metalima su Ag, Au, Al i Cu. Pomoću modela elektronskih traka mogu da se objasne električna svojstva metala, a i drugih čvrstih supstanci. Prema sposobnosti provođenja električne struje čvrste supstance dele se na provodnike (metali), sa najvećom provodljivošću, izolatore, koji imaju visok električni otpor i malu provodljivost i poluprovodnike, koji su po veličini električnog otpora između provodnika i izolatora. 16
25 Slika. Model elektronskih traka-nastajanje elektronskih traka preklapanjem atomskih orbitala kod litijuma, 1s s 1 a) b) Slika 3. a)valentna traka Na b) preklapanje valentne i provodne trake kod Mg Električna provodljivost metala se sa porastom temperature smanjuje. Objašnjenje: sa sniženjem temperature smanjuju se amplitude vibracija pozitivnih jona, tako da oni tada u manjoj meri ometaju kretanje elektrona i provodljivost metala raste. U blizini termodinamičke nule (0 K) mnogi čisti metali postaju superprovodnici, tj. imaju beskonačno mali električni otpor. Poluprovodnici Potpuno popunjena valentna i prazna provodna traka razdvojene su znatno širom zabranjenom zonom nego kod metala (1 ev po atomu). Zato na sobnoj T mali broj elektrona ima dovoljnu energiju da iz valentne pređe u provodnu traku, i električna provodljivost je mala na sobnoj T. Sa porastom T raste broj elektrona koji prelaze u provodnu traku i raste provodljivost poluprovodnika. Tipični primeri su silicijum i germanijum. Dopiranjem primesama (arsen, bor) povećava se električna provodljivost poluprovodnika. Primese su atomi koji imaju veći (As) ili manji (B) broj elektrona od atoma poluprovodnika. Time se stvaraju novi energijski nivoi u oblasti zabranjene zone, koji omogućavaju poluprovodnost i na sobnim temperaturama. U slučaju dopiranja arsenom, postoji n-poluprovodljivost (negativna), a u slučaju bora, p- poluprovodljivost (pozitivna). Kod n-tipa javljaju se elektroni u provodnoj traci, a kod p- tipa nastaje praznina u prvobitno popunjenoj valentnoj traci. Izolatori Širina zabranjene zone je velika, na primer ~ 6 ev po atomu kod dijamanta. Ni sa porastom temperature ne dolazi do prelaza elektrona iz valentne u provodnu traku, Slika 5. 17
26 Slika 4. Poluprovodnik silicijum a) dopiran arsenom postaje poluprovodnik n-tipa, b) dopiran borom postaje poluprovodnik p-tipa Slika 5. Shematski prikaz elektronskih traka a) metala, b) poluprovodnika c) izolatora 18
UNIVERZITET U NIŠU ELEKTRONSKI FAKULTET SIGNALI I SISTEMI. Zbirka zadataka
 UNIVERZITET U NIŠU ELEKTRONSKI FAKULTET Goran Stančić SIGNALI I SISTEMI Zbirka zadataka NIŠ, 014. Sadržaj 1 Konvolucija Literatura 11 Indeks pojmova 11 3 4 Sadržaj 1 Konvolucija Zadatak 1. Odrediti konvoluciju
UNIVERZITET U NIŠU ELEKTRONSKI FAKULTET Goran Stančić SIGNALI I SISTEMI Zbirka zadataka NIŠ, 014. Sadržaj 1 Konvolucija Literatura 11 Indeks pojmova 11 3 4 Sadržaj 1 Konvolucija Zadatak 1. Odrediti konvoluciju
Kontrolni zadatak (Tačka, prava, ravan, diedar, poliedar, ortogonalna projekcija), grupa A
 Kontrolni zadatak (Tačka, prava, ravan, diedar, poliedar, ortogonalna projekcija), grupa A Ime i prezime: 1. Prikazane su tačke A, B i C i prave a,b i c. Upiši simbole Î, Ï, Ì ili Ë tako da dobijeni iskazi
Kontrolni zadatak (Tačka, prava, ravan, diedar, poliedar, ortogonalna projekcija), grupa A Ime i prezime: 1. Prikazane su tačke A, B i C i prave a,b i c. Upiši simbole Î, Ï, Ì ili Ë tako da dobijeni iskazi
HEMIJSKA VEZA TEORIJA VALENTNE VEZE
 TEORIJA VALENTNE VEZE Kovalentna veza nastaje preklapanjem atomskih orbitala valentnih elektrona, pri čemu je region preklapanja između dva jezgra okupiran parom elektrona. - Nastalu kovalentnu vezu opisuje
TEORIJA VALENTNE VEZE Kovalentna veza nastaje preklapanjem atomskih orbitala valentnih elektrona, pri čemu je region preklapanja između dva jezgra okupiran parom elektrona. - Nastalu kovalentnu vezu opisuje
SEKUNDARNE VEZE međumolekulske veze
 PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
3.1 Granična vrednost funkcije u tački
 3 Granična vrednost i neprekidnost funkcija 2 3 Granična vrednost i neprekidnost funkcija 3. Granična vrednost funkcije u tački Neka je funkcija f(x) definisana u tačkama x za koje je 0 < x x 0 < r, ili
3 Granična vrednost i neprekidnost funkcija 2 3 Granična vrednost i neprekidnost funkcija 3. Granična vrednost funkcije u tački Neka je funkcija f(x) definisana u tačkama x za koje je 0 < x x 0 < r, ili
Osnovni primer. (Z, +,,, 0, 1) je komutativan prsten sa jedinicom: množenje je distributivno prema sabiranju
 RAČUN OSTATAKA 1 1 Prsten celih brojeva Z := N + {} N + = {, 3, 2, 1,, 1, 2, 3,...} Osnovni primer. (Z, +,,,, 1) je komutativan prsten sa jedinicom: sabiranje (S1) asocijativnost x + (y + z) = (x + y)
RAČUN OSTATAKA 1 1 Prsten celih brojeva Z := N + {} N + = {, 3, 2, 1,, 1, 2, 3,...} Osnovni primer. (Z, +,,,, 1) je komutativan prsten sa jedinicom: sabiranje (S1) asocijativnost x + (y + z) = (x + y)
PRAVA. Prava je u prostoru određena jednom svojom tačkom i vektorom paralelnim sa tom pravom ( vektor paralelnosti).
 PRAVA Prava je kao i ravan osnovni geometrijski ojam i ne definiše se. Prava je u rostoru određena jednom svojom tačkom i vektorom aralelnim sa tom ravom ( vektor aralelnosti). M ( x, y, z ) 3 Posmatrajmo
PRAVA Prava je kao i ravan osnovni geometrijski ojam i ne definiše se. Prava je u rostoru određena jednom svojom tačkom i vektorom aralelnim sa tom ravom ( vektor aralelnosti). M ( x, y, z ) 3 Posmatrajmo
DISKRETNA MATEMATIKA - PREDAVANJE 7 - Jovanka Pantović
 DISKRETNA MATEMATIKA - PREDAVANJE 7 - Jovanka Pantović Novi Sad April 17, 2018 1 / 22 Teorija grafova April 17, 2018 2 / 22 Definicija Graf je ure dena trojka G = (V, G, ψ), gde je (i) V konačan skup čvorova,
DISKRETNA MATEMATIKA - PREDAVANJE 7 - Jovanka Pantović Novi Sad April 17, 2018 1 / 22 Teorija grafova April 17, 2018 2 / 22 Definicija Graf je ure dena trojka G = (V, G, ψ), gde je (i) V konačan skup čvorova,
OBRTNA TELA. Vladimir Marinkov OBRTNA TELA VALJAK
 OBRTNA TELA VALJAK P = 2B + M B = r 2 π M = 2rπH V = BH 1. Zapremina pravog valjka je 240π, a njegova visina 15. Izračunati površinu valjka. Rešenje: P = 152π 2. Površina valjka je 112π, a odnos poluprečnika
OBRTNA TELA VALJAK P = 2B + M B = r 2 π M = 2rπH V = BH 1. Zapremina pravog valjka je 240π, a njegova visina 15. Izračunati površinu valjka. Rešenje: P = 152π 2. Površina valjka je 112π, a odnos poluprečnika
Elementi spektralne teorije matrica
 Elementi spektralne teorije matrica Neka je X konačno dimenzionalan vektorski prostor nad poljem K i neka je A : X X linearni operator. Definicija. Skalar λ K i nenula vektor u X se nazivaju sopstvena
Elementi spektralne teorije matrica Neka je X konačno dimenzionalan vektorski prostor nad poljem K i neka je A : X X linearni operator. Definicija. Skalar λ K i nenula vektor u X se nazivaju sopstvena
Doc. dr Milena Đukanović
 Doc. dr Milena Đukanović milenadj@ac.me ČVRSTO AGREGATNO STANJE: Materijale u čvrstom agregatnom stanju možemo podijeliti na: Monokristalne Polikristalne Polimerne Amorfne. Riječ kristal se do kraja srednjeg
Doc. dr Milena Đukanović milenadj@ac.me ČVRSTO AGREGATNO STANJE: Materijale u čvrstom agregatnom stanju možemo podijeliti na: Monokristalne Polikristalne Polimerne Amorfne. Riječ kristal se do kraja srednjeg
numeričkih deskriptivnih mera.
 DESKRIPTIVNA STATISTIKA Numeričku seriju podataka opisujemo pomoću Numeričku seriju podataka opisujemo pomoću numeričkih deskriptivnih mera. Pokazatelji centralne tendencije Aritmetička sredina, Medijana,
DESKRIPTIVNA STATISTIKA Numeričku seriju podataka opisujemo pomoću Numeričku seriju podataka opisujemo pomoću numeričkih deskriptivnih mera. Pokazatelji centralne tendencije Aritmetička sredina, Medijana,
1 UPUTSTVO ZA IZRADU GRAFIČKOG RADA IZ MEHANIKE II
 1 UPUTSTVO ZA IZRADU GRAFIČKOG RADA IZ MEHANIKE II Zadatak: Klipni mehanizam se sastoji iz krivaje (ekscentarske poluge) OA dužine R, klipne poluge AB dužine =3R i klipa kompresora B (ukrsne glave). Krivaja
1 UPUTSTVO ZA IZRADU GRAFIČKOG RADA IZ MEHANIKE II Zadatak: Klipni mehanizam se sastoji iz krivaje (ekscentarske poluge) OA dužine R, klipne poluge AB dužine =3R i klipa kompresora B (ukrsne glave). Krivaja
SISTEMI NELINEARNIH JEDNAČINA
 SISTEMI NELINEARNIH JEDNAČINA April, 2013 Razni zapisi sistema Skalarni oblik: Vektorski oblik: F = f 1 f n f 1 (x 1,, x n ) = 0 f n (x 1,, x n ) = 0, x = (1) F(x) = 0, (2) x 1 0, 0 = x n 0 Definicije
SISTEMI NELINEARNIH JEDNAČINA April, 2013 Razni zapisi sistema Skalarni oblik: Vektorski oblik: F = f 1 f n f 1 (x 1,, x n ) = 0 f n (x 1,, x n ) = 0, x = (1) F(x) = 0, (2) x 1 0, 0 = x n 0 Definicije
Teorijske osnove informatike 1
 Teorijske osnove informatike 1 9. oktobar 2014. () Teorijske osnove informatike 1 9. oktobar 2014. 1 / 17 Funkcije Veze me du skupovima uspostavljamo skupovima koje nazivamo funkcijama. Neformalno, funkcija
Teorijske osnove informatike 1 9. oktobar 2014. () Teorijske osnove informatike 1 9. oktobar 2014. 1 / 17 Funkcije Veze me du skupovima uspostavljamo skupovima koje nazivamo funkcijama. Neformalno, funkcija
ČVRSTO STANJE. Amorfno & Kristalno čvrsto stanje. Najureñenije stanje materije. Postoje dva oblika švrstog stanja:
 ČVRSTO STANJE Najureñenije stanje materije Postoje dva oblika švrstog stanja: Amorfno & Kristalno čvrsto stanje Amorfno čvrsto stanje nema dobro ureñenu strukturu, postoji samo ureñenost kratkog dometa
ČVRSTO STANJE Najureñenije stanje materije Postoje dva oblika švrstog stanja: Amorfno & Kristalno čvrsto stanje Amorfno čvrsto stanje nema dobro ureñenu strukturu, postoji samo ureñenost kratkog dometa
41. Jednačine koje se svode na kvadratne
 . Jednačine koje se svode na kvadrane Simerične recipročne) jednačine Jednačine oblika a n b n c n... c b a nazivamo simerične jednačine, zbog simeričnosi koeficijenaa koeficijeni uz jednaki). k i n k
. Jednačine koje se svode na kvadrane Simerične recipročne) jednačine Jednačine oblika a n b n c n... c b a nazivamo simerične jednačine, zbog simeričnosi koeficijenaa koeficijeni uz jednaki). k i n k
Pismeni ispit iz matematike Riješiti sistem jednačina i diskutovati rješenja sistema u zavisnosti od parametra: ( ) + 1.
 Pismeni ispit iz matematike 0 008 GRUPA A Riješiti sistem jednačina i diskutovati rješenja sistema u zavisnosti od parametra: λ + z = Ispitati funkciju i nacrtati njen grafik: + ( λ ) + z = e Izračunati
Pismeni ispit iz matematike 0 008 GRUPA A Riješiti sistem jednačina i diskutovati rješenja sistema u zavisnosti od parametra: λ + z = Ispitati funkciju i nacrtati njen grafik: + ( λ ) + z = e Izračunati
Inženjerska grafika geometrijskih oblika (5. predavanje, tema1)
 Inženjerska grafika geometrijskih oblika (5. predavanje, tema1) Prva godina studija Mašinskog fakulteta u Nišu Predavač: Dr Predrag Rajković Mart 19, 2013 5. predavanje, tema 1 Simetrija (Symmetry) Simetrija
Inženjerska grafika geometrijskih oblika (5. predavanje, tema1) Prva godina studija Mašinskog fakulteta u Nišu Predavač: Dr Predrag Rajković Mart 19, 2013 5. predavanje, tema 1 Simetrija (Symmetry) Simetrija
OTPORNOST MATERIJALA
 3/8/03 OTPORNOST ATERIJALA Naponi ANALIZA NAPONA Jedinica u Si-sistemu je Paskal (Pa) Pa=N/m Pa=0 6 Pa GPa=0 9 Pa F (N) kn/cm =0 Pa N/mm =Pa Jedinična površina (m ) U tečnostima pritisak jedinica bar=0
3/8/03 OTPORNOST ATERIJALA Naponi ANALIZA NAPONA Jedinica u Si-sistemu je Paskal (Pa) Pa=N/m Pa=0 6 Pa GPa=0 9 Pa F (N) kn/cm =0 Pa N/mm =Pa Jedinična površina (m ) U tečnostima pritisak jedinica bar=0
( ) ( ) 2 UNIVERZITET U ZENICI POLITEHNIČKI FAKULTET. Zadaci za pripremu polaganja kvalifikacionog ispita iz Matematike. 1. Riješiti jednačine: 4
 UNIVERZITET U ZENICI POLITEHNIČKI FAKULTET Riješiti jednačine: a) 5 = b) ( ) 3 = c) + 3+ = 7 log3 č) = 8 + 5 ć) sin cos = d) 5cos 6cos + 3 = dž) = đ) + = 3 e) 6 log + log + log = 7 f) ( ) ( ) g) ( ) log
UNIVERZITET U ZENICI POLITEHNIČKI FAKULTET Riješiti jednačine: a) 5 = b) ( ) 3 = c) + 3+ = 7 log3 č) = 8 + 5 ć) sin cos = d) 5cos 6cos + 3 = dž) = đ) + = 3 e) 6 log + log + log = 7 f) ( ) ( ) g) ( ) log
Eliminacijski zadatak iz Matematike 1 za kemičare
 Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Iskazna logika 3. Matematička logika u računarstvu. novembar 2012
 Iskazna logika 3 Matematička logika u računarstvu Department of Mathematics and Informatics, Faculty of Science,, Serbia novembar 2012 Deduktivni sistemi 1 Definicija Deduktivni sistem (ili formalna teorija)
Iskazna logika 3 Matematička logika u računarstvu Department of Mathematics and Informatics, Faculty of Science,, Serbia novembar 2012 Deduktivni sistemi 1 Definicija Deduktivni sistem (ili formalna teorija)
Osnovne teoreme diferencijalnog računa
 Osnovne teoreme diferencijalnog računa Teorema Rolova) Neka je funkcija f definisana na [a, b], pri čemu važi f je neprekidna na [a, b], f je diferencijabilna na a, b) i fa) fb). Tada postoji ξ a, b) tako
Osnovne teoreme diferencijalnog računa Teorema Rolova) Neka je funkcija f definisana na [a, b], pri čemu važi f je neprekidna na [a, b], f je diferencijabilna na a, b) i fa) fb). Tada postoji ξ a, b) tako
Operacije s matricama
 Linearna algebra I Operacije s matricama Korolar 3.1.5. Množenje matrica u vektorskom prostoru M n (F) ima sljedeća svojstva: (1) A(B + C) = AB + AC, A, B, C M n (F); (2) (A + B)C = AC + BC, A, B, C M
Linearna algebra I Operacije s matricama Korolar 3.1.5. Množenje matrica u vektorskom prostoru M n (F) ima sljedeća svojstva: (1) A(B + C) = AB + AC, A, B, C M n (F); (2) (A + B)C = AC + BC, A, B, C M
Univerzitet u Nišu, Prirodno-matematički fakultet Prijemni ispit za upis OAS Matematika
 Univerzitet u Nišu, Prirodno-matematički fakultet Prijemni ispit za upis OAS Matematika Rešenja. Matematičkom indukcijom dokazati da za svaki prirodan broj n važi jednakost: + 5 + + (n )(n + ) = n n +.
Univerzitet u Nišu, Prirodno-matematički fakultet Prijemni ispit za upis OAS Matematika Rešenja. Matematičkom indukcijom dokazati da za svaki prirodan broj n važi jednakost: + 5 + + (n )(n + ) = n n +.
Ispitivanje toka i skiciranje grafika funkcija
 Ispitivanje toka i skiciranje grafika funkcija Za skiciranje grafika funkcije potrebno je ispitati svako od sledećih svojstava: Oblast definisanosti: D f = { R f R}. Parnost, neparnost, periodičnost. 3
Ispitivanje toka i skiciranje grafika funkcija Za skiciranje grafika funkcije potrebno je ispitati svako od sledećih svojstava: Oblast definisanosti: D f = { R f R}. Parnost, neparnost, periodičnost. 3
2 tg x ctg x 1 = =, cos 2x Zbog četvrtog kvadranta rješenje je: 2 ctg x
 Zadatak (Darjan, medicinska škola) Izračunaj vrijednosti trigonometrijskih funkcija broja ako je 6 sin =,,. 6 Rješenje Ponovimo trigonometrijske funkcije dvostrukog kuta! Za argument vrijede sljedeće formule:
Zadatak (Darjan, medicinska škola) Izračunaj vrijednosti trigonometrijskih funkcija broja ako je 6 sin =,,. 6 Rješenje Ponovimo trigonometrijske funkcije dvostrukog kuta! Za argument vrijede sljedeće formule:
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu
 Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Analitička geometrija 1. Tačka 1. MF000 Neka su A(1, 1) i B(,11) tačke u koordinatnoj ravni Oxy. Ako tačka S deli duž AB
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Analitička geometrija 1. Tačka 1. MF000 Neka su A(1, 1) i B(,11) tačke u koordinatnoj ravni Oxy. Ako tačka S deli duž AB
XI dvoqas veжbi dr Vladimir Balti. 4. Stabla
 XI dvoqas veжbi dr Vladimir Balti 4. Stabla Teorijski uvod Teorijski uvod Definicija 5.7.1. Stablo je povezan graf bez kontura. Definicija 5.7.1. Stablo je povezan graf bez kontura. Primer 5.7.1. Sva stabla
XI dvoqas veжbi dr Vladimir Balti 4. Stabla Teorijski uvod Teorijski uvod Definicija 5.7.1. Stablo je povezan graf bez kontura. Definicija 5.7.1. Stablo je povezan graf bez kontura. Primer 5.7.1. Sva stabla
RAČUNSKE VEŽBE IZ PREDMETA POLUPROVODNIČKE KOMPONENTE (IV semestar modul EKM) IV deo. Miloš Marjanović
 Univerzitet u Nišu Elektronski fakultet RAČUNSKE VEŽBE IZ PREDMETA (IV semestar modul EKM) IV deo Miloš Marjanović MOSFET TRANZISTORI ZADATAK 35. NMOS tranzistor ima napon praga V T =2V i kroz njega protiče
Univerzitet u Nišu Elektronski fakultet RAČUNSKE VEŽBE IZ PREDMETA (IV semestar modul EKM) IV deo Miloš Marjanović MOSFET TRANZISTORI ZADATAK 35. NMOS tranzistor ima napon praga V T =2V i kroz njega protiče
IZVODI ZADACI (I deo)
 IZVODI ZADACI (I deo) Najpre da se podsetimo tablice i osnovnih pravila:. C`=0. `=. ( )`= 4. ( n )`=n n-. (a )`=a lna 6. (e )`=e 7. (log a )`= 8. (ln)`= ` ln a (>0) 9. = ( 0) 0. `= (>0) (ovde je >0 i a
IZVODI ZADACI (I deo) Najpre da se podsetimo tablice i osnovnih pravila:. C`=0. `=. ( )`= 4. ( n )`=n n-. (a )`=a lna 6. (e )`=e 7. (log a )`= 8. (ln)`= ` ln a (>0) 9. = ( 0) 0. `= (>0) (ovde je >0 i a
MATRICE I DETERMINANTE - formule i zadaci - (Matrice i determinante) 1 / 15
 MATRICE I DETERMINANTE - formule i zadaci - (Matrice i determinante) 1 / 15 Matrice - osnovni pojmovi (Matrice i determinante) 2 / 15 (Matrice i determinante) 2 / 15 Matrice - osnovni pojmovi Matrica reda
MATRICE I DETERMINANTE - formule i zadaci - (Matrice i determinante) 1 / 15 Matrice - osnovni pojmovi (Matrice i determinante) 2 / 15 (Matrice i determinante) 2 / 15 Matrice - osnovni pojmovi Matrica reda
III VEŽBA: FURIJEOVI REDOVI
 III VEŽBA: URIJEOVI REDOVI 3.1. eorijska osnova Posmatrajmo neki vremenski kontinualan signal x(t) na intervalu definisati: t + t t. ada se može X [ k ] = 1 t + t x ( t ) e j 2 π kf t dt, gde je f = 1/.
III VEŽBA: URIJEOVI REDOVI 3.1. eorijska osnova Posmatrajmo neki vremenski kontinualan signal x(t) na intervalu definisati: t + t t. ada se može X [ k ] = 1 t + t x ( t ) e j 2 π kf t dt, gde je f = 1/.
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu
 Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Trigonometrijske jednačine i nejednačine. Zadaci koji se rade bez upotrebe trigonometrijskih formula. 00. FF cos x sin x
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Trigonometrijske jednačine i nejednačine. Zadaci koji se rade bez upotrebe trigonometrijskih formula. 00. FF cos x sin x
Zavrxni ispit iz Matematiqke analize 1
 Građevinski fakultet Univerziteta u Beogradu 3.2.2016. Zavrxni ispit iz Matematiqke analize 1 Prezime i ime: Broj indeksa: 1. Definisati Koxijev niz. Dati primer niza koji nije Koxijev. 2. Dat je red n=1
Građevinski fakultet Univerziteta u Beogradu 3.2.2016. Zavrxni ispit iz Matematiqke analize 1 Prezime i ime: Broj indeksa: 1. Definisati Koxijev niz. Dati primer niza koji nije Koxijev. 2. Dat je red n=1
M086 LA 1 M106 GRP. Tema: Baza vektorskog prostora. Koordinatni sustav. Norma. CSB nejednakost
 M086 LA 1 M106 GRP Tema: CSB nejednakost. 19. 10. 2017. predavač: Rudolf Scitovski, Darija Marković asistent: Darija Brajković, Katarina Vincetić P 1 www.fizika.unios.hr/grpua/ 1 Baza vektorskog prostora.
M086 LA 1 M106 GRP Tema: CSB nejednakost. 19. 10. 2017. predavač: Rudolf Scitovski, Darija Marković asistent: Darija Brajković, Katarina Vincetić P 1 www.fizika.unios.hr/grpua/ 1 Baza vektorskog prostora.
1. razred gimnazije- opšti i prirodno-matematički smer STRUKTURA MOLEKULA HEMIJSKA VEZA
 EMIJSKE VEZE 1 razred gimnazije- opšti i prirodno-matematički smer STRUKTURA MLEKULA Molekul je najsitnija čestica koja se sastoji od dva ili više istih atoma, a to su molekuli elemenata: Cl 2, 2, N 2,
EMIJSKE VEZE 1 razred gimnazije- opšti i prirodno-matematički smer STRUKTURA MLEKULA Molekul je najsitnija čestica koja se sastoji od dva ili više istih atoma, a to su molekuli elemenata: Cl 2, 2, N 2,
IZRAČUNAVANJE POKAZATELJA NAČINA RADA NAČINA RADA (ISKORIŠĆENOSTI KAPACITETA, STEPENA OTVORENOSTI RADNIH MESTA I NIVOA ORGANIZOVANOSTI)
 IZRAČUNAVANJE POKAZATELJA NAČINA RADA NAČINA RADA (ISKORIŠĆENOSTI KAPACITETA, STEPENA OTVORENOSTI RADNIH MESTA I NIVOA ORGANIZOVANOSTI) Izračunavanje pokazatelja načina rada OTVORENOG RM RASPOLOŽIVO RADNO
IZRAČUNAVANJE POKAZATELJA NAČINA RADA NAČINA RADA (ISKORIŠĆENOSTI KAPACITETA, STEPENA OTVORENOSTI RADNIH MESTA I NIVOA ORGANIZOVANOSTI) Izračunavanje pokazatelja načina rada OTVORENOG RM RASPOLOŽIVO RADNO
MEĐUMOLEKULSKE SILE JON-DIPOL DIPOL VODONIČNE NE VEZE DIPOL DIPOL-DIPOL DIPOL-INDUKOVANI INDUKOVANI JON-INDUKOVANI DISPERZNE SILE
 MEĐUMLEKULSKE SILE JN-DIPL VDNIČNE NE VEZE DIPL-DIPL JN-INDUKVANI DIPL DIPL-INDUKVANI INDUKVANI DIPL DISPERZNE SILE MEĐUMLEKULSKE SILE jake JNSKA VEZA (metal-nemetal) KVALENTNA VEZA (nemetal-nemetal) METALNA
MEĐUMLEKULSKE SILE JN-DIPL VDNIČNE NE VEZE DIPL-DIPL JN-INDUKVANI DIPL DIPL-INDUKVANI INDUKVANI DIPL DISPERZNE SILE MEĐUMLEKULSKE SILE jake JNSKA VEZA (metal-nemetal) KVALENTNA VEZA (nemetal-nemetal) METALNA
Osnovne veličine, jedinice i izračunavanja u hemiji
 Osnovne veličine, jedinice i izračunavanja u hemiji Pregled pojmova veličina i njihovih jedinica koje se koriste pri osnovnim izračunavanjima u hemiji dat je u Tabeli 1. Tabela 1. Veličine i njihove jedinice
Osnovne veličine, jedinice i izračunavanja u hemiji Pregled pojmova veličina i njihovih jedinica koje se koriste pri osnovnim izračunavanjima u hemiji dat je u Tabeli 1. Tabela 1. Veličine i njihove jedinice
I.13. Koliki je napon između neke tačke A čiji je potencijal 5 V i referentne tačke u odnosu na koju se taj potencijal računa?
 TET I.1. Šta je Kulonova sila? elektrostatička sila magnetna sila c) gravitaciona sila I.. Šta je elektrostatička sila? sila kojom međusobno eluju naelektrisanja u mirovanju sila kojom eluju naelektrisanja
TET I.1. Šta je Kulonova sila? elektrostatička sila magnetna sila c) gravitaciona sila I.. Šta je elektrostatička sila? sila kojom međusobno eluju naelektrisanja u mirovanju sila kojom eluju naelektrisanja
OM2 V3 Ime i prezime: Index br: I SAVIJANJE SILAMA TANKOZIDNIH ŠTAPOVA
 OM V me i preime: nde br: 1.0.01. 0.0.01. SAVJANJE SLAMA TANKOZDNH ŠTAPOVA A. TANKOZDN ŠTAPOV PROZVOLJNOG OTVORENOG POPREČNOG PRESEKA Preposavka: Smičući napon je konsanan po debljini ida (duž pravca upravnog
OM V me i preime: nde br: 1.0.01. 0.0.01. SAVJANJE SLAMA TANKOZDNH ŠTAPOVA A. TANKOZDN ŠTAPOV PROZVOLJNOG OTVORENOG POPREČNOG PRESEKA Preposavka: Smičući napon je konsanan po debljini ida (duž pravca upravnog
KVADRATNA FUNKCIJA. Kvadratna funkcija je oblika: Kriva u ravni koja predstavlja grafik funkcije y = ax + bx + c. je parabola.
 KVADRATNA FUNKCIJA Kvadratna funkcija je oblika: = a + b + c Gde je R, a 0 i a, b i c su realni brojevi. Kriva u ravni koja predstavlja grafik funkcije = a + b + c je parabola. Najpre ćemo naučiti kako
KVADRATNA FUNKCIJA Kvadratna funkcija je oblika: = a + b + c Gde je R, a 0 i a, b i c su realni brojevi. Kriva u ravni koja predstavlja grafik funkcije = a + b + c je parabola. Najpre ćemo naučiti kako
Geometrija (I smer) deo 1: Vektori
 Geometrija (I smer) deo 1: Vektori Srdjan Vukmirović Matematički fakultet, Beograd septembar 2013. Vektori i linearne operacije sa vektorima Definicija Vektor je klasa ekvivalencije usmerenih duži. Kažemo
Geometrija (I smer) deo 1: Vektori Srdjan Vukmirović Matematički fakultet, Beograd septembar 2013. Vektori i linearne operacije sa vektorima Definicija Vektor je klasa ekvivalencije usmerenih duži. Kažemo
Elektrotehnički fakultet univerziteta u Beogradu 17.maj Odsek za Softversko inžinjerstvo
 Elektrotehnički fakultet univerziteta u Beogradu 7.maj 009. Odsek za Softversko inžinjerstvo Performanse računarskih sistema Drugi kolokvijum Predmetni nastavnik: dr Jelica Protić (35) a) (0) Posmatra
Elektrotehnički fakultet univerziteta u Beogradu 7.maj 009. Odsek za Softversko inžinjerstvo Performanse računarskih sistema Drugi kolokvijum Predmetni nastavnik: dr Jelica Protić (35) a) (0) Posmatra
10. STABILNOST KOSINA
 MEHANIKA TLA: Stabilnot koina 101 10. STABILNOST KOSINA 10.1 Metode proračuna koina Problem analize tabilnoti zemljanih maa vodi e na određivanje odnoa između rapoložive mičuće čvrtoće i proečnog mičućeg
MEHANIKA TLA: Stabilnot koina 101 10. STABILNOST KOSINA 10.1 Metode proračuna koina Problem analize tabilnoti zemljanih maa vodi e na određivanje odnoa između rapoložive mičuće čvrtoće i proečnog mičućeg
S t r a n a 1. 1.Povezati jonsku jačinu rastvora: a) MgCl 2 b) Al 2 (SO 4 ) 3 sa njihovim molalitetima, m. za so tipa: M p X q. pa je jonska jačina:
 S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
Zadatak 1 Dokazati da simetrala ugla u trouglu deli naspramnu stranu u odnosu susednih strana.
 Zadatak 1 Dokazati da simetrala ugla u trouglu deli naspramnu stranu u odnosu susednih strana. Zadatak 2 Dokazati da se visine trougla seku u jednoj tački ortocentar. 1 Dvostruki vektorski proizvod Važi
Zadatak 1 Dokazati da simetrala ugla u trouglu deli naspramnu stranu u odnosu susednih strana. Zadatak 2 Dokazati da se visine trougla seku u jednoj tački ortocentar. 1 Dvostruki vektorski proizvod Važi
VJEŽBE 3 BIPOLARNI TRANZISTORI. Slika 1. Postoje npn i pnp bipolarni tranziostori i njihovi simboli su dati na slici 2 i to npn lijevo i pnp desno.
 JŽ 3 POLAN TANZSTO ipolarni tranzistor se sastoji od dva pn spoja kod kojih je jedna oblast zajednička za oba i naziva se baza, slika 1 Slika 1 ipolarni tranzistor ima 3 izvoda: emitor (), kolektor (K)
JŽ 3 POLAN TANZSTO ipolarni tranzistor se sastoji od dva pn spoja kod kojih je jedna oblast zajednička za oba i naziva se baza, slika 1 Slika 1 ipolarni tranzistor ima 3 izvoda: emitor (), kolektor (K)
Računarska grafika. Rasterizacija linije
 Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
Analitička geometrija
 1 Analitička geometrija Neka su dati vektori a = a 1 i + a j + a 3 k = (a 1, a, a 3 ), b = b 1 i + b j + b 3 k = (b 1, b, b 3 ) i c = c 1 i + c j + c 3 k = (c 1, c, c 3 ). Skalarni proizvod vektora a i
1 Analitička geometrija Neka su dati vektori a = a 1 i + a j + a 3 k = (a 1, a, a 3 ), b = b 1 i + b j + b 3 k = (b 1, b, b 3 ) i c = c 1 i + c j + c 3 k = (c 1, c, c 3 ). Skalarni proizvod vektora a i
18. listopada listopada / 13
 18. listopada 2016. 18. listopada 2016. 1 / 13 Neprekidne funkcije Važnu klasu funkcija tvore neprekidne funkcije. To su funkcije f kod kojih mala promjena u nezavisnoj varijabli x uzrokuje malu promjenu
18. listopada 2016. 18. listopada 2016. 1 / 13 Neprekidne funkcije Važnu klasu funkcija tvore neprekidne funkcije. To su funkcije f kod kojih mala promjena u nezavisnoj varijabli x uzrokuje malu promjenu
5 Ispitivanje funkcija
 5 Ispitivanje funkcija 3 5 Ispitivanje funkcija Ispitivanje funkcije pretodi crtanju grafika funkcije. Opšti postupak ispitivanja funkcija koje su definisane eksplicitno y = f() sadrži sledeće elemente:
5 Ispitivanje funkcija 3 5 Ispitivanje funkcija Ispitivanje funkcije pretodi crtanju grafika funkcije. Opšti postupak ispitivanja funkcija koje su definisane eksplicitno y = f() sadrži sledeće elemente:
5. Karakteristične funkcije
 5. Karakteristične funkcije Profesor Milan Merkle emerkle@etf.rs milanmerkle.etf.rs Verovatnoća i Statistika-proleće 2018 Milan Merkle Karakteristične funkcije ETF Beograd 1 / 10 Definicija Karakteristična
5. Karakteristične funkcije Profesor Milan Merkle emerkle@etf.rs milanmerkle.etf.rs Verovatnoća i Statistika-proleće 2018 Milan Merkle Karakteristične funkcije ETF Beograd 1 / 10 Definicija Karakteristična
Trigonometrija 2. Adicijske formule. Formule dvostrukog kuta Formule polovičnog kuta Pretvaranje sume(razlike u produkt i obrnuto
 Trigonometrija Adicijske formule Formule dvostrukog kuta Formule polovičnog kuta Pretvaranje sume(razlike u produkt i obrnuto Razumijevanje postupka izrade složenijeg matematičkog problema iz osnova trigonometrije
Trigonometrija Adicijske formule Formule dvostrukog kuta Formule polovičnog kuta Pretvaranje sume(razlike u produkt i obrnuto Razumijevanje postupka izrade složenijeg matematičkog problema iz osnova trigonometrije
Apsolutno neprekidne raspodele Raspodele apsolutno neprekidnih sluqajnih promenljivih nazivaju se apsolutno neprekidnim raspodelama.
 Apsolutno neprekidne raspodele Raspodele apsolutno neprekidnih sluqajnih promenljivih nazivaju se apsolutno neprekidnim raspodelama. a b Verovatno a da sluqajna promenljiva X uzima vrednost iz intervala
Apsolutno neprekidne raspodele Raspodele apsolutno neprekidnih sluqajnih promenljivih nazivaju se apsolutno neprekidnim raspodelama. a b Verovatno a da sluqajna promenljiva X uzima vrednost iz intervala
4 Numeričko diferenciranje
 4 Numeričko diferenciranje 7. Funkcija fx) je zadata tabelom: x 0 4 6 8 fx).17 1.5167 1.7044 3.385 5.09 7.814 Koristeći konačne razlike, zaključno sa trećim redom, odrediti tačku x minimuma funkcije fx)
4 Numeričko diferenciranje 7. Funkcija fx) je zadata tabelom: x 0 4 6 8 fx).17 1.5167 1.7044 3.385 5.09 7.814 Koristeći konačne razlike, zaključno sa trećim redom, odrediti tačku x minimuma funkcije fx)
KERAMIKA, BETON I DRVO
 VJEŽBE: četvrtak, 12:15-14:00 KERAMIKA, BETON I DRVO Vježba 1. Ionske i kovalentne strukture Prof.dr.sc. Lidija Ćurković STRUKTURA ČVRSTIH (krutih) TVARI ovisi o: 1. VRSTI VEZA IZMEĐU STRUKTURNIH JEDINICA
VJEŽBE: četvrtak, 12:15-14:00 KERAMIKA, BETON I DRVO Vježba 1. Ionske i kovalentne strukture Prof.dr.sc. Lidija Ćurković STRUKTURA ČVRSTIH (krutih) TVARI ovisi o: 1. VRSTI VEZA IZMEĐU STRUKTURNIH JEDINICA
MEHANIKA FLUIDA. Isticanje kroz otvore sa promenljivim nivoom tečnosti
 MEHANIKA FLUIDA Isticanje kroz otvore sa promenljivim nivoom tečnosti zadatak Prizmatična sud podeljen je vertikalnom pregradom, u kojoj je otvor prečnika d, na dve komore Leva komora je napunjena vodom
MEHANIKA FLUIDA Isticanje kroz otvore sa promenljivim nivoom tečnosti zadatak Prizmatična sud podeljen je vertikalnom pregradom, u kojoj je otvor prečnika d, na dve komore Leva komora je napunjena vodom
4.7. Zadaci Formalizam diferenciranja (teorija na stranama ) 343. Znajući izvod funkcije x arctg x, odrediti izvod funkcije x arcctg x.
 4.7. ZADACI 87 4.7. Zadaci 4.7.. Formalizam diferenciranja teorija na stranama 4-46) 340. Znajući izvod funkcije arcsin, odrediti izvod funkcije arccos. Rešenje. Polazeći od jednakosti arcsin + arccos
4.7. ZADACI 87 4.7. Zadaci 4.7.. Formalizam diferenciranja teorija na stranama 4-46) 340. Znajući izvod funkcije arcsin, odrediti izvod funkcije arccos. Rešenje. Polazeći od jednakosti arcsin + arccos
Geometrija (I smer) deo 2: Afine transformacije
 Geometrija (I smer) deo 2: Afine transformacije Srdjan Vukmirović Matematički fakultet, Beograd septembar 2013. Transformacije koordinata tačaka Transformacije koordinata tačaka Pretpostavimo da za bazne
Geometrija (I smer) deo 2: Afine transformacije Srdjan Vukmirović Matematički fakultet, Beograd septembar 2013. Transformacije koordinata tačaka Transformacije koordinata tačaka Pretpostavimo da za bazne
Ispit održan dana i tačka A ( 3,3, 4 ) x x + 1
 Ispit održan dana 9 0 009 Naći sve vrijednosti korjena 4 z ako je ( ) 8 y+ z Data je prava a : = = kroz tačku A i okomita je na pravu a z = + i i tačka A (,, 4 ) Naći jednačinu prave b koja prolazi ( +
Ispit održan dana 9 0 009 Naći sve vrijednosti korjena 4 z ako je ( ) 8 y+ z Data je prava a : = = kroz tačku A i okomita je na pravu a z = + i i tačka A (,, 4 ) Naći jednačinu prave b koja prolazi ( +
PARCIJALNI IZVODI I DIFERENCIJALI. Sama definicija parcijalnog izvoda i diferencijala je malo teža, mi se njome ovde nećemo baviti a vi ćete je,
 PARCIJALNI IZVODI I DIFERENCIJALI Sama definicija parcijalnog ivoda i diferencijala je malo teža, mi se njome ovde nećemo baviti a vi ćete je, naravno, naučiti onako kako vaš profesor ahteva. Mi ćemo probati
PARCIJALNI IZVODI I DIFERENCIJALI Sama definicija parcijalnog ivoda i diferencijala je malo teža, mi se njome ovde nećemo baviti a vi ćete je, naravno, naučiti onako kako vaš profesor ahteva. Mi ćemo probati
7 Algebarske jednadžbe
 7 Algebarske jednadžbe 7.1 Nultočke polinoma Skup svih polinoma nad skupom kompleksnih brojeva označavamo sa C[x]. Definicija. Nultočka polinoma f C[x] je svaki kompleksni broj α takav da je f(α) = 0.
7 Algebarske jednadžbe 7.1 Nultočke polinoma Skup svih polinoma nad skupom kompleksnih brojeva označavamo sa C[x]. Definicija. Nultočka polinoma f C[x] je svaki kompleksni broj α takav da je f(α) = 0.
KOMUTATIVNI I ASOCIJATIVNI GRUPOIDI. NEUTRALNI ELEMENT GRUPOIDA.
 KOMUTATIVNI I ASOCIJATIVNI GRUPOIDI NEUTRALNI ELEMENT GRUPOIDA 1 Grupoid (G, ) je asocijativa akko važi ( x, y, z G) x (y z) = (x y) z Grupoid (G, ) je komutativa akko važi ( x, y G) x y = y x Asocijativa
KOMUTATIVNI I ASOCIJATIVNI GRUPOIDI NEUTRALNI ELEMENT GRUPOIDA 1 Grupoid (G, ) je asocijativa akko važi ( x, y, z G) x (y z) = (x y) z Grupoid (G, ) je komutativa akko važi ( x, y G) x y = y x Asocijativa
TAČKA i PRAVA. , onda rastojanje između njih računamo po formuli C(1,5) d(b,c) d(a,b)
 TAČKA i PRAVA Najpre ćemo se upoznati sa osnovnim formulama i njihovom primenom.. Rastojanje između dve tačke Ako su nam date tačke Ax (, y) i Bx (, y ), onda rastojanje između njih računamo po formuli
TAČKA i PRAVA Najpre ćemo se upoznati sa osnovnim formulama i njihovom primenom.. Rastojanje između dve tačke Ako su nam date tačke Ax (, y) i Bx (, y ), onda rastojanje između njih računamo po formuli
konst. Električni otpor
 Sveučilište J. J. Strossmayera u sijeku Elektrotehnički fakultet sijek Stručni studij Električni otpor hmov zakon Pri protjecanju struje kroz vodič pojavljuje se otpor. Georg Simon hm je ustanovio ovisnost
Sveučilište J. J. Strossmayera u sijeku Elektrotehnički fakultet sijek Stručni studij Električni otpor hmov zakon Pri protjecanju struje kroz vodič pojavljuje se otpor. Georg Simon hm je ustanovio ovisnost
INTEGRALNI RAČUN. Teorije, metodike i povijest infinitezimalnih računa. Lucija Mijić 17. veljače 2011.
 INTEGRALNI RAČUN Teorije, metodike i povijest infinitezimalnih računa Lucija Mijić lucija@ktf-split.hr 17. veljače 2011. Pogledajmo Predstavimo gornju sumu sa Dodamo još jedan Dobivamo pravokutnik sa Odnosno
INTEGRALNI RAČUN Teorije, metodike i povijest infinitezimalnih računa Lucija Mijić lucija@ktf-split.hr 17. veljače 2011. Pogledajmo Predstavimo gornju sumu sa Dodamo još jedan Dobivamo pravokutnik sa Odnosno
Osnove elektrotehnike I popravni parcijalni ispit VARIJANTA A
 Osnove elektrotehnike I popravni parcijalni ispit 1..014. VARIJANTA A Prezime i ime: Broj indeksa: Profesorov prvi postulat: Što se ne može pročitati, ne može se ni ocijeniti. A C 1.1. Tri naelektrisanja
Osnove elektrotehnike I popravni parcijalni ispit 1..014. VARIJANTA A Prezime i ime: Broj indeksa: Profesorov prvi postulat: Što se ne može pročitati, ne može se ni ocijeniti. A C 1.1. Tri naelektrisanja
2log. se zove numerus (logaritmand), je osnova (baza) log. log. log =
 ( > 0, 0)!" # > 0 je najčešći uslov koji postavljamo a još je,, > 0 se zove numerus (aritmand), je osnova (baza). 0.. ( ) +... 7.. 8. Za prelazak na neku novu bazu c: 9. Ako je baza (osnova) 0 takvi se
( > 0, 0)!" # > 0 je najčešći uslov koji postavljamo a još je,, > 0 se zove numerus (aritmand), je osnova (baza). 0.. ( ) +... 7.. 8. Za prelazak na neku novu bazu c: 9. Ako je baza (osnova) 0 takvi se
Riješeni zadaci: Nizovi realnih brojeva
 Riješei zadaci: Nizovi realih brojeva Nizovi, aritmetički iz, geometrijski iz Fukciju a : N R azivamo beskoači) iz realih brojeva i ozačavamo s a 1, a,..., a,... ili a ), pri čemu je a = a). Aritmetički
Riješei zadaci: Nizovi realih brojeva Nizovi, aritmetički iz, geometrijski iz Fukciju a : N R azivamo beskoači) iz realih brojeva i ozačavamo s a 1, a,..., a,... ili a ), pri čemu je a = a). Aritmetički
Pismeni ispit iz matematike GRUPA A 1. Napisati u trigonometrijskom i eksponencijalnom obliku kompleksni broj, zatim naći 4 z.
 Pismeni ispit iz matematike 06 007 Napisati u trigonometrijskom i eksponencijalnom obliku kompleksni broj z = + i, zatim naći z Ispitati funkciju i nacrtati grafik : = ( ) y e + 6 Izračunati integral:
Pismeni ispit iz matematike 06 007 Napisati u trigonometrijskom i eksponencijalnom obliku kompleksni broj z = + i, zatim naći z Ispitati funkciju i nacrtati grafik : = ( ) y e + 6 Izračunati integral:
Program testirati pomoću podataka iz sledeće tabele:
 Deo 2: Rešeni zadaci 135 Vrednost integrala je I = 2.40407 42. Napisati program za izračunavanje koeficijenta proste linearne korelacije (Pearsonovog koeficijenta) slučajnih veličina X = (x 1,..., x n
Deo 2: Rešeni zadaci 135 Vrednost integrala je I = 2.40407 42. Napisati program za izračunavanje koeficijenta proste linearne korelacije (Pearsonovog koeficijenta) slučajnih veličina X = (x 1,..., x n
Zadaci iz trigonometrije za seminar
 Zadaci iz trigonometrije za seminar FON: 1. Vrednost izraza sin 1 cos 6 jednaka je: ; B) 1 ; V) 1 1 + 1 ; G) ; D). 16. Broj rexea jednaqine sin x cos x + cos x = sin x + sin x na intervalu π ), π je: ;
Zadaci iz trigonometrije za seminar FON: 1. Vrednost izraza sin 1 cos 6 jednaka je: ; B) 1 ; V) 1 1 + 1 ; G) ; D). 16. Broj rexea jednaqine sin x cos x + cos x = sin x + sin x na intervalu π ), π je: ;
3. razred gimnazije- opšti i prirodno-matematički smer ALKENI. Aciklični nezasićeni ugljovodonici koji imaju jednu dvostruku vezu.
 ALKENI Acikliči ezasićei ugljovodoici koji imaju jedu dvostruku vezu. 2 4 2 2 2 (etile) viil grupa 3 6 2 3 2 2 prope (propile) alil grupa 4 8 2 2 3 3 3 2 3 3 1-bute 2-bute 2-metilprope 5 10 2 2 2 2 3 2
ALKENI Acikliči ezasićei ugljovodoici koji imaju jedu dvostruku vezu. 2 4 2 2 2 (etile) viil grupa 3 6 2 3 2 2 prope (propile) alil grupa 4 8 2 2 3 3 3 2 3 3 1-bute 2-bute 2-metilprope 5 10 2 2 2 2 3 2
Kaskadna kompenzacija SAU
 Kaskadna kompenzacija SAU U inženjerskoj praksi, naročito u sistemima regulacije elektromotornih pogona i tehnoloških procesa, veoma često se primenjuje metoda kaskadne kompenzacije, u čijoj osnovi su
Kaskadna kompenzacija SAU U inženjerskoj praksi, naročito u sistemima regulacije elektromotornih pogona i tehnoloških procesa, veoma često se primenjuje metoda kaskadne kompenzacije, u čijoj osnovi su
Računarska grafika. Rasterizacija linije
 Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
Računarska grafika Osnovni inkrementalni algoritam Drugi naziv u literaturi digitalni diferencijalni analizator (DDA) Pretpostavke (privremena ograničenja koja se mogu otkloniti jednostavnim uopštavanjem
Linearna algebra 2 prvi kolokvij,
 1 2 3 4 5 Σ jmbag smjer studija Linearna algebra 2 prvi kolokvij, 7. 11. 2012. 1. (10 bodova) Neka je dano preslikavanje s : R 2 R 2 R, s (x, y) = (Ax y), pri čemu je A: R 2 R 2 linearan operator oblika
1 2 3 4 5 Σ jmbag smjer studija Linearna algebra 2 prvi kolokvij, 7. 11. 2012. 1. (10 bodova) Neka je dano preslikavanje s : R 2 R 2 R, s (x, y) = (Ax y), pri čemu je A: R 2 R 2 linearan operator oblika
Ministarstvo prosvete i sporta Republike Srbije Druxtvo matematiqara Srbije Prvi razred A kategorija
 18.02006. Prvi razred A kategorija Dokazati da kruжnica koja sadrжi dva temena i ortocentar trougla ima isti polupreqnik kao i kruжnica opisana oko tog trougla. Na i najve i prirodan broj koji je maƭi
18.02006. Prvi razred A kategorija Dokazati da kruжnica koja sadrжi dva temena i ortocentar trougla ima isti polupreqnik kao i kruжnica opisana oko tog trougla. Na i najve i prirodan broj koji je maƭi
IZVODI ZADACI ( IV deo) Rešenje: Najpre ćemo logaritmovati ovu jednakost sa ln ( to beše prirodni logaritam za osnovu e) a zatim ćemo
 IZVODI ZADACI ( IV deo) LOGARITAMSKI IZVOD Logariamskim izvodom funkcije f(), gde je >0 i, nazivamo izvod logarima e funkcije, o jes: (ln ) f ( ) f ( ) Primer. Nadji izvod funkcije Najpre ćemo logarimovai
IZVODI ZADACI ( IV deo) LOGARITAMSKI IZVOD Logariamskim izvodom funkcije f(), gde je >0 i, nazivamo izvod logarima e funkcije, o jes: (ln ) f ( ) f ( ) Primer. Nadji izvod funkcije Najpre ćemo logarimovai
Verovatnoća i Statistika I deo Teorija verovatnoće (zadaci) Beleške dr Bobana Marinkovića
 Verovatnoća i Statistika I deo Teorija verovatnoće zadaci Beleške dr Bobana Marinkovića Iz skupa, 2,, 00} bira se na slučajan način 5 brojeva Odrediti skup elementarnih dogadjaja ako se brojevi biraju
Verovatnoća i Statistika I deo Teorija verovatnoće zadaci Beleške dr Bobana Marinkovića Iz skupa, 2,, 00} bira se na slučajan način 5 brojeva Odrediti skup elementarnih dogadjaja ako se brojevi biraju
nvt 1) ukoliko su poznate struje dioda. Struja diode D 1 je I 1 = I I 2 = 8mA. Sada je = 1,2mA.
 IOAE Dioda 8/9 I U kolu sa slike, diode D su identične Poznato je I=mA, I =ma, I S =fa na 7 o C i parametar n= a) Odrediti napon V I Kolika treba da bude struja I da bi izlazni napon V I iznosio 5mV? b)
IOAE Dioda 8/9 I U kolu sa slike, diode D su identične Poznato je I=mA, I =ma, I S =fa na 7 o C i parametar n= a) Odrediti napon V I Kolika treba da bude struja I da bi izlazni napon V I iznosio 5mV? b)
INTELIGENTNO UPRAVLJANJE
 INTELIGENTNO UPRAVLJANJE Fuzzy sistemi zaključivanja Vanr.prof. Dr. Lejla Banjanović-Mehmedović Mehmedović 1 Osnovni elementi fuzzy sistema zaključivanja Fazifikacija Baza znanja Baze podataka Baze pravila
INTELIGENTNO UPRAVLJANJE Fuzzy sistemi zaključivanja Vanr.prof. Dr. Lejla Banjanović-Mehmedović Mehmedović 1 Osnovni elementi fuzzy sistema zaključivanja Fazifikacija Baza znanja Baze podataka Baze pravila
Sume kvadrata. mn = (ax + by) 2 + (ay bx) 2.
 Sume kvadrata Koji se prirodni brojevi mogu prikazati kao zbroj kvadrata dva cijela broja? Propozicija 1. Ako su brojevi m i n sume dva kvadrata, onda je i njihov produkt m n takoder suma dva kvadrata.
Sume kvadrata Koji se prirodni brojevi mogu prikazati kao zbroj kvadrata dva cijela broja? Propozicija 1. Ako su brojevi m i n sume dva kvadrata, onda je i njihov produkt m n takoder suma dva kvadrata.
FTN Novi Sad Katedra za motore i vozila. Teorija kretanja drumskih vozila Vučno-dinamičke performanse vozila: MAKSIMALNA BRZINA
 : MAKSIMALNA BRZINA Maksimalna brzina kretanja F O (N) F OI i m =i I i m =i II F Oid Princip određivanja v MAX : Drugi Njutnov zakon Dokle god je: F O > ΣF otp vozilo ubrzava Kada postane: F O = ΣF otp
: MAKSIMALNA BRZINA Maksimalna brzina kretanja F O (N) F OI i m =i I i m =i II F Oid Princip određivanja v MAX : Drugi Njutnov zakon Dokle god je: F O > ΣF otp vozilo ubrzava Kada postane: F O = ΣF otp
MATEMATIKA 2. Grupa 1 Rexea zadataka. Prvi pismeni kolokvijum, Dragan ori
 MATEMATIKA 2 Prvi pismeni kolokvijum, 14.4.2016 Grupa 1 Rexea zadataka Dragan ori Zadaci i rexea 1. unkcija f : R 2 R definisana je sa xy 2 f(x, y) = x2 + y sin 3 2 x 2, (x, y) (0, 0) + y2 0, (x, y) =
MATEMATIKA 2 Prvi pismeni kolokvijum, 14.4.2016 Grupa 1 Rexea zadataka Dragan ori Zadaci i rexea 1. unkcija f : R 2 R definisana je sa xy 2 f(x, y) = x2 + y sin 3 2 x 2, (x, y) (0, 0) + y2 0, (x, y) =
Klasifikacija blizu Kelerovih mnogostrukosti. konstantne holomorfne sekcione krivine. Kelerove. mnogostrukosti. blizu Kelerove.
 Klasifikacija blizu Teorema Neka je M Kelerova mnogostrukost. Operator krivine R ima sledeća svojstva: R(X, Y, Z, W ) = R(Y, X, Z, W ) = R(X, Y, W, Z) R(X, Y, Z, W ) + R(Y, Z, X, W ) + R(Z, X, Y, W ) =
Klasifikacija blizu Teorema Neka je M Kelerova mnogostrukost. Operator krivine R ima sledeća svojstva: R(X, Y, Z, W ) = R(Y, X, Z, W ) = R(X, Y, W, Z) R(X, Y, Z, W ) + R(Y, Z, X, W ) + R(Z, X, Y, W ) =
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu
 Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Planimetrija. Sličnost trouglova. GF 000 Dužine stranica trougla su 5cm, cm i 8cm. Dužina najduže stranice njemu sličnog
Zadaci sa prethodnih prijemnih ispita iz matematike na Beogradskom univerzitetu Planimetrija. Sličnost trouglova. GF 000 Dužine stranica trougla su 5cm, cm i 8cm. Dužina najduže stranice njemu sličnog
STRUKTURA ATOMA. Dalton (1803) Tomson (1904) Raderford (1911) Bor (1913) Šredinger (1926)
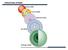 Dalton (1803) Tomson (1904) Raderford (1911) Bor (1913) Šredinger (1926) TALASNO MEHANIČKI MODEL ATOMA Hipoteza de Brolja Elektroni i fotoni imaju dvojnu prirodu: talasnu i korpuskularnu. E = hν E = mc
Dalton (1803) Tomson (1904) Raderford (1911) Bor (1913) Šredinger (1926) TALASNO MEHANIČKI MODEL ATOMA Hipoteza de Brolja Elektroni i fotoni imaju dvojnu prirodu: talasnu i korpuskularnu. E = hν E = mc
radni nerecenzirani materijal za predavanja R(f) = {f(x) x D}
 Matematika 1 Funkcije radni nerecenzirani materijal za predavanja Definicija 1. Neka su D i K bilo koja dva neprazna skupa. Postupak f koji svakom elementu x D pridružuje točno jedan element y K zovemo funkcija
Matematika 1 Funkcije radni nerecenzirani materijal za predavanja Definicija 1. Neka su D i K bilo koja dva neprazna skupa. Postupak f koji svakom elementu x D pridružuje točno jedan element y K zovemo funkcija
Pri međusobnom spajanju atoma nastaje energetski stabilniji sistem. To se postiže:
 HEMIJSKE VEZE Pri međusobnom spajanju atoma nastaje energetski stabilniji sistem. To se postiže: - prelaskom atoma u pozitivno i negativno naelektrisane jone koji se međusobno privlače, jonska veza - sparivanjem
HEMIJSKE VEZE Pri međusobnom spajanju atoma nastaje energetski stabilniji sistem. To se postiže: - prelaskom atoma u pozitivno i negativno naelektrisane jone koji se međusobno privlače, jonska veza - sparivanjem
Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design
 Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
(P.I.) PRETPOSTAVKA INDUKCIJE - pretpostavimo da tvrdnja vrijedi za n = k.
 1 3 Skupovi brojeva 3.1 Skup prirodnih brojeva - N N = {1, 2, 3,...} Aksiom matematičke indukcije Neka je N skup prirodnih brojeva i M podskup od N. Ako za M vrijede svojstva: 1) 1 M 2) n M (n + 1) M,
1 3 Skupovi brojeva 3.1 Skup prirodnih brojeva - N N = {1, 2, 3,...} Aksiom matematičke indukcije Neka je N skup prirodnih brojeva i M podskup od N. Ako za M vrijede svojstva: 1) 1 M 2) n M (n + 1) M,
Otpornost R u kolu naizmjenične struje
 Otpornost R u kolu naizmjenične struje Pretpostavimo da je otpornik R priključen na prostoperiodični napon: Po Omovom zakonu pad napona na otporniku je: ( ) = ( ω ) u t sin m t R ( ) = ( ) u t R i t Struja
Otpornost R u kolu naizmjenične struje Pretpostavimo da je otpornik R priključen na prostoperiodični napon: Po Omovom zakonu pad napona na otporniku je: ( ) = ( ω ) u t sin m t R ( ) = ( ) u t R i t Struja
Betonske konstrukcije 1 - vežbe 3 - Veliki ekscentricitet -Dodatni primeri
 Betonske konstrukcije 1 - vežbe 3 - Veliki ekscentricitet -Dodatni primeri 1 1 Zadatak 1b Čisto savijanje - vezano dimenzionisanje Odrediti potrebnu površinu armature za presek poznatih dimenzija, pravougaonog
Betonske konstrukcije 1 - vežbe 3 - Veliki ekscentricitet -Dodatni primeri 1 1 Zadatak 1b Čisto savijanje - vezano dimenzionisanje Odrediti potrebnu površinu armature za presek poznatih dimenzija, pravougaonog
, 81, 5?J,. 1o~",mlt. [ BO'?o~ ~Iel7L1 povr.sil?lj pt"en:nt7 cf~ ~ <;). So. r~ ~ I~ + 2 JA = (;82,67'11:/'+2-[ 4'33.10'+ 7M.
 J r_jl v. el7l1 povr.sl?lj pt"en:nt7 cf \ L.sj,,;, ocredz' 3 Q),sof'stvene f1?(j'me")7e?j1erc!je b) po{o!.aj 'i1m/' ce/y11ra.[,p! (j'j,a 1lerc!/e
J r_jl v. el7l1 povr.sl?lj pt"en:nt7 cf \ L.sj,,;, ocredz' 3 Q),sof'stvene f1?(j'me")7e?j1erc!je b) po{o!.aj 'i1m/' ce/y11ra.[,p! (j'j,a 1lerc!/e
SEMINAR IZ KOLEGIJA ANALITIČKA KEMIJA I. Studij Primijenjena kemija
 SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
a M a A. Može se pokazati da je supremum (ako postoji) jedinstven pa uvodimo oznaku sup A.
 3 Infimum i supremum Definicija. Neka je A R. Kažemo da je M R supremum skupa A ako je (i) M gornja meda skupa A, tj. a M a A. (ii) M najmanja gornja meda skupa A, tj. ( ε > 0)( a A) takav da je a > M
3 Infimum i supremum Definicija. Neka je A R. Kažemo da je M R supremum skupa A ako je (i) M gornja meda skupa A, tj. a M a A. (ii) M najmanja gornja meda skupa A, tj. ( ε > 0)( a A) takav da je a > M
- pravac n je zadan s točkom T(2,0) i koeficijentom smjera k=2. (30 bodova)
 MEHANIKA 1 1. KOLOKVIJ 04/2008. grupa I 1. Zadane su dvije sile F i. Sila F = 4i + 6j [ N]. Sila je zadana s veličinom = i leži na pravcu koji s koordinatnom osi x zatvara kut od 30 (sve komponente sile
MEHANIKA 1 1. KOLOKVIJ 04/2008. grupa I 1. Zadane su dvije sile F i. Sila F = 4i + 6j [ N]. Sila je zadana s veličinom = i leži na pravcu koji s koordinatnom osi x zatvara kut od 30 (sve komponente sile
